Лабораторные маркеры рака легких
Комплексное лабораторное исследование, направленное на определение наличия злокачественного новообразования легких, степени его распространенности, оценки эффективности лечения и возможности развития рецидивов.
Синонимы русские
Рак легкого; злокачественные опухоли легкого; комплексное лабораторное обследование.
Синонимы английские
Lung cancer; comprehensive laboratory examination.
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Детям в возрасте до 1 года не принимать пищу в течение 30-40 минут до исследования.
- Детям в возрасте от 1 до 5 лет не принимать пищу в течение 2-3 часов до исследования.
- Исключить из рациона жирную пищу в течение 24 часов до исследования.
- Не принимать пищу в течение 8 часов до исследования, можно пить чистую негазированную воду.

- Исключить физическое и эмоциональное перенапряжение в течение 30 минут до исследования.
- Не курить в течение 24 часов до исследования.
Общая информация об исследовании
К лабораторным маркерам рака легких относятся некоторые специфические вещества, определение которых позволяет предположить наличие злокачественного новообразования, степень его распространенности и оценить проводимое лечение. Это опухолевые маркеры, которые чаще всего являются сложными белками или пептидами, гликопротеинами. Они синтезируются опухолевыми клетками или окружающими опухоль нормальными клетками в повышенных концентрациях.
Раковый эмбриональный антиген (РЭА) является гликопротеином и относится к классу онкоэмбриональных маркеров. Преимущественно синтезируется в органах желудочно-кишечного тракта плода, а после рождения его уровень резко снижается. Он также обнаруживается в тканях органов пищеварения и у взрослых людей, но в значительно меньшем количестве. Определение уровня РЭА используется для диагностики ряда злокачественных опухолей. К ним относятся рак толстой и прямой кишки, поджелудочной железы, легкого, молочной железы. В большинстве случаев РЭА является показателем аденогенных опухолей, в частности аденокарциномы и крупноклеточного рака легкого. Его определение используется в составе комплексной диагностики для определения стадии заболевания, оценки эффективности лечения у больных с раком легкого с исходно повышенным уровнем РЭА, для мониторинга возможности развития рецидивов рака. Следует отметить, что концентрация РЭА увеличивается у 20-50 % больных с доброкачественными заболеваниями кишечника, поджелудочной железы, печени и легких, при пневмонии, бронхитах, туберкулезе, эмфиземе, муковисцидозе, а также при некоторых аутоиммунных заболеваниях. Показатель повышается при обострении болезни, но в случае улучшения самочувствия возвращается к норме. При злокачественном же процессе уровень РЭА неуклонно растет на протяжении всего периода заболевания.
Определение уровня РЭА используется для диагностики ряда злокачественных опухолей. К ним относятся рак толстой и прямой кишки, поджелудочной железы, легкого, молочной железы. В большинстве случаев РЭА является показателем аденогенных опухолей, в частности аденокарциномы и крупноклеточного рака легкого. Его определение используется в составе комплексной диагностики для определения стадии заболевания, оценки эффективности лечения у больных с раком легкого с исходно повышенным уровнем РЭА, для мониторинга возможности развития рецидивов рака. Следует отметить, что концентрация РЭА увеличивается у 20-50 % больных с доброкачественными заболеваниями кишечника, поджелудочной железы, печени и легких, при пневмонии, бронхитах, туберкулезе, эмфиземе, муковисцидозе, а также при некоторых аутоиммунных заболеваниях. Показатель повышается при обострении болезни, но в случае улучшения самочувствия возвращается к норме. При злокачественном же процессе уровень РЭА неуклонно растет на протяжении всего периода заболевания.
Антиген плоскоклеточной карциномы (SCCA) является гликопротеином с молекулярной массой 48 кДа и маркером плоскоклеточного рака. В норме небольшое количество антигена вырабатывается внутри клеток эпителия кожи, шейки матки, анального канала и не высвобождается во внеклеточное пространство. При плоскоклеточном раке отмечается увеличение секреции антигена опухолевыми клетками, что, возможно, играет роль в процессах инвазии и метастазирования карциномы. Повышение концентрации антигена может отмечаться при плоскоклеточном раке шейки матки, пищевода, легкого, влагалища. У больных плоскоклеточным раком легкого чувствительность показателя составляет 50-60 %, а специфичность около 80 %. Определение данного маркера может быть использовано для оценки эффективности лечения у больных с раком легкого с исходно повышенным уровнем SCCA и для мониторинга больных плоскоклеточным раком для доклинического выявления рецидивов заболевания. Показатель может быть повышен при некоторых доброкачественных заболеваниях кожи, при туберкулезе.
Нейронспецифическая энолаза (НСЕ/NSE) – это одна из структурных разновидностей фермента энолазы, участвующего в процессах гликолиза. У плода он обнаруживается в клетках нервной и легочной ткани, у взрослых людей – преимущественно в нейроэндокринных образованиях. Повышение NSE часто наблюдается при мелкоклеточном раке легкого, а также при медуллярном раке щитовидной железы, феохромоцитоме, нейроэндокринных опухолях кишечника и поджелудочной железы и нейробластоме. Мелкоклеточный рак легкого (МКРЛ) по сути является анапластическим процессом и обладает нейроэндокринными свойствами. Например, для этого вида рака характерна секреция адренокортикотропного гормона (АКТГ), антидиуретического гормона (АДГ), а также нейронспецифической энолазы. Другие виды рака легкого объединяются под общим названием немелкоклеточный рак легкого (НМРЛ). Эта группа заболеваний, в отличие от МКРЛ, не обладает нейроэндокринными свойствами, и для нее не характерна продукция избыточного количества NSE. Данный маркер обладает высокими показателями чувствительности (44-87 % в зависимости от стадии заболевания) и специфичностью для мелкоклеточного рака легкого.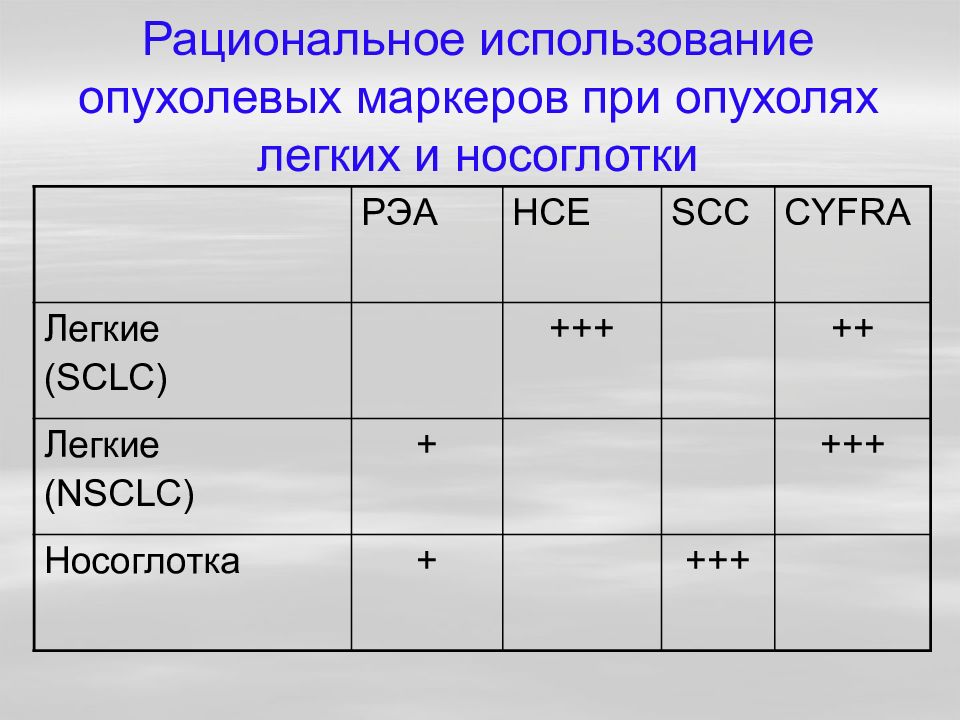 Его определение рекомендуется для дифференциальной диагностики опухолей легкого и для оценки эффективности лечения. Данный лабораторный показатель оказывается особенно полезным, когда рутинные методы диагностики не могут быть выполнены из-за тяжести заболевания или сопутствующей патологии.
Его определение рекомендуется для дифференциальной диагностики опухолей легкого и для оценки эффективности лечения. Данный лабораторный показатель оказывается особенно полезным, когда рутинные методы диагностики не могут быть выполнены из-за тяжести заболевания или сопутствующей патологии.
Раковый антиген СА 19-9 является высокомолекулярным гликопротеином, который в норме вырабатывается клетками эпителия желудочно-кишечного тракта. Его уровень повышается практически у всех пациентов с опухолями желудочно-кишечного тракта и особенно поджелудочной железы.
Раковый антиген СА 72-4 – это высокомолекулярный муциноподобный гликопротеин, который вырабатывается во многих тканях плода и в норме практически не обнаруживается у взрослого человека. Производство СА 72-4 увеличивается практически у всех пациентов со злокачественными опухолями железистого генеза, особенно при раке желудка, муцинозном раке яичников. Уровень представленных маркеров может быть повышен при опухолях иной локализации: колоректальном раке, раке легких, а также заболеваниях печени (гепатитах и циррозе), доброкачественных опухолях яичников, воспалительных заболеваниях желудочно-кишечного тракта. Они являются неспецифичными показателями и могут использоваться в качестве дополнительных маркеров злокачественных процессов в комплексной диагностике рака легких.
Они являются неспецифичными показателями и могут использоваться в качестве дополнительных маркеров злокачественных процессов в комплексной диагностике рака легких.
Для чего используется исследование?
- Для комплексной диагностики рака легкого;
- для дифференциальной диагностики форм рака легкого: плоскоклеточная карцинома, мелкоклеточный, немелкоклеточный рак легкого;
- для оценки стадии онкологического процесса;
- для оценки эффективности лечения (оперативного и консервативной терапии) у больных с раком легкого;
- для мониторинга возможности развития рецидивов рака легкого в процессе длительного наблюдения после завершения лечения.
Когда назначается исследование?
- При подозрении на злокачественное новообразование легких или иных локализаций и мониторинге состояния в процессе диагностированного заболевания.
Что означают результаты?
Референсные значения
Отдельно для каждого показателя, входящего в комплекс:
Причины повышения:
- рак легкого;
- рак другой локализации: рак толстой и прямой кишки, поджелудочной железы, молочной железы, рак шейки матки, влагалища, пищевода, нейробластома, феохромацитома;
- заболевания легких: пневмония, бронхит, туберкулез, эмфизем, муковисцидоз;
- заболевания печени: гепатит, цирроз, печеночная недостаточность;
- хроническая почечная недостаточность;
- панкреатит;
- аутоиммунные заболевания.

Причины понижения:
- хирургическое удаление злокачественной опухоли;
- успешная терапия онкологического заболевания;
- ремиссия доброкачественной опухоли.
Что может влиять на результат?
- Пол;
- возраст;
- наличие сопутствующей патологии;
- терапевтическое и хирургическое лечение.
Скачать пример результата
Важные замечания
- Отрицательный результат анализа не исключает наличия онкологического заболевания легких.
- Диагностика рака легкого является комплексной и основана на клинических проявлениях заболевания, результатах лабораторных и инструментальных исследований.
Кто назначает исследование?
Онколог, пульмонолог, терапевт, врач общей практики, хирург.
Литература
- Долгов В.В., Меньшиков В.В. Клиническая лабораторная диагностика: национальное руководство.
 – Т. I., Т. II – М. : ГЭОТАР-Медиа, 2012.
– Т. I., Т. II – М. : ГЭОТАР-Медиа, 2012. - Fauci, Braunwald, Kasper, Hauser, Longo, Jameson, Loscalzo Harrison’s principles of internal medicine, 17th edition, 2009.
- Jaume Trape et al. Increased plasma concentrations of tumour markers in the absence of neoplasia. Clin Chem Lab Med 2011;49(10):1605–1620.
- Chernecky C. C. Laboratory Tests and Diagnostic Procedures / С.С. Chernecky, В.J. Berger; 5th ed. – Saunder Elsevier, 2008.
- Hayat, M.A. Methods of Cancer Diagnosis, Therapy, and Prognosis. Springer Dewey, 2010.
Опухолевые маркеры: Рак легкого
В соответствии с основными гистологическими типами бронхогенного рака целесообразно использовать следующие ОМ:
| Мелкоклеточный рак лёгкого (МКРЛ): | |
|---|---|
| Гистологическая верификация | Основной маркер |
| Мелкоклеточный рак лёгкого (МКРЛ) | НСЕ и CYFRA21. 1 1 |
| Немелкоклеточный рак лёгкого (НМКРЛ): | |
| Плоскоклеточная карцинома | CYFRA21.1 |
| Крупноклеточная карцинома | CYFRA21.1 и РЭА |
| Неизвестная | CYFRA21.1, НСЕ и РЭА |
Диагноз. Хотя определение опухолевых маркеров не может заменить гистологические результаты, оно может быть очень полезным, когда невозможно установить окончательный диагноз с помощью биопсии (приблизительно в 20% случаев). Например, нахождение НСЕ в тканях и в сыворотке пациентов, у которых отсутствует гистологическое доказательство, может свидетельствовать в пользу МКРЛ. Аналогично этому, высокий сывороточный уровень CYFRA21.1 даёт основание подозревать НМКРЛ, и, в частности, плоскоклеточную карциному.
Прогноз. Сывороточные уровни CYFRA21.1, НСЕ и РЭА коррелируют с массой опухоли: высокие концентрации опухолевых маркеров отражают распространённую стадию заболевания и предвещают плохой прогноз. Скорость снижения уровня опухолевого маркера после операции может быть неким индикатором оставшейся опухолевой массы и эффективности терапии.
Скорость снижения уровня опухолевого маркера после операции может быть неким индикатором оставшейся опухолевой массы и эффективности терапии.
Мониторинг опухолевых маркеров, концентрация которых на момент диагностирования повышена, оказывается наиболее уместным для дальнейшего мониторинга. Так же, как и в случае других карцином, скорость снижения уровня соответствующего маркера после операции обеспечивает информацию относительно состояния пациента. Скорость снижения уровней маркеров после первичной операции является индикатором радикальности операции и показателем прогноза. Период полужизни составляет: для РЭА – 2-3 суток, для НСЕ – сутки, для CYFRA21/1 – несколько часов. Если концентрация опухолевых маркеров снижается медленнее и/или не достигает нормальных значений, это свидетельствует о наличии остаточной опухоли или некорректном стадировании (наличие скрытых метастазов, не идентифицированных на момент первичного стадирования).
Риск рецидива при раке лёгкого высок (70-90%), и опухолевые маркеры используют для выявления субклинического рецидива. Повышение опухолевых маркеров регистрируют за несколько месяцев до появления клинических симптомов. Выигрыш во времени может быть использован для проведения дополнительного обследования и начала терапии.
Повышение опухолевых маркеров регистрируют за несколько месяцев до появления клинических симптомов. Выигрыш во времени может быть использован для проведения дополнительного обследования и начала терапии.
Контроль эффективности терапии. Уровни опухолевых маркеров отражают ответ на химиотерапию. Если терапия эффективна, повышенные исходные уровни опухолевых маркеров снижается довольно быстро – в течение недели или к концу первого цикла химиотерапии. В противоположность этому, неэффективность терапии связана с устойчиво повышенным или транзиторно снижавшимся уровнем. Повышение уровней маркеров в целом показывает прогрессирование заболевания, часто за несколько недель или месяцев до того, как это станет возможным выявить с помощью существующих инструментальных методов. Будет ли раннее лечение, предпринятое единственно на основании повышения уровня маркеров, увеличивать выживаемость или улучшать качество жизни, пока неясно.
Значения CYFRA21.1 зависят от функции почек и могут повышаться при почечной недостаточности.
Онкомаркеры. Важный сигнал или деньги на ветер?
ПСА, СА125, СА242, СА15-5 и многие другие анализы известные как онкомаркеры. Насколько они точны и когда их стоит сдавать? Помогут ли они в раннем выявлении опухолей?
Что такое онкомаркеры?
Представим теоретическую ситуацию — врач дал направление на онкомаркеры, сейчас даже не будем выяснять, на какие именно: • Какие чувства испытывает пациент, получив такое направление и ожидая результата? • Какие эмоции вызовет цифра на бланке, если она окажется вне границ нормы? • Ужас, страх, отчаяние. А нужны ли они нам?
Давайте разберемся насколько точны онкомаркеры и когда нужно определять их уровень. Мы будем использовать данные только очень серьезных источников: статистические данные Всемирной Организации здравоохранения и международные рекомендации разработанные Национальной Академией Клинической Биохимии (NACB, США) и Европейской Группой по Изучению Опухолевых Маркеров (EGTM), конечно с адаптацией к Российской действительности.
Давайте разберемся с самого начала:
Онкомаркерами называют те или иные вещества, которые определяют в биологических жидкостях организма (чаще всего речь идет о сыворотке крови), так же онкомаркеры могут выявлять в экстрактах или парафиновых блоках тканей. Идеальный маркер должен обладать двумя характеристиками: • чувствительность — это процент положительных результатов у людей с опухолью • специфичность — это процент здоровых людей, у которых тест дает отрицательный результат
Идеальными были бы 100% чувствительность и 100% специфичность. При этом онкомаркер должен быть характерным для какого-то конкретного вида опухолей.
К сожалению, подобных маркеров еще не обнаружено, поэтому всегда сохраняется право на ошибку, как в сторону ложного диагноза, так и в сторону ложного спокойствия.
Важность диагностики опухолей
По данным Всемирной Организации Здравоохранения (ВОЗ) ежегодно 6 миллионов человек в мире умирает от злокачественных опухолей. И ежегодно выявляется более 10 миллионов новых случаев онкологических заболеваний. По прогнозам ВОЗ в ближайшие 20 лет ситуация будет только ухудшаться — смертность возрастет до 10 миллионов в год, в заболеваемость до 15 миллионов в год.
По прогнозам ВОЗ в ближайшие 20 лет ситуация будет только ухудшаться — смертность возрастет до 10 миллионов в год, в заболеваемость до 15 миллионов в год.
При этом до 40% случаев рака можно было избежать, сократив осознанные контакты с канцерогенами и 30% смертей можно предотвратить, выявляя опухоли на ранних этапах.
Какие онкомаркеры нам известны
Перечень известных онкомаркеров стремится к бесконечности. Большая часть из них очень специфичны и не известны врачам общей практики. Чаще всего врачей, которые не специализируются на ведении больных с онкопатологией, интересуют следующие:
- ПСА (простат-специфический антиген) — антиген характерный для ткани предстательной железы, его уровень в крови повышается как при злокачественных, так и при доброкачественных заболеваниях простаты. Кроме того уровень ПСА может быть повышен после травм, пальпации, механического раздражения железы или эякуляции накануне сдачи анализа.
- СА125 антиген, присутствующий в нормальной ткани эндометрия.
 Он проникает в кровоток только в случае повреждения природных барьеров. Его уровни в крови могут удваиваться во время менструации и при эндометриозе. Значительное повышение уровня СА125 происходит при раке яичников (в 80% случаев) и других органов женской половой системы, опухолях молочной и поджелудочной желез, прямой кишки, желудка легких и печени. Из доброкачественных заболеваний к повышению уровня этого маркера приводят воспалительные заболевания органов женской половой системы, гепатиты, циррозы и аутоиммунные заболевания.
Он проникает в кровоток только в случае повреждения природных барьеров. Его уровни в крови могут удваиваться во время менструации и при эндометриозе. Значительное повышение уровня СА125 происходит при раке яичников (в 80% случаев) и других органов женской половой системы, опухолях молочной и поджелудочной желез, прямой кишки, желудка легких и печени. Из доброкачественных заболеваний к повышению уровня этого маркера приводят воспалительные заболевания органов женской половой системы, гепатиты, циррозы и аутоиммунные заболевания. - СА15-3 антиген, наиболее характерный для опухолевых клеток из молочной железы, его уровень может увеличиваться и при злокачественных опухолях других локализаций (желудка, печени, поджелудочной железы и органов женской репродуктивной системы). Кроме того его уровень повышается при доброкачественных заболеваниях молочных желез и аутоиммунных процессах
- СА19-9 антиген, который вырабатывается клетками карциномы поджелудочной железы, реже опухолей желудка (второй по значимости маркёр этих опухолей), печени и молочной железы.
 Из доброкачественных заболеваний к повышению его уровня приводят гепатиты и цирроз, холецистит и муковисцидоз.
Из доброкачественных заболеваний к повышению его уровня приводят гепатиты и цирроз, холецистит и муковисцидоз. - СА242 это маркёр злокачественных опухолей желудочно-кишечного тракта, в основном повышается при опухолях поджелудочной железы, кишечника и желудка, но может быть повышен и при доброкачественных заболеваниях этих органов.
- СЕА (он же РЕА- раково-эмбриональный антиген) обнаруживается в некоторых тканях взрослых в очень малых количествах. При опухолевых процессах концентрация РЭА в крови значительно повышается. Рост концентрации этого маркера происходит при колоректальном раке, раке лёгкого, молочной или поджелудочной желез, метастазах злокачественных опухолей в печень, костную ткань, опухолях простаты и яичников. При этом повышение происходит и при доброкачественных заболеваниях кишечника, печени и легких, особенно у заядлых курильщиков.
А теперь, давайте узнаем, в каких случаях стоит проводить подобный анализ.
Самые распространенные опухоли.

Достаточно часто люди боятся рака в целом. Но провериться на все болезни нельзя, поэтому посмотрим статистику ВОЗ и узнаем, какие опухоли уносят больше всего жизней у жителей России.
Мужчины:
- Раки трахеи, бронхов и легких- 27,8%
- Опухоли желудка — 12,55
- Раки толстой и прямой кишки — 11,8 %
- Рак предстательной железы — 7,7%
- Опухоли слизистых рта и ротоглотки 5,0%
- 35,3% приходится на смерти от всех остальных видов опухолей
Женщины:
- Опухоли молочных желез — 17,8%
- Опухоли прямой и толстой кишки — 16,5%
- Опухоли желудка — 10,9%
- Раки трахеи, бронхов и легких — 6,8%
- Опухоли поджелудочной железы 5,9%
- 42,2% приходится на смерти от всех остальных видов опухолей
А теперь рассмотрим возможности использования онкомаркеров для выявления и лечения людей с этими опухолями.
Раки трахеи, бронхов и легких
Маркерами которые могут быть использованы для определения прогнозов при раке легкого считаются НСЕ, РЕА и CYFRA21. 1. НСЕ (нейрон-специфическая энолаза)-характерна только для одного вида этого рака-для мелкоклеточного. Для остальных видов рака легкого используются РЕА и CYFRA21.1. Ни один из этих маркеров не может быть использован для диагностики, так как специфичность их очень низка (другими словами выявляется достаточно много ложноположительных результатов при низкой чувствительности метода. Однако эти маркеры необходимы для оценки результатов лечения- при сравнении уровней их до начала терапии и в процессе лечения. Так же они могут применяться после хирургического лечения для выявления рецидива.
1. НСЕ (нейрон-специфическая энолаза)-характерна только для одного вида этого рака-для мелкоклеточного. Для остальных видов рака легкого используются РЕА и CYFRA21.1. Ни один из этих маркеров не может быть использован для диагностики, так как специфичность их очень низка (другими словами выявляется достаточно много ложноположительных результатов при низкой чувствительности метода. Однако эти маркеры необходимы для оценки результатов лечения- при сравнении уровней их до начала терапии и в процессе лечения. Так же они могут применяться после хирургического лечения для выявления рецидива.
Опухоли молочных желез
Опухоли молочной железы являются самой частой причиной смерти женщин от онкологических заболеваний. Особенностью этих опухолей являются хорошие результаты лечения на ранних стадиях, поэтому очень важно своевременное выявление. При раке молочной железы наибольшее значение имеют РЭА и СА15.3 . Доказано, что у женщинам, перенесших радикальное лечение, повышение СА15.3 практически всегда говорит о рецидиве болезни. Динамика уровней этого маркера в процессе лечения отражает эффективность выбранного метода терапии. Однако учитывая низкую специфичность СА15.3 не рекомендуется использовать его для скрининга рака молочной железы
Динамика уровней этого маркера в процессе лечения отражает эффективность выбранного метода терапии. Однако учитывая низкую специфичность СА15.3 не рекомендуется использовать его для скрининга рака молочной железы
Опухоли прямой и толстой кишки
Если колоректальный рак выявлен на ранней стадии, то 5-илетняя выживаемость после лечения достигает 90%, это очень хороший показатель в онкологии. Самым частым маркером этого вида опухолей является РЭА. Однако и здесь в рекомендациях экспертов мы видим картину схожую с предыдущими. Динамика РЭА может использоваться для выявления прогрессирования после проведенного лечения, особенно важен этот маркер для выявления прогрессирования после удаления метастазов из печени. Но его определение не используется для скрининга колоректального рака.
Опухоли предстательной железы
В России определение ПСА используется для скрининга рака предстательной железы при ежегодных диспансерных обследованиях мужчин старше 50 лет. В США и странах Европы так же рекомендовано определение этого маркера всем мужчинам старше 50 лет, а при отягощенной наследственности от 40-45 лет. Однако, полагаясь на результаты теста, необходимо учитывать несколько интересных фактов о данном маркере:
Однако, полагаясь на результаты теста, необходимо учитывать несколько интересных фактов о данном маркере:
- ПСА информативен только в сочетании с пальцевым ректальным исследованием
- При сдаче крови на анализ необходима соответствующая подготовка
- При оценке результата необходимо использовать возрастные нормы
- Мужчинам старше 75 лет подобный скрининг не назначается, так как лечение неклинических форм рака предстательной железы только ухудшает прогноз для жизни
- Данные исследований, опубликованные в 2011 году подтвердили, что раннее выявление рака предстательной железы благодаря скринингу в долгосрочной перспективе никак не повлияло на специфическую продолжительность жизни.
Поэтому даже такой специфичный и привычный маркер как ПСА сдает свои позиции в ранней диагностике.
Опухоли женской репродуктивной системы
Опухоли женской репродуктивной системы являются причиной примерно 10% смертей от злокачественных опухолей. Они не вошли в наш первоначальный список, так как в статистике ВОЗ они разделены по опухолям отдельных органов (опухоли эндометрия, шейки матки, яичников и т.д).
Они не вошли в наш первоначальный список, так как в статистике ВОЗ они разделены по опухолям отдельных органов (опухоли эндометрия, шейки матки, яичников и т.д).
Среди них, рак яичников уносит больше всего женских жизней. Для дифференциальной диагностики между доброкачественными и злокачественными процессами при выявлении патологических образований в малом тазу можно использовать СА125. Этот маркер используется для дальнейшего наблюдения за пролеченными пациентками, а его уровни в динамике для оценки эффективности терапии. Анализ СА125 не рекомендуется экспертами для скрининга у женщин без каких-либо жалоб. Однако это исследование следует проводить каждые 6 месяцев совместно с УЗИ органов малого таза у женщин с высокой наследственной предрасположенностью — при наличии мутаций в генах BRCA1 и BRCA2.
Когда онкомаркеры действительно необходимы
Определение большей части онкомаркеров имеет значение и должно быть использовано при наличии клинических проявления опухоли и ее инструментальном подтверждении для дифференциальной диагностики или мониторинга эффективности терапии.
В качестве скрининга анализ на онкомаркеры не стоит использовать. Однако это не говорит о том, что маркер не способствует раннему выявлению опухолей, а лишь о том, что подобное обследование не улучшает прогноз средней группы людей. При этом никто не сможет сказать, как оно повлияет на жизнь конкретного человека.
Крайне важно, чтобы любое обследование назначал врач, который владеет достаточными знаниями и может трактовать результат анализа во благо пациента. Это поможет не только сохранить здоровье, а также избежать стрессовых ситуаций и лишних материальных трат.
Раннее выявление опухолей способно спасти миллионы жизней. Где место онкомаркеров в этом процессе?
Комоза Валентин Александрович
врач онколог-хирург ГАУЗ БООД
Cyfra-21-1 (Фрагмент Цитокератина 19) — узнать цены на анализ и сдать в Москве
Метод определения
Хемилюминесцентный иммуноанализ на микрочастицах
Исследуемый материал
Сыворотка крови
Доступен выезд на дом
Маркёр немелкоклеточного рака лёгких.
Цитокератины – семейство структурных белков эпителиальных клеток, которые кодируются различными генами и экспрессируются различным образом в соответствии с типом эпителия. Их известно более 20. Молекулярная масса 30 000 Да.
В злокачественно изменённых клетках эпителия экспрессия присущих ему цитокератинов многократно повышается, и растворимые фрагменты поступают в кровь, лимфу и другие жидкости организма.
Их выявление используют для диагностики и мониторинга терапии некоторых видов эпителиальных опухолей с помощью тест-системы Cyfra 21-1. Она включает два вида моноклональных антител, позволяющих выявлять растворимый фрагмент цитокератина 19, который ассоциирован, главным образом, с плоскоклеточными опухолями.
Повышение концентрации Cyfra 21-1 наиболее характерно для немелкоклеточного рака лёгких (НМКРЛ, англ. — NSCLC). Но отсутствие органной или опухолевой специфичности данного маркёра не позволяет рекомендовать исследование Cyfra 21-1 в целях скрининга рака лёгких при отсутствии клинических проявлений или у людей с высоким риском онкологических заболеваний. Это исследование не заменяет клинические и гистологические методы исследования при первичной диагностике, хотя может быть полезно в тех случаях, когда постановка окончательного диагноза по биопсии в силу каких-либо причин невозможна.
Это исследование не заменяет клинические и гистологические методы исследования при первичной диагностике, хотя может быть полезно в тех случаях, когда постановка окончательного диагноза по биопсии в силу каких-либо причин невозможна.
Поскольку большинство злокачественных опухолей лёгкого гетерогенны по гистологической структуре, Европейской группой по онкомаркёрам (EGTM) рекомендовано использование при раке лёгкого 3 онкомаркёров, являющихся наиболее приемлемыми кандидатами для последующего мониторинга — нейроспецифическая энолаза (NSE, см. тест №209), Cyfra 21-1 и раковоэмбриональный антиген (РЭА, см. тест №141).
Гистологическое строение опухоли
| Гистологическое строение опухоли | Основной маркёр |
| Мелкоклеточная карцинома | NSE и Cyfra 21-1 |
| Немелкоклеточная карцинома (НМКРЛ): | |
| Аденокарцинома | Cyfra 21-1 и РЭА |
| Плоскоклеточная карцинома | Cyfra 21-1 |
| Крупноклеточная карцинома | Cyfra 21-1 и РЭА |
| Неизвестная | Cyfra 21-1, NSE и РЭА |
В большинстве случаев степень повышения концентрации Cyfra 21-1 в крови коррелирует со стадией заболевания, что может использоваться в прогностических целях. Однако, умеренное повышение уровня маркёра не исключает разные варианты вида опухоли и прогредиентное течение заболевания.
Однако, умеренное повышение уровня маркёра не исключает разные варианты вида опухоли и прогредиентное течение заболевания.
Повышенная концентрация Cyfra 21-1 на момент постановки диагноза позволяет использовать этот маркёр для последующего наблюдения. CYFRA 21-1, РЭА и CA-125 (в ИНВИТРО тест № 143) являются независимыми прогностическими факторами высокой важности при немелкоклеточном раке лёгких, а NSE — при мелкоклеточном раке лёгких.
Степень снижения концентрации маркёра после хирургической операции дает полезную информацию об эффективности терапии или резидуальной опухоли. Скорость снижения уровня маркёра после оперативного вмешательства соотносится с его периодом полувыведения из крови – временем, за которое концентрация вещества в крови, при отсутствии поступления, снижается вдвое (для CYFRA 21-1 – несколько часов). Медленное снижение или снижение, но не до уровня референсных значений, позволяет предположить сохранение остатков опухоли. При последующем наблюдении, рост концентрации маркёра может быть признаком рецидива.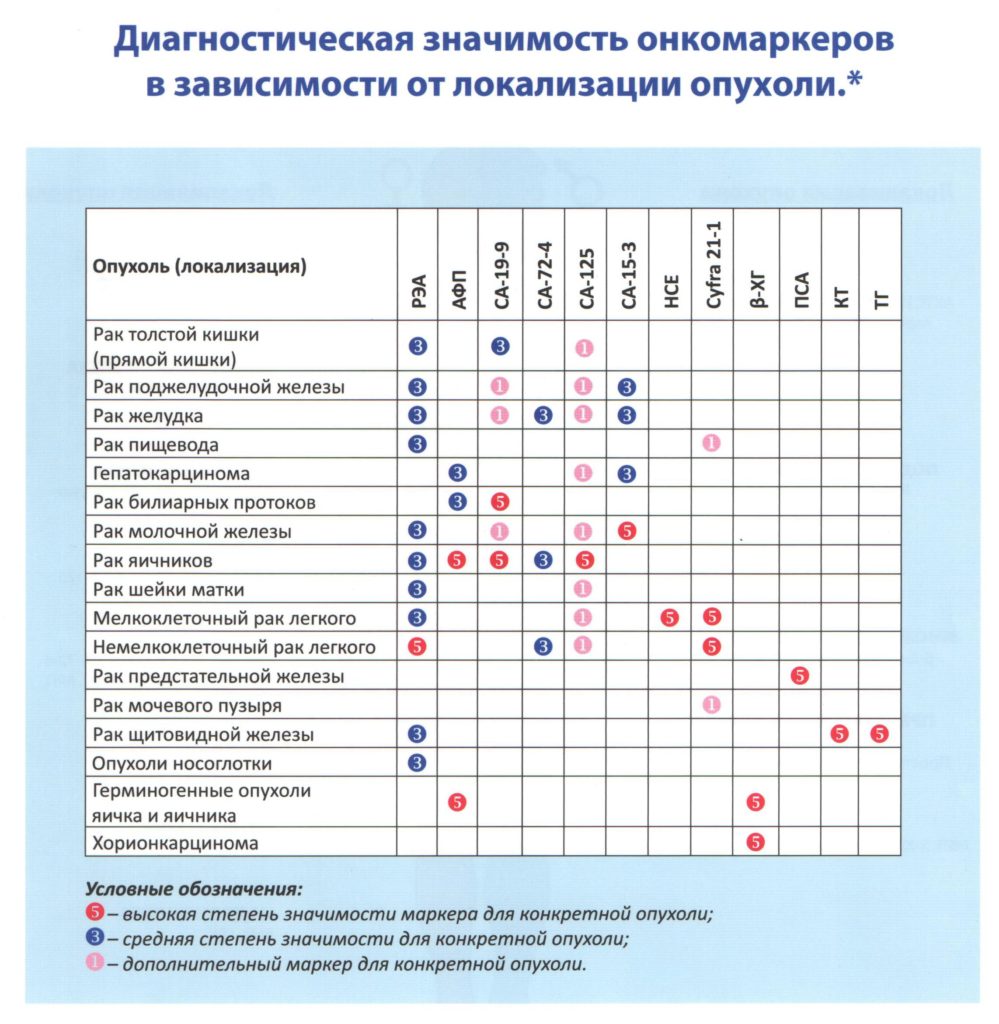 Такое увеличение может наблюдаться более чем за год до обнаружения признаков её роста по клиническим симптомам и использоваться как повод для более раннего использования рентгенологических методов обследования.
Такое увеличение может наблюдаться более чем за год до обнаружения признаков её роста по клиническим симптомам и использоваться как повод для более раннего использования рентгенологических методов обследования.
Показана целесообразность использования Cyfra 21-1 для мониторинга инвазивного рака мочевого пузыря. Клиническое значение этого маркёра при раке шейки матки, опухолях головы и шеи, раке пищевода и некоторых других плоскоклеточных карциномах продолжает исследоваться. Сывороточный уровень Cyfra 21-1 зависит от функции почек и может слабо увеличиваться при почечной недостаточности (до 10 мг/мл). Ложноположительные результаты могут наблюдаться у лиц с хроническими гепатитами и фиброзом лёгких. В группе курильщиков, по данным исследований, уровень маркёра не увеличен по сравнению с контролем. Беременность не влияет на результаты исследований.
Пределы определения: 0,50 нг/мл-10100 нг/мл
Литература
-
Шелепова В.
 М. Клиническое значение определения растворимого фрагмента цитокератина 19 — Cyfra 21-1. — Лаборатория, 2004, № 2, с. 3 — 6.
М. Клиническое значение определения растворимого фрагмента цитокератина 19 — Cyfra 21-1. — Лаборатория, 2004, № 2, с. 3 — 6. -
Vogl M., Muller M. Tumor Markers: Review and Clinical Application. (IFCC Series), 2002.
-
Wu A. Tietz clinical guide to laboratory tests. Saunders, 2006, p. 326 — 327.
-
-
Karnak D., Ulubay G., Kayacan O. et al.. Evaluation of Cyfra 21-1: a potential tumor marker for non-small cell lung carcinomas. — Lung, 2001, № 179(1), p. 57 — 65.
Диагностика рака легких в лаборатории СИНЭВО
Рак легких — самый страшный вид онкологических заболеваний, летальность от которого крайне высока. Ежегодно в мире от рака легких умирает 1,37 миллиона людей.
В 90% случаев развитие рака легких связано с курением. Табачный дым содержит более 3 000 химических составляющих, в том числе и опасных канцерогенов, которые провоцируют образование и рост раковых клеток.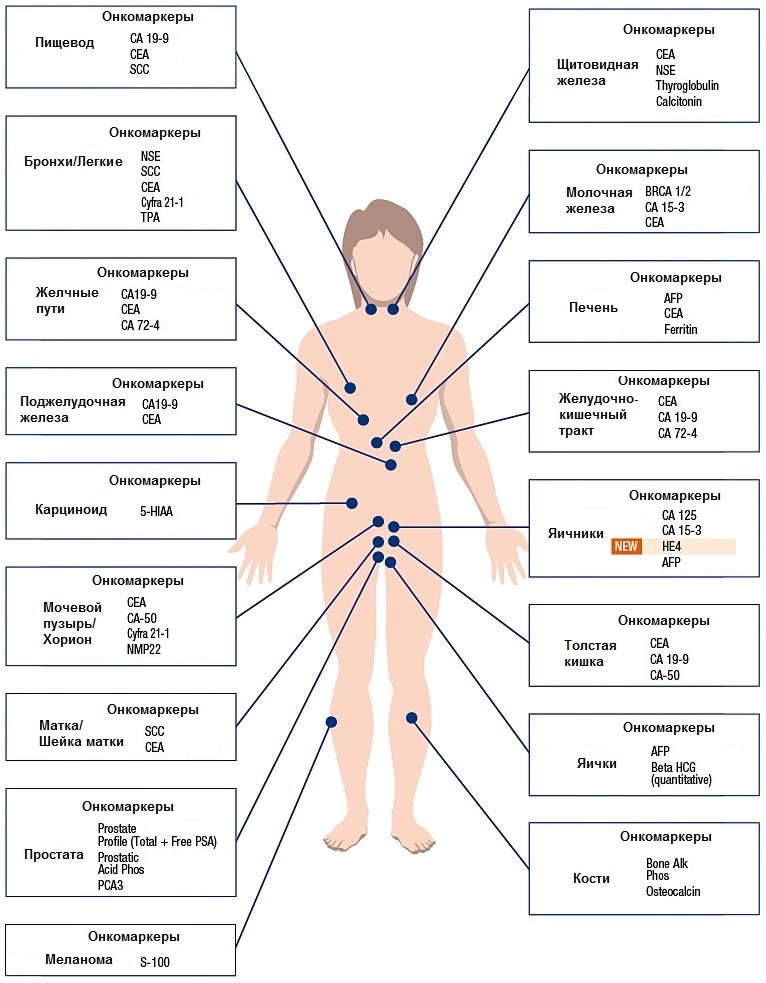 И чем дольше курит человек и чем больше выкуривает, тем выше вероятность развития онкологии. Люди, которые вдыхают табачный дым, пассивные курильщики, также подвержены опасности развития рака легких.
И чем дольше курит человек и чем больше выкуривает, тем выше вероятность развития онкологии. Люди, которые вдыхают табачный дым, пассивные курильщики, также подвержены опасности развития рака легких.
Причины развития
Риск возникновения рака легких увеличивается при определенных условиях труда: при контакте в работе с асбестом, радионуклидами, ураном, мышьяком, хромом и другими токсичными химическими веществами. Развитию заболевания способствует радиация и высокое загрязнение атмосферного воздуха: выхлопные газы от машин, заводов и электростанций. Хронические воспалительные процессы в бронхах предрасполагают развитие рака. Злоупотребление алкоголем, неправильное питание, физическая инертность увеличивает вероятность возникновения онкологического заболевания. Риск развития рака возрастает у людей, родственники которых перенесли рак легких.
Первоначально рак легких протекает незаметно, как правило, отсутствуют какие-либо симптомы заболевания. При прогрессировании заболевания появляются неспецифичные признаки: постоянный сухой или мокрый кашель с мокротой, хрипы в груди и одышка, выраженная слабость организма. Для рака легких характерна тупая боль в груди или спине, которая сохраняется длительное время и усиливается при глубоком дыхании. Наблюдается утолщение кончиков пальцев. Тревожными симптомами являются непроизвольная резкая потеря веса, частые простудные заболевания, а также бронхиты и пневмонии. На более поздних стадиях появляется боль в костях и в суставах, паралич частей лица, хрипота или изменение голоса, трудности при глотании. При появлении таких признаков необходимо срочно обратится к врачу.
Для рака легких характерна тупая боль в груди или спине, которая сохраняется длительное время и усиливается при глубоком дыхании. Наблюдается утолщение кончиков пальцев. Тревожными симптомами являются непроизвольная резкая потеря веса, частые простудные заболевания, а также бронхиты и пневмонии. На более поздних стадиях появляется боль в костях и в суставах, паралич частей лица, хрипота или изменение голоса, трудности при глотании. При появлении таких признаков необходимо срочно обратится к врачу.
Диагностика
Для диагностики рака легких назначают:
- рентгенографию грудной клетки или компьютерную томографию, которые позволяют выявить рак, определить особенность опухоли и ее распространенность;
- биопсию мокроты, которая позволяет диагностировать рак и определить его тип.
Анализы при раке легких
Дополнительно назначаются лабораторные исследования:
Помните, предотвратить рак легких легче, чем предотвратить возникновение любого другого типа онкологического заболевания. Достаточно отказаться от курения и вероятность заболеть раком значительно уменьшится. Дополнение рациона большим количеством фруктов и овощей, умеренность в потреблении алкогольных напитков, регулярные физические нагрузки снижают риск возникновения онкологических заболеваний.
Достаточно отказаться от курения и вероятность заболеть раком значительно уменьшится. Дополнение рациона большим количеством фруктов и овощей, умеренность в потреблении алкогольных напитков, регулярные физические нагрузки снижают риск возникновения онкологических заболеваний.
Сдать анализы рак легких можно в любом пункте Синэво в Минске, Гомеле, Бресте, Гродно, Витебске, Могилеве, Бобруйске, Барановичах, Солигорске, Слуцке, Полоцке, Новополоцке, Орше, Жлобине, Светлогорске, Молодечно, Лиде, Пинске, Борисове, Речице, Мозыре, Сморгони.
Сдать онкомаркеры | Ранняя диагностика рака
Что такое онкомаркеры?
Маркеры опухолевых клеток или онкомаркеры представляют собой вещества, часто белки, которые вырабатываются тканями собственно раковой опухоли или организмом в ответ на рост раковых клеток.
Совсем недавно были внедрены и другие типы онкологических маркеров, основанные на определениях изменений в генетическом материале (РНК, ДНК) пациентов, что существенно увеличивает точность при ранней диагностике рака.
Зачем нужны онкомаркеры?
Прежде всего, онкомаркеры или маркеры опухолевых клеток используются для своевременного обнаружения или диагностики раковых клеток. Используется так же при оценке эффективности лечения и назначения более действенной противораковой терапии, и соответственно отражает возможный прогноз или вероятный исход злокачественной онкологии.
Диагноз злокачественного онкологического заболевания не ставится только по результатам анализа на онкомаркеры. Для достоверной диагностики необходимо учесть много факторов и данные комплексного обследования, назначенного врачом-онкологом.
Какие онкомаркеры мы применяем?
Мы применяем большинство известных маркеров для ранней диагностики различных раковых заболеваний: печени, желудка, легких, молочных желез, матки, поджелудочной железы и т.д. А так же для диагностики возможности развития злокачественной онкологии плода при беременности, не используя инвазивные методы диагностики.
Онкомаркеры печени
Альфа-фетопротеин (AFP или АФП) используется в качестве маркера опухоли, чтобы помочь обнаружить и диагностировать раковые заболевания печени. Показан для пациентов с хроническими заболеваниями печени (цирроз, гепатиты В и С) из-за пожизненного риска развития злокачественной онкологии печени, особенно гепатоцеллюлярной карциномы. Помимо диагностики онкологии печени, используется при ранней диагностике опухолей яичников и яичек.
Антиген СА 19-9 (CA19-9) — повышен примерно у 65% больных с раком желчных протоков (холангиокарцинома), он может быть использован, для мониторинга лечения и ранней диагностики у людей с этим типом рака (в основном используется для диагностики рака поджелудочной железы).
Онкомаркеры молочной железы
Раковый антиген 15-3 (CA15-3), который представляет собой белок, вырабатываемый различными онкоклетками, в частности, клетками рака молочной железы. Так же увеличение уровня CA 15-3 встречается при эндометриозе, воспалительных заболеваниях органов таза и заболеваниях печени, показатель может увеличиваться и при беременности.
Так же увеличение уровня CA 15-3 встречается при эндометриозе, воспалительных заболеваниях органов таза и заболеваниях печени, показатель может увеличиваться и при беременности.
Онкомаркеры поджелудочной железы
Антиген СА 19-9 (СА19-9) — используется для ранней диагностики рака поджелудочной железы, а так же для оценки эффективности лечения этого заболевания.
Онкомаркеры яичников
Антиген СА 125 (СА125) — применяется для ранней диагностики рака яичников (эпителиального типа) и мониторинга эффективности лечения этого заболевания. Его увеличение может, встречается при воспалительных заболеваниях органов малого таза и беременности, поэтому обязательно проконсультируйтесь со специалистом на предмет целесообразности данного диагностического теста.
Раковый антиген СА 72-4 (СА72-4) — помимо ранней диагностики рака желудка и кишечника, предназначен для определения злокачественных новообразований яичников.
Опухолевый маркер НЕ 4 (HEP4) — относительно новый онкомаркерный тест для скрининга злокачественных опухолей яичников.
Прогностическая вероятность (значение ROMA) (включает определение антигена СА 125 и опухолевого маркера) — используется для определения вероятности развития рака яичников. Применяется в виде ROMA1 и ROMA2 в зависимости от наличия пост- и пременопаузы у женщин.
Онкомаркеры кишечника
Раковый антиген СА 242 (СА 242) — используется для ранней диагностики рака толстого кишечника и прямой кишки (колоректальной аденокарциномы).
Раковый антиген СА 72-4 (СА72-4) — также предназначен для диагностики колоректального рака. Его диагностическая чувствительность составляет почти 80%, что позволяет использовать его для скрининга этой онкопатологии.
Определение гемоглобина в кале количественным иммунохроматографическим методом (FOB Gold Test) — онкомаркер ранней диагностики и риска развития колоректального рака (рак прямой и ободочной кишки).
Онкомаркеры желудка
Раковый антиген СА 72-4 (СА72-4) — помимо диагностирования рака яичников и
кишечника, также предназначен для диагностики рака желудка. Имеет высокую диагностическую чувствительность при определении рецидивов этого заболевания.
Онкомаркеры кожи
Белок S-100 (S100 протеин) — используется в виде сыворотки соответствующего белка для определения злокачественной меланомы. Дополнительно используется в качестве скрининга пациентов с повреждениями головного мозга.
Онкомаркеры мочевыделительной системы
Бета-2-микроглобулин (B2M) — используется при диагностике онкологии почек. Чаще в виде анализа мочи. Дополнительно используется при определении онкологии лимфатической системы.
Специфический антиген рака мочевого пузыря (UBC) — используется в виде анализа мочи, для диагностики рака мочевого пузыря. Чувствительность при определении карциномы мочевого пузыря составляет почти 90%.
Чувствительность при определении карциномы мочевого пузыря составляет почти 90%.
Онкомаркеры матки
Антиген плоскоклеточной карциномы (SCCA или ТA4) — является определителем карциномы шейки матки. Помимо этого используется для определения раковых клеток при карциномах пищевода, легких, кожи и т.д.
записаться на процедуру
Онкомаркеры легких и бронхов
Нейрон-специфическая енолаза (NSE) — используется для определения ракового процесса в легких и является основным первичным диагностическим тестом при мелкоклеточном раке. Чувствительность данного теста составляет почти 82% при злокачественной онкологии бронхов. Дополнительно используется при диагностике нейробластомы, семиномы и АПУДомы.
Фрагмент цитокератина 19 (Cyfra 21-1) — диагностический тест для определения немелкоклеточного рака легких. В качестве дополнительного назначения используется при оценке эффективности онкотерапии при раке мочевого пузыря.
В качестве дополнительного назначения используется при оценке эффективности онкотерапии при раке мочевого пузыря.
Онкомаркеры простаты
Простатоспецифический антиген (ПСА) общий (TPSA) — используется для ранней диагностики карциномы простаты, а так же скрининг диагностики рака простаты мужчин старше 40 лет.
Простатоспецифический антиген (ПСА) свободный (FPSA) — используется для дифференциальной диагностики непосредственно рака простаты и доброкачественного увеличения предстательной железы.
Дополнительные онкомаркерные исследования
Исследование кала на трансферрин и гемоглобин — применяется при опредлении опухолевого процесса в печени и тонком кишечнике.
Раково-эмбриональный антиген (РЭА) — используется для ранней диагностики пациентов с диагнозом рак толстой кишки. Так же может быть использован в качестве онкомаркера для рака щитовидной железы, прямой кишки, легких, молочной железы, печени, поджелудочной железы, желудка, яичников.
Так же может быть использован в качестве онкомаркера для рака щитовидной железы, прямой кишки, легких, молочной железы, печени, поджелудочной железы, желудка, яичников.
Хромогранин А (CgА) — применяется для диагностики опухолей нейроэндокринного генеза. К ним относятся карциноидные опухоли, инсулиномы, мелкоклеточный рак легкого и нейробластомы.
Если Вы задумались, где пройти обследование для исключения онкопатологии и сдать кровь на онокмаркеры в Москве, обращайтесь в Клинический госпиталь на Яузе. У нас Вы пройдёте комплексную диагностику, получите консультацию компетентных специалистов и исключите все онкологические риски.
Почему мы
- Врачи. Специалисты нашего медицинского центра имеют высокую квалификацию и опыт работы, в том числе и в зарубежных клиниках.
- Все основные онкомаркеры У нас проводится широкий спектр исследований на онкомаркеры различных органов
- Экспертная диагностика.
 Современный диагностический комплекс госпиталя позволяет с высокой точностью проводить как скрининг, так и более углубленные исследования (лучевые, эндоскопические, генетические) для определения онкологических заболеваний.
Современный диагностический комплекс госпиталя позволяет с высокой точностью проводить как скрининг, так и более углубленные исследования (лучевые, эндоскопические, генетические) для определения онкологических заболеваний. - Генетическая лаборатория Наши генетики помогут подобрать метод генетической диагностики для выявления наследственной предрасположенности к раку молочной железы, яичников, органов желудочно-кишечного тракта, кожи, крови, почек, предстательной железы и многих других видов рака.
- Комплексность. Собственная высокотехнологичная лечебная база позволяет не только диагностировать, но и успешно лечить раковые патологии с применением химиотерапии (в т. ч. таргетными препаратами), хирургии любой сложности.
- Мы ценим ваше время. Все лечебно-диагностические отделения расположены в одном здании госпиталя, что экономит ваше время и силы.
Цены на услуги Вы можете посмотреть в прайсе или уточнить по телефону, указанному на сайте.
KDL. Онкомаркеры. Анализы и цены
Алергология. ImmunoCAP. Индивидуальные аллергены, IgE
Аллергокомпоненты ImmunoCAP
Аллергокомпоненты деревьев
Аллергокомпоненты животных и птиц
Аллергокомпоненты плесени
Аллергокомпоненты трав
Пищевые аллергокомпоненты
Аллергология. ImmunoCAP. Комплексные исследования IgE (результат по каждому аллергену)
Аллергология. ImmunoCAP. Панели аллергенов IgE, скрининг (результат СУММАРНЫЙ)
Аллергология. ImmunoCAP. Фадиатоп
Аллергология. Immulite. Индивидуальные аллергены
Аллергены гельминтов, IgE
Аллергены грибов (кандида и плесневых), IgE
Аллергены деревьев, IgE
Аллергены животных и птиц, IgE
Аллергены клещей домашней пыли, IgE
Аллергены лекарств и химических веществ, IgE
Аллергены насекомых, IgE
Аллергены пыли, IgE
Аллергены ткани, IgE
Аллергены трав, IgE
Бактериальные аллегены (стафилококк), IgE
Пищевые аллергены, IgE
Пищевые аллергены, IgG
Аллергология. Immulite. Комплексы аллергенов, IgE (результат по каждому аллргену)
Immulite. Комплексы аллергенов, IgE (результат по каждому аллргену)
Аллергология. Immulite. Панели аллергенов, скрининг (результат СУММАРНЫЙ)
Аллергены деревьев, IgE (панель)
Аллергены животных и птиц, IgE (панель)
Аллергены трав, IgE (панель)
Ингаляционные аллергены, IgE (панель)
Пищевые аллергены, IgE (панель)
Аллергология. Immulite. Панели пищевых аллергенов IgG (результат СУММАРНЫЙ)
Аллергология. ImmunoCAP. Индивидуальные аллергены, IgE
Аллергены деревьев, IgE
Аллергены животных и птиц, IgE
Аллергены пыли, IgE
Аллергены трав, IgE
Пищевые аллергены, IgE
Аллергология. RIDA. Комплексы аллергенов, IgE
Аллергология. RIDA. Комплексы аллергенов, IgE (результат по каждому аллргену)
Аллергология. Местные анестетики, IgE
Биохимические исследования крови
Диагностика анемий
Липидный обмен
Обмен белков
Обмен пигментов
Обмен углеводов
Специфические белки
Ферменты
Электролиты и микроэлементы
Биохимические исследования мочи
Разовая порция мочи
Суточная порция мочи
Витамины, аминокислоты, жирные кислоты
Гематология
Гемостаз (коагулограмма)
Генетические исследования
HLA-типирование
Исследование генетических полиморфизмов методом пиросеквенирования
Исследование генетических полиморфизмов методом ПЦР
Молекулярно-генетический анализ мужского бесплодия
Гистологические исследования
Гистологические исследования лаборатории UNIM
Гормоны биологических жидкостей
Гормоны гипофиза и гипофизарно-адреналовой системы
Гормоны крови
Гормоны гипофиза и гипофизарно-адреналовой системы
Маркеры остеопороза
Пренатальная диагностика
Ренин-альдостероновая система
Тесты репродукции
Функция органов пищеварения
Функция щитовидной железы
Гормоны мочи
Диагностика методом ПЦР
COVID-19
Андрофлор, иследование биоценоза (муж)
Вирус герпеса VI типа
Вирус Варицелла-Зостер (ветряной оспы)
Вирус герпеса VI типа
Вирус простого герпеса I, II типа
Вирус Эпштейна-Барр
Вирусы группы герпеса
Возбудитель туберкулеза
ВПЧ (вирус папилломы человека)
Грибы рода кандида
Листерии
Парвовирус
Респираторные инфекции
Стрептококки (вкл. S.agalactie)
S.agalactie)
Токсоплазма
Урогенитальные инфекции, ИППП
Урогенитальные инфекции, комплексные исследования
Урогенитальные инфекции, условные патогены
Фемофлор, исследование биоценоза (жен)
Флороценоз, иследование биоценоза (жен)
Цитомегаловирус
Диагностика методом ПЦР, кал
Кишечные инфекции
Диагностика методом ПЦР, клещ
Клещевые инфекции
Диагностика методом ПЦР, кровь.
Вирус Варицелла-Зостер (ветряной оспы)
Вирус герпеса VI типа
Вирус простого герпеса I, II типа
Вирус Эпштейна-Барр
ВИЧ
Возбудитель туберкулеза
Гепатит D
Гепатит G
Гепатит А
Гепатит В
Гепатит С
Листерии
Парвовирус
Токсоплазма
Цитомегаловирус
Жидкостная цитология
Изосерология
Иммуногистохимические исследования
Иммунологические исследования
Иммунограмма (клеточный иммунитет)
Интерфероновый статус, базовое исследование
Интерфероновый статус, чувствительность к препаратам
Оценка гуморального иммунитета
Специальные иммунологические исследования
Исследование абортуса
Исследование мочевого камня
Исследование парапротеинов. Скрининг и иммунофиксация
Скрининг и иммунофиксация
Исследования слюны
Исследования слюны
Комплексные исследования
Лекарственный мониторинг
Маркеры аутоиммунных заболеваний
Антифосфолипидный синдром (АФС)
Аутоиммунные заболевания легких и сердца
Аутоиммунные неврологические заболевания
Аутоиммунные поражения ЖКТ и целиакия
Аутоиммунные поражения печени
Аутоиммунные поражения почек и васкулиты
Аутоиммунные эндокринопатии и бесплодие
Диагностика артритов
Пузырные дерматозы
Системные ревматические заболевания
Эли-тесты
Микробиологические исследования (посевы)
Посев крови на стерильность
Посев на гемофильную палочку
Посев на грибы (Candida)
Посев на грибы (возбудители микозов кожи и ногтей)
Посев на дифтерию
Посев на микоплазмы и уреаплазмы
Посев на пиогенный стрептококк
Посев на стафилококк
Посевы кала
Посевы мочи
Посевы на микрофлору (конъюнктива)
Посевы на микрофлору (отделяемое)
Посевы на микрофлору (урогенитальный тракт женщины)
Посевы на микрофлору (урогенитальный тракт мужчины)
Посевы на микрофлору ЛОР-органы)
Ускоренные посевы с расширенной антибиотикограммой
Неинвазивная диагностика болезней печени
Программы неинвазивной диагностики болезней печени
Неинвазивный пренатальный ДНК-тест (НИПТ)
Неинвазивный пренатальный тест (пол/резус плода)
Общеклинические исследования
Исследование назального секрета
Исследование секрета простаты
Исследования кала
Исследования мочи
Исследования эякулята
Микроскопическое исследование биологических жидкостей
Микроскопия на наличие патогенных грибов и паразитов
Микроскопия отделяемого урогенитального тракта
Онкогематология
Иммунофенотипирование при лимфопролиферативных заболеваниях
Миелограмма
Молекулярная диагностика миелопролиферативных заболеваний
Цитохимические исследования клеток крови и костного мозга
Онкогенетика
Онкомаркеры
Пищевая непереносимость, IgG4
Полногеномные исследования и панели наследственных заболеваний
Пренатальный скрининг
Серологические маркеры инфекций
Аденовирус
Бруцеллез
Вирус HTLV
Вирус Варицелла-Зостер (ветряной оспы)
Вирус герпеса VI типа
Вирус Коксаки
Вирус кори
Вирус краснухи
Вирус эпидемического паротита
Вирус Эпштейна-Барр
Вирусы простого герпеса I и II типа
ВИЧ
Гепатит D
Гепатит А
Гепатит В
Гепатит Е
Гепатит С
Грибковые инфекции
Дифтерия
Кишечные инфекции
Клещевые инфекции
Коклюш и паракоклюш
Коронавирус
Менингококк
Паразитарные инвазии
Парвовирус
Респираторные инфекции
Сифилис
Столбняк
Токсоплазма
Туберкулез
Урогенитальные инфекции
Хеликобактер
Цитомегаловирус
Специализированные лабораторные исследования.
Дыхательный тест
Микробиоценоз по Осипову
Тяжелые металлы и микроэлементы
Тяжелые металлы и микроэлементы в волосах
Тяжелые металлы и микроэлементы в крови
Тяжелые металлы и микроэлементы в моче
Услуги
Выезд на дом
ЭКГ
Установление родства
Химико-токсикологические исследования
Хромосомный микроматричный анализ
Цитогенетические исследования
Цитологические исследования
Анализы крови и опухолевые маркеры при немелкоклеточном раке легкого
Информацию о важности тестирования биомаркеров и действенных генетических мутаций можно найти в этой недавней статье.
Когда мне поставили диагноз метастатическая аденокарцинома легкого, мой особый вид НМРЛ, это считалось довольно «ванильной» разновидностью рака легких. В моем образце ткани не было известных действенных мутаций, поэтому меня сразу же посадили на коктейль из карбоплатина, алимты и авастина.Начато лечение. Казалось, я справился с этим довольно хорошо. А потом почти сразу меня начали спрашивать о моих маркерах крови.
Казалось, я справился с этим довольно хорошо. А потом почти сразу меня начали спрашивать о моих маркерах крови.
Стоит ли искать маркеры крови?
Честно говоря, я понятия не имел, о чем они говорили. В ожидании своего первоначального диагноза я провел много исследований рака легких и не нашел ничего, что указывало бы на то, что мне следует искать маркеры крови. Обеспокоенные знакомые неоднократно спрашивали меня об уровне моего карциноэмбрионального антигена (РЭА).Это магическое число должно было сказать мне, работает ли мое лечение, очевидно, но я понятия не имел, какие у меня были числа CEA. Это меня беспокоило. 2
Вот меня лечил человек, которого считали одним из ведущих онкологов, специализирующихся на раке легких — конечно, он следил за этими цифрами. Но когда я спросил о них, он просто сказал, что у меня нет маркеров крови, которые бы нам что-то сказали. Так почему же так много людей спрашивали меня о них?
О повышении уровней КЭА
По правде говоря, маркеры крови очень полезны для прогнозирования или мониторинга некоторых типов рака, особенно рака поджелудочной железы или толстой кишки, и оказывается, что многие люди, спрашивающие меня о моих уровнях CEA, имели опыт лечения рака толстой кишки, где это число — более надежный показатель успеха лечения.
Поэтому через пару лет после начала лечения для меня стало неожиданностью, когда мой онколог выразил некоторую озабоченность по поводу повышения моего уровня РЭА. У меня создалось впечатление, что это бесполезные числа — в конце концов, он сам так сказал. Но это было во время другого лечения. Я прекратил химиотерапию и несколько месяцев принимал целевые препараты.
Признаки прогрессирования опухоли
Спустя какое-то время после биопсии и до того, как я показал прогрессирование опухоли во время химиотерапии, мутация в моей опухоли стала применимой.Мы знали, что это может произойти, или, по крайней мере, возможно, основываясь на быстрых темпах генетических исследований, проводимых в области рака. Как только мы подтвердили прогрессирование, мне сделали жидкую биопсию, а затем я начал нацеливаться на лучшую возможную мутацию, которая обнаружилась. Но был ряд признаков того, что целевой препарат не работал, в том числе внезапное повышение моих показателей CEA.
Оказывается, эти цифры относятся к НМРЛ, хотя и только в определенных случаях, хотя сами по себе они не могут быть полностью достоверными. Они не являются подходящими предикторами рака, поскольку повышенные уровни нескольких типов этих маркеров могут возникать у здоровых людей по разным причинам. И они были бесполезны для измерения успеха в течение моего начального периода лечения.
Они не являются подходящими предикторами рака, поскольку повышенные уровни нескольких типов этих маркеров могут возникать у здоровых людей по разным причинам. И они были бесполезны для измерения успеха в течение моего начального периода лечения.
Но они могут быть очень полезны для индикации рецидива рака после успешного лечения. Или, в моем случае, индикатор того, что моя опухоль продолжает прогрессировать при таргетной терапии. Внезапный всплеск этих чисел вызвал достаточно беспокойства, чтобы переоценить мое состояние и заставить меня отказаться от одного препарата и перейти на другой.
Маленький кусочек пазла
Само по себе число CEA было лишь небольшой частью диагностической головоломки, о которой я, возможно, больше не услышу во время моих регулярных наблюдений. И они могут быть полезны, а могут и не быть полезными для других пациентов с раком легких. На данный момент кажется, что только пациенты с несколькими действенными мутациями, вероятно, увидят какую-либо пользу от мониторинга этих уровней, и, возможно, только с ограниченным значением.
Тем не менее, сложный процесс лечения запущенного рака легких зависит от постоянно расширяющегося набора инструментов.Я рад, что там есть этот номер, даже если он почти не используется, и я никогда не ожидаю, что услышу его снова. И кто знает, может быть, в следующий раз, когда я буду искать новое лечение, меня познакомят с еще одним маркером или мутацией, о которых сегодня никто не знает.
Примечание редактора. Нам очень грустно сообщить, что 21 октября 2018 г. скончался Джеффри Пёльманн. Информационно-пропагандистские усилия и письма Джеффри продолжают доходить до многих. По нему будет очень не хватать.
В этой статье представлены мнения, мысли и опыт автора; ни один из этих материалов не был оплачен рекламодателями.Команда LungCancer.net не рекомендует и не поддерживает какие-либо продукты или методы лечения, обсуждаемые здесь. Узнайте больше о том, как мы поддерживаем редакционную честность здесь.
Маркеры опухоли крови могут предупреждать о прогрессировании рака легких — ScienceDaily
На протяжении многих лет онкологи знали, что рак может выделять сложные молекулы в кровь и что уровни этих молекул можно легко измерить. Эти так называемые «опухолевые маркеры» традиционно связаны с одним доминирующим типом рака, например, специфическим антигеном простаты (PSA), связанным с раком простаты, карциноэмбриональным антигеном (CEA) с колоректальным раком, CA125 с раком яичников, CA19.9 к раку поджелудочной железы и CA27.29 к раку груди. Однако настоящая проблема заключалась в том, чтобы определить практическое использование этих маркеров. Похоже, что они бесполезны в качестве средства скрининга здоровых людей на предмет наличия рака.
Эти так называемые «опухолевые маркеры» традиционно связаны с одним доминирующим типом рака, например, специфическим антигеном простаты (PSA), связанным с раком простаты, карциноэмбриональным антигеном (CEA) с колоректальным раком, CA125 с раком яичников, CA19.9 к раку поджелудочной железы и CA27.29 к раку груди. Однако настоящая проблема заключалась в том, чтобы определить практическое использование этих маркеров. Похоже, что они бесполезны в качестве средства скрининга здоровых людей на предмет наличия рака.
Теперь исследование онкологического центра Университета Колорадо начало дальнейшее определение потенциала этих маркеров, изучая тип рака, обычно не связанный с ними, — немелкоклеточный рак легкого (НМРЛ). Исследование предполагает, что эти опухолевые маркеры могут быть полезны не для выявления заболеваний, а для мониторинга терапевтических результатов у пациентов с уже установленным заболеванием.
«Если вы спросите некоторых онкологов, они могут сказать, что нет смысла проверять эти маркеры при раке легких, поскольку он не выражает их», — говорит Д. Росс Камидж, доктор медицинских наук, председатель Джойс Зефф по исследованию рака легких в Университете Онкологический центр Колорадо и директор отделения торакальной онкологии Медицинской школы CU. Однако, когда Камидж и его коллеги исследовали уровни четырех маркеров, классически связанных с другими видами рака, а именно CEA, CA125, CA19.9 и CA27.29, они обнаружили, что если бы все четыре были проверены, по крайней мере один из них был повышен в 95% случаев. распространенный немелкоклеточный рак легкого (НМРЛ).В некоторых случаях выражен только один маркер; другие выражали несколько маркеров вместе.
Росс Камидж, доктор медицинских наук, председатель Джойс Зефф по исследованию рака легких в Университете Онкологический центр Колорадо и директор отделения торакальной онкологии Медицинской школы CU. Однако, когда Камидж и его коллеги исследовали уровни четырех маркеров, классически связанных с другими видами рака, а именно CEA, CA125, CA19.9 и CA27.29, они обнаружили, что если бы все четыре были проверены, по крайней мере один из них был повышен в 95% случаев. распространенный немелкоклеточный рак легкого (НМРЛ).В некоторых случаях выражен только один маркер; другие выражали несколько маркеров вместе.
В последние годы для некоторых пациентов с распространенным НМРЛ стали возможны драматические противораковые реакции при целенаправленной терапии, применяемой против конкретных мутаций. Сосредоточив внимание на некоторых из наиболее ярких примеров НМРЛ с «онкогенной зависимостью», в частности, на случаях продвинутого EGFR, ALK или ROS1-положительного НМРЛ, получавших соответствующую таргетную терапию EGFR, ALK или ROS1, группа из Колорадо смогла изучить способность этих маркеров опухолей крови отражать как начальные терапевтические результаты, так и более позднее развитие устойчивости к лечению.
У 126 пациентов с онкогенно-зависимым раком легкого IV стадии опухолевые маркеры были зафиксированы до и после начала лечения.
Среди пациентов, получающих таргетное лечение, у 59 процентов пациентов отмечалось первоначальное повышение уровня маркеров в течение первых четырех недель терапии, при этом повышенные уровни позже падали ниже исходных значений в 58 процентах случаев.
«Эти данные означают, что вам не следует беспокоиться о повышении уровня маркеров в первые несколько недель таргетной терапии при отсутствии других доказательств, таких как ухудшение симптомов, поскольку в большинстве случаев все проходит.Возможно, онкомаркеры вообще не следует проверять в этот ранний период », — говорит Камидж.
Хотя опухолевые маркеры могут быть не очень полезными для прогнозирования начального успеха или неудачи, после того, как целевое лечение приносит пользу пациенту, увеличение опухолевых маркеров от их самой низкой точки может предоставить полезную информацию о развитии резистентности. Когда у пациента прогрессировал рак в организме, у 53% пациентов наблюдалось повышение уровня онкомаркеров крови на 10 и более процентов.Однако, если прогрессирование ограничивалось мозгом, онкомаркеры повышались только в 22 процентах случаев.
Когда у пациента прогрессировал рак в организме, у 53% пациентов наблюдалось повышение уровня онкомаркеров крови на 10 и более процентов.Однако, если прогрессирование ограничивалось мозгом, онкомаркеры повышались только в 22 процентах случаев.
«Ясно, что эти маркеры не заменяют рутинных обследований, направленных на выявление прогрессирования, особенно в мозге», — говорит Камидж. «Тем не менее, именно здесь, возможно, стоит оценить искусство медицины. Если маркеры растут, но компьютерная томография показывает, что все в порядке, возможно, эти данные должны подтолкнуть вас к более подробному сканированию — например, ПЭТ / Компьютерная томография. Или, если все лучшие снимки тела стабильны, возможно, рост онкомаркеров должен подтолкнуть вас к тому, чтобы провести сканирование мозга с большей тщательностью в поисках скрытого участка прогрессирования.«
Несмотря на то, что пациенты в этом ретроспективном исследовании прошли несколько различных типов сканирования и заборов крови с разной частотой, данные по-прежнему показывают, что повышение онкомаркеров при терапии может происходить задолго до рентгенологических изменений прогрессирования (до 84 дней). Хотя Камидж говорит, что для полной проверки способности этих маркеров действовать в качестве системы раннего предупреждения необходимо проспективное рандомизированное исследование, реальный вопрос может заключаться в том, имеет ли значение обнаружение прогрессирования на несколько месяцев раньше.
Хотя Камидж говорит, что для полной проверки способности этих маркеров действовать в качестве системы раннего предупреждения необходимо проспективное рандомизированное исследование, реальный вопрос может заключаться в том, имеет ли значение обнаружение прогрессирования на несколько месяцев раньше.
«Если адаптация вашего плана лечения на более раннем этапе прогрессирования по сравнению с более поздним не влияет на результаты, система раннего предупреждения могла бы просто дать каждому больше времени, чтобы подумать о вещах», — говорит он. Однако, особенно в отношении онкогенно-зависимого рака легких, в котором национальные руководящие принципы теперь поддерживают использование таких стратегий, как направленное облучение для контроля небольших очагов резистентного к лечению заболевания, Камидж оптимистично считает, что система раннего предупреждения о прогрессировании может быть очень полезной.
«Олигопрогрессивное состояние дает нам терапевтические возможности, которых у нас не было бы, если бы прогрессирование было более распространенным», — говорит он. «Развитие средств улавливания этой более ранней« стадии »развития у большего числа людей определенно требует дальнейшего изучения».
«Развитие средств улавливания этой более ранней« стадии »развития у большего числа людей определенно требует дальнейшего изучения».
Идентифицирован новый маркер для ранней диагностики рака легких — ScienceDaily
Белок, называемый изоцитратдегидрогеназа (IDh2), присутствует в больших количествах при раке легких и может быть обнаружен в крови, что делает его неинвазивным диагностическим маркером рака легких, согласно к исследованию, опубликованному в Clinical Cancer Research , журнале Американской ассоциации исследований рака.
«Это исследование является первым, в котором сообщается об идентификации IDh2 как нового биомаркера для диагностики немелкоклеточного рака легких (НМРЛ) с использованием большого количества клинических образцов», — сказал Джи Хе, доктор медицины, доктор философии, директор. лаборатории торакальной хирургии при Пекинском медицинском колледже и Китайской академии медицинских наук в Пекине. «Рак легкого имеет высокий уровень смертности, в основном из-за поздней диагностики. С увеличением старения населения мы, вероятно, увидим рост заболеваемости раком легких и потребность в улучшенных биомаркерах для ранней диагностики.Мы определили IDh2 как эффективный биомаркер плазмы с высокой чувствительностью и специфичностью при диагностике НМРЛ, особенно аденокарциномы легкого ».
С увеличением старения населения мы, вероятно, увидим рост заболеваемости раком легких и потребность в улучшенных биомаркерах для ранней диагностики.Мы определили IDh2 как эффективный биомаркер плазмы с высокой чувствительностью и специфичностью при диагностике НМРЛ, особенно аденокарциномы легкого ».
Рак легких — основная причина смерти от рака как у мужчин, так и у женщин в Соединенных Штатах и во всем мире. В настоящее время для обнаружения рака легких в крови используются определенные биомаркеры, включая CEA, Cyfra21-1 и CA125, но, по словам Хе, эти маркеры не очень чувствительны.
Он и его коллеги обнаружили, что IDh2 может быть обнаружен в крови больных раком легких с 76-процентной чувствительностью и 77-процентной специфичностью.Когда они использовали математическую модель, чтобы объединить обнаружение IDh2 с обнаружением существующих маркеров CEA, Cyfra21-1 и CA125, чувствительность увеличилась до 86 процентов.
«Исходя из имеющихся данных, IDh2 может использоваться для обнаружения рака легких 1 стадии; однако также возможно, что IDh2 может быть использован для обнаружения предрака, но необходимы дальнейшие исследования, чтобы рассмотреть эту возможность», — сказал он.
Он и его коллеги использовали образцы крови, взятые у 943 пациентов с НМРЛ и 479 здоровых людей из контрольной группы, зачисленных в период с 2007 по 2011 год в Институт рака и больницу Китайской академии медицинских наук.Ни у одного из участников исследования не было диагноза рака, и они не лечились от рака за три года до исследования. Используя методы под названием ELISA и ECL, они измерили уровни IDh2, CEA, Cyfra21-1 и CA125 в крови участников.
Затем исследователи разделили образцы на обучающий набор и тестовый набор для проверки эффективности обнаружения IDh2. Они обнаружили, что данные, полученные из тестового набора, были такими же хорошими, как и из обучающего набора, демонстрируя надежность IDh2 в качестве биомаркера для диагностики рака легких.
Средние уровни IDh2 у пациентов с двумя типами рака легких, аденокарциномой и плоскоклеточной карциномой, были в 2,7 раза и 2,2 раза выше, соответственно, по сравнению со здоровым контролем.
Исследователи также обнаружили, что объединение обнаружения всех четырех маркеров — IDh2, CEA, Cyfra21-1 и CA125 — помогло лучше классифицировать различные типы аденокарциномы по сравнению с обнаружением только с помощью IDh2.
Он и его коллеги планируют провести многоцентровое клиническое исследование для дальнейшей валидации IDh2.
«Наше исследование также предполагает, что IDh2 может участвовать в развитии рака легких и может быть хорошей мишенью для лечения НМРЛ», — сказал Хе. Его команда в настоящее время изучает молекулярные механизмы, которые увеличивают IDh2 у пациентов с раком легких, и его клинические последствия.
сывороточных опухолевых маркеров, используемых для мониторинга результатов лечения НМРЛ | Таргетированная онкология
D. Ross Camidge, MD, PhD
Согласно ретроспективному анализу, проведенному в одном центре, для мониторинга терапевтических результатов у пациентов с аденокарциномой легких IV стадии можно использовать четыре сывороточных маркера опухолей, которые обычно используются при других солидных опухолях.Изучаемые маркеры представляли собой карциноэмбриональный антиген (СЕА), СА125, СА19.9 и СА27.29. Эти маркеры традиционно связаны с колоректальным раком, раком яичников, поджелудочной железы и молочной железы, соответственно, и ранее подробно не исследовались при немелкоклеточном раке легкого (НМРЛ).
«Если вы спросите некоторых онкологов, они могут сказать, что нет смысла проверять эти маркеры при раке легких, потому что он не выражает их», — сказал ведущий автор Д. Росс Камидж, доктор медицинских наук, председатель кафедры легких Джойс Зефф. Исследования рака в Онкологическом центре Университета Колорадо и директор отделения торакальной онкологии Медицинской школы Университета Колорадо.
Однако, когда Камидж и его коллеги исследовали уровни этих маркеров, которые классически связаны с другими видами рака, они обнаружили, что если были проверены все 4 маркера, по крайней мере, один из них был повышен в 95% распространенных НМРЛ. В некоторых случаях экспрессируется только 1 маркер, тогда как в других выражается несколько маркеров.
В последние годы для некоторых пациентов с распространенным НМРЛ стали возможны драматические противоопухолевые реакции с использованием целенаправленной терапии против конкретных мутаций. Сосредоточив внимание на некоторых из наиболее ярких примеров НМРЛ с онкогенной зависимостью, а именно на случаях продвинутого EGFR, ALK или ROS1-положительного НМРЛ, получавших соответствующую таргетную терапию EGFR, ALK или ROS1, группа из Колорадо смогла изучить потенциал этих маркеров опухолей крови отражать как начальные терапевтические результаты, так и более позднее развитие устойчивости к лечению.
В ходе исследования 142 пациента были проанализированы на перестройки генов, EGFR (50), ALK (60), ROS1 (4) и KRAS (28). Они сообщили об отсутствии значимой разницы и частоты повышения между 4 маркерами (рисунок). Только CA27.29 достоверно отличался по онкогену (реже в KRAS) (P = 0,016). Camidge и его коллеги сообщили, что среднее время до надира у пациентов, получавших терапию ингибитором тирозинкиназы (TKI) в случаях EGFR и ALK, составляло 16,4 и 20 недель соответственно.
Интересно, что 24 из 41 (59%) пациентов с EGFR, ALK или ROS1 продемонстрировали первоначальное повышение уровней опухолевых маркеров в течение первых 4 недель терапии TKI, которое впоследствии упало ниже исходного уровня у 58% этих пациентов.Позже повышение уровня маркера ≥10% от надира наблюдалось в 53% случаев системного и 22% прогрессирования только центральной нервной системы.
«Эти данные означают, что вам не следует беспокоиться о повышении маркеров в первые несколько недель таргетной терапии при отсутствии других доказательств, таких как ухудшение симптомов, поскольку в большинстве случаев все проходит», — сказал Камидж. Кроме того, «если вы собираетесь использовать эти уровни маркеров, чтобы попытаться заранее определить, работает ли ваше лечение или нет, первые 4 недели — это просто шум.Это полезное наблюдение «.
Кроме того, «если вы собираетесь использовать эти уровни маркеров, чтобы попытаться заранее определить, работает ли ваше лечение или нет, первые 4 недели — это просто шум.Это полезное наблюдение «.
Искусство медицины Хотя опухолевые маркеры могут быть не очень полезными для прогнозирования первоначального успеха или неудачи, после того, как пациенту оказывается положительное влияние на целевое лечение, повышение опухолевых маркеров от их самой низкой точки может предоставить полезную информацию о развитии резистентности. Когда у пациента прогрессировал рак в организме, рост онкомаркеров крови на ≥10% наблюдался у 53% пациентов.
Однако в случаях прогрессирования головного мозга исследователи отметили, что опухолевые маркеры увеличиваются только в 22% случаев.«Маркер не имеет тенденции повышаться, если болезнь прогрессирует только в головном мозге, что является проблемой при раке легких, поскольку метастазы в головном мозге являются обычным явлением», — сказал Камидж. «И не у всех, кто прогрессирует в теле. Мы все еще пытаемся выяснить, какую степень изменения следует называть «прогрессией маркера». Мы использовали изменение на 10%, но это был только наш первый анализ. Проверка этих маркеров не заменяет сканирование, особенно сканирование мозга. Но когда вы их используете, это дополнительная информация, которая в опытных руках может дать вам время, чтобы побудить вас выполнить сканирование раньше или более детальное сканирование, если маркер поднимается, но первое сканирование предполагает, что все выглядит нормальный.Вот где следует ценить искусство медицины. Если маркеры растут, но компьютерная томография показывает, что все в порядке, возможно, эти данные должны подтолкнуть врача к более подробному сканированию — например, ПЭТ / КТ ».
Мы все еще пытаемся выяснить, какую степень изменения следует называть «прогрессией маркера». Мы использовали изменение на 10%, но это был только наш первый анализ. Проверка этих маркеров не заменяет сканирование, особенно сканирование мозга. Но когда вы их используете, это дополнительная информация, которая в опытных руках может дать вам время, чтобы побудить вас выполнить сканирование раньше или более детальное сканирование, если маркер поднимается, но первое сканирование предполагает, что все выглядит нормальный.Вот где следует ценить искусство медицины. Если маркеры растут, но компьютерная томография показывает, что все в порядке, возможно, эти данные должны подтолкнуть врача к более подробному сканированию — например, ПЭТ / КТ ».
Несмотря на то, что пациенты в этом ретроспективном исследовании прошли многократное сканирование и забор крови, данные все же показывают, что повышение опухолевых маркеров при терапии может происходить задолго до рентгенологических изменений прогрессирования (до 84 дней). Хотя Камидж говорит, что для полной проверки способности этих маркеров действовать в качестве системы раннего предупреждения необходимо проспективное рандомизированное исследование, реальный вопрос может заключаться в том, имеет ли значение обнаружение прогрессирования на несколько месяцев раньше.
Хотя Камидж говорит, что для полной проверки способности этих маркеров действовать в качестве системы раннего предупреждения необходимо проспективное рандомизированное исследование, реальный вопрос может заключаться в том, имеет ли значение обнаружение прогрессирования на несколько месяцев раньше.
Олигопрогрессивное заболевание С 2012 года исследователям известно, что рак легких можно описать как олигопрогрессивное заболевание, при котором высокоэффективная таргетная терапия может подавить рак и позволить только одному клону болезни прогрессировать. В этом состоянии «клиницисты могут быть гораздо более агрессивными в отношении использования местной терапии, такой как лучевая терапия, для уничтожения клона, но позволяя пациенту продолжать целевую терапию», — сказал Камидж.
Раннее обнаружение болезни может повлиять на решение врача о методе лечения, добавил он.«Если адаптация вашего плана лечения на более ранней стадии по сравнению с более поздней по мере прогрессирования не влияет на результаты, система раннего предупреждения может просто дать каждому больше времени для размышлений». Однако, особенно в отношении онкогенного рака легких, в котором национальные руководящие принципы теперь поддерживают использование таких стратегий, как направленное облучение для контроля небольших очагов резистентного к лечению заболевания, Камидж оптимистично считает, что система раннего предупреждения о прогрессировании может быть очень полезной.
Однако, особенно в отношении онкогенного рака легких, в котором национальные руководящие принципы теперь поддерживают использование таких стратегий, как направленное облучение для контроля небольших очагов резистентного к лечению заболевания, Камидж оптимистично считает, что система раннего предупреждения о прогрессировании может быть очень полезной.
«Олигопрогрессивное состояние дает нам терапевтические возможности, которых у нас не было бы, если бы прогрессирование было более распространенным», — говорит он.«Разработка методов, позволяющих уловить эту раннюю стадию развития у большего числа людей, безусловно, требует дальнейшего изучения».
Следующие шаги Камидж видит следующие шаги в исследовании, используя формализованное клиническое испытание для определения истинного потенциала опухолевых маркеров и их потенциала для получения преимущества во времени. «Это может привести к увеличению доли олигопрогрессивных заболеваний, и я думаю, что мне также хотелось бы видеть их в качестве потенциального маркера минимального остаточного заболевания после радикального лечения или маркера повторного пострадикального лечения.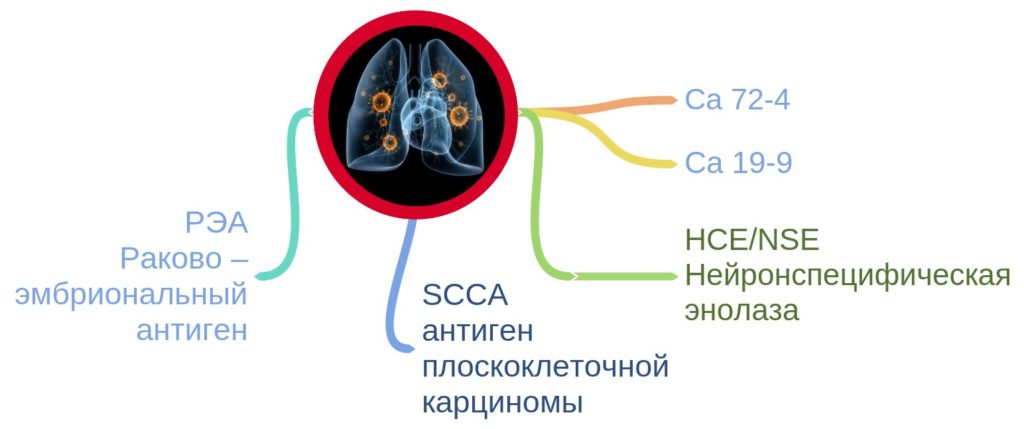
Эти маркеры существуют уже много лет, но «они не были полностью исследованы при раке легких», — сказал Камидж. «И они бесплатно доступны большинству практикующих онкологов через их биохимические лаборатории. Это возможность начать сбор данных «.
Ссылка :
Нунан С.А., Патил Т., Гао Д. и др. Краткий отчет: Исходные данные и характеристики лечения сывороточных онкомаркеров при аденокарциноме легкого с онкогенной зависимостью IV стадии [напечатано в Интернете 23 августа 2017 г.].J Thorac Oncol. pii: S1556-0864 (17) 30680-9. DOI: 10.1016 / j.jtho.2017.08.005.
Роль CEA, CYFRA21-1 и NSE в мониторинге ответа опухоли на ниволумаб у пациентов с запущенным немелкоклеточным раком легкого (НМРЛ) | Journal of Translational Medicine
Пациенты и характеристики опухолей
Семьдесят из 74 пациентов подлежали оценке на маркеры сыворотки и оценку ответа после 4 циклов ниволумаба (4 пациента были исключены из анализа гемолизированных исходных образцов). Три пациента прекратили прием ниволумаба из-за токсичности до первой оценки компьютерной томографии. Клинико-патологические характеристики представлены в таблице 1. Средний возраст составлял 70 лет (диапазон 44–85), 69% пациентов составляли мужчины. НМРЛ включал 54 аденокарциномы (77%), 15 плоскоклеточных карцином (22%) и один случай неустановленного типа (БДУ) (1%). Большинство пациентов были курильщиками (87%), имели метастазы (96%) и ECOG PS 0–1 (92%). Среднее количество предшествующих линий лечения составляло 2 (диапазон 1–6).Среднее значение сывороточных уровней трех маркеров на исходном уровне (до лечения) составляло 6,6 нг / мл для CEA (диапазон 0,8–2615), 5 нг / мл для CYFRA21-1 (диапазон 0,2–126,4) и 7,5 нг / мл. мл (диапазон 3,1–46,8) для NSE. Значения до лечения, превышающие верхний нормальный предел CEA, CYFRA 21-1 и NSE, были обнаружены у 40 (57%), 45 (64%) и 14 (20%) пациентов соответственно. Во 2-м и 3-м циклах данные по CEA были доступны для 59 и 54 пациентов соответственно, тогда как данные по CYFRA 21-1 были доступны для 57 и 54 пациентов, соответственно.
Три пациента прекратили прием ниволумаба из-за токсичности до первой оценки компьютерной томографии. Клинико-патологические характеристики представлены в таблице 1. Средний возраст составлял 70 лет (диапазон 44–85), 69% пациентов составляли мужчины. НМРЛ включал 54 аденокарциномы (77%), 15 плоскоклеточных карцином (22%) и один случай неустановленного типа (БДУ) (1%). Большинство пациентов были курильщиками (87%), имели метастазы (96%) и ECOG PS 0–1 (92%). Среднее количество предшествующих линий лечения составляло 2 (диапазон 1–6).Среднее значение сывороточных уровней трех маркеров на исходном уровне (до лечения) составляло 6,6 нг / мл для CEA (диапазон 0,8–2615), 5 нг / мл для CYFRA21-1 (диапазон 0,2–126,4) и 7,5 нг / мл. мл (диапазон 3,1–46,8) для NSE. Значения до лечения, превышающие верхний нормальный предел CEA, CYFRA 21-1 и NSE, были обнаружены у 40 (57%), 45 (64%) и 14 (20%) пациентов соответственно. Во 2-м и 3-м циклах данные по CEA были доступны для 59 и 54 пациентов соответственно, тогда как данные по CYFRA 21-1 были доступны для 57 и 54 пациентов, соответственно.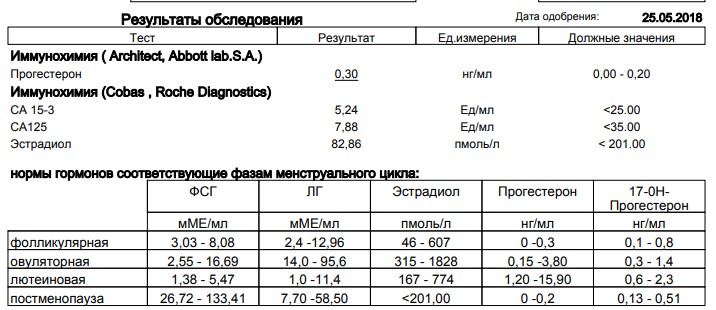 В то же время балльные данные по NSE были доступны для 58 и 50 пациентов соответственно.
В то же время балльные данные по NSE были доступны для 58 и 50 пациентов соответственно.
Таблица 1 Клинико-патологические характеристики
Корреляция между уровнями сывороточных маркеров, клинико-патологическими особенностями и ответом опухоли
Не было обнаружено значительной корреляции между исходными уровнями маркеров в сыворотке крови и возрастом или полом. Аномальные исходные уровни СЕА были обнаружены у курильщиков (p = 0,048) и аденокарцином (p <0,001). Аномальные, но не значимые, исходные уровни CYFRA21-1 были обнаружены в плоскоклеточных опухолях.Не было обнаружено связи между исходным уровнем NSE и характеристиками пациента и рака (данные не показаны). В среднем пациенты получали 6 циклов ниволумаба (диапазон от 1 до 36), а первая оценка компьютерной томографии проводилась в среднем через 6,9 недель, что соответствует 4 циклам ниволумаба. В целом контроль заболевания был достигнут у 24/67 пациентов (35,8%, 4 PR и 20 SD). Возраст, пол, гистология, стадия, состояние здоровья по шкале ECOG, привычка к курению и исходные уровни сыворотки не коррелировали с ответом на ниволумаб (данные не показаны). После 4 курсов ниволумаба медианные уровни CEA и NSE оставались довольно стабильными по сравнению с исходным уровнем (5,1 нг / мл и 7,4 нг / мл соответственно), в то время как медианные уровни CYFRA 21-1 упали до 2,7 нг / мл. Интересно, что у тех пациентов, которые получили DCR, мы наблюдали снижение всех трех сывороточных маркеров со значительной разницей между респондентами и не отвечающими (Таблица 2). В целом снижение CEA, CYFRA 21-1 и NSE ≥ 20% произошло у 13/49 (26%), 17/50 (34%) и 16/44 (36%) пациентов, соответственно, а также у CEA и CYFRA 21- 1 снижение было связано с благоприятным DCR (таблица 3).С RECIST снижение ≥ 20% CEA было достигнуто у 43,5% респондеров и у 11,5% не ответивших (p = 0,021), в то время как снижение CYFRA21-1 на ≥ 20% произошло у 62,5% респондеров и у 7,7%. % не ответивших (p <0,001). Интересно, что мы наблюдали, что ответ опухоли произошел у 87,5% пациентов с уменьшением CYFRA21-1 ≥ 20%, уже представленным после 1-го цикла (p = 0,008), и у 80% пациентов со снижением CEA ≥ 20%, уже представленным после 2-й цикл (р = 0,033) (данные не показаны).
После 4 курсов ниволумаба медианные уровни CEA и NSE оставались довольно стабильными по сравнению с исходным уровнем (5,1 нг / мл и 7,4 нг / мл соответственно), в то время как медианные уровни CYFRA 21-1 упали до 2,7 нг / мл. Интересно, что у тех пациентов, которые получили DCR, мы наблюдали снижение всех трех сывороточных маркеров со значительной разницей между респондентами и не отвечающими (Таблица 2). В целом снижение CEA, CYFRA 21-1 и NSE ≥ 20% произошло у 13/49 (26%), 17/50 (34%) и 16/44 (36%) пациентов, соответственно, а также у CEA и CYFRA 21- 1 снижение было связано с благоприятным DCR (таблица 3).С RECIST снижение ≥ 20% CEA было достигнуто у 43,5% респондеров и у 11,5% не ответивших (p = 0,021), в то время как снижение CYFRA21-1 на ≥ 20% произошло у 62,5% респондеров и у 7,7%. % не ответивших (p <0,001). Интересно, что мы наблюдали, что ответ опухоли произошел у 87,5% пациентов с уменьшением CYFRA21-1 ≥ 20%, уже представленным после 1-го цикла (p = 0,008), и у 80% пациентов со снижением CEA ≥ 20%, уже представленным после 2-й цикл (р = 0,033) (данные не показаны).
Таблица 2 Вариации CEA, CYFRA 21-1 и NSE в зависимости от ответа на ниволумаб
Таблица 3 Снижение маркеров ≥ 20% по сравнению с исходным уровнем и ответ опухоли (R)
Многофакторный анализ, включающий переменные для возраста, пола, снижения CEA и CYFRA ≥ 20%, показал, что снижение CYFRA21-1 ≥ 20% было независимым положительным прогностическим фактором для DCR (HR 4,36, 95% ДИ 1,7–11,3, p = 0,002 ) (Таблица 4). Интересно, что мы заметили, что уменьшение ≥ 20% онкомаркеров было очевидным уже в начале терапии.В частности, снижение по крайней мере на 20% уже было очевидным после 1-го, 2-го и 3-го цикла у 5%, 20% и 28% пациентов с CEA, у 15%, 37% и 39% пациентов с CYFRA21- 1 и у 26%, 22% и 34% пациентов с NSE, соответственно (данные не показаны). Наконец, анализируя опухолевые маркеры на основе гистотипа, мы наблюдали, что пациенты с аденокарциномой достигли DCR, когда снижение CEA и CYFRA21-1 было ≥ 20%, со значительной разницей в ответе по сравнению с пациентами со снижением маркера <20% (CEA , 77% против 40%, p = 0. 043; CYFRA21-1, 92% против 35%, p = 0,001). Среди пациентов с плоскоклеточной карциномой мы наблюдали снижение ≥20% для CYFRA21-1 и NSE, но только снижение CYFRA21-1 приводило к DCR (p = 0,033). В обоих гистологических типах снижение уровня NSE ≥ 20% не было значимо связано с DCR (данные не показаны).
043; CYFRA21-1, 92% против 35%, p = 0,001). Среди пациентов с плоскоклеточной карциномой мы наблюдали снижение ≥20% для CYFRA21-1 и NSE, но только снижение CYFRA21-1 приводило к DCR (p = 0,033). В обоих гистологических типах снижение уровня NSE ≥ 20% не было значимо связано с DCR (данные не показаны).
Таблица 4 Способность CEA и CYFRA 21-1 прогнозировать DCR (CR + PR + SD) в многомерном анализе
Связь между CEA, CYFRA 21-1, NSE и PFS
В целом, медиана PFS у 67 пациентов составила 1.9 месяцев (95% ДИ 1,7–2,2 месяца). Возраст, пол, гистология, PS, курение, предыдущее лечение и исходные уровни маркеров сыворотки не были связаны с PFS. Напротив, более длительная ВБП наблюдалась у пациентов с нормальными исходными значениями CEA (2,7 месяца против 1,7 месяца, p = 0,026) и со снижением CEA и CYFRA21-1 на ≥20% после 4 циклов ниволумаба (CEA: 7,1 против 1,9 месяцев. , p = 0,028; CYFRA21-1: 7,9 против 1,9 месяца, p <0,001). Не было обнаружено значимой связи между снижением NSE ≥ 20% и ВБП (4.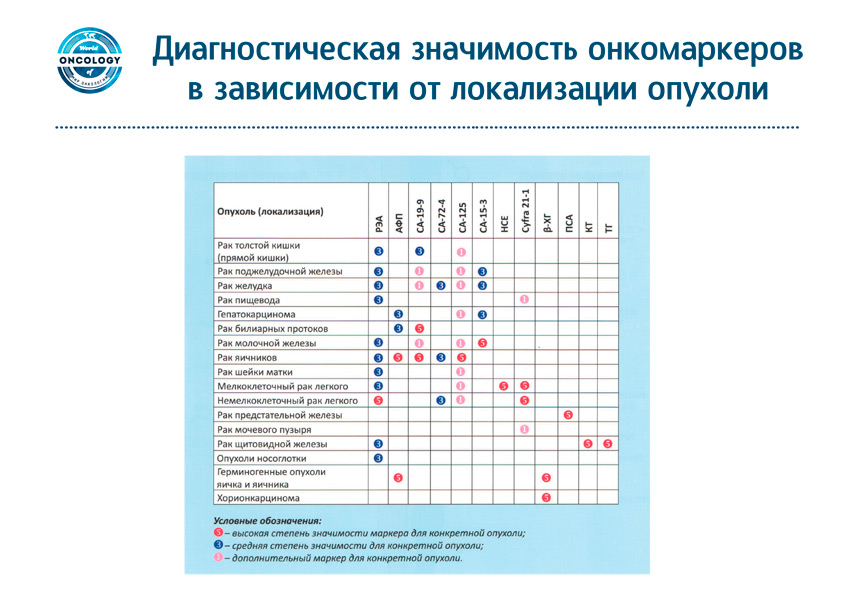 7 против 1,9 месяцев, p = 0,300) (рис.1). Многофакторный анализ, включающий термины для пола, возраста, CEA, CYFRA21-1 и снижение NSE ≥ 20%, подтвердил положительную прогностическую роль только для снижения CYFRA21-1 ≥ 20% (HR = 0,35, 95% ДИ 0,20–0,60, p <0,001) (данные не показаны). Что касается гистологии, снижение маркера улучшило ВБП у пациентов с аденокарциномой (CEA, 7,1 против 1,9 месяца, p = 0,013; CYFRA21-1, 7,9 против 1,9 месяца, p <0,001; NSE, 5,9 против 1,9 месяца, p = 0,067), тогда как у пациентов с ВБП при плоскоклеточной карциноме улучшилось только у пациентов со снижением CYFRA21-1 ≥ 20% (6.1 против 1,7 месяца, p = 0,032).
7 против 1,9 месяцев, p = 0,300) (рис.1). Многофакторный анализ, включающий термины для пола, возраста, CEA, CYFRA21-1 и снижение NSE ≥ 20%, подтвердил положительную прогностическую роль только для снижения CYFRA21-1 ≥ 20% (HR = 0,35, 95% ДИ 0,20–0,60, p <0,001) (данные не показаны). Что касается гистологии, снижение маркера улучшило ВБП у пациентов с аденокарциномой (CEA, 7,1 против 1,9 месяца, p = 0,013; CYFRA21-1, 7,9 против 1,9 месяца, p <0,001; NSE, 5,9 против 1,9 месяца, p = 0,067), тогда как у пациентов с ВБП при плоскоклеточной карциноме улучшилось только у пациентов со снижением CYFRA21-1 ≥ 20% (6.1 против 1,7 месяца, p = 0,032).
Рис.1
Выживаемость без прогрессирования согласно CEA, CYFRA21-1 и NSE Снижение ≥ 20%
Связь между CEA, CYFRA 21-1, NSE и OS
Для всей исследуемой популяции медиана последующего наблюдения составила 10,7 месяца (диапазон 5,0–16,8) для подвергнутых цензуре пациентов и 3,1 месяца (диапазон 0,1–13,2) для умерших пациентов. Связь между клинико-патологическими характеристиками и маркерами сыворотки крови с OS показана в таблице 5. Среднее время выживания составляло 9.2 месяца (95% ДИ 5,3–13,2). За исследуемый период умерло 40 пациентов (57,1%). В однофакторном анализе статистически значимый прогностический эффект был обнаружен для ряда предшествующих линий лечения (n = 1, 6,1 месяца, 95% ДИ = 3,6–8,5; n ≥ 2, 12,2 месяца, 95% ДИ = 8,2–13,3, p = 0,036) и ответа на терапию (13,5 месяцев для респондентов против 6,4 месяца для пациентов, не ответивших, p <0,001). Исходно нормальные уровни маркеров были достоверно связаны с лучшей общей выживаемостью: 12,1 месяца для CEA <5 нг / мл против 5.6 месяцев для CEA ≥ 5 нг / мл, p = 0,035; 13,2 месяца для CYFRA21-1 <3,3 нг / мл против 5,6 месяца для CYFRA21-1 ≥ 3,3 нг / мл, p = 0,005 и 10,0 месяца для NSE <13,4 нг / мл против 2,2 месяца для NSE ≥ 13,4 нг / мл, p = 0,028.
Связь между клинико-патологическими характеристиками и маркерами сыворотки крови с OS показана в таблице 5. Среднее время выживания составляло 9.2 месяца (95% ДИ 5,3–13,2). За исследуемый период умерло 40 пациентов (57,1%). В однофакторном анализе статистически значимый прогностический эффект был обнаружен для ряда предшествующих линий лечения (n = 1, 6,1 месяца, 95% ДИ = 3,6–8,5; n ≥ 2, 12,2 месяца, 95% ДИ = 8,2–13,3, p = 0,036) и ответа на терапию (13,5 месяцев для респондентов против 6,4 месяца для пациентов, не ответивших, p <0,001). Исходно нормальные уровни маркеров были достоверно связаны с лучшей общей выживаемостью: 12,1 месяца для CEA <5 нг / мл против 5.6 месяцев для CEA ≥ 5 нг / мл, p = 0,035; 13,2 месяца для CYFRA21-1 <3,3 нг / мл против 5,6 месяца для CYFRA21-1 ≥ 3,3 нг / мл, p = 0,005 и 10,0 месяца для NSE <13,4 нг / мл против 2,2 месяца для NSE ≥ 13,4 нг / мл, p = 0,028.
Таблица 5 ОС по клиникофатологическим характеристикам
Кроме того, также снижение ≥20% CEA или CYFRA21-1 после 4 циклов ниволумаба представляет собой положительный прогностический фактор (таблица 6). В частности, кривые выживаемости Каплана-Мейера показали, что пациенты со снижением CEA или CYFRA21-1 ≥ 20% выживали дольше, чем пациенты без снижения маркера (15 месяцев против 9.9 месяцев, p = 0,026 и 14,6 месяцев против 10 месяцев, p = 0,019 соответственно) (рис. 2). Многофакторный анализ, учитывающий пол, возраст, предыдущие направления терапии и исходные уровни CEA, CYFRA21-1 и NSE, показал лучший прогноз для пациентов с большим количеством терапий (≥ 2 строк: HR = 0,67, 95% ДИ 0,48–0,94 , p = 0,022) и с нормальным исходным уровнем CEA или CYFRA21-1 (CEA ≤ 5 нг / мл: HR = 0,70, 95% ДИ 0,49–1,01, p = 0,057; CYFRA21-1 ≤ 3,3 нг / мл: HR = 0,68. , 95% ДИ 0,46–1,01, p = 0,055). Многофакторный анализ, учитывающий снижение CEA и CYFRA21-1 на ≥ 20%, не показал статистически значимых результатов, но имел тенденцию к лучшему прогнозу для пациентов со снижением CYFRA21-1 ≥ 20% (HR = 0.55, 95% ДИ 0,28–1,07, p = 0,079) (данные не показаны). Наконец, что касается гистологических подтипов, не наблюдалось значительной разницы в OS между пациентами с аденокарциномой и плоскоклеточной карциномой (медиана OS 9,2 против 9,8 месяцев).
В частности, кривые выживаемости Каплана-Мейера показали, что пациенты со снижением CEA или CYFRA21-1 ≥ 20% выживали дольше, чем пациенты без снижения маркера (15 месяцев против 9.9 месяцев, p = 0,026 и 14,6 месяцев против 10 месяцев, p = 0,019 соответственно) (рис. 2). Многофакторный анализ, учитывающий пол, возраст, предыдущие направления терапии и исходные уровни CEA, CYFRA21-1 и NSE, показал лучший прогноз для пациентов с большим количеством терапий (≥ 2 строк: HR = 0,67, 95% ДИ 0,48–0,94 , p = 0,022) и с нормальным исходным уровнем CEA или CYFRA21-1 (CEA ≤ 5 нг / мл: HR = 0,70, 95% ДИ 0,49–1,01, p = 0,057; CYFRA21-1 ≤ 3,3 нг / мл: HR = 0,68. , 95% ДИ 0,46–1,01, p = 0,055). Многофакторный анализ, учитывающий снижение CEA и CYFRA21-1 на ≥ 20%, не показал статистически значимых результатов, но имел тенденцию к лучшему прогнозу для пациентов со снижением CYFRA21-1 ≥ 20% (HR = 0.55, 95% ДИ 0,28–1,07, p = 0,079) (данные не показаны). Наконец, что касается гистологических подтипов, не наблюдалось значительной разницы в OS между пациентами с аденокарциномой и плоскоклеточной карциномой (медиана OS 9,2 против 9,8 месяцев). Следует отметить, что ОС была значительно увеличена только среди пациентов с аденокарциномой со снижением CEA ≥ 20% (медиана OS, 14,8 против 9,9 месяцев, p = 0,054) (данные не показаны).
Следует отметить, что ОС была значительно увеличена только среди пациентов с аденокарциномой со снижением CEA ≥ 20% (медиана OS, 14,8 против 9,9 месяцев, p = 0,054) (данные не показаны).
Таблица 6 OS в зависимости от исходного уровня в сыворотке и снижение CEA, CYFRA и NSE ≥ 20%
Рис.2
Общая выживаемость согласно CEA и CYFRA21-1 Снижение ≥ 20%
Рак легких | Лабораторные тесты онлайн
Источники, использованные в текущем обзоре
2018 обзор выполнен Имадом Тархони, доктором медицины, кандидатом наук, отделение клеточной и молекулярной медицины, Медицинский центр Университета Раш.
Spirtas, R., et al. (Декабрь 1994 г.) Злокачественная мезотелиома: связанный риск воздействия асбеста. Профессиональная экологическая медицина. Доступно на сайте www.ncbi.nlm.nih.gov/pmc/articles/PMC1128120/pdf/oenvmed00060-0012.pdf. По состоянию на 15 сентября 2018 г.
(2014) Департамент здравоохранения и социальных служб. Управляющее резюме. Последствия курения для здоровья — 50 лет прогресса: отчет главного врача. Доступно на сайте www.surgeongeneral.gov/library/reports/50-years-of-progress/exec-summary.pdf. По состоянию на 15 сентября 2018 г.
(22 февраля 2016 г., с изменениями) Факторы риска рака легких. Американское онкологическое общество. Доступно на сайте www.race.org/cancer/lung-cancer/prevention-and-early-detection.html. По состоянию на 15 сентября 2018 г.
(16 мая 2016 г., пересмотрено) о немелкоклеточном раке легкого. Американское онкологическое общество. Доступно в Интернете по адресу www.cancer.org/content/dam/CRC/PDF/Public/8703.00.pdf. По состоянию на 15 сентября 2018 г.
(2017) Скрининг рака легких. Рекомендации сети Национального комплексного онкологического центра для пациентов. Доступно в Интернете по адресу www.nccn.org/patients/guidelines/lung_screening. По состоянию на 15 сентября 2018 г.
(19 мая 2017 г.) Сотрудники NCI.Пресс-релиз. FDA предоставило ускоренное одобрение бригатиниба для лечения метастатического немелкоклеточного рака легкого. Доступно в Интернете по адресу https://www.cancer.gov/news-events/cancer-currents-blog/2017/brigatinib-fda-lung-cancer. По состоянию на 15 сентября 2018 г.
(16 июня 2017 г., обновлено) Скрининг рака легких (PDQ) — Версия для пациентов. Рак легких. Национальный институт рака. Доступно в Интернете по адресу www.cancer.gov/types/lung/patient/lung-screening-pdq. По состоянию на 15 сентября 2018 г.
(23 июня 2017 г., пересмотрено) Тесты на немелкоклеточный рак легкого.Раннее выявление, диагностика и постановка. Американское онкологическое общество. Доступно в Интернете по адресу www.cancer.org/cancer/non-small-cell-lung-cancer/detection-diagnosis-staging/how-diagnposed.html. По состоянию на 15 сентября 2018 г.
Reddy, K.P., et al. (1 ноября 2017 г.). Смертность от рака легких, связанная с курением и отказом от курения среди людей, живущих с ВИЧ, в США. JAMA Intern Med. Доступно на сайте http://dx.doi.org/10.1001/jamainternmed.2017.4349. По состоянию на 15 сентября 2018 г.
JAMA Intern Med. Доступно на сайте http://dx.doi.org/10.1001/jamainternmed.2017.4349. По состоянию на 15 сентября 2018 г.
(6 декабря 2017 г.) NCI Staff. Пресс-релиз. FDA одобрило использование алектиниба для начального лечения ALK-положительного рака легких. Доступно в Интернете на сайте www.cancer.gov/news-events/cancer-currents-blog/2017/alectinib-fda-untreated-lung-cancer. По состоянию на 15 сентября 2018 г.
(2018) Рак легкого — немелкоклеточный рак легкого. Руководство Национальной комплексной сети по борьбе с раком для пациентов. Доступно в Интернете по адресу www.nccn.org/patients/guidelines/lung-nsclc. По состоянию на 15 сентября 2018 г.
(20 февраля 2018 г., обновлено) Tan, W.W., et al. Немелкоклеточный рак легкого. Основы практики. Medscape. Доступно на сайте https://emedicine.medscape.com/article/279960-overview. По состоянию на 15 сентября 2018 г.
(13 марта 2018 г.) Рак легкого: диагностика и лечение. Клиника Майо. Доступно в Интернете по адресу www. mayoclinic.org/diseases-conditions/lung-cancer/diagnosis-treatment/drc-20374627. По состоянию на 15 сентября 2018 г.
mayoclinic.org/diseases-conditions/lung-cancer/diagnosis-treatment/drc-20374627. По состоянию на 15 сентября 2018 г.
(30 марта 2018 г., обновлено) Лечение немелкоклеточного рака легких (PDQ) — Версия для пациентов. Рак легких. Национальный институт рака.Доступно в Интернете на сайте www.cancer.gov/types/lung/patient/non-small-cell-lung-treatment-pdq. По состоянию на 15 сентября 2018 г.
(6/2018) Рак в фактах и цифрах, 2018. Американское онкологическое общество. Доступно в Интернете по адресу https://www.cancer.org/content/dam/cancer-org/research/cancer-facts-and-statistics/annual-cancer-facts-and-figures/2018/cancer-facts-and-figures -2018.pdf. Дата обращения 01.10.2018.
(3 февраля 2017 г.) UPtoDate.com. Доступно на сайте https://www.uptodate.com. Дата обращения 03.10.2018.
(2018) LungCancer.org. Доступно в Интернете по адресу https://www.lungcancer.org/find_information/publications/163-lung_cancer_101/269-non-small_cell_lung_cancer_treatment. Дата обращения 03.10.2018.
Дата обращения 03.10.2018.
(декабрь 2013 г.) Целевая группа по профилактическим услугам США. Заключительные рекомендации, Рак легкого: скрининг. Доступно в Интернете по адресу https://www.uspreventiveservicestaskforce.org/Page/Document/RecommendationStatementFinal/lung-cancer-screening. По состоянию на декабрь 2018 г.
Источники, использованные в предыдущих обзорах
(пересмотрена 12 июля 2013 г.).Рак легких (немелкоклеточный). Американское онкологическое общество [Он-лайн информация]. Доступно в Интернете по адресу [Он-лайн информация]. Доступно в Интернете по адресу http://www.cancer.org/cancer/lungcancer-non-smallcell/detailedguide/index. По состоянию на июль 2013 г.
(от 6 июня 2013 г.). Рак легких (малая клетка). Американское онкологическое общество [Он-лайн информация]. Доступно в Интернете по адресу http://www.cancer.org/cancer/lungcancer-smallcell/detailedguide/index. По состоянию на июль 2013 г.
(от 15 августа 2012 г. ). Карциноидная опухоль легких.Американское онкологическое общество [Он-лайн информация]. Доступно в Интернете по адресу http://www.cancer.org/cancer/lungcarcinoidtumor/detailedguide/index. По состоянию на июль 2013 г.
). Карциноидная опухоль легких.Американское онкологическое общество [Он-лайн информация]. Доступно в Интернете по адресу http://www.cancer.org/cancer/lungcarcinoidtumor/detailedguide/index. По состоянию на июль 2013 г.
Тан, В. и Хук, С. (Обновлено 23 июля 2013 г.) Немелкоклеточный рак легкого. Справочник по Medscape [Он-лайн информация]. Доступно в Интернете по адресу http://emedicine.medscape.com/article/279960-overview#showall. По состоянию на июль 2013 г.
Маркман М. (Обновлено 15 июля 2013 г.) Генетика немелкоклеточного рака легкого. Справочник по Medscape [Он-лайн информация].Доступно в Интернете по адресу http://emedicine.medscape.com/article/1689988-overview. По состоянию на июль 2013 г.
Тан, В. и Магфор, И. (обновлено 27 декабря 2012 г.). Мелкоклеточный рак легких. Справочник по Medscape [Он-лайн информация]. Доступно в Интернете по адресу http://emedicine.medscape.com/article/280104-overview. По состоянию на июль 2013 г.
(обновлено 17 апреля 2012 г. ). Рак легких и окружающая среда. Центры по контролю и профилактике заболеваний [он-лайн информация]. Доступно в Интернете по адресу http: // ephtracking.cdc.gov/showCancerLcEnv.action. По состоянию на июль 2013 г.
). Рак легких и окружающая среда. Центры по контролю и профилактике заболеваний [он-лайн информация]. Доступно в Интернете по адресу http: // ephtracking.cdc.gov/showCancerLcEnv.action. По состоянию на июль 2013 г.
Chen, Y. (Обновлено 24 августа 2011 г.). Обновлено: И-Бин Чен, доктор медицинских наук. Рак легких. Медицинская энциклопедия MedlinePlus [Он-лайн информация]. Доступно в Интернете по адресу http://www.nlm.nih.gov/medlineplus/ency/article/007270.htm. По состоянию на июль 2013 г.
(17 сентября 2012 г.). Что вам нужно знать о раке легких ™. Национальный институт рака [Он-лайн информация]. Доступно в Интернете по адресу http://www.cancer.gov/cancertopics/wyntk/lung. По состоянию на июль 2013 г.
Нельсон Р. (17 июля 2013 г.). Скрининг рака легких приносит пользу тем, кто подвержен высокому риску. Medscape Today News from N Engl J Med v 369: 245-254 [Он-лайн информация]. Доступно в Интернете по адресу http://www.medscape.com/viewarticle/807979. По состоянию на июль 2013 г.
По состоянию на июль 2013 г.
сотрудников клиники Мэйо (17 апреля 2012 г.). Рак легких. Клиника Мэйо [Он-лайн информация]. Доступно в Интернете по адресу http://www.mayoclinic.com/print/lung-cancer/DS00038/METHOD=print&DSECTION=all. По состоянию на июль 2013 г.
Чен, Ю.(Обновлено 24 августа 2011 г.). Рак легких — немелкоклеточный. Медицинская энциклопедия MedlinePlus [Он-лайн информация]. Доступно в Интернете по адресу http://www.nlm.nih.gov/medlineplus/ency/article/007194.htm. По состоянию на июль 2013 г.
Дагдейл, Д. (Обновлено 24 августа 2011 г.). Рак легких — мелкоклеточный. Медицинская энциклопедия MedlinePlus [Он-лайн информация]. Доступно в Интернете по адресу http://www.nlm.nih.gov/medlineplus/ency/article/000122.htm. По состоянию на июль 2013 г.
Нельсон Р. (7 мая 2013 г.). ACCP издает новые рекомендации по скринингу рака легких.Medscape Today Новости из Сундук . 2013; 143 (5_suppl): e78S-e92S. [Он-лайн информация]. Доступно в Интернете по адресу http://www. medscape.com/viewarticle/803769. По состоянию на июль 2013 г.
medscape.com/viewarticle/803769. По состоянию на июль 2013 г.
Ellison, G. et. al. (2013). Тестирование мутации EGFR при раке легкого, обзор доступных методов и их использования для анализа образцов опухолевой ткани и цитологии. Medscape Today Новости из J Clin Pathol . 2013; 66 (2): 79-89. [Он-лайн информация]. Доступно в Интернете по адресу http://www.medscape.com/viewarticle/778512.По состоянию на июль 2013 г.
Вест, Х. Дж. (13 февраля 2013 г.). KRAS + Рак легкого реагирует на таргетную терапию. Новости Medscape Today. Ланцет Онкол . v14 38-47. [Он-лайн информация]. Доступно в Интернете по адресу http://www.medscape.com/viewarticle/779075. По состоянию на июль 2013 г.
Маркман М. (Обновлено 15 июля 2013 г.). Генетика немелкоклеточного рака легкого. Справочник по Medscape [Он-лайн информация]. Доступно в Интернете по адресу http://emedicine.medscape.com/article/1689988-overview. По состоянию на июль 2013 г.
Андерсон, С. (2011). Лабораторные методы анализа мутаций KRAS. Ссылка на Medscape от Expert Rev Mol Diagn . v11 (6) 635-642 [Он-лайн информация]. Доступно в Интернете по адресу http://www.medscape.com/viewarticle/746638. По состоянию на июль 2013 г.
Лабораторные методы анализа мутаций KRAS. Ссылка на Medscape от Expert Rev Mol Diagn . v11 (6) 635-642 [Он-лайн информация]. Доступно в Интернете по адресу http://www.medscape.com/viewarticle/746638. По состоянию на июль 2013 г.
| Альфа-фетопротеин (AFP) | Печень, зародышевый рак яичников или семенников | Также повышен во время беременности | Помогите диагностировать, контролировать лечение и определить рецидив | Кровь |
| CA 15-3 (Раковый антиген 15-3) | Рак груди и другие заболевания, включая легкие, яичники | Также повышен при доброкачественных заболеваниях груди | Стадия заболевания, мониторинг лечения и определение рецидива | Кровь |
| CA 19-9 (Раковый антиген 19-9) | Поджелудочная железа, иногда кишечник и желчные протоки | Также повышен при панкреатите и воспалительном заболевании кишечника | Стадия заболевания, мониторинг лечения и определение рецидива | Кровь |
| CA-125 (раковый антиген 125) | Яичники | Также повышен при эндометриозе, некоторых других заболеваниях и состояниях; не рекомендуется в качестве общего экрана | Помогите диагностировать, контролировать лечение и определить рецидив | Кровь |
| Кальцитонин | Медуллярная карцинома щитовидной железы | Также повышен при пернициозной анемии и тиреоидите | Помогите диагностировать, контролировать лечение и определить рецидив | Кровь |
| Карциноэмбриональный антиген (CEA) | кишечник, легкое, грудь, щитовидная железа, поджелудочная железа, печень, шейка матки и мочевой пузырь | Повышен при других состояниях, таких как гепатит, ХОБЛ, колит, панкреатит, и у курильщиков сигарет | Наблюдать за лечением и определять рецидивы | Кровь |
| ХГЧ (хорионический гонадотропин человека) | Яичек и трофобластическая болезнь | Повышение при беременности, недостаточность яичек | Помогите диагностировать, контролировать лечение и определить рецидив | Кровь, моча |
| Гер-2 / neu | Грудь | , который присутствует в нескольких копиях в 20-30% случаев инвазивного рака груди | Определить прогноз и назначить лечение | Ткань |
| Моноклональные иммуноглобулины | Множественная миелома и макроглобулинемия Вальденстрема | Избыточное производство иммуноглобулина или антител, обычно обнаруживаемое электрофорезом белков | Помощь в диагностике, контролировать лечение и определять рецидив | Кровь, моча |
| Рецепторы эстрогенов | Грудь | Повышение заболеваемости гормонозависимым раком | Определить прогноз и назначить лечение | Ткань |
| Рецепторы прогестерона | Грудь | Повышение заболеваемости гормонозависимым раком | Определить прогноз и назначить лечение | Ткань |
| PSA (простатоспецифический антиген) | Простата | Повышается при доброкачественной гиперплазии предстательной железы, простатите и с возрастом | Скрининг и помощь в диагностике, мониторинге лечения и определении рецидива | Кровь |
| Тиреоглобулин | Щитовидная железа | Используется после удаления щитовидной железы для оценки лечения | Определить рецидив | Кровь |
| Другие опухолевые маркеры используются реже | ||||
| B2M (бета-2-микроглобулин) | Множественная миелома и лимфомы | Присутствует при многих других состояниях, включая болезнь Крона и гепатит. |



 – Т. I., Т. II – М. : ГЭОТАР-Медиа, 2012.
– Т. I., Т. II – М. : ГЭОТАР-Медиа, 2012. Он проникает в кровоток только в случае повреждения природных барьеров. Его уровни в крови могут удваиваться во время менструации и при эндометриозе. Значительное повышение уровня СА125 происходит при раке яичников (в 80% случаев) и других органов женской половой системы, опухолях молочной и поджелудочной желез, прямой кишки, желудка легких и печени. Из доброкачественных заболеваний к повышению уровня этого маркера приводят воспалительные заболевания органов женской половой системы, гепатиты, циррозы и аутоиммунные заболевания.
Он проникает в кровоток только в случае повреждения природных барьеров. Его уровни в крови могут удваиваться во время менструации и при эндометриозе. Значительное повышение уровня СА125 происходит при раке яичников (в 80% случаев) и других органов женской половой системы, опухолях молочной и поджелудочной желез, прямой кишки, желудка легких и печени. Из доброкачественных заболеваний к повышению уровня этого маркера приводят воспалительные заболевания органов женской половой системы, гепатиты, циррозы и аутоиммунные заболевания. Из доброкачественных заболеваний к повышению его уровня приводят гепатиты и цирроз, холецистит и муковисцидоз.
Из доброкачественных заболеваний к повышению его уровня приводят гепатиты и цирроз, холецистит и муковисцидоз.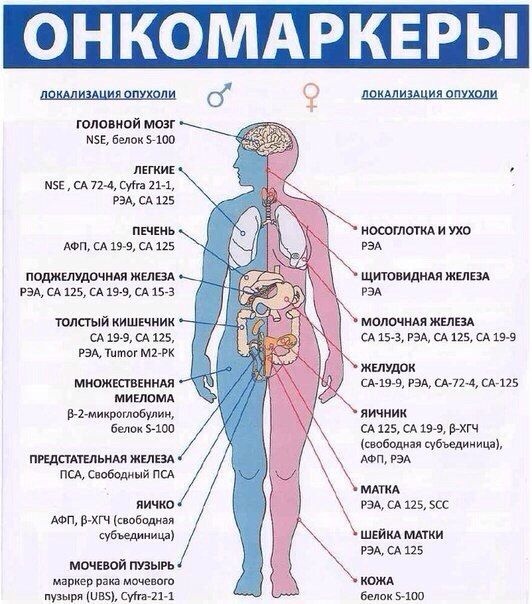 М. Клиническое значение определения растворимого фрагмента цитокератина 19 — Cyfra 21-1. — Лаборатория, 2004, № 2, с. 3 — 6.
М. Клиническое значение определения растворимого фрагмента цитокератина 19 — Cyfra 21-1. — Лаборатория, 2004, № 2, с. 3 — 6.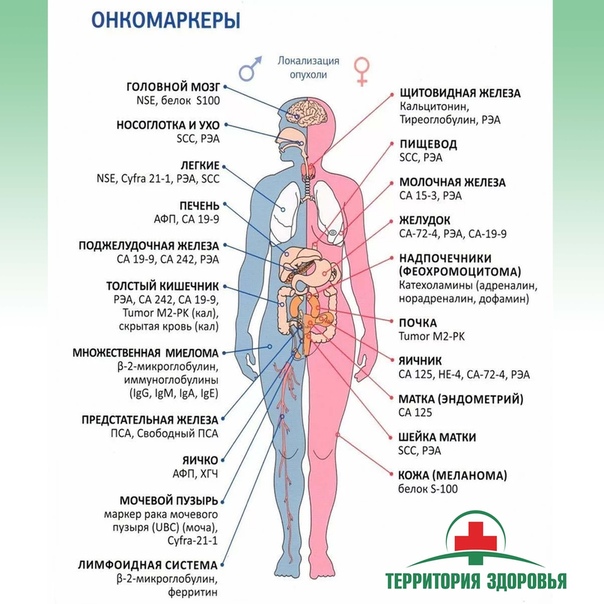 Современный диагностический комплекс госпиталя позволяет с высокой точностью проводить как скрининг, так и более углубленные исследования (лучевые, эндоскопические, генетические) для определения онкологических заболеваний.
Современный диагностический комплекс госпиталя позволяет с высокой точностью проводить как скрининг, так и более углубленные исследования (лучевые, эндоскопические, генетические) для определения онкологических заболеваний.