Почему болят животики у малышей?
Почему болят животики у малышей?
С таким детским, но совсем не простым вопросом мы обратились к НАТАЛЬЕ ВАСИЛЬЕВНЕ АВДЕЕВОЙ — кандидату медицинских наук, члену Российской гастроэнтерологической ассоциации, гастроэнтерологу многопрофильного медицинского центра «Александрия».
— Наталья Васильевна, здравствуйте. Расскажите о болях в животе, возникающих у малышей? Например, колики — в чем их причина и что делать родителям?
— Причин, почему у ребенка может болеть живот, действительно, очень много. У детей грудного возраста причиной могут быть так называемые «колики», как физиологические, так и вызванные, например, пищевой аллергией. Профилактикой пищевой аллергии, если грудное вскармливание невозможно по каким-либо причинам, является использование лечебных смесей, которые содержат расщепленный белок коровьего молока и сниженное количество лактозы. Это уменьшает нагрузку на пищеварительный тракт ребенка, дает ему возможность поддерживать нормальное переваривание, снижает риск газообразования и других проявлений.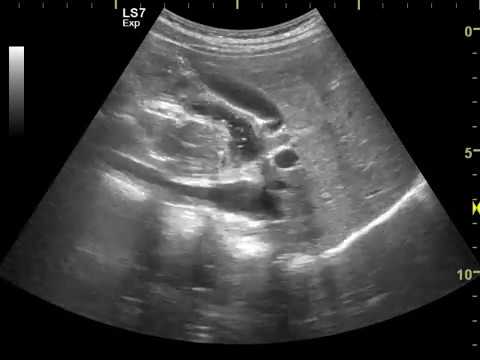 Еще одна частая причина болей в животе у малыша — холестатические нарушения (задержка желчи). Данная проблема может возникать на фоне прорезывания зубов, нарушения графика введения прикормов (раннее введение, продукты не рекомендованные по возрасту). Определяется это на УЗИ брюшной полости. Для коррекции этих нарушений используются желчегонные препараты. Нарушения стула (диарея, запоры), как правило, перекликаются с вышеназванными причинами. Еще одно проявление пищевой аллергии — кожные высыпания. Конечно, существует ряд заболеваний, дающих похожие симптомы, но чаще всего мамы маленьких детей сталкиваются именно с этими проблемами.
Еще одна частая причина болей в животе у малыша — холестатические нарушения (задержка желчи). Данная проблема может возникать на фоне прорезывания зубов, нарушения графика введения прикормов (раннее введение, продукты не рекомендованные по возрасту). Определяется это на УЗИ брюшной полости. Для коррекции этих нарушений используются желчегонные препараты. Нарушения стула (диарея, запоры), как правило, перекликаются с вышеназванными причинами. Еще одно проявление пищевой аллергии — кожные высыпания. Конечно, существует ряд заболеваний, дающих похожие симптомы, но чаще всего мамы маленьких детей сталкиваются именно с этими проблемами.
— Теперь расскажите про детей дошкольного и школьного возраста. Есть ли заболевания, дающие боли в животе, не связанные с желудочно-кишечным трактом?
— Разные заболевания ЖКТ также могут давать боли в животе. Гастриты, дуодениты, холециститы, колиты и т.д. Но даже, например, при пневмонии может быть боль в животе. Конечно, там своя симптоматика — повышение температуры, интоксикация, дыхательные расстройства, но боль в животе, как неспецифический признак, может пневмонии сопутствовать. При заболевании почек — пиелонефрите может болеть не только поясница, но и живот. При неврологических заболеваниях на фоне повышенных регулярных психоэмоциональных нагрузок, вегетативных расстройствах нервной системы дети могут жаловаться на тошноту, боли в животе, укачивание в транспорте. Причинами болей в животе могут стать различные инфекции, как паразитарные, так и кишечные. У дошкольников — гельминтные инфекции, лямблиоз, энтеровирусные и ротавирусные инфекции. У школьников одной из причин болей в животе могут быть травмы, полученные при падениях, ушибах и т.д.
При заболевании почек — пиелонефрите может болеть не только поясница, но и живот. При неврологических заболеваниях на фоне повышенных регулярных психоэмоциональных нагрузок, вегетативных расстройствах нервной системы дети могут жаловаться на тошноту, боли в животе, укачивание в транспорте. Причинами болей в животе могут стать различные инфекции, как паразитарные, так и кишечные. У дошкольников — гельминтные инфекции, лямблиоз, энтеровирусные и ротавирусные инфекции. У школьников одной из причин болей в животе могут быть травмы, полученные при падениях, ушибах и т.д.
— Часто школьники болеют гастродуоденитами. Почему они появляются?
— Гастродуоденит считается хронической патологией, но он может протекать без обострений несколько лет. Огромную роль в появлении заболевания играет наследственность. Если у ближайших родственников имеются такие заболевания, как гастрит, язвенная болезнь желудка и/или 12-перстной кишки, гастроэзофагеальный рефлюкс, то у детей риск возникновения гастродуоденита гораздо выше. Если, например, возникает повышенная кислотность, появляется риск данных заболеваний. Может увеличивать риск воспалительных изменений и прием некоторых лекарств, пищевая аллергия, инфекции, моторные нарушения верхних отделов пищеварительного тракта.
Если, например, возникает повышенная кислотность, появляется риск данных заболеваний. Может увеличивать риск воспалительных изменений и прием некоторых лекарств, пищевая аллергия, инфекции, моторные нарушения верхних отделов пищеварительного тракта.
— Как наблюдаться детям с гастритами?
— Этим детям нужно динамическое наблюдение. Как известно, заболевания ЖКТ обостряются весной и осенью, поэтому именно в эти периоды рекомендуются контрольные визиты к гастроэнтерологу, проведение инструментального и лабораторного обследования. Известно, что иммунная система как общего, так и местного иммунитета слизистых пищеварительного тракта весной и осенью имеет предрасположенность к развитию воспаления, что приводит к появлению заболевания либо обострению имеющегося. Поэтому в эти периоды показано проведение лечения: желчегонная терапия, ферментные препараты, цитопротекторы — антациды, витамины, в том числе использование физиолечения, что позволяет снизить лекарственную нагрузку на организм и удлинить периоды ремиссии.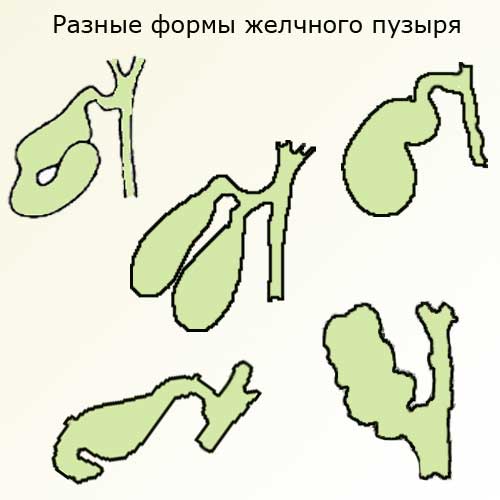
— Часто родители слышат от врачей о перегибе желчного пузыря у ребенка. Что это и чем грозит? Какие советы вы можете дать родителям?
— Перегибы желчного пузыря могут быть фиксированные и лабильные. Иногда, приводя на очередное УЗИ ребенка, мама говорит: «Как же так? В прошлый раз был перегиб, а сейчас его не находят. Куда он делся?» Такое вполне возможно — это лабильный перегиб желчного пузыря. Как только состояние улучшается, основное заболевание компенсируется, этот перегиб может исчезнуть. Сам по себе перегиб не страшен, если нет других причин, вызывающих застой желчи. Вот если есть перегиб, да еще и, например, наличие дуоденита или гастродуоденита, моторные нарушения верхних отделов пищеварительного тракта, лямблиоз либо систематическое нарушение режима питания и диеты, то перегиб может быть одним из факторов, систематической задержки желчи и способствующих развитию в дальнейшем холецистита, желчекаменной болезни. Если у ребенка есть перегиб желчного пузыря, рекомендуется следить за его режимом питания, диетой, весной и осенью профилактически пить желчегонные препараты или травы (если нет аллергии).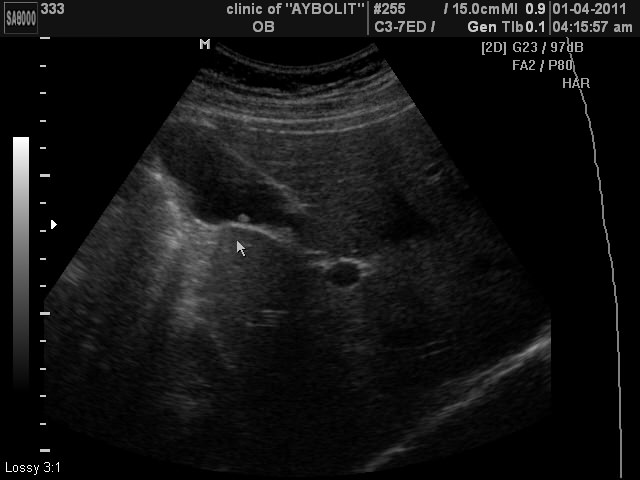 Предпочтительнее ромашку, у шиповника выше риск аллергических реакций. Обычный профилактический курс состоит из двух месяцев в следующем режиме: курсами по две недели два месяца подряд (две недели прием, две недели перерыв, две недели прием).
Предпочтительнее ромашку, у шиповника выше риск аллергических реакций. Обычный профилактический курс состоит из двух месяцев в следующем режиме: курсами по две недели два месяца подряд (две недели прием, две недели перерыв, две недели прием).
— Говорят, что диагноза «дисбактериоз» как такового не существует. Что делать, если ребенку поставили такой диагноз?
— В международной классификации болезней действительно нет такого диагноза. Данное состояние может стать риском развития или прогрессирования течения какой-либо патологии. Слизистая кишечника в норме имеет мукоидную систему секрета желез и пристеночную микрофлору. И если этот комплекс не нарушен, значит защитные силы организма работают в полную силу, что имеет огромное значение для состояния здоровья. Во-первых, мал риск аллергии, во-вторых, наличие дисбиотических нарушений может очень плохо сказаться на течении самых разных болезней из-за повышенной нагрузки на органы токсинами.
Нет анализов, которые были бы доступными в практическом здравоохранении и в то же время являлись «золотым стандартом» для диагностики дисбактериоза. Как показано многими исследованиями, посев кала на дисбактериоз, далек от идеала. Однако мы все-равно пользуемся им на практике у детей первого года жизни. Есть также косвенный анализ, который не показывает наличие микробов, но говорит об изменении биохимического состава микрофлоры — биохимический анализ кала на короткоцепочечные жирные кислоты. Уменьшение или повышение уровня этих кислот будет свидетельствовать о нарушении защитной функции кишечника. Есть также анализ кала на углеводы, с помощью которого мы можем определить наличие лактазной недостаточности. Вот эти исследования могут быть нам полезны при диагностике нарушений работы кишечника у детей.
Как показано многими исследованиями, посев кала на дисбактериоз, далек от идеала. Однако мы все-равно пользуемся им на практике у детей первого года жизни. Есть также косвенный анализ, который не показывает наличие микробов, но говорит об изменении биохимического состава микрофлоры — биохимический анализ кала на короткоцепочечные жирные кислоты. Уменьшение или повышение уровня этих кислот будет свидетельствовать о нарушении защитной функции кишечника. Есть также анализ кала на углеводы, с помощью которого мы можем определить наличие лактазной недостаточности. Вот эти исследования могут быть нам полезны при диагностике нарушений работы кишечника у детей.
Кроме этого, для установления правильного диагноза необходимы дополнительные исследования:
- Узи органов брюшной полости.
- Кроме этого детям раннего, дошкольного возраста и младшего школьного возраста- узи области пищевода, желудка и 12-перстной кишки, что позволяет выявить патологию на ранней стадии, не прибегая к инвазивным исследованиям ( например, фиброгастродуоденоскопии)
- Лабораторные исследования:
— общеклинические: общий анализ крови, общий анализ мочи, копрология
— биохимическое исследование крови- Асат, Алат, билирубин, амилаза и тд
-анализ кала на яйца глист и простейших
— иммуноферментный анализ крови- определение антител к паразитам, хеликобактер пилори и другим инфекциям, которые могут быть причиной боли в животе
— ПЦР- исследование крови и кала для определения ДНК возбудителя
— бактериологический анализ кала на дисбактериоз
4)консультации специалистов- гастроэнтеролог, аллерголог-иммунолог, инфекционист, педиатр, невролог, детский хирург, физиотерапевт
Все эти исследования и консультации специалистов можно пройти в клинике Александрия на пр. Гагарина, 50 и улице Ошарской,65
Гагарина, 50 и улице Ошарской,65
Перегиб желчного пузыря у ребенка – причины, симптомы и лечение
Сделали УЗИ и обнаружили перегиб желчного пузыря. А что с этим делать?
Виды перегибов желчного пузыря
Этим вопросом занимается гастроэнтеролог и педиатр. На соответствующем УЗИ надо установить, какой вид перегиба. Чаще встречается непостоянный, или лабильный, перегиб. Это проверяется изменением положения тела, при котором желчный пузырь расправляется. Такой перегиб не требует лечения. Но бывает постоянный, или фиксированный, перегиб. Такому перегибу не поможет смена позы. Это врожденная патология желчного пузыря, которая требует соблюдения диеты и применения ряда лечебных мероприятий. Если не предпринимать никаких мер, то есть риск возникновения осложнений. Могут быть боли в области правого подреберья, нарушение пищеварительной функции, тошнота, привкус горечи во рту. Порой такой пузырь является предрасполагающим фактором к возникновению желчного осадка на стенке пузыря и пусковым механизмом камнеобразования.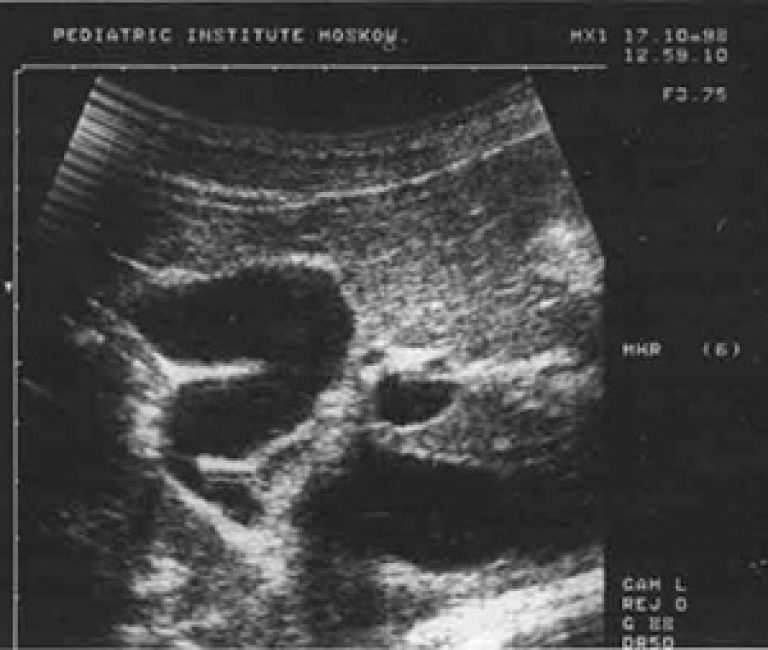
Особенности лечения загибов желчного пузыря
Конечно же, это состояние носит доброкачественный характер, но может и значительно нарушать качество жизни. Чтобы этого не произошло, надо соблюдать несколько основных мер. Одна из них порой тяжело дается не только ребенку, но и взрослому. Это диета, которая предполагает резкое ограничение или отказ от жирного, жареного, копченого, острого и соленого. Неплохо бы регулярно проводить лечебную физкультуру в виде простых упражнений, целью которых является изменение положения тела с напряжением мышц брюшного пресса, что помогает перемещению желчи в пузыре. Также периодически неплохо применять препараты, которые вызывают желчегонный эффект. Конечно же, при наличии фиксированного перегиба желчного пузыря надо ежегодно проверять его состояние с помощью УЗИ. Ультразвуковое исследование совсем не вредно и не имеет ограничений. Неплохо бы периодически проверять работу печени и кишечника с помощью анализов крови и кала. Обычно это биохимический анализ крови и анализ кала на копрологию.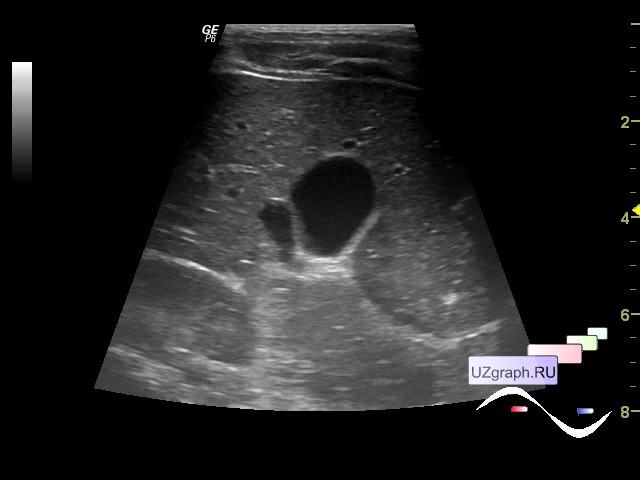 Соблюдая рекомендации гастроэнтеролога, можно очень даже комфортно жить с перегибом желчного пузыря и избежать неприятных осложнений.
Соблюдая рекомендации гастроэнтеролога, можно очень даже комфортно жить с перегибом желчного пузыря и избежать неприятных осложнений.
Синдром сгущения желчи у новорожденных и детей раннего возраста. Факторы риска, терапия, прогноз. Разбор клинического случая
Журнал «Медицинский совет» №18/2020
DOI: 10.21518/2079-701X-2020-18-134-141
А.Н. Горяйнова1, Е.В. Беленович2, А.А. Худякова2, Ю.А. Бронникова2, Л.В. Чурилова2
1 Российская медицинская академия непрерывного профессионального образования; 125993, Россия, Москва, ул. Баррикадная, д. 2/1, стр. 1
2 Детская городская клиническая больница им. З.А. Башляевой; 125373, Россия, Москва, ул. Героев Панфиловцев, д. 28
Синдром сгущения желчи, или билиарный сладж, вызывающий обструкцию общего желчного протока и нарушение пассажа желчи в двенадцатиперстную кишку, занимает второе место среди «хирургических желтух» у новорожденных и детей раннего возраста. Ранняя диагностика синдрома необходима для своевременного проведения консервативной терапии, позволяющей избежать оперативного вмешательства и таких осложнений, как острый панкреатит, острый холецистит, желчнокаменная болезнь. К факторам риска синдрома сгущения желчи относятся недоношенность, экстремально низкая масса при рождении, длительное парентеральное питание, назначение диуретиков, цефалоспоринов III поколения. В случае угрозы билиарного сладжа показано проведение УЗИ органов брюшной полости в динамике и выявление характерных для этого синдрома признаков: дилатации общего желчного протока более 3 мм, наличие неоднородного осадка в желчном пузыре и общем желчном протоке. В статье дается клинический разбор случая синдрома сгущения желчи у девочки, родившейся с экстремально низкой массой и гестационным возрастом 29 нед. Состояние новорожденной при рождении очень тяжелое. Тяжесть состояния обусловлена синдромом дыхательных расстройств 1-го типа, сразу же интубирована, начата ИВЛ.
Ранняя диагностика синдрома необходима для своевременного проведения консервативной терапии, позволяющей избежать оперативного вмешательства и таких осложнений, как острый панкреатит, острый холецистит, желчнокаменная болезнь. К факторам риска синдрома сгущения желчи относятся недоношенность, экстремально низкая масса при рождении, длительное парентеральное питание, назначение диуретиков, цефалоспоринов III поколения. В случае угрозы билиарного сладжа показано проведение УЗИ органов брюшной полости в динамике и выявление характерных для этого синдрома признаков: дилатации общего желчного протока более 3 мм, наличие неоднородного осадка в желчном пузыре и общем желчном протоке. В статье дается клинический разбор случая синдрома сгущения желчи у девочки, родившейся с экстремально низкой массой и гестационным возрастом 29 нед. Состояние новорожденной при рождении очень тяжелое. Тяжесть состояния обусловлена синдромом дыхательных расстройств 1-го типа, сразу же интубирована, начата ИВЛ. В возрасте 1 мес. 10 дней девочка переведена из отделения реанимации и интенсивной терапии в отделение для новорожденных. По данным УЗИ желчный пузырь овальной формы, размерами 26 х 6 мм, объемом 0,5 мл, имеется лабильный перегиб в области тела и шейки, стенки утолщены до 2 мм, слоистые, повышенной эхогенности, в просвете гиперэхогенное содержимое (замазкообразная желчь), что позволило сделать вывод о наличии синдрома сгущения желчи. Сразу же после УЗИ назначена урсодезоксихолевая кислота 20 мг/кг/сут, спустя 10 дней доза препарата была увеличена до 30 мг/кг/сут. Спустя две недели ребенок был выписан домой в удовлетворительном состоянии без признаков синдрома сгущения желчи. Знание факторов риска билиарного сладжа позволяет своевременно назначить инструментальное обследование, обеспечить раннюю диагностику и назначение консервативной терапии, исключить хирургические методы лечения.
В возрасте 1 мес. 10 дней девочка переведена из отделения реанимации и интенсивной терапии в отделение для новорожденных. По данным УЗИ желчный пузырь овальной формы, размерами 26 х 6 мм, объемом 0,5 мл, имеется лабильный перегиб в области тела и шейки, стенки утолщены до 2 мм, слоистые, повышенной эхогенности, в просвете гиперэхогенное содержимое (замазкообразная желчь), что позволило сделать вывод о наличии синдрома сгущения желчи. Сразу же после УЗИ назначена урсодезоксихолевая кислота 20 мг/кг/сут, спустя 10 дней доза препарата была увеличена до 30 мг/кг/сут. Спустя две недели ребенок был выписан домой в удовлетворительном состоянии без признаков синдрома сгущения желчи. Знание факторов риска билиарного сладжа позволяет своевременно назначить инструментальное обследование, обеспечить раннюю диагностику и назначение консервативной терапии, исключить хирургические методы лечения.
Для цитирования: Горяйнова А.Н., Беленович Е.В., Худякова А. А., Бронникова Ю.А., Чурилова Л.В. Синдром сгущения желчи у новорожденных и детей раннего возраста: факторы риска, терапия, прогноз. Разбор клинического случая. Медицинский Совет. 2020;(18):134-141. https://doi.org/10.21518/2079-701X-2020-18-134-141
А., Бронникова Ю.А., Чурилова Л.В. Синдром сгущения желчи у новорожденных и детей раннего возраста: факторы риска, терапия, прогноз. Разбор клинического случая. Медицинский Совет. 2020;(18):134-141. https://doi.org/10.21518/2079-701X-2020-18-134-141
Конфликт интересов: автор заявляет об отсутствии конфликта интересов.
Bile thickening syndrome in newborns and young children: risk factors, therapy, prognosis. А clinical case study
Aleksandra N. Goryaynova1, Elena V. Belenovich2, Anastasiya A. Khudyakova2, Yuliya A. Bronnikova2, Lyudmila V. Churilova2
1 Russian Medical Academy of Continuous Professional Education; 2/1, Bldg. 1, Barrikadnaya St., Moscow, 125993, Russia
2 Bashlyaeva City Children’s Clinical Hospital; 28, Geroev Panfilovtsev St., Moscow, 125373, Russia
Children with chronic diseases, such as neurological, neuromuscular, respiratory, in particular cystic fibrosis, hereditary, metabolic, oncological, and congenital heart defects often suffer from malnutrition, often accompanied by stunted growth.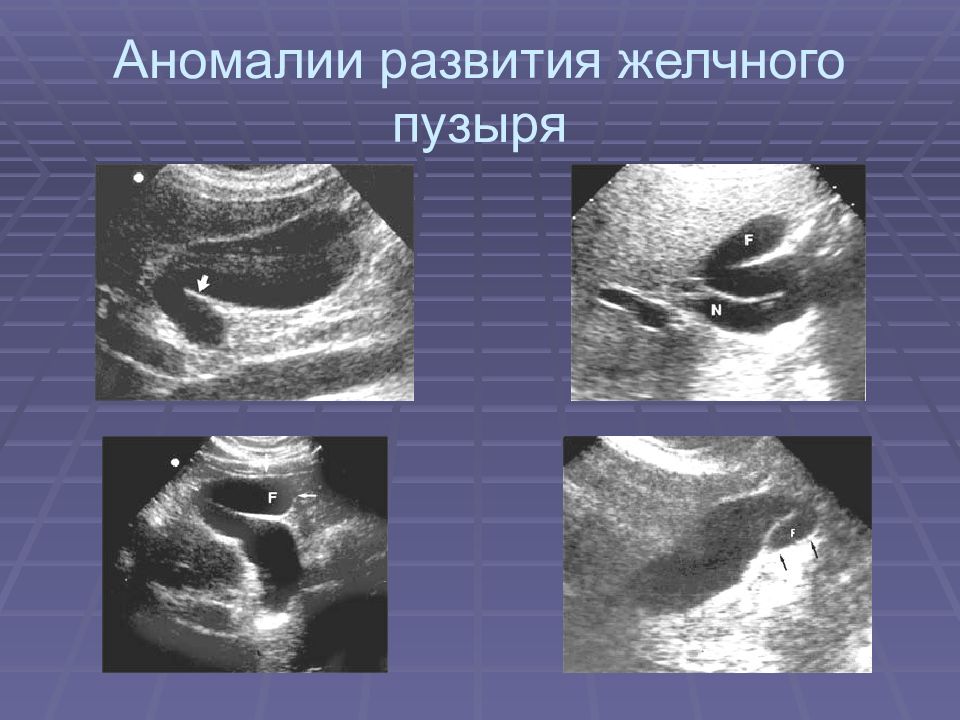 The main reason leading to a change in nutritional status is inadequate intake of nutrients and energy with increased nutrient requirements or various eating problems. Lack of nutrient status correction and continued malnutrition contribute to major body changes that worsen disease progression, increase the risk of death and reduce patients’ quality of life. To fully cover the body’s nutrient needs, the use of specialized enteric nutrition is a priority. Sufficient clinical experience has been accumulated, confirming the high effectiveness of the use of enteral nutrition formulas in children with malnutrition through gastrointestinal feeding. It has been proved that this method of delivery of food is safe for patients, improves nutritional status, simplifies care, as well as reduces the duration of hospitalization, the frequency of respiratory and infectious complications and, consequently, the cost of treatment and rehabilitation. The article presents the assortment of “Nutriсia” formulas for enteral nutrition, which allows a differentiated approach to nutrition of patients depending on the clinical situation.
The main reason leading to a change in nutritional status is inadequate intake of nutrients and energy with increased nutrient requirements or various eating problems. Lack of nutrient status correction and continued malnutrition contribute to major body changes that worsen disease progression, increase the risk of death and reduce patients’ quality of life. To fully cover the body’s nutrient needs, the use of specialized enteric nutrition is a priority. Sufficient clinical experience has been accumulated, confirming the high effectiveness of the use of enteral nutrition formulas in children with malnutrition through gastrointestinal feeding. It has been proved that this method of delivery of food is safe for patients, improves nutritional status, simplifies care, as well as reduces the duration of hospitalization, the frequency of respiratory and infectious complications and, consequently, the cost of treatment and rehabilitation. The article presents the assortment of “Nutriсia” formulas for enteral nutrition, which allows a differentiated approach to nutrition of patients depending on the clinical situation.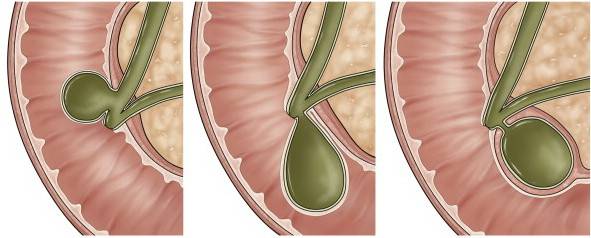 Nutritional problems in patients with neurological disorders and ways of their correction are described in detail. The advantage of using domestic enteric nutrition through feeding tube for the correction of nutritional deficiencies. Timely assigned nutritional support is a highly effective method of correction of nutritional deficiencies or preventing their development in children with chronic diseases.
Nutritional problems in patients with neurological disorders and ways of their correction are described in detail. The advantage of using domestic enteric nutrition through feeding tube for the correction of nutritional deficiencies. Timely assigned nutritional support is a highly effective method of correction of nutritional deficiencies or preventing their development in children with chronic diseases.
For citation: Goryaynova A.N., Belenovich E.V., Khudyakova A.A., Bronnikova Yu.A., Churilova L.V. Bile thickening syndrome in newborns and young children: risk factors, therapy, prognosis. А clinical case study. Meditsinskiy sovet = Medical Council. 2020;(18):134-141. (In Russ.) https://doi.org/10.21518/2079-701X-2020-18-134-141
Conflict of interest: the author declare no conflict of interest.
ВВЕДЕНИЕ
Синдром сгущения желчи – это экстрапеченочная обструкция билиарного тракта билиарным сладжем (слизистыми или желчными пробками) без признаков врожденной билиарной мальформации, без дефекта синтеза желчных кислот и без повреждения гепатоцитов [1]. Экстрапеченочные отделы билиарного тракта включают общий печеночный проток, общий желчный проток, пузырный проток и желчный пузырь. Как следует из определения синдрома сгущения желчи, для него не характерно развитие гепатоцитолиза и повышение гепатоспецифичного фермента аланинаминотрансферазы. Ведущим клиническим симптомом является появление ахоличного стула вследствие нарушения пассажа желчи в двенадцатиперстную кишку.
Экстрапеченочные отделы билиарного тракта включают общий печеночный проток, общий желчный проток, пузырный проток и желчный пузырь. Как следует из определения синдрома сгущения желчи, для него не характерно развитие гепатоцитолиза и повышение гепатоспецифичного фермента аланинаминотрансферазы. Ведущим клиническим симптомом является появление ахоличного стула вследствие нарушения пассажа желчи в двенадцатиперстную кишку.
Синдром сгущения желчи (Inspissated bile syndrome, или синдром «грязной желчи») относится к редким причинам холестаза: у детей раннего возраста встречается в среднем в 1,36–6,2% всех вероятных причин конъюгированной (прямой) гипербилирубинемии [2, 3]. Среди основных вариантов «хирургических желтух» на долю синдрома сгущения желчи приходится 8,2% [4], лидирующее положение занимает билиарная атрезия (81,1%), третье место принадлежит аномалии развития общего желчного протока (7%). В подавляющем большинстве случаев синдром характерен для детей первых трех месяцев жизни, может развиваться без предрасполагающих факторов и существовать только как радиологический диагноз, когда УЗИ выявляет осадок в желчном пузыре и общем желчном протоке [3, 5].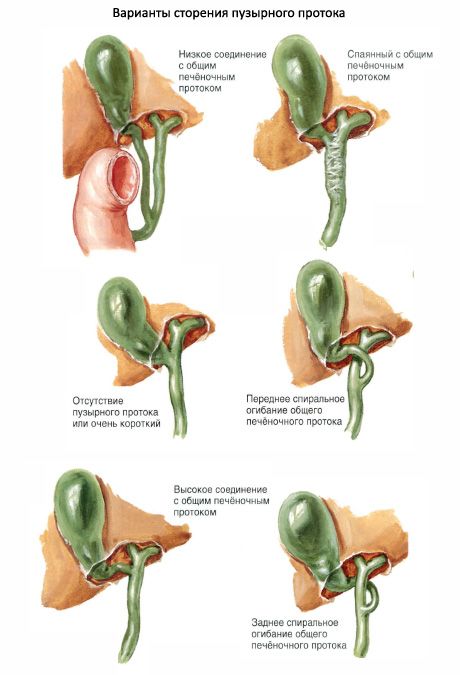
ЭТИОЛОГИЯ, ПАТОГЕНЕЗ, ФАКТОРЫ РИСКА, ПРОГНОЗ
Считается, что билиарный сладж (синдром сгущения желчи) был впервые описан в 70-х гг. прошлого века благодаря появлению ультразвукового исследования [6]. Однако еще в 1916 г. были приведены примеры обструкции общего желчного протока пробками из густой, вязкой желчи [7]. Образование сладжа зависит от физико-химического взаимодействия компонентов желчи (сложного раствора с многими составляющими), нарушения функции слизистой желчного пузыря и его моторики [6, 8]. В состав сладжа в первую очередь входят кристаллы моногидрата холестерина и билирубината кальция, взвешенные (или преципитированные) в слизи желчного пузыря. Кроме основных компонентов, сладж может включать другие соли кальция, протеин-липидные комплексы, муцин и ксенобиотики, в частности цефтриаксон [8]. Цефтриаксон экскретируется в мочу, но значительное его количество (от 30 до 60%) экскретируется в желчь как бивалентный анион [9], и в желчном пузыре его концентрация повышается в 20–150 раз [10]. Подобно билирубину, цефтриаксон может выпадать в осадок в виде комплексного соединения «кальций + цефтриаксон». Среди пациентов, получавших цефтриаксон, образование билиарного сладжа отмечается в 25–46% случаев [11].
Подобно билирубину, цефтриаксон может выпадать в осадок в виде комплексного соединения «кальций + цефтриаксон». Среди пациентов, получавших цефтриаксон, образование билиарного сладжа отмечается в 25–46% случаев [11].
Синдром сгущения желчи может разрешиться спонтанно (в 48,1% случаев, по данным E. Fitzpatrick et al.) или на фоне терапии урсодезоксихолиевой кислотой (УДХК), в 6,6% случаев имеет место образование камней в общем желчном протоке или в желчном пузыре, около 4% детей требуют оперативного вмешательства [3]. Билиарный сладж может иметь такие осложнения, как билиарные колики, острый панкреатит, острый холецистит [6].
Ведущими факторами риска синдрома сгущения желчи в 47% случаев являются гемолиз, сепсис и недоношенность.
Однако, кроме них, играют роль следующие [5, 6, 12–19]:
-
Низкая масса при рождении -
Парентеральное питание -
Дегидратация (назначение диуретиков) -
Гемотрансфузии -
Кистозный фиброз -
Врожденные заболевания сердца -
Интракраниальные, интраабдоминальные и ретроперитонеальные кровоизлияния -
Парез кишечника -
Длительное голодание, быстрая потеря массы -
Цефалоспорины III поколения (цефотаксим и цефтриаксон) -
Терапия октреотидом -
Трансплантация костного мозга или других органов
Среди перечисленных факторов риска особое место занимает парентеральное питание: доказано, что уже через 3 нед.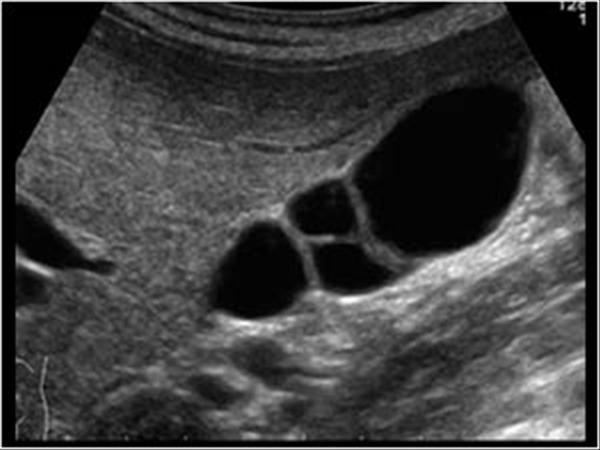 полного парентерального питания билиарный сладж выявляется не менее чем у 6% пациентов, через 4–6 нед.– у 50%, после 6 нед. – у 100% [20].
полного парентерального питания билиарный сладж выявляется не менее чем у 6% пациентов, через 4–6 нед.– у 50%, после 6 нед. – у 100% [20].
МЕТОДЫ ДИАГНОСТИКИ БИЛИАРНОГО СЛАДЖА
Для подтверждения синдрома сгущения желчи или выявления его ранних признаков используются инструментальные методы, в первую очередь УЗИ. Основными признаками синдрома сгущения желчи являются умеренная дилатация интрапеченочных отделов билиарного тракта, увеличение диаметра общего желчного протока (иногда до 12,3 мм), густая вязкая желчь (осадок низкой эхогенности) в желчном пузыре и желчных протоках (рис. 1) [3, 5].
Рисунок 1. Синдром сгущения желчи. Дилатация общего желчного протока. Билиарный сладж в общем желчном протоке [21]
Figure 1. Bile thickening syndrome. Dilatation of the common bile duct. Biliary sludge in the common bile duct [21]
Диаметр общего желчного протока у детей первых 3 мес. жизни не должен превышать 1–1,2 мм. Как показали результаты УЗИ, проанализированных E. Fitzpatrick в 2010 г. у 878 детей первых трех месяцев жизни с холестазом, дилатация общего желчного протока более 1,2 мм (от 1,2 до 12,3 мм) была обнаружена в 9% случаев. На долю детей с синдромом сгущения желчи в этой группе приходилось 71,1%. Доказано, что дилатация общего желчного протока более 3 мм характерна для синдрома сгущения желчи (чувствительность 100% и специфичность 87%). Ниже мы приводим ультразвуковые признаки изменения желчи, полностью подтверждающие дословный перевод термина “Inspissated bile syndrome” – синдром «грязной желчи» (исследование проведено врачом отделения лучевой диагностики больницы им. З.А. Башляевой Ю.А. Бронниковой). На фотографиях с монитора (рис. 2А) видно, что содержимое желчного пузыря неоднородно, при внимательном осмотре обращает внимание осадок в области дна. Использование более чувствительного датчика и увеличение изображения на экране монитора (рис.
жизни не должен превышать 1–1,2 мм. Как показали результаты УЗИ, проанализированных E. Fitzpatrick в 2010 г. у 878 детей первых трех месяцев жизни с холестазом, дилатация общего желчного протока более 1,2 мм (от 1,2 до 12,3 мм) была обнаружена в 9% случаев. На долю детей с синдромом сгущения желчи в этой группе приходилось 71,1%. Доказано, что дилатация общего желчного протока более 3 мм характерна для синдрома сгущения желчи (чувствительность 100% и специфичность 87%). Ниже мы приводим ультразвуковые признаки изменения желчи, полностью подтверждающие дословный перевод термина “Inspissated bile syndrome” – синдром «грязной желчи» (исследование проведено врачом отделения лучевой диагностики больницы им. З.А. Башляевой Ю.А. Бронниковой). На фотографиях с монитора (рис. 2А) видно, что содержимое желчного пузыря неоднородно, при внимательном осмотре обращает внимание осадок в области дна. Использование более чувствительного датчика и увеличение изображения на экране монитора (рис.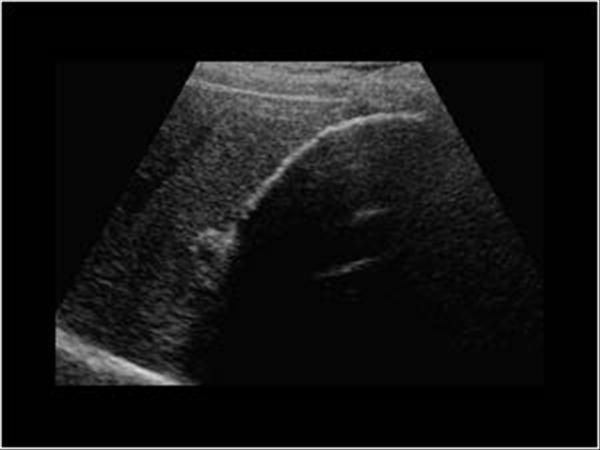 2B) позволяет более четко рассмотреть наличие осадка в желчном пузыре и подтвердить наличие синдрома сгущения желчи [22, 23].
2B) позволяет более четко рассмотреть наличие осадка в желчном пузыре и подтвердить наличие синдрома сгущения желчи [22, 23].
Рисунок 2. УЗИ органов брюшной полости. Синдром сгущения желчи у девочки с врожденным пороком сердца
Figure 2. Abdominal ultrasound imaging. Bile thickening syndrome in a girl with congenital heart disease
А – в области дна желчного пузыря и частично стенок взвесь со слабой эхогенностью; В – изображение выполнено с помощью более чувствительного датчика, хорошо определяется неоднородная взвесь в просвете желчного пузыря (выполнено Ю.А. Бронниковой, врачом отделения лучевой диагностики больницы им. З.А. Башляевой).
В диагностически трудных случаях для подтверждения синдрома сгущения желчи проводится магнитнорезонансная холангиография [1]. В пользу синдрома сгущения желчи свидетельствуют маленький желчный пузырь, диффузная дилатация интрапеченочных и экстрапеченочных желчных протоков, резкое сужение общего желчного протока после зоны дилатации (рис.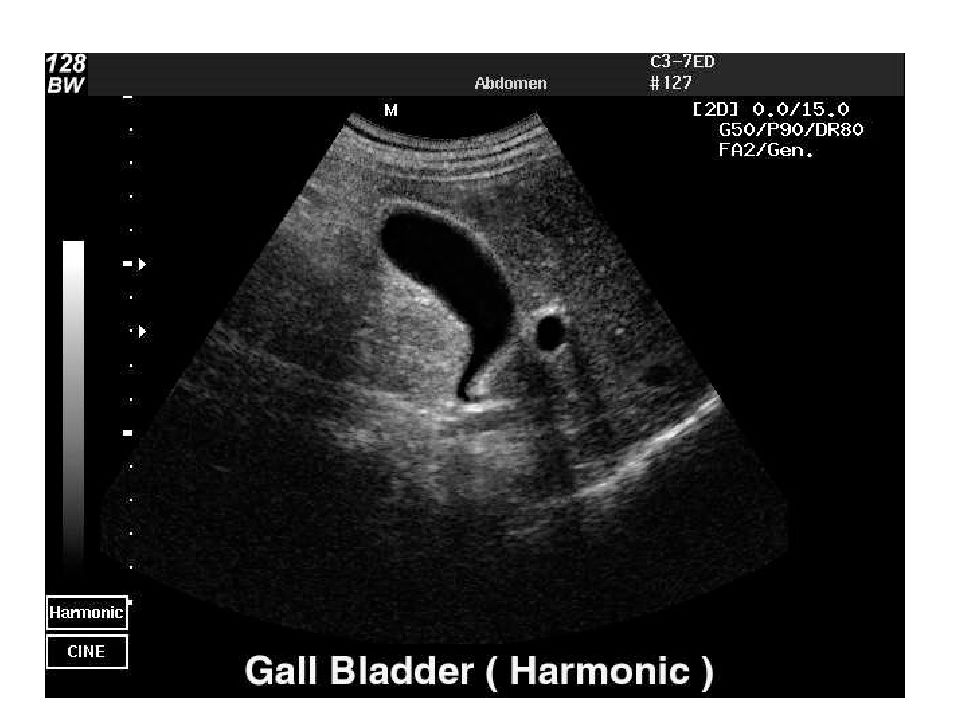 3).
3).
Рисунок 3. Синдром сгущения желчи
Figure 3. Bile thickening syndrome
УЗИ (А, В): умеренная дилатация интрапеченочных желчных протоков, дилатированный общий желчный проток, заполненный неоднородной эхогенной массой. Магнитно-резонансная холангиография (С): маленький желчный пузырь, умеренная дилатация интра- и экстрапеченочных желчных протоков, внезапный обрыв общего желчного протока, отсутствие пассажа желчи в двенадцатиперстную кишку [1].
Для диагностики синдрома сгущения желчи используется также и интраоперативная холангиография через пунктированный желчный пузырь, позволяющая выявить полную обструкцию общего желчного протока с дилатацией пузырного протока и печеночного протока (рис. 4).
Рисунок 4. Синдром сгущения желчи. Чрескожная холецистохолангиография через пунктированный желчный пузырь. Дилатация и обрыв общего желчного протока и умеренная дилатация интрапеченочных желчных протоков [24, 25]
Figure 4. Bile thickening syndrome. Percutaneous cholecystocholangiography via a gallbladder puncture. Dilatation and rupture of the common bile duct and moderate dilatation of the intrahepatic bile ducts [24, 25]
Bile thickening syndrome. Percutaneous cholecystocholangiography via a gallbladder puncture. Dilatation and rupture of the common bile duct and moderate dilatation of the intrahepatic bile ducts [24, 25]
Терапия синдрома сгущения желчи у детей раннего возраста включает хирургические и консервативные методы. В оперативном лечении, позволяющем восстановить пассаж желчи в двенадцатиперстную кишку, нуждаются менее 4% детей с синдромом сгущения желчи (рис. 4). Исторически первым хирургическим вмешательством была лапаротомия с последующей ирригацией через доступ в общий желчный проток или желчный пузырь, выполненная W.E. Ladd в 1935 г. [7, 26].
В настоящее время существуют два основных варианта оперативного лечения билиарного сладжа: открытый хирургический дренаж с последующим лаважем желчных протоков физиологическим раствором и урсодезоксихолевой кислотой (УДХК) и чрескожная пункция желчного пузыря под контролем УЗИ с проведением холецистографии и дренированием желчных протоков [1, 4, 13, 21, 25–30].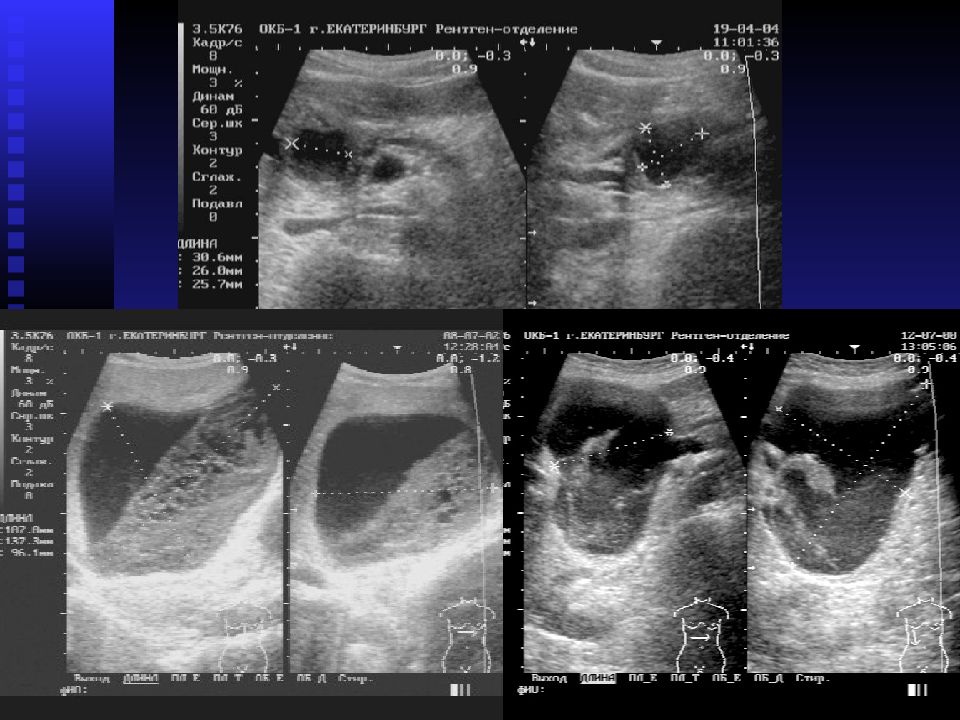 С целью предупреждения утечки желчи нередко используется чрескожная транспеченочная пункция желчного пузыря [13, 21, 26, 30]
С целью предупреждения утечки желчи нередко используется чрескожная транспеченочная пункция желчного пузыря [13, 21, 26, 30]
Показаниями для консультации хирургом и решения вопроса об оперативном лечении ребенка с синдромом сгущения желчи являются:
-
Дилатация общего желчного протока более 3 мм [1, 3] -
Персистирующая желтуха и изменения в биохимическом анализе крови: нарастание уровня ферментов АЛТ и АСТ, щелочной фосфатазы, общего и прямого билирубина, ГГТП [1, 25] -
Отсутствие эффекта от проводимой консервативной терапии
Оперативное лечение позволяет полностью восстановить пассаж желчи в двенадцатиперстную кишку (рис. 5).
Рисунок 5. Полное восстановление пассажа желчи в двенадцатиперстную кишку после успешного оперативного лечения билиарного сладжа: изменение окраски стула в течение 5 дней [25]
Figure 5. Complete restoration of the bile passage into the duodenum after successful surgical treatment of biliary sludge: stool discoloration within 5 days [25]
Недостатками оперативного вмешательства являются осложнения и необходимость длительного доступа (в среднем 26 дней) к желчным протокам для их дренирования и лаважа [13]. Одним из частых осложнений (до 50% случаев) считается смещение катетера, требующее его переустановки [13], кроме этого, возможны кровотечения, билиарный перитонит и другие инфекции [26].
Одним из частых осложнений (до 50% случаев) считается смещение катетера, требующее его переустановки [13], кроме этого, возможны кровотечения, билиарный перитонит и другие инфекции [26].
Консервативная терапия синдрома сгущения желчи у новорожденных и детей раннего возраста. Принципы консервативной терапии синдрома сгущения желчи в первую очередь включают анализ проводимой медикаментозной терапии и исключение из нее средств, способных вызвать сгущение желчи. Новорожденным, находящимся на искусственном вскармливании, рекомендуется назначение адаптированных смесей, обогащенных среднецепочечными триглицеридами. Обязательным является назначение УДХК 20–30 мг/кг/сут, жирорастворимых витаминов (табл. 1) [6, 19, 24].
Таблица 1. Дозы жирорастворимых витаминов у новорожденных и детей раннего возраста c холестазом (C. Dani et al., 2015 г.) [31]
Table 1. Doses of fat-soluble vitamins in newborns and young children with cholestasis (C. Dani et al., 2015) [31]
Dani et al., 2015) [31]
|
Витамин |
Доза |
|---|---|
|
A |
5000–25000 ед/сут |
|
D |
800–5000 ед/сут |
|
E |
15–25 ед/кг/сут |
|
K |
2,5–5 мг дважды в неделю, возможен ежедневный прием |
В качестве альтернативы инвазивному хирургическому вмешательству рекомендуется использование полиненасыщенных жирных кислот (рис. 6), например 20%-ной жировой эмульсии для парентерального питания SMOFlipid [32]. В 1000 мл SMOFlipid содержится 60 г очищенного масла соевых бобов, 60 г среднецепочечных триглицеридов, 50 г очищенного оливкового масла, 30 г рыбьего жира, обогащенного омега-3 полиненасыщенными жирными кислотами (α-линоленовой, эйкозапентаеновой и докозагексаеновой).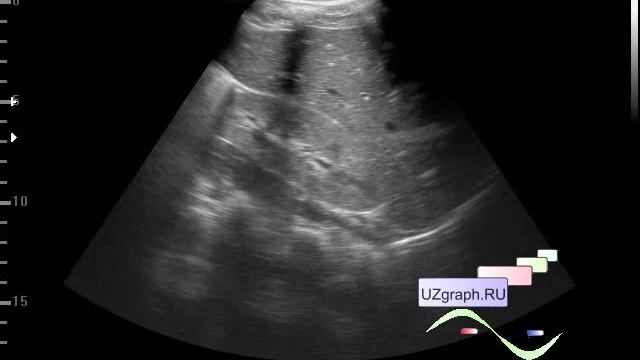
Теоретическая осмолярность эмульсии составляет 380 мосм/кг, биоусвояемость – 100%, по размерам частиц и биологическим свойствам SMOFlipid идентична эндогенным хиломикронам. Каждые 200 г жира в литре 20%-ной эмульсии SMOFlipid содержат 0,6 г α-линоленовой, 0,6 г эйкозапентаеновой и 0,1 г докозагексаеновой кислот. W.Y. Jun et al. [32] рекомендуют одновременное назначение УДХК 20 мг/кг/сут и жировой эмульсии 1,5 г/кг/сут в течение 3 нед. Скорость внутривенного введения жировой эмульсии 1 мл/ч [32].
Рисунок 6. Пассаж желчи в двенадцатиперстную кишку после 3-недельной консервативной терапии УДХК и 20%-ной жировой эмульсией SMOFlipid [32]
Figure 6. Bile passage into the duodenum after 3 weeks of conservative therapy with UDCA and SMOFlipid 20% lipid emulsion [32]
Полиненасыщенные жирные кислоты могут назначаться внутрь в капсулах (препарат Omacor, W.Y. Jun et al.) как замена внутривенному введению жировой эмульсии. Каждая капсула Omacor содержит 460 мг этилового эфира эйкозапентаеновой и 380 мг этилового эфира докозагексаеновой кислоты. Согласно рекомендациям [32], новорожденным и детям раннего возраста с синдромом сгущения желчи рекомендуется по ½ капсулы Omacor 4 раза в день в течение 3–4 мес. Авторы исследования [32] считают, что омега-3 полиненасыщенные жирные кислоты могут играть роль холеретиков. Механизм действия полиненасыщенных жирных кислот включает улучшение клиренса липидов, индукцию окисления печеночных жирных кислот, модуляцию воспаления и метаболизм желчных кислот [33–35].
Каждая капсула Omacor содержит 460 мг этилового эфира эйкозапентаеновой и 380 мг этилового эфира докозагексаеновой кислоты. Согласно рекомендациям [32], новорожденным и детям раннего возраста с синдромом сгущения желчи рекомендуется по ½ капсулы Omacor 4 раза в день в течение 3–4 мес. Авторы исследования [32] считают, что омега-3 полиненасыщенные жирные кислоты могут играть роль холеретиков. Механизм действия полиненасыщенных жирных кислот включает улучшение клиренса липидов, индукцию окисления печеночных жирных кислот, модуляцию воспаления и метаболизм желчных кислот [33–35].
КЛИНИЧЕСКИЙ СЛУЧАЙ
Девочка Г. родилась на 29-й нед. гестации с массой 900,0 г и оценкой по шкале Апгар 3/5 баллов. Неонатальный и кардиоскрининг отрицательные, группа крови 0(I) первая, Rh (+), фенотип CcDEe, Kell отрицательный.
Матери ребенка 23 года, беременность первая, протекавшая с токсикозом в первом триместре и гестозом. Роды оперативные (экстренное кесарево сечение из-за нарастающей гипоксии плода), в ягодичном предлежании. Околоплодные воды светлые. Группа крови матери 0(I), Rh (+). Во время беременности у матери ребенка выявлен высокий титр антител класса IgG к токсоплазме и CMV.
Околоплодные воды светлые. Группа крови матери 0(I), Rh (+). Во время беременности у матери ребенка выявлен высокий титр антител класса IgG к токсоплазме и CMV.
Состояние новорожденной при рождении очень тяжелое. Тяжесть состояния обусловлена синдромом дыхательных расстройств 1-го типа, сразу же интубирована, начата ИВЛ. Спустя 6 мин. после начала ИВЛ переведена в отделение реанимации и интенсивной терапии. Там эндотрахеально введен сурфактант. На 6-е сут. жизни была переведена на осциллаторную ИВЛ, на которой находилась до 23 сут. жизни. В отделении реанимации отмечалось однократное повышение СРБ до 220,9 мг/л, постоянно регистрировалось повышение щелочной фосфатазы (от 871 до 1500 ед/л), АлАт и АсАт были в пределах нормы.
В возрасте 1 мес. 10 дней девочка переведена из отделения реанимации и интенсивной терапии в отделение для новорожденных №2 ДГКБ им. З.А. Башляевой в состоянии средней степени тяжести с диагнозом «Недоношенность 29 нед. Постконцептуальный возраст 35–36 нед.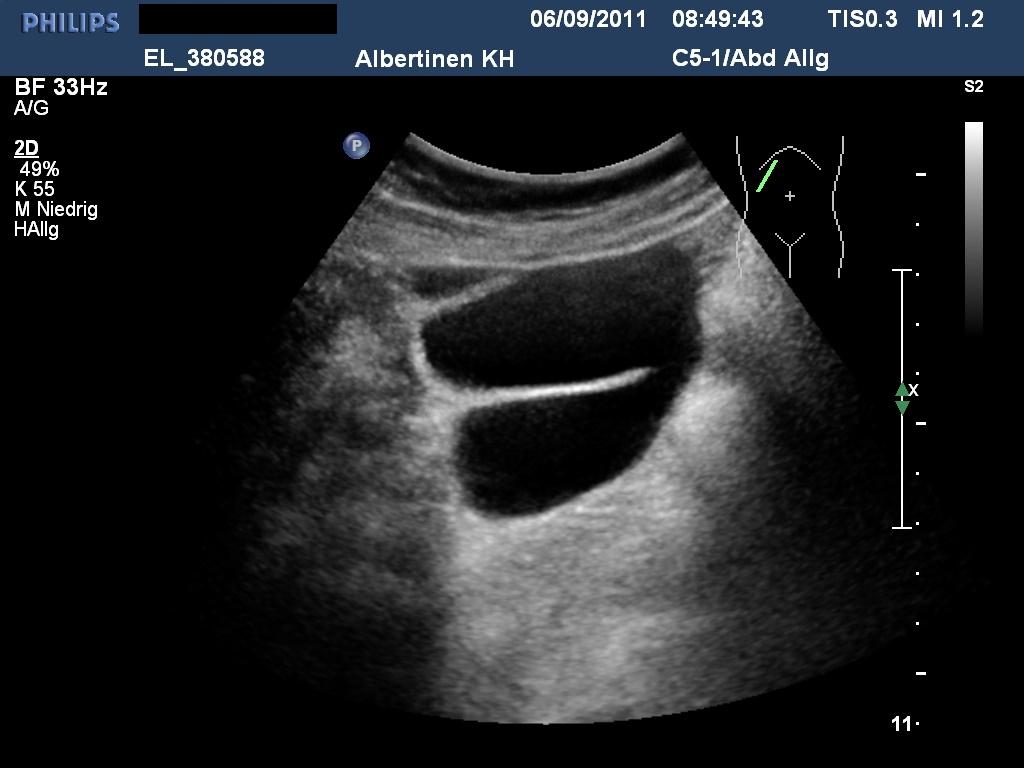 Бронхолегочная дисплазия, новая форма, среднетяжелое течение. ДН 0–1-й степени. Гипоксическиишемическое поражение ЦНС I–II степени, синдром угнетения безусловно-рефлекторной деятельности, синдром вегетовисцеральной дисфункции. Врожденная пневмония, реконвалесцент. Функционирующие фетальные коммуникации: открытый артериальный проток. Открытое овальное окно. НК-0. Анемия недоношенных. Неонатальная тромбоцитопения. Транзиторная неонатальная гипогликемия».
Бронхолегочная дисплазия, новая форма, среднетяжелое течение. ДН 0–1-й степени. Гипоксическиишемическое поражение ЦНС I–II степени, синдром угнетения безусловно-рефлекторной деятельности, синдром вегетовисцеральной дисфункции. Врожденная пневмония, реконвалесцент. Функционирующие фетальные коммуникации: открытый артериальный проток. Открытое овальное окно. НК-0. Анемия недоношенных. Неонатальная тромбоцитопения. Транзиторная неонатальная гипогликемия».
Вес при поступлении в отделение 2000,0 г. Кожные покровы розовые, стул окрашен.
Терапия в отделении для новорожденных больницы им. З.А. Башляевой
- Лечебно-охранительный режим (находится в условиях термокроватки)
- Энтеральное кормление (соска/зонд) каждые 3 ч по 45–50 мл сцеженным грудным молоком, докорм смесью «ПреНАН»
- Элькар 30% по 5 капель 3 раза в сутки per os
- Витамин Д3 по 2 капли (1000 МЕ) х 1 раз в сутки. Мальтофер 5 мг/кг/сут (4 капли х 1 раз в сутки)
- Витамин Е 10% 2 капли х 1 раз в сутки
- Фолиевая кислота 50 мкг х 1 раз в сутки
В больнице им. З.А. Башляевой состояние средней тяжести, назначенный объем питания усваивает, кожные покровы розовые, стул окрашен. Однако, учитывая наличия факторов риска синдрома сгущения желчи (экстремально низкая масса при рождении, гестационный возраст 29 нед.) и имеющиеся ранее в отделении реанимации признаки холестаза (постоянное повышение щелочной фосфатазы), для исключения билиарного сладжа на 11-й день госпитализации проведено УЗИ органов брюшной полости.
З.А. Башляевой состояние средней тяжести, назначенный объем питания усваивает, кожные покровы розовые, стул окрашен. Однако, учитывая наличия факторов риска синдрома сгущения желчи (экстремально низкая масса при рождении, гестационный возраст 29 нед.) и имеющиеся ранее в отделении реанимации признаки холестаза (постоянное повышение щелочной фосфатазы), для исключения билиарного сладжа на 11-й день госпитализации проведено УЗИ органов брюшной полости.
По данным УЗИ желчный пузырь овальной формы, размером 26 х 6 мм, объемом 0,5 мл. Имеется лабильный перегиб в области тела и шейки, стенки утолщены до 2 мм, слоистые, повышенной эхогенности, в просвете гиперэхогенное содержимое (замазкообразная желчь). Наличие замазкообразной желчи позволило сделать вывод о наличии синдрома сгущения желчи. Сразу же после УЗИ назначена урсодезоксихолевая кислота (УДХК) 20 мг/кг/сут. В этот же день взята кровь для проведения биохимического анализа крови. В биохимическом анализе крови выявлено незначительное повышение уровня общего билирубина и щелочной фосфатазы (табл. 2). Оставлена назначенная доза УДХК (20 мг/кг/сут).
2). Оставлена назначенная доза УДХК (20 мг/кг/сут).
Таблица 2. Биохимический анализ крови на 11-й день госпитализации
Table 2. Biochemical blood test on Day 11 of hospitalization
|
Показатель |
Результат |
Норма |
|---|---|---|
|
Общий билирубин |
27 мкмоль/л |
1,7–21 |
|
Прямой билирубин |
5 мкмоль/л |
0–5 |
|
АсАт |
36 ед/л |
0–35 |
|
АлАт |
15 ед/л |
0–45 |
|
ЛДГ |
576 ед/л |
0–430 |
|
Щелочная фосфатаза |
788 ед/л |
0–727 |
|
Глюкоза |
5,3 ммоль/л |
1,9–5,5 |
|
ГГТП |
179 ед/д |
0–200 |
|
СРБ |
9 мг/л |
0–10 |
Спустя 10 дней от начала терапии УДХК на 21-й день госпитализации ребенка в больницу им. З.А. Башляевой повторно проведено УЗИ органов брюшной полости.
З.А. Башляевой повторно проведено УЗИ органов брюшной полости.
Результаты повторного УЗИ
Желчный пузырь овальной формы, размерами 30 х 5 мм, объемом 0,4 мл. Имеется лабильный перегиб в области тела и шейки. Стенки неравномерной толщины, максимум до 1,5 мм, повышенной эхогенности, в просвете желчного пузыря гиперэхогенные включения до 3 мм в диаметре, без акустической дорожки, контуры неровные, нечеткие (замазкообразная желчь). Общий желчный проток диаметром до 5 мм, прослеживается на расстоянии до 20 мм, стенки неровные, нечеткие, просвет гипоэхогенный.
Полученные результаты (наличие в просвете желчного пузыря гиперэхогенных включений без акустической дорожки с нечеткими контурами, увеличение диаметра общего желчного протока до 5 мм) позволили подтвердить наличие синдрома сгущения желчи. Следует обратить внимание, что окраска стула в день повторного проведения УЗИ была обычной, но, учитывая отрицательную динамику по данным УЗИ, в этот же день доза УДХК была увеличена до 30 мг/кг/сут.
На следующий день после проведения УЗИ и увеличения дозы УДХК у ребенка появился ахоличный стул (рис. 7). В этот же день был взят биохимический анализ крови (табл. 3).
Таблица 3. Биохимический анализ крови на 21-й день госпитализации
Table 3. Biochemical blood test on Day 21 of hospitalization
|
Показатель |
Результат |
Норма |
|---|---|---|
|
Общий билирубин |
46 мкмоль/л |
1,7–21 |
|
Прямой билирубин |
21 мкмоль/л |
0–5 |
|
АсАт |
50 ед/л |
0–35 |
|
АлАт |
21 ед/л |
0–45 |
|
ЛДГ |
608 ед/л |
0–430 |
|
Щелочная фосфатаза |
744 ед/л |
0–727 |
|
Глюкоза |
4,6 ммоль/л |
1,9–5,5 |
|
ГГТП |
189 ед/д |
0–200 |
|
СРБ |
37,7 мг/л |
0–10 |
В биохимическом анализе крови выявлена отрицательная динамика: конъюгированная гипербилирубинемия (общий билирубин 46 мкмоль/л, прямой билирубин 31 мкмоль/л), сохранялось повышение щелочной фосфатазы. В связи с появлением ахоличного стула, увеличением диаметра общего желчного протока более 3 мм (в нашем случае до 5 мм), нарастанием холестаза, несмотря на проводимую терапию УДХК, девочка была осмотрена детским хирургом для решения вопроса о необходимости оперативного лечения.
В связи с появлением ахоличного стула, увеличением диаметра общего желчного протока более 3 мм (в нашем случае до 5 мм), нарастанием холестаза, несмотря на проводимую терапию УДХК, девочка была осмотрена детским хирургом для решения вопроса о необходимости оперативного лечения.
Рисунок 7. Ахоличный стул у девочки 2 мес. с синдромом сгущения желчи
Figure 7. Acholic stool in a 2-month-old girl with bile thickening syndrome
Учитывая отсутствие синдрома гепатоцитолиза, незначительное повышение общего билирубина, снижение щелочной фосфатазы по сравнению с предыдущим анализом и нормальный уровень ГГТП, было принято решение о продолжении консервативной терапии (УДХК) и наблюдении за ребенком в динамике. На второй день после увеличения дозы УДХК появилось окрашивание стула, на третий день окраска стала более интенсивной.
Терапия УДХК была продолжена в дозе 30 мг/кг/сут. Спустя две недели ребенок был выписан домой в удовлетворительном состоянии без признаков синдрома сгущения желчи. Представленный клинический случай демонстрирует раннюю диагностику синдрома сгущения желчи и его благоприятный исход у 2-месячного ребенка на фоне терапии УДХК без оперативного вмешательства.
ЗАКЛЮЧЕНИЕ
Синдром сгущения желчи относится к редким причинам холестаза у новорожденных и детей раннего возраста, в некоторых случаях требующим оперативного вмешательства. Знание факторов риска билиарного сладжа позволяет своевременно назначить инструментальное обследование, в первую очередь УЗИ, обеспечить раннюю диагностику синдрома сгущения желчи и назначение консервативной терапии, исключить хирургические методы лечения.
Список литературы / References
- G1. Chen S.M., Liao Y.Y., Lin C.P. Inspissated bile syndrome: A rare cause of neonatal cholestasis. Pediatr Neonatol. 2020;61(4):449-450. https://doi.org/10.1016/j.pedneo.2020.03.002.
- Gottesman L.E., Del Vecchio M.T., Aronoff S.C. Etiologies of conjugated hyperbilirubinemia in infancy: a systematic review of 1692 subjects. BMC Pediatrics. 2015;15:192. https://doi.org/10.1186/s12887-015-0506-5.
- Fitzpatrick F., Jardine R., Farrant P., Karani J., Davenport M., Mieli-Vergani G., Baker A. Predictive Value of Bile Duct Dimensions Measured by Ultrasound in Neonates Presenting With Cholestasis. J Pediatr Gastroenterol Nutr. 2010;51(1):55-60. https://doi.org/10.1097/MPG.0b013e3181d1b226.
- Davenport M., Betalli P., D’Antiga L., Cheeseman P., Mieli-Vergani G., Howard E.R. The spectrum of surgical jaundice in infancy. J Pediatr Surg. 2003;38(10):1471-1479. https://doi.org/10.1016/s0022-3468(03)00498-6.
- Gubernick J.A., Rosenberg H.K., Ilaslan H., Kessler A. US approach to jaundice in infants and children. Radiographics. 2000;20(1):173-195. https://doi.org/10.1148/radiographics.20.1.g00ja25173.
- Ko C.W., Sekijim J.H., Lee S.P. Biliary sludge. Ann Intern Med. 1999; 130(4 Pt. 1):301-311. https://doi.org/10.7326/0003-4819-130-4-199902160-00016.
- Ladd W.E. Congenital obstruction of the bile ducts. Annals of Surgery. 1935;102(4):742-751. https://doi.org/10.1097/00000658-193510000-00021.
- Ko C.W., Murakami C., Sekijima J.H., Kim M.H., McDonald G.B., Lee S.P. Chemical composition of gallbladder sludge in patients after marrow transplantation. Am J Gastroenterol. 1996;91(6):1207-1210. Available at: https://pubmed.ncbi.nlm.nih.gov/8651172.
- Kim Y.S., Kestell M.F., Lee SP. Gall-bladder sludge: lessons from ceftriaxone. J Gastroenterol Hepatol. 1992;7(6):618-621. https://doi.org/10.1111/j.1440-1746.1992.tb01496.x.
- Park H.Z., Lee S.P., Schy A.L. Ceftriaxone-associated gallbladder sludge. Identification of calcium-ceftriaxone salt as a major component of gallbladder precipitate. Gastroenterology. 1991;100(6):1665-1670. https://doi.org/10.1016/0016-5085(91)90667-A.
- Shiffman M.L., Keith F.B., Moore E.W. Pathogenesis of ceftriaxone-associated biliary sludge. in vitro studies of calcium-ceftriaxone binding and solubility. Gastroenterology. 1990;99(6):1772-1778. https://doi.org/10.1016/0016-5085(90)90486-k.
- Володин Н.Н., Мухина Ю.Г., Чубарова А.И. (ред.). Неонатология. В: Володин Н.Н., Мухина Ю.Г. (ред.). Детские болезни. М.: Династия; 2011. Т. 1. 512 с.
- Bollu B.K., Dawrant M.J., Thacker K., Thomas G., Chenapragadda M., Gaskin K., Shun A. Inspissated bile syndrome; Safe and effective minimally invasive treatment with percutaneous cholecystostomy in neonates and infants. J Pediatr Surg. 2016;51(12):2119-2122. https://doi.org/10.1016/j.jpedsurg.2016.09.053.
- Miloh T., Rosenberg H.K., Kochin I., Kerkar N. Inspissated bile syndrome in a neonate treated with cefotaxime: sonographic aid to diagnosis, management, and follow-up. J Ultrasound Med. 2009;28(4):541-544. https://doi.org/10.7863/jum.2009.28.4.541.
- Rozmanic V., Banac S., Ivosevic D., Cace N. Biliary colic and sonographic evidence of pseudocholelithiasos 36 h after treatment with ceftriaxone. J Paediatr Child Health. 2006;42(10):658-661. Available at: https://www.researchgate.net/publication/6818041_Biliary_colic_and_sonographic_evidence_of_pseudocholelithiasos_36_h_after_treatment_with_ceftriaxone.
- Schaad U.B., Tschäppeler H., Lentze M.J. Transient formation of precipitations in the gallbladder associated with ceftriaxone therapy. Pediatr Infect Dis. 1986;5(6):708-710. https://doi.org/10.1097/00006454-198611000-00026.
- Bor O., Dinleyici E.C., Kebapci M., Aydogdu S.D. Ceftriaxone-associated biliary sludge and pseudocholelithiasis during childhood: a prospective study. Pediatr Int. 2004;46(3):322-344. https://doi.org/10.1111/j.1328-0867.2004.01884.x.
- Klar A., Branski D., Akerman Y., Nadjari M., Berkun Y., Moise J. et al. Sludge ball, pseudolithiasis, cholelithiasis and choledocholithiasis from intrauterine life to 2 years: a 13-year follow- up. J Pediatr Gastroenterol Nutr. 2005;40(4):477-480. https://doi.org/10.1097/01.mpg.0000151749.01631.21.
- Jain A., Poddar U., Elhence P., Tripathi A., Shava U., Yachha S.K. Cholestasis in a neonate with ABO haemolytic disease of newborn following transfusion of ABO group-specific red cells compatible with neonatal serum: inspissated bile syndrome. Blood Transfus. 2014;12(4):621-623. https://doi.org/10.2450/2014.0099-14.
- Messing B., Bories C., Kuntslinger F., Bernier J.J. Does total parenteral nutrition induce gallbladder sludge formation and lithiasis? Gastroenterology. 1983;84(5 Pt. 1):1012-1019. Available at: https://pubmed.ncbi.nlm.nih.gov/6403401.
- Chang S.H., Joo S.M., Yoon C.S., Lee K.H., Lee S.M. Percutaneous Transhepatic Biliary Drainage in a Two-Month-Old Infant with Inspissated Bile Syndrome. Yonsei Med J. 2018;59(7):904-907. https://doi.org/10.3349/ymj.2018.59.7.904.
- Hernanz-Schulman M., Ambrosino M.M., Freeman P.C., Quinn C.B. Common bile duct in children: sonographic dimensions. Radiology. 1995;195(1):193-195. https://doi.org/10.1148/radiology.195.1.7892467.
- Carroll B.A., Oppenheimer D.A., Muller H.H. High-frequency real-time ultrasound of the neonatal biliary system. Radiology. 1982;145(2):437-440. https://doi.org/10.1148/radiology.145.2.7134449.
- Heaton N.D., Davenport M., Howard E.R. Intraluminal biliary obstruction. Arch Dis Child. 1991;66(12):1395-1398. https://doi.org/10.1136/adc.66.12.1395.
- Berger S., Schibli S., Stranzinger E., Cholewa D. One-stage laparoscopic surgery for inspissated bile syndrome: case report and review of surgical techniques. Springerplus. 2013;2:648. https://doi.org/10.1186/2193-1801-2-648.
- Sideeka N, Shaikh R, Chaudry G. Single Procedure Saline Lavage for Treatment of Inspissated Bile. Case Rep Radiol. 2020;2020:8816599. https://doi.org/10.1155/2020/8816599.
- Gunnarsdóttir A, Holmqvist P, Arnbjörnsson E, Kullendorff CM. Laparoscopic aided cholecystostomy as a treatment of inspissated bile syndrome. J Pediatr Surg. 2008;43(4):e33-e55. https://doi.org/10.1016/j.jpedsurg.2007.12.068.
- Gao Z.G., Shao M., Xiong Q.X., Tou J.F., Liu W.G. Laparoscopic cholecystostomy and bile duct lavage for treatment of inspissated bile syndrome: a single-center experience. World J Pediatr. 2011;7(3):269-271. https://doi.org/10.1007/s12519-011-0321-5.
- Lieber J., Piersma F.E., Sturm E. et al. Surgical treatment of inspissated bile syndrome using a 2-stage pure laparoscopic approach: a case report. J Pediatr Surg. 2012; 47(12):e47-50. https://doi.org/10.1016/j.jpedsurg.2012.09.043.
- Helin R., Bhat R., Rao B. Ultrasound-guided percutaneous cholecystostomy for acute neonatal biliary obstruction. Neonatology. 2007;91(4):266-270. https://doi.org/10.1159/000098174.
- Dani C., Pratesi S., Raimondi F., Romagnoli C. Italian guidelines for the management and treatment of neonatal cholestasis. Ital J Pediatr. 2015;:41:69. https://doi.org/10.1186/s13052-015-0178-7.
- Jun W.Y., Cho M.J., Han H.S., Bae S.H. Use of Omega-3 Polyunsaturated Fatty Acids to Treat Inspissated Bile Syndrome: A Case Report. Pediatr Gastroenterol Hepatol Nutr. 2016;19(4):286-290. https://doi.org/10.5223/pghn.2016.19.4.286.
- Jonkers I.J., Smelt A.H., Princen H.M., Kuipers F., Romijn J.A., Boverhof R. et al. Fish oil increases bile acid synthesis in male patients with hypertriglyceridemia. J Nutr. 2006;136(4):987-991. https://doi.org/10.1093/jn/136.4.987.
- Bae S.H., Park H.S., Han H.S., Yun I.J. Omega-3 polyunsaturated fatty acid for cholestasis due to bile duct paucity. Pediatr Gastroenterol Hepatol Nutr. 2014;17(2):121-124. https://doi.org/10.5223/pghn.2014.17.2.121.
- Nandivada P., Carlson S.J., Chang M.I., Cowan E., Gura K.M., Puder M. Treatment of parenteral nutrition-associated liver disease: the role of lipid emulsions. Adv Nutr. 2013;4(6):711-717. https://doi.org/10.3945/an.113.004770.
Симптомы дискинезии желчевыводящих путей и холецистита у детей
Дискинезия — это нарушение оттока желчи по желчевыводящим путям.
Выделяют два типа нарушения моторики желчевыводящих путей:
- Гиперкинетический (когда усилены сокращения желчного пузыря).
- Гипокинетический (когда стенки пузыря и протоков расслаблены, а отток желчи замедлен).
Причины заболевания
- Перенесенный гепатит
- Кишечные инфекции
- Лямблиоз
- Гельминтоз
- Аномалии развития желчного пузыря и желчных протоков и др.
Симптомы
Симптомы при гиперкинетической дискинезии:
- Интенсивная приступообразная боль в правом подреберье, иногда отдающая в правое плечо и лопатку. Боль появляется из-за погрешности в диете, физической нагрузки, стрессовой ситуации.
- Тошнота, реже рвота. Болевой приступ более выражен при сочетании этой формы с гипертонией сфинктеров.
Симптомы при гипокинетической дискинезии:
- Постоянная, неинтенсивная боль в правом подреберье, сопровождающаяся чувством переполнения, тяжести в животе, тошнотой, привкусом горечи во рту, снижением аппетита.
- Нарушения стула (запор или диарея).
- Иногда изменяется цвет кала: он становится светлым.
- Опасность гипокинезии желчного пузыря заключается в том, что при застое желчи усиливается всасывание жидкости и водорастворимых веществ, повышается концентрация холестерина и билирубина в желчи, что способствует образованию сгустков, а в дальнейшем и камней в желчном пузыре.
Методы диагностики при дискинезии
С помощью УЗИ желчного пузыря оценивается форма, размеры, деформации желчного пузыря, состояние протоков, наличие камней.
Дуоденальное зондирование у детей с дискинезией желчевыводящих путей позволяет оценить объем порций желчи, ее микроскопический и биохимический состав. При исследовании дуоденального содержимого могут быть обнаружены признаки воспаления, склонность к формированию камней, лямблии и др.
Своевременная диагностика и адекватное лечение дискинезии с учетом ее типа позволяет нормализовать процессы желчеотведения и пищеварения, предупредить воспаление и раннее камнеобразование в желчевыводящих путях у детей. Длительное нарушение в работе желчевыводящей системы может приводить к развитию холецистита, холангита, желчнокаменной болезни, дисбактериоза кишечника.
Результаты анализа крови также свидетельствуют о наличии в организме воспалительного процесса. В таких случаях ребенка нередко необходимо госпитализировать, чтобы провести обследование и назначить правильное лечение.
Профилактика
Дети с дискинезией желчевыводящих путей нуждаются в диспансерном наблюдении педиатра, детского невролога и гастроэнтеролога, контроле УЗИ, проведении курсов желчегонной терапии дважды в год, оздоровительном отдыхе в специализированных санаториях. Необходимо следить за питанием и режимом ребенка, его эмоциональным состоянием.
Подробнее о детской гастроэнтерологии в клинике «ЮгМед»
причины, симптомы и эффективное лечение
Деформация желчного пузыря у ребенка выявляется после рождения или в подростковом возрасте. Заболевание характеризуется нарушениями выделения желчи и диспепсическими симптомами: тошнота, боль, рвота и др. При своевременном выявлении болезни прогноз благоприятный. Комплексный подход к лечению, основанный на применении лекарственных средств и соблюдении диеты, позволяет устранить проявления патологии.
Основные причины
Деформация желчного пузыря у ребенка: симптомы и лечение
К причинам деформации желчного пузыря в детском возрасте относят несколько факторов. Как правило, все случаи патологии могут иметь наследственный или приобретенный характер. Это влияет на клинические проявления и подходы к терапии. Врожденные аномалии возникают в период беременности. В их возникновении большую роль имеют негативные воздействия на организм матери и плод: вредные привычки, прием лекарственных препаратов, воздействие лучевой энергии и др.
Приобретенные факторы, встречающиеся у детей, следующие:
- избыточная масса тела, в том числе ожирение. Увеличение количества жировой клетчатки вокруг органов приводит к изменению положения желчного пузыря, что может осложниться его деформацией;
- тяжелые или длительные физические нагрузки. Если ребенок занимается в спортивной секции, то подъем тяжестей может стать причиной опущения органов в брюшной полости;
- аномалии расположения желчного пузыря, которые на фоне дискинезии желчевыводящих путей или болезней печени приводят к деформации органа.
Установление конкретных причин развития заболевания необходимо для подбора лечебных мероприятий. Ребенка с симптомами патологии осматривают педиатр и врачи смежных специальностей, что позволяет уточнить диагноз и своевременно начать лечение.
Классификация патологии
У 25-30% детей встречаются аномалии строения желчного пузыря. Выделяют несколько видов изменений органа по клинической классификации:
- изменение взаимоотношения стенок в результате воспалительных изменений;
- перегиб в области шейки органа;
- вращение дна желчного пузыря относительно тела;
- при врожденной форме заболевания часто выявляется s-образная деформация;
- сужение тела органа.
На характер клинических проявлений влияет степень выраженности деформации. Если орган изменен не сильно, то болезнь протекает скрыто — у ребенка отсутствуют симптомы патологии или они появляются на фоне погрешностей в диете. При выраженных изменениях в строении органа клинические признаки наблюдаются постоянно.
Клинические проявления
Причины деформации и симптомы тесно связаны
Проявления деформации желчного пузыря в детском возрасте отличаются у каждого пациента. Связано это с тем, что выраженность патологических изменений у больных отличается. К основным симптомам патологии относят:
- боль в правом подреберье, имеющая характер острого приступа. Подобный гипертонически-гиперкинетический тип болезни встречается наиболее часто. При гипотонически-гипокинетическом типе болевые ощущения выражены слабо и встречаются постоянно;
- тошнота и рвота, усиливающиеся после приема жирной пищи. Если они возникают чаще, чем 2 раза в час, то могут свидетельствовать о развитии негативных последствий болезни;
- нарушения стула в виде запора. Это связано с недостатком поступления желчи в тонкий кишечник и нарушением процессов пищеварения;
- изжога, появляющаяся в результате гастро-эзофагального рефлюкса. Ребенок ощущает неприятные ощущения за грудиной, которые усиливаются после трапезы. При этом отмечается чувство горечи в ротовой полости;
- метеоризм, развивающийся при попадании щелочного содержимого двенадцатиперстной кишки в желудок;
- общая слабость и повышенная потливость, связанные с нарушением пищеварения и недостаточным всасыванием питательных веществ из продуктов питания.
Степень тяжести заболевания у пациентов отличается. Как правило, дети долгое время могут скрывать неприятные ощущения и не жаловаться родителям. Обращение в больницу часто связано с острой болью в правом подреберье, которая приводит к изменению поведения ребенка.
Негативные последствия
Желчный пузырь — важный для пищеварения орган, выделяющий желчь в двенадцатиперстную кишку. Если его строение нарушено в результате деформации, то это может привести к осложнениям различной степени тяжести. Наиболее тяжелыми из них являются следующие:
- перегиб органа, сопровождающийся нарушением кровообращения и некрозом. В этом случае стенка желчного пузыря разрывается и его содержимое попадает в брюшную полость, вызывая перитонит;
- нарушение оттока желчи приводит к ее сгущению и создает предпосылку для развития желчнокаменной болезни.
Для предупреждения негативных последствий деформации органа родителям следует обращаться за медицинской помощью при первом появлении симптомов. Самолечение и использование народных методов недопустимо.
Диагностика
Врожденные аномалии и приобретенные состояния выявляются на УЗИ
Диагностика заболевания проводится врачом-педиатром или гастроэнтерологом. Специалист проводит обследование по следующему алгоритму:
- Сбор жалоб и давности их наличия. Врач беседует с ребенком и родителями. У последних узнает информацию о питании, физических нагрузках и перенесенных ранее заболеваниях.
- При внешнем осмотре оценивается мягкость и безболезненность живота. Проводится пальпация края печени. Он должен быть эластичным и безболезнен
- В биохимическом анализе крови возможно повышение билирубина и печеночных ферментов: АсАТ, АлАТ и щелочной фосфатазы. В клиническом анализе у небольшого количества больных выявляется увеличение количества лейкоцитов.
- Ультразвуковое исследование желчного пузыря — «золотой стандарт» диагностики. Во время исследования, врач получает возможность установить размер органа и выявить наличие в нем дефектов: деформацию стенок, наличие стеноза, перегиб и др. УЗИ рекомендуется проводить натощак.
- В тяжелых диагностических случаях может проводиться исследование протоков желчного пузыря с помощью эндоскопических методов. При этом могут быть удалены камни и другие патологические образования, создающие застой желчи.
- При наличии сопутствующих болезней внутренних органов проводятся консультации со смежными врачами и дополнительные исследования.
Интерпретировать результаты обследования должен только врач. Неправильная постановка диагноза и попытки самолечения способствуют прогрессированию патологии и развитию осложнений.
Подходы к терапии
Основная цель лечения — устранить боль и нормализовать отток желчи из желчного пузыря. Этого можно достичь с помощью лекарственных препаратов. Наиболее часто используют медикаменты следующих групп:
- спазмолитические средства, расслабляющие гладкую мускулатуру желчного пузыря и обеспечивающие нормальное течение желчи из органа. Спазмолитики используются в виде таблеток, а также инъекций, что зависит от клинической картины патологии;
- желчегонные препараты на основе урсодезоксихолевой кислоты. Они обеспечивают нормализацию оттока желчи, а также защищают клетки печени от повреждения;
- пробиотики, содержащие живые микроорганизмы, и эубиотики, способствующие росту нормальной микрофлоры толстого кишечника показаны детям с деформациями желчного пузыря. Препараты улучшают процесс пищеварения и прогноз для ребенка;
- витамины и минеральные комплексы;
- если первичное поражение желчного пузыря связано с бактериальной инфекцией, то больному подбирают антибиотики широкого спектра действия.
При выраженной деформации желчного пузыря эффективность консервативного лечения ограничена. В этом случае ребенку может быть выполнено хирургическое вмешательство, направленное на устранение перегиба или скручивания органа. Частота операций у больных — не более 5%.
Лекарственные препараты назначаются только врачом. Они имеют противопоказания, связанные с возрастом и сопутствующими болезнями, что необходимо учитывать при их применении.
Изменения питания
Лечение заболевания всегда включает диетотерапию. Специалисты отмечают, что правильное питание позволяет снизить выраженность проявлений патологии и уменьшить частоту их возникновения. В связи с этим,детям и их родителям рекомендуют соблюдать следующие принципы:
- дробный прием пищи небольшими порциями 5-6 раз за день. При этом 4 трапезы основные, а две являются перекусами;
- из питания исключаются жареные, копченые, острые и жирные блюда, а также бобовые культуры и пряности. Аналогичное ограничение распространяется на фастфуд и полуфабрикаты;
- среди напитков следует ограничить какао, черный чай и кофе;
- кондитерские изделия, содержащие большое количество углеводов — конфеты, варенье, шоколад и др., также исключаются из ежедневного питания.
В рационе увеличивают количество нежирных сортов мяса и рыбы. Их можно готовить на пару вместе с овощами. Положительный эффект наблюдается при употреблении некислых овощей, растительных масел с полиненасыщенными жирными кислотами, овощей и кисломолочных продуктов небольшой жирности.
Родителям важно помнить, что вне острого периода болезни, когда симптомы исчезают, следует продолжать придерживаться правильного питания. Ребенку не следует покупать сладости, посещать рестораны быстрого питания и пр. Это может привести к обострению заболевания и стать причиной развития осложнений.
Прогноз при деформации желчного пузыря у детей благоприятный. Заболевание при своевременном выявлении хорошо поддается терапии и не сопровождается рецидивами при соблюдении диеты. В тех случаях, когда обращение за медицинской помощью откладывалось, лекарственные средства имеют низкую эффективность. Проведение хирургического вмешательства позволяет устранить изменения в желчном пузыре и нормализовать отток желчи и процесс пищеварения.
Также интересно почитать: у ребенка под глазами синяки
Перегиб желчного пузыря у ребенка – как распознать и лечить опасное состояние?
Желчный пузырь – орган небольших размеров, располагающийся на поверхности печени. Он состоит из дна, тела и шейки, которые плавно переходят друг в друга. По мере роста и взросления ребенка орган изменяет свою форму и объем. Нарушение данного процесса может вызывать такую патологию, как перегиб желчного пузыря у ребенка.
Перегиб желчного пузыря – виды
Загиб желчного пузыря у ребенка – патологическое состояние, сопровождающееся нарушением расположения органа. В большинстве случаев врачи диагностируют врожденную форму – загиб желчного пузыря у новорожденного, сформированный еще на этапе внутриутробного этапа. В результате развития приспособительных реакций внутренние органы привыкают к недостатку желчи, нарушению ее оттока.
В результате подвижности желчного пузыря может развиваться приобретенная форма его перегиба. Кроме того, такое нарушение может возникать в результате воспалительных процессов, неправильного питания ребенка. Независимо от характера перегиба (врожденной и приобретенной формы), требуется специфическая терапия, которая подбирается с учетом типа перегиба желчного пузыря:
- фиксированный;
- нефиксированный (лабильный).
Фиксированный перегиб желчного пузыря у ребенка
Врожденный перегиб желчного пузыря у ребенка в большинстве случаев имеет фиксированную форму. Он характеризуется постоянным, неизменным видом и положением органа относительно печени. Диагностируется патология постоянно, независимо от количества процедур диагностики. На каждом УЗИ врач фиксирует неправильную форму желчного пузыря. Перегиб в большинстве случаев возникает в области шейки – как самого тонкого места пузыря.
Нефиксированный перегиб желчного пузыря у ребенка
Нефиксированный или лабильный перегиб желчного пузыря у ребенка – форма патологии, которая имеет временный характер. Диагностировать ее с помощью УЗИ можно не всегда. Отличается наличием неустойчивого перегиба – его форма и место расположения могут изменяться. При проведении обследования в некоторых случаях перегиб может отсутствовать и снова появляться при последующей процедуре. Зачастую предположить наличие патологии можно только по характерной симптоматике, которая и становится показанием для комплексного обследования ребенка.
Загиб желчного пузыря – причины
Факторы, провоцирующие развитие перегиба, могут отличаться и нередко зависят от формы патологии. Так, врожденный загиб желчного пузыря обусловлен нарушением одного из внутриутробных этапов развития плода.
К нарушениям формирования внутренних органов у будущего малыша приводят:
- гормональные сбои у мамы;
- хронические воспалительные процессы в организме;
- инфекции внутренних органов;
- хронические заболевания органов пищеварительной системы, в результате которых малыш недополучает питательные вещества;
- генетическая предрасположенность (научно не доказана).
Среди причин, вызывающих приобретенный перегиб желчного пузыря у ребенка, специалисты выделяют:
- повышенную физическую активность ребенка;
- неправильный рацион – сладости и фастфуд плохо отражаются на работе печени и состоянии желчного пузыря.
Загиб желчного пузыря у ребенка – симптомы
Когда у ребенка возникает загиб желчного пузыря, симптомы патологии появляются не сразу. Их характер напрямую зависит от того, в каком месте пузыря возникает патология. Оценивая наблюдаемые признаки и симптомы, врачам удается сделать первые предположения о характере нарушения и локализации перегиба. Эта информация имеет решающее значение при выборе методов терапии патологического процесса.
Перегиб тела желчного пузыря у ребенка
По характерным признакам мама может самостоятельно определить перегиб желчного пузыря у ребенка – симптомы патологии имеют выраженный характер. Перегиб в области тела желчного пузыря может сопровождаться появлением следующих симптомов:
- болезненные ощущения в области живота;
- боли в ключице, грудине, под лопаткой;
- тошнота, усилившаяся после приема пищи;
- рвота;
- налет на поверхности языка;
- трещинки в уголках рта.
Загиб шейки желчного пузыря
Когда возникает загиб желчного пузыря у грудничка в данной форме специалисты на УЗИ наблюдают удлинение шейки пузыря или отвисание его тела. В результате подобных изменений увеличивается риск омертвления шейки. Подобная ситуация чревата попаданием желчи непосредственно в брюшную полость и развитием перитонита. Из-за этих особенностей ранняя диагностика играет важную роль, позволяя предупредить названные осложнения.
Заподозрить загиб желчного пузыря, симптомы данного нарушения можно только при правильной оценке состояния ребенка. Перегиб шейки желчного пузыря у ребенка сопровождает следующая клиническая картина:
- боли в области живота, локализующиеся в районе левого подреберья;
- вздутие живота;
- приступы тошноты;
- повышение температуры тела.
Перегиб дна желчного пузыря у ребенка
При данном типе нарушения признаки загиба желчного пузыря характеризуются болезненными ощущениями в области живота. Боль отдает в правое подреберье. Параллельно с болезненными ощущениями наблюдаются и другие симптомы:
- тошнота;
- рвота;
- неустойчивость стула (диарея).
В случае присоединения инфекции на фоне нарушенного оттока желчи появляются дополнительные симптомы перегиба:
- повышенная потливость;
- горечь во рту;
- землистый оттенок лица.
Двойной перегиб желчного пузыря у ребенка
Перекручивание желчного пузыря в нескольких местах является редкой формой патологии. В качестве факторов, провоцирующих развитие перекрута, специалисты называют увеличение размеров пузыря. Боли при загибе желчного пузыря в двух местах отличаются большей интенсивностью. В остальном симптомы этой формы патологии не отличаются от названных выше видов.
Чем опасен перегиб желчного пузыря у ребенка?
Если врачам не удается вовремя диагностировать загиб желчного пузыря, последствия данной патологии не заставляют себя долго ждать. Желчный пузырь является резервуаром для хранения желчи, поэтому нарушение его размера и формы приводит к сбою ее нормального оттока. Развивается застой, который способен спровоцировать активизацию микроорганизмов, запускающих воспалительный процесс. Ребенок начинает ощущать сильные боли в области живота.
Перегиб желчного пузыря у ребенка чреват следующими осложнениями:
- нарушение функций печени;
- отставание ребенка в развитии из-за неполной усвояемости питательных веществ;
- развитие хронических патологий желудочно-кишечного тракта;
- желтуха.
Загиб желчного пузыря у ребенка – лечение
Когда у ребенка диагностирован приобретенный загиб желчного пузыря, лечение назначают незамедлительно. Если же патология имеет врожденный характер, протекает бессимптомно, специалисты придерживаются выжидательной тактики. Появление симптомов, болезненных ощущений требует медицинского вмешательства. Характер терапии при перегибе желчного пузыря определяется:
- выраженностью болей;
- возрастом пациента;
- наличием сопутствующих патологий.
Лечение в большинстве случаев имеет консервативный характер. Детям назначают лекарственные препараты, обладающие желчегонным действием. В комплексном лечении перегиба желчного пузыря у ребенка используют также:
- обезболивающие;
- спазмолитики;
- физиопроцедуры.
Загиб желчного пузыря – препараты
После того как диагностирован загиб желчного пузыря у ребенка, врачи разрабатывают индивидуальный план терапии. Медикаменты подбирают с учетом возраста пациента, стадии и выраженности патологического процесса. Терапия направлена на исключение причины, вызывавшей перегиб органа. В большинстве случаев желчегонные средства при загибе желчного пузыря составляют основу лечения. Для ликвидации патологии врачи используют следующие группы лекарств:
1. Холеретики – средства, стимулирующие процессы образования желчи, ее секрецию. Представителями этой группы лекарств являются:
2. Тонизирующие средства – применяются для коррекции нормального функционирования вегетативной нервной системы:
3. Холекинетики – желчегонные средства, стимулирующие сократительную активность желчного пузыря, снижающие давление и тонус желчевыводящих путей:
- Одестон;
- Ксилит;
- Гепабене;
- Флакумин;
- Конвафлавин.
4. Спазмолитики – способствуют расслаблению мышц желчевыводящих путей, снижают давление в них, снижают боль. К ним относятся:
- Папаверин;
- Но-Шпа;
- Дюспаталин;
- Мебеверин.
5. Ферментативные препараты – помогают наладить нормальное пищеварение:
- Мезим;
- Фестал;
- Креон.
Диета при загибе желчного пузыря у ребенка
Питание при загибе желчного пузыря требует отдельного внимания. Для выздоровления ребенку необходимо соблюдать диету. Она предполагает исключение из рациона следующих продуктов:
- жирные сорта мяса;
- рыба;
- жареные блюда;
- кондитерские изделия;
- чипсы и фастфуд.
Когда возникает перегиб желчного пузыря у ребенка в меню малыша вводят блюда и продукты, способствующие оттоку желчи. Примером таковых может быть запеченная тыква, свежий тыквенный сок (по стакану в день). Рацион должен содержать достаточное количество овощей и фруктов, молока и молочнокислых продуктов. Питание должно быть дробным, 6 раз в сутки.
Гимнастика при загибе желчного пузыря
Врачи утверждают, что специальные упражнения при загибе желчного пузыря помогают восстановить нормальную работу органа. Для этого следует выполнить вместе с ребенком несколько простых упражнений:
- В положении лежа на спине выпрямляют ноги, стопы смыкают, руки разводят в стороны. На выдохе подтягивают колени к груди, обхватывая их руками. Возвращаются в исходное положение.
- Укладывают ребенка на спину, выпрямляют ноги и смыкают стопы. Руки кладут под голову. На выдохе просят медленно приподнять ноги на 45 градусов, возвращаются в исходное положение.
Загиб желчного пузыря – операция
Когда диагностируется двойной перегиб желчного пузыря у ребенка, лечение проводят хирургическим путем. В таком случае происходит полное перекрытие оттока желчи. Для его восстановления осуществляется лапароскопическая операция, предполагающая резекцию желчного пузыря. Проводят ее под общим наркозом. Метод малотравматичен, восстановление наступает быстро. Спустя несколько дней дети выписываются из стационара, за ними устанавливается диспансерное наблюдение.
Синдром сгущения желчи у новорожденных и детей раннего возраста: факторы риска, терапия, прогноз. Разбор клинического случая | Горяйнова
1. Chen S.M., Liao Y.Y., Lin C.P. Inspissated bile syndrome: A rare cause of neonatal cholestasis. Pediatr Neonatol. 2020;61(4):449–450. doi: 10.1016/j.pedneo.2020.03.002.
2. Gottesman L.E., Del Vecchio M.T., Aronoff S.C. Etiologies of conjugated hyperbilirubinemia in infancy: a systematic review of 1692 subjects. BMC Pediatrics. 2015;15:192. doi: 10.1186/s12887-015-0506-5.
3. Fitzpatrick F., Jardine R., Farrant P., Karani J., Davenport M., Mieli-Vergani G., Baker A. Predictive Value of Bile Duct Dimensions Measured by Ultrasound in Neonates Presenting With Cholestasis. J Pediatr Gastroenterol Nutr. 2010;51(1):55–60. doi: 10.1097/MPG.0b013e3181d1b226.
4. Davenport M., Betalli P., D’Antiga L., Cheeseman P., Mieli-Vergani G., Howard E.R. The spectrum of surgical jaundice in infancy. J Pediatr Surg. 2003;38(10):1471–1479. doi: 10.1016/s0022-3468(03)00498-6.
5. Gubernick J.A., Rosenberg H.K., Ilaslan H., Kessler A. US approach to jaundice in infants and children. Radiographics. 2000;20(1):173–195. doi: 10.1148/radiographics.20.1.g00ja25173.
6. Ko C.W., Sekijim J.H., Lee S.P. Biliary sludge. Ann Intern Med. 1999; 130(4 Pt. 1):301–311. doi: 10.7326/0003-4819-130-4-199902160-00016.
7. Ladd W.E. Congenital obstruction of the bile ducts. Annals of Surgery. 1935;102(4):742–751. doi: 10.1097/00000658-193510000-00021.
8. Ko C.W., Murakami C., Sekijima J.H., Kim M.H., McDonald G.B., Lee S.P. Chemical composition of gallbladder sludge in patients after marrow transplantation. Am J Gastroenterol. 1996;91(6):1207–1210. Available at: https://pubmed.ncbi.nlm.nih.gov/8651172.
9. Kim Y.S., Kestell M.F., Lee SP. Gall-bladder sludge: lessons from ceftriaxone. J Gastroenterol Hepatol. 1992;7(6):618–621. doi: 10.1111/j.1440-1746.1992.tb01496.x.
10. Park H.Z., Lee S.P., Schy A.L. Ceftriaxone-associated gallbladder sludge. Identification of calcium-ceftriaxone salt as a major component of gallbladder precipitate. Gastroenterology. 1991;100(6):1665–1670. doi: 10.1016/0016-5085(91)90667-A.
11. Shiffman M.L., Keith F.B., Moore E.W. Pathogenesis of ceftriaxone-associated biliary sludge. in vitro studies of calcium-ceftriaxone binding and solubility. Gastroenterology. 1990;99(6):1772–1778. doi: 10.1016/0016-5085(90)90486-k.
12. Володин Н.Н., Мухина Ю.Г., Чубарова А.И. (ред.). Неонатология. В: Володин Н.Н., Мухина Ю.Г. (ред.). Детские болезни. М.: Династия; 2011. Т. 1. 512 с.
13. Bollu B.K., Dawrant M.J., Thacker K., Thomas G., Chenapragadda M., Gaskin K., Shun A. Inspissated bile syndrome; Safe and effective minimally invasive treatment with percutaneous cholecystostomy in neonates and infants. J Pediatr Surg. 2016;51(12):2119–2122. doi: 10.1016/j.jpedsurg.2016.09.053.
14. Miloh T., Rosenberg H.K., Kochin I., Kerkar N. Inspissated bile syndrome in a neonate treated with cefotaxime: sonographic aid to diagnosis, management, and follow-up. J Ultrasound Med. 2009;28(4):541–544. doi: 10.7863/jum.2009.28.4.541.
15. Rozmanic V., Banac S., Ivosevic D., Cace N. Biliary colic and sonographic evidence of pseudocholelithiasos 36 h after treatment with ceftriaxone. J Paediatr Child Health. 2006;42(10):658–661. Available at: https://www.researchgate.net/publication/6818041_Biliary_colic_and_sonographic_evidence_of_pseudocholelithiasos_36_h_after_treatment_with_ceftriaxone.
16. Schaad U.B., Tschäppeler H., Lentze M.J. Transient formation of precipitations in the gallbladder associated with ceftriaxone therapy. Pediatr Infect Dis. 1986;5(6):708–710. doi: 10.1097/00006454-198611000-00026.
17. Bor O., Dinleyici E.C., Kebapci M., Aydogdu S.D. Ceftriaxone-associated biliary sludge and pseudocholelithiasis during childhood: a prospective study. Pediatr Int. 2004;46(3):322–344. doi: 10.1111/j.1328-0867.2004.01884.x.
18. Klar A., Branski D., Akerman Y., Nadjari M., Berkun Y., Moise J. et al. Sludge ball, pseudolithiasis, cholelithiasis and choledocholithiasis from intrauterine life to 2 years: a 13-year follow- up. J Pediatr Gastroenterol Nutr. 2005;40(4):477–480. doi: 10.1097/01.mpg.0000151749.01631.21.
19. Jain A., Poddar U., Elhence P., Tripathi A., Shava U., Yachha S.K. Cholestasis in a neonate with ABO haemolytic disease of newborn following transfusion of ABO group-specific red cells compatible with neonatal serum: inspissated bile syndrome. Blood Transfus. 2014;12(4):621–623. doi: 10.2450/2014.0099-14.
20. Messing B., Bories C., Kuntslinger F., Bernier J.J. Does total parenteral nutrition induce gallbladder sludge formation and lithiasis? Gastroenterology. 1983;84(5 Pt. 1):1012–1019. Available at: https://pubmed.ncbi.nlm.nih.gov/6403401.
21. Chang S.H., Joo S.M., Yoon C.S., Lee K.H., Lee S.M. Percutaneous Transhepatic Biliary Drainage in a Two-Month-Old Infant with Inspissated Bile Syndrome. Yonsei Med J. 2018;59(7):904–907. doi: 10.3349/ymj.2018.59.7.904.
22. Hernanz-Schulman M., Ambrosino M.M., Freeman P.C., Quinn C.B. Common bile duct in children: sonographic dimensions. Radiology. 1995;195(1):193–195. doi: 10.1148/radiology.195.1.7892467.
23. Carroll B.A., Oppenheimer D.A., Muller H.H. High-frequency real-time ultrasound of the neonatal biliary system. Radiology. 1982;145(2):437–440. doi: 10.1148/radiology.145.2.7134449.
24. Heaton N.D., Davenport M., Howard E.R. Intraluminal biliary obstruction. Arch Dis Child. 1991;66(12):1395–1398. doi: 10.1136/adc.66.12.1395.
25. Berger S., Schibli S., Stranzinger E., Cholewa D. One-stage laparoscopic surgery for inspissated bile syndrome: case report and review of surgical techniques. Springerplus. 2013;2:648. doi: 10.1186/2193-1801-2-648.
26. Sideeka N, Shaikh R, Chaudry G. Single Procedure Saline Lavage for Treatment of Inspissated Bile. Case Rep Radiol. 2020;2020:8816599. doi: 10.1155/2020/8816599.
27. Gunnarsdóttir A, Holmqvist P, Arnbjörnsson E, Kullendorff CM. Laparoscopic aided cholecystostomy as a treatment of inspissated bile syndrome. J Pediatr Surg. 2008;43(4):e33–e55. doi: 10.1016/j.jpedsurg.2007.12.068.
28. Gao Z.G., Shao M., Xiong Q.X., Tou J.F., Liu W.G. Laparoscopic cholecystostomy and bile duct lavage for treatment of inspissated bile syndrome: a single-center experience. World J Pediatr. 2011;7(3):269–271. doi: 10.1007/s12519-011-0321-5.
29. Lieber J., Piersma F.E., Sturm E. et al. Surgical treatment of inspissated bile syndrome using a 2-stage pure laparoscopic approach: a case report. J Pediatr Surg. 2012; 47(12):e47–50. doi: 10.1016/j.jpedsurg.2012.09.043.
30. Helin R., Bhat R., Rao B. Ultrasound-guided percutaneous cholecystostomy for acute neonatal biliary obstruction. Neonatology. 2007;91(4):266–270. doi: 10.1159/000098174.
31. Dani C., Pratesi S., Raimondi F., Romagnoli C. Italian guidelines for the management and treatment of neonatal cholestasis. Ital J Pediatr. 2015;:41:69. doi: 10.1186/s13052-015-0178-7.
32. Jun W.Y., Cho M.J., Han H.S., Bae S.H. Use of Omega-3 Polyunsaturated Fatty Acids to Treat Inspissated Bile Syndrome: A Case Report. Pediatr Gastroenterol Hepatol Nutr. 2016;19(4):286–290. doi: 10.5223/pghn.2016.19.4.286.
33. Jonkers I.J., Smelt A.H., Princen H.M., Kuipers F., Romijn J.A., Boverhof R. et al. Fish oil increases bile acid synthesis in male patients with hypertriglyceridemia. J Nutr. 2006;136(4):987–991. doi: 10.1093/jn/136.4.987.
34. Bae S.H., Park H.S., Han H.S., Yun I.J. Omega-3 polyunsaturated fatty acid for cholestasis due to bile duct paucity. Pediatr Gastroenterol Hepatol Nutr. 2014;17(2):121–124. doi: 10.5223/pghn.2014.17.2.121.
35. Nandivada P., Carlson S.J., Chang M.I., Cowan E., Gura K.M., Puder M. Treatment of parenteral nutrition-associated liver disease: the role of lipid emulsions. Adv Nutr. 2013;4(6):711-717. doi: 10.3945/an.113.004770.
Произошла ошибка при настройке вашего пользовательского файла cookie
Произошла ошибка при настройке вашего пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie.Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.
Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie. - Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie.Чтобы исправить это, установите правильное время и дату на своем компьютере. - Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.
Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в cookie-файлах может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт
не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к
остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Отличие атрезии желчных протоков от других причин холестатической желтухи
Am Surg. Авторская рукопись; доступно в PMC 2017 20 октября.
Опубликован в окончательной редакции как:
Am Surg.2014 сен; 80 (9): 827–831.
PMCID: PMC5649385
NIHMSID: NIHMS
6
Отделение детской хирургии, Детская клиника Немур, Джэксонвилл, Флорида
Запросы на перепечатку и перепечатку адресуйте Дэниелу К. Роби, доктору медицины, Отделение детской хирургии, Детская клиника «807 Вей». , Jacksonville, FL 32207. gro.sruomen@eibord См. Другие статьи в PMC, в которых цитируется опубликованная статья.
Abstract
Диагностика атрезии желчных протоков (БА) у младенцев с холестатической желтухой (ХБ) требует диагностической хирургии с холангиографией.Однако отсутствие стандартизированного подхода к предоперационной оценке младенцев с КС может привести к большому количеству отрицательных результатов хирургического обследования. Мы проанализировали наш опыт с CJ и BA, чтобы определить предоперационные параметры, которые могут надежно идентифицировать BA. Младенцы, обследованные на возможную БА в течение 5-летнего периода, были ретроспективно рассмотрены. Рассмотрены дооперационные клинические показатели и результаты биопсии печени. Статистический анализ проводился с помощью критерия Стьюдента t и точного критерия Фишера ( P <0.05). Было идентифицировано 20 пациентов, 10 с БА и 10 без (50% отрицательных результатов исследования). Выделение ядерной холесцинтиграфии (HIDA) в желудочно-кишечный тракт отсутствовало при всех БА и у 8 из 10 - без БА. Гепатомегалия чаще встречалась в группе БА (OR = 9,3, P = 0,07). БА имела более высокие средние (± стандартная ошибка) уровни гамма-глутамилтранспептидазы в сыворотке (542 ± 130 против 139 ± 25,8 Ед / л у не-БА, P = 0,03). Между двумя группами были незначительные различия по полу, типу кормления, воздействию парного парентерального питания и сепсису.Хотя наш небольшой размер выборки ограничивает выводы, мы предлагаем проводить скрининг младенцев с КС путем измерения уровней GGT, отсутствия гепатомегалии, наличия желчного стула и / или экскреции при сканировании HIDA, чтобы пройти кожную биопсию печени, учитывая более низкую вероятность необходимости в БА.
Наличие холестатической желтухи (ХЖ) в возрасте двух недель у здорового младенца требует исследования для определения основной причины. 1 Его этиология включает многочисленные причины в двух широких группах: обструктивные поражения и гепатоцеллюлярные состояния.Диагностика требует обширного рентгенологического и лабораторного исследования. 2 После этого обследования, за исключением инвазивных диагностических процедур, биопсии печени и открытой холангиографии, наиболее частыми оставшимися причинами остаются атрезия желчных протоков (БА) и неонатальный гепатит (НГ).
Ранняя диагностика БА имеет решающее значение, потому что портоеюностомия до 45–60 дней жизни дает младенцу наилучшие шансы на выживание с родной печенью. 2 Учитывая приоритет раннего лечения БА, экспертный комитет Североамериканского общества педиатрической гастроэнтерологии, гепатологии и питания рекомендует биопсию печени, когда причина КС не может быть определена после неинвазивных лабораторных и визуализирующих исследований. 1 Для окончательного диагноза БА требуется хирургическое обследование и интраоперационная холангиография для подтверждения отсутствия открытой внепеченочной билиарной системы. Если открытых протоков не обнаружено, хирург приступает к портоеюностомии с еюноэюностомией по Ру, процедурой Касаи. 2 У тех, у кого есть открытые желчные протоки, операция не будет терапевтической и подвергнет младенцев риску лапаротомии и анестезии.
Таким образом, представляет интерес определение прогностических предоперационных клинических показателей и диагностических тестов, позволяющих отличить БА от НГ и других причин КС.Мы проанализировали наш опыт, чтобы усовершенствовать диагностический подход, который позволяет раннюю стадию БА и сводит к минимуму нетерапевтическое хирургическое вмешательство.
Методы
После получения одобрения институционального наблюдательного совета, электронные медицинские записи для наших офисов были запрошены с использованием стандартных диагностических и процедурных кодов для регистрации всех случаев с CJ () за 5-летний период с 2009 по 2013 год. 3, 4 Обзор записей выявил всех младенцев с БА и детей с КС, которые прошли обследование на БА с помощью открытой или лапароскопической биопсии печени и холангиографии.Пациенты, которым выполнялась только чрескожная биопсия печени без открытого хирургического вмешательства, были исключены.
Таблица 1
ICD-9-CM и Коды CPT , используемые для выявления случаев для обзора
| Коды ICD-9-CM | Диагностика | |
|---|---|---|
| 573,8 | Другое уточненные заболевания печени | |
| 573,9 | Неуточненное заболевание печени | |
| 576,8 | Другие уточненные заболевания желчевыводящих путей | |
| Спайки желчных протоков [любые] | ||
| Атрофия желчных путей проток [любой] | ||
| Киста желчного протока [любой] | ||
| Гипертрофия желчного протока [любой] | ||
| Застой желчного протока [любой] | ||
| желчного протока [любого] | ||
| Исключая | ||
| Врожденная киста холедоха (751.69) | ||
| 751,61 | Атрезия желчных путей | |
| Врожденная: | ||
| Отсутствие желчного протока или прохода | ||
| Гипоплазия протока 10 (общая) | ||
| Обструкция желчного протока (общего) или прохода | ||
| Стриктура желчного протока (общий) или прохода | ||
| 774,6 | Неуточненная желтуха плода и новорожденного | желтуха плода и новорожденного |
| Неонатальная гипербилирубинемия (преходящая) | ||
| Физиологическая желтуха БДУ у новорожденного | ||
| CPT | Процедура | |
| 47700 | ||
| 47700 | или без биопсии печени, с холангио или без него графия | |
| 47701 | Портоэнтеростомия (e.г., процедура Касаи) | |
| 47100 | Биопсия печени клин | |
| 47605 | Холецистэктомия; с холангиографией |
Рассмотренные клинические параметры включали пол, гестационный возраст, способ питания (энтеральное против парентерального), сепсис в анамнезе, трансфузии, размер и твердость печени, а также возраст в неделях на момент операции. Особый интерес представлял цвет стула (ахолический против желтого или зеленого) и то, был ли стул зеленым за неделю до операции.Лабораторные показатели включали сывороточные уровни билирубина (общего и прямого) и ферментов печени, аспартаттрансаминазы (AST), аланинтрансаминазы, щелочной фосфатазы и гамма-глутамилтранспептидазы (GGT). В радиологических отчетах представлены результаты ультразвукового исследования (УЗИ) и ядерной холесцинтиграфии (гепатобилиарная иминодиуксусная кислота [HIDA]). В отчетах о патологии были представлены микроскопические данные при биопсии печени, включая пролиферацию желчных протоков, желчных пробок, портальный фиброз, мостовидный фиброз, трансформацию многоядерных гигантских клеток, миелоидную метаплазию, воспалительный инфильтрат и гепатоцеллюлярный отек.
Рассмотрены результаты открытой холангиографии. Те, у кого желчные протоки были помутнены, не имели БА (не БА), и никаких дополнительных хирургических вмешательств не проводилось. Диагноз БА поставлен при отсутствии помутнения желчного дерева. Пациенты с БА немедленно приступили к процедуре Касаи. Их записи были проанализированы на предмет устранения желтухи (уровень билирубина в сыворотке менее 2 мг / дл), возникновения холангита и необходимости трансплантации.
Двухвыборочный непарный тест t был использован для сравнения непрерывных переменных между пациентами с БА и без БА.Точный тест Фишера проанализировал различия в соотношениях дихотомических переменных. Для обоих значение P < 0,05 достигло значимости. Отношения шансов с соответствующими 95-процентными доверительными интервалами были рассчитаны для категориальных переменных в одномерном анализе. Для выбранных тестов рассчитывались чувствительность, специфичность, положительная прогностическая ценность (PPV) и отрицательная прогностическая ценность (NPV). Кривая Каплана-Мейера была построена для определения выживаемости с нативной печенью.
Результаты
Было обследовано 19 младенцев на предмет возможной БА, у одного — на мальротацию, и было обнаружено, что у них БА во время операции.У десяти была БА, и им была выполнена немедленная портоеюностомия по Касаи; 10 младенцев имели открытые желчные протоки и, следовательно, не имели БА (не БА;). Средний возраст на момент операции был эквивалентен для двух групп (BA, 65 дней, диапазон от 3 до 112 дней; без BA, 53 дня, от 29 до 90 дней). Из клинических и лабораторных переменных, перечисленных в «Материалах и методах», только GGT достигла значимости (среднее ± стандартная ошибка среднего; BA, 542 ± 130 против 139 ± 25,8 Ед / л у не-BA, P = 0,03). По остальным признакам физического и лабораторного обследований эти две группы не различались.У всех пациентов с БА уровень GGT в сыворотке был выше 300 Ед / л, что дает 100-процентную специфичность и 67-процентную чувствительность ().
Таблица 2
Сравнение отдельных показателей пациентов с билиарной атрезией и без нее
| Атрезия желчных путей (n = 10) | Атрезия желчных путей (n = 10) | P Значение | ||||
|---|---|---|---|---|---|---|
| Пол (самец) | 5: 5 | 9: 1 | 0,14 | |||
| Гепатомегалия | 8 | 3 | 0.07 | |||
| Пигментированный стул | 2 | 5 | 0,35 | |||
| GGT (Ед / л; среднее ± SEM) | 542 ± 130 (n = 6) | 139 ± 25,8 (n = 5) | 0,028 | |||
| История сепсиса | 2 | 4 | 0,63 | |||
| Кормление (формула против груди ) | 8: 2 | 4: 6 | 900 0105 (> 7 дней) | 0 | 3 | 0.210 |
Таблица 3
Чувствительность, специфичность, а также положительные и отрицательные прогностические значения для различения пациентов с атрезией желчных путей и без нее
| Чувствительность | Специфичность | PPV 96 | 9 | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| GGT> 300 U / L | 67% | 100% | 100% | 71% | |||||||||||||||||||||||
| HIDA без выделения | 100% | 20% | 56% | 902 | 9010 Экскреция HIDA в желудочно-кишечный тракт отсутствовала у всех девяти пациентов с БА, прошедших исследование, и у 8 из 10 пациентов без БА ().УЗИ было выполнено у 9 пациентов с БА и у 10 пациентов без БА. Желчный пузырь не был замечен у двух пациентов с БА и трех пациентов без БА. Общий желчный проток был зарегистрирован у шести пациентов с БА и у всех 10 пациентов без БА. Особого упоминания о знаке треугольной нити при фокусированном исследовании бифуркации портала сделано не было. Образцы биопсии печени клина были получены у 19 пациентов (девять пациентов с БА, 10 без БА) во время операции и предоставили патологические диагнозы и состояния, связанные с БА и КС (). Первоначально предполагалось, что один пациент без БА имел БА на основании предоперационной чрескожной биопсии печени, имел нормальную холангиограмму и открытую биопсию печени, показывающую неонтатальный гигантоклеточный гепатит (ННГКН).У другого пациента без БА с неспецифическими патологическими данными позже был обнаружен синдром Аладжиля. Таблица 4Патологические диагнозы при биопсии печени у пациентов с и без атрезии желчных путей с холестатической желтухой *
Среднее послеоперационное наблюдение пациентов с БА после процедуры Касаи составило 30.3 месяца (). У восьми не было желтухи с родной печенью. Желтуха исчезла у этих пациентов в среднем через 54 дня (7 из 8 в течение 90 дней и один через 98 дней) после Касаи. Двум пациентам, у которых желтуха исчезла через 122 и 236 дней, с тех пор была проведена успешная трансплантация пятерых. Не было пациентов с БА с кистозной БА или синдромом билиарной атрезии – мальформации селезенки и одного пациента с гетеротаксией и единственной селезенкой. График Каплана-Мейера выживаемости без желтухи с нативной печенью (сплошная линия) в днях.Показан 95-процентный доверительный интервал (пунктирные линии). ОбсуждениеНаши результаты подчеркивают важность демонстрации экскреции с желчью при сканировании HIDA и биохимических доказательств гепатоцеллюлярного воспаления с повышением уровня GGT в сыворотке при обследовании ребенка с КС и подозрением на БА. Появление HIDA в двенадцатиперстной кишке исключило диагноз БА (100% NPV). Во всех случаях БА был повышен уровень ГГТ в сыворотке выше 300 Ед / л (100% PPV). По отдельности ни то, ни другое не было диагностическим; в нашей ограниченной серии два исследования предсказали диагноз, который был подтвержден при открытой холангиографии. Серийная документация цвета стула — зеленого в младенчестве — дает прямые клинические доказательства экскреции с желчью; при БА стул ахолический. 2 Несмотря на важность открытия, мы отметили, что несколько врачей обследовали и задокументировали цвет стула, и им приходилось полагаться на записи медсестер, чтобы установить пигмент стула. Поскольку в течение 1 недели после операции у 50% пациентов, не страдающих БА, стул был зеленым, важно документировать его цвет, и это может предотвратить сканирование HIDA. Lee and Chai, 5 в серии из 146 младенцев с неонатальным холестазом, из которых 35 имели БА, обнаружили, что цвет стула очень чувствителен при БА (83%), но с меньшей специфичностью (51%). БА прогрессирует, цвет стула может прогрессировать от зеленого до ахолического. Из двух пациентов с БА в нашей серии с пигментированным стулом один был очень молодым, а другой — недоношенным, поэтому диагноз мог выявить болезнь на ранней стадии. В своей более крупной серии исследований Ли и Чай 5 наблюдали, что у двоих пигментированный стул стал ахолическим позже в ходе болезни. Универсальная программа скрининга с использованием цветных карт стула на Тайване отражает ее важность в ранней диагностике и лечении БА. 6, 7 Другие отметили связь БА с повышенным GGT. 8–12 Исследование Tang и соавторов отметило значительную разницу между пациентами с БА и неонатальным гепатитом (средний уровень 353 против 115, соответственно, оба выражены в Ед / л; P < 0,001) для Уровень GGT выше 300, чувствительность 38 процентов и специфичность 98 процентов. 11 Они отметили, что соотношение GGT / AST больше 2, что позволяет прогнозировать БА с высокой степенью вероятности (отношение шансов, 8.0; P < 0,001). В нашей серии это соотношение не предсказывало БА (83% БА, 40% не БА). Мета-анализ, проведенный Rendon-Macias и его коллегами 10 , обнаружил, что оптимальный порог повышения уровня GGT изменяется с возрастом: более 150 для возраста менее четырех недель; более 250, от четырех до восьми недель; и более 300, более восьми недель. Хотя наличие гепатомегалии не достигло значимости (80% БА, 30% не БА; P = 0.07) и ощутимо «твердая» печень в меньшей степени (50 против 30% соответственно), Ли и Чай обнаружили размах печени более 4 см (чувствительность 77%, специфичность 51%) и твердую печень (80 и 65%). % соответственно), чтобы быть полезной оценкой в бакалавриате. 5 Gupta и соавторы 8 сообщили, что край печени, который был твердым и острым (в отличие от мягкого и гладкого), был одним из пяти клинических признаков, предсказывающих БА в 87% случаев (82 из 120). США и HIDA являются основными радиологическими тестами при оценке CJ.Младенцы с БА могут иметь вздутие желчного пузыря на УЗИ и идентифицируемую КБД на УЗИ, наблюдение в нашей серии и другие отметили. Другие исследователи описали более конкретные результаты УЗИ, полезные для выявления пациентов с БА. 13–17 У девяти пациентов с БА Choi и его коллеги 13 описали признак «треугольной нити», который отсутствовал у других девяти пациентов без БА. Миттал и соавторы 14 также обнаружили, что этот признак специфичен (97%), но не чувствителен (23%).Отсутствие желчного пузыря было специфическим признаком БА (100%), но также не было чувствительным (23%). Другие предполагают, что желчный пузырь при БА имеет характерно ненормальный вид («псевдожелчный пузырь» или «призрачная триада желчного пузыря»: атретический желчный пузырь длиной менее 1,9 см, тонкая и нечеткая стенка, неправильный или дольчатый контур). 15, 17 Высокая чувствительность и низкая специфичность HIDA-сканирования у пациентов без БА были хорошо задокументированы. 18–22 Специфичность невыделения HIDA колеблется от 3521 до 74%. 18 20-процентная специфичность в нашем исследовании может быть особенно низкой, но может быть объяснена тем, что мы включили только тех пациентов, которые впоследствии подверглись хирургическому обследованию. В другие серии включены все младенцы с КС, в том числе те, которые не подвергались хирургическому вмешательству. Предварительное выделение желчи урсодезоксихолевой кислотой перед сканированием HIDA может улучшить выведение нуклида и, следовательно, специфичность до 89 с 54%. 19 Детские гастроэнтерологи в рамках своей профессиональной организации отдают предпочтение чрескожной биопсии печени перед операцией при отсутствии четкого диагноза. 1 Недавнее исследование, в котором проверялась интерпретация биопсий печени и клина, проведенная патологами, имеющими опыт лечения детских заболеваний печени, сообщило о 91-процентной точности диагностики БА. 23 Наиболее частыми патологическими находками были пролиферация желчных протоков, портальный фиброз и отсутствие синусоидального фиброза. Хотя предоперационная биопсия полезна в диагностике БА, встречаются ложноположительные и ложноотрицательные интерпретации. Путаницы в интерпретацию биопсии печени вносит переход от разрастания желчных протоков к их постепенному исчезновению по мере прогрессирования воспаления и фиброза.Если желтуха не исчезнет, может потребоваться повторная биопсия. 24 Другие элементы в анамнезе, по-видимому, не позволяют отличить пациентов с БА от пациентов без БА, в частности, события, которые, как известно, способствуют развитию КС в младенчестве. Недоношенность, переливание крови, сепсис и парентеральное питание были характерными чертами как пациентов с БА, так и пациентов без БА в нашей серии. В заключение, различение младенцев CJ с BA от младенцев без BA требует вдумчивой и тщательной оценки, чтобы уменьшить отрицательный коэффициент исследования.Мы считаем, что пошаговый подход, аналогичный подходам, предлагаемым другими, с быстрым исследованием тех, у кого прогнозируется БА, является наиболее подходящим. 20, 21, 25, 26 Наш подход включает в себя регистрацию ключевых клинических данных (цвет стула и размер печени), измерение уровней GGT в сыворотке и выполнение радиологического тестирования (США, HIDA) и возможной чрескожной центральной биопсии печени индивидуально для каждого пациента. FootnotesПредставлено на ежегодном научном собрании, программе последипломного образования и Юго-восточном педиатрическом хирургическом конгрессе на Юго-восточном хирургическом конгрессе, Саванна, Джорджия, 22–25 февраля 2014 г. Ссылки1. Мойер В., Фриз Д. К., Уитингтон П. Ф. и др. Руководство по оценке холестатической желтухи у младенцев: рекомендации Североамериканского общества детской гастроэнтерологии, гепатологии и питания. J Pediatr Gastroenterol Nutr. 2004. 39: 115–28. [PubMed] [Google Scholar] 2. Мураджи Т. Раннее выявление атрезии желчных путей: прошлое, настоящее и будущее. Эксперт Рев Гастроэнтерол Гепатол. 2012; 6: 583–9. [PubMed] [Google Scholar] 3. Американская медицинская ассоциация. 2013 МКБ-9-CM для больниц.Чикаго, Иллинойс: Американская медицинская ассоциация; 2013. [Google Scholar] 4. Американская медицинская ассоциация. CPT. Профессиональное издание 2012 года для врачей. Чикаго, Иллинойс: Американская медицинская ассоциация; 2012. [Google Scholar] 5. Ли В.С., Чай П.Ф. Клинические особенности, позволяющие дифференцировать атрезию желчных путей от других причин холестаза новорожденных. Ann Acad Med Singapore. 2010; 39: 648–54. [PubMed] [Google Scholar] 6. Lien TH, Chang MH, Wu JF и др. Влияние программы скрининга цветных карт детского стула на 5-летний исход атрезии желчных путей на Тайване.Гепатология. 2011; 53: 202–8. [PubMed] [Google Scholar] 7. Hsiao CH, Chang MH, Chen HL, et al. Универсальный скрининг на атрезию желчных путей с использованием цветовой карты детского стула на Тайване. Гепатология. 2008; 47: 1233–10. [PubMed] [Google Scholar] 8. Гупта Д.К., Шринивас М., Баджпай М. Клиническая оценка AIIMS: надежное средство отличить неонатальный гепатит от внепеченочной билиарной атрезии. Индийский J Pediatr. 2001; 68: 605–8. [PubMed] [Google Scholar] 9. Сан С., Чен Дж, Чжэн С. и др. Анализ клинических параметров, которые способствуют неправильной диагностике атрезии желчных путей.J Ped Surg. 2013; 48: 1490–4. [PubMed] [Google Scholar] 10. Рендон-Масиас М.Э., Вилласис-Кивер А., Кастранеда-Муцино Г. и др. Повышение точности гамма-глутамилтрансферазы для дифференциальной диагностики атрезии желчных путей по корреляции с возрастом. Turk J Pediatr. 2008; 50: 253–9. [PubMed] [Google Scholar] 11. Тан К.С., Хуанг Л.Т., Хуанг Ю.Х. и др. Гамма-глутамилтрансфераза в диагностике атрезии желчных путей. Acta Paediatr Tw. 2007. 48: 196–200. [PubMed] [Google Scholar] 12. Ямагива И., Ивафучи М., Обата К. и др.Изменения предоперационного времени в тестах функции печени при атрезии желчных путей: его полезность в распознавании атрезии желчных путей в раннем младенчестве. Acta Paediatr Jpn. 1996; 38: 506–12. [PubMed] [Google Scholar] 13. Чой СО, Пак WH, Ву СК. Признак треугольного пуповины: сонографический результат, применимый для диагностики атрезии желчных протоков. J Pediatr Surg. 1996; 31: 363–6. [PubMed] [Google Scholar] 14. Миттал В., Саксена А.К., Сохи К.С. и др. Роль абдоминальной сонографии в предоперационной диагностике атрезии внепеченочных желчных протоков у детей младше 90 дней.Дж. М. Дж. Рентген. 2011; 196: W438–15. [PubMed] [Google Scholar] 15. Азиз С., Вайлд Y, Розенталь П. и др. Признак псевдожелчного пузыря при атрезии желчных путей — ловушка визуализации. Pediatr Radiol. 2011; 41: 620–6. [Бесплатная статья PMC] [PubMed] [Google Scholar] 16. Sun Y, Zheng S, Qian Q. Ультразвуковая оценка в дифференциальной диагностике билиарной атрезии и синдрома детского гепатита. Pediatr Surg Int. 2011; 27: 675–9. [PubMed] [Google Scholar] 17. Тан-Кендрик А.П., Фуа КБ, Оои BC и др. Атрезия желчных путей: постановка диагноза по триаде призраков желчного пузыря.Pediatr Radiol. 2003; 33: 311–5. [PubMed] [Google Scholar] 18. Гилмор С.М., Хершкоп М., Райфен Р. и др. Исход гепатобилиарного сканирования при синдроме неонатального гепатита. J Nucl Med. 1997; 38: 1279–82. [PubMed] [Google Scholar] 19. Поддар У., Бхаттачарья А., Тхапа Б.Р. и др. Гепатобилиарная сцинтиграфия с добавлением урсодезоксихолевой кислоты при оценке желтухи новорожденных. J Nucl Med. 2004; 45: 1488–92. [PubMed] [Google Scholar] 20. Арора Н.К., Кохли Р., Гупта Д.К. и др. Сканирование иминодиацетата технеция-99m-меброфенина в печени и последовательные интерпретации уровней GGT в сыворотке для дифференциации атрезии внепеченочных желчных протоков и гепатита новорожденных.Acta Paediatr. 2001; 90: 975–81. [PubMed] [Google Scholar] 21. Пак У.Х., Чхве С.О., Ли Х.Дж. и др. Новый диагностический подход к атрезии желчевыводящих путей с акцентом на ультразвуковой признак треугольного пуповины: сравнение ультразвукового исследования, гепатобилиарной сцинтиграфии и пункционной биопсии печени при оценке инфантильного холестаза. J Ped Surg. 1997; 11: 1555–9. [PubMed] [Google Scholar] 22. Лай М.В., Чанг М.Х., Сюй С.К. и др. Дифференциальный диагноз атрезии внепеченочных желчных протоков от гепатита новорожденных: проспективное исследование.J Pediatr Gastroenterol Nutr. 1994; 18: 121–7. [PubMed] [Google Scholar] 23. Руссо П., Маги Дж. К., Бойтнотт Дж. И др. Разработка и валидация системы гистологической оценки холестаза в младенчестве консорциума исследователей атрезии желчных путей. Clin Gastroenterol Hepatol. 2011; 9: 357–62. [Бесплатная статья PMC] [PubMed] [Google Scholar] 24. Ага ММ. Патологический диагноз атрезии желчных путей при биопсии печени: проблема в тканях? J Gastroenterol Hepatol. 2009; 24: 936–8. [PubMed] [Google Scholar] 25. Roquete MLV, Ferreira AR, Fagundes EDT и др.Точность эхогенного изображения перипортального увеличения при ультразвуковом исследовании и гистопатологии в дифференциальной диагностике атрезии желчных путей. J Pediatr. 2008; 84: 331–6. [PubMed] [Google Scholar] 26. Хартли Дж. Л., Давенпорт М., Келли Д. А.. Атрезия желчевыводящих путей. Ланцет. 2009; 374: 1704–13. [PubMed] [Google Scholar] Атрезия желчных путей | Симптомы и лечениеЧто вызывает атрезию желчных путей?Причины атрезии желчных путей до конца не изучены. У некоторых детей может возникнуть атрезия желчных путей из-за неправильного формирования желчных протоков во время беременности.У других детей с атрезией желчных путей желчные протоки могут быть повреждены иммунной системой организма в ответ на вирусную инфекцию, приобретенную после рождения. Кто подвержен риску атрезии желчных путей?Атрезия желчных путей — редкое заболевание. Примерно у одного из 15 000–20 000 детей желчные протоки отсутствуют. Атрезия желчных путей поражает девочек больше, чем мальчиков. В пределах одной семьи заболеванием может быть только один ребенок в паре близнецов или только один ребенок в одной семье.Азиаты и афроамериканцы страдают чаще, чем кавказцы. Нет никакой связи с лекарствами, принимаемыми во время беременности. Есть ли у детей с атрезией желчных путей другие сопутствующие аномалии?От 10 до 15 процентов младенцев с атрезией желчных путей могут родиться с другими проблемами в:
Каковы симптомы атрезии желчных путей?Младенцы с атрезией желчных путей обычно кажутся здоровыми при рождении.Симптомы болезни обычно проявляются в течение первых двух недель — двух месяцев жизни. Симптомы включают:
Как диагностируется атрезия желчных путей?Желтуха может присутствовать при других заболеваниях печени, поэтому для постановки правильного диагноза необходимо провести несколько анализов.
Холангиограмма — это процедура, которая проводится во время операции. В этой процедуре краситель вводится через желчный пузырь и проходит через желчные протоки.Делается рентген, чтобы узнать, нормально ли краситель попадает в кишечник и печень. У младенцев с атрезией желчных путей краситель обычно не выходит из желчного пузыря из-за закупорки протоков. Если протоки в норме или открыты (проходимы) и краска течет должным образом, атрезия желчных путей исключена. Затем проводится более крупная биопсия печени (образец ткани), чтобы найти причину заболевания печени. Атрезия желчных путей диагностируется, когда холангиограмма показывает, что желчные протоки не открыты.Затем младенцы обычно подвергаются операции, называемой процедурой Касаи. Как лечится атрезия желчных путей?Атрезия желчных путей не лечится лекарствами. Выполняется процедура Касаи (также известная как гепатопортоэнтеростомия). Процедура Касаи — это операция по восстановлению оттока желчи из печени в кишечник. Он назван в честь разработавшего его хирурга. Хирург удаляет поврежденные протоки за пределами печени (так называемые внепеченочные протоки) и выявляет меньшие протоки, которые все еще открыты и выводят желчь.Затем хирург прикрепляет петлю кишечника к этой части печени, чтобы желчь могла течь прямо из оставшихся здоровых желчных протоков в кишечник. После этой процедуры младенцы обычно находятся в больнице от семи до 10 дней для выздоровления. Для снижения риска инфицирования назначается длительная антибактериальная терапия, также могут использоваться дополнительные лекарства для улучшения оттока желчи и максимального успеха операции Под руководством опытного хирурга процедура Касаи оказывается успешной у 60–85 процентов пациентов.Это означает, что из печени вытекает желчь и уровень желтухи снижается. Процедура Касаи не является лекарством от атрезии желчных путей, но она позволяет детям расти и сохранять хорошее здоровье в течение нескольких, а иногда и многих лет. Около 25% пациентов, которые проходят процедуру Касаи, не нуждаются в трансплантации печени. У 15-40 процентов пациентов процедура Касаи не работает. Если это так, трансплантация печени может решить эту проблему. Успех процедуры Касаи связан с:
Питание и атрезия желчных путейУ детей с заболеваниями печени метаболизм быстрее, чем у здоровых детей.Это означает, что детям с атрезией желчных путей может потребоваться больше калорий. Ребенок с атрезией желчных путей и желтухой не может правильно усваивать жиры. Это связано с тем, что в кишечник попадает недостаточно желчи. Из-за повреждения печени также может быть потеря витаминов и белка.
Хотя пищеварение может вернуться в норму после операции, могут потребоваться дополнительные витамины или масло MCT. Каковы осложнения атрезии желчных путей и что с ними можно сделать?Осложнения сразу после операции минимальны.Большинство проблем возникает из-за прогрессирования заболевания печени.
Повышенное давление в этих венах может вызвать внезапное и сильное кровотечение в желудке и кишечнике. Хотя это может быть очень серьезным осложнением, при своевременной и опытной медицинской помощи кровотечение обычно можно остановить. Иногда для этого требуются специальные процедуры, при которых в аномальные сосуды вводят отвердитель (склерозирующий).
По мере обострения болезни могут возникать и другие осложнения цирроза. Каковы долгосрочные перспективы?На долгосрочную выживаемость после процедуры Касаи влияет прогрессирующее заболевание печени (цирроз) и развитие портальной гипертензии (высокое кровяное давление в воротной вене, по которой кровь поступает в печень). Почти половине всех младенцев, перенесших процедуру Касаи, требуется трансплантация печени до 5 лет. У детей старшего возраста может сохраняться хороший отток желчи и отсутствие желтухи. У некоторых детей может развиться портальная гипертензия, желудочно-кишечное кровотечение, скопление жидкости в брюшной полости (асцит) и увеличение селезенки (гиперспленизм). Восемьдесят пять процентов всех детей с атрезией желчных путей нуждаются в трансплантации печени до достижения ими 20-летнего возраста.Остальные 15 процентов в той или иной степени страдают заболеванием печени. С их заболеванием можно справиться без пересадки. Пересадка печениЕсли после процедуры Касаи отток желчи по-прежнему недостаточен, в конечном итоге будет рассмотрен вопрос о трансплантации печени. Операция по пересадке печени удаляет поврежденную печень и заменяет ее новой печенью от донора. После трансплантации требуется постоянный пожизненный уход. Также необходим частый контакт с врачами и другими членами бригады трансплантологов. Сколиоз: лечение, симптомы и причиныСколиоз вызывает искривление позвоночника в одну сторону. Искривление может быть в любой части позвоночника, но чаще всего поражаются верхний отдел позвоночника и нижняя часть спины. Сколиоз чаще всего встречается на поздних стадиях детства или в раннем подростковом возрасте, когда человек все еще быстро растет. Это чаще встречается у женщин, чем у мужчин. Сколиоз не всегда заметен, но некоторые люди с этим заболеванием могут наклоняться в сторону или иметь неровные плечи или бедра из-за искривления позвоночника. В большинстве случаев пациенту не требуется лечение, потому что кривая часто незначительно прогрессирует. Однако, в зависимости от степени искривления и возраста ребенка, врачи могут порекомендовать сочетание фиксации спины и физиотерапии. Очень небольшому количеству людей со сколиозом может потребоваться операция. Возможные осложнения сколиоза включают хроническую боль, затрудненное дыхание и снижение способности выполнять упражнения. В этой статье мы даем обзор сколиоза, включая его причины, симптомы и лечение. У человека со сколиозом будет изгиб позвоночника в сторону С или S. Чтобы врач мог диагностировать сколиоз, угол Кобба — мера кривизны — должен составлять не менее 10 градусов. Сколиоз может появиться в любом возрасте, но часто он проявляется в возрасте от 10 до 12 лет или в подростковом возрасте. Хотя сколиоз у младенцев встречается редко, детский сколиоз может поражать людей в возрасте до 3 лет. В большинстве случаев причина сколиоза неизвестна.Врачи называют это идиопатическим сколиозом. В других случаях сколиоз может быть связан с церебральным параличом, мышечной дистрофией или расщелиной позвоночника. Как вариант, это может быть врожденная аномалия. Врачи классифицируют изгибы позвоночника как структурные и неструктурные. Структурная кривая постоянна и может быть вызвана заболеванием или травмой. Неструктурный изгиб является временным, что означает, что позвоночник структурно нормален. В любом случае врач попытается найти и исправить или вылечить причину. В большинстве случаев сколиоз у детей и подростков протекает в легкой форме и не требует лечения. При изгибе от 10 до 25 градусов врач обычно будет проходить осмотры с пациентом с интервалами в 3, 6 или 12 месяцев, чтобы проверить, меняется ли состояние. При изгибе от 25 до 40 градусов врач может порекомендовать фиксацию. Если кривая больше, чем это, а скелет все еще незрелый, врач может порекомендовать операцию. При выборе вариантов лечения врач учитывает следующие факторы:
ПовязкаПри детском сколиозе врач может использовать гипсовую повязку вместо фиксации, чтобы помочь позвоночнику ребенка вырасти в обычное положение. Гипс прикрепляется к внешней стороне тела младенца, и они будут носить его постоянно. Поскольку большинство младенцев быстро растут, врачу необходимо будет регулярно менять гипс. ОртезЕсли у человека умеренный сколиоз, а кости все еще растут, врач может порекомендовать скобу.Ортез предотвратит дальнейшее искривление, но не вылечит или не обратит вспять сколиоз. Обычно человеку необходимо носить бандаж постоянно, даже ночью. Его эффективность, как правило, коррелирует с количеством часов в день, которые человек носит бандаж. Ортез обычно не ограничивает возможности человека. Если они хотят заниматься физической активностью, они могут снять скобу. Когда кости перестают расти, бандаж больше не нужен. Существует два типа ортезов: Грудно-пояснично-крестцовый ортез (TLSO) TLSO пластиковый, а его конструкция означает, что он аккуратно облегает изгибы тела. Обычно его не видно под одеждой. Подтяжка Milwaukee Это полноценный ортез для торса с шейным кольцом с упорами для подбородка и затылка. Врачи оставляют за собой право использовать бандаж Milwaukee на тот случай, если TLSO не подходит или неэффективен. Лечение хиропрактикиНекоторые люди посещают мануального терапевта, чтобы облегчить боль и дискомфорт при сколиозе. Хиропрактики манипулируют позвоночником и предлагают альтернативные методы лечения. Они утверждают, что перестройка позвоночника способствует заживлению и благополучию. Хиропрактика может улучшить качество жизни человека со сколиозом. Однако это не лекарство, поскольку оно не устраняет искривление позвоночника. Исследования не доказали, что хиропрактические манипуляции помогают при сколиозе. Людям, желающим посетить мануального терапевта, следует выбрать того, кто специализируется на сколиозе. Лечение хиропрактики у неспециалиста может ухудшить симптомы. УпражненияПри сколиозе могут помочь различные упражнения, и эксперты предлагают ряд стратегий. Однако все они стремятся выровнять позвоночник, грудную клетку, плечи и таз для достижения типичной осанки. Авторы исследования 2016 года заявили, что появляется все больше свидетельств того, что упражнения могут помочь в лечении сколиоза.Однако они отметили, что исследователям необходимо провести дополнительные исследования, чтобы определить, какие упражнения наиболее эффективны. В тяжелых случаях сколиоз может прогрессировать со временем. В этих случаях врач может порекомендовать спондилодез. Эта операция уменьшает искривление позвоночника и предотвращает ухудшение сколиоза. Хирург может использовать металлические стержни, крючки, винты или проволоку, чтобы удерживать часть позвоночника прямо, пока кость заживает. Они также могут использовать костные трансплантаты, чтобы помочь костям зажить. Обычно дети могут вернуться в школу через 4–6 недель и могут заниматься спортом через 3–6 месяцев.Им следует в течение года избегать занятий спортом, вызывающим раздражение спины, например верховой ездой и контактными видами спорта. В некоторых случаях им может потребоваться носить спинной бандаж около 6 месяцев для поддержки позвоночника. Врач порекомендует спондилодез только в том случае, если он ожидает, что польза перевешивает риски. Риски включают:
Нейрохирург может присутствовать во время операции по поводу сколиоза. Сколиоз обычно проявляется в младенчестве или подростковом возрасте.Симптомы различаются в зависимости от возраста человека. Симптомы у подростковНаиболее частая форма сколиоза возникает в подростковом возрасте и известна как подростковый идиопатический сколиоз. Это может повлиять на людей в возрасте от 10 до 18 лет. Симптомы могут включать следующее:
Некоторые виды сколиоза могут вызывать боль в спине, но обычно это не очень болезненно .Этот симптом чаще встречается у пожилых людей. Симптомы у младенцевСимптомы у младенцев могут включать:
Если младенец не получит лечения от сколиоза, он будет больше подвержен риску возникновения проблем в дальнейшей жизни, таких как нарушение функции сердца и легких. Ниже приведены некоторые из возможных причин сколиоза:
Факторы риска сколиоза включают:
Ассоциация сколиоза Великобритании описывает семь основных типов сколиоза:
|
