Фармаклон: Альфарона – интраназальная форма
Состав:
Активные вещества: Интерферон альфа-2b человеческий рекомбинантный – не менее 50 000 МЕ. Вспомогательные вещества: полиглюкин, натрия хлорид, натрия фосфат однозамещенный 2-водный, натрия фосфат двузамещенный
Отпускается
без рецепта
Хранить
в холодильнике
О препарате
АЛЬФАРОНА (интерферон альфа-2b, 50 000 МЕ) идентичен человеческому интерферону, обладает иммуностимулирующим, противовирусным, противовоспалительным и противомикробным действием и показан к применению для профилактики и лечения гриппа и других ОРВИ, особенно в начальных стадиях заболевания. Препарат разрешен детям с первых дней жизни и взрослым. Препарат вводиться интраназально (капли в нос).
Препарат разрешен детям с первых дней жизни и взрослым. Препарат вводиться интраназально (капли в нос).
Форма выпуска, состав и упаковка
Лиофилизат для приготовления раствора для интраназального введения 50000 МЕ
Показания к применению
Профилактика и лечение ОРВИ, гриппа у взрослых и детей на начальных стадиях заболевания.
Противопоказания
Индивидуальная непереносимость препаратов интерферона, аллергические заболевания, протекающие в тяжелой форме.
инструкция по применению. Официальный сайт
Состав:
действующее вещество: interferon alfa-2b;
1 мл препарата содержит интерферона альфа-2b рекомбинантного человека 100 000 МЕ
Вспомогательные вещества: трометамол, трометамола гидрохлорид, гипромеллоза, натрия эдетат, лизина гидрохлорид, калия хлорид, метилпарагидроксибензоат (Е 218), вода для инъекций.
Лекарственная форма. Спрей назальный.
Основные физико-химические свойства: прозрачная бесцветная жидкость.
Фармакологическая группа. Интерфероны. Код АТХ L03A В05.
Фармакологические свойства. ЛАФЕРОБИОН — противовирусное, противомикробное, противовоспалительное и иммуномодулирующее средство. Биологическое действие интерферона характеризуется следующими эффектами: — подавляет репликацию вирусов (аденовирусов, вирусов гриппа и др.) За счет ингибирующего действия на процессы транскрипции и трансляции; антипролиферативным — угнетает размножение клеток (большинства ДНК и РНК-содержащих вирусов) иммуномодуляция — усиление фагоцитарной активности макрофагов и специфической цитотоксичности лимфоцитов относительно клеток-мишеней. Интерферон инициирует синтез специфического фермента — протеинкиназы, которая препятствует трансляции благодаря фосфорилированию одного из инициирующих факторов этого процесса; активизирует специфическую, рибонуклеазу, которая повреждает матричную РНК вируса. К эффектам интерферона относятся также: стимуляция продукции других цитокинов, индукция специфических ферментов.
Интерферон инициирует синтез специфического фермента — протеинкиназы, которая препятствует трансляции благодаря фосфорилированию одного из инициирующих факторов этого процесса; активизирует специфическую, рибонуклеазу, которая повреждает матричную РНК вируса. К эффектам интерферона относятся также: стимуляция продукции других цитокинов, индукция специфических ферментов.
Клинические характеристики.
Показания.
Профилактика и лечение острых респираторных вирусных инфекций (ОРВИ):
— у пациентов, часто и длительно страдающих заболеваниями верхних дыхательных путей
— при контакте с больными ОРВИ;
— при переохлаждении;
— при сезонном повышении заболеваемости.
Противопоказания. Повышенная чувствительность к интерферона альфа-2b и других компонентов, входящих в состав препарата, тяжелые формы аллергических заболеваний в анамнезе применения во время беременности и в период кормления грудью.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий. Не рекомендуется одновременное применение интраназальных сосудосуживающих препаратов, поскольку они способствуют сухости слизистой оболочки носа.
Не рекомендуется одновременное применение интраназальных сосудосуживающих препаратов, поскольку они способствуют сухости слизистой оболочки носа.
Особенности применения. Препарат содержит метилпарагидроксибензоат, который может вызывать аллергические реакции, в том числе отсроченные, в исключительных случаях бронхоспазм.
Не следует применять препарат при нарушении целостности и маркировки упаковки, при изменении физических свойств (цвета или прозрачности жидкости) и после истечения срока годности.
Во избежание распространения инфекции, рекомендуется индивидуальное использование флакона.
Применение в период беременности или кормления грудью. Применение противопоказано.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами. Не влияет.
Способ применения и дозы.
Препарат вводят в каждый носовой ход.
1 спрей-доза = 1 короткое нажатие на дозатор.
Схема применения спрея назального:
1. Снять защитный колпачок с флакона.
Снять защитный колпачок с флакона.
2. Активировать микродозатор-распылитель нажатием (пробное распыление),
3. Находясь в вертикальном положении, поместить конец насадки в носовой ход и нажать на насос-дозатор. Повторить ввод в другой носовой ход.
4. После применения закрыть флакон колпачком.
При первых признаках заболевания ОРВИ (в течение 5 дней)
Взрослым — по 3 спрей-дозы в каждый носовой ход 5-6 раз в день (разовая доза — 30000 МЕ, суточная доза 150000-180000 МЕ).
Дети. Детям в возрасте от 1 до 3 лет — по 2 спрей-дозы в каждый носовой ход 3-4 раза в день (разовая доза-20000 МЕ, суточная доза — 60 000-80 000 МЕ).
Детям в возрасте от 3 до 14 лет — по 2 спрей-дозы в каждый носовой ход 4-5 раз в день (разовая доза -20000 МЕ, суточная доза — 80 000-100 000 МЕ),
Детям в возрасте от 14 до 18 лет — по 3 спрей-дозы в каждый носовой ход 5-6 раз в день (разовая доза -30000 МЕ, суточная доза — 150 000-180 000 МЕ).
Для профилактики респираторных вирусных инфекций взрослым.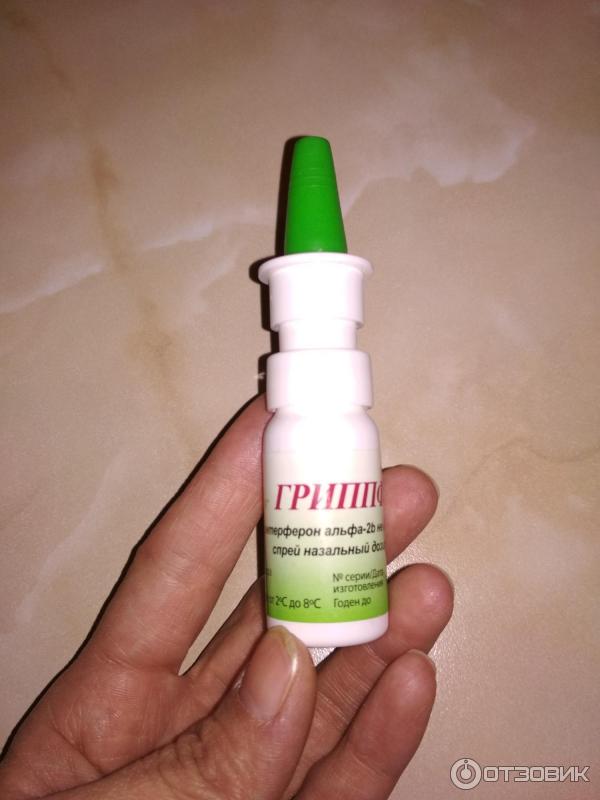
При контакте с больным и при переохлаждении — по 3 спрей-дозы 2 раза в день в течение 5-7 дней. При необходимости профилактические курсы повторяют. При однократном контакте достаточно однократного применения.
При сезонном повышении заболеваемости — однократно утром с интервалом 1-2 суток.
Дети. Препарат применяют детям в возрасте от 1 года при первых признаках заболевания ОРВИ.
Передозировки. Не исследовались.
Побочные реакции.
В единичных случаях — кожная сыпь.
В случае появления нежелательных реакций следует проконсультироваться с врачом.
Срок годности. 2 года. Срок годности после вскрытия флакона, при условии хранения при температуре от 2 до 8 °С — 10 суток.
Условия хранения. Хранить в оригинальной упаковке для защиты от действия света при температуре от 2 до 8 °С.
Хранить в недоступном для детей месте.
Упаковка. По 5 мл во флаконе, закупоренном микродозатором-распылителем; по 1 флакону в пачке из картона.
Категория отпуска. Без рецепта.
Производитель. ООО «ФЗ« БИОФАРМА », Украина.
Местонахождение производителя и его адрес места осуществления деятельности.
Украина, 09100, Киевская обл., г. Белая Церковь, ул. Киевская, 37.
Детальнее о производителе
Генферон Лайт спрей в нос, противовирусное, интерферон 50 тыс. МЕ + таурин 1мг/доза, 100 доз
Краткое описание
При интраназальном применении за счет высокой концентрации в очаге инфекции достигается выраженный местный противовирусный и иммуностимулирующий эффект Показан для профилактики и лечения гриппа и ОРВИ у взрослых и детей старше 14 лет.
Фармакологическое действие
Генферон Лайт — комбинированный препарат, действие которого обусловлено входящими в его состав компонентам. Оказывает местное и системное действие.
Оказывает местное и системное действие.
Интерферон альфа-2 оказывает противовирусное, антибактериальное и иммуномодулирующее действие. Под воздействием интерферона альфа-2 в организме усиливается активность естественных киллеров, Т-хелперов, фагоцитов, а также интенсивность дифференцировки В-лимфоцитов. Активизация лейкоцитов, содержащихся во всех слоях слизистой оболочки, обеспечивает их активное участие в ликвидации первичных патологических очагов и обеспечивает восстановление продукции секреторного иммуноглобулина А.
Интерферон альфа-2 также непосредственно ингибирует репликацию и транскрипцию вирусов, хламидий.
Таурин, входящий в состав препарата, обладает регенерирующими, репаративными, мембранно- и гепатопротективными, антиоксидантными, противовоспалительными свойствами.
Анестезин является местным анестетиком. Уменьшает проницаемость клеточной мембраны для ионов натрия, вытесняет ионы кальция из рецепторов, расположенных на внутренней поверхности мембраны, блокирует проведение нервных импульсов. Препятствует возникновению болевых импульсов в окончаниях чувствительных нервов и их проведению по нервным волокнам.
Препятствует возникновению болевых импульсов в окончаниях чувствительных нервов и их проведению по нервным волокнам.
Показания
В качестве компонента комплексной терапии — для лечения стрых респираторных вирусных инфекций и других инфекционных заболеваний бактериальной и вирусной этиологии у детей;
— для лечения инфекционно-воспалительных заболеваний урогенитального тракта у детей и женщин, в том числе беременных.
Способ
применения и дозировка
Препарат может применяться как вагинально, так и ректально. Способ введения, доза и длительность курса
зависят от возраста, конкретной клинической ситуации и определяются лечащим врачом.
У взрослых и детей старше 7 лет Генферон Лайт применяют в дозе 250 000 ME интерферона альфа-2b на суппозиторий. У детей до 7 лет безопасным является применение препарата в дозе 125 000 ME интерферона альфа-2b на суппозиторий. У женщин, находящихся на 13-40 неделе беременности, препарат применяется в дозе 250 000 MEинтерферона альфа-2b на суппозиторий.
У детей до 7 лет безопасным является применение препарата в дозе 125 000 ME интерферона альфа-2b на суппозиторий. У женщин, находящихся на 13-40 неделе беременности, препарат применяется в дозе 250 000 MEинтерферона альфа-2b на суппозиторий.
Рекомендуемые дозы и режимы лечения:
Острые респираторные вирусные инфекции и другие острые заболевания вирусной природы у детей: по 1 суппозиторию ректально 2 раза в день с 12-часовым интервалом параллельно основной терапии в течение 5 дней. При сохранении симптоматики курс лечения повторяется после 5-дневного интервала.
Хронические инфекционно-воспалительные заболевания вирусной этиологии у детей: по 1 суппозиторию ректально 2 раза в день с 12-часовым интервалом параллельно стандартной терапии в течение 10 дней. Затем в течение 1-3 месяцев — по 1 суппозиторию ректально на ночь через день.
Острые инфекционно-воспалительные заболевания урогенитального тракта у детей: по 1 суппозиторию ректально 2 раза в день с 12-часовым интервалом в течение 10 дней.
Инфекционно-воспалительные заболевания урогенитального тракта у беременных: по 1 суппозиторию вагинально 2 раза в день с 12-часовым интервалом в течение 10 дней.
Инфекционно-воспалительные заболевания урогенитального тракта у женщин: по 1 суппозиторию (250 000 ME) вагинально или ректально (в зависимости от характера заболевания) 2 раза в день с 12-часовым интервалом в течение 10 дней. При затяжных формах 3 раза в неделю через день по 1 суппозиторию в течение 1-3 месяцев.
Побочные действия
Препарат хорошо переносится больными. Возможны местные аллергические реакции (ощущение зуда и жжения во влагалище). Данные явления обратимы и исчезают в течение 72 часов после прекращения введения. Продолжение лечения возможно после консультации с врачом.
До настоящего времени не наблюдалось тяжелых или опасных для жизни побочных явлений. Могут наблюдаться явления, возникающие при применении всех видов интерферона альфа-2b, такие как озноб, повышение температуры, утомляемость, потеря аппетита, мышечные и головные боли, боли в суставах, потливость, а также лейко- и тромбоцитопения, но чаще они встречаются при превышении суточной дозы свыше 10 000 000 ME. В этих случаях рекомендуется консультация лечащего врача для решения вопроса о необходимости отмены препарата или снижения дозы.
В этих случаях рекомендуется консультация лечащего врача для решения вопроса о необходимости отмены препарата или снижения дозы.
Как и для любого другого препарата интерферона альфа, и случае повышения температуры после его введения возможен однократный прием парацетамола в дозе 500-1000 мг для взрослых и 250 мг для детей.
Противопоказания
Индивидуальная непереносимость интерферона и других веществ,
входящих в состав препарата;
— 1 триместр беременности.
С осторожностью: обострение аллергических и аутоиммунных заболеваний.
Передозировка
Случаи передозировки Генферона Лайт не зарегистрированы. При случайном единовременном введении большего числа суппозиториев, чем было предписано врачом, следует приостановить дальнейшее введение на 24 часа, после чего лечение можно возобновить по предписанной схеме.
Особые
указания
Генферон Лайт не влияет на выполнение потенциально опасных видов деятельности, требующих особого внимания и быстрых реакций (управление транспортными средствами, машинным оборудованием и т.п.).
Взаимодействие с другими препаратами
Генферон Лайт наиболее эффективен в качестве компонента комплексной терапии. При сочетании с антибактериальными, фунгицидными и противовирусными препаратами наблюдается взаимное потенцирование действия, что позволяет добиться высокого суммарного терапевтического эффекта.
Условия
хранения
class=»h4-mobile»>
Страница не найдена |
Страница не найдена |
404. Страница не найдена
Страница не найдена
Архив за месяц
ПнВтСрЧтПтСбВс
12
12
1
3031
12
15161718192021
25262728293031
123
45678910
12
17181920212223
31
2728293031
1
1234
567891011
12
891011121314
11121314151617
28293031
1234
12
12345
6789101112
567891011
12131415161718
19202122232425
3456789
17181920212223
24252627282930
12345
13141516171819
20212223242526
2728293031
15161718192021
22232425262728
2930
Архивы
Мар
Апр
Май
Июн
Июл
Авг
Сен
Окт
Ноя
Дек
Метки
Настройки
для слабовидящих
Противовирусные капли в нос Для лечения ОРВИ и гриппа
Противовирусные капли в нос — очень удобное средство от гриппа и ОРВИ. Насколько они эффективны ? Читайте ниже.
Насколько они эффективны ? Читайте ниже.
Противовирусные капли в нос Интерфероны
Самая большая группа противовирусных препаратов применяемых в виде капель, спреев и мазей на слизистую носа — интерфероны. Действующее вещество у них всех — интерферон. Полипептид, обладающий противовирусным и иммуномодулирующим действием.
При интраназальном применении, т. е. при нанесении лекарства на слизистую носа в любом виде интерферон не всасывается, а действует местно — на слизистой, на вирусы, которые ещё не проникли в кровь.
Поэтому, препараты для интраназального применения эффективны в отношении вирусных инфекций, как профилактическое средство. А так же, как лечебное средство в первые 3 дня от начала болезни. Причём, чем раньше начато лечение, тем лучше результат.
Начиная с четвёртого дня от начала болезни интерфероны для интраназального применения бесполезны. И применять их не имеет смысла. Концентрации действующего вещества в рекомендуемых дозах разных назальных интерферонов отличаются в десятки, сотни и, даже, в тысячи раз.
К интерфероновым интраназальным препаратам относятся Российские: Интерферон, Грипферон, Виферон гель, Виферон мазь, Генферон лайт спрей и Украинские: Назоферон и Лаферон Назальный.За пределами стран бывшего СНГ интраназальное применение интерферонов не практикуется.
Показания к применению у всех препаратов аналогичные: профилактика и лечениие ОРВИ, гриппа и герпетической инфекции.
Интерферон человеческий лейкоцитарный сухой
Производится ОАО Биомед Московская обл. Единственный в этой группе препарат, полученный из крови доноров под действием вирусов. Все остальные лекарства относятся к рекомбинантным интерферонам.
Действующее вещество — интерферон альфа-2b. В одной ампуле содержится 1000 МЕ интерферона, в 1 мл — 500 МЕ, в 1 капле примерно 20 МЕ действующего вещества. Самый известный и самый старый из «интерферонов». Выпускается в виде сухого порошка в ампулах. Применяется эндоназально (в каплях в нос) или в ингаляциях (через небулайзер).
Введение лекарства инъекционно категорически запрещено!
В начале болезни интерферон может сильно облегчить и даже оборвать её дальнейшее развитие. Эффективен также для профилактики при ОРВИ и гриппе.
Ампулу вскрывают непосредственно перед применением. В неё до метки наливают кипячёную воду комнатной температуры. Разведённый препарат хранится в холодильнике до 24 часов. Разрешён детям с рождения и взрослым в одинаковой дозе.
Схема профилактики: по 2 капли в каждый носовой ход 2 р/д или по одной ингаляции 2 р/д от десяти дней до одного месяца. Схема лечения: по 5 капель в каждый носовой ход через 2 часа не меньше пяти р/д или в ингаляциях каждые два часа 3-4 р/д в течение первых 3-х дней болезни.
Гриппферон Противовирусные капли в нос
Впервые появился в 1999 г. Российская разработка, производится ЗАО «Фирн М» г.Москва. Отличается от предыдущего тем, что интерферон в нём рекомбинантный (подобный человеческому интерферону альфа-2 В, но полученный генноинженерным способом). И находится в виде готового раствора, не требует специального приготовления перед употреблением. Формы выпуска препарата: капли в нос и назальный спрей. В гриппфероне интерферон находится в концентрации в 20 раз более высокой, чем в предыдущем лекарстве: 10 000 МЕ интерферона — в 1-ом мл, 400 МЕ — в 1-ой капле. Разрешается с рождения.
И находится в виде готового раствора, не требует специального приготовления перед употреблением. Формы выпуска препарата: капли в нос и назальный спрей. В гриппфероне интерферон находится в концентрации в 20 раз более высокой, чем в предыдущем лекарстве: 10 000 МЕ интерферона — в 1-ом мл, 400 МЕ — в 1-ой капле. Разрешается с рождения.
Профилактическая схема: по 1-ой капле или 1-ому впрыскиванию в каждую ноздрю 1-2 р/д от 2-х до 4-х недель.
Схема лечения: детям от рождения до одного года по 1-ой капле или впрыскиванию в каждую ноздрю, от 3-х до 4-х р/д. Детям от одного до трёх лет по две капли от 3-х до 4-х р/д. Детям старше 3х лет и взрослым по две капли в каждую ноздрю от 4-х до 6-ти р/д. Курс лечения 3 дня. Далее применять лекарство не имеет смысла.
Назоферон Противовирусные капли в нос
Производится ПАО «Фармак» Киев. Препарат аналогичен двум предыдущим. Особенно он схож с гриппфероном, также содержит рекомбинантный интерферон альфа-2В, но в концентрации в 10 раз большей, чем в гриппфероне. А именно: 100 000 МЕ — в 1-ом мл и 4 000 МЕ — в 1-ой капле. Выпускается в виде капель и спрея. Капли разрешены с рождения, спрей — с 1-го года.
А именно: 100 000 МЕ — в 1-ом мл и 4 000 МЕ — в 1-ой капле. Выпускается в виде капель и спрея. Капли разрешены с рождения, спрей — с 1-го года.
Схема лечения: детям от рождения до одного года – по 1 капле в каждую ноздрю 5 р/д, от 1-го до 3х лет — 3- 4 р/д в день по 2 капли или по 2 впрыскивания спрея в каждую ноздрю, детям от 3-х до 14-ти лет – 4-5 р/д по 2 капли или по 2 впрыскивания спрея в каждую ноздрю, взрослым – 5-6 р/ д по три впрыскивания спрея или 3 капли в каждую ноздрю. Курс лечения (согласно инструкции) 3-5 дней
С целью профилактики назначается в возрастной дозировке 1 раз в день утром через день.
Лаферон назальный Противовирусные капли в нос
Производится ООО «Научно-производственная кампания Инфармбиотек» г.Киев. Лекарство производится в виде сухого порошка, упакованного в герметичные флаконы. И требует разведения, перед применением кипяченой водой комнатной температуры, как и первый препарат. К флакону прилагается специальный колпачок-капельница.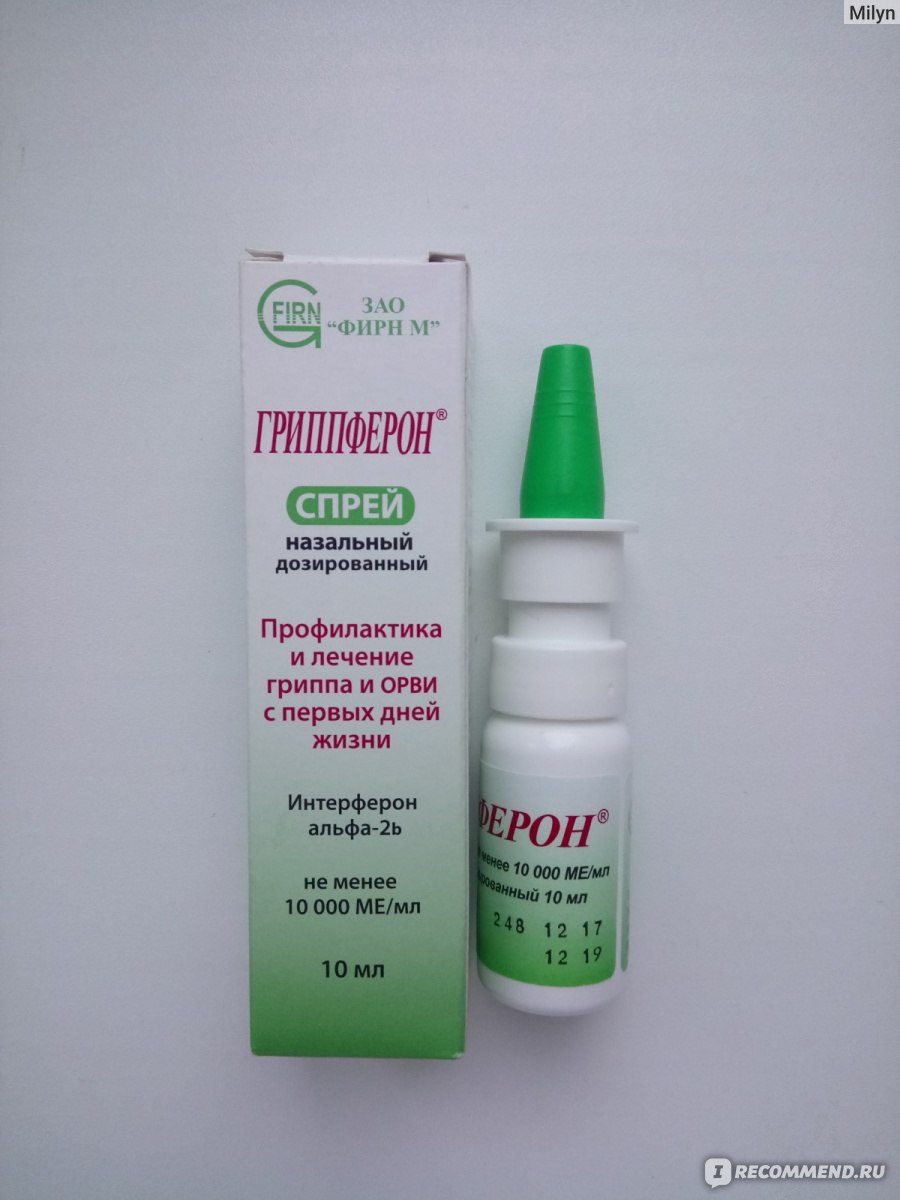 Что делает его значительно более удобным, чем первый препарат, описанный в этой статье, к которому нужно было искать пипетку. В нём содержится всё тот же рекомбинантный интерферон, вдвое большей концентрации, чем в назофероне: 200 000 МЕ — в 1 мл, и 8 000 МЕ — в 1 капле.
Что делает его значительно более удобным, чем первый препарат, описанный в этой статье, к которому нужно было искать пипетку. В нём содержится всё тот же рекомбинантный интерферон, вдвое большей концентрации, чем в назофероне: 200 000 МЕ — в 1 мл, и 8 000 МЕ — в 1 капле.
Схема лечения: Детям от рождения до 1-го года — по 1 капле в каждый носовой ход восемь раз в день, детям от 1-го до 7 лет — по 2-3 капли в каждый носовой ход восемь раз в день, детям от 7-ми до 14-ти лет по 4 капли в каждый носовой ход восемь раз в день, взрослым по 5-6 капель 8-10 раз в день в каждый носовой ход. Курс лечения 3-5 дней.
В профилактических целях рекомендуется по 1-2 капли 4 раза в день 10-30 дней.
Генферон лайт спрей
Содержит всё тот же рекомбинантный интерферон. Рекомендован для взрослых и детей старше 14-ти лет. Т. к. это лекарство пока не прошло клинические испытания на детях. Содержит 50 000 МЕ интерферона в 1 дозе. Это в 2500 раз больше, чем в 1 капле (дозе) интерферона лейкоцитарного человеческого сухого.
Схема лечения: по 1 дозе в каждую ноздрю три раза в день. Курс лечения 3-5 дней.
Профилактическая схема: в инструкции рекомендуется только экстренная профилактика при контакте с больным по той же схеме, что и для лечения, но на протяжении 5-7 дней.
Виферон
Также рекомбинантный интерферон, который можно применять интраназально. Гель и мазь виферон предназначены для нанесения на слизистую оболочку носа и миндалин для профилактики ОРВИ, и для лечения в первые дни болезни. А также в качестве местного лечения при герпетической инфекции.
Гель и мазь сохраняются поверхности дольше, чем капли, за счёт этого увеличивается продолжительность действия лекарства. Но при этом лекарство всё равно действует местно, только в месте нанесения. Концентрация интерферона в 1г мази 40 000 МЕ, в 1г геля — 36 000МЕ.
С целью лечения мазь или гель наносят на заранее подсушенную слизистую носа или поверхность миндалин от 3-х до 5-ти р/д в течение пяти дней.
С целью профилактики — два р/д в на протяжении 2-х-4-х недель.
Другие назальные противовирусные средства
Оксолиновая мазь
Противовирусное средство наружного применения. Одно из самых старых противовирусных средств. Появилась в СССР в 1970-м году, за пределами бывшего СНГ не признана и не зарегистрирована.
Наносится на слизистые оболочки или на кожу и действует непосредственно на вирусы, находящиеся на слизистой, до их проникновения в кровь. С поверхности слизистой носа и кожи оксолиновая мазь частично всасывается, но не оказывает на вирусы, уже попавшие в кровоток никакого воздействия. Токсического, местнораздражающего и других вредных влияний на организм человека также не оказывает.
Для профилактики и лечения гриппа и ОРВИ предназначена 0,25% назальная мазь, её наносят на слизистую оболочку 3-4 р/д, как с целью профилактики в период повышения заболеваемости, так и для лечения в первые дни болезни. 3% оксолиновая мазь предназначена для лечения вирусных заболеваний кожи: бородавок, контагиозного моллюска, герпеса.
3% оксолиновая мазь предназначена для лечения вирусных заболеваний кожи: бородавок, контагиозного моллюска, герпеса.
Деринат Противовирусные капли в нос
Относится к иммуномодуляторам, индукторам эндогенного интерферона. Впервые выпущен в 1996 г. ЗАО «ФП «Техномедсервис» г.Москва. Деринат — дезоксирибонуклеат натрия — лекарство животного происхождения (экстракт из молок осетровых рыб). Повышает противобактериальный, противогрибковый, противовирусный иммунитет, а также активирует процессы восстановления поврежденных тканей.
Деринат стимулирует Т и В- лимфоциты и макрофаги (ускоряет обмен веществ внутри этих клеток, в результате усиливается их активность, в том числе ускоряется синтез интерферонов и иммуноглобулинов).
Выпускается в растворе для внутримышечного введения. Внутримышечно применяется при тяжёлых заболеваниях (туберкулёз, эндометрит) а также для восстановительной терапии при ожогах, пролежнях, трофических язвах, язве желудка.
Для профилактики и лечения гриппа и ОРВИ применяется 0,25% раствор. Для эндоназального применения есть деринат во флаконе-капельнице.
Для эндоназального применения есть деринат во флаконе-капельнице.
Деринат, в отличие от интерферонов, всасывается с поверхности слизистой носа и распределяется по лимфатическим путям. Т.е этот препарат приэндоназальном применении даёт не только местный (в месте нанесения) системный эффект на весь организм вцелом. Его можно применять не только в первые дни болезни, в более поздние сроки: он восстанавливает иммунитет и способствует восстанавлению поврежденных тканей. Разрешён с рождения.
Для лечения гриппа и ОРВИ
Деринат применяется детям любого возраста начиная с рождения и взрослым по следующей схеме: первые два дня ч/з каждые два часа по две капли в каждую ноздрю, 5-6 р/д, с третьего дня по две капли в каждую ноздрю 3-4 р/д в день до полного исчезновения симптомов.
Для профилактики
По две капли 3-4 р/д в течение всего эпид. сезона. Успешно применяется в виде полоскания при стоматитах, как глазные капли при конъюнктивитах и дистрофических заболеваниях глаз. Деринат применяется также для лечения при ОРВИ и затяжных бронхитах и пневмониях в ингаляциях через небулайзер. Для ингаляции берут 0,25% дерината и физ. раствор в равных пропорциях . Ингаляции проводят два р/д в день от 5-ти до 10-ти дней. Наибольший эффект даёт небулайзерная терапия, при размере распыляемых частиц более 5 мкм Надеюсь
Деринат применяется также для лечения при ОРВИ и затяжных бронхитах и пневмониях в ингаляциях через небулайзер. Для ингаляции берут 0,25% дерината и физ. раствор в равных пропорциях . Ингаляции проводят два р/д в день от 5-ти до 10-ти дней. Наибольший эффект даёт небулайзерная терапия, при размере распыляемых частиц более 5 мкм Надеюсь
Вы выбрали для своего ребёнка противовирусные капли в нос. Желаю Вам Здоровья!
Интерферонотерапия ОРВИ у детей
Реферат
Целью нашего исследования была оценка эффективности и переносимости назального спрея Laferobionum ® (100 000 МЕ / мл)
у детей с острыми респираторными вирусными инфекциями. Материалы и методы. В исследование включены 84 ребенка в возрасте от 12 до 18 лет. Дети основной группы (42 человека) дополнительно к стандартному лечению ОРВИ получали спрей Лаферобион ® .Препарат назначали детям 12–14 лет по 2 спрея в каждый носовой ход 4–5 раз в сутки через равные промежутки времени (за исключением времени сна), детям 14–18 лет — по 3 спрея на каждую. носовой ход 5–6 раз в день через равные промежутки времени (исключая время сна). Курс лечения для всех испытуемых составил 5 дней. Дети контрольной группы получали стандартное лечение ОРВИ без Лаферобиона ® . Объективные исследования включали: аускультацию сердца и легких, обследование кожи и слизистых оболочек, измерение пульса, артериального давления и температуры тела.Всем пациентам в лаборатории «Лечебно-диагностический центр Днепропетровской медицинской академии» проводился общий анализ крови, общий анализ мочи, выявление возбудителя методом прямой иммунофлуоресценции (в мазках из носовых ходов). Результаты. В неэпидемический период ведущими вирусными возбудителями острых респираторных вирусных инфекций были респираторно-синцитиальный вирус и аденовирусы. Основными клиническими проявлениями ОРВИ у наблюдаемых больных были признаки общепоспалительного и катарального синдромов.У всех пациентов течение заболевания не было тяжелым. Данные физикального обследования, проведенного перед началом лечения, свидетельствовали об отсутствии клинически значимых отклонений со стороны сердечно-сосудистой системы у детей основной и контрольной групп.
носовой ход 5–6 раз в день через равные промежутки времени (исключая время сна). Курс лечения для всех испытуемых составил 5 дней. Дети контрольной группы получали стандартное лечение ОРВИ без Лаферобиона ® . Объективные исследования включали: аускультацию сердца и легких, обследование кожи и слизистых оболочек, измерение пульса, артериального давления и температуры тела.Всем пациентам в лаборатории «Лечебно-диагностический центр Днепропетровской медицинской академии» проводился общий анализ крови, общий анализ мочи, выявление возбудителя методом прямой иммунофлуоресценции (в мазках из носовых ходов). Результаты. В неэпидемический период ведущими вирусными возбудителями острых респираторных вирусных инфекций были респираторно-синцитиальный вирус и аденовирусы. Основными клиническими проявлениями ОРВИ у наблюдаемых больных были признаки общепоспалительного и катарального синдромов.У всех пациентов течение заболевания не было тяжелым. Данные физикального обследования, проведенного перед началом лечения, свидетельствовали об отсутствии клинически значимых отклонений со стороны сердечно-сосудистой системы у детей основной и контрольной групп. Артериальное давление и частота сердечных сокращений у испытуемых обеих групп находились в пределах возрастных ограничений и соответствовали температурной реакции. Анализируя динамику клинических симптомов ОРВИ в обеих группах, следует отметить стойкую тенденцию к снижению температуры тела у пациентов как основной, так и контрольной групп.Однако в группе пациентов, получавших Лаферобион ® , снижение температурной кривой происходило быстрее, ее нормализация отмечалась уже на 4-е сутки терапии у 100% пациентов, тогда как в контрольной группе на 4-е сутки после начала терапии. При заболевании температура тела оставалась субфебрильной у 12 (28,6%), на 5-е сутки — у 2 (4,8%) детей. Общий анализ крови у детей основной и контрольной групп в начале заболевания выявил лейкопению разной степени тяжести, относительный лимфоцитоз, повышение скорости оседания эритроцитов (СОЭ).На 5-й день терапии у пациентов основной группы количество лейкоцитов нормализовалось, относительный лимфоцитоз сохранялся на фоне снижения СОЭ.
Артериальное давление и частота сердечных сокращений у испытуемых обеих групп находились в пределах возрастных ограничений и соответствовали температурной реакции. Анализируя динамику клинических симптомов ОРВИ в обеих группах, следует отметить стойкую тенденцию к снижению температуры тела у пациентов как основной, так и контрольной групп.Однако в группе пациентов, получавших Лаферобион ® , снижение температурной кривой происходило быстрее, ее нормализация отмечалась уже на 4-е сутки терапии у 100% пациентов, тогда как в контрольной группе на 4-е сутки после начала терапии. При заболевании температура тела оставалась субфебрильной у 12 (28,6%), на 5-е сутки — у 2 (4,8%) детей. Общий анализ крови у детей основной и контрольной групп в начале заболевания выявил лейкопению разной степени тяжести, относительный лимфоцитоз, повышение скорости оседания эритроцитов (СОЭ).На 5-й день терапии у пациентов основной группы количество лейкоцитов нормализовалось, относительный лимфоцитоз сохранялся на фоне снижения СОЭ. В то время как в контрольной группе количество лейкоцитов в периферической крови оставалось ниже при повышенном уровне СОЭ. В течение всего периода наблюдения оценивали наличие и характер возможных осложнений ОРВИ. Общая продолжительность периода наблюдения составила 14 дней. За период наблюдения ни у одного из пациентов основной или контрольной групп осложнений не выявлено.Во время клинического исследования не было зарегистрировано побочных реакций, которые могли быть связаны с приемом Лаферобиона ® . У детей основной группы не было случаев обострения имеющихся хронических заболеваний, а у 1 (2,4%) человека из контрольной группы было обострение хронического тонзиллита. Оценка эффективности терапии препаратом проводилась на 5-й день лечения. Поскольку одним из критериев эффективности было отсутствие клинических признаков заболевания по окончании терапии, мы рассчитали долю пациентов в группах, у которых через 5 дней не было клинических признаков ОРВИ (более 1 балла). дни лечения.
В то время как в контрольной группе количество лейкоцитов в периферической крови оставалось ниже при повышенном уровне СОЭ. В течение всего периода наблюдения оценивали наличие и характер возможных осложнений ОРВИ. Общая продолжительность периода наблюдения составила 14 дней. За период наблюдения ни у одного из пациентов основной или контрольной групп осложнений не выявлено.Во время клинического исследования не было зарегистрировано побочных реакций, которые могли быть связаны с приемом Лаферобиона ® . У детей основной группы не было случаев обострения имеющихся хронических заболеваний, а у 1 (2,4%) человека из контрольной группы было обострение хронического тонзиллита. Оценка эффективности терапии препаратом проводилась на 5-й день лечения. Поскольку одним из критериев эффективности было отсутствие клинических признаков заболевания по окончании терапии, мы рассчитали долю пациентов в группах, у которых через 5 дней не было клинических признаков ОРВИ (более 1 балла). дни лечения. Эффективность терапии Лаферобионом ® составила 100%. Эффективность лечения лаферобионом ® в определенной степени зависела от этиологии заболевания: при ОРВИ, вызванных респираторно-синцитиальным вирусом, влияние терапии интерфероном на течение заболевания было менее значительным, чем при ОРВИ. инфекции, вызванные вирусами гриппа и парагриппа. При отсутствии субъективных жалоб со стороны обследуемых и отрицательных изменений объективного и лабораторного обследования переносимость лечения у всех пациентов, получавших Лаферобион ® , была оценена как «хорошая». Выводы. Интерферонотерапия, в частности использование рекомбинантных интерферонов α-2b (Laferobionum ® ), является одним из важнейших компонентов лечения острых респираторных вирусных заболеваний у детей. Использование интерферона для интраназального введения, способствующего саногенезу ОРЗ, ускорит процесс выздоровления, предотвратит развитие бактериальных осложнений.
Эффективность терапии Лаферобионом ® составила 100%. Эффективность лечения лаферобионом ® в определенной степени зависела от этиологии заболевания: при ОРВИ, вызванных респираторно-синцитиальным вирусом, влияние терапии интерфероном на течение заболевания было менее значительным, чем при ОРВИ. инфекции, вызванные вирусами гриппа и парагриппа. При отсутствии субъективных жалоб со стороны обследуемых и отрицательных изменений объективного и лабораторного обследования переносимость лечения у всех пациентов, получавших Лаферобион ® , была оценена как «хорошая». Выводы. Интерферонотерапия, в частности использование рекомбинантных интерферонов α-2b (Laferobionum ® ), является одним из важнейших компонентов лечения острых респираторных вирусных заболеваний у детей. Использование интерферона для интраназального введения, способствующего саногенезу ОРЗ, ускорит процесс выздоровления, предотвратит развитие бактериальных осложнений.
Рекомендации
Абатуров А.Е., Волосовец А.П., Юлиш Е.И.Индукция молекулярных механизмов неспецифической защиты респираторного тракта. Киев: Приватна друкарня ФО-II Сторожук О.В.; 2012. 240 с. (На русском).
Бекетова Г.В. Интерфероны в лечении ОРЗ у детей. Ліки Украины. 2011; 3: 106-9. (На русском).
Беш Л.В. Оценка эффективности препаратов интерферона при лечении ОРВИ у больных детей.Здоровые Ребенка. 2015: 2 (61): 32-6. (На украинском языке). DOI: 10.22141 / 2224-0551.2.61.2015.75045.
Василевский И.В., Лавриненко А.В. Клиническая и фармакологическая замена интерферона в клинической практике. Здравоохранение. 2016; 7: 51-63. (На русском).
Заплатников А.Л., Коровина Н.А., Гирина А.А., Суздаленко А.В., Леписева И.В. Современные возможности иммонопрофилактики ОРЗ у часто болеющих детей.Педиатрическая фармакология. 2008; 1: 21-6. (На русском).
Захарова И.Н., Чебуркин А.В., Малиновская В.В. и др. Значение интерфероновой системы в формировании иммунного ответа у детей с острыми респираторными вирусными инфекциями. Вопросы практической педиатрии. 2009; 4 (6): 38-45. (На русском).
Вопросы практической педиатрии. 2009; 4 (6): 38-45. (На русском).
Кузнецов С.В., Копейченко ТС. Интерферонотерапия ОРВИ у детей. Актуальная инфектология.2016; 1 (10): 48-50. (На украинском языке). DOI: 10.22141 / 2312-413x.1.10.2016.74543.
Лободанов С.А., Файзулоев Е.Б., Никонова А.А. и др. Этиология ОРВИ: новые аспекты. Санитарный врач. 2011; 10: 049-52. (На русском).
Марушко Ю.В., Голубовская Ю.Е, Марушко Е.Ю. Использование рекомбинантного интерферона альфа-2b в педиатрической практике. Здоровые Ребенка. 2016; 2 (70): 81-6. (На украинском языке). DOI: 10.22141 / 2224-0551.2.70.2016.73817.
Нестерова И.В.Препараты интерферона альфа в клинической практике. Российский аллергологический журнал. 2010; 2: 43-52. (На русском).
Нянковский С.Л., Нянковская О.С., Яцула МС. Клинические особенности применения интерферонов в лечении ОРВИ у детей. Здоровые Ребенка. 2015; 5 (64): 7-12. (На украинском языке). DOI: 10.22141 / 2224-0551.5.65.2015.74904.
Попкова Н.И., Якупова Р.С. Роль вирусов в развитии респираторных заболеваний у детей.Альманах молодой науки. 2013; 1: 28-31. (На русском).
Тютюнников С.В., Антонов Ю.А., Кузякин Г.В., Налимова И.С. Влияние топического рекомбинантного интерферона альфа-2b на концентрацию цитокинов в слюне больных гриппом A / h2N1. Вестник современной клинической медицины. 2014; 7 (Приложение 1): 106-12. (На русском). DOI: 10.20969 / VSKM.2014.7 (добавление 1) .1-166.
Хмелевской В.И., Провоторов В.Ю., Киселева В.В., Девянин О.А.Альфа-интерферон в клинической практике. 2014; 5 (19): 34-8. (На русском). DOI: 10.20514 / 2226-6704-2014-0-5-34-38.
Юлиш Е.И., Чернышова О.Е. Этиопатогенетическая терапия острых респираторных вирусных инфекций у детей. Здоровые Ребенка. 2014; 1 (52): 71-5. (На русском). DOI: 10.22141 / 2224-0551.1.52.2014.75622.
Channappanavar R, Fehr AR, Vijay R, et al. Нарушение регуляции интерферона I типа и воспалительные реакции моноцитов-макрофагов вызывают летальную пневмонию у мышей, инфицированных SARS-CoV. Клеточный микроб-хозяин. 2016 10 февраля; 19 (2): 181-93. DOI: 10.1016 / j.chom.2016.01.007.
Клеточный микроб-хозяин. 2016 10 февраля; 19 (2): 181-93. DOI: 10.1016 / j.chom.2016.01.007.
Дэвидсон С. МакКейб TM, Кротта С. и др. IFNλ является сильнодействующим противогриппозным лекарственным средством без побочных воспалительных эффектов лечения IFNα. EMBO Mol Med. 2016 1 сентября; 8 (9): 1099-112. DOI: 10.15252 / emmm.201606413.
Gao L, Yu S, Chen Q, et al. Рандомизированное контролируемое испытание назального спрея низких доз рекомбинантных человеческих интерферонов альфа-2b для профилактики острых респираторных вирусных инфекций у призывников.Вакцина. 17 июня 2010 г .; 28 (28): 4445-51. DOI: 10.1016 / j.vaccine.2010.03.062.
Гарсия-Састре А., Егоров А., Матасов Д. и др. Вирус гриппа А, лишенный гена NS1, реплицируется в интерферон-дефицитных системах. Вирусология. 1998 20 декабря; 252 (2): 324-30. DOI: 10.1006 / viro.1998.9508.
Горицка М., Дюрант Л. Р., Перейра С. и др. Передача сигналов рецептора альфа / бета интерферона усиливает раннюю продукцию провоспалительных цитокинов в легких во время респираторно-синцитиальной вирусной инфекции. J Virol. 2014 июн; 88 (11): 6128-36. DOI: 10.1128 / JVI.00333-14.
J Virol. 2014 июн; 88 (11): 6128-36. DOI: 10.1128 / JVI.00333-14.
Макрис С., Полсен М., Йоханссон С. Интерфероны типа I как регуляторы воспаления легких. Фронт Иммунол. 2017 10 марта; 8: 259. DOI: 10.3389 / fimmu.2017.00259.
Nan Y, Nan G, Zhang YJ. Индукция интерферона вирусами РНК и антагонизм вирусными патогенами. Вирусы. 2014 12 декабря; 6 (12): 4999-5027. DOI: 10.3390 / v6124999.
Ногалес А., Мартинес-Собридо Л., Топхэм Д. Д. и др.Аминокислотные изменения белка NS1 D189N и V194I влияют на интерфероновую реакцию, термочувствительность и вирулентность циркулирующих вирусов гриппа человека h4N2. J Virol. 2017 14 февраля; 91 (5). pii: e01930-16. DOI: 10.1128 / JVI.01930-16.
Seo SU, Kwon HJ, Ko HJ и др. Передача сигналов интерферона типа I регулирует моноциты и нейтрофилы Ly6C (hi) во время острой вирусной пневмонии у мышей. PLoS Pathog. 2011 Февраль; 7 (2): e1001304. DOI: 10.1371 / journal.ppat.1001304.
Многоцентровое рандомизированное проспективное исследование по лечению детского бронхиолита с помощью распыления интерферона α1b
Аннотация
Фон
Респираторно-синцитиальный вирус (RSV) является основной причиной бронхиолита у младенцев, а интерферон (IFN) α является коммерческим противовирусным препаратом. Распыление IFN α1b может быть эффективным методом лечения. В этом многоцентровом проспективном исследовании изучались терапевтические эффекты и безопасность доставки IFN α1b с помощью распыления при детском бронхиолите.
Распыление IFN α1b может быть эффективным методом лечения. В этом многоцентровом проспективном исследовании изучались терапевтические эффекты и безопасность доставки IFN α1b с помощью распыления при детском бронхиолите.
Методы и выводы
Были включены
пациентов с бронхиолитом, госпитализированных в 22 больницы, которые соответствовали критериям включения, и случайным образом разделены на четыре группы: контрольная группа, группа для внутримышечных инъекций IFN, группы распыления IFN 1 (1 мкг / кг) и группы распыления IFN 2 (2 мкг / кг).Все пациенты наблюдались 7 дней. Были оценены терапевтические эффекты и безопасность различных доз доставки IFN и способов доставки. Изменение степени тяжести кашля, по оценке исследователей и родителей, между 1 и 3 днями значительно различается между группами, получавшими небулайзирование IFN 2, и контрольной группой. Изменение оценки свистящего дыхания по Лоуэллу между 3 и 5 днями значительно различается между IFN-распылителем 1 и контрольной группой. Между четырьмя группами не было значительных различий в отношении количества дней подряд с лихорадкой, трехвогнутым признаком, утомляемостью и сонливостью и потерей аппетита.Случаев тяжелых осложнений, рецидива лихорадки и регресса психического статуса не было.
Между четырьмя группами не было значительных различий в отношении количества дней подряд с лихорадкой, трехвогнутым признаком, утомляемостью и сонливостью и потерей аппетита.Случаев тяжелых осложнений, рецидива лихорадки и регресса психического статуса не было.
Выводы
IFN-α1b может более эффективно облегчить кашель и хрипы при бронхиолите. Распыление IFN-α1b имело значительные преимущества в сокращении продолжительности свистящего дыхания и облегчении кашля.
Образец цитирования: Chen L, Shi M, Deng Q, Liu W, Li Q, Ye P, et al. (2020) Многоцентровое рандомизированное проспективное исследование по лечению детского бронхиолита с помощью распыления интерферона α1b.PLoS ONE 15 (2):
e0228391.
https://doi.org/10.1371/journal.pone.0228391
Редактор: Стефания А. Кормье, Университет штата Луизиана, США
Поступила: 7 октября 2019 г .; Принята к печати: 14 января 2020 г . ; Опубликовано: 21 февраля 2020 г.
; Опубликовано: 21 февраля 2020 г.
Авторские права: © 2020 Chen et al. Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Доступность данных: Все соответствующие данные находятся в рукописи и ее файлах с вспомогательной информацией.
Финансирование: LC было профинансировано Программой поддержки Департамента науки и технологий провинции Сычуань (№ 2015SZ0152). HL финансировалась Программой поддержки Департамента науки и технологий провинции Сычуань (№ 2013SZ0040). Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Конкурирующие интересы: LC был профинансирован Программой поддержки Департамента науки и технологий провинции Сычуань (№ 2015SZ0152). HL финансировалась Программой поддержки Департамента науки и технологий провинции Сычуань (№ 2013SZ0040). Авторы заявили, что не существует никаких конкурирующих интересов.
HL финансировалась Программой поддержки Департамента науки и технологий провинции Сычуань (№ 2013SZ0040). Авторы заявили, что не существует никаких конкурирующих интересов.
Введение
Бронхиолит — одно из наиболее распространенных острых воспалительных заболеваний нижних дыхательных путей, встречающихся у младенцев и детей раннего возраста, особенно зимой и весной [1].В развивающихся странах зарегистрировано около 34 миллионов случаев бронхиолита, вызванного респираторно-синцитиальным вирусом (РСВ), среди детей в возрасте до 5 лет [2]. В США бронхиолит является основной причиной госпитализации детей младше 1 года. Основными симптомами бронхиолита являются одышка и затрудненное дыхание, а тяжелые случаи могут быть опасными для жизни. Что еще более важно, результаты нескольких ретроспективных и проспективных эпидемиологических исследований показали, что риск детской астмы и аллергического ринита в 5-6 раз выше среди пациентов, которые заразились бронхиолитом, вызванным RSV, в раннем детстве, что значительно увеличивает экономическое и психологическое бремя для общества. и пострадавшие семьи [3].
и пострадавшие семьи [3].
В настоящее время не хватает эффективных средств лечения бронхиолита. Согласно сводке «Консенсуса экспертов по диагностике, лечению и профилактике бронхиолита» [4] о терапевтических исследованиях, проведенных в последние годы, доступных препаратов для этиологического лечения с подтвержденной терапевтической эффективностью нет, вероятно, потому, что бронхиолит чаще всего вызывается RSV. , риновирус, метапневмовирус и другие респираторные вирусы [5]. Более того, симптоматическое лечение, включая глюкокортикоиды, бронходилататоры и гипертонический солевой раствор, не имеет доказательной поддержки высокого уровня [6].Хотя большинство случаев проходят самостоятельно, возникновение тяжелых случаев и долгосрочные последствия потенциальной последующей астмы подчеркивают необходимость новых стратегий лечения.
В обзоре патогенеза бронхиолита наше внимание было привлечено к влиянию интерферона α (IFN-α) на активацию организма иммунной системы против вирусных инфекций. Инвазия экзогенных вирусов активирует экспрессию IFN-α через взаимодействие с рецепторами распознавания образов. IFN-α в основном продуцируется лейкоцитами, фибробластами и клетками ткани, инфицированной вирусом, на ранних стадиях вирусной инфекции.Индуцируя экспрессию различных белков с противовирусной и иммунной ролью, IFN-α оказывает противовирусное действие, ограничивая распространение вируса в пораженной области и подавляя репликацию вируса [7]. Экзогенный IFN-α является лекарственным средством, продаваемым на рынке, но имеет ограниченное клиническое применение в педиатрии, поскольку препарат вводится внутримышечно. Однако недавние достижения в области распыления могут предоставить альтернативный метод доставки лекарств. Несколько предварительных исследований показали, что рецепторы IFN-α экспрессируются в эпителиальных клетках дыхательных путей [8], и обнаружили, что распыление IFN-α1b (основного противовирусного подтипа в китайской популяции) [9] привело к значительному облегчение симптомов на животных моделях и в случаях бронхиолита [10–11].
Инвазия экзогенных вирусов активирует экспрессию IFN-α через взаимодействие с рецепторами распознавания образов. IFN-α в основном продуцируется лейкоцитами, фибробластами и клетками ткани, инфицированной вирусом, на ранних стадиях вирусной инфекции.Индуцируя экспрессию различных белков с противовирусной и иммунной ролью, IFN-α оказывает противовирусное действие, ограничивая распространение вируса в пораженной области и подавляя репликацию вируса [7]. Экзогенный IFN-α является лекарственным средством, продаваемым на рынке, но имеет ограниченное клиническое применение в педиатрии, поскольку препарат вводится внутримышечно. Однако недавние достижения в области распыления могут предоставить альтернативный метод доставки лекарств. Несколько предварительных исследований показали, что рецепторы IFN-α экспрессируются в эпителиальных клетках дыхательных путей [8], и обнаружили, что распыление IFN-α1b (основного противовирусного подтипа в китайской популяции) [9] привело к значительному облегчение симптомов на животных моделях и в случаях бронхиолита [10–11]. Поэтому мы провели многоцентровое рандомизированное открытое проспективное исследование для изучения терапевтической эффективности и безопасности распыления IFN-α1b в случаях детского бронхиолита.
Поэтому мы провели многоцентровое рандомизированное открытое проспективное исследование для изучения терапевтической эффективности и безопасности распыления IFN-α1b в случаях детского бронхиолита.
Материалы и методы
Предметы и группировки
Было проведено рандомизированное открытое контролируемое многоцентровое исследование. Исследование было рассмотрено и одобрено этическим комитетом больницы Второго университета Западного Китая (№ 2014-022). Это клиническое испытание было зарегистрировано в Китайском реестре клинических испытаний (No.ChiCTR-IPR-14005413). Исследователи, участвовавшие в исследовании, прошли обширную стандартизированную подготовку. В период с декабря 2014 г. по апрель 2016 г. в 22 больницах третичного общего профиля или специализированных больницах в провинции Сычуань было зарегистрировано 675 пациентов с бронхиолитом, которые соответствовали критериям включения. Информированное согласие было предоставлено в письменной форме родителями пациента. Исследователь, который не участвовал в наборе, диагностике и оценке лечения, сообщил клиническому персоналу информацию о группах пациентов на основе унифицированных кодов, которые были случайным образом присвоены с помощью таблицы случайных чисел в соответствии с порядком поступления.Субъекты были случайным образом разделены на четыре группы, то есть контрольную группу, группу внутримышечной инъекции интерферона, группу распыления низких доз интерферона и группу распыления высоких доз интерферона (четыре группы будут называться контрольной группой, инъекцией интерферона, Распыление IFN 1 и распыление IFN 2). Все авторы имели доступ к информации, которая могла идентифицировать отдельных участников во время или после сбора данных, и обязались не разглашать эту информацию.
Исследователь, который не участвовал в наборе, диагностике и оценке лечения, сообщил клиническому персоналу информацию о группах пациентов на основе унифицированных кодов, которые были случайным образом присвоены с помощью таблицы случайных чисел в соответствии с порядком поступления.Субъекты были случайным образом разделены на четыре группы, то есть контрольную группу, группу внутримышечной инъекции интерферона, группу распыления низких доз интерферона и группу распыления высоких доз интерферона (четыре группы будут называться контрольной группой, инъекцией интерферона, Распыление IFN 1 и распыление IFN 2). Все авторы имели доступ к информации, которая могла идентифицировать отдельных участников во время или после сбора данных, и обязались не разглашать эту информацию.
Критерии включения, исключения и исключения
Критерии включения.
(1) Диагностика бронхиолита при первом посещении больницы. Диагностические критерии основывались на диагностических критериях вирусного бронхиолита и основных показаниях к госпитализации в «Руководстве по ведению внебольничной пневмонии у детей» (пересмотренное издание 2013 г. ) »[12] и« Консенсусе экспертов по диагностике, лечению и профилактике. бронхиолита (издание 2014 г.) »Специализированной группой респираторных заболеваний Общества педиатров Китайской медицинской ассоциации [13].(2) возраст 0–12 месяцев и продолжительность заболевания ≤ 48 часов.
) »[12] и« Консенсусе экспертов по диагностике, лечению и профилактике. бронхиолита (издание 2014 г.) »Специализированной группой респираторных заболеваний Общества педиатров Китайской медицинской ассоциации [13].(2) возраст 0–12 месяцев и продолжительность заболевания ≤ 48 часов.
Критериями исключения были следующие: (1) пациенты с тяжелым бронхиолитом, в том числе пациенты с шоком или расстройствами сознания, рецидивирующим апноэ или медленным и нерегулярным дыханием; (2) пациенты, принимающие системные глюкокортикоиды, противовирусные препараты, препараты традиционной китайской медицины (ТКМ) с противовирусным действием и другие иммуномодуляторы в течение 2 недель до госпитализации; (3) пациенты с бронхолегочной дисплазией, шоком, врожденными пороками сердца, сердечной недостаточностью, нарушениями функции печени, почек и кроветворения, эпилепсией и другими нарушениями центральной нервной системы; (4) пациенты с известной аллергией на продукты интерферона.
Критерии исключения были следующими: (1) пациенты, которые не соответствовали диагнозу бронхиолита после включения в лечение; (2) пациенты, у которых во время исследования наблюдались аллергические реакции, нежелательные явления или серьезные нежелательные явления; (3) пациенты, которые добровольно отказались от участия в исследовании; (4) пациенты, которым врач посоветовал прекратить исследование; (5) пациенты с серьезными нарушениями протокола.
Протокол исследования
Этим четырем группам назначали строго ограниченное симптоматическое лечение, которое включало жаропонижающие, анальгетики, аспирацию мокроты, если необходимо, во время ингаляции кислорода, ингаляцию будесонида с агонистами рецептора β2 и перорально вводимые агонисты рецептора β2.Любое использование неисследованных противовирусных агентов было строго запрещено, а при использовании системных глюкокортикоидов велись подробные записи. Контрольной группе проводилось только симптоматическое лечение. В дополнение к симптоматическому лечению, пациентам, получавшим инъекцию IFN, вводили внутримышечно IFN-α1b (от Kexing Biotech Co., Ltd, Шэньчжэнь, Китай, 10 мкг, один раз в день), пациентам, получавшим IFN-распыление 1, вводили IFN-α1b. (1 мкг / кг, доза выбрана и пересмотрена из [11]), растворенная в 4 мл 0.9% физиологический раствор для инъекций, спрессованный и распыленный (распылителями от PARI GmbH, Штарнберг, Германия) в течение 20 минут два раза в день, а пациентам в распылении IFN 2 вводили распыленный IFN-α1b (2 мкг / кг, доза была выбрана и изменена из [11]) по 20 минут дважды в день. Продолжительность использования IFN-α1b для всех трех обработанных групп составляла 7 дней. Доступ к протоколу можно получить, связавшись с соответствующими авторами.
Продолжительность использования IFN-α1b для всех трех обработанных групп составляла 7 дней. Доступ к протоколу можно получить, связавшись с соответствующими авторами.
Результаты
- Общее состояние
Температура тела, частота дыхания, пульс и другие показатели жизненно важных функций пациентов регистрировались ежедневно с регулярными интервалами в течение периода наблюдения. - Наблюдались и регистрировались изменения кашля, хрипов, оксигенации, хрипов и трех вогнутого признака (впадины в надгрудинной ямке, надключичной ямке и межреберном промежутке). Кашель оценивался с помощью визуальной аналоговой шкалы, которую оценивали тот же врач отделения и родители пациента через фиксированные промежутки времени. Свистящее дыхание оценивалось врачом отделения с помощью прибора для оценки респираторного дистресс-синдрома (баллы по оценке свистящего дыхания Лоуэлла), как показано в таблице 1. Оксигенацию оценивали посредством чрескожного измерения насыщения кислородом.
 Другие факторы ежедневно оценивались врачом отделения через определенные промежутки времени.
Другие факторы ежедневно оценивались врачом отделения через определенные промежутки времени. - Показатели безопасности включали изменения температуры пациента, частоту появления гриппоподобных симптомов, сыпь, усталость и сонливость, потерю аппетита и другие побочные эффекты во время периода лечения.
Степень облегчения симптомов в каждой группе определялась путем измерения разницы между днями 1 и 3, днями 3 и 5, а также днями 5 и 7. Для оценки эффекта различных методы лечения ИФН по облегчению симптомов статистическими методами.
Статистические методы
Для обработки данных использовался
SPSS 16.0. Данные измерений были выражены с использованием. Тест Колмогорова – Смирнова использовался для проверки нормальности распределения данных. Для искаженных данных сравнение между четырьмя группами проводилось с использованием критерия Краскела – Уоллиса, а попарные сравнения — с использованием критерия U Манна – Уитни. Для нормально распределенных данных сравнение между четырьмя группами проводилось с использованием одностороннего дисперсионного анализа. Парные сравнения проводились с использованием критерия наименьшего значимого различия.Данные подсчета анализировали с использованием критерия хи-сукаред. Пороговое значение P составляло 0,05 и было скорректировано методом Бонферрони для множественных сравнений.
Парные сравнения проводились с использованием критерия наименьшего значимого различия.Данные подсчета анализировали с использованием критерия хи-сукаред. Пороговое значение P составляло 0,05 и было скорректировано методом Бонферрони для множественных сравнений.
Результаты
Общее состояние включенных пациентов
В общей сложности 675 пациентов были зарегистрированы в 22 центрах, в том числе 600 допустимых и 75 выбывших пациентов, что составляет 11,1%. Причины отсева включали просьбы родителей о досрочной выписке, неполную информацию в CRF (Форме описания случая) и пероральный прием лекарств традиционной китайской медицины родителями.600 достоверных случаев были разделены на четыре группы по 150 случаев в каждой группе (рис. 1). Пациенты включали 407 мальчиков и 193 девочки с соотношением мужчин и женщин 2,1: 1. Возрастной диапазон составлял 243,91 ± 7,16 дней, и 97,8% пациентов были ханьской национальности. Длительность заболевания при включении составила 1,28 ± 0,48 дня.
Были проанализированы исходные данные всех групп. Не было значительных различий в возрасте, оценке кашля, оцененной исследователями, оценке кашля, оцененной родителями, оценке хрипов Лоуэлла и насыщении кислородом между группами (таблица 2).Не было значительных различий по полу, лихорадке, патологическим результатам рентгенографического исследования грудной клетки и применению антибиотиков при включении в группы. Частота появления трех-вогнутого знака в контрольной группе была значительно ниже, чем в других группах (таблица 3).
Сравнение средств от кашля
Сравнение оценок кашля, оцененных исследователями в разные моменты времени, показало, что различия в баллах между 1 и 3 днями и между 3 и 5 днями были статистически значимыми среди четырех групп, тогда как различия между 5 и 7 днями не были ( Таблица 4, значения p были равны 0.003, 0,005 и 0,280 соответственно).
Парные сравнения между парами из четырех групп показали, что в отношении разницы в баллах между 1 и 3 днями распыление IFN 2 значительно отличается от контрольной группы (значение p было <0,001), тогда как инъекция IFN и распыление IFN 1 достоверно не отличался от контрольной группы. Что касается различий в баллах между 3 и 5 днями, инъекции IFN, распыление IFN 1 и распыление IFN 2 значительно отличались от контрольной группы ( p = 0.004, 0,003 и 0,009 соответственно) (Таблица 5).
Что касается различий в баллах между 3 и 5 днями, инъекции IFN, распыление IFN 1 и распыление IFN 2 значительно отличались от контрольной группы ( p = 0.004, 0,003 и 0,009 соответственно) (Таблица 5).
При сравнении показателей кашля, оцененных родителями в разные моменты времени, разница в баллах между 1 и 3 днями была статистически значимой среди четырех групп, тогда как баллы между 3 и 5 и 5 и 7 днями существенно не различались (Таблица 6, значения p были <0,001, 0,042 и 0,075 соответственно).
Попарные сравнения между четырьмя группами показали, что в отношении различий в баллах между 1 и 3 днями инъекции IFN и распыление IFN 2 значительно отличались от контрольной группы (значения p были равны 0.001 и <0,001 соответственно). Что касается различий в баллах между 3 и 5 днями, не было значимых результатов при сравнении трех групп IFN с контрольной группой, а также не было статистически значимых различий в парных сравнениях между тремя группами IFN (таблица 7).
Сравнение облегчения хрипов
Сравнение различий в оценке хрипов Лоуэлла между разными временными точками среди четырех групп показало, что разница в баллах между 3 и 5 днями была статистически значимой, тогда как различия между днями 1 и 3, 5 и 7 не были (таблица 8, p значения были <0.001, 0,165 и 0,149 соответственно).
Попарные сравнения между четырьмя группами показали, что не было значительных различий в отношении различий в баллах между 1 и 3 днями. Что касается различий в баллах между 3 и 5 днями, только распыление IFN 1 достоверно отличалось от контрольной группы (таблица 9 значение p было <0,001).
Замечания по технике безопасности
Не было сообщений о побочных эффектах, связанных с введением IFN, таких как боль, отек или покраснение в области инъекции и бронхоспазм.Для облегчения статистического анализа сыпь после лечения, рецидив лихорадки после снижения и регресс психического статуса были включены в качестве побочных явлений. Результаты этого анализа показали отсутствие серьезных осложнений, рецидива лихорадки после уменьшения симптомов и регресса психического статуса. У трех пациентов появилась сыпь; один случай появился через 2 дня в контрольной группе, и два случая появились между 4 и 6 днями при распылении IFN 1. Два случая показали легкую степень плохого психического статуса и плохого аппетита через 5 дней после лечения при распылении IFN 1, которые исчезли после 1 день симптоматического лечения.
Результаты этого анализа показали отсутствие серьезных осложнений, рецидива лихорадки после уменьшения симптомов и регресса психического статуса. У трех пациентов появилась сыпь; один случай появился через 2 дня в контрольной группе, и два случая появились между 4 и 6 днями при распылении IFN 1. Два случая показали легкую степень плохого психического статуса и плохого аппетита через 5 дней после лечения при распылении IFN 1, которые исчезли после 1 день симптоматического лечения.
Обсуждение
Возможность лечения с помощью распыления IFN
Доказательные исследования показывают, что существует ограниченное количество лекарств с подтвержденной клинической эффективностью при бронхиолите. IFN — один из ключевых эндогенных противовирусных факторов в организме человека. Исследования показали, что антивирусные эффекты, оказываемые IFN-α1b, в первую очередь достигаются за счет индукции продукции антивирусных белков и активации клеточного иммунитета. Ли и др. сообщили о лечении модели мышей, инфицированных RSV, распыленным IFN-α1b [10], и их результаты показали, что IFN-α1b может значительно ингибировать распространение вируса и смягчить интерстициальное воспаление легких. Многочисленные клинические исследования на небольшой выборке показали, что IFN-α1b может эффективно облегчать клинические проявления. Многоцентровое исследование Shang et al. также показали аналогичные результаты [11].
Многочисленные клинические исследования на небольшой выборке показали, что IFN-α1b может эффективно облегчать клинические проявления. Многоцентровое исследование Shang et al. также показали аналогичные результаты [11].
Многочисленные исследования продемонстрировали терапевтическую эффективность внутримышечных инъекций ИФН при бронхиолите [8]. Поскольку очаг поражения бронхиолита расположен в бронхиолах, теоретически местное действие лекарств, доставляемых посредством распыления, может иметь следующие преимущества: (1) быстрое начало терапевтического эффекта благодаря прямому пути действия; (2) прямое действие лекарства из-за большого разнообразия рецепторов лекарства в слизистой оболочке дыхательных путей и подслизистой оболочке; (3) сокращение использования системных лекарств со случайным увлажнением дыхательных путей и разжижением мокроты; (4) снижение травматизма по сравнению с внутримышечной инъекцией у педиатрических пациентов и большее соблюдение пациентом режима лечения. Следовательно, ингаляция распыленного IFN имеет потенциальные перспективы для будущего клинического применения.
Следовательно, ингаляция распыленного IFN имеет потенциальные перспективы для будущего клинического применения.
Доставка лекарств распылением должна удовлетворять некоторым основным требованиям. Распыленные частицы должны иметь соответствующий размер, биологические свойства распыленных частиц IFN должны быть стабильными, и лекарство должно иметь возможность проникать в эпителиальные клетки слизистой оболочки, чтобы оказывать свое действие. Фармакокинетическое исследование вдыхания распыленного IFN-α1b на кроликах показало, что по сравнению с обычной внутримышечной инъекцией, вдыхание распыленного IFN-α1b значительно увеличивает концентрацию IFN-α1b в легких с более длительным временем пребывания в легких.Концентрация IFN-α1b через 12 часов была в четыре раза выше, чем при внутримышечной инъекции, время пика концентрации в крови было значительно отложено до 8 часов, а уровни препарата в почечной ткани постоянно оставались низкими. Это косвенно демонстрирует клиническую осуществимость доставки IFN-α1b с помощью распыления [15].
Анализ эффективности лечения бронхиолита с помощью распыления IFN-α1b
В этом исследовании мы оптимизировали дизайн протокола, чтобы уменьшить смещение данных.Мы строго контролировали случайное распределение случаев, обеспечивая взаимную независимость между персоналом, участвующим в сборе клинических данных, и теми, кто участвует в групповом распределении. Кроме того, мы уменьшили потенциальную систематическую ошибку, вызванную различиями в естественной продолжительности заболевания бронхиолитом, ограничив продолжительность заболевания при включении в исследование до 48 часов. Кроме того, выбор младенцев моложе 1 года в качестве возраста включения обеспечил, чтобы всем пациентам было приблизительно 8 месяцев на момент включения в исследование.Мы также снизили субъективность при наблюдении за клиническими симптомами, попросив родителей и врачей пациента предоставить независимые баллы по двум основным симптомам, кашлю и хрипу, которые оценивались с использованием международно признанной визуальной аналоговой шкалы и шкалы Лоуэлла соответственно. Вторичные симптомы оценивались по количеству последовательных дней появления. Наконец, были введены строгие ограничения на лечебные мероприятия.
Вторичные симптомы оценивались по количеству последовательных дней появления. Наконец, были введены строгие ограничения на лечебные мероприятия.
Основываясь на вышеупомянутых стратегиях, наши результаты показывают, что с точки зрения исходных данных при включении в это исследование использовалось рандомизированное проспективное включение, которое исключало пациентов с тяжелым бронхиолитом и сопутствующими заболеваниями на основе заранее установленных критериев исключения.
Следует отметить, что результаты при зачислении указывают на значительные различия в трехвогнутом знаке. В частности, в контрольной группе была наименьшая частота трех вогнутых признаков. Эти различия, однако, не влияют на интерпретацию наших результатов.
Баллы, предоставленные исследователями и родителями пациентов для основного симптома, кашля, показали в целом согласованные результаты. Оба результата показывают, что распыление IFN в высоком уровне, введенное в течение 2 дней после появления симптомов, могло более значительно облегчить кашель по сравнению с контрольным лечением. Более того, межгрупповые сравнения показали, что на 3-й и 5-й дни лечения уменьшение кашля было одинаковым в группах, получавших внутримышечную инъекцию и небулайзерную терапию.
Более того, межгрупповые сравнения показали, что на 3-й и 5-й дни лечения уменьшение кашля было одинаковым в группах, получавших внутримышечную инъекцию и небулайзерную терапию.
Что касается основного симптома, свистящего дыхания, баллы Лоуэлла показывают, что не было значительных различий в различиях баллов между 1 и 3 днями. На 5 день лечения эффективность распыления с низким содержанием ИФН была выше, чем у контрольного лечения. , но не было значительных различий между обработанными группами в отношении способа доставки.
Результаты нашего проспективного когортного исследования показали, что по сравнению с контрольной группой введение IFN-α1b могло эффективно облегчить хрипы и кашель при бронхиолите. Что касается способа доставки лекарственного средства, распыление высоких доз IFN-α1b показало значительные преимущества в сокращении продолжительности свистящего дыхания и облегчении кашля, а также во избежание дискомфорта и неудобств пациентов и их родителей, вызванных внутримышечными инъекциями. Во время исследования мы не столкнулись с какими-либо проблемами безопасности пациентов, связанными с использованием распыления IFN-α1b.
Во время исследования мы не столкнулись с какими-либо проблемами безопасности пациентов, связанными с использованием распыления IFN-α1b.
В этом исследовании есть несколько ограничений. Сначала пациенты были госпитализированы на 7 дней. В Китае принято следить за тем, чтобы симптомы не повторялись. В этом исследовании после 5-го дня не наблюдалось дальнейшего видимого улучшения показателей. Во-вторых, исследование было многоцентровым, включая многочисленные больницы, расположенные в развивающихся регионах. Критерии приема на работу не могли строго соблюдаться из-за недостатка опыта у некоторых клинических врачей, который будет улучшен за счет повышения квалификации в будущих исследованиях.В-третьих, тест на вирус не был проанализирован в этом исследовании, так как данные были недоступны в некоторых центрах. Для лечения бронхиолита очень важно знать вирусную этиологию. Между тем, данные о необходимости поддерживающей терапии в этом исследовании отсутствовали. Важно оценить эффективность IFN-α1b. Эти данные будут собраны в будущих исследованиях.
Эти данные будут собраны в будущих исследованиях.
В будущем мы будем стремиться наблюдать за иммунологическими изменениями у пациентов и следить за рецидивами хрипов. Это обеспечит более полную клиническую основу для лечения бронхиолита с помощью распыления IFN-α1b у педиатрических пациентов.
Благодарности
Мы благодарим детей, принявших участие в исследовании, и их родителей.
Авторы заявляют об отсутствии конфликта интересов.
Роль спонсоров: спонсоры не играли никакой роли в дизайне исследования, сборе и анализе или интерпретации данных, а также в подготовке рукописи.
Ссылки
- 1.
Kyu HH, Pinho C, Wagner JA, Brown JC, Bertozzi-Villa A, Charlson FJ и др.Глобальное и национальное бремя болезней и травм среди детей и подростков в период с 1990 по 2013 год: результаты исследования глобального бремени болезней 2013 года. JAMA Pediatr. 2016; 170: 267–87. pmid: 26810619 - 2.
Наир Х. , Нокес Д.Д., Гесснер Б.Д., Дхерани М., Мадхи С.А., Синглтон Р.Дж. и др. Глобальное бремя острых инфекций нижних дыхательных путей, вызванных респираторно-синцитиальным вирусом у детей раннего возраста: систематический обзор и метаанализ. Ланцет. 2010; 375: 1545–55. pmid: 20399493
, Нокес Д.Д., Гесснер Б.Д., Дхерани М., Мадхи С.А., Синглтон Р.Дж. и др. Глобальное бремя острых инфекций нижних дыхательных путей, вызванных респираторно-синцитиальным вирусом у детей раннего возраста: систематический обзор и метаанализ. Ланцет. 2010; 375: 1545–55. pmid: 20399493 - 3.Meissner HC. Вирусный бронхиолит у детей. N Engl J Med 2016; 374: 62–72. pmid: 26735994
- 4.
Редакционная коллегия, Китайский журнал педиатрии, Специализированная группа респираторных заболеваний, Общество педиатров, Китайская медицинская ассоциация. Документ о консенсусе экспертов по диагностике и лечению бронхиолита (2014 г.). Чжунхуа Эр Кэ За Чжи. 2015; 53: 168–71. pmid: 26165011 - 5.
Миллер Е.К., Гебрецадик Т., Кэрролл К.Н., Дюпон В.Д., Мохамед Ю.А., Морин Л.Л. и др.Вирусная этиология детского бронхиолита, крупа и заболеваний верхних дыхательных путей в течение 4 лет подряд. Pediatr Infect Dis J. 2013; 32: 950–55. pmid: 23694832 - 6.
Флорин Т. А., Plint AC, Zorc JJ. Вирусный бронхиолит. Ланцет. 2017; 389: 211–24. pmid: 27549684
А., Plint AC, Zorc JJ. Вирусный бронхиолит. Ланцет. 2017; 389: 211–24. pmid: 27549684 - 7.
Роннблом Л. Важность системы интерферона типа I в аутоиммунных заболеваниях. Clin Exp Rheumatol. 2016; 34: 21–24. pmid: 27586799 - 8.
Шен К., Чжан Г, Шан И, Сюй Б, Фу З, Цао Л. и др.Консенсус специалистов по педиатрическому клиническому применению рекомбинантного человеческого интерферона α1b. Китайский журнал прикладной клинической педиатрии. 2015; 30: 1214–19. - 9.
де Верд Н.А., Нгуен Т. Интерфероны и их рецепторы — распределение и регуляция. Immunol Cell Biol. 2012; 90: 483–91. pmid: 22410872 - 10.
Ли И, Чжан Г., Сюй Д. Лечение респираторно-синцитиального вируса распылением IFN α-1b. Медицинский журнал национальных сил обороны в Северо-Западном Китае.2010; 31: 203–5. - 11.
Шан И, Хуанг И, Лю Э, Чен Кью, Цао Л, Лу Минь и др. Многоцентровое клиническое исследование по лечению острого бронхиолита у детей распыленным рекомбинантным человеческим интерфероном α-1b. Китайский журнал практической педиатрии. 2014; 29: 840–44
Китайский журнал практической педиатрии. 2014; 29: 840–44 - 12.
Группа специалистов по респираторным заболеваниям, Общество педиатров, Китайская медицинская ассоциация, Редакционный совет, Китайский журнал педиатрии. Руководство по ведению внебольничной пневмонии у детей (пересмотренное издание 2013 г.) (Ⅰ).Чжунхуа Эр Кэ За Чжи. 2013,51 (10): 745–752. pmid: 24406226 - 13.
Редакционная коллегия, Китайский журнал педиатрии, Специализированная группа респираторных заболеваний, Педиатрическое общество, Китайская медицинская ассоциация. Консенсус экспертов по диагностике, лечению и профилактике бронхиолита (издание 2014 г.). Чжунхуа Эр Кэ За Чжи. 2015,53 (3): 168–171. pmid: 26165011 - 14.
Лоуэлл Д.И., Листер Г., Фон Клосс Х, Маккарти П. Свистящее дыхание у младенцев: ответ на адреналин.Педиатрия 1987; 87: 939–45 - 15.
Лю Дж., Лю Дж., Чжу Л., Ван Д., Ю Дж., Лю Дж. Биораспределение и метаболический путь интерферона-α-1b, вводимого кроликами при вдыхании аэрозолей. Вестник медицины. 2013; 32: 1–5.
Вестник медицины. 2013; 32: 1–5.
Может ли повышение уровня интерферонов, основных борцов с вирусами в организме, победить COVID-19? | Наука
Валери Маккарти получила инъекцию плацебо или интерферона.
Стив Фиш
Автор: Мередит Вадман,
Science ’ s Отчетность о COVID-19 поддерживается Пулитцеровским центром.
* Обновление, 21 июля, 16:05: Университет Саутгемптона и компания Synairgen опубликовали первые результаты рандомизированного контролируемого исследования интерферона при инфекции SARS-CoV-2, о чем они объявили 20 июля.
В ходе исследования был обследован 101 пациент, госпитализированный с COVID-19. У тех, кто вдыхал экспериментальный интерферон первого типа, производимый Synairgen, на 79% меньше вероятность развития тяжелого заболевания и более чем в два раза выше вероятность полного выздоровления через 28 дней, чем у пациентов, получавших плацебо. Оба результата достигли статистической значимости. Акции компании взлетели более чем на 500% на этой новости.
У тех, кто вдыхал экспериментальный интерферон первого типа, производимый Synairgen, на 79% меньше вероятность развития тяжелого заболевания и более чем в два раза выше вероятность полного выздоровления через 28 дней, чем у пациентов, получавших плацебо. Оба результата достигли статистической значимости. Акции компании взлетели более чем на 500% на этой новости.
Связанные
Том Уилкинсон, врач-респиратор из Саутгемптонского университета и главный исследователь исследования, сказал, что результаты показывают, что интерферон-бета, интерферон первого типа, уже одобренный в инъекционной форме для лечения рассеянного склероза, «имеет огромный потенциал в качестве ингаляционного препарата. … Противодействие воздействию SARS-CoV-2.”
Другие наблюдатели предупредили, что небольшой размер исследования делает его результаты далеко не окончательными.
Уилкинсон сказал, что трое из 101 пациента отозвали свое согласие, а из остальных участников 48 получали активное лекарство и 50 получали плацебо.
Он добавил, что публичная компания была вынуждена по закону о ценных бумагах объявить результаты. «Мы усиленно работаем над публикацией», — добавил он.
Спонсоры теперь стремятся привлечь к участию в исследовании еще 300 негоспитализированных пациентов — пожилых пациентов и пациентов с заболеваниями, у которых симптомы заболевания не превышают 3 дней. Набрать это число может быть непросто, поскольку в Великобритании число новых случаев ежедневно снижается до нескольких сотен.
В нашей оригинальной статье, опубликованной 8 июля, изучались возможности интерферона как лекарственного средства для лечения COVID-19, особенно у недавно инфицированных людей, и упоминались исследования в Саутгемптоне.Прочтите здесь:
30 апреля результат теста Валери Маккарти подтвердил, что ее мучительная усталость и сильные головные боли были вызваны новым коронавирусом. Ее не госпитализировали, но уже на следующий день медсестра из Медицинского центра Стэнфордского университета сделала 52-летней марафонке укол, содержащий либо плацебо, либо естественный борец с вирусом: интерферон.
Маккарти был пациентом 16 в клиническом испытании, которое, как ожидается, поможет заполнить огромный пробел в лечении COVID-19: у врачей нет лекарств, которые, как было доказано на ранней стадии, предотвращают инфекцию или помогают победить вирус до этого. закрепляется.До сих пор было показано, что два научно подтвержденных метода лечения COVID-19 — ремдесивир и дексаметазон — работают только у госпитализированных пациентов с серьезными заболеваниями.
Но небольшое количество недавних статей предполагает, что новый коронавирус выполняет часть своей смертоносной работы, отключая интерфероны, мощные белки, которые являются передовыми защитниками организма от вирусного вторжения. Если это так, то синтетические интерфероны, назначенные до или вскоре после заражения, могут приручить вирус до того, как он вызовет серьезное заболевание — долгожданная возможность, которую подтверждают дополнительные недавние исследования.
Несколько интерферонов были одобрены несколько десятилетий назад Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США, их иммуностимулирующая способность была использована против болезней, включая рак и гепатит. Согласно препринту medRxiv, в ходе раннего нерандомизированного профилактического испытания в больнице в китайской провинции Хубэй ни один из 2415 медицинских работников, которые ежедневно принимали носовые капли с интерфероном, не заразился вирусом.
Согласно препринту medRxiv, в ходе раннего нерандомизированного профилактического испытания в больнице в китайской провинции Хубэй ни один из 2415 медицинских работников, которые ежедневно принимали носовые капли с интерфероном, не заразился вирусом.
Стэнфордское испытание — одно из десятков, которые сейчас испытывают интерфероны против COVID-19, в том числе у людей, которые не болеют, но, возможно, подверглись воздействию вируса (см. Таблицу внизу).Первые результаты контролируемого исследования в Саутгемптонском университете ожидаются к августу.
«Каждое исследование каждого вида показало, что если вы индуцируете интерфероны до появления вируса, вирус проигрывает», — говорит Андреас Вак, иммунолог из Института Фрэнсиса Крика. «Чем раньше вы сможете его дать, тем лучше, и лучшее, что вы можете сделать, — это дать его до того, как появится вирус».
Время имеет решающее значение, — добавляет Мириам Мерад, иммунолог из Медицинской школы Икана на горе Синай.«Будет важно знать, когда давать эти лекарства». Она и другие говорят, что если их вводить слишком поздно в ходе инфекции, они могут подлить масла в огонь неконтролируемого воспаления, которое является признаком тяжелой формы COVID-19. «Интерфероны — сильные противовирусные препараты», — говорит Мерад. «Но они также активируют иммунные клетки и могут вызывать иммунопатологию».
Она и другие говорят, что если их вводить слишком поздно в ходе инфекции, они могут подлить масла в огонь неконтролируемого воспаления, которое является признаком тяжелой формы COVID-19. «Интерфероны — сильные противовирусные препараты», — говорит Мерад. «Но они также активируют иммунные клетки и могут вызывать иммунопатологию».
Интерфероны — это молекулярные мессенджеры, которые запускают немедленную интенсивную локальную реакцию, когда вирус вторгается в клетку. Они запускают производство множества белков, которые атакуют вирус на каждой стадии инвазии и репликации, и предупреждают неинфицированные соседние клетки, чтобы они подготовили свою собственную защиту.Интерфероны также помогают привлекать иммунные клетки к месту заражения и активировать их по прибытии.
Но SARS-CoV-2, вирус, вызывающий COVID-19, отключает эту защиту, блокируя мощные интерфероны, которые его вызывают, — говорит Бенджамин теновер, вирусолог из Mount Sinai. Он и его коллеги изучали инфекцию SARS-CoV-2 на различных моделях: клетки легких и бронхов человека, хорьки, ткань легких умерших пациентов с COVID-19 и кровь живых. Практически в каждой системе «интерферон плохо подавляется», — говорит тенОвер.По мере того как он отключает интерфероны, его команда сообщила в мае в Cell , вирус также увеличивает выработку хемокинов, другого набора молекул-мессенджеров, которые вызывают отдаленные иммунные клетки и вызывают воспаление.
Практически в каждой системе «интерферон плохо подавляется», — говорит тенОвер.По мере того как он отключает интерфероны, его команда сообщила в мае в Cell , вирус также увеличивает выработку хемокинов, другого набора молекул-мессенджеров, которые вызывают отдаленные иммунные клетки и вызывают воспаление.
Выводы из статьи, принятой в Science , от группы под руководством иммунолога Бенджамина Терьера из больницы Кочин в Париже, перекликаются с выводами TenOever. Команда Терьера также изучила кровь 50 пациентов с COVID-19, обнаружив поразительно пониженную активность интерферона и повышенные хемокины у тех, чье заболевание стало тяжелым и критическим, но не у тех, кто в конечном итоге заболел легкой или средней степенью.Terrier утверждает, что местная репликация вируса, не сдерживаемая интерферонами, вызывает воспаление, повреждающее ткани, как и армии иммунных клеток, призванные издалека. В результате возникает неконтролируемая воспалительная реакция, уносящая жизни многих людей.
Но не все убеждены в том, что вирус сам ответственен за бездействие интерферонов. Является ли низкий уровень интерферонов причиной или следствием тяжелого заболевания? — спрашивает Жан-Лоран Казанова, генетик-инфекционист из Университета Рокфеллера.С 2015 года он обнаружил три унаследованные мутации, которые существенно подавляют реакцию на интерферон, что повышает вероятность того, что генетическая предрасположенность играет роль в некоторых случаях тяжелой формы COVID-19.
Некоторые данные ставят под сомнение представление о том, что интерфероны вообще подавляются. В одном отчете, опубликованном в журнале Cell Host & Microbe Цзянвэем Вангом из Пекинского медицинского колледжа и его коллегами в прошлом месяце, обнаружена сильная экспрессия многочисленных интерферон-стимулированных генов (ISG), часто используемых в качестве маркера активности интерферона, в легочной жидкости. восьми пациентов с COVID-19.Точно так же в неопубликованных данных Джон Цанг, системный иммунолог из Национального института аллергии и инфекционных заболеваний США, обнаружил устойчивую экспрессию ISG в иммунных клетках в крови 35 тяжело больных COVID-19.
Тем не менее, по крайней мере, пять исследований с апреля показали, что обработка или предварительная обработка интерфероном оказывает защитное действие на клетки и на мышей, инфицированных SARS-CoV-2. Эти исследования параллельны более ранним, в которых были обнаружены положительные эффекты раннего введения интерферона у мышей, инфицированных кузенами нового коронавируса, тяжелым острым респираторным синдромом (SARS) и ближневосточным респираторным синдромом.Эти данные подтверждают, что использование интерферонов в качестве лечения COVID-19, особенно на ранних стадиях заражения, говорит защитники.
Но остается еще много предостережений. Во-первых, при применении в виде лекарств мощные интерфероны I типа могут иметь ужасные побочные эффекты, о чем знают пациенты, которые месяцами принимали их от рака и других болезней. Побочные эффекты включают гриппоподобные симптомы, головную боль, рвоту и депрессию. Но лечение COVID-19 не требует непрерывного приема в течение нескольких месяцев, и одно исследование с хроническим гепатитом показало, что синтетический интерферон III типа имеет меньше побочных эффектов, чем интерферон I типа. (Интерфероны типа I имеют рецепторы на каждой клетке тела, а у интерферонов типа III их нет.)
(Интерфероны типа I имеют рецепторы на каждой клетке тела, а у интерферонов типа III их нет.)
Испытание Маккарти относилось к интерферону III типа. Ее предупредили о «головных болях и усталости», но не отговорили. «Я подумала:« Я уже устала… ничего страшного », — говорит она.
Две статьи, опубликованные в журнале Science в прошлом месяце, предполагают, что интерфероны III типа могут быть вредными, если их вводить на поздних стадиях инфицирования. В одной статье группа Вака сообщила, что у мышей встречающийся в природе интерферон III типа нарушает восстановление легких, критически важное для выздоровления от гриппа; в другом — группа под руководством иммунолога Ивана Занони из Бостонской детской больницы сообщила об аналогичных результатах на мышах, а также обнаружила интерфероны III типа в легочной жидкости тяжелобольных пациентов с COVID-19.«Главный посыл для медиков, — говорит Занони, — таков:« Если вы хотите назначать интерфероны III типа в качестве противовирусных препаратов, давайте им как можно раньше ».
Элеонора Фиш, иммунолог из Университета Торонто, которая вместе с коллегами запускает два превентивных испытания интерферона, говорит, что данные уже указывают на безопасность интерферонов. Она и ее коллеги опубликовали результаты неконтролируемого исследования 77 госпитализированных пациентов в Ухане, Китай, в журнале Frontiers in Immunology. Они сообщили, что пациенты, получавшие интерферон I типа (с противовирусными препаратами или без них), имели более низкие уровни ключевого биомаркера воспаления, чем другие пациенты, а также избавились от вируса на 7 дней раньше.Подобные многообещающие результаты были получены в результате неконтролируемых исследований, которые Фиш опубликовал несколько лет назад, в которых изучались эффекты лекарств у пациентов, госпитализированных с SARS и Эболой. «Это представление о том, что [интерфероны] вредны позже, я просто хочу выбросить это в окно», — говорит Фиш.
Даже когда ученые спорят о биологии, лежащей в основе, они прекрасно понимают, что только контролируемые клинические испытания дадут ответы на их вопросы. Что касается Маккарти, то через 8 недель после первого отрицательного теста на вирус она изо всех сил пытается медленно пробежать 3 километра.Она до сих пор не знает, получали ли она плацебо или интерферон. Как и всем остальным, ей придется дождаться результатов испытания.
Что касается Маккарти, то через 8 недель после первого отрицательного теста на вирус она изо всех сил пытается медленно пробежать 3 километра.Она до сих пор не знает, получали ли она плацебо или интерферон. Как и всем остальным, ей придется дождаться результатов испытания.
Проверка силы интерферона
Десятки клинических испытаний используют интерфероны, собственные средства защиты организма от вирусов против COVID-19. Вот подборка испытаний синтетических интерферонов на ранних стадиях инфицирования или на неинфицированных людях.
| Местоположение | Тип интерферона | Метод | Сроки | Дата начала исследования | Предназначен для включения в исследование | |||
|---|---|---|---|---|---|---|---|---|
| Госпиталь Шиян Тайхэ, Китай | Неинфицированные медицинские препараты типа I | 21 января | 2944 (комплектные) | |||||
9 U. K. сайты, включая университетскую больницу Саутгемптона K. сайты, включая университетскую больницу Саутгемптона | Тип I | Вдыхал | В течение 1 дня после + теста | 30 марта | 400 | |||
| Больница Логман Хаким, Тегеран, Иран | Тип I | Инъекция В течение 10 дней появления симптомов | 15 апреля | 40 | ||||
| Hamilton Health Sciences | Тип I | Инъекция | В течение 3 дней после поступления в больницу или клиническое ухудшение | 21 апреля | 4000 | |||
| Тип III | Инъекция | В течение 3 дней после + теста | 25 апреля | 120 | ||||
| Больница Джона Хопкинса | Тип III | Инъекция | Зараженные люди или в тот же день | 29 мая | 164 | |||
| Больница общего профиля Массачусетса | Впрыск | В течение 3 дней после + теста | 22 июня | 20 |
Клинические испытания. Gov
Gov
ИНТЕРФЕРОН ПЕРЕДАЕТСЯ ПРОТИВ НЕКОТОРЫХ ИНФЕКЦИЙ, В ТОМ ЧИСЛЕ ПРОДОЛЖИТЕЛЬНОСТИ
Доктор Мериган считает, что интерфероны окажутся наиболее полезными при лечении хронических вирусных инфекций и при долгосрочном применении против некоторых видов рака. Он считает, что в обоих случаях эти вещества, скорее всего, будут использоваться вместе с другими лекарствами. По его словам, на некоторые такие исследования, вероятно, уйдут годы, и только сейчас появляется достаточно материалов для выполнения этих работ.
Причина того, что интерферон был настолько дефицитным и дорогим в прошлые годы, заключалась в том, что его можно было получить только из обработанных клеток крови человека, побочного продукта донорства крови.С помощью методов сплайсинга генов стало возможным производить практически неограниченные запасы, изменяя генетику лабораторных бактерий так, чтобы они выращивали человеческие интерфероны.
По словам доктора Меригана, интерферон, производимый из клеток крови человека, стоит около 200 долларов за миллион единиц, что на самом деле является небольшой суммой. По этой цене доктор Тиррелл потратил бы 3000 долларов или больше на поставку интерферона каждому человеку в его тестах. Интерферон, продуцируемый бактериями, часто бесплатно предоставляется исследовательским группам компаниями, которые его производят, для проведения исследований и испытаний препарата.Но доктор Мериган сказал, что, по его мнению, коммерческая цена упала примерно до 20 долларов за миллион единиц и, вероятно, будет падать дальше.
По этой цене доктор Тиррелл потратил бы 3000 долларов или больше на поставку интерферона каждому человеку в его тестах. Интерферон, продуцируемый бактериями, часто бесплатно предоставляется исследовательским группам компаниями, которые его производят, для проведения исследований и испытаний препарата.Но доктор Мериган сказал, что, по его мнению, коммерческая цена упала примерно до 20 долларов за миллион единиц и, вероятно, будет падать дальше.
Недавние исследования показали, что у некоторых пациентов наблюдается дефицит интерферона, сказала доктор Лоис Эпштейн из Калифорнийского университета в Сан-Франциско, в то время как у других может быть его избыток. По ее словам, пока никто не знает значения перепроизводства или недопроизводства. Либо это может быть результатом болезни или части защиты организма от нее.Таким образом, неизвестно, будет ли разумно попытаться «исправить» дисбаланс.
Например, примерно у половины заболевших системной красной волчанкой, серьезным заболеванием, затрагивающим иммунную систему, в крови наблюдается чрезмерное количество интерферона, и анализы показывают, что это ненормальный интерферон. Пока неизвестно, является ли это причиной, следствием или чем-то совершенно не связанным с течением болезни.
Пока неизвестно, является ли это причиной, следствием или чем-то совершенно не связанным с течением болезни.
Когда ученые изучали интерфероны, стало ясно, что они являются сложной частью естественной внутренней защиты организма.Например, вирусные инфекции, кажется, побуждают клетки-мусорщики, называемые макрофагами, вырабатывать интерферон как часть процесса усиления защиты клеток. Тем не менее, в некоторых случаях кажется, что интерфероны усиливают, а в других случаях снижают эффективность других защитных клеток, называемых естественными клетками-киллерами.
В целом считается, что интерфероны действуют посредством своего воздействия на клетки, включая побуждение некоторых клеток производить другие вещества, которые в настоящее время изучаются. «То, что мы видим, — это семейство новых белков, которые активируются интерфероном», — сказал д-р.Ральф В.Ф. Харди, директор по наукам о жизни E. @ I. du Pont de Nemours & Company. Он сказал, что будет естественным шагом в будущем в исследованиях найти гены, несущие инструкции по созданию этих вторичных веществ, и клонировать эти гены для дальнейшего изучения. Но он отказался сообщить, поступают ли так ученые Du Pont.
Но он отказался сообщить, поступают ли так ученые Du Pont.
Альфа-интерферон
Как действует это лекарство?
Интерфероны (интерфероны) изменяют иммунную систему.Интерфероны — это природные белки, которые стимулируют иммунную систему организма при наличии заболевания. Доза интерферона добавляется к типу интерферона, который обычно вырабатывается организмом. Интерфероны могут быть полезны при лечении гепатита, некоторых форм рака и гемангиом.
Как дается лекарство?
Интерферон вводится в виде инъекции либо в вену (IV), либо под кожу (часто называемую «Sub-Q»), либо в мышцу (IM). Его можно сделать в больнице, клинике или дома.
Каковы побочные эффекты?
У детей обычно меньше побочных эффектов, чем у взрослых.
Ожидается
- гриппоподобные симптомы, такие как:
- лихорадка
- озноб
- ломота в теле
- головная боль
- усталость
Иногда
- тошнота, рвота
- понос
- вкусовых изменений
- потеря аппетита
- депрессия
- Выпадение волос
- сыпь
- спастическая диплегия (скованность в обеих ногах)
- понизить артериальное давление
Редкий
- учащение пульса
- нерегулярное сердцебиение
- боль в груди
- одышка
- путаница
- Онемение кистей и стоп
- низкие показатели крови
- низкий уровень кальция
- высокий уровень калия
- боль в спине
- изъятий
- психоз
Когда мне позвонить в клинику?
- лихорадка или озноб, не купируемые ацетаминофеном (таким как Тайленол®)
- продолжающаяся рвота или диарея
- кашель
- боль в груди
- одышка
- кровотечение
- необычный синяк
- нерегулярное сердцебиение
- Проблемы с использованием рук или ног
- путаница
- изъятий
- признаки аллергической реакции:
- внезапная сыпь или крапивница
- зуд
- хрипы
- проблемы с дыханием — звоните 911
Что еще мне нужно знать?
У детей с нарушениями свертываемости крови или количеством тромбоцитов менее 50 000 это лекарство не следует вводить суб-Q (непосредственно под кожу) или внутримышечно (в мышцу).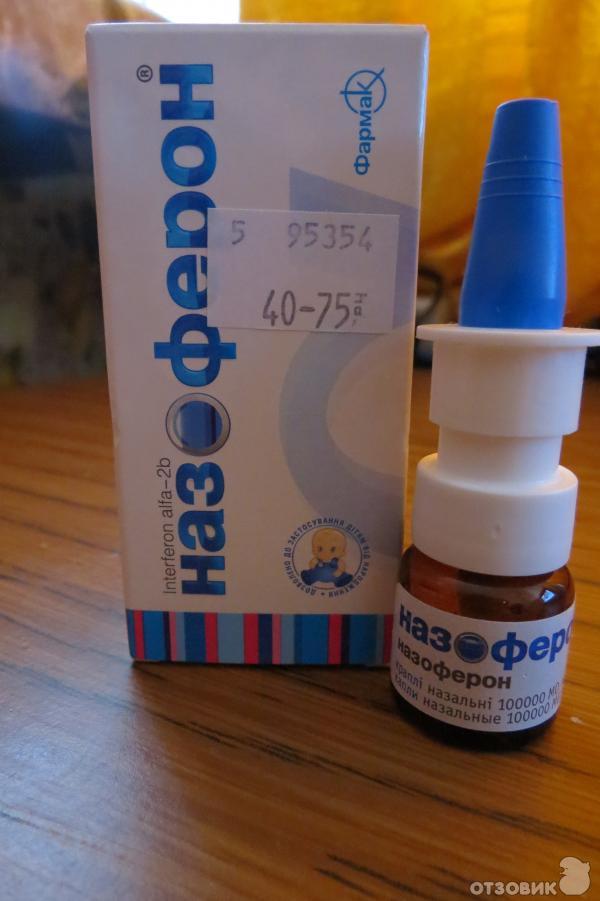
Интерферон нельзя давать детям или подросткам с историей депрессии или суицидального поведения.
Побочные эффекты можно уменьшить, если дать дозу на ночь.
Гриппоподобные симптомы обычно проходят после повторных доз. Ацетаминофен (например, Тайленол®) или ибупрофен (например, Адвил®) можно использовать для предотвращения или уменьшения температуры и головных болей.
Соблюдайте осторожность при вождении или работе с механизмами во время приема интерферона, поскольку могут произойти изменения психического статуса.
Вы и ваш ребенок должны знать названия всех лекарств, которые он принимает. Поделитесь этой информацией со всеми, кто заботится о вашем ребенке.
Не меняйте марки интерферона. Это может изменить дозу.
Проконсультируйтесь с врачом, практикующей медсестрой или фармацевтом, прежде чем давать любые других рецептурных или безрецептурных лекарств, трав или витаминов.
Всегда следите за тем, чтобы у вас под рукой было достаточно лекарств.Каждый раз, когда вы пополняете рецепт, проверяйте, сколько доз осталось. Если запасных частей не осталось, аптеке потребуется 2 или 3 дня, чтобы связаться с клиникой для обновления рецепта.
Проверьте этикетку на срок годности. Храните альфа-интерферон в холодильнике, в сухом или смешанном виде. После смешивания его можно хранить в холодильнике в течение 1 месяца, но только 24 часа при комнатной температуре.
Если вы приняли слишком много или неправильное лекарство, немедленно позвоните в гематологическую / онкологическую клинику.Если ваш ребенок без сознания или у него припадок, позвоните по телефону 911.
Вопросы?
Это не относится к вашему ребенку, но содержит общую информацию. Если у вас есть вопросы, звоните в гематологическую / онкологическую клинику или аптеку.
Последнее обновление 7/2016 © Copyright
Вернуться к началу
Использование интерферона-бета во время беременности не влияет на размер ребенка
Лечение женщин с рассеянным склерозом (РС) терапией интерфероном-бета во время беременности не влияет на гестационный возраст ребенка, вес при рождении, длину или размер головы, сообщают исследователи.
Исследование с этими выводами «Связь между воздействием интерферона-бета во время беременности и измерениями родов у потомства женщин с рассеянным склерозом» было недавно опубликовано в журнале PLoS ONE .
Лечение интерфероном-бета (IFN-бета) является основой одобренных методов лечения рассеянного склероза. Хотя текущие руководящие принципы рекомендуют прекращение курения во время беременности, мелкомасштабные исследования демонстрируют противоречивые данные о безопасности пренатального воздействия IFN-бета.
Теперь группа исследователей из Каролинского института в Швеции исследовала, рождались ли дети, рожденные женщинами с РС, пренатально подвергавшиеся воздействию IFN-бета меньше, чем те, которые не подвергались пренатальному воздействию какой-либо терапии, модифицирующей РС. .
Для этой цели исследователи использовали наборы данных из Швеции и Финляндии. В период с 2005 по 2014 год в Швеции было выявлено в общей сложности 411 беременностей, подвергшихся воздействию бета-интерферона, в то время как в финских отчетах было выявлено 232 беременности, соответствующие этим критериям.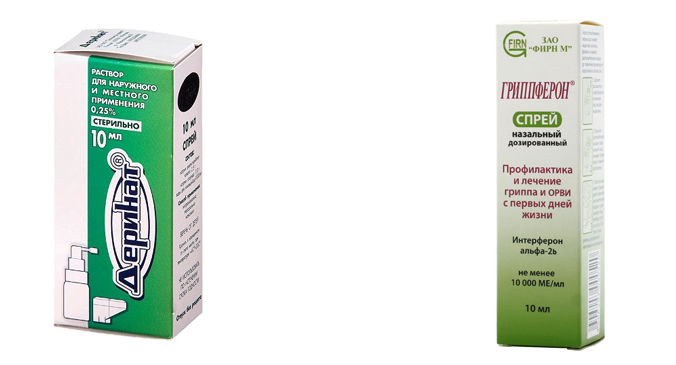
Данные сравнивались с беременностями, не подвергавшимися лечению, модифицирующим заболевание, которые включали 835 беременностей в Швеции и 331 в Финляндии. Окно воздействия IFN-бета рассматривалось от шести месяцев до последней менструации пациентки до конца беременности.
Результаты показали, что шведские младенцы, подвергшиеся воздействию IFN-бета, были в среднем на 28 граммов тяжелее, на 0,01 см длиннее и имели окружность головы на 0,14 см больше. Финские младенцы были на 50 граммов легче, на 0,02 см короче и имели 0.Окружность головы на 22 см меньше по сравнению с младенцами без облучения. Однако в целом эти различия не были статистически значимыми.
По мнению группы, такие различия в весе, длине тела или размере головы ребенка, вероятно, связаны с другими факторами и не связаны с воздействием IFN-бета.
Исследователи также отметили отсутствие различий в сроках беременности между группами, подвергавшимися воздействию, и группами, не подвергавшимися воздействию, и между братьями и сестрами, подвергавшимися воздействию IFN-бета, и братьями и сестрами, не подвергавшимися воздействию IFN-бета.
«Таким образом, данные этого крупного популяционного исследования указывают на отсутствие связи между воздействием IFN-бета и ростом плода или гестационным возрастом среди младенцев женщин с РС», — пишут исследователи.«Воздействие IFN-бета во время беременности не влияет на вес при рождении, длину тела или окружность головы».
Следует отметить, что в сентябре Европейское агентство по лекарственным средствам (EMA) объявило, что женщин с рецидивирующим РС можно лечить IFN-бета во время беременности и грудного вскармливания, а именно с помощью Biogen’s Plegridy (пегинтерферон бета-1a) и Avonex (интерферон бета-1a). и Ребиф (интерферон бета-1а) от Merck KGaA (известный как EMD Serono в Северной Америке).
Рекомендация Комитета EMA по лекарственным средствам для человека (CHMP) была основана на данных Европейского реестра беременных с интерфероном бета и национальных регистров здравоохранения Финляндии и Швеции, которые использовались в этом исследовании.
Обладая более чем трехлетним опытом работы в сфере медицинских коммуникаций, Катарина имеет степень бакалавра. в биомедицинских науках и степень магистра. в неврологии. Помимо написания статей, она участвовала в ориентированных на пациента переводческих и клинических исследованиях.
в биомедицинских науках и степень магистра. в неврологии. Помимо написания статей, она участвовала в ориентированных на пациента переводческих и клинических исследованиях.
Всего сообщений: 1,053
Патрисия имеет докторскую степень в области медицинской микробиологии и инфекционных заболеваний в Медицинском центре Лейденского университета в Лейдене, Нидерланды.Она изучала прикладную биологию в Universidade do Minho и была научным сотрудником постдокторантуры в Instituto de Medicina Molecular в Лиссабоне, Португалия. Ее работа была сосредоточена на молекулярно-генетических особенностях инфекционных агентов, таких как вирусы и паразиты.
Рассмотрение подходов, поддерживающая терапия, фармакологическая терапия
Буссе В.В., Герн Дж.Э., Дик Е.С. Роль респираторных вирусов при астме. Ciba Found Symp .1997. 206: 208-13; обсуждение 213-9. [Медлайн].
Белла Дж, Россманн МГ. Обзор: риновирусы и их рецепторы ICAM. Дж. Структ Биол . 1999, декабрь 1. 128 (1): 69-74. [Медлайн].
Greve JM, Davis G, Meyer AM, Forte CP, Yost SC, Marlor CW и др.Основным рецептором риновируса человека является ICAM-1. Ячейка . 1989 10 марта. 56 (5): 839-47. [Медлайн].
Сарая Т., Курай Д., Исии Х., Ито А., Сасаки Ю., Нива С. и др. Эпидемиология вирус-индуцированных обострений астмы: особое внимание уделяется роли риновируса человека. Передний микробиол . 2014. 5: 226. [Медлайн].
Ройстон Л., Таппарел С. Риновирусы и респираторные энтеровирусы: не так просто, как ABC. Вирусы .2016 11 января. 8 (1): [Medline].
Бочков Ю.А., Уоттерс К., Ашраф С., Григгс Т.Ф., Деврис М.К., Джексон Д.Д. и др. Связанный с кадгерином член семьи 3, продукт гена восприимчивости к детской астме, опосредует связывание и репликацию риновируса С. Proc Natl Acad Sci U S A . 2015 28 апреля. 112 (17): 5485-90. [Медлайн].
Bønnelykke K, Sleiman P, Nielsen K, Kreiner-Møller E, Mercader JM, Belgrave D, et al. Полногеномное ассоциативное исследование идентифицирует CDHR3 как локус восприимчивости к астме в раннем детстве с тяжелыми обострениями. Нат Генет . 2014 Январь 46 (1): 51-5. [Медлайн].
Лесслер Дж., Райх Н.Г., Брукмейер Р., Perl TM, Нельсон К.Э., Каммингс Д.А. Инкубационные периоды ОРВИ: систематический обзор. Ланцет Infect Dis . 2009 Май. 9 (5): 291-300. [Медлайн].
Melchjorsen J, Sørensen LN, Paludan SR. Экспрессия и функция хемокинов при вирусных инфекциях: от молекулярных механизмов до функции in vivo. Дж Лейкок Биол .2003 Сентябрь 74 (3): 331-43. [Медлайн].
Сообщение SD, Johnston SL. Защитная функция хозяина эпителия дыхательных путей при здоровье и болезни: клинические предпосылки. Дж Лейкок Биол . 2004 г., 75 (1): 5-17. [Медлайн].
Doyle WJ, Casselbrant ML, Li-Korotky HS, Doyle AP, Lo CY, Turner R, et al. Генотип интерлейкина 6 -174 C / C предсказывает более серьезную риновирусную болезнь. J Заразить Dis . 2010 15 января. 201 (2): 199-206. [Медлайн].[Полный текст].
Дженнингс Л.С., Андерсон Т.П., Верно А.М., Бейнон К.А., Мердок ДР. Вирусная этиология острых респираторных инфекций у детей, поступающих в стационар: роль полимеразной цепной реакции и демонстрация множественных инфекций. Pediatr Infect Dis J . 2004 23 ноября (11): 1003-7. [Медлайн].
Martin ET, Fairchok MP, Stednick ZJ, Kuypers J, Englund JA. Эпидемиология множественных респираторных вирусов у посетителей детских учреждений. J Заразить Dis . 2013 Март 207 (6): 982-9. [Медлайн].
Jin Y, Yuan XH, Xie ZP, Gao HC, Song JR, Zhang RF и др. Распространенность и клиническая характеристика недавно идентифицированного вида человеческого риновируса С у детей с острыми респираторными инфекциями. Дж. Клин Микробиол . 2009 Сентябрь 47 (9): 2895-900. [Медлайн]. [Полный текст].
Пелтола В., Джартти Т., Путто-Лаурила А., Мертсола Дж., Вайнионпяя Р., Варис М. и др. Риновирусные инфекции у детей: ретроспективное и проспективное исследование на базе больниц. J Med Virol . 2009 Октябрь 81 (10): 1831-8. [Медлайн].
Йошида Л.М., Сузуки М., Ямамото Т., Нгуен Х.А., Нгуен С.Д., Нгуен А.Т. и др. Вирусные патогены, ассоциированные с острыми респираторными инфекциями у детей из центральных районов Вьетнама. Pediatr Infect Dis J . 2010 29 января (1): 75-7. [Медлайн].
Мур Х.С., Джейкоби П., Тейлор А., Харнетт Дж., Боуман Дж., Райли ТВ и др. Взаимодействие респираторных вирусов и патогенных бактерий в верхних дыхательных путях бессимптомных детей аборигенов и неаборигенов. Pediatr Infect Dis J . 2010 июн.29 (6): 540-5. [Медлайн].
Moreira LP, Kamikawa J, Watanabe AS, Carraro E, Leal E, Arruda E, et al. Частота видов риновирусов человека у амбулаторных детей с острыми респираторными инфекциями на уровне первичной медико-санитарной помощи в Бразилии. Pediatr Infect Dis J . 2011 30 июля (7): 612-4. [Медлайн].
Мак Р.К., Цзе Л.Й., Лам В.Й., Вонг Г.В., Чан П.К., Леунг Т.Ф. Клинический спектр риновирусных инфекций человека у госпитализированных детей Гонконга. Pediatr Infect Dis J . 2011 Сентябрь 30 (9): 749-53. [Медлайн].
Wishaupt JO, Russcher A, Smeets LC, Versteegh FG, Hartwig NG. Клиническое влияние ОТ-ПЦР на острые респираторные инфекции у детей: контролируемое клиническое испытание. Педиатрия . 2011 ноябрь 128 (5): e1113-20. [Медлайн].
Miller EK, Bugna J, Libster R, Shepherd BE, Scalzo PM, Acosta PL и др. Риновирусы человека при тяжелых респираторных заболеваниях у младенцев с очень низкой массой тела при рождении. Педиатрия . 2012 Январь 129 (1): e60-7. [Медлайн]. [Полный текст].
Фрай AM, Лу X, Olsen SJ, Chittaganpitch M, Sawatwong P, Chantra S и др. Человеческие риновирусные инфекции в сельских районах Таиланда: эпидемиологические доказательства риновируса как патогена, так и стороннего наблюдателя PLoS One . 2011 29 марта. 6 (3): e17780. [Медлайн]. [Полный текст].
Мирон Д., Сруго И., Кра-Оз З., Кенесс Ю., Вольф Д., Амирав И. и др. Единственный возбудитель острого бронхиолита: играет ли роль другие организмы, кроме респираторно-синцитиального вируса ?. Pediatr Infect Dis J . 2010 29 января (1): e7-e10. [Медлайн].
O’Callaghan-Gordo C, Bassat Q, Morais L, Díez-Padrisa N, Machevo S, Nhampossa T. и др. Этиология и эпидемиология вирусной пневмонии среди госпитализированных детей в сельских районах Мозамбика: эндемичный по малярии район с высокой распространенностью вируса иммунодефицита человека. Pediatr Infect Dis J . 2011 30 января (1): 39-44. [Медлайн].
García-García ML, Calvo C, Pozo F, Villadangos PA, Pérez-Breña P, Casas I.Спектр респираторных вирусов у детей с внебольничной пневмонией. Pediatr Infect Dis J . 2012 31 августа (8): 808-13. [Медлайн].
Louie JK, Roy-Burman A, Guardia-Labar L, Boston EJ, Kiang D, Padilla T. и др. Риновирус, связанный с тяжелыми инфекциями нижних дыхательных путей у детей. Pediatr Infect Dis J . 2009 г., 28 (4): 337-9. [Медлайн].
van Piggelen RO, van Loon AM, Krediet TG, Verboon-Maciolek MA.Риновирус человека вызывает тяжелую инфекцию у недоношенных детей. Pediatr Infect Dis J . 2010 Апрель 29 (4): 364-5. [Медлайн].
Ван Леувен Дж.С., Гуссенс Л.К., Хендрикс Р.М., Ван Дер Пален Дж., Лустуш А., Тио Б.Дж. Равная вирулентность риновируса и респираторно-синцитиального вируса у младенцев, госпитализированных по поводу инфекции нижних дыхательных путей. Pediatr Infect Dis J . 2012 31 января (1): 84-6. [Медлайн].
Гарсия К., Сориано-Фальяс А., Лозано Дж., Леос Н., Гомес А.М., Рамило О. и др.Снижение врожденного иммунного ответа цитокинов коррелирует с тяжестью заболевания у детей с респираторно-синцитиальным вирусом и риновирусным бронхиолитом человека. Pediatr Infect Dis J . 2012 31 января (1): 86-9. [Медлайн].
Hung IF, Zhang AJ, To KK, Chan JF, Zhu SH, Zhang R и др. Неожиданно более высокая заболеваемость и смертность госпитализированных пожилых пациентов, связанных с риновирусом, по сравнению с инфекцией дыхательных путей вирусом гриппа. Int J Mol Sci .2017 26 января, 18 (2): [Medline].
Sperber SJ, Shah LP, Gilbert RD, Ritchey TW, Monto AS. Эхинацея пурпурная для профилактики экспериментальных риновирусных простуд. Клиническая инфекция . 2004 15 мая. 38 (10): 1367-71. [Медлайн].
Pappas DE, Hendley JO, Hayden FG, Winther B. Профиль симптомов простудных заболеваний у детей школьного возраста. Pediatr Infect Dis J . 2008 27 января (1): 8-11. [Медлайн].
Винтер Б., МакКью К., Эш К., Рубино-младший, Хендли Дж.Загрязнение окружающей среды риновирусом и передача на пальцы здоровых людей в результате повседневной жизнедеятельности. J Med Virol . 2007 Октябрь 79 (10): 1606-10. [Медлайн].
Linsuwanon P, Payungporn S, Samransamruajkit R, Theamboonlers A, Poovorawan Y. Рецидивирующие человеческие риновирусные инфекции у младенцев с рефрактерным хрипом. Emerg Infect Dis . 2009 июн.15 (6): 978-80. [Медлайн]. [Полный текст].
Miller EK, Lu X, Erdman DD, Poehling KA, Zhu Y, Griffin MR, et al.Госпитализации детей раннего возраста, связанные с риновирусом. J Заразить Dis . 2007 15 марта. 195 (6): 773-81. [Медлайн].
Джексон Д.И., Гангнон Р.Э., Эванс М.Д., Роберг К.А., Андерсон Е.Л., Паппас Т.Э. и др. Свистящие риновирусные заболевания в раннем возрасте предсказывают развитие астмы у детей из группы высокого риска. Am J Respir Crit Care Med . 2008 г., 1. 178 (7): 667-72. [Медлайн]. [Полный текст].
Луи К., Трой Н.М., Гарратт Л.В., Иосифидис Т., Боско А., Бакли А.Г. и др.Влияние риновирусной инфекции человека на разборку белков плотного соединения эпителия дыхательных путей и трансэпителиальную проницаемость. Exp Lung Res . 2016 11. 1-16 октября. [Медлайн].
Shariff S, Shelfoon C, Holden NS, Traves SL, Wiehler S, Kooi C и др. Инфекция эпителиальных клеток риновирусом человека модулирует миграцию гладких мышц дыхательных путей. Am J Respir Cell Mol Biol . 2017 июн 56 (6): 796-803. [Медлайн].
Glanville N, Peel TJ, Schröder A, Aniscenko J, Walton RP, Finotto S и др.Дефицит Tbet вызывает зависимую от Т-хелперов эозинофилию дыхательных путей и гиперсекрецию слизи в ответ на риновирусную инфекцию. Патоген PLoS . 2016 Сентябрь 12 (9): e1005913. [Медлайн].
Arden KE, Faux CE, O’Neill NT, McErlean P, Nitsche A, Lambert SB и др. Молекулярная характеристика и отличительные особенности нового риновируса человека (ВСР) С, HRVC-QCE, обнаруженного у детей с лихорадкой, кашлем и хрипом в течение 2003 г. J Clin Virol . 2010 Март.47 (3): 219-23. [Медлайн].
Iwane MK, Prill MM, Lu X, Miller EK, Edwards KM, Hall CB и др. Виды человеческого риновируса, связанные с госпитализацией детей раннего возраста в США по поводу острых респираторных заболеваний. J Заразить Dis . 2011 декабрь 1. 204 (11): 1702-10. [Медлайн].
Calvo C, García-García ML, Blanco C, Pozo F, Flecha IC, Pérez-Breña P. Роль риновируса у госпитализированных младенцев с инфекциями дыхательных путей в Испании. Pediatr Infect Dis J .2007 октября, 26 (10): 904-8. [Медлайн].
Джексон DJ. Роль риновирусных инфекций в развитии астмы у детей раннего возраста. Curr Opin Allergy Clin Immunol . 2010 Апрель 10 (2): 133-8. [Медлайн]. [Полный текст].
Wilkinson TM, Hurst JR, Perera WR, et al. Эффект взаимодействия между бактериальной и риновирусной инфекцией нижних дыхательных путей при обострениях ХОБЛ. Сундук . Февраль 2006. 129 (2): 317-24.
Джексон Д.И., Гангнон Р.Э., Эванс М.Д., Роберг К.А., Андерсон Е.Л., Паппас Т.Э. и др.Свистящие риновирусные заболевания в раннем возрасте предсказывают развитие астмы у детей из группы высокого риска. Am J Respir Crit Care Med . 2008 г., 1. 178 (7): 667-72. [Медлайн]. [Полный текст].
Gern JE. Риновирус и начало астмы. Curr Opin Allergy Clin Immunol . 2009 Февраль 9 (1): 73-8. [Медлайн]. [Полный текст].
Martinez FD. Истоки астмы и хронической обструктивной болезни легких в раннем возрасте. Proc Am Thorac Soc .2009 1 мая. 6 (3): 272-7. [Медлайн]. [Полный текст].
Calvo C, Casas I, García-García ML, Pozo F, Reyes N, Cruz N, et al. Роль респираторных инфекций риновируса С у больных и здоровых детей в Испании. Pediatr Infect Dis J . 2010 29 августа (8): 717-20. [Медлайн].
Rosenthal LA, Avila PC, Heymann PW, Martin RJ, Miller EK, Papadopoulos NG, et al. Вирусные инфекции дыхательных путей и астма: курс впереди. J Allergy Clin Immunol .2010 июн. 125 (6): 1212-7. [Медлайн]. [Полный текст].
Оленек Дж. П., Ким В. К., Ли В. М., Ван Ф., Паппас Т. Э., Салазар Л. Е. и др. Еженедельное наблюдение за детьми, больными астмой, на предмет инфекций и болезней в период простуд. J Allergy Clin Immunol . 2010 май. 125 (5): 1001-1006.e1. [Медлайн]. [Полный текст].
Busse WW, Lemanske RF Jr, Gern JE. Роль вирусных респираторных инфекций в обострениях астмы и астмы. Ланцет .2010 сентябрь 4. 376 (9743): 826-34. [Медлайн]. [Полный текст].
Миллер Э.К. Новые виды риновирусов человека и их значение в обострении астмы и ремоделировании дыхательных путей. Immunol Allergy Clin North Am . 30 ноября 2010 г. (4): 541-52, vii. [Медлайн]. [Полный текст].
Джонстон С.Л., Паттемор П.К., Сандерсон Г., Смит С., Лампе Ф., Джозефс Л. и др. Общественное исследование роли вирусных инфекций в обострениях астмы у детей 9-11 лет. BMJ . 1995 г. 13 мая. 310 (6989): 1225-9. [Медлайн]. [Полный текст].
Gavala ML, Bertics PJ, Gern JE. Риновирусы, аллергическое воспаление и астма. Иммунол Рев. . 2011 Июль 242 (1): 69-90. [Медлайн]. [Полный текст].
Guilbert TW, Singh AM, Danov Z, Evans MD, Jackson DJ, Burton R и др. Снижение функции легких после дошкольных заболеваний, связанных с хрипами, риновирусами у детей с риском развития астмы. J Allergy Clin Immunol .2011 Сентябрь 128 (3): 532-8.e1-10. [Медлайн]. [Полный текст].
Джексон Д. Д., Леманске Р. Ф. младший. Роль респираторных вирусных инфекций в возникновении астмы у детей. Immunol Allergy Clin North Am . 2010, 30 ноября (4): 513-22, vi. [Медлайн]. [Полный текст].
Джартти Т., Корппи М. Риновирус-индуцированный бронхиолит и развитие астмы. Педиатр Аллергии Иммунол . 2011 июн. 22 (4): 350-5. [Медлайн].
Миллер Е.К., Уильямс СП, Гебретсадик Т., Кэрролл К.Н., Дюпон В.Д., Мохамед Я.А. и др.Хозяин и вирусные факторы, связанные с тяжестью заболевания дыхательных путей младенцев, связанного с риновирусом человека. J Allergy Clin Immunol . 2011 Апрель 127 (4): 883-91. [Медлайн]. [Полный текст].
Озкан С., Тойран М., Чивелек Э., Эркочоглу М., Алтас А.Б., Албайрак Н. и др. Оценка респираторных вирусных патогенов при обострениях астмы в детстве. Дж Астма . 2011 ноябрь 48 (9): 888-93. [Медлайн].
Smuts HE, Workman LJ, Zar HJ.Риновирусная инфекция у африканских детей раннего возраста с острым хрипом. BMC Infect Dis . 2011 15 марта, 11:65. [Медлайн]. [Полный текст].
Пелтола В., Хейккинен Т., Руусканен О, Джартти Т., Хови Т., Килпи Т. и др. Временная связь между циркуляцией риновирусов в обществе и инвазивным пневмококковым заболеванием у детей. Pediatr Infect Dis J . 2011 июн.30 (6): 456-61. [Медлайн].
Копонен П., Карьялайнен М.К., Корппи М.Полиморфизм IL10, риновирус-индуцированный бронхиолит и детская астма. J Allergy Clin Immunol . 2013 январь 131 (1): 249-50. [Медлайн].
Maggini S, Beveridge S, Suter M. Комбинация высоких доз витамина C и цинка от простуды. J Int Med Res . 2012. 40 (1): 28-42. [Медлайн].
Ruuskanen O, Lahti E, Jennings LC, Murdoch DR. Вирусная пневмония. Ланцет . 2011 апр. 9. 377 (9773): 1264-75. [Медлайн].
Laham FR, Trott AA, Bennett BL, Kozinetz CA, Jewell AM, Garofalo RP, et al. Концентрация ЛДГ в промывной жидкости для носа как биохимический прогностический фактор тяжести бронхиолита. Педиатрия . 2010 февраль 125 (2): e225-33. [Медлайн]. [Полный текст].
Jain S, Self WH, Wunderink RG, Fakhran S, Balk R, Bramley AM и др. Внебольничная пневмония, требующая госпитализации среди взрослых в США. N Engl J Med . 2015 30 июля. 373 (5): 415-27.[Медлайн].
Рид А.Б., Андерсон Т.Л., Кули Л., Уильямсон Дж., Макгрегор А.Р. Вспышка инфекций, вызванных человеческим риновирусом типа C, в отделении интенсивной терапии новорожденных. Pediatr Infect Dis J . 2011 30 декабря (12): 1096-5. [Медлайн].
Лю Ю., Хилл М.Г., Клозе Т., Чен З., Уоттерс К., Бочков Ю.А. и др. Атомная структура риновируса С, вида вируса, связанного с тяжелой формой астмы у детей. Proc Natl Acad Sci U S A . 2016 9 августа.113 (32): 8997-9002. [Медлайн].
Андерсон П. Преходящий риск инсульта у детей после инфицирования. Медицинские новости Medscape. Доступно на http://www.medscape.com/viewarticle/830210. Доступ: 23 августа 2014 г.
Hills NK, Sidney S, Fullerton HJ. Время и количество незначительных инфекций как факторов риска развития артериального ишемического инсульта у детей. Неврология . 2014 20 августа [Medline].
Gambarino S, Costa C, Elia M, Sidoti F, Mantovani S, Gruosso V, et al.Разработка ОТ-ПЦР в реальном времени для обнаружения и количественной оценки риновирусов человека. Мол Биотехнология . 2009 Июль 42 (3): 350-7. [Медлайн].
Rogers BB, Shankar P, Jerris RC, Kotzbauer D, Anderson EJ, Watson JR, et al. Влияние экспресс-теста респираторной панели на результаты лечения пациентов. Арч Патол Лаборатория Мед . 2015 май. 139 (5): 636-41. [Медлайн].
Chen EC, Miller SA, DeRisi JL, Chiu CY. Использование панвирусного микроматрицы (Virochip) для скрининга клинических образцов на вирусные патогены. J Vis Exp . 2011 27 апреля. [Medline]. [Полный текст].
Бюхер С., Марди С., Ван В., Дуонг В., Вонг С., Нотатин М. и др. Использование подхода множественной ПЦР / ОТ-ПЦР для оценки вирусных причин гриппоподобных заболеваний в Камбодже в течение трех подряд засушливых сезонов. J Med Virol . 2010 Октябрь 82 (10): 1762-72. [Медлайн].
Do DH, Laus S, Leber A, Marcon MJ, Jordan JA, Martin JM, et al. Одноэтапный анализ ПЦР в реальном времени для быстрого обнаружения риновирусов. Дж Мол Диагн . 2010 января 12 (1): 102-8. [Медлайн]. [Полный текст].
Gambarino S, Costa C, Elia M, Sidoti F, Mantovani S, Gruosso V, et al. Разработка ОТ-ПЦР в реальном времени для обнаружения и количественной оценки риновирусов человека. Мол Биотехнология . 2009 Июль 42 (3): 350-7. [Медлайн].
Faux CE, Arden KE, Lambert SB, Nissen MD, Nolan TM, Chang AB и др. Полезность опубликованных праймеров для ПЦР в обнаружении риновирусной инфекции человека. Emerg Infect Dis . 2011 17 февраля (2): 296-8. [Медлайн]. [Полный текст].
Сингх М. Горячий увлажненный воздух от простуды. Кокрановская база данных Syst Rev . 2004. CD001728. [Медлайн].
Кому KKW, Yip CCY, Yuen KY. Риновирус — от скамейки к постели. J Formos Med Assoc . 2017 июл.116 (7): 496-504. [Медлайн].
Shehab N, Schaefer MK, Kegler SR, Budnitz DS. Побочные эффекты от лекарств от кашля и простуды после вывода с рынка продуктов, предназначенных для младенцев. Педиатрия . 2010 декабрь 126 (6): 1100-7. [Медлайн].
Hayden FG, Herrington DT, Coats TL, Kim K, Cooper EC, Villano SA и др. Эффективность и безопасность перорального плеконарила для лечения простуды, вызванной пикорнавирусами, у взрослых: результаты 2 двойных слепых рандомизированных плацебо-контролируемых исследований. Клиническая инфекция . 15 июня 2003 г., 36 (12): 1523-32. [Медлайн].
Сингх М., Сингх М. Горячий и увлажненный воздух от простуды. Кокрановская база данных Syst Rev . 2013 г. 4 июня. CD001728. [Медлайн].
Paul IM, Beiler JS, King TS, Clapp ER, Vallati J, Berlin CM Jr. Втирка паром, вазелин и отсутствие лечения для детей с ночным кашлем и симптомами простуды. Педиатрия . 2010 декабрь 126 (6): 1092-9. [Медлайн].
Смертность младенцев, связанная с лекарствами от кашля и простуды — два штата, 2005 г. MMWR Morb Mortal Wkly Rep . 2007 12 января. 56 (1): 1-4.[Медлайн].
Calvo C, Garcia ML, Pozo F, Reyes N, Pérez-Breña P, Casas I. Роль риновируса C в явно опасных для жизни событиях у младенцев, Испания. Emerg Infect Dis . 2009 Сентябрь 15 (9): 1506-8. [Медлайн]. [Полный текст].
Де Саттер А.И., Сарасват А, ван Дриель МЛ. Антигистаминные препараты от насморка. Кокрановская база данных Syst Rev . 2015 29 ноября. CD009345. [Медлайн].
Science M, Johnstone J, Roth DE, Guyatt G, Loeb M.Цинк для лечения простуды: систематический обзор и метаанализ рандомизированных контролируемых исследований. CMAJ . 2012 г. 10 июля. 184 (10): E551-61. [Медлайн].
Eby GA. Терапевтическая эффективность ионного цинка при простуде. Клинические инфекционные болезни . 01 февраля 2008 г. 46 (3): 483-384.
Карузо Т.Дж., Пробер К.Г., Гвалтни Дж.М. мл. Лечение обычных простудных заболеваний с помощью цинка: структурированный обзор. Клиническая инфекция . 2007 сентября 1. 45 (5): 569-74. [Медлайн].
Сингх М., Дас РР. Цинк от простуды. Кокрановская база данных Syst Rev . 2011 16 февраля. CD001364. [Медлайн].
Сингх М., Дас РР. Цинк от насморка. Кокрановская база данных Syst Rev . 2013 18 июня. CD001364. [Медлайн].
Рональд Б. Тернер. 57. Простуда. Под редакцией Джона Э. Беннета, доктора медицины, Рафаэля Долина, доктора медицины и Мартина Дж.Blaser, MD. Принципы и практика инфекционных заболеваний Манделла, Дугласа и Беннета . 8-е издание. Филадельфия: Saunders, компания Elsevier Inc .; 2015. 748-752.
Saper RB, Rash R. Цинк: важнейший микроэлемент. Врач Фам . 2009 May 1. 79 (9): 768-72. [Медлайн].
Гвалтни Дж. М. младший, Винтер Б., Патри Дж. Т., Хендли Дж. Комбинированное противовирусно-антимедиаторное лечение простуды. J Заразить Dis .2002 15 июля. 186 (2): 147-54. [Медлайн].
Hayward G, Thompson MJ, Perera R, Del Mar CB, Glasziou PP, Heneghan CJ. Кортикостероиды при простуде. Кокрановская база данных Syst Rev . 2015 Октябрь 13, CD008116. [Медлайн].
Джартти Т., Лехтинен П., Ванто Т., Хартиала Дж., Вуоринен Т., Мякеля М.Дж. и др. Оценка эффективности преднизолона при раннем одышке, вызванной риновирусом или респираторно-синцитиальным вирусом. Pediatr Infect Dis J .2006 июн.25 (6): 482-8. [Медлайн].
Швитцер Г. Как средства массовой информации не раскрывают улики. BMJ . 2003. 326: 1403e4.
Turner RB, Wecker MT, Pohl G, Witek TJ, McNally E., St George R, et al. Эффективность тремакамры, растворимой молекулы межклеточной адгезии 1, для экспериментальной риновирусной инфекции: рандомизированное клиническое испытание. ЯМА . 1999, 19 мая. 281 (19): 1797-804. [Медлайн].
Акото С., Дэвис, Делавэр, Э.Дж.Тучные клетки допускают репликацию риновируса: потенциальные последствия для обострений астмы. Clin Exp Allergy . 2017 Март 47 (3): 351-360. [Медлайн].
Хан М., Хонг Дж. Й., Джайпалли С., Раджпут С., Лей Дж., Хинд Дж. Л. и др. IFN-γ блокирует развитие фенотипа астмы у новорожденных мышей, инфицированных риновирусом, путем ингибирования врожденных лимфоидных клеток 2 типа. Am J Respir Cell Mol Biol . 2017 Февраль 56 (2): 242-251. [Медлайн].
Hayden FG, Turner RB, Gwaltney JM, Chi-Burris K, Gersten M, Hsyu P, et al.Фаза II, рандомизированные, двойные слепые, плацебо-контролируемые исследования 2-процентной суспензии назального спрея рупринривира для профилактики и лечения экспериментально индуцированной риновирусной простуды у здоровых добровольцев. Противомикробные агенты Chemother . 2003 декабрь 47 (12): 3907-16. [Медлайн]. [Полный текст].
Gern JE, Mosser AG, Swenson CA, Rennie PJ, England RJ, Shaffer J, et al. Ингибирование репликации риновируса in vitro и in vivo с помощью физиологического раствора с кислотным буфером. J Заразить Dis .2007 15 апреля 195 (8): 1137-43. [Медлайн].
Schwartz AR, Togo Y, Hornick RB, Tominaga S, Gleckman RA. Оценка эффективности аскорбиновой кислоты в профилактике индуцированной инфекции риновируса 44 у человека. J Заразить Dis . 1973 Октябрь 128 (4): 500-5. [Медлайн].
Guedán A, Swieboda D, Charles M, Toussaint M, Johnston SL, Asfor A, et al. Исследование роли протеинкиназы D в репликации риновирусов человека. Дж. Вирол .2017 г. 1. 91 (9): [Medline].
Берман Р., Цзян Д., Ву Кью, Чу Х.В. α1-Антитрипсин снижает риск заражения риновирусом в первичных эпителиальных клетках дыхательных путей человека, подвергающихся воздействию сигаретного дыма. Int J Chron Obstruct Pulmon Dis . 2016. 11: 1279-86. [Медлайн].
Ли Дж. Дж., Шим А., Чон Дж. Ю., Ли Си, Ко Г. Дж., Чо Г. Дж. Разработка интраназальных нанотехнологий итраконазола и их иммунологической активности для терапии риновирусной инфекции. Коллоиды Surf B Биоинтерфейсы . 2016 г. 1. 143: 336-41. [Медлайн].
Shim A, Song JH, Kwon BE, Lee JJ, Ahn JH, Kim YJ и др. Лечебно-профилактическая активность итраконазола против риновирусной инфекции человека на мышиной модели. Научный руководитель . 2016 15 марта. 6: 23110. [Медлайн].
Stokes CA, Kaur R, Edwards MR, Mondhe M, Robinson D, Prestwich EC и др. Воспалительные реакции, индуцированные риновирусом человека, ингибируются липосомами, содержащими фосфатидилсерин. Иммунол слизистой оболочки . 2016 Сентябрь 9 (5): 1303-16. [Медлайн].
Cagno V, Civra A, Kumar R, Pradhan S, Donalisio M, Sinha BN и др. Экстракты коры фикуса религиозного L. подавляют инфицирование риновирусом человека и респираторно-синцитиальным вирусом in vitro. Дж. Этнофармакол . 2015 24 декабря. 176: 252-7. [Медлайн].
Hemilä H, Chalker E. Витамин C для профилактики и лечения простуды. Кокрановская база данных Syst Rev .2013 31 января. CD000980. [Медлайн].
Тернер РБ, Бауэр Р., Велькарт К., Халси ТК, Гангеми Дж. Д. Оценка Echinacea angustifolia при экспериментальных риновирусных инфекциях. N Engl J Med . 2005 28 июля. 353 (4): 341-8. [Медлайн].
Schoop R, Klein P, Suter A, Johnston SL. Эхинацея в профилактике индуцированных риновирусных простуд: метаанализ. Клин Тер . 2006 28 февраля (2): 174-83. [Медлайн].
Барретт Б., Браун Р., Ракель Д., Мундт М., Боун К., Барлоу С. и др.Эхинацея для лечения простуды: рандомизированное исследование. Энн Интерн Мед. . 2010 21 декабря. 153 (12): 769-77. [Медлайн]. [Полный текст].
Тернер РБ, Бидерманн К.А., Морган Дж. М., Кесвик Б., Эртель К. Д., Баркер М. Ф. Эффективность органических кислот в очищающих средствах для рук для предотвращения риновирусных инфекций. Противомикробные агенты Chemother . 2004 июл. 48 (7): 2595-8. [Медлайн]. [Полный текст].
Halperin SA, Eggleston PA, Beasley P, Suratt P, Hendley JO, Gröschel DH, et al.Обострения астмы у взрослых при экспериментальной риновирусной инфекции. Am Rev Respir Dis . 1985 ноябрь 132 (5): 976-80. [Медлайн].
Сингх М., Дас РР. Цинк от насморка. Кокрановская база данных Syst Rev . 2011 16 февраля. CD001364. [Медлайн].
Costa LF, Queiróz DA, da Silveira HL, Neto MB, de Paula NT, Oliveira TF и др. Риновирус человека и тяжесть заболевания у детей. Педиатрия . 2014 13 января.[Медлайн].
Де Саттер А.И., ван Дриэль М.Л., Кумар А.А., Лесслар О., Скрт А. Комбинации пероральных антигистаминных, противоотечных и анальгетиков при простуде. Кокрановская база данных Syst Rev . 2012 15 февраля. 2: CD004976. [Медлайн].
Fox S. Тяжелый детский риновирус, связанный с коинфекциями RSV. Доступно на http://www.medscape.com/viewarticle/819204. Доступ: 19 января 2014 г.

 Другие факторы ежедневно оценивались врачом отделения через определенные промежутки времени.
Другие факторы ежедневно оценивались врачом отделения через определенные промежутки времени. , Нокес Д.Д., Гесснер Б.Д., Дхерани М., Мадхи С.А., Синглтон Р.Дж. и др. Глобальное бремя острых инфекций нижних дыхательных путей, вызванных респираторно-синцитиальным вирусом у детей раннего возраста: систематический обзор и метаанализ. Ланцет. 2010; 375: 1545–55. pmid: 20399493
, Нокес Д.Д., Гесснер Б.Д., Дхерани М., Мадхи С.А., Синглтон Р.Дж. и др. Глобальное бремя острых инфекций нижних дыхательных путей, вызванных респираторно-синцитиальным вирусом у детей раннего возраста: систематический обзор и метаанализ. Ланцет. 2010; 375: 1545–55. pmid: 20399493 А., Plint AC, Zorc JJ. Вирусный бронхиолит. Ланцет. 2017; 389: 211–24. pmid: 27549684
А., Plint AC, Zorc JJ. Вирусный бронхиолит. Ланцет. 2017; 389: 211–24. pmid: 27549684 Китайский журнал практической педиатрии. 2014; 29: 840–44
Китайский журнал практической педиатрии. 2014; 29: 840–44 Вестник медицины. 2013; 32: 1–5.
Вестник медицины. 2013; 32: 1–5.