Противотуберкулезные препараты | GxP News
Активностью в отношении M.tuberculosis обладает значительное число препаратов, отличающихся по происхождению, химической структуре и механизму действия. В основу современных классификаций положена клиническая эффективность и переносимость противотуберкулезных препаратов (ПТП).
Наиболее распространенной является классификация, согласно которой все ПТП подразделяются на препараты:
I ряда (изониазид, рифампицин, пиразинамид, стрептомицин, этамбутол) и II ряда (этионамид, протионамид, циклосерин, капреомицин, канамицин, амикацин, рифабутин, ципрофлоксацин, офлоксацин, парааминосалициловая кислота (ПАСК).
В классификацию ПТП Международного союза борьбы с туберкулезом и болезнями легких (МСТБЛ) не включены капреомицин, амикацин, рифабутин и фторхинолоны, входящие в стандарты химиотерапии многих стран.
Классификация противотуберкулезных препаратов Международного союза борьбы с туберкулезом
- I группа (препараты высокой эффективности): Изониазид, Рифампицин
- II группа (препараты средней эффективности): Стрептомицин, Канамицин, Виомицин, Циклосерин, Этамбутол, Этионамид, Протионамид, Пиразинамид
- III группа (препараты низкой эффективности): ПАСК, тиоацетазон
Наиболее высокой активностью в отношении микобактерий туберкулеза обладают изониазид и рифампицин, поэтому стратегия современной химиотерапии пациентов с впервые выявленным туберкулезом строится на использовании сочетания именно этих препаратов. Комбинирование изониазида и рифампицина с другими ПТП I ряда (пиразинамид, стрептомицин и этамбутол) позволяет достичь излечения большинства пациентов. Наряду с комбинацией монокомпонентных средств применяются комбинированные ПТП, представляющие собой различные сочетания препаратов I ряда.
Комбинирование изониазида и рифампицина с другими ПТП I ряда (пиразинамид, стрептомицин и этамбутол) позволяет достичь излечения большинства пациентов. Наряду с комбинацией монокомпонентных средств применяются комбинированные ПТП, представляющие собой различные сочетания препаратов I ряда.
Препараты II ряда, или резервные, используются для лечения полирезистентного туберкулеза. Выбор препаратов и длительность их применения зависят от формы туберкулеза, клинического течения, характера предыдущего лечения, чувствительности M.tuberculosis и переносимости ПТП пациентами.
Комбинированные противотуберкулезные препараты
В настоящее время используется ряд комбинированных ПТП. Создание части из них обусловлено рекомендованными ВОЗ протоколами краткосрочной химиотерапии туберкулеза, включающей две фазы лечения: начальную и фазу продолжения. Комбинированные ПТП представляют различные сочетания препаратов I ряда: рифампицина, изониазида, пиразинамида, этамбутола. Использование комбинированных ПТП наиболее оправданно в период амбулаторного лечения и у пациентов, которые высказывают опасение или недоверие к приему большого числа таблеток.
При приеме комбинированных ПТП следует помнить об особенностях нежелательного действия каждого из компонентов и возможности суммирования нежелательных реакций.
Источник: Практическое руководство по антиинфекционной химиотерапии
Вернуться на главную страницу Глоссария
Противотуберкулезные препараты
Лечение туберкулеза остается на современном этапе важной задачей отечественной медицины, так как отмечается рост частоты кли-ническихформ туберкулеза. Тенденция кувеличениюзаболеваемости туберкулезом обусловлена рядом причин, как социально-экономического характера, так и появлением штаммов бактерий туберкулеза, устойчивых к традиционным ЛС. Терапия туберкулеза в настоящее время характеризуется комплексностью (одновременно назначается 2-4 медикамента) и длительностью (курс лечения от 3 мес. до 1 года и более). Противотуберкулезные препараты различают по степени активности туберкулостатического действия на два ряда
.
Наиболее высокой активностью в отношении микробактерий туберкулеза обладает изониазид и рифампицин, которые составляют основу современной стратегии химиотерапии туберкулеза.
Изониазид (МНН) — действует бактерицидно на микобактерии, выпускаются таб., р-р для инъекций. Сп. Б (Россия и др. страны).
Рифампицин (МНН) — полусинтетический АБ из группы рифам-пицинов, оказывает бактерицидное действие, высокоактивен в от
ношении микобактерий туберкулеза (применяется с начала 70-х гг.), поэтому относится к препаратам I ряда. Выпускаются капс., таб., порошокдля инъекций. Сп. Б (Россия, Германия, Индия), Бенемицин (Польша), Римактан (Швейцария) и др. В Государственном реестре ЛС Рифампицин зарегистрирован в 11 торговых названиях, в 3 лекарственных формах; предложения 7 стран.
Классификация противотуберкулезных препаратов по степени активности туберкулостатического действия
Классификация противотуберкулезных препаратов по степени активности туберкулостатического действия
Рифабутин (МНН) — входит в группу рифампицинов, внедрен в клиническую практику сравнительно недавно, поэтому относится к препаратам II ряда. Сп. Б. Микобутин — капс. (Италия), Р-Бутин (Индия).
Сп. Б. Микобутин — капс. (Италия), Р-Бутин (Индия).
Этамбутол (МНН) — относится к препаратам I ряда со средней эффективностью, оказывает бактериостатическое действие, характеризуется низкой токсичностью. Выпускаются таб., капс. Сп. Б (Россия, Польша, Индия), Комбутол (Индия), Сурал (Венгрия) и др. В Государственном реестре ЛС Этамбутол зарегистрирован в 9 торговых названиях, в 3 лекарственных формах; предложения 6 стран.
Согласно рекомендованным ВОЗ протоколам краткосрочной химиотерапии туберкулеза, больным назначаются комбинированные противотуберкулезные препараты, представляющие собой различные сочетания препаратов первого ряда с обязательным содержанием ри-фампицина и изониазида; есть комбинации еще с пиридоксином — витамином В6, необходимость в котором обусловлена изониазидом.
Рифакомб, Рифакомб плюс — таб., содержащие комбинации ри-фампицина, изониазида с добавлением пиридоксина или пиразина-мида. Выпускаются таб., покрытые оболочкой Сп. Б (Индия).
Противотуберкулезные препараты — презентация онлайн
1.
 Дисциплина «Фармакология» Лекция 16. Тема: Противотуберкулезные препараты
Дисциплина «Фармакология» Лекция 16. Тема: Противотуберкулезные препараты
Преподаватель: кмн Сизова В.В.
2. Туберкулёз
– это хроническая инфекционная
болезнь, вызванная Mycobacterium
tuberculosis, характеризующаяся
образованием гранулем в
пораженных органах, развитием
гиперчувствительности замедленного
типа и преимущественным
поражением легких.
До 1940-х гг. человечество не знало действительно эффективных противотуберкулезных
средств, и диагноз «туберкулез» обычно означал для больного приговор. В 1944 г. из
лучистого гриба был выделен стрептомицин. Спустя два года открыта
противотуберкулезная активность парааминосалициловой кислоты, а в 1952 г. –
производных гидразида изоникотиновой кислоты, в 1970-е гг. стали использоваться
рифампицин и этамбутол. Были разработаны эффективные схемы лечения
туберкулеза, что позволило сделать прогноз о скором искоренении этого заболевания
в нашей стране и на земном шаре.
3. Лечение туберкулеза
Ежегодно туберкулез уносит порядка 1,5 миллионов человеческих жизней, или 4000
жизней в день. По предварительным данным Центрального НИИ организации и
информатизации здравоохранения, на конец 2013 года в стране на учете
состояло 211,9 тыс. больных туберкулезом. Это меньше, чем в 2009 году, когда в
стране насчитывалось 262,7 больных. При этом стабильно высоким остается
количество пациентов с множественной лекарственной устойчивостью возбудителя
туберкулеза: 34 778 в 2013-м году против 34 838 в 2012-м.
Лечение туберкулеза
Лечение делится на патогенетическое это
противотуберкулезные препараты и
симптоматическое.
Арсенал противотуберкулезных средств
включает синтетические вещества и
антибиотики, которые различаются по
активности на микобактерии и
переносимости.
4. Классификация противотуберкулезных средств
Классификация современных противотуберкулезных средств и тактика их
применения построены на основе рекомендаций международного союза
борьбы с туберкулезом и заболеваниями легких (1997 г) и центральным НИИ
туберкулеза РАМН Противотуберкулезные средства – это группа
химиотерапевтических средств, подавляющих жизнедеятельность и рост
микобактерий-возбудителей туберкулеза.
Для лечения туберкулеза используют антибиотики и синтетические
противотуберкулезные средства, которые по активности делятся
на три группы:
Препараты 1-го ряда
Антибиотики
Синтетические
Рифампицин
Изониазид
Препараты 2-го ряда
Антибиотики Синтетические
Циклосерин Этионамид
Стрептомицин
Канамицин
Этамбутол
Пиразинамид
Протионамид
ПАСК
5. Лечение туберкулеза
Синтетические противотуберкулезные средства действуют только на микобактерии
туберкулеза. Антибиотики обладают широким спектром действия.
Учитывая то обстоятельство, что лечение туберкулеза длительное (12-18 месяцев)
микобактерии достаточно быстро приобретают устойчивость ко всем препаратам,
однако следует помнить, что к одним она возникает быстрее (стрептомицин), к
другим – относительно медленнее.
Для уменьшения скорости развития устойчивости обычно
комбинируют несколько препаратов.
На заре противотуберкулёзной химиотерапии была выработана
и предложена трёхкомпонентная схема терапии первой линии:
• стрептомицин
• изониазид
• пара-аминосалициловая кислота (ПАСК).
Эта схема стала классической. Она царствовала во фтизиатрии долгие
десятилетия и позволила спасти жизни огромному числу больных туберкулёзом, однако
на сегодняшний день исчерпала себя в виду высокой токсичности ПАСК и
невозможности длительного применения стрептомицина.
6. Стрептомицин (Streptomycini sulfas)
Стрептомицин — антибиотик широкого спектра действия, принадлежит к семейству
аминогликозидов, является бактерицидным в отношении широкого спектра
грамположительных и грамотрицательных бактерий.
Фармакологические свойства. Стрептомицин подавляет синтез
белка бактерий. МВТ быстро становятся устойчивыми к стрептомицину,
\ если препарат используется как монотерапия.
Однако когда стрептомицин назначается в комбинации с другими
противотуберкулезными препаратами (изониазид, рифампицин), то становится
бактерицидным и предотвращает появление резистентных МВТ. Стрептомицин в
основном активен в отношении популяций МВТ, содержащихся в полостях распада,
где рН низкий.
Стрептомицин не всасывается из кишечника, в связи с этим он вводится
внутримышечно. После введения препарат проникает в большинство тканей
организма. Концентрация его очень низка в нормальной ЦСЖ (цереброспинальной
жидкости), но при менингите — относительно выше.
Стрептомицин проникает через плаценту. Поскольку он почти полностью
выводится из организма через почки, дозировку препарата необходимо уменьшать
для больных со сниженной функцией почек и в старших возрастных группах.
7. Стрептомицин (Streptomycini sulfas)
Способ применения и дозы
Стрептомицин для внутримышечного
введения выпускается в виде
порошка, содержащегося во флаконах.
Для приготовления раствора во
флакон добавляют дистиллированную
воду. Раствор следует
приготавливать непосредственно
перед введением. Необходимо
контролировать, чтобы место ежедневной инъекции стрептомицина
менялось при каждом введении.
Ежедневные в/м введения в один и тот же
участок очень болезненны.
Поскольку инъекции стрептомицина
болезненны, детям его назначают
только при большой необходимости.
Дозировка стрептомицина.
Ежедневно для взрослых. В возрасте до 40 лет: масса тела до 50
кг — 0,75 г в одной дозе; свыше 50 кг— 1,0 г. С 40-60 лет: 0,75 г.
Старше 60 лет: 0,5 г. Для детей: 10 мг/кг, не превышая 0,75г.
Интермиттирующий режим.
Взрослые: масса тела до 50 кг — 0,75 г; масса тела свыше 50 кг
— 1,0 г. Дети — 15 мг/кг, но не более 0,75 г.
Rp.: Streptomycini sulfatis 0,5
D.t.d. N 10 in flac.
S. Содержимое флакона растворить в 2 мл 0,5% р-ра
новокаина. Вводить в/м по 1 фл. 2 раза в сутки 5 сут.
Основные побочные реакции:
Кожная гиперчувствительность и ототоксичность
(повреждение восьмого краниального нерва). Или
других побочных эффектов практическое значение имеют:
ангионевротический отек, эозинофилия, сывороточная
болезнь. Реже возникают гемолитическая анемия,
агранулоцитоз, тромбоцитопения.
Кожные реакции — сыпи и лихорадка обычно возникают
на 2-3 нед применения стрептомицина.
9. Противотуберкулезные средства первого ряда (высокоэффективные) Рифампицин (рифоцин) Rifampicinum
Механизм действия: угнетает синтез РНК
Cпектр действия – широкий. Оказывает выраженное действие на
микобактерии туберкулеза и ГР+микроорганизмы. В высоких
концентрациях активен в отношении и ГР- бактерий: кишечной палочки,
шигелл, сальмонелл, отдельных представителей синегнойной палочки и
протея
Характер действия: оказывает бактериостатическое и бактерицидное
действие. При приеме внутрь по активности приближается к изониазиду.
Хорошо всасывается из ж-к-т. Максимальная концентрация в крови
обнаруживается через 2-4 часа. Легко проникает через биологические
барьеры, в том числе, ГЭБ. Терапевтический эффект сохраняется 8-12
часов. Выделяется с желчью, частично с мочой, бронхиальными и слезными
железами.
10. Рифампицин (рифоцин) Rifampicinum
Показания к применению: Лечение всех форм туберкулеза.
К препарату довольно быстро развивается устойчивость микобактерий,
поэтому его целесообразно комбинировать с другими
противотуберкулезными препаратами. Назначают внутрь, а рифамицин – в/м
и в/в, местно.
Побочное действие: гепатотоксичность, головная боль, нарушение
координации движений, нарушение зрения; нарушение менструального
цикла; лейкопения.
Рифампицин выпускается в капсулах, таблетках, ампулах и в виде сиропа
отдельно, а также в составе комбинационных препаратов. Больных
необходимо предупреждать, что при приеме рифампицина моча, пот, слезы
могут приобрести розово-красный цвет.
Форма выпуска. Капсулы по 0,15 г, в упаковке 20 штук; для детей капсулы
по 0,05 г, в упаковке 30 ш тук, ампулы по 0,15 г № 10.
11. Синтетические препараты: Изониазид (тубазид) Isoniazidum
– производное ГИНК (гидразид изоникотиновой кислоты). Препарат эффективен в отношении
микобактерий туберкулеза и возбудителя проказы. На микобактерии может оказывать в
зависимости от концентрации бактериостатическое или бактерицидное действие.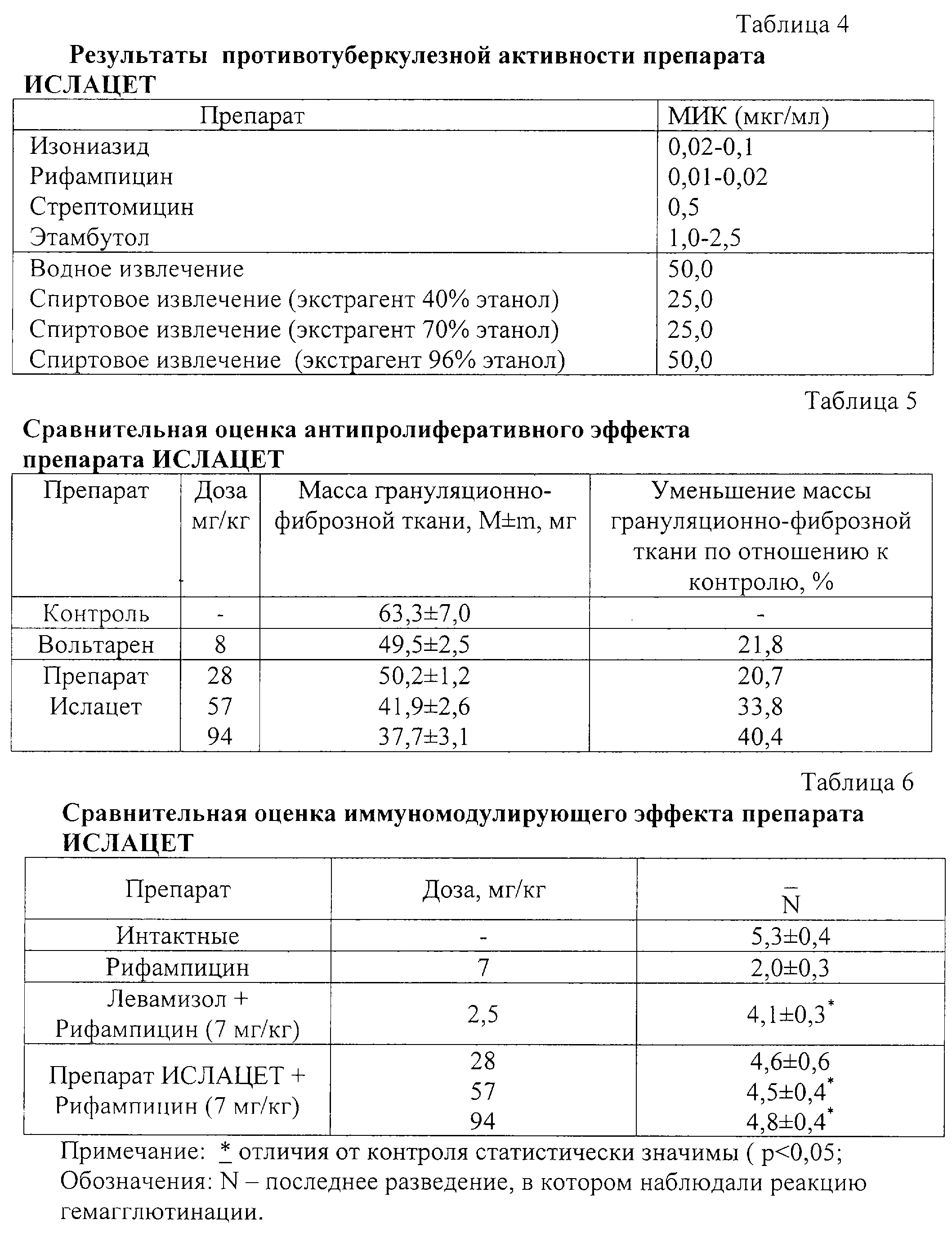
Резистентность микобактерий к препарату развивается медленно. Из ЖКТ всасывается хорошо,
через 1-2 часа накапливается в плазме крови в максимальных концентрациях, равномерно и
легко проникает через тканевые барьеры, в том числе через ГЭБ, равномерно распределяется
по всем тканям. Изониазид действует на микобактерии туберкулеза, расположенные как
внутриклеточно, так и внеклеточно. Используют при всех формах туберкулеза и для
профилактики. Назначают препарат, в основном, внутрь. При необходимости применяют
парентерально в/в или в/м, для промывания серозных полостей и свищевых ходов. Выводится
препарат преимущественно через почки.
Побочное действие: нейротоксичность, проявляется в виде невритов,
в том числе поражением зрительного нерва; бессонница;
судороги; расстройство памяти; нарушения равновесия;
у некоторых больных отмечается сухость во рту, тошнота,
запоры, рвота, легкая анемия.
Форма выпуска. Порошок, таблетки, в упаковке 100 штук
по 0,1 и 0,3 г; в ампулах 10% -ный раствор по 5 мл, в упаковке
10штук.
12. Препараты парааминосалициловой кислоты (ПАСК) НАТРИЯ ПАРА-АМИНОСАЛИЦИЛАТ (Natrii para-aminosalicylas)
Фармакологическое действие. Обладает бактериостатической
активностью в отношении микобактерий туберкулеза.
Показания к применению. Различные формы туберкулеза.
Способ применения и дозы. Внутрь по 3—4 г 3 раза в день, детям
по 0,2 г/(кг в сутки) (не более 10 г в сутки) в 3 — 4 приема.
Внутривенно (капельно) по 250—450 мл 3%-ного раствора
5—6 раз в неделю.
Побочное действие. Расстройства желудочно-кишечного тракта, аллергические
реакции, лихорадочная реакция, астматические явления, эозинофилия. При
нарушении техники внутривенного введения возможен шок.
Противопоказания. Нефрит, гепатиты, цирроз, амилоидоз, язвенная болезнь желудка и
двенадцатиперстной кишки, микседема, декомпенсированный порок сердца.
Внутривенное введение противопоказано при тромбофлебитах, нарушении
свертываемости крови.
Форма выпуска. Порошок, таблетки по 0,5 г, в упаковке 150 штук, таблетки,
Порошок, таблетки по 0,5 г, в упаковке 150 штук, таблетки,
растворимые в кишечнике, по 0,5 г, в упаковке 150 штук, таблетки по 0,5 г, покрытые
оболочкой, в упаковке 100штук, гранулы в упаковке по 100г.
13. Этамбутол (Ethambutolum)
оказывает избирательное действие на микобактерии туберкулеза.
Механизм действия: угнетение синтеза РНК.
Устойчивость микобактерий к этамбутолу развивается медленно.
Этамбутол назначают при разных формах туберкулеза, обычно в
комбинации с другими противотуберкулезными средствами.
Способ применения и дозы. Внутрь, 1 раз в день (после завтрака),
первичным больным, ранее не принимавшим
противотуберкулезные препараты, — по 15 мг/кг; больным, ранее
принимавшим противотуберкулезные препараты, — по 25 мг/кг.
Курс лечения 2 месяца. Затем препарат назначают в
поддерживающих дозах.
Побочное действие. Возможны ухудшения зрения,
аллергические реакции.
Противопоказания. Неврит зрительного нерва, катаракта,
воспалительные заболевания глаз, диабетическая ретинопатия,
беременность.
Форма выпуска. Таблетки, в упаковке 100 штук по 0,1 и 0,4 г.
14. препараты средней эффективности (препараты второго ряда) Этионамид (Aethionamidum)
Синтетическое противотуберкузное средство. Спектр действия
включает микобактерии туберкулеза и лепры. Устойчивость
микобактерий туберкулеза к препарату возникает быстро, поэтому
его всегда применяют в комбинации с другими
противотуберкулезными препаратами. Назначается внутрь, ректально
и внутривенно.
Побочные эффекты: диспепсические расстройства; Гепатит;
ортостатический коллапс; нарушения ЦНС; нарушения
периферической нервной системы.
Циклосерин (Cycloserinum)
Механизм действия — нарушает синтез клеточной стенки.
Спектр действия — широкий, активен в отношении микобактерий
туберкулеза, как вне, так и внутриклеточных.
Характер действия: действует бактерицидно. Устойчивость микобактерий
туберкулеза к циклосерину развивается относительно медленно.
Побочные эффекты: нервно-психические нарушения; головные боли;
головокружение; тремор; судороги; возбуждение или депрессия; психозы
15.
 КОМБИНИРОВАННЫЕ ПРЕПАРАТЫ
КОМБИНИРОВАННЫЕ ПРЕПАРАТЫ
На основе противотуберкулёзных средств I ряда — изониазида, рифампицина, пиразинамида,
этмбутола — создан ряд комбинированных таблетированных препаратов, таких как рифинаг,
рифатер, рифакомб, майрин, майрин П, фтизоэтам, фтизопирам. Главная цель разработки и
применения этих препаратов — сокращение суточного числа таблеток, принимаемых
пациентом, и обеспечение на этой основе более высокой комплаентности.
Дозы компонентов, включенных в комбинированные препараты, соответствуют их суточным
дозам, рекомендованным ВОЗ.
Комбинированные противотуберкулёзные препараты
Число компонентов
Торговое
название
Рифинаг
2-компонентные
3-компонентные
4-компонентные
Компоненты
рифампицин 0,15 г + изониазид 0,1 г
рифампицин 0,3 г + изониазид 0,15 г
Фтизоэтам
изониазид 0,15 г + этамбутол 0,4
Фтизопирам
изониазид 0,15 г + пиразинамид 0,5 г
Рифакомб
рифампицин 0,15 г + изониазид 0,1 г + пиридоксин 0,1 г
Рифатер
рифампицин 0,15 г + изониазид 0,05 + пиразинамид 0,3 г
Майрин
рифампицин 0,15 г + изониазид 0,075 г + этамбутол 0,3 г
Майрин П
рифампицин 0,12 г + изониазид 0,06 г +
этамбутол 0,225 г + пиразинамид 0,3 г
16.
 Примеры рецептов:
Примеры рецептов:
Rp.: Tab. Isoniazidi 0,3 N 100
D.S. В 1-е сутки по 1 т. 3 раза в день,
затем по 2 т. После еды 1 раз в сутки.
Rp.: Sol. Isoniazidi 10% — 5 ml
D.t.d. N 60 in amp.
S. в/м по 5 мл 2 раза в сутки в
течение 2 мес.
Rp.: Dragee Natrii para-aminosalicylatis 0,5
D.t.d. N 100
S. по 6 драже 3 раза в сутки через
0,5-1,0 ч после еды, запивать щелочной
минеральной водой или молоком.
Rp.: Rifampicini 0,15
D.t.d. N 100 in caps.
S. по 3 капсулы 1 раз в сутки за 1 ч.
до еды
Rp.: Cycloserini 0,25
D.t.d. N 30 in caps.
S. по 1 капсуле 3 раз в сутки
непосредственно перед едой в течение 10
суток.
Rp.: Tab. Ethambutoli 0,4 N 100
D.S. по 2 таблетки 1 раз в сутки после
завтрака.
Rp.: Dragee Ethionamidi 0,25
D.t.d. N 50
S. по 1 драже 3 раза в сутки после еды.
Rp.: Tab. «Phtizopyramum» N 50
D.S. по 1 таблетки 1 раз в сутки после
завтрака.
17.
 Спасибо за внимание
Спасибо за внимание
%PDF-1.4
%
1 0 obj
>
endobj
2 0 obj
>
endobj
3 0 obj
>
endobj
4 0 obj
>
endobj
5 0 obj
>
endobj
6 0 obj
>
stream
2019-10-14T23:47:45+03:002019-10-16T11:24:40ZAdobe InDesign CC (Windows)2019-10-16T11:24:40Zurn:uuid:6032D14A-8EBE-4E75-8F88-AA5E76CA699Exmp.did:007931646413E6119827FB9E81F5B9ECxmp.id:43ca549b-dec9-ea41-a458-b5eef1191da2proof:pdfxmp.iid:f914a47d-905f-6142-be8b-1c288917aad6xmp.did:0409121b-7a14-a043-8bf0-f57e667151bfxmp.did:007931646413E6119827FB9E81F5B9ECdefault
application/pdf
False1.43-Heights(TM) PDF Security Shell 4.8.25.2 (http://www.pdf-tools.com)
endstream
endobj
7 0 obj
>
endobj
8 0 obj
>
/XObject >
/Font >
>>
/Contents 70 0 R
/TrimBox [8.50394 8.50394 847.559 603.78]
/Group 71 0 R
/ArtBox [8.50394 8.50394 847.559 603. 78]
78]
/BleedBox [0 0 856.063 612.283]
/StructParents 0
/Parent 2 0 R
>>
endobj
9 0 obj
>
/XObject >
>>
/Contents 79 0 R
/Parent 2 0 R
/Rotate 360
>>
endobj
10 0 obj
>
/Font >
>>
/Contents 84 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 1
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
11 0 obj
>
/Font >
>>
/Contents 85 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 3
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
12 0 obj
>
/Font >
>>
/Contents 86 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 4
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
13 0 obj
>
/Font >
>>
/Contents 87 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 5
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
14 0 obj
>
/Font >
>>
/Contents 88 0 R
/ArtBox [8. 50394 8.50394 428.031 603.78]
50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 6
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
15 0 obj
>
/Font >
>>
/Contents 89 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 7
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
16 0 obj
>
/Font >
>>
/Contents 91 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 8
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
17 0 obj
>
/Font >
/Properties >
>>
/Contents 98 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 9
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
18 0 obj
>
/Font >
>>
/Contents 100 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 10
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
19 0 obj
>
/Font >
>>
/Contents 101 0 R
/ArtBox [8. 50394 8.50394 428.031 603.78]
50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 11
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
20 0 obj
>
/Font >
>>
/Contents 102 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 12
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
21 0 obj
>
/Font >
>>
/Contents 104 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 13
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
22 0 obj
>
/Font >
>>
/Contents 105 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 14
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
23 0 obj
>
/Font >
>>
/Contents 107 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 15
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
24 0 obj
>
/Font >
>>
/Contents 108 0 R
/ArtBox [8. 50394 8.50394 428.031 603.78]
50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 16
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
25 0 obj
>
/Font >
>>
/Contents 110 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 17
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
26 0 obj
>
/Font >
>>
/Contents 112 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 18
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
27 0 obj
>
/Font >
>>
/Contents 113 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 19
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
28 0 obj
>
/Font >
>>
/Contents 114 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 20
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
29 0 obj
>
/Font >
>>
/Contents 115 0 R
/ArtBox [8. 50394 8.50394 428.031 603.78]
50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 21
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
30 0 obj
>
/Font >
>>
/Contents 116 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 22
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
31 0 obj
>
/Font >
>>
/Contents 117 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 23
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
32 0 obj
>
/Font >
>>
/Contents 118 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 24
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
33 0 obj
>
/Font >
>>
/Contents 119 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 25
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
34 0 obj
>
/Font >
>>
/Contents 120 0 R
/ArtBox [8. 50394 8.50394 428.031 603.78]
50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 26
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
35 0 obj
>
/Font >
>>
/Contents 121 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 27
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
36 0 obj
>
/Font >
>>
/Contents 122 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 28
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
37 0 obj
>
/Font >
>>
/Contents 123 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 29
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
38 0 obj
>
/Font >
>>
/Contents 124 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 30
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
39 0 obj
>
/Font >
>>
/Contents 125 0 R
/ArtBox [8. 50394 8.50394 428.031 603.78]
50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 31
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
40 0 obj
>
/Font >
>>
/Contents 126 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 32
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
41 0 obj
>
/Font >
>>
/Contents 127 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 33
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
42 0 obj
>
/Font >
>>
/Contents 128 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 34
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
43 0 obj
>
/Font >
>>
/Contents 129 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 35
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
44 0 obj
>
/Font >
>>
/Contents 130 0 R
/ArtBox [8. 50394 8.50394 428.031 603.78]
50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 36
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
45 0 obj
>
/Font >
>>
/Contents 131 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 37
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
46 0 obj
>
/Font >
>>
/Contents 132 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 38
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
47 0 obj
>
/Font >
>>
/Contents 133 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 39
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
48 0 obj
>
/Font >
>>
/Contents 134 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 40
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
49 0 obj
>
/Font >
>>
/Contents 135 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 41
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
50 0 obj
>
/Font >
>>
/Contents 136 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 42
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
51 0 obj
>
/Font >
>>
/Contents 137 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 43
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
52 0 obj
>
/Font >
>>
/Contents 139 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 44
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
53 0 obj
>
/Font >
>>
/Contents 140 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 45
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
54 0 obj
>
/Font >
>>
/Contents 141 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 46
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
55 0 obj
>
/Font >
>>
/Contents 142 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 47
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
56 0 obj
>
/Font >
>>
/Contents 143 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 48
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
57 0 obj
>
/Font >
>>
/Contents 144 0 R
/ArtBox [8.50394 8.50394 428.031 603.78]
/BleedBox [0 0 436.535 612.283]
/StructParents 49
/TrimBox [8.50394 8.50394 428.031 603.78]
/Parent 2 0 R
>>
endobj
58 0 obj
>
>>
/Contents 148 0 R
/Parent 2 0 R
>>
endobj
59 0 obj
>
endobj
60 0 obj
>
/A3 >
/A5 >
/A6 >
/A7 >
/A8 >
/Pa0 >
/Pa1 >
/Pa10 >
/Pa11 >
/Pa12 >
/Pa13 >
/Pa14 >
/Pa15 >
/Pa16 >
/Pa17 >
/Pa18 >
/Pa2 >
/Pa21 >
/Pa23 >
/Pa24 >
/Pa25 >
/Pa26 >
/Pa28 >
/Pa29 >
/Pa3 >
/Pa5 >
/Pa6 >
/Pa7 >
/Pa9 >
>>
endobj
61 0 obj
>
endobj
62 0 obj
>
endobj
63 0 obj
>
endobj
64 0 obj
>
endobj
65 0 obj
>
endobj
66 0 obj
>
endobj
67 0 obj
>
stream
Противотуберкулезные лекарственные препараты — Справочник лекарств
Противотуберкулезные препараты – это обширная группа синтетических химиотерапевтических лекарственных средств, которые угнетают рост, размножение и активность микобактерии туберкулеза.
Туберкулез – это чрезвычайно распространенное тяжелое инфекционное заболевание с хроническим течением.
Вызывают туберкулез особые возбудители – микобактерии (палочки Коха). Они устойчивы к большинству современных антибактериальных препаратов в силу особенностей строения своей клеточной стенки и обмена веществ.
Различают туберкулез органов дыхания (туберкулез легких – до 95% всех случаев туберкулеза), а также внелегочной туберкулез (туберкулез почек и мочевыводящих путей, органов брюшной полости, кожи, костей, суставов, головного и спинного мозга и т.д.).
Особую опасность представляет лекарственно-устойчивый туберкулез (до 30% всех случаев туберкулеза), который очень тяжело поддается лечению и часто заканчивается смертью.
По данным Центра медицинской статистики Министерства здравоохранения Украины заболеваемость туберкулезом составляет 62-64 случая на 100 000 населения, что говорит о достаточно широком распространении туберкулеза среди украинцев.
Лечение туберкулеза длительное и комплексное. С этой целью используют особую группу антибактериальных средств – противотуберкулезные препараты.
Показания к применению
Противотуберкулезные препараты показаны при туберкулезе разных форм, локализации и степени тяжести.
Антибиотики и фторхинолоны применяют также при других инфекционных заболеваниях (дыхательных, мочевыводящих путей, желудочно-кишечного тракта и т.д.), вызванных чувствительными к этим препаратам бактериями.
Фармакологическое действие
Противотуберкулезные препараты оказывают негативное влияние на микобактерии за счет нарушения синтез клеточной стенки, ДНК, РНК, белков, а также дыхательных ферментов возбудителя туберкулеза.
Противотуберкулезные препараты могут оказывать как туберкулоцидное действие (убивать микобактерии), так и туберкулостатическое действие (замедлять рост и размножение возбудителей туберкулеза).
Большинство противотуберкулезных препаратов (за исключением антибиотиков и фторхинолонов) имеют узкий спектр антибактериального действия – влияют только на микобактерии туберкулеза. Отдельные противотуберкулезные препараты также эффективны относительно микобактерий лепры – возбудителей проказы.
Классификация противотуберкулезных препаратов
Противотуберкулезные препараты классифицируют на:
- противотуберкулезные антибиотики: рифампицин, рифамицин, рифабутин, циклосерин, капреомицин, стрептомицин, канамицин, амикацин, линезолид;
- гидразиды изоникотиновой кислоты: изониазид, фтивазид;
- производные тиокарбамида: протионамид, этионамид;
- производные аминосалициловой кислоты: натрия парааминосалицилат;
- фторхинолоны: ломефлоксацин, офлоксацин, левофлоксацин, ципрофлоксацин;
- производные разных химических групп: пиразинамид, этамбутол, теризидон, бедаквилин, претоманид, деламанид.
Кроме того, существуют комбинированные противотуберкулезные препараты, содержащие: рифампицин + изониазид; рифампицин + пиразинамид + изониазид; рифампицин + пиразинамид + этамбутол + изониазид; рифампицин + этамбутол + изониазид; натрия парааминосалицилат + изониазид; ломефлоксацин + пиразинамид + протионамид + этамбутол.
Также противотуберкулезные препараты классифицируют на:
- препараты I ряда – основные: изониазид, фтивазид, рифампицин, рифамицин, рифабутин, стрептомицин, этамбутол, натрия парааминосалицилат;
- препараты II ряда – резервные: циклосерин, капреомицин, канамицин, амикацин, протионамид, этионамид, пиразинамид;
- препараты для лечения лекарственно-устойчивого туберкулеза: ломефлоксацин, офлоксацин, левофлоксацин, ципрофлоксацин, линезолид, бедаквилин, претоманид, деламанид.
Основы лечения туберкулеза
Лечение туберкулеза проводят в особых закрытых или полузакрытых медицинских учреждениях – туберкулезных диспансерах.
Все противотуберкулезные препараты назначаются исключительно узкоспециализированным врачом – фтизиатром.
Лечение туберкулеза всегда комплексное – предполагает достаточно длительный прием 3-4 противотуберкулезных препаратов (по индивидуальным схемам).
Курс лечения туберкулеза составляет от 6 до 12 месяцев; лекарственно-резистентного туберкулеза – до 18 месяцев.
Крайне обязательным в терапии туберкулеза является полноценное питание пациента – употребление мясных, молочных продуктов, овощей и фруктов, а также санаторно-курортное лечение в местах с теплым морским климатом.
Особенности лечения туберкулеза
В комплексном лечении туберкулеза обязательно комбинируют противотуберкулезные препараты I и II ряда. Препараты I ряда более активны по отношению к возбудителям туберкулеза, однако к ним у микобактерий быстро возникает устойчивость (резистентность). Препараты же II ряда менее активны, но влияют на бактерии, устойчивые к препаратам I ряда.
Все противотуберкулезные препараты достаточно токсичны, вызывают большое количество побочных эффектов.
Для профилактики или снижения тяжелых побочных эффектов изониазида (лекарственного гепатита, судорог, нарушений памяти, психозов) целесообразно применять препараты витамина В 6 – пиридоксина.
Рифампицин, рифамицин, рифабутин окрашивают все биологические жидкости организма (мочу, слюну, слезы, сперму, влагалищный секрет) в красно-оранжевый цвет, однако этого не стоит пугаться, поскольку подобный эффект не представляет опасности для жизни и здоровья пациента.
Противотуберкулезные средства — презентация на Slide-Share.ru 🎓
1
Первый слайд презентации: Противотуберкулезные средства
Изображение слайда
2
Слайд 2: микобактерия туберкулеза
Изображение слайда
3
Слайд 3
Изображение слайда
4
Слайд 4
Изображение слайда
5
Слайд 5
Изображение слайда
6
Слайд 6: Противотуберкулёзные препараты — препараты, активные по отношению к палочке Ко́ха ( лат. Mycobactérium tuberculósis ) и другим возбудителям туберкулёза
Изображение слайда
7
Слайд 7
Изображение слайда
8
Слайд 8: Классификация противотуберкулёзных препаратов
Препараты I ряда
Препараты II ряда
Изониазид
Рифампицин
Этамбутол
Стрептомицин
Пиразинамид
Канамицин
Амикацин
Ципрофлоксацин
Офлоксацин
Циклосерин
Парааминосалициловая кислота (ПАСК)
Изображение слайда
9
Слайд 9
Изображение слайда
10
Слайд 10
Классификация противотуберкулезных средств по происхождению:
синтетические препараты ─ действуют только на микобактерии туберкулеза: изониазид, этамбутол, этионамид, парааминосалициловая кислота(ПАСК), пиразинамид ;
антибиотики ─ имеют широкий противомикробный спектр: рифампицин, стрептомицин, канамицин, амикацин, кларитромицин
Изображение слайда
11
Слайд 11
Классификация по эффективности:
группа А ─ наиболее эффективные препараты: изониазид, рифампицин ;
группа В ─ препараты средней эффективности: этамбутол, стрептомицин, канамицин, циклосерин ;
группа С ─ препараты с умеренной эффективностью: парааминосалициловая кислота(ПАСК) в виде натриевой соли.
Изображение слайда
12
Слайд 12
Изображение слайда
13
Слайд 13
Изображение слайда
14
Слайд 14: Препараты группы А
1.Изониазид ( тубазид )
Isoniazidum
Изображение слайда
15
Слайд 15
Изображение слайда
16
Слайд 16
Изображение слайда
17
Слайд 17
Изображение слайда
18
Слайд 18
Изображение слайда
19
Слайд 19: Препараты группы А
2.Рифампицин ( бенемицин )
Rifampicinum ( Капс. по 0,15 и 0,3 N.20,100Внутрь по 0,45 1 раз в сутки за 1 час до еды
Изображение слайда
20
Слайд 20
Изображение слайда
21
Слайд 21: Препараты группы В
Стрептомицина сульфат Streptomycini sulfas
Флаконы по 0,5. Содержимое флакона 1,0 сух.в-ва растворить в 1-5 мл воды для инъекций; 0,9% р- ра NaCl или 0,25-0,5% р- ра новокаина ; в/м суточную дозу (1,0 ) в один прием. В первые 3-5 дней лечения- по 0,5 2 раза в день.
Изображение слайда
22
Слайд 22: Препараты группы В
1.Этамбутол — Ethambutolum
2.Пиразинамид — Pirazinamidum
Изображение слайда
23
Слайд 23
Изображение слайда
24
Слайд 24
Изображение слайда
25
Слайд 25
Изображение слайда
26
Слайд 26
Изображение слайда
27
Слайд 27
Изображение слайда
28
Слайд 28
Изображение слайда
29
Слайд 29
Изображение слайда
30
Слайд 30
Изображение слайда
31
Слайд 31: Препараты группы В
Циклосерин ( Cycloserinum ) — резервный ЛП. Внутрь по 0,25 г 3 раза в день.
Изображение слайда
32
Последний слайд презентации: Противотуберкулезные средства: Препараты группы С
Натрия пара- аминосалицилат
Natrii para-aminosalicylas
Табл. по 0,5 N.100.Внутрь по 3,0-4,0 3 раза в день через 1 час после еды, запивая молоком или щелочной водой
Изображение слайда
Научная деятельность кафедры
1. Изучена цитоморфология, иммунология, клиника, лекарственная устойчивость микобактерий туберкулеза и осложнения остропрогрессирующего туберкулеза легких и клинико-лабораторные проявления осложнений, в том числе инфекционно-токсического шока, как одного из ведущих осложнений казеозной пневмонии, и разработана методика химиотерапии и патогенетического комплексного лечения для снижения летальности данной тяжелой категории пациентов.
2. Изучены клинические проявления, диагностика и разработана классификация побочных реакций и медикаментозных осложнений на противотуберкулезные препараты при стандартных и индивидуализированных режимах химиотерапии и предложена методика комплексного лечения и профилактики для повышения эффективности больных туберкулезом.
3. Определены критерии и разработан алгоритм дифференциальной диагностики диссеминированного и инфильтративного туберкулеза, казеозной пневмонии и плевральных выпотов с неспецифическими воспалительными заболеваниями легких и плевры.
4. Определены особенности клинического течения и разработан алгоритм диагностики оппортунистических инфекций легких (кандидоз и микобактериоз легких, бактериальная, пневмоцистная и вирусная пневмония) у больных туберкулезом на поздних стадиях ВИЧ-инфекции с иммунодефицитом для своевременного назначения этиологического лечения для снижения летальности данной тяжелой категории пациентов.
5. Изучены особенности эпидемиологии, клиники и диагностики коморбидности новой короновирусной инфекции и туберкулеза у больных на поздних стадиях ВИЧ-инфекции с иммунодефицитом для своевременного назначения этиологического лечения, снижение летальности данной тяжелой категории пациентов и ограничения их эпидемиологической опасности для здорового населения.
Основные научные направления, разрабатываемые на кафедре
1. Эффективность стандартных и индивидуализированных режимов химиотерапии у впервые выявленных больных туберкулезом, сочетанным с ВИЧ-инфекцией, при различном уровне региональной и индивидуальной лекарственной устойчивости возбудителя в гражданских и пенитенциарных противотуберкулезных учреждениях
2. Диагностика, клиника и лечение больных туберкулезом, сочетанным с ВИЧ-инфекцией, молодого возраста
3. Клинические проявления и эффективность комплексного лечения больных туберкулезом, сочетанным с ВИЧ-инфекцией, с выделением микобактерий туберкулеза и нетуберкулезных микобактерий
4. Диагностика и дифференциальная диагностика оппортунистических заболеваний легких (апипичными микобактериозами, бактериальной, пневмоцистной, грибковой и вирусной пневмонией, саркомой Капоши) у больных туберкулезом органов дыхания на поздних стадиях ВИЧ-инфекции с иммунодефицитом.
5. Клиника и диагностика коморбидности новой короновирусной инфекции (COVID-19) и туберкулеза органов дыхания у больных на поздних стадиях ВИЧ-инфекции с иммунодефицитом.
современных противотуберкулезных препаратов и их классификация. Часть I. Лекарства первого ряда
Лечение туберкулеза: Руководство для национальных программ. Всемирная организация здравоохранения, WHO / TB / 97.220, 1997.
Всемирная организация здравоохранения. Руководство по лечению туберкулеза. Документ WHO / HTM / TB / 2009.420, ВОЗ, Женева, 2010 г.
Сводное руководство ВОЗ по лечению лекарственно-устойчивого туберкулеза, Всемирная организация здравоохранения, Женева, 2019 г .; Лицензия: CC BY-NC-SA 3.0 МПО.
Информационные бюллетени Ликвидация туберкулеза: общая информация. Октябрь 2011 г .; https://www.cdc.gov/tb/publications/factsheets/general/tb.htm.
Р. Байер и Д. Уилкинсон, Lancet , 345 (8964), 1545–1548 (1995).
CAS
PubMed
Google ученый
J. M. Grange, Int. J. Tuberc. Lung Dis. , 1 (4), 293 — 296 (1997).
CAS
PubMed
Google ученый
Всемирная организация здравоохранения. Руководство по программному ведению лекарственно-устойчивого туберкулеза: www.who.int/tb/challenges/mdr/programmatic_guidelines_for_mdrtb/en/; Дата последнего доступа: 12 декабря 2012 г. Дата последнего обновления: 2011 г.
Всемирная организация здравоохранения. Руководство по программному ведению лекарственно-устойчивого туберкулеза. WHO / HTM / TB / 2006.361, Всемирная организация здравоохранения, Женева, 2006 г.
Всемирная организация здравоохранения. Справочник-компаньон к руководствам ВОЗ по программному ведению лекарственно-устойчивого туберкулеза. WHO / HTM / TB / 2014.11, Всемирная организация здравоохранения, Женева, 2014.
Всемирная организация здравоохранения. Руководство по программному ведению лекарственно-устойчивого туберкулеза. Экстренное обновление, 2008 г., WHO / HTM / TB / 2008.402, Всемирная организация здравоохранения, Женева, 2008 г.
Использование бедаквилина в лечении туберкулеза с множественной лекарственной устойчивостью.Временное руководство по политике. Всемирная организация здравоохранения, 2013.
Всемирная организация здравоохранения. Применение деламанида в лечении туберкулеза с множественной лекарственной устойчивостью. Временное руководство по политике, 2014 г.
А. Рендон, С. Тибери, А. Скардигли и др., Дж. Торак. Дис. , 8 (10), 2666 — 2671 (2016).
PubMed
PubMed Central
Google ученый
Э. Харамилло, СЕССИЯ 5, июн.1, 2017. Внедрение новых и перепрофилированных противотуберкулезных препаратов. Политика ВОЗ в отношении лечения лекарственно-устойчивого туберкулеза. Глобальная программа по борьбе с туберкулезом, ВОЗ / штаб-квартира / подразделение LDR, Женева, 2017.
П. Пуркан, И. Ихсанавати, Д. Наталья и др., Ukr. Biochem. J. , 88 (5), 71 — 81 (2016).
CAS
PubMed
Google ученый
Y.-Q. Ху, С. Чжан, Ф. Чжао и др., евро. J. Med. Chem., 133 , 255 — 267 (2017).
CAS
PubMed
Google ученый
Р. Тандон и М. Нат, Mini-Rev. Med. Chem. , 17, (6), 549 — 570 (2017).
CAS
PubMed
Google ученый
З. Рыхтарчикова, М. Кратки, М. Газдова и др., Molecules , 19 , 3851 — 3868 (2014).
PubMed
PubMed Central
Google ученый
М. О. Родригес, Дж. Б. Кантос, К. Р. М. Д’Ока и др., Bioorg. Med. Chem. , 21 (22), 6910 — 6914 (2013).
CAS
PubMed
Google ученый
D. K. Beena, G. Khare, S. Kidwai, et al., Eur. J. Med. Chem. , 81, , 301 — 313 (2014).
PubMed
Google ученый
Дж. П. Раваль, Н. Х. Патель, Х.V. Patel и др., Chem. Res. , 20, , 274 — 279 (2011).
CAS
Google ученый
G. F. dos S. Fernandes, P. S. de Souza, L. B. Marino, et al., Eur. J. Med. Chem. , 123 , 523 — 531 (2016).
G. F. dos S. Fernandes, P. C. de Souza, E. Moreno-Viguri, et al., J. Med. Chem. , 60 (20), 8647 — 8660 (2017).
Х. С. Н. Кумар, Т. Парамасивам, Ф. Джумаат и др., Med. Chem. Res. , 23 , 269 — 279 (2014).
Google ученый
П. Кумар, П. Рават, П. Сингх и др., Int. J. Pharm. Sci. Res. , 4 (6), 2080 — 2093 (2013).
CAS
Google ученый
Н. Ананд, К. Упадхьяя, Р. П. Трипати, Chem.Биол. Интерфейс , 5 (2), 84 — 127 (2015).
CAS
Google ученый
Б. Придо, Л. Э. Виа, М. Д. Циммерман и др., Nat. Med. , 21, , 1223 — 1227 (2015).
CAS
PubMed
PubMed Central
Google ученый
W. Manosuthi, S. Wiboonchutikul, S. Sungkanuparph, AIDS Res. Ther. , 13 , 22 (2016).
PubMed
PubMed Central
Google ученый
M. Asif, World J. Org. Chem. , 1 , 14 — 19 (2013).
Google ученый
А. Н. Унисса, Л. Е. Ханна, С. Сваминатан, Chem. Биол. Drug Des. , 87 , 537 — 550 (2016).
Google ученый
Т. Равал и С. Бутани, Indian J. Pharm. Sci. , 78 (1), 8 — 16 (2016).
CAS
PubMed
PubMed Central
Google ученый
«Adis Insight: Rifalazil (ABI 1648; KRM 1648; PA 1648)», Adis Insight, Springer International Publishing AG, 2016.
KE Dooley, CD Mitnick, MA DeGroote, et al. ., Clin. Заразить. Дис. , 55 (4), 572 — 581 (2012).
PubMed
PubMed Central
Google ученый
K.-W. Джо, В. Джи, Ю. Хонг и др., Respir. Med. , 107, , 292 — 297 (2013).
PubMed
Google ученый
K. E. Dooley, P. Sayre, J. Borland, et al., J. Acquired Immune Defic. Syndr. , 62 (1), 21 — 27 (2013).
CAS
Google ученый
Т. Р. Стерлинг, Н. А. Скотт, Дж. М. Миро и др., AIDS (Лондон, США), , 30, (10), 1607 — 1615 (2016).
A. Jindani, T. S. Harrison, A. J. Nunn, et al., N. Engl. J. Med. , 371 (17), 1599 — 1608 (2014).
PubMed
PubMed Central
Google ученый
Лечение туберкулеза, Руководство по лечению лекарственно-чувствительного туберкулеза и уход за пациентами, ОБНОВЛЕНИЕ 2017 г., Всемирная организация здравоохранения, 2017 г.
Профилактика туберкулеза в течение 1 месяца с эффективностью 9 месяцев, Инфекционное заболевание. Респираторная инфекция. Дис. News , Healio, 2018.
M. Njire, Y. Tan, J. Mugweru, et al., Adv. Med. Sci. , 61 (1), 63 — 71 (2016).
PubMed
Google ученый
С. Саркар, А. Гангули и Х. Х. Сану, Mycobact. Дис. , 6 , 209 (2016).
Google ученый
Y. S. Kwon, Chonnam Med. J. , 53 (2), 103 — 109 (2017).
CAS
PubMed
PubMed Central
Google ученый
Z. Ahmad, S. Tyagi, A. Minkowski и др., Indian J. Med. Res. , , 136, (5), 808 — 814 (2012).
CAS
PubMed
PubMed Central
Google ученый
Я. Зитко, Б. Сервусова, П. Патерова и др., Molecules , 18 (12), 14807 — 14825 (2013).
CAS
PubMed
PubMed Central
Google ученый
О. Джандурек, М. Таухман, П. Патерова и др., Molecules , 22 , 223 — 243 (2017).
PubMed Central
Google ученый
С. Чжоу, С. Ян и Г.Huang, J. Enzyme Inhib. Med. Chem. , 32 (1), 1183 — 1186 (2017).
CAS
PubMed
PubMed Central
Google ученый
Н. Д. Сегретти, К. К. Симоэс, М. Ф. Корреа и др., Tuberculosis , 99 , 11e16 (2016).
Google ученый
М. Ф. Корреа и Дж. П. С. Фернандес, Curr. Protein Pept.Sci. , 17, (3), 213 — 219 (2016).
CAS
PubMed
Google ученый
GB Migliori and A. Zumla, in: Infectious Diseases , 4th Ed., J. Cohen, WG Powderly, and SM Opal (eds.), Elsevier, Amsterdam, 2017, pp. 1264 — 1276 .e2.
К. Кумар и А. В. Нарсайя, Org. Commun. , 7 (1), 28 — 33 (2014).
Google ученый
М. Асиф, Эликсир. Фармация , 53 , 11774 — 11778 (2012).
Google ученый
Х. Сафи, С. Лингараджу, А. Амин и др., Nat. Genet. , 45, , 1190 — 1197 (2013).
CAS
PubMed
PubMed Central
Google ученый
К. Шуберт, Б. Зигер, Ф. Мейер и др., mBio , 8 (1), e02213 — 16 (2017).
Р.Э. Ли, М. Протопопова, Э. Крукс и др., J. Comb. Chem. , 5 (2), 172 — 187 (2003).
CAS
PubMed
Google ученый
Протопопова М. Н., в: Достижения в области медицины туберкулеза, , М. Куросо и В. Денни (ред.), Future Science Ltd. — Unitec House, Лондон (2016), гл. 7, pp. 104 — 118.
D. Machado, M. Girardini, M.Viveiros и M. Pieroni, Front Microbiol. , 9 , 1367 (2018).
PubMed
PubMed Central
Google ученый
О. К. Онайоле, П. Говендер и П. Д. ван Хелден, евро. J. Med. Chem. , 45, , 2075 — 2079 (2010).
CAS
PubMed
Google ученый
Борисов С.Е., Богородская Е.М., Волченков Г.В. и др., Клубень. Lung Dis. , 96 (3), 6 — 18 (2018).
Google ученый
M. J. Boeree, N. Heinrich, R. Aarnoutse и др., Lancet Infect. Дис. , 17, (1), 39 — 49 (2017).
CAS
PubMed
PubMed Central
Google ученый
Б. П. Гольдштейн, J. Antibiot. , 67 (9), 625 — 630 (2014).
CAS
PubMed
Google ученый
C. Vilcheze, Jr., W. Jacobs, Microbiol. Спектр , 2 (4), МГМ2 — 0014-2013 (2014).
Y. Zhang, W. Shi, W. Zhang, and D. Mitchison, Microbiol. Спектр , 2 (4), 1 — 12 (2014).
Google ученый
Н. Дуки, С. Рамбаран, Н.Padayatchi, et al., J. Antimicrob. Chemother. , 73 , 1138 — 1151 (2018).
CAS
PubMed
PubMed Central
Google ученый
Дж. Бэкон, Л. Дж. Алдервик, Дж. А. Оллнатт и др., PLoS One , 9 (2), e87329 (2014).
PubMed
PubMed Central
Google ученый
J. A. Caminero (ed.), Guidelines for Clinical and Operational Management of Drug-Resistant Tuberculosis , International Union Against Tuberculosis and Lung Disease, Paris, France, 2013.
Д. Фальзон, Ф. Мирзаев, Ф. Варес и др., евро. Респир. J. , 45 , 150 — 160 (2015).
PubMed
Google ученый
Д. К. Бэй и Р. Дж. Тернер, Малые насосы с множественной лекарственной устойчивостью, , Springer International Publishing, Швейцария, 2016 г., стр. 45 — 71.
Google ученый
J. Sun, Z.Дэн, Янь А., Biochem. Биофиз. Res. Commun. , 453 (2), 254 — 267 (2014).
CAS
PubMed
Google ученый
Y. Xu, J. Wu, S. Liao, et al., Ann. Clin. Microbiol. Противомикробный. , 16 (1), 1 — 13 (2017).
Google ученый
Всемирная организация здравоохранения. Справочник-компаньон к руководствам ВОЗ по программному ведению лекарственно-устойчивого туберкулеза.Всемирная организация здравоохранения. WHO / HTM / TB / 2014.11, Женева, 2014.
D. Falzon, H. J. Schunemann, E. Harausz и др., Рекомендации Всемирной организации здравоохранения по лечению лекарственно-устойчивого туберкулеза, обновление 2016 г., Eur. Респир. J. , 49 (3), 1602308 (2017).
PubMed
PubMed Central
Google ученый
Т. Х. Келлер, А. Пичота, З. Инь, Curr. Opin. Chem. Биол. , 10, , 357 — 361 (2006).
CAS
PubMed
Google ученый
G. Piccaro, G. Poce, M. Biava, et al., J. Antibiot. , 68, , 711 — 714 (2015).
CAS
PubMed
Google ученый
Классификация препаратов для лечения туберкулеза с множественной лекарственной устойчивостью (МЛУ-ТБ): доказательства и перспективы — Rendon
Туберкулез с множественной лекарственной устойчивостью (МЛУ) (ТБ) (определяемый как устойчивость как минимум к изониазиду и рифампицину), имеет актуальную эпидемиологическое воздействие: в 2014 г. было зарегистрировано 480 000 случаев заболевания и 190 000 случаев смерти; 10% из них соответствуют критериям ТБ с широкой лекарственной устойчивостью (ШЛУ) [МЛУ-ТБ с дополнительной устойчивостью к любому фторхинолону и по крайней мере к одному инъекционному препарату второго ряда (SLD)] (капреомицину, канамицину или амикацину) ( 1,2).
Борьба с МЛУ-ТБ — одно из восьми основных вмешательств, направленных на ликвидацию ТБ (3,4). Несмотря на достигнутый прогресс, не более 60% случаев МЛУ-ТБ, 40% случаев ШЛУ-ТБ и <20% случаев со схемами устойчивости за пределами ШЛУ-ТБ достигают успеха в лечении (5,6). Кроме того, в своем отчете за 2015 год (1) ВОЗ подчеркнула, что из 480 000 случаев МЛУ-ТБ только 25% были выявлены [123 000] и 50% излечены.
Схемы лечения МЛУ / ШЛУ-ТБ по-прежнему очень длительны, токсичны и дороги, хотя недавно были рекомендованы более короткие схемы (7,8).
Предыдущие руководящие принципы Всемирной организации здравоохранения (ВОЗ) классифицировали противотуберкулезные препараты на пять основных групп на основе иерархии соображений безопасности и / или эффективности (2,7,9). Эта классификация возникла в 2006 году и обновлялась в 2008, 2011 и, наконец, в 2016 году на основе новых данных, особенно в отношении препаратов бывшей группы 5 (10–31).
Обоснование противотуберкулезного лечения
Исторические принципы, полученные в результате рандомизированных клинических испытаний (РКИ), по-прежнему остаются в силе: (I) комбинирование различных эффективных лекарств для предотвращения отбора устойчивых мутантов M.туберкулез ; и (II) продление лечения для стерилизации инфицированных тканей и, следовательно, предотвращения рецидива (1,9,10).
По крайней мере четыре препарата, которые могут быть эффективными, составляют схему, из которых по крайней мере два являются основными (или «основными» препаратами), а два — сопутствующими препаратами (2,10,11). Основными лекарствами являются те, которые способны убить M. tuberculosis на любой из его метаболических фаз. Напротив, роль сопутствующих препаратов заключается в поддержке основных, защите их действия и предотвращении выбора дальнейшей устойчивости.В то время как один из основных препаратов должен обладать хорошей бактерицидной активностью, другой должен обладать хорошей стерилизующей активностью, и их необходимо поддерживать в течение всего периода лечения. В то время как бактерицидные препараты эффективно уменьшают основную массу быстро размножающихся бацилл (снижая инфекционность и предотвращая прогрессирование болезни), стерилизующие препараты заботятся о популяции спящих и полудремящих бацилл, позволяя вылечить и предотвратить рецидивы. Лучшие стерилизующие препараты могут сократить продолжительность лечения, в то время как сопутствующие препараты больше не нужны после бактериологической конверсии (2,10,11).При подтверждении устойчивости или токсичности основного препарата его следует заменить другим с аналогичной эффективностью (бактерицидным и стерилизующим). Аналогичным образом следует заменить сопутствующий препарат другим с аналогичным действием.
Классификация противотуберкулезных препаратов и история ее обновления
Выбор препаратов основан на их эффективности и токсичности. Основываясь на этом принципе, в рекомендациях ВОЗ 2008 г., а затем 2011 г. предлагался диапазон из пяти групп: от группы 1 (которая включала препараты первого ряда) до групп 2–5, которые включали ЛВС.В группу 5 вошли препараты с потенциально ограниченной клинической эффективностью или ограниченными доказательствами (2,5,10,11) ( Рисунок 1 ). Чтобы ясно показать нынешнюю и будущую эволюцию группы лекарств, мы произвольно включили в группу 5 препараты , диаграмма 1 , новые препараты деламанид и бедаквилин, для которых до недавнего времени были доступны ограниченные доказательства.
Рис. 1 Сравнительный анализ препаратов, включенных в предыдущие классификации и рекомендации Всемирной организации здравоохранения (ВОЗ) от 2016 года.Чтобы продемонстрировать возможность повышения эффективности некоторых препаратов, изначально не включенных в группу 5, мы произвольно включили в эту группу деламанид и бедаквилин.
В недавней публикации (2) Каминеро и Скардигли предложили новую возможную классификацию (, таблица 1, ), в то время как новая классификация ВОЗ 2016 г. предложила иерархию из пяти групп (7), включая группы от A до D: фторхинолоны входят в состав группа A, инъекционные препараты второго ряда в группе B, другие основные SLD в группе C и дополнительные агенты в группе D (где наркотики разделены на подгруппы D1, D2 и D3) ( Рисунок 1 ).Эта классификация специально разработана для случаев устойчивого к рифампицину (диагностированного с помощью Xpert) или МЛУ-ТБ (7).
Таблица 1 Предложение по пересмотренной классификации противотуберкулезных препаратов первого и второго ряда, опубликованное между классификациями Всемирной организации здравоохранения 2011 и 2016 годов [адаптировано из (1)]
Полная таблица
Эта рукопись, принадлежащая проекту ERS / ALAT SinTB (проект координации исследований), описывает обоснование перехода от классификаций ВОЗ 2008 и 2011 годов к 2016 году ( Рисунок 1 ), а также обсуждает возможные будущие изменения.
Группа 1 против группы А
Все потенциально эффективные препараты бывшей группы 1 должны быть включены в схему, учитывая, что изониазид, рифампицин и пиразинамид являются основными препаратами, а этамбутол — сопутствующим препаратом. Изониазид в высоких дозах следует добавлять в схему лечения МЛУ / ШЛУ-ТБ, если мутация katG не документирована с помощью зондового анализа генотипа (Quest Diagnostics, Мэдисон, Нью-Джерси, США), но ее не следует причислять к четырем активным лекарствам ( 2,10,11).
Однако самые последние данные свидетельствуют о том, что это может быть не полностью правдой, что может дополнительно поддерживать систематическое добавление изониазида в высоких дозах даже при наличии мутации katG (12).
Мутация
InhA на самом деле придает очень низкий уровень устойчивости (который достаточно совместим с нормальными дозами изониазида), в то время как мутация katG отвечает за различные уровни лекарственной устойчивости, большинство из этих штаммов имеют низкий или средний уровень устойчивости. Следовательно, во многих случаях устойчивости к изониазиду при наличии мутации katG, вероятно, будут эффективны высокие дозы изониазида (12).
Пиразинамид следует использовать всегда, хотя его тест на лекарственную чувствительность ненадежен, так как он не входит в число четырех активных препаратов (2,10,11).
В новой классификации и с целью лечения МЛУ-ТБ пиразинамид и этамбутол были включены в группу D1 (7) ( Рисунок 1 ).
Фторхинолоны (особенно более позднего поколения: левофлоксацин или моксифлоксацин в высоких дозах) являются основными лекарственными средствами, обладающими бактерицидной и стерилизующей активностью. Они обеспечивают хорошую переносимость и предсказывают благоприятный исход лечения МЛУ-ТБ (2,10,11,13).
На основании этих характеристик они были переведены в группу A (7).
Группа 2 по сравнению с группой B
Бывшая группа 2 включала инъекционные SLD (2,10,11), обладающие бактерицидной (но не стерилизующей) активностью и профилем безопасности хуже, чем фторхинолоны (совокупная токсичность, приводящая к глухоте или проблемам с почками). Они были включены в группу B, которая следует сразу за фторхинолонами (2) ( Рисунок 1 ). Возможность использования стрептомицина в исключительных случаях для лечения МЛУ-ТБ (особенно в отдельных случаях ШЛУ-ТБ, ранее не использовавших этот препарат, и с тестами на лекарственную чувствительность, показывающими чувствительность), возможно, заслуживает дальнейшего обсуждения.
Группы 3 и 4 по сравнению с группой C
Поскольку препараты бывшей группы 1 не рассматривались симметрично для лечения МЛУ-ТБ, следующей группой в иерархическом порядке была группа 4, которая включала этионамид / протионамид, циклосерин / теризидон и ПАСК.
Обладая бактерицидной активностью, они являются основными SLD, хотя с высокой частотой нежелательных явлений, некоторые из которых являются очень серьезными. По этой причине они были включены в группу C, за исключением PAS, который был понижен до группы D3 из-за худшей переносимости в этой группе препаратов (7).
Из-за улучшенных данных об их эффективности и переносимости линезолид и клофазимин были повышены до группы C (7).
В связи с новыми недавними данными, необходимо особое обсуждение линезолида, деламанида и бедаквилина.
Линезолид
Линезолид является основным пероральным препаратом. Накапливается все больше доказательств его эффективности, включая метаанализы и два РКИ, в дополнение к обсервационным исследованиям.К сожалению, текущая стоимость и документально подтвержденная токсичность (14-22) препятствовали его более широкому использованию. Однако стоимость генерического соединения гарантированного качества снижается (21), и в недавнем отчете предполагается, что переносимость можно повысить, снизив начальную дозу или изменив ее во время лечения [например, с использованием терапевтического мониторинга лекарственных средств (TDM)] (23). .
Деламанид и бедаквилин
Накапливается информация о благоприятном профиле безопасности и эффективности как для деламанида, так и для бедаквилина, включая индивидуальное применение в соответствии с существующими рекомендациями (24), применение после 6 месяцев (24) и у детей (25) и даже комбинированное применение (26).
Бедаквилин — это базовый препарат, нацеленный как на активно размножающиеся, так и на спящие бациллы. Доступные доказательства включают РКИ (27,28) и обсервационные исследования, в том числе опыт программ сострадательного использования (26,29). Бедаквилин ускоряет бактериологическое превращение, увеличивая при этом долю конвертеров и скорость излечения (27,28). Основное беспокойство относительно безопасности бедаквилина вызывает необъяснимое более высокое число смертей в группе бедаквилина в РКИ (28), поскольку его наиболее частой побочной реакцией является увеличение интервала QTc на электрокардиограмме (ЭКГ) (24,27,28).Важно отметить его перекрестную резистентность с клофазимином, хотя недавние данные, кажется, указывают на то, что это может быть неклинически значимым (22).
Деламанид из-за его бактерицидной и стерилизующей активности также может считаться основным лекарственным средством (30,31). Он не проявляет перекрестной устойчивости с другими противотуберкулезными препаратами (30,31), эффективен в увеличении как бактериологической конверсии, так и результатов лечения, а также снижает смертность (30-32). Поскольку он также увеличивает QTc, мониторинг ЭКГ также необходим, как и бедаквилин.
Недавно были получены неофициальные данные о том, что оба препарата можно назначать более 6 месяцев, что деламанид безопасен для детей и что эти два препарата можно сочетать (25,26,33).
Какие препараты можно повысить
Линезолид, бедаквилин и деламанид могут изменить мрачный прогноз пациентов с МЛУ-ТБ с устойчивостью к фторхинолонам (некоторые клиницисты называют эти случаи пре-ШЛУ, используя неутвержденное определение) (2) ( Рисунок 1 ).
Недавно появились новые данные о карбапенемах с профилем сопутствующего препарата. Имипенем / циластатин и меропенем в сочетании с клавулановой кислотой, по-видимому, обладают многообещающей активностью, хотя хорошо переносятся (34–37). В прямом сравнении меропенем показывает лучшие результаты, чем имипенем (37). Первоначальный клинический опыт применения эртапенема позволяет предположить, что он может быть эффективным препаратом для лечения МЛУ-ТБ на дому, поскольку его можно вводить внутримышечно один раз в день (38).
Важно отметить, что недавние данные свидетельствуют о том, что эта категория лекарств, ввиду ее бактерицидной активности, может играть роль основного лекарственного средства (39).
Будущие сценарии
Линезолид, деламанид и бедаквилин могут играть более важную роль в лечении МЛУ-ТБ как у взрослых, так и у детей, учитывая их профиль «основного лекарственного средства». При определенных условиях деламанид и бедаквилин можно рассматривать для комбинированного применения (26), хотя необходимы дополнительные доказательства РКИ.
Также необходимы дальнейшие исследования, чтобы установить, могут ли высокие дозы моксифлоксацина и рифабутина играть будущую роль в арсенале МЛУ-ТБ.
Мы надеемся, что дальнейшие доказательства будут сопровождаться снижением стоимости этих соединений; недавнее включение обоих из них в список препаратов, прошедших предварительную квалификацию Глобального фонда по лекарственным средствам, обнадеживает.
Благодарности
Нет.
Конфликт интересов: Эта рукопись является частью деятельности проекта ERS / ALAT SinTB.
Заявление об ограничении ответственности: Только авторы несут ответственность за взгляды, выраженные в этой статье, и они не обязательно представляют решения и политику своих учреждений.
Список литературы
- Всемирная организация здравоохранения. Глобальный отчет о туберкулезе. 2015. Доступно в Интернете: http://apps.who.int/iris/bitstream/10665/1
/1/978 65059_eng.pdf - Каминеро Дж. А., Скардигли А. Классификация противотуберкулезных препаратов: новое предложение, основанное на самых последних данных.Eur Respir J 2015; 46: 887-93. [Crossref] [PubMed]
- Lönnroth K, Migliori GB, Abubakar I, et al. На пути к ликвидации туберкулеза: рамки действий для стран с низким уровнем заболеваемости. Eur Respir J 2015; 45: 928-52. [PubMed]
- Д’Амброзио Л., Дара М., Тадолини М. и др. Ликвидация туберкулеза: теория и практика в Европе. Eur Respir J 2014; 43: 1410-20. [Crossref] [PubMed]
- Falzon D, Gandhi N, Migliori GB, et al. Устойчивость к фторхинолонам и инъекционным препаратам второго ряда: влияние на исходы ТБ с множественной лекарственной устойчивостью.Eur Respir J 2013; 42: 156-68. [Crossref] [PubMed]
- Migliori GB, Sotgiu G, Gandhi NR, et al. Лекарственная устойчивость помимо туберкулеза с широкой лекарственной устойчивостью: метаанализ индивидуальных данных пациентов. Eur Respir J 2013; 42: 169-79. [Crossref] [PubMed]
- Всемирная организация здравоохранения. Рекомендации ВОЗ по лечению лекарственно-устойчивого туберкулеза. Обновление 2016 г. Доступно в Интернете: http://www.who.int/tb/MDRTBguidelines2016.pdf
- Сотгиу Г., Тибери С., Д’Амброзио Л. и др.Быстрее за меньшие деньги: новый «укороченный» режим лечения туберкулеза с множественной лекарственной устойчивостью. Eur Respir J 2016. [Epub перед печатью]. [Crossref] [PubMed]
- Falzon D, Jaramillo E, Schünemann HJ, et al. Рекомендации ВОЗ по программному ведению лекарственно-устойчивого туберкулеза: обновление 2011 г. Eur Respir J 2011; 38: 516-28. [Crossref] [PubMed]
- Каминеро Дж. А., Сотгиу Г., Зумла А. и др. Лучшее лекарственное лечение туберкулеза с множественной и широкой лекарственной устойчивостью.Lancet Infect Dis 2010; 10: 621-9. [Crossref] [PubMed]
- Caminero JA. редактор. Руководство по клиническому и оперативному ведению туберкулеза с лекарственной устойчивостью. Париж, Франция: Международный союз борьбы с туберкулезом и болезнями легких, 2013 г.
- Cambau E, Viveiros M, Machado D и др. Пересмотр тестирования чувствительности при МЛУ-ТБ с помощью стандартизированной количественной фенотипической оценки в европейском многоцентровом исследовании. Журнал Antimicrob Chemother 2015; 70: 686-96. [Crossref] [PubMed]
- Johnston JC, Shahidi NC, Sadatsafavi M и др.Результаты лечения туберкулеза с множественной лекарственной устойчивостью: систематический обзор и метаанализ. PLoS One 2009; 4: e6914. [Crossref] [PubMed]
- Сотгиу Г., Сентис Р., Д’Амброзио Л. и др. Эффективность, безопасность и переносимость схем, содержащих линезолид, при лечении МЛУ-ТБ и ШЛУ-ТБ: систематический обзор и метаанализ. Eur Respir J 2012; 40: 1430-42. [Crossref] [PubMed]
- Chang KC, Yew WW, Tam CM, et al. Лекарства группы 5 ВОЗ и туберкулез с сложной множественной лекарственной устойчивостью: систематический обзор с когортным анализом и метаанализом.Противомикробные агенты Chemother 2013; 57: 4097-104. [Crossref] [PubMed]
- Ли М., Ли Дж., Кэрролл М.В. и др. Линезолид для лечения хронического туберкулеза с широкой лекарственной устойчивостью. N Engl J Med 2012; 367: 1508-18. [Crossref] [PubMed]
- Тан С., Яо Л., Хао Х и др. Эффективность, безопасность и переносимость линезолида для лечения ШЛУ-ТБ: исследование в Китае. Eur Respir J 2015; 45: 161-70. [Crossref] [PubMed]
- Вильяр М., Сотджиу Г., Д’Амброзио Л. и др.Безопасность, переносимость и эффективность линезолида при лечении туберкулеза с множественной и широкой лекарственной устойчивостью. Eur Respir J 2011; 38: 730-3. [Crossref] [PubMed]
- Де Лоренцо С., Сентис Р., Д’Амброзио Л. и др. Об эффективности и переносимости линезолида. Eur Respir J 2012; 39: 770-2. [Crossref] [PubMed]
- Sotgiu G, Pontali E, Migliori GB. Линезолид для лечения МЛУ- / ШЛУ-туберкулеза: имеющиеся данные и сценарии на будущее. Eur Respir J 2015; 45: 25-9. [Crossref] [PubMed]
- Сотгиу Г., Сентис Р., Д’Амброзио Л. и др.Низкие минимальные ингибирующие концентрации линезолида против штаммов туберкулеза с множественной лекарственной устойчивостью. Eur Respir J 2015; 45: 287-9. [Crossref] [PubMed]
- Cox H, Ford N. Линезолид для лечения сложного лекарственно-устойчивого туберкулеза: систематический обзор и метаанализ. Int J Tuberc Lung Dis 2012; 16: 447-54. [Crossref] [PubMed]
- Srivastava S, Peloquin CA, Sotgiu G, et al. Терапевтическое управление лекарственными средствами: будущее лечения туберкулеза с множественной лекарственной устойчивостью? Eur Respir J 2013; 42: 1449-53.[Crossref] [PubMed]
- Pontali E, Sotgiu G, D’Ambrosio L, et al. Бедаквилин и туберкулез с множественной лекарственной устойчивостью: систематический и критический анализ данных. Eur Respir J 2016; 47: 394-402. [Crossref] [PubMed]
- Тадолини М., Гарсия-Пратс А.Дж., Д’Амброзио Л. и др. Сострадательное использование новых лекарств у детей и подростков с туберкулезом с множественной и широкой лекарственной устойчивостью: ранний опыт и проблемы. Eur Respir J 2016; 48: 938-43.[Crossref] [PubMed]
- Тадолини М., Лингтсанг Р.Д., Тибери С. и др. Первый случай туберкулеза с широкой лекарственной устойчивостью, полученный как деламанидом, так и бедаквилином. Eur Respir J 2016; 48: 935-8. [Crossref] [PubMed]
- Diacon AH, Pym A, Grobusch M, et al. Диарилхинолин TMC207 для лечения туберкулеза с множественной лекарственной устойчивостью. N Engl J Med 2009; 360: 2397-405. [Crossref] [PubMed]
- Diacon AH, Pym A, Grobusch MP, et al. Туберкулез с множественной лекарственной устойчивостью и конверсия посевов бедаквилином.N Engl J Med 2014; 371: 723-32. [Crossref] [PubMed]
- Tiberi S, De Lorenzo S, Centis R и др. Бедаквилин в случаях МЛУ / ШЛУ-ТБ: первый опыт сострадательного использования. Eur Respir J 2014; 43: 289-92. [Crossref] [PubMed]
- Gler MT, Skripconoka V, Sanchez-Garavito E, et al. Деламанид при туберкулезе легких с множественной лекарственной устойчивостью. N Engl J Med 2012; 366: 2151-60. [Crossref] [PubMed]
- Скрипконока В., Даниловиц М., Пеме Л. и др. Деламанид улучшает результаты и снижает смертность при туберкулезе с множественной лекарственной устойчивостью.Eur Respir J 2013; 41: 1393-400. [Crossref] [PubMed]
- Wells CD, Gupta R, Hittel N, et al. Долгосрочная оценка смертности больных туберкулезом с множественной лекарственной устойчивостью, получавших деламанид. Eur Respir J 2015; 45: 1498-501. [Crossref] [PubMed]
- Эспозито С., Д’Амброзио Л., Тадолини М. и др. Помощь ERS / WHO Tuberculosis Consilium по ведению детей с туберкулезом с широкой лекарственной устойчивостью: тематическое исследование сострадательного использования деламанида. Eur Respir J 2014; 44: 811-5.[Crossref] [PubMed]
- De Lorenzo S, Alffenaar JW, Sotgiu G, et al. Эффективность и безопасность меропенема-клавуланата, добавленного к схемам, содержащим линезолид, при лечении МЛУ / ШЛУ-ТБ. Eur Respir J 2013; 41: 1386-92. [Crossref] [PubMed]
- Тибери С., Сотджиу Г., Д’Амброзио Л. и др. Эффективность и безопасность имипенема-клавуланата, добавленного к оптимизированному фоновому режиму (ОБР) по сравнению с контрольными режимами ОБР при лечении туберкулеза с множественной и широкой лекарственной устойчивостью.Clin Infect Dis 2016; 62: 1188-90. [Crossref] [PubMed]
- Тибери С., Пайен М.С., Сотгиу Г. и др. Эффективность и безопасность схем, содержащих меропенем / клавуланат, при лечении МЛУ- и ШЛУ-ТБ. Eur Respir J 2016; 47: 1235-43. [Crossref] [PubMed]
- Тибери С., Сотджиу Г., Д’Амброзио Л. и др. Сравнение эффективности и безопасности схем, содержащих имипенем / клавуланат, и схем, содержащих меропенем / клавуланат, при лечении МЛУ- и ШЛУ-ТБ. Eur Respir J 2016; 47: 1758-66.[Crossref] [PubMed]
- Тибери С., Д’Амброзио Л., Де Лоренцо С. и др. Эртапенем в лечении туберкулеза с множественной лекарственной устойчивостью: первый клинический опыт. Eur Respir J 2016; 47: 333-6. [Crossref] [PubMed]
- Диакон А.Х., ван дер Мерве Л., Барнард М. и др. β-Лактамы против туберкулеза — новый трюк для старой собаки? N Engl J Med 2016; 375: 393-4. [Crossref] [PubMed]
Цитируйте эту статью как: Rendon A, Tiberi S, Scardigli A, D’Ambrosio L, Centis R, Caminero JA, Migliori GB.Классификация препаратов для лечения туберкулеза с множественной лекарственной устойчивостью (МЛУ-ТБ): доказательства и перспективы. J Thorac Dis 2016; 8 (10): 2666-2671. DOI: 10.21037 / jtd.2016.10.14
Классификация новых противотуберкулезных препаратов: обоснование и перспективы на будущее
https://doi.org/10.1016/j.ijid.2016.10.026Получение прав и содержание
Основные моменты
- •
Всемирная организация здравоохранения (ВОЗ) 2016 Руководящие принципы по туберкулезу с множественной лекарственной устойчивостью (МЛУ-ТБ) предлагают перегруппировать противотуберкулезные препараты для лечения МЛУ-ТБ.
- •
Классификация противотуберкулезных препаратов помогает клиницисту разработать соответствующую схему лечения ТБ с множественной / широкой лекарственной устойчивостью.
- •
Начато обсуждение возможных будущих изменений групп противотуберкулезных препаратов.
- •
На основании недавних данных о некоторых соединениях, значение некоторых лекарств, вероятно, в будущем будет увеличиваться или уменьшаться.
- •
Если профиль эффективности и безопасности линезолида, бедаквилина и деламанида подтвердится, они могут подняться в иерархии противотуберкулезных препаратов.
Резюме
Классификация противотуберкулезных препаратов (ТБ) важна, поскольку она помогает клиницисту разработать соответствующий режим противотуберкулезной терапии для случаев ТБ с множественной лекарственной устойчивостью (МЛУ) и широкой лекарственной устойчивостью (ШЛУ), которые не соответствуют критериям более короткой схемы лечения МЛУ-ТБ. Всемирная организация здравоохранения (ВОЗ) недавно одобрила пересмотр классификации новых противотуберкулезных препаратов на основе имеющихся данных по каждому препарату. В предыдущих руководствах ВОЗ выбор препаратов основывался на эффективности и токсичности постепенно, от препаратов первого ряда группы 1 и препаратов второго ряда групп 2–5 до препаратов группы 5 с потенциально ограниченной эффективностью или ограниченной эффективностью. клинические данные.В пересмотренной классификации ВОЗ, направленной исключительно на ведение случаев лекарственной устойчивости, лекарства снова перечислены в иерархическом порядке от группы A до группы D. Параллельно независимо предлагается возможная будущая классификация. Цель данной статьи — описать эволюцию классификации ВОЗ по туберкулезу (с учетом независимо предложенной новой классификации) и недавние изменения в рекомендациях ВОЗ, а также прокомментировать различия между ними. Также обсуждаются последние данные о препаратах бывшей группы 5.
Ключевые слова
Противотуберкулезные препараты
МЛУ / ШЛУ-ТБ
Фторхинолоны
Линезолид
Бедаквилин
Деламанид;
Рекомендуемые статьиЦитирующие статьи (0)
© 2016 Автор (ы). Опубликовано Elsevier Ltd от имени Международного общества инфекционных болезней.
Рекомендуемые статьи
Ссылки на статьи
(PDF) ВВЕДЕНИЕ ТУБЕРКУЛЕЗНОЙ БОЛЕЗНИ И КЛАССИФИКАЦИЯ ПРОТИВОТУБЕРКУЛЕЗНЫХ ПРЕПАРАТОВ
www.wjpps.com Vol 8, Issue 4, 2019.
651
Vicky et al. World Journal of Pharmacy and Pharmaceutical Sciences
9. Ибрагим Абубакар, 1 Хелен Рут Стэгг, 1 Хилари Уитворт, 2 и Аджит Лалвани, Как следует интерпретировать результат анализа высвобождения гамма-интерферона при туберкулезной инфекции, грудная клетка,
2013.
10. Джованни Сотджиу, 1 Розелла Сентис, 2 Лия Д’амброзио, 2 и Джованни Баттиста Мильори2
Лечение туберкулеза и лекарственные препараты, Cold Spring Harb Perspect Med., 2015
Май.
11. Мохаммад Асиф, Обзор мощного противотуберкулезного агента Изониазид и его
аналогов, Международный журнал фармацевтической химии, 19 ноября 2015 г.
12. Джастин Т. Денхолм1,2 и Эмма С. Макбрайд1, Использование противотуберкулезных средств терапия для
латентной туберкулезной инфекции, Infect Drug Resist, 2010; 3: 63–72.
13. Вероник Дартуа, Путь противотуберкулезных препаратов: от крови к очагам поражения до
микобактериальных клеток, Nat Rev Microbiol, март, 2014 г .; 12 (3): 159–167.
14. Сусмита Саркар, Адвайта Гангули и Хун Х. Суну, Текущий обзор противотуберкулезных препаратов
: метаболизм и токсичность, микобактериальные заболевания, 2016.
15. С. Тибери a, b, M. Mu˜noz- Torricoc, R. Duarted, M. Dalcolmoe, L. D’Ambrosiof, g, G.-B.
Migliori g, Новые препараты и перспективы новых схем противотуберкулеза,
Pulmonology, 2018.
16. Хосе А. Каминеро, Анна Скардигли Классификация противотуберкулезных препаратов: новое предложение
, основанное на самых последних данных. Европейский респираторный журнал 2015.
17. Симон Тибери a, Анна Скардигли b, Розелла Сентис c, Лия Д’Амброзио c, d, Марсела
Муньос-Торрико e, Мигель Ангель Салазар-Лезама e, Классификация новых противотуберкулезных препаратов
препараты: обоснование и перспективы на будущее, Международный журнал инфекционных заболеваний,
2017; 56: 181–184.
18. Хуан Карлос Паломино * и Ананди Мартин, Механизмы лекарственной устойчивости в
Mycobacterium tuberculosis, Антибиотики, 2014; 3: 317-340.
19. Маркос Абдо Арбекс, Марилия де Кастро Лима Варелла, Элио Рибейру де Сикейра,
Фернандо Аугусто Фиуса де Мелло, Противотуберкулезные препараты: лекарственные взаимодействия, побочные эффекты
и использование в особых ситуациях. Часть 1: Препараты первого ряда, J Bras Pneumol, 2010; 36 (5):
626-640.
20. Обзор лекарственных средств изониазида, публикация Содхганга.
21. Unissa AN1, Subbian S2, Hanna LE3, Сельвакумар Н., Обзор механизмов действия и устойчивости к изониазиду
у Mycobacterium tuberculosis, Infect Genet Evol, ноябрь
2016; 45: 474-492.
% PDF-1.7
%
7440 0 объект
>
эндобджxref
7440 89
0000000016 00000 н.
0000007062 00000 н.
0000007465 00000 н.
0000007502 00000 н.
0000007588 00000 н.
0000007665 00000 н.
0000007698 00000 н.
0000007799 00000 н.
0000007828 00000 н.
0000008064 00000 н.
0000008853 00000 н.
0000009002 00000 н.
0000009041 00000 н.
0000009090 00000 н.
0000009139 00000 п.
0000009288 00000 п.
0000009401 00000 п.
0000009516 00000 н.
0000009615 00000 н.
0000009741 00000 н.
0000009856 00000 н.
0000009981 00000 н.
0000010108 00000 п.
0000010236 00000 п.
0000010335 00000 п.
0000012510 00000 п.
0000014491 00000 п.
0000016499 00000 п.
0000018571 00000 п.
0000020792 00000 п.
0000022949 00000 п.
0000023325 00000 п.
0000023673 00000 п.
0000025701 00000 п.
0000025945 00000 п.
0000026172 00000 п.
0000027973 00000 п.
0000028097 00000 п.
0000028246 00000 п.
0000028370 00000 п.
0000028519 00000 п.
0000028907 00000 п.
0000029138 00000 н.
0000029252 00000 п.
0000029640 00000 п.
0000032135 00000 п.
0000032191 00000 п.
0000032579 00000 п.
0000032632 00000 п.
0000035282 00000 п.
0000035670 00000 п.
0000035789 00000 п.
0000035938 00000 п.
0000046137 00000 п.
0000046178 00000 п.
0000046255 00000 п.
0000046736 00000 п.
0000046813 00000 п.
0000047257 00000 п.
0000047334 00000 п.
0000047821 00000 п.
0000047898 00000 п.
0000047930 00000 п.
0000048007 00000 п.
0000049808 00000 п.
0000050136 00000 п.
0000050205 00000 п.
0000050323 00000 п.
0000052124 00000 п.
0000055622 00000 п.
0000056001 00000 п.
0000056078 00000 п.
0000056492 00000 п.
0000056569 00000 п.
0000056834 00000 п.
0000056884 00000 п.
0000056916 00000 п.
0000056993 00000 п.
0000059087 00000 п.
0000059410 00000 п.
0000059479 00000 п.
0000059597 00000 п.
0000061691 00000 п.
0000072176 00000 п.
0000072534 00000 п.
0000072611 00000 п.
0000342199 00000 п.
0000006765 00000 н.
0000002117 00000 н.
трейлер
] / Назад 1538549 / XRefStm 6765 >>
startxref
0
%% EOF7528 0 объект
> поток
hYy \ S? & 4! @ «* Pi @ Vp4jDq \ m / An @ +} * Ԫ`
Q [VgʢU [soN ٿ {Результаты национальных и международных лабораторий
Предпосылки .Чтобы вылечить лекарственно-устойчивый (ЛУ) туберкулез (ТБ), противотуберкулезное лечение должно проводиться в соответствии с тестом на лекарственную чувствительность (ТЛЧ) Mycobacterium tuberculosis . В этом исследовании мы сравнили традиционное ТЛЧ, проводимое в Минске, Беларусь, стране с высоким бременем лекарственной устойчивости, с обширным гено- и фенотипическим анализом, проведенным в наднациональной справочной лаборатории ВОЗ по борьбе с туберкулезом в Копенгагене, Дания, для пациентов с коинфекцией ТБ / ВИЧ. Впоследствии результаты ТЛЧ были связаны со схемой лечения и исходом. Методы . Было включено 30 пациентов с коинфекцией ТБ / ВИЧ из Минска, и была применена описательная статистика. Результатов . По данным Минска, 10 (33%) больных ТБ / ВИЧ имели лекарственно-чувствительный ТБ. Двое (7%) имели ТБ с монорезистентным к изониазиду, 8 (27%) имели ТБ с множественной лекарственной устойчивостью (МЛУ), 5 (17%) ТБ с преэкстенсивной лекарственной устойчивостью (preXDR) и 5 (17%) имели широкую лекарственную устойчивость ( ШЛУ) ТБ. В отношении препаратов первой линии рифампицин и изониазид между Минском и Копенгагеном было подписано соглашение о ТЛЧ для 90% пациентов.По противотуберкулезным препаратам второго ряда расхождения были более выраженными. У 14 (47%) пациентов возникли разногласия по крайней мере по одному препарату, а 4 (13%) пациента были классифицированы как больные МЛУ-ТБ в Минске, но были классифицированы как имеющие пре-ШЛУ-ТБ на основании результатов ТЛЧ в Копенгагене. Первоначально все пациенты получали стандартное противотуберкулезное лечение рифампицином, изониазидом, пиразинамидом и этамбутолом. Однако это подходило только для 40% пациентов на основе ТЛЧ. В среднем, пациенты с лекарственно-устойчивым туберкулезом были переведены на 4 (IQR 3-5) активных препарата через 1 год.5 месяцев (1-2 IQR). После корректировки лечения продолжительность лечения составила 8 месяцев (IQR 2-11). Четыре (22%) пациента с лекарственно-устойчивым туберкулезом получали лечение более 18 месяцев. Всего за 24 месяца наблюдения умерли шестнадцать (53%) пациентов. Выводы . Мы обнаружили высокую согласованность результатов ТЛЧ к рифампицину и изониазиду в лабораториях Минска и Копенгагена, тогда как расхождения для препаратов второго ряда были более выраженными. Для пациентов с лекарственно-устойчивым туберкулезом лечение часто было недостаточным, и соответствующие корректировки откладывались.Этот пример из Минска, Беларусь, подчеркивает два важных момента в ведении ЛУ-ТБ: срочную необходимость внедрения быстрых молекулярных ТЛЧ и наличие препаратов второго ряда во всех странах с тяжелым бременем ЛУ-ТБ. Тщательно разработанные индивидуальные схемы лечения в соответствии с схемами ТЛЧ, вероятно, улучшат исход болезни для пациентов и уменьшат передачу лекарственно-устойчивых штаммов Mycobacterium tuberculosis .
1. Введение
Туберкулез (ТБ) продолжает оставаться серьезной угрозой для здоровья населения, особенно из-за лекарственно-устойчивого ТБ (ЛУ-ТБ) [1].Особую озабоченность вызывает рост заболеваемости ВИЧ-ассоциированным ТБ и ТБ с множественной лекарственной устойчивостью (МЛУ-ТБ) в Восточной Европе. В этом регионе уровень заболеваемости МЛУ-ТБ является одним из самых высоких в мире: от 12-40% среди новых случаев ТБ до 30-70% среди ранее пролеченных [1, 2]. В Беларуси одни из самых высоких показателей МЛУ-ТБ в регионе (около 40% и 70% среди новых и ранее леченных пациентов, соответственно) [1, 3]. В то время как первое является индикатором плохого инфекционного контроля и продолжающейся передачи Mycobacterium tuberculosis ( Mtb ), второе указывает на ненадлежащее ведение, когда во время лечения развивается новая или дополнительная резистентность.
В Восточной Европе ВИЧ-инфицированное население особенно уязвимо для заражения туберкулезом из-за пересечения групп риска и, как правило, более высокого риска заболевания туберкулезом из-за более выраженного иммунодефицита. В результате распространенность коинфекции Mtb и ВИЧ в этом регионе увеличивается [1, 4, 5].
Диагностика ТБ и определение паттернов лекарственной чувствительности с использованием обычных фенотипических методов на основе посевов (т. Е. Посев на твердой или жидкой среде) может занять много времени (до нескольких месяцев), что может помешать своевременному началу активного лечения.Это особенно проблематично в условиях высокой распространенности МЛУ-ТБ. Доступ к экспресс-тестам на генотипную лекарственную чувствительность (ТЛЧ) на основе ДНК может позволить быструю корректировку терапии в соответствии с моделями резистентности, потенциально помогая улучшить клинические исходы и уменьшить количество осложнений для отдельных пациентов, а также помочь уменьшить передачу с резистентным Mtb напрягает в обществе.
Исход лечения пациентов с ТБ / ВИЧ в Восточной Европе, особенно с МЛУ-ТБ, оставляет желать лучшего, при этом годовой уровень смертности составляет примерно 30% и выше [6, 7].Ведение МЛУ-ТБ, особенно в контексте ВИЧ-инфекции, может быть сложным. Крайне важно как можно быстрее разработать индивидуальные схемы приема лекарств, основанные на конкретных моделях восприимчивости Mtb . В ситуациях, когда модели восприимчивости недоступны и пациенты лечатся эмпирически, существует высокий риск неоптимальных схем лечения с ограниченным количеством активных препаратов, что может привести к лекарственной устойчивости [8].
В этом исследовании мы изучали ведение пациентов с ТБ / ВИЧ, сравнивая результаты ТЛЧ, полученные от Республиканского научно-практического центра пульмонологии и туберкулеза, Минск, Беларусь (Минск), и Наднациональной справочной лаборатории ВОЗ по борьбе с туберкулезом (Копенгаген) в Копенгагене. , Дания.Затем мы стремились оценить адекватность используемых схем лечения и выживаемость пациентов в соответствии с паттернами ТЛЧ. Кроме того, мы сравниваем результаты фенотипического ТЛЧ с результатами быстрого генотипического ТЛЧ на основе ДНК и результатов полногеномного секвенирования (WGS) и описываем геномную эпидемиологию вовлеченных штаммов Mtb .
2. Методы
В рамках международного проспективного когортного исследования ТБ: ВИЧ (https://www.chip.dk), последовательные ВИЧ-положительные пациенты из Минска с диагнозом ТБ в период с 01.01.2011 по 31.12. / 2013 [9].Демографические и клинические данные были собраны в стандартных формах истории болезни на дату постановки диагноза ТБ (исходный уровень), а также через 6, 12 и 24 месяца после этого. Была собрана конкретная информация о лечении туберкулеза, а также результаты проведенных на местном уровне ТЛЧ для Mtb . За участниками наблюдали в течение двух лет после постановки диагноза ТБ, даты смерти или потери для последующего наблюдения. Этическое одобрение было получено в соответствии с местными правилами и законодательством.
2.1. Лабораторные методы
Для противотуберкулезных препаратов первого ряда в Минске использовались стандартные фенотипические методы анализа на твердой среде Левенштейна-Йенсена (LJ) и жидкой пробирке с индикатором роста микобактерий (MGIT) в период с 2011 по 2013 год.Для препаратов второго ряда ТЛЧ проводилось как фенотипически на MGIT, так и для некоторых пациентов генотипически с помощью GenoType MTBDR sl (Hain Lifescience, Нерен, Германия) (ограниченная доступность в 2011-2015 годах).
Культуры Mtb на твердой среде LJ хранились на месте и впоследствии отправлялись в SRL в соответствии с международными правилами перевозки материалов класса III (материал категории A в соответствии с Правилами перевозки опасных грузов IATA, https: // www. iata.org / en / programs / cargo / dgr /) для фенотипического и генотипического ТЛЧ. В Копенгагене все штаммы были субкультивированы в Dubos перед проведением ТЛЧ. Первоначально фенотипическое ТЛЧ проводилось для четырех препаратов первого ряда: изониазида (H), рифампицина (R), этамбутола (E) и пиразинамида (Z). Только в случае какой-либо устойчивости к препаратам первого ряда проводилось ТЛЧ к препаратам второго ряда. К ним относятся аминогликозиды (стрептомицин (S), амикацин (Am), канамицин (Km) и капреомицин (Cm)), фторхинолоны (моксифлоксацин (Mfx), офлоксацин (Ofx)), этионамид (Eto) и линезолид (Lzd).Фенотипическое ТЛЧ проводилось на MGIT 960, и все препараты были предоставлены производителем. Набор MGIT 960 SIRE (Becton Dickinson) содержал лиофилизированные флаконы с низкой (критической) и высокой концентрацией для препаратов первого ряда. Для препаратов 2-го ряда использовались рекомендуемые критические концентрации [10]. Система сообщала о результатах как о чувствительных или устойчивых. Когда был получен результат «стойкий», флакон проверяли на чистоту и проверяли повторным тестированием.
Генотипическое ТЛЧ проводилось с использованием анализа с использованием линейного зонда (LPA) GenoType MTBDR plus и sl (Hain Lifescience, Нерен, Германия), в последнем случае, если была обнаружена фенотипическая устойчивость к препаратам первого ряда или если субкультура не смогла расти.Анализ и интерпретация результатов проводились в соответствии с инструкциями производителя (https://www.hain-lifescience.de/en/). Среди препаратов первого ряда устойчивость к изониазиду и рифампицину определялась путем обнаружения мутаций в генах inhA / katG и в гене rpoB штаммов Mtb соответственно. Среди препаратов второго ряда устойчивость к фторхинолонам определялась мутациями в генах gyrA и gyrB; а устойчивость к аминогликозидам определяли путем выявления мутаций в генах rrs и eis [11].
Полногеномное секвенирование (WGS) было выполнено для всех образцов культуры Mtb , как описано ранее [12]. Полученные файлы FastQ были загружены в PhyResSe, поисковую систему по устойчивости к фило, используемую для поиска мутаций, вызывающих устойчивость (https://bioinf.fz-borstel.de/mchips/phyresse/) [13].
В дополнение к мутациям, перечисленным выше, WGS разрешил дополнительное тестирование генотипической чувствительности для следующих препаратов: этамбутол (путем обнаружения мутаций в гене embB), пиразинамид (мутации в генах pncA и rpsA), стрептомицин (мутации в rpsL ген), этионамид (мутации в генах mshA и ethA), линезолид (мутации в гене rplC) и пара-аминосалициловая кислота (PAS) (мутация в thyA).Были включены все штаммы с символом a. Последовательности депонированы в Европейском нуклеотидном архиве под регистрационным номером проекта PRJEB38234.
2.2. Статистика и определения исследований
пациентов с ТБ / ВИЧ из Минска () были стратифицированы в соответствии с доступностью образцов культур Mtb , а описательная статистика использовалась для сравнения исходных демографических и клинических характеристик. Кроме того, группа с доступными образцами Mtb () была подробно охарактеризована в соответствии со схемами устойчивости и лечения (Рисунок 1).Результаты ТЛЧ, полученные в Минске, сравнивались с фенотипическими ТЛЧ, LPA и WGS, проведенными в Копенгагене.
Пациенты были сгруппированы в соответствии со следующими моделями устойчивости: лекарственно-чувствительный (ЛУ) ТБ, МЛУ-ТБ, пре-ШЛУ-ТБ и ШЛУ-ТБ (таблица 1). В Копенгагене Mtb в образцах считались устойчивыми, если устойчивость была обнаружена в любом из анализов (фенотипических, LPA или WGS). Конкретные схемы лечения были проанализированы для каждого пациента и включали начальное противотуберкулезное лечение и любые последующие изменения.
Терминология устойчивости Определение Лекарственно-чувствительный ТБ (DS-TB) противотуберкулезные препараты первой линии Монорезистентный ТБ Mtb , устойчивый только к одному противотуберкулезному препарату первого ряда Лекарственно-устойчивый ТБ (ЛУ-ТБ) По крайней мере, МЛУ-ТБ, комбинированная терминология для любого из перечисленных ниже Определения ТБ с множественной лекарственной устойчивостью (МЛУ-ТБ) Mtb , устойчивый как минимум к изониазиду и рифампицину ТБ с предэкстенсивной лекарственной устойчивостью (preXDR-TB) Mtb и устойчивый к изониазиду рифампицин и любой фторхинолон или , инъекционное средство второй линии, но не оба одновременно ТБ с широкой лекарственной устойчивостью (ШЛУ-ТБ) Mtb , устойчивый к изониазиду и рифампицину и к любому фторхинолону и по крайней мере к одному из трех инъекционных препаратов второго ряда (капреомицин, канамицин и амикацин) 74 03 Mycobacterium tuberculosis.
3. Результаты
Всего в исследование было включено 62 пациента из Минска. Из них 55 (89%) имели положительный результат посева на Mtb . Образцы от 30 пациентов (55% всех положительных результатов посева) хранились на месте и отправлялись в Копенгаген (рис. 1). В таблице 2 представлены исходные клинические и демографические характеристики пациентов с / без образцов культуры Mtb и показано, что эти две группы сопоставимы. Большинство пациентов в обеих группах составляли молодые мужчины с историей употребления инъекционных наркотиков (ПИН), тюремного заключения и / или чрезмерного употребления алкоголя.Несмотря на то, что большинству пациентов был поставлен диагноз ВИЧ-инфекция за несколько лет до постановки диагноза ТБ, лишь небольшая часть пациентов получала антиретровирусную терапию (АРТ) на момент постановки диагноза ТБ, и у большинства было низкое количество клеток CD4 (Таблица 2).
Итого Образец да, (%) Номер образца, (%) 30 Пол Мужской, (%) 22 (73) 28 (88) 0.( %) 19 (63) 24 (75) 0,319 История заключения, (%) 5 (17) 12 (38) 0,090 История превышения потребление алкоголя, (%) 19 (63) 15 (47) 0.213 Mtb положительный результат посева Да, (%) 30 (100) 25 (78) 0,0015 МЛУ-ТБ Да, (%) 18 (%) 18 ( 60) 16 (50) 0,456 ТБ Распространенный, (%) 12 (40) 6 (19) 0,060 Гепатит С %)
24 (80) 23 (72) 0.454 Продолжительность ВИЧ до ТБ Месяцы, медиана (IQR) 88 (44-136) 67 (25-120) 0,535 Исходная антиретровирусная терапия Да, ( %) 15 (50) 14 (44) 0,622 Число CD4 клеток / мм 3 , медиана (IQR) 85 (22-171) 126 (57- 310) 0,097 Сокращения: исходный уровень = дата диагноза ТБ; IQR = межквартильный размах; = число; МЛУ-ТБ = ТБ с множественной лекарственной устойчивостью; Mtb = Mycobacterium tuberculosis ; ТБ = туберкулез; Положительные антитела к гепатиту С. В Копенгагене 7 из 30 образцов (23%) не смогли вырасти. Для образцов, полностью чувствительных на основе фенотипического ТЛЧ, генотипическое ТЛЧ не проводилось, за исключением WGS, который проводился для всех образцов, но не удался для 8 (27%). Для образцов, в которых была обнаружена фенотипическая устойчивость или не было роста культуры, был проведен анализ LPA (блок-схема).
3.1. Образцы тестов на лекарственную чувствительность
Результаты ТЛЧ
, предоставленные Минском и Копенгагеном, представлены в таблицах 3 и 4.Были доступны результаты ТЛЧ ко всем четырем препаратам первого ряда из Минска, за исключением 11 случаев, когда не было зарегистрировано ТЛЧ к пиразинамиду. ТЛЧ к препаратам второго ряда в Минске включало аминогликозиды (S, Amk / Km и Cm), фторхинолоны (Ofx, Lfx), Eto / Pto, Cs и PAS. ТЛЧ для Mfx и Lzd не проводились в Минске в течение периода исследования, тогда как ТЛЧ для Lfx, Cs и PAS не проводились в Копенгагене (Таблица 3).
PID Место анализа Изониазид Рифампицин этамбутол пиразинамид стрептомицин Амикацин канамицин Капреомицин Moxifloxacin Офлоксацин Левофлоксацин E- / протионамид Линезолид Циклосерин p- Амино-салициловая кислота Линия ТБ 1 Минск S S S S S S 68 68
68 S
68 S S
Копенгаген Pheno S S S S 74 74 74 74 74 74 74 WGS S S S S S S S S S 74
74
2 Минск S S S R S S S R S S Pheno S S S S 911 74 LPA S S S S S EAS 3 Минск S S S S S Копенгаген Pheno S S S 74 74 74 74 74 74 74 74 74 74 74 74 LPA 91 174 WGS S S S S S S S S 74 4 Минск S S S S S S S S S Pheno S S S S LPA 74 74 74 74 74 74 74 74 74 74 74 WGS S S S S S 9106 8 S
S S S S Пекин 5 Минск S S S S S S S S S S Копенгаген Pheno S S 68 S
68
LPA S S S S EAS 6 Минск S S S S S1174 Копенгаген LPA S
S S S S S S EAS 7 Минск S S S S S S S 910 68 S S Копенгаген Pheno S S S S 74 WGS S S S S S S 68
68
Урал 8 Минск S S S S R S S S S
S Копенгаген Pheno Неудачный LPA S S S S S Не удалось S1174 9 Минск S S S Копенгаген Pheno Неудачный 74
S S S S S WGS Ошибка Минск
S S S S S S S S S Копенгаген S
LPA S S S S S S S EAS Монорезистентный TB S S S S S S S S S S S Copen S S S S S S S S S S 68 LPA S
S S S S 9117 4 WGS R S S S S S S S S S Минск
Минск
R S S S S S S S S S S S S S S LPA 74 74 74 WGS R S S S S S S S S S LAM ТБ с множественной лекарственной устойчивостью 74 74 74 13 Минск R R S S S S S
S LPA S S S S S S S S EAS 14 Минск R R S S Копенгаген Pheno S S S S 74 74 74 74 74 Н / Д WGS Отказ 74 74 74 74 74 74 74 74 R R R R R 9 1068 S
S S S S S S Копенгаген Pheno R R R S S S S R S LPA R R 74
911 S WGS R R R R R S S 68
68 S
68 S
68 S
Пекин 16 Минск R R R R S S S S S R R Копенгаген Pheno R R R 68 R
68 R
68 R
68
LPA R R S S S S S 74
74
74
74 74
74
74
74
74
74 R R S R S S S S S LAM 73
Минск
R R R S S S S S S S S Копенгаген Pheno Неудачный LP1174
LP
S S S S WGS Неудачный 74 74 74 74 74 74 74 74 R R R R R S S S S S S R R S S R S R S S S R S LPA R R 68
68
S
WGS R R R S R S S Пекин
19 Минск R R R R S S S S S
Копенгаген Pheno R R R R R S S S S S R S LPA R R R R WGS R R R R R S S S S S 74
911 Минск R R R R R S S S S S S Pheno R R R R R S R S S S R S LPA R R R R R S WGS R R R R R S S S S S 68 L
TBree TBree лекарственно устойчивый
21 Минск R R S S S R R Копенгаген 910 68 Pheno
R R S R R R R R S S S S LP
LP
LP
R
R R R R S S WGS Неудачный 22 Минск R R S R R R S S Копенгаген Pheno Не удалось 9117 4 LPA R R R R R S S 23 Минск R R R R 68
68
68
68 R
68
R R Копенгаген Pheno Отказ LP
LP
R R S S WGS Неудачный 24 Минск1068
Минск R S S R S R Копенгаген Pheno Неудачный 74 74 74 74 74 74 74 74 LPA R R R R R S S WG
R R S S S S 9106 8 S
LAM 25 Минск R R R R R S S S R Копенгаген Pheno R R R R R 910 S S S LPA R R S S S R 74
74
74 74 74 74 74 74 74 74 74 74 74 WGS
R R R R R S S S R R Пекин Туберкулез с широкой лекарственной устойчивостью Минск R
S R R R R R S S S S R R R R S S S S LPA 68
68
68 LPA
68 R R
R S S WGS 910 73 R R R S R R R R S S Пекин R R R R R R R R S S S R
R R R R R S R R R S LP
LP
LP
R R R R R WGS R 91 068 R
R R S R R R R R Пекин Минск
R R R S R S R R R S S 74 LPA R R R R R R R WGS Неудачный 91 174 29 Минск R R R R R R R R 68 S
68 S
68 S Копенгаген
Pheno R R R R R R R S R R R LP
LP
R R R R R R R 73
S R R R R R Пекин 30 91 073 Минск R R R R R R R R R S 73
S Pheno R R R R R R R R R R R R R R LP R
R R R R R R WGS RGS R R R R R R Пекин 9114 1
Сокращения: PID = идентификационный номер пациента.ТЛЧ = тестирование лекарственной чувствительности. LPA = анализ линейного зонда. Фен = фенотипическая устойчивость. R = стойкий. S = чувствительный. WGS = полногеномное секвенирование. Генотипическую устойчивость определяли путем обнаружения мутаций в генах inhA / katG для изониазида, в гене rpoB для рифампицина, в гене embB для этамбутола и в гене pncA для пиразинамида. Устойчивость к препаратам второго ряда определялась для класса препаратов путем обнаружения следующих мутаций: аминогликозиды (амикацин, капреомицин и канамицин) в генах rrs и eis; стрептомицин в гене rpsL; фторхинолоны (моксифлоксацин, левофлоксацин и офлоксацин) в генах gyrA и gyrB.EAS = евро-американская суперлиния, LAM = латиноамериканско-средиземноморская линия. В Минске ТЛЧ проводилось в Республиканском научно-практическом центре пульмонологии и туберкулеза, Минск, Беларусь. В Копенгагене ТЛЧ проводилась в наднациональной справочной лаборатории ВОЗ по борьбе с туберкулезом, Копенгаген, Дания. Лекарственно-чувствительный ТБ = Mtb , чувствительный ко всем противотуберкулезным препаратам первого ряда. Монорезистентный ТБ = Mtb устойчив только к одному противотуберкулезному препарату первого ряда. ТБ с множественной лекарственной устойчивостью = Mtb , устойчивый как минимум к изониазиду и рифампицину.Преэкстенсивная лекарственная устойчивость = Mtb устойчивость к изониазиду и рифампицину и либо к любому фторхинолону, либо к инъекционным препаратам второго ряда, но не к обоим. Обширная лекарственная устойчивость = Mtb устойчивы к изониазиду и рифампицину, а также к любому фторхинолону и по крайней мере к одному из трех инъекционных препаратов второго ряда.
Тип туберкулеза Минск
(%)Копенгаген
(%)значение число активных препаратов Количество активных препаратов после 1-го изменения схемы лечения, медиана (диапазон) RSPCPT SRL RSPCPT SRL DS TB 73 10 (3310,310) 12 (40.0)
0,79 4 (4-4) 4 (4-4) 2 (2-3) 2 (2-3) ТБ, устойчивый к изониазиду 2 (6,7 ) 2 (6,6) 1,00 4 (3-4) 4 (3-4) 5 (4-5) 5 (4-5) МЛУ-ТБ 8 (26,7) 3 (10,0) 0,18 0 (0-5) 0 (0-0) 5 (1-5) 4 (1-5) preXDR-TB 5 (16.7) 9 (30,0) 0,36 1 (0-1) 1 (0-1) 4 (1-5) 3 (1-4) XDR-TB 5 (16,7) 4 (13,3) 1,00 0 (0-1) 0 (0-1) 3 (2-3) 3 (1-4) В Минске тестирование лекарственной чувствительности (ТЛЧ) проводилось в Республиканском научно-практическом центре пульмонологии и туберкулеза, Минск, Беларусь.В Копенгагене ТЛЧ проводилась в наднациональной справочной лаборатории ВОЗ по борьбе с туберкулезом, Копенгаген, Дания. ТЛЧ = тест на лекарственную чувствительность. ЛУ-ТБ = лекарственно-чувствительный ТБ; Mycobacterium tuberculosis , чувствительная ко всем противотуберкулезным препаратам первого ряда. МЛУ-ТБ = ТБ с множественной лекарственной устойчивостью; Mycobacterium tuberculosis , устойчивая как к изониазиду, так и к рифампицину. preXDR-TB = преэкстенсивный ТБ с лекарственной устойчивостью; Mycobacterium tuberculosis, устойчивая к изониазиду и рифампицину, а также к любому фторхинолону или инъекционным препаратам второго ряда, но не к обоим.ШЛУ-ТБ = обширная лекарственная устойчивость; Mycobacterium tuberculosis , устойчивая к изониазиду и рифампицину, а также к любому фторхинолону и по крайней мере к одному из трех инъекционных препаратов второго ряда. Как сообщается. По результатам комбинированного фенотипического ТЛЧ, линейного зондового анализа (LPA) и полногеномного секвенирования (WGS). В случае расхождений считался худший результат. Хорошее согласие между двумя лабораториями наблюдалось при сравнении результатов фенотипического ТЛЧ к препаратам первого ряда (таблицы 3 и 4): 18 из 23 случаев с доступными результатами были идентичными (78%).У двух пациентов (PID 13 и 14) был обнаружен МЛУ-ТБ в Минске, но у одного пациента (PID 26) были обнаружены расхождения в фенотипических тестах на рифампицин: резистентный в Минске и чувствительный в Копенгагене. Другой пациент (PID 18) был инфицирован Mtb , устойчивым к этамбутолу и пиразинамиду в Минске и чувствительным в Копенгагене, а PID 15 имел Mtb , устойчивых к этамбутолу в Минске и чувствительных в Копенгагене (Таблица 3).
Среди фенотипических ТЛЧ к препаратам второго ряда расхождения были замечены для 7 из 11 образцов Mtb , из которых Mtb были чувствительны к этим препаратам в Минске, но устойчивы в Копенгагене.Несколько других незначительных расхождений наблюдались в ТЛЧ к аминогликозидам (таблица 3).
Согласно паттернам восприимчивости, полученным из Минска, штаммов Mtb от 10 (33,3%) пациентов были классифицированы как полностью лекарственно-устойчивый туберкулез; 2 (6,7%) — монорезистентный к изониазиду; 8 (26,7%) — МЛУ-ТБ; 5 (16,7%) как пре-ШЛУ-ТБ и 5 (16,7%) как ШЛУ-ТБ (таблица 4). В Копенгагене лекарственно-устойчивый туберкулез был диагностирован у 12 пациентов (40,0%).
При сравнении результатов лабораторий Минска и Копенгагена для пациентов с лекарственно-устойчивым туберкулезом, МЛУ-ТБ был обнаружен у 8 из 30 (26.7%) против 3 из 30 (10,0%),; preXDR-TB был обнаружен у 5 из 30 (16,7%) против 8 из 30 (30,0%); и ШЛУ-ТБ был обнаружен у 5 из 30 (16,7%) против 7 из 30 (13,3%), соответственно (таблица 4).
3.2. Схемы лечения ТБ и выживаемость
Схемы противотуберкулезного лечения для каждого пациента представлены на Рисунке 2. Двадцать восемь (93%) пациентов начали лечение по стандартной схеме из четырех препаратов первой линии (RHZE), и из них: четыре (14%) добавляли стрептомицин. Все пациенты с лекарственно-устойчивым туберкулезом, согласно результатам Минска (), получали стандартные противотуберкулезные препараты первого ряда, но в течение различной продолжительности, включая длительные интенсивные фазы лечения (рис. 2).Средняя продолжительность лечения лекарственного туберкулеза составила 9,5 месяцев (IQR 7,3–10,0 месяцев). Три пациента с лекарственно-устойчивым туберкулезом умерли: один в течение первого месяца лечения, когда туберкулез был указан как причина смерти, и двое из-за причин, не связанных с туберкулезом, после завершения противотуберкулезного лечения.
Среди двух пациентов с монорезистентным к изониазиду туберкулезом 1 умер от туберкулеза через 3 дня после начала режима RHZES.
Пациенты с как минимум МЛУ-ТБ () по данным Минска перешли с начального лечения первой линии на терапию второй линии в среднем через 1 месяц (IQR 1-2 месяца).Схемы второго ряда были стандартизированы и включали один фторхинолон (Ofx или Lfx), один аминогликозид (в основном Cm и, реже, Am), Cs, Eto и PAS. Пиразинамид также широко использовался в схемах второго ряда, несмотря на сообщения о резистентности. Схемы второго ряда содержали в среднем 6 препаратов. Однако среднее количество активных лекарств составляло 4 (IQR 3-5) согласно национальным результатам ТЛЧ и 3 (IQR 2-4) согласно результатам ТЛЧ, полученным в Копенгагене. После первой корректировки лечения 8 пациентов по Минску и 10 пациентов по результатам ТЛЧ Копенгагена получили 3 или менее активных препарата.Дальнейшие переключения лечения были направлены либо на замену лекарств в пределах того же класса лекарств (например, Ofx на Lfx), либо на сокращение количества лекарств (также сокращение количества активных лекарств) (Рисунок 2). Средняя продолжительность лечения препаратами второго ряда для пациентов с как минимум МЛУ-ТБ составляла 12 месяцев (IQR 10–21). Двенадцать пациентов (67%) как минимум с МЛУ-ТБ умерли в течение 24 месяцев после начала лечения: 8 (67%) из-за ТБ и 4 (33%) по каким-либо другим причинам (Рисунок 2). Для тех, кто был жив в 24 месяца (), продолжительность лечения составляла от 10 до 26 месяцев.
3.3. Линии
Половина успешно генотипированных штаммов принадлежала к линии 2 (Пекин) (), из них 7 (63%) имели как минимум МЛУ-ТБ и 7 умерли. Среди людей другого происхождения 4 (36%) имели как минимум МЛУ-ТБ и 5 (45%) умерли. Небольшое количество не позволило провести дальнейший анализ.
4. Обсуждение
Сравнивая ТЛЧ Mtb между национальной лабораторией в Минске, учреждением с высокой распространенностью МЛУ-ТБ со средним уровнем дохода и наднациональной референс-лабораторией ВОЗ по борьбе с туберкулезом в Копенгагене, мы обнаружили хороший уровень соответствия для первого противотуберкулезные препараты ряда, тогда как были некоторые разногласия по препаратам второго ряда.Кроме того, было выявлено несколько проблем в ведении пациентов с ТБ / ВИЧ в Минске, в частности, в ведении пациентов с лекарственно-устойчивым туберкулезом. В Копенгагене проверка качества ТЛЧ Mtb из Минска включала как фенотипические, так и генотипические тесты, а именно LPA и WGS. В целом, ТЛЧ, проведенное в Минске, было надежным, а результаты фенотипических ТЛЧ к препаратам первого ряда для пациентов с лекарственно-устойчивым туберкулезом были почти идентичны в двух лабораториях, за исключением двух пациентов, у которых был зарегистрирован местный МЛУ-ТБ, но DS- ТБ в Копенгагене.Для пиразинамида и этамбутола фенотипическое ТЛЧ обычно является сложной задачей, но результаты ТЛЧ для этих двух препаратов были очень последовательными и схожими между лабораториями с небольшими расхождениями [14].
Все пациенты с лекарственно-устойчивым туберкулезом лечились четырьмя препаратами первой линии в течение интенсивной фазы, а затем 2-3 препаратами в фазе продолжения, как правило, в соответствии с местными руководящими принципами, рекомендующими более длительную продолжительность лечения в случае коинфекции ВИЧ на тот момент.
На момент сбора данных фенотипический ТЛЧ к основным препаратам второго ряда (фторхинолоны и аминогликозиды) был доступен и проводился всем 30 пациентам в Минске.Хотя фенотипическое ТЛЧ к препаратам второго ряда не проводилось в Копенгагене для пациентов с лекарственно-устойчивым туберкулезом, результаты ТЛЧ в Минске очень соответствовали результатам WGS в Копенгагене. Таким образом, среди пациентов с лекарственно-устойчивым туберкулезом наблюдались расхождения в моделях резистентности к препаратам второго ряда, но они также включали расхождения между фенотипом, LPA и WGS внутри Копенгагенской лаборатории. Это несоответствие между различными методами в Копенгагене наблюдалось в первую очередь, но не исключительно, в отношении аминогликозидов.Хотя LPA и в некоторой степени WGS преимущественно включают хорошо задокументированные мутации, могут быть менее известные мутации, которые проявляются фенотипически, но еще не зафиксированы генетическим анализом. Кроме того, продолжают возникать или обнаруживаются / описываются новые мутации.
В нашем исследовании большинство пациентов с лекарственно-устойчивым туберкулезом потратили не менее одного месяца на эмпирическое лечение, содержащее RHZE, до перехода на схему второго ряда. Несмотря на доступность ТЛЧ к препаратам как первого, так и второго ряда, все пациенты с лекарственно-устойчивым туберкулезом получали стандартное лечение препаратами второго ряда, включая пациентов с (до) ШЛУ.Таким образом, лечение было неоптимальным для многих пациентов с (пред) ШЛУ-ТБ. Согласно результатам Копенгагена, пациенты с лекарственно-устойчивым туберкулезом получали меньшее количество активных препаратов. Хотя количество препаратов было достаточным для некоторых пациентов (например, 4 препарата), схемы казались слабыми по своей эффективности, и наличие ранних результатов ТЛЧ потенциально могло позволить избежать неэффективных и более токсичных препаратов [15]. Другое важное наблюдение заключается в том, что, несмотря на то, что во время лечения стали доступны схемы ТЛЧ, пациенты не были переведены на более эффективный режим.Это могло отражать снижение доступности лекарств во время исследования и, возможно, впоследствии улучшилось [16, 17]. Бедаквилин, например, не был доступен во время исследования, но теперь он есть.
На момент сбора данных рекомендованная продолжительность лечения МЛУ-ТБ составляла 18-24 месяца [18]. Среднюю продолжительность лечения МЛУ-ТБ в нашем исследовании было трудно оценить, поскольку большинство пациентов умерли во время лечения. В последнее время более короткая продолжительность лечения стала возможной только для некоторых пациентов с МЛУ-ТБ, что подчеркивает важность быстрых ТЛЧ к препаратам второго ряда для исключения (пред) ШЛУ-ТБ [19, 20].
ТЛЧ играет важную роль в ведении больных туберкулезом в условиях высокой распространенности лекарственно-устойчивого туберкулеза. В идеале, ТЛЧ следует проводить до начала противотуберкулезной терапии, особенно у пациентов с ТБ в анамнезе или известных контактов с ЛУ-ТБ, чтобы направлять клиническое ведение. Использование быстрых молекулярных тестов сокращает время диагностики лекарственной устойчивости до нескольких дней и может помочь не только в назначении лечения, но и в борьбе с продолжающейся передачей туберкулеза. Это особенно важно в условиях высокой распространенности МЛУ-ТБ, где быстрое ТЛЧ к препаратам второго ряда может помочь исключить резистентность и позволить скорректировать лечение.
В некоторых случаях мы наблюдали несоответствие между фенотипическими и генотипическими паттернами устойчивости. Это явление, описанное ранее, подчеркивает необходимость использования обоих методов в настоящее время [14, 21]. Это связано с тем, что не все молекулярные механизмы устойчивости к лекарствам известны, и постоянно описываются новые гены, обеспечивающие устойчивость [12, 22, 23]. С другой стороны, в нескольких исследованиях было документально подтверждено, что некоторые клинически значимые мутации устойчивости могут быть упущены из виду при фенотипических ТЛЧ [21, 24].Таким образом, хотя быстрые молекулярные ТЛЧ для Mtb в настоящее время имеют первостепенное значение в диагностике ТБ, особенно в условиях высокой распространенности ЛУ-ТБ, фенотипическое ТЛЧ по-прежнему играет важную роль в ведении ТБ, особенно для препаратов второго ряда и новых препаратов.
Пациенты, участвовавшие в нашем исследовании, начали лечение ТБ в период с 2011 по 2013 годы. В то время в руководствах ВОЗ уже рекомендовались быстрые молекулярные ТЛЧ, такие как GeneXpert и LPA, для определения чувствительности к рифампицину и изониазиду до начала лечения [18].Однако в Минске этого пока не реализовали. В настоящее время ВОЗ рекомендует GeneXpert в качестве основного диагностического инструмента, и при обнаружении устойчивости к рифампицину следует провести LPA для препаратов второго ряда.
В последние годы стали доступны новые молекулярные методы, применимые непосредственно к первичным образцам. Например, теперь у нас есть FlouroType MTBDR (Hain Lifescience, Нерен, Германия) и Deeplex Myc-TB (GenoScreen, Лилль, Франция). Это может помочь еще больше сократить время до начала целевого индивидуального лечения [25].
Половина из штаммов Mtb , успешно генотипированных в нашем исследовании, принадлежала к сполиготипу Beijing, штамму линии 2 (11/22), что соответствует предыдущим результатам из Минска [26]. Было высказано предположение, что некоторые линии, включая линию 2, могут быть более вирулентными, чем другие [27]. Поскольку ни один из исследуемых штаммов не был идентичным, мы не обнаружили признаков недавней передачи Mtb между пациентами (данные не показаны).
Что касается ограничений исследования, размер выборки был небольшим, что привело к ограниченной статистической мощности.Однако наши данные о распространенности МЛУ-ТБ репрезентативны для Беларуси (и Минска), где распространенность МЛУ-ТБ составляет примерно 40% [1]. Кроме того, все пациенты в исследовании были инфицированы ТБ / ВИЧ; таким образом, было невозможно оценить влияние ВИЧ на передачу Mtb и развитие устойчивости. Также стоит отметить, что руководство по лечению МЛУ-ТБ в Беларуси недавно было пересмотрено, и теперь они рекомендуют пероральные схемы и избегание наиболее токсичных препаратов, особенно аминогликозидов.Кроме того, в Беларуси стали доступны новые препараты (например, линезолид, клофазимин, бедаквилин и деламанид).
Насколько нам известно, это первое исследование, дающее подробное описание противотуберкулезного лечения отдельных больных ТБ в соответствии с моделями лекарственной устойчивости Mtb . Для врачей-фтизиатров в других странах это хороший пример важности быстрых ТЛЧ и соответствия между моделями резистентности и своевременным назначением адекватного противотуберкулезного лечения. В целом, известно, что исходы у пациентов с лекарственно-устойчивым туберкулезом плохие, с вероятностью успеха примерно 50-60% [1, 5].Исследования показали, что успех лечения существенно повышается при использовании адекватных схем лечения (с точки зрения эффективности и количества эффективных лекарств) [28].
В заключение, мы обнаружили некоторые несоответствия между фенотипическими результатами ТЛЧ в Беларуси и международной справочной лабораторией в Копенгагене. Это особенно верно в отношении препаратов второго ряда, что затрудняет раннее выявление и начало индивидуального лечения пациентов с лекарственно-устойчивым туберкулезом. Наши результаты свидетельствуют о широком внедрении и валидации быстрых ТЛЧ во всех областях с высоким бременем лекарственно-устойчивого туберкулеза с одновременной широкой доступностью лекарств для лечения лекарственно-устойчивого туберкулеза.Приветствуется проведение будущих исследований для отслеживания устойчивости и схем лечения, переносимости лекарств и результатов лечения пациентов.
Доступность данных
База данных содержит личную информацию и поэтому не является общедоступной. Руководящий комитет «ТБ: ВИЧ» поощряет подачу концепций для исследовательских предложений. Концепции могут быть представлены на рассмотрение с использованием концепции онлайн-исследования (https://www.chip.dk/Studies/TBHIV/Submitresearch-concept). Концепция будет оценена Руководящим комитетом на предмет научной значимости, актуальности для ТБ: исследование ВИЧ, дизайн, осуществимость и совпадение с уже утвержденными проектами.Все предлагающие получат обратную связь. В случае утверждения будет создана рабочая группа, состоящая из лиц, предлагающих предложения, членов Руководящего комитета и сотрудников координационного и статистического центров. С исследованием TB: HIV можно ознакомиться по адресу https://www.chip.dk/Studies/TBHIV, где доступны все соответствующие документы. Для подачи заявки на исследование, пожалуйста, свяжитесь с Дарьей Подлекаревой ([email protected]) и Оле Кирком ([email protected]). Все последовательности Mycobacterium tuberculosis , полученные в рамках исследования TB: HIV, депонированы в Европейском нуклеотидном архиве под номером доступа проекта PRJEB38234.
Этическое разрешение
Исследование ВИЧ / ТБ было наблюдательным когортным исследованием, и пациенты не подвергались никаким экспериментальным вмешательствам, а также исследование не вмешивалось в клиническое ведение пациента. В ходе исследования была собрана информация только из историй болезни. Образцы мокроты и крови были собраны в рамках обычного ухода. Исследование проводилось в соответствии с действующими этическими стандартами, включая Хельсинкскую декларацию ВМА, и было одобрено «Этическим комитетом Республиканского научно-практического центра пульмонологии и туберкулеза», Минск, Беларусь, протоколом № 1 от 01.11.2011. .
Согласие
Письменное информированное согласие было получено в соответствии с местным законодательством.
Конфликты интересов
Ни один из соавторов не заявляет о конфликте интересов.
Вклад авторов
DNP, DBF, OK, TL и JDL разработали концепцию и дизайн исследования, имели полный доступ ко всем данным в исследовании и взяли на себя ответственность за целостность и точность данных. анализ. DNP и DBF провели статистический анализ и написали первый проект отчета под руководством OK и TL.DBF отвечал за лабораторную часть проекта (культивирование Mtb и выполнение DST и WGS). HH и IK отвечали за успеваемость в Минске, Беларусь. AS, AV, DK и AS координировали исследование в Минске, Беларусь, и собирали данные. JDL была руководителем исследования и несла общую ответственность. Все авторы интерпретировали данные, критически рассмотрели и прокомментировали проект отчета. Все авторы одобрили окончательную версию отчета. Дарья Н. Подлекарева и Дорте Бек Фолквардсен разделили первое авторство и внесли равный вклад в эту работу.Оле Кирк и Трэлс Лиллебек разделили последнее авторство и внесли равный вклад в эту работу.
Благодарности
Мы благодарим пациентов, принявших участие в исследовании, и персонал больниц, участвующих в исследовательской группе по ТБ: ВИЧ. Группа по изучению туберкулеза: ВИЧ в Минске, Беларусь, состоит из сотрудников Белорусского государственного медицинского университета, кафедры инфекционных болезней (И. Карпов (ИП), А. Василенко) и Республиканского научно-практического центра пульмонологии и туберкулеза (А. .Скрахина (П.И.), Х. Гуревич, Д. Климук, А. Скрахин, О. Кондратенко, А. Залуцкая). Мы благодарим Aase Bengaard Andersen, MD (D.M.Sc), и Joanne Reekie, старшего статистика, доктора философии, за чтение рукописи и предоставление критического обзора. Это исследование финансировалось Седьмой рамочной программой Европейского Союза по исследованиям (FP7 / 2007–2013), технологическим разработкам и демонстрациям в рамках грантового соглашения EuroCoord № 260694, Датским советом по независимым исследованиям, Датским национальным исследовательским фондом (грант 126), Augustinus Фонден (Дания) и А.Фонд П. Мёллера (Дания).
Лекарственные средства для лечения туберкулеза
Аминосалициловая кислота Аминосалицилатный препарат, используемый для достижения ремиссии при язвенном колите. Циклосерин Антибиотик широкого спектра действия, используемый для лечения туберкулеза и некоторых инфекций мочевыводящих путей (ИМП). Капреомицин Аминогликозидный антибиотик, применяемый в качестве вспомогательного препарата при туберкулезе. Этионамид Противотуберкулезное средство второй линии, применяемое для лечения туберкулеза, когда другие методы лечения не помогли. Ампренавир Ингибитор протеазы, используемый для лечения ВИЧ-инфекции. Рифапентин Антибиотик, применяемый при лечении туберкулеза легких. Спарфлоксацин Фторхинолоновый антибиотик, используемый для лечения бактериальных респираторных инфекций и синусита. Рифалазил Исследован для применения / лечения атеросклероза, бактериальной инфекции и заболеваний периферических сосудов. Pretomanid Часть схемы из трех препаратов, используемой для лечения туберкулеза легких с широкой и множественной лекарственной устойчивостью. Виомицин Виомицин является важным компонентом лекарственного коктейля, который в настоящее время используется для борьбы с инфекциями Mycobacterium tuberculosis. Бедаквилин Диарилхинолиновый антимикобактериальный препарат, используемый в сочетании с другими антибактериальными средствами для лечения туберкулеза легких с множественной лекарственной устойчивостью (МЛУ-ТБ). Энвиомицин Циклический основной пептид, родственный виомицину. Он выделен из индуцированного мутанта Streptomyces griseoverticillatus var. tuberacticus и действует как противотуберкулезное средство с меньшей ототоксичностью, чем тубератиномицин. Пазуфлоксацин Пазуфлоксацин проходит клинические испытания NCT025 (Протокол клинических испытаний ушных капель пазуфлоксацина мезилат).
Протионамид Противотуберкулезное производное тиоамида, используемое для лечения туберкулеза и лепры с множественной лекарственной устойчивостью (МЛУ). Амитиозон Амитиозон использовался в исследованиях по лечению внутриклеточной инфекции Mycobacterium Avium. Деламанид Антибиотик, используемый для лечения туберкулеза с множественной лекарственной устойчивостью. Теризидон Теризидон использовался в испытаниях, посвященных лечению туберкулеза, инфекций ВИЧ, туберкулеза с множественной лекарственной устойчивостью и туберкулеза с широкой лекарственной устойчивостью. Моринамид Пиразиновый противотуберкулезный агент второй линии. Тиокарлид Без аннотации Этамбутол Противотуберкулезное средство, используемое для профилактики и лечения туберкулеза (ТБ). Пиразинамид Противотуберкулезное средство, используемое в качестве компонента лечения туберкулеза (ТБ). Рифабутин Антибиотик, используемый для лечения комплексного заболевания микобактерий avium у пациентов с ВИЧ. Изониазид Антибиотик, используемый для лечения микобактериальных инфекций; чаще всего используют в сочетании с другими антимикобактериальными средствами для лечения активного или латентного туберкулеза. Рифампицин Антибиотик, используемый для лечения нескольких типов микобактериальных инфекций, включая комплекс Mycobacterium avium, проказу и в сочетании с другими антибактериальными средствами для лечения латентного или активного туберкулеза. Стрептомицин Аминогликозидный антибиотик, показанный для лечения микобактерий туберкулеза с множественной лекарственной устойчивостью и различных нетуберкулезных инфекций. Рифамицин Антибактериальное средство, используемое для лечения диареи путешественников. Пиридоксин Витамин, используемый для коррекции дефицита витамина B6 и лечения тошноты во время беременности. Сульфаметоксазол Пероральный сульфонамидный антибиотик в комбинации с триметопримом, используемый для лечения различных инфекций мочевыводящих путей, дыхательной системы и желудочно-кишечного тракта.
