Anti-HBs (антитела к HBs-антигену вируса гепатита B)
Метод определения
Иммуноферментный анализ (ИФА).
Исследуемый материал
Сыворотка крови
Доступен выезд на дом
Онлайн-регистрация
Показатель наличия защитного иммунитета против вируса гепатита В.
Anti-HBs-антитела появляются в фазе выздоровления после острого гепатита В, обычно через 3 — 4 месяца после элиминации HBsAg (так называемая фаза «окна»). Продолжительность фазы окна может варьировать от 1 месяца до 1 года, в зависимости от состояния иммунной системы больного.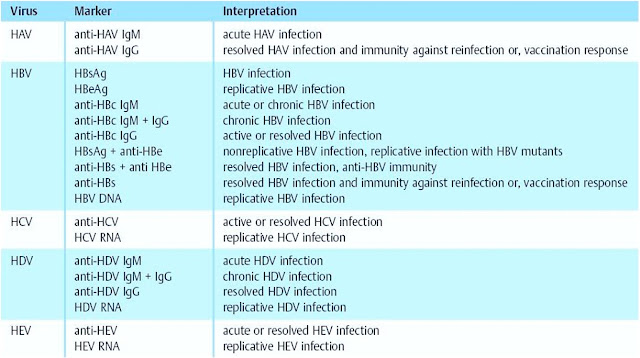 В этот период «окна» важно обследовать пациента на anti-HBc IgM.
В этот период «окна» важно обследовать пациента на anti-HBc IgM.
Anti-HBs-антитела особенно важны в обеспечении иммунной защиты против данного вируса, поэтому количественное определение анти-HBs-антител обычно используют в контроле эффективности иммунитета при вакцинации против гепатита В. Со временем, титр антител снижается вплоть до необнаружения. Иногда возможна пожизненная циркуляция anti-HBs-антител. Появление анти-HBs на фоне клинического улучшения у больного гепатитом В и исчезновение HBsAg является хорошим прогностическим признаком и показателем выздоровления.
При хроническом течении гепатита В возможно параллельное определение поверхностного антигена и антител к нему. Обнаружение анти-HBs в острой фазе гепатита В параллельно с HBsAg свидетельствует о неблагоприятном прогнозе заболевания.
Особенности инфекции. Гепатит B (ВГВ, HВV) острое системное вирусное заболевание. Характеризуется поражением печени и различными внепечёночными проявлениями. Протекает остро или хронически, в желтушной (35%) или безжелтушной (65%) формах. Вирус гепатита В является ретровирусом семейства гепаднавирусов — Hepadnaviridae, содержит ДНК, чрезвычайно устойчив во внешней среде (к УФ-лучам, температуре, детергентам). Гепатит В передаётся с кровью и биологическими жидкостями парентеральным, трансплацентарным, половым и бытовым путями. Группу повышенного риска составляют лица, практикующие внутривенную наркоманию, беспорядочные половые связи, а также медицинские работники, пациенты, нуждающиеся в гемодиализе или переливаниях крови, заключённые, члены семей HBs-положительных лиц, новорождённые от HBs-положительных матерей.
Протекает остро или хронически, в желтушной (35%) или безжелтушной (65%) формах. Вирус гепатита В является ретровирусом семейства гепаднавирусов — Hepadnaviridae, содержит ДНК, чрезвычайно устойчив во внешней среде (к УФ-лучам, температуре, детергентам). Гепатит В передаётся с кровью и биологическими жидкостями парентеральным, трансплацентарным, половым и бытовым путями. Группу повышенного риска составляют лица, практикующие внутривенную наркоманию, беспорядочные половые связи, а также медицинские работники, пациенты, нуждающиеся в гемодиализе или переливаниях крови, заключённые, члены семей HBs-положительных лиц, новорождённые от HBs-положительных матерей.
Проникая в организм, вирус гепатита попадает в макрофаги крови и разносится по организму. Репликация вируса происходит в лимфатических узлах, костном мозге, фолликулах селезёнки, макрофагах, гепатоцитах. Повреждение печени обусловлено, в основном, за счёт иммунного лизиса; также вирус оказывает прямое цитопатическое действие. Сходство антигенов вируса с антигенами системы гистосовместимости человека обусловливает возникновение аутоиммунных («системных») реакций.
Сходство антигенов вируса с антигенами системы гистосовместимости человека обусловливает возникновение аутоиммунных («системных») реакций.
Поверхностные (HBsAg) и сердцевинные (HBcAg) белки вируса являются антигенами, обусловливая выработку anti-HBs и anti-HBс соответственно. Сердцевинный антиген, попадая в кровь, расщепляется на более устойчивые составные части, одна из которых HBe-Ag также несёт антигеные свойства. На неё и вырабатываются anti-HBe антитела. Генетическая изменчивость HВV способствует «ускользанию» вируса из-под иммунного ответа. С этим связаны трудности в лабораторной диагностике (серонегативный гепатит В), а также хронизация заболевания. Появление атипичных участков ДНК в геноме вируса приводит к фульминантному течению гепатита В.
Инкубационный период в среднем составляет 50 дней, но может растягиваться до 6 месяцев. В конце инкубационного периода повышаются уровни печёночных трансаминаз, увеличиваются печень и селезёнка. Возможно повышение концентрации билирубина до 2 — 2,5 нормальных значений, хотя это не приводит к потемнению мочи. Встречаются гриппоподобный, артралгический, диспептический или смешанный варианты клинического течения продромы. Наиболее неблагоприятным является течение продромы по типу сывороточной болезни (зуд, мигрирующие околосуставные высыпания).
Возможно повышение концентрации билирубина до 2 — 2,5 нормальных значений, хотя это не приводит к потемнению мочи. Встречаются гриппоподобный, артралгический, диспептический или смешанный варианты клинического течения продромы. Наиболее неблагоприятным является течение продромы по типу сывороточной болезни (зуд, мигрирующие околосуставные высыпания).
Острый период (2 — 12 дней) протекает с интоксикационным синдромом: снижением аппетита, диспепсией, инверсией сна. В трети случаев возникает желтуха: резко повышается уровень билирубина, слизистые оболочки и кожа окрашиваются в различные оттенки жёлтого цвета, появляется зуд. Наиболее тревожным симптомом является снижение протромбинового индекса и альбумина крови, свидетельствующие о печёночно-клеточной недостаточности. Осложнение заболевания печёночной энцефалопатией свидетельствует об острой гепатодистрофии. Бурный гуморальный иммунный ответ зачастую приводит к появлению иммунных комплексов, оседающих на эндотелии сосудов почек, щитовидной железы, половых органов и др. Возникают васкулиты. В программе системных проявлений HBV-инфекции могут возникать аутоиммунный тиреоидит, хронический гастрит, синдром Шегрена, идеопатическая тромбоцитопеническая пурпура, узелковый периартериит, гломерулонефрит, синдром Гийена Барре, ревматоидный артрит и др.
Возникают васкулиты. В программе системных проявлений HBV-инфекции могут возникать аутоиммунный тиреоидит, хронический гастрит, синдром Шегрена, идеопатическая тромбоцитопеническая пурпура, узелковый периартериит, гломерулонефрит, синдром Гийена Барре, ревматоидный артрит и др.
Фаза выздоровления характеризуется исчезновением признаков холестаза, нормализацией процессов обмена веществ, восстановлением функции печени, на первый план выходят системные проявления заболевания. По сравнению с другими вирусными гепатитами, гепатит В имеет более системный характер, менее благоприятно протекает у детей. Хроническое течение возникает в 5% случаев. «Здоровые носители» HBsAg, также как и больные хроническим гепатитом В, подвержены высокому риску развития цирроза печени и гепато-целлюлярной карциномы. Системные проявления не всегда исчезают вместе с излечением гепатита В.
Разработанные на сегодняшний день вакцины не вызывают вакцино-обусловленного гепатита В, т. к. представляют собой генно-инженерный HBs-антиген. Однако вакцинопрофилактика обеспечивает защиту от гепатита В только на 5 — 7 лет. До вакцинации, по итогам вакцинации и по прошествии 5 лет после вакцинации необходимо исследовать уровень anti-HBs-антител.
к. представляют собой генно-инженерный HBs-антиген. Однако вакцинопрофилактика обеспечивает защиту от гепатита В только на 5 — 7 лет. До вакцинации, по итогам вакцинации и по прошествии 5 лет после вакцинации необходимо исследовать уровень anti-HBs-антител.
Анти- HBs (Anti-HBs)
Анти- HBs (Anti-HBs)
Anti-HBs — Количественное определение в крови специфических защитных постинфекционных или поствакцинальных антител против вирусного гепатита В. Вирус обладает сложной структурой. Основным антигеном оболочки является HBsAg – поверхностный антиген вируса. Существуют биохимические и физико-химические особенности HBsAg, которые позволяют разделить его на несколько субтипов. К каждому субтипу вырабатываются свои специфические антитела. Разные подтипы антигена обнаруживаются в разных регионах мира. Анти-HBs-антитела начинают появляться в крови на 4-12-й неделе после заражения, но сразу связываются с HBsAg, поэтому в определяемом количестве их можно обнаружить только после исчезновения HBsAg. Период между исчезновением антигена и появлением антител (период «окна», или «серологический пробел») может составлять от 1 недели до нескольких месяцев. Титры антител растут медленно, достигая максимума через 6-12 месяцев, и сохраняются в большом количестве более 5 лет. У некоторых выздоравливающих антитела обнаруживаются в крови в течение многих лет (иногда пожизненно). Анти-HBs также образуются при попадании антигенного материала вируса при вакцинации против ВГВ и свидетельствуют об эффективном иммунном ответе на вакцину. Но поствакцинальные антитела не так длительно сохраняются в крови, как постинфекционные. Определение Анти-HBs используют для решения вопроса о целесообразности вакцинации. Например, при положительном анализе введение вакцины не требуется, потому что специфический иммунитет и так существует.
Период между исчезновением антигена и появлением антител (период «окна», или «серологический пробел») может составлять от 1 недели до нескольких месяцев. Титры антител растут медленно, достигая максимума через 6-12 месяцев, и сохраняются в большом количестве более 5 лет. У некоторых выздоравливающих антитела обнаруживаются в крови в течение многих лет (иногда пожизненно). Анти-HBs также образуются при попадании антигенного материала вируса при вакцинации против ВГВ и свидетельствуют об эффективном иммунном ответе на вакцину. Но поствакцинальные антитела не так длительно сохраняются в крови, как постинфекционные. Определение Анти-HBs используют для решения вопроса о целесообразности вакцинации. Например, при положительном анализе введение вакцины не требуется, потому что специфический иммунитет и так существует.
Подготовка к исследованию
Специальной подготовки не требуется.
Не курить в течение 30 минут до сдачи крови.
Показания к исследованию
Каждые 3-6 месяцев при контроле за хроническим вирусным гепатитом В и его лечением.
При наличии данных о перенесённом гепатите неизвестной этиологии.
При обследовании пациентов из группы высокого риска заразиться ВГВ.
При решении вопроса о необходимости вакцинации против вирусного гепатита В.
Через несколько месяцев или лет после введения вакцины.
Интерпретация
Референсные значения – отрицательно
Положительный результат
Фаза выздоровления после перенесённого гепатита В (при этом в анализах HBsAg отсутствует).
Эффективная вакцинация (ревакцинация потребуется не ранее чем через 5 лет).
Инфицирование другим субтипом вируса гепатита В (при одновременном обнаружении anti-HBs и HBsAg).
Отрицательный результат
Отсутствие вирусного гепатита В (при отрицательных результатах других исследований).
Отсутствие поствакцинального иммунитета.
Вирусный гепатит В в инкубационном, остром или хроническом периоде (при положительных результатах анализа на другие антигены и антитела).
Сомнительный результат
Специфические антитела присутствуют в крови в небольшом количестве (вакцинация может быть отложена на год).
Рекомендуется повторение анализа через некоторое время (в зависимости от клинической ситуации и решения врача).
На результаты могут влиять
У пациентов после переливания крови или компонентов плазмы вероятен ложноположительный результат. Присутствие anti-HBs-антител не является абсолютным показателем полного выздоровления от вирусного гепатита В и полноценной защиты от повторного инфицирования. Учитывая наличие разных серологических подтипов гепатита В, существует вероятность присутствия в крови антител к поверхностным антигенам одного типа и фактическое инфицирование организма вирусом гепатита В другого субтипа. У таких пациентов антитела к HBs и HBs-антиген могут выявляться в крови одновременно.
Назначается в комплексе с
HBsAg
anti-HBcore, суммарные антитела
HBeAg
anti-HBe, антитела
HBV, ДНК,ПЦР ( в плазме) качественный
HBV, ДНК, ПЦР ( в плазме) количественный
anti-HDV, антитела
Anti-HCV, антитела, ИФА
Биохимический анализ крови при заболеваниях ЖКТ
Anti-HBs (антитела к HBs-антигену вируса гепатита B)
Исследуемый материал
Сыворотка крови
Метод определения
Иммуноферментный анализ (ИФА).
Показатель наличия защитного иммунитета против вируса гепатита В.
Anti-HBs-антитела появляются в фазе выздоровления после острого гепатита В, обычно через 3 — 4 месяца после элиминации HBsAg (так называемая фаза «окна»). Продолжительность фазы окна может варьировать от 1 месяца до 1 года, в зависимости от состояния иммунной системы больного. В этот период «окна» важно обследовать пациента на anti-HBc IgM.
Anti-HBs-антитела особенно важны в обеспечении иммунной защиты против данного вируса, поэтому количественное определение анти-HBs-антител обычно используют в контроле эффективности иммунитета при вакцинации против гепатита В. Со временем, титр антител снижается вплоть до необнаружения. Иногда возможна пожизненная циркуляция anti-HBs-антител. Появление анти-HBs на фоне клинического улучшения у больного гепатитом В и исчезновение HBsAg является хорошим прогностическим признаком и показателем выздоровления.
При хроническом течении гепатита В возможно параллельное определение поверхностного антигена и антител к нему. Обнаружение анти-HBs в острой фазе гепатита В параллельно с HBsAg свидетельствует о неблагоприятном прогнозе заболевания.
Особенности инфекции. Гепатит B (ВГВ, HВV) острое системное вирусное заболевание. Характеризуется поражением печени и различными внепечёночными проявлениями. Протекает остро или хронически, в желтушной (35%) или безжелтушной (65%) формах. Вирус гепатита В является ретровирусом семейства гепаднавирусов — Hepadnaviridae, содержит ДНК, чрезвычайно устойчив во внешней среде (к УФ-лучам, температуре, детергентам). Гепатит В передаётся с кровью и биологическими жидкостями парентеральным, трансплацентарным, половым и бытовым путями. Группу повышенного риска составляют лица, практикующие внутривенную наркоманию, беспорядочные половые связи, а также медицинские работники, пациенты, нуждающиеся в гемодиализе или переливаниях крови, заключённые, члены семей HBs-положительных лиц, новорождённые от HBs-положительных матерей.
Проникая в организм, вирус гепатита попадает в макрофаги крови и разносится по организму. Репликация вируса происходит в лимфатических узлах, костном мозге, фолликулах селезёнки, макрофагах, гепатоцитах. Повреждение печени обусловлено, в основном, за счёт иммунного лизиса; также вирус оказывает прямое цитопатическое действие. Сходство антигенов вируса с антигенами системы гистосовместимости человека обусловливает возникновение аутоиммунных («системных») реакций.
Поверхностные (HBsAg) и сердцевинные (HBcAg) белки вируса являются антигенами, обусловливая выработку anti-HBs и anti-HBс соответственно. Сердцевинный антиген, попадая в кровь, расщепляется на более устойчивые составные части, одна из которых HBe-Ag также несёт антигеные свойства. На неё и вырабатываются anti-HBe антитела. Генетическая изменчивость HВV способствует «ускользанию» вируса из-под иммунного ответа. С этим связаны трудности в лабораторной диагностике (серонегативный гепатит В), а также хронизация заболевания. Появление атипичных участков ДНК в геноме вируса приводит к фульминантному течению гепатита В.
Появление атипичных участков ДНК в геноме вируса приводит к фульминантному течению гепатита В.
Инкубационный период в среднем составляет 50 дней, но может растягиваться до 6 месяцев. В конце инкубационного периода повышаются уровни печёночных трансаминаз, увеличиваются печень и селезёнка. Возможно повышение концентрации билирубина до 2 — 2,5 нормальных значений, хотя это не приводит к потемнению мочи. Встречаются гриппоподобный, артралгический, диспептический или смешанный варианты клинического течения продромы. Наиболее неблагоприятным является течение продромы по типу сывороточной болезни (зуд, мигрирующие околосуставные высыпания).
Острый период (2 — 12 дней) протекает с интоксикационным синдромом: снижением аппетита, диспепсией, инверсией сна. В трети случаев возникает желтуха: резко повышается уровень билирубина, слизистые оболочки и кожа окрашиваются в различные оттенки жёлтого цвета, появляется зуд. Наиболее тревожным симптомом является снижение протромбинового индекса и альбумина крови, свидетельствующие о печёночно-клеточной недостаточности. Осложнение заболевания печёночной энцефалопатией свидетельствует об острой гепатодистрофии. Бурный гуморальный иммунный ответ зачастую приводит к появлению иммунных комплексов, оседающих на эндотелии сосудов почек, щитовидной железы, половых органов и др. Возникают васкулиты. В программе системных проявлений HBV-инфекции могут возникать аутоиммунный тиреоидит, хронический гастрит, синдром Шегрена, идеопатическая тромбоцитопеническая пурпура, узелковый периартериит, гломерулонефрит, синдром Гийена Барре, ревматоидный артрит и др.
Осложнение заболевания печёночной энцефалопатией свидетельствует об острой гепатодистрофии. Бурный гуморальный иммунный ответ зачастую приводит к появлению иммунных комплексов, оседающих на эндотелии сосудов почек, щитовидной железы, половых органов и др. Возникают васкулиты. В программе системных проявлений HBV-инфекции могут возникать аутоиммунный тиреоидит, хронический гастрит, синдром Шегрена, идеопатическая тромбоцитопеническая пурпура, узелковый периартериит, гломерулонефрит, синдром Гийена Барре, ревматоидный артрит и др.
Фаза выздоровления характеризуется исчезновением признаков холестаза, нормализацией процессов обмена веществ, восстановлением функции печени, на первый план выходят системные проявления заболевания. По сравнению с другими вирусными гепатитами, гепатит В имеет более системный характер, менее благоприятно протекает у детей. Хроническое течение возникает в 5% случаев. «Здоровые носители» HBsAg, также как и больные хроническим гепатитом В, подвержены высокому риску развития цирроза печени и гепато-целлюлярной карциномы. Системные проявления не всегда исчезают вместе с излечением гепатита В.
Системные проявления не всегда исчезают вместе с излечением гепатита В.
Разработанные на сегодняшний день вакцины не вызывают вакцино-обусловленного гепатита В, т. к. представляют собой генно-инженерный HBs-антиген. Однако вакцинопрофилактика обеспечивает защиту от гепатита В только на 5 — 7 лет. До вакцинации, по итогам вакцинации и по прошествии 5 лет после вакцинации необходимо исследовать уровень anti-HBs-антител.
HBsAg, качественный тест (HBs-антиген, поверхностный антиген вируса гепатита B, «австралийский» антиген)
Исследуемый материал
Сыворотка крови
Метод определения
Иммуноферментный анализ (ИФА).
Основной маркёр инфицирования вирусом гепатита В
Внимание. При положительных и сомнительных реакциях, срок выдачи результата может быть увеличен до 2-х рабочих дней.
HBsAg — поверхностный антиген вируса гепатита В, основной маркёр острого и хронического гепатита В — представляет собой белковую молекулу (липопротеин), ответственную за адсорбцию вируса на поверхности гепатоцитов (клеток печени). После встраивания вируса в геном печёночных клеток они начинают продуцировать вирусную ДНК и белки, и новые молекулы HBsAg поступают в кровь.
После встраивания вируса в геном печёночных клеток они начинают продуцировать вирусную ДНК и белки, и новые молекулы HBsAg поступают в кровь.
В большинстве случаев HBsAg обнаруживается уже в инкубационном периоде и при остром течении гепатита выявляется в крови в течение 5 — 6 месяцев. Обнаружение поверхностного антигена вируса гепатита В в крови дольше 6 месяцев после начала болезни свидетельствует о возможной хронизации процесса. Возможно пожизненное носительство HBsAg.
HBsAg способен активизировать клеточные протоонкогены. Через достаточно длительный срок (более 20 лет) возможно развитие гепатокарциномы.
Особенности инфекции. Гепатит B (ВГВ, HВV) острое системное вирусное заболевание. Характеризуется поражением печени и различными внепечёночными проявлениями. Протекает остро или хронически, в желтушной (35%) или безжелтушной (65%) формах. Вирус гепатита В является ретровирусом семейства гепаднавирусов — Hepadnaviridae, содержит ДНК, чрезвычайно устойчив во внешней среде (к УФ-лучам, температуре, детергентам). Гепатит В передаётся с кровью и биологическими жидкостями парентеральным, трансплацентарным, половым и бытовым путями. Группу повышенного риска составляют лица, практикующие внутривенную наркоманию, беспорядочные половые связи, а также медицинские работники, пациенты, нуждающиеся в гемодиализе или переливаниях крови, заключённые, члены семей HBs-положительных лиц, новорождённые от HBs-положительных матерей.
Гепатит В передаётся с кровью и биологическими жидкостями парентеральным, трансплацентарным, половым и бытовым путями. Группу повышенного риска составляют лица, практикующие внутривенную наркоманию, беспорядочные половые связи, а также медицинские работники, пациенты, нуждающиеся в гемодиализе или переливаниях крови, заключённые, члены семей HBs-положительных лиц, новорождённые от HBs-положительных матерей.
Проникая в организм, вирус гепатита попадает в макрофаги крови и разносится по организму. Репликация вируса происходит в лимфатических узлах, костном мозге, фолликулах селезёнки, макрофагах, гепатоцитах. Повреждение печени обусловлено, в основном, за счёт иммунного лизиса; также вирус оказывает прямое цитопатическое действие. Сходство антигенов вируса с антигенами системы гистосовместимости человека обусловливает возникновение аутоиммунных («системных») реакций.
Поверхностные (HBsAg) и сердцевинные (HBcAg) белки вируса являются антигенами, обусловливая выработку anti-HBs и anti-HBscore соответственно. Сердцевинный антиген, попадая в кровь, расщепляется на более устойчивые составные части, одна из которых HBe-Ag также несёт антигенные свойства. На неё и вырабатываются anti-HBe антитела. Генетическая изменчивость HВV способствует «ускользанию» вируса из-под иммунного ответа. С этим связаны трудности в лабораторной диагностике (серонегативный гепатит В), а также хронизация заболевания. Появление атипичных участков ДНК в геноме вируса приводит к фульминантному течению гепатита В.
Сердцевинный антиген, попадая в кровь, расщепляется на более устойчивые составные части, одна из которых HBe-Ag также несёт антигенные свойства. На неё и вырабатываются anti-HBe антитела. Генетическая изменчивость HВV способствует «ускользанию» вируса из-под иммунного ответа. С этим связаны трудности в лабораторной диагностике (серонегативный гепатит В), а также хронизация заболевания. Появление атипичных участков ДНК в геноме вируса приводит к фульминантному течению гепатита В.
Инкубационный период в среднем составляет 50 дней, но может растягиваться до 6 месяцев. В конце инкубационного периода повышаются уровни печёночных трансаминаз, увеличиваются печень и селезёнка. Возможно повышение концентрации билирубина до 2 — 2,5 нормальных значений, хотя это не приводит к потемнению мочи. Встречаются гриппоподобный, артралгический, диспептический или смешанный варианты клинического течения продромы. Наиболее неблагоприятным является течение продромы по типу сывороточной болезни (зуд, мигрирующие околосуставные высыпания).
Острый период (2 — 12 дней) протекает с интоксикационным синдромом: снижением аппетита, диспепсией, инверсией сна. В трети случаев возникает желтуха: резко повышается уровень билирубина, слизистые оболочки и кожа окрашиваются в различные оттенки жёлтого цвета, появляется зуд. Наиболее тревожным симптомом является снижение протромбинового индекса и альбумина крови, свидетельствующие о печёночно-клеточной недостаточности. Осложнение заболевания печёночной энцефалопатией свидетельствует об острой гепатодистрофии. Бурный гуморальный иммунный ответ зачастую приводит к появлению иммунных комплексов, оседающих на эндотелии сосудов почек, щитовидной железы, половых органов и др. Возникают васкулиты. В программе системных проявлений HBV-инфекции могут возникать аутоиммунный тиреоидит, хронический гастрит, синдром Шегрена, идеопатическая тромбоцитопеническая пурпура, узелковый периартериит, гломерулонефрит, синдром Гийена Барре, ревматоидный артрит и др.
Фаза выздоровления характеризуется исчезновением признаков холестаза, нормализацией процессов обмена веществ, восстановлением функции печени, на первый план выходят системные проявления заболевания. По сравнению с другими вирусными гепатитами, гепатит В имеет более системный характер, менее благоприятно протекает у детей. Хроническое течение возникает в 5% случаев. «Здоровые носители» HBsAg, также как и больные хроническим гепатитом В, подвержены высокому риску развития цирроза печени и гепатоцеллюлярной карциномы. Системные проявления не всегда исчезают вместе с излечением гепатита В.
Разработанные на сегодняшний день вакцины не вызывают вакцино-обусловленного гепатита В, т. к. представляют собой генно-инженерный HBs-антиген. Однако вакцинопрофилактика обеспечивает защиту от гепатита В только на 5 — 7 лет. До вакцинации, по итогам вакцинации и по прошествии 5 лет после вакцинации необходимо исследовать уровень anti-HBs-антител.
| Уровень anti-HBs (Ед/л) | Рекомендуемые сроки
ревакцинации |
| менее 10 | Немедленно |
| 11 — 100 | Через 3 — 6 месяцев |
| 101 — 1000 | Через 1 год |
| 1001 — 10000 | Через 3,5 года |
| более 10000 | Через 7 лет |
Оформление заявок для проведения исследований в ООО «ИНВИТРО» осуществляется по паспорту или документу, его заменяющему (миграционная карта, временная регистрация по месту жительства, удостоверение военнослужащего, справка из паспортного стола при утере паспорта, регистрационная карта учёта из гостиницы). Предъявленный документ в обязательном порядке должен содержать информацию о временной или постоянной регистрации на территории РФ и фотографию. При отсутствии паспорта (документа его заменяющего) пациент вправе оформить анонимную заявку для сдачи биоматериала. При анонимном обследовании, заявке и полученному от клиента образцу биоматериала присваивается номер, известный только пациенту, и медперсоналу, оформлявшему заказ.
! Результаты исследований, выполненных анонимно, не могут быть представлены для госпитализации, профессиональных осмотров и не подлежат регистрации в ОРУИБ.
Вирусный гепатит В | Биомедика
Вирусный гепатит В (HBV) – воспалительное заболевание печени, которое вызывается ДНК-содержащим вирусом гепатита В. Ежегодно в мире регистрируется около 58 миллионов больных только острой формой инфекции. Всего же, по оценке экспертов ВОЗ, в разных странах мира общая численность больных гепатитом В и носителей превышает 1млрд. А по данным Центра по изучению клиники и болезней, предающихся, половым путем (Франция), в настоящее время в мире гепатитом В заражено более 2 млрд. человек.
В подавляющем большинстве случаев при условии своевременной диагностики и адекватного лечения больные острым гепатитом B успешно выздоравливают и приобретают пожизненный иммунитет к повторному заражению. Но если же у инфицированного человека снижен иммунитет, острый период болезни проходит незамеченным, то постепенно течение инфекции затягивается и становится хроническим. В этом случае заболевание медленно прогрессирует и может в дальнейшем перейти в цирроз печени (риск 10-20%) и даже рак печени.
Источником инфекции при гепатите В является больной человек или вирусоноситель. Передается вирус с любой биологической жидкостью организма, но в первую очередь с кровью. Передача вируса происходит через нарушенные кожные и слизистые покровы, при гемотрансфузиях инфицированной кровью, использовании препаратов из зараженной крови и плохо стерилизованного инструментария. Возможна также передача гепатита В новорожденному от инфицированной матери при родах или после. HBV отличается исключительно высокой инфекционностью.
В организме больного вирусом гепатита В обнаруживаются лабораторным методом маркеры – антигены и антитела, определение которых дает разную информацию, в том числе диагностическую и прогностическую. В зависимости от сочетания этих маркеров можно судить об активности и опасности процесса. При активном вирусном процессе естественное течение заболевания, чаще всего, приводит к формированию в печени фиброза с переходом в цирроз или первичный рак печени.
Именно поэтому, при обнаружении вирусного гепатита В рекомендуется провести ряд лабораторных исследований для определения тактики лечения.Все эти анализы на гепатит В могут быть выполнены в лаборатории медицинского центра «Биомедика», но помните – только лечащий врач может правильно интерпретировать полученные результаты .
Маркеры гепатита В
Поверхностный антиген (HBsAg, австралийский антиген) является основным серологическим маркером BГВ. Он может быть обнаружен в крови при остром или хроническом гепатите. Этот антиген, чаще всего, вызывает образование антител к HBsAg, как часть нормальной иммунной реакции на инфекцию.
Положительный анализ крови на HBs антиген означает наличие острой или хронической HBV-инфекции (носительство HBs антигена) и возможность передачи вируса здоровым людям.
Отрицательный тест означает с большой долей вероятности отсутствие вируса гепатита В в крови.
Антитела к поверхностному антигену (анти-HBsAg) представляют собой протекционные антитела, которые вырабатываются в ответ на попадание в организм поверхностного антигена гепатита B.
Положительный тест означает, что человек защищен иммунитетом от попадания вируса гепатита В по одной из двух причин:
- Успешно была сделана прививка от гепатита B;
- Организм справился с острой инфекцией и человек не может заразиться гепатитом снова.
Ядерный «е» антиген гепатита B (HBeAg) является белком, который свидетельствует об активной репликации HBV в тканях печени.
Положительный тест означает высокую инфекционность крови и высокий риск передачи вируса другим людям. Так, его обнаружение в крови беременной указывает на высокую опасность инфицирования новорожденного HBV. Этот маркер используется также для контроля эффективности лечения хронического гепатита В. У большинства больных хроническим гепатитом с высокой активностью процесса HBeAg сохраняется на длительный срок (до нескольких лет).
Антитела к HBeAg (анти-HBe) представляют собой белки, которые образуются в организме в ответ на «e» антиген гепатита B.
В случае благоприятного развития вируса гепатита В у больных постепенно происходит замещение в крови HBеAg на антитела к нему (сероконверсия HBеAg – анти-HBе). На ранней стадии сероконверсии оба эти маркёра могут обнаруживаться одновременно.
Исчезновение HBeAg и быстрое нарастание титра анти-HBе у больного практически исключает угрозу хронизации HBV. Отсутствие такой динамики и выявление монотонно низких концентраций анти-НВе, наоборот, может свидетельствовать о развитии хронического HBV с невысокой репликативной активностью (HBeAg-негативный хронический HBV).
Длительное сохранение HBеAg в крови больного и отсутствие анти-HBе может быть показателем угрозы развития хронического гепатита с высокой репликативной активностью HBV (HBеAg-позитивный хронический ГВ). Таким образом, динамический контроль за системой HBeAg – антиНВе позволяет уже в острую стадию гепатита В надежно прогнозировать его исход.
Антитела к сердцевинному антигену (анти-HBcоr) представляет собой антитела, которые вырабатываются в организме в ответ на присутствие в организме части вируса гепатита, называемого «основной антиген» или «сердцевинный антиген». Смысл этого теста часто зависит от результатов двух других тестов: анти-HBs и HBsAg.
IgM антитела к сердцевинному антигену (анти-HBcorM) используется для выявления острой инфекции.
Положительный тест означает инфицированность вирусом гепатита В в течение последних 6-12 месяцев или обострение хронической инфекции.
Описанные маркеры HBV определяются в клинической практике методом ИФА и позволяют правильно определить тактику лечения острого и хронического гепатита В.
Определение ДНК вирусного гепатита В
Определение ДНК HBV – тест на присутствие ДНК вируса гепатита В у пациента в крови методом ПЦР.
Положительный тест означает, что вирус активно размножается в организме человека и такой человек несет потенциальную опасность заражения вирусом гепатита В.
Количественное определение ДНК HBV (вирусная нагрузка) – это тест на определение количества единиц ДНК вируса гепатита В, которые присутствуют в определенном объеме крови.
Количественный метод определения содержания ДНК вируса в плазме дает важную информацию об интенсивности развития заболевания, об эффективности лекарственной терапии и о развитии резистентности к антивирусным препаратам. От вирусной нагрузки зависят не только дозы препаратов, но и длительность лечения и прогнозы.
Лечение вирусного гепатита В
Основу лечения вирусного гепатита В составляют противовирусные препараты. Цель этого лечения – подавление размножения вируса, снижение воспаления и регресс фиброзного процесса, профилактика цирроза и рака.
Для лечения хронического гепатита В используются препараты интерферона и аналоги нуклеозидов. Тактику лечения теми или иными препаратами определяет лечащий врач в зависимости от целого ряда обстоятельств, в первую очередь, активности вирусного процесса, а также состояния печени по данным биохимических анализов, УЗИ и степени фиброза. Для определения степени фиброза существуют безопасные и информативные методы – эластометерия (на специальном аппарате) и фибротест (по маркерам фиброза в крови).
В настоящее время в клиническую практику внедрены современные противовирусные препараты прямого антивирусного действия – аналоги нуклеозидов, которые вводятся в виде таблеток, быстро и эффективно подавляют размножение вируса. Большинство из них не имеет выраженных побочных действий, что выгодно отличает их от интерферонов.
Вирус гепатита В может сопровождаться вирусом D, который попадает в организм человека только вместе с вирусом В. Этот вирус быстро и часто вызывает в печени необратимые изменения и требует назначения противовирусной терапии как можно раньше для предотвращения формирования цирроза.
Лечение вирусного гепатита В длительное, повторяющимися курсами, если вирус активируется после успешно проведенного курса противовирусного лечения. Вирус гепатита В требует пожизненного контроля. Только в этом случае можно сохранить навсегда нормальную здоровую печень без цирроза или рака печени. С вирусным гепатитом В можно успешно бороться.
В медицинском центре «Биомедика» нашим пациентам могут быть выполнены все необходимые лабораторные исследования на определение вируса гепатита В, сделаны УЗИ органов брюшной полости и проведена консультация врача-инфекциониста (гепатолога). Наши специалисты имеют высшую квалификационную категорию, регулярно участвуют в международных конференциях гепатологов и имеют клинический опыт современной терапии хронического гепатита В.
Вопросы и ответы – «ГЕПАТИТ.РУ»
- Главная
- Вопросы и ответы
Вопрос: у меня 22 недели беременности, получила ответ на анализ крови на гепатит, вот что он показал: ПЦР диагностика гепатита С — ОТРИЦАТЕЛЬНАЯ, антитела к вирусу гепатита С — спектр (ИФА) СЛАБО положительный, cor(+), ns3(-), ns4(-), ns5(-), антитела к вирусу гепатита С суммарные (ИФА) положительный. получаеться у меня гепатит С?
Ответ: Наличие антител, тем более сомнительных, не означает диагноз гепатит С. Надо перепроверить еще раз и сделать анализ ПЦР.
Вопрос: Добрый день! В 2007 году был острый гепатит В, при выписке анти-HBsAg 2,161(0,111),все остальные показатели отрицательные. Через 7 месяцев анти-HBsAg 0,240(0,107), все остальные отрицательные, в том числе и HBV. Меня сняли с учета. Теперь беременность 30 недель, повысился биллирубин, терапевт ставит под вопросом синдром Жильбера, гепатолог говорит, что даже при всех тех давних результатах на гепатит В, не исключена его хронизация . Подскажите, пожалуйста, возможна ли хронизация гепатита В? И стоит ли сдать снова анализы? Заранее благодарна.
Ответ: О хроническом вирусном гепатите В можно говорить только в том случае, если у вас HBsAg положительный. Возможно скрытое течение вирусного гепатита В в случае, если острый вирусный гепатит закончился без формирования иммунитета — anti-HBs отрицательный. В этом случае среди маркеров гепатита должен обнаруживаться anti-HBcor, может быть и anti-HBe.
Если есть подозрение на синдром Жильбера, то надо сделать генетический анализ.
Вопрос: Здравствуйте! Мой доктор поставил диагноз: хронический вирусный гепатит С после того как я сдал анализ: core-NS 3,5 сумм. — положительно. Теперь мне надо сдать анализ PCR RNA HCV количеств. Надо было перед этим анализом сдавать еще PCR RNA HCV качествен. или количеств. все сразу покажет. За ранее спасибо
Ответ: Если качественный анализ будет отрицательный, то количественный делать бессмысленно при отсутствии вируса.
Вопрос: Здравствуйте! Скажите пожалуйста,мне на днях поставили первую прививку от гепатита В,а сегодня я нашла свою карту о прививках и выяснилось,что мне их уже ставили в 2007году,но я об этом совсем забыла.Повторная прививка как-то может навредить моему здоровью,если эти прививки мне уже были поставлены ранее.Заранее спасибо
Ответ: Нет, не повредит. Но на всякий случай сделайте анализ anti-HBs количественный, что бы определить, действует ли ваша прививка, Количество антител должно быть больше 100. Если меньше, то надо делать прививку заново.
Вопрос: Здравствуйте! У меня хронический гепатит В с 2011 года, прохожу курс ПВТ препаратом СЕБИВО, по 1 табл в день. ПЦР- сразу через 3месяца после начала приема. Но сейчас ощущаю на себе побочки. Делала узи щитовидной железы, сдавала кровь на гормоны, в итоге-диффузный зоб. Гормоны в норме, а узи показывает увеличение щитовидки. В «женской части»-кольпит, и подозрение на воспаление либо эндометриоз. Узи брюшной полости показало-хронический холецистит. Возможно ли дальше продолжать ПВТ? И можно ли во время ПВТ одновременно лечить остальные заболевания?
Результаты моего последнего исследования: вирус гепатита В(колич)-не обнаружен, референсные значения-не обнаружен. anti HBcor total- положительный. anti- HBS(колич.)-0 мЕд/мл. anti-HBe-положительный.
Ответ: В вашей ситуации для продолжения терапии надо оценивать степень фиброза. Я не встречалась со случаями побочного действия аналогов нуклеозидов на щитовидную железу и другими перечисленными вами. Лечить их обязательно нужно без всякой зависимости от вирусного гепатита. Те анализы, которые вы делали для контроля эффективности не имеет смысла делать, они не изменятся.
Вопрос: Моему близкому родственнику был установлен диагноз гепатит с, и так же были снижены тромбоциты, отослали к гематологу, где врач прописал гормональные преднизалон, но при снижении дозы тромбоциты так же падают. И врач кроме преднизалона не может не чего сделать. Соотвественно лечение гепатита с при сниженных тромбоцитах врач не начинает замкнутый круг, узи печени показал что все в норме. Подскажите что делать
Ответ: Найти грамотного гепатолога. Если в печени все в порядке, то тромбоциты падают не из-за печени. При низком фиброзе нет необходимости начинать ПВТ в такой ситуации.
Всего: 12 страниц
Вы можете задать вопрос на нашем форуме
HBsAg подтверждающий – что это такое? Свойства и показания
Материал для исследования: сыворотка крови.
Метод определения: твердофазный иммуноферментный анализ (ELISA).
Исследование проводится с использованием тест системы производства Вектор Бест (Россия).
Вирусный гепатит В — ДНК — содержащий вирус. Имеет несколько антигенов — HВsAg — поверхностный антиген, HBcAg — сердцевинный антиген, HBeAg — антиген инфекционности.
HBsAg — поверхностный антиген вируса гепатита В, основной маркер острого и хронического гепатита В — представляет собой белковую молекулу (липопротеин), ответственную за адсорбцию вируса на поверхности гепатоцитов (клеток печени). После встраивания вируса в геном печеночных клеток они начинают продуцировать вирусную ДНК и белки, и новые молекулы HBsAg поступают в кровь.
В большинстве случаев HBsAg обнаруживается уже в инкубационном периоде и при остром течении гепатита выявляется в крови в течение 5-6 мес. Обнаружение поверхностного антигена вируса гепатита В в крови дольше 6 месяцев после начала болезни свидетельствует о возможной хронизации процесса. Возможно пожизненное носительство HBsAg. HBsAg способен активизировать клеточные протоонкогены. Через достаточно длительный срок (более 20 лет) возможно развитие гепатокарциномы.
Поверхностные (HBs-Ag) и сердцевинные (HBc-Ag) белки вируса являются антигенами, обусловливая выработку антител anti-HBs и anti-HBs-core соответственно. Сердцевинный антиген, попадая в кровь, расщепляется на более устойчивые составные части, одна из которых HBe-Ag также несет антигенные свойства. На нее и вырабатываются anti-HBe антитела. Генетическая изменчивость HВV способствует «ускользанию» вируса из-под иммунного ответа. С этим связаны трудности в лабораторной диагностике (серонегативный гепатит В), а также хронизация заболевания.
Подготовка к исследованию: Не требуется.
Исследование проводится в случае обнаружения в сыворотке HBs-антигена. Подтверждающее исследование включает повтор теста на HBsAg и пробы с иммуноингибированием и разведением. При подтверждении первичного положительного результата выдается ответ: HBsAg — «положительно», HBsAg (подтверждающий) — «положительно».
В редких случаях при проведении подтверждающего теста проба с иммуноингибированием не подтверждает специфичности положительного результата. В таких случаях выдается ответ HBsAg — «результат повторно положительный, неподтвержденный». Это означает вероятность каких-либо неспецифических влияний компонентов сыворотки. В таком случае рекомендуется через некоторое время повторить тестирование.
Общие сведения о тесте на поверхностные антитела к гепатиту B
Тест на поверхностные антитела к гепатиту B (HBsAb) ищет антитела, которые ваша иммунная система вырабатывает в ответ на поверхностный белок вируса гепатита B. Поверхностные антитела против гепатита B также называют анти-HBs, и их не следует путать с HBsAg, что означает поверхностный антиген гепатита B.
ERproductions Ltd / Getty Images
Что такое поверхностные антитела к гепатиту В?
Когда вы подвергаетесь воздействию гепатита B, ваше тело вырабатывает иммунную реакцию против него как захватчика.Это происходит независимо от того, подверглись ли вы контакту с кровью или половым путем, или если вы вакцинированы вакциной против гепатита В.
Вирус гепатита В имеет на своей поверхности белки (антигены), которые заставляют вашу иммунную систему вырабатывать антитела. В вакцине образец содержит только белок, а не сам вирус.
Первая реакция вашего организма при контакте с гепатитом B — это выработка антител IgM к гепатиту B . Эти ранние антитела вырабатываются для борьбы с несколькими частями вируса, включая его ядро.Эти антитела видны при первоначальном ответе, но в конечном итоге они исчезают.
Затем ваша иммунная система начинает вырабатывать антител IgG . Он продолжает вырабатывать эти антитела всю оставшуюся жизнь. Таким образом, ваша иммунная система всегда готова атаковать вирус гепатита B.
Цель теста
Этот тест на HBsAb может быть проведен, чтобы выяснить, ранее был ли он заражен гепатитом B или была ли ваша вакцинация успешной.Это также можно сделать, если у вас гепатит В, чтобы увидеть, выздоравливаете ли вы.
Несмотря на то, что вакцинация младенцев и детей от гепатита B является стандартом (с 1991 г.), многие взрослые не были вакцинированы в детстве и могут подвергаться риску. Также возможно, что ваши уровни антител снизятся с годами, и если результаты теста отрицательный, может понадобиться бустер.
Как проводится тест
Тест на HBsAb проводится путем взятия образца крови, который отправляется в лабораторию для анализа.Ваш врач получит результаты и оценит их с учетом вашей истории вакцинации, риска заражения, симптомов и результатов других тестов на гепатит.
Интерпретация результатов
Ваш тест может быть положительным или отрицательным, но результаты также могут интерпретироваться по-разному в зависимости от других выполненных тестов на гепатит.
Положительно
Если HBsAb положительный (присутствуют антитела), это обычно означает, что вы излечились от инфекции гепатита B и имеете некоторый иммунитет или что вы когда-то получали вакцинацию против гепатита B и имеете иммунитет.Взаимодействие с другими людьми
отрицательный
Если ваш тест на HBsAb отрицательный, это может означать много разных вещей, но в целом это означает, что у вас нет иммунитета к вирусу гепатита B.
Если ваши другие тесты на гепатит В (как на HBsAb, так и на другие тесты на гепатит) отрицательны, это означает, что вы либо не инфицированы, либо находитесь на очень ранней стадии инкубации инфекции, до того момента, когда будут образовываться антитела.
Если ваш тест на HBsAb отрицательный, ваш врач может порекомендовать вам вакцину.
отрицательно, но другие анализы на гепатит положительны
Ваш тест на HBsAb может быть отрицательным, даже если другие тесты на гепатит B положительны, показывая активную или хроническую инфекцию. Необходимы дальнейшие тесты, особенно на поверхностный антиген гепатита B (HBsAg), который показывает, что сам вирус циркулирует в вашем кровотоке. и что у вас активная или хроническая инфекция.
Продолжение
Спросите своего врача, есть ли у вас дополнительные вопросы о тесте и о том, почему он проводится.Если ваш HBsAb положительный, это означает, что вы были инфицированы в прошлом или получили вакцину и теперь у вас иммунитет.
Многие люди, инфицированные вирусом гепатита B, не имеют очевидных факторов риска заражения. Для передачи вируса требуется лишь небольшое количество крови (подумайте: открытая рана на руке, касающаяся предмета, который болезнь, возможно, задела). Даже совместного использования зубной щетки или поцелуев достаточно, чтобы передать инфекцию.
Если ваш тест на HBsAb отрицательный, но другие тесты на гепатит положительны, вашему врачу потребуется дополнительное обследование.Возможно, у вас активная инфекция, за которой следует внимательно следить, или у вас сейчас развилась хроническая инфекция гепатита B.
Хронические инфекции могут привести к осложнениям, некоторые из которых могут быть такими серьезными, как цирроз или рак печени, поэтому очень важно проконсультироваться с врачом и разработать план действий, будь то лечение или тщательный мониторинг.
Слово от Verywell
Если все ваши тесты на гепатит отрицательны, это означает, что вы не подвергались воздействию вируса (или не получали прививку) и не имеете иммунитета.В этом случае поговорите со своим врачом о вакцинации, о том, есть ли у вас факторы риска заражения гепатитом В.
В заключение, даже те, кто имеет иммунитет к гепатиту B благодаря иммунизации, все еще подвержены риску заражения другими типами гепатита.
Что такое Anti-HBS, что означает положительный и отрицательный Anti-HBS?
Гепатит В или, другими словами, желтуха — это вирусное заболевание печени. Вирус гепатита B (HBV) может передаваться через кровь, половым путем или может передаваться ребенку в утробе матери, он может развиваться как острый или хронический.После передачи гепатита в организм в течение 6 недель — 6 месяцев у вас могут появиться такие симптомы, как грипп, и другие симптомы могут не проявляться. Лабораторный тест показывает, что если HBsAG положительный, это означает, что поверхностный антиген гепатита B указывает на то, что человек инфицирован, в то время как Anti-HBS указывает на то, что у человека выработался иммунитет к болезни.
Если у человека был вирус гепатита В, переданный ранее или если человек был вакцинирован, положительные уровни Anti-HBS определены лабораторными тестами.
Что такое Anti-HBS?
Вирус гепатита В, вызывающий воспалительную инфекцию в печени; Он передается от человека к человеку при половом акте, контакте с биологическими жидкостями, нестерильными средствами по уходу за телом и кровью. Вирус гепатита В, который может передаваться от матери к плоду во время беременности, представляет собой опасное для жизни заболевание, которое нарушает работу печени. Anti-RLS — это лабораторный тест, позволяющий определить, вырабатывает ли в организме человека, предположительно инфицированного вирусом гепатита B, защитный белок против поверхностного антигена гепатита B.Проще говоря, Anti RLS также можно определить как тест для определения иммунитета человека к вирусу гепатита B. Когда человек сталкивается с вирусом гепатита В, иммунная система пытается обнаружить и уничтожить вирус. Для этого он производит антитела против антигена, идентифицированного как HBsAG, на поверхности вируса гепатита B. Положительное значение анти-HBC IGG указывает на то, что пожизненный иммунитет достигается за счет антител, вырабатываемых после первых антител, образовавшихся после контакта с вирусом гепатита B.
Значение Anti HBC IGG, которое не дает информации о выздоровлении или хроническом течении болезни, поэтому не имеет самостоятельного значения. Эти антитела, которые вырабатываются организмом и образуют защитный механизм, называются Anti-HBS. Анти-HBA — это продукт борьбы организма с вирусом гепатита B, который знаменует полное исчезновение инфекции. Эти антитела также обеспечивают постоянный иммунитет в организме. Затем организм готов вырабатывать антитела против антигенов, присутствующих на поверхности вируса, когда он сталкивается с вирусом гепатита B.Другими словами, болезнь уничтожается организмом до того, как она вызовет инфекцию. Измеряя уровень этих антител в организме в лаборатории, значение Anti-RLS дает положительный или отрицательный результат.
Цель теста Anti-HBS — определить, был ли человек ранее инфицирован или вакцинирован от вируса гепатита B. В некоторых случаях, например при неполной вакцинации, уровень антител может снижаться, поэтому этот тест можно использовать для определения необходимости повторной вакцинации.Для анти-HBS врач берет кровь у пациента и отправляет ее в лабораторию для анализа и оценивает ее вместе с результатом теста на гепатит.
Что означает положительный результат «Анти-HBS»?
Anti-HBS — это тип лабораторного теста, который проводится на людях, предположительно больных гепатитом B. Тест, который можно использовать для определения того, был ли человек уже иммунизирован путем воздействия вируса гепатита B или вакцинации, может также может использоваться для определения того, был ли вирус уничтожен организмом и приобрел ли иммунитет на всю жизнь.Тест на анти-HBS также используется для проверки того, сохраняется ли вакцина или, другими словами, вырабатывает ли организм антитела против HBsAG, который определяется как поверхностный антиген вируса гепатита B. Перед введением вакцины против гепатита B также проводится тест на анти-RLS, чтобы определить, обладает ли человек иммунитетом к этому вирусу.
На вопрос «что является положительным по отношению к HBS *» можно ответить следующим образом; Результат лабораторного теста, проведенного с помощью метода анализа крови, известного как Elisa, показывает, что значение анти-HBS положительное, что указывает на то, что человек невосприимчив к вирусу гепатита B.Положительное значение анти-HBS, которое указывает на то, что человек защищен от вируса гепатита B на всю жизнь, может быть получено путем вакцинации или вследствие инфекции. Хотя значение анти-HBS выше 5 мМЕ / мл, оно считается положительным, но значение от 5 до 12 мМЕ / мл после вакцинации показывает, что вакцина не сохраняется. Значения выше 12 мМЕ / мл указывают на то, что вакцина сохраняется и полностью иммунизируется. Тест на анти-RLS не определяет, был ли иммунитет приобретен после контакта с вирусом гепатита B или после вакцинации.Чтобы понять это, необходим тест Anti Hepatitis Core, известный как Anti HBC.
Что означает положительный результат «Анти-HBS»?
Когда результат анти-HBS получен лабораторным тестом, отрицательное значение означает, что в организме нет иммунитета против вируса гепатита B. Таким образом можно ответить на часто задаваемый вопрос: «Что означает отрицательный результат анти-HBS?». Для людей, не получивших вакцину против гепатита B, вполне нормально иметь анти-HBS. Однако тот факт, что отрицательный результат Anti-HBS не означает, что человек не болеет гепатитом B и не заражен инфекцией.Чтобы понять это состояние, необходимо проверить уровень HBsAg, известный как тест на поверхностный антиген гепатита B. Отрицательное значение, полученное по уровню анти-HBS в 5,0 мМЕ / мл, указывает на то, что организм не вырабатывает антитела против антигена, идентифицированного как HBsAG, на поверхности вируса гепатита B в присутствии гепатита B из-за острого или хронического гепатита. Рекомендуется вакцинировать человека в случае отрицательного значения анти-HBS, что свидетельствует о том, что человек не подвергался воздействию вируса гепатита B или не был вакцинирован ранее.Гепатит B, распространенность которого во всем мире составляет 5%, может привести к смертельным заболеваниям, таким как рак печени, и пациенту напоминают, что он может легко получить защиту с помощью вакцинации.
Результат Anti-HBS
Тест
Anti-HBS используется для проверки того, подвергался ли человек воздействию вируса гепатита B раньше, и обеспечивала ли вакцина против гепатита B защиту с помощью лабораторного теста. Анти-HBS, который принимается примерно через два дня после сдачи крови, четко определяет, имеет ли человек иммунитет к вирусу гепатита B.Результат теста включает референсный диапазон Anti-HBS и положительные или отрицательные значения, указывающие результат теста. Значения ниже 5,0 мМЕ / мл считаются отрицательными, а результаты выше этого значения — положительными. Однако вакцина против вируса гепатита B должна быть 12 мМЕ / мл и выше для полной защиты.
Если у вас есть дополнительные вопросы о вирусе гепатита B и тесте на анти-HBS, вы можете связаться с нами по телефону 0090 216 444 39 49 .
Влияние вариантов детерминанта «а»
Abstract
При хроническом гепатите В (ХГВ) устойчивость поверхностного антигена гепатита В (HBs Ag) иногда ассоциируется с антителами (Ab) к HBs (анти-HBs).Чтобы оценить гипотезу выбора вариантов иммунного ускользания HBs Ag у пациентов с ХГВ, вариабельность гена S HBV была определена для пациентов, постоянно несущих как HBs Ag, так и анти-HBs антитела, и пациентов, исключительно положительных по HBs Ag. Мы отобрали 14 пациентов, у которых были представлены оба маркера (группа I) в нескольких последовательных образцах, и 12 пациентов, положительных только по HBs Ag (группа II). Ген, кодирующий HBs Ag, был амплифицирован и клонирован, и по меньшей мере 15 клонов на пациента были секвенированы и проанализированы.Количество изменений остатков в S-белке было в 2,7 раза чаще у пациентов группы I, чем у пациентов группы II, и происходило в основном в детерминанте «а» главной гидрофильной области (MHR), с 9,52 против 2,43 изменений на 100 остатков ( P = 0,009) соответственно. Десять пациентов (71%) из группы I и только трое (25%) из группы II показали как минимум два остаточных изменения MHR. Наиболее частые изменения у пациентов группы I были расположены в положениях s145, s129, s126, s144 и s123, как описано для вариантов иммунного ускользания.У пациентов с ХГВ сосуществование HBs Ag и анти-HBs Ab связано с увеличением вариабельности детерминанты «a», что предполагает отбор мутантов иммунного ускользания HBV во время хронического носительства. Последствия этого процесса отбора в отношении эффективности вакцины, диагностики и клинической эволюции остаются частично неизвестными.
Более 350 миллионов человек, или 5% населения мира, являются хроническими носителями вируса гепатита B (HBV), и эта инфекция представляет собой глобальную проблему общественного здравоохранения (21).У многих пациентов, хронически инфицированных HBV, что определяется по сохранению более 6 месяцев поверхностного антигена гепатита B (HBs Ag), разовьются опасные для жизни заболевания, такие как цирроз печени и гепатоцеллюлярная карцинома. Было подсчитано, что до 30% из них умрут от последствий заражения (20).
При естественном течении инфекции HBV выведение вируса, вероятно, является результатом тесной координации как гуморальной, так и клеточной иммунной систем. В целом, опосредованный антителами иммунный ответ на белки HBV направлен на удаление циркулирующих частиц HBV, тогда как клеточные эффекторы вносят вклад в устранение инфицированных гепатоцитов (30).Биологически клиренс вируса классически характеризуется появлением анти-HBs-антител (Ab) в серологическом профиле.
При хронической инфекции гепатита В можно выделить две клинически важные фазы. В то время как фаза иммунной толерантности обычно характеризуется небольшим повреждением печени и присутствием е-антигена гепатита В (HBe Ag) в сыворотке, вторую фазу можно охарактеризовать как более агрессивную для печени, с отбором HBe Ag-отрицательных вариантов и обнаружение антител к HBe.В конечном итоге хронические носители могут быть классифицированы как неактивные носители с низкой репликацией вируса и антителами к HBe и нормальными биохимическими маркерами печени или как пациенты с хроническим гепатитом с аномальными уровнями ферментов печени и более высокой вирусной нагрузкой (23).
Примечательно, что в нескольких отчетах описана персистенция HBs-Ag, связанного с анти-HBs-антителами, у 10–25% пациентов с хроническим гепатитом B (ХГВ) (19, 27). Механизм, лежащий в основе присутствия как HBs Ag, так и анти-HBs антител, остается неизвестным, но одной из возможностей может быть отбор мутантов, ускользающих от иммунитета.
Ген оболочки HBV имеет три открытые рамки считывания (ORF), PreS1, PreS2 и S, которые кодируют три белка, малый, средний и большой HBs Ag, транслируемые с разных мРНК. Общий для всех трех белков доминантный эпитоп «а» расположен в положениях кодонов от 124 до 147 в основной гидрофильной области (MHR) гена S. Эта детерминанта является одной из основных мишеней анти-HBs-антител в ходе начального иммунного ответа при остром гепатите B.
В результате могут появиться иммунные варианты HBs Ag с мутациями в одном или нескольких сайтах детерминанты «а». селективного давления на белок S.Действительно, эти ускользающие мутанты в основном возникают у вакцинированных пациентов или у пациентов с ортотопической трансплантацией печени, получавших моноклональные или поликлональные антитела к HBs Ag (5, 7, 11). Некоторые из распространенных изменений остатков Ag HBs для иммунного ускользания включают G145R, D144A, P142S, Q129H I / T126N / A и M133L (36). Эксперименты по сайт-направленному мутагенезу, в которых каждая аминокислота была заменена всеми другими возможными остатками, с тех пор подтвердили, что аминокислоты в положениях с 141 по 145 имеют решающее значение для связывания антител против HBs, индуцированных рекомбинантной вакциной против HBV (33).Более того, ускользающая мутация в детерминанте «а» может также возникать при естественном течении инфекции HBV, что приводит к активной репликации вируса и заболеванию печени, несмотря на сероконверсию в анти-HBs у пациентов с хроническим гепатитом B (1, 13, 25, 28, 38, 39). Аналогичным образом, в нескольких отчетах были идентифицированы мутанты HBs Ag в образцах сыворотки, которые дали положительный результат как на HBs Ag, так и на анти-HBs (3, 19, 26). Однако ограничениями этих предыдущих исследований было ограниченное количество клонов или пациентов, рассматриваемых для анализа, и тот факт, что распространенность встречающихся в природе мутаций в детерминанте «а» остается неизвестной для пациентов с ХГВ.Как практическое следствие, обнаружение анти-HBs, связанных с вариантами S, у хронических носителей может привести к ошибочному диагнозу бывшей вирусной инфекции гепатита B, если диагностический тест не может обнаружить мутировавший HBs Ag. Механизм, лежащий в основе появления анти-HBs у пациентов с хроническим гепатитом B, остается неясным, но одной из причин может быть отбор вариантов иммунного ускользания HBs Ag. Чтобы оценить эту гипотезу, вариабельность гена HBV S у носителей ХГВ была определена для пациентов, несущих как HBs Ag, так и анти-HBs антитела, и пациентов, положительных только по HBs Ag.
МАТЕРИАЛЫ И МЕТОДЫ
Пациенты и сыворотки.
Восемьсот шестьдесят шесть пациентов регулярно наблюдаются в больнице Ла-Пити-Сальпетриер по поводу хронического гепатита, определяемого HBs Ag-носительством в течение более 6 месяцев. Хотя подавляющее большинство из них (91,1%) не выработали определяемых антител к HBs во время последующего наблюдения, 77 пациентов (8,9%) одновременно несут как HBs Ag, так и антитела против HBs. Для этого исследования мы протестировали 26 сывороток пациентов с ХГВ, отобранных на основе их статуса антител к HBs.Критерии отбора пациентов как с HBs Ag, так и с анти-HBs были в основном сосредоточены на титрах анти-HBs, по крайней мере, в три раза превышающих аналитический порог метода (10 мМЕ / мл) по крайней мере при трех посещениях подряд.
Обнаружение серологических маркеров HBV.
Измерения HBs Ag, анти-HBs-антител, HBe Ag и анти-HBe-антител проводились с использованием стандартных иммуноферментных анализов на основе микрочастиц (HBs Ag V2.0, anti-HBs V2.0, HBe Ag 2.0 и анти-HBe). -HBe 2.0) (анализ AxSYM; Abbott, Rungis, France). Количественную оценку вирусной нагрузки ДНК HBV проводили с использованием коммерчески доступных анализов Hybrid Capture II Digene (Abbott, Rungis, Франция) и HBV Monitor Cobas (Roche Diagnostics, Meylan, Франция).
Извлечение и амплификация полноразмерного генома HBV.
ДНК HBV экстрагировали из 200 мкл сыворотки каждого пациента с помощью мини-набора QIAmp DNA Blood (QIAGEN, Les Ulis, FRANCE) и собирали в 60 мкл воды. Амплификацию ДНК HBV проводили в соответствии с методом, описанным Günther et al., с небольшими изменениями (12). Вкратце, ПЦР проводили в 50-мкл реакционной смеси, содержащей 10 мкл ДНК-матрицы HBV, 2 мМ MgSO 4 , 0,2 мМ концентрации каждого дезоксинуклеозидтрифосфата, 60 мМ Tris-SO 4 (pH 8,9), 18 мМ (NH 4 ) 2 SO 4 , 0,2 мкМ (каждый) праймеров P1 (5′-CCG GAA AGC TTG AGC TCT TCT TTT TCA CCT CTG CCT AAT CA-3 ‘) и P2 (5’- CCG GAA AGC TTG AGC TCT TCA AAA AGT TGC ATG GTG CTG G-3 ‘) и 1 мкл ДНК-полимеразы высокой точности Taq Platinum (Invitrogen, Cergy-Pontoise, Франция) на термоциклере (двигатель ДНК PTC-200 ; MJ Research).После горячего старта и денатурации при 94 ° C в течение 1,5 мин было выполнено 45 циклов с денатурацией при 94 ° C в течение 30 с, отжигом при 56 ° C в течение 30 с и элонгацией при 68 ° C в течение 3,5 мин.
В случае неудачной амплификации с использованием полноразмерного подхода был разработан метод амплификации гена, кодирующего S-белок. ПЦР с использованием специфических праймеров VTS1 (5′-TTC TTG GAA CAA GAG CTA C-3 ‘) и VT1022 (5′-GCA AAG CCC AAA AGA CCC ACA AT-3’) в тех же условиях, что описаны выше, но с временем элонгации 1 мин выполняли для амплификации полного гена S.
Клонирование полноразмерного генома HBV.
После амплификации ПЦР и электрофореза продукты ПЦР выделяли из агарозного геля, очищали с использованием набора для экстракции геля QIAquick (QIAGEN, Les Ulis, Франция) и клонировали с использованием набора для клонирования ПЦР TOPO XL (Invitrogen, Cergy-Pontoise, Франция). Плазмиды получали с помощью наборов Qiaprep 8 Turbo miniprep (QIAGEN, Les Ulis, Франция).
Секвенирование гена S.
Нуклеотидную последовательность гена S определяли с помощью BigDye Terminator v3.Готовый реакционный набор для 1 цикла секвенирования и запуск на секвенаторе ДНК ABI 3100 (Applied Biosystems, Les Ulis, Франция). Праймеры, использованные для секвенирования S ORF, приведены в таблице. Анализ последовательности выполняли с помощью программного обеспечения Seqscape (Applied Biosystems, Les Ulis, Франция), программного обеспечения Clustal (34a) и программного обеспечения Mutation Master (http://tandem.bu.edu/tools.html). Вкратце, геномные последовательности, полученные для гена S HBV, сравнивали со всеми эталонными последовательностями HBV, используемыми на веб-сайте NCBI, для определения генотипа HBV (www.ncbi.nlm.nih.gov/projects/genotyping/) следующим образом (даны номера доступа): subtype A, {«type»: «entrez-nucleotide», «attrs»: {«text»: «X02763», «term_id»: «59418», «term_text»: «X02763»}} X02763, {«type»: «entrez-нуклеотид», «attrs»: {«text»: «X51970», «term_id»: «1155012» , «term_text»: «X51970»}} X51970 и {«type»: «entrez-нуклеотид», «attrs»: {«text»: «AF0
«,» term_id «:» 22135711 «,» term_text «:» AY0
«}} AY0
и {» type «:» entrez-нуклеотид «,» attrs «: {» текст «:» AY0
«,» term_id «:» 22135726 «,» term_text «:» AY0
«}} AY0
.
ТАБЛИЦА 1.
Обзор праймеров для амплификации и секвенирования, используемых в данном исследовании
| Праймер | Последовательность (5′-3 ‘) | Полярность a | Домен | Позиции | ||
|---|---|---|---|---|---|---|
| VTS1 TTCTTGGAACAAGAGCTAC | S / Pol пре S1 | 2831-2850 | ||||
| CHBV3 CCTGCTGGTGGCTCCAGTT | S / preS2 Pol | |||||
| VT301 CTTGGCCAAAATTCGCAGTCCCC | S | HBs Ag / Pol | 299-311 | |||
| SEQ11REV | GAGCAGGAGTCGTGCAGGT | AS | HBs Ag / Pol | 521-539 | 521-539 | 997-1019 |
Статистический анализ.
Сравнения проводились с использованием теста Манна-Уитни или теста t для количественных данных. Статистическая значимость была определена при уровне P <0,05. Данные были проанализированы с использованием NCSS 2001 (Кейсвилл, Юта).
РЕЗУЛЬТАТЫ
Характеристики пациентов.
Среди 864 хронически инфицированных HBV пациентов, наблюдаемых в больнице Ла-Пити-Сальпетриер, 77 (8,9%) были идентифицированы как несущие как HBs Ag, так и анти-HBs антитела в последовательных образцах.Чтобы проанализировать механизмы, лежащие в основе присутствия HBs Ag и анти-HBs у хронически инфицированных пациентов, мы выбрали две группы пациентов на основе их серологического статуса.
Четырнадцать пациентов с ХГВ, у которых при последовательных посещениях были представлены как HBs Ag, так и анти-HBs, составили группу I, в то время как 12 пациентов с ХГВ, положительных только по HBs Ag, представляли группу II. Согласно классическому описанию, все пациенты были также положительны на другие маркеры инфекции HBV, такие как anti-HBc и HBe Ag или anti-HBe.Важно отметить, что, как указано в таблице, уровни анти-HBs у пациентов из группы I были довольно высокими, со средним титром 81 МЕ / л (диапазон от 43 до 512).
ТАБЛИЦА 2.
Основные характеристики пациента a
| Группа ( n ) | Пациент | Серологические маркеры | Вирусная нагрузка (лог-копий / мл) | Генотип | Последующее наблюдение (мес) | Предыдущее или текущее лечение | Мутации, связанные с устойчивостью к ламивудину | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| HBs Ag | Титр антител к HBs (МЕ / литр) | HBe Ag | Anti-HBe | Интерферон | Нуклеозид | 2 аналог нуклеозида| 2 | | |||||||||||||||||||||||||||||||
| I (14) | P1 | + | 43 | + | — | > 6 | D | 8 | LAM | 9017 | 512 | + | + | > 6 | A | 43 | LAM | |||||||||||||||||||||
| P1 | + | E | 33 | LAM | L180M / M204V | |||||||||||||||||||||||||||||||||
| P7 | + | 105 | — | + | > 6 | C | 29 | |||||||||||||||||||||||||||||||
| P10 | + | 72 | — | + | 3 | |||||||||||||||||||||||||||||||||
| P11 | + | 46 | + | — | 3.9 | C | 16 | LAM | V173L / L180M / M204V | |||||||||||||||||||||||||||||
| P12 | + | 286 | + | |||||||||||||||||||||||||||||||||||
| P13 | + | 48 | — | + | > 6 | E | 25 | 62 | + | — | > 6 | A | 8 | |||||||||||||||||||||||||
| P16 | + | B | 102 | Есть | ||||||||||||||||||||||||||||||||||
| P17 | + | 47 | + | — | > 6 | C | 36 | Да | ||||||||||||||||||||||||||||||
| P18 | + | 101 | + | — | > 6 | |||||||||||||||||||||||||||||||||
| P20 | + | 127 | — | + | 3.6 | A, E | 24 | |||||||||||||||||||||||||||||||
| P21 | + | 434 | + | — | C | C | ||||||||||||||||||||||||||||||||
| II (12) | P1 | + | <10 | + | + | > 6 | E | 24 | Да | L172 LAM | P2 | + | <10 | + | + | > 6 | B | 36 | LAM | |||||||||||||||||||
| + | > 6 | C | 42 | Да | LAM / ADV | L180M / M204V | ||||||||||||||||||||||||||||||||
| P5 | + | <10177 | + | > 6 | D | 39 | ||||||||||||||||||||||||||||||||
| P6 | + | <10 | + | + | + | + | + | 9 | E | 49 | Да | LAM | ||||||||||||||||||||||||||
| P7 | + | <10 | + | — | 1 9017 9017 907 901 | 6 | ||||||||||||||||||||||||||||||||
| P8 | + | <10 | + | — | 4.9 | B | 43 | <10 | — | + | > 6 | B | 46 | Есть | LAM / ADV | L180M / M204I | ||||||||||||||||||||||
| P | — | 5 | C | 28 | ||||||||||||||||||||||||||||||||||
| P11 | + | <10 | + | — | > 6 | B | 49 | Да | LAM / ADV | L180M / M204V | ||||||||||||||||||||||||||||
| P12 | + | <10 | 60 | |||||||||||||||||||||||||||||||||||
| P13 | + | <10 | + | — | > 6 | E | 36 | E | 36 Две группы были сопоставимы по статусу HBe Ag (9 HBe Ag-позитивных пациентов в каждой группе), статусу анти-HBe антител (6 пациентов в обеих группах) и вирусной нагрузке выше 6 log копий / мл (10 и 11 пациентов I и II групп соответственно).Сохранение неизменного серологического статуса также принималось во внимание при отборе пациентов, что продемонстрировано медианным статусом HBs Ag при последующем наблюдении в течение 35 и 92 месяцев для пациентов из групп I и II, соответственно. Распределение генотипов HBV было неоднородным в обеих группах, и в группе I наблюдались две коинфекции разных генотипов. Девять пациентов из группы I и восемь пациентов из группы II получали лечение от своих инфекций либо интерфероном, либо аналогом нуклеозида (или нуклеотида). .Что еще более важно, у двух пациентов из группы I и у четырех пациентов из группы II развилась устойчивость к ламивудину, о чем свидетельствует наличие мутаций устойчивости к ламивудину в гене полимеразы. Секвенирование S-области HBV и статистическое сравнение.Подход клонирования-секвенирования был использован для изучения полных последовательностей S-кодирующих генов для пациентов из каждой группы. Две пары праймеров были сконструированы для обеспечения возможности амплификации всего S-гена и, из-за перекрытия ORF, N-конца гена, кодирующего полимеразу.Сначала было выполнено сравнение всех последовательностей клонов от каждого пациента; затем все последовательности клонов, полученные от уникального пациента, сравнивали с согласованной последовательностью того же генотипа для выявления необычных остатков. Чтобы стандартизировать наше сравнение, мы произвольно выбрали в качестве эталонных последовательностей те, которые используются в инструменте генотипирования NCBI (www.ncbi.nlm.nih.gov/projects/genotyping/) (31). Были проанализированы полноразмерные последовательности, полученные из всех клонов, и процент замен остатков сравнили между двумя группами (рис.). Распределение изменений было неоднородным по S ORF, и изменения были более преобладающими для группы I, чем для группы II. Для простоты представления полноразмерный S-белок (226 аминокислот [аа]) далее был разделен на три области: N-концевую область (от 1 до 99 аминокислот), MHR (от 100 до 169 аминокислот), которая содержит детерминант «а» (от 124 до 147 аминокислот) и С-концевой участок (от 170 до 226 аминокислот) (34, 35). Наиболее яркое накопление остаточных изменений наблюдалось в области, охватывающей детерминант «а».В этой области количество замен остатков для группы I было в два-четыре раза выше, чем для группы II. Частоты замен остатков в S-белке в изолятах от пациентов с HBs Ag / анти-HBs (группа I) (черные столбцы, n = 14) и только HBs Ag-положительных пациентов (серые столбцы, n = 12 ), анализируемых с интервалами по 10 аминокислот в каждом. Каждая полоса представляет собой процент мутировавших остатков для всех клонов в каждом интервале из 10 аминокислот на группу.Изменения остатков, связанные с генотипическим полиморфизмом, не учитывались. Две перекрывающиеся рамки белков S и полимеразы представлены в нижней части диаграммы. Общий анализ последовательностей белка S для каждого пациента, независимо от серологического статуса, подтвердил гетерогенное распределение изменений остатков. Действительно, самая высокая частота изменений остатков наблюдалась в пределах детерминанты «а» (6,25 мутированных остатков на 100 аминокислот). MHR (3.74 мутантных остатка на 100 аминокислот) и С-концевая часть белка (3,58 мутантных остатка на 100 аминокислот) показали меньшую вариабельность, но немного больше, чем у N-концевой области (2,64 мутантных остатка на 100 аминокислот). (Таблица ). Для статистического анализа N-концевой участок был взят в качестве фонового уровня вариабельности, поскольку он, вероятно, меньше подвержен влиянию иммунного давления или противовирусного лечения. ТАБЛИЦА 3.Распределение аминокислотных изменений в полноразмерном S-белке и его различных областях
| |||||||||||||||||||||||||||||
