Перинатальная энцефалопатия (ПЭП) — мифы и реальность
Аббревиатура ПЭП (перинатальная энцефалопатия) знакома многим родителям детей первого года жизни. К сожалению, в нашей стране этот диагноз очень распространен и активно ставиться детскими неврологами. Помимо страхов и волнений родителей из-за возможных отрицательных прогнозов состояния здоровья ребенка, такой диагноз влечет за собой медикаментозное лечение, медотводы от прививок, долгую череду внеплановых неврологических осмотров и массажей.
Что же такое ПЭП и насколько она опасна для малыша?
Сегодня термин ПЭП не применяется, как устаревший. Современная неврология использует определение – перинатальная асфиксия или гипоксически-ишемическая перинатальная энцефалопатия.
Причиной перинатальной асфиксии является дефицит кислорода в крови и/или снижение показателей мозгового кровотока у плода перед родами или новорожденного в родах или первые часы жизни.
В России данный диагноз выставляют каждому 5-му младенцу, в то время как в странах Европы и Северной Америки от 1 до 8 случаев на 1000 новорожденных.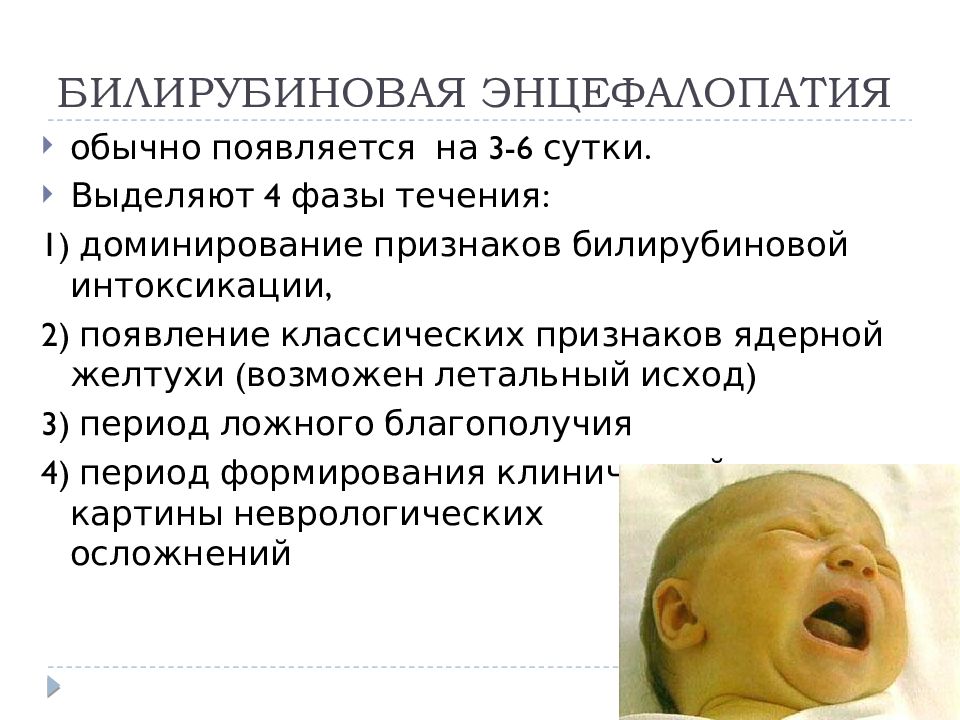 Налицо огромная гипердиагностика.
Налицо огромная гипердиагностика.
По данным крупных западных исследований, прогноз перинатальной энцефалопатии зависит от степени тяжести данного состояния, которую примерно можно соотнести с оценкой по шкале Апгар.
Легкая степень (Апгар 6-7 баллов) – в 97-100% случаев полное восстановление без последствий и без медикаментозного лечения.
Средняя степень (Апгар 4-5 баллов) – в 20-35% случаев приводит к неврологическим нарушениям.
Тяжелая степень (Апгар 0-3 балла) – крайне высокий риск стойкой неврологической патологии
Таким образом, если у Вашего ребенка оценка по Апгар была выше 7 баллов, не было никаких осложнений после рождения, ребенка вовремя выписали из роддома без дополнительных обследований и лечения, малыш развивается в соответствии с возрастными нормами, хорошо ест, прибавляет в весе и т.д., однако врач ставит Вашему ребенку диагноз ПЭП, то правомочность такого диагноза под большим сомнением.
Назначение в данном случае медикаментозной терапии (актовегин, кавинтон, циннаризин, энцефабол и др.) никак не обосновано. Как было сказано выше, исследования показали, что у 97-100% пациентов при шкале Апгар 6-7 баллов и обоснованно выставленной легкой степени тяжести ПЭП без какого-либо медикаментозного лечения полностью отсутствуют какие-либо неврологические последствия. А в оставшихся менее 3% случаев изменения минимальны и не проявляются ни снижением IQ, ни задержкой развития или двигательными нарушениями.
Если Вы думаете, что Вашему ребенку возможно поставили необоснованный диагноз ПЭП и назначили медикаментозное лечение, не стоит полностью игнорировать данную ситуацию. Ради его здоровья подумайте об альтернативной консультации детского невролога, который руководствуется принципами доказательной медицины. Это поможет принять правильное решение, избежать приема ненужных лекарств и сохранить спокойствие в Вашей семье в такие важные первые месяцы жизни малыша.
В Детской клинике ЕМС опытные детские неврологи всегда готовы прийти на помощь детям и их родителям с первых дней жизни малыша, в том числе, если малыш родился с низким весом и/или перинатальными нарушениями нервной системы. В распоряжении врачей клиники современное оборудование для диагностики и лечения маленьких пациентов по стандартам мировой доказательной медицины (УЗИ головного мозга, ЭЭГ, КТ, МРТ и др.).
В распоряжении врачей клиники современное оборудование для диагностики и лечения маленьких пациентов по стандартам мировой доказательной медицины (УЗИ головного мозга, ЭЭГ, КТ, МРТ и др.).
ГИПОКСИЧЕСКИ-ИШЕМИЧЕСКАЯ ЭНЦЕФАЛОПАТИЯ У НОВОРОЖДЁННЫХ, РОЖДЁННЫХ В ТЯЖЁЛОЙ АСФИКСИИ | Зарубин
1. Зарубин А.А., Голуб И.Е., Богданова А.Д., Мельников В.А., Ионушене С.В., Федорова О.С. Применение лечебной гипотермии при лечении тяжёлой интранатальной асфиксии [Электронный ресурс] // Universum: Медицина и фармакология: электрон. научн. журн. — 2015. — № 11. — Режим доступа: www.7universum.com/ru/med/archive/item/2714 (дата обращения 10.01.2016).
2. Зарубин А.А., Голуб И.Е., Федорова О.С., Мельников В.А., Богданова А.Д. Системная лечебная гипотермия в терапии тяжёлой асфиксии у новорождённых // Анестезиология и реаниматология. — 2016. — № 4. -С. 269-272
— 2016. — № 4. -С. 269-272
3. Ианг И., Розенберг Г.А. Повреждение гемато-энцефалического барьера при острых и хронических цереброваскулярных заболеваниях // Журнал национальной ассоциации по борьбе с инсультом «Stroke». Российское издание. — 2012. — № 1. — С. 91-96
4. Иванов Д.О. Нарушения обмена глюкозы у новорождённых. — СПб.: Изд-во Н-Л, 2011. — 100 с
5. Иова А.С., Щугарева Л.М., Гармашов Ю.А. Пути повышения чувствительности шкалы комы Глазго у детей (педиатрическая шкала комы Глазго — Санкт-Петербург) // Матер. I Всерос. конф. по детской нейрохирургии. — М., 2003. — С. 134-135
6. Пальчик А.Б., Шабалов Н.П. Гипоксически-ишемическая энцефалопатия новорождённых. — М.: МЕДпресс-информ, 2009. — 253 с
— 253 с
7. Петренко Ю.В., Иванов Д.О., Курзина Е.А. Оценка органной недостаточности у новорождённых // Бюллетень Федерального Центра сердца, крови и эндокринологии им. В.А. Алмазова. — 2011. — № 2. — С. 43-50
8. Салмина А.Б., Окунева О.С., Таранушенко Т.Е., Фурсов А.А., Прокопенко С.В., Михуткина С.В., Малиновская Н.А., Тагаева Г.А. Роль нейронастроглиальных взаимодействий в дизрегуляции энергетического метаболизма при ишемическом перинатальном поражении головного мозга // Анналы клинической и экспериментальной неврологии. — 2008. — № 3. -С. 44-51
9. Abu-Shaweesh J.M. (2011). Respiratory disorders in preterm and term infants. In: Martin R.J., Fanaroff A.A., Walsh M.C. (eds.). Fanaroff and Martin’s neonatal perinatal medicine: diseases of the fetus and infant, (2), 1141-1170.
10. Anderson P. (2012). Neuropeptide could be biomarker for stroke. J. Am. Coll. Cardiol., 60, 346-354.
11. Azzopardi D. (2014). TOBY study group. Predictive value of the amplitude integrated EEG in infants with hypoxic ischaemic encephalopathy: data from a randomized trial of therapeutic hypothermia. Arch. Dis. Child Fetal Neonatal Ed., 99, 80-82.
12. Azzopardi D., Strohm B., Marlow N. (2014). Effects of hypothermia for perinatalasphyxia on childhood outcomes. N. Engl. J. Med., 371, 140-149.
13. Barkovich A.J. (2005). Magnetic resonance techniques in the assessment of myelin and myelination. J. Inherit. Metab. Dis., 28, 311-343.
14. Chakkarapani E., Dingley J., Aquilina K., Osredkar D., Liu X., Thoresen M. (2013). Effects of xenon and hypothermia on cerebrovascular pressure reactivity in newborn global hypoxic-ischemic pig model. J. Cereb. Blood Flow Metab, 33, 1752-1760.
Chakkarapani E., Dingley J., Aquilina K., Osredkar D., Liu X., Thoresen M. (2013). Effects of xenon and hypothermia on cerebrovascular pressure reactivity in newborn global hypoxic-ischemic pig model. J. Cereb. Blood Flow Metab, 33, 1752-1760.
15. Cowan F.M., de Vries LS. (2005). The internal capsule in neonatal imaging. Semin. Fetal Neonatal Med., 10 (5), 461-474.
16. Da Silva S., Hennebert N., Denis R., Wayenberg J.-L. (2000). Clinical value of a single postnatal lactate measurement after intrapartum asphyxia. Acta Paediatr., 89 (3), 320-223.
17. De Vries L.S., Groenendaal F. (2010). Patterns of neonatal hypoxic-ischemic brain injury. Neuroradiology, 52 (6), 555-566.
18. Edwards A.D., Brocklehurst P., Gunn A.J., Halliday H., Juszczak E., Levene M. Strohm B., Thoresen M., Whitelaw A., Azzopardi D. (2010). Neurological outcomes at 18 months of age after moderate hypothermia for perinatal hypoxic ischaemic encephalopathy: synthesis and meta-analysis of trial data. Br. Med. J., 340, 363.
Edwards A.D., Brocklehurst P., Gunn A.J., Halliday H., Juszczak E., Levene M. Strohm B., Thoresen M., Whitelaw A., Azzopardi D. (2010). Neurological outcomes at 18 months of age after moderate hypothermia for perinatal hypoxic ischaemic encephalopathy: synthesis and meta-analysis of trial data. Br. Med. J., 340, 363.
19. Elmandy H., El-Machad A.R., El-Bahrawy H., El-Gohary T., El-Barbary A., Aly H. (2010). Pediatrics. Human recombinant erythropoietin in asphyxia neonatorum: pilot trial. Pediatrics, 125 (5), 1135-1142.
20. Fan X., Kavelaars A., Heijnen C.J., Groenendaal F., van Bel F. (2010). Pharmacological neuroprotection after perinatal hypoxic-ischemic brain injury. Curr. Neurophar-macol, 8 (4), 324-334.
21. Field D., Juszczak E., Linsell L. (2013). Neonatal ECMO study of temperature (NEST): a randomized controlled trial. Pediatrics, 132, e1247-e1256.
Neonatal ECMO study of temperature (NEST): a randomized controlled trial. Pediatrics, 132, e1247-e1256.
22. Frymoyer A., Lee S., Bonifacio S.L., Meng L., Lucas S.S., Guglielmo B.J., Sun Y., Verotta D. (2013). Every 36-h gentamicin dosing in neonates with hypoxic-ischemic encephalopathy receiving hypothermia.J. Perinatol., 33, 778-782.
23. Gonzales-Portillo G.S., Reyes S., Aguirre D. (2014). Stem cell therapy for neonatal hypoxic-ischemic encephalopathy. Front. Neurol., 5, 147.
24. Hellstrom-Westas L., Rosén I., de Vries L.S., Greisen G. (2006). Amplitude-integrated EEG classification and interpretation in preterm and term infants. NeoReviews, 7 (2), 76-87.
25. Hill A., Volpe J. J. (1994). Neurologic disorders. In: Avery G.B, Fletcher M.A, MacDonald M.G. (eds.). Neonatology: Pathophysiology and management of the newborn. Philadelphia NY, 1117-1138.
J. (1994). Neurologic disorders. In: Avery G.B, Fletcher M.A, MacDonald M.G. (eds.). Neonatology: Pathophysiology and management of the newborn. Philadelphia NY, 1117-1138.
26. Holmes G.L. (2005). Effects of seizures on brain development: lessons from the laboratory. Pediatr. Neurol., 33 (1), 1-11.
27. Huang B.Y., Castillo M. (2008). Hypoxic-ischemic brain injury: imaging findings from birth to adulthood. Radiographics, 28 (2), 417-439.
28. Jacobs S.E., Berg M., Hunt R. (2013). Cooling for newborns with hypoxic ischaemic encephalopathy. Cochrane Database Syst. Rev., 1, CD003311.
29. Jeanie L.Y., Cheong J.L., Coleman L., Hunt R.W., Lee K.J., Doyle L.W., Inder T.E., Jacobs S. E. (2012). Prognostic utility of magnetic resonance imaging in neonatal hypoxic-ischemic encephalopathy: substudy of a randomized trial. Arch. Pediatr. Adolesc. Med., 166, 634-640.
E. (2012). Prognostic utility of magnetic resonance imaging in neonatal hypoxic-ischemic encephalopathy: substudy of a randomized trial. Arch. Pediatr. Adolesc. Med., 166, 634-640.
30. Jing L., Yue S. (2010). Clinical characteristics, diagnosis and management of respiratory distress syndrome in full-term neonates. Chin. Med. J., 123 (19), 2640-2644.
31. Kecskes Z., Healy G., Jensen A. (2005). Fluid restriction for term infants with hypoxic-ischaemic encephalopathy following perinatal asphyxia. Cochrane Database Syst. Rev., CD004337.
32. Liu J., Li J., Gu M. (2007). The correlation between myocardial function and cerebral hemodynamics in term infants with hypoxic-ischemic encephalopathy. J. Trop. Pediatr., 53 (1), 44-48.
33. Massaro A.N., Chang T., Kadom N., Tsuchida T., Scafidi J., Glass P., McCarter R., Baumgart S., Vezina G., Nelson K.B. (2012). Biomarkers of brain injury in neonatal encephalopathy treated with hypothermia. J. Pediatr., 161 (3). 434-440.
Massaro A.N., Chang T., Kadom N., Tsuchida T., Scafidi J., Glass P., McCarter R., Baumgart S., Vezina G., Nelson K.B. (2012). Biomarkers of brain injury in neonatal encephalopathy treated with hypothermia. J. Pediatr., 161 (3). 434-440.
34. Murray D.M., Boylan G.B., Ryan C.A., Connolly S. (2009). Early EEG findings in hypoxic-ischemic encephalopathy predict outcomes at 2 years. Pediatrics, 124, 459-467.
35. Natarajan G., Shankaran S., Laptook A.R., Pappas A., Bann C.M., McDonald S.A., Das R., Higgins D., Hintz S.R., Vohr B.R. (2013). Apgar scores at 10 min and outcomes at 6-7 years following hypoxic-ischaemic encephalopathy. Arch. Dis. Child Fetal Neonatal Ed., 98, 473-479.
36. Perlman J.M. (2006). Intervention strategies for neonatal hypoxic-ischemic cerebral injury. Clin. Ther., 28 (9), 1353-1365.
Clin. Ther., 28 (9), 1353-1365.
37. Pin T.W., Eldridge B., Galea M.P. (2009). A review of developmental outcomes of term infants with post-asphyxia neonatal encephalopathy. Eur. J. Paediatr. Neurol., 13 (3), 224-234.
38. Pressler R.M., Boylan G.B., Morton M., Binniea C.D., Rennieb J.M. (2001). Early serial EEG in hypoxic ischaemic encephalopathy. Clin. Neurophys., 112, 31-37.
39. Rutherford M., Ramenghi L.A., Edwards A.D., Brocklehurst P., Halliday H., Levene M., Strohm B., Thoresen M., Whitelaw A.D. (2010). Assessment of brain tissue injury after moderate hypothermia in neonates with hypoxic-ischaemic encephalopathy: a nested substudy of a randomised controlled trial. Lancet Neurol., 9, 39-45.
40. Sabir H., Jary S., Tooley J., Liu X., Thoresen M. (2012). Increased inspired oxygen in the first hours of life is associated with adverse outcome in newborns treated for perinatal asphyxia with therapeutic hypothermia. J. Pediatr., 161 (3), 409-416.
Sabir H., Jary S., Tooley J., Liu X., Thoresen M. (2012). Increased inspired oxygen in the first hours of life is associated with adverse outcome in newborns treated for perinatal asphyxia with therapeutic hypothermia. J. Pediatr., 161 (3), 409-416.
41. Sarnat H.B., Sarnat M.S. (1976). Neonatal encephalopathy following fetal distress: A clinical and electro-encphalographic study. Arch. Neur., 33, 696-705.
42. Shah P. (2010). Hypothermia: a systematic review and meta-analysis of clinical trials. Seminars in Fetal and Neonatal Medicine, 15 (5), 238-246.
43. Shankaran S., Barnes P.D., Hintz S.R. (2012). Brain injury following trial of hypothermia for neonatal hypoxic-ischaemic encephalopathy. Arch. Dis. Child Fetal Neonatal Ed., 97, 398-404.
44. Shankaran S., Pappas A., McDonald S.A. (2011). Predictive value of an early amplitude integrated electroencephalogram and neurologic examination. Pediatrics, 128, 112-120.
Shankaran S., Pappas A., McDonald S.A. (2011). Predictive value of an early amplitude integrated electroencephalogram and neurologic examination. Pediatrics, 128, 112-120.
45. Shankaran S., Pappas A., Scott A., McDonald S.A., Vohr B.R., Hintz S.R., Epi M.S., Yolton K., Gustafson K.E., Theresa M. (2012). Childhood outcomes after hypothermia for neonatal encephalopathy. N. Engl. J. Med., 36, 2085-2092.
46. Shellhaas R.A., Ng C.M., Dillon C.H., Barks J.D., Bhatt-Mehta V. (2013). Population pharmacokinetics of phenobarbital in infants with neonatal encephalopathy treated with therapeutic hypothermia. Pediatr. Crit. Care Med, 14, 194-202.
47. Thoresen M., Hellström-Westas L., Liu X., de Vries L.S. (2010). Effect of hypothermia onamplitude-integrated electroencephalogram in infants with asphyxia. Pediatrics, 126, 131-139.
Pediatrics, 126, 131-139.
48. Thoresen M., Tooley J., Liu X., Jary S., Fleming P., Luyt K., Jain A., Cairns P., Harding D., Sabir H. (2013). Time is brain: starting therapeutic hypothermia within three hours after birth improves motor outcome in asphyxiated newborns. Neonatology, 104, 228-233.
49. Traudt C.M., McPherson R.J., Bauer L.A. (2013). Concurrent erythropoietin and hypothermia treatment improve outcomes in a term nonhuman primate model of perinatal asphyxia. Dev. Neurosci., 35, 491-503.
50. Vohr B.R., Stephens B.E., McDonald S.A. (2013). Cerebral palsy and growth failure at 6 to 7 years. Pediatrics, 132, 905-914.
51. Zanelli S.A., Stanley D.P., Kaufman D. (2012). Hy-poxicischemic encephalopathy [Электронный ресурс]. Available at: http://emedicine.medscape.com/article/973501 (date of access: 25.09.2012).
Hy-poxicischemic encephalopathy [Электронный ресурс]. Available at: http://emedicine.medscape.com/article/973501 (date of access: 25.09.2012).
Кузбасская научная медицинская библиотека — Пальчик, А. Б. Гипоксически-ишемическая энцефалопатия новорожденных / А. Б. Пальчик, А. П. Шабалов. — 5-е изд., испр. и доп. — Москва : МЕДпресс-информ, 2020.
Ввведение
Глава I. Эпидемиология и факторы риска возникновения гипоксически-ишемической энцефалопатии
Глава II. Этиология и патогенез гипоксическиишемической энцефалопатии
Глава III. Основные механизмы нейрохимических нарушений при гипоксически-ишемических поражениях головного мозга у новорожденных
Глава IV. Основные представления о патоморфологии гипоксических поражений головного мозга у новорожденных
Глава V. Морфофункциональные изменения в нейронных сетях при гипоксии и ишемии (модификация нейронов): пластичность и регенерация
Глава VI.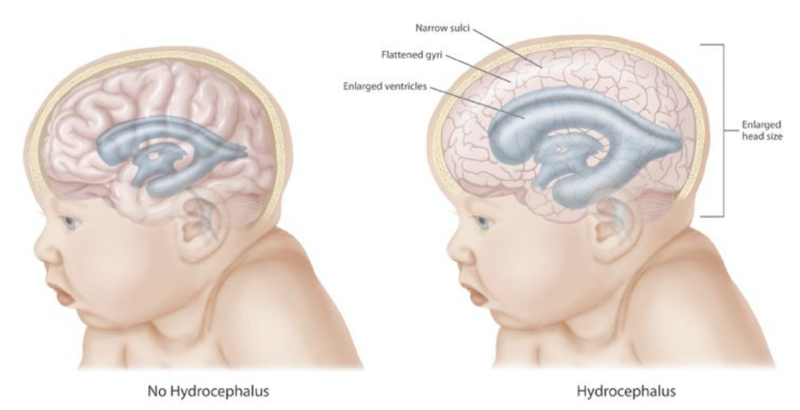 Клиническая картина гипоксически-ишемических поражений головного мозга новорожденных
Клиническая картина гипоксически-ишемических поражений головного мозга новорожденных
6.1 Нормальный и девиантный неврологический статус новорожденного
6.2 Классификации гипоксической энцефалопатии (фазовый принцип)
6.3 Классификации перинатальных поражений нервной системы (синдромологический принцип)
6.4 Особенности ряда синдромов гипоксических поражений мозга у новорожденных
6.4.1 Синдром угнетения центральной нервной системы
6.4.2 Синдром повышенной нервно-рефлекторной возбудимости
6.4.3 Синдром внутричерепной гипертензии. Гидроцефальный синдром
6.4.4 Судорожный синдром
6.4.5 Кома
6.4.6 Синдром двигательных расстройств
6.5 Клинические особенности гипоксических поражений головного мозга у недоношенных детей
6.6 Течение гипоксических поражений головного мозга и клиническая картина восстановительного периода
Глава VII. Диагностика гипоксически-ишемических поражений мозга у новорожденных
7. 1 Клиническая диагностика
1 Клиническая диагностика
7.1.1 Схемы неврологического обследования новорожденного
7.1.2 Шкала оценки поведения новорожденного T.B.Brazelton
7.1.3 Неврологическая оценка доношенного новорожденного, по H.F.R.Prechtl
7.1.4 Французская схема неврологического осмотра новорожденного
7.1.5 Неврологическая оценка новорожденного
7.1.6 Скрининг-схемы оценки состояния нервной системы новорожденного (профиль угнетения-раздражения)
7.2 Ультразвуковая диагностика
7.2.1 Нейросонография
7.2.2 Доиплерография
7.3 Аксиальная компьютерная томография
7.4 Магнитно-резонансная томография
7.5 Позитронно-эмиссионная томография
7.6 Околоинфракрасная спектроскопия
7.7 Магнитно-резонансная спектроскопия
7.8 Определение величины внутричерепного давления
7.9 Нейрофизиологическая диагностика
7.9.1 Электроэнцефалография
7. 9.1.1 Рутинная ЭЭГ
9.1.1 Рутинная ЭЭГ
7.9.1.2 ЭЭГ-картирование
7.9.1.3 Низкочастотная ЭЭГ, или ЭЭГ полного диапазона
7.9.1.4 Суммарная (амплитудная) ЭЭГ и мониторинг мозговой активности
7.9.1.5 Полиграфия
7.9.2 Вызванные потенциалы головного мозга
7.9.2.1 Слуховые стволовые вызванные потенциалы
7.9.2.2 Соматосенсорные вызванные потенциалы
7.9.2.3 Зрительные вызванные потенциалы
7.9.3 Электромиография и электронейромиография
7.10 Видеозапись спонтанной двигательной активности плода, новорожденного и грудного ребенка
7.11 Биохимическая диагностика
Глава VIII. Прогноз при перинатальных поражениях головного мозга гипоксического генеза
Глава IX. Лечение и профилактика
9.1 Лечение в остром периоде гипоксических поражений головного мозга новорожденных
9.2 Лечение последствий гипоксических поражений головного мозга новорожденных
9. 3 Профилактика гипоксических поражений головного мозга у новорожденных
3 Профилактика гипоксических поражений головного мозга у новорожденных
Глава X. Некоторые актуальные проблемы в представлениях о гипоксических поражениях головного мозга новорожденных
10.1 Границы понятий гипоксических поражений головного мозга новорожденных, гипоксически-ишемической и неонатальной энцефалопатии
10.2 Сравнительная характеристика классификаций гипоксических поражений головного мозга у новорожденных
10.3 Границы понятий нормального и девиантного неврологического статуса новорожденного и ребенка раннего возраста
10.4 Проблемы диагностики гипоксических поражений головного мозга новорожденных
10.5 Корректность лечения гипоксических поражений головного мозга новорожденных
10.6 Взаимоотношение теоретической науки, нейронауки и клинической неонатальной неврологии
Заключение
Энцефалопатия головного мозга у детей
Энцефалопатия головного мозга у детей. Гипоксически-ишемическая энцефалопатия у новорожденных.
Гимранов Ринат Фазылжанович
Невролог, нейрофизиолог, стаж — 33 года;
Профессор неврологии, доктор медицинских наук;
Клиника восстановительной неврологии.Об авторе
Дата публикации: 30 января, 2020
Обновлено: 25 марта, 2021
Рождение малыша – большой праздник для его родителей, но далеко не всегда долгожданный ребенок оказывается полностью здоров. Все чаще у новорожденных и детей до года встречается патология – энцефалопатия головного мозга, диагностика и лечение которой затруднены невыраженными симптомами и признаками, а последствия не оказанной своевременно помощи, бывают тяжелыми: эпилепсия, паралич, смерть.
Все чаще у новорожденных и детей до года встречается патология – энцефалопатия головного мозга, диагностика и лечение которой затруднены невыраженными симптомами и признаками, а последствия не оказанной своевременно помощи, бывают тяжелыми: эпилепсия, паралич, смерть.
Заболевание представляет собой не инфекционное поражение тканей головного мозга. Из-за аномалии или гибели нейронов нарушается деятельность ЦНС. Перестают развиваться отделы, отвечающие за когнитивные функции.
Детская энцефалопатия – грозный диагноз, но не всегда окончательный приговор. Если отклонение в развитии обнаружено своевременно, то при лечении есть шанс на выздоровление.
Содержание статьи:
Причины
Глубина поражения мозговых клеток зависит от снабжения этого важнейшего органа кислородом через систему кровообращения. Помешать этому может масса факторов:
- Инфекции, перенесенные матерью в период беременности.
- Травмы, полученные во время родов.
 При родовспоможении, бывает, страдает головной и спинной мозг, особенно опасными считаются ЧМТ.
При родовспоможении, бывает, страдает головной и спинной мозг, особенно опасными считаются ЧМТ.
- Хронические болезни матери.
- Слишком большие размеры и вес плода. Это затрудняет роды, увеличивает время рождения, что приводит к гипоксии.
- Отравления матери и плода тяжело влияют на формирующуюся ЦНС. Подобная ситуация создается при приеме лекарственных препаратов, курении, употреблении алкоголя или наркотиков во время беременности.
- Неблагоприятные экологические условия в месте проживания также играют свою негативную роль.
Патологические роды – главная по частоте причина детских энцефалопатий. Пережатие пуповины, обвитие ее вокруг шейки младенца, приводят к тяжелой гипоксии мозга.
Лечится ли энцефалопатия головного мозга у новорожденных и детей до 1 года зависит от того, какие симптомы проявились и какими причинами была вызвана.
Пластичность и запас прочности мозга у младенцев создают предпосылки для восстановления нервных функций. Нужно только помочь деткам.
Нужно только помочь деткам.
Классификация
Детям до 1 года часто ставят диагноз неуточненная энцефалопатия, что это такое понять просто: врачи не могут сразу установить причину развития дегенеративных явлений в мозгу. Но в большинстве случаев удается выяснить из-за чего развилась болезнь. При этом опираются на симптомы и вероятную причину патологии.
Выделяют несколько распространённых типов:
- Гипоксически-ишемическая энцефалопатия у новорожденного ребенка – грудничка означает, что малышу не хватало кислорода, это в период перед родами опасно. Диагностируется сразу после рождения, проявляется в расстройствах возбудимости нервной системы с первых дней жизни. Проявления варьируют от судорог до комы.
- Эпилептический тип. Характеризуется приступами эпилепсии, судорогами, во время которых из-за аномальной электроактивности ЦНС гибнут нейроны. Это приводит к развитию отклонений в поведении ребенка, торможению его развития.

- Билирубиновый тип возникает при чрезмерном содержании в крови белка – билирубина, что проявляется желтухой, сопровождается вялостью. Рефлексы проявляются слабо, со склонностью к угасанию;
- Резидуальный вариант вызван инфекциями, развившимися в первые дни жизни. Типичным признаком являются головные боли, отставание в неврологическом развитии.
- Сосудистая энцефалопатия провоцируется врожденными или приобретенными проблемами с кровообращением сосудов шеи и черепной коробки. Подобные нарушения приводят к хроническому кислородному голоданию, постепенному отмиранию клеток мозга. Проявлениями являются перепады настроения, приступы неадекватного поведения.
- Травматическая энцефалопатия у новорожденного грудничка значит, что он получил повреждение во время родов или сразу после. Травма негативно воздействовала на созревание, затруднила кровообращение в шейном отделе позвоночника. Выражается в задержке развития, нестандартном поведении, расстройстве сна.

Гипоксически-ишемическая и травматическая энцефалопатия у детей обнаруживаются в первые месяцы жизни по типичным симптомам, затем проводится уточняющая диагностика.
Лечение начинают после того, как предварительные выводы специалистов подтвердятся.
Диагностика
Наиболее распространенный тип – постгипоксическая энцефалопатия у новорожденных детей.
Это последствия нехватки кислорода из-за слишком затянувшихся родов или переношенной беременности.
Также от нехватки кислорода зародыш может страдать еще в утробе, если мать регулярно курит или подвергается пассивному курению.
При постановке диагноза используются аппаратные методы и анализы для оценки состояния коры головного мозга, состоятельности кровеносной системы:
- Анализ крови на уровень билирубина.
- Допплерография – исследование кровотока сосудов шеи и головы с помощью УЗИ.
- Электроэнцефалография, позволяющая оценить степень активности работы мозга.

- Нейросонография – вариант процедуры УЗИ мозга или эхоэнцефалографии. В качестве «окна» используется родничок, врачи могут оценить состояние мозга, скопления спинномозговой жидкости, изменения структуры, крупные кровоизлияния.
После получения результатов, врачи, в зависимости от состояния малыша, подбирают методы лечения.
Лечение
Как вылечить энцефалопатию у ребенка и возможно ли это, – решает врач после проведения анализов и установления формы заболевания, его тяжести.
Для избавления от последствий болезни потребуется комплексная терапия. Включающая медикаменты и физиотерапевтические процедуры.
Даже тяжелые первоначально младенцы, благодаря адекватной терапии и уходу, способны восстанавливать нервную деятельность. И к возрасту детского сада ничем не отстают от сверстников.
Схема лечения назначается строго каждому пациенту, в зависимости от состояния новорожденного и причин патологии.
Используются медикаменты следующих категорий:
- вазодилататоры, расширяющие сосуды;
- ноотропы, улучшающие проводимость нейронов;
- антиконвульсанты, для снятия приступов судорог;
- психолептики, снимающие гипервозбудимость.
В остром периоде гипоксии и сразу после него, может быть полезным применение нейропротекторов. Это вещества, повышающие выживаемость нейронов в условиях дефицита кислорода.
Также потребуется проходить курсы физиотерапии:
- лечебный массаж;
- лекарственный электрофорез;
- амплипульстерапия.
Результаты лечения зависят от первоначальной степени тяжести болезни. Если синдром проявлялся в легкой форме, то возможно его вылечить полностью.
Детская энцефалопатия 2 и 3 тяжести приводят к развитию тяжелых осложнений, стойкому неврологическому дефициту. К сожалению, нарушения бывают и не совместимы с дальнейшей жизнью. Но такие случаи носят эпизодический характер.
Но такие случаи носят эпизодический характер.
Была ли эта статья полезна?
Вы можете подписаться на нашу рассылку и узнать много интересного о лечение заболевания, научных достижений и инновационных решений:
ДОБАВИТЬ/ПОСМОТРЕТЬ КОММЕНТАРИИ
Гимранов Ринат Фазылжанович
https://newneuro.ru/wp-content/uploads/2018/12/logo-e1544205275245.png
Записаться к специалисту
×
Перинатальная энцефалопатия: причины, симптомы и лечение
Перинатальная энцефалопатия — целый ряд заболеваний (отклонений в работе) центральной нервной системы у новорожденных. Заболевание может проявляться по-разному, а потому его весьма непросто диагностировать, особенно у младенцев. С этим и связан тот факт, что симптомы энцефалопатии зачастую расцениваются педиатрами как признаки совсем других заболеваний. В итоге лечению заболевания не уделяется необходимого внимания в раннем возрасте, когда наиболее велика вероятность полного выздоровления. Прогрессирующее заболевание при взрослении ребенка зачастую также диагностируется симптоматически, и лечение назначается соответствующее.
Заболевание может проявляться по-разному, а потому его весьма непросто диагностировать, особенно у младенцев. С этим и связан тот факт, что симптомы энцефалопатии зачастую расцениваются педиатрами как признаки совсем других заболеваний. В итоге лечению заболевания не уделяется необходимого внимания в раннем возрасте, когда наиболее велика вероятность полного выздоровления. Прогрессирующее заболевание при взрослении ребенка зачастую также диагностируется симптоматически, и лечение назначается соответствующее.
Избавление от ПЭП без остеопатического воздействия на первопричины возникновения заболевания, если не полностью невозможно (все-таки организм является саморегулирующей системой, которая вполне способна справиться с рядом серьезных заболеваний), то существенно затруднено. Конечно, не следует пренебрегать и другими методами лечения — как показывает практика, наиболее эффективны как раз комплексные процедуры.
Симптомы и последствия перинатальной энцефалопатии
Симптомы заболевания проявляются по-разному в различные периоды жизни ребенка. Для простоты классификации и улучшения диагностики принято выделять три основных периода ПЭП: острый (в течение первого месяца жизни), восстановительный (до 1 года, реже до 2 лет — в основном у недоношенных детей) и исход заболевания. Существует вероятность, что организм ребенка — как саморегулирующая система, с точки зрения остеопатии, — может полностью восстановиться и нейтрализовать симптомы болезни, адаптировавшись к ним. Это не означает полного выздоровления, так как последствия ПЭП могут проявиться в более позднем возрасте. Поэтому при возникновении подозрений на заболевание необходимо сразу же показать ребенка врачу-остеопату, который сможет поставить правильный диагноз и назначить грамотное адекватное лечение, направленное на избавление организма не от последствий, а от причин болезни.
Для простоты классификации и улучшения диагностики принято выделять три основных периода ПЭП: острый (в течение первого месяца жизни), восстановительный (до 1 года, реже до 2 лет — в основном у недоношенных детей) и исход заболевания. Существует вероятность, что организм ребенка — как саморегулирующая система, с точки зрения остеопатии, — может полностью восстановиться и нейтрализовать симптомы болезни, адаптировавшись к ним. Это не означает полного выздоровления, так как последствия ПЭП могут проявиться в более позднем возрасте. Поэтому при возникновении подозрений на заболевание необходимо сразу же показать ребенка врачу-остеопату, который сможет поставить правильный диагноз и назначить грамотное адекватное лечение, направленное на избавление организма не от последствий, а от причин болезни.
Основные симптомы перинатальной энцефалопатии
В острый период развития заболевания наблюдаются:
- синдром угнетения ЦНС. Характеризуется общей вялостью новорожденных, сниженной реакцией на внешние раздражители, наличием спонтанных двигательных рефлексов;
- коматозный синдром.
 Обычно развивается быстро и внезапно, вызывая бессознательное состояние у ребенка. Может проявляться в остром нарушении жизненно важных функций организма;
Обычно развивается быстро и внезапно, вызывая бессознательное состояние у ребенка. Может проявляться в остром нарушении жизненно важных функций организма; - повышенная нервно-рефлекторная возбудимость. Проявляется в виде тремора конечностей и ненормально-возбужденной реакцией на внешние раздражители;
- повышенное черепное давление с последующим гипертензионно-гидроцефальным синдромом и непропорциональным увеличением размера черепа;
- судороги.
В восстановительный период к этим симптомам могут добавляться:
- двигательные нарушения. Проявляются по-разному, но общим является то, что ребенок полностью или частично не контролирует свои движения;
- задержка психомоторного развития (ЗПР). Проявляется в замедленном развитии, проблемах с речью, нарушении памяти, проблемах с вниманием и т.д.;
- эпилептические припадки.
Признаки заболевания могут проявляться как комбинированно, так и поодиночке. Причем в разном возрасте. При обнаружении хотя бы одного симптома рекомендуется обратиться к специалисту-остеопату для проведения более детального обследования.
Причем в разном возрасте. При обнаружении хотя бы одного симптома рекомендуется обратиться к специалисту-остеопату для проведения более детального обследования.
Исходом заболевания могут быть:
- выздоровление;
- минимальная мозговая дисфункция;
- умственное недоразвитие;
- ДЦП;
- невротические заболевания;
- эпилепсия;
- гидроцефалия.
Как показывает практика, при легких формах перинатальной энцефалопатии вероятность полного выздоровления достаточно велика. Особенно при правильном остеопатическом лечении, которое может сочетаться с другими методами воздействия на детский организм.
При более тяжелой форме понадобится более длительное лечение, которое в силу различных факторов может не иметь стопроцентной результативности. Некоторые проблемы с памятью, вниманием, координацией движений у ребенка могут сохраняться как в течение длительного периода, так и на протяжении всей жизни. Но остеопатия способствует если и не полному излечению, то существенной минимизации симптомов перинатальной энцефалопатии.
Но остеопатия способствует если и не полному излечению, то существенной минимизации симптомов перинатальной энцефалопатии.
Факторы риска
К факторам риска, повышающим опасность возникновения заболевания, относятся:
- хронические болезни матери. Зачастую они не передаются ребенку напрямую, так как не являются наследственными, но на генетическом уровне обуславливают проявления различных патологий и отклонений в развитии плода и уже родившегося ребенка;
- инфекционные заболевания, перенесенные во время беременности. Очень опасны недолеченные патологии, которые могут проявиться на фоне общего ослабления иммунитета организма из-за беременности;
- неправильное питание. В период вынашивания плода организм матери должен получать весь необходимый набор белков, витаминов и минеральных веществ. Питание должно быть сбалансированным и согласовываться с врачом — во избежание возникновения пищевой аллергии и расстройств органов пищеварения;
- слишком молодой возраст матери.
 Организм девушки может быть просто неготовым к вынашиванию полноценного и здорового ребенка. В случае слишком юного возраста или недостаточного физического развития будущей матери она должна находиться под постоянным контролем специалиста в течение всего периода беременности и после родов;
Организм девушки может быть просто неготовым к вынашиванию полноценного и здорового ребенка. В случае слишком юного возраста или недостаточного физического развития будущей матери она должна находиться под постоянным контролем специалиста в течение всего периода беременности и после родов; - нарушение обмена веществ в организме матери. Так как ее организм тесно взаимосвязан с организмом будущего ребенка, любые нарушения отражаются на питании и здоровье плода. Поэтому столь важно правильное питание, о котором говорилось ранее, а также безотказная работа органов, отвечающих за обмен веществ в организме;
- патологии во время беременности. Очень опасны ранние и поздние токсикозы, стрессы, физические нагрузки и другие факторы, которые могут привести к прерыванию и ненормальному течению беременности;
- неблагоприятная экологическая обстановка. К сожалению, сегодня этот фактор опаснее многих других, ведь избежать воздействия вредных внешних проявления зачастую невозможно.
 Рекомендуется обратиться к специалистам (в том числе и остеопату), которые помогут в значительной мере нейтрализовать неблагоприятное воздействие окружающей среды;
Рекомендуется обратиться к специалистам (в том числе и остеопату), которые помогут в значительной мере нейтрализовать неблагоприятное воздействие окружающей среды; - недоношенность или переношенность плода.
- Таким образом, большинство факторов риска связаны
именно со здоровьем матери. Поэтому в период беременности она должна тщательно следить за своим самочувствием, прислушиваясь к совету хорошего врача. Параллельно с другими специалистами рекомендуется регулярно посещать остеопата, который также будет следить за ходом протекания беременности и сможет скорректировать вероятные отклонения остеопатическими методами, без применения лекарств, способных навредить будущему ребенку.
Опасность перинатальной энцефалопатии
Как и многие другие младенческие заболевания, не будучи вылеченной на ранних стадиях, перинатальная энцефалопатия прогрессирует с возрастом и может проявляться в виде самых различных нарушений, которые на первый взгляд покажутся не связанными:
- синдром частой заболеваемости.
 Это могут быть как частые простуды, так и периодические недомогания, связанные с плохим самочувствием, повышенной утомляемостью, головными болями и т.д.;
Это могут быть как частые простуды, так и периодические недомогания, связанные с плохим самочувствием, повышенной утомляемостью, головными болями и т.д.; - хронические заболевания дыхательной системы. Могут проявляться на фоне частых ОРЗ, постепенно переходя в хроническую форму. При отсутствии грамотного остеопатического лечения с возрастом могут перерасти в астму и другие не менее опасные заболевания;
- отставание в развитии. Могут проявляться в не очень явной форме, как затруднения в учебе, особенно в точных науках и творческих дисциплинах;
- нарушения осанки. Незаметные родовые травмы и нарушения в работе ЦНС, возникшие еще на этапе беременности, в дальнейшем нередко приводят к искривлению позвоночника и появлению таких серьезных заболеваний, как сколиоз, со всеми вытекающими из него последствиями, влекущими опускание внутренних органов и их частичную или полную дисфункцию;
- нарушения в работе внутренних органов, системы обмена веществ и системы кровообращения.
 Обычно эти нарушения неизменно влекут за собой другие заболевания, так как из-за нарушенного кровотока различные участки организма начинают недополучать кислород, что приводит к гибели клеток и дисфункции.
Обычно эти нарушения неизменно влекут за собой другие заболевания, так как из-за нарушенного кровотока различные участки организма начинают недополучать кислород, что приводит к гибели клеток и дисфункции.
Как расценивают перинатальную энцефалопатию специалисты-остеопаты
С точки зрения остеопатии весь комплекс заболеваний ЦНС, объединяемых под этим термином, является последствием механических нарушений в теле плода новорожденного ребенка. Причем возникнуть они могут еще на этапе беременности или позже — при сложных родах и/или кесаревом сечении. Причинами, приводящими к появлению заболевания, являются:
- дисфункция позвоночного столба или отдельных его участков;
- нарушения в работе внутренних органов;
- продолжительное кислородное голодание;
- нарушение кровообращения.
Но даже в том случае, если во время беременности плод развивался нормально, существует большая вероятность получения повреждения во время родов, так как, проходя между костями таза, плод поворачивается на 360 градусов, что может вызвать нарушения в структуре скелета, мышечных тканях. Наиболее часто наблюдается нарушения в положении шейных позвонков. В большинстве случаев в первые недели роста ребенка последствия повреждений полностью нейтрализуются организмом самостоятельно. Но так бывает далеко не всегда, любые изменения или отклонения в развитии могут привести к осложнениям, которые впоследствии спровоцируют нарушения кровоснабжения мозга и проявление перинатального расстройства.
Наиболее часто наблюдается нарушения в положении шейных позвонков. В большинстве случаев в первые недели роста ребенка последствия повреждений полностью нейтрализуются организмом самостоятельно. Но так бывает далеко не всегда, любые изменения или отклонения в развитии могут привести к осложнениям, которые впоследствии спровоцируют нарушения кровоснабжения мозга и проявление перинатального расстройства.
Как диагностируется перинатальная энцефалопатия у новорожденных и младенцев
Существует ряд безопасных методов исследования головного мозга, которым могут подвергаться новорожденные. Они позволяют составить полную клиническую картину, определить наличие заболевания, его степень, характер течения. Наиболее информативной и эффективной является нейросонография, которая точно выявляет наличие поврежденных участков в мозгу младенца. Дополнительно к ней можно провести доплерографию — для оценки кровотока в сосудах головного мозга.
В случае выявления отклонений в развитии рекомендуется пройти электроэнцефалографическое обследование, направленное на определение степени задержки в развитии. Эта процедура также позволяет выявить очаги эпилептического поражения и оценить степень их активности и опасности для организма.
Эта процедура также позволяет выявить очаги эпилептического поражения и оценить степень их активности и опасности для организма.
В некоторых случаях также рекомендуется осмотр окулиста, который поможет выяснить степень поражения путем оценки состояния зрительных нервов и анализа глазного дна.
Лечение энцефалопатии остеопатическими методами
Хороший врач-остеопат способен диагностировать ранние симптомы заболевания и составить полную картину его течения. Это дает возможность назначить грамотное лечение, способствующее адаптации организма к новым условиям, запуску и стимуляции его функций саморегулирования.
Воздействия остеопата — в зависимости от течения и сложности заболевания — направляются, в первую очередь, на пораженные участки тела, чтобы снять болевые ощущения и спазмы, образующиеся в результате неправильного развития и нарушений в системе кровообращения. Параллельно с этим специалист осуществляет комплекс процедур с целью нормализации работы мозга. Обычно для этого применяются различные техники мышечно-энергетического воздействия, которые позволяют мануальным путем восстановить равновесие натяжения внутричерепных оболочек. Это способствует восстановлению микропульсаций костей черепа и самого мозга, нормализации кровообращения.
Обычно для этого применяются различные техники мышечно-энергетического воздействия, которые позволяют мануальным путем восстановить равновесие натяжения внутричерепных оболочек. Это способствует восстановлению микропульсаций костей черепа и самого мозга, нормализации кровообращения.
После нормализации мозговой деятельности организм получает мощный стимул к саморегуляции и избавлению от энцефалопатии. Дальнейшие действия остеопата заключаются в том, чтобы помочь телу малыша справиться с болезнью. Для этого применяется мануальная терапия, массаж, лечебная физкультура и другие методики, которые, по мнению специалиста, смогут помочь скорейшему выздоровлению.
Как показывает практика, перинатальная энцефалопатия у новорожденных излечивается полностью в 30% случаев — при раннем обнаружении и грамотном лечении. Еще примерно в 20–30% — обычно при тяжелых и среднетяжелых случаях течения — новорожденные излечиваются не полностью. Какие-то симптомы при этом остаются, но зачастую часть из них удается скорректировать комплексной терапией, включающей как ЛФК, остеопатию, массажные техники, так и особое воспитание, обучение и т.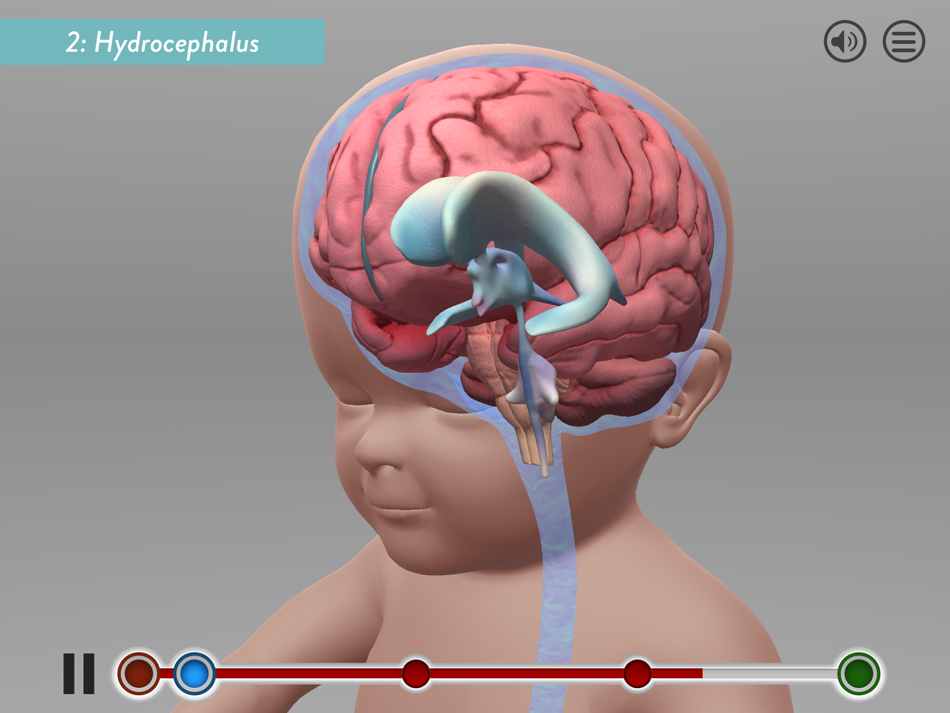 д.
д.
К сожалению, во многих случаях, когда перинатальная энцефалопатия проявляется в форме серьезного поражения клеток коры головного мозга, избавиться от заболевания невозможно. Причина в гибели клеток мозга и нарушении нейронных связей, которые не могут быть восстановлены из-за недостатка или отсутствия физических носителей в мозге ребенка. Даже в этих случаях остеопатия может помочь снять некоторые неврологические симптомы, но полное восстановление мозговой деятельности оказывается невозможным.
Важно, чтобы возможная энцефалопатия новорожденных диагностировалась на самых ранних стадиях развития — в первые месяцы жизни ребенка. Чтобы поспособствовать этому, рекомендуется посетить остеопата на 3 месяце жизни, для проведения полного обследования. Специалист назначит необходимые анализы и проведет самостоятельные осмотр, что в комплексе позволит обнаружить симптомы и выявить возможное наличие заболевания.
Нередко при обнаружении ПЭП врачи-педиатры советуют начинать медикаментозное лечение. Причем делать это необходимо с раннего младенческого возраста. Каждый родитель должен осознавать, что такой подход далеко не всегда действенен и способен скорее навредить ребенку. Дело в том, что организм новорожденного достаточно слаб, но при этом сбалансирован и способен к адаптации и саморегуляции. Воздействие на него сильнодействующих лекарств приводит к необратимым изменениям, которые даже остеопат не сможет нейтрализовать. Поэтому, если у ребенка диагностирована перинатальная энцефалопатия или имеются серьезные подозрения на ее наличие, рекомендуется пройти обследование также и у остеопата. Остеопатические техники более тонкие и деликатные, а потому — эффективные. Они точечно воздействуют на участки тела и мозга, нервную систему ребенка, приводя ее в нормальное состояние.
Причем делать это необходимо с раннего младенческого возраста. Каждый родитель должен осознавать, что такой подход далеко не всегда действенен и способен скорее навредить ребенку. Дело в том, что организм новорожденного достаточно слаб, но при этом сбалансирован и способен к адаптации и саморегуляции. Воздействие на него сильнодействующих лекарств приводит к необратимым изменениям, которые даже остеопат не сможет нейтрализовать. Поэтому, если у ребенка диагностирована перинатальная энцефалопатия или имеются серьезные подозрения на ее наличие, рекомендуется пройти обследование также и у остеопата. Остеопатические техники более тонкие и деликатные, а потому — эффективные. Они точечно воздействуют на участки тела и мозга, нервную систему ребенка, приводя ее в нормальное состояние.
Профилактика заболевания
Наиболее действенным методом профилактики является соблюдение матерью режима в период беременности. В большинстве случаев новорожденные отличаются хорошим здоровьем, если мама заботится о своем организме (а значит, и о малыше).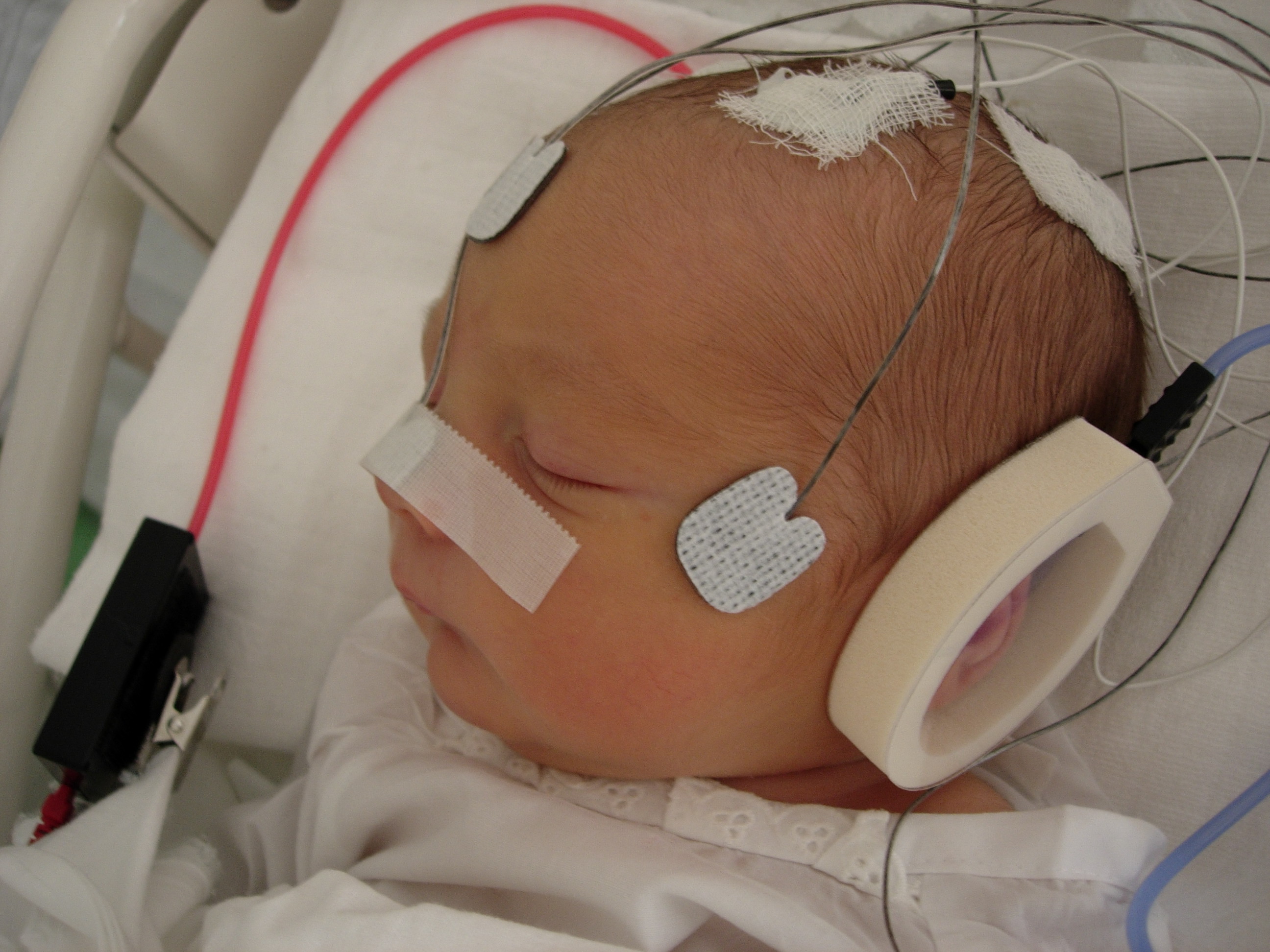 Также рекомендуется регулярное посещение врача-остеопата, который поможет следить за здоровьем в предродовой период.
Также рекомендуется регулярное посещение врача-остеопата, который поможет следить за здоровьем в предродовой период.
Очень важно и внимание к здоровью и состоянию ребенка в первые недели и месяцы его жизни. Любые отклонения в развитии, аномалии и патологии должны выявляться и фиксироваться специалистом для точной диагностики и лечения.
Энцефалопатия новорожденного — хотя и очень серьезный диагноз, но еще не приговор. Это заболевание вполне эффективно лечится.
процедуры связанные с заболеванием
Иммуннообусловленные эпилепсии у детей | Белоусова
1. Vezzani A., French J., Bartfai Т., Baram T.Z. The role of inflammation in epilepsy. Nat Rev Neurol 2011; 7: 1: 31 —40.
2. RiaziK., Galic M.A., Pittman Q.J. Contributions of peripheral inflammation to seizure susceptibilityxytokines and brain excitability. Epilepsy Res 2010; 89: 34-42.
RiaziK., Galic M.A., Pittman Q.J. Contributions of peripheral inflammation to seizure susceptibilityxytokines and brain excitability. Epilepsy Res 2010; 89: 34-42.
3. Ravizza Т., Balosso S., Aronica E., Vezzani A. Epilepsy: Mechanisms, Models, and Translational Perpsectives. J.M. Rho (ed). Boca Raton: CRC Press 2010; 45-59.
4. Armangue Т., Petit-PedrolM., Dalmau J. Autoimmune Encephalitis in Children. J Child Neurol 2012; 27:11:1460-1469.
5. Dalmau J. Clinical experience and laboratory investigations in patients with anti-NMDAR encephalitis. Lancet Neurol 2011; 10: 1:63-74.
6. Bien C.G., Vincent A. Immune-mediated pediatric epilepsies. In Handbook of Clinical Neurology, Vol. Ill (3rd series) Pediatric Neurology Part I. O. Dulac, M. Lassonde, H.B. Sarnat (eds). ElsevierB.V., 2013; 565.
Ill (3rd series) Pediatric Neurology Part I. O. Dulac, M. Lassonde, H.B. Sarnat (eds). ElsevierB.V., 2013; 565.
7. Haberlandt E., Bast Т., Ebner A. et al. Limbic encephalitis in children and adolescents. Arch Dis Child 2011; 96: 186-191.
8. Darnell R.B., PosnerJ.B. A new cause of limbic encephalopa-thy. Brain 2005; 128: 1745-1746.
9. Yu E.G., Lee J., Seo D. W., Lee M. Clinical Manifestations and Treatment Response of Steroid in Pediatric Hashimoto En-cephalopathy. J Child Neurol 2014; 29: 938-942.
10. Gul Mert G., Horoz O.O., Herguner M.O. et al. Hashimoto’s encephalopathy: four cases and review of literature. Inter J Neurosci 2014; 124: 4: 302-306.
11. OlmezL., Moses H., Sriram S. etal. Diagnostic and therapeutic aspects of Hashimoto’s encephalopathy. J Neurol Sci 2013; 331:67-71.
OlmezL., Moses H., Sriram S. etal. Diagnostic and therapeutic aspects of Hashimoto’s encephalopathy. J Neurol Sci 2013; 331:67-71.
12. Varadkar S., Bien C.G., Kruse C.A. et al. Rasmussen’s encephalitis: clinical features, pathobiology, and treatment advances. Lancet Neurol 2014; 13: 195-205.
13. Ramaswamy V, Walsh J.G., SinclairD.B. etal. Inflammasome induction in Rasmussen’s encephalitis: cortical and associated white matter pathogenesis. J Neuroinflammation 2013; 13: 10:152.
14. Wang D., Blumcke L., Gui Q. et al. Clinico-pathological investigations of Rasmussen encephalitis suggest multifocal disease progression and associated focal cortical dysplasia. Epileptic Disord2013; 15:1:32-43.
15. Dawodu CO., Akinbo D.D. Rasmussen’s encephalitis. Niger J ClinPract2013; 16: 1: 113-115.
Dawodu CO., Akinbo D.D. Rasmussen’s encephalitis. Niger J ClinPract2013; 16: 1: 113-115.
16. Pike M. Opsoclonus-myoclonus syndrome. In Handbook of Clinical Neurology, Vol. 112 (3rd series) Pediatric Neurology Part II O. Dulac, M. Lassonde, H.B. Sarnat (eds). Elsevier B.V, 2013; 1209-1211.
17. Байдун Л.В., Семыкина Л.И., Петрухин А.С. и др. Опсо-клонус-миоклонус-синдром у детей. Журн неврол и пси-хиат 2007; 2: 4-11. (Baidun L.V, Semikina L.I., Petruchin A.S. et al. Opsoclonus-myoclonus syndrome u detei. Zhurn Nevrol i Psikhiatr 2007; 2:4-11.)
18. SahuJ.K., Prasad K. Opsoclonus-myoclonus syndrome. Pract Neurol 2011; 11: 160-166.
19. Cross J.H. Fever and fever-related epilepsies. Epilepsia 2012; 53: Suppl 4: 3-8.
Epilepsia 2012; 53: Suppl 4: 3-8.
20. Сивкова М.Н., Богданов Э.И., Зайкова Ф.М. и др. Феб-рильно-обусловленная рефрактерная эпилептическая энцефалопатия у детей. Журн неврол и психиат 2013; 113: 6: 11—16. (Sivkova S.N., Bogdanov E.I., ZakovaF.M. et al. Fever-induced refractory epileptic encephalopathy of children. Zhurn Nevrol iPsikhiat 2013; 113: 6: 11-16.)
21. Auvin S., Bellavoine V, Merdariu D. et al. Hemiconvulsion-hemiplegia-epilepsy syndrome: Current understandings. Eur J Pediat Neurol 2012; 16: 5: 413-421.
22. Tenney J.R., Schapiro M.B. Child Neurology: Hemiconvulsion-hemiplegia-epilepsy syndrome. Neurology 2012; 79: el—e4.
НИЗКОТЕХНОЛОГИЧНАЯ ОБЩАЯ ЛЕЧЕБНАЯ ГИПОТЕРМИЯ У ДЕТЕЙ С ТЯЖЕЛОЙ ГИПОКСИЧЕСКИ-ИШЕМИЧЕСКОЙ ЭНЦЕФАЛОПАТИЕЙ НА ЭТАПАХ РОДДОМА, ТРАНСПОРТИРОВКИ И СПЕЦИАЛИЗИРОВАННОГО УЧРЕЖДЕНИЯ.
 МЕТОДИЧЕСКИЕ РЕКОМЕДАЦИИ | Задворнов
МЕТОДИЧЕСКИЕ РЕКОМЕДАЦИИ | Задворнов
Иванов, Д.О. Руководство по перинатологии /Иванов Д.О. – СПб.: Информ-Навигатор, 2015. – 1216 с.
Пальчик, А.В. Гипоксически-ишемическая энцефалопатия новорожденных /Пальчик А.В. – СПб.: Питер, 2000
Volpe, J.J. Neurology of newborn. 5th ed. /Volpe J.J. – Philadelphia: WB Saunders, 2008
Long-term clinical efficacy of mild hypothermia therapy in neonates with hypoxic-ischemic encephalopathy: a Meta analysis /Cao C.Q., Li Y.N., Yang X.M., Gong Y.G., Wang F., Li W.G. //Zhongguo Dang Dai Er Ke Za Zhi. – 2015. – V. 17(2). – P. 122-127
Cooling for newborns with hypoxic ischaemic encephalopathy /Jacobs S.E., Berg M., Hunt R., Tarnow-Mordi W.O., Inder T.E., Davis P.G. //Cochrane Database Syst. Rev. – 2013. – V. 31(1). – P. CD003311
Методика проведения лечебной гипотермии детям, родившимся в состоянии асфиксии /Антонов А.Г., Ионов О.В., Киртбая А.Р., Балашова Е.Н., Никитина И. В., Рындин А.Ю., Морошник Е.В., Дегтярев Д.Н. //Анестезиология и реаниматология. – 2014. – ¹ 6. – С. 76-77
В., Рындин А.Ю., Морошник Е.В., Дегтярев Д.Н. //Анестезиология и реаниматология. – 2014. – ¹ 6. – С. 76-77
Амплитудно-интегрированная электроэнцефалография и селективная церебральная гипотермия в неонатологической практике /Дегтярев Д.Н., Ионов О.В., Киртбая А.Р., Ушакова Л.В., Boone T., Амирханова Д.Ю., Кириллова Е.А., Никифоров Д.В. – М.: Локус Станди, 2013. – 60 с.
Протокол проведения лечебной гипотермии детям, родившимся в асфиксии /Ионов О.В., Балашова Е.Н., Киртбая А.Р., Антонов А.Г., Морошник Е.В., Дегтярев Д.Н. //Неонатология: новости, мнения, обучение. – 2014. – №2. – С. 81-83
Детская неврология: клинич. реком., вып. 3 /Гузеева В.И. и др. – М., 2015. – 336 с.
Иванов, Д.О. Нарушение теплового баланса у новорожденных детей. Приложение № 3, клинический протокол ведения новорожденных детей гестационного возраста 35 недель и более, перенесших тяжелую сочетанную и интранатальную асфиксию с использованием системной пассивной гипотермии для защиты мозга новорожденных с гипоксически-ишемической энцефалопатией /Иванов Д. О. – СПб.: Изд-во Н-Л, 2012
О. – СПб.: Изд-во Н-Л, 2012
Специализированная реанимация новорожденного /Надишаускене Р.Й. и др. – Литва: Центр исследования кризисов, Университет наук здоровья Литвы, 2012. – 396 с.
Infant Cooling Evaluation Collaboration. Whole-body hypothermia for term and near-term newborns with hypoxic-ischemic encephalopathy: a randomized controlled trial /Jacobs S.E., Morley C.J., Inder T.E. et al. //Arch. Pediat. Adolesc. Med. – 2011. – V. 165(8). – P. 692-700
National Institute of Child Health and Human Development Neonatal Research Network. Whole-body hypothermia for neonates with hypoxic-ischemic encephalopathy /Shankaran S., Laptook A.R., Ehrenkranz R.A., Tyson J.E., McDonald S.A., Donovan E.F. et al. //N. Engl. J. Med. – 2005. – V. 353(15). – P. 1574-1584
Selective head cooling with mild systemic hypothermia after neonatal hypoxic-ischemic encephalopathy: a multicenter randomized controlled trial in China /Zhou W.H., Cheng G.Q., Shao X. M., Liu X.Z., Shan R.B., Zhuang D.Y. et al. China Study Group. //J. Pediat. – 2010. – V. 157(3). – P. 367-372
M., Liu X.Z., Shan R.B., Zhuang D.Y. et al. China Study Group. //J. Pediat. – 2010. – V. 157(3). – P. 367-372
Hypothermia and neonatal encephalopathy /Committee on Fetus and Newborn, Papile L.A., Baley J.E., Benitz W., Cummings J., Carlo W.A., Eichenwald E., Kumar P., Polin R.A., Tan R.C., Wang K.S. //Pediatrics. – 2014
Selective head cooling with mild systemic hypothermia after neonatal encephalopathy: multicentre randomized trial /Gluckman P.D., Wyatt J.S., Azzopardi D., Ballard R., Edwards A.D., Ferriero D.M. et al. //Lancet. – 2005. – V. 365(9460). – P. 663-670
Pharmacokinetics and pharmacodynamics of medication in asphyxiated newborns during controlled hypothermia: The PharmaCool multicenter study /de Haan T.R., Bijleveld Y.A., van der Lee J.H., Groenendaal F., van den Broek M.P., Rademaker C.M. et al. //BMC Pediatr. – 2012. – V. 22. – P. 12-45
Необходимость распознавания множественных этиологий для оптимального ведения
Front Pediatr. 2019; 7: 142.
2019; 7: 142.
, 1, 2 , 1, 3, 4 и 1, 2, 3, 4, 5,
64 *
4 Сайма Аслам
1 Педиатрия, Национальный родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
Тэмми Стрикленд
1 Педиатрия, Национальный родильный дом , Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити-колледж в Дублине, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Больница Университета Кумб для женщин и младенцев, Дублин, Ирландия
Элеонора Дж. .Моллой
1 Педиатрия, Национальный родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити College Dublin, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Университетская больница для женщин и младенцев Кумб, Дублин, Ирландия
5 Неонатология, Детская больница Богоматери, Дримна, Ирландия
1 Педиатрия, национальная Родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити-колледж Дублина, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Coombe Women’s и больница Университета младенцев, Дублин, Ирландия
5 Неонатология, Детская больница Богоматери, Дримна, Ирландия
Отредактировал: Микко Холлман, Университет Оулу, Финляндия
Рецензент: Георг Шмольцер, Университет Альберты, Канада; Аакаш Пандита, Институт медицинских наук им. Санджая Ганди, Индия
Санджая Ганди, Индия
Эта статья была отправлена в раздел «Неонатология» журнала «Границы в педиатрии»
Поступила в редакцию 15 октября 2018 г .; Принят в печать 26 марта 2019 г.
Авторские права © 2019 Aslam, Strickland and Molloy.
Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License (CC BY). Использование, распространение или воспроизведение на других форумах разрешено при условии указания автора (авторов) и правообладателя (ов) и ссылки на оригинальную публикацию в этом журнале в соответствии с принятой академической практикой. Запрещается использование, распространение или воспроизведение без соблюдения этих условий.
Эта статья цитируется в других статьях в PMC.
Abstract
Неонатальная энцефалопатия (NE) связана с высокой смертностью и заболеваемостью. Факторы, предрасполагающие к NE, могут быть антенатальными, перинатальными или их комбинацией. Антенатальные материнские факторы, семейные факторы, генетическая предрасположенность, гипоксическая ишемическая энцефалопатия, инфекции, плацентарные аномалии, тромбофилия, дефекты коагуляции и метаболические нарушения — все это вовлечено в патогенез NE. В настоящее время терапевтическая гипотермия — единственное доступное лечение, независимо от этиологии.Распознавание этиологии вовлеченного НЭ может также помочь в проведении таких исследований, как метаболические исследования и обследования на сепсис, для обеспечения оптимального лечения. Понимание этиологии NE может позволить разработать целевую дополнительную терапию, связанную с основным механизмом, и разработать превентивные стратегии.
В настоящее время терапевтическая гипотермия — единственное доступное лечение, независимо от этиологии.Распознавание этиологии вовлеченного НЭ может также помочь в проведении таких исследований, как метаболические исследования и обследования на сепсис, для обеспечения оптимального лечения. Понимание этиологии NE может позволить разработать целевую дополнительную терапию, связанную с основным механизмом, и разработать превентивные стратегии.
Ключевые слова: неонатальная энцефалоптия, этиология, антенатальная, перинатальная, таргетная дополнительная терапия
Введение
Неонатальная энцефалопатия (НЭ) — сложное заболевание новорожденных, характеризующееся измененным уровнем сознания, судорогами, плохим тонусом. для инициирования или поддержания дыхания (1) и связан с полиорганной дисфункцией (2).Заболеваемость NE оценивается в 3 случая на 1000 живорождений (3). NE может быть результатом широкого спектра причин и является клиническим термином, не определяющим этиологию. Единственное доступное лечение — это терапевтическая гипотермия (ТГ) с максимальной пользой, если начать в первые 6 часов жизни (4). Существует несколько причин НЭ, таких как гипоксическая ишемическая энцефалопатия (ГИЭ), перинатальные инфекции, аномалии плаценты, метаболические нарушения, коагулопатии и сосудистый инсульт новорожденных (). Однако более чем в половине случаев причина НЭ остается неустановленной (5).
Единственное доступное лечение — это терапевтическая гипотермия (ТГ) с максимальной пользой, если начать в первые 6 часов жизни (4). Существует несколько причин НЭ, таких как гипоксическая ишемическая энцефалопатия (ГИЭ), перинатальные инфекции, аномалии плаценты, метаболические нарушения, коагулопатии и сосудистый инсульт новорожденных (). Однако более чем в половине случаев причина НЭ остается неустановленной (5).
Многофакторная этиология неонатальной энцефалопатии. Многие факторы предрасполагают к возникновению неонатальной энцефалопатии либо по отдельности, либо в комбинации, включая (A) Факторы риска до зачатия, (B) Сопутствующие заболевания или события у матери до родов / во время родов, (C) Патология плаценты, (D) Гипоксия-ишемия, (E) Перинатальная инфекция, (F) Неонатальный инсульт или тромбофилия, (G) Метаболические нарушения и (H) Генетические и эпигенетические аномалии. ПРОМ, длительный разрыв плодных оболочек; ЗВУР, ограничение внутриутробного развития.
ПРОМ, длительный разрыв плодных оболочек; ЗВУР, ограничение внутриутробного развития.
Использование термина NE vs. HIE противоречиво. Было предложено использовать термин NE для доношенных и поздних недоношенных новорожденных, у которых не было выявленных дозорных событий (6, 7). Трудно доказать наличие церебральной гипоксической ишемии, за исключением моделей на животных и конкретных случаев неонатального инсульта. Все текущие параметры, включая pH и судороги, неспецифичны (7). Некоторые из паттернов черепно-мозговых травм, наблюдаемых у пациентов с NE, могут быть воспроизведены на животных моделях с помощью гипоксии-ишемии, но это не доказывает, что все NE вызваны HIE (7).Несколько опубликованных популяционных исследований показали, что факторы риска до родов и неасфиксии связаны с НЭ (6). Напротив, некоторые авторы утверждают, что ГИЭ является причиной НЭ в 50–80% случаев на основании клинических критериев, критериев ЭЭГ и МРТ (1). Поэтому в этом обзоре мы использовали термин NE, и мы стремились изучить различные этиологии, связанные с NE.
Материнские факторы
Материнская гипертензия (16%) была важным фактором дородового риска НЭ в реестре неонатальной энцефалопатии Оксфордской сети штата Вермонт ( n = 4 165).Также была более высокая частота клинического хориоамнионита, длительного разрыва плодных оболочек и гипотиреоза матери. Хотя острый асфиксический эпизод был зарегистрирован в 15% случаев, связь с воспалением была обнаружена у 24% (5).
Популяционное исследование в Западной Австралии показало, что социально-экономический статус, семейный анамнез судорог, неврологические проблемы и зачатие после лечения бесплодия были независимыми факторами риска до зачатия для NE ( n = 164) (8).Заболевание щитовидной железы матери, кровотечение во время беременности, вирусные заболевания, преэклампсия, аномальная плацента, задержка внутриутробного развития и переношенность были другими важными факторами риска в дородовой период (8). Идентифицируемые дородовые факторы риска НЭ были обнаружены в 69% случаев, внутриродовые факторы риска — в 5%, как дородовые, так и во время родов — в 24% и отсутствие фактора риска — в 2%. Только в 4% случаев внутриродовая гипоксия была выявлена без каких-либо факторов риска до родов или до зачатия (9). Было обнаружено, что ограничение роста в развитых странах и беременность двойней в развивающихся странах связаны с НЭ.Заболевание щитовидной железы у матери, дородовое наблюдение, инфекция, роды и тактика ведения родов должны стать важными модификаторами в исследовании 27 новорожденных с НЭ и 100 детей контрольной группы (3). Дородовые (74 против 18%), внутриродовые (67 против 19%) и острые внутриродовые события (33 против 2%) более вероятны у младенцев с НЭ по сравнению с контрольной группой. Следовательно, в неонатальном клиническом анамнезе подробный материнский анамнез важен и может быть путем к профилактическим стратегиям в будущем.
Из 45 новорожденных с NE 36% имели дозорные эпизоды, 40% имели хориоамнионит и 11% имели оба этих заболевания.Если данные дозорных событий были исключены, то возраст матери> 35 лет (ОР 2,5; 95% ДИ 1,1–5,6) и инфекция мочевыводящих путей во время беременности (ОР 2,6; 95% ДИ 1,0–6,5) были потенциальными факторами дородового риска для NE (10).
Гипоксия-ишемия
Хотя концепция гипоксии-ишемии четко выражена в моделях на животных, она может не подходить для использования во всех случаях неонатальной NE у человека. «Дозу» и продолжительность гипоксии, а также степень ишемии можно напрямую измерить на животной модели.Однако у новорожденных людей это неизвестно, если нет контрольного события, и впоследствии не используются суррогатные маркеры гипоксии. Badawi et al. показали, что асфиксия во время родов считается сопутствующим фактором в 29% случаев НЭ и самостоятельным фактором только в 4% случаев (9). Было обнаружено, что внутриродовая гипоксия-ишемия является одним из факторов, способствующих развитию НЭ в 30% случаев в развитых и 60% в развивающихся странах (3). Американский колледж акушеров и Американская академия педиатрии определили дозорное событие в своем документе о неонатальной энцефалопатии и неврологических исходах (Obstet Gynecol 2014).Следующее соответствует острому пери- или интранатальному событию: дозорное гипоксическое или ишемическое событие, возникающее непосредственно перед или во время родов и родоразрешения, например разрыв матки или тяжелая отслойка плаценты; паттерны пульсометра плода, соответствующие острым послеродовым или интранатальным событиям; сроки и тип травм головного мозга, основанные на исследованиях изображений, согласующихся с этиологией острого послеродового или внутриродового события, и отсутствуют доказательства других проксимальных или дистальных факторов, которые могли бы быть способствующими факторами.Кроме того, сочетание низких баллов по шкале Апгарса, ацидемии, аномального кардиотокографа, изменений МРТ, согласующихся с гипоксией-ишемией и полиорганной дисфункцией, — все это связано с гипоксически-ишемической этиологией, но в равной степени может быть изменено сепсисом или другими причинами NE. Асфиксичные родовые явления и воспаление присутствовали только в 12,6% случаев церебрального паралича (11). У новорожденных с NE ( n = 405) следующие факторы были независимо связаны с NE ( p -значение = 0,001), включая: только 1 дородовой период (гестационный возраст> 41 недели) и 7 факторов во время родов, включая длительный разрыв плодных оболочек, аномальные кардиотокограф, густой меконий, дозорные события, дистоция плеча, тугая затылочная пуповина и отказ вакуума (12).В когорте из 26 новорожденных с дозорными событиями NE (ОР 74,9, 95% ДИ 11,9-бесконечность, p <0,001) и отслеживание ЧСС плода категории 3 (28,0% против 4,0%, p = 0,002) были сильно связанный с NE (13). В когорте из 45 новорожденных у 36% были дозорные события, а у 11% были как дозорные, так и хориоамнионит (10).
Нейровизуализация с использованием магнитно-резонансной томографии, традиционной, диффузионной и спектроскопии в период от 24 до 96 часов жизни дает полезные рекомендации относительно возможных сроков возникновения церебрального инсульта, особенно диффузных аномалий.Аномалии, вызванные травмой головного мозга, становятся наиболее очевидными через 7 дней при использовании качественной МРТ, диффузии и спектроскопии. Глубокое ядерное серое вещество или водораздел кортикального повреждения развиваются по четко определенному типу повреждения мозга и типичны для гипоксически-ишемического повреждения мозга у новорожденного. Генетические и метаболические причины могут быть исследованы, если на МРТ существует другая картина травмы головного мозга или эволюция травмы. Признаки того, что послеродовая гипоксия-ишемия не была причиной НЭ, предлагаются на МРТ: порэнцефалия, очаговый артериальный инфаркт, венозный инфаркт, изолированное внутрипаренхиматозное или внутрижелудочковое кровоизлияние или атипичные паттерны метаболических энцефалопатий.
При NE, связанном с острым дозорным событием (HIE), типичная картина повреждения на МРТ показала вовлечение базальных ганглиев, таламуса с ассоциированной задней конечностью внутренней капсулы и, в тяжелых случаях, вовлечение ствола мозга (14). При NE без задокументированного дозорного события вовлечение базальных ганглиев или таламуса (BGT) также связано с изменениями белого вещества в 50% случаев (14). BGT с обширным повреждением белого вещества (WM) был обнаружен в 14%, BGT с WM от легкой до умеренной — в 56%, изолированное таламическое повреждение — в 5%, умеренное повреждение WM — только у 2% и легкое WM или нормальное — у 23% в 48%. младенцы с ГИЭ.Внутренняя капсула была аномальной у 93% пациентов с умеренным и тяжелым повреждением WM и была связана со смертью и ХП у 86% пациентов (15).
Картина повреждения головного мозга может указывать на возможную причину, например, повреждение коркового вещества и белого вещества (очаговое / мультифокальное) может быть связано с плацентарной недостаточностью и хориоамнионитом. Ранняя категоризация пациентов в соответствии с типом травмы головного мозга может привести к другому терапевтическому подходу, поскольку на животных моделях было показано, что разные уровни гипотермии защищают от повреждения коры головного мозга или глубокого серого вещества, поэтому для получения максимальной пользы могут потребоваться специфические для пациента протоколы гипотермии.Точно так же в моделях на животных разные режимы охлаждения, системное и селективное, приводят к разной температуре мозга (16).
Трудно окончательно установить наличие, продолжительность и степень гипоксии и ишемии у новорожденных, поэтому использовались суррогатные маркеры, такие как pH и судороги (7). Следовательно, биомаркеры мультиорганного поражения могут быть полезны для диагностики или оценки тяжести гипоксической ишемии и прогнозирования исхода при NE. Сердечный тропонин является маркером ишемии миокарда у новорожденных и детей и высвобождается из миоцитов после повреждения их мембраны.Сердечный тропонин I (cTnI) был значительно выше у новорожденных с ГИЭ в первые 48 часов по сравнению с контрольной группой ( p <0,0005) (17). Сердечный TnI был повышен у новорожденных с более высокой степенью НЭ и у тех, кому потребовались инотропы (18). Пороговое значение <0,22 нг / мл для нормотермических и <0,15 нг / мл для гипотермических младенцев с NE предсказывало нормальный исход развития нервной системы (19).
Гипоксия приводит к усилению эритропоэза и выбросу незрелых ядерных эритроцитов (nRBC) в кровоток (20).ЯРБК пуповинной крови были значительно выше у новорожденных, подвергшихся асфиксии, по сравнению с контрольной группой, а также коррелировали с апгаром через 1 мин, pH и развитием NE (20). Количество ядерных эритроцитов на 100 лейкоцитов было выше у новорожденных с НЭ по сравнению с контрольной группой, младенцев с НЭ средней / тяжелой или легкой степени ( p = 0,016) и у новорожденных с плохим исходом нервного развития ( p = 0,03) 21). Следовательно, стандартизованное измерение воздействия клинической гипоксии было бы полезным с использованием комбинации этих маркеров и могло бы помочь в определении времени инсульта и корреляции с доклиническими моделями на животных.
Инфекция
Риск спастического церебрального паралича (ДЦП) и квадриплегического ДЦП повышался при сочетании инфекции и асфиксии (22). Уровни интерлейкина (ИЛ) -6 через 6 часов связаны с отклонениями от нормы неврологического обследования (23). NE, инотропная поддержка, судороги без менингита, потребность в интубации и более низкий 5-минутный апгар были более вероятны у новорожденных с ХП при наличии инфекции у матери по сравнению с ХП без инфекции (22).
Материнские и ранние неонатальные инфекции представляют собой диагностическую проблему.Ведутся споры о том, может ли скрытая инфекция, не обнаруживаемая обычными методами культивирования, быть связана с неврологическим повреждением во всех возрастных группах. Полимеразная цепная реакция (ПЦР) выявила 11 случаев бактериемии у энцефалопатических новорожденных в Африке, у которых был отрицательный результат посева крови (NE n = 201). ПЦР в сочетании с посевом крови привела к обнаружению бактериальных продуктов в 8,9% случаев НЭ по сравнению с 3,1% при использовании одного посева крови (24). В метаанализе стрептококк группы B (GBS) был связан с NE в 0.58% случаев и смертность были выше при использовании СГБ плюс НЭ по сравнению с одним НЭ (25). В когорте из 45 новорожденных 40% имели хориоамнионит и 11% имели как дозорные события, так и хориоамнионит (10).
Терапевтическая гипотермия задерживает рост и пик ответа с-реактивного белка (СРБ), а также приводит к снижению количества лейкоцитов и нейтрофилов по сравнению с нормотермными новорожденными (26). Это влияние гипотермии на задержку развития естественных воспалительных маркеров следует учитывать при выборе лечения антибиотиками и продолжительности лечения новорожденных с НЭ.
Следовательно, полное обследование на сепсис имеет важное значение у всех детей с НЭ. Стандартных рекомендаций по выполнению люмбальной пункции во всех случаях НЭ не существует, и их можно выбирать в каждом конкретном случае. Кандидатами могут быть младенцы с повышенным WCC и CRP или факторами риска септического риска. Существуют также технические и практические проблемы для поясничной пункции у младенцев с NE, которые являются ригидными из-за TH, а также часто изначально имеют отек мозга при ультразвуковом исследовании черепа.
Аномалии плаценты
Поражение пуповины, хориоамнионит, васкулит плода, меконий хориональной пластинки и тромботическая васкулопатия плода часто встречались в плацентарных поражениях у пациентов с NE ( n = 23) (27).Поражения плаценты, указывающие на тромбоз и снижение фетоплацентарного кровотока, являются значимыми и независимыми факторами риска НЭ ( n = 93) (28). Наличие более одного поражения плаценты увеличивает вероятность НЭ, но не было никакой корреляции между патологией плаценты и картиной повреждения на МРТ ( n = 56) (29). Аномальная патология плаценты была обнаружена у 29% новорожденных с дозорными событиями и у 73% младенцев без дозорных явлений ( p = 0,0001), перенесших терапевтическую гипотермию (30).Воспалительные поражения плаценты чаще наблюдались у новорожденных без дозорных событий ( p = 0,002) (30). Хронический виллит был связан с повреждением базальных ганглиев (BGT), тогда как наличие ядерных эритроцитов, снижение созревания плаценты и хронический виллит также приводили к повреждению белого вещества / водораздела вместе с вовлечением BGT ( n = 95) (31).
Доказательства связи хориоамнионита с НЭ разнообразны. Предполагается, что время инфицирования и степень воспалительного ответа могут привести либо к прекондиционированию, либо к сенсибилизации и могут вызвать либо защитный эффект, либо дальнейшее усиление перинатального повреждения головного мозга, соответственно (32).Этот эффект был продемонстрирован на животных моделях. Липополисахарид (ЛПС), вводимый за 4–6 ч до 20 и 50 мин воздействия HI, приводил к усилению травм головного мозга. Однако введение LPS за 24 часа до 50-минутного воздействия HI привело к значительному ослаблению травм головного мозга (32). КА выявлена у 8 новорожденных с признаками перинатальной асфиксии (всего n = 23) (27). Младенцы с NE и TH имели более высокие шансы на наличие CA по сравнению с младенцами, которые не получали TH ( n = 98) (33).CA, васкулит и фунизит были связаны с NE степени I, виллитом с NE II и фунизитом с III степенью у 141 новорожденного с NE и 309 контрольных (29). CA был связан с более низким риском черепно-мозговой травмы и плохим когнитивным исходом по сравнению с не-CA (скорректированный OR 0,3; 95% CI 0,1–0,7, p = 0,004) у новорожденных с NE ( n = 258), хотя только У 20 новорожденных были гистологические доказательства СА. В той же когорте новорожденные с признаками сепсиса имели более высокие шансы на повреждение водораздела и аномальные нейромоторные показатели, чем у новорожденных без каких-либо клинических признаков ( p = 0.007) (34). У 120 младенцев с сочетанием перинатального ацидоза, NE и хориоамнионита с ответом плода или без него и пятнистый / диффузный хронический виллит были независимо связаны с тяжестью NE (35). Единственным индивидуальным предиктором патологического исхода нервного развития через 22-24 месяца после терапии гипотермией был диффузный хронический виллит. Гистологическая CA имела низкую прогностическую ценность для развития энцефалопатии и смерти у NE ( n = 51) (36), но материнская лихорадка ( n = 336) во время родов была независимым фактором для NE (скорректированное OR 4.72, 95% ДИ 1,28–17,4) (37). Клинический хориоамнионит был связан с более высокими уровнями IL-6, IL-8 в пуповинной крови и регулировался активацией нормальных Т-клеток, экспрессируемых и секретируемых (RANTES) в NE ( n = 61). В когорте из 67 новорожденных с хориоамнионитом NE, независимо от того, были ли клинические или гистологические данные связаны со стойким метаболическим ацидозом, это может предсказать плохой неврологический исход (38).
Патология плаценты описывается как «черный ящик» беременности. Стандартизированная классификация результатов патологии плаценты важна для дальнейшего определения этиологии NE (39).
Нарушения обмена веществ
Нарушения обмена веществ являются редкими причинами НЭ, но их всегда следует учитывать. Врожденные нарушения метаболизма (ВЭМ) присутствуют в неонатальном периоде после нормального периода выздоровления и отсутствия признаков перинатальной асфиксии, но неврологические и полиорганные поражения могут проявляться как НЭ (40). Митохондриальные нарушения также являются важной причиной НЭ (41).
Амплитудная интегрированная электроэнцефалограмма (аЭЭГ) была отклонена от нормы у 27 новорожденных с ВЭМ, причем наиболее устойчивыми признаками были аномальная фоновая активность и судороги.Не было различий в аЭЭГ для энцефалопатии, связанной с IEM или NE, и дифференцировать можно было только на основании клинического подозрения (42). Единственное метаболическое расстройство с диагностической ЭЭГ — это некетотическая гиперглицинемия с первоначальным паттерном «подавление-всплеск», переходящим в гипсаритмию в раннем или среднем младенчестве и диагностируемое путем измерения уровня глицина в спинномозговой жидкости (42). Имеются также отдельные сообщения о случаях ИЭМ, таких как дефицит сульфитоксидазы и цитохрома С, проявляющийся как НЭ (43, 44).
Результаты МРТ могут варьироваться в зависимости от типа врожденной ошибки метаболизма (ВЭМ) и могут варьироваться от поражения белого вещества до поражения глубоких серых ядер. Митохондриальные энцефалопатии имеют симметричное двустороннее распределение и изначально могут быть диагностированы как NE (45). Следует учитывать метаболические нарушения, если нет явных явлений во время родов, стойкий лактоацидоз и / или гипогликемия (45) и начато обследование. Различные паттерны повреждений на МРТ головного мозга могут помочь дифференцировать метаболические нарушения от НЭ.Поражение Globus Pallidus часто встречается при IEM по сравнению с NE, хотя картина повреждения при дефиците сульфитоксидазы и дефиците фактора молибдена может имитировать NE (46).
Изолированные приступы связаны с такими расстройствами, как: судороги, связанные с пиридоксином, некетотическая гиперглицинемия (НКГ), дефицит дигидропиримидиндегидрогеназы, дефицит сульфитоксидазы (либо изолированный, либо как часть дефицита кофактора молибдена), трансаминазы 4-аминобутират-аминотрансферазы (ГАБТрансферазы). ) дефицит, судороги, связанные с фолиевой кислотой, дефицит 3-фосфоглицератдегидрогеназы, дефицит гуанидиноацетатметилтрансферазы (GAMT) и дефицит переносчика глюкозы (GLUT-1).У младенцев с полиорганными поражениями, судорогами, метаболическим ацидозом, молочной железой, гипераммониемией могут быть: органическая ацидемия, дефекты цикла мочевины, пероксисомальные нарушения (например, синдром Зеллвегера) или митохондриальные нарушения.
Подробный семейный анамнез для установления факторов риска, таких как родство родителей или ранее пораженный ребенок, важен, поскольку большинство врожденных нарушений метаболизма имеют аутосомно-рецессивное или материнское наследование. Базовые исследования, такие как электролиты, аммиак, сывороточные аминокислоты, лактат, ацилкарнитин и органическая кислота в моче, могут быть рассмотрены при NE (40).Есть проблемы с метаболическим тестированием, так как их может потребоваться повторить, если ребенок очень плохо себя чувствует с полиорганной дисфункцией во время отбора образцов (46). Недавние исследования показали большой потенциал метаболомики как биомаркеров NE. Было показано, что содержание сукцината повышено у детей с НЭ, которые серьезно пострадали (47).
Тромбофилия и неонатальный инсульт
Асфиксия (в 4% случаев) участвует в патогенезе неонатального инсульта (48). Фокальные клонические приступы являются наиболее частым проявлением неонатального инсульта (49), и 6 младенцев с инсультом были обнаружены в когорте NE ( n = 124) (50).Эти дети обычно страдали судорогами и имели худшие исходы с точки зрения нервного развития, чем остальная когорта. Нарушения свертывания крови, такие как полицитемия, лейденский фактор V, нарушения гемоглобина и мутации протромбина, не были обнаружены у 4 из 6 обследованных пациентов (50).
В моделях на животных повышенные уровни гомоцистеина приводили к увеличению провоспалительных цитокинов, таких как фактор некроза опухоли альфа (TNFα), интерлейкин 1 бета (IL-1β) и IL-6 в гиппокампе и коре головного мозга.Это провоспалительное состояние может быть ответственным за нейрональные и цереброваскулярные эффекты, наблюдаемые у взрослых (51). Роль гомоцистеина или полиморфизмов в гене метилентетрагидрофолатредуктазы в возникновении неонатального повреждения головного мозга неясна (52). В когорте из 118 новорожденных с НЭ повреждение белого вещества / водораздела с большей вероятностью было связано с гипогликемией, полиморфизмом метилентетрагидрофолатредуктазы (MTHFR) и уровнями гомоцистеина в плазме в верхнем квартиле нормы (52).
Генетические и эпигенетические аномалии
Отсутствуют опубликованные данные, связывающие генетическую предрасположенность с развитием NE. У 40 пациентов с NE генетическая изменчивость протромбических факторов, таких как протромбин G20210A, фактор V Leiden G1691A и метилентетрагидрофолатредуктаза [MTHFR] C677T, и ген фактора некроза опухоли не повлияли на оценку NE, ЭЭГ, смерть, краниальное УЗИ (США) , неврологический исход при выписке через 6 и 12 месяцев. Полиморфизм гена интерлейкина-6 (IL-6 174GC) имел защитный эффект и был связан с нормальной ЭЭГ, краниальным УЗИ и неврологическим обследованием при выписке (53).В ретроспективном исследовании «случай-контроль» с участием 11 новорожденных с NE у матерей была обнаружена более высокая частота полиморфизма MTHFR (7 гомозиготных и 4 гетерозиготных) по сравнению с контрольной группой (54). Генетический полиморфизм может увеличивать риск или тяжесть неонатального повреждения головного мозга при NE, и его следует учитывать (53).
В рамках лонгитюдного исследования родителей и детей, проведенного Avon, было проведено генотипирование 7611 доношенных детей, и мерилом воздействия было наличие одного или нескольких минорных аллелей в одном из 3 SNP (rs2284411, rs2498804, rs1835740).Первичным результатом была необходимость реанимации при рождении, что было связано с rs1835740 (55). Требуются более крупные международные совместные исследования для определения необходимого количества пациентов для изучения генетических связей и разделения пациентов по этиологии.
Другая категория младенцев с генетической причиной неонатальной энцефалопатии — это дети с миопатиями и энцефалопатиями новорожденных. Пациенты, унаследовавшие миопатию (центронуклеарную миопатию), могут иметь неонатальный дистресс, гипотонию и признаки, указывающие на ГИЭ (56).Врожденная миотоническая дистрофия 1 типа характеризуется гипотонией и тяжелой генерализованной слабостью при рождении, часто с дыхательной недостаточностью, умственной отсталостью и ранней смертью. Это вызвано экспансией тринуклеотидного повтора CTG в некодирующей области DMPK .
В будущем подробное генотипирование, включая более легкий доступ к методам микроматриц в клинических условиях, предоставит больше информации, позволяющей индивидуализированный уход и потенциально классифицировать младенцев по генотипу.
Нейровизуализация
На МРТ можно увидеть различные модели травм, но это не исключает HIE как причины травмы. Характер повреждения зависит от тяжести, продолжительности и повторяемости гипоксической ишемии и может привести к поражению базальных ганглиев, таламуса, ствола мозга и / или белого вещества головного мозга в различных сочетаниях (1). При глубокой гипоксии преобладает повреждение более глубоких серых структур, то есть базальных ганглиев и таламуса. Объясняется это тем, что эти участки миелинизированы и имеют более высокую скорость метаболизма.Состояния, которые уменьшают, а не вызывают полное прекращение кровотока, такие как анемия и гиповолемия, связаны с повреждением коры головного мозга и сохранением более глубоких серых структур (57). В когорте из 245 пациентов с NE 197 (80%) результаты МРТ соответствовали острому перинатальному инсульту. МРТ у 40 младенцев (16%) были нормальными. У 9 младенцев (4%) были выявлены признаки тромбоза / инфаркта, генетических нарушений, антенатального инсульта и митохондрий (дефицит комплекса I) на МРТ в дополнение к гипоксическому ишемическому инсульту.Нейровизуализация у 8 (3%) младенцев с клиническим диагнозом НЭ показала либо врожденную ошибку метаболизма, нервно-мышечное расстройство, либо отсутствие диагноза, и эти результаты не соответствовали гипоксической ишемии (48). Плацентарный виллит высокой степени неизвестной этиологии ( n = 4) был обнаружен в когорте из 36 пациентов, связанных с повреждением белого вещества, вторичным по отношению к воспалению / окислительному стрессу в перинатальном периоде (58).
Значение для терапии
Все младенцы с NE могут не в одинаковой степени выиграть от переохлаждения.Следовательно, выявление точной этиологии в каждом случае NE имеет значение для лечения, поскольку есть некоторые излечимые причины, которые требуют быстрого определения для оптимального лечения. Использование бактериальной ПЦР для выявления инфекции у новорожденных с NE может быть более полезным, чем только посев крови с низким выходом бактерий, а также гипотермия может уменьшить воспалительную реакцию. Гистология плаценты отражает внутриматочную среду и может прояснить основную этиологию. Все новорожденные с риском IEM должны быть обследованы на предмет метаболических нарушений, так как этим пациентам могут быть полезны специфические методы лечения, а не гипотермия.Точно так же скрининг на тромбофилию следует рассматривать у пациентов из группы риска, таких как пациенты с инсультом, семейный анамнез тромбофилии. Подробная оценка этиологии NE важна для выявления излечимых причин и категоризации этой гетерогенной группы новорожденных, чтобы можно было подобрать соответствующее лечение в соответствии с этиологией и улучшением отдаленных результатов. Точно так же будет полезно стратифицировать большие многоцентровые когорты младенцев с NE по этиологии, чтобы полностью понять этиологию, реакцию на лечение гипотермией и отдаленные результаты.
Авторские взносы
SA: основной автор; ТС: помогал с поиском релевантных статей и рисунка; ЭМ: автор-руководитель.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Ссылки
1. Volpe JJ. Неонатальная энцефалопатия: неадекватный термин для гипоксически-ишемической энцефалопатии.Энн Нейрол. (2012) 72: 156–66. 10.1002 / ana.23647 [PubMed] [CrossRef] [Google Scholar] 2. Шах П., Рип Хаген С., Бейен Дж, Перлман М. Мультиорганная дисфункция у младенцев с постасфиксиальной гипоксически-ишемической энцефалопатией. Arch Dis Child Fetal Neonatal Ed. (2004) 89: F152 – F155. 10.1136 / adc.2002.023093 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 3. Куринчук Дж. Дж., Уайт-Конинг М., Бадави Н. Эпидемиология неонатальной энцефалопатии и гипоксически-ишемической энцефалопатии. Early Hum Dev. (2010) 86: 329–38.10.1016 / j.earlhumdev.2010.05.010 [PubMed] [CrossRef] [Google Scholar] 4. Джейкобс С.Е., Берг М., Хант Р., Тарнов-Морди В.О., Индер Т.Э., Дэвис П.Г.
Охлаждение новорожденных с гипоксической ишемической энцефалопатией. База данных Cochr Syst Rev. (2013) 1: CD003311
10.1002 / 14651858.CD003311.pub3 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 5. Нельсон К.Б., Бингхэм П., Эдвардс Э.М., Хорбар Д.Д., Кенни М.Дж., Индер Т. и др. . Антецеденты неонатальной энцефалопатии в реестре энцефалопатии Оксфордской сети Вермонта. Педиатрия.(2012) 130: 878–86. 10.1542 / peds.2012-0714 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 6. Нельсон КБ. Это HIE?
И почему это важно Acta Paediatr. (2007) 96: 1113–4. 10.1111 / j.1651-2227.2007.00364.x [PubMed] [CrossRef] [Google Scholar] 7. Дамманн О., Ферриеро Д., Грессенс П.
Неонатальная энцефалопатия или гипоксически-ишемическая энцефалопатия?
Соответствующая терминология имеет значение Pediatr Res. (2011) 70: 1-2. 10.1203 / PDR.0b013e318223f38d [PubMed] [CrossRef] [Google Scholar] 8. Бадави Н., Куринчук Дж. Дж., Кио Дж. М., Алессандри Л. М., О’Салливан Ф., Бертон П. Р. и др.. Факторы дородового риска энцефалопатии новорожденных: исследование случай-контроль в Западной Австралии. BMJ. (1998) 317: 1549–53. 10.1136 / bmj.317.7172.1549 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 9. Бадави Н., Куринчук Дж. Дж., Кио Дж. М., Алессандри Л. М., О’Салливан Ф., Бертон П. Р. и др. . Факторы риска внутриутробной энцефалопатии новорожденных: исследование случай-контроль в Западной Австралии. BMJ. (1998) 317: 1554–8. 10.1136 / bmj.317.7172.1554 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 10. Паркер SJ, Kuzniewicz M, Niki H, Wu YW.Факторы дородового и внутриродового риска гипоксически-ишемической энцефалопатии в когорте новорожденных в США. J Pediatr. (2018) 203: 163–9. 10.1016 / j.jpeds.2018.08.028 [PubMed] [CrossRef] [Google Scholar] 11. Адамсон С.Дж., Алессандри Л.М., Бадави Н., Бертон П.Р., Пембертон П.Дж., Стэнли Ф. Предикторы неонатальной энцефалопатии у доношенных новорожденных. BMJ. (1995) 311: 598–602
10.1136 / bmj.311.7005.598 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 12. Мартинес-Биарж М., Диез-Себастьян Дж., Вустхофф Си-Джей, Меркури Е., Коуэн FM.Дородовые и внутриродовые факторы, предшествующие неонатальной гипоксически-ишемической энцефалопатии. Педиатрия. (2013) 132: e952 – e959
10.1542 / peds.2013-0511 [PubMed] [CrossRef] [Google Scholar] 13. Торбенсон В.Е., Толчер М.К., Несбитт К.М., Колби К.Э., Эль-Нашар С.А., Гостоут Б.С. и др. . Внутриродовые факторы, связанные с неонатальной гипоксической ишемической энцефалопатией: исследование случай-контроль. BMC Беременность и роды. (2017) 17: 415
10.1186 / s12884-017-1610-3 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 14. Резерфорд М., Маламатениу К., МакГиннесс А., Оллсоп Дж., Биарж М.М., Конселл С.Магнитно-резонансная томография при гипоксически-ишемической энцефалопатии. Early Hum Dev. (2010) 86: 351–60. 10.1016 / j.earlhumdev.2010.05.014 [PubMed] [CrossRef] [Google Scholar] 15. Okereafor A, Allsop J, Counsell SJ, Fitzpatrick J, Azzopardi D, Rutherford MA и др. . Характер черепно-мозговой травмы у новорожденных, подвергшихся перинатальным дозорным событиям. Педиатрия. (2008) 121: 906–14. 10.1542 / peds.2007-0770 [PubMed] [CrossRef] [Google Scholar] 16. Мецлер М., Говиндан Р., Аль-Шаргаби Т., Везина Г., Андескавадж Н., Ван И и др.. Характер черепно-мозговой травмы и снижение вариабельности сердечного ритма у новорожденных с гипоксической ишемической энцефалопатией. Pediatr Res. (2017) 82: 438–43. 10.1038 / pr.2017.94 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 17. Симович AM, Игрутинович З., Обрадович С., Ристич Д., Вулетич Б., Раданович М. Значение сердечного тропонина I второго поколения в раннем скрининге гипоксически-ишемической энцефалопатии после перинатальной асфиксии. Srp Arh Celok Lek. (2012) 140: 600–5. [PubMed] [Google Scholar] 18. Шастри А.Т., Самарасекара С., Мунираман Х., Кларк П.Концентрации сердечного тропонина I у новорожденных с гипоксически-ишемической энцефалопатией. Acta Paediatr. (2012) 101: 26–9. 10.1111 / j.1651-2227.2011.02432.x [PubMed] [CrossRef] [Google Scholar] 19. Лю X, Chakkarapani E, Stone J, Thoresen M. Влияние компрессий сердца и лечения гипотермии на сердечный тропонин I у новорожденных с перинатальной асфиксией. Реанимация. (2013) 84: 1562–7. 10.1016 / j.resuscitation.2013.07.003 [PubMed] [CrossRef] [Google Scholar] 20. Гош Б., Миттал С., Кумар С., Дадхвал В. Прогнозирование перинатальной асфиксии с ядросодержащими эритроцитами в пуповинной крови новорожденных.Int J Gynaecol Obstet. (2003) 81: 267–71. 10.1016 / S0020-7292 (03) 00124-3 [PubMed] [CrossRef] [Google Scholar] 21. Уолш Б.Х., Бойлан Г.Б., Мюррей Д.М. Ядерные эритроциты и ранняя ЭЭГ: прогнозирование стадии Сарната и двухлетнего исхода. Early Hum Dev. (2011) 87: 335–9. 10.1016 / j.earlhumdev.2011.01.041 [PubMed] [CrossRef] [Google Scholar] 22. Нельсон КБ, Гретер Дж. Потенциально удушающие состояния и спастический церебральный паралич у младенцев с нормальной массой тела при рождении. Am J Obstet Gynecol. (1998) 179: 507–13. 10.1016 / S0002-9378 (98) 70387-4 [PubMed] [CrossRef] [Google Scholar] 23.Шалак Л.Ф., Лапток А.Р., Джафри Х.С., Рамило О., Перлман Дж. Клинический хориоамнионит, повышенные цитокины и травмы головного мозга у доношенных детей. Педиатрия. (2002) 110: 673–80. 10.1542 / peds.110.4.673 [PubMed] [CrossRef] [Google Scholar] 24. Танн CJ, Nkurunziza P, Nakakeeto M, Oweka J, Kurinczuk JJ, Were J и др. . Распространенность патогенов кровотока выше в случаях неонатальной энцефалопатии по сравнению с контрольной группой, использующей новую панель ПЦР-анализов в реальном времени. PLoS ONE. (2014) 9: e97259. 10.1371 / journal.pone.0097259 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 25.Танн С.Дж., Мартинелло К.А., Саду С., Лоун Дж.Э., Сил А.С., Вега-Поблете М. и др.
Группа исследователей неонатальной энцефалопатии GBS. неонатальная энцефалопатия со стрептококками группы b во всем мире: систематический обзор, наборы данных исследовательских групп и метаанализ. Clin Infect Dis. (2017) 65 (Suppl_2): S173–89. 10.1093 / cid / cix662 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 26. Chakkarapani E, Davis J, Thoresen M. Терапевтическая гипотермия задерживает ответ C-реактивного белка и подавляет количество лейкоцитов и тромбоцитов у младенцев с неонатальной энцефалопатией.Arch Dis Child Fetal Neonatal Ed. (2014) 99: F458 – F463. 10.1136 / archdischild-2013-305763 [PubMed] [CrossRef] [Google Scholar] 27. Wintermark P, Boyd T, Gregas MC, Labrecque M, Hansen A. Патология плаценты у новорожденных с асфиксией, отвечающая критериям терапевтической гипотермии. Am J Obstet Gynecol. (2010) 203: 579.e1–9. 10.1016 / j.ajog.2010.08.024 [PubMed] [CrossRef] [Google Scholar] 28. Макдональд Д.Г., Келехан П., Макменамин Дж.Б., Горман В.А., Мэдден Д., Тоббия И.Н. и др. . Плацентарная тромботическая васкулопатия плода связана с неонатальной энцефалопатией.Hum Pathol. (2004) 35: 875–80
10.1016 / j.humpath.2004.02.014 [PubMed] [CrossRef] [Google Scholar] 29. Hayes BC, Cooley S, Donnelly J, Doherty E, Grehan A, Madigan C и др. . Плацента у младенцев> 36 недель беременности с неонатальной энцефалопатией: исследование случай-контроль. Arch Dis Child Fetal Neonatal Ed. (2013) 98: F233–9. 10.1136 / archdischild-2012-301992 [PubMed] [CrossRef] [Google Scholar] 30. Чанг Т., Рейес Т.Дж., Пласетек Дж., Массаро А.Н., Нельсон КБ.
Неонатальная энцефалопатия, дозорные явления и плацента.J Neonatal Perinatal Med. (2012) 5: 41–8. 10.3233 / NPM-2012-54211 [CrossRef] [Google Scholar] 31. Хартеман Дж. К., Никкельс П. Г., Бендерс М. Дж., Кви А., Грюнендал Ф., де Фрис Л. С.. Патология плаценты у доношенных детей с гипоксически-ишемической неонатальной энцефалопатией и ассоциация с магнитно-резонансной томографией повреждения головного мозга. J Pediatr. (2013) 163: 968–995.
10.1016 / j.jpeds.2013.06.010 [PubMed] [CrossRef] [Google Scholar] 32. Эклинд С., Маллард С., Арвидссон П., Хагберг Х. Липополисахарид вызывает как первичную, так и вторичную фазу сенсибилизации в развивающемся мозге крысы.Pediatr Res. (2005) 58: 112–6
10.1203 / 01.PDR.0000163513.03619.8D [PubMed] [CrossRef] [Google Scholar] 33. Нельсон Д.Б., Лаке А.М., Макинтайр Д.Д., Санчес П.Дж., Левено К.Дж., Чалак Л.Ф. Акушерские предшественники лечения новорожденного с помощью охлаждения тела. Am J Obstet Gynecol. (2014) 211: 155.e1–6. 10.1016 / j.ajog.2014.02.013 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 34. Дженстер М., Бонифачо С.Л., Рюэль Т., Роджерс Е.Е., Там Э.У., Партридж Дж.С. и др.
Инфекция матери или новорожденного: связь с исходами неонатальной энцефалопатии.Pediatr Res. (2014) 76: 93–9. 10.1038 / pr.2014.47 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 35. Мир И.Н., Джонсон-Велч С.Ф., Нельсон Д.Б., Браун Л.С., Розенфельд С.Р., Чалак Л.Ф. Патология плаценты связана с тяжестью неонатальной энцефалопатии и неблагоприятными исходами развития после гипотермии. Am J Obstet Gynecol. (2015) 213: 849.e1–7. 10.1016 / j.ajog.2015.09.072 [PubMed] [CrossRef] [Google Scholar] 36. Шалак Л., Джонсон-Велч С., Перлман Дж. М.. Хориоамнионит и неонатальная энцефалопатия у доношенных детей с ацидемией плода: гистопатологические корреляции.Pediatr Neurol. (2005) 33: 162–5. 10.1016 / j.pediatrneurol.2005.04.005 [PubMed] [CrossRef] [Google Scholar] 37. Impey L, Greenwood C, MacQuillan K, Reynolds M, Sheil O. Лихорадка в родах и неонатальная энцефалопатия: проспективное когортное исследование. BJOG. (2001) 108: 594–7. 10.1111 / j.1471-0528.2001.00145.x [PubMed] [CrossRef] [Google Scholar] 38. Джонсон CT, Бурд I, Рагхунатан Р., Нортингтон Ф. Дж., Грэм Э.М. Перинатальное воспаление / инфекция и его связь с коррекцией метаболического ацидоза при гипоксически-ишемической энцефалопатии.J Perinatol. (2016) 36: 448–52. 10.1038 / jp.2015.221 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 39. Кларк П., Мунираман Х., Гарднер Д., Венкатеш В., Керли А., Виктор С. и др. . Исследование неонатальной энцефалопатии: часто теряемый плацентарный «черный ящик». Pediatr Dev Pathol. (2015) 18: 343–4. 10.2350 / 15-02-1611-LET.1 [PubMed] [CrossRef] [Google Scholar] 40. Tan ES. Врожденные нарушения обмена веществ, проявляющиеся как неонатальная энцефалопатия: практические советы клиницистам. Ann Acad Med Singapore. (2008) 37 (12 доп.): 94–3. [PubMed] [Google Scholar] 41. Узиэль Г., Геззи Д., Зевиани М. Инфантильная митохондриальная энцефалопатия. Semin Fetal Neonatal Med. (2011) 16: 205–15. 10.1016 / j.siny.2011.04.003 [PubMed] [CrossRef] [Google Scholar] 42. Олишар М., Шани Э., Айгюн С., Аззопарди Д., Хант Р.В., Тоет М.С. и др. . Амплитудно-интегрированная электроэнцефалография у новорожденных с врожденными нарушениями обмена веществ. Неонатология. (2012) 102: 203–11. 10.1159 / 000339567 [PubMed] [CrossRef] [Google Scholar] 43. Хобсон Э., Томас С., Крофтон П. М., Мюррей А. Д., Дин Дж. К., Ллойд Д.Изолированная недостаточность сульфитоксидазы имитирует признаки гипоксической ишемической энцефалопатии. Eur J Pediatr. (2005) 164: 655–9. 10.1007 / s00431-005-1729-5 [PubMed] [CrossRef] [Google Scholar] 44. Уиллис Т.А., Дэвидсон Дж., Грей Р.Г., Поултон К., Рамани П., Уайтхаус В. Дефицит цитохромоксидазы, проявляющийся как асфиксия при рождении. Dev Med Child Neurol. (2000) 42: 414–7. 10.1017 / S0012162200000761 [PubMed] [CrossRef] [Google Scholar] 45. Khong PL, Lam BC, Tung HK, Wong V, Chan FL, Ooi GC. МРТ неонатальной энцефалопатии.Clin Radiol. (2003) 58: 833–44. 10.1016 / S0009-9260 (03) 00261-7 [PubMed] [CrossRef] [Google Scholar] 46. Enns GM.
Врожденные нарушения обмена веществ, маскирующиеся под гипоксически-ишемическую энцефалопатию. NeoReviews. (2005) 12: e549 – e558. 10.1542 / neo.6-12-e549 [CrossRef] [Google Scholar] 47. Уолш Б.Х., Бродхерст Д.И., Мандал Р., Вишарт Д.С., Бойлан Г.Б., Кенни Л.С. и др. . Метаболомный профиль пуповинной крови при гипоксической ишемической энцефалопатии новорожденных. PLoS ONE. (2012) 7: e50520. 10.1371 / journal.pone.0050520 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 48.Коуэн Ф., Резерфорд М., Грюнендал Ф., Экен П., Меркури Э., Байддер Г.М. и др. . Происхождение и сроки поражения головного мозга у доношенных детей с неонатальной энцефалопатией. Ланцет. (2003) 361: 736–42
10.1016 / S0140-6736 (03) 12658-X [PubMed] [CrossRef] [Google Scholar] 49. Ян М.М., Camfield PR. Исход неонатального инсульта у доношенных детей без значительной асфиксии при рождении. Eur J Pediatr. (1998) 157: 846–8. 10.1007 / s004310050950 [PubMed] [CrossRef] [Google Scholar] 50. Рамасвами В., Миллер С.П., Баркович А.Дж., Партридж Дж.С., Ферриеро Д.М.Перинатальный инсульт у доношенных детей с неонатальной энцефалопатией. Неврология. (2004) 62: 2088–91. 10.1212 / 01.WNL.0000129909.77753.C4 [PubMed] [CrossRef] [Google Scholar] 51. Scherer EB, Loureiro SO, Vuaden FC, da Cunha AA, Schmitz F, Kolling J, et al. . Легкая гипергомоцистеинемия увеличивает уровни ацетилхолинэстеразы мозга и провоспалительных цитокинов в различных тканях. Mol Neurobiol. (2014) 50: 589–96. 10.1007 / s12035-014-8660-6 [PubMed] [CrossRef] [Google Scholar] 52. Harteman JC, Groenendaal F, Benders MJ, Huisman A, Blom HJ, de Vries LS.Роль тромбофильных факторов у доношенных детей с неонатальной энцефалопатией. Pediatr Res. (2013) 73: 80–6. 10.1038 / pr.2012.150 [PubMed] [CrossRef] [Google Scholar] 53. Calkavur S, Akisu M, Olukman O, Balim Z, Berdeli A, Cakmak B и др. . Генетические факторы, влияющие на краткосрочный исход развития нервной системы у доношенных новорожденных с гипоксически-ишемической энцефалопатией. J Int Med Res. (2011) 39: 1744–56. 10.1177 / 147323001103
7 [PubMed] [CrossRef] [Google Scholar] 54. Додельсон де Кремер Р., Гроссо С. Материнская мутация 677C> T в гене метилентетрагидрофолатредуктазы, связанная с тяжелым повреждением головного мозга у потомства.Clin Genet. (2005) 67: 69–80. [PubMed] [Google Scholar] 55. Odd D, Váradi A, Rajatileka S, Molnár E, Luyt K. Связь между реанимацией новорожденных и однонуклеотидным полиморфизмом rs1835740. Acta Paediatr. (2016) 105: e307–12. 10.1111 / apa.13421 [PubMed] [CrossRef] [Google Scholar] 56. Bruyland M, Liebaers I, Sacre L, Vandeplas Y, De Meirleir L, Martin JJ. Неонатальная миотубулярная миопатия с вероятным X-сцепленным наследованием: наблюдения за новой семьей с обзором литературы. J Neurol.(1984) 231: 220–2. 10.1007 / BF00313942 [PubMed] [CrossRef] [Google Scholar] 57. Баркович А.Дж., Вестмарк К., Партридж К., Сола А., Ферриеро Д.М. Перинатальная асфиксия: результаты МРТ в первые 10 дней. AJNR Am J Neuroradiol. (1995) 16: 427–38. [PubMed] [Google Scholar] 58. Barrett MJ, Donoghue V, Mooney EE, Slevin M, Persaud T., Twomey E, et al. . Изолированное острое некистозное повреждение белого вещества у доношенных детей с неонатальной энцефалопатией. Arch Dis Child Fetal Neonatal Ed. (2013) 98: F158 – F160. 10.1136 / archdischild-2011-301505 [PubMed] [CrossRef] [Google Scholar]
Необходимость распознавания множественных этиологий для оптимального управления
Front Pediatr.2019; 7: 142.
, 1, 2 , 1, 3, 4 и 1, 2, 3, 4, 5,
64 *
4 Сайма Аслам
1 Педиатрия, Национальный родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
Тэмми Стрикленд
1 Педиатрия, Национальный родильный дом , Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити-колледж в Дублине, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Больница Университета Кумб для женщин и младенцев, Дублин, Ирландия
Элеонора Дж. .Моллой
1 Педиатрия, Национальный родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити College Dublin, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Университетская больница для женщин и младенцев Кумб, Дублин, Ирландия
5 Неонатология, Детская больница Богоматери, Дримна, Ирландия
1 Педиатрия, национальная Родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити-колледж Дублина, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Coombe Women’s и больница Университета младенцев, Дублин, Ирландия
5 Неонатология, Детская больница Богоматери, Дримна, Ирландия
Отредактировал: Микко Холлман, Университет Оулу, Финляндия
Рецензент: Георг Шмольцер, Университет Альберты, Канада; Аакаш Пандита, Институт медицинских наук им. Санджая Ганди, Индия
Эта статья была отправлена в раздел «Неонатология» журнала «Границы в педиатрии»
Поступила в редакцию 15 октября 2018 г .; Принят в печать 26 марта 2019 г.
Авторские права © 2019 Aslam, Strickland and Molloy.
Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License (CC BY). Использование, распространение или воспроизведение на других форумах разрешено при условии указания автора (авторов) и правообладателя (ов) и ссылки на оригинальную публикацию в этом журнале в соответствии с принятой академической практикой. Запрещается использование, распространение или воспроизведение без соблюдения этих условий.
Эта статья цитируется в других статьях в PMC.
Abstract
Неонатальная энцефалопатия (NE) связана с высокой смертностью и заболеваемостью. Факторы, предрасполагающие к NE, могут быть антенатальными, перинатальными или их комбинацией. Антенатальные материнские факторы, семейные факторы, генетическая предрасположенность, гипоксическая ишемическая энцефалопатия, инфекции, плацентарные аномалии, тромбофилия, дефекты коагуляции и метаболические нарушения — все это вовлечено в патогенез NE. В настоящее время терапевтическая гипотермия — единственное доступное лечение, независимо от этиологии.Распознавание этиологии вовлеченного НЭ может также помочь в проведении таких исследований, как метаболические исследования и обследования на сепсис, для обеспечения оптимального лечения. Понимание этиологии NE может позволить разработать целевую дополнительную терапию, связанную с основным механизмом, и разработать превентивные стратегии.
Ключевые слова: неонатальная энцефалоптия, этиология, антенатальная, перинатальная, таргетная дополнительная терапия
Введение
Неонатальная энцефалопатия (НЭ) — сложное заболевание новорожденных, характеризующееся измененным уровнем сознания, судорогами, плохим тонусом. для инициирования или поддержания дыхания (1) и связан с полиорганной дисфункцией (2).Заболеваемость NE оценивается в 3 случая на 1000 живорождений (3). NE может быть результатом широкого спектра причин и является клиническим термином, не определяющим этиологию. Единственное доступное лечение — это терапевтическая гипотермия (ТГ) с максимальной пользой, если начать в первые 6 часов жизни (4). Существует несколько причин НЭ, таких как гипоксическая ишемическая энцефалопатия (ГИЭ), перинатальные инфекции, аномалии плаценты, метаболические нарушения, коагулопатии и сосудистый инсульт новорожденных (). Однако более чем в половине случаев причина НЭ остается неустановленной (5).
Многофакторная этиология неонатальной энцефалопатии. Многие факторы предрасполагают к возникновению неонатальной энцефалопатии либо по отдельности, либо в комбинации, включая (A) Факторы риска до зачатия, (B) Сопутствующие заболевания или события у матери до родов / во время родов, (C) Патология плаценты, (D) Гипоксия-ишемия, (E) Перинатальная инфекция, (F) Неонатальный инсульт или тромбофилия, (G) Метаболические нарушения и (H) Генетические и эпигенетические аномалии.ПРОМ, длительный разрыв плодных оболочек; ЗВУР, ограничение внутриутробного развития.
Использование термина NE vs. HIE противоречиво. Было предложено использовать термин NE для доношенных и поздних недоношенных новорожденных, у которых не было выявленных дозорных событий (6, 7). Трудно доказать наличие церебральной гипоксической ишемии, за исключением моделей на животных и конкретных случаев неонатального инсульта. Все текущие параметры, включая pH и судороги, неспецифичны (7). Некоторые из паттернов черепно-мозговых травм, наблюдаемых у пациентов с NE, могут быть воспроизведены на животных моделях с помощью гипоксии-ишемии, но это не доказывает, что все NE вызваны HIE (7).Несколько опубликованных популяционных исследований показали, что факторы риска до родов и неасфиксии связаны с НЭ (6). Напротив, некоторые авторы утверждают, что ГИЭ является причиной НЭ в 50–80% случаев на основании клинических критериев, критериев ЭЭГ и МРТ (1). Поэтому в этом обзоре мы использовали термин NE, и мы стремились изучить различные этиологии, связанные с NE.
Материнские факторы
Материнская гипертензия (16%) была важным фактором дородового риска НЭ в реестре неонатальной энцефалопатии Оксфордской сети штата Вермонт ( n = 4 165).Также была более высокая частота клинического хориоамнионита, длительного разрыва плодных оболочек и гипотиреоза матери. Хотя острый асфиксический эпизод был зарегистрирован в 15% случаев, связь с воспалением была обнаружена у 24% (5).
Популяционное исследование в Западной Австралии показало, что социально-экономический статус, семейный анамнез судорог, неврологические проблемы и зачатие после лечения бесплодия были независимыми факторами риска до зачатия для NE ( n = 164) (8).Заболевание щитовидной железы матери, кровотечение во время беременности, вирусные заболевания, преэклампсия, аномальная плацента, задержка внутриутробного развития и переношенность были другими важными факторами риска в дородовой период (8). Идентифицируемые дородовые факторы риска НЭ были обнаружены в 69% случаев, внутриродовые факторы риска — в 5%, как дородовые, так и во время родов — в 24% и отсутствие фактора риска — в 2%. Только в 4% случаев внутриродовая гипоксия была выявлена без каких-либо факторов риска до родов или до зачатия (9). Было обнаружено, что ограничение роста в развитых странах и беременность двойней в развивающихся странах связаны с НЭ.Заболевание щитовидной железы у матери, дородовое наблюдение, инфекция, роды и тактика ведения родов должны стать важными модификаторами в исследовании 27 новорожденных с НЭ и 100 детей контрольной группы (3). Дородовые (74 против 18%), внутриродовые (67 против 19%) и острые внутриродовые события (33 против 2%) более вероятны у младенцев с НЭ по сравнению с контрольной группой. Следовательно, в неонатальном клиническом анамнезе подробный материнский анамнез важен и может быть путем к профилактическим стратегиям в будущем.
Из 45 новорожденных с NE 36% имели дозорные эпизоды, 40% имели хориоамнионит и 11% имели оба этих заболевания.Если данные дозорных событий были исключены, то возраст матери> 35 лет (ОР 2,5; 95% ДИ 1,1–5,6) и инфекция мочевыводящих путей во время беременности (ОР 2,6; 95% ДИ 1,0–6,5) были потенциальными факторами дородового риска для NE (10).
Гипоксия-ишемия
Хотя концепция гипоксии-ишемии четко выражена в моделях на животных, она может не подходить для использования во всех случаях неонатальной NE у человека. «Дозу» и продолжительность гипоксии, а также степень ишемии можно напрямую измерить на животной модели.Однако у новорожденных людей это неизвестно, если нет контрольного события, и впоследствии не используются суррогатные маркеры гипоксии. Badawi et al. показали, что асфиксия во время родов считается сопутствующим фактором в 29% случаев НЭ и самостоятельным фактором только в 4% случаев (9). Было обнаружено, что внутриродовая гипоксия-ишемия является одним из факторов, способствующих развитию НЭ в 30% случаев в развитых и 60% в развивающихся странах (3). Американский колледж акушеров и Американская академия педиатрии определили дозорное событие в своем документе о неонатальной энцефалопатии и неврологических исходах (Obstet Gynecol 2014).Следующее соответствует острому пери- или интранатальному событию: дозорное гипоксическое или ишемическое событие, возникающее непосредственно перед или во время родов и родоразрешения, например разрыв матки или тяжелая отслойка плаценты; паттерны пульсометра плода, соответствующие острым послеродовым или интранатальным событиям; сроки и тип травм головного мозга, основанные на исследованиях изображений, согласующихся с этиологией острого послеродового или внутриродового события, и отсутствуют доказательства других проксимальных или дистальных факторов, которые могли бы быть способствующими факторами.Кроме того, сочетание низких баллов по шкале Апгарса, ацидемии, аномального кардиотокографа, изменений МРТ, согласующихся с гипоксией-ишемией и полиорганной дисфункцией, — все это связано с гипоксически-ишемической этиологией, но в равной степени может быть изменено сепсисом или другими причинами NE. Асфиксичные родовые явления и воспаление присутствовали только в 12,6% случаев церебрального паралича (11). У новорожденных с NE ( n = 405) следующие факторы были независимо связаны с NE ( p -значение = 0,001), включая: только 1 дородовой период (гестационный возраст> 41 недели) и 7 факторов во время родов, включая длительный разрыв плодных оболочек, аномальные кардиотокограф, густой меконий, дозорные события, дистоция плеча, тугая затылочная пуповина и отказ вакуума (12).В когорте из 26 новорожденных с дозорными событиями NE (ОР 74,9, 95% ДИ 11,9-бесконечность, p <0,001) и отслеживание ЧСС плода категории 3 (28,0% против 4,0%, p = 0,002) были сильно связанный с NE (13). В когорте из 45 новорожденных у 36% были дозорные события, а у 11% были как дозорные, так и хориоамнионит (10).
Нейровизуализация с использованием магнитно-резонансной томографии, традиционной, диффузионной и спектроскопии в период от 24 до 96 часов жизни дает полезные рекомендации относительно возможных сроков возникновения церебрального инсульта, особенно диффузных аномалий.Аномалии, вызванные травмой головного мозга, становятся наиболее очевидными через 7 дней при использовании качественной МРТ, диффузии и спектроскопии. Глубокое ядерное серое вещество или водораздел кортикального повреждения развиваются по четко определенному типу повреждения мозга и типичны для гипоксически-ишемического повреждения мозга у новорожденного. Генетические и метаболические причины могут быть исследованы, если на МРТ существует другая картина травмы головного мозга или эволюция травмы. Признаки того, что послеродовая гипоксия-ишемия не была причиной НЭ, предлагаются на МРТ: порэнцефалия, очаговый артериальный инфаркт, венозный инфаркт, изолированное внутрипаренхиматозное или внутрижелудочковое кровоизлияние или атипичные паттерны метаболических энцефалопатий.
При NE, связанном с острым дозорным событием (HIE), типичная картина повреждения на МРТ показала вовлечение базальных ганглиев, таламуса с ассоциированной задней конечностью внутренней капсулы и, в тяжелых случаях, вовлечение ствола мозга (14). При NE без задокументированного дозорного события вовлечение базальных ганглиев или таламуса (BGT) также связано с изменениями белого вещества в 50% случаев (14). BGT с обширным повреждением белого вещества (WM) был обнаружен в 14%, BGT с WM от легкой до умеренной — в 56%, изолированное таламическое повреждение — в 5%, умеренное повреждение WM — только у 2% и легкое WM или нормальное — у 23% в 48%. младенцы с ГИЭ.Внутренняя капсула была аномальной у 93% пациентов с умеренным и тяжелым повреждением WM и была связана со смертью и ХП у 86% пациентов (15).
Картина повреждения головного мозга может указывать на возможную причину, например, повреждение коркового вещества и белого вещества (очаговое / мультифокальное) может быть связано с плацентарной недостаточностью и хориоамнионитом. Ранняя категоризация пациентов в соответствии с типом травмы головного мозга может привести к другому терапевтическому подходу, поскольку на животных моделях было показано, что разные уровни гипотермии защищают от повреждения коры головного мозга или глубокого серого вещества, поэтому для получения максимальной пользы могут потребоваться специфические для пациента протоколы гипотермии.Точно так же в моделях на животных разные режимы охлаждения, системное и селективное, приводят к разной температуре мозга (16).
Трудно окончательно установить наличие, продолжительность и степень гипоксии и ишемии у новорожденных, поэтому использовались суррогатные маркеры, такие как pH и судороги (7). Следовательно, биомаркеры мультиорганного поражения могут быть полезны для диагностики или оценки тяжести гипоксической ишемии и прогнозирования исхода при NE. Сердечный тропонин является маркером ишемии миокарда у новорожденных и детей и высвобождается из миоцитов после повреждения их мембраны.Сердечный тропонин I (cTnI) был значительно выше у новорожденных с ГИЭ в первые 48 часов по сравнению с контрольной группой ( p <0,0005) (17). Сердечный TnI был повышен у новорожденных с более высокой степенью НЭ и у тех, кому потребовались инотропы (18). Пороговое значение <0,22 нг / мл для нормотермических и <0,15 нг / мл для гипотермических младенцев с NE предсказывало нормальный исход развития нервной системы (19).
Гипоксия приводит к усилению эритропоэза и выбросу незрелых ядерных эритроцитов (nRBC) в кровоток (20).ЯРБК пуповинной крови были значительно выше у новорожденных, подвергшихся асфиксии, по сравнению с контрольной группой, а также коррелировали с апгаром через 1 мин, pH и развитием NE (20). Количество ядерных эритроцитов на 100 лейкоцитов было выше у новорожденных с НЭ по сравнению с контрольной группой, младенцев с НЭ средней / тяжелой или легкой степени ( p = 0,016) и у новорожденных с плохим исходом нервного развития ( p = 0,03) 21). Следовательно, стандартизованное измерение воздействия клинической гипоксии было бы полезным с использованием комбинации этих маркеров и могло бы помочь в определении времени инсульта и корреляции с доклиническими моделями на животных.
Инфекция
Риск спастического церебрального паралича (ДЦП) и квадриплегического ДЦП повышался при сочетании инфекции и асфиксии (22). Уровни интерлейкина (ИЛ) -6 через 6 часов связаны с отклонениями от нормы неврологического обследования (23). NE, инотропная поддержка, судороги без менингита, потребность в интубации и более низкий 5-минутный апгар были более вероятны у новорожденных с ХП при наличии инфекции у матери по сравнению с ХП без инфекции (22).
Материнские и ранние неонатальные инфекции представляют собой диагностическую проблему.Ведутся споры о том, может ли скрытая инфекция, не обнаруживаемая обычными методами культивирования, быть связана с неврологическим повреждением во всех возрастных группах. Полимеразная цепная реакция (ПЦР) выявила 11 случаев бактериемии у энцефалопатических новорожденных в Африке, у которых был отрицательный результат посева крови (NE n = 201). ПЦР в сочетании с посевом крови привела к обнаружению бактериальных продуктов в 8,9% случаев НЭ по сравнению с 3,1% при использовании одного посева крови (24). В метаанализе стрептококк группы B (GBS) был связан с NE в 0.58% случаев и смертность были выше при использовании СГБ плюс НЭ по сравнению с одним НЭ (25). В когорте из 45 новорожденных 40% имели хориоамнионит и 11% имели как дозорные события, так и хориоамнионит (10).
Терапевтическая гипотермия задерживает рост и пик ответа с-реактивного белка (СРБ), а также приводит к снижению количества лейкоцитов и нейтрофилов по сравнению с нормотермными новорожденными (26). Это влияние гипотермии на задержку развития естественных воспалительных маркеров следует учитывать при выборе лечения антибиотиками и продолжительности лечения новорожденных с НЭ.
Следовательно, полное обследование на сепсис имеет важное значение у всех детей с НЭ. Стандартных рекомендаций по выполнению люмбальной пункции во всех случаях НЭ не существует, и их можно выбирать в каждом конкретном случае. Кандидатами могут быть младенцы с повышенным WCC и CRP или факторами риска септического риска. Существуют также технические и практические проблемы для поясничной пункции у младенцев с NE, которые являются ригидными из-за TH, а также часто изначально имеют отек мозга при ультразвуковом исследовании черепа.
Аномалии плаценты
Поражение пуповины, хориоамнионит, васкулит плода, меконий хориональной пластинки и тромботическая васкулопатия плода часто встречались в плацентарных поражениях у пациентов с NE ( n = 23) (27).Поражения плаценты, указывающие на тромбоз и снижение фетоплацентарного кровотока, являются значимыми и независимыми факторами риска НЭ ( n = 93) (28). Наличие более одного поражения плаценты увеличивает вероятность НЭ, но не было никакой корреляции между патологией плаценты и картиной повреждения на МРТ ( n = 56) (29). Аномальная патология плаценты была обнаружена у 29% новорожденных с дозорными событиями и у 73% младенцев без дозорных явлений ( p = 0,0001), перенесших терапевтическую гипотермию (30).Воспалительные поражения плаценты чаще наблюдались у новорожденных без дозорных событий ( p = 0,002) (30). Хронический виллит был связан с повреждением базальных ганглиев (BGT), тогда как наличие ядерных эритроцитов, снижение созревания плаценты и хронический виллит также приводили к повреждению белого вещества / водораздела вместе с вовлечением BGT ( n = 95) (31).
Доказательства связи хориоамнионита с НЭ разнообразны. Предполагается, что время инфицирования и степень воспалительного ответа могут привести либо к прекондиционированию, либо к сенсибилизации и могут вызвать либо защитный эффект, либо дальнейшее усиление перинатального повреждения головного мозга, соответственно (32).Этот эффект был продемонстрирован на животных моделях. Липополисахарид (ЛПС), вводимый за 4–6 ч до 20 и 50 мин воздействия HI, приводил к усилению травм головного мозга. Однако введение LPS за 24 часа до 50-минутного воздействия HI привело к значительному ослаблению травм головного мозга (32). КА выявлена у 8 новорожденных с признаками перинатальной асфиксии (всего n = 23) (27). Младенцы с NE и TH имели более высокие шансы на наличие CA по сравнению с младенцами, которые не получали TH ( n = 98) (33).CA, васкулит и фунизит были связаны с NE степени I, виллитом с NE II и фунизитом с III степенью у 141 новорожденного с NE и 309 контрольных (29). CA был связан с более низким риском черепно-мозговой травмы и плохим когнитивным исходом по сравнению с не-CA (скорректированный OR 0,3; 95% CI 0,1–0,7, p = 0,004) у новорожденных с NE ( n = 258), хотя только У 20 новорожденных были гистологические доказательства СА. В той же когорте новорожденные с признаками сепсиса имели более высокие шансы на повреждение водораздела и аномальные нейромоторные показатели, чем у новорожденных без каких-либо клинических признаков ( p = 0.007) (34). У 120 младенцев с сочетанием перинатального ацидоза, NE и хориоамнионита с ответом плода или без него и пятнистый / диффузный хронический виллит были независимо связаны с тяжестью NE (35). Единственным индивидуальным предиктором патологического исхода нервного развития через 22-24 месяца после терапии гипотермией был диффузный хронический виллит. Гистологическая CA имела низкую прогностическую ценность для развития энцефалопатии и смерти у NE ( n = 51) (36), но материнская лихорадка ( n = 336) во время родов была независимым фактором для NE (скорректированное OR 4.72, 95% ДИ 1,28–17,4) (37). Клинический хориоамнионит был связан с более высокими уровнями IL-6, IL-8 в пуповинной крови и регулировался активацией нормальных Т-клеток, экспрессируемых и секретируемых (RANTES) в NE ( n = 61). В когорте из 67 новорожденных с хориоамнионитом NE, независимо от того, были ли клинические или гистологические данные связаны со стойким метаболическим ацидозом, это может предсказать плохой неврологический исход (38).
Патология плаценты описывается как «черный ящик» беременности. Стандартизированная классификация результатов патологии плаценты важна для дальнейшего определения этиологии NE (39).
Нарушения обмена веществ
Нарушения обмена веществ являются редкими причинами НЭ, но их всегда следует учитывать. Врожденные нарушения метаболизма (ВЭМ) присутствуют в неонатальном периоде после нормального периода выздоровления и отсутствия признаков перинатальной асфиксии, но неврологические и полиорганные поражения могут проявляться как НЭ (40). Митохондриальные нарушения также являются важной причиной НЭ (41).
Амплитудная интегрированная электроэнцефалограмма (аЭЭГ) была отклонена от нормы у 27 новорожденных с ВЭМ, причем наиболее устойчивыми признаками были аномальная фоновая активность и судороги.Не было различий в аЭЭГ для энцефалопатии, связанной с IEM или NE, и дифференцировать можно было только на основании клинического подозрения (42). Единственное метаболическое расстройство с диагностической ЭЭГ — это некетотическая гиперглицинемия с первоначальным паттерном «подавление-всплеск», переходящим в гипсаритмию в раннем или среднем младенчестве и диагностируемое путем измерения уровня глицина в спинномозговой жидкости (42). Имеются также отдельные сообщения о случаях ИЭМ, таких как дефицит сульфитоксидазы и цитохрома С, проявляющийся как НЭ (43, 44).
Результаты МРТ могут варьироваться в зависимости от типа врожденной ошибки метаболизма (ВЭМ) и могут варьироваться от поражения белого вещества до поражения глубоких серых ядер. Митохондриальные энцефалопатии имеют симметричное двустороннее распределение и изначально могут быть диагностированы как NE (45). Следует учитывать метаболические нарушения, если нет явных явлений во время родов, стойкий лактоацидоз и / или гипогликемия (45) и начато обследование. Различные паттерны повреждений на МРТ головного мозга могут помочь дифференцировать метаболические нарушения от НЭ.Поражение Globus Pallidus часто встречается при IEM по сравнению с NE, хотя картина повреждения при дефиците сульфитоксидазы и дефиците фактора молибдена может имитировать NE (46).
Изолированные приступы связаны с такими расстройствами, как: судороги, связанные с пиридоксином, некетотическая гиперглицинемия (НКГ), дефицит дигидропиримидиндегидрогеназы, дефицит сульфитоксидазы (либо изолированный, либо как часть дефицита кофактора молибдена), трансаминазы 4-аминобутират-аминотрансферазы (ГАБТрансферазы). ) дефицит, судороги, связанные с фолиевой кислотой, дефицит 3-фосфоглицератдегидрогеназы, дефицит гуанидиноацетатметилтрансферазы (GAMT) и дефицит переносчика глюкозы (GLUT-1).У младенцев с полиорганными поражениями, судорогами, метаболическим ацидозом, молочной железой, гипераммониемией могут быть: органическая ацидемия, дефекты цикла мочевины, пероксисомальные нарушения (например, синдром Зеллвегера) или митохондриальные нарушения.
Подробный семейный анамнез для установления факторов риска, таких как родство родителей или ранее пораженный ребенок, важен, поскольку большинство врожденных нарушений метаболизма имеют аутосомно-рецессивное или материнское наследование. Базовые исследования, такие как электролиты, аммиак, сывороточные аминокислоты, лактат, ацилкарнитин и органическая кислота в моче, могут быть рассмотрены при NE (40).Есть проблемы с метаболическим тестированием, так как их может потребоваться повторить, если ребенок очень плохо себя чувствует с полиорганной дисфункцией во время отбора образцов (46). Недавние исследования показали большой потенциал метаболомики как биомаркеров NE. Было показано, что содержание сукцината повышено у детей с НЭ, которые серьезно пострадали (47).
Тромбофилия и неонатальный инсульт
Асфиксия (в 4% случаев) участвует в патогенезе неонатального инсульта (48). Фокальные клонические приступы являются наиболее частым проявлением неонатального инсульта (49), и 6 младенцев с инсультом были обнаружены в когорте NE ( n = 124) (50).Эти дети обычно страдали судорогами и имели худшие исходы с точки зрения нервного развития, чем остальная когорта. Нарушения свертывания крови, такие как полицитемия, лейденский фактор V, нарушения гемоглобина и мутации протромбина, не были обнаружены у 4 из 6 обследованных пациентов (50).
В моделях на животных повышенные уровни гомоцистеина приводили к увеличению провоспалительных цитокинов, таких как фактор некроза опухоли альфа (TNFα), интерлейкин 1 бета (IL-1β) и IL-6 в гиппокампе и коре головного мозга.Это провоспалительное состояние может быть ответственным за нейрональные и цереброваскулярные эффекты, наблюдаемые у взрослых (51). Роль гомоцистеина или полиморфизмов в гене метилентетрагидрофолатредуктазы в возникновении неонатального повреждения головного мозга неясна (52). В когорте из 118 новорожденных с НЭ повреждение белого вещества / водораздела с большей вероятностью было связано с гипогликемией, полиморфизмом метилентетрагидрофолатредуктазы (MTHFR) и уровнями гомоцистеина в плазме в верхнем квартиле нормы (52).
Генетические и эпигенетические аномалии
Отсутствуют опубликованные данные, связывающие генетическую предрасположенность с развитием NE. У 40 пациентов с NE генетическая изменчивость протромбических факторов, таких как протромбин G20210A, фактор V Leiden G1691A и метилентетрагидрофолатредуктаза [MTHFR] C677T, и ген фактора некроза опухоли не повлияли на оценку NE, ЭЭГ, смерть, краниальное УЗИ (США) , неврологический исход при выписке через 6 и 12 месяцев. Полиморфизм гена интерлейкина-6 (IL-6 174GC) имел защитный эффект и был связан с нормальной ЭЭГ, краниальным УЗИ и неврологическим обследованием при выписке (53).В ретроспективном исследовании «случай-контроль» с участием 11 новорожденных с NE у матерей была обнаружена более высокая частота полиморфизма MTHFR (7 гомозиготных и 4 гетерозиготных) по сравнению с контрольной группой (54). Генетический полиморфизм может увеличивать риск или тяжесть неонатального повреждения головного мозга при NE, и его следует учитывать (53).
В рамках лонгитюдного исследования родителей и детей, проведенного Avon, было проведено генотипирование 7611 доношенных детей, и мерилом воздействия было наличие одного или нескольких минорных аллелей в одном из 3 SNP (rs2284411, rs2498804, rs1835740).Первичным результатом была необходимость реанимации при рождении, что было связано с rs1835740 (55). Требуются более крупные международные совместные исследования для определения необходимого количества пациентов для изучения генетических связей и разделения пациентов по этиологии.
Другая категория младенцев с генетической причиной неонатальной энцефалопатии — это дети с миопатиями и энцефалопатиями новорожденных. Пациенты, унаследовавшие миопатию (центронуклеарную миопатию), могут иметь неонатальный дистресс, гипотонию и признаки, указывающие на ГИЭ (56).Врожденная миотоническая дистрофия 1 типа характеризуется гипотонией и тяжелой генерализованной слабостью при рождении, часто с дыхательной недостаточностью, умственной отсталостью и ранней смертью. Это вызвано экспансией тринуклеотидного повтора CTG в некодирующей области DMPK .
В будущем подробное генотипирование, включая более легкий доступ к методам микроматриц в клинических условиях, предоставит больше информации, позволяющей индивидуализированный уход и потенциально классифицировать младенцев по генотипу.
Нейровизуализация
На МРТ можно увидеть различные модели травм, но это не исключает HIE как причины травмы. Характер повреждения зависит от тяжести, продолжительности и повторяемости гипоксической ишемии и может привести к поражению базальных ганглиев, таламуса, ствола мозга и / или белого вещества головного мозга в различных сочетаниях (1). При глубокой гипоксии преобладает повреждение более глубоких серых структур, то есть базальных ганглиев и таламуса. Объясняется это тем, что эти участки миелинизированы и имеют более высокую скорость метаболизма.Состояния, которые уменьшают, а не вызывают полное прекращение кровотока, такие как анемия и гиповолемия, связаны с повреждением коры головного мозга и сохранением более глубоких серых структур (57). В когорте из 245 пациентов с NE 197 (80%) результаты МРТ соответствовали острому перинатальному инсульту. МРТ у 40 младенцев (16%) были нормальными. У 9 младенцев (4%) были выявлены признаки тромбоза / инфаркта, генетических нарушений, антенатального инсульта и митохондрий (дефицит комплекса I) на МРТ в дополнение к гипоксическому ишемическому инсульту.Нейровизуализация у 8 (3%) младенцев с клиническим диагнозом НЭ показала либо врожденную ошибку метаболизма, нервно-мышечное расстройство, либо отсутствие диагноза, и эти результаты не соответствовали гипоксической ишемии (48). Плацентарный виллит высокой степени неизвестной этиологии ( n = 4) был обнаружен в когорте из 36 пациентов, связанных с повреждением белого вещества, вторичным по отношению к воспалению / окислительному стрессу в перинатальном периоде (58).
Значение для терапии
Все младенцы с NE могут не в одинаковой степени выиграть от переохлаждения.Следовательно, выявление точной этиологии в каждом случае NE имеет значение для лечения, поскольку есть некоторые излечимые причины, которые требуют быстрого определения для оптимального лечения. Использование бактериальной ПЦР для выявления инфекции у новорожденных с NE может быть более полезным, чем только посев крови с низким выходом бактерий, а также гипотермия может уменьшить воспалительную реакцию. Гистология плаценты отражает внутриматочную среду и может прояснить основную этиологию. Все новорожденные с риском IEM должны быть обследованы на предмет метаболических нарушений, так как этим пациентам могут быть полезны специфические методы лечения, а не гипотермия.Точно так же скрининг на тромбофилию следует рассматривать у пациентов из группы риска, таких как пациенты с инсультом, семейный анамнез тромбофилии. Подробная оценка этиологии NE важна для выявления излечимых причин и категоризации этой гетерогенной группы новорожденных, чтобы можно было подобрать соответствующее лечение в соответствии с этиологией и улучшением отдаленных результатов. Точно так же будет полезно стратифицировать большие многоцентровые когорты младенцев с NE по этиологии, чтобы полностью понять этиологию, реакцию на лечение гипотермией и отдаленные результаты.
Авторские взносы
SA: основной автор; ТС: помогал с поиском релевантных статей и рисунка; ЭМ: автор-руководитель.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Ссылки
1. Volpe JJ. Неонатальная энцефалопатия: неадекватный термин для гипоксически-ишемической энцефалопатии.Энн Нейрол. (2012) 72: 156–66. 10.1002 / ana.23647 [PubMed] [CrossRef] [Google Scholar] 2. Шах П., Рип Хаген С., Бейен Дж, Перлман М. Мультиорганная дисфункция у младенцев с постасфиксиальной гипоксически-ишемической энцефалопатией. Arch Dis Child Fetal Neonatal Ed. (2004) 89: F152 – F155. 10.1136 / adc.2002.023093 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 3. Куринчук Дж. Дж., Уайт-Конинг М., Бадави Н. Эпидемиология неонатальной энцефалопатии и гипоксически-ишемической энцефалопатии. Early Hum Dev. (2010) 86: 329–38.10.1016 / j.earlhumdev.2010.05.010 [PubMed] [CrossRef] [Google Scholar] 4. Джейкобс С.Е., Берг М., Хант Р., Тарнов-Морди В.О., Индер Т.Э., Дэвис П.Г.
Охлаждение новорожденных с гипоксической ишемической энцефалопатией. База данных Cochr Syst Rev. (2013) 1: CD003311
10.1002 / 14651858.CD003311.pub3 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 5. Нельсон К.Б., Бингхэм П., Эдвардс Э.М., Хорбар Д.Д., Кенни М.Дж., Индер Т. и др. . Антецеденты неонатальной энцефалопатии в реестре энцефалопатии Оксфордской сети Вермонта. Педиатрия.(2012) 130: 878–86. 10.1542 / peds.2012-0714 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 6. Нельсон КБ. Это HIE?
И почему это важно Acta Paediatr. (2007) 96: 1113–4. 10.1111 / j.1651-2227.2007.00364.x [PubMed] [CrossRef] [Google Scholar] 7. Дамманн О., Ферриеро Д., Грессенс П.
Неонатальная энцефалопатия или гипоксически-ишемическая энцефалопатия?
Соответствующая терминология имеет значение Pediatr Res. (2011) 70: 1-2. 10.1203 / PDR.0b013e318223f38d [PubMed] [CrossRef] [Google Scholar] 8. Бадави Н., Куринчук Дж. Дж., Кио Дж. М., Алессандри Л. М., О’Салливан Ф., Бертон П. Р. и др.. Факторы дородового риска энцефалопатии новорожденных: исследование случай-контроль в Западной Австралии. BMJ. (1998) 317: 1549–53. 10.1136 / bmj.317.7172.1549 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 9. Бадави Н., Куринчук Дж. Дж., Кио Дж. М., Алессандри Л. М., О’Салливан Ф., Бертон П. Р. и др. . Факторы риска внутриутробной энцефалопатии новорожденных: исследование случай-контроль в Западной Австралии. BMJ. (1998) 317: 1554–8. 10.1136 / bmj.317.7172.1554 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 10. Паркер SJ, Kuzniewicz M, Niki H, Wu YW.Факторы дородового и внутриродового риска гипоксически-ишемической энцефалопатии в когорте новорожденных в США. J Pediatr. (2018) 203: 163–9. 10.1016 / j.jpeds.2018.08.028 [PubMed] [CrossRef] [Google Scholar] 11. Адамсон С.Дж., Алессандри Л.М., Бадави Н., Бертон П.Р., Пембертон П.Дж., Стэнли Ф. Предикторы неонатальной энцефалопатии у доношенных новорожденных. BMJ. (1995) 311: 598–602
10.1136 / bmj.311.7005.598 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 12. Мартинес-Биарж М., Диез-Себастьян Дж., Вустхофф Си-Джей, Меркури Е., Коуэн FM.Дородовые и внутриродовые факторы, предшествующие неонатальной гипоксически-ишемической энцефалопатии. Педиатрия. (2013) 132: e952 – e959
10.1542 / peds.2013-0511 [PubMed] [CrossRef] [Google Scholar] 13. Торбенсон В.Е., Толчер М.К., Несбитт К.М., Колби К.Э., Эль-Нашар С.А., Гостоут Б.С. и др. . Внутриродовые факторы, связанные с неонатальной гипоксической ишемической энцефалопатией: исследование случай-контроль. BMC Беременность и роды. (2017) 17: 415
10.1186 / s12884-017-1610-3 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 14. Резерфорд М., Маламатениу К., МакГиннесс А., Оллсоп Дж., Биарж М.М., Конселл С.Магнитно-резонансная томография при гипоксически-ишемической энцефалопатии. Early Hum Dev. (2010) 86: 351–60. 10.1016 / j.earlhumdev.2010.05.014 [PubMed] [CrossRef] [Google Scholar] 15. Okereafor A, Allsop J, Counsell SJ, Fitzpatrick J, Azzopardi D, Rutherford MA и др. . Характер черепно-мозговой травмы у новорожденных, подвергшихся перинатальным дозорным событиям. Педиатрия. (2008) 121: 906–14. 10.1542 / peds.2007-0770 [PubMed] [CrossRef] [Google Scholar] 16. Мецлер М., Говиндан Р., Аль-Шаргаби Т., Везина Г., Андескавадж Н., Ван И и др.. Характер черепно-мозговой травмы и снижение вариабельности сердечного ритма у новорожденных с гипоксической ишемической энцефалопатией. Pediatr Res. (2017) 82: 438–43. 10.1038 / pr.2017.94 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 17. Симович AM, Игрутинович З., Обрадович С., Ристич Д., Вулетич Б., Раданович М. Значение сердечного тропонина I второго поколения в раннем скрининге гипоксически-ишемической энцефалопатии после перинатальной асфиксии. Srp Arh Celok Lek. (2012) 140: 600–5. [PubMed] [Google Scholar] 18. Шастри А.Т., Самарасекара С., Мунираман Х., Кларк П.Концентрации сердечного тропонина I у новорожденных с гипоксически-ишемической энцефалопатией. Acta Paediatr. (2012) 101: 26–9. 10.1111 / j.1651-2227.2011.02432.x [PubMed] [CrossRef] [Google Scholar] 19. Лю X, Chakkarapani E, Stone J, Thoresen M. Влияние компрессий сердца и лечения гипотермии на сердечный тропонин I у новорожденных с перинатальной асфиксией. Реанимация. (2013) 84: 1562–7. 10.1016 / j.resuscitation.2013.07.003 [PubMed] [CrossRef] [Google Scholar] 20. Гош Б., Миттал С., Кумар С., Дадхвал В. Прогнозирование перинатальной асфиксии с ядросодержащими эритроцитами в пуповинной крови новорожденных.Int J Gynaecol Obstet. (2003) 81: 267–71. 10.1016 / S0020-7292 (03) 00124-3 [PubMed] [CrossRef] [Google Scholar] 21. Уолш Б.Х., Бойлан Г.Б., Мюррей Д.М. Ядерные эритроциты и ранняя ЭЭГ: прогнозирование стадии Сарната и двухлетнего исхода. Early Hum Dev. (2011) 87: 335–9. 10.1016 / j.earlhumdev.2011.01.041 [PubMed] [CrossRef] [Google Scholar] 22. Нельсон КБ, Гретер Дж. Потенциально удушающие состояния и спастический церебральный паралич у младенцев с нормальной массой тела при рождении. Am J Obstet Gynecol. (1998) 179: 507–13. 10.1016 / S0002-9378 (98) 70387-4 [PubMed] [CrossRef] [Google Scholar] 23.Шалак Л.Ф., Лапток А.Р., Джафри Х.С., Рамило О., Перлман Дж. Клинический хориоамнионит, повышенные цитокины и травмы головного мозга у доношенных детей. Педиатрия. (2002) 110: 673–80. 10.1542 / peds.110.4.673 [PubMed] [CrossRef] [Google Scholar] 24. Танн CJ, Nkurunziza P, Nakakeeto M, Oweka J, Kurinczuk JJ, Were J и др. . Распространенность патогенов кровотока выше в случаях неонатальной энцефалопатии по сравнению с контрольной группой, использующей новую панель ПЦР-анализов в реальном времени. PLoS ONE. (2014) 9: e97259. 10.1371 / journal.pone.0097259 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 25.Танн С.Дж., Мартинелло К.А., Саду С., Лоун Дж.Э., Сил А.С., Вега-Поблете М. и др.
Группа исследователей неонатальной энцефалопатии GBS. неонатальная энцефалопатия со стрептококками группы b во всем мире: систематический обзор, наборы данных исследовательских групп и метаанализ. Clin Infect Dis. (2017) 65 (Suppl_2): S173–89. 10.1093 / cid / cix662 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 26. Chakkarapani E, Davis J, Thoresen M. Терапевтическая гипотермия задерживает ответ C-реактивного белка и подавляет количество лейкоцитов и тромбоцитов у младенцев с неонатальной энцефалопатией.Arch Dis Child Fetal Neonatal Ed. (2014) 99: F458 – F463. 10.1136 / archdischild-2013-305763 [PubMed] [CrossRef] [Google Scholar] 27. Wintermark P, Boyd T, Gregas MC, Labrecque M, Hansen A. Патология плаценты у новорожденных с асфиксией, отвечающая критериям терапевтической гипотермии. Am J Obstet Gynecol. (2010) 203: 579.e1–9. 10.1016 / j.ajog.2010.08.024 [PubMed] [CrossRef] [Google Scholar] 28. Макдональд Д.Г., Келехан П., Макменамин Дж.Б., Горман В.А., Мэдден Д., Тоббия И.Н. и др. . Плацентарная тромботическая васкулопатия плода связана с неонатальной энцефалопатией.Hum Pathol. (2004) 35: 875–80
10.1016 / j.humpath.2004.02.014 [PubMed] [CrossRef] [Google Scholar] 29. Hayes BC, Cooley S, Donnelly J, Doherty E, Grehan A, Madigan C и др. . Плацента у младенцев> 36 недель беременности с неонатальной энцефалопатией: исследование случай-контроль. Arch Dis Child Fetal Neonatal Ed. (2013) 98: F233–9. 10.1136 / archdischild-2012-301992 [PubMed] [CrossRef] [Google Scholar] 30. Чанг Т., Рейес Т.Дж., Пласетек Дж., Массаро А.Н., Нельсон КБ.
Неонатальная энцефалопатия, дозорные явления и плацента.J Neonatal Perinatal Med. (2012) 5: 41–8. 10.3233 / NPM-2012-54211 [CrossRef] [Google Scholar] 31. Хартеман Дж. К., Никкельс П. Г., Бендерс М. Дж., Кви А., Грюнендал Ф., де Фрис Л. С.. Патология плаценты у доношенных детей с гипоксически-ишемической неонатальной энцефалопатией и ассоциация с магнитно-резонансной томографией повреждения головного мозга. J Pediatr. (2013) 163: 968–995.
10.1016 / j.jpeds.2013.06.010 [PubMed] [CrossRef] [Google Scholar] 32. Эклинд С., Маллард С., Арвидссон П., Хагберг Х. Липополисахарид вызывает как первичную, так и вторичную фазу сенсибилизации в развивающемся мозге крысы.Pediatr Res. (2005) 58: 112–6
10.1203 / 01.PDR.0000163513.03619.8D [PubMed] [CrossRef] [Google Scholar] 33. Нельсон Д.Б., Лаке А.М., Макинтайр Д.Д., Санчес П.Дж., Левено К.Дж., Чалак Л.Ф. Акушерские предшественники лечения новорожденного с помощью охлаждения тела. Am J Obstet Gynecol. (2014) 211: 155.e1–6. 10.1016 / j.ajog.2014.02.013 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 34. Дженстер М., Бонифачо С.Л., Рюэль Т., Роджерс Е.Е., Там Э.У., Партридж Дж.С. и др.
Инфекция матери или новорожденного: связь с исходами неонатальной энцефалопатии.Pediatr Res. (2014) 76: 93–9. 10.1038 / pr.2014.47 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 35. Мир И.Н., Джонсон-Велч С.Ф., Нельсон Д.Б., Браун Л.С., Розенфельд С.Р., Чалак Л.Ф. Патология плаценты связана с тяжестью неонатальной энцефалопатии и неблагоприятными исходами развития после гипотермии. Am J Obstet Gynecol. (2015) 213: 849.e1–7. 10.1016 / j.ajog.2015.09.072 [PubMed] [CrossRef] [Google Scholar] 36. Шалак Л., Джонсон-Велч С., Перлман Дж. М.. Хориоамнионит и неонатальная энцефалопатия у доношенных детей с ацидемией плода: гистопатологические корреляции.Pediatr Neurol. (2005) 33: 162–5. 10.1016 / j.pediatrneurol.2005.04.005 [PubMed] [CrossRef] [Google Scholar] 37. Impey L, Greenwood C, MacQuillan K, Reynolds M, Sheil O. Лихорадка в родах и неонатальная энцефалопатия: проспективное когортное исследование. BJOG. (2001) 108: 594–7. 10.1111 / j.1471-0528.2001.00145.x [PubMed] [CrossRef] [Google Scholar] 38. Джонсон CT, Бурд I, Рагхунатан Р., Нортингтон Ф. Дж., Грэм Э.М. Перинатальное воспаление / инфекция и его связь с коррекцией метаболического ацидоза при гипоксически-ишемической энцефалопатии.J Perinatol. (2016) 36: 448–52. 10.1038 / jp.2015.221 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 39. Кларк П., Мунираман Х., Гарднер Д., Венкатеш В., Керли А., Виктор С. и др. . Исследование неонатальной энцефалопатии: часто теряемый плацентарный «черный ящик». Pediatr Dev Pathol. (2015) 18: 343–4. 10.2350 / 15-02-1611-LET.1 [PubMed] [CrossRef] [Google Scholar] 40. Tan ES. Врожденные нарушения обмена веществ, проявляющиеся как неонатальная энцефалопатия: практические советы клиницистам. Ann Acad Med Singapore. (2008) 37 (12 доп.): 94–3. [PubMed] [Google Scholar] 41. Узиэль Г., Геззи Д., Зевиани М. Инфантильная митохондриальная энцефалопатия. Semin Fetal Neonatal Med. (2011) 16: 205–15. 10.1016 / j.siny.2011.04.003 [PubMed] [CrossRef] [Google Scholar] 42. Олишар М., Шани Э., Айгюн С., Аззопарди Д., Хант Р.В., Тоет М.С. и др. . Амплитудно-интегрированная электроэнцефалография у новорожденных с врожденными нарушениями обмена веществ. Неонатология. (2012) 102: 203–11. 10.1159 / 000339567 [PubMed] [CrossRef] [Google Scholar] 43. Хобсон Э., Томас С., Крофтон П. М., Мюррей А. Д., Дин Дж. К., Ллойд Д.Изолированная недостаточность сульфитоксидазы имитирует признаки гипоксической ишемической энцефалопатии. Eur J Pediatr. (2005) 164: 655–9. 10.1007 / s00431-005-1729-5 [PubMed] [CrossRef] [Google Scholar] 44. Уиллис Т.А., Дэвидсон Дж., Грей Р.Г., Поултон К., Рамани П., Уайтхаус В. Дефицит цитохромоксидазы, проявляющийся как асфиксия при рождении. Dev Med Child Neurol. (2000) 42: 414–7. 10.1017 / S0012162200000761 [PubMed] [CrossRef] [Google Scholar] 45. Khong PL, Lam BC, Tung HK, Wong V, Chan FL, Ooi GC. МРТ неонатальной энцефалопатии.Clin Radiol. (2003) 58: 833–44. 10.1016 / S0009-9260 (03) 00261-7 [PubMed] [CrossRef] [Google Scholar] 46. Enns GM.
Врожденные нарушения обмена веществ, маскирующиеся под гипоксически-ишемическую энцефалопатию. NeoReviews. (2005) 12: e549 – e558. 10.1542 / neo.6-12-e549 [CrossRef] [Google Scholar] 47. Уолш Б.Х., Бродхерст Д.И., Мандал Р., Вишарт Д.С., Бойлан Г.Б., Кенни Л.С. и др. . Метаболомный профиль пуповинной крови при гипоксической ишемической энцефалопатии новорожденных. PLoS ONE. (2012) 7: e50520. 10.1371 / journal.pone.0050520 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 48.Коуэн Ф., Резерфорд М., Грюнендал Ф., Экен П., Меркури Э., Байддер Г.М. и др. . Происхождение и сроки поражения головного мозга у доношенных детей с неонатальной энцефалопатией. Ланцет. (2003) 361: 736–42
10.1016 / S0140-6736 (03) 12658-X [PubMed] [CrossRef] [Google Scholar] 49. Ян М.М., Camfield PR. Исход неонатального инсульта у доношенных детей без значительной асфиксии при рождении. Eur J Pediatr. (1998) 157: 846–8. 10.1007 / s004310050950 [PubMed] [CrossRef] [Google Scholar] 50. Рамасвами В., Миллер С.П., Баркович А.Дж., Партридж Дж.С., Ферриеро Д.М.Перинатальный инсульт у доношенных детей с неонатальной энцефалопатией. Неврология. (2004) 62: 2088–91. 10.1212 / 01.WNL.0000129909.77753.C4 [PubMed] [CrossRef] [Google Scholar] 51. Scherer EB, Loureiro SO, Vuaden FC, da Cunha AA, Schmitz F, Kolling J, et al. . Легкая гипергомоцистеинемия увеличивает уровни ацетилхолинэстеразы мозга и провоспалительных цитокинов в различных тканях. Mol Neurobiol. (2014) 50: 589–96. 10.1007 / s12035-014-8660-6 [PubMed] [CrossRef] [Google Scholar] 52. Harteman JC, Groenendaal F, Benders MJ, Huisman A, Blom HJ, de Vries LS.Роль тромбофильных факторов у доношенных детей с неонатальной энцефалопатией. Pediatr Res. (2013) 73: 80–6. 10.1038 / pr.2012.150 [PubMed] [CrossRef] [Google Scholar] 53. Calkavur S, Akisu M, Olukman O, Balim Z, Berdeli A, Cakmak B и др. . Генетические факторы, влияющие на краткосрочный исход развития нервной системы у доношенных новорожденных с гипоксически-ишемической энцефалопатией. J Int Med Res. (2011) 39: 1744–56. 10.1177 / 147323001103
7 [PubMed] [CrossRef] [Google Scholar] 54. Додельсон де Кремер Р., Гроссо С. Материнская мутация 677C> T в гене метилентетрагидрофолатредуктазы, связанная с тяжелым повреждением головного мозга у потомства.Clin Genet. (2005) 67: 69–80. [PubMed] [Google Scholar] 55. Odd D, Váradi A, Rajatileka S, Molnár E, Luyt K. Связь между реанимацией новорожденных и однонуклеотидным полиморфизмом rs1835740. Acta Paediatr. (2016) 105: e307–12. 10.1111 / apa.13421 [PubMed] [CrossRef] [Google Scholar] 56. Bruyland M, Liebaers I, Sacre L, Vandeplas Y, De Meirleir L, Martin JJ. Неонатальная миотубулярная миопатия с вероятным X-сцепленным наследованием: наблюдения за новой семьей с обзором литературы. J Neurol.(1984) 231: 220–2. 10.1007 / BF00313942 [PubMed] [CrossRef] [Google Scholar] 57. Баркович А.Дж., Вестмарк К., Партридж К., Сола А., Ферриеро Д.М. Перинатальная асфиксия: результаты МРТ в первые 10 дней. AJNR Am J Neuroradiol. (1995) 16: 427–38. [PubMed] [Google Scholar] 58. Barrett MJ, Donoghue V, Mooney EE, Slevin M, Persaud T., Twomey E, et al. . Изолированное острое некистозное повреждение белого вещества у доношенных детей с неонатальной энцефалопатией. Arch Dis Child Fetal Neonatal Ed. (2013) 98: F158 – F160. 10.1136 / archdischild-2011-301505 [PubMed] [CrossRef] [Google Scholar]
Необходимость распознавания множественных этиологий для оптимального управления
Front Pediatr.2019; 7: 142.
, 1, 2 , 1, 3, 4 и 1, 2, 3, 4, 5,
64 *
4 Сайма Аслам
1 Педиатрия, Национальный родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
Тэмми Стрикленд
1 Педиатрия, Национальный родильный дом , Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити-колледж в Дублине, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Больница Университета Кумб для женщин и младенцев, Дублин, Ирландия
Элеонора Дж. .Моллой
1 Педиатрия, Национальный родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити College Dublin, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Университетская больница для женщин и младенцев Кумб, Дублин, Ирландия
5 Неонатология, Детская больница Богоматери, Дримна, Ирландия
1 Педиатрия, национальная Родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити-колледж Дублина, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Coombe Women’s и больница Университета младенцев, Дублин, Ирландия
5 Неонатология, Детская больница Богоматери, Дримна, Ирландия
Отредактировал: Микко Холлман, Университет Оулу, Финляндия
Рецензент: Георг Шмольцер, Университет Альберты, Канада; Аакаш Пандита, Институт медицинских наук им. Санджая Ганди, Индия
Эта статья была отправлена в раздел «Неонатология» журнала «Границы в педиатрии»
Поступила в редакцию 15 октября 2018 г .; Принят в печать 26 марта 2019 г.
Авторские права © 2019 Aslam, Strickland and Molloy.
Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License (CC BY). Использование, распространение или воспроизведение на других форумах разрешено при условии указания автора (авторов) и правообладателя (ов) и ссылки на оригинальную публикацию в этом журнале в соответствии с принятой академической практикой. Запрещается использование, распространение или воспроизведение без соблюдения этих условий.
Эта статья цитируется в других статьях в PMC.
Abstract
Неонатальная энцефалопатия (NE) связана с высокой смертностью и заболеваемостью. Факторы, предрасполагающие к NE, могут быть антенатальными, перинатальными или их комбинацией. Антенатальные материнские факторы, семейные факторы, генетическая предрасположенность, гипоксическая ишемическая энцефалопатия, инфекции, плацентарные аномалии, тромбофилия, дефекты коагуляции и метаболические нарушения — все это вовлечено в патогенез NE. В настоящее время терапевтическая гипотермия — единственное доступное лечение, независимо от этиологии.Распознавание этиологии вовлеченного НЭ может также помочь в проведении таких исследований, как метаболические исследования и обследования на сепсис, для обеспечения оптимального лечения. Понимание этиологии NE может позволить разработать целевую дополнительную терапию, связанную с основным механизмом, и разработать превентивные стратегии.
Ключевые слова: неонатальная энцефалоптия, этиология, антенатальная, перинатальная, таргетная дополнительная терапия
Введение
Неонатальная энцефалопатия (НЭ) — сложное заболевание новорожденных, характеризующееся измененным уровнем сознания, судорогами, плохим тонусом. для инициирования или поддержания дыхания (1) и связан с полиорганной дисфункцией (2).Заболеваемость NE оценивается в 3 случая на 1000 живорождений (3). NE может быть результатом широкого спектра причин и является клиническим термином, не определяющим этиологию. Единственное доступное лечение — это терапевтическая гипотермия (ТГ) с максимальной пользой, если начать в первые 6 часов жизни (4). Существует несколько причин НЭ, таких как гипоксическая ишемическая энцефалопатия (ГИЭ), перинатальные инфекции, аномалии плаценты, метаболические нарушения, коагулопатии и сосудистый инсульт новорожденных (). Однако более чем в половине случаев причина НЭ остается неустановленной (5).
Многофакторная этиология неонатальной энцефалопатии. Многие факторы предрасполагают к возникновению неонатальной энцефалопатии либо по отдельности, либо в комбинации, включая (A) Факторы риска до зачатия, (B) Сопутствующие заболевания или события у матери до родов / во время родов, (C) Патология плаценты, (D) Гипоксия-ишемия, (E) Перинатальная инфекция, (F) Неонатальный инсульт или тромбофилия, (G) Метаболические нарушения и (H) Генетические и эпигенетические аномалии.ПРОМ, длительный разрыв плодных оболочек; ЗВУР, ограничение внутриутробного развития.
Использование термина NE vs. HIE противоречиво. Было предложено использовать термин NE для доношенных и поздних недоношенных новорожденных, у которых не было выявленных дозорных событий (6, 7). Трудно доказать наличие церебральной гипоксической ишемии, за исключением моделей на животных и конкретных случаев неонатального инсульта. Все текущие параметры, включая pH и судороги, неспецифичны (7). Некоторые из паттернов черепно-мозговых травм, наблюдаемых у пациентов с NE, могут быть воспроизведены на животных моделях с помощью гипоксии-ишемии, но это не доказывает, что все NE вызваны HIE (7).Несколько опубликованных популяционных исследований показали, что факторы риска до родов и неасфиксии связаны с НЭ (6). Напротив, некоторые авторы утверждают, что ГИЭ является причиной НЭ в 50–80% случаев на основании клинических критериев, критериев ЭЭГ и МРТ (1). Поэтому в этом обзоре мы использовали термин NE, и мы стремились изучить различные этиологии, связанные с NE.
Материнские факторы
Материнская гипертензия (16%) была важным фактором дородового риска НЭ в реестре неонатальной энцефалопатии Оксфордской сети штата Вермонт ( n = 4 165).Также была более высокая частота клинического хориоамнионита, длительного разрыва плодных оболочек и гипотиреоза матери. Хотя острый асфиксический эпизод был зарегистрирован в 15% случаев, связь с воспалением была обнаружена у 24% (5).
Популяционное исследование в Западной Австралии показало, что социально-экономический статус, семейный анамнез судорог, неврологические проблемы и зачатие после лечения бесплодия были независимыми факторами риска до зачатия для NE ( n = 164) (8).Заболевание щитовидной железы матери, кровотечение во время беременности, вирусные заболевания, преэклампсия, аномальная плацента, задержка внутриутробного развития и переношенность были другими важными факторами риска в дородовой период (8). Идентифицируемые дородовые факторы риска НЭ были обнаружены в 69% случаев, внутриродовые факторы риска — в 5%, как дородовые, так и во время родов — в 24% и отсутствие фактора риска — в 2%. Только в 4% случаев внутриродовая гипоксия была выявлена без каких-либо факторов риска до родов или до зачатия (9). Было обнаружено, что ограничение роста в развитых странах и беременность двойней в развивающихся странах связаны с НЭ.Заболевание щитовидной железы у матери, дородовое наблюдение, инфекция, роды и тактика ведения родов должны стать важными модификаторами в исследовании 27 новорожденных с НЭ и 100 детей контрольной группы (3). Дородовые (74 против 18%), внутриродовые (67 против 19%) и острые внутриродовые события (33 против 2%) более вероятны у младенцев с НЭ по сравнению с контрольной группой. Следовательно, в неонатальном клиническом анамнезе подробный материнский анамнез важен и может быть путем к профилактическим стратегиям в будущем.
Из 45 новорожденных с NE 36% имели дозорные эпизоды, 40% имели хориоамнионит и 11% имели оба этих заболевания.Если данные дозорных событий были исключены, то возраст матери> 35 лет (ОР 2,5; 95% ДИ 1,1–5,6) и инфекция мочевыводящих путей во время беременности (ОР 2,6; 95% ДИ 1,0–6,5) были потенциальными факторами дородового риска для NE (10).
Гипоксия-ишемия
Хотя концепция гипоксии-ишемии четко выражена в моделях на животных, она может не подходить для использования во всех случаях неонатальной NE у человека. «Дозу» и продолжительность гипоксии, а также степень ишемии можно напрямую измерить на животной модели.Однако у новорожденных людей это неизвестно, если нет контрольного события, и впоследствии не используются суррогатные маркеры гипоксии. Badawi et al. показали, что асфиксия во время родов считается сопутствующим фактором в 29% случаев НЭ и самостоятельным фактором только в 4% случаев (9). Было обнаружено, что внутриродовая гипоксия-ишемия является одним из факторов, способствующих развитию НЭ в 30% случаев в развитых и 60% в развивающихся странах (3). Американский колледж акушеров и Американская академия педиатрии определили дозорное событие в своем документе о неонатальной энцефалопатии и неврологических исходах (Obstet Gynecol 2014).Следующее соответствует острому пери- или интранатальному событию: дозорное гипоксическое или ишемическое событие, возникающее непосредственно перед или во время родов и родоразрешения, например разрыв матки или тяжелая отслойка плаценты; паттерны пульсометра плода, соответствующие острым послеродовым или интранатальным событиям; сроки и тип травм головного мозга, основанные на исследованиях изображений, согласующихся с этиологией острого послеродового или внутриродового события, и отсутствуют доказательства других проксимальных или дистальных факторов, которые могли бы быть способствующими факторами.Кроме того, сочетание низких баллов по шкале Апгарса, ацидемии, аномального кардиотокографа, изменений МРТ, согласующихся с гипоксией-ишемией и полиорганной дисфункцией, — все это связано с гипоксически-ишемической этиологией, но в равной степени может быть изменено сепсисом или другими причинами NE. Асфиксичные родовые явления и воспаление присутствовали только в 12,6% случаев церебрального паралича (11). У новорожденных с NE ( n = 405) следующие факторы были независимо связаны с NE ( p -значение = 0,001), включая: только 1 дородовой период (гестационный возраст> 41 недели) и 7 факторов во время родов, включая длительный разрыв плодных оболочек, аномальные кардиотокограф, густой меконий, дозорные события, дистоция плеча, тугая затылочная пуповина и отказ вакуума (12).В когорте из 26 новорожденных с дозорными событиями NE (ОР 74,9, 95% ДИ 11,9-бесконечность, p <0,001) и отслеживание ЧСС плода категории 3 (28,0% против 4,0%, p = 0,002) были сильно связанный с NE (13). В когорте из 45 новорожденных у 36% были дозорные события, а у 11% были как дозорные, так и хориоамнионит (10).
Нейровизуализация с использованием магнитно-резонансной томографии, традиционной, диффузионной и спектроскопии в период от 24 до 96 часов жизни дает полезные рекомендации относительно возможных сроков возникновения церебрального инсульта, особенно диффузных аномалий.Аномалии, вызванные травмой головного мозга, становятся наиболее очевидными через 7 дней при использовании качественной МРТ, диффузии и спектроскопии. Глубокое ядерное серое вещество или водораздел кортикального повреждения развиваются по четко определенному типу повреждения мозга и типичны для гипоксически-ишемического повреждения мозга у новорожденного. Генетические и метаболические причины могут быть исследованы, если на МРТ существует другая картина травмы головного мозга или эволюция травмы. Признаки того, что послеродовая гипоксия-ишемия не была причиной НЭ, предлагаются на МРТ: порэнцефалия, очаговый артериальный инфаркт, венозный инфаркт, изолированное внутрипаренхиматозное или внутрижелудочковое кровоизлияние или атипичные паттерны метаболических энцефалопатий.
При NE, связанном с острым дозорным событием (HIE), типичная картина повреждения на МРТ показала вовлечение базальных ганглиев, таламуса с ассоциированной задней конечностью внутренней капсулы и, в тяжелых случаях, вовлечение ствола мозга (14). При NE без задокументированного дозорного события вовлечение базальных ганглиев или таламуса (BGT) также связано с изменениями белого вещества в 50% случаев (14). BGT с обширным повреждением белого вещества (WM) был обнаружен в 14%, BGT с WM от легкой до умеренной — в 56%, изолированное таламическое повреждение — в 5%, умеренное повреждение WM — только у 2% и легкое WM или нормальное — у 23% в 48%. младенцы с ГИЭ.Внутренняя капсула была аномальной у 93% пациентов с умеренным и тяжелым повреждением WM и была связана со смертью и ХП у 86% пациентов (15).
Картина повреждения головного мозга может указывать на возможную причину, например, повреждение коркового вещества и белого вещества (очаговое / мультифокальное) может быть связано с плацентарной недостаточностью и хориоамнионитом. Ранняя категоризация пациентов в соответствии с типом травмы головного мозга может привести к другому терапевтическому подходу, поскольку на животных моделях было показано, что разные уровни гипотермии защищают от повреждения коры головного мозга или глубокого серого вещества, поэтому для получения максимальной пользы могут потребоваться специфические для пациента протоколы гипотермии.Точно так же в моделях на животных разные режимы охлаждения, системное и селективное, приводят к разной температуре мозга (16).
Трудно окончательно установить наличие, продолжительность и степень гипоксии и ишемии у новорожденных, поэтому использовались суррогатные маркеры, такие как pH и судороги (7). Следовательно, биомаркеры мультиорганного поражения могут быть полезны для диагностики или оценки тяжести гипоксической ишемии и прогнозирования исхода при NE. Сердечный тропонин является маркером ишемии миокарда у новорожденных и детей и высвобождается из миоцитов после повреждения их мембраны.Сердечный тропонин I (cTnI) был значительно выше у новорожденных с ГИЭ в первые 48 часов по сравнению с контрольной группой ( p <0,0005) (17). Сердечный TnI был повышен у новорожденных с более высокой степенью НЭ и у тех, кому потребовались инотропы (18). Пороговое значение <0,22 нг / мл для нормотермических и <0,15 нг / мл для гипотермических младенцев с NE предсказывало нормальный исход развития нервной системы (19).
Гипоксия приводит к усилению эритропоэза и выбросу незрелых ядерных эритроцитов (nRBC) в кровоток (20).ЯРБК пуповинной крови были значительно выше у новорожденных, подвергшихся асфиксии, по сравнению с контрольной группой, а также коррелировали с апгаром через 1 мин, pH и развитием NE (20). Количество ядерных эритроцитов на 100 лейкоцитов было выше у новорожденных с НЭ по сравнению с контрольной группой, младенцев с НЭ средней / тяжелой или легкой степени ( p = 0,016) и у новорожденных с плохим исходом нервного развития ( p = 0,03) 21). Следовательно, стандартизованное измерение воздействия клинической гипоксии было бы полезным с использованием комбинации этих маркеров и могло бы помочь в определении времени инсульта и корреляции с доклиническими моделями на животных.
Инфекция
Риск спастического церебрального паралича (ДЦП) и квадриплегического ДЦП повышался при сочетании инфекции и асфиксии (22). Уровни интерлейкина (ИЛ) -6 через 6 часов связаны с отклонениями от нормы неврологического обследования (23). NE, инотропная поддержка, судороги без менингита, потребность в интубации и более низкий 5-минутный апгар были более вероятны у новорожденных с ХП при наличии инфекции у матери по сравнению с ХП без инфекции (22).
Материнские и ранние неонатальные инфекции представляют собой диагностическую проблему.Ведутся споры о том, может ли скрытая инфекция, не обнаруживаемая обычными методами культивирования, быть связана с неврологическим повреждением во всех возрастных группах. Полимеразная цепная реакция (ПЦР) выявила 11 случаев бактериемии у энцефалопатических новорожденных в Африке, у которых был отрицательный результат посева крови (NE n = 201). ПЦР в сочетании с посевом крови привела к обнаружению бактериальных продуктов в 8,9% случаев НЭ по сравнению с 3,1% при использовании одного посева крови (24). В метаанализе стрептококк группы B (GBS) был связан с NE в 0.58% случаев и смертность были выше при использовании СГБ плюс НЭ по сравнению с одним НЭ (25). В когорте из 45 новорожденных 40% имели хориоамнионит и 11% имели как дозорные события, так и хориоамнионит (10).
Терапевтическая гипотермия задерживает рост и пик ответа с-реактивного белка (СРБ), а также приводит к снижению количества лейкоцитов и нейтрофилов по сравнению с нормотермными новорожденными (26). Это влияние гипотермии на задержку развития естественных воспалительных маркеров следует учитывать при выборе лечения антибиотиками и продолжительности лечения новорожденных с НЭ.
Следовательно, полное обследование на сепсис имеет важное значение у всех детей с НЭ. Стандартных рекомендаций по выполнению люмбальной пункции во всех случаях НЭ не существует, и их можно выбирать в каждом конкретном случае. Кандидатами могут быть младенцы с повышенным WCC и CRP или факторами риска септического риска. Существуют также технические и практические проблемы для поясничной пункции у младенцев с NE, которые являются ригидными из-за TH, а также часто изначально имеют отек мозга при ультразвуковом исследовании черепа.
Аномалии плаценты
Поражение пуповины, хориоамнионит, васкулит плода, меконий хориональной пластинки и тромботическая васкулопатия плода часто встречались в плацентарных поражениях у пациентов с NE ( n = 23) (27).Поражения плаценты, указывающие на тромбоз и снижение фетоплацентарного кровотока, являются значимыми и независимыми факторами риска НЭ ( n = 93) (28). Наличие более одного поражения плаценты увеличивает вероятность НЭ, но не было никакой корреляции между патологией плаценты и картиной повреждения на МРТ ( n = 56) (29). Аномальная патология плаценты была обнаружена у 29% новорожденных с дозорными событиями и у 73% младенцев без дозорных явлений ( p = 0,0001), перенесших терапевтическую гипотермию (30).Воспалительные поражения плаценты чаще наблюдались у новорожденных без дозорных событий ( p = 0,002) (30). Хронический виллит был связан с повреждением базальных ганглиев (BGT), тогда как наличие ядерных эритроцитов, снижение созревания плаценты и хронический виллит также приводили к повреждению белого вещества / водораздела вместе с вовлечением BGT ( n = 95) (31).
Доказательства связи хориоамнионита с НЭ разнообразны. Предполагается, что время инфицирования и степень воспалительного ответа могут привести либо к прекондиционированию, либо к сенсибилизации и могут вызвать либо защитный эффект, либо дальнейшее усиление перинатального повреждения головного мозга, соответственно (32).Этот эффект был продемонстрирован на животных моделях. Липополисахарид (ЛПС), вводимый за 4–6 ч до 20 и 50 мин воздействия HI, приводил к усилению травм головного мозга. Однако введение LPS за 24 часа до 50-минутного воздействия HI привело к значительному ослаблению травм головного мозга (32). КА выявлена у 8 новорожденных с признаками перинатальной асфиксии (всего n = 23) (27). Младенцы с NE и TH имели более высокие шансы на наличие CA по сравнению с младенцами, которые не получали TH ( n = 98) (33).CA, васкулит и фунизит были связаны с NE степени I, виллитом с NE II и фунизитом с III степенью у 141 новорожденного с NE и 309 контрольных (29). CA был связан с более низким риском черепно-мозговой травмы и плохим когнитивным исходом по сравнению с не-CA (скорректированный OR 0,3; 95% CI 0,1–0,7, p = 0,004) у новорожденных с NE ( n = 258), хотя только У 20 новорожденных были гистологические доказательства СА. В той же когорте новорожденные с признаками сепсиса имели более высокие шансы на повреждение водораздела и аномальные нейромоторные показатели, чем у новорожденных без каких-либо клинических признаков ( p = 0.007) (34). У 120 младенцев с сочетанием перинатального ацидоза, NE и хориоамнионита с ответом плода или без него и пятнистый / диффузный хронический виллит были независимо связаны с тяжестью NE (35). Единственным индивидуальным предиктором патологического исхода нервного развития через 22-24 месяца после терапии гипотермией был диффузный хронический виллит. Гистологическая CA имела низкую прогностическую ценность для развития энцефалопатии и смерти у NE ( n = 51) (36), но материнская лихорадка ( n = 336) во время родов была независимым фактором для NE (скорректированное OR 4.72, 95% ДИ 1,28–17,4) (37). Клинический хориоамнионит был связан с более высокими уровнями IL-6, IL-8 в пуповинной крови и регулировался активацией нормальных Т-клеток, экспрессируемых и секретируемых (RANTES) в NE ( n = 61). В когорте из 67 новорожденных с хориоамнионитом NE, независимо от того, были ли клинические или гистологические данные связаны со стойким метаболическим ацидозом, это может предсказать плохой неврологический исход (38).
Патология плаценты описывается как «черный ящик» беременности. Стандартизированная классификация результатов патологии плаценты важна для дальнейшего определения этиологии NE (39).
Нарушения обмена веществ
Нарушения обмена веществ являются редкими причинами НЭ, но их всегда следует учитывать. Врожденные нарушения метаболизма (ВЭМ) присутствуют в неонатальном периоде после нормального периода выздоровления и отсутствия признаков перинатальной асфиксии, но неврологические и полиорганные поражения могут проявляться как НЭ (40). Митохондриальные нарушения также являются важной причиной НЭ (41).
Амплитудная интегрированная электроэнцефалограмма (аЭЭГ) была отклонена от нормы у 27 новорожденных с ВЭМ, причем наиболее устойчивыми признаками были аномальная фоновая активность и судороги.Не было различий в аЭЭГ для энцефалопатии, связанной с IEM или NE, и дифференцировать можно было только на основании клинического подозрения (42). Единственное метаболическое расстройство с диагностической ЭЭГ — это некетотическая гиперглицинемия с первоначальным паттерном «подавление-всплеск», переходящим в гипсаритмию в раннем или среднем младенчестве и диагностируемое путем измерения уровня глицина в спинномозговой жидкости (42). Имеются также отдельные сообщения о случаях ИЭМ, таких как дефицит сульфитоксидазы и цитохрома С, проявляющийся как НЭ (43, 44).
Результаты МРТ могут варьироваться в зависимости от типа врожденной ошибки метаболизма (ВЭМ) и могут варьироваться от поражения белого вещества до поражения глубоких серых ядер. Митохондриальные энцефалопатии имеют симметричное двустороннее распределение и изначально могут быть диагностированы как NE (45). Следует учитывать метаболические нарушения, если нет явных явлений во время родов, стойкий лактоацидоз и / или гипогликемия (45) и начато обследование. Различные паттерны повреждений на МРТ головного мозга могут помочь дифференцировать метаболические нарушения от НЭ.Поражение Globus Pallidus часто встречается при IEM по сравнению с NE, хотя картина повреждения при дефиците сульфитоксидазы и дефиците фактора молибдена может имитировать NE (46).
Изолированные приступы связаны с такими расстройствами, как: судороги, связанные с пиридоксином, некетотическая гиперглицинемия (НКГ), дефицит дигидропиримидиндегидрогеназы, дефицит сульфитоксидазы (либо изолированный, либо как часть дефицита кофактора молибдена), трансаминазы 4-аминобутират-аминотрансферазы (ГАБТрансферазы). ) дефицит, судороги, связанные с фолиевой кислотой, дефицит 3-фосфоглицератдегидрогеназы, дефицит гуанидиноацетатметилтрансферазы (GAMT) и дефицит переносчика глюкозы (GLUT-1).У младенцев с полиорганными поражениями, судорогами, метаболическим ацидозом, молочной железой, гипераммониемией могут быть: органическая ацидемия, дефекты цикла мочевины, пероксисомальные нарушения (например, синдром Зеллвегера) или митохондриальные нарушения.
Подробный семейный анамнез для установления факторов риска, таких как родство родителей или ранее пораженный ребенок, важен, поскольку большинство врожденных нарушений метаболизма имеют аутосомно-рецессивное или материнское наследование. Базовые исследования, такие как электролиты, аммиак, сывороточные аминокислоты, лактат, ацилкарнитин и органическая кислота в моче, могут быть рассмотрены при NE (40).Есть проблемы с метаболическим тестированием, так как их может потребоваться повторить, если ребенок очень плохо себя чувствует с полиорганной дисфункцией во время отбора образцов (46). Недавние исследования показали большой потенциал метаболомики как биомаркеров NE. Было показано, что содержание сукцината повышено у детей с НЭ, которые серьезно пострадали (47).
Тромбофилия и неонатальный инсульт
Асфиксия (в 4% случаев) участвует в патогенезе неонатального инсульта (48). Фокальные клонические приступы являются наиболее частым проявлением неонатального инсульта (49), и 6 младенцев с инсультом были обнаружены в когорте NE ( n = 124) (50).Эти дети обычно страдали судорогами и имели худшие исходы с точки зрения нервного развития, чем остальная когорта. Нарушения свертывания крови, такие как полицитемия, лейденский фактор V, нарушения гемоглобина и мутации протромбина, не были обнаружены у 4 из 6 обследованных пациентов (50).
В моделях на животных повышенные уровни гомоцистеина приводили к увеличению провоспалительных цитокинов, таких как фактор некроза опухоли альфа (TNFα), интерлейкин 1 бета (IL-1β) и IL-6 в гиппокампе и коре головного мозга.Это провоспалительное состояние может быть ответственным за нейрональные и цереброваскулярные эффекты, наблюдаемые у взрослых (51). Роль гомоцистеина или полиморфизмов в гене метилентетрагидрофолатредуктазы в возникновении неонатального повреждения головного мозга неясна (52). В когорте из 118 новорожденных с НЭ повреждение белого вещества / водораздела с большей вероятностью было связано с гипогликемией, полиморфизмом метилентетрагидрофолатредуктазы (MTHFR) и уровнями гомоцистеина в плазме в верхнем квартиле нормы (52).
Генетические и эпигенетические аномалии
Отсутствуют опубликованные данные, связывающие генетическую предрасположенность с развитием NE. У 40 пациентов с NE генетическая изменчивость протромбических факторов, таких как протромбин G20210A, фактор V Leiden G1691A и метилентетрагидрофолатредуктаза [MTHFR] C677T, и ген фактора некроза опухоли не повлияли на оценку NE, ЭЭГ, смерть, краниальное УЗИ (США) , неврологический исход при выписке через 6 и 12 месяцев. Полиморфизм гена интерлейкина-6 (IL-6 174GC) имел защитный эффект и был связан с нормальной ЭЭГ, краниальным УЗИ и неврологическим обследованием при выписке (53).В ретроспективном исследовании «случай-контроль» с участием 11 новорожденных с NE у матерей была обнаружена более высокая частота полиморфизма MTHFR (7 гомозиготных и 4 гетерозиготных) по сравнению с контрольной группой (54). Генетический полиморфизм может увеличивать риск или тяжесть неонатального повреждения головного мозга при NE, и его следует учитывать (53).
В рамках лонгитюдного исследования родителей и детей, проведенного Avon, было проведено генотипирование 7611 доношенных детей, и мерилом воздействия было наличие одного или нескольких минорных аллелей в одном из 3 SNP (rs2284411, rs2498804, rs1835740).Первичным результатом была необходимость реанимации при рождении, что было связано с rs1835740 (55). Требуются более крупные международные совместные исследования для определения необходимого количества пациентов для изучения генетических связей и разделения пациентов по этиологии.
Другая категория младенцев с генетической причиной неонатальной энцефалопатии — это дети с миопатиями и энцефалопатиями новорожденных. Пациенты, унаследовавшие миопатию (центронуклеарную миопатию), могут иметь неонатальный дистресс, гипотонию и признаки, указывающие на ГИЭ (56).Врожденная миотоническая дистрофия 1 типа характеризуется гипотонией и тяжелой генерализованной слабостью при рождении, часто с дыхательной недостаточностью, умственной отсталостью и ранней смертью. Это вызвано экспансией тринуклеотидного повтора CTG в некодирующей области DMPK .
В будущем подробное генотипирование, включая более легкий доступ к методам микроматриц в клинических условиях, предоставит больше информации, позволяющей индивидуализированный уход и потенциально классифицировать младенцев по генотипу.
Нейровизуализация
На МРТ можно увидеть различные модели травм, но это не исключает HIE как причины травмы. Характер повреждения зависит от тяжести, продолжительности и повторяемости гипоксической ишемии и может привести к поражению базальных ганглиев, таламуса, ствола мозга и / или белого вещества головного мозга в различных сочетаниях (1). При глубокой гипоксии преобладает повреждение более глубоких серых структур, то есть базальных ганглиев и таламуса. Объясняется это тем, что эти участки миелинизированы и имеют более высокую скорость метаболизма.Состояния, которые уменьшают, а не вызывают полное прекращение кровотока, такие как анемия и гиповолемия, связаны с повреждением коры головного мозга и сохранением более глубоких серых структур (57). В когорте из 245 пациентов с NE 197 (80%) результаты МРТ соответствовали острому перинатальному инсульту. МРТ у 40 младенцев (16%) были нормальными. У 9 младенцев (4%) были выявлены признаки тромбоза / инфаркта, генетических нарушений, антенатального инсульта и митохондрий (дефицит комплекса I) на МРТ в дополнение к гипоксическому ишемическому инсульту.Нейровизуализация у 8 (3%) младенцев с клиническим диагнозом НЭ показала либо врожденную ошибку метаболизма, нервно-мышечное расстройство, либо отсутствие диагноза, и эти результаты не соответствовали гипоксической ишемии (48). Плацентарный виллит высокой степени неизвестной этиологии ( n = 4) был обнаружен в когорте из 36 пациентов, связанных с повреждением белого вещества, вторичным по отношению к воспалению / окислительному стрессу в перинатальном периоде (58).
Значение для терапии
Все младенцы с NE могут не в одинаковой степени выиграть от переохлаждения.Следовательно, выявление точной этиологии в каждом случае NE имеет значение для лечения, поскольку есть некоторые излечимые причины, которые требуют быстрого определения для оптимального лечения. Использование бактериальной ПЦР для выявления инфекции у новорожденных с NE может быть более полезным, чем только посев крови с низким выходом бактерий, а также гипотермия может уменьшить воспалительную реакцию. Гистология плаценты отражает внутриматочную среду и может прояснить основную этиологию. Все новорожденные с риском IEM должны быть обследованы на предмет метаболических нарушений, так как этим пациентам могут быть полезны специфические методы лечения, а не гипотермия.Точно так же скрининг на тромбофилию следует рассматривать у пациентов из группы риска, таких как пациенты с инсультом, семейный анамнез тромбофилии. Подробная оценка этиологии NE важна для выявления излечимых причин и категоризации этой гетерогенной группы новорожденных, чтобы можно было подобрать соответствующее лечение в соответствии с этиологией и улучшением отдаленных результатов. Точно так же будет полезно стратифицировать большие многоцентровые когорты младенцев с NE по этиологии, чтобы полностью понять этиологию, реакцию на лечение гипотермией и отдаленные результаты.
Авторские взносы
SA: основной автор; ТС: помогал с поиском релевантных статей и рисунка; ЭМ: автор-руководитель.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Ссылки
1. Volpe JJ. Неонатальная энцефалопатия: неадекватный термин для гипоксически-ишемической энцефалопатии.Энн Нейрол. (2012) 72: 156–66. 10.1002 / ana.23647 [PubMed] [CrossRef] [Google Scholar] 2. Шах П., Рип Хаген С., Бейен Дж, Перлман М. Мультиорганная дисфункция у младенцев с постасфиксиальной гипоксически-ишемической энцефалопатией. Arch Dis Child Fetal Neonatal Ed. (2004) 89: F152 – F155. 10.1136 / adc.2002.023093 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 3. Куринчук Дж. Дж., Уайт-Конинг М., Бадави Н. Эпидемиология неонатальной энцефалопатии и гипоксически-ишемической энцефалопатии. Early Hum Dev. (2010) 86: 329–38.10.1016 / j.earlhumdev.2010.05.010 [PubMed] [CrossRef] [Google Scholar] 4. Джейкобс С.Е., Берг М., Хант Р., Тарнов-Морди В.О., Индер Т.Э., Дэвис П.Г.
Охлаждение новорожденных с гипоксической ишемической энцефалопатией. База данных Cochr Syst Rev. (2013) 1: CD003311
10.1002 / 14651858.CD003311.pub3 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 5. Нельсон К.Б., Бингхэм П., Эдвардс Э.М., Хорбар Д.Д., Кенни М.Дж., Индер Т. и др. . Антецеденты неонатальной энцефалопатии в реестре энцефалопатии Оксфордской сети Вермонта. Педиатрия.(2012) 130: 878–86. 10.1542 / peds.2012-0714 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 6. Нельсон КБ. Это HIE?
И почему это важно Acta Paediatr. (2007) 96: 1113–4. 10.1111 / j.1651-2227.2007.00364.x [PubMed] [CrossRef] [Google Scholar] 7. Дамманн О., Ферриеро Д., Грессенс П.
Неонатальная энцефалопатия или гипоксически-ишемическая энцефалопатия?
Соответствующая терминология имеет значение Pediatr Res. (2011) 70: 1-2. 10.1203 / PDR.0b013e318223f38d [PubMed] [CrossRef] [Google Scholar] 8. Бадави Н., Куринчук Дж. Дж., Кио Дж. М., Алессандри Л. М., О’Салливан Ф., Бертон П. Р. и др.. Факторы дородового риска энцефалопатии новорожденных: исследование случай-контроль в Западной Австралии. BMJ. (1998) 317: 1549–53. 10.1136 / bmj.317.7172.1549 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 9. Бадави Н., Куринчук Дж. Дж., Кио Дж. М., Алессандри Л. М., О’Салливан Ф., Бертон П. Р. и др. . Факторы риска внутриутробной энцефалопатии новорожденных: исследование случай-контроль в Западной Австралии. BMJ. (1998) 317: 1554–8. 10.1136 / bmj.317.7172.1554 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 10. Паркер SJ, Kuzniewicz M, Niki H, Wu YW.Факторы дородового и внутриродового риска гипоксически-ишемической энцефалопатии в когорте новорожденных в США. J Pediatr. (2018) 203: 163–9. 10.1016 / j.jpeds.2018.08.028 [PubMed] [CrossRef] [Google Scholar] 11. Адамсон С.Дж., Алессандри Л.М., Бадави Н., Бертон П.Р., Пембертон П.Дж., Стэнли Ф. Предикторы неонатальной энцефалопатии у доношенных новорожденных. BMJ. (1995) 311: 598–602
10.1136 / bmj.311.7005.598 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 12. Мартинес-Биарж М., Диез-Себастьян Дж., Вустхофф Си-Джей, Меркури Е., Коуэн FM.Дородовые и внутриродовые факторы, предшествующие неонатальной гипоксически-ишемической энцефалопатии. Педиатрия. (2013) 132: e952 – e959
10.1542 / peds.2013-0511 [PubMed] [CrossRef] [Google Scholar] 13. Торбенсон В.Е., Толчер М.К., Несбитт К.М., Колби К.Э., Эль-Нашар С.А., Гостоут Б.С. и др. . Внутриродовые факторы, связанные с неонатальной гипоксической ишемической энцефалопатией: исследование случай-контроль. BMC Беременность и роды. (2017) 17: 415
10.1186 / s12884-017-1610-3 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 14. Резерфорд М., Маламатениу К., МакГиннесс А., Оллсоп Дж., Биарж М.М., Конселл С.Магнитно-резонансная томография при гипоксически-ишемической энцефалопатии. Early Hum Dev. (2010) 86: 351–60. 10.1016 / j.earlhumdev.2010.05.014 [PubMed] [CrossRef] [Google Scholar] 15. Okereafor A, Allsop J, Counsell SJ, Fitzpatrick J, Azzopardi D, Rutherford MA и др. . Характер черепно-мозговой травмы у новорожденных, подвергшихся перинатальным дозорным событиям. Педиатрия. (2008) 121: 906–14. 10.1542 / peds.2007-0770 [PubMed] [CrossRef] [Google Scholar] 16. Мецлер М., Говиндан Р., Аль-Шаргаби Т., Везина Г., Андескавадж Н., Ван И и др.. Характер черепно-мозговой травмы и снижение вариабельности сердечного ритма у новорожденных с гипоксической ишемической энцефалопатией. Pediatr Res. (2017) 82: 438–43. 10.1038 / pr.2017.94 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 17. Симович AM, Игрутинович З., Обрадович С., Ристич Д., Вулетич Б., Раданович М. Значение сердечного тропонина I второго поколения в раннем скрининге гипоксически-ишемической энцефалопатии после перинатальной асфиксии. Srp Arh Celok Lek. (2012) 140: 600–5. [PubMed] [Google Scholar] 18. Шастри А.Т., Самарасекара С., Мунираман Х., Кларк П.Концентрации сердечного тропонина I у новорожденных с гипоксически-ишемической энцефалопатией. Acta Paediatr. (2012) 101: 26–9. 10.1111 / j.1651-2227.2011.02432.x [PubMed] [CrossRef] [Google Scholar] 19. Лю X, Chakkarapani E, Stone J, Thoresen M. Влияние компрессий сердца и лечения гипотермии на сердечный тропонин I у новорожденных с перинатальной асфиксией. Реанимация. (2013) 84: 1562–7. 10.1016 / j.resuscitation.2013.07.003 [PubMed] [CrossRef] [Google Scholar] 20. Гош Б., Миттал С., Кумар С., Дадхвал В. Прогнозирование перинатальной асфиксии с ядросодержащими эритроцитами в пуповинной крови новорожденных.Int J Gynaecol Obstet. (2003) 81: 267–71. 10.1016 / S0020-7292 (03) 00124-3 [PubMed] [CrossRef] [Google Scholar] 21. Уолш Б.Х., Бойлан Г.Б., Мюррей Д.М. Ядерные эритроциты и ранняя ЭЭГ: прогнозирование стадии Сарната и двухлетнего исхода. Early Hum Dev. (2011) 87: 335–9. 10.1016 / j.earlhumdev.2011.01.041 [PubMed] [CrossRef] [Google Scholar] 22. Нельсон КБ, Гретер Дж. Потенциально удушающие состояния и спастический церебральный паралич у младенцев с нормальной массой тела при рождении. Am J Obstet Gynecol. (1998) 179: 507–13. 10.1016 / S0002-9378 (98) 70387-4 [PubMed] [CrossRef] [Google Scholar] 23.Шалак Л.Ф., Лапток А.Р., Джафри Х.С., Рамило О., Перлман Дж. Клинический хориоамнионит, повышенные цитокины и травмы головного мозга у доношенных детей. Педиатрия. (2002) 110: 673–80. 10.1542 / peds.110.4.673 [PubMed] [CrossRef] [Google Scholar] 24. Танн CJ, Nkurunziza P, Nakakeeto M, Oweka J, Kurinczuk JJ, Were J и др. . Распространенность патогенов кровотока выше в случаях неонатальной энцефалопатии по сравнению с контрольной группой, использующей новую панель ПЦР-анализов в реальном времени. PLoS ONE. (2014) 9: e97259. 10.1371 / journal.pone.0097259 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 25.Танн С.Дж., Мартинелло К.А., Саду С., Лоун Дж.Э., Сил А.С., Вега-Поблете М. и др.
Группа исследователей неонатальной энцефалопатии GBS. неонатальная энцефалопатия со стрептококками группы b во всем мире: систематический обзор, наборы данных исследовательских групп и метаанализ. Clin Infect Dis. (2017) 65 (Suppl_2): S173–89. 10.1093 / cid / cix662 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 26. Chakkarapani E, Davis J, Thoresen M. Терапевтическая гипотермия задерживает ответ C-реактивного белка и подавляет количество лейкоцитов и тромбоцитов у младенцев с неонатальной энцефалопатией.Arch Dis Child Fetal Neonatal Ed. (2014) 99: F458 – F463. 10.1136 / archdischild-2013-305763 [PubMed] [CrossRef] [Google Scholar] 27. Wintermark P, Boyd T, Gregas MC, Labrecque M, Hansen A. Патология плаценты у новорожденных с асфиксией, отвечающая критериям терапевтической гипотермии. Am J Obstet Gynecol. (2010) 203: 579.e1–9. 10.1016 / j.ajog.2010.08.024 [PubMed] [CrossRef] [Google Scholar] 28. Макдональд Д.Г., Келехан П., Макменамин Дж.Б., Горман В.А., Мэдден Д., Тоббия И.Н. и др. . Плацентарная тромботическая васкулопатия плода связана с неонатальной энцефалопатией.Hum Pathol. (2004) 35: 875–80
10.1016 / j.humpath.2004.02.014 [PubMed] [CrossRef] [Google Scholar] 29. Hayes BC, Cooley S, Donnelly J, Doherty E, Grehan A, Madigan C и др. . Плацента у младенцев> 36 недель беременности с неонатальной энцефалопатией: исследование случай-контроль. Arch Dis Child Fetal Neonatal Ed. (2013) 98: F233–9. 10.1136 / archdischild-2012-301992 [PubMed] [CrossRef] [Google Scholar] 30. Чанг Т., Рейес Т.Дж., Пласетек Дж., Массаро А.Н., Нельсон КБ.
Неонатальная энцефалопатия, дозорные явления и плацента.J Neonatal Perinatal Med. (2012) 5: 41–8. 10.3233 / NPM-2012-54211 [CrossRef] [Google Scholar] 31. Хартеман Дж. К., Никкельс П. Г., Бендерс М. Дж., Кви А., Грюнендал Ф., де Фрис Л. С.. Патология плаценты у доношенных детей с гипоксически-ишемической неонатальной энцефалопатией и ассоциация с магнитно-резонансной томографией повреждения головного мозга. J Pediatr. (2013) 163: 968–995.
10.1016 / j.jpeds.2013.06.010 [PubMed] [CrossRef] [Google Scholar] 32. Эклинд С., Маллард С., Арвидссон П., Хагберг Х. Липополисахарид вызывает как первичную, так и вторичную фазу сенсибилизации в развивающемся мозге крысы.Pediatr Res. (2005) 58: 112–6
10.1203 / 01.PDR.0000163513.03619.8D [PubMed] [CrossRef] [Google Scholar] 33. Нельсон Д.Б., Лаке А.М., Макинтайр Д.Д., Санчес П.Дж., Левено К.Дж., Чалак Л.Ф. Акушерские предшественники лечения новорожденного с помощью охлаждения тела. Am J Obstet Gynecol. (2014) 211: 155.e1–6. 10.1016 / j.ajog.2014.02.013 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 34. Дженстер М., Бонифачо С.Л., Рюэль Т., Роджерс Е.Е., Там Э.У., Партридж Дж.С. и др.
Инфекция матери или новорожденного: связь с исходами неонатальной энцефалопатии.Pediatr Res. (2014) 76: 93–9. 10.1038 / pr.2014.47 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 35. Мир И.Н., Джонсон-Велч С.Ф., Нельсон Д.Б., Браун Л.С., Розенфельд С.Р., Чалак Л.Ф. Патология плаценты связана с тяжестью неонатальной энцефалопатии и неблагоприятными исходами развития после гипотермии. Am J Obstet Gynecol. (2015) 213: 849.e1–7. 10.1016 / j.ajog.2015.09.072 [PubMed] [CrossRef] [Google Scholar] 36. Шалак Л., Джонсон-Велч С., Перлман Дж. М.. Хориоамнионит и неонатальная энцефалопатия у доношенных детей с ацидемией плода: гистопатологические корреляции.Pediatr Neurol. (2005) 33: 162–5. 10.1016 / j.pediatrneurol.2005.04.005 [PubMed] [CrossRef] [Google Scholar] 37. Impey L, Greenwood C, MacQuillan K, Reynolds M, Sheil O. Лихорадка в родах и неонатальная энцефалопатия: проспективное когортное исследование. BJOG. (2001) 108: 594–7. 10.1111 / j.1471-0528.2001.00145.x [PubMed] [CrossRef] [Google Scholar] 38. Джонсон CT, Бурд I, Рагхунатан Р., Нортингтон Ф. Дж., Грэм Э.М. Перинатальное воспаление / инфекция и его связь с коррекцией метаболического ацидоза при гипоксически-ишемической энцефалопатии.J Perinatol. (2016) 36: 448–52. 10.1038 / jp.2015.221 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 39. Кларк П., Мунираман Х., Гарднер Д., Венкатеш В., Керли А., Виктор С. и др. . Исследование неонатальной энцефалопатии: часто теряемый плацентарный «черный ящик». Pediatr Dev Pathol. (2015) 18: 343–4. 10.2350 / 15-02-1611-LET.1 [PubMed] [CrossRef] [Google Scholar] 40. Tan ES. Врожденные нарушения обмена веществ, проявляющиеся как неонатальная энцефалопатия: практические советы клиницистам. Ann Acad Med Singapore. (2008) 37 (12 доп.): 94–3. [PubMed] [Google Scholar] 41. Узиэль Г., Геззи Д., Зевиани М. Инфантильная митохондриальная энцефалопатия. Semin Fetal Neonatal Med. (2011) 16: 205–15. 10.1016 / j.siny.2011.04.003 [PubMed] [CrossRef] [Google Scholar] 42. Олишар М., Шани Э., Айгюн С., Аззопарди Д., Хант Р.В., Тоет М.С. и др. . Амплитудно-интегрированная электроэнцефалография у новорожденных с врожденными нарушениями обмена веществ. Неонатология. (2012) 102: 203–11. 10.1159 / 000339567 [PubMed] [CrossRef] [Google Scholar] 43. Хобсон Э., Томас С., Крофтон П. М., Мюррей А. Д., Дин Дж. К., Ллойд Д.Изолированная недостаточность сульфитоксидазы имитирует признаки гипоксической ишемической энцефалопатии. Eur J Pediatr. (2005) 164: 655–9. 10.1007 / s00431-005-1729-5 [PubMed] [CrossRef] [Google Scholar] 44. Уиллис Т.А., Дэвидсон Дж., Грей Р.Г., Поултон К., Рамани П., Уайтхаус В. Дефицит цитохромоксидазы, проявляющийся как асфиксия при рождении. Dev Med Child Neurol. (2000) 42: 414–7. 10.1017 / S0012162200000761 [PubMed] [CrossRef] [Google Scholar] 45. Khong PL, Lam BC, Tung HK, Wong V, Chan FL, Ooi GC. МРТ неонатальной энцефалопатии.Clin Radiol. (2003) 58: 833–44. 10.1016 / S0009-9260 (03) 00261-7 [PubMed] [CrossRef] [Google Scholar] 46. Enns GM.
Врожденные нарушения обмена веществ, маскирующиеся под гипоксически-ишемическую энцефалопатию. NeoReviews. (2005) 12: e549 – e558. 10.1542 / neo.6-12-e549 [CrossRef] [Google Scholar] 47. Уолш Б.Х., Бродхерст Д.И., Мандал Р., Вишарт Д.С., Бойлан Г.Б., Кенни Л.С. и др. . Метаболомный профиль пуповинной крови при гипоксической ишемической энцефалопатии новорожденных. PLoS ONE. (2012) 7: e50520. 10.1371 / journal.pone.0050520 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 48.Коуэн Ф., Резерфорд М., Грюнендал Ф., Экен П., Меркури Э., Байддер Г.М. и др. . Происхождение и сроки поражения головного мозга у доношенных детей с неонатальной энцефалопатией. Ланцет. (2003) 361: 736–42
10.1016 / S0140-6736 (03) 12658-X [PubMed] [CrossRef] [Google Scholar] 49. Ян М.М., Camfield PR. Исход неонатального инсульта у доношенных детей без значительной асфиксии при рождении. Eur J Pediatr. (1998) 157: 846–8. 10.1007 / s004310050950 [PubMed] [CrossRef] [Google Scholar] 50. Рамасвами В., Миллер С.П., Баркович А.Дж., Партридж Дж.С., Ферриеро Д.М.Перинатальный инсульт у доношенных детей с неонатальной энцефалопатией. Неврология. (2004) 62: 2088–91. 10.1212 / 01.WNL.0000129909.77753.C4 [PubMed] [CrossRef] [Google Scholar] 51. Scherer EB, Loureiro SO, Vuaden FC, da Cunha AA, Schmitz F, Kolling J, et al. . Легкая гипергомоцистеинемия увеличивает уровни ацетилхолинэстеразы мозга и провоспалительных цитокинов в различных тканях. Mol Neurobiol. (2014) 50: 589–96. 10.1007 / s12035-014-8660-6 [PubMed] [CrossRef] [Google Scholar] 52. Harteman JC, Groenendaal F, Benders MJ, Huisman A, Blom HJ, de Vries LS.Роль тромбофильных факторов у доношенных детей с неонатальной энцефалопатией. Pediatr Res. (2013) 73: 80–6. 10.1038 / pr.2012.150 [PubMed] [CrossRef] [Google Scholar] 53. Calkavur S, Akisu M, Olukman O, Balim Z, Berdeli A, Cakmak B и др. . Генетические факторы, влияющие на краткосрочный исход развития нервной системы у доношенных новорожденных с гипоксически-ишемической энцефалопатией. J Int Med Res. (2011) 39: 1744–56. 10.1177 / 147323001103
7 [PubMed] [CrossRef] [Google Scholar] 54. Додельсон де Кремер Р., Гроссо С. Материнская мутация 677C> T в гене метилентетрагидрофолатредуктазы, связанная с тяжелым повреждением головного мозга у потомства.Clin Genet. (2005) 67: 69–80. [PubMed] [Google Scholar] 55. Odd D, Váradi A, Rajatileka S, Molnár E, Luyt K. Связь между реанимацией новорожденных и однонуклеотидным полиморфизмом rs1835740. Acta Paediatr. (2016) 105: e307–12. 10.1111 / apa.13421 [PubMed] [CrossRef] [Google Scholar] 56. Bruyland M, Liebaers I, Sacre L, Vandeplas Y, De Meirleir L, Martin JJ. Неонатальная миотубулярная миопатия с вероятным X-сцепленным наследованием: наблюдения за новой семьей с обзором литературы. J Neurol.(1984) 231: 220–2. 10.1007 / BF00313942 [PubMed] [CrossRef] [Google Scholar] 57. Баркович А.Дж., Вестмарк К., Партридж К., Сола А., Ферриеро Д.М. Перинатальная асфиксия: результаты МРТ в первые 10 дней. AJNR Am J Neuroradiol. (1995) 16: 427–38. [PubMed] [Google Scholar] 58. Barrett MJ, Donoghue V, Mooney EE, Slevin M, Persaud T., Twomey E, et al. . Изолированное острое некистозное повреждение белого вещества у доношенных детей с неонатальной энцефалопатией. Arch Dis Child Fetal Neonatal Ed. (2013) 98: F158 – F160. 10.1136 / archdischild-2011-301505 [PubMed] [CrossRef] [Google Scholar]
Необходимость распознавания множественных этиологий для оптимального управления
Front Pediatr.2019; 7: 142.
, 1, 2 , 1, 3, 4 и 1, 2, 3, 4, 5,
64 *
4 Сайма Аслам
1 Педиатрия, Национальный родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
Тэмми Стрикленд
1 Педиатрия, Национальный родильный дом , Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити-колледж в Дублине, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Больница Университета Кумб для женщин и младенцев, Дублин, Ирландия
Элеонора Дж. .Моллой
1 Педиатрия, Национальный родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити College Dublin, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Университетская больница для женщин и младенцев Кумб, Дублин, Ирландия
5 Неонатология, Детская больница Богоматери, Дримна, Ирландия
1 Педиатрия, национальная Родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити-колледж Дублина, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Coombe Women’s и больница Университета младенцев, Дублин, Ирландия
5 Неонатология, Детская больница Богоматери, Дримна, Ирландия
Отредактировал: Микко Холлман, Университет Оулу, Финляндия
Рецензент: Георг Шмольцер, Университет Альберты, Канада; Аакаш Пандита, Институт медицинских наук им. Санджая Ганди, Индия
Эта статья была отправлена в раздел «Неонатология» журнала «Границы в педиатрии»
Поступила в редакцию 15 октября 2018 г .; Принят в печать 26 марта 2019 г.
Авторские права © 2019 Aslam, Strickland and Molloy.
Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License (CC BY). Использование, распространение или воспроизведение на других форумах разрешено при условии указания автора (авторов) и правообладателя (ов) и ссылки на оригинальную публикацию в этом журнале в соответствии с принятой академической практикой. Запрещается использование, распространение или воспроизведение без соблюдения этих условий.
Эта статья цитируется в других статьях в PMC.
Abstract
Неонатальная энцефалопатия (NE) связана с высокой смертностью и заболеваемостью. Факторы, предрасполагающие к NE, могут быть антенатальными, перинатальными или их комбинацией. Антенатальные материнские факторы, семейные факторы, генетическая предрасположенность, гипоксическая ишемическая энцефалопатия, инфекции, плацентарные аномалии, тромбофилия, дефекты коагуляции и метаболические нарушения — все это вовлечено в патогенез NE. В настоящее время терапевтическая гипотермия — единственное доступное лечение, независимо от этиологии.Распознавание этиологии вовлеченного НЭ может также помочь в проведении таких исследований, как метаболические исследования и обследования на сепсис, для обеспечения оптимального лечения. Понимание этиологии NE может позволить разработать целевую дополнительную терапию, связанную с основным механизмом, и разработать превентивные стратегии.
Ключевые слова: неонатальная энцефалоптия, этиология, антенатальная, перинатальная, таргетная дополнительная терапия
Введение
Неонатальная энцефалопатия (НЭ) — сложное заболевание новорожденных, характеризующееся измененным уровнем сознания, судорогами, плохим тонусом. для инициирования или поддержания дыхания (1) и связан с полиорганной дисфункцией (2).Заболеваемость NE оценивается в 3 случая на 1000 живорождений (3). NE может быть результатом широкого спектра причин и является клиническим термином, не определяющим этиологию. Единственное доступное лечение — это терапевтическая гипотермия (ТГ) с максимальной пользой, если начать в первые 6 часов жизни (4). Существует несколько причин НЭ, таких как гипоксическая ишемическая энцефалопатия (ГИЭ), перинатальные инфекции, аномалии плаценты, метаболические нарушения, коагулопатии и сосудистый инсульт новорожденных (). Однако более чем в половине случаев причина НЭ остается неустановленной (5).
Многофакторная этиология неонатальной энцефалопатии. Многие факторы предрасполагают к возникновению неонатальной энцефалопатии либо по отдельности, либо в комбинации, включая (A) Факторы риска до зачатия, (B) Сопутствующие заболевания или события у матери до родов / во время родов, (C) Патология плаценты, (D) Гипоксия-ишемия, (E) Перинатальная инфекция, (F) Неонатальный инсульт или тромбофилия, (G) Метаболические нарушения и (H) Генетические и эпигенетические аномалии.ПРОМ, длительный разрыв плодных оболочек; ЗВУР, ограничение внутриутробного развития.
Использование термина NE vs. HIE противоречиво. Было предложено использовать термин NE для доношенных и поздних недоношенных новорожденных, у которых не было выявленных дозорных событий (6, 7). Трудно доказать наличие церебральной гипоксической ишемии, за исключением моделей на животных и конкретных случаев неонатального инсульта. Все текущие параметры, включая pH и судороги, неспецифичны (7). Некоторые из паттернов черепно-мозговых травм, наблюдаемых у пациентов с NE, могут быть воспроизведены на животных моделях с помощью гипоксии-ишемии, но это не доказывает, что все NE вызваны HIE (7).Несколько опубликованных популяционных исследований показали, что факторы риска до родов и неасфиксии связаны с НЭ (6). Напротив, некоторые авторы утверждают, что ГИЭ является причиной НЭ в 50–80% случаев на основании клинических критериев, критериев ЭЭГ и МРТ (1). Поэтому в этом обзоре мы использовали термин NE, и мы стремились изучить различные этиологии, связанные с NE.
Материнские факторы
Материнская гипертензия (16%) была важным фактором дородового риска НЭ в реестре неонатальной энцефалопатии Оксфордской сети штата Вермонт ( n = 4 165).Также была более высокая частота клинического хориоамнионита, длительного разрыва плодных оболочек и гипотиреоза матери. Хотя острый асфиксический эпизод был зарегистрирован в 15% случаев, связь с воспалением была обнаружена у 24% (5).
Популяционное исследование в Западной Австралии показало, что социально-экономический статус, семейный анамнез судорог, неврологические проблемы и зачатие после лечения бесплодия были независимыми факторами риска до зачатия для NE ( n = 164) (8).Заболевание щитовидной железы матери, кровотечение во время беременности, вирусные заболевания, преэклампсия, аномальная плацента, задержка внутриутробного развития и переношенность были другими важными факторами риска в дородовой период (8). Идентифицируемые дородовые факторы риска НЭ были обнаружены в 69% случаев, внутриродовые факторы риска — в 5%, как дородовые, так и во время родов — в 24% и отсутствие фактора риска — в 2%. Только в 4% случаев внутриродовая гипоксия была выявлена без каких-либо факторов риска до родов или до зачатия (9). Было обнаружено, что ограничение роста в развитых странах и беременность двойней в развивающихся странах связаны с НЭ.Заболевание щитовидной железы у матери, дородовое наблюдение, инфекция, роды и тактика ведения родов должны стать важными модификаторами в исследовании 27 новорожденных с НЭ и 100 детей контрольной группы (3). Дородовые (74 против 18%), внутриродовые (67 против 19%) и острые внутриродовые события (33 против 2%) более вероятны у младенцев с НЭ по сравнению с контрольной группой. Следовательно, в неонатальном клиническом анамнезе подробный материнский анамнез важен и может быть путем к профилактическим стратегиям в будущем.
Из 45 новорожденных с NE 36% имели дозорные эпизоды, 40% имели хориоамнионит и 11% имели оба этих заболевания.Если данные дозорных событий были исключены, то возраст матери> 35 лет (ОР 2,5; 95% ДИ 1,1–5,6) и инфекция мочевыводящих путей во время беременности (ОР 2,6; 95% ДИ 1,0–6,5) были потенциальными факторами дородового риска для NE (10).
Гипоксия-ишемия
Хотя концепция гипоксии-ишемии четко выражена в моделях на животных, она может не подходить для использования во всех случаях неонатальной NE у человека. «Дозу» и продолжительность гипоксии, а также степень ишемии можно напрямую измерить на животной модели.Однако у новорожденных людей это неизвестно, если нет контрольного события, и впоследствии не используются суррогатные маркеры гипоксии. Badawi et al. показали, что асфиксия во время родов считается сопутствующим фактором в 29% случаев НЭ и самостоятельным фактором только в 4% случаев (9). Было обнаружено, что внутриродовая гипоксия-ишемия является одним из факторов, способствующих развитию НЭ в 30% случаев в развитых и 60% в развивающихся странах (3). Американский колледж акушеров и Американская академия педиатрии определили дозорное событие в своем документе о неонатальной энцефалопатии и неврологических исходах (Obstet Gynecol 2014).Следующее соответствует острому пери- или интранатальному событию: дозорное гипоксическое или ишемическое событие, возникающее непосредственно перед или во время родов и родоразрешения, например разрыв матки или тяжелая отслойка плаценты; паттерны пульсометра плода, соответствующие острым послеродовым или интранатальным событиям; сроки и тип травм головного мозга, основанные на исследованиях изображений, согласующихся с этиологией острого послеродового или внутриродового события, и отсутствуют доказательства других проксимальных или дистальных факторов, которые могли бы быть способствующими факторами.Кроме того, сочетание низких баллов по шкале Апгарса, ацидемии, аномального кардиотокографа, изменений МРТ, согласующихся с гипоксией-ишемией и полиорганной дисфункцией, — все это связано с гипоксически-ишемической этиологией, но в равной степени может быть изменено сепсисом или другими причинами NE. Асфиксичные родовые явления и воспаление присутствовали только в 12,6% случаев церебрального паралича (11). У новорожденных с NE ( n = 405) следующие факторы были независимо связаны с NE ( p -значение = 0,001), включая: только 1 дородовой период (гестационный возраст> 41 недели) и 7 факторов во время родов, включая длительный разрыв плодных оболочек, аномальные кардиотокограф, густой меконий, дозорные события, дистоция плеча, тугая затылочная пуповина и отказ вакуума (12).В когорте из 26 новорожденных с дозорными событиями NE (ОР 74,9, 95% ДИ 11,9-бесконечность, p <0,001) и отслеживание ЧСС плода категории 3 (28,0% против 4,0%, p = 0,002) были сильно связанный с NE (13). В когорте из 45 новорожденных у 36% были дозорные события, а у 11% были как дозорные, так и хориоамнионит (10).
Нейровизуализация с использованием магнитно-резонансной томографии, традиционной, диффузионной и спектроскопии в период от 24 до 96 часов жизни дает полезные рекомендации относительно возможных сроков возникновения церебрального инсульта, особенно диффузных аномалий.Аномалии, вызванные травмой головного мозга, становятся наиболее очевидными через 7 дней при использовании качественной МРТ, диффузии и спектроскопии. Глубокое ядерное серое вещество или водораздел кортикального повреждения развиваются по четко определенному типу повреждения мозга и типичны для гипоксически-ишемического повреждения мозга у новорожденного. Генетические и метаболические причины могут быть исследованы, если на МРТ существует другая картина травмы головного мозга или эволюция травмы. Признаки того, что послеродовая гипоксия-ишемия не была причиной НЭ, предлагаются на МРТ: порэнцефалия, очаговый артериальный инфаркт, венозный инфаркт, изолированное внутрипаренхиматозное или внутрижелудочковое кровоизлияние или атипичные паттерны метаболических энцефалопатий.
При NE, связанном с острым дозорным событием (HIE), типичная картина повреждения на МРТ показала вовлечение базальных ганглиев, таламуса с ассоциированной задней конечностью внутренней капсулы и, в тяжелых случаях, вовлечение ствола мозга (14). При NE без задокументированного дозорного события вовлечение базальных ганглиев или таламуса (BGT) также связано с изменениями белого вещества в 50% случаев (14). BGT с обширным повреждением белого вещества (WM) был обнаружен в 14%, BGT с WM от легкой до умеренной — в 56%, изолированное таламическое повреждение — в 5%, умеренное повреждение WM — только у 2% и легкое WM или нормальное — у 23% в 48%. младенцы с ГИЭ.Внутренняя капсула была аномальной у 93% пациентов с умеренным и тяжелым повреждением WM и была связана со смертью и ХП у 86% пациентов (15).
Картина повреждения головного мозга может указывать на возможную причину, например, повреждение коркового вещества и белого вещества (очаговое / мультифокальное) может быть связано с плацентарной недостаточностью и хориоамнионитом. Ранняя категоризация пациентов в соответствии с типом травмы головного мозга может привести к другому терапевтическому подходу, поскольку на животных моделях было показано, что разные уровни гипотермии защищают от повреждения коры головного мозга или глубокого серого вещества, поэтому для получения максимальной пользы могут потребоваться специфические для пациента протоколы гипотермии.Точно так же в моделях на животных разные режимы охлаждения, системное и селективное, приводят к разной температуре мозга (16).
Трудно окончательно установить наличие, продолжительность и степень гипоксии и ишемии у новорожденных, поэтому использовались суррогатные маркеры, такие как pH и судороги (7). Следовательно, биомаркеры мультиорганного поражения могут быть полезны для диагностики или оценки тяжести гипоксической ишемии и прогнозирования исхода при NE. Сердечный тропонин является маркером ишемии миокарда у новорожденных и детей и высвобождается из миоцитов после повреждения их мембраны.Сердечный тропонин I (cTnI) был значительно выше у новорожденных с ГИЭ в первые 48 часов по сравнению с контрольной группой ( p <0,0005) (17). Сердечный TnI был повышен у новорожденных с более высокой степенью НЭ и у тех, кому потребовались инотропы (18). Пороговое значение <0,22 нг / мл для нормотермических и <0,15 нг / мл для гипотермических младенцев с NE предсказывало нормальный исход развития нервной системы (19).
Гипоксия приводит к усилению эритропоэза и выбросу незрелых ядерных эритроцитов (nRBC) в кровоток (20).ЯРБК пуповинной крови были значительно выше у новорожденных, подвергшихся асфиксии, по сравнению с контрольной группой, а также коррелировали с апгаром через 1 мин, pH и развитием NE (20). Количество ядерных эритроцитов на 100 лейкоцитов было выше у новорожденных с НЭ по сравнению с контрольной группой, младенцев с НЭ средней / тяжелой или легкой степени ( p = 0,016) и у новорожденных с плохим исходом нервного развития ( p = 0,03) 21). Следовательно, стандартизованное измерение воздействия клинической гипоксии было бы полезным с использованием комбинации этих маркеров и могло бы помочь в определении времени инсульта и корреляции с доклиническими моделями на животных.
Инфекция
Риск спастического церебрального паралича (ДЦП) и квадриплегического ДЦП повышался при сочетании инфекции и асфиксии (22). Уровни интерлейкина (ИЛ) -6 через 6 часов связаны с отклонениями от нормы неврологического обследования (23). NE, инотропная поддержка, судороги без менингита, потребность в интубации и более низкий 5-минутный апгар были более вероятны у новорожденных с ХП при наличии инфекции у матери по сравнению с ХП без инфекции (22).
Материнские и ранние неонатальные инфекции представляют собой диагностическую проблему.Ведутся споры о том, может ли скрытая инфекция, не обнаруживаемая обычными методами культивирования, быть связана с неврологическим повреждением во всех возрастных группах. Полимеразная цепная реакция (ПЦР) выявила 11 случаев бактериемии у энцефалопатических новорожденных в Африке, у которых был отрицательный результат посева крови (NE n = 201). ПЦР в сочетании с посевом крови привела к обнаружению бактериальных продуктов в 8,9% случаев НЭ по сравнению с 3,1% при использовании одного посева крови (24). В метаанализе стрептококк группы B (GBS) был связан с NE в 0.58% случаев и смертность были выше при использовании СГБ плюс НЭ по сравнению с одним НЭ (25). В когорте из 45 новорожденных 40% имели хориоамнионит и 11% имели как дозорные события, так и хориоамнионит (10).
Терапевтическая гипотермия задерживает рост и пик ответа с-реактивного белка (СРБ), а также приводит к снижению количества лейкоцитов и нейтрофилов по сравнению с нормотермными новорожденными (26). Это влияние гипотермии на задержку развития естественных воспалительных маркеров следует учитывать при выборе лечения антибиотиками и продолжительности лечения новорожденных с НЭ.
Следовательно, полное обследование на сепсис имеет важное значение у всех детей с НЭ. Стандартных рекомендаций по выполнению люмбальной пункции во всех случаях НЭ не существует, и их можно выбирать в каждом конкретном случае. Кандидатами могут быть младенцы с повышенным WCC и CRP или факторами риска септического риска. Существуют также технические и практические проблемы для поясничной пункции у младенцев с NE, которые являются ригидными из-за TH, а также часто изначально имеют отек мозга при ультразвуковом исследовании черепа.
Аномалии плаценты
Поражение пуповины, хориоамнионит, васкулит плода, меконий хориональной пластинки и тромботическая васкулопатия плода часто встречались в плацентарных поражениях у пациентов с NE ( n = 23) (27).Поражения плаценты, указывающие на тромбоз и снижение фетоплацентарного кровотока, являются значимыми и независимыми факторами риска НЭ ( n = 93) (28). Наличие более одного поражения плаценты увеличивает вероятность НЭ, но не было никакой корреляции между патологией плаценты и картиной повреждения на МРТ ( n = 56) (29). Аномальная патология плаценты была обнаружена у 29% новорожденных с дозорными событиями и у 73% младенцев без дозорных явлений ( p = 0,0001), перенесших терапевтическую гипотермию (30).Воспалительные поражения плаценты чаще наблюдались у новорожденных без дозорных событий ( p = 0,002) (30). Хронический виллит был связан с повреждением базальных ганглиев (BGT), тогда как наличие ядерных эритроцитов, снижение созревания плаценты и хронический виллит также приводили к повреждению белого вещества / водораздела вместе с вовлечением BGT ( n = 95) (31).
Доказательства связи хориоамнионита с НЭ разнообразны. Предполагается, что время инфицирования и степень воспалительного ответа могут привести либо к прекондиционированию, либо к сенсибилизации и могут вызвать либо защитный эффект, либо дальнейшее усиление перинатального повреждения головного мозга, соответственно (32).Этот эффект был продемонстрирован на животных моделях. Липополисахарид (ЛПС), вводимый за 4–6 ч до 20 и 50 мин воздействия HI, приводил к усилению травм головного мозга. Однако введение LPS за 24 часа до 50-минутного воздействия HI привело к значительному ослаблению травм головного мозга (32). КА выявлена у 8 новорожденных с признаками перинатальной асфиксии (всего n = 23) (27). Младенцы с NE и TH имели более высокие шансы на наличие CA по сравнению с младенцами, которые не получали TH ( n = 98) (33).CA, васкулит и фунизит были связаны с NE степени I, виллитом с NE II и фунизитом с III степенью у 141 новорожденного с NE и 309 контрольных (29). CA был связан с более низким риском черепно-мозговой травмы и плохим когнитивным исходом по сравнению с не-CA (скорректированный OR 0,3; 95% CI 0,1–0,7, p = 0,004) у новорожденных с NE ( n = 258), хотя только У 20 новорожденных были гистологические доказательства СА. В той же когорте новорожденные с признаками сепсиса имели более высокие шансы на повреждение водораздела и аномальные нейромоторные показатели, чем у новорожденных без каких-либо клинических признаков ( p = 0.007) (34). У 120 младенцев с сочетанием перинатального ацидоза, NE и хориоамнионита с ответом плода или без него и пятнистый / диффузный хронический виллит были независимо связаны с тяжестью NE (35). Единственным индивидуальным предиктором патологического исхода нервного развития через 22-24 месяца после терапии гипотермией был диффузный хронический виллит. Гистологическая CA имела низкую прогностическую ценность для развития энцефалопатии и смерти у NE ( n = 51) (36), но материнская лихорадка ( n = 336) во время родов была независимым фактором для NE (скорректированное OR 4.72, 95% ДИ 1,28–17,4) (37). Клинический хориоамнионит был связан с более высокими уровнями IL-6, IL-8 в пуповинной крови и регулировался активацией нормальных Т-клеток, экспрессируемых и секретируемых (RANTES) в NE ( n = 61). В когорте из 67 новорожденных с хориоамнионитом NE, независимо от того, были ли клинические или гистологические данные связаны со стойким метаболическим ацидозом, это может предсказать плохой неврологический исход (38).
Патология плаценты описывается как «черный ящик» беременности. Стандартизированная классификация результатов патологии плаценты важна для дальнейшего определения этиологии NE (39).
Нарушения обмена веществ
Нарушения обмена веществ являются редкими причинами НЭ, но их всегда следует учитывать. Врожденные нарушения метаболизма (ВЭМ) присутствуют в неонатальном периоде после нормального периода выздоровления и отсутствия признаков перинатальной асфиксии, но неврологические и полиорганные поражения могут проявляться как НЭ (40). Митохондриальные нарушения также являются важной причиной НЭ (41).
Амплитудная интегрированная электроэнцефалограмма (аЭЭГ) была отклонена от нормы у 27 новорожденных с ВЭМ, причем наиболее устойчивыми признаками были аномальная фоновая активность и судороги.Не было различий в аЭЭГ для энцефалопатии, связанной с IEM или NE, и дифференцировать можно было только на основании клинического подозрения (42). Единственное метаболическое расстройство с диагностической ЭЭГ — это некетотическая гиперглицинемия с первоначальным паттерном «подавление-всплеск», переходящим в гипсаритмию в раннем или среднем младенчестве и диагностируемое путем измерения уровня глицина в спинномозговой жидкости (42). Имеются также отдельные сообщения о случаях ИЭМ, таких как дефицит сульфитоксидазы и цитохрома С, проявляющийся как НЭ (43, 44).
Результаты МРТ могут варьироваться в зависимости от типа врожденной ошибки метаболизма (ВЭМ) и могут варьироваться от поражения белого вещества до поражения глубоких серых ядер. Митохондриальные энцефалопатии имеют симметричное двустороннее распределение и изначально могут быть диагностированы как NE (45). Следует учитывать метаболические нарушения, если нет явных явлений во время родов, стойкий лактоацидоз и / или гипогликемия (45) и начато обследование. Различные паттерны повреждений на МРТ головного мозга могут помочь дифференцировать метаболические нарушения от НЭ.Поражение Globus Pallidus часто встречается при IEM по сравнению с NE, хотя картина повреждения при дефиците сульфитоксидазы и дефиците фактора молибдена может имитировать NE (46).
Изолированные приступы связаны с такими расстройствами, как: судороги, связанные с пиридоксином, некетотическая гиперглицинемия (НКГ), дефицит дигидропиримидиндегидрогеназы, дефицит сульфитоксидазы (либо изолированный, либо как часть дефицита кофактора молибдена), трансаминазы 4-аминобутират-аминотрансферазы (ГАБТрансферазы). ) дефицит, судороги, связанные с фолиевой кислотой, дефицит 3-фосфоглицератдегидрогеназы, дефицит гуанидиноацетатметилтрансферазы (GAMT) и дефицит переносчика глюкозы (GLUT-1).У младенцев с полиорганными поражениями, судорогами, метаболическим ацидозом, молочной железой, гипераммониемией могут быть: органическая ацидемия, дефекты цикла мочевины, пероксисомальные нарушения (например, синдром Зеллвегера) или митохондриальные нарушения.
Подробный семейный анамнез для установления факторов риска, таких как родство родителей или ранее пораженный ребенок, важен, поскольку большинство врожденных нарушений метаболизма имеют аутосомно-рецессивное или материнское наследование. Базовые исследования, такие как электролиты, аммиак, сывороточные аминокислоты, лактат, ацилкарнитин и органическая кислота в моче, могут быть рассмотрены при NE (40).Есть проблемы с метаболическим тестированием, так как их может потребоваться повторить, если ребенок очень плохо себя чувствует с полиорганной дисфункцией во время отбора образцов (46). Недавние исследования показали большой потенциал метаболомики как биомаркеров NE. Было показано, что содержание сукцината повышено у детей с НЭ, которые серьезно пострадали (47).
Тромбофилия и неонатальный инсульт
Асфиксия (в 4% случаев) участвует в патогенезе неонатального инсульта (48). Фокальные клонические приступы являются наиболее частым проявлением неонатального инсульта (49), и 6 младенцев с инсультом были обнаружены в когорте NE ( n = 124) (50).Эти дети обычно страдали судорогами и имели худшие исходы с точки зрения нервного развития, чем остальная когорта. Нарушения свертывания крови, такие как полицитемия, лейденский фактор V, нарушения гемоглобина и мутации протромбина, не были обнаружены у 4 из 6 обследованных пациентов (50).
В моделях на животных повышенные уровни гомоцистеина приводили к увеличению провоспалительных цитокинов, таких как фактор некроза опухоли альфа (TNFα), интерлейкин 1 бета (IL-1β) и IL-6 в гиппокампе и коре головного мозга.Это провоспалительное состояние может быть ответственным за нейрональные и цереброваскулярные эффекты, наблюдаемые у взрослых (51). Роль гомоцистеина или полиморфизмов в гене метилентетрагидрофолатредуктазы в возникновении неонатального повреждения головного мозга неясна (52). В когорте из 118 новорожденных с НЭ повреждение белого вещества / водораздела с большей вероятностью было связано с гипогликемией, полиморфизмом метилентетрагидрофолатредуктазы (MTHFR) и уровнями гомоцистеина в плазме в верхнем квартиле нормы (52).
Генетические и эпигенетические аномалии
Отсутствуют опубликованные данные, связывающие генетическую предрасположенность с развитием NE. У 40 пациентов с NE генетическая изменчивость протромбических факторов, таких как протромбин G20210A, фактор V Leiden G1691A и метилентетрагидрофолатредуктаза [MTHFR] C677T, и ген фактора некроза опухоли не повлияли на оценку NE, ЭЭГ, смерть, краниальное УЗИ (США) , неврологический исход при выписке через 6 и 12 месяцев. Полиморфизм гена интерлейкина-6 (IL-6 174GC) имел защитный эффект и был связан с нормальной ЭЭГ, краниальным УЗИ и неврологическим обследованием при выписке (53).В ретроспективном исследовании «случай-контроль» с участием 11 новорожденных с NE у матерей была обнаружена более высокая частота полиморфизма MTHFR (7 гомозиготных и 4 гетерозиготных) по сравнению с контрольной группой (54). Генетический полиморфизм может увеличивать риск или тяжесть неонатального повреждения головного мозга при NE, и его следует учитывать (53).
В рамках лонгитюдного исследования родителей и детей, проведенного Avon, было проведено генотипирование 7611 доношенных детей, и мерилом воздействия было наличие одного или нескольких минорных аллелей в одном из 3 SNP (rs2284411, rs2498804, rs1835740).Первичным результатом была необходимость реанимации при рождении, что было связано с rs1835740 (55). Требуются более крупные международные совместные исследования для определения необходимого количества пациентов для изучения генетических связей и разделения пациентов по этиологии.
Другая категория младенцев с генетической причиной неонатальной энцефалопатии — это дети с миопатиями и энцефалопатиями новорожденных. Пациенты, унаследовавшие миопатию (центронуклеарную миопатию), могут иметь неонатальный дистресс, гипотонию и признаки, указывающие на ГИЭ (56).Врожденная миотоническая дистрофия 1 типа характеризуется гипотонией и тяжелой генерализованной слабостью при рождении, часто с дыхательной недостаточностью, умственной отсталостью и ранней смертью. Это вызвано экспансией тринуклеотидного повтора CTG в некодирующей области DMPK .
В будущем подробное генотипирование, включая более легкий доступ к методам микроматриц в клинических условиях, предоставит больше информации, позволяющей индивидуализированный уход и потенциально классифицировать младенцев по генотипу.
Нейровизуализация
На МРТ можно увидеть различные модели травм, но это не исключает HIE как причины травмы. Характер повреждения зависит от тяжести, продолжительности и повторяемости гипоксической ишемии и может привести к поражению базальных ганглиев, таламуса, ствола мозга и / или белого вещества головного мозга в различных сочетаниях (1). При глубокой гипоксии преобладает повреждение более глубоких серых структур, то есть базальных ганглиев и таламуса. Объясняется это тем, что эти участки миелинизированы и имеют более высокую скорость метаболизма.Состояния, которые уменьшают, а не вызывают полное прекращение кровотока, такие как анемия и гиповолемия, связаны с повреждением коры головного мозга и сохранением более глубоких серых структур (57). В когорте из 245 пациентов с NE 197 (80%) результаты МРТ соответствовали острому перинатальному инсульту. МРТ у 40 младенцев (16%) были нормальными. У 9 младенцев (4%) были выявлены признаки тромбоза / инфаркта, генетических нарушений, антенатального инсульта и митохондрий (дефицит комплекса I) на МРТ в дополнение к гипоксическому ишемическому инсульту.Нейровизуализация у 8 (3%) младенцев с клиническим диагнозом НЭ показала либо врожденную ошибку метаболизма, нервно-мышечное расстройство, либо отсутствие диагноза, и эти результаты не соответствовали гипоксической ишемии (48). Плацентарный виллит высокой степени неизвестной этиологии ( n = 4) был обнаружен в когорте из 36 пациентов, связанных с повреждением белого вещества, вторичным по отношению к воспалению / окислительному стрессу в перинатальном периоде (58).
Значение для терапии
Все младенцы с NE могут не в одинаковой степени выиграть от переохлаждения.Следовательно, выявление точной этиологии в каждом случае NE имеет значение для лечения, поскольку есть некоторые излечимые причины, которые требуют быстрого определения для оптимального лечения. Использование бактериальной ПЦР для выявления инфекции у новорожденных с NE может быть более полезным, чем только посев крови с низким выходом бактерий, а также гипотермия может уменьшить воспалительную реакцию. Гистология плаценты отражает внутриматочную среду и может прояснить основную этиологию. Все новорожденные с риском IEM должны быть обследованы на предмет метаболических нарушений, так как этим пациентам могут быть полезны специфические методы лечения, а не гипотермия.Точно так же скрининг на тромбофилию следует рассматривать у пациентов из группы риска, таких как пациенты с инсультом, семейный анамнез тромбофилии. Подробная оценка этиологии NE важна для выявления излечимых причин и категоризации этой гетерогенной группы новорожденных, чтобы можно было подобрать соответствующее лечение в соответствии с этиологией и улучшением отдаленных результатов. Точно так же будет полезно стратифицировать большие многоцентровые когорты младенцев с NE по этиологии, чтобы полностью понять этиологию, реакцию на лечение гипотермией и отдаленные результаты.
Авторские взносы
SA: основной автор; ТС: помогал с поиском релевантных статей и рисунка; ЭМ: автор-руководитель.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Ссылки
1. Volpe JJ. Неонатальная энцефалопатия: неадекватный термин для гипоксически-ишемической энцефалопатии.Энн Нейрол. (2012) 72: 156–66. 10.1002 / ana.23647 [PubMed] [CrossRef] [Google Scholar] 2. Шах П., Рип Хаген С., Бейен Дж, Перлман М. Мультиорганная дисфункция у младенцев с постасфиксиальной гипоксически-ишемической энцефалопатией. Arch Dis Child Fetal Neonatal Ed. (2004) 89: F152 – F155. 10.1136 / adc.2002.023093 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 3. Куринчук Дж. Дж., Уайт-Конинг М., Бадави Н. Эпидемиология неонатальной энцефалопатии и гипоксически-ишемической энцефалопатии. Early Hum Dev. (2010) 86: 329–38.10.1016 / j.earlhumdev.2010.05.010 [PubMed] [CrossRef] [Google Scholar] 4. Джейкобс С.Е., Берг М., Хант Р., Тарнов-Морди В.О., Индер Т.Э., Дэвис П.Г.
Охлаждение новорожденных с гипоксической ишемической энцефалопатией. База данных Cochr Syst Rev. (2013) 1: CD003311
10.1002 / 14651858.CD003311.pub3 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 5. Нельсон К.Б., Бингхэм П., Эдвардс Э.М., Хорбар Д.Д., Кенни М.Дж., Индер Т. и др. . Антецеденты неонатальной энцефалопатии в реестре энцефалопатии Оксфордской сети Вермонта. Педиатрия.(2012) 130: 878–86. 10.1542 / peds.2012-0714 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 6. Нельсон КБ. Это HIE?
И почему это важно Acta Paediatr. (2007) 96: 1113–4. 10.1111 / j.1651-2227.2007.00364.x [PubMed] [CrossRef] [Google Scholar] 7. Дамманн О., Ферриеро Д., Грессенс П.
Неонатальная энцефалопатия или гипоксически-ишемическая энцефалопатия?
Соответствующая терминология имеет значение Pediatr Res. (2011) 70: 1-2. 10.1203 / PDR.0b013e318223f38d [PubMed] [CrossRef] [Google Scholar] 8. Бадави Н., Куринчук Дж. Дж., Кио Дж. М., Алессандри Л. М., О’Салливан Ф., Бертон П. Р. и др.. Факторы дородового риска энцефалопатии новорожденных: исследование случай-контроль в Западной Австралии. BMJ. (1998) 317: 1549–53. 10.1136 / bmj.317.7172.1549 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 9. Бадави Н., Куринчук Дж. Дж., Кио Дж. М., Алессандри Л. М., О’Салливан Ф., Бертон П. Р. и др. . Факторы риска внутриутробной энцефалопатии новорожденных: исследование случай-контроль в Западной Австралии. BMJ. (1998) 317: 1554–8. 10.1136 / bmj.317.7172.1554 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 10. Паркер SJ, Kuzniewicz M, Niki H, Wu YW.Факторы дородового и внутриродового риска гипоксически-ишемической энцефалопатии в когорте новорожденных в США. J Pediatr. (2018) 203: 163–9. 10.1016 / j.jpeds.2018.08.028 [PubMed] [CrossRef] [Google Scholar] 11. Адамсон С.Дж., Алессандри Л.М., Бадави Н., Бертон П.Р., Пембертон П.Дж., Стэнли Ф. Предикторы неонатальной энцефалопатии у доношенных новорожденных. BMJ. (1995) 311: 598–602
10.1136 / bmj.311.7005.598 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 12. Мартинес-Биарж М., Диез-Себастьян Дж., Вустхофф Си-Джей, Меркури Е., Коуэн FM.Дородовые и внутриродовые факторы, предшествующие неонатальной гипоксически-ишемической энцефалопатии. Педиатрия. (2013) 132: e952 – e959
10.1542 / peds.2013-0511 [PubMed] [CrossRef] [Google Scholar] 13. Торбенсон В.Е., Толчер М.К., Несбитт К.М., Колби К.Э., Эль-Нашар С.А., Гостоут Б.С. и др. . Внутриродовые факторы, связанные с неонатальной гипоксической ишемической энцефалопатией: исследование случай-контроль. BMC Беременность и роды. (2017) 17: 415
10.1186 / s12884-017-1610-3 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 14. Резерфорд М., Маламатениу К., МакГиннесс А., Оллсоп Дж., Биарж М.М., Конселл С.Магнитно-резонансная томография при гипоксически-ишемической энцефалопатии. Early Hum Dev. (2010) 86: 351–60. 10.1016 / j.earlhumdev.2010.05.014 [PubMed] [CrossRef] [Google Scholar] 15. Okereafor A, Allsop J, Counsell SJ, Fitzpatrick J, Azzopardi D, Rutherford MA и др. . Характер черепно-мозговой травмы у новорожденных, подвергшихся перинатальным дозорным событиям. Педиатрия. (2008) 121: 906–14. 10.1542 / peds.2007-0770 [PubMed] [CrossRef] [Google Scholar] 16. Мецлер М., Говиндан Р., Аль-Шаргаби Т., Везина Г., Андескавадж Н., Ван И и др.. Характер черепно-мозговой травмы и снижение вариабельности сердечного ритма у новорожденных с гипоксической ишемической энцефалопатией. Pediatr Res. (2017) 82: 438–43. 10.1038 / pr.2017.94 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 17. Симович AM, Игрутинович З., Обрадович С., Ристич Д., Вулетич Б., Раданович М. Значение сердечного тропонина I второго поколения в раннем скрининге гипоксически-ишемической энцефалопатии после перинатальной асфиксии. Srp Arh Celok Lek. (2012) 140: 600–5. [PubMed] [Google Scholar] 18. Шастри А.Т., Самарасекара С., Мунираман Х., Кларк П.Концентрации сердечного тропонина I у новорожденных с гипоксически-ишемической энцефалопатией. Acta Paediatr. (2012) 101: 26–9. 10.1111 / j.1651-2227.2011.02432.x [PubMed] [CrossRef] [Google Scholar] 19. Лю X, Chakkarapani E, Stone J, Thoresen M. Влияние компрессий сердца и лечения гипотермии на сердечный тропонин I у новорожденных с перинатальной асфиксией. Реанимация. (2013) 84: 1562–7. 10.1016 / j.resuscitation.2013.07.003 [PubMed] [CrossRef] [Google Scholar] 20. Гош Б., Миттал С., Кумар С., Дадхвал В. Прогнозирование перинатальной асфиксии с ядросодержащими эритроцитами в пуповинной крови новорожденных.Int J Gynaecol Obstet. (2003) 81: 267–71. 10.1016 / S0020-7292 (03) 00124-3 [PubMed] [CrossRef] [Google Scholar] 21. Уолш Б.Х., Бойлан Г.Б., Мюррей Д.М. Ядерные эритроциты и ранняя ЭЭГ: прогнозирование стадии Сарната и двухлетнего исхода. Early Hum Dev. (2011) 87: 335–9. 10.1016 / j.earlhumdev.2011.01.041 [PubMed] [CrossRef] [Google Scholar] 22. Нельсон КБ, Гретер Дж. Потенциально удушающие состояния и спастический церебральный паралич у младенцев с нормальной массой тела при рождении. Am J Obstet Gynecol. (1998) 179: 507–13. 10.1016 / S0002-9378 (98) 70387-4 [PubMed] [CrossRef] [Google Scholar] 23.Шалак Л.Ф., Лапток А.Р., Джафри Х.С., Рамило О., Перлман Дж. Клинический хориоамнионит, повышенные цитокины и травмы головного мозга у доношенных детей. Педиатрия. (2002) 110: 673–80. 10.1542 / peds.110.4.673 [PubMed] [CrossRef] [Google Scholar] 24. Танн CJ, Nkurunziza P, Nakakeeto M, Oweka J, Kurinczuk JJ, Were J и др. . Распространенность патогенов кровотока выше в случаях неонатальной энцефалопатии по сравнению с контрольной группой, использующей новую панель ПЦР-анализов в реальном времени. PLoS ONE. (2014) 9: e97259. 10.1371 / journal.pone.0097259 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 25.Танн С.Дж., Мартинелло К.А., Саду С., Лоун Дж.Э., Сил А.С., Вега-Поблете М. и др.
Группа исследователей неонатальной энцефалопатии GBS. неонатальная энцефалопатия со стрептококками группы b во всем мире: систематический обзор, наборы данных исследовательских групп и метаанализ. Clin Infect Dis. (2017) 65 (Suppl_2): S173–89. 10.1093 / cid / cix662 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 26. Chakkarapani E, Davis J, Thoresen M. Терапевтическая гипотермия задерживает ответ C-реактивного белка и подавляет количество лейкоцитов и тромбоцитов у младенцев с неонатальной энцефалопатией.Arch Dis Child Fetal Neonatal Ed. (2014) 99: F458 – F463. 10.1136 / archdischild-2013-305763 [PubMed] [CrossRef] [Google Scholar] 27. Wintermark P, Boyd T, Gregas MC, Labrecque M, Hansen A. Патология плаценты у новорожденных с асфиксией, отвечающая критериям терапевтической гипотермии. Am J Obstet Gynecol. (2010) 203: 579.e1–9. 10.1016 / j.ajog.2010.08.024 [PubMed] [CrossRef] [Google Scholar] 28. Макдональд Д.Г., Келехан П., Макменамин Дж.Б., Горман В.А., Мэдден Д., Тоббия И.Н. и др. . Плацентарная тромботическая васкулопатия плода связана с неонатальной энцефалопатией.Hum Pathol. (2004) 35: 875–80
10.1016 / j.humpath.2004.02.014 [PubMed] [CrossRef] [Google Scholar] 29. Hayes BC, Cooley S, Donnelly J, Doherty E, Grehan A, Madigan C и др. . Плацента у младенцев> 36 недель беременности с неонатальной энцефалопатией: исследование случай-контроль. Arch Dis Child Fetal Neonatal Ed. (2013) 98: F233–9. 10.1136 / archdischild-2012-301992 [PubMed] [CrossRef] [Google Scholar] 30. Чанг Т., Рейес Т.Дж., Пласетек Дж., Массаро А.Н., Нельсон КБ.
Неонатальная энцефалопатия, дозорные явления и плацента.J Neonatal Perinatal Med. (2012) 5: 41–8. 10.3233 / NPM-2012-54211 [CrossRef] [Google Scholar] 31. Хартеман Дж. К., Никкельс П. Г., Бендерс М. Дж., Кви А., Грюнендал Ф., де Фрис Л. С.. Патология плаценты у доношенных детей с гипоксически-ишемической неонатальной энцефалопатией и ассоциация с магнитно-резонансной томографией повреждения головного мозга. J Pediatr. (2013) 163: 968–995.
10.1016 / j.jpeds.2013.06.010 [PubMed] [CrossRef] [Google Scholar] 32. Эклинд С., Маллард С., Арвидссон П., Хагберг Х. Липополисахарид вызывает как первичную, так и вторичную фазу сенсибилизации в развивающемся мозге крысы.Pediatr Res. (2005) 58: 112–6
10.1203 / 01.PDR.0000163513.03619.8D [PubMed] [CrossRef] [Google Scholar] 33. Нельсон Д.Б., Лаке А.М., Макинтайр Д.Д., Санчес П.Дж., Левено К.Дж., Чалак Л.Ф. Акушерские предшественники лечения новорожденного с помощью охлаждения тела. Am J Obstet Gynecol. (2014) 211: 155.e1–6. 10.1016 / j.ajog.2014.02.013 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 34. Дженстер М., Бонифачо С.Л., Рюэль Т., Роджерс Е.Е., Там Э.У., Партридж Дж.С. и др.
Инфекция матери или новорожденного: связь с исходами неонатальной энцефалопатии.Pediatr Res. (2014) 76: 93–9. 10.1038 / pr.2014.47 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 35. Мир И.Н., Джонсон-Велч С.Ф., Нельсон Д.Б., Браун Л.С., Розенфельд С.Р., Чалак Л.Ф. Патология плаценты связана с тяжестью неонатальной энцефалопатии и неблагоприятными исходами развития после гипотермии. Am J Obstet Gynecol. (2015) 213: 849.e1–7. 10.1016 / j.ajog.2015.09.072 [PubMed] [CrossRef] [Google Scholar] 36. Шалак Л., Джонсон-Велч С., Перлман Дж. М.. Хориоамнионит и неонатальная энцефалопатия у доношенных детей с ацидемией плода: гистопатологические корреляции.Pediatr Neurol. (2005) 33: 162–5. 10.1016 / j.pediatrneurol.2005.04.005 [PubMed] [CrossRef] [Google Scholar] 37. Impey L, Greenwood C, MacQuillan K, Reynolds M, Sheil O. Лихорадка в родах и неонатальная энцефалопатия: проспективное когортное исследование. BJOG. (2001) 108: 594–7. 10.1111 / j.1471-0528.2001.00145.x [PubMed] [CrossRef] [Google Scholar] 38. Джонсон CT, Бурд I, Рагхунатан Р., Нортингтон Ф. Дж., Грэм Э.М. Перинатальное воспаление / инфекция и его связь с коррекцией метаболического ацидоза при гипоксически-ишемической энцефалопатии.J Perinatol. (2016) 36: 448–52. 10.1038 / jp.2015.221 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 39. Кларк П., Мунираман Х., Гарднер Д., Венкатеш В., Керли А., Виктор С. и др. . Исследование неонатальной энцефалопатии: часто теряемый плацентарный «черный ящик». Pediatr Dev Pathol. (2015) 18: 343–4. 10.2350 / 15-02-1611-LET.1 [PubMed] [CrossRef] [Google Scholar] 40. Tan ES. Врожденные нарушения обмена веществ, проявляющиеся как неонатальная энцефалопатия: практические советы клиницистам. Ann Acad Med Singapore. (2008) 37 (12 доп.): 94–3. [PubMed] [Google Scholar] 41. Узиэль Г., Геззи Д., Зевиани М. Инфантильная митохондриальная энцефалопатия. Semin Fetal Neonatal Med. (2011) 16: 205–15. 10.1016 / j.siny.2011.04.003 [PubMed] [CrossRef] [Google Scholar] 42. Олишар М., Шани Э., Айгюн С., Аззопарди Д., Хант Р.В., Тоет М.С. и др. . Амплитудно-интегрированная электроэнцефалография у новорожденных с врожденными нарушениями обмена веществ. Неонатология. (2012) 102: 203–11. 10.1159 / 000339567 [PubMed] [CrossRef] [Google Scholar] 43. Хобсон Э., Томас С., Крофтон П. М., Мюррей А. Д., Дин Дж. К., Ллойд Д.Изолированная недостаточность сульфитоксидазы имитирует признаки гипоксической ишемической энцефалопатии. Eur J Pediatr. (2005) 164: 655–9. 10.1007 / s00431-005-1729-5 [PubMed] [CrossRef] [Google Scholar] 44. Уиллис Т.А., Дэвидсон Дж., Грей Р.Г., Поултон К., Рамани П., Уайтхаус В. Дефицит цитохромоксидазы, проявляющийся как асфиксия при рождении. Dev Med Child Neurol. (2000) 42: 414–7. 10.1017 / S0012162200000761 [PubMed] [CrossRef] [Google Scholar] 45. Khong PL, Lam BC, Tung HK, Wong V, Chan FL, Ooi GC. МРТ неонатальной энцефалопатии.Clin Radiol. (2003) 58: 833–44. 10.1016 / S0009-9260 (03) 00261-7 [PubMed] [CrossRef] [Google Scholar] 46. Enns GM.
Врожденные нарушения обмена веществ, маскирующиеся под гипоксически-ишемическую энцефалопатию. NeoReviews. (2005) 12: e549 – e558. 10.1542 / neo.6-12-e549 [CrossRef] [Google Scholar] 47. Уолш Б.Х., Бродхерст Д.И., Мандал Р., Вишарт Д.С., Бойлан Г.Б., Кенни Л.С. и др. . Метаболомный профиль пуповинной крови при гипоксической ишемической энцефалопатии новорожденных. PLoS ONE. (2012) 7: e50520. 10.1371 / journal.pone.0050520 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 48.Коуэн Ф., Резерфорд М., Грюнендал Ф., Экен П., Меркури Э., Байддер Г.М. и др. . Происхождение и сроки поражения головного мозга у доношенных детей с неонатальной энцефалопатией. Ланцет. (2003) 361: 736–42
10.1016 / S0140-6736 (03) 12658-X [PubMed] [CrossRef] [Google Scholar] 49. Ян М.М., Camfield PR. Исход неонатального инсульта у доношенных детей без значительной асфиксии при рождении. Eur J Pediatr. (1998) 157: 846–8. 10.1007 / s004310050950 [PubMed] [CrossRef] [Google Scholar] 50. Рамасвами В., Миллер С.П., Баркович А.Дж., Партридж Дж.С., Ферриеро Д.М.Перинатальный инсульт у доношенных детей с неонатальной энцефалопатией. Неврология. (2004) 62: 2088–91. 10.1212 / 01.WNL.0000129909.77753.C4 [PubMed] [CrossRef] [Google Scholar] 51. Scherer EB, Loureiro SO, Vuaden FC, da Cunha AA, Schmitz F, Kolling J, et al. . Легкая гипергомоцистеинемия увеличивает уровни ацетилхолинэстеразы мозга и провоспалительных цитокинов в различных тканях. Mol Neurobiol. (2014) 50: 589–96. 10.1007 / s12035-014-8660-6 [PubMed] [CrossRef] [Google Scholar] 52. Harteman JC, Groenendaal F, Benders MJ, Huisman A, Blom HJ, de Vries LS.Роль тромбофильных факторов у доношенных детей с неонатальной энцефалопатией. Pediatr Res. (2013) 73: 80–6. 10.1038 / pr.2012.150 [PubMed] [CrossRef] [Google Scholar] 53. Calkavur S, Akisu M, Olukman O, Balim Z, Berdeli A, Cakmak B и др. . Генетические факторы, влияющие на краткосрочный исход развития нервной системы у доношенных новорожденных с гипоксически-ишемической энцефалопатией. J Int Med Res. (2011) 39: 1744–56. 10.1177 / 147323001103
7 [PubMed] [CrossRef] [Google Scholar] 54. Додельсон де Кремер Р., Гроссо С. Материнская мутация 677C> T в гене метилентетрагидрофолатредуктазы, связанная с тяжелым повреждением головного мозга у потомства.Clin Genet. (2005) 67: 69–80. [PubMed] [Google Scholar] 55. Odd D, Váradi A, Rajatileka S, Molnár E, Luyt K. Связь между реанимацией новорожденных и однонуклеотидным полиморфизмом rs1835740. Acta Paediatr. (2016) 105: e307–12. 10.1111 / apa.13421 [PubMed] [CrossRef] [Google Scholar] 56. Bruyland M, Liebaers I, Sacre L, Vandeplas Y, De Meirleir L, Martin JJ. Неонатальная миотубулярная миопатия с вероятным X-сцепленным наследованием: наблюдения за новой семьей с обзором литературы. J Neurol.(1984) 231: 220–2. 10.1007 / BF00313942 [PubMed] [CrossRef] [Google Scholar] 57. Баркович А.Дж., Вестмарк К., Партридж К., Сола А., Ферриеро Д.М. Перинатальная асфиксия: результаты МРТ в первые 10 дней. AJNR Am J Neuroradiol. (1995) 16: 427–38. [PubMed] [Google Scholar] 58. Barrett MJ, Donoghue V, Mooney EE, Slevin M, Persaud T., Twomey E, et al. . Изолированное острое некистозное повреждение белого вещества у доношенных детей с неонатальной энцефалопатией. Arch Dis Child Fetal Neonatal Ed. (2013) 98: F158 – F160. 10.1136 / archdischild-2011-301505 [PubMed] [CrossRef] [Google Scholar]
Необходимость распознавания множественных этиологий для оптимального управления
Front Pediatr.2019; 7: 142.
, 1, 2 , 1, 3, 4 и 1, 2, 3, 4, 5,
64 *
4 Сайма Аслам
1 Педиатрия, Национальный родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
Тэмми Стрикленд
1 Педиатрия, Национальный родильный дом , Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити-колледж в Дублине, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Больница Университета Кумб для женщин и младенцев, Дублин, Ирландия
Элеонора Дж. .Моллой
1 Педиатрия, Национальный родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити College Dublin, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Университетская больница для женщин и младенцев Кумб, Дублин, Ирландия
5 Неонатология, Детская больница Богоматери, Дримна, Ирландия
1 Педиатрия, национальная Родильный дом, Дублин, Ирландия
2 Школа медицины и медицинских наук UCD, Университетский колледж Дублина, Дублин, Ирландия
3 Институт трансляционной медицины Тринити-колледжа, Академическая педиатрия, Тринити-колледж Дублина, Национальная детская больница, Дублин, Ирландия
4 Педиатрия, Coombe Women’s и больница Университета младенцев, Дублин, Ирландия
5 Неонатология, Детская больница Богоматери, Дримна, Ирландия
Отредактировал: Микко Холлман, Университет Оулу, Финляндия
Рецензент: Георг Шмольцер, Университет Альберты, Канада; Аакаш Пандита, Институт медицинских наук им. Санджая Ганди, Индия
Эта статья была отправлена в раздел «Неонатология» журнала «Границы в педиатрии»
Поступила в редакцию 15 октября 2018 г .; Принят в печать 26 марта 2019 г.
Авторские права © 2019 Aslam, Strickland and Molloy.
Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License (CC BY). Использование, распространение или воспроизведение на других форумах разрешено при условии указания автора (авторов) и правообладателя (ов) и ссылки на оригинальную публикацию в этом журнале в соответствии с принятой академической практикой. Запрещается использование, распространение или воспроизведение без соблюдения этих условий.
Эта статья цитируется в других статьях в PMC.
Abstract
Неонатальная энцефалопатия (NE) связана с высокой смертностью и заболеваемостью. Факторы, предрасполагающие к NE, могут быть антенатальными, перинатальными или их комбинацией. Антенатальные материнские факторы, семейные факторы, генетическая предрасположенность, гипоксическая ишемическая энцефалопатия, инфекции, плацентарные аномалии, тромбофилия, дефекты коагуляции и метаболические нарушения — все это вовлечено в патогенез NE. В настоящее время терапевтическая гипотермия — единственное доступное лечение, независимо от этиологии.Распознавание этиологии вовлеченного НЭ может также помочь в проведении таких исследований, как метаболические исследования и обследования на сепсис, для обеспечения оптимального лечения. Понимание этиологии NE может позволить разработать целевую дополнительную терапию, связанную с основным механизмом, и разработать превентивные стратегии.
Ключевые слова: неонатальная энцефалоптия, этиология, антенатальная, перинатальная, таргетная дополнительная терапия
Введение
Неонатальная энцефалопатия (НЭ) — сложное заболевание новорожденных, характеризующееся измененным уровнем сознания, судорогами, плохим тонусом. для инициирования или поддержания дыхания (1) и связан с полиорганной дисфункцией (2).Заболеваемость NE оценивается в 3 случая на 1000 живорождений (3). NE может быть результатом широкого спектра причин и является клиническим термином, не определяющим этиологию. Единственное доступное лечение — это терапевтическая гипотермия (ТГ) с максимальной пользой, если начать в первые 6 часов жизни (4). Существует несколько причин НЭ, таких как гипоксическая ишемическая энцефалопатия (ГИЭ), перинатальные инфекции, аномалии плаценты, метаболические нарушения, коагулопатии и сосудистый инсульт новорожденных (). Однако более чем в половине случаев причина НЭ остается неустановленной (5).
Многофакторная этиология неонатальной энцефалопатии. Многие факторы предрасполагают к возникновению неонатальной энцефалопатии либо по отдельности, либо в комбинации, включая (A) Факторы риска до зачатия, (B) Сопутствующие заболевания или события у матери до родов / во время родов, (C) Патология плаценты, (D) Гипоксия-ишемия, (E) Перинатальная инфекция, (F) Неонатальный инсульт или тромбофилия, (G) Метаболические нарушения и (H) Генетические и эпигенетические аномалии.ПРОМ, длительный разрыв плодных оболочек; ЗВУР, ограничение внутриутробного развития.
Использование термина NE vs. HIE противоречиво. Было предложено использовать термин NE для доношенных и поздних недоношенных новорожденных, у которых не было выявленных дозорных событий (6, 7). Трудно доказать наличие церебральной гипоксической ишемии, за исключением моделей на животных и конкретных случаев неонатального инсульта. Все текущие параметры, включая pH и судороги, неспецифичны (7). Некоторые из паттернов черепно-мозговых травм, наблюдаемых у пациентов с NE, могут быть воспроизведены на животных моделях с помощью гипоксии-ишемии, но это не доказывает, что все NE вызваны HIE (7).Несколько опубликованных популяционных исследований показали, что факторы риска до родов и неасфиксии связаны с НЭ (6). Напротив, некоторые авторы утверждают, что ГИЭ является причиной НЭ в 50–80% случаев на основании клинических критериев, критериев ЭЭГ и МРТ (1). Поэтому в этом обзоре мы использовали термин NE, и мы стремились изучить различные этиологии, связанные с NE.
Материнские факторы
Материнская гипертензия (16%) была важным фактором дородового риска НЭ в реестре неонатальной энцефалопатии Оксфордской сети штата Вермонт ( n = 4 165).Также была более высокая частота клинического хориоамнионита, длительного разрыва плодных оболочек и гипотиреоза матери. Хотя острый асфиксический эпизод был зарегистрирован в 15% случаев, связь с воспалением была обнаружена у 24% (5).
Популяционное исследование в Западной Австралии показало, что социально-экономический статус, семейный анамнез судорог, неврологические проблемы и зачатие после лечения бесплодия были независимыми факторами риска до зачатия для NE ( n = 164) (8).Заболевание щитовидной железы матери, кровотечение во время беременности, вирусные заболевания, преэклампсия, аномальная плацента, задержка внутриутробного развития и переношенность были другими важными факторами риска в дородовой период (8). Идентифицируемые дородовые факторы риска НЭ были обнаружены в 69% случаев, внутриродовые факторы риска — в 5%, как дородовые, так и во время родов — в 24% и отсутствие фактора риска — в 2%. Только в 4% случаев внутриродовая гипоксия была выявлена без каких-либо факторов риска до родов или до зачатия (9). Было обнаружено, что ограничение роста в развитых странах и беременность двойней в развивающихся странах связаны с НЭ.Заболевание щитовидной железы у матери, дородовое наблюдение, инфекция, роды и тактика ведения родов должны стать важными модификаторами в исследовании 27 новорожденных с НЭ и 100 детей контрольной группы (3). Дородовые (74 против 18%), внутриродовые (67 против 19%) и острые внутриродовые события (33 против 2%) более вероятны у младенцев с НЭ по сравнению с контрольной группой. Следовательно, в неонатальном клиническом анамнезе подробный материнский анамнез важен и может быть путем к профилактическим стратегиям в будущем.
Из 45 новорожденных с NE 36% имели дозорные эпизоды, 40% имели хориоамнионит и 11% имели оба этих заболевания.Если данные дозорных событий были исключены, то возраст матери> 35 лет (ОР 2,5; 95% ДИ 1,1–5,6) и инфекция мочевыводящих путей во время беременности (ОР 2,6; 95% ДИ 1,0–6,5) были потенциальными факторами дородового риска для NE (10).
Гипоксия-ишемия
Хотя концепция гипоксии-ишемии четко выражена в моделях на животных, она может не подходить для использования во всех случаях неонатальной NE у человека. «Дозу» и продолжительность гипоксии, а также степень ишемии можно напрямую измерить на животной модели.Однако у новорожденных людей это неизвестно, если нет контрольного события, и впоследствии не используются суррогатные маркеры гипоксии. Badawi et al. показали, что асфиксия во время родов считается сопутствующим фактором в 29% случаев НЭ и самостоятельным фактором только в 4% случаев (9). Было обнаружено, что внутриродовая гипоксия-ишемия является одним из факторов, способствующих развитию НЭ в 30% случаев в развитых и 60% в развивающихся странах (3). Американский колледж акушеров и Американская академия педиатрии определили дозорное событие в своем документе о неонатальной энцефалопатии и неврологических исходах (Obstet Gynecol 2014).Следующее соответствует острому пери- или интранатальному событию: дозорное гипоксическое или ишемическое событие, возникающее непосредственно перед или во время родов и родоразрешения, например разрыв матки или тяжелая отслойка плаценты; паттерны пульсометра плода, соответствующие острым послеродовым или интранатальным событиям; сроки и тип травм головного мозга, основанные на исследованиях изображений, согласующихся с этиологией острого послеродового или внутриродового события, и отсутствуют доказательства других проксимальных или дистальных факторов, которые могли бы быть способствующими факторами.Кроме того, сочетание низких баллов по шкале Апгарса, ацидемии, аномального кардиотокографа, изменений МРТ, согласующихся с гипоксией-ишемией и полиорганной дисфункцией, — все это связано с гипоксически-ишемической этиологией, но в равной степени может быть изменено сепсисом или другими причинами NE. Асфиксичные родовые явления и воспаление присутствовали только в 12,6% случаев церебрального паралича (11). У новорожденных с NE ( n = 405) следующие факторы были независимо связаны с NE ( p -значение = 0,001), включая: только 1 дородовой период (гестационный возраст> 41 недели) и 7 факторов во время родов, включая длительный разрыв плодных оболочек, аномальные кардиотокограф, густой меконий, дозорные события, дистоция плеча, тугая затылочная пуповина и отказ вакуума (12).В когорте из 26 новорожденных с дозорными событиями NE (ОР 74,9, 95% ДИ 11,9-бесконечность, p <0,001) и отслеживание ЧСС плода категории 3 (28,0% против 4,0%, p = 0,002) были сильно связанный с NE (13). В когорте из 45 новорожденных у 36% были дозорные события, а у 11% были как дозорные, так и хориоамнионит (10).
Нейровизуализация с использованием магнитно-резонансной томографии, традиционной, диффузионной и спектроскопии в период от 24 до 96 часов жизни дает полезные рекомендации относительно возможных сроков возникновения церебрального инсульта, особенно диффузных аномалий.Аномалии, вызванные травмой головного мозга, становятся наиболее очевидными через 7 дней при использовании качественной МРТ, диффузии и спектроскопии. Глубокое ядерное серое вещество или водораздел кортикального повреждения развиваются по четко определенному типу повреждения мозга и типичны для гипоксически-ишемического повреждения мозга у новорожденного. Генетические и метаболические причины могут быть исследованы, если на МРТ существует другая картина травмы головного мозга или эволюция травмы. Признаки того, что послеродовая гипоксия-ишемия не была причиной НЭ, предлагаются на МРТ: порэнцефалия, очаговый артериальный инфаркт, венозный инфаркт, изолированное внутрипаренхиматозное или внутрижелудочковое кровоизлияние или атипичные паттерны метаболических энцефалопатий.
При NE, связанном с острым дозорным событием (HIE), типичная картина повреждения на МРТ показала вовлечение базальных ганглиев, таламуса с ассоциированной задней конечностью внутренней капсулы и, в тяжелых случаях, вовлечение ствола мозга (14). При NE без задокументированного дозорного события вовлечение базальных ганглиев или таламуса (BGT) также связано с изменениями белого вещества в 50% случаев (14). BGT с обширным повреждением белого вещества (WM) был обнаружен в 14%, BGT с WM от легкой до умеренной — в 56%, изолированное таламическое повреждение — в 5%, умеренное повреждение WM — только у 2% и легкое WM или нормальное — у 23% в 48%. младенцы с ГИЭ.Внутренняя капсула была аномальной у 93% пациентов с умеренным и тяжелым повреждением WM и была связана со смертью и ХП у 86% пациентов (15).
Картина повреждения головного мозга может указывать на возможную причину, например, повреждение коркового вещества и белого вещества (очаговое / мультифокальное) может быть связано с плацентарной недостаточностью и хориоамнионитом. Ранняя категоризация пациентов в соответствии с типом травмы головного мозга может привести к другому терапевтическому подходу, поскольку на животных моделях было показано, что разные уровни гипотермии защищают от повреждения коры головного мозга или глубокого серого вещества, поэтому для получения максимальной пользы могут потребоваться специфические для пациента протоколы гипотермии.Точно так же в моделях на животных разные режимы охлаждения, системное и селективное, приводят к разной температуре мозга (16).
Трудно окончательно установить наличие, продолжительность и степень гипоксии и ишемии у новорожденных, поэтому использовались суррогатные маркеры, такие как pH и судороги (7). Следовательно, биомаркеры мультиорганного поражения могут быть полезны для диагностики или оценки тяжести гипоксической ишемии и прогнозирования исхода при NE. Сердечный тропонин является маркером ишемии миокарда у новорожденных и детей и высвобождается из миоцитов после повреждения их мембраны.Сердечный тропонин I (cTnI) был значительно выше у новорожденных с ГИЭ в первые 48 часов по сравнению с контрольной группой ( p <0,0005) (17). Сердечный TnI был повышен у новорожденных с более высокой степенью НЭ и у тех, кому потребовались инотропы (18). Пороговое значение <0,22 нг / мл для нормотермических и <0,15 нг / мл для гипотермических младенцев с NE предсказывало нормальный исход развития нервной системы (19).
Гипоксия приводит к усилению эритропоэза и выбросу незрелых ядерных эритроцитов (nRBC) в кровоток (20).ЯРБК пуповинной крови были значительно выше у новорожденных, подвергшихся асфиксии, по сравнению с контрольной группой, а также коррелировали с апгаром через 1 мин, pH и развитием NE (20). Количество ядерных эритроцитов на 100 лейкоцитов было выше у новорожденных с НЭ по сравнению с контрольной группой, младенцев с НЭ средней / тяжелой или легкой степени ( p = 0,016) и у новорожденных с плохим исходом нервного развития ( p = 0,03) 21). Следовательно, стандартизованное измерение воздействия клинической гипоксии было бы полезным с использованием комбинации этих маркеров и могло бы помочь в определении времени инсульта и корреляции с доклиническими моделями на животных.
Инфекция
Риск спастического церебрального паралича (ДЦП) и квадриплегического ДЦП повышался при сочетании инфекции и асфиксии (22). Уровни интерлейкина (ИЛ) -6 через 6 часов связаны с отклонениями от нормы неврологического обследования (23). NE, инотропная поддержка, судороги без менингита, потребность в интубации и более низкий 5-минутный апгар были более вероятны у новорожденных с ХП при наличии инфекции у матери по сравнению с ХП без инфекции (22).
Материнские и ранние неонатальные инфекции представляют собой диагностическую проблему.Ведутся споры о том, может ли скрытая инфекция, не обнаруживаемая обычными методами культивирования, быть связана с неврологическим повреждением во всех возрастных группах. Полимеразная цепная реакция (ПЦР) выявила 11 случаев бактериемии у энцефалопатических новорожденных в Африке, у которых был отрицательный результат посева крови (NE n = 201). ПЦР в сочетании с посевом крови привела к обнаружению бактериальных продуктов в 8,9% случаев НЭ по сравнению с 3,1% при использовании одного посева крови (24). В метаанализе стрептококк группы B (GBS) был связан с NE в 0.58% случаев и смертность были выше при использовании СГБ плюс НЭ по сравнению с одним НЭ (25). В когорте из 45 новорожденных 40% имели хориоамнионит и 11% имели как дозорные события, так и хориоамнионит (10).
Терапевтическая гипотермия задерживает рост и пик ответа с-реактивного белка (СРБ), а также приводит к снижению количества лейкоцитов и нейтрофилов по сравнению с нормотермными новорожденными (26). Это влияние гипотермии на задержку развития естественных воспалительных маркеров следует учитывать при выборе лечения антибиотиками и продолжительности лечения новорожденных с НЭ.
Следовательно, полное обследование на сепсис имеет важное значение у всех детей с НЭ. Стандартных рекомендаций по выполнению люмбальной пункции во всех случаях НЭ не существует, и их можно выбирать в каждом конкретном случае. Кандидатами могут быть младенцы с повышенным WCC и CRP или факторами риска септического риска. Существуют также технические и практические проблемы для поясничной пункции у младенцев с NE, которые являются ригидными из-за TH, а также часто изначально имеют отек мозга при ультразвуковом исследовании черепа.
Аномалии плаценты
Поражение пуповины, хориоамнионит, васкулит плода, меконий хориональной пластинки и тромботическая васкулопатия плода часто встречались в плацентарных поражениях у пациентов с NE ( n = 23) (27).Поражения плаценты, указывающие на тромбоз и снижение фетоплацентарного кровотока, являются значимыми и независимыми факторами риска НЭ ( n = 93) (28). Наличие более одного поражения плаценты увеличивает вероятность НЭ, но не было никакой корреляции между патологией плаценты и картиной повреждения на МРТ ( n = 56) (29). Аномальная патология плаценты была обнаружена у 29% новорожденных с дозорными событиями и у 73% младенцев без дозорных явлений ( p = 0,0001), перенесших терапевтическую гипотермию (30).Воспалительные поражения плаценты чаще наблюдались у новорожденных без дозорных событий ( p = 0,002) (30). Хронический виллит был связан с повреждением базальных ганглиев (BGT), тогда как наличие ядерных эритроцитов, снижение созревания плаценты и хронический виллит также приводили к повреждению белого вещества / водораздела вместе с вовлечением BGT ( n = 95) (31).
Доказательства связи хориоамнионита с НЭ разнообразны. Предполагается, что время инфицирования и степень воспалительного ответа могут привести либо к прекондиционированию, либо к сенсибилизации и могут вызвать либо защитный эффект, либо дальнейшее усиление перинатального повреждения головного мозга, соответственно (32).Этот эффект был продемонстрирован на животных моделях. Липополисахарид (ЛПС), вводимый за 4–6 ч до 20 и 50 мин воздействия HI, приводил к усилению травм головного мозга. Однако введение LPS за 24 часа до 50-минутного воздействия HI привело к значительному ослаблению травм головного мозга (32). КА выявлена у 8 новорожденных с признаками перинатальной асфиксии (всего n = 23) (27). Младенцы с NE и TH имели более высокие шансы на наличие CA по сравнению с младенцами, которые не получали TH ( n = 98) (33).CA, васкулит и фунизит были связаны с NE степени I, виллитом с NE II и фунизитом с III степенью у 141 новорожденного с NE и 309 контрольных (29). CA был связан с более низким риском черепно-мозговой травмы и плохим когнитивным исходом по сравнению с не-CA (скорректированный OR 0,3; 95% CI 0,1–0,7, p = 0,004) у новорожденных с NE ( n = 258), хотя только У 20 новорожденных были гистологические доказательства СА. В той же когорте новорожденные с признаками сепсиса имели более высокие шансы на повреждение водораздела и аномальные нейромоторные показатели, чем у новорожденных без каких-либо клинических признаков ( p = 0.007) (34). У 120 младенцев с сочетанием перинатального ацидоза, NE и хориоамнионита с ответом плода или без него и пятнистый / диффузный хронический виллит были независимо связаны с тяжестью NE (35). Единственным индивидуальным предиктором патологического исхода нервного развития через 22-24 месяца после терапии гипотермией был диффузный хронический виллит. Гистологическая CA имела низкую прогностическую ценность для развития энцефалопатии и смерти у NE ( n = 51) (36), но материнская лихорадка ( n = 336) во время родов была независимым фактором для NE (скорректированное OR 4.72, 95% ДИ 1,28–17,4) (37). Клинический хориоамнионит был связан с более высокими уровнями IL-6, IL-8 в пуповинной крови и регулировался активацией нормальных Т-клеток, экспрессируемых и секретируемых (RANTES) в NE ( n = 61). В когорте из 67 новорожденных с хориоамнионитом NE, независимо от того, были ли клинические или гистологические данные связаны со стойким метаболическим ацидозом, это может предсказать плохой неврологический исход (38).
Патология плаценты описывается как «черный ящик» беременности. Стандартизированная классификация результатов патологии плаценты важна для дальнейшего определения этиологии NE (39).
Нарушения обмена веществ
Нарушения обмена веществ являются редкими причинами НЭ, но их всегда следует учитывать. Врожденные нарушения метаболизма (ВЭМ) присутствуют в неонатальном периоде после нормального периода выздоровления и отсутствия признаков перинатальной асфиксии, но неврологические и полиорганные поражения могут проявляться как НЭ (40). Митохондриальные нарушения также являются важной причиной НЭ (41).
Амплитудная интегрированная электроэнцефалограмма (аЭЭГ) была отклонена от нормы у 27 новорожденных с ВЭМ, причем наиболее устойчивыми признаками были аномальная фоновая активность и судороги.Не было различий в аЭЭГ для энцефалопатии, связанной с IEM или NE, и дифференцировать можно было только на основании клинического подозрения (42). Единственное метаболическое расстройство с диагностической ЭЭГ — это некетотическая гиперглицинемия с первоначальным паттерном «подавление-всплеск», переходящим в гипсаритмию в раннем или среднем младенчестве и диагностируемое путем измерения уровня глицина в спинномозговой жидкости (42). Имеются также отдельные сообщения о случаях ИЭМ, таких как дефицит сульфитоксидазы и цитохрома С, проявляющийся как НЭ (43, 44).
Результаты МРТ могут варьироваться в зависимости от типа врожденной ошибки метаболизма (ВЭМ) и могут варьироваться от поражения белого вещества до поражения глубоких серых ядер. Митохондриальные энцефалопатии имеют симметричное двустороннее распределение и изначально могут быть диагностированы как NE (45). Следует учитывать метаболические нарушения, если нет явных явлений во время родов, стойкий лактоацидоз и / или гипогликемия (45) и начато обследование. Различные паттерны повреждений на МРТ головного мозга могут помочь дифференцировать метаболические нарушения от НЭ.Поражение Globus Pallidus часто встречается при IEM по сравнению с NE, хотя картина повреждения при дефиците сульфитоксидазы и дефиците фактора молибдена может имитировать NE (46).
Изолированные приступы связаны с такими расстройствами, как: судороги, связанные с пиридоксином, некетотическая гиперглицинемия (НКГ), дефицит дигидропиримидиндегидрогеназы, дефицит сульфитоксидазы (либо изолированный, либо как часть дефицита кофактора молибдена), трансаминазы 4-аминобутират-аминотрансферазы (ГАБТрансферазы). ) дефицит, судороги, связанные с фолиевой кислотой, дефицит 3-фосфоглицератдегидрогеназы, дефицит гуанидиноацетатметилтрансферазы (GAMT) и дефицит переносчика глюкозы (GLUT-1).У младенцев с полиорганными поражениями, судорогами, метаболическим ацидозом, молочной железой, гипераммониемией могут быть: органическая ацидемия, дефекты цикла мочевины, пероксисомальные нарушения (например, синдром Зеллвегера) или митохондриальные нарушения.
Подробный семейный анамнез для установления факторов риска, таких как родство родителей или ранее пораженный ребенок, важен, поскольку большинство врожденных нарушений метаболизма имеют аутосомно-рецессивное или материнское наследование. Базовые исследования, такие как электролиты, аммиак, сывороточные аминокислоты, лактат, ацилкарнитин и органическая кислота в моче, могут быть рассмотрены при NE (40).Есть проблемы с метаболическим тестированием, так как их может потребоваться повторить, если ребенок очень плохо себя чувствует с полиорганной дисфункцией во время отбора образцов (46). Недавние исследования показали большой потенциал метаболомики как биомаркеров NE. Было показано, что содержание сукцината повышено у детей с НЭ, которые серьезно пострадали (47).
Тромбофилия и неонатальный инсульт
Асфиксия (в 4% случаев) участвует в патогенезе неонатального инсульта (48). Фокальные клонические приступы являются наиболее частым проявлением неонатального инсульта (49), и 6 младенцев с инсультом были обнаружены в когорте NE ( n = 124) (50).Эти дети обычно страдали судорогами и имели худшие исходы с точки зрения нервного развития, чем остальная когорта. Нарушения свертывания крови, такие как полицитемия, лейденский фактор V, нарушения гемоглобина и мутации протромбина, не были обнаружены у 4 из 6 обследованных пациентов (50).
В моделях на животных повышенные уровни гомоцистеина приводили к увеличению провоспалительных цитокинов, таких как фактор некроза опухоли альфа (TNFα), интерлейкин 1 бета (IL-1β) и IL-6 в гиппокампе и коре головного мозга.Это провоспалительное состояние может быть ответственным за нейрональные и цереброваскулярные эффекты, наблюдаемые у взрослых (51). Роль гомоцистеина или полиморфизмов в гене метилентетрагидрофолатредуктазы в возникновении неонатального повреждения головного мозга неясна (52). В когорте из 118 новорожденных с НЭ повреждение белого вещества / водораздела с большей вероятностью было связано с гипогликемией, полиморфизмом метилентетрагидрофолатредуктазы (MTHFR) и уровнями гомоцистеина в плазме в верхнем квартиле нормы (52).
Генетические и эпигенетические аномалии
Отсутствуют опубликованные данные, связывающие генетическую предрасположенность с развитием NE. У 40 пациентов с NE генетическая изменчивость протромбических факторов, таких как протромбин G20210A, фактор V Leiden G1691A и метилентетрагидрофолатредуктаза [MTHFR] C677T, и ген фактора некроза опухоли не повлияли на оценку NE, ЭЭГ, смерть, краниальное УЗИ (США) , неврологический исход при выписке через 6 и 12 месяцев. Полиморфизм гена интерлейкина-6 (IL-6 174GC) имел защитный эффект и был связан с нормальной ЭЭГ, краниальным УЗИ и неврологическим обследованием при выписке (53).В ретроспективном исследовании «случай-контроль» с участием 11 новорожденных с NE у матерей была обнаружена более высокая частота полиморфизма MTHFR (7 гомозиготных и 4 гетерозиготных) по сравнению с контрольной группой (54). Генетический полиморфизм может увеличивать риск или тяжесть неонатального повреждения головного мозга при NE, и его следует учитывать (53).
В рамках лонгитюдного исследования родителей и детей, проведенного Avon, было проведено генотипирование 7611 доношенных детей, и мерилом воздействия было наличие одного или нескольких минорных аллелей в одном из 3 SNP (rs2284411, rs2498804, rs1835740).Первичным результатом была необходимость реанимации при рождении, что было связано с rs1835740 (55). Требуются более крупные международные совместные исследования для определения необходимого количества пациентов для изучения генетических связей и разделения пациентов по этиологии.
Другая категория младенцев с генетической причиной неонатальной энцефалопатии — это дети с миопатиями и энцефалопатиями новорожденных. Пациенты, унаследовавшие миопатию (центронуклеарную миопатию), могут иметь неонатальный дистресс, гипотонию и признаки, указывающие на ГИЭ (56).Врожденная миотоническая дистрофия 1 типа характеризуется гипотонией и тяжелой генерализованной слабостью при рождении, часто с дыхательной недостаточностью, умственной отсталостью и ранней смертью. Это вызвано экспансией тринуклеотидного повтора CTG в некодирующей области DMPK .
В будущем подробное генотипирование, включая более легкий доступ к методам микроматриц в клинических условиях, предоставит больше информации, позволяющей индивидуализированный уход и потенциально классифицировать младенцев по генотипу.
Нейровизуализация
На МРТ можно увидеть различные модели травм, но это не исключает HIE как причины травмы. Характер повреждения зависит от тяжести, продолжительности и повторяемости гипоксической ишемии и может привести к поражению базальных ганглиев, таламуса, ствола мозга и / или белого вещества головного мозга в различных сочетаниях (1). При глубокой гипоксии преобладает повреждение более глубоких серых структур, то есть базальных ганглиев и таламуса. Объясняется это тем, что эти участки миелинизированы и имеют более высокую скорость метаболизма.Состояния, которые уменьшают, а не вызывают полное прекращение кровотока, такие как анемия и гиповолемия, связаны с повреждением коры головного мозга и сохранением более глубоких серых структур (57). В когорте из 245 пациентов с NE 197 (80%) результаты МРТ соответствовали острому перинатальному инсульту. МРТ у 40 младенцев (16%) были нормальными. У 9 младенцев (4%) были выявлены признаки тромбоза / инфаркта, генетических нарушений, антенатального инсульта и митохондрий (дефицит комплекса I) на МРТ в дополнение к гипоксическому ишемическому инсульту.Нейровизуализация у 8 (3%) младенцев с клиническим диагнозом НЭ показала либо врожденную ошибку метаболизма, нервно-мышечное расстройство, либо отсутствие диагноза, и эти результаты не соответствовали гипоксической ишемии (48). Плацентарный виллит высокой степени неизвестной этиологии ( n = 4) был обнаружен в когорте из 36 пациентов, связанных с повреждением белого вещества, вторичным по отношению к воспалению / окислительному стрессу в перинатальном периоде (58).
Значение для терапии
Все младенцы с NE могут не в одинаковой степени выиграть от переохлаждения.Следовательно, выявление точной этиологии в каждом случае NE имеет значение для лечения, поскольку есть некоторые излечимые причины, которые требуют быстрого определения для оптимального лечения. Использование бактериальной ПЦР для выявления инфекции у новорожденных с NE может быть более полезным, чем только посев крови с низким выходом бактерий, а также гипотермия может уменьшить воспалительную реакцию. Гистология плаценты отражает внутриматочную среду и может прояснить основную этиологию. Все новорожденные с риском IEM должны быть обследованы на предмет метаболических нарушений, так как этим пациентам могут быть полезны специфические методы лечения, а не гипотермия.Точно так же скрининг на тромбофилию следует рассматривать у пациентов из группы риска, таких как пациенты с инсультом, семейный анамнез тромбофилии. Подробная оценка этиологии NE важна для выявления излечимых причин и категоризации этой гетерогенной группы новорожденных, чтобы можно было подобрать соответствующее лечение в соответствии с этиологией и улучшением отдаленных результатов. Точно так же будет полезно стратифицировать большие многоцентровые когорты младенцев с NE по этиологии, чтобы полностью понять этиологию, реакцию на лечение гипотермией и отдаленные результаты.
Авторские взносы
SA: основной автор; ТС: помогал с поиском релевантных статей и рисунка; ЭМ: автор-руководитель.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Ссылки
1. Volpe JJ. Неонатальная энцефалопатия: неадекватный термин для гипоксически-ишемической энцефалопатии.Энн Нейрол. (2012) 72: 156–66. 10.1002 / ana.23647 [PubMed] [CrossRef] [Google Scholar] 2. Шах П., Рип Хаген С., Бейен Дж, Перлман М. Мультиорганная дисфункция у младенцев с постасфиксиальной гипоксически-ишемической энцефалопатией. Arch Dis Child Fetal Neonatal Ed. (2004) 89: F152 – F155. 10.1136 / adc.2002.023093 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 3. Куринчук Дж. Дж., Уайт-Конинг М., Бадави Н. Эпидемиология неонатальной энцефалопатии и гипоксически-ишемической энцефалопатии. Early Hum Dev. (2010) 86: 329–38.10.1016 / j.earlhumdev.2010.05.010 [PubMed] [CrossRef] [Google Scholar] 4. Джейкобс С.Е., Берг М., Хант Р., Тарнов-Морди В.О., Индер Т.Э., Дэвис П.Г.
Охлаждение новорожденных с гипоксической ишемической энцефалопатией. База данных Cochr Syst Rev. (2013) 1: CD003311
10.1002 / 14651858.CD003311.pub3 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 5. Нельсон К.Б., Бингхэм П., Эдвардс Э.М., Хорбар Д.Д., Кенни М.Дж., Индер Т. и др. . Антецеденты неонатальной энцефалопатии в реестре энцефалопатии Оксфордской сети Вермонта. Педиатрия.(2012) 130: 878–86. 10.1542 / peds.2012-0714 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 6. Нельсон КБ. Это HIE?
И почему это важно Acta Paediatr. (2007) 96: 1113–4. 10.1111 / j.1651-2227.2007.00364.x [PubMed] [CrossRef] [Google Scholar] 7. Дамманн О., Ферриеро Д., Грессенс П.
Неонатальная энцефалопатия или гипоксически-ишемическая энцефалопатия?
Соответствующая терминология имеет значение Pediatr Res. (2011) 70: 1-2. 10.1203 / PDR.0b013e318223f38d [PubMed] [CrossRef] [Google Scholar] 8. Бадави Н., Куринчук Дж. Дж., Кио Дж. М., Алессандри Л. М., О’Салливан Ф., Бертон П. Р. и др.. Факторы дородового риска энцефалопатии новорожденных: исследование случай-контроль в Западной Австралии. BMJ. (1998) 317: 1549–53. 10.1136 / bmj.317.7172.1549 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 9. Бадави Н., Куринчук Дж. Дж., Кио Дж. М., Алессандри Л. М., О’Салливан Ф., Бертон П. Р. и др. . Факторы риска внутриутробной энцефалопатии новорожденных: исследование случай-контроль в Западной Австралии. BMJ. (1998) 317: 1554–8. 10.1136 / bmj.317.7172.1554 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 10. Паркер SJ, Kuzniewicz M, Niki H, Wu YW.Факторы дородового и внутриродового риска гипоксически-ишемической энцефалопатии в когорте новорожденных в США. J Pediatr. (2018) 203: 163–9. 10.1016 / j.jpeds.2018.08.028 [PubMed] [CrossRef] [Google Scholar] 11. Адамсон С.Дж., Алессандри Л.М., Бадави Н., Бертон П.Р., Пембертон П.Дж., Стэнли Ф. Предикторы неонатальной энцефалопатии у доношенных новорожденных. BMJ. (1995) 311: 598–602
10.1136 / bmj.311.7005.598 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 12. Мартинес-Биарж М., Диез-Себастьян Дж., Вустхофф Си-Джей, Меркури Е., Коуэн FM.Дородовые и внутриродовые факторы, предшествующие неонатальной гипоксически-ишемической энцефалопатии. Педиатрия. (2013) 132: e952 – e959
10.1542 / peds.2013-0511 [PubMed] [CrossRef] [Google Scholar] 13. Торбенсон В.Е., Толчер М.К., Несбитт К.М., Колби К.Э., Эль-Нашар С.А., Гостоут Б.С. и др. . Внутриродовые факторы, связанные с неонатальной гипоксической ишемической энцефалопатией: исследование случай-контроль. BMC Беременность и роды. (2017) 17: 415
10.1186 / s12884-017-1610-3 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 14. Резерфорд М., Маламатениу К., МакГиннесс А., Оллсоп Дж., Биарж М.М., Конселл С.Магнитно-резонансная томография при гипоксически-ишемической энцефалопатии. Early Hum Dev. (2010) 86: 351–60. 10.1016 / j.earlhumdev.2010.05.014 [PubMed] [CrossRef] [Google Scholar] 15. Okereafor A, Allsop J, Counsell SJ, Fitzpatrick J, Azzopardi D, Rutherford MA и др. . Характер черепно-мозговой травмы у новорожденных, подвергшихся перинатальным дозорным событиям. Педиатрия. (2008) 121: 906–14. 10.1542 / peds.2007-0770 [PubMed] [CrossRef] [Google Scholar] 16. Мецлер М., Говиндан Р., Аль-Шаргаби Т., Везина Г., Андескавадж Н., Ван И и др.. Характер черепно-мозговой травмы и снижение вариабельности сердечного ритма у новорожденных с гипоксической ишемической энцефалопатией. Pediatr Res. (2017) 82: 438–43. 10.1038 / pr.2017.94 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 17. Симович AM, Игрутинович З., Обрадович С., Ристич Д., Вулетич Б., Раданович М. Значение сердечного тропонина I второго поколения в раннем скрининге гипоксически-ишемической энцефалопатии после перинатальной асфиксии. Srp Arh Celok Lek. (2012) 140: 600–5. [PubMed] [Google Scholar] 18. Шастри А.Т., Самарасекара С., Мунираман Х., Кларк П.Концентрации сердечного тропонина I у новорожденных с гипоксически-ишемической энцефалопатией. Acta Paediatr. (2012) 101: 26–9. 10.1111 / j.1651-2227.2011.02432.x [PubMed] [CrossRef] [Google Scholar] 19. Лю X, Chakkarapani E, Stone J, Thoresen M. Влияние компрессий сердца и лечения гипотермии на сердечный тропонин I у новорожденных с перинатальной асфиксией. Реанимация. (2013) 84: 1562–7. 10.1016 / j.resuscitation.2013.07.003 [PubMed] [CrossRef] [Google Scholar] 20. Гош Б., Миттал С., Кумар С., Дадхвал В. Прогнозирование перинатальной асфиксии с ядросодержащими эритроцитами в пуповинной крови новорожденных.Int J Gynaecol Obstet. (2003) 81: 267–71. 10.1016 / S0020-7292 (03) 00124-3 [PubMed] [CrossRef] [Google Scholar] 21. Уолш Б.Х., Бойлан Г.Б., Мюррей Д.М. Ядерные эритроциты и ранняя ЭЭГ: прогнозирование стадии Сарната и двухлетнего исхода. Early Hum Dev. (2011) 87: 335–9. 10.1016 / j.earlhumdev.2011.01.041 [PubMed] [CrossRef] [Google Scholar] 22. Нельсон КБ, Гретер Дж. Потенциально удушающие состояния и спастический церебральный паралич у младенцев с нормальной массой тела при рождении. Am J Obstet Gynecol. (1998) 179: 507–13. 10.1016 / S0002-9378 (98) 70387-4 [PubMed] [CrossRef] [Google Scholar] 23.Шалак Л.Ф., Лапток А.Р., Джафри Х.С., Рамило О., Перлман Дж. Клинический хориоамнионит, повышенные цитокины и травмы головного мозга у доношенных детей. Педиатрия. (2002) 110: 673–80. 10.1542 / peds.110.4.673 [PubMed] [CrossRef] [Google Scholar] 24. Танн CJ, Nkurunziza P, Nakakeeto M, Oweka J, Kurinczuk JJ, Were J и др. . Распространенность патогенов кровотока выше в случаях неонатальной энцефалопатии по сравнению с контрольной группой, использующей новую панель ПЦР-анализов в реальном времени. PLoS ONE. (2014) 9: e97259. 10.1371 / journal.pone.0097259 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 25.Танн С.Дж., Мартинелло К.А., Саду С., Лоун Дж.Э., Сил А.С., Вега-Поблете М. и др.
Группа исследователей неонатальной энцефалопатии GBS. неонатальная энцефалопатия со стрептококками группы b во всем мире: систематический обзор, наборы данных исследовательских групп и метаанализ. Clin Infect Dis. (2017) 65 (Suppl_2): S173–89. 10.1093 / cid / cix662 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 26. Chakkarapani E, Davis J, Thoresen M. Терапевтическая гипотермия задерживает ответ C-реактивного белка и подавляет количество лейкоцитов и тромбоцитов у младенцев с неонатальной энцефалопатией.Arch Dis Child Fetal Neonatal Ed. (2014) 99: F458 – F463. 10.1136 / archdischild-2013-305763 [PubMed] [CrossRef] [Google Scholar] 27. Wintermark P, Boyd T, Gregas MC, Labrecque M, Hansen A. Патология плаценты у новорожденных с асфиксией, отвечающая критериям терапевтической гипотермии. Am J Obstet Gynecol. (2010) 203: 579.e1–9. 10.1016 / j.ajog.2010.08.024 [PubMed] [CrossRef] [Google Scholar] 28. Макдональд Д.Г., Келехан П., Макменамин Дж.Б., Горман В.А., Мэдден Д., Тоббия И.Н. и др. . Плацентарная тромботическая васкулопатия плода связана с неонатальной энцефалопатией.Hum Pathol. (2004) 35: 875–80
10.1016 / j.humpath.2004.02.014 [PubMed] [CrossRef] [Google Scholar] 29. Hayes BC, Cooley S, Donnelly J, Doherty E, Grehan A, Madigan C и др. . Плацента у младенцев> 36 недель беременности с неонатальной энцефалопатией: исследование случай-контроль. Arch Dis Child Fetal Neonatal Ed. (2013) 98: F233–9. 10.1136 / archdischild-2012-301992 [PubMed] [CrossRef] [Google Scholar] 30. Чанг Т., Рейес Т.Дж., Пласетек Дж., Массаро А.Н., Нельсон КБ.
Неонатальная энцефалопатия, дозорные явления и плацента.J Neonatal Perinatal Med. (2012) 5: 41–8. 10.3233 / NPM-2012-54211 [CrossRef] [Google Scholar] 31. Хартеман Дж. К., Никкельс П. Г., Бендерс М. Дж., Кви А., Грюнендал Ф., де Фрис Л. С.. Патология плаценты у доношенных детей с гипоксически-ишемической неонатальной энцефалопатией и ассоциация с магнитно-резонансной томографией повреждения головного мозга. J Pediatr. (2013) 163: 968–995.
10.1016 / j.jpeds.2013.06.010 [PubMed] [CrossRef] [Google Scholar] 32. Эклинд С., Маллард С., Арвидссон П., Хагберг Х. Липополисахарид вызывает как первичную, так и вторичную фазу сенсибилизации в развивающемся мозге крысы.Pediatr Res. (2005) 58: 112–6
10.1203 / 01.PDR.0000163513.03619.8D [PubMed] [CrossRef] [Google Scholar] 33. Нельсон Д.Б., Лаке А.М., Макинтайр Д.Д., Санчес П.Дж., Левено К.Дж., Чалак Л.Ф. Акушерские предшественники лечения новорожденного с помощью охлаждения тела. Am J Obstet Gynecol. (2014) 211: 155.e1–6. 10.1016 / j.ajog.2014.02.013 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 34. Дженстер М., Бонифачо С.Л., Рюэль Т., Роджерс Е.Е., Там Э.У., Партридж Дж.С. и др.
Инфекция матери или новорожденного: связь с исходами неонатальной энцефалопатии.Pediatr Res. (2014) 76: 93–9. 10.1038 / pr.2014.47 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 35. Мир И.Н., Джонсон-Велч С.Ф., Нельсон Д.Б., Браун Л.С., Розенфельд С.Р., Чалак Л.Ф. Патология плаценты связана с тяжестью неонатальной энцефалопатии и неблагоприятными исходами развития после гипотермии. Am J Obstet Gynecol. (2015) 213: 849.e1–7. 10.1016 / j.ajog.2015.09.072 [PubMed] [CrossRef] [Google Scholar] 36. Шалак Л., Джонсон-Велч С., Перлман Дж. М.. Хориоамнионит и неонатальная энцефалопатия у доношенных детей с ацидемией плода: гистопатологические корреляции.Pediatr Neurol. (2005) 33: 162–5. 10.1016 / j.pediatrneurol.2005.04.005 [PubMed] [CrossRef] [Google Scholar] 37. Impey L, Greenwood C, MacQuillan K, Reynolds M, Sheil O. Лихорадка в родах и неонатальная энцефалопатия: проспективное когортное исследование. BJOG. (2001) 108: 594–7. 10.1111 / j.1471-0528.2001.00145.x [PubMed] [CrossRef] [Google Scholar] 38. Джонсон CT, Бурд I, Рагхунатан Р., Нортингтон Ф. Дж., Грэм Э.М. Перинатальное воспаление / инфекция и его связь с коррекцией метаболического ацидоза при гипоксически-ишемической энцефалопатии.J Perinatol. (2016) 36: 448–52. 10.1038 / jp.2015.221 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 39. Кларк П., Мунираман Х., Гарднер Д., Венкатеш В., Керли А., Виктор С. и др. . Исследование неонатальной энцефалопатии: часто теряемый плацентарный «черный ящик». Pediatr Dev Pathol. (2015) 18: 343–4. 10.2350 / 15-02-1611-LET.1 [PubMed] [CrossRef] [Google Scholar] 40. Tan ES. Врожденные нарушения обмена веществ, проявляющиеся как неонатальная энцефалопатия: практические советы клиницистам. Ann Acad Med Singapore. (2008) 37 (12 доп.): 94–3. [PubMed] [Google Scholar] 41. Узиэль Г., Геззи Д., Зевиани М. Инфантильная митохондриальная энцефалопатия. Semin Fetal Neonatal Med. (2011) 16: 205–15. 10.1016 / j.siny.2011.04.003 [PubMed] [CrossRef] [Google Scholar] 42. Олишар М., Шани Э., Айгюн С., Аззопарди Д., Хант Р.В., Тоет М.С. и др. . Амплитудно-интегрированная электроэнцефалография у новорожденных с врожденными нарушениями обмена веществ. Неонатология. (2012) 102: 203–11. 10.1159 / 000339567 [PubMed] [CrossRef] [Google Scholar] 43. Хобсон Э., Томас С., Крофтон П. М., Мюррей А. Д., Дин Дж. К., Ллойд Д.Изолированная недостаточность сульфитоксидазы имитирует признаки гипоксической ишемической энцефалопатии. Eur J Pediatr. (2005) 164: 655–9. 10.1007 / s00431-005-1729-5 [PubMed] [CrossRef] [Google Scholar] 44. Уиллис Т.А., Дэвидсон Дж., Грей Р.Г., Поултон К., Рамани П., Уайтхаус В. Дефицит цитохромоксидазы, проявляющийся как асфиксия при рождении. Dev Med Child Neurol. (2000) 42: 414–7. 10.1017 / S0012162200000761 [PubMed] [CrossRef] [Google Scholar] 45. Khong PL, Lam BC, Tung HK, Wong V, Chan FL, Ooi GC. МРТ неонатальной энцефалопатии.Clin Radiol. (2003) 58: 833–44. 10.1016 / S0009-9260 (03) 00261-7 [PubMed] [CrossRef] [Google Scholar] 46. Enns GM.
Врожденные нарушения обмена веществ, маскирующиеся под гипоксически-ишемическую энцефалопатию. NeoReviews. (2005) 12: e549 – e558. 10.1542 / neo.6-12-e549 [CrossRef] [Google Scholar] 47. Уолш Б.Х., Бродхерст Д.И., Мандал Р., Вишарт Д.С., Бойлан Г.Б., Кенни Л.С. и др. . Метаболомный профиль пуповинной крови при гипоксической ишемической энцефалопатии новорожденных. PLoS ONE. (2012) 7: e50520. 10.1371 / journal.pone.0050520 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 48.Коуэн Ф., Резерфорд М., Грюнендал Ф., Экен П., Меркури Э., Байддер Г.М. и др. . Происхождение и сроки поражения головного мозга у доношенных детей с неонатальной энцефалопатией. Ланцет. (2003) 361: 736–42
10.1016 / S0140-6736 (03) 12658-X [PubMed] [CrossRef] [Google Scholar] 49. Ян М.М., Camfield PR. Исход неонатального инсульта у доношенных детей без значительной асфиксии при рождении. Eur J Pediatr. (1998) 157: 846–8. 10.1007 / s004310050950 [PubMed] [CrossRef] [Google Scholar] 50. Рамасвами В., Миллер С.П., Баркович А.Дж., Партридж Дж.С., Ферриеро Д.М.Перинатальный инсульт у доношенных детей с неонатальной энцефалопатией. Неврология. (2004) 62: 2088–91. 10.1212 / 01.WNL.0000129909.77753.C4 [PubMed] [CrossRef] [Google Scholar] 51. Scherer EB, Loureiro SO, Vuaden FC, da Cunha AA, Schmitz F, Kolling J, et al. . Легкая гипергомоцистеинемия увеличивает уровни ацетилхолинэстеразы мозга и провоспалительных цитокинов в различных тканях. Mol Neurobiol. (2014) 50: 589–96. 10.1007 / s12035-014-8660-6 [PubMed] [CrossRef] [Google Scholar] 52. Harteman JC, Groenendaal F, Benders MJ, Huisman A, Blom HJ, de Vries LS.Роль тромбофильных факторов у доношенных детей с неонатальной энцефалопатией. Pediatr Res. (2013) 73: 80–6. 10.1038 / pr.2012.150 [PubMed] [CrossRef] [Google Scholar] 53. Calkavur S, Akisu M, Olukman O, Balim Z, Berdeli A, Cakmak B и др. . Генетические факторы, влияющие на краткосрочный исход развития нервной системы у доношенных новорожденных с гипоксически-ишемической энцефалопатией. J Int Med Res. (2011) 39: 1744–56. 10.1177 / 147323001103
7 [PubMed] [CrossRef] [Google Scholar] 54. Додельсон де Кремер Р., Гроссо С. Материнская мутация 677C> T в гене метилентетрагидрофолатредуктазы, связанная с тяжелым повреждением головного мозга у потомства.Clin Genet. (2005) 67: 69–80. [PubMed] [Google Scholar] 55. Odd D, Váradi A, Rajatileka S, Molnár E, Luyt K. Связь между реанимацией новорожденных и однонуклеотидным полиморфизмом rs1835740. Acta Paediatr. (2016) 105: e307–12. 10.1111 / apa.13421 [PubMed] [CrossRef] [Google Scholar] 56. Bruyland M, Liebaers I, Sacre L, Vandeplas Y, De Meirleir L, Martin JJ. Неонатальная миотубулярная миопатия с вероятным X-сцепленным наследованием: наблюдения за новой семьей с обзором литературы. J Neurol.(1984) 231: 220–2. 10.1007 / BF00313942 [PubMed] [CrossRef] [Google Scholar] 57. Баркович А.Дж., Вестмарк К., Партридж К., Сола А., Ферриеро Д.М. Перинатальная асфиксия: результаты МРТ в первые 10 дней. AJNR Am J Neuroradiol. (1995) 16: 427–38. [PubMed] [Google Scholar] 58. Barrett MJ, Donoghue V, Mooney EE, Slevin M, Persaud T., Twomey E, et al. . Изолированное острое некистозное повреждение белого вещества у доношенных детей с неонатальной энцефалопатией. Arch Dis Child Fetal Neonatal Ed. (2013) 98: F158 – F160. 10.1136 / archdischild-2011-301505 [PubMed] [CrossRef] [Google Scholar]
ГИЭ — Гипоксическая ишемическая энцефалопатия
Перинатальная гипоксически-ишемическая энцефалопатия (ГИЭ) — один из наиболее серьезных и опасных для жизни типов повреждения мозга младенцев, которое может возникают во время родов.ГИЭ возникает, когда поступление кислорода и крови в мозг ребенка ограничено или прервано во время родов (перинатальная асфиксия), что приводит к гибели клеток мозга через короткие промежутки времени.
Что такое гипоксическая ишемическая энцефалопатия (ГИЭ)?
ГИЭ — это очень серьезный тип повреждения мозга младенца, который возникает во время родов, когда мозг ребенка лишен крови и кислорода. Из-за недостатка крови и кислорода клетки головного мозга ребенка умирают в считанные минуты.
Энцефалопатия — это медицинское слово, которое используется для обозначения различных родственных состояний, возникающих в результате травмы головного мозга.Гипоксическая ишемическая энцефалопатия (ГИЭ) — это особый тип повреждения головного мозга, вызванный комбинацией (1) гипоксии — нарушения циркуляции кислорода; и (2) ишемия — ограничение кровотока. Перинатальный ГИЭ возникает, когда кровь и кислород, поступающие в мозг, одновременно снижаются или прекращаются во время родов или сразу после них. ГИЭ — относительно редкое событие, которое происходит примерно у 3 из 1000 рождений.
Что вызывает гипоксическую ишемическую энцефалопатию (ГИЭ)?
ГИЭ вызывается острой потерей притока крови и кислорода к мозгу ребенка во время родов или во время беременности.Недостаток кислорода и крови приводит к тому, что клетки развивающегося мозга ребенка быстро разлагаются, а затем умирают. Кислородная недостаточность, вызывающая ГИЭ, обычно вызвана акушерскими осложнениями во время родов и родоразрешения, но также может быть результатом пренатальных осложнений или событий. Осложнения, которые могут вызвать ГИЭ, включают:
Роды и Осложнения при родах:
Осложнения новорожденных:
Последствия ГИЭ
ГИЭ — чрезвычайно серьезный тип черепно-мозговой травмы.Несмотря на то, что это происходит менее чем в 0,05% всех рождений, ГИЭ является одной из ведущих причин младенческой смертности в США каждый год.
Помимо опасности для жизни, ГИЭ вызывает необратимое повреждение головного мозга. Примерно 15-20% новорожденных с диагнозом ГИЭ умрут в первую неделю. Из оставшихся выживших 25% получат необратимые повреждения головного мозга различной степени тяжести. Повреждения головного мозга в результате ГИЭ часто приводят к физическим недостаткам и когнитивным нарушениям.
У меньшего процента детей с ГИЭ хорошие результаты.Эти дети полностью выздоравливают и испытывают лишь легкие симптомы неврологической травмы, если таковые имеются. Нет данных о продолжительности жизни 80-85% детей с ГИЭ, как выживают в первую неделю жизни. Но очевидно, что в тяжелых случаях это влияет на прогнозируемую продолжительность жизни.
Симптомы ГИЭ
Симптомы ГИЭ сразу после рождения будут существенно различаться в зависимости, главным образом, от тяжести основного повреждения головного мозга:
Легкая ГИЭ
- Сухожильные рефлексы ненормальны, а мышцы жесткие в первые несколько дней
- Сильная раздражительность, проблемы с кормлением, чрезмерный плач или сон
- Симптомы легкой ГИЭ часто проходят в течение нескольких недель
Умеренная ГИЭ
- Отсутствие мышечного тонуса (синдром гибкого ребенка) с отсутствием рефлексов
- Невозможно хватка и плохой сосательный рефлекс
- Спорадическое апноэ
- Припадки (обычно в течение первого дня)
Тяжелая ГИЭ
- Экстремальные приступы, частота которых увеличивается в первые 2 дня
- Не реагирует на внешние раздражители
- Нерегулярное дыхание
- Крайняя гипотония (как тряпичная кукла)
- Abno нормальный контроль глаз или движение с расширенными зрачками
- Аномальная частота сердечных сокращений и артериальное давление
- Кардиореспираторная недостаточность (часто со смертельным исходом)
Лечение ГИЭ
Основное лечение ГИЭ, набирающее обороты в последние годы, — охлаждение тела и головы.Это лечение обычно называют терапевтическим переохлаждением. Лечебная гипотермия направлена на снижение температуры тела ребенка ниже нормы сразу после рождения. Это эффективно замедляет процессы распада и повреждения клеток в головном мозге. Замедляя этот процесс, терапия гипотермии направлена на минимизацию долгосрочного воздействия ГИЭ. К сожалению, повреждение мозга от гипоксии новорожденного носит постоянный характер и не может быть просто исправлено хирургическим вмешательством или лекарствами. Итак, ОТО — это постоянная травма.Варианты лечения включают терапию и лекарства, которые помогают справиться с последствиями любого повреждения головного мозга. Младенцы с тяжелыми травмами ГИЭ часто нуждаются в пожизненной поддержке и приспособлении.
Но есть также удивительные истории выздоровления от ГИЭ, когда ребенок получил необратимую травму с фантастическим исходом. Истории успеха после ОТО не редкость. В конце концов, масштабы травмы ребенка, а это не утешение для родителей, часто не до конца понимают до тех пор, пока ребенок не станет намного старше.
Scientific Sources
Yıldız, et al. «Неонатальная гипоксическая ишемическая энцефалопатия: обновленная информация о патогенезе заболевания и лечении». Экспертный обзор нейротерапии 17.5 (2017): 449-459.
Моллой, Элеонора Дж. И Синтия Биэр. «Неонатальная энцефалопатия против гипоксически-ишемической энцефалопатии». (2018): 574-574.
Finder, Mikael, et al. «Двухлетние исходы развития нервной системы после легкой гипоксической ишемической энцефалопатии в эпоху терапевтического гипотермии.» JAMA pediatrics 174.1 (2020): 48-55.
Greco, P., et al.» Патофизиология гипоксически-ишемической энцефалопатии: обзор прошлого и взгляд в будущее «. Acta Neurologica Belgica 120.2 (2020): 277-288.
Неонатальная энцефалопатия и гипоксически-ишемическая энцефалопатия (ГИЭ)
Неонатальная энцефалопатия (NE) — это широкий термин, обозначающий неврологическую дисфункцию у младенцев. Неонатальная энцефалопатия может быть вызвана множеством причин (1).Кислородная недостаточность при рождении (асфиксия при рождении) — одна из наиболее частых причин неонатальной энцефалопатии. Медицинские работники могут использовать термины гипоксически-ишемическая энцефалопатия (ГИЭ), перинатальная асфиксия , внутриутробная асфиксия и родовая асфиксия взаимозаменяемо с неонатальной энцефалопатией, хотя это несколько разные состояния.
Что такое неонатальная энцефалопатия (NE)?
«Неонатальная энцефалопатия» включает любую форму дисфункции центральной нервной системы, вызванную повреждением головного мозга.Этот термин используется при обсуждении травм у детей, рожденных на сроке беременности 35 недель или позже (дети, которые либо родились поздно, либо доношены) (1, 2). По оценкам, неонатальная энцефалопатия встречается примерно у двух-девяти из 1000 живорождений (2) и может быть вызвана множеством факторов. К ним относятся следующие (3):
Заболевания, связанные с неонатальной энцефалопатией
У младенцев с неонатальной энцефалопатией или гипоксически-ишемической энцефалопатией могут быть другие связанные диагнозы, в том числе:
Что означает диагноз неонатальной энцефалопатии?
Диагноз неонатальной энцефалопатии может означать многое.Проще говоря, это означает, что у ребенка определенная степень дисфункции мозга. Иногда из-за травмы внутри головного мозга возникает отек. Во многих случаях у ребенка не остается необратимых повреждений или долгосрочных последствий, особенно если энцефалопатия своевременно распознается и лечится.
К сожалению, в некоторых случаях последствия неонатальной энцефалопатии выявляются в более позднем возрасте; когда ребенок достигает четырех-пяти лет и начинает пропускать важные этапы развития (4).Неонатальная энцефалопатия может привести к долгосрочным состояниям, таким как церебральный паралич, задержка в развитии или нарушение обучаемости.
Признаки и симптомы неонатальной энцефалопатии
Энцефалопатия новорожденных может быть легкой, средней или тяжелой степени в зависимости от ее симптомов. Признаки и симптомы энцефалопатии могут включать следующие (2):
- Низкая Оценка по шкале Апгар
- Слабый или отсутствующий плач при рождении / родах
- Изъятия
- Требовать реанимации
- Аномальный уровень сознания: Ребенок гиперактивен, раздражителен, апатичен, заторможен (не очень внимателен).
- Нарушения тонуса и рефлекса: Такие, как гипотония (хромота или гибкость конечностей) и / или гипертонус (жесткость или спастичность мышц).
- Отсутствие примитивных рефлексов
- Апноэ : Периоды, при которых ребенок перестает дышать на 20 секунд или более.
- Проблемы с кормлением
- Проблемы с дыханием
- Лихорадка
- Скованность в шее: Часто встречается при менингите или менингоэнцефалите.
- Гипотония
- Органная недостаточность
- Гипер- или гипогликемия
Судороги у новорожденных — один из наиболее частых признаков неонатальной энцефалопатии. Важно отметить, что судороги у младенцев не выглядят так же, как у детей ; Признаки судорог у младенцев обычно менее заметны. У некоторых детей с припадками наблюдаются повторяющиеся подергивания или циклические движения конечностей, или им может казаться, что они тупо смотрят в пространство.Эти эпизоды могут повлиять на сознание ребенка. Эти припадки необходимо быстро диагностировать с помощью ЭЭГ и лечить, чтобы предотвратить ухудшение состояния мозга (5).
Лечение неонатальной энцефалопатии
Все средние и тяжелые случаи неонатальной энцефалопатии требуют лечения, которое проводится в отделении интенсивной терапии новорожденных (NICU) (2). Поскольку существует множество различных основных механизмов, которые могут вызвать неонатальную энцефалопатию, лечение и лечение травмы в высшей степени индивидуализировано.Некоторые виды энцефалопатии необходимо лечить с помощью терапевтической гипотермии (охлаждения мозга). Однако не все типы энцефалопатии лечатся одинаково. Например, энцефалопатия, вызванная бактериями или вирусом, лечится путем борьбы с основной инфекцией. Ключевые методы лечения включают (2):
- Вентиляция: Младенцев с энцефалопатией из-за респираторных заболеваний можно поместить на вентилятор, чтобы регулировать их дыхание и обеспечить адекватную оксигенацию.Медицинские работники должны избегать гипероксии и гипоксемии (слишком много или слишком мало кислорода).
- Приступы : Частью лечения неонатальной энцефалопатии является борьба с приступами. Некоторые лекарства можно использовать для лечения судорог. Кроме того, для регулярного наблюдения за приступами следует использовать мониторинг ЭЭГ.
- Лечение, связанное с кровью: Младенцам с мозговым кровотечением можно давать продукты крови (например, эритроциты и свежезамороженную плазму) или физиологический раствор для устранения проблем с кровяным давлением.Следует поддерживать перфузию мозга и органов и избегать гипертонии, гипотонии и гипервязкости.
- IV: Младенцам, перенесшим инсульт, можно вводить жидкости и лекарства внутривенно для предотвращения проблем со свертыванием крови.
- Лекарство: Младенцам с энцефалопатией, вызванной инфекцией, могут быть назначены противовирусные препараты или антибиотики для контроля инфекции (в зависимости от типа инфекции).
Причины неонатальной энцефалопатии
Неонатальная энцефалопатия может быть вызвана широким спектром осложнений во время или во время родов, включая следующие.
Асфиксия при рождении (недостаток кислорода в головном мозге)
В утробе матери младенцы получают кислород из крови, которая проходит от матери к плаценте и пуповине. Все, что мешает этому пути, может вызвать у ребенка недостаток кислорода (7). Некоторые примеры причин асфиксии при рождении включают:
Основные состояния материнского здоровья
Определенные состояния здоровья могут повысить риск беременности. Эти состояния здоровья несут с собой более высокий риск родовой травмы, что требует более тщательного наблюдения и более частых посещений дородового наблюдения.Эти условия включают (8):
Рождение с травмой
Очень важно, чтобы младенцы рожали опытные акушеры, гинекологи или другой медицинский персонал, обладающий необходимыми знаниями методов и процедур для сложных родов. Если медицинский персонал родит ребенка способом, который не соответствует стандартам ухода, у ребенка могут быть травматические роды (8). Последствия травматических родов не всегда очевидны — внешнего кровотечения может и не быть.Иногда возникает внутреннее кровотечение (мозговое кровотечение). У младенцев могут сразу же появиться признаки неврологической дисфункции — например, в виде судорог — или — в некоторых случаях — неврологическая дисфункция у ребенка проявляется только по мере того, как они растут и начинают пропускать основные этапы развития. Причины травматических родов могут включать:
Профилактика неонатальной энцефалопатии (NE)
Многие состояния, вызывающие неонатальную энцефалопатию (NE), имеют известные факторы риска. Это означает, что медицинский персонал может предотвратить неблагоприятные исходы, должным образом следя за здоровьем матери и ребенка и при необходимости проводя вмешательства.
Многие из этих событий влияют на ребенка во время схваток и родов. Из-за рисков, связанных с родами, частота сердечных сокращений ребенка должна постоянно контролироваться с помощью монитора сердечного ритма плода (9). Этот монитор предупредит медицинскую бригаду, если у ребенка начнется недостаток кислорода, что будет проявляться как неутешительное исследование сердца (дистресс плода). При возникновении дистресса плода врач должен сразу же родить ребенка, часто с помощью кесарева сечения (самый быстрый и безопасный способ родить ребенка, находящегося в бедственном положении).
Одним из ключевых моментов, которые очень важны для предотвращения неонатальной энцефалопатии у младенцев, является надлежащая техника для использования вакуумных экстракторов или щипцов , если в этом возникнет необходимость . Не должно быть ни перекручивания головы или шеи, ни чрезмерного натяжения, ни тяги более 20 минут (10). Если во время использования вакуум-экстрактор сработает 3 раза, врач должен перейти к кесареву сечению (11). Эти инструменты должны использоваться только врачами, которые соблюдают стандарты оказания медицинской помощи, в том числе квалифицированные.
Если у ребенка кровоизлияние в мозг в результате родов или родоразрешения, кровотечение необходимо незамедлительно распознать и лечить, чтобы можно было избежать энцефалита и таких необратимых состояний, как церебральный паралич. Это может включать:
- Лекарства, помогающие остановить или замедлить кровотечение
- Лекарства для повышения артериального давления и объема крови
- Вентиляционная опора для ребенка (дыхательный аппарат)
- Лекарства для уменьшения воспаления
- Тщательный мониторинг внутричерепного артериального давления
Беременные женщины должны проходить регулярные дородовые осмотры, которые оценивают как их здоровье, так и здоровье их ребенка.Пренатальные тесты включают нестрессовые тесты и биофизические профили (BPP). Если у матери беременность высокого риска, следует чаще проводить пренатальные анализы и направлять ее к специалисту по беременности и родам. Эти пренатальные тесты, если их провести правильно, могут выявить основные состояния здоровья, которые могут означать, что ребенок подвергается более высокому риску получения родовой травмы.
Во время дородовых посещений врачи должны уделять пристальное внимание результатам анализов, особенно сердцебиению ребенка. Эти записи вместе с результатами УЗИ предупредят медицинскую бригаду о проблемах со здоровьем, которые могут быть у ребенка, в том числе если ребенок лишен кислорода.Если это происходит, мать может быть госпитализирована, чтобы медицинская бригада могла внимательно наблюдать за ребенком. Иногда ребенка приходится рожать раньше, чтобы предотвратить необратимое повреждение мозга из-за недостатка кислорода и / или питательных веществ.
Юридические центры ABC: поверенные по неонатальной энцефалопатии
Если у вашего ребенка неонатальная энцефалопатия, рассмотрите возможность рассмотрения вашего дела адвокатом по родовым травмам. Некоторым детям с неонатальной энцефалопатией требуется круглосуточный уход, медицинская помощь, реабилитация и терапия и другие услуги.Иск о родовой травме может помочь покрыть расходы на уход за ребенком.
Обратитесь к поверенным по травмам при родах в юридических центрах ABC (Reiter & Walsh, P.C.), чтобы получить бесплатную 100% конфиденциальную оценку дела. Мы фокусируем только на родовых травмах, в отличие от других фирм, которые говорят, что фокусируются только на родовых травмах, но имеют списки случаев, полные укусов собак, автокатастроф и неисправностей медицинских устройств.
Родовая травма требует глубоких знаний медицины, юридических вопросов, проблем радиологии и планирования ухода в связи с детской инвалидностью.Адвокаты по травмам при родах в юридических центрах ABC имеют почти 100-летний опыт работы.
Вы бы не доверили врачу широкого профиля деликатную микрохирургию. Зачем доверять дело о родовой травме специалисту по травмам?
Обзор бесплатного случая | Доступно 24/7 | Никаких комиссий, пока мы не выиграем
Телефон (бесплатный): 888-419-2229
Нажмите кнопку онлайн-чата в своем браузере
Заполните нашу онлайн-форму для связи
Видео: Адвокаты по неонатальной энцефалопатии обсуждают гипоксически-ишемическую энцефалопатию (ГИЭ)
Источники:
- Краткое содержание: неонатальная энцефалопатия и неврологический исход, второе издание.Отчет Рабочей группы Американского колледжа акушеров и гинекологов по неонатальной энцефалопатии. Obstet Gynecol 2014; 123: 896.
- Wu, Y. (10 июля 2019 г.). Клиника, диагностика и лечение энцефалопатии новорожденных. Получено 4 октября 2019 г. с сайта https://www.uptodate.com/contents/clinical-features-diagnosis-and-treatment-of-neonatal-encephalopathy/print.
- Tan, S., & Wu, Y. (27 июля 2018 г.). Этиология и патогенез неонатальной энцефалопатии. Получено 8 октября 2019 г. с сайта https: // www.uptodate.com/contents/etiology-and-pathogenesis-of-neonatal-encephalopathy?topicRef=6216&source=see_link.
- Задержки развития и родовые травмы: юридические центры ABC. (нет данных). Получено 9 октября 2019 г. с сайта https://www.abclawcenters.com/practice-areas/types-of-birth-injuries/signs-milestones-developmental-delays/.
- Детские припадки (неонатальные припадки): Адвокаты по родовым травмам. (нет данных). Получено 9 октября 2019 г. с сайта https://www.abclawcenters.com/practice-areas/neonatal-birth-injuries/seizures/.
- Терапия гипотермией: лечение гипоксически-ишемической энцефалопатии. (нет данных). Получено 8 октября 2019 г. с сайта https://www.abclawcenters.com/practice-areas/treatments-and-therapies-for-birth-injuries/hypothermia-cooling/.
- Гипоксическая ишемическая энцефалопатия Адвокаты: асфиксия при рождении. (нет данных). Получено 8 октября 2019 г. с сайта https://www.abclawcenters.com/practice-areas/prenatal-birth-injuries/fetus-or-newborn-medical-problems/hypoxic-ischemic-encephalopathy/birth-asphyxia-hypoxic-ischemic. -энцефалопатия-поверенные /.
- Беременность с высоким риском: Адвокаты по родовым травмам. (нет данных). Получено 9 октября 2019 г. с сайта https://www.abclawcenters.com/practice-areas/prenatal-birth-injuries/maternal-medical-conditions/high-risk-pregnancy/.
- Адвокаты по родовой травме: Адвокаты по церебральному параличу. (нет данных). Получено 8 октября 2019 г. с сайта https://www.

 При родовспоможении, бывает, страдает головной и спинной мозг, особенно опасными считаются ЧМТ.
При родовспоможении, бывает, страдает головной и спинной мозг, особенно опасными считаются ЧМТ.
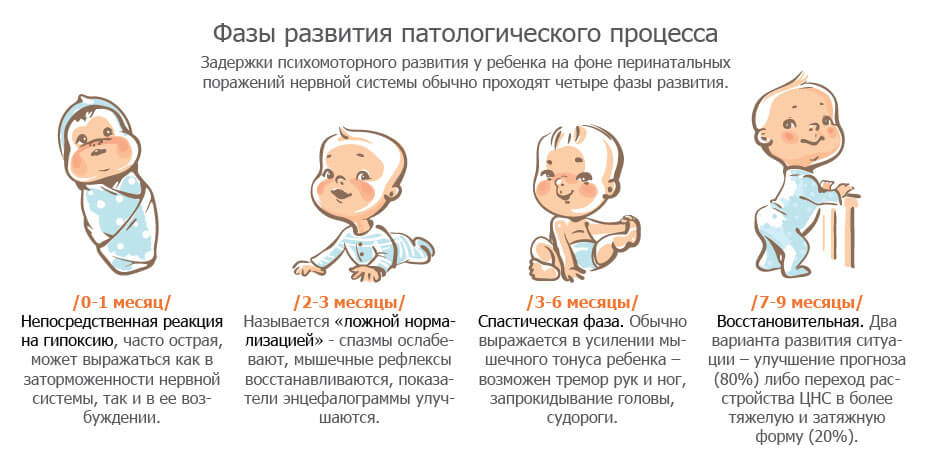

 Организм девушки может быть просто неготовым к вынашиванию полноценного и здорового ребенка. В случае слишком юного возраста или недостаточного физического развития будущей матери она должна находиться под постоянным контролем специалиста в течение всего периода беременности и после родов;
Организм девушки может быть просто неготовым к вынашиванию полноценного и здорового ребенка. В случае слишком юного возраста или недостаточного физического развития будущей матери она должна находиться под постоянным контролем специалиста в течение всего периода беременности и после родов; Рекомендуется обратиться к специалистам (в том числе и остеопату), которые помогут в значительной мере нейтрализовать неблагоприятное воздействие окружающей среды;
Рекомендуется обратиться к специалистам (в том числе и остеопату), которые помогут в значительной мере нейтрализовать неблагоприятное воздействие окружающей среды; Это могут быть как частые простуды, так и периодические недомогания, связанные с плохим самочувствием, повышенной утомляемостью, головными болями и т.д.;
Это могут быть как частые простуды, так и периодические недомогания, связанные с плохим самочувствием, повышенной утомляемостью, головными болями и т.д.; Обычно эти нарушения неизменно влекут за собой другие заболевания, так как из-за нарушенного кровотока различные участки организма начинают недополучать кислород, что приводит к гибели клеток и дисфункции.
Обычно эти нарушения неизменно влекут за собой другие заболевания, так как из-за нарушенного кровотока различные участки организма начинают недополучать кислород, что приводит к гибели клеток и дисфункции.