Фасциолез у человека: пути заражения и цикл развития: причины, симптомы, диагностика, лечение
Основной источник инвазии для человека — овцы и крупный рогатый скот. Человек заражается при питье загрязнённой адолескариями воды, употреблении овощей и зелени (обычно водяного кресс-салата). Фасциолёз распространён практически во всех регионах мира, но более широко в странах Азии, Африки и Южной Америки. В Европе наибольшее число случаев фасциолёза зарегистрировано в Португалии и Франции. В некоторых регионах России и в странах СНГ регистрируют спорадические случаи, отдельные вспышки иногда возникают в Средней Азии, Закавказье.
F. hepatica паразитирует в желчных ходах печени многих травоядных животных и изредка у человека. В сутки одна особь откладывает в среднем 25 тыс. яиц. Основным источником заражения служат инвазированные травоядные сельскохозяйственные животные, главным образом крупный рогатый скот. Человек большой роли в эпидемическом процессе фасциолеза не играет, так как является лишь случайным хозяином паразита.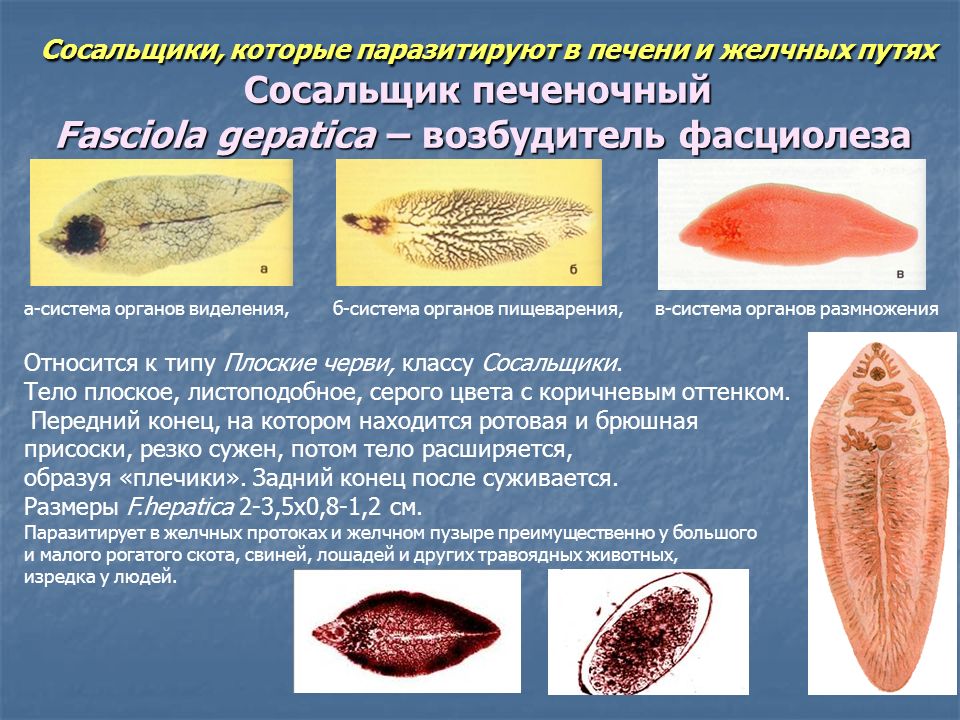
Яйца фасциол зимой в водоемах и на пастбищах сохраняются до 2-х лет. Личинки паразитов, находящиеся в теле моллюсков, могут перезимовывать и выходить из них ранней весной. Адолескарии при 100% относительной влажности переносят температурные колебания в пределах от -18 до +42 °С; в условиях относительной влажности 25-30% они погибают при 36 °С. В сухом сене инцистированные адолескарии могут выживать в течение нескольких месяцев, а во влажной почве и воде сохраняются жизнеспособными до 1 года.
Человек заражается при употреблении в пищу дикорастущих растений (кресс-салат водяной, кок-сагыз, дикий лук, щавель), произрастающих в стоячих или медленно текущих водоемах, а также на влажных пастбищах, где могут обитать инвазированные моллюски. Можно заразиться и при питье воды из загрязненных адолескариями водоемов или купании в них, а также при употреблении в пищу обычных огородных овощей (салат, лук), для полива которых использовалась вода из таких источников. Пик заражения приходится на летние месяцы.
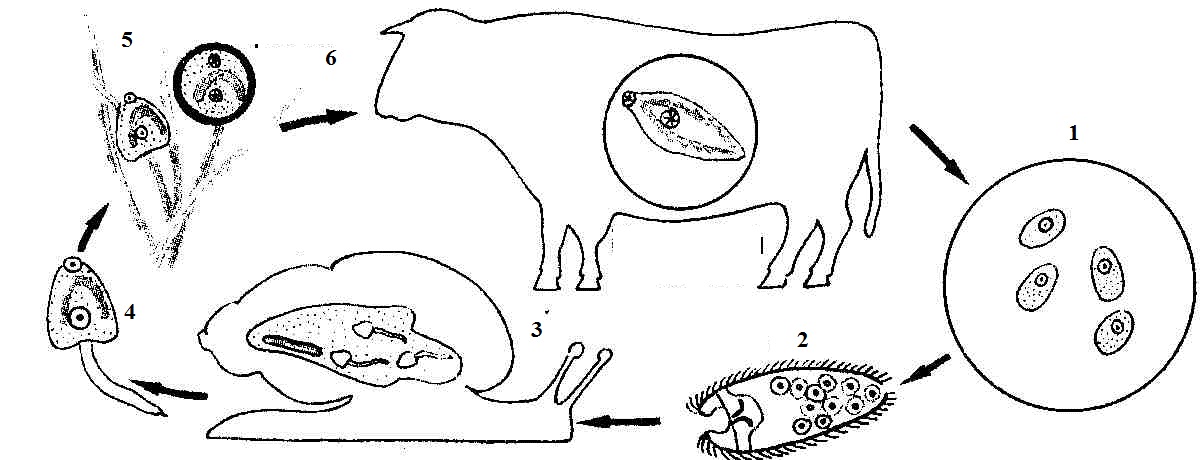
Цикл развития фасциолёза
Вместе с калом яйца попадают во внешнюю среду. Дальнейшее их развитие происходит в воде. При температуре 20-30 °С в яйцах через две недели развиваются мирацидии. При более низких температурах развитие яиц замедляется, при температуре выше 40 °С мирацидии погибают. В темноте яйца развиваются быстрее, но мирацидии из них не выходят. Продолжительность жизни мирацидия в воде составляет не более 2-3 дней. Проникнув во внутренние органы брюхоногих моллюсков Lymnea truncatula и других видов Lymnea, мирацидии превращаются в спороцисты, в которых развиваются редии. В редиях образуются либо второе поколение редий, либо хвостатые церкарий. Они выходят из моллюска через 2-3 месяца после его заражения и в течение ближайших 8 часов инцистируются, прикрепляясь к водным растениям или к поверхностной пленке воды. Инцистированная личинка печеночной двуустки — адолескарий — попадает в желудочно-кишечный тракт окончательного хозяина при питье воды из водоемов, поедании растительности с заливных лугов, либо при использовании зараженной воды для бытовых нужд (мытье овощей и фруктов, полив грядок и т. п.). Попав в кишечник окончательного хозяина с пищей (околоводные и водные растения) или с водой, адолескарий эксцистируются, и личинки проникают через стенку кишечника, мигрируют в брюшную полость, а затем через капсулу и паренхиму печени — в желчные протоки. Второй путь миграции — гематогенный, через кишечные вены в воротную вену, а затем в желчные протоки печени. От момента попадания адолескариев в организм дефинитивного хозяина до развития половозрелой стадии проходит 3-4 месяца. Срок жизни фасциол в организме человека составляет 5 лет и более.
п.). Попав в кишечник окончательного хозяина с пищей (околоводные и водные растения) или с водой, адолескарий эксцистируются, и личинки проникают через стенку кишечника, мигрируют в брюшную полость, а затем через капсулу и паренхиму печени — в желчные протоки. Второй путь миграции — гематогенный, через кишечные вены в воротную вену, а затем в желчные протоки печени. От момента попадания адолескариев в организм дефинитивного хозяина до развития половозрелой стадии проходит 3-4 месяца. Срок жизни фасциол в организме человека составляет 5 лет и более.
Продвигаясь по печеночной ткани, фасциолы повреждают капилляры, паренхиму, желчные протоки. Образуются ходы, которые в дальнейшем превращаются в фиброзные тяжи. Иногда фасциолы током крови заносятся в другие органы, наиболее часто — в легкие, где инкапсулируются и погибают, не достигая половой зрелости. Кроме того, молодые фасциолы заносят из кишечника в печень микрофлору, вызывающую распад застойной желчи, что обусловливает интоксикацию организма, образование микроабсцессов и микронекрозов.
Фасциолез, вызванный Fasciola hepatica, распространен в большинстве стран мира. Особенно часто он встречается в тех регионах Европы, Среднего Востока, Южной Америки и Австралии, где развито животноводство. В основном регистрируются спорадические случаи, однако во Франции, на Кубе, в Иране и Чили были зарегистрированы вспышки с поражением сотен людей. Описаны вспышки фасциолеза в Прибалтике, Узбекистане и Грузии. Самая большая известная вспышка фасциолеза произошла в Иране в 1989 г., когда заболели свыше 10 тыс. человек, в том числе около 4 тыс. детей. В прошлом веке в Перу пораженность школьников в некоторых деревнях достигала 34%.
Наиболее интенсивные очаги, связанные с F. gigantica, отмечены во Вьетнаме и в других странах Юго-Восточной Азии, на Гавайских островах и в некоторых странах тропической Африки.
[12], [13], [14], [15], [16], [17], [18], [19], [20], [21]
причины, симптомы, диагностика и лечение
Фасциолез – это паразитарная инвазия, вызываемая печеночной или гигантской двуусткой и характеризующаяся преимущественным поражением гепатобилиарной системы. Течение фасциолеза сопровождается недомоганием, лихорадкой, крапивницей, тошнотой, болями в правом подреберье, увеличением размеров печени, желтухой. В диагностике фасциолеза информативны серологические методы (ИФА, РИФ, РИГА), исследование дуоденального содержимого и фекалий на яйца гельминтов, УЗИ печени и желчевыводящих путей. В комплексную терапию фасциолеза включают диету, прием антигельминтных средств (триклабендазол, празиквантел), желчегонных, антигистаминных препаратов.
Течение фасциолеза сопровождается недомоганием, лихорадкой, крапивницей, тошнотой, болями в правом подреберье, увеличением размеров печени, желтухой. В диагностике фасциолеза информативны серологические методы (ИФА, РИФ, РИГА), исследование дуоденального содержимого и фекалий на яйца гельминтов, УЗИ печени и желчевыводящих путей. В комплексную терапию фасциолеза включают диету, прием антигельминтных средств (триклабендазол, празиквантел), желчегонных, антигистаминных препаратов.
Общие сведения
Фасциолез — внекишечный гельминтоз, обусловленный паразитированием в паренхиме печени и желчных путях печеночной или гигантской фасциолы (сосальщика). Наряду с описторхозом, клонорхозом, парагонимозом, шистосомозами фасциолез относится к наиболее распространенным трематодозам человека. Фасциолез, вызываемый печеночным сосальщиком, распространен в Австралии, странах Европы и Южной Америки. Фасциолез, связанный с гигантским сосальщиком, встречается в Африке, Восточной Азии, районах Средней Азии и Закавказья. Описаны, как спорадические, так и массовые вспышки заболевания, охватывавшие сотни человек. Согласно имеющимся данным, фасциолезом поражено от 2,5 до 17 млн. населения планеты.
Описаны, как спорадические, так и массовые вспышки заболевания, охватывавшие сотни человек. Согласно имеющимся данным, фасциолезом поражено от 2,5 до 17 млн. населения планеты.
Фасциолёз
Причины фасциолеза
Характеристика возбудителя
Возбудителями фасциолеза выступают два вида трематод (сосальщиков): двуустка печеночная (Fasciola hepatica) и двуустка гигантская (Fasciola gigantea). Печеночная фасциола имеет тело плоской листовидной формы, на головном конце которого расположено 2 присоски. Длина взрослого паразита 20-30 мм, ширина 8-12 мм. Гигантская фасциола имеет более крупные размеры: длину 33-76 мм, ширину 5-12 мм.
Механизм передачи
Окончательными хозяевами сосальщиков служат травоядные сельскохозяйственные животные, реже – человек. Паразитируя в желчевыводящей системе, гельминты откладывают яйца, которые с испражнениями попадают в окружающую среду и свое дальнейшее развитие проходят в пресной воде. Там вышедшие из яиц личиночные стадии (мирацидии) внедряются в тело брюхоногих моллюсков, являющихся промежуточными хозяевами возбудителя фасциолеза.
Во внутренних органах моллюсков мирацидии превращаются сначала в спороцисты, а затем в хвостатые церкарии. Через 1-2 месяца церкарии снова выходят в воду, инцистируются, превращаясь в адолескарий, и прикрепляются к поверхности водных растений или водной пленке. В этой стадии личинки становятся инвазионными, т. е способными вызывать фасциолез у животных и человека.
Заражение животных фасциолезом происходит при поедании травы на выпасе, загрязненной личинками двуустки; инфицирование человека возможно при употреблении в пищу дикорастущих или огородных растений, полив которых осуществлялся водой из пресных водоемов; питье некипяченой воды; во время купания и т. д. В желудочно-кишечном тракте личинки фасциолы высвобождаются из оболочек, через стенку кишечника выходят в брюшную полость, где через капсулу внедряются в паренхиму печени и таким образом попадают в желчные протоки. Возможен гематогенный путь миграции – через кишечные и воротную вены в печеночные протоки.
Через 3-4 месяца паразитирования в организме окончательного хозяина фасциолы достигают половозрелой стадии и начинают откладывать яйца. В гепатобилиарной системе человека возбудители фасциолеза способны паразитировать 5-10 и более лет.
Патогенез
Развивающиеся в миграционную фазу инвазии токсико-аллергические реакции связаны с сенсибилизацией организма антигенами личинок, а также механическим травмированием тканей на пути их продвижения. В хронической стадии фасциолеза патологические эффекты обусловлены паразитированием гельминтов в желчных протоках. Половозрелые гельминты вызывают повреждение печеночной паренхимы с развитием микроабсцессов и фиброзных изменений печени.
Скапливаясь в желчных ходах, фасциолы могут способствовать их обструкции и нарушению оттока желчи, развитию пролиферативного (а в случае присоединения вторичной инфекции – гнойного) холангита. Общетоксическое воздействие на организм при фасциолезе обусловлено поступлением в кровь продуктов жизнедеятельности гельминтов и распада печеночной ткани. В исходе длительного течения фасциолеза может развиваться цирроз печени и портальная гипертензия.
В исходе длительного течения фасциолеза может развиваться цирроз печени и портальная гипертензия.
Симптомы фасциолеза
В развитии фасциолеза выделяют инкубационный период, острую (миграционную) и хроническую (связанную с паразитированием взрослых гельминтов) стадии. В зависимости от инвазирующей дозы, инкубационный период может длиться от 1 до 8 недель.
В миграционную фазу главным образом выражены общетоксические и аллергические симптомы. Больные фасциолезом жалуются на подъемы температуры, слабость, недомогание, головную боль. Лихорадка может быть субфебрильной или высокой (до 39-40°С), носить ремитирующий или волнообразный характер. На этом фоне появляется крапивница и кожный зуд, отек Квинке, высокая (до 80-85%) эозинофилия в крови. Развиваются диспепсические расстройства: тошнота, рвота, боли в эпигастрии и правом подреберье; происходит увеличение размеров печени, сопровождающееся желтухой. В раннем периоде часто развивается аллергический миокардит, характеризующийся загрудинными болями, артериальной гипертензией, тахикардией. Через несколько недель клинические проявления острого фасциолеза значительно или полностью стихают.
Через несколько недель клинические проявления острого фасциолеза значительно или полностью стихают.
Спустя 3-6 месяцев заболевание вступает в хроническую стадию, симптомы которой обусловлены непосредственным поражением печени и желчных путей. Течение хронического фасциолеза сопровождается гепатомегалией, приступообразными болями в правом боку; в периоды обострения – желтухой. Длительная инвазия приводит к развитию диспепсического синдрома, анемии, гепатита, цирроза печени.
Вторичное инфицирование чревато возникновением гнойного холецистита и холангита, абсцессов печени, стриктуры желчных путей. В литературе описаны казуистические случаи фасциолеза с нетипичной локализацией сосальщиков в головном мозге, легких, молочных железах, евстахиевых трубах, гортани, подкожных абсцессах.
Диагностика
Чаще всего фасциолез диагностируется уже в хронической стадии, когда с беспокоящими жалобами больные обращаются к терапевту или гастроэнтерологу. Предположительный диагноз основывается на совокупности эпидемиологических данных и клинических данных. В пользу фасциолеза свидетельствует наличие ранее зафиксированных случаев инвазии на данной территории, групповая заболеваемость, употребление в пищу салатных растений, питье воды из открытых источников или использование ее для мытья посуды, фруктов, овощей и пр.
Предположительный диагноз основывается на совокупности эпидемиологических данных и клинических данных. В пользу фасциолеза свидетельствует наличие ранее зафиксированных случаев инвазии на данной территории, групповая заболеваемость, употребление в пищу салатных растений, питье воды из открытых источников или использование ее для мытья посуды, фруктов, овощей и пр.
- Методы выявления возбудителя. В раннем периоде фасциолеза диагноз подтверждается серологическими методами (РИФ, ИФА, РИГА, РСК). В хронической стадии информативно обнаружение яиц фасциол в фекалиях или дуоденальном содержимом. Паразиты могут быть обнаружены с помощью ультразвукового исследования печени и желчного пузыря, КТ печени.
- Биохимия крови. В биохимических пробах печени отмечается повышение активности трансаминаз и щелочной фосфатазы, гипопротеинемия, гипоальбуминемия.
Фасциолез необходимо отличать от описторхоза, клонорхоза, вирусных гепатитов, панкреатита, холангита, холецистита другой этиологии.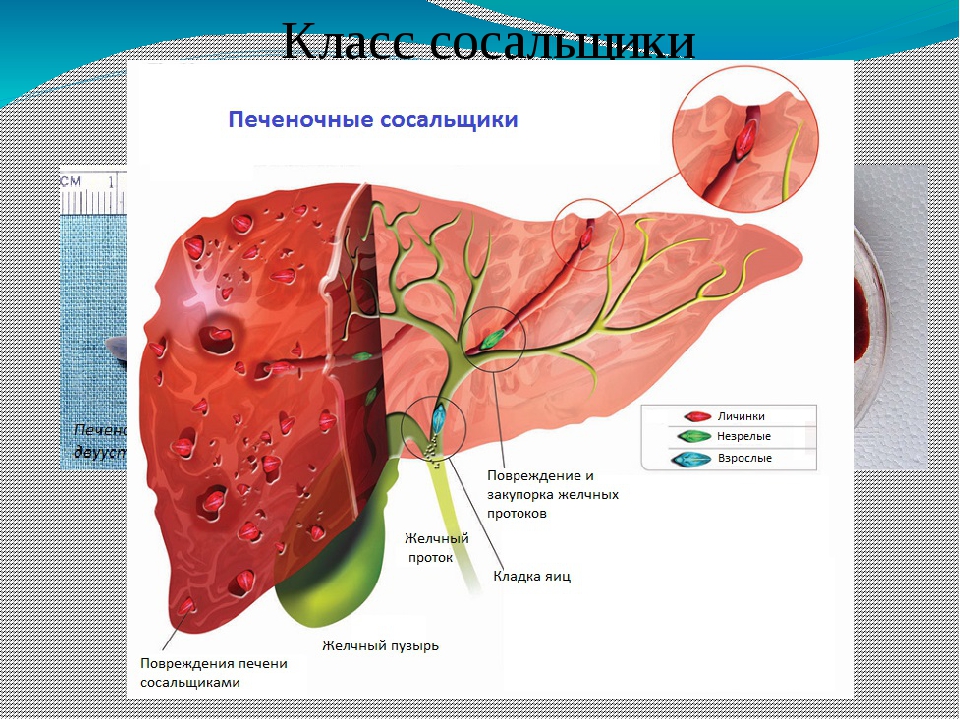
Лечение фасциолеза
Лечение фасциолеза проводится стационарно. В острую фазу назначается щадящая диета, десенсибилизирующие препараты; при развитии миокардита и гепатита показаны глюкокортикостероиды. К противопаразитарной терапии переходят только после стихания острых явлений. В качестве этиотропных препаратов при фасциолезе используются триклабендазол, гексахлорпараксилол, празиквантел. С целью изгнания погибших фасциол из желчных протоков назначаются желчегонные средства.
Контрольное паразитологическое обследование (анализ кала на яйца гельминтов, дуоденальное зондирование с исследованием порций желчи) проводится спустя 3 и 6 месяцев. В случае развития гнойных осложнений требуется назначение антибиотиков и проведение хирургического вмешательства (дренирования абсцесса печени, дренирования желчных протоков и др.).
Прогноз и профилактика
Ранняя диагностика фасциолеза позволяет провести своевременную терапию и добиться выздоровления. При высокоинтенсивной инвазии или вторичной бактериальной инфекции прогноз может быть серьезным, вплоть до летального исхода. Индивидуальная профилактика фасциолеза заключается в недопущении употребления сырой воды из водоемов, плохо промытой огородной зелени. Меры общественного контроля включают очистку водоемов, их защиту от фекального загрязнения, ликвидацию промежуточных хозяев фасциолеза – моллюсков, ветеринарное обследование и дегельминтизацию скота, санитарно-просветительскую работу.
При высокоинтенсивной инвазии или вторичной бактериальной инфекции прогноз может быть серьезным, вплоть до летального исхода. Индивидуальная профилактика фасциолеза заключается в недопущении употребления сырой воды из водоемов, плохо промытой огородной зелени. Меры общественного контроля включают очистку водоемов, их защиту от фекального загрязнения, ликвидацию промежуточных хозяев фасциолеза – моллюсков, ветеринарное обследование и дегельминтизацию скота, санитарно-просветительскую работу.
Фасциолез, ответы на основные вопросы
Что такое фасциолез?
Термин фасциолёз используется в медицине и ветеринарии для обозначения состояния людей и животных, зараженных печёночной (Fasciola hepatica) или гигантской двуусткой (Fasciola gigantica).
В большинстве случаев, фасциолез не представляет серьезной опасности для здоровья человека и многие люди, зараженные двуустками, не знают, что контактировали с этой инфекцией. Тем не менее, в определенных ситуациях, заражение печеночными двуустками может вызвать опасные осложнения и продолжительные последствия. По этой причине, все люди, которые заразились двуустками, должны пройти лечение.
По этой причине, все люди, которые заразились двуустками, должны пройти лечение.
В этой статье мы собрали ответы на все основные вопросы относительно фасциолеза, лечения и предотвращения этой болезни у людей.
Мы начнем ответы с описания жизненного цикла двуусток. Эта информация поможет вам правильно понять смысл всех остальных рекомендаций относительно решения этой проблемы.
Жизненный цикл развития возбудителей фасциолеза
С биологической точки зрения, печеночная и гигантская двуустка это плоские черви. В медицине их и некоторые другие похожие виды глистов (например, описторхоз, клонорхоз), называют трематодами.
Основными носителями фасциолеза являются коровы, козы и овцы. Жизненный цикл возбудителей фасциолеза начинается, когда кал крупного или мелкого скота, зараженного двуустками, попадает в пресные водоемы.
В теплой воде, в течение 9-14 дней, из содержащихся в кале яиц двуусток, появляются личинки, которые далее проникают в организм пресноводных улиток.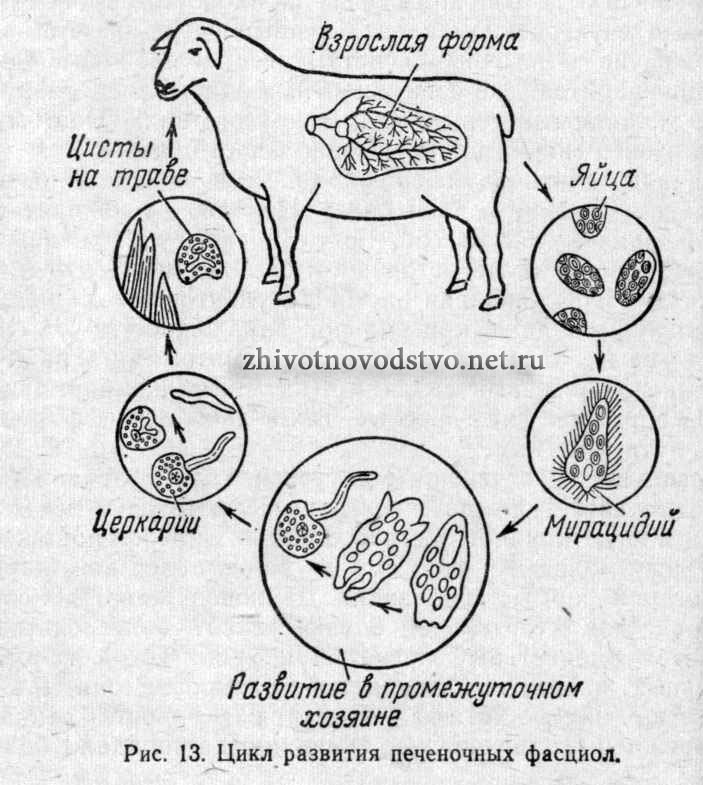 Это обязательная фаза развития, без которой личинки не могут стать заразными для человека или домашних животных.
Это обязательная фаза развития, без которой личинки не могут стать заразными для человека или домашних животных.
В организме водных улиток личинки двуусток развиваются и размножаются в течение нескольких недель. После этого они снова выходят в воду и остаются в ней, покрывшись защитной оболочкой, либо прилипают к стеблям растений, произрастающих вблизи водоемов.
симптомы болезни, профилактика и лечение Фасциолеза , причины заболевания и его диагностика на EUROLAB
Фасциолез (fascioliasis) — инвазия из группы трематодозов с преимущественным поражением печени и желчевыделительной системы.
Возбудителями фасциолеза являются два сосальщика рода Fasciola (Linnaeus, 1758), семейства Fasciolidae (Railliet,1895) — Fasciola hepatica и Fasciola gigantica.
Родовое наименование происходит от латинского саовэ. fascia — «тесемочка», «повязочка», «ленточка». И действительно, фасциола гигантская похожа на ленточку.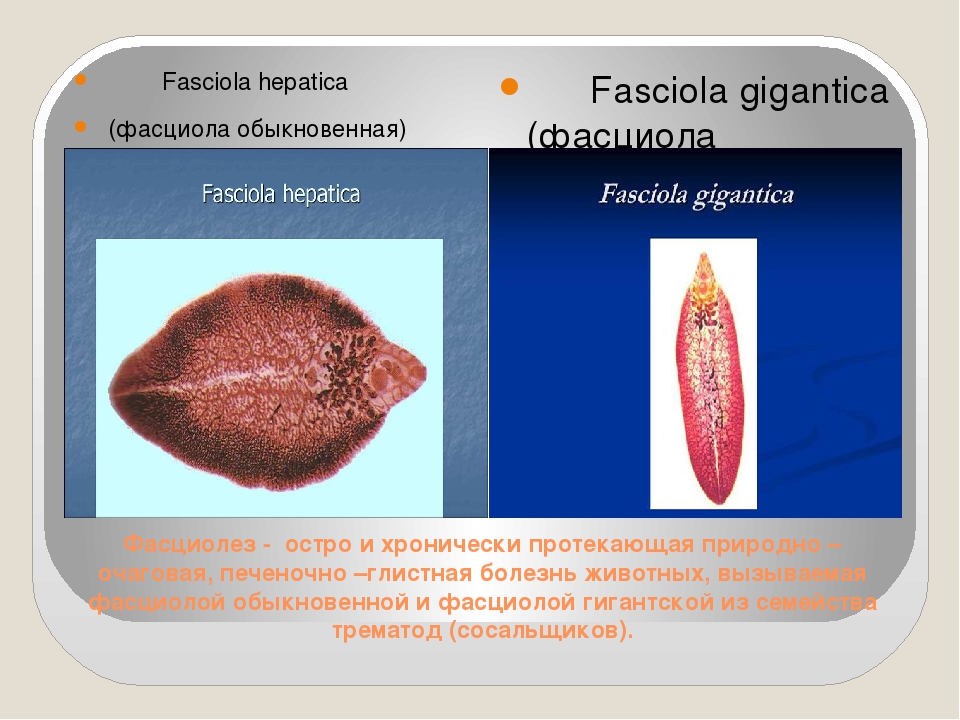
F. hepatica — крупная трематода с листовидно удлиненной формы телом длиной 20 — 30 мм, шириной 8-13 мм. На переднем конусовидном конце находится полушаровидная ротовая присоска. Более крупная брюшная присоска располагается вблизи от ротовой, за конусовидной частью тела гельминта. Глотка и пищевод очень короткие, от последнего отходят две сильно ветвящиеся и слепо заканчивающиеся петли кишечника. Два ветвистых семенника занимают срединную часть тела. Над ними находится непарный яичник в виде веточки коралла, оленьего рога. Мощно развитые желточники тянутся вдоль боковых краев, сливаясь в задней четверти тела. Петлистая небольшая матка лежит между протоками желточников и брюшной присоской.
Яйца F. hepatica крупные, овальные, покрыты гладкой двухконтурной оболочкой золотисто-желтого цвета. Они имеют на одном полюсе крышечку, на противоположном — бугорок. Размеры яиц 130 — 140 х 70 — 90 мкм.
Fasciola gigantica в отличие от F.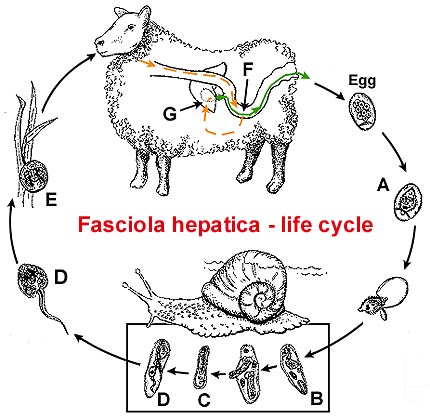 hepatica имеет большие размеры (длина до 7 — 8 см при ширине до 12 мм) и более удлиненную форму. Яйца более крупные (150 — 190 х 75 — 90 мкм).
hepatica имеет большие размеры (длина до 7 — 8 см при ширине до 12 мм) и более удлиненную форму. Яйца более крупные (150 — 190 х 75 — 90 мкм).
Биологию фасциол изучил немецкий ученый Лейкарт. У человека фасциолез в 1760 г. описал знаменитый натуралист и путешественник Петр Симон Паллас.
Фасциолез — биогельминтоз, зооноз. Окончательными хозяевами возбудителя являются животные — крупный и мелкий рогатый скот, лошади, верблюды, грызуны, редко человек. У человека регистрируется в виде спорадических случаев почти во всех странах мира. К 1992 году в мире было зарегистрировано 15 тысяч случаев фасциолеза людей, проживающих в 40 странах мира, в том числе в 19 странах Европы (А. М. Сазанов, 1994). Это далеко не полное отражение истинной ситуации. Во Франции, на Кубе, в Чили зарегистрированы вспышки фасциолеза. В некоторых деревнях Перу 4,5 — 34% детей младше 15 лет, в одном из районов Малави 2,4% из 3900 жителей выделяли яйца фасциол.
Спорадические случаи фасциолеза постоянно регистрируются в Закавказье, Средней Азии, Украине.
Фасциолез — один из наиболее опасных и широко распространенных гельминтозов сельскохозяйственных животных. Он регистрируется на всех континентах земного шара и приносит большой ущерб животноводческим хозяйствам из-за массовой гибели животных при эпизоотиях, значительной потери живого веса, снижения надоев молока, уменьшения настрига шерсти у овец, выбраковки пораженной печени и др.
При фасциолезе крупного рогатого скота каждое животное теряет от 24 до 41 кг живого веса, за год — 223 кг молока от коровы.
Извазированность травоядных животных — крупного рогатого скота и овец в странах Закавказья, Средней Азии, Молдове, Белоруссии исчисляется 50 — 80%. В лесостепной зоне Украины фасциолез регистрируется у 70 — 83% животных.
Анализ литературы свидетельствует о значительном распространении фасциолеза у животных на территории стран тропического и субтропического климата. Например, в Эфиопии от 47 до 100% коров, овец и коз в некоторых провинциях инвазированы фасциолами.
Животные заражаются фасциолезом при поедании травы на выпасе, свежескошенного сена с заболоченных участков и при заглатывании адолескариев с водой из биотопов моллюсков.
Источником инфекции при фасциолезе человека служат инвазированные животные. Факторами заражения являются загрязненные адолескариями салатные травы, водяной кресс, кок-сагыз, щавель, огородная зелень. Человек заражается при употреблении в немытом виде салатных трав, при питье прудовой воды, использовании ее для мытья зелени, фруктов, овощей, ягод, проглаты вании адолескарий во время купания. Адолескарии в воде, влаж ной почве сохраняют жизнестойкость до 2-х лет.
Жизненный цикл.
Фасциолез — пероральный биогельминтоз. Окончательные хозяева — преимущественно растительноядные животные — как домашние (крупный и мелкий рогатый скот, лошадь, кролик, верблюд, осел и др.), так и дикие (белка, бобр, серна, олень, антилопа, косуля, тур, кенгуру и др.), а также человек.
Промежуточным хозяином является пресноводный моллюск, чаще малый прудовик рода Galba (Limnaea truncatula).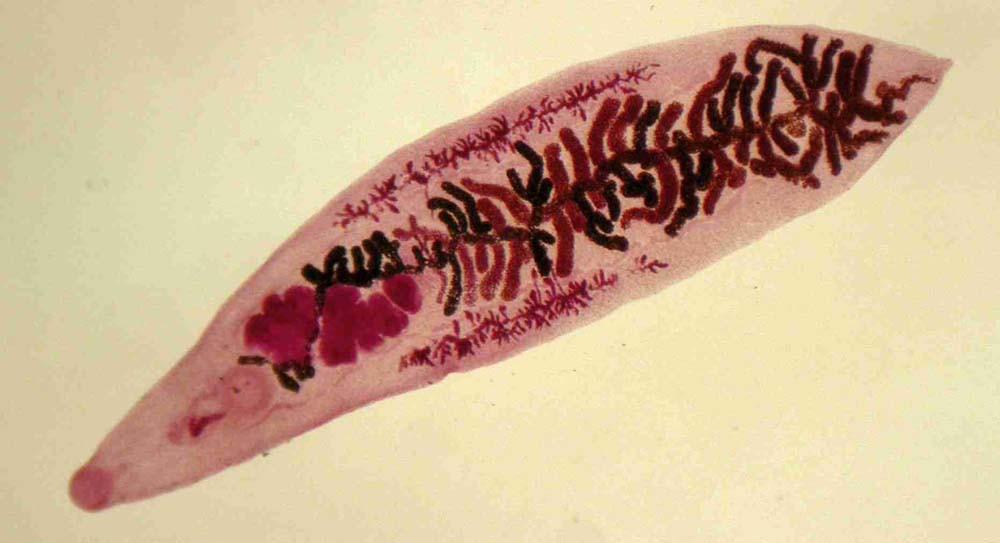 Эти моллюски в большом количестве обитают в хорошо прогреваемых мелких (часто временных) водоемах со стоячей водой, на низменных заболоченных лугах и пастбищах, на которых обычно и пасутся травоядные животные.
Эти моллюски в большом количестве обитают в хорошо прогреваемых мелких (часто временных) водоемах со стоячей водой, на низменных заболоченных лугах и пастбищах, на которых обычно и пасутся травоядные животные.
У окончательного хозяина фасциолы локализуются в желчных протоках печени, живут до 5 лет, откладывая за это время до 2 млн яиц. Яйца выделяются наружу с испражнениями, дальнейшее развитие осуществляется только при условии попадания в воду.
Оптимальная температура, необходимая для развития личинки в яйце, колеблется в пределах 22 — 29°С. При температуре ниже 10°С развитие приостанавливается, а высокие температуры (30°С и больше) действуют губительно. В оптимальных условиях эмбриогенез продолжается 17-18 суток. Сформировавшийся за это время мирацидий вылупляется из яйца в воду на свету.
Свободно плавающий в воде мирацидий внедряется в тело промежуточного хозяина — моллюска. Спустя 1,5 — 2,5 месяца в нем развивается путем партеногенеза большое количество хвостатых личинок — церкариев размером 0,23 — 0,26 х 0,2 мм. После выхода в воду в течение ближайших 8 часов церкарии, отбросив хвост, инцистируются на водных растениях, иногда на поверхности воды и превращаются в стадию адолескария — инвазионнную личинку. Адолескарии могут длительное время сохраняться в воде и на растениях, но быстро погибают при высыхании.
После выхода в воду в течение ближайших 8 часов церкарии, отбросив хвост, инцистируются на водных растениях, иногда на поверхности воды и превращаются в стадию адолескария — инвазионнную личинку. Адолескарии могут длительное время сохраняться в воде и на растениях, но быстро погибают при высыхании.
Заражение человека происходит при заглатывании адолескариев при питье воды, при купании либо при употреблении в пищу салатных трав (водяной кресс, дикорастущий кок-сагыз, щавель), а животных — на выпасе.
Попавшие в желудочно-кишечный тракт личинки фасциолы освобождаются от оболочек и проникают в печень и желчный пузырь, а иногда и в другие органы. Существуют два пути проникновения личинок: тканевой и гематогенный.
В первом случае они проникают через стенку кишечника в брюшную полость, продвигаются к печени и через глиссонову капсулу в ее паренхиму, а затем в желчные протоки, где через 3 — 4 месяца достигают половой зрелости. Во втором случае личинки внедряются в кровеносные сосуды кишечника и по системе воротной вены попадают в печень. В этом случае личинка может быть занесена в любой орган, давая необычную локализацию созревшей особи — в грудной железе, коже, легких и др.
В этом случае личинка может быть занесена в любой орган, давая необычную локализацию созревшей особи — в грудной железе, коже, легких и др.
В клинике фасциолеза, как и при других печеночных трематодозах, четко выделяются ранняя острая и хроническая фазы инвазии.
Инкубационный период составляет 1-8 недель. Фасциолез в ранней фазе протекает как острое аллергическое заболевание. Инвазия начинается остро с общих симптомов: подъема температуры, слабости, головной боли, недомогания. На этом фоне проявляются и аллергические симптомы: высокая лихорадка, желтуха, кожный зуд, высыпания на коже, крапивница, боли в животе, тошнота, рвота, что сопровождается высокой эозинофилией (до 80 — 85%) и лейкоцитозом. При пальпации печень увеличена, плотна, болезненна. Иногда в острой фазе выражены признаки аллергического миокардита — загрудинные боли, тахикардия, приглушенность тонов сердца, транзиторная артериальная гипертония. В некоторых случаях возникают изменения со стороны органов дыхания.
При неосложненном течении инвазии острые проявления сенсибилизации постепенно стихают, эозинофилия снижается до 5 — 15%.
Хроническая фаза протекает в двух основных вариантах: в виде относительно компенсированного хронического гастродуоденита с явлениями холепатии, иногда панкреатопатии. При присоединении вторичной инфекции возникает картина бактериального холецистохолангита или холангиогепатита с болевым и диспепсическим синдромами, нарушением функций печени.
Возможно развитие гнойного холангита, абсцессов печени, обтурационной желтухи. При интенсивной и длительной инвазии возможны цирротические изменения в печени. Из осложнений следует также отметить случаи извращенной локализации фасциол в легких, мозгу, грудной железе, в подкожны абсцессах и др.
Прогноз при присоединении вторичной инфекции серьезны.
Диагностика острой фазы фасциолеза трудна, диагноз можно только предположить при оценке анамнестиских, эпидемиологических и клинических данных: употребление в пищу немытых салатных трав, кок-сагыза, щавеля, питье прудовой воды, мытье посуды, фруктов, ягод этой водой и острое начало болезни с явлениями острого аллергоза. Не исключается возможность группового заболевания туристов, геологов и др.
Не исключается возможность группового заболевания туристов, геологов и др.
В настоящее время для диагностики используют иммунологические методы — серологические тест-системы, РЭМА, РИФ, РСК.
В более поздние сроки (через 2,5 — 3 месяца после заражения) диагноз подтверждается обнаружением яиц фасциол в дуоденальном содержимом и в кале.
Следует помнить, что при случайном употреблении в пищу фасциолезной печени (это бывает при нарушении ветеринарно-санитарной экспертизы) в кале появляются так называемые транзитные яйца. Это не результат заражения и болезни, а результат разрушения фасциолы в кишечнике человека и освобождения яиц из матки гельминта.
Поэтому для установления истины надо повторно исследовать кал через 7-10 дней, исключив на это время из пищевого рациона обследуемого печень, паштеты, ливерные колбасы и т. д., а также повторить зондирование.
В острой стадии фасциолеза с яркими аллергическими проявлениями проводят десенсибилизирующую терапию (антигистаминные препараты, кальция хлорид), при развитии гепатита, миокардита назначают преднизолон в дозе 30-40 мг в сутки в течение 5-7 дней с быстрым снижением и отменой препарата.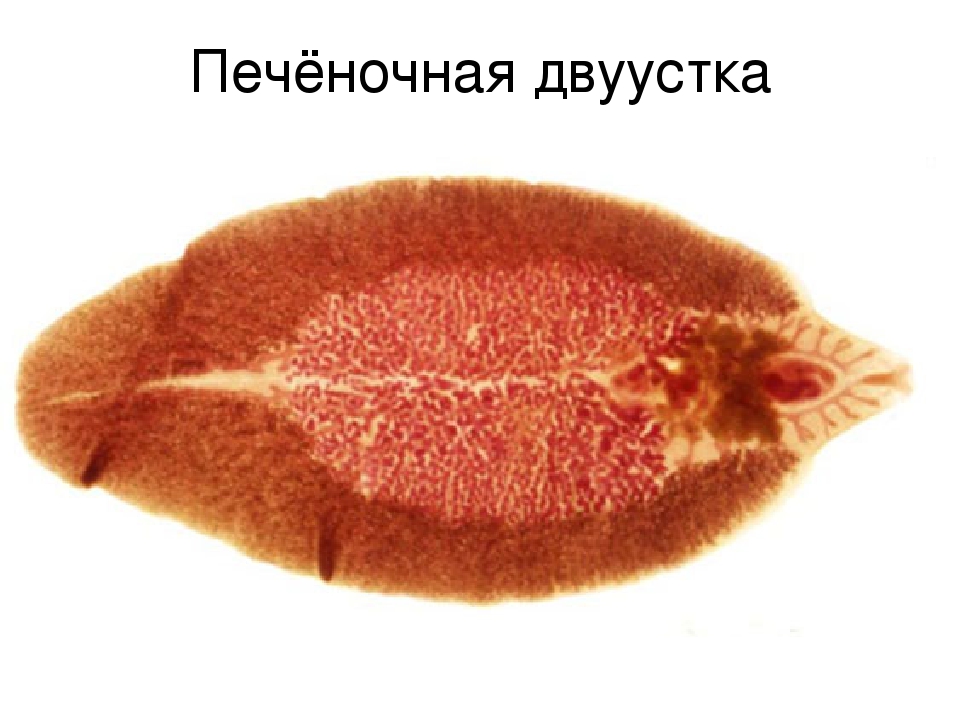 При стихании острых явлений назначают хлоксил в дозе 60 мг на 1 кг массы тела в сутки в 3 приема после еды в течение 5 дней. В хронической стадии лечение фасциолеза проводят хлоксилом, препаратами, устраняющими холестаз, общеукрепляющими средствами. При присоединении бактериальной инфекции желчных путей предварительно назначают антибиотики.
При стихании острых явлений назначают хлоксил в дозе 60 мг на 1 кг массы тела в сутки в 3 приема после еды в течение 5 дней. В хронической стадии лечение фасциолеза проводят хлоксилом, препаратами, устраняющими холестаз, общеукрепляющими средствами. При присоединении бактериальной инфекции желчных путей предварительно назначают антибиотики.
Фасциолез: лечение, симптомы, профилактика. Возбудитель болезни.
Фасциолез— остро и хронически протекающее зоонозное трематодозное заболевание домашних и диких парнокопытных животных сопровождающееся нарушением работы органов пищеварения, отеками, анемией из за чего снижается их продуктивность.
Возбудитель болезни – трематода фасциола обыкновенная и фасциола гигантика. Паразитируют данные фасциолы у животных в желчных протоках печени, желчном пузыре, питаясь при этом кровью и тканями животного.
Морфология. Фасциола обыкновенная (печеночная двуустка) имеет листовидную форму, длина которой 2-3см, ширина около 1см. Фасциола гигантская имеет вытянутую форму, достигая при этом 7,5см длины. На передней части тела у фасциолы находится выступ, где располагаются ротовая и брюшная присоски; матка находится в передней части тела, позади брюшной присоски, петли которой запутаны в клубок и имеют форму розетки. Яичники и семенники занимают среднею часть паразита. Яйца фасциол под микроскопом — имеют овальную форму, желтый цвет, длина их составляет 120-0,149мм, ширина 0,070-0,090мм. На одном полюсе яйца имеется крышечка.
Фасциола гигантская имеет вытянутую форму, достигая при этом 7,5см длины. На передней части тела у фасциолы находится выступ, где располагаются ротовая и брюшная присоски; матка находится в передней части тела, позади брюшной присоски, петли которой запутаны в клубок и имеют форму розетки. Яичники и семенники занимают среднею часть паразита. Яйца фасциол под микроскопом — имеют овальную форму, желтый цвет, длина их составляет 120-0,149мм, ширина 0,070-0,090мм. На одном полюсе яйца имеется крышечка.
Биология возбудителя. Являясь биогельминтами фасциолы развиваются с участием двух хозяев—дефинитивного и промежуточного. Основным хозяином являются жвачные животные. Промежуточные хозяева — пресноводные моллюски различных видов. Трематоды откладывают яйца, которые в организме животного транзитом проходят через кишечник и с фекалиями попадают во внешнею среду. За 10-20 дней в яйце на влажном субстрате при температуре 12-10 градусов формируется личинка-мирацидий. Выйдя из яйца мирацидий начинает плавать в воде, где и попадает в промежуточного хозяина, где и происходит его бесполое размножение (стадии спороциста, редия, церкарий) на все эти стадии у паразита уходит 2-2,5 месяца.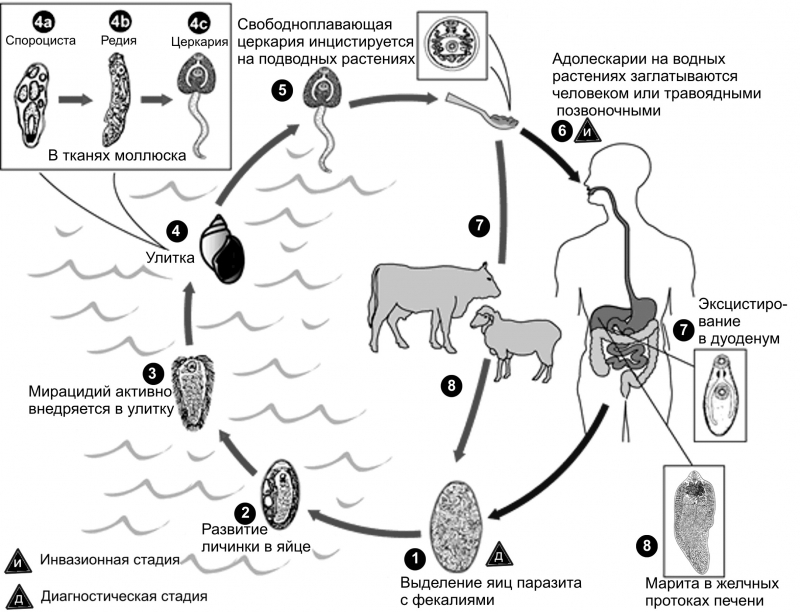 Затем зрелые церкарии покидают тело молюска, и плавая в воде быстро инцистируются, превращаясь при этом в адолескарий. В дальнейшем адолескарии используя клейкий секрет прикрепляются к траве где сохраняются до окончания пастбищного периода животных. Животные заражаются на пастбище заглатывая цисты. В кишечнике трематоды освобождаются от цистных оболочек и через стенку кишечника брюшную полость, капсулу и строму печени мигрируют в желчные ходы. Миграция и развитие до половозрелой стадии занимают 3,5-4,5 месяца. Фасциола в печени домашних животных может жить до 4-5лет и более.
Затем зрелые церкарии покидают тело молюска, и плавая в воде быстро инцистируются, превращаясь при этом в адолескарий. В дальнейшем адолескарии используя клейкий секрет прикрепляются к траве где сохраняются до окончания пастбищного периода животных. Животные заражаются на пастбище заглатывая цисты. В кишечнике трематоды освобождаются от цистных оболочек и через стенку кишечника брюшную полость, капсулу и строму печени мигрируют в желчные ходы. Миграция и развитие до половозрелой стадии занимают 3,5-4,5 месяца. Фасциола в печени домашних животных может жить до 4-5лет и более.
Эпизоотология. Источником возбудителя инвазии являются зараженные фасциолами животные. Из сельскохозяйственных животных к заболеванию наиболее восприимчивы мелкий и крупный рогатый скот, в меньшей степени свиньи, лошади и др. Наименьшая зараженность малюсками бывает весной, к осени она постепенно усиливается. Копрологически фасциолез начинают диагносцировать в ветлабораториях в конце ноября, в декабре. Молодняк поражается значительно меньше, чем взрослые животные. С возрастом интенсивность инвазии у животных повышается.
Молодняк поражается значительно меньше, чем взрослые животные. С возрастом интенсивность инвазии у животных повышается.
Патогенез. При миграции фасциолы разрушают кишечную и особенно печеночную ткань, нарушая в ней кровообращение. Одновременно занося в печень имеющуюся в организме микрофлору. Растущие паразиты давят на ткани, раздражая и травмируя шипами кутикулы стенки желчных ходов, закупоривают, а иногда разрывают желчные протоки печени, выделяя при этом токсины, которые способствуют развитию аллергии в организме животного.
Основные патологофизиологические, биохимические и функциональные изменения при фасциолезе в первую очередь происходят в печени и уже только после этого происходят нарушения в деятельности других органов и систем организма животного.
В зависимости от интенсивности инвазии, резистентности организма животного и стадии болезни при проведении исследования крови отмечаем снижение количества эритроцитов, гемоглобина, кальция и фосфора, при одновременном повышение количества билирубина и что наиболее характерно для инвазионных заболеваний — отмечаем эозинофилию. В результате патогенного воздействия фасциол на организм больных животных количество витамина А в организме может снижаться в десятки раз, в 5-6 и более раз снижается содержание витамина В-12. В период миграции фасциол в печени происходит активизация находящихся в печени споровых бактерий. Вызывая при этом «черную болезнь» — некротический гепатит.
В результате патогенного воздействия фасциол на организм больных животных количество витамина А в организме может снижаться в десятки раз, в 5-6 и более раз снижается содержание витамина В-12. В период миграции фасциол в печени происходит активизация находящихся в печени споровых бактерий. Вызывая при этом «черную болезнь» — некротический гепатит.
Иммунитут при фасциолезе мало изучен. Врожденный и возрастной иммунитет при этой болезни отсутствует.
Клинические признаки и течение. Клинические признаки зависят от интенсивности инвазии, вида фасциол, условий кормления и содержания животных, резистентности их организма.
Если в организме животного паразитируют единичные фасциолы, то владельцы животных и ветспециалисты не отмечают ни каких симптомов со стороны печени и желудочно- кишечного тракта. У здоровых животных, имеющих хорошую резистентность организма фасциолез протекает бессимптомно или очень со слабо выраженными клиническими признаками.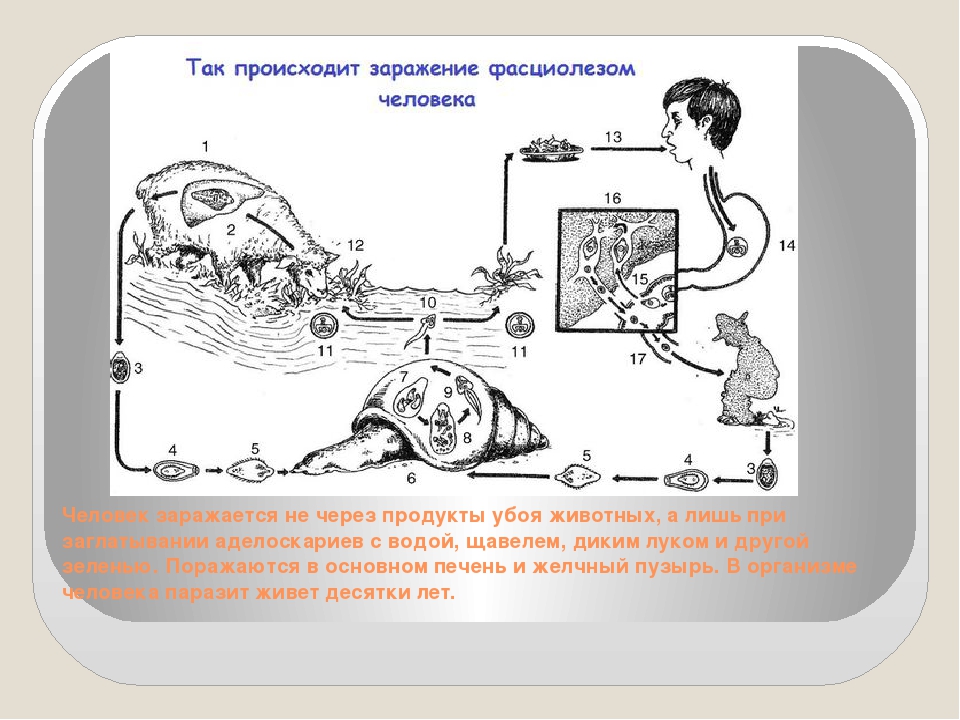 В то же время у животных ослабленных неполноценным, некачественным кормлением, при наличие сопутствующих заболеваний симптомы фасциолеза резко выражены, а очень слабые животные могут погибнуть.
В то же время у животных ослабленных неполноценным, некачественным кормлением, при наличие сопутствующих заболеваний симптомы фасциолеза резко выражены, а очень слабые животные могут погибнуть.
При фасциолезе различают острое и хроническое течение.
У овец через 1,5-2.5 мес. после заражения на пастбище владельцы животного отмечают прогрессирующую бледность коньюктивы (матово-белый цвет), а у отдельных животных желтушность слизистых оболочек. При проведении клинического осмотра регистрируем постоянную лихорадку (повышение температуры тела до 41,2-41,6 градусов), животное теряет аппетит, отмечаем нарушения со стороны желудочно-кишечного тракта вплоть до кровавого поноса, запор, тимпанию, угнетенное состояние, со стороны сердца тахикардию (до 100-180 ударов в мин), аритмию, снижение кровяного давления. Со стороны легких-поверхностное учащенное дыхание и одышку. Печень при пальпации увеличена и болезненная, брюшные мышцы напряжены.
У крупного рогатого скота при остром течение, которое бывает сравнительно редко владельцы животных и ветспециалисты отмечают: сильное угнетение, резкое сокращение вплоть до прекращения образования молока, повышенную кожную чувствительность, при пальпации увеличение и болезненность печени, у стельных коров- аборты, которые сопровождаются задержанием последа, переходящим в гнойный эндометрит.
Хроническое течение фасциолеза у овец и крупного рогатого скота бывает в период паразитирования половозрелых фасциол и сопровождается теми же клиническими признаками что и острое течение, но с менее выраженными клиническими признаками.
У овец дополнительно кроме общих клинических признаков отмечаем брюшную водянку, отек подчелюстного пространства, желтушность слизистых оболочек и прогрессирующее исхудание.
У молодых коров и молодняка крупного рогатого скота до 2 летнего возраста симптомы фасциолеза те же, что и у овец: угнетенное состояние, сонливость, бледность слизистых оболочек,склера имеет «фарфоровый» вид, глаза западают, кашель, печень при пальпации увеличена и болезненна, развивается истощение, происходит снижение молочной продуктивности, отмечаем выпадение шерсти, волос становится грубым без блеска.
Патологоанатомические изменения. При вскрытие павших и забиваемых на мясо фасциолезных животных в желчных путях печени и частично в тканях, расположенных по пути миграции к ней паразитов находим самих фасциол.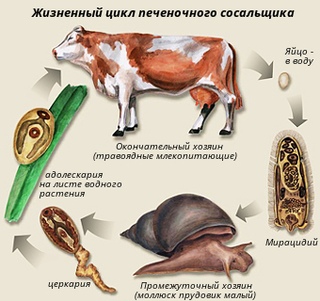 В печени отмечаем разрывы слизистой оболочки, клеточный инфильтрат, узелковые некротические очажки величиной с булавочную головку. В 12-ти перстной и начальной части тощей кишки мелкоточечные кровоизлияния. При остром течение фасциолеза-явления перигепатита, слипчивый перитонит, перфорирование и частичное разрушение печени, желчный пузырь расширен, в брюшной полости находим эксудат. На поверхности печени ветврач обнаруживает большое количество кровоточащих отверстий. При хроническом течение фасциолеза выявляем признаки хронического холангита, хронического паренхиматозного и интерстициального гепатита, желчные ходы расширены,пропитаны известь, выступают на поверхности в виде тяжей, а в запущенных случаях- цирроз печени. При проведении ветсанэкспертизы печени на разрезе выдавливаются фасциолы.
В печени отмечаем разрывы слизистой оболочки, клеточный инфильтрат, узелковые некротические очажки величиной с булавочную головку. В 12-ти перстной и начальной части тощей кишки мелкоточечные кровоизлияния. При остром течение фасциолеза-явления перигепатита, слипчивый перитонит, перфорирование и частичное разрушение печени, желчный пузырь расширен, в брюшной полости находим эксудат. На поверхности печени ветврач обнаруживает большое количество кровоточащих отверстий. При хроническом течение фасциолеза выявляем признаки хронического холангита, хронического паренхиматозного и интерстициального гепатита, желчные ходы расширены,пропитаны известь, выступают на поверхности в виде тяжей, а в запущенных случаях- цирроз печени. При проведении ветсанэкспертизы печени на разрезе выдавливаются фасциолы.
Диагноз. Прижизненный диагноз на фасциолез ветспециалистами ставится с учетом эпизоотологических, клинических данных и самое главное результатов гельмин- токапрологических исследований проб кала в ветеринарной лаборатории. В лабораториях наиболее распространен простой метод последовательных промываний, его недостаток невысокая эффективность (60%) Наиболее эффективен метод Щербовича и флотации с раствором нитрата свинца. Сейчас для диагностики фасциолеза получают распространение серологические и аллергические методы исследований. Посмертная и послеубойная диагностика для ветспециалиста не затруднительна, особенно когда паразиты достигли половой зрелости. Их обычно обнаруживают на разрезе в крупных желчных протоках печени и экссудате из брюшной полости.
В лабораториях наиболее распространен простой метод последовательных промываний, его недостаток невысокая эффективность (60%) Наиболее эффективен метод Щербовича и флотации с раствором нитрата свинца. Сейчас для диагностики фасциолеза получают распространение серологические и аллергические методы исследований. Посмертная и послеубойная диагностика для ветспециалиста не затруднительна, особенно когда паразиты достигли половой зрелости. Их обычно обнаруживают на разрезе в крупных желчных протоках печени и экссудате из брюшной полости.
Лечение. Для дегельминтизации в сельхозпредприятиях и у владельцев ЛПХ, КФХ применяют различные антгельментики: политрем, битионол, албендазол однократно в дозе 10мг на кг массы тела, фазинекс, рафоксанид однократно в виде суспензий через рот из расчета по АДВ: овцам-5 или 10мг. А кр.р.ск-6-12мг на 1 кг массы тела. Клозантел (фасковерм) овцам и крупному рогатому скоту вводят подкожно или внутримышечно по 1мл на 10кг или 1мл на 20кг живой массы тела.
Ацемидофен выпускают в порошке. Применяют при остром фасциолезе в дозе 150мг/кг. Для дегельминтизации фасциолеза применяют и другие антгельминтики.
Профилактика. Для профилактики фасциолеза хозяйства должны проводить комплекс мероприятий в который входит: использование культурных пастбищ, надлежащее оборудование мест водопоя, организация полноценного кормления, смена пастбищных участков каждые 2месяца, а если такая возможность отсутствует проводим однократную смену пастбищ в середине пастбищного сезона- в июле-августе. Проведение профилактической преимагинальной дегельминтизации в Центральном Федеральном округе в октябре-ноябре, лечебной — против половозрелых фасциол в январе-феврале, но не позднее чем за 45дней до начала пастбищного сезона.
Нельзя использовать для выпаса овец и кр.р.ск. заболоченные и сильно увлажненные пойменные луга с наличием на них промежуточных хозяев-прудовиков. Сено убранное с таких пастбищ рекомендуется скармливать животным не ранее чем через 3-6месяцев после его уборки. Владельцы ЛПХ, КФХ и сельхозпредприятия являющиеся стационарно неблагополучными по фасциолезу, в своих хозяйствах проводят плановые профилактические дегельминтизации согласно инструкции.
Владельцы ЛПХ, КФХ и сельхозпредприятия являющиеся стационарно неблагополучными по фасциолезу, в своих хозяйствах проводят плановые профилактические дегельминтизации согласно инструкции.
Для уничтожения моллюсков-промежуточных хозяев фасциол-проводится осушение заболоченных участков с использованием большой и малой мелиорации. Моллюсков можно уничтожать путем выжигания пересохшей травы на подсохших заболоченных участках, а также раствором медного купороса в концентрации 1:5000. Для профилактики фасциолеза следует практиковать круглогодичное стойловое содержание животных.
виды, причины, признаки, симптомы, лечение
Фасциолез – представляет собой внекишечный гельминтоз, обусловленный патологическим влиянием паразита на паренхиму печени и желчевыводящие протоки. Подобный недуг, относится к категории наиболее распространённых глистных инвазий человеческого организма. Источником недуга является возбудитель, которым может быть двуустка печёночная или двуустка гигантская. Помимо этого, клиницисты выделяют несколько путей заражения таким микроорганизмом.
Помимо этого, клиницисты выделяют несколько путей заражения таким микроорганизмом.
Онлайн консультация по заболеванию «Фасциолез».
Задайте бесплатно вопрос специалистам: Инфекционист.
В симптоматике преобладают неспецифические клинические проявления, которые характерны для большинства патологий печени. Сюда стоит отнести болезненность в зоне правого подреберья, тошноту, желтуху и увеличение размеров поражённого органа.
Поставить правильный диагноз можно на основании данных, полученных во время лабораторно-инструментальных обследований пациента. В терапии недуга преобладают консервативные методики, но при необходимости проводят хирургическое вмешательство.
Возбудителем фасциолеза человека могут стать два микроорганизма – печёночная и гигантская двуустка. Они относятся к одному подвиду, так как имеют большое количество общих морфологических признаков. Кроме этого, они могут спариваться друг с другом. Основным их отличием являются объёмы — печёночная двуустка в длину составляет до трёх сантиметров, а в ширину до 1. 3 см, а гигантская достигает восьми сантиметров в длину и двенадцати миллиметров в ширину.
3 см, а гигантская достигает восьми сантиметров в длину и двенадцати миллиметров в ширину.
Переносчиками выступают сельскохозяйственный скот, но только травоядной группы. Паразитирует фасциола в гепатобилиарной системе, в которой гельминты откладывают яйца, а они, в свою очередь, попадают в окружающую среду вместе с фекалиями животного, а дальнейшее развитие осуществляют в пресных водоёмах.
Биология развития фасциол
Пути заражения фасциолезом следующие:
- потребление в пищу обсеменённых дикорастущих растений – сюда можно отнести щавель и кресс-салат, огородную зелень и дикий лук;
- употребление сырой воды из сомнительных водоёмов;
- плохая санитарная обработка огородной зелени и овощей;
- употребление в пищу фасциолезной печени животного – при этом происходит попадание в кишечник человека транзиторных яиц, которые не провоцируют развитие недуга, но выявляются во время лабораторного изучения каловых масс;
- случайное попадание загрязнённой воды в ротовую полость во время купания.

Во всех случаях, кроме последнего, личинки возбудителя высвобождаются из своих оболочек в ЖКТ, после чего проникают в брюшину через стенку кишечника. Затем фасциола внедряется в паренхиму печени и проникает в желчевыводящие протоки. Не исключается иной путь миграции такого микроорганизма – гематогенный, т. е. с потоком крови.
Спустя примерно четыре месяца после попадания в организм человека, фасциолы достигают стадии половой зрелости и могут откладывать яйца. Сроки паразитирования могут варьироваться от пяти до десяти и более лет.
Гастроэнтерологи выделяют несколько стадий прогрессирования фасциолеза у людей, а именно:
- инкубационную фазу – это период с момента заглатывания фасциолы до появления первой симптоматики. Длиться такой период может от нескольких дней до трёх месяцев. Продолжительность зависит от таких факторов – количество проглоченных микроорганизмов и состояние иммунной системы человека;
- инвазивную или острую – выражается в миграции возбудителя недуга по желчным протокам;
- латентную или скрытую – длится от двух месяцев до нескольких лет и характеризуется бессимптомным протеканием.
 В таких случаях обнаружить протекание болезни можно лишь во время лабораторного изучения каловых масс или крови, а также при прохождении УЗИ. Такие мероприятия могут проводиться для диагностирования совершенно другого недуга или в качестве профилактической меры;
В таких случаях обнаружить протекание болезни можно лишь во время лабораторного изучения каловых масс или крови, а также при прохождении УЗИ. Такие мероприятия могут проводиться для диагностирования совершенно другого недуга или в качестве профилактической меры; - хроническую – отличается волнообразным течением и высокой вероятностью развития тяжёлых осложнений.
По локализации фасциолез может возникать не только в печени и желчных протоках, очень редко фасциолы поражают:
- головной мозг;
- лёгкие;
- органы зрения;
- евстахиевы трубы;
- гортань.
Фасциола
Исходя из того, в какой фазе протекает заболевание, будет отличаться его клиническая картина.
Первые симптомы фасциолеза, проявляемые в миграционную фазу, характеризуются следующим образом:
- возрастанием показателей температуры вплоть до лихорадки;
- общей слабостью и недомоганием;
- интенсивными головными болями;
- появлением высыпаний по типу крапивницы;
- гепатомегалией;
- сильным кожным зудом.

В инвазивную фазу недуга помимо вышеуказанных признаков наблюдаются следующие клинические проявления:
- боли в области эпигастрия и в зоне под правыми рёбрами;
- желтушность кожных покровов и видимых слизистых;
- повышение температуры до 40–42 градусов;
- постоянная тошнота;
- снижение или полное отсутствие аппетита;
- нарушение акта дефекации, что выражается в сильной диарее;
- повышенное газообразование;
- кашель и кровохарканье;
- одышка и ощущение болей в области грудины;
- гепатоспленомегалия – это состояние, при котором наблюдается одновременное увеличение печени и селезёнки;
- брюшная водянка;
- анемия.
Для хронического протекания, во время стадии обострения наиболее характерны такие симптомы:
- колебания АД от нормальных значений до высоких;
- нарушение ЧСС;
- приступообразные боли в правом боку;
- постоянная тяжесть в проекции поражённого органа;
- желчная колика;
- отвращение к жирной пище;
- тошнота;
- головокружение;
- желтуха.

Крайне редко фасциолез локализуется в глазном яблоке – при этом будет наблюдаться монокулярная слепота.
При появлении первых признаков необходимо как можно быстрее обратиться за помощью к терапевту или гастроэнтерологу. Именно такие специалисты могут провести первичный осмотр, назначить лабораторно-инструментальные обследования, на основании результатов которых поставят правильный диагноз и составят наиболее эффективную тактику лечения фасциолеза у человека.
Первый этап диагностических мероприятий направлен на работу врача с пациентом и включает в себя:
- изучение жизненного анамнеза больного – позволит выявить наиболее вероятный путь заражения фасциолами;
- тщательный физикальный осмотр пациента, включающий в себя пальпацию передней стенки брюшной полости, в частности в области правого подреберья, изучение состояния кожного покрова, а также измерение показателей давления, пульса и температуры;
- детальный опрос пациента – необходимо для выяснения начала проявления и интенсивности выраженности симптоматики недуга.
 Это даст возможность специалисту определить фазу протекания болезни.
Это даст возможность специалисту определить фазу протекания болезни.
Лабораторная диагностика фасциолеза предусматривает осуществление:
- клинического и биохимического анализа крови – для выявления анемии и признаков протекания патологического процесса;
- общего анализа урины;
- микроскопических исследований каловых масс – в фекалиях можно обнаружить яйца возбудителя;
- определения уровня АЛТ и АСТ, а также щелочной фосфатазы;
- серологических методов – РПГА и ИФА;
- изучения дуоденального содержимого.
В дополнение потребуется выполнение инструментальных обследований пациента, которые предполагают проведение:
- УЗИ брюшной полости;
- КТ печени;
- МРТ.
УЗИ брюшной полости
Фасциолез необходимо дифференцировать от таких недугов:
Для нейтрализации возбудителя болезни зачастую достаточно консервативных методик терапии, среди которых:
- приём лекарственных препаратов;
- соблюдение щадящего рациона;
- физиотерапевтические процедуры;
- применение народных средств – только после одобрения лечащего врача.

Медикаментозное лечение фасциолеза направлено на использование:
- противопаразитарных и антибактериальных средств – продолжительность терапии и суточная норма рассчитывается в индивидуальном порядке для каждого пациента;
- глюкокортикостероидов;
- жаропонижающих средств;
- антигистаминных веществ;
- блокаторов протонной помпы – при сильных болях в желудке;
- сорбентов и ферментов;
- спазмолитиков;
- желчегонных препаратов;
- специальных растворов для купирования обезвоживания, что может развиваться на фоне упорной рвоты или диареи.
Спустя три месяца и полгода с начала противопаразитарной терапии, осуществляется контрольное паразитологическое обследование, включающее в себя изучение фекалий на наличие яиц гельминтов и дуоденальное зондирование.
Общая программа лечения обязательно включает в себя соблюдение диеты. Диетотерапия предполагает полный отказ от:
- жирных и острых блюд;
- мучных и кондитерских изделий;
- морепродуктов и субпродуктов;
- копчёностей и солений;
- спиртных напитков.

В то же время основу рациона должны составлять:
- вегетарианские первые блюда;
- диетические сорта рыбы и мяса;
- каши, приготовленные на водной основе. Особое предпочтение стоит отдать гречке и рису;
- кисломолочная продукция;
- овощи, после прохождения ими термической обработки;
- запечённые фрукты;
- зелёный или травяной чай.
Все рекомендации касательно питания предоставляет гастроэнтеролог.
При неэффективности консервативного лечения, а также при развитии осложнений показано хирургическое вмешательство, которое может быть направлено на дренирование желчевыводящих путей или абсцесса печени.
Фасциолез – это довольно опасное заболевание, которое очень часто приводит к развитию таких осложнений:
Во избежание развития подобной болезни профилактика фасциолеза включает в себя:
- исключение употребления сырой воды из сомнительных водоёмов;
- контроль над тем, чтобы огородная зелень была тщательно промыта очищенной водой;
- своевременное обследование и дегельминтизация скота;
- регулярное посещение гастроэнтеролога для прохождения профилактического обследования.

Своевременное диагностирование и терапия болезни позволяет добиться полного выздоровления пациента. Игнорирование симптомов и нежелание обращаться за квалифицированной помощью чревато развитием осложнений, которые могут привести к летальному исходу.
Поделиться статьей:
Все ли корректно в статье с медицинской точки зрения?
Ответьте только в том случае, если у вас есть подтвержденные медицинские знания
Продолжающаяся зоонозная трематодная инфекция
Зоонозные трематодные инфекции являются областью забытых тропических болезней, которые вызывают большой интерес для глобального и общественного здравоохранения из-за связанной с ними заболеваемости. Фасциолез человека — это трематодный зооноз, представляющий интерес для общественного здравоохранения. От него страдают примерно 50 миллионов человек во всем мире, и более 180 миллионов подвержены риску заражения как в развитых, так и в слаборазвитых странах. Единая парадигма здоровья — это область, которая стремится решить проблему зоонозных инфекций с помощью комплексного и устойчивого подхода.В этом обзоре предпринята попытка рассмотреть основные проблемы в лечении фасциолеза человека и животных с использованием ценных идей, полученных от единой парадигмы здоровья до глобального здравоохранения и многопрофильной интеграции.
Единая парадигма здоровья — это область, которая стремится решить проблему зоонозных инфекций с помощью комплексного и устойчивого подхода.В этом обзоре предпринята попытка рассмотреть основные проблемы в лечении фасциолеза человека и животных с использованием ценных идей, полученных от единой парадигмы здоровья до глобального здравоохранения и многопрофильной интеграции.
1. Введение
Фасциолез — это болезнь жвачных животных, вызываемая двумя основными паразитическими трематодами, Fasciola hepatica и F. gigantica . За последние два десятилетия фасциолез человека получил признание как заболевание первостепенной важности. Человеческий фасциолез в настоящее время классифицируется как трематодная инфекция растительного / пищевого происхождения, обычно передающаяся при употреблении в пищу метацеркарий, инцистированных на листьях, которые едят как овощи [1].Фасциолез широко распространен среди пастушеских сообществ в странах с низким уровнем дохода из-за их постоянной тесной связи с домашним скотом, который они содержат.
Фасциолез был впервые зарегистрирован еще в 2000 году до нашей эры. Фасциолез животных вызывает серьезные заболевания среди овец и крупного рогатого скота, вызывая тяжелое физическое истощение. Это приводит к убыткам животноводческой отрасли Северной и Южной Америки в размере более 2 миллиардов долларов в год. Человеческий фасциолез также вызывает серьезные заболевания и заболеваемость, в основном среди фермеров с низким доходом.На сегодняшний день ни одна человеческая смерть не была напрямую связана с фасциолезом. Этот факт отводит болезни низкий приоритет и способствует тому, что ей не уделяется должного внимания как серьезной причине, вызывающей озабоченность в области общественного здравоохранения. Человеческий фасциолез в настоящее время причислен к зоонозам пищевых / растительных трематод как забытое тропическое заболевание (NTD) [2].
2. Материалы и методы
Мы провели поиск литературы по фасциолезу человека и животных за последние 15 лет. Мы провели поиск ресурсов PubMed / MEDLINE, HINARI / PubMed, местных, региональных и институциональных электронных библиотек, таких как электронная библиотека NIH, CDC, ВОЗ и IHI (Институт здравоохранения Ифакара, Танзания), East African Medical Journal и африканские журналы общественного здравоохранения, а также переносчиков и зоонозов для следующих основных ключевых слов: «фасциолез», «фасциолез человека», «зоонозы», «двуустка печени фасциолы», «фасциола гепатика», «фасциола гигантская», «фасциолез, F. hepatica »,« фасциолез F. gigantica »,« эпидемиология фасциолеза человека »,« распространение фасциолеза человека »,« тенденции в исследованиях фасциолеза »и« вспышки фасциолеза ». Мы провели поиск опубликованной литературы с 2000 по 2015 год. Мы также сослались на признанные полные статьи из учебников, а также на резюме и рефераты, содержащие различимое содержание. Мы выбрали ссылки, подходящие для включения в обзор. Мы исключили статьи и статьи / публикации, не переведенные на английский язык, которые были посвящены только болезням животных без зоонозного аспекта.Этот поиск позволил нам включить 92 наиболее релевантных ссылки из 300.
hepatica »,« фасциолез F. gigantica »,« эпидемиология фасциолеза человека »,« распространение фасциолеза человека »,« тенденции в исследованиях фасциолеза »и« вспышки фасциолеза ». Мы провели поиск опубликованной литературы с 2000 по 2015 год. Мы также сослались на признанные полные статьи из учебников, а также на резюме и рефераты, содержащие различимое содержание. Мы выбрали ссылки, подходящие для включения в обзор. Мы исключили статьи и статьи / публикации, не переведенные на английский язык, которые были посвящены только болезням животных без зоонозного аспекта.Этот поиск позволил нам включить 92 наиболее релевантных ссылки из 300.
3. Текущее состояние
Фасциолез — это в первую очередь болезнь жвачных животных, хотя за последние два десятилетия фасциолез человека приобрел значение как серьезное заболевание человека [1] . Человеческий фасциолез обычно характеризуется гипоэндемическим характером, с низкими и стабильными уровнями распространенности среди определенной популяции и обычно имеет очаговое эндемическое распространение. Однако на сегодняшний день сообщения поступали со всех континентов, кроме Антарктиды, что свидетельствует о широком космополитическом распространении [2].
Однако на сегодняшний день сообщения поступали со всех континентов, кроме Антарктиды, что свидетельствует о широком космополитическом распространении [2].
Среди зоонозных паразитарных болезней фасциолез человека в настоящее время классифицируется как трематодная инфекция, передаваемая через растения / продукты питания, с более высокой распространенностью среди сельскохозяйственных сообществ в странах с низким уровнем доходов [3, 4]. Трематоды растительного / пищевого происхождения включают в себя Fasciola hepatica, F. gigantica, и Fasciolopsis buski (семейство Fasciolidae), Gastrodiscoides hominis (семейство Gastrodiscidae), Watsonius 70008 и Paradiscidae, Watsonius 8 . Fasciola hepatica и F. gigantica инфицируют печень [5].
Фасциолиды и гастродисцид вызывают важные зоонозы, распространенные во многих странах, в то время как W. watsoni и F. elongatus были переданы человеку только случайно. Современный климат и глобальные изменения, по-видимому, все больше влияют на распространение гельминтозов, передаваемых улитками [6]. Это хороший пример возникающих / возобновляющихся паразитарных заболеваний во многих странах как следствие различных явлений, связанных с изменениями климата и окружающей среды, а также социально-экономической деятельностью человека [5, 7].
Это хороший пример возникающих / возобновляющихся паразитарных заболеваний во многих странах как следствие различных явлений, связанных с изменениями климата и окружающей среды, а также социально-экономической деятельностью человека [5, 7].
Несмотря на последние разработки в методах диагностики и эпиднадзора, в некоторых странах до сих пор полностью отсутствуют данные о фасциолезе человека. Это может быть связано с тем, что заболевание не является эндемическим, но более вероятно из-за неполной регистрации / диагностики, особенно в условиях ограниченных ресурсов. Недооцененное глобальное бремя болезни на сегодняшний день составляет примерно от 35 до 72 миллионов человек, а еще 180 миллионов подвержены риску заражения [8–10]. Обильные данные, подтверждающие инфицирование животных Fasciola , доступны во многих тропических развивающихся странах и регионах, с соответствующим присутствием видов улиток, ответственных за передачу.Таким образом, вероятность передачи фасциолеза животных человеку высока там, где обычна близость человека к домашним животным [3, 6].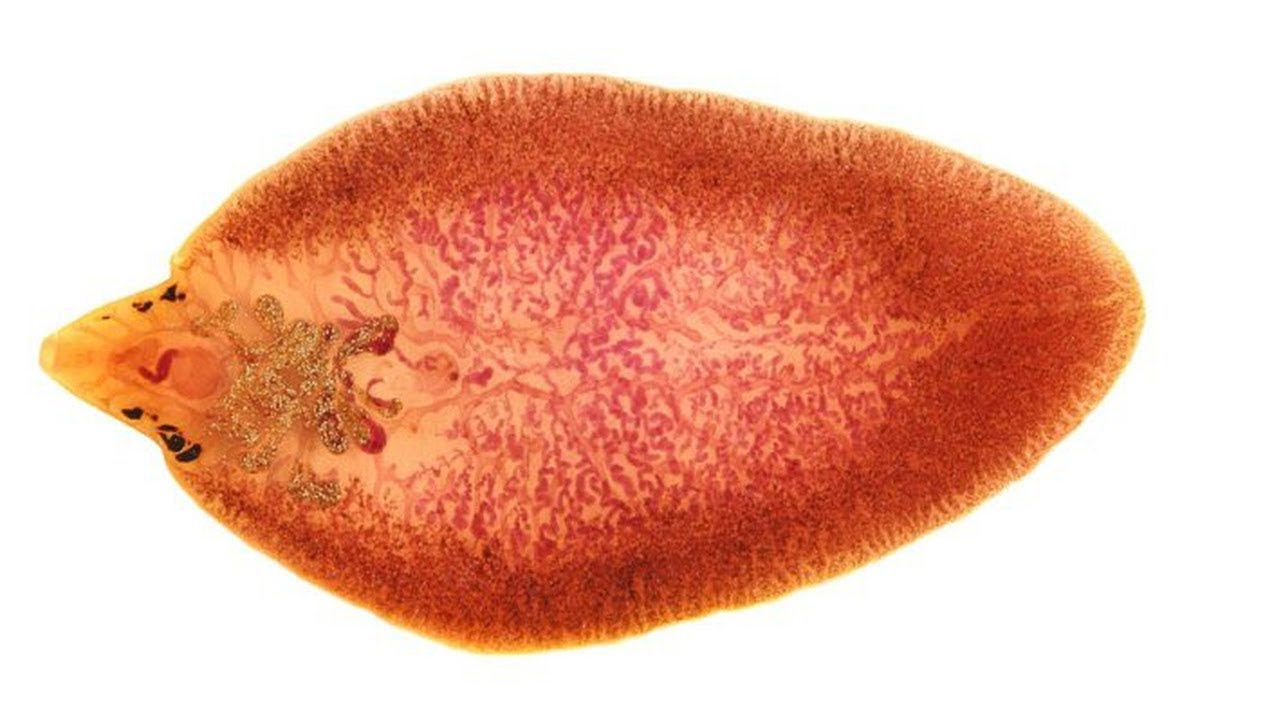
Хотя подходящая среда и взаимодействия для передачи были созданы во многих потенциально эндемичных районах, надежные методы диагностики и наблюдения, позволяющие установить наличие фасциолеза человека, обычно отсутствуют [2, 11, 12]. Кажущаяся редкость инфицирования человека фасциолезом в таких регионах недооценивает распространенность заболевания [9].Поскольку местные врачи могут не быть полностью осведомлены о фасциолезе человека, они могут принять фасциолез за другие заболевания с аналогичной клинической картиной [3, 13].
3.1. Распространение фасциолеза человека
На сегодняшний день фасциолез человека выявлен во многих странах. Наивысшая распространенность зарегистрирована в Боливии, Перу, Кубе, Китае, Испании, дельте Нила в Египте, центральных районах Вьетнама и Северном Иране [1, 14]. Фасциолез крупного рогатого скота является причиной большинства случаев передачи и равномерно распространяется по миру, вызывая 29% зоонозов [15].Гиперэндемичность фасциолеза человека была отмечена в регионе Ближнего Востока и Северной Африки (MENA) [16, 17], особенно в Египте [10, 18], Эфиопии [19], Иране [14, 20], Ираке [21], Сирии.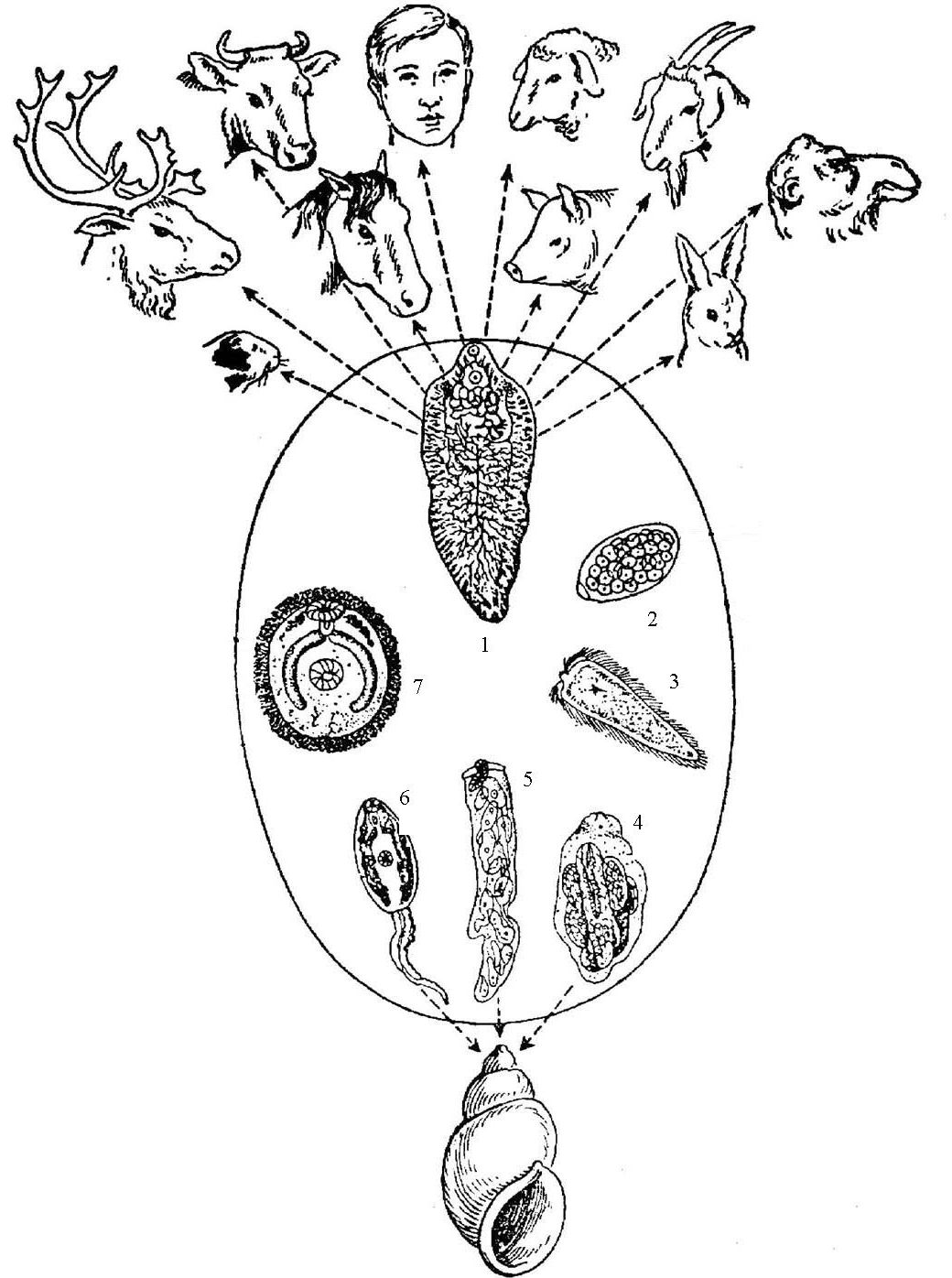 [16] и Саудовская Аравия [2].
[16] и Саудовская Аравия [2].
Самый высокий уровень распространенности зарегистрирован в южноамериканских высокогорных районах Боливии и Перу [9, 22]. Высокая распространенность фасциолеза у человека была связана с недавними изменениями климата, населенными пунктами и социально-экономической деятельностью [4, 7, 23]. Также в Южной Америке, Аргентина [3], Бразилия [24] и Мексика [25] недавно сообщили об эпидемиях человеческого фасциолиза.В Юго-Восточной Азии (ЮВА) и на Индийском субконтиненте, Камбоджа [7], Китай [26-28], Вьетнам [5], Сингапур [29], Филиппины и Индия [30-32] также недавно сообщили о росте числа случаев заболевания. болезней, которые ранее не наблюдались в национальных или региональных системах здравоохранения.
3.2. Фасциолез человека в Европе и Америке
Европа также имеет долгую историю болезни в Италии [33, 34] и Испании [1, 11], Турции [35–37], Великобритании [38, 39], Франции [6 ] и Греции [40]. Отдельные случаи зарегистрированы также из Северной Америки [41] и Кубы [42, 43]. Согласно недавним обзорам [1, 44, 45], фасциолез, вероятно, является самой распространенной паразитарной инфекцией в мире. С увеличением количества поездок, открытой свободной торговли в сочетании с экономической деятельностью и миграцией людей из сельских районов в города фасциолез должен стать серьезным заболеванием, представляющим интерес для общественного здравоохранения, путешествий и торговой медицины [15, 45–48].
Согласно недавним обзорам [1, 44, 45], фасциолез, вероятно, является самой распространенной паразитарной инфекцией в мире. С увеличением количества поездок, открытой свободной торговли в сочетании с экономической деятельностью и миграцией людей из сельских районов в города фасциолез должен стать серьезным заболеванием, представляющим интерес для общественного здравоохранения, путешествий и торговой медицины [15, 45–48].
3.3. Жизненный цикл Fasciola
Знание жизненного цикла паразита может способствовать стратегиям контроля, направленным либо на млекопитающего-хозяина, либо на переносчика.Зараженные млекопитающие, включая не только крупный рогатый скот, овец, буйволов, ослов и свиней, но также лошадей, коз, дромадеров, верблюдов, лам и других травоядных, переносят овулировавшие яйца со стулом в источники пресной воды [12, 19]. Поскольку червь Fasciola обитает в желчных протоках таких животных, его неэмбрионированные яйца попадают в кишечник с желчью и выводятся с фекалиями. Пресная вода необходима для развития промежуточных стадий вида Fasciola у улиток. Ресничный мирацидий вылупляется из яйца.Он вынашивает улитку из рода Lymnaea и развивается в спороцисту. Следующими стадиями развития являются редии и церкарии [5, 9], которые позже покидают улитку. Церкария может инфицировать окончательного хозяина-млекопитающего, включая людей, пассивно, когда хозяин пьет инфицированную воду, или может инфицировать листья, и хозяин-млекопитающее заражается, когда ест листья, содержащие метацеркарии [16].
Проглоченные эксцисты метацеркарии в двенадцатиперстной кишке мигрируют в брюшную полость и, наконец, достигают печени.Они проходят через капсулу печени и примерно через 12 недель попадают в желчные протоки, где начинают откладывать яйца. У инфицированных развивается гиперплазия желчных протоков. Клинически пациенты теряют аппетит, у них появляется тошнота и диарея. Часто наблюдаются крапивница, острая боль в эпигастрии, желтуха, эозинофилия и гепатомегалия. В хронической фазе заболевания возникает гиперплазия желчного пузыря и желчного эпителия, что приводит к обструкции желчевыводящих путей. Когда живые взрослые черви в инфицированной печени попадают в область горла, они вызывают дискомфорт.По прошествии примерно одного-двух месяцев развивается реакция гиперчувствительности в области глотки. Термин «синдром Хальзуна» описывает возникшую в результате удушающую иммунологическую реакцию в области глотки [6, 11, 16].
Факторы, которые, как отмечалось, способствуют увеличению передачи фасциолеза человеку, включают (i) высокую плотность популяций людей и животных, живущих в непосредственной близости, (ii) наличие скотобоен и влажных рынков, работающих с элементарной гигиеной, ограниченную холодовую цепь для распределения и низкий уровень инспекции мяса и мер биобезопасности, (iii) широкое потребление сырой / недоваренной крови, мяса, тканей органов и субпродуктов и потребление сырых листовых овощей, и (iv) использование неочищенных источников воды для домашнего использования и / или использование неочищенных сточных вод и сточных вод для сельского хозяйства [5, 6].
3.4. Улитки-переносчики и распространение фасциолеза в Африке
Распространение F. hepatica и F . gigantica паразитов распространены повсеместно, в основном они связаны с одинаково глобальным распределением жизнеспособных промежуточных хозяев пресноводных улиток [3, 5]. Распределение видов лимфатических улиток можно обобщить как преимущественно умеренное, на большей высоте более 2500 м над уровнем моря для Lymnaea truncatula, L.rubiginosa, и связанный с ними паразит, F. hepatica, , а L. rupestris и L. natalensis вместе со своим типичным паразитом F. gigantica имеют более тропическое / субтропическое распространение на более низких высотах, ниже 2000 м [ 17, 49, 50].
В нескольких странах Африки и Азии следует учитывать, что F. hepatica и F. gigantica сосуществуют, особенно в районах водосбора Нила, горных хребтов великих озер и рукавов рифтовой долины.В таких средах меняющиеся высоты и климатические условия благоприятствуют соответствующим переносчикам улиток [4, 11, 50]. Дифференциальный специфический диагноз, относящийся к яйцеклеткам и специфическим антигенам, представляет интерес из-за разницы в их передаче, эпидемиологии и мерах контроля [51]. В последнее время также упоминались смешанные инфекции и гибридизация [52–54].
Обследования, проведенные в гиперэндемичной долине дельты Нила в Египте [4, 18] и бассейне реки Тана в Эфиопии [19], обнаружили высокую связь между фасциолезом и шистосомозом, а также множеством других кишечных паразитов [19].Также было отмечено гендерное распределение с перекосом как по интенсивности, так и по преобладанию в сторону девочек в возрастной группе 9–11 лет среди молодого ключевого населения. Коинфекция и распространение в детском возрасте создают дополнительную разницу в клинической картине и этиологии паразитарных заболеваний на континенте, особенно в сельских районах, где разводят животных [4, 19].
Среди других африканских стран, сообщающих о разрозненных случаях заболевания фасциолезом человека, — Камерун [55], Чад [56], Сенегал [57], Южная Африка [58] и Зимбабве [59].С другой стороны, о фасциолезе животных широко сообщалось почти во всех странах африканского экваториального пояса [19], а также восточной, центральной, западной и южной Африки [4, 49, 50, 60, 61]. Кроме того, благоприятная климатическая и экологическая картина способствует легкой передаче инфекции от человека (рис. 1).
С другой стороны, странно, что в этих потенциально эндемичных регионах не появилось никаких опубликованных исследований или отчетов о заболевании людей.
3.5. Лечение
Триклабендазол (TCBZ) — препарат выбора при лечении фасциолеза.Однако в дополнение к изменяющейся структуре заболевания в литературе появились сообщения о резистентности к TCBZ [62–64], хотя не все они могут отражать подлинные случаи резистентности. Тем не менее, любые сообщения о резистентности вызывают беспокойство, потому что на сегодняшний день TCBZ — единственный препарат, показавший высокую эффективность против мигрирующей и ювенильной стадий инфекции [1, 3]. Устойчивость к препарату потенциально может свести на нет любые недавние успехи, достигнутые в усилиях по борьбе и лечению фасциолеза человека и животных.
3.6. Диагноз
Диагноз фасциолеза значительно изменился за три десятилетия, с тех пор как он стал заболеванием, имеющим первостепенное значение для человека. Обнаружение яиц в образцах стула пациентов до сих пор считается наиболее убедительным диагнозом на клиническом уровне [2, 9, 11]. Новые улучшенные копрологические тесты на антигены [65], серологические тесты и тесты ELISA [52, 66], радиологическая диагностика и визуализация [30, 67, 68], а также высокоспецифичные молекулярные методы [26, 69] были разработаны и в настоящее время являются отличительной чертой звуковых и научных исследований в данной области [1, 70].Выявление устойчивых штаммов, дифференциация острых и хронических стадий инфекции и выявление повторных инфекций после лечения все еще остаются проблемой на клиническом уровне.
Геопространственное распределение улиток-переносчиков и передачи паразитов [59, 71, 72] и зоонозная эпидемиология [3, 27] являются недавними областями развития в области прогнозирования и планирования эпидемий фасциолеза человека. Модельные препараты и вмешательства [62, 73] также являются областями новых исследований по эффективному лечению фасциолеза человека и животных.
4. Проблемы, вызывающие непосредственное беспокойство в связи с фасциолезом в наименее развитых странах
Хотя фасциолез был признан заболеванием, имеющим важное значение для человека, он по-прежнему считается в первую очередь болезнью животных, особенно овец и крупного рогатого скота [74]. Недостаточная осведомленность представляет собой серьезное препятствие на пути эффективного лечения фасциолеза человека [1, 2]. К сожалению, во многих наименее развитых странах, страдающих от бедности и инфекционных заболеваний, человеческий фасциолез не является признанным заболеванием и не подлежит регистрации.Осведомленность и сенсибилизация являются ключевыми первыми шагами к любым запланированным стратегиям вмешательства.
К счастью, на сегодняшний день не зарегистрировано смертей, непосредственно связанных с инфицированием человека фасциолезом. Это неизбежно приписывает этой болезни низкий приоритет в сфере оказания неотложной медицинской помощи, что делает ее одной из наиболее игнорируемых тропических болезней [75]. Сообщается также, что заболевание гораздо чаще встречается среди девочек школьного возраста. Связанное с этим влияние болезни на заболеваемость и количество лет жизни с поправкой на инвалидность (DALY) вызывает большее беспокойство [16, 36].Последующие хронические заболевания приводят к значительному снижению качества жизни, ожидаемой продолжительности и продуктивности, поскольку взрослый червь может жить более 10 лет в подходящем хозяине [4, 19].
Имеются лишь разрозненные сообщения о вспышках фасциолеза на орошаемых сельскохозяйственных территориях, свободных от домашних животных [18, 19]. Наибольшая доля зарегистрированных случаев носит зоонозный характер, поэтому любые стратегии вмешательства в идеале должны также решать проблему на ветеринарном уровне.О фасциолезе человека почти не сообщают в тех странах, где он широко распространен [4, 76, 77]. В таких областях следует внедрять программы бдительного надзора и скрининга с упором на междисциплинарное участие представителей различных профессий [5, 54].
Глобальная осведомленность и единый медицинский подход к зоонозам на сегодняшний день являются наиболее комплексным подходом к фасциолезу [45]. По-прежнему требуются постоянные усилия, в том числе меры контроля за торговлей и путешествиями, чтобы ограничить распространение инфицированных животных из одной страны в другую.Улучшенные программы гигиены воды и пищевых продуктов являются еще одним важным компонентом программ контроля [44, 74]. Вовлечение заинтересованных сторон и политическая воля для поддержки таких стратегий имеют решающее значение для эффективного внедрения этих вмешательств.
Окончательные сообщения о лекарственной устойчивости к триклабендазолу [78] следует тщательно исследовать и искать альтернативные варианты лечения. Разработка вакцин также должна стать областью будущих исследований. Смешанные инфекции с другими трематодами или кишечными паразитами [17, 79–81] затрудняют раннее выявление фасциолеза.Запоздалые и пропущенные диагнозы, особенно среди молодого ключевого населения, усиливают влияние болезни на DALY [82, 83].
5. Вызовы будущего
В XXI веке произошел расцвет знаний о фасциолезе человека, о чем свидетельствует количество публикаций по этой теме за последние 10 лет. Полное внедрение этих новых знаний и их воплощение в ощутимые результаты остается проблемой для наименее развитых стран (НРС). Население НРС подвержено наибольшему риску заболевания по следующим причинам: (i) плохой доступ к этому новому комплексу знаний, (ii) ограниченные ресурсы для практического использования, или (iii) наличие этих ограниченных ресурсов, предназначенных для «Более опасные» проблемы, чем фасциолез [1, 2, 45].Цикл бедности и болезни действительно представляет собой порочный автокаталитический каскад.
Типичный сценарий осложняющего инфекционного контроля зоонозных инфекций, включая фасциолез, в Африке к югу от Сахары включает: (а) глобальное потепление и гражданские беспорядки, (б) близость к домашним животным, (в) миграцию из сельских в городские районы с бедным персоналом и водой. и гигиена пищевых продуктов, и (d) слабые системы биобезопасности и надзора. Следовательно, программы борьбы с фасциолезом человека должны иметь комплексный подход, при котором учитываются все факторы, способствующие наличию заболевания [44, 75].
Достигнуты новейшие достижения в области диагностики, наблюдения и лечения фасциолеза. Однако развивающиеся страны и особенно общины с низкими доходами не могут получить доступ к этим достижениям из-за бедности. Из-за тяжелого бремени болезней, гражданских беспорядков и конкуренции за ограниченные ресурсы неудивительно, что почти нет сообщений о фасциолезе человека из этих регионов [2, 4]. Программы борьбы должны сначала рассмотреть возможность проведения кампаний по усилению осведомленности и повышения осведомленности как о масштабах, так и о воздействии фасциолиза человека на людей и животных [44].
Нынешний «Комплексный глобальный подход к болезням« Единое здоровье »» представляет собой, безусловно, наиболее полное и совместное решение не только для лечения фасциолеза человека, но и для большинства зоонозных заболеваний в целом [44, 85]. Классический пример проблем, которые он решает, лучше всего можно сформулировать в недавней кампании «Go Green» как здорового подхода к современному искусственному образу жизни. Разделение на отдельные разделы, такие как питание и профилактическая медицина, сельское хозяйство и промышленность, привело к беспрецедентному увеличению потребления свежих, сырых / зеленых фруктов и овощей [86, 87].Однако это плохо подкрепляется безопасностью воды, контролем за использованием удобрений и пестицидов и управлением отходами. Потребление плохо контролируемых, выращенных и хранимых свежих зеленых овощей способствовало увеличению распространения растительных / пищевых трематод, включая фасциолез, среди многих других проблем со здоровьем [48, 83].
Контролируемые клинические испытания по изучению зарегистрированных случаев резистентности Fasciola к триклабендазолу и битионолу представляют собой области, представляющие непосредственный исследовательский интерес.Дальнейшая разработка вариантов химиотерапии, таких как мирра производный мирзид и нитазоксанид [19, 73, 88], а также другие новые вмешательства, нацеленные на промежуточных хозяев улиток [71, 89], могут обеспечить столь необходимую альтернативную химиотерапию. Стратегии борьбы с животными-резервуарами и активный надзор за очагами заболеваний позволяют осуществлять раннее вмешательство, в то время как повышение безопасности пищевых продуктов и воды в сочетании с возможной разработкой вакцины жизненно важно для стратегий профилактики фасциолеза человека.Чтобы добиться успеха, все это должно быть подкреплено тщательной осведомленностью, информационными кампаниями и политической волей для максимального использования [75, 90].
Человеческий фасциолез воспринимается как «забытая тропическая болезнь бедности» с низким значением [16, 42, 45, 87]. По мере того, как вмешательства и решения этой болезни разрабатываются в более развитых странах / сообществах, структуры поддержки, основные удобства и простое междисциплинарное сотрудничество одинаково быстро деградируют в сообществах с самым низким уровнем дохода и особенно высоким риском заражения [74, 75].Наглядным примером является обилие ветеринарных отчетов о фасциолезе животных из стран Африки к югу от Сахары, которым противопоставлено почти полное пренебрежение зоонозами человека медицинским сообществом и общественным здравоохранением [49, 50, 53]. Удивительно, что человеческий фасциолез до сих пор не регистрируется во многих из этих стран.
Однако из-за преобладающих в настоящее время простых и быстрых путешествий по всему миру, открытых рынков и свободной торговли, культурного туризма и массовой культурной и национальной интеграции проблемы развивающихся стран могут перекинуться на более развитые страны [39, 45, 46].Начало непредсказуемых климатических изменений и их влияние на экобиологию, гражданские беспорядки и простые естественные законы эволюции — это факторы, которые изменили характер распространения зоонозов [47, 48]. Например, недавняя глобальная угроза, вызванная вспышкой вируса Эбола в Западной Африке, является новым напоминанием о далеко идущих последствиях неожиданных вспышек болезни на континенте [75, 91]. Человеческий фасциолез по-прежнему не летален, и результаты вмешательств, проводимых в большинстве гиперэндемичных регионов, доказывают, что с ним можно эффективно бороться, если не искоренить.Как NTD, это должно быть осязаемой целью [74, 87].
6. Заключение
Тот факт, что отчеты о человеческом фасциолезе в наименее развитых странах отсутствуют, представляет собой особенно сложную проблему. Эти страны уже сильно обременены различными заболеваниями и не имеют доступа к адекватным ресурсам. Таким образом, несмотря на значительный прогресс в диагностике и борьбе с фасциолезом человека в более развитых странах, это заболевание продолжает оставаться серьезной проблемой общественного здравоохранения [84, 92].
Распад междисциплинарного сотрудничества в сочетании с политическими и гражданскими беспорядками еще больше увековечивает распространенность многих болезней, включая фасциолез, в развивающихся странах. Мы предлагаем, чтобы меры борьбы с фасциолезом включали (i) общую и клиническую осведомленность, (ii) интегрированное и междисциплинарное сотрудничество, (iii) постоянные вмешательства, поддерживаемые политической волей, и (iv) разработку вакцин и лекарств.
Конфликт интересов
Th
Фасциолоз
Фасциолоз , также известный как Фасциолез , Фасциолаз , дистоматоз и гниль печени 9000, гриппозная гниль 9 (глистная гниль печени 9167 печеночная двуустка обыкновенная) и Fasciola gigantica .Это заболевание относится к трематодным зоонозам, передаваемым растениями. В Европе, Америке и Океании вызывает беспокойство только F. hepatica , но распространение обоих видов частично совпадает во многих областях Африки и Азии. [1]
Окончательный диапазон хозяев очень широк и включает многих травоядных млекопитающих, включая человека. Жизненный цикл включает пресноводных улиток как промежуточных хозяев паразита. [2] В последнее время мировая потеря продуктивности животных из-за фасциолеза по консервативным оценкам составила более 3 долларов США.2 миллиарда в год. [3] Кроме того, фасциолез теперь признан новым заболеванием человека: по оценкам Всемирной организации здравоохранения (ВОЗ) 2,4 миллиона человек инфицированы Fasciola , а еще 180 миллионов находятся в группе риска. [4]
Fasciola hepatica
Этиология
Фасциолез вызывается двумя дигенетическими трематодами: F. hepatica и F. gigantica . Взрослые двуустки обоих видов локализуются в желчных протоках печени или желчного пузыря. F. hepatica имеет размеры от 2 до 3 см и имеет космополитическое распространение. F. gigantica имеет длину от 4 до 10 см, а распространение этого вида ограничено тропиками и было зарегистрировано в Африке, на Ближнем Востоке, в Восточной Европе, а также в Южной и Восточной Азии. [2] В домашнем скоте в Японии описаны диплоидные (2n = 20), триплоидные (3n = 30) и химерные сосальщики (2n / 3n), многие из которых воспроизводятся партеногенетически. В результате этой нечеткой классификации сосальщиков в Японии обычно называют Fasciola spp. [5] Недавние отчеты, основанные на анализе митохондриальных генов, показали, что японцы Fasciola spp. более близок к F. gigantica , чем к F. hepatica . [6] В Индии у слонов был описан вид под названием F. jacksoni . [7]
Географическое распространение
Фасциолоз человека и животных встречается во всем мире. [2] В то время как фасциолез животных распространен в странах с высокой продуктивностью крупного рогатого скота и овец, фасциолез человека встречается, за исключением Западной Европы, в развивающихся странах.Фасциолез возникает только в тех областях, где существуют подходящие условия для промежуточных хозяев.
Фасциолез человека
Исследования, проведенные в последние годы, показали, что фасциолоз человека является важной проблемой общественного здравоохранения. [8] Человеческий фасциолоз был зарегистрирован в странах Европы, Америки, Азии, Африки и Океании. Заболеваемость людей растет в 51 стране на пяти континентах. [9] [10] Общий анализ показывает, что ожидаемая корреляция между фасциолозом животных и человека проявляется только на базовом уровне.Высокая распространенность среди людей не обязательно обнаруживается в районах, где фасциолоз представляет собой серьезную ветеринарную проблему. Например, в Южной Америке гиперэндемия и мезоэндемия встречаются в Боливии и Перу, где ветеринарная проблема менее важна, тогда как в таких странах, как Уругвай, Аргентина и Чили, фасциолез человека носит спорадический или гипоэндемический характер. [10]
Европа
В Европе фасциолез человека встречается в основном во Франции, Испании, Португалии и бывшем СССР. [10] Франция считается важным эндемичным для человека районом. С 1970 по 1982 год в девяти французских больницах было зарегистрировано в общей сложности 5863 случая фасциолоза человека. [11] Что касается бывшего Советского Союза, то почти все зарегистрированные случаи были из Таджикской Республики. [10] Несколько статей касались фасциолеза человека в Турции. [12] Недавно в некоторых частях Турции было проведено серологическое исследование фасциолоза человека. Серологически установлено, что распространенность заболевания составляет 3 человека.01% в провинции Анталия и от 0,9 до 6,1% в провинции Испарта Средиземноморского региона Турции. [13] В других европейских странах фасциолез носит спорадический характер, и возникновение болезни обычно сочетается с поездками в эндемичные районы.
Америка
В Северной Америке заболевание носит очень спорадический характер. В Мексике зарегистрировано 53 случая. В Центральной Америке фасциолез является проблемой для здоровья человека на Карибских островах, особенно в зонах Пуэрто-Рико и Кубы.Провинции Пинар-дель-Рио и Вилья-Клара — кубинские регионы, где фасциолез был гиперэндемичным. В Южной Америке фасциолез человека является серьезной проблемой в Боливии, Перу и Эквадоре. Эти страны Анд считаются регионом с самой высокой распространенностью фасциолеза человека в мире. Известные районы гиперэндемии человека расположены преимущественно на высокогорной равнине, называемой альтиплано. В северной части Боливии на Альтиплано распространенность, выявленная в некоторых сообществах, составила до 72% и 100% в копрологических и серологических исследованиях, соответственно. [9] В Перу по всей стране встречается F. hepatica у людей. Самые высокие показатели распространенности были зарегистрированы в Арекипе, долине Мантаро, долине Кахамарка и регионе Пуно. [1] В других странах Южной Америки, таких как Аргентина, Уругвай, Бразилия, Венесуэла и Колумбия, человеческий фасциолоз носит спорадический характер, несмотря на высокую распространенность фасциолеза у крупного рогатого скота.
Африка
В Африке случаи заболевания людей фасциолезом, за исключением северных районов, зарегистрированы нечасто.Наибольшая распространенность была зафиксирована в Египте, где болезнь распространена среди общин, проживающих в дельте Нила. [1]
Азия
В Азии больше всего случаев заболевания людей было зарегистрировано в Иране, особенно в провинции Гилан на берегу Каспийского моря. Было отмечено, что в Иране выявлено более 10 000 случаев заболевания людей. В Восточной Азии фасциолез человека носит спорадический характер. Несколько случаев было зарегистрировано в Японии, Кореях, Вьетнаме и Таиланде. [9]
Австралия и Океания
В Австралии фасциолез человека встречается очень редко (зарегистрировано всего 12 случаев).В Новой Зеландии F. hepatica никогда не обнаруживали у людей. [9]
Фасциолоз животных
Страны, где неоднократно регистрировался фасциолез домашнего скота:
- Европа: Великобритания, Ирландия, Франция, Португалия, Испания, Швейцария, Италия, Нидерланды, Турция, Германия, Польша
- Азия: Россия, Таиланд, Ирак, Иран, Китай, Вьетнам, Индия, Непал, Япония, Корея, [Филиппины
- Африка: Кения, Зимбабве, Нигерия, Египет, Гамбия, Марокко
- Австралия и Океания: Австралия, Новая Зеландия
- Америка: США, Мексика, Куба, Перу, Чили, Уругвай, Аргентина, Ямайка, Бразилия
8 сентября 2007 года сотрудники ветеринарной службы Южного Котабато, Филиппины, заявили, что лабораторные анализы образцов от коров, карабао и лошадей в 10 городах провинции и одиноком городе показали уровень заражения 89.5%, внезапное увеличение числа положительных случаев среди крупного рогатого скота из-за неустойчивых погодных условий в этом районе. Их необходимо немедленно лечить, чтобы не допустить осложнений при суррах и геморрагических сепсисах. Сурра уже затронула все барангаи города Сураллы. [14]
Источник инфекции для человека и передача
Человек F. hepatica Инфекция определяется наличием промежуточных хозяев улиток, домашних травоядных животных, климатических условий и пищевых привычек человека. [8] Овцы, козы и крупный рогатый скот считаются основными резервуарами животных. Хотя другие животные могут быть инфицированы, они обычно не имеют большого значения для передачи болезней человеку. С другой стороны, некоторые авторы заметили, что ослы и свиньи способствуют передаче болезней в Боливии. [15] Среди диких животных было продемонстрировано, что перидоместные крысы ( Rattus rattus ) могут играть важную роль в распространении, а также в передаче паразита на Корсике. [16] Во Франции нутрия ( Myocastor coypus ) была подтверждена как дикий резервуарный хозяин F. hepatica . [17] Люди заражаются при употреблении в пищу водных растений, содержащих инфицированные метацеркарии. [18] Некоторые виды водных овощей известны как переносчики инфекции человека. В Европе — Nasturtium officinale (кресс-салат обыкновенный), N. silvestris , Rorippa amphibia (дикий кресс-салат), Taraxacum dens leonis (листья одуванчика), Valerianella olitora (листья ягненка). Сообщалось, что (мята колосистая) является источником заражения людей. [9] В Северном Боливии на Альтиплано некоторые авторы предположили, что некоторые водные растения, такие как берё-берё (кресс-салат), водоросли (водоросли), кьоско и тортора, могут выступать в качестве источника инфекции для людей. [19] Поскольку церкарий F. hepatica также инцистируют на поверхности воды, люди могут заразиться, выпив свежую неочищенную воду, содержащую метацеркарии. [8] Кроме того, экспериментальное исследование показало, что люди, потребляющие сырые блюда из печени из свежей печени, инфицированной молодыми сосальщиками, могут заразиться. [20]
Промежуточные хозяева
Galba truncatula — самый частый промежуточный хозяин F. hepatica в Европе и Южной Америке.
Основные статьи: Fasciola hepatica # Жизненный цикл и Fasciola gigantica # Промежуточные хозяева
Промежуточные хозяева F. hepatica — пресноводные улитки семейства Lymnaeidae. [2] [21] Улитки из семейства Planorbidae очень редко выступают в качестве промежуточного хозяина для F. hepatica . [1]
Патогенез
Развитие инфекции у дефинитивного хозяина делится на две фазы: паренхиматозную (мигрирующую) фазу и билиарную фазу . [22] Паренхиматозная фаза начинается, когда выделенные молодые сосальщики проникают через стенку кишечника. После проникновения в кишечник сосальщики мигрируют в брюшную полость и проникают в печень или другие органы. F. hepatica имеет сильную склонность к тканям печени. [23] Иногда могут возникать эктопические локализации сосальщиков, такие как легкие, диафрагма, стенка кишечника, почки и подкожная ткань. [8] [24] Во время миграции сосальщиков ткани механически разрушаются, и вокруг путей миграции сосальщиков возникает воспаление. Вторая фаза (желчная фаза) начинается, когда паразиты попадают в желчные протоки печени. В желчных протоках сосальщики созревают, питаются кровью и производят яйца. Гипертрофия желчных протоков, связанная с закупоркой просвета, возникает в результате повреждения тканей.
Клинические признаки
У человека
Гипертрофия желчных протоков в печени, вызванная F. hepatica (секция печени; коза)
Взрослые двуустки Fasciola hepatica в желчных протоках (печень козла)
Течение фасциолеза у человека имеет 4 основных фазы: [9]
- Фаза инкубации : от попадания метацеркарий в организм до появления первых симптомов; период: от нескольких дней до 3 месяцев; зависит от количества проглоченных метацеркарий и иммунного статуса хозяина
- Инвазивная или острая фаза : миграция двуустки в желчные протоки.Эта фаза является результатом механического разрушения ткани печени и брюшины мигрирующими молодыми сосальщиками, вызывающими локальные и / или общие токсические и аллергические реакции. [25] Основные симптомы этой фазы:
- Скрытая фаза : Эта фаза может длиться месяцами или годами. Доля бессимптомных субъектов в этой фазе неизвестна. Они часто обнаруживаются во время семейного скрининга после того, как пациенту поставлен диагноз. [9]
- Хроническая или обструктивная фаза :
Эта фаза может развиваться через месяцы или годы после первоначального заражения.Взрослые сосальщики в желчных протоках вызывают воспаление и гиперплазию эпителия. Возникающие в результате холангит и холецистит в сочетании с большим количеством сосальщиков достаточны, чтобы вызвать механическую обструкцию желчных протоков. На этой стадии желчная колика, боль в эпигастрии, непереносимость жирной пищи, тошнота, желтуха, зуд, болезненность в правом верхнем квадранте живота и т. Д. Являются клиническими проявлениями, неотличимыми от холангита, холецистита и холелитиаза другого происхождения.Увеличение печени может быть связано с увеличением селезенки или асцитом. В случае непроходимости желчный пузырь обычно увеличен и отечен с утолщением стенки. Часто встречаются фиброзные спайки желчного пузыря с соседними органами. Литиаз желчного протока или желчного пузыря встречается часто, камни обычно маленькие и множественные. [9]
У животных
Клинические признаки фасциолеза всегда тесно связаны с инфекционной дозой (количеством проглоченных метацеркарий).У овец, как наиболее частых окончательных хозяев, клинические проявления делятся на 4 типа: [22] [23]
- Острый фасциолез I типа : инфекционная доза составляет более 5000 метацеркарий, попавших внутрь. Овцы внезапно умирают без каких-либо предшествующих клинических признаков. У овец могут наблюдаться асцит, кровотечение из живота, желтуха, бледность плодных оболочек, слабость.
- Острый фасциолез II типа : инфекционная доза составляет 1000-5000 метацеркарий, попавших внутрь.Как и выше, овцы умирают, но на короткое время проявляют бледность, потерю кондиции и асцит.
- Подострый фасциолоз : инфекционная доза составляет 800–1000 метацеркарий при приеме внутрь. Овцы вялые, анемичные и могут умереть. Похудание является доминирующим признаком.
- Хронический фасциолоз : инфекционная доза составляет 200-800 метацеркарий при приеме внутрь. Бессимптомное или постепенное развитие бутылочной челюсти и асцита (вентральный отек), исхудание, похудание.
В крови анемия, гипоальбуминемия и эозинофилия могут наблюдаться при всех типах фасциолеза. [23] Повышение активности ферментов печени, таких как глутаматдегидрогеназа (GLDH), гамма-глутамилтрансфераза (GGT) и лактатдегидрогеназа (LDH), выявляется при подостром или хроническом фасциолозе через 12-15 недель после приема метацеркарий. . [26] [27] Экономический эффект фасциолеза у овец заключается в внезапной гибели животных, а также в снижении привеса и производства шерсти. [28] [29] У коз и крупного рогатого скота клинические проявления аналогичны овцам.Однако приобретенная устойчивость к инфекции F. hepatica хорошо известна у взрослого крупного рогатого скота. [30] [31] Телята восприимчивы к болезням, но обычно требуется более 1000 метацеркарий, чтобы вызвать клинический фасциолоз. В этом случае болезнь похожа на болезнь овец и характеризуется потерей веса, анемией, гипоальбуминемией и (после заражения 10000 метацеркариями) смертью. [24] Важность фасциолеза крупного рогатого скота заключается в экономических потерях, вызванных повреждением печени при убое, и производственных потерях, особенно из-за снижения привеса. [32]
У овец, а иногда и крупного рогатого скота, поврежденная ткань печени может инфицироваться бактериями Clostridium C. novyi типа B. Бактерии выделяют токсины в кровоток, что приводит к так называемой болезни черных. Лечения нет, и смерть наступает быстро. Поскольку C. novyi широко распространена в окружающей среде, черная болезнь встречается там, где пересекаются популяции печеночных двуусток и овец. [33]
Устойчивость к инфекции
Механизмы устойчивости были изучены несколькими авторами у разных видов животных.Эти исследования могут помочь лучше понять иммунный ответ на F. hepatica у хозяина и необходимы при разработке вакцины против паразита. Было установлено, что крупный рогатый скот приобретает устойчивость к заражению F. hepatica и F. gigantica , когда они были сенсибилизированы первичным патентом или инфекцией, сокращенной лекарственным средством. [30] Устойчивость к фасциолезу была также зарегистрирована у крыс. [34] С другой стороны, овцы и козы не устойчивы к повторному заражению F.hepatica . [35] [36] Однако есть свидетельства того, что две породы овец, в частности индонезийская овца с тонким хвостом и красная овца масаи, устойчивы к F. gigantica . [37] [38] Сообщений о резистентности у людей нет.
Диагноз
У людей диагноз фасциолоза обычно устанавливается паразитологически, обнаруживая яйца двуустки в кале, и иммунологически — с помощью ELISA и вестерн-блоттинга.Копрологические исследования стула сами по себе, как правило, неадекватны, поскольку у инфицированных людей важные клинические проявления возникают задолго до того, как в стуле обнаруживаются яйца. Более того, при многих инфекциях человека яйца двуустки часто не обнаруживаются в фекалиях даже после многократных исследований фекалий. [8] [39] Кроме того, яйца F. hepatica , F. gigantica и Fasciolopsis buski морфологически неотличимы. [39] Таким образом, иммунонологические методы, такие как ELISA и иммуноэлектротрансферный блот, также называемый вестерн-блоттингом, являются наиболее важными методами диагностики F.hepatica инфекция. Эти иммунологические тесты основаны на обнаружении видоспецифических антител в сыворотке крови. Используемые антигенные препараты в основном были получены из экстрактов экскреторных / секреторных продуктов взрослых червей или с частично очищенными фракциями. [40] Недавно были использованы очищенные нативные и рекомбинантные антигены, например рекомбинантная L-подобная протеаза катепсина F. hepatica . [41] Методы, основанные на обнаружении антигена (циркулирующего в сыворотке или фекалиях), используются реже.Кроме того, биохимические и гематологические исследования сыворотки крови человека подтверждают точный диагноз (эозинофилия, повышение уровня ферментов печени). Также можно использовать УЗИ и РТГ брюшной полости, биопсию печени и пунктированного желчного пузыря. Ложный фасциолоз (псевдофасциолоз) означает присутствие яиц в стуле не в результате фактической инфекции, а в результате недавнего проглатывания инфицированной печени, содержащей яйца. Этой ситуации (с ее вероятностью ошибочного диагноза) можно избежать, если за несколько дней до повторного исследования кала пациент будет соблюдать диету без печени. [40] У животных прижизненная диагностика основана преимущественно на исследованиях фекалий и иммунологических методах. Однако необходимо учитывать клинические признаки, биохимический и гематологический профиль, время года, климатические условия, эпидемиологическую ситуацию и обследования улиток. [2] [22] Как и у людей, исследования фекалий ненадежны. Кроме того, яйца двуустки обнаруживаются в фекалиях через 8–12 недель после заражения. Несмотря на это, в некоторых странах исследование кала по-прежнему является единственным диагностическим инструментом.В то время как копрологический диагноз фасциолоза возможен через 8–12 недель после инфицирования (WPI), специфические антитела F. hepatica распознаются с помощью ELISA или вестерн-блоттинга через 2–4 недели после заражения. [42] [43] Таким образом, эти методы обеспечивают раннее обнаружение инфекции.
Лечение и профилактика
Антигельминтики
У человека
Для высокой эффективности и безопасности триклабендазол (Эгатен) в дозе 10–12 мг / кг является препаратом выбора при фасциолозе человека. [44] Альтернативы лекарственным препаратам для человека отсутствуют. С другой стороны, нитазоксаниды успешно применялись при лечении фасциолоза человека в Мексике. [45] Битионол — еще один препарат выбора, используемый для лечения F. hepatica . [46] Совсем недавно Миразид, египетский препарат, сделанный из мирры, был исследован в качестве перорального средства для лечения заболеваний, вызванных трематодами, включая фасциолез. [47]
У животных
Формула триклабендазола
Для борьбы с фасциолезом у животных использовался ряд препаратов.Лекарства различаются по эффективности, способу действия, цене и жизнеспособности. Фасциолициды (препараты против Fasciola spp.) Делятся на пять основных химических групп: [48]
- Галогенированные фенолы : битионол (Bitin), гексахлорофен (Bilevon), нитроксинил (Trodax)
- Салициланилиды : клозантел (Flukiver, Supaverm), рафоксанид (Flukanide, Ranizole)
- Бензимидазолы : триклабендазол (Fasinex), альбендазол (Vermitan, Valbazen), мебендазол (Telmin), люксабендазол (Fluxacur)
- Сульфаниламиды : клорсулон (Ivomec Plus)
- Феноксиалканы : диамфенетид (корибан)
Триклабендазол (Фазинекс) считается наиболее распространенным препаратом из-за его высокой эффективности против взрослых и молодых сосальщиков.Триклабендазол используется для борьбы с фасциолезом домашнего скота во многих странах. Тем не менее, длительное ветеринарное применение триклабендазола привело к появлению устойчивости к F. hepatica . Устойчивость к триклабендазолу у животных была впервые описана в Австралии, [49] , позже в Ирландии [50] и Шотландии [51] и совсем недавно в Нидерландах. [52] Учитывая этот факт, ученые приступили к разработке нового лекарства. a b c d e h Mas-Coma, S; Барг, доктор медицины, Эстебан Дж. Г. (1999). «Человеческий фасциолез». В Далтоне, JP. Фасциолез . Уоллингфорд, Оксон, Великобритания: CABI Pub. С. 411–34. Ibarra F, Vera Y, Quiroz H, et al. (февраль 2004 г.). «Определение эффективной дозы экспериментального фасциолицида у естественно и экспериментально зараженного крупного рогатого скота». Вет. Паразитол. 120 (1-2): 65–74. DOI: 10.1016 / j.vetpar.2003.12.005. PMID 15019144. http://linkinghub.elsevier.com/retrieve/pii/S0304401703005053.
Внешние ссылки
определение фасциолоза и синонимов фасциолоза (на английском языке)
Фасциолоз , также известный как фасциолез , фасциолаз , дистоматоз и гниль печени , является важным гельминтозом , вызываемым двумя трепетами. печеночная двуустка обыкновенная) и Fasciola gigantica .Это заболевание относится к трематодным зоонозам, передаваемым растениями. В Европе, Америке и Океании вызывает беспокойство только F. hepatica , но распространение обоих видов частично совпадает во многих областях Африки и Азии. [1]
Окончательный диапазон хозяев очень широк и включает многих травоядных млекопитающих, включая человека. Жизненный цикл включает пресноводных улиток как промежуточных хозяев паразита. [2] В последнее время мировая потеря продуктивности животных из-за фасциолеза по консервативным оценкам составила более 3 долларов США.2 миллиарда в год. [3] Кроме того, фасциолез теперь признан новым заболеванием человека: по оценкам Всемирной организации здравоохранения (ВОЗ) 2,4 миллиона человек инфицированы Fasciola , а еще 180 миллионов находятся в группе риска. [4]
Fasciola hepatica
Этиология
Фасциолез вызывается двумя дигенетическими трематодами: F. hepatica и F. gigantica . Взрослые двуустки обоих видов локализуются в желчных протоках печени или желчного пузыря. F. hepatica имеет размеры от 2 до 3 см и имеет космополитическое распространение. F. gigantica имеет длину от 4 до 10 см, а распространение этого вида ограничено тропиками и было зарегистрировано в Африке, на Ближнем Востоке, в Восточной Европе, а также в Южной и Восточной Азии. [2] В домашнем скоте в Японии описаны диплоидные (2n = 20), триплоидные (3n = 30) и химерные сосальщики (2n / 3n), многие из которых воспроизводятся партеногенетически. В результате этой нечеткой классификации сосальщиков в Японии обычно называют Fasciola spp. [5] Недавние отчеты, основанные на анализе митохондриальных генов, показали, что японцы Fasciola spp. более близок к F. gigantica , чем к F. hepatica . [6] В Индии у слонов был описан вид под названием F. jacksoni . [7]
Географическое распространение
Фасциолоз человека и животных встречается во всем мире. [2] В то время как фасциолез животных распространен в странах с высокой продуктивностью крупного рогатого скота и овец, фасциолез человека встречается, за исключением Западной Европы, в развивающихся странах.Фасциолез возникает только в тех областях, где существуют подходящие условия для промежуточных хозяев.
Фасциолоз человека
Исследования, проведенные в последние годы, показали, что фасциолоз человека является важной проблемой общественного здравоохранения. [8] Человеческий фасциолоз был зарегистрирован в странах Европы, Америки, Азии, Африки и Океании. Заболеваемость людей растет в 51 стране на пяти континентах. [9] [10] Общий анализ показывает, что ожидаемая корреляция между фасциолозом животных и человека проявляется только на базовом уровне.Высокая распространенность среди людей не обязательно обнаруживается в районах, где фасциолоз представляет собой серьезную ветеринарную проблему. Например, в Южной Америке гиперэндемия и мезоэндемия встречаются в Боливии и Перу, где ветеринарная проблема менее важна, тогда как в таких странах, как Уругвай, Аргентина и Чили, фасциолез человека носит спорадический или гипоэндемический характер. [10]
Европа
В Европе фасциолез человека встречается в основном во Франции, Испании, Португалии и бывшем СССР. [10] Франция считается важным эндемичным для человека районом. С 1970 по 1982 год в девяти французских больницах было зарегистрировано в общей сложности 5863 случая фасциолоза человека. [11] Что касается бывшего Советского Союза, то почти все зарегистрированные случаи были из Таджикской Республики. [10] Несколько статей касались фасциолеза человека в Турции. [12] Недавно в некоторых частях Турции было проведено серологическое исследование фасциолоза человека. Серологически установлено, что распространенность заболевания составляет 3 человека.01% в провинции Анталия и от 0,9 до 6,1% в провинции Испарта Средиземноморского региона Турции. [13] В других европейских странах фасциолез носит спорадический характер, и возникновение болезни обычно сочетается с поездками в эндемичные районы.
Америка
В Северной Америке заболевание носит очень спорадический характер. В Мексике зарегистрировано 53 случая. В Центральной Америке фасциолез является проблемой для здоровья человека на Карибских островах, особенно в зонах Пуэрто-Рико и Кубы.Провинции Пинар-дель-Рио и Вилья-Клара — это регионы Кубы, где фасциолез был гиперэндемичным. В Южной Америке фасциолез человека является серьезной проблемой в Боливии, Перу и Эквадоре. Эти страны Анд считаются регионом с самой высокой распространенностью фасциолеза человека в мире. Известные районы гиперэндемии человека расположены преимущественно на высокогорной равнине, называемой альтиплано. В северной части Боливии на Альтиплано распространенность, выявленная в некоторых сообществах, составила до 72% и 100% в копрологических и серологических исследованиях, соответственно. [9] В Перу по всей стране встречается F. hepatica у людей. Самые высокие показатели распространенности были зарегистрированы в Арекипе, долине Мантаро, долине Кахамарка и регионе Пуно. [1] В других странах Южной Америки, таких как Аргентина, Уругвай, Бразилия, Венесуэла и Колумбия, человеческий фасциолоз носит спорадический характер, несмотря на высокую распространенность фасциолеза у крупного рогатого скота.
Африка
В Африке случаи заболевания людей фасциолезом, за исключением северных районов, зарегистрированы нечасто.Наибольшая распространенность была зафиксирована в Египте, где болезнь распространена среди общин, проживающих в дельте Нила. [1]
Азия
В Азии больше всего случаев заболевания людей было зарегистрировано в Иране, особенно в провинции Гилан на берегу Каспийского моря. Было отмечено, что в Иране выявлено более 10 000 случаев заболевания людей. В Восточной Азии фасциолез человека носит спорадический характер. Несколько случаев было зарегистрировано в Японии, Кореях, Вьетнаме и Таиланде. [9]
Австралия и Океания
В Австралии фасциолез человека встречается очень редко (зарегистрировано всего 12 случаев).В Новой Зеландии F. hepatica никогда не обнаруживали у людей. [9]
Фасциолоз животных
Страны, где неоднократно регистрировался фасциолез домашнего скота:
- Европа: Великобритания, Ирландия, Франция, Португалия, Испания, Швейцария, Италия, Нидерланды, Турция, Германия, Польша
- Азия: Россия, Таиланд, Ирак, Иран, Китай, Вьетнам, Индия, Непал, Япония, Корея, Филиппины
- Африка: Кения, Зимбабве, Нигерия, Египет, Гамбия, Марокко
- Австралия и Океания: Австралия, Новая Зеландия
- Америка: США, Мексика, Куба, Перу, Чили, Уругвай, Аргентина, Ямайка, Бразилия
8 сентября 2007 года сотрудники ветеринарной службы Южного Котабато, Филиппины, заявили, что лабораторные анализы образцов от коров, карабао и лошадей в 10 городах провинции и одиноком городе показали уровень заражения 89.5%, внезапное увеличение числа положительных случаев среди крупного рогатого скота из-за неустойчивых погодных условий в этом районе. Их необходимо лечить немедленно, чтобы не допустить осложнений при сурра и геморрагическом сепсисе. Сурра уже затронула все барангаи города Сураллы. [14]
Источник инфекции для человека и передача
Человек F. hepatica Инфекция определяется наличием промежуточных хозяев улиток, домашних травоядных животных, климатических условий и пищевых привычек человека. [8] Овцы, козы и крупный рогатый скот считаются основными резервуарами животных. Хотя другие животные могут быть инфицированы, они обычно не имеют большого значения для передачи болезней человеку. С другой стороны, некоторые авторы заметили, что ослы и свиньи способствуют передаче болезней в Боливии. [15] Среди диких животных было продемонстрировано, что перидоместные крысы ( Rattus rattus ) могут играть важную роль в распространении, а также в передаче паразита на Корсике. [16] Во Франции нутрия ( Myocastor coypus ) была подтверждена как дикий резервуарный хозяин F. hepatica . [17] Люди заражаются при употреблении в пищу водных растений, содержащих инфицированные метацеркарии. [18] Некоторые виды водных овощей известны как переносчики инфекции человека. В Европе — Nasturtium officinale (кресс-салат обыкновенный), N. silvestris , Rorippa amphibia (дикий кресс-салат), Taraxacum dens leonis (листья одуванчика), Valerianella olitora (листья ягненка). Сообщалось, что (мята колосистая) является источником заражения людей. [9] В Северном Боливии на Альтиплано некоторые авторы предположили, что некоторые водные растения, такие как берё-берё (кресс-салат), водоросли (водоросли), кьоско и тортора, могут выступать в качестве источника инфекции для людей. [19] Поскольку церкарий F. hepatica также инцистируют на поверхности воды, люди могут заразиться, выпив свежую неочищенную воду, содержащую метацеркарии. [8] Кроме того, экспериментальное исследование показало, что люди, потребляющие сырые блюда из печени из свежей печени, инфицированной молодыми сосальщиками, могут заразиться. [20]
Промежуточные хозяева
Galba truncatula — самый частый промежуточный хозяин F. hepatica в Европе и Южной Америке.
Основные статьи: Fasciola hepatica # Жизненный цикл и Fasciola gigantica # Промежуточные хозяева
Промежуточные хозяева F. hepatica — пресноводные улитки семейства Lymnaeidae. [2] [21] Улитки из семейства Planorbidae очень редко выступают в качестве промежуточного хозяина для F. hepatica . [1]
Патогенез
Развитие инфекции у дефинитивного хозяина делится на две фазы: паренхиматозную (мигрирующую) фазу и билиарную фазу . [22] Паренхиматозная фаза начинается, когда выделенные молодые сосальщики проникают через стенку кишечника. После проникновения в кишечник сосальщики мигрируют в брюшную полость и проникают в печень или другие органы. F. hepatica имеет сильную склонность к тканям печени. [23] Иногда могут возникать эктопические локализации сосальщиков, такие как легкие, диафрагма, стенка кишечника, почки и подкожная ткань. [8] [24] Во время миграции сосальщиков ткани механически разрушаются, и вокруг путей миграции сосальщиков возникает воспаление. Вторая фаза (желчная фаза) начинается, когда паразиты попадают в желчные протоки печени. В желчных протоках сосальщики созревают, питаются кровью и производят яйца. Гипертрофия желчных протоков, связанная с закупоркой просвета, возникает в результате повреждения тканей.
Клинические признаки
У человека
Гипертрофия желчных протоков в печени, вызванная F. hepatica (разрез печени; коза)
Взрослые двуустки Fasciola hepatica в желчных протоках (печень козла)
Течение фасциолеза у человека имеет 4 основных фазы: [9]
- Фаза инкубации : от попадания метацеркарий в организм до появления первых симптомов; период: от нескольких дней до 3 месяцев; зависит от количества проглоченных метацеркарий и иммунного статуса хозяина
- Инвазивная или острая фаза : миграция двуустки в желчные протоки.Эта фаза является результатом механического разрушения ткани печени и брюшины мигрирующими молодыми сосальщиками, вызывающими локальные и / или общие токсические и аллергические реакции. [25] Основные симптомы этой фазы:
- Скрытая фаза : Эта фаза может длиться месяцами или годами. Доля бессимптомных субъектов в этой фазе неизвестна. Они часто обнаруживаются во время семейного скрининга после того, как пациенту поставлен диагноз. [9]
- Хроническая или обструктивная фаза :
Эта фаза может развиваться через месяцы или годы после первоначального заражения.Взрослые сосальщики в желчных протоках вызывают воспаление и гиперплазию эпителия. Возникающие в результате холангит и холецистит в сочетании с большим количеством сосальщиков достаточны, чтобы вызвать механическую обструкцию желчных протоков. На этой стадии желчная колика, боль в эпигастрии, непереносимость жирной пищи, тошнота, желтуха, зуд, болезненность в правом верхнем квадранте живота и т. Д. Являются клиническими проявлениями, неотличимыми от холангита, холецистита и холелитиаза другого происхождения.Увеличение печени может быть связано с увеличением селезенки или асцитом. В случае непроходимости желчный пузырь обычно увеличен и отечен с утолщением стенки. Часто встречаются фиброзные спайки желчного пузыря с соседними органами. Литиаз желчного протока или желчного пузыря встречается часто, камни обычно маленькие и множественные. [9]
У животных
Клинические признаки фасциолеза всегда тесно связаны с инфекционной дозой (количеством проглоченных метацеркарий).У овец, как наиболее частых окончательных хозяев, клинические проявления делятся на 4 типа: [22] [23]
- Острый фасциолез I типа : инфекционная доза составляет более 5000 метацеркарий, попавших внутрь. Овцы внезапно умирают без каких-либо предшествующих клинических признаков. У овец могут наблюдаться асцит, кровотечение из живота, желтуха, бледность плодных оболочек, слабость.
- Острый фасциолез II типа : инфекционная доза составляет 1000-5000 метацеркарий, попавших внутрь.Как и выше, овцы умирают, но на короткое время проявляют бледность, потерю кондиции и асцит.
- Подострый фасциолоз : инфекционная доза составляет 800–1000 метацеркарий при приеме внутрь. Овцы вялые, анемичные и могут умереть. Похудание является доминирующим признаком.
- Хронический фасциолоз : инфекционная доза составляет 200-800 метацеркарий при приеме внутрь. Бессимптомное или постепенное развитие бутылочной челюсти и асцита (вентральный отек), исхудание, похудание.
В крови анемия, гипоальбуминемия и эозинофилия могут наблюдаться при всех типах фасциолеза. [23] Повышение активности ферментов печени, таких как глутаматдегидрогеназа (GLDH), гамма-глутамилтрансфераза (GGT) и лактатдегидрогеназа (LDH), выявляется при подостром или хроническом фасциолозе через 12-15 недель после приема метацеркарий. . [26] [27] Экономический эффект фасциолеза у овец заключается в внезапной гибели животных, а также в снижении привеса и производства шерсти. [28] [29] У коз и крупного рогатого скота клинические проявления аналогичны овцам.Однако приобретенная устойчивость к инфекции F. hepatica хорошо известна у взрослого крупного рогатого скота. [30] [31] Телята восприимчивы к болезням, но обычно требуется более 1000 метацеркарий, чтобы вызвать клинический фасциолоз. В этом случае болезнь похожа на болезнь овец и характеризуется потерей веса, анемией, гипоальбуминемией и (после заражения 10000 метацеркариями) смертью. [24] Важность фасциолеза крупного рогатого скота заключается в экономических потерях, вызванных повреждением печени при убое, и производственных потерях, особенно из-за снижения привеса. [32]
У овец, а иногда и крупного рогатого скота, поврежденная ткань печени может инфицироваться бактериями Clostridium C. novyi типа B. Бактерии выделяют токсины в кровоток, что приводит к так называемой болезни черных. Лечения нет, и смерть наступает быстро. Поскольку C. novyi широко распространена в окружающей среде, черная болезнь встречается там, где пересекаются популяции печеночных двуусток и овец. [33]
Устойчивость к инфекции
Механизмы устойчивости были изучены несколькими авторами у разных видов животных.Эти исследования могут помочь лучше понять иммунный ответ на F. hepatica у хозяина и необходимы при разработке вакцины против паразита. Было установлено, что крупный рогатый скот приобретает устойчивость к заражению F. hepatica и F. gigantica , когда они были сенсибилизированы первичным патентом или инфекцией, сокращенной лекарственным средством. [30] Устойчивость к фасциолезу была также зарегистрирована у крыс. [34] С другой стороны, овцы и козы не устойчивы к повторному заражению F.hepatica . [35] [36] Однако есть свидетельства того, что две породы овец, в частности индонезийская овца с тонким хвостом и красная овца масаи, устойчивы к F. gigantica . [37] [38] Сообщений о резистентности у людей нет.
Диагноз
У людей диагноз фасциолоза обычно устанавливается паразитологически, обнаруживая яйца двуустки в кале, и иммунологически — с помощью ELISA и вестерн-блоттинга.Копрологические исследования стула сами по себе, как правило, неадекватны, поскольку у инфицированных людей важные клинические проявления возникают задолго до того, как в стуле обнаруживаются яйца. Более того, при многих инфекциях человека яйца двуустки часто не обнаруживаются в фекалиях даже после многократных исследований фекалий. [8] [39] Кроме того, яйца F. hepatica , F. gigantica и Fasciolopsis buski морфологически неотличимы. [39] Таким образом, иммунонологические методы, такие как ELISA и иммуноэлектротрансферный блот, также называемый вестерн-блоттингом, являются наиболее важными методами диагностики F.hepatica инфекция. Эти иммунологические тесты основаны на обнаружении видоспецифических антител в сыворотке крови. Используемые антигенные препараты в основном были получены из экстрактов экскреторных / секреторных продуктов взрослых червей или с частично очищенными фракциями. [40] Недавно были использованы очищенные нативные и рекомбинантные антигены, например рекомбинантный катепсин F. hepatica L [требуется значений ] -подобная протеаза. [41] Методы, основанные на обнаружении антигена (циркулирующего в сыворотке или фекалиях), используются реже.Кроме того, биохимические и гематологические исследования сыворотки крови человека подтверждают точный диагноз (эозинофилия, повышение уровня ферментов печени). Также можно использовать УЗИ и RTG [ разрешение ] брюшной полости, биопсию печени и пунктировку желчного пузыря. Ложный фасциолоз (псевдофасциолоз) означает присутствие яиц в стуле не в результате фактической инфекции, а в результате недавнего проглатывания инфицированной печени, содержащей яйца. Этой ситуации (с ее вероятностью ошибочного диагноза) можно избежать, если за несколько дней до повторного исследования кала пациент будет соблюдать диету без печени. [40] У животных прижизненная диагностика основана преимущественно на исследованиях фекалий и иммунологических методах. Однако необходимо учитывать клинические признаки, биохимический и гематологический профиль, время года, климатические условия, эпидемиологическую ситуацию и обследования улиток. [2] [22] Как и у людей, исследования фекалий ненадежны. Кроме того, яйца двуустки обнаруживаются в фекалиях через 8–12 недель после заражения. Несмотря на это, в некоторых странах исследование кала по-прежнему является единственным диагностическим инструментом.В то время как копрологический диагноз фасциолоза возможен через 8–12 недель после инфицирования (WPI), специфические антитела F. hepatica распознаются с помощью ELISA или вестерн-блоттинга через 2–4 недели после заражения. [42] [43] Таким образом, эти методы обеспечивают раннее обнаружение инфекции.
Лечение и профилактика
Антигельминтики
У человека
Из-за высокой эффективности и безопасности триклабендазол (Эгатен) в дозе 10–12 мг / кг является препаратом выбора при фасциолозе человека. [44] Лечение празиквантелом неэффективно. [45] [46] Имеются сообщения о случаях успешного применения нитазоксанида для лечения фасциолоза человека в Мексике. [47] Имеются также сообщения об успешном использовании битионола. [48]
Совсем недавно Миразид, египетский препарат, изготовленный из мирры, был исследован в качестве перорального средства для лечения заболеваний, вызванных трематодами, включая фасциолез. [49]
У животных
Формула триклабендазола
Для борьбы с фасциолезом у животных использовался ряд препаратов.Лекарства различаются по эффективности, способу действия, цене и жизнеспособности. Фасциолициды (препараты против Fasciola spp.) Делятся на пять основных химических групп: [50]
Триклабендазол (Фазинекс) считается наиболее распространенным препаратом из-за его высокой эффективности против взрослых и молодых сосальщиков. Триклабендазол используется для борьбы с фасциолезом домашнего скота во многих странах. Тем не менее, длительное ветеринарное применение триклабендазола привело к появлению устойчивости к F.hepatica . У животных устойчивость к триклабендазолу впервые была описана в Австралии, [51] , позже в Ирландии [52] и Шотландии [53] и совсем недавно в Нидерландах. [54] Учитывая этот факт, ученые приступили к разработке нового лекарства. Недавно в Мексике был успешно протестирован новый фасциолицид на естественно и экспериментально зараженном рогатом скоте. Этот новый препарат называется «соединение альфа» и по химическому составу очень похож на триклабендазол. a b c d e h Mas-Coma, S; Барг, доктор медицины, Эстебан Дж. Г. (1999). «Человеческий фасциолез». В Далтоне, JP. Фасциолез . Уоллингфорд, Оксон, Великобритания: CABI Pub. С. 411–34. Ibarra F, Vera Y, Quiroz H, et al. (февраль 2004 г.). «Определение эффективной дозы экспериментального фасциолицида у естественно и экспериментально зараженного крупного рогатого скота». Вет. Паразитол. 120 (1–2): 65–74. DOI: 10.1016 / j.vetpar.2003.12.005. PMID 15019144. http://linkinghub.elsevier.com/retrieve/pii/S0304401703005053.
Внешние ссылки
фасциолопсисов. Причины, симптомы, лечение фасциолопсис
Fasciolopsis: Паразит, являющийся крупнейшим кишечным сосальщиком человека.Известен в науке как Fasciolopsis buski и широко известен как гигантская кишечная двуустка. Заражение происходит главным образом в Азии и на Индийском субконтиненте, особенно в районах, где люди разводят свиней и потребляют пресноводные растения. Незрелые яйца двуустки в фекалиях человека попадают в пресную воду, где они вылупляются и образуют так называемые мирацидии. При контакте с улитками-хозяевами мирацидии проникают в них и образуют церкарии. Церкарии поражают различные растения, такие как водяной каштан, лотос (на корнях), водяной бамбук и другие водные овощи.Люди заражаются при употреблении этих сырых овощей. Большинство инфекций протекает легко и бессимптомно. Тяжелая инфекция может вызвать тошноту, диарею, нарушение всасывания или кишечную непроходимость. Диагноз ставится путем микроскопической идентификации яиц двуустки или, реже, взрослых двуусток в стуле или рвотных массах. Празиквантел — препарат выбора для лечения.
Инфекция фасциолопсиса известна как фасциолопсис.
DPDx — Fasciolopsiasis — Центры по контролю за заболеваниями
и… Возбудитель: трематода Fasciolopsis buski … Возбудитель, жизненный цикл и географическое распространение
Очистка от паразитов — Fasciolopsis buski —
Альтернативное лекарство … Fasci Fasciolopsis buski обитает в тонком кишечнике человека и свиней. Имея длину до 80 мм, это одна из самых крупных трематод, встречающихся у человека.


 В таких случаях обнаружить протекание болезни можно лишь во время лабораторного изучения каловых масс или крови, а также при прохождении УЗИ. Такие мероприятия могут проводиться для диагностирования совершенно другого недуга или в качестве профилактической меры;
В таких случаях обнаружить протекание болезни можно лишь во время лабораторного изучения каловых масс или крови, а также при прохождении УЗИ. Такие мероприятия могут проводиться для диагностирования совершенно другого недуга или в качестве профилактической меры;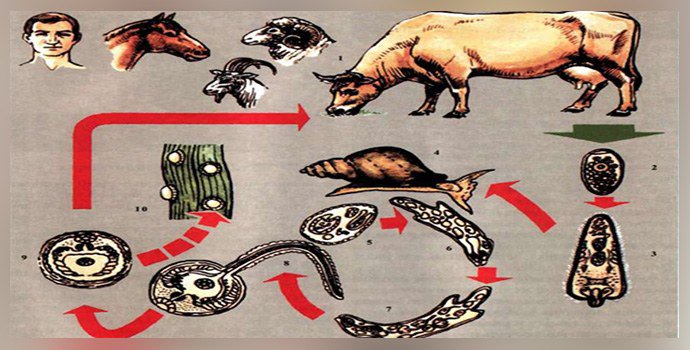

 Это даст возможность специалисту определить фазу протекания болезни.
Это даст возможность специалисту определить фазу протекания болезни.