Подводные камни при лечении больных хроническим гепатитом с, инфицированных генотипами 2 и 3 вируса гепатита с Текст научной статьи по специальности «Клиническая медицина»
ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Подводные камни при лечении больных хроническим гепатитом С, инфицированных генотипами 2 и 3 вируса гепатита С
О.О. Знойко1, К. Р. Дудина1, А.Н. Козина1, Д.О. Ленкова1, О.В. Калинина2, Н.Д. Ющук1
ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России — ФБУН «Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Пастера»
Проанализированы результаты клинико-лабораторного обследования 29 больных хроническим гепатитом С (ХГС), инфицированных 2 и 3 генотипами НСУ, получавших противовирусную терапию (ПВТ) пегили-рованным интерфероном и рибавирином в течение 24 нед. Выполнена оценка роли комплекса факторов -предикторов отсутствия устойчивого вирусологического ответа на двойную ПВТ у больных ХГС, инфицированных генотипами 2 и 3 НСУ, с учетом особенностей вирусного генома. В исследуемой группе лечение оказалось неэффективным в 14% (4/29) случаев. У пациентов, не ответивших на ПВТ, были выявлены как известные предикторы неуспеха двойной ПВТ (такие как ожирение, стеатоз печени и исходно высокий уровень виремии), так и факторы, связанные с особенностями вируса. У 2 пациентов основной причиной неэффективности лечения является наличие рекомбинантного варианта RF2k/1b НСУ, не выявляемого стандартными коммерческими тест-системами при определении генотипа вируса. В одном случае при сек-венировании установлена микст-инфекция генотипами 1Ь и 3а НСУ. Рекомендовано определять генотип НСУ до начала ПВТ тест-системами, в которых предусмотрены возможность субтипирования генотипа 1 по NS5В-области или проведение секвенирования NS5B-региона генома НСУ.
Выполнена оценка роли комплекса факторов -предикторов отсутствия устойчивого вирусологического ответа на двойную ПВТ у больных ХГС, инфицированных генотипами 2 и 3 НСУ, с учетом особенностей вирусного генома. В исследуемой группе лечение оказалось неэффективным в 14% (4/29) случаев. У пациентов, не ответивших на ПВТ, были выявлены как известные предикторы неуспеха двойной ПВТ (такие как ожирение, стеатоз печени и исходно высокий уровень виремии), так и факторы, связанные с особенностями вируса. У 2 пациентов основной причиной неэффективности лечения является наличие рекомбинантного варианта RF2k/1b НСУ, не выявляемого стандартными коммерческими тест-системами при определении генотипа вируса. В одном случае при сек-венировании установлена микст-инфекция генотипами 1Ь и 3а НСУ. Рекомендовано определять генотип НСУ до начала ПВТ тест-системами, в которых предусмотрены возможность субтипирования генотипа 1 по NS5В-области или проведение секвенирования NS5B-региона генома НСУ.
Ключевые слова:
хронический гепатит С, лечение, предикторы устойчивый вирусологический ответ, генотипы 2 и 3, вирус гепатита С, рекомбинантные варианты НСУ
«Pitfalls» in the treatment of patients with chronic hepatitis C infected with genotype 2 or 3 hepatitis C virus
O. O. Znoyko1, K.R. Dudina1, A.N. Kozina1, D.O. Lenkova1, O.V. Kalinina2, N.D. Yushchuk1
O. Znoyko1, K.R. Dudina1, A.N. Kozina1, D.O. Lenkova1, O.V. Kalinina2, N.D. Yushchuk1
1 State University of Medicine and Dentistry named after A.I. Evdokimov
2 Saint-Petersburg Pasteur Epidemiology and Microbiology Research Institute
The results of clinical and laboratory examination of 29 patients with chronic hepatitis C infected with genotype 2 or 3 HCV, treated with pegylated interferon and ribavirin for 24 weeks were analyzed. The evaluation of the role of factors, predictors of SVR in patients with chronic hepatitis C infected with genotype 2 or 3 HCV, taking into account the characteristics of the viral genome was performed. In the studied group treatment was ineffective in 14% (4/29) of cases. Patients who did not respond to therapy, have known predictors of failure (such as obesity, the presence of hepatic steatosis and initially high viral load), as well as factors related to the characteristics of the virus. In two patients, the main cause of treatment failure was the presence of a recombinant variant RF2k/1b HCV, undetectable by standard commercial test systems when determining the genotype of the virus. In one case, sequencing revealed the presence of mixed infection genotypes 1b and 3a HCV. It is recommended to determine the HCV genotype prior to the antiviral therapy by testing with systems, which allow subtyping genotype 1 NS5V-region, or sequencing of the NS5B-region HCV genome.
In two patients, the main cause of treatment failure was the presence of a recombinant variant RF2k/1b HCV, undetectable by standard commercial test systems when determining the genotype of the virus. In one case, sequencing revealed the presence of mixed infection genotypes 1b and 3a HCV. It is recommended to determine the HCV genotype prior to the antiviral therapy by testing with systems, which allow subtyping genotype 1 NS5V-region, or sequencing of the NS5B-region HCV genome.
Keywords:
chronic hepatitis C, treatment, predictors of SVR, genotypes 2 and 3 hepatitis C virus, HCV recombinant variants
Несмотря на то что уже на протяжении многих лет изучаются факторы, являющиеся предикторами ответа на противовирусную терапию (ПВТ) при лечении хронического гепатита С (ХГС), в большом объеме научного материала по данному поводу встречается ряд противоречий, касающихся роли этих факторов в успешности ПВТ при лечении больных, инфицированных генотипами 2 и 3 вируса гепатита (НСУ). Большинством исследований подтверждено, что такие факторы, как высокий исходный уровень вирусной нагрузки (УВН), отсутствие быстрого вирусологического ответа (БВО), выраженный фиброз или цирроз печени, стеатоз печени и высокий индекс массы тела (ИМТ), являются независимым предиктором неуспеха терапии, и это в большей степени относится к генотипу 3, а не к генотипу 2 НСУ. Однако, как показывают исследования, ни один из обсуждаемых факторов не играет роли абсолютного предиктора неуспеха лечения [1-4].
Большинством исследований подтверждено, что такие факторы, как высокий исходный уровень вирусной нагрузки (УВН), отсутствие быстрого вирусологического ответа (БВО), выраженный фиброз или цирроз печени, стеатоз печени и высокий индекс массы тела (ИМТ), являются независимым предиктором неуспеха терапии, и это в большей степени относится к генотипу 3, а не к генотипу 2 НСУ. Однако, как показывают исследования, ни один из обсуждаемых факторов не играет роли абсолютного предиктора неуспеха лечения [1-4].
При обсуждении генетически детерминированных факторов в роли генотипов полиморфизмов гена ИЛ-28В человека у больных ХГС как предикторов успеха лечения возникает очень много противоречий. В начале изучения значимости этих факторов было показано, что их влияние четко прослеживается только при инфицировании генотипом 1 НСУ [5]. Однако в дальнейшем были получены убедительные данные о том, что эти генетические маркеры имеют такое же важное предсказательное значение при инфицировании генотипами 3 и 2 НСУ [6, 7]. И совсем мало изучен аспект, касающийся свойств вируса, которым был инфицирован пациент при анализе случаев неудачи терапии. В последние годы появились публикации, касающиеся клинического значения рекомби-нантных вариантов НСУ и их роли в отсутствии достижения устойчивого вирусологического ответа (УВО) у больных, инфицированных генотипом 2 НСУ (по данным генотипиро-вания коммерческими тест-системами) [8]. В связи с этим целью исследования был анализ комплекса факторов — предикторов отсутствия УВО на двойную ПВТ у больных ХГС, инфицированных генотипами 2 и 3 НСУ, с учетом особенностей вирусного генома.
И совсем мало изучен аспект, касающийся свойств вируса, которым был инфицирован пациент при анализе случаев неудачи терапии. В последние годы появились публикации, касающиеся клинического значения рекомби-нантных вариантов НСУ и их роли в отсутствии достижения устойчивого вирусологического ответа (УВО) у больных, инфицированных генотипом 2 НСУ (по данным генотипиро-вания коммерческими тест-системами) [8]. В связи с этим целью исследования был анализ комплекса факторов — предикторов отсутствия УВО на двойную ПВТ у больных ХГС, инфицированных генотипами 2 и 3 НСУ, с учетом особенностей вирусного генома.
Материал и методы
Проанализированы данные 29 пациентов с ХГС, инфицированных 2 или 3 генотипами НСУ, закончивших двойную ПВТ пегилированным интерфероном (пег-ИФН) и рибавири-ном (РИБ), дозируемым по массе тела, в течение 24 нед.
До начала двойной ПВТ всем пациентам проведено следующее лабораторно-инструментальное обследование: клинические анализы крови и мочи; биохимический анализ крови; определение маркеров вирусных гепатитов, ВИЧ, РНК НСУ в крови количественным методом полимеразной цепной реакции (ПЦР), генотипирование НСУ и определение генотипов полиморфизмов гена человека ИЛ-28В с использованием коммерческих тест-систем. 1ЬгоБсап 502 F01301». 5 молодым людям в возрасте от 19 до 30 лет с отсутствием клинико-лабораторных данных за выраженный фиброз или цирроз печени терапия была назначена без предварительной оценки стадии фиброза методом транзиентной фиброэластометрии.
1ЬгоБсап 502 F01301». 5 молодым людям в возрасте от 19 до 30 лет с отсутствием клинико-лабораторных данных за выраженный фиброз или цирроз печени терапия была назначена без предварительной оценки стадии фиброза методом транзиентной фиброэластометрии.
Задачи исследования: оценка частоты неэффективности двойной ПВТ у больных ХГС; анализ наличия известных неблагоприятных факторов, влияющих на эффективность лечения в группе пациентов с отсутствием УВО: высокого индекса массы тела (ИМТ), выраженного фиброза по данным транзиентной эластографии, наличие стеатоза печени по данным УЗИ, высокого исходного уровня виремии НСУ, наличия быстрого и раннего вирусологического ответов (БВО и РВО) на фоне лечения и особенностей генома ВГС.
Результаты и обсуждение
В исследование включено 20 (69%) мужчин и 9 (31%) женщин. Средний возраст пациентов составил 35 лет (от 18 до 46 лет). Среди больных ХГС, получивших курс ПВТ, преобладали (76%, 22/29) пациенты, инфицированные генотипом 3 НСУ.
Среди больных ХГС, получивших курс ПВТ, преобладали (76%, 22/29) пациенты, инфицированные генотипом 3 НСУ.
Анализ генетически детерминированных факторов пациентов (варианты полиморфизмов гена ИЛ-28В человека, связанные с чувствительностью к лечению интерфероном) у больных исследуемой группы показал, что носителями благоприятного генотипа СС гб12979860 гена ИЛ-28В являлись 48% (14/29) больных. Однако в группе пациентов, инфицированных генотипом 2 НСУ, благоприятный генотип СС гена ИЛ-28В регистрировался гораздо реже, чем при инфицировании генотипом 3 НСУ (14% (1/7) и 59% (13/22), соответственно). В 20% (6/29) случаев пациенты являлись носителями генотипа ТТ гб12979860, имеющего отрицательное предсказательное значение в достижении УВО (при инфицировании генотипом 2 НСУ — 29% (2/7), генотипом 3 НСУ — 18%, 4/22). Носительство благоприятного генотипа ТТ гб8099917 гена ИЛ-28В человека было определено у большинства — 72% (21/29) больных ХГС (при инфицировании генотипом 2 НСУ — 57% (4/7), генотипом 3 НСУ — 77% (17/22). Генотип GG гб8099917 гена ИЛ-28В, ассоциирующийся с низкой частотой ответа на терапию, выявлен в 10% (3/29) случаев, при этом необходимо отметить, что все пациенты, имевшие генотип GG гб8099917, были инфицированы генотипом 3 НСУ.
Генотип GG гб8099917 гена ИЛ-28В, ассоциирующийся с низкой частотой ответа на терапию, выявлен в 10% (3/29) случаев, при этом необходимо отметить, что все пациенты, имевшие генотип GG гб8099917, были инфицированы генотипом 3 НСУ.
Анализ исходного уровня вирусной нагрузки (УВН) у пациентов показал, что высокий уровень до начала лечения (>800 000 МЕ/мл) был зарегистрирован в 59% (17/29) случаев. В группе пациентов, инфицированных генотипом
2 HCV, исходный УВН находился в пределах от 3,19х104 до 2,73х107 МЕ/мл. У пациентов, инфицированных генотипом 3 HCV, минимальное значение вирусной нагрузки до начала ПВТ составило 1,20х104 МЕ/мл, максимальное -7,18х106 МЕ/мл. Оценка вирусной нагрузки после первых 4 нед терапии в анализируемой группе пациентов показала, что достижение БВО, т.е. неопределяемый УВН было отмечено в 76% (22/29) случаев. В то же время в группе пациентов, инфицированных генотипом 2 HCV, неопределяемый УВН был выявлен в 71% (5/7), а при инфицировании генотипом
3 HCV — в 77% (17/22) случаев. У 7 пациентов на 4-й неделе лечения при использовании количественного метода детекции уровня виремии был зарегистрирован неопределяемый УВН, а у 2 из них — был <15 МЕ/мл, что было расценено как отсутствие БВО. Частота достижения полного РВО составила 97% (28/29). У 1 пациента, инфицированного генотипом 2 HCV, зарегистрирован частичный РВО — чРВО (снижение уровня виремии более чем на 2 Log от исходного), и только
У 7 пациентов на 4-й неделе лечения при использовании количественного метода детекции уровня виремии был зарегистрирован неопределяемый УВН, а у 2 из них — был <15 МЕ/мл, что было расценено как отсутствие БВО. Частота достижения полного РВО составила 97% (28/29). У 1 пациента, инфицированного генотипом 2 HCV, зарегистрирован частичный РВО — чРВО (снижение уровня виремии более чем на 2 Log от исходного), и только
у него на момент окончания терапии регистрировали определяемый уровень виремии.
Через 24 нед после окончания ПВТ частота достижения УВО составила 86 % (25/29). При инфицировании генотипом 2 НСУ частота достижения УВО — 71% (5/7), а при инфицировании генотипом 3 НСУ — 91% (20/22). Таким образом, в исследуемой группе лечение оказалось неэффективным в 14% (4/29) случаев (табл. 1).
Клинико-лабораторные данные пациентов, не ответивших на противовирусную терапию, представлены в табл. 2.
2.
У пациентов, не ответивших на ПВТ, коррекцию дозы на фоне лечения проводили только в отношении рибавирина в связи с развитием нежелательных явлений. Длительность коррекции (снижение дозы/отмена препарата) не превышала 7 дней, что не могло повлиять на исход терапии.
Как следует из данных, представленных в табл. 2, у пациентов, не ответивших на ПВТ, имелся комплекс известных неблагоприятных предикторов эффективности лечения,
Таблица 1. Характеристика пациентов, инфицированных генотипами 2 и 3 HCV, получавших пег-ИФН + РИБ в течение 24 нед
OI Z Пол Возраст, годы Ъ ¡£ I-» Стадия фиброза METAVIR Генотип HCV коммер. Тест-система Генотип HCV секвенирование Исходная ВН БВО РВО УВО IL28B (rs12979860) IL28B (rs8099917)
1 Ж 36 23 F0 2 2а 2,35х106 БВО РВО УВО CT TT
2 М 36 22 F2 2 — 3,19х104 БВО РВО УВО CT TG
3 Ж 31 23 F2 2 2а 5,90х104 БВО РВО УВО CT TG
4 М 30 22 F2 2 — 1,14х106 БВО РВО УВО TT TT
5 М 33 31 F1 2 2k 4,10х106 БВО РВО УВО CC TT
6 М 40 36 F2 2 2k/1b 2,73х107 Нет БВО чРВО Нет УВО TT TG
7 М 38 30 F2 2 2k/1b 1,23х107 Нет БВО РВО Нет УВО CT TT
8 М 39 37 F2 3 1Ь+3а 4,72х106 < 15 МЕ/мл РВО Нет УВО CC TT
9 Ж 45 33 F3 3а 3а 3,44х106 Нет БВО РВО Нет УВО CC TT
10 М 35 28 — 3 3в 6,61х105 БВО РВО УВО CC TT
11 М 18 27 — 3 3а 3,96х105 БВО РВО УВО CC TT
12 М 34 30 — 3 3а 1,02х106 БВО РВО УВО CC TT
13 М 28 37 F0 3 3а 1,20х104 БВО РВО УВО ТТ TG
14 Ж 37 19 — 3 3а 5,03х104 БВО РВО УВО TT GG
15 М 46 20 F1 3а 3а 9,8х105 БВО РВО УВО CC TT
16 Ж 41 24 F0 3а 3а 1,17х106 Нет БВО РВО УВО CC TT
17 М 42 33 F3 3 3а 3,59х106 БВО РВО УВО TT GG
18 М 43 29 F1 3а 3а 7,80х105 БВО РВО УВО CC TT
19 М 31 31 F1 3 3а 2,05х105 БВО РВО УВО CT TT
20 Ж 26 23 F0 3 — 4,43х105 БВО РВО УВО CT TT
21 М 37 25 F3 3 — 4,20х106 Нет БВО РВО УВО CC TT
22 М 37 22 — 3 — 6,24х105 БВО РВО УВО TT GG
23 М 35 28 F0 3а — 4,68х105 БВО РВО УВО CT TT
24 Ж 33 20 F2 3а — 7,18х106 БВО РВО УВО CC TT
25 Ж 39 24 F0 3 — 8,34х104 БВО РВО УВО CT TT
26 М 36 26 F2 3а — 2,87х106 <15 МЕ/мл РВО УВО CC TT
27 М 37 25 F2 3 — 5,99х106 БВО РВО УВО CT TG
28 М 38 29 F1 3 — 8,66х105 БВО РВО УВО CC TT
29 Ж 26 25 F2 3 — 1,28х106 БВО РВО УВО CC TT
Примечание.
са ¡г а.
1 М 36 Нет F2 2 2k/1b 27 327 265 -/+ Нет БВО чРВО НетУВО TT TG
2 М 30 Нет F2 2 2k/1b 12 360 029 -/+ Нет БВО РВО НетУВО CT TT
3 М 27 Нет F2 3 1b+3a 4 720 000 -/- <15 МЕ/мл РВО НетУВО CC TT
4 Ж 33 Стеатоз F3 3а 3а 3 445 292 -/+ Нет БВО РВО НетУВО CC TT
причем главным из них является исходно высокий УВН, что наблюдалось в 100% случаев. В 100% случаев регистрировались исходно высокий УВН и отсутствие БВО на фоне лечения (главные из известных факторов — предикторов отсутствия эффективности ПВТ как у больных с генотипом 1 ВГС, так и с генотипами 2 и 3 [9, 10]).
Как следует из данных табл. 2, у одной пациентки с генотипом 3 НСУ выявлено 5 хорошо известных независимых предикторов неуспеха двойной ПВТ: высокий ИМТ, стадия фиброза печени F3, наличие стеатоза печени, исходно высокий УВН, отсутствие БВО. Влияние высокого ИМТ на эффективность ПВТ при ХГС широко обсуждается в научной литературе. В работе А. АЫо (2012 г.) было убедительно показано влияние ожирения на эффективность лечения больных, инфицированных генотипами 2 и 3 НСУ. При сравнении эффективность лечения пациентов с ИМТ <30 и >30 кг/м2 было продемонстрировано, что, с одной стороны, при инфицировании генотипами 2 и 3 НСУ высокий ИМТ коррелирует с наличием стеатоза печени (независимый предиктор неуспешной терапии) и более высоким исходным УВН НСУ, с другой — достоверно меньшей частотой достижения РВО. Авторами доказано, что при наличии ожирения факмакокинетические показатели, такие как концентрация интерферона и рибавирина в крови больных на фоне лечения, были достоверно ниже (концентрация интерферона, определялась на 3-й и 29-й день лечения, а рибавирина на 29-й день лечения и на 12-й неделе лечения — ключевые временные точки для каждого препарата, определяющие его максимальное терапевтическое воздействие). Безусловно, все перечисленные факторы оказали влияние на эффективность ПВТ, что нашло свое отражение и в окончательных результатах исследования — только 62% пациентов с ИМТ >30 кг/м2 достигли УВО, а у пациентов с ИМТ <30 кг/м2 эффективность лечения составила 89% [11].
Влияние высокого ИМТ на эффективность ПВТ при ХГС широко обсуждается в научной литературе. В работе А. АЫо (2012 г.) было убедительно показано влияние ожирения на эффективность лечения больных, инфицированных генотипами 2 и 3 НСУ. При сравнении эффективность лечения пациентов с ИМТ <30 и >30 кг/м2 было продемонстрировано, что, с одной стороны, при инфицировании генотипами 2 и 3 НСУ высокий ИМТ коррелирует с наличием стеатоза печени (независимый предиктор неуспешной терапии) и более высоким исходным УВН НСУ, с другой — достоверно меньшей частотой достижения РВО. Авторами доказано, что при наличии ожирения факмакокинетические показатели, такие как концентрация интерферона и рибавирина в крови больных на фоне лечения, были достоверно ниже (концентрация интерферона, определялась на 3-й и 29-й день лечения, а рибавирина на 29-й день лечения и на 12-й неделе лечения — ключевые временные точки для каждого препарата, определяющие его максимальное терапевтическое воздействие). Безусловно, все перечисленные факторы оказали влияние на эффективность ПВТ, что нашло свое отражение и в окончательных результатах исследования — только 62% пациентов с ИМТ >30 кг/м2 достигли УВО, а у пациентов с ИМТ <30 кг/м2 эффективность лечения составила 89% [11].
Как отражено в таблице 2, все больные, инфицированные генотипом 3 НСУ и не ответившие на ПВТ, являлись носителями благоприятных генотипов гб12979860 и гб8099917 гена ИЛ-28В, в то время как пациенты, инфицированные генотипом 2 НСУ, — носители неблагоприятных аллелей гб12979860 (ТТ и СТ), 1 пациент — носитель неблагоприятной аллели гб8099917 указанных полиморфизмов. Обращает на себя внимание тот факт, что у 2 пациентов, не ответивших на ПВТ и инфицированных генотипом 2 НСУ по данным коммерческих тест-систем, при секвениро-
вании NSßB-региона HCV (РНК была выделена из образца сыворотки крови, взятой до начала ПВТ) выявлен реком-бинантный вариант RF2k/1b HCV. Поскольку часть генома у данного варианта вируса принадлежит субтипу 1b HCV, влияние неблагоприятных полиморфизмов гена ИЛ-28В могло сказаться на эффективности ПВТ, так как при генотипе 1b HCV показано максимальное значение генетических факторов человека (ген ИЛ-28В) для достижения УВО. В настоящее время не вызывает сомнение, что инфицирование ре-комбинантным вариантом RF2k/1b HCV является таким же неблагоприятным предиктором эффективности ПВТ, как и инфицирование генотипом 1 HCV. Показано, что эффективность лечения у пациентов, инфицированных рекомбинант-ным вариантом RF2k/1b HCV, не превышает 20-40% [12, 13] при двойной ПВТ и 25% даже в результате применения высокоэффективной безинтерфероновой терапии софосбу-виром и рибавирином в течение 12 нед [8].
В настоящее время не вызывает сомнение, что инфицирование ре-комбинантным вариантом RF2k/1b HCV является таким же неблагоприятным предиктором эффективности ПВТ, как и инфицирование генотипом 1 HCV. Показано, что эффективность лечения у пациентов, инфицированных рекомбинант-ным вариантом RF2k/1b HCV, не превышает 20-40% [12, 13] при двойной ПВТ и 25% даже в результате применения высокоэффективной безинтерфероновой терапии софосбу-виром и рибавирином в течение 12 нед [8].
Из 2 больных, инфицированных генотипом 3 HCV, в одном случае выявлено при секвенировании наличие микст-инфекции генотипами 1b и 3а HCV в исходном образце, полученном до начала терапии, что, безусловно, могло повлиять на исход лечения. Подобные случаи описаны в научной литературе. Так, по данным V. Morel и соавт., в 2010 г. у пациента, не достигшего УВО после окончания 24-недельного курса пег-ИФН+РИБ, был идентифицирован рекомбинант-ный вариант RF2k/1b HCV, хотя до начала терапии у него был выделен только изолят вируса субтипа 3а.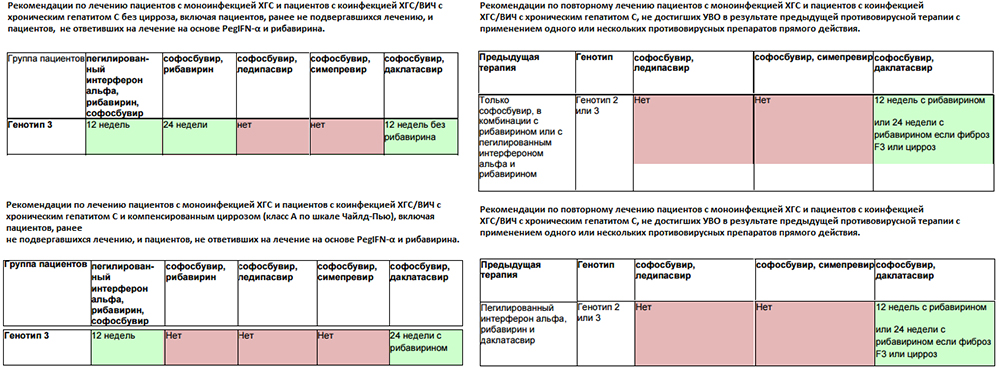 Авторы сделали заключение, что данный пациент был инфицирован исходно обоими вариантами вируса гепатита С и, возможно, высокий УВН субтипа 3а до начала терапии не позволял идентифицировать оба варианта вируса [14].
Авторы сделали заключение, что данный пациент был инфицирован исходно обоими вариантами вируса гепатита С и, возможно, высокий УВН субтипа 3а до начала терапии не позволял идентифицировать оба варианта вируса [14].
Таким образом, проведенный анализ неблагоприятных факторов ответа на ПВТ показал, что, с одной стороны, у большинства больных были выявлены хорошо известные предикторы неуспеха двойной ПВТ (такие как ожирение, стеатоз печени и исходно высокий УВН). С другой стороны, у больных ХГС, инфицированных генотипами 2 и 3 HCV, у которых преимущественно достигался УВО, были выявлены подводные камни — особенности генома вируса или наличие микст-инфекции, что, по всей видимости, повлияло на эффективность лечения. Так, у пациентов, инфицированных генотипом 2 HCV и не ответивших на ПВТ, основной причиной неэффективности лечения, вероятно, был рекомбинантный вариант RF2k/1b HCV, который обычно не выявляется стан-
дартными коммерческими тест-системами при определении генотипа вируса.
В исследуемой группе при ретроспективном анализе у 1 пациента была определена микст-инфекция разными генотипами НСУ еще до начала ПВТ, что также могло привести к неудаче лечения. Рекомбинантный вариант RF2k/1b НСУ и смешанное инфицирование генотипами 1 и 3 НСУ предусматривает более длительный курс ПВТ, однако пациентам был проведен стандартный 24-недельный курс.
При обследовании пациентов с использованием коммерческих тест-систем не всегда можно выявить микст-инфицирование разными генотипами вируса гепатита С. Практика показывает, что иногда у пациентов, имевших неуспешный опыт ПВТ, впоследствии при обследовании определяется другой генотип НСУ, отличный от выявленного при первичном обследовании. Это указывает на необходимость обязательного определения генотипа НСУ у больного
после неуспешной ПВТ, чтобы избежать неудачи при повторной терапии. В идеале определять генотип НСУ до начала ПВТ необходимо тест-системами, в которых в качестве мишени для генотипирования используется 5’UTR-регион и предусмотрена возможность субтипирования генотипа 1 по NS5В-области, что должно позволить выявлять как наличие микст-инфекции разными генотипами НСУ, так и меж-генотипные рекомбинантные формы. Альтернативой такого подхода может быть более дорогостоящая методика определения генотипа вируса — секвенирование NS5B региона генома НСУ.
В идеале определять генотип НСУ до начала ПВТ необходимо тест-системами, в которых в качестве мишени для генотипирования используется 5’UTR-регион и предусмотрена возможность субтипирования генотипа 1 по NS5В-области, что должно позволить выявлять как наличие микст-инфекции разными генотипами НСУ, так и меж-генотипные рекомбинантные формы. Альтернативой такого подхода может быть более дорогостоящая методика определения генотипа вируса — секвенирование NS5B региона генома НСУ.
Работа выполнена при поддержке Российского научного фонда (приоритетное направление деятельности РНФ «Проведение фундаментальных научных исследований и поисковых научных исследований отдельными научными группами», соглашение № 14-15-00546).
СВЕДЕНИЯ ОБ АВТОРАХ
Знойко Ольга Олеговна — доктор медицинских наук, профессор кафедры инфекционных болезней и эпидемиологии ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России Е-шаН: [email protected]
А.И. Евдокимова» Минздрава России Е-шаН: [email protected]
Дудина Кристина Рубеновна — доктор медицинских наук, доцент кафедры инфекционных болезней и эпидемиологии ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России Е-шаН: [email protected]
Козина Анастасия Николаевна — аспирант кафедры инфекционных болезней и эпидемиологии ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России E-maiL: [email protected]
Ленкова Дарья Олеговна — аспирант кафедры инфекционных болезней и эпидемиологии ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России E-maiL: [email protected]
Калинина Ольга Викторовна — доктор биологических наук, ведущий научный сотрудник лаборатории молекулярной микробиологии ФБУН «Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Пастера» E-maiL: [email protected]
Пастера» E-maiL: [email protected]
Ющук Николай Дмитриевич — академик РАН, доктор медицинских наук, профессор, президент ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России, заведующий кафедрой инфекционных болезней и эпидемиологии E-maiL: prof.uyБ[email protected]
ЛИТЕРАТУРА
1. Aziz H., Raza A., Waheed Y. et al. Analysis of variables and interactions among variables associated with a sustained virological response to pegylated interferon alfa-2a plus ribavirin in hepatitis C virus genotype 3-infected patients // Int. J. Infect. Dis. 2012. Vol. 16, N 8. P. e597 e602. doi: 10.1016/j.ijid.2012.03.012.
2. Restivo L., Zampino R., Guerrera B. et al. Steatosis is the predictor of relapse in HCV genotype 3- but not 2-infected patients treated with 12 weeks of pegylated interferon-a-2a plus ribavirin and RVR // J. Viral Hepat. 2012. Vol. 19. P. 346-352. doi: 10.1111/ j.1365-2893.2011. 01555.x.
Viral Hepat. 2012. Vol. 19. P. 346-352. doi: 10.1111/ j.1365-2893.2011. 01555.x.
3. Shiffman M.L., Suter F., Bacon B.R., Nelson D. et al. Peginterferon alfa-2a and ribavirin for 16 or 24 weeks in HCV genotype 2 or 3 // N. Engl. J. Med. 2007. Vol. 357. P. 124 134. doi: 10.1056/NEJMoa066403.
4. Dalgard O., Bjoro K., Ring-Larsen H. et al. Pegylated interferon alfa and ribavirin for 14 versus 24 weeks in patients with hepatitis C
virus genotype 2 or 3 and rapid virological response // Hepatology. 2008. Vol. 47. P. 35 42. doi: 10.1002/hep.21975.
5. Stattermayer A.F., Stauber R., Hofer H. et al. Impact of IL28B genotype on the early and sustained virologie response in treatment-naïve patients with chronic hepatitis C // Clin. Gastroenterol. Hepatol. 2011. Vol. 9, N 4. P. 344e2 350e2. doi: 10.1016/j.cgh. 2010.07.019.
doi: 10.1016/j.cgh. 2010.07.019.
6. Firdaus R., Biswas A., Saha K. et al. Impact of host IL28B rs12979860, rs8099917 in interferon responsiveness and advanced liver disease in chronic genotype 3 hepatitis C patients // PLoS One. 2014. Vol. 9, N 6. Article ID e99126. doi: 10.1371/journal.pone.0099126.
7. Eslam M., Leung R., Romero-Gomez M. et al. IFNL3 polymorphisms predict response to therapy in chronic hepatitis C genotype 2/3 infection // J. Hepatol. 2014. Vol. 61, N 2. P. 235-241. doi: 10.1016/ j.jhep.2014.03.039.
8. Hedskog C., Doehle B., Chodavarapu K. et al. Characterization of hepatitis C virus intergenotypic recombinant strains and associated virological response to sofosbuvir/ribavirin // Hepatology. 2015. Vol. 61, N 2. P. 471-480. doi: 10.1002/hep.27361.
9. Yu M.L., Dai C.Y., Huang J.F. et al. A randomised study of peginterferon and ribavirin for 16 versus 24 weeks in patients with genotype 2 chronic hepatitis C // Gut. 2007. Vol. 56. P. 553-559. doi: 10.1136/gut.2006.102558.
Yu M.L., Dai C.Y., Huang J.F. et al. A randomised study of peginterferon and ribavirin for 16 versus 24 weeks in patients with genotype 2 chronic hepatitis C // Gut. 2007. Vol. 56. P. 553-559. doi: 10.1136/gut.2006.102558.
10. Galan R.J., Cidoncha E.C., Martin M.F. et al. Antiviral regimen complexity index as an independent predictor of sustained virologie response in patients with chronic hepatitis C // J. Manag. Care Pharm. 2013. Vol. 19, N 6. P. 448-453.
11. Alsio A., Rembeck K., Askarieh G. et al. Impact of obesity on the bioavailability of peginterferon-a2a and ribavirin and treatment outcome
for chronic hepatitis C genotype 2 or 3 // PLoS One. 2012. VoL. 7, N 5. Article ID e37521. doi: 10.1371/journaL.pone.0037521.
12. Karchava M., Waldenstrom J., Parker M. et aL. High incidence of the hepatitis C virus recombinant 2k/1b in Georgia: Recommendations for testing and treatment // HepatoL. Res. 2015. VoL. 45. N 13. P. 12921298. doi: 10.1111/hepr.12505.
Res. 2015. VoL. 45. N 13. P. 12921298. doi: 10.1111/hepr.12505.
13. Николаева Л.И., Сапронов Г.В., Колотвин А.В. и др. Гепатит С при инфицировании рекомбинантной формой вируса RF2k/1b: течение и терапия // Эпидемиология и инфекц. бол. 2014. № 3. С. 9-15.
14. MoreL V., Descamps V., Francois C., Fournier C. et aL. Emergence of a genomic variant of the recombinant 2k/1b strain during a mixed Hepatitis C infection: a case report // J. CLin. ViroL. 2010. VoL. 47, N 4. P. 382-386. doi: 10.1016/j.jcv.2010.01.011.
REFERENCES
1. Aziz H., Raza A., Waheed Y. et al. Analysis of variables and interactions among variables associated with a sustained virological response to pegylated interferon alfa-2a plus ribavirin in hepatitis C virus genotype 3-infected patients. Int J Infect Dis. 2012; Vol.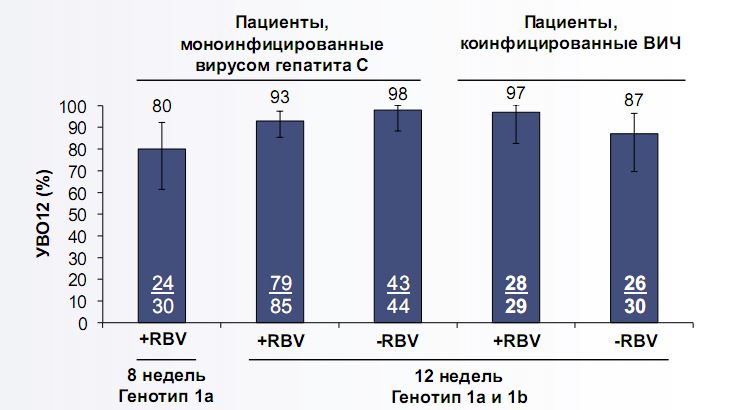 16 (8): e597 602. doi: 10.1016/j.ijid.2012.03.012.
16 (8): e597 602. doi: 10.1016/j.ijid.2012.03.012.
2. Restivo L., Zampino R., Guerrera B. et al. Steatosis is the predictor of relapse in HCV genotype 3- but not 2-infected patients treated with 12 weeks of pegylated interferon-a-2a plus ribavirin and RVR. J Viral Hepat. 2012; Vol. 19: 346-352. doi: 10.1111/ j.1365-2893.2011.01555.x.
3. Shiffman M.L., Suter F., Bacon B.R., Nelson D. et al. Peginterferon alfa-2a and ribavirin for 16 or 24 weeks in HCV genotype 2 or 3. N Engl J Med. 2007; Vol. 357: 124 34. doi: 10.1056/NEJMoa066403.
4. Dalgard O., Bjoro K., Ring-Larsen H. et al. Pegylated interferon alfa and ribavirin for 14 versus 24 weeks in patients with hepatitis C virus genotype 2 or 3 and rapid virological response. Hepatology. 2008; Vol. 47: 35 42. doi: 10.1002/hep.21975.
5. Stattermayer A.F., Stauber R., Hofer H. et al. Impact of IL28B genotype on the early and sustained virologic response in treatment-naïve patients with chronic hepatitis C. Clin Gastroenterol Hepatol. 2011; Vol. 9 (4): 344e2 50e2. doi: 10.1016/j.cgh.2010.07.019.
Stattermayer A.F., Stauber R., Hofer H. et al. Impact of IL28B genotype on the early and sustained virologic response in treatment-naïve patients with chronic hepatitis C. Clin Gastroenterol Hepatol. 2011; Vol. 9 (4): 344e2 50e2. doi: 10.1016/j.cgh.2010.07.019.
6. Firdaus R., Biswas A., Saha K. et al. Impact of host IL28B rs12979860, rs8099917 in interferon responsiveness and advanced liver disease in chronic genotype 3 hepatitis C patients. PLoS One. 2014; Vol. 9 (6). Article ID e99126. doi: 10.1371/journal.pone.0099126.
7. Eslam M., Leung R., Romero-Gomez M. et al. IFNL3 polymorphisms predict response to therapy in chronic hepatitis C genotype 2/3 infection. J Hepatol. 2014; Vol. 61 (2): 235-41. doi: 10.1016/j.jhep. 2014.03.039.
8. Hedskog C., Doehle B., Chodavarapu K. et al. Characterization of hepatitis C virus intergenotypic recombinant strains and associated virological response to sofosbuvir/ribavirin. Hepatology. 2015; Vol. 61 (2): 471-80. doi: 10.1002/hep.27361.
Hepatology. 2015; Vol. 61 (2): 471-80. doi: 10.1002/hep.27361.
9. Yu M.L., Dai C.Y., Huang J.F. et al. A randomised study of peginterferon and ribavirin for 16 versus 24 weeks in patients with genotype 2 chronic hepatitis C. Gut. 2007; Vol. 56: 553-9. doi: 10.1136/ gut.2006.102558.
10. Galan R.J., Cidoncha E.C., Martin M.F. et al. Antiviral regimen complexity index as an independent predictor of sustained virologic response in patients with chronic hepatitis C. J Manag Care Pharm. 2013; Vol. 19 (6): 448-53.
11. Alsio A., Rembeck K., Askarieh G. et al. Impact of obesity on the bioavailability of peginterferon-a2a and ribavirin and treatment outcome for chronic hepatitis C genotype 2 or 3. PLoS One. 2012; Vol. 7 (5). Article ID e37521. doi: 10.1371/journal.pone.0037521.
12. Karchava M. , Waldenstrom J., Parker M. et al. High incidence of the hepatitis C virus recombinant 2k/1b in Georgia: Recommendations for testing and treatment. Hepatol Res. 2015; Vol. 45 (13): 1292-8. doi: 10.1111/hepr.12505.
, Waldenstrom J., Parker M. et al. High incidence of the hepatitis C virus recombinant 2k/1b in Georgia: Recommendations for testing and treatment. Hepatol Res. 2015; Vol. 45 (13): 1292-8. doi: 10.1111/hepr.12505.
13. Nikolaeva L.I., Sapronov G.V., Kolotvin A.V. et al. Hepatitis C infection in the form of recombinant virus RF2k/1b: state of the disease and therapy. Epidemiologiya i infektsionnye bolezni [Epidemiology and infectious diseases]. 2014; 3: 9-15. (in Russian)
14. Morel V., Descamps V., Francois C., Fournier C. et al. Emergence of a genomic variant of the recombinant 2k/1b strain during a mixed Hepatitis C infection: a case report. J Clin Virol. 2010; Vol. 47 (4): 382-6. doi: 10.1016/j.jcv.2010.01.011.
Для пациентов с 3 генотипом вируса гепатита C появилось эффективное лекарство
Препарат глекапревир/пибрентасвир доказал свою эффективность и переносимость у пациентов с 3 генотипом вируса гепатита C, независимо от наличия цирроза или предыдущего опыта лечения.
В исследование, результаты которого были опубликованы в научном журнале Journal of Viral Hepatology, были включены данные, полученные в ходе пяти клинических испытаний 2 или 3 фазы. Общее количество участников составило 693 человека.
95% наивных пациентов без цирроза достигли устойчивого вирусологического ответа в течение 12 недель после окончания курса терапии (УВО12). В группе пациентов, принимавших препарат в течение 8 недель, УВО12 достигли 198 пациентов из 208, в группе, получавшей 12-недельный курс, — 280 из 294.
В группе наивных пациентов с циррозом, получавших препарат в течение 12 недель, УВО12 достигли 97% (67 человек из 69). Об этом сообщает портал Infectious Disease Advisor.
Среди людей, ранее проходивших лечение интерферон- или софосбувир-содержащей терапией, 90% пациентов без цирроза, получавших глекапревир/пибрентасвир в течение 12 недель, достигли УВО12 (44 человека из 49). В аналогичной группе, получавшей препарат в течение 16 недель, УВО12 достигли 95% пациентов (21 из 22).
Среди пациентов с циррозом, получавших препарат в течение 16 недель, УВО12 достигли 94% (48 из 51).
Согласно выводам исследователей, применение глекапревира/пибрентасвира рекомендовано в течение 8 и 12 недель наивным пациентам как с циррозом, так и без него, и в течение 16 недель пациентам, имеющим опыт лечения, независимо от наличия или отсутствия цирроза.
3 генотип вируса гепатита C является вторым по распространенности (после 1 генотипа) на территории России. Препарат глекапревир/пибрентасвир, выпускаемый фармацевтической компанией AbbVie, зарегистрирован в нашей стране под торговым наименованием «Мавирет». В список Жизненно необходимых и важнейших лекарственных препаратов (ЖНВЛП) в настоящее время не входит.
Прорыв в лечении гепатита С
Новая комбинация терапии гепатита С с использованием препарата Совриад (симепревир) – прорыв в лечении гепатита С
Компания «Янссен», фармацевтическое подразделение «Джонсон & Джонсон», объявила об одобрении Министерством здравоохранения РФ изменений в инструкцию препарата Совриад (симепревир), включающих терапию хронического гепатита С генотипа 1 в сочетании с препаратом софосбувир у взрослых пациентов с компенсированными заболеваниями печени (в том числе с циррозом печени без коинфекции ВИЧ), ранее не получавших лечение или у которых предшествующее лечение не было эффективным. Терапия симепревиром в комбинации с софосбувиром знаменует значительный прорыв в лечении хронического гепатита С.
Терапия симепревиром в комбинации с софосбувиром знаменует значительный прорыв в лечении хронического гепатита С.
Хронический гепатит С — одно из самых распространенных инфекционных заболеваний во всем мире. Каждый год вирус поражает 3-4 миллиона человек, и около 150 миллионов пациентов страдают хронической формой гепатита С и подвержены риску развития цирроза и/или рака печени.
Совриад (симепревир) – ингибитор протеазы второй волны с кратностью приема один раз в сутки и доказанным клиническим эффектом. Препарат предназначен для лечения различных групп пациентов с хроническим гепатитом С, включая пациентов с компенсированным циррозом печени, выпускается в форме капсул и принимается один раз в сутки по одной капсуле. Совриад (симепревир) блокирует работу фермента протеазы, который позволяет вирусу гепатита С выживать и воспроизводиться в инфицированных клетках человека.
В комбинации с софосбувиром данная терапия – доказанный путь к излечению хронического гепатита С, вызванного вирусом генотипа 1, проверенный в клинических условиях и в реальной практике у более, чем 1000 пациентов..gif) Кроме того, это первая и единственная одобренная безинтерфероновая схема без NS5A-ингибитора, эффективность которой не зависит от рибавирина.
Кроме того, это первая и единственная одобренная безинтерфероновая схема без NS5A-ингибитора, эффективность которой не зависит от рибавирина.
«Получение одобрения новой инструкции препарата Совриад (симепревир) Минздравом РФ является еще одним шагом к расширению возможностей современной терапии хронического гепатита С. — сказала Екатерина Погодина, исполнительный директор фармацевтического подразделения «Джонсон & Джонсон» по России. — Новая комбинация препаратов симепревир и софосбувир — это значительный прорыв в терапии гепатита С, эффективность схемы лечения которого больше не зависит от интерферона. Рада отметить очередной успех компании «Янссен» на пути обеспечения российским пациентам доступа к наиболее эффективным и безопасным препаратам и схемам лечения, которые позволят улучшить качество их жизни».
Уникальная программа лечения гепатита С
ЕMC предлагает новую, уникальную для России программу лечения гепатита С, позволяющую с вероятностью 95-100% полностью избавиться от заболевания.
Доказанная эффективность программы 95-100%!
Программа основана на применении инновационного противовирусного препарата, появление которого в 2014 году стало настоящим прорывом в медицине.
Преимущества новой программы:
Эффективность лечения – 95-100%
Возможность использования у пациентов с циррозом печени и сопутствующей патологией.
Высокая переносимость: в клинических испытаниях более 98% пациентов смогли полностью пройти курс.
Новая программа, разработанная специалистами-гепатологами Европейского медицинского центра, основана на инновационном препарате Викейра Пак и одобрена для лечения пациентов с гепатитом С (1-й генотип подтипов а и b), коинфекцией хронического гепатита С и вируса иммунодефицита человека 1-го типа (ВИЧ-1), а также пациентов после трансплантации печени. Эффективность лечения не зависит от того, получал ли до этого пациент интерфероновую терапию или нет.
Уникальная программа лечения гепатита С в EMC представлена в 3 вариантах, в которых Викейра Пак используется в качестве моно-терапии или в сочетании с рибавирином.
Внимание! Препараты уже включены в стоимость лечения!
Варианты программы:
Optima – для пациентов без цирроза и сопутствующих заболеваний
Optima Plus – для пациентов без цирроза, с сопутствующими заболеваниями
Ultra – для пациентов с циррозом
Перед каждой программой выполняется углубленное обследование – скрининг.
Ведущие специалисты программы:
Бакулин И. Г. – гастроэнтеролог-гепатолог, главный гастроэнтеролог г. Москвы, д. м. н., профессор. Автор более 200 научных публикаций, соавтор 6 монографий, член Европейской ассоциации по заболеваниям печени (EASL), Американской ассоциации изучения печени (AASLD), Российского общества по изучению заболеваний печени (РОПИП).
Блохина Н. П. – инфекционист-гепатолог, д.
 м. н., профессор, специализация – лечение вирусных гепатитов, автор более 70 публикаций, в том числе 7 учебно-методических пособий и 56 научных работ. Член Международного общества по изучению инфекционных болезней (International Society for Infectious Diseases (ISID)).
м. н., профессор, специализация – лечение вирусных гепатитов, автор более 70 публикаций, в том числе 7 учебно-методических пособий и 56 научных работ. Член Международного общества по изучению инфекционных болезней (International Society for Infectious Diseases (ISID)).Нурмухаметова У. А. – инфекционист-гепатолог, к. м. н. Автор более 40 публикаций, член Международного общества по изучению инфекционных болезней (International Society for Infectious Diseases (ISID)).
Полунина Т. Е. – гастроэнтеролог-гепатолог, д. м. н., профессор МГМСУ, Руководитель гепатологического центра EMC. Автор более 100 научных публикаций, член Европейской ассоциации по заболеваниям печени (EASL), Американской ассоциации изучения печени (AASLD), Российского общества по изучению заболеваний печени (РОПИП).
Программа лечения рассчитана на 12 недель.
Этапы прохождения программы для пациента с гепатитом С:
- Запись на консультацию к гепатологу клиники ЕМС или ведущему специалисту программы для назначения предпрограммного скрининга.

Скрининг – углубленное инструментальное и лабораторное обследование – для выявления типа вируса, стадии заболевания, наличия сопутствующей патологии.
Консультация ведущего специалиста, определение программы лечения: Optima, Optima Plus или Ultra.
Прохождение программы: прием препаратов, промежуточные анализы и консультации лечащего врача.
Завершающие программу обследования.
Что такое Викейра Пак
Препарат Викейра Пак был зарегистрирован в США в конце 2014 года, в начале 2015 года появился в Европейском союзе, а сейчас доступен и в России, что обусловлено высокой востребованностью действительно эффективных в отношении вируса гепатита С препаратов: только в России количество больных гепатитом С составляет, по разным данным, от 3,5 до 4,7 млн человек. Появление нового препарата, эффективно подавляющего размножение вируса гепатита С, стало настоящим прорывом в медицине.
Викейра Пак используется в сочетании с рибавирином или без него – в зависимости от стадии заболевания, выраженности цирроза печени, наличия сопутствующей патологии. Клинические исследования, проведенные с участием свыше 2300 пациентов из более чем 25 стран, показали: данная схема терапии демонстрирует 95-100% эффективность. Менее чем у 2% наблюдалась вирусологическая неудача. Препараты обладают высокой переносимостью: более 98% пациентов смогли полностью пройти курс.
Клинические исследования, проведенные с участием свыше 2300 пациентов из более чем 25 стран, показали: данная схема терапии демонстрирует 95-100% эффективность. Менее чем у 2% наблюдалась вирусологическая неудача. Препараты обладают высокой переносимостью: более 98% пациентов смогли полностью пройти курс.
Запись на лечение гепатита С
Запись пациентов на прием по новой уникальной программе лечения гепатита С в EMC уже началась. Программа доступна и для иногородних пациентов: присутствие пациента требуется на этапе первого обследования и консультации ведущего специалиста, на промежуточных консультациях и обследованиях у лечащего врача (их количество зависит от программы: Optima, Optima Plus или Ultra), а также на завершающих лечение консультациях.
Новая уникальная программа лечения гепатита С позволяет полностью избавиться от заболевания с вероятностью 95-100%.
Имеются противопоказания, согласно рекомендациям Управления по контролю за пищевыми продуктами и лекарственными препаратами США (FDA), лечение проводится по назначению и под контролем врача.
Результаты лечения хронического гепатита C (генотип 3а) у мужчин в зависимости от индекса массы тела
1. Бакулин И.Г., Новоженов В.Г., Колобанова Е.В. Недостаточность питания у больных хроническими заболеваниями печени // Воен.-мед. журн. — 2002. — № 2. С. 44-49.
2. Бакулин И.Г., Новоженов В.Г., Иванова М.А. Оценка элементного статуса у больных хроническим гепатитом С, устойчивых к противовирусной терапии // Воен.-мед. журн. 2005. — № 11. — С. 62-63.
3. Блюм X. Гепатит С: современное состояние проблемы // Рос. журн. гастроэнтерол., гепатол., колопроктол. 2005. — Т. 15, № 1. — С. 20-25.
4. Болезни печени и желчевыводящих путей // Под ред. Ивашкина В.Т. — М.: Издательский дом «М-Вести», 2002. 432 с.
5. Бурневич Э.З. Новый взгляд на прогнозирование устойчивого вирусологического ответа при лечении гепатита С // Вирусные гепатиты, достижения и перспективы. 2003. — № 1 (16). — С. 6-8.
6. Васенко В.И. Эффективность и стоимость лечения гепатита С у молодых мужчин отечественным интерфероном-альфа (реафероном). Материалы дис. .канд. мед. наук. — М., 2002.
Материалы дис. .канд. мед. наук. — М., 2002.
7. Васенко В.И., Плюснин С.В., Киселев А.В., Хазанов А.И. Эффективность лечения гепатита С у молодых мужчин реафероном — отечественным интерфероном-а // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2003.-Т. 13, №2.-С. 51-58.
8. Волкова М.А. Интерфероны и их противовирусное действие // Вирусные гепатиты: достижения и перспективы. Информационный бюллетень. — 1999.-№2.-С. 3-11.
9. Горбаков В.В. Вирусный гепатит С. Распространенность, течение, диагностика, лечение. // Материалы дис. . д-ра мед. наук. — М., 1998.
10. Бессесен Д., Кушнер Р. Избыточный вес и ожирение. Профилактика, диагностика и лечение // М.: ЗАО «Издательство БИНОМ», 2004. С. 24-28.
11. Ершов Ф.И., Коваленко A.JL, Аспель Ю.В., Романцов М.Г. Циклоферон в терапии вирусных гепатитов и ВИЧ-инфекций // С-Петербург: Союз художников. 1999. — С. 40.
12. Жданов К.В., Лобзин Ю.В., Мукомолов С.Л. и др. Генотипы и их взаимосвязь с морфологическими изменениями в печени у больных хроническим гепатитом С // Рос. журн. гастроэнтерол. гепатол., колопроктол. 2000. — Т. 10, № 5 (Прилож. № 11). — С. 79.
журн. гастроэнтерол. гепатол., колопроктол. 2000. — Т. 10, № 5 (Прилож. № 11). — С. 79.
13. Заключение международной конференции по гепатиту С // Клиническая фармакология и терапия. 2000. — № 9 (1). — С. 10-11.
14. Ивашкин В.Т., Маевская М.В., Лапшин А.В., Павлов Ч.С. и др. Веро-рибавирин в лечении больных хроническим гепатитом С // Рос. журн. гастроэнтерол., гепатол., колопроктол. 2003. — Т. 13, № 6. — С. 80-84.
15. Игнатова Т.М. Естественное течение хронической HCV-инфекции // Рос. журн. гастроэнтерол., гепатол., колопроктол. 2002. — Т. 12, № 2. — С. 20-30.
16. Игнатова Т.М. Хронический гепатит С: клинико-морфологическая характеристика, течение и лечение: Автореф. дис. . д-ра мед. наук. — М., 2000.
17. Игнатова Т.М., Серов В.В. Патогенез хронического гепатита С // Арх. пат. — 2001. -№3.- С. 54-59.
18. Калинина О.В., Мукомолов С.Л. Молекулярная эпидемиология гепатита С // Вирусные гепатиты: Информ. Бюллетень. 2000. — № 3 (10). — С. 9-15.
19. Карнейро де Мура М. Неалкогольный стеатогепатит // Клин, перспективы гастроэнтерол., гепатол. 2001. — № 3. — С. 12-15.
Неалкогольный стеатогепатит // Клин, перспективы гастроэнтерол., гепатол. 2001. — № 3. — С. 12-15.
20. Карпов В.В. Хронический гепатит С // Иммунопатол., аллергол., инфектол. 2000. — № 2. — С. 9-15.
21. Корнеева О.Н., Драпкина О.М., Буеверов А.О., Ивашкин В.Т. Неалкогольная жировая болезнь печени как проявление метаболического синдрома // Клин, перспективы гастроэнтерол., гепатол. 2005. — № 4. -С. 21-24.
22. Латентные формы вирусных гепатитов В, С и D: Диагностика, лечение и профилактика: Метод, рекомендации. М.: Воениздат, 2002. — С. 28-32.
23. Лесняк О.М. Аутоиммунные и ревматические аспекты инфицированности вирусом гепатита С // Клиническая медицина. 1999. — № 12. — С. 14-19.
24. Лопаткина Т.Н. Опыт лечения хронического гепатита С высокими дозами интерферона альфа. // Вирусные гепатита: достижения и перспективы. Инф. бюллетень, № 3 (7). 1999. — С. 16-19.
25. Майер К.-П. Естественное течение и диагностика вирусного гепатита С // Рос. журн. гастроэнтерол. гепатол., колопроктол. 2000. — Т. 10, № 4. — С. 21-23.
гепатол., колопроктол. 2000. — Т. 10, № 4. — С. 21-23.
26. Майер К.-П. Гепатит и последствия гепатита: Пер. с нем. / Под ред. А.А. Шептулина. М.: ГЭОТАР-Медицина, 1999. — С. 423.
27. Максимов С.Л., Ющук Н.Д., Ефремова Л.В., Максимова Р.Ф. и др. Острый вирусный гепатит С: клиника, диагностика // Гепатит С (Российский консенсус). Москва, 2000. — С. 88-89.
28. Мамаев С.Н., Лукина Е.А., Шульпекова Ю.О., Ивашкин В.Т. и др. Механизмы иммунного «ускользания» при хроническом гепатите С // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2002. Т. 12, № 2. — С. 55-61.
29. Мельниченко Г.А. Ожирение в практике эндокринолога // Рус. мед. журн. — 2001.-Т. 9, №2.-С. 82-87.
30. Мельниченко П.И., Огарков П.И., Смирнов А.В. и др. Актуальные проблемы профилактики вирусных гепатитов в Вооруженных Силах // Актуальные проблемы гепатологии: эпидемиология вирусных гепатитов: Прил. к 323-му т. Воен.-мед. журн. М., 2002. — С. 26-28.
31. Мухин Н.А. Практическая гепатология // Пособие по материалам «Школы гепатолога». Москва, 2004. — С. 6-294.
Москва, 2004. — С. 6-294.
32. Никитин И.Г. Клиника, диагностика и этиопатогенетическое лечение хронического HCV-гепатита: Автореф. дис. .д-ра мед. наук. М., 2000.
33. Никитин И.Г. Лечение хронического гепатита С: вчера, сегодня, завтра // Рос. журн. гастроэнтерол., гепатол., колопроктол. 2002. — Т. 12, № 6. — С. 11-16.
34. Никитин И.Г., Сторожаков Г.И. Пегилированные препараты: современное состояние проблемы и перспективы // Вирусные гепатиты, достижения и перспективы. 2001. — № 3 (13). — С. 3-8.
35. Никулкина Е.Н., Крель П.Е., Карпов В.В., Попова И.В. Оценка эффективности начальных высоких доз интерферона-а при хроническом гепатите С // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2001. — Т. 11, № 1.-С. 16.
36. Никулкина Е.Н., Крель П.Е., Лопаткина Т.Н. и др. Комбинированная терапия пегинтерфероном а-2Ь (ПегИнтроном) и рибавирином (Ребетолом) первичных больных хроническим гепатитом С // Клин. фарм. тер. — 2004. -№2.-С. 48-52.
37. Оленина Л.В. , Соболев Б.Н. Тканевой тропизм вируса гепатита С. // Вирусные гепатиты. Инф. бюллетень № 1(5), 1999, С. 11-17.
, Соболев Б.Н. Тканевой тропизм вируса гепатита С. // Вирусные гепатиты. Инф. бюллетень № 1(5), 1999, С. 11-17.
38. Онищенко Г.Г., Дементьева Л.А. Распространение вирусных гепатитов как угроза национальной безопасности // Журн. микробиол. 2003. — № 4. -С. 93-99.
39. Павлов А.И., Плюснин С.В., Хазанов А И. и др. Этиологические факторы циррозов печени с летальными исходами // Рос. журн. гастроэнтерол., гепатол., колопроктол. 2005. — Т. 15, № 2. — С. 68-72.
40. Павлов Ч.С. Гепатит С: естественное течение и подходы к терапии // Клин, перспективы гастроэнтерол., гепатол. — 2001. — № 3. С. 2-6.
41. Пасечников В.Д., Чуков С.З. Некоторые вопросы эпидемиологии, диагностики и лечения гепатоцеллюлярной карциномы // Рос. журн. гастроэнтерол., гепатол., колопроктол. 2002. — Т. 12, № 2. — С. 30-37.
42. Пинцани М. Эволюция фиброза печени: от гепатита к циррозу // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2002. Т. 12, № 5. — С. 4-9.
43. Плюснин С.В., Васенко В. И., Хазанов А.И. Эффективность лечения хронического гепатита С отечественным реафероном в течение 12 месяцев //
И., Хазанов А.И. Эффективность лечения хронического гепатита С отечественным реафероном в течение 12 месяцев //
44. Рос. журн. гастроэнтерол., гепатол., колопроктол. 2001. — Т. 11, № 5. — С. 85.
45. Плюсннн С.В., Васенко В.И., Хазанов А.И. Эффективность лечения хронического гепатита С отечественным реафероном в течение 6 месяцев // Рос. журн. гастроэнтерол., гепатол., колопроктол. 2001. — Т. 11, № 5. -С. 86.
46. Плюснин С.В., Васенко В.И., Хазанов А.И. Сравнительная характеристика эффективности и стоимости лечения хронического гепатита С отечественным и зарубежным интерфероном // Клин, аспекты авиационной медицины. -М., 2002. С. 257-259.
47. Попов В.Ф. Лекарственные формы интерферонов. М.: Триада X, 2002. -С. 136.
48. Рахманова А.Г., Паньков Н.С., Бадья С.А., Кукушкина М.В. Факторы прогрессирующего течения гепатита С // Гепатит С (Российский консенсус). Москва, 2000. — С. 112-113.
49. Раци Г. Комбинированная терапия при хронических вирусных гепатитах // Рос. журн. гастроэнтерол., гепатол., колопроктол. 2003. — Т. 13, № 5. -С. 58-65.
журн. гастроэнтерол., гепатол., колопроктол. 2003. — Т. 13, № 5. -С. 58-65.
50. Семендяева М.Е., Алешина Т.В., Бакулина И.Ф. Возможности оптимизации противовирусной терапии //’ Гепатит В, С, D и G — проблемы изучения, диагностики, лечения и профилактики. — Москва, 2001. С. 310-311.
51. Согласительная конференция по лечению гепатита С (Париж, Франция, 2728 февраля 2002 г.) // Медицинская кафедра. 2003. — № 1. — С. 127-141.
52. Соринсон С.Н. Вирусные гепатиты. // СПб.: ТЕЗА, 1998. С. 201-325.
53. Соринсон С.Н., Корочкина О.В. Интерферонотерапия гепатита С в ранние сроки путь достижения предпочтительных результатов. Тез. докладов. Симпозиум «Новые формулы в лечении гепатита С», 1999. — С. 1-3.
54. Соринсон С.Н., Корочкина О.В. Острая фаза гепатита С: диагностика, перспективы интерферонотерапии // Росс, журнал гастроэнтерологии, гепатологии и колопроктологии. 1999. — Т. 9, № 1. — С. 41-44.
55. Соринсон С. Н. Особенности патогенеза и течения гепатита С. Оптимальные сроки лечения интерфероном.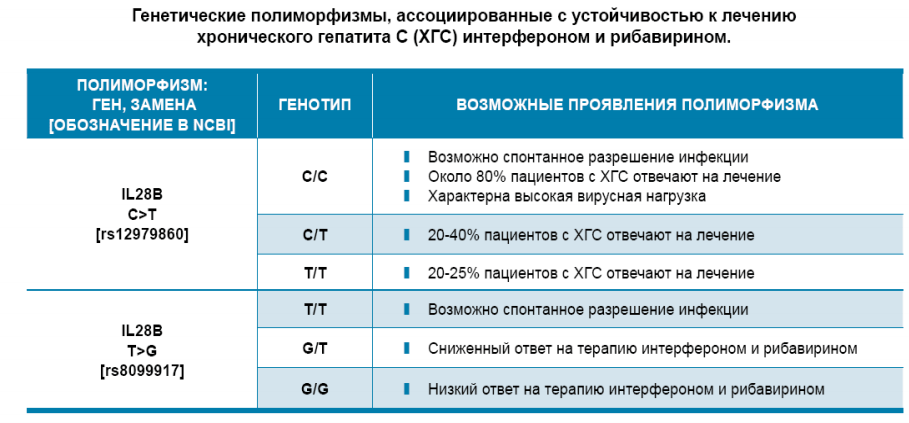 // Вирусные гепатиты. Инф. бюллетень, № 1, 1998, С. 3-8.
// Вирусные гепатиты. Инф. бюллетень, № 1, 1998, С. 3-8.
56. Суздальцев А., Юрченко Н.Г. Парентеральные гепатиты у наркоманов // Гепатит В, С, D и G проблемы изучения, диагностики, лечения и профилактики. — Москва, 1999. — С. 219.
57. Сюткин В.Е., Лопаткина Т.Н., Попова И.В. Факторы риска прогрессирования поражения печени при хроническом гепатите вирусной этиологии // Кремлевская мед. (клин, вестн.). 2000. — № 1. — С. 40-44.
58. Танащук Е.Л. Хронические заболевания печени у лиц, злоупотребляющих алкоголем, инфицированных вирусами геиатита: Автореф. дис. . канд. мед. наук.-М., 1999.
59. Хазанов А.И., Васильев А.П., Пехташев С.Г. и др. О дополнительных повреждающих факторах в развитии вирусных циррозов печени // Рос. журн. гастроэнтерол. гепатол., колопроктол. — 2001. — Т. 11 (Прилож. № 12). — С. 29.
60. Хазанов А.И., Пономарев С.В., Кубенский Е.Н. и др. Этиологические профили, диагностика и исходы острых вирусных гепатитов у больных, леченных стационарно в последние 20 лет // Рос. мед. вести. 2000. — Т. 5, №2.-С. 30-35.
мед. вести. 2000. — Т. 5, №2.-С. 30-35.
61. Хлопова И.Н., Чешик С.Г., Козлова А.В., Самохвалов Е.Н. Опыт применения Реаферона-А при остром вирусном гепатите С при различных генотипах HCV // Гепатит С (Российский консенсус). Москва, 2000. — С. 158.
62. Хронический вирусный гепатит / Под ред. Серовой В.В., Апросиной З.Г. — М.: Медицина. 2002. — С. 384.
63. Шахгильдян И.В. Современная эпидемиологическая характеристика гепатитов В и С в Российской Федерации // Вирусные гепатиты: достижения и перспективы. 1999. — № 3 (7). — С. 9-16.
64. Шахгильдян И.В. Вирусные гепатиты В и С в России: Эпидемиологическая характеристика и основные направления их профилактики // Актуальные проблемы гепатологии: эпидемиология вирусных гепатитов: Прил. К 323-му т. Воен.-мед. журн. -М., 2002. С. 12-18.
65. Шерлок Ш., Дули Д. Заболевания печени и желчных путей. Пер. с англ./ Под ред. 3. Г. Апросиной, Н. А. Мухина. М.: Гэотар Медицина, 1999. — С. 864.
66. Язенок Н.С. Комбинированное лечение хронического гепатита С (генотип За) российскими противовирусными препаратами (реаферон, интераль, веро-рибавирин, рибамидил): эффективность и безопасность.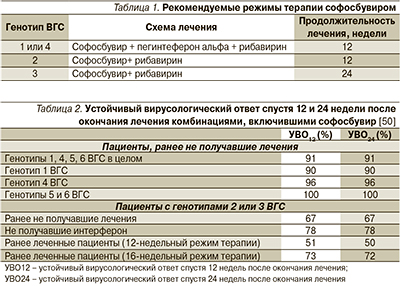 Материалы дис. .канд. мед. наук. -М., 2005.
Материалы дис. .канд. мед. наук. -М., 2005.
67. Ярков А.Н., Сафонов А.Д., Павлова JI.C. К вопросу дифференциальной диагностики острых и хронических форм HCV-инфекции // Гепатит В, С, D и G — проблемы изучения, диагностики, лечения и профилактики. Москва, 2001.-С. 408-409.
68. Ястребова О.Н. Гепатит С. — Информационно-методическое пособие. — Кольцово, 1999.-С. 23.
69. Abrignani S., Houghton М., Hsu Н.Н. Perspectives for a vaccine against hepatitis С virus // J. Hepatology. 1999. — Vol. 31 (Suppl. 1). — P. 259-263.
70. Alberti A., Chemello L., Benvegnu L. Natural history of hepatitis С // J. Hepatology. 1999. — Vol. 31, suppl. 1. — P. 17-24.
71. Alberti A., Benvegnu L. Management of hepatitis С // J. Hepatol. 2003. -Vol. 38.-P. 104-118.
72. Alberti A., Boccato S., Vario A., Benvegnu L. Therapy of acute hepatitis С // Hepatology. 2002. — Vol. 36. — P. 195-200.
73. Alter H.J., Kruszon Moran D., Nainan O.V. et al. The prevalence of hepatitis С viremia in the USA, 1988 through 1994 // N. Engl. Med. — 1999. — Vol. 341. -P. 556-562.
Engl. Med. — 1999. — Vol. 341. -P. 556-562.
74. Alter H.J., Seef L.B. Recovery, persistence and sequelae in hepatitis С virus infection: a prospective on longterm outcome // Semin. Liver Dis. 2000. -Vol. 20.-P. 17-35.
75. Angulo P. Non-alcoholic fatty liver disease // New Engl. J. Med. — 2002. -Vol. 346.-P. 1221-1231.
76. Arii S., Yamaoka Y., Futagawa S. et al. Results of surgical and nonsurgical treatment for small-sized hepatocellular carcinomas: a retrospective and nationwide survey in Japan // Hepatology. 2000. — Vol. 32. — P. 1224-1229.
77. Armstrong G.L. et al. The past incidence of hepatitis С virus infection: implications for the future burden of chronic liver disease in the United States // Hepatology. -2000. Vol. 31. — P. 777-782.
78. Bacon B.R. Chronic hepatitis С and normal ALT: consideration for treatment // Amer. J. Gastroenterol. 2004. — Vol. 99, № 9. — P. 1706-1707.
79. Bartenschlager R., Lohmann V. Replication of hepatitis С virus (Review Article) // J. Gen. Virol. 2000. — Vol. 81. — P. 1631-1648.
Gen. Virol. 2000. — Vol. 81. — P. 1631-1648.
80. Beckingham I.J., Krige J.E.J. Liver tumours // BMJ. 2001. — Vol. 322 — P. 478479.
81. Bekkering F.C., Brower J.T., Hansen B.E. et al. Hepatitis С viral kinetics in difficult to treat patients receiving high dose interferon and ribavirin // J. Hepatol. 2001. — Vol. 34. — P. 435-440.
82. Berg Т., Sarrazin C., Herrmprm E. et al. Prediction of treatment outcome in patients with chronic hepatitis C: significance of baseline parameters and viral dynamics during therapy // Hepatology. 2003. — Vol. 37. — P. 600-609.
83. Bosch F.X., Ribes J., Borras J. Epidemiology of primary liver cancer // Semin. Liver Dis. 1999. — Vol. 19. — P. 271-286.
84. Bressler В., Guindi M., Tomlinson G. et al. High body mass index is an independent risk factor for nonresponse to antiviral treatment in chronic hepatitis С // Hepatology. 2003. — Vol. 38. — P. 639-644.
85. Browning J.D., Szczepaniak L.S., Dobbins R. et al. Prevalence of hepatic steatosis in an urban population in the United States: impact of ethnicity // Hepatology.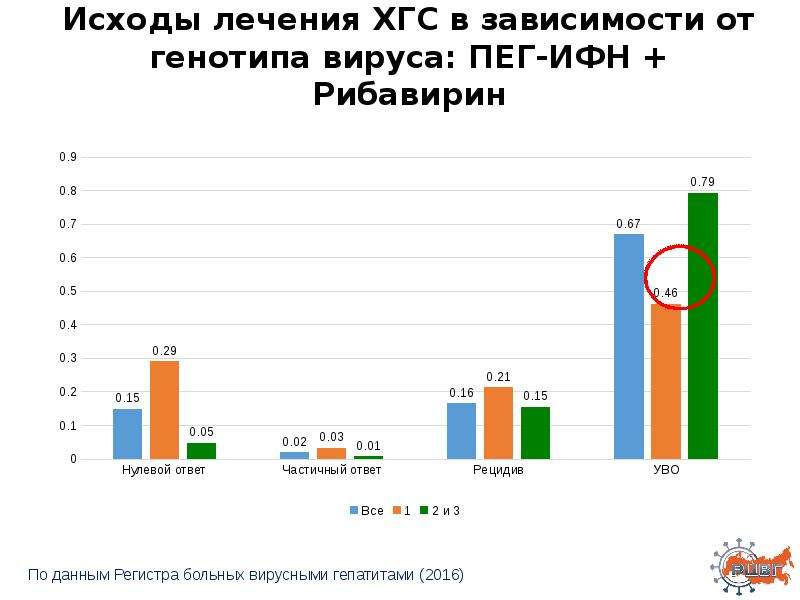 2004. — Vol. 40. — P. 1387-1395.
2004. — Vol. 40. — P. 1387-1395.
86. Bruix J., Sherman M., Llovet J.M. et al. Clinical Management of Hepatocellular Carcinoma. Conclusions of the Barcelona-2000 EASL Conference // J. Hepatology. 2001. — Vol. 35. — № 3. — P. 421-430.
87. Buti M., Medina M., Casado M. et al. A cost-effectiveness analysis of peginterferon-alpha-2b plus ribavirin for the treatment of naive patients with chronic hepatitis С // Aliment. Pharmacol. Ther. 2003. — Vol. 17. — P. 687-694.
88. Cacciola I., Pollicino Т., Souadrito G. et al. Occult hepatitis В virus infection in patients with chronic hepatitis С liver disease // New Engl. J. Med. 1999. -Vol. 341.-P. 22-26.
89. Camma C., Giunta M., Andreone P., Craxi A. Interferon and prevention of hepatocellular carcinoma in viral cirrhosis: an evidence-based approach // J. Hepatol. 2001. — Vol.34, № 4. — P. 593-602.
90. Camma C., Bruno S., Schepis F. et al. Retreatment with interferon plus ribavirin of chronic hepatitis С non-responders to interferon monotherapy: a meta-analysis of individual patient data // Gut.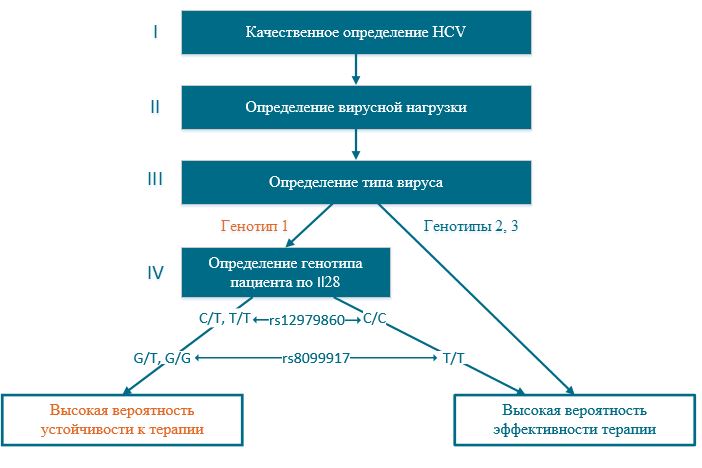 2002. — Vol.51. — P. 864-869.
2002. — Vol.51. — P. 864-869.
91. Chapoutot C., Esslimani M., Joomaye Z. et al. Liver iron excess in patients with hepatocellular carcinoma developed on viral С cirrhosis // Gut. 2000. — Vol. 46. -P. 163-165.
92. Chen M., Sallberg M., Sonnerborg A. et al. Limited humoral immunity in hepatitis С virus infection // Gastroenterology. 1999. — Vol. 116, № 1, P. 135143.
93. Colombo M. Hepatitis С virus and hepatocellular carcinoma // Semin. Liver Dis. 1999. — Vol. 19. — P. 263-269.
94. Davis G.L., Albright J.E., Cook S.F., Rosenberg D.M. Projecting future complications of chronic hepatitis С in the United States // Liver. Transpl. -2003.-Vol. 9. -P. 331-338.
95. De Mitri M.S., Mele L., Morsica G., Chen C.H. et al. Effect of increasing dose of interferon on the evolution of hepatitis С virus lb quasispecies // J. Med. Virol. 2000. — Vol. 60. — P. 133-138.
96. De Mitri M.S., Mele L., Chen C.H. et al. Comparison of serum and liver hepatitis С virus quasispecies in HCV-related hepatocellular carcinoma // J. Hepatol. 1998. — Vol. 29. — № 6. — P. 887-892.
Hepatol. 1998. — Vol. 29. — № 6. — P. 887-892.
97. Desch S., Vaeth Т., Tamba M. et al. Efficacy and safety of an initial daily dosing regiment of interferon-alpha-2a in treatment naive patients with chronic hepatitis С and HCV genotype 1 // Europ. J. Med. Res. — 2001. — Vol. 6, № 6. — P. 242-246.
98. Deuffic-Burban S., Wong J.B., Valleron A.J. et al. Comparing the public health burden of chronic hepatitis С and HIV infection in France // J. Hepatol. 2004. -Vol. 40.-P. 319-326.
99. Di Bisceglie A., Hoofhagle J. Optimal therapy of hepatitis С // Hepatology. — 2002. Vol. 36. — P. 121-127.
100. Dove L.M., Alonzo J., Wright T.L. Clinicopathological conference: hepatitis С in patients with human immunodeficiency virus infection // Hepatology. 2000. -Vol. 32.-P. 147-152.
101. EASL International Consensus Conference on Hepatitis С // J. Hepatology. — 1999.-Vol. 339.-P. 956-961.
102. El-Serag H.B., Mason A.C. Rising incidence of hepatocellular carcinoma in the United States // New Engl. J. Med. 1999. — Vol. 340. — P. 745-750.
J. Med. 1999. — Vol. 340. — P. 745-750.
103. El-Serag H.B., Davila J.A., Petersen N.J., McGlynn K.A. The continuing increase in the incidence of hepatocellular carcinoma in the United States: an update // Ann. Intern. Med. 2003. — Vol. 139. — P. 817-823.
104. El-Serag H.B., Hampel H., Yeh C., Rabeneck L. Extrahepatic manifestations of hepatitis С among United States male veterans // Hepatology. 2003. — Vol. 36. -P. 1439-1445.
105. Falck-Ytter Y., Kale H., Mullen K.D. et al. Surprisingly small effect of antiviral treatment in patients with hepatitis С // Ann. Intern. Med. 2002. — Vol. 136. -P. 288-292.
106. Farci P., Purcell R.H. Clinical significance of hepatitis С virus genotypes and quasispecies // Semin. Liver Dis. 2000. — V;l. 20. — P. 103-126.
107. Ferrari C., Urbani S., Penna A. et al. Immunopatogenesis of hepatitis С virus infection // J. Hepatol. 1999. — Vol. 31, suppl. 1. — P. 31-38.
108. Fontaine H., Chaix M.L., Lagneau J.L. et al. Recoveri from chronic hepatitis С in long-term responders to ribavirin plus interferon-a // Lancet. — 2000. -Vol. 356. P. 41-43.
— 2000. -Vol. 356. P. 41-43.
109. Fook-Hong N., Kai-Chiu C., Chi-Sing C. et al. High alpha-fetoprotein level in HCV-related nodular liver cell dysplasia // Am. J. Gastroenterol. 1999. -Vol. 94. — P. 2296-2297.
110. Forns X., Bukh J., Purcell R.H. The challenge of developing a vaccine against hepatitis С vims // J. Hepatol. 2002. — Vol. 37. — P. 684-695.
111. Forns X., Bukh J. The molecular biology of hepatitis С virus. Genotypes and quasispecies // Clin. Liver Dis. 1999. — Vol. 3. — P. 693-716.
112. Fried M.W., Shiffman M.L., Reddy R. et al. Peginterferon-alpha-2a plus ribavirin for chronic hepatitis С virus infection // N. Engl. J. Med. 2002. -Vol. 347. — P. 975-982.
113. Fried M.W. Side effects of therapy of hepatitis С and their management // Hepatology. 2002. — Vol. 36. — P. 237-244.
114. Fujie H., Yotsuyanagi H., Moriya K. et al. Steatosis and intrahepatic hepatitis С virus in chronic hepatitis // J. Med. Virol. 1999. — Vol. 59. — P. 141-145.
115. Gane E. The natural history and outcome of liver transplantation in hepatitis С virus infected recipients // Liver. Transpl. 2003. — Vol. 9. — P. 28-34.
Gane E. The natural history and outcome of liver transplantation in hepatitis С virus infected recipients // Liver. Transpl. 2003. — Vol. 9. — P. 28-34.
116. Gerlach J.T., Diepolder H.M., Zachoval R. et al. Acute hepatitis C: high rate of both spontaneous and treatment-induced viral clearance // Gastroenterology. -2003.-Vol. 125.-P. 80-88.
117. Glue P. et al. Pegylated interferon-a-2b: pharmacokinetics, pharmacodynamics, safety and preliminary efficacy data // Clin. Pharm. Ther. 2000. — Vol. 68. -P. 556-567.
118. Grando-Lemaire V., Guettier C., Chevret S., Beaugrand M. Hepatocellular carcinoma without cirrhosis in the West: epidemiological factors and histopathology of the non-tumorous liver // J. Hepatol. 1999. — Vol. 31. — P. 508513.
119. Hadziyannis S.J., Sette jr H., Morgan T.R. et al. Peginterferon alfa-2a and ribavirin combination therapy in chronic hepatitis C. A randomized study of treatment duration and ribavirin dose // Ann. Intern. Med. 2004. — Vol. 140. -P. 346-355.
-P. 346-355.
120. Handbook of liver diseases // Churchill Livingstone, 2004 2nd ed. P. 52-56.
121. Heathcote E., Shiftman M.,Cooksley W. et al. Peginterferon-alpha-2a in patients with chronic hepatitis С and cirrhosis // N. Engl. J. Med. 2000. — Vol. 343. -P. 1673-1680.
122. Herrine S., Brown R., Esposito S. et al. Efficacy and safety of peginterferon alpha-2a (Pegasys) combination therapies in patients who relapsed on Rebetron therapies // Hepatology. 2002. — Vol. 36. — P. 359.
123. Herve S., Savoye G., Riachi G. et al. Chronic hepatitis С with normal or abnormal aminotransferase levels: is it the same entity? // Europ. J. Gastroenterol. Hepatol. 2001. — Vol. 13. — P. 495-500.
124. Hezode C., Lonjon I., Roudot-Thoraval F. et al. Impact of smoking on histological liver lesions in chronic hepatitis С // Gut. 2003. — Vol. 52. — P. 126129.
125. Hoofnagle J. Course and outcome of hepatitis С // Hepatology. 2002. — Vol. 36. suppl. 1.-P. 21-29.
126. Hourigan L. F., Macdonald G.A., Purdie D. et al. Fibrosis in chronic hepatitis С correlates significantly with body mass index and steatosis // Hepatology. -1999.-Vol. 29.-P. 1215-1219.
F., Macdonald G.A., Purdie D. et al. Fibrosis in chronic hepatitis С correlates significantly with body mass index and steatosis // Hepatology. -1999.-Vol. 29.-P. 1215-1219.
127. Hu K.Q., Tong V.J. The long-term outcomes of patients with compensated hepatitis С virus-related cirrhosis and history of parenteral exposure in the United States // Hepatology. 1999. — Vol. 29. — P. x311-1316.
128. Jacobson Brown P.M., Neuman M.G. Immunopatogenesis of hepatitis С viral infection: Thl/Th3 responses and the role of cytokines // Clin. Biochem. 2001. -Vol. 34, №3.-P. 167-171.
129. Jacobson I.M., Ahmed F., Russo M.W. et al. Interferon alfa-2b (correction of alfa-2b) and ribavirin for patients with chronic hepatitis С and normal ALT // Amer. J. Gastroenterol. 2004. — Vol. 99, № 9. — P. 1700-1705.
130. Jaeckel E., CornbergM., Wedemeyer H. et al. Treatment of acute hepatitis С with interferon-alpha-2b //N. Engl. J. Med. 2001. — Vol. 345. — P. 1452-1457.
131. Jen J., Laughlin M. , Chung C. et al. Ribavirin dosing in chronic hepatitis C: application of population pharmacokinetic-pharmacodynamic models // Clin. Pharmacol. Ther. 2002. — Vol. 72. — P. 349-361.
, Chung C. et al. Ribavirin dosing in chronic hepatitis C: application of population pharmacokinetic-pharmacodynamic models // Clin. Pharmacol. Ther. 2002. — Vol. 72. — P. 349-361.
132. Jennie R. et al. Acute hepatitis С // Hepatology. 2001. — Vol. 33, № 2. — P. 321327.
133. Kao J.-H., Liu C.-J.,Chen P.-J. et al. Low incidence of hepatitis С virus transmission between spouses: a prospective study // J. Gastroenterol. 2000. -Vol. 15.-P. 391-395.
134. Kasahara A., Hayashi N., Mochizuki K. et al. Risk factors for hepatocellular carcinoma and its incidence after interferon treatment in patients with chronic hepatitis С // Hepatology. 1998. — Vol. 27. — P. 1394-1402.
135. Kojiro M. Premalignant lesions of hepatocellular carcinoma: pathologic viewpoint // J. Hepatobiliary Pancreat. Surg. 2000. — Vol. 7. — P. 535-541.
136. Kronenberger В., Herrmann E., Micol F. et al. Viral kinetics during antiviral therapy in patients with chronic hepatitis С and persistently normal ALT levels // J.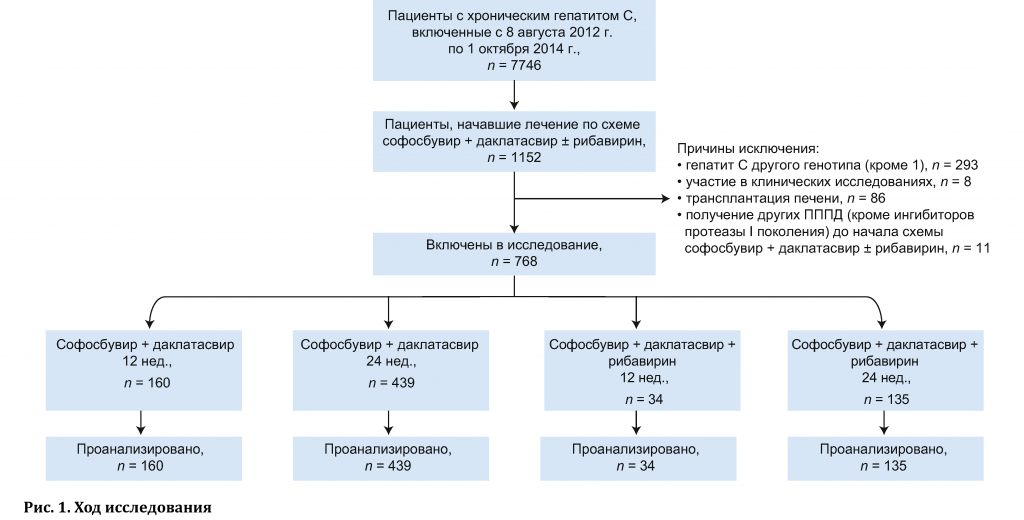 Hepatol. 2004. — Vol. 40, № 6. — P. 1442-1449.
Hepatol. 2004. — Vol. 40, № 6. — P. 1442-1449.
137. Kuntz E., Kuntz H.-D. Hepatology principles and practice springer — Verlag. Berlin, Heiderberg, 2002. — P. 83-84.
138. Lamarre D., Anderson P.C.,Bailey M. et al. An NS3 protease inhibitor with antiviraleffects in humans infected with hepatitis С virus // Nature. 2003. -Vol. 426.-P. 186-189.
139. Lindsay К., Trepo C., Heintges T. et al. A randomized, double-blind trial comparing pegylated interferon-alpha-2b to interferon-alpha-2b as initial treatment for chronic hepatitis С // Hepatology. 2001. — Vol. 34. — P. 395-403.
140. Manns M., McHutchison J., Gordon S. et al. Peginterferon-alpha-2b plus ribavirin compared with interferon-alpha-2b plus ribavirin for initial treatment of chronic hepatitis C: a randomised trial // Laroet. 2001. — Vol. 358. — P. 958-965.
141. Marcellin P. Hepatitis C: the clinical spectrum of the disease // J. Hepatol. -1999. Vol. 31,suppl. l.-P. 9-16.
142. Marcellin P., Asselah Т. , Boyer N. Fibrosis and disease progression in hepatitis С // Hepatology. 2002. — Vol. 36, suppl. l.-P. 47-56.
, Boyer N. Fibrosis and disease progression in hepatitis С // Hepatology. 2002. — Vol. 36, suppl. l.-P. 47-56.
143. Marco V., Almasio P., Vaccaro A. et al. Combined treatment of relapse of chronic hepatitis С with high-dose alpha 2b interferon plus ribavirin for 6 or 12 months // J. Hepatol. 2000. — Vol. 33. — P. 456-462.
144. Marusawa H., Osaki Y., Kimura T. et a1. High prevalence of anti-hepatitis В virus serological markers in patients with hepatitis С virus-related chronic liver disease in Japan// Gut. 1999. — Vol. 45. — P. 284-288.
145. Mayo M.J. Extrahepatic manifestations of hepatitis С infection // Am. J. Med. Sci. 2003. — Vol. 325, № 3. — P. 135-148.
146. Mc Cullough A. Obesity and its nurturing effect on hepatitis С // Hepatology. -2003.-Vol. 38.-P. 557-559.
147. Moradpour D., Brass V., Gosert R. et al. Hepatitis C: molecular virology and antiviral targets // Trends Mol. Med. 2002. — Vol. 8. — P. 476-482.
148. Nagayama K., Kurosaki M., Enomoto N. et al. Characteristics of hepatitis С viral genome associated with disease progression // Hepatology. — 2000: -Vol. 31.-P. 745-750.
et al. Characteristics of hepatitis С viral genome associated with disease progression // Hepatology. — 2000: -Vol. 31.-P. 745-750.
149. National Institute of Health Consensus development conference statement: Management of hepatitis C: 2002 // Hepatology. 2002. — Vol. 36, № 5 (suppl. 1). — P. 3-19.
150. Negro F., Samii K., Rubbia-Brandt L. et al. Hemochromatosis gene mutations in chronic hepatitis С patients with and without liver siderosis // J. Med. Virol. — 2000.-Vol. 60.-P. 21-27.
151. Neumann A.U., Lam N.P., Dahari H. et al. Hepatitis С viral dynamics in vivo and the antiviral efficacy of interferon alpha therapy // Science. 1998. -Vol. 282.-P. 103-107.
152. Neumann U.P., Berg Т., Bahra M. et al. Long-term outcome of liver transplants for chronic hepatitis C: a 10-year follow up // Transplantation. 2004. — Vol. 77. -P. 226-231.
153. Nevens F., Roskams Т., Van Vlierberghe H. et al. A pilot study of therapeutic vaccination with envelope protein El in 35 patients with chronic hepatitis С // Hepatology.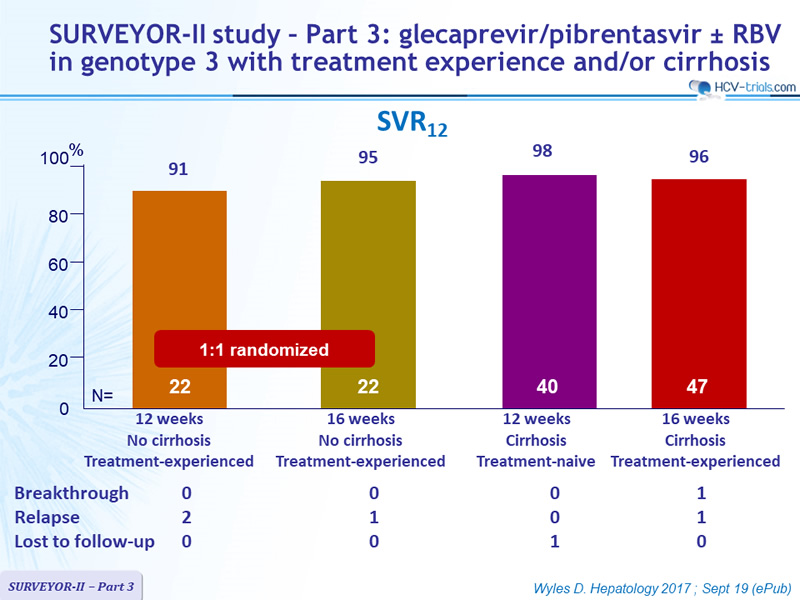 2003. — Vol. 38. — P. 1290-1296.
2003. — Vol. 38. — P. 1290-1296.
154. Nishiguchi S., Shiomi S., Nakatani S. et al. Prevention of hepatocellular carcinoma in patients with chronic active hepatitis С and cirrhosis // Lancet. -2001.-Vol. 357.-P. 196-197.
155. Okoshi S., Takeda Y., Takimoto M. et al. Molecular dissection of hepatitis С virus expression // Intervirology. 2001. — Vol. 44, № 1. — P. 21-28.
156. Ortiz V., Berenguer M., Rayon J. et al. Contribution of obesity to hepatitis C-related fibrosis progression // Am. J. Gastroenterol. 2002. — Vol. 97. — P. 24082414.
157. Pagliaro L., Peri V., Linea C. et al. Natural history of chronic hepatitis С // Ital. J. Gastroenterol. Hepatol. 1999. — Vol. 31. — P. 28-44.
158. Parana R., Vitvitski L., Andrade Z. et al. Acute sporadic non-A, non-B hepatitis in Northeastern Brazil: etiology and natural history // J. Hepatology. 1999. -Vol. 30. — P. 289-293.
159. Parkin D.M. Global cancer statistics in the year 2000 // Lancet oncol. 2001. -Vol.2. -P. 533-543.
-P. 533-543.
160. Pawlotsky J.M. Use and interpretation of virological tests for hepatitis С // Hepatology. 2002. — Vol. 36. — P. 65-73.
161. Pawlotsky J.M., McHutchison J.G. Hepatitis C. Development of new drugs and clinical trials: promises and pitfalls // Hepatology. 2004. — Vol. 39. — P. 554-567.
162. Paydas S., Kilic В., Sahin B. et al. Prevalence of hepatitis С virus infection in patients with lymphoproliferative disorders in Southern Turkey // Br. J. Cancer. -1999. Vol. 80. — P. 1303-1305.
163. Penin F., Dubuisson J., Rey F.A. et al. Structural biology of hepatitis С virus // Hepatology. 2004. — Vol. 39. — P. 5-19.
164. Persico M., Persico E., Suozzo R. et al. Natural history of hepatitis С virus carriers with persistently normal aminotransferase levels // Gastroenterology. —2000.-Vol. 118.-P. 760-764.
165. Porru S., Placidi D., Carta A. et al. Primary liver cancer and occupation in men: a case-control study in a high-incidence area in Northern Italy // Int. J. Cancer.2001. Vol. 94, № 6. — P. 878-883.
J. Cancer.2001. Vol. 94, № 6. — P. 878-883.
166. Powell E.E., Edwards-Smith C.J., Hay J.L. et al. Host genetic factors influence progression in chronic hepatitis С // Hepatology. 2000. — Vol. 31. — P. 828-833.
167. Reddy K., Wright Т., Pockros P. et al. Efficacy and safety of Pegylated (40-kd) interferon alpha-2a compared with interferon alpha-2a in noncirrhotic patients with chronic hepatitis С // Hepatology. 2001. — Vol. 33. — P. 433-438.
168. Rodger A.J., Roberts S., Lanigan A. et al. Assessment of long-term outcomes of community-acquired hepatitis С infection in cohort with sera stored from 1971 to 1975 // Hepatology. 2000. — Vol. 32. — P. 582-587.
169. Rubbia-Brandt L., Quadri R., Adid K. et al. Hepatocyte steatosis is a cytopathic effect of hepatitis С virus genotype 3 // J. Hepatol. 2000. — Vol. 33. — P. 106-115.
170. Saracco G., Olivero A., Ciancio A. et al. Therapy of chronic hepatitis C: a critical review // Curr. Drug Targets Infect. Disort. 2003. — Vol. 3. — P. 25-32.
— Vol. 3. — P. 25-32.
171. Schott P., Hartmann H., Ramadori G. Hepatitis С virus-associated mixed cryoglobulinemia. Clinical manifestations, histopatological changes, mechanisms of cryoprecipitation and options of treatment // Histol Histopatol. 2001. — Vol. 16.-P. 1275-1285.
172. Seeff L.B., Hollinger F.B., Alter H.J. et al. Long-term mortality and morbidity of transfusion-associated non-A, non-B, and type С hepatitis: A National Heart, Lung, and Blood Institute Collaborative study // Hepatology. 2001. — Vol. 33. -P. 455-463.
173. Seeff L.B., Miller R.N., Rabkin C.S. et al. 45-year follow-up of hepatitis С virus infection in healthy young adults // Ann. Intern. Med. 2000. — Vol. 132. — P. 105111.
174. Seeff L.B. Natural history of chronic hepatitis С // Hepatology. 2002. -Vol. 36, suppl. l.-P. 35-46.
175. Shakil A.O., McGuire В., Crippin J. et al. A pilot study of interferon alfa and ribavirin combination in liver transplant recipients with recurrent hepatitis С // Hepatology. 2002. — Vol. 36. — P. 1253-1258.
2002. — Vol. 36. — P. 1253-1258.
176. Shiffman M.L. Management of interferon therapy non-responders // Clin. Liver. Dis.-2001.-Vol. 5.-P. 1025-1043.
177. Shiffman M.L., Hofmann C., Contos M. et al. A randomized, controlled trial of maintenance interferon therapy for patients with chronic hepatitis С virus and persistent viremia // Gastroenterology. 1999. — Vol. 117. — P. 1164-1172.
178. Shiffman M.L. et al. Retreatment of HCV non-responders with peginterferon and ribavirin: results from the lead-in phase of the HALT-C // Trial. Hepatology. -2002. Vol. 36. — P. 295.
179. Shiffman M.L., Vargas H.E., Everson G.T. Controversies in the management of hepatitis С virus infection after liver transplantation // Liver Transpl. 2003. -Vol. 9.-P. 1129-1144.
180. Shiffman M.L. Use of high-dose interferon in the treatment of chronic hepatitis С // Semin. Liver. Dis. 1999. — Vol. 19, suppl. l.-P. 25-33.
181. Shiratori Y., Yoshida H., Omata M. Different clinico-pathological features of hepatocellular carcinoma in relation to causative agents // J.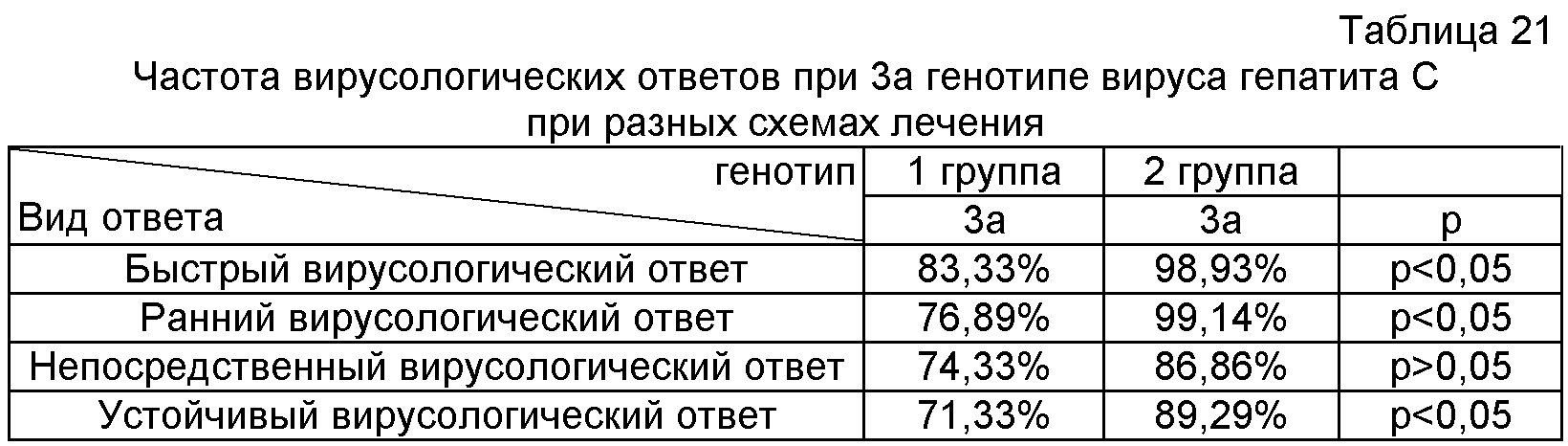 Gastroenterol. -2001.-Vol. 36.-P. 73-78.
Gastroenterol. -2001.-Vol. 36.-P. 73-78.
182. Siebert U., Sroczynski G., Rossol S. et al. Cost effectiveness of peginterferon alpha-2b plus ribavirin versus interferon alpha-2b plus ribavirin for initial treatment of chronic hepatitis С // Gut. 200\ — Vol. 52. — P. 425-432.
183. Simmonds P. Viral heterogeneity of hepatitis С virus // J. Hepatology. — 1999. -Vol.31 (Suppl. 1).-P. 54-60.
184. Simmonds P. SGM 2000 Fleming Lecture. The origin and evolution of hepatitis С viruses in humans // J. Gen. Virol. 2001. — Vol. 82. — P. 693-712.
185. Takayama Т., Hirohashi M. et al. Malignant transformation of adenomatous hyperplasia to hepatocellular carcinoma // Lancet. 1999. — Vol. 336. — P. 1150.
186. Takayama Т., Makuushi M. Ablation of hepatocellular carcinoma // Jpn. J. Clin. Oncol. 2001. — Vol. 31, № 7. — P. 297-298.
187. Tanabe G., Nuruki K., Baba Y. et al. A ccuparison of hepatocellular carcinoma associated with HBV or HCV infection // Hepatogastroenterology. 1999. -Vol. 46. — P. 2442-2446.
1999. -Vol. 46. — P. 2442-2446.
188. Torres В., Martin J.L., Caballero A. et al. HCV in serum, peripheral blood mononuclear cells and lymphocyte subpopulations in C-hepatitis patients // Hepatol. Res. 2000. — Vol. 18, № 2. — P. 141-151.
189. Tran T.T., Martin P. Chronic hepatitis С // Curr. Treat. Options Gastroenterol. -2001. Vol. 4, № 6. — P. 503-510.
190. Wasmuth H.E., Stolte C., Geier A. et al. The preasence of non-organ-specific autoantibodies is associated with a negative response to combination therapy with interferon and ribavirine for chronic hepatitis С // BMC Infect. Dis. — 2003. -№ 4. P. 4.
191. WHO. Prevention and management of the global epidemic of obesity: Report of the WHO consultation on obesity. — Geneva, 1997.
192. Wiese M., Berr F., Lafrenz M. et al. Low frequency of cirrhosis in a hepatitis С (genotype lb) single-source outbreak in Germany: a 20-year multicenter study // Hepatology. -2000. Vol. 32. — P. 91-96.
193. Wong W., Fu A.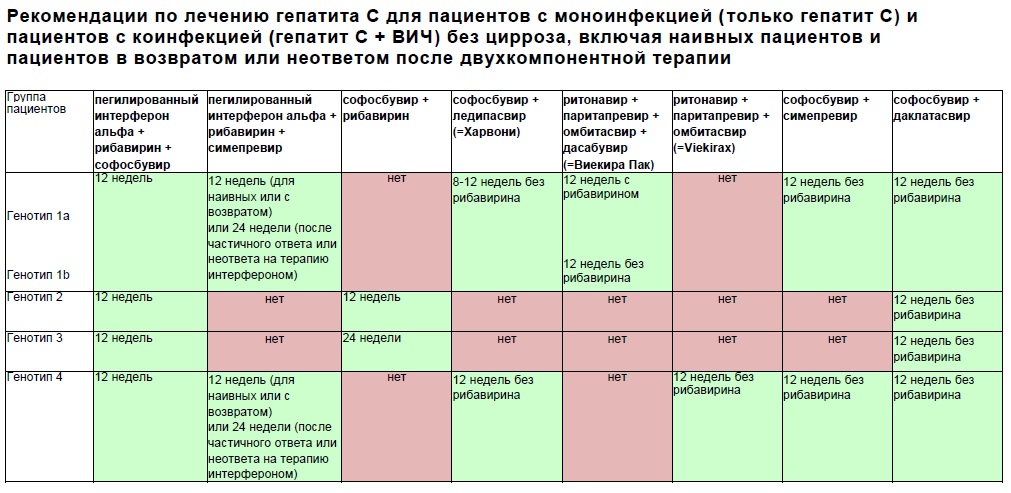 , George J. et al. Thyrotoxicosis induced by alpha-interferon therapy in chronic viral hepatitis С // Endocrinol (Oxf). — 2002. Vol. 56, № 6. -P. 793-798.
, George J. et al. Thyrotoxicosis induced by alpha-interferon therapy in chronic viral hepatitis С // Endocrinol (Oxf). — 2002. Vol. 56, № 6. -P. 793-798.
194. World Health Organization. Hepatitis С global prevalence // Wkly Epidemiol. Rec. — 2002. — Vol. 77. — P. 41-48.
195. Yu S., Zhao N., Zi X. The relationship between cyanotoxin (microcystin, MC) in pond-ditch water and primary liver cancer in China // Zhonghua Zhong Liu Za Zhi. 2001. — Vol. 23, № 2. — P. 96-99.
196. Zeuzem S., FeinmanS., Rasenack J. et al. Peginterferon-alpha-2a in patients with chronic hepatitis С // N. Engl. J. Med. 2000. — Vol. 343. — P. 1666-1672.
197. Zignego A., Brechot C. Extrahepatic manifestations of HCV infection: facts and controversies // J. Hepatol. 1999. — Vol. 31. — P. 369-376.
198. Zitrin I.M., Laurinaitis M., Qu 1. et al. Immunological responses in patients who have spontaneously eradicated hepatitis С virus infection // Viral. Immunol. -2000.-Vol. 13, №4.-P. 521-531.
199.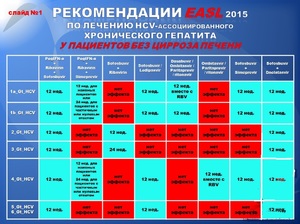 Zylberberg H., Thires V., Lagorce D. et al. Epidemiological and virological analysis of couples infected with hepatitis С virus // Gut. 1999. — Vol. 45. — P. 112-116.
Zylberberg H., Thires V., Lagorce D. et al. Epidemiological and virological analysis of couples infected with hepatitis С virus // Gut. 1999. — Vol. 45. — P. 112-116.
лечение и диагностика причин, симптомов в Москве
Общее описание
Гепатит С – это хроническое антропонозное вирусное заболевания, вызываемое инфицированием вирусом гепатита С. Возникает воспаление печеночных клеток-гепатоцитов и их повреждение. Вирусный гепатит С бывает хроническим и острым.
По данным ВОЗ во всем мире болеют хроническим гепатитом С около 150-170 миллионов человек. Приблизительно у 10-15% людей заболевание переходит т в цирроз печени и, возможно, рак.
Ежегодно от цирроза печени и рака, связанных с гепатитом С, умирают около 350-500 тыс. человек.
Причины возникновения гепатита С
Основным механизмом заражения является передача здоровому человеку от больного вируса гепатита С через кровь.
Пути передачи гепатита С
- Использование парентеральных наркотиков при совместном использовании устройств для инъекций
- При оказании медицинской помощи (повторное использование или недостаточная стерилизация медицинского оборудования- шприцев и игл)
- При переливании крови и/или продуктов крови, зараженной вирусом гепатита С
- При незащищенном половом акте с больным гепатитом С
- Передача от матери, инфицированной вирусом гепатита С, внутриутробно ее ребенку
- Гепатит С не передается через грудное вскармливание, пищевые продукты, воду, при бытовых контактах (объятиях, поцелуях)
Симптомы гепатита С
От момента заражения до клинических проявлений проходит от 2-4 недель до 6-12 месяцев. Клинические проявления самого заболевания являются нестрого специфическими:
Клинические проявления самого заболевания являются нестрого специфическими:
- Общая слабость
- Снижение аппетита
- Повышенная утомляемость
- Диспепсия, проявляющаяся в виде тошноты, горечи во рту, чередования запоров с диареей, боли в эпигастрии и в правом подреберье
- Иногда наблюдается субфебрилитет
- Редко желтушность кожный покровов, склер
Появление симптомов
- Увеличение в объеме живота, сосудистые звездочки на коже живота, нарастание слабости, наличие “головы медузы”
- Стойкая желтуха
- Кровоточивость десен
- Кожный зуд
Диагностика:
Основные способы диагностики гепатита С:
- Биохимический анализ крови (на маркеры повреждения печени и оценки функции — уровень АЛТ, АСТ, ГГТП, общего белка и его фракций, билирубина, уровень креатинина, мочевины, глюкозы)
- Короткая коагулограмма
- Общий анализ крови (количество лейкоцитов, тромбоцитов, уровень гемоглобина, СОЭ)
- Определение ВИЧ-инфекции, HBsAg, Anti-HBc, anti-HBs, anti-HAV
- Количественное определение РНК вируса гепатита С
- Определение генотипа вируса гепатита С
Лечение гепатита С
Назначается специфическая противовирусная терапия. Существуют множество схем лечения и зависит от генотипа вируса гепатита С:
Существуют множество схем лечения и зависит от генотипа вируса гепатита С:
- генотип HCV 1a: 12 недель — ледипасвир и софосбувир или от 12 до 24 недель — паритапревир, омбитасвир, дасабувир и рибавирин
- генотип HCV 1b: 12 недель — ледипасвир и софобусвир или 12 недель — паритапревир, омбитасвир и дисабувир
- генотип HCV 2: от 12 до 16 недель — софосбувир и рибавирин. генотип HCV 3: 12 недель – софосбувир, рибавирин и пегилированный интерферон или 12 недель – даклатасвир исофосбувир
Эксперты обсудили кратчайший путь к победе над гепатитом С » Медвестник
Между тем эксперты подчеркивают, что российская инфекционная служба способна взять курс на победу над этой социально значимой инфекцией. О проблемах лечения и элиминации хронического гепатита С эксперты говорили в рамках пресс-мероприятия, организованного компанией AbbVie и приуроченного ко Всемирному дню борьбы с гепатитом, который отмечается 28 июля.
По оценке Всемирной организации здравоохранения (ВОЗ), вирусом гепатита С инфицировано не менее 71 миллиона человек в мире, и ежегодно он уносит жизни почти 400 тысяч человек только от цирроза печени и гепатоцеллюлярной карциномы (ГЦК)1.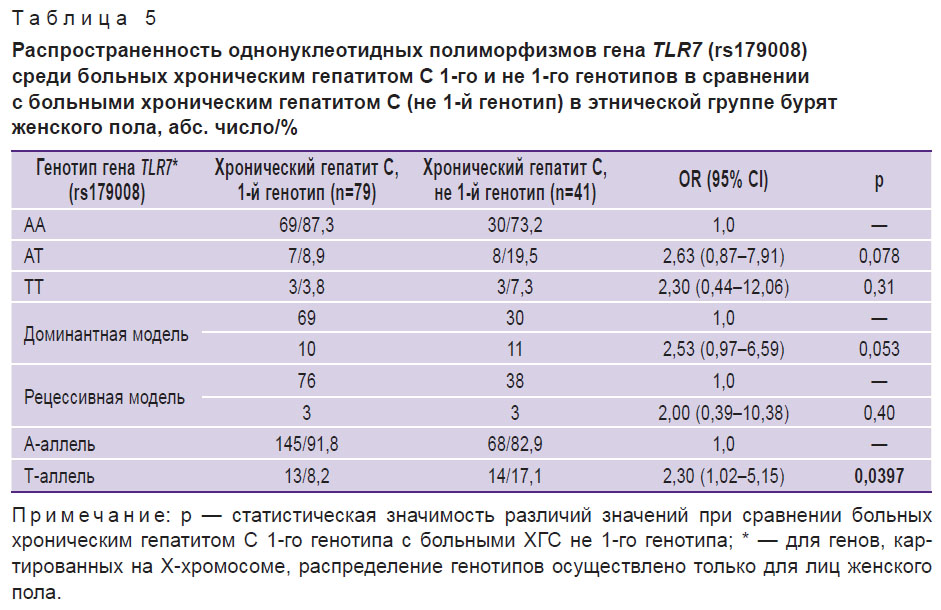 В России, по данным Референс-центра по мониторингу за вирусными гепатитами Роспотребнадзора РФ, оценочное число случаев хронического вирусного гепатита С составляет от 3 до 5 миллионов. Частота регистрации хронического гепатита С в России в 2019 году, по данным Росстата2, составила 30,90 случаев на 100 тысяч населения, или 45 376 вновь выявленных случаев заболевания.
В России, по данным Референс-центра по мониторингу за вирусными гепатитами Роспотребнадзора РФ, оценочное число случаев хронического вирусного гепатита С составляет от 3 до 5 миллионов. Частота регистрации хронического гепатита С в России в 2019 году, по данным Росстата2, составила 30,90 случаев на 100 тысяч населения, или 45 376 вновь выявленных случаев заболевания.
За 31 год с открытия вируса гепатита С (ВГС) ученые кардинально изменили представления о его влиянии на организм. Список проявлений, провоцируемых ВГС, расширился с фиброза, цирроза печени и ГЦК до внушительного перечня серьезных хронических заболеваний, некоторые из которых входят в первую тройку причин смертности, в том числе как минимум 7 видов онкологических заболеваний3.
«Доказано, что вирус гепатита С оказывает системное влияние на организм, – подчеркнул профессор, начальник кафедры инфекционных болезней Военно-медицинской академии имени С.М. Кирова, главный внештатный инфекционист Комитета по здравоохранению г.
Санкт-Петербурга, член-корреспондент РАН Константин Жданов. – Он поражает не только печень, но и другие органы и системы организма, нередко являясь причиной таких серьезных патологий, как сахарный диабет, злокачественные новообразования, сердечно-сосудистые заболевания и другие. Поэтому сегодня во всем мире подчеркивается важность раннего начала лечения хронического гепатита С для предотвращения развития этих заболеваний».
Уязвимость пациентов с хроническими заболеваниями печени подчеркивалась и на фоне эпидемии COVID-194. Европейская ассоциация по изучению заболеваний печени (EASL) в своем заявлении призвала обратить особое внимание на пациентов с заболеваниями печени на продвинутых стадиях в связи с предположительно более высоким риском инфицирования из-за связанной с циррозом иммунной дисфункции. EASL также подчеркнула, что несбалансированное распределение ресурсов здравоохранения в условиях эпидемии COVID-19 может негативно сказаться на лечении пациентов с хроническими заболеваниями печени, которые по-прежнему требуют активной медицинской помощи.
За относительно короткий срок с момента открытия вируса гепатита С удалось не только изучить его свойства и влияние на организм, но и разработать высокоэффективную терапию. Первые попытки лечения хронического гепатита С (ХГС) препаратами интерферона достигали лишь 20% эффективности и длились до 78 недель. Терапия ХГС стремительно менялась: от комбинированных схем на основе интерферона до полностью безинтерфероновых противовирусных режимов с эффективностью более 95%. Первые препараты прямого действия были активны только в отношении отдельных генотипов ВГС. Вершиной эволюции стали пангенотипные схемы последнего поколения, которые благодаря высокой противовирусной активности позволили сократить длительность лечения до 8 недель.
«Современные препараты для лечения ХГС предоставляют нам универсальный подход и позволяют решать большинство медицинских проблем в этой области, – рассказал Константин Жданов. – Сейчас не составляет особого труда подобрать схему терапии для трудных пациентов с ХГС и циррозом печени, хронической болезнью почек или другими сопутствующими патологиями.
При этом во время лечения пациентам уже не приходится часто обращаться к специалисту для контроля процесса терапии, как раньше. Дополнительное преимущество пангенотипных схем – упрощение диагностики. Короткий 8-недельный курс позволяет вылечить больше пациентов при сокращении нагрузки на систему здравоохранения».
Восьминедельная терапия оказалась выгодной и удобной не только для системы здравоохранения, но и для пациентов. Участники исследования5, проведенного в США и Европе, отметили, что после эффективности и безопасности, которые занимали первые места среди наиболее важных критериев терапии, короткий курс лечения был для них важнейшей характеристикой.
Достижения медицинской науки в области изучения влияния гепатита С и его терапии в числе прочего легли в основу события, изменившего отношение к вирусным гепатитам. В 2016 году страны — члены Всемирной организации здравоохранения приняли первую в истории Стратегию сектора здравоохранения, предусматривающую элиминацию вирусных гепатитов как проблему общественного здравоохранения. Среди ключевых задач Стратегии до 2030 года – выявление не менее 90% инфицированных вирусными гепатитами B и С, снижение заболеваемости на 90% и смертности — на 65%. Многие страны мира уже внедрили меры, необходимые для элиминации гепатита С. В России до сих пор много проблем, препятствующих увеличению охвата лечением пациентов с хроническим гепатитом С, хотя вопрос о важности элиминации вирусных гепатитов регулярно поднимается экспертным и пациентским сообществами.
Среди ключевых задач Стратегии до 2030 года – выявление не менее 90% инфицированных вирусными гепатитами B и С, снижение заболеваемости на 90% и смертности — на 65%. Многие страны мира уже внедрили меры, необходимые для элиминации гепатита С. В России до сих пор много проблем, препятствующих увеличению охвата лечением пациентов с хроническим гепатитом С, хотя вопрос о важности элиминации вирусных гепатитов регулярно поднимается экспертным и пациентским сообществами.
В частности, в ноябре 2019 года данная тема обсуждалась в рамках круглого стола на Всероссийском конгрессе пациентов6. Резолюция с рекомендациями по ключевым проблемам, требующим решения для достижения элиминации хронического гепатита С, по итогам обсуждения была направлена в Минздрав, Совет Федерации, Государственную думу.
«В настоящее время каждый регион на свое усмотрение решает, в каком объеме обеспечивать медицинской помощью пациентов с хроническим гепатитом С, – подчеркнула главный внештатный инфекционист Министерства здравоохранения Челябинской области, д. м.н. Ольга Сагалова. – В Челябинской области пациенты бесплатно проходят полную диагностику и получают лечение современным безинтерфероновыми препаратами. Далеко не во всех регионах пациентам предоставляется возможность бесплатного полного обследования, необходимого для назначения лечения. Кроме того, охват терапией в России недостаточен для того, чтобы остановить нарастание заболеваемости гепатитом С. Пока в России количество пациентов, получающих лечение в течение года, значительно меньше зарегистрированных новых случаев за этот же период».
м.н. Ольга Сагалова. – В Челябинской области пациенты бесплатно проходят полную диагностику и получают лечение современным безинтерфероновыми препаратами. Далеко не во всех регионах пациентам предоставляется возможность бесплатного полного обследования, необходимого для назначения лечения. Кроме того, охват терапией в России недостаточен для того, чтобы остановить нарастание заболеваемости гепатитом С. Пока в России количество пациентов, получающих лечение в течение года, значительно меньше зарегистрированных новых случаев за этот же период».
По данным «Коалиции по готовности к лечению» (ITPC)7, в 2018 году за счет бюджетов различных уровней было приобретено около 15 713 курсов терапии, в то время как, согласно данным Роспотребнадзора, в том же году было зарегистрировано 48 052 новых случая вирусного гепатита С.
«Мы стремимся внести значительный вклад в элиминацию хронического гепатита С», — отметил региональный вице-президент AbbVie в России и СНГ Энтони Вонг.
Для этого компания разработала препараты, направленные на ускорение элиминации ХГС.
«AbbVie также работает над внедрением эффективных решений, которые позволяют улучшить доступность диагностики и лечения, что чрезвычайно важно для достижения цели элиминации», – подчеркнул он.
Источник: AbbVie
__________________________
1. Всемирная организация здравоохранения. Информационный бюллетень. Гепатит С. Электронный источник. Проверен 07.07.2020 https://www.who.int/ru/news-room/fact-sheets/detail/hepatitis-c
2. Письмо Федеральной службы государственной статистики от 19.06.2020 № 08-08-3/2079ДР в ответ на запрос компании AbbVie.
3. SaadQadwai, TayyabaRehman, JonathanBarsa, ZeeshanSolangi, andEdwardLebovics. Review Article Hepatitis C Virus and Nonliver Solid Cancers: Is There an Association between HCV and Cancers of the Pancreas, Thyroid, Kidney, Oral Cavity, Breast, Lung, and Gastrointestinal Tract?Gastroenterology Research and Practice, Volume 2017, Article ID 8349150, 11 pages https://doi. org/10.1155/2017/8349150; Peng Wang, Zhaohai Jing, Changjiang Liu, Meihua Xu, Pei Wang, Xiao Wang, Yulei Yin, Ying Cui, Dunlin Ren, Xiaopang Rao. Hepatitis C virus infection and risk of thyroid cancer: A systematic review and meta-analysis. Arab Journal of Gastroenterology 18 (2017), 1–5; Stanislas Pol, Anaïs Vallet-Pichard and Olivier Hermine, Extrahepatic cancers and chronic HCV infection, GASTROENTEROLOGY & HEPATOLOGY, VOLUME 15, MAY 2018, р. 283; Xiangdong Liu, Yanqing Chen, Youxin Wang, Xiaohua Dong, Junming Wang, Jianhua Tang, Kristina Sundquist, Jan Sundquist & Jianguang Ji. Cancer risk in patients with hepatitis C virus infection: a population-based study in Sweden. 2016. Cancer Medicine published by John Wiley & Sons Ltd.
org/10.1155/2017/8349150; Peng Wang, Zhaohai Jing, Changjiang Liu, Meihua Xu, Pei Wang, Xiao Wang, Yulei Yin, Ying Cui, Dunlin Ren, Xiaopang Rao. Hepatitis C virus infection and risk of thyroid cancer: A systematic review and meta-analysis. Arab Journal of Gastroenterology 18 (2017), 1–5; Stanislas Pol, Anaïs Vallet-Pichard and Olivier Hermine, Extrahepatic cancers and chronic HCV infection, GASTROENTEROLOGY & HEPATOLOGY, VOLUME 15, MAY 2018, р. 283; Xiangdong Liu, Yanqing Chen, Youxin Wang, Xiaohua Dong, Junming Wang, Jianhua Tang, Kristina Sundquist, Jan Sundquist & Jianguang Ji. Cancer risk in patients with hepatitis C virus infection: a population-based study in Sweden. 2016. Cancer Medicine published by John Wiley & Sons Ltd.
4.EASL. Care of patients with liver disease during the COVID-19 pandemic: EASL-ESCMID Position Paper.
5. Welzel TM, Yang M, Sajeev G, et al. Assessing patient preferences for treatment decisions for new direct acting antiviral (DAA) therapies for chronic hepatitis C virus infections [published online June 25, 2019].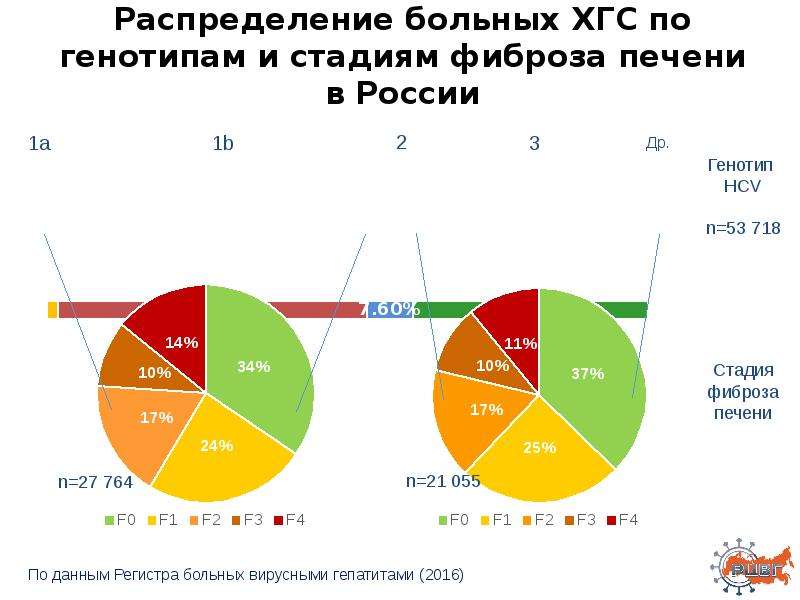 AdvTher. doi:10.1007/s12325-019-01012-6
AdvTher. doi:10.1007/s12325-019-01012-6
6.Вместе против гепатита. Официальный сайт МРОО «Вместе против гепатита». Возможности есть – плана работы нет. Электронный источник. Проверен 07.07.2020 https://www.protivgepatita.ru/news/current-events-moo/1073-2019-12-21-20-33-56
7.Коалиция по готовности к лечению (ITPCRU). Результаты мониторинга закупок препаратов для лечения гепатита С в России в 2018 году. Электронный источник. Проверен 07.07.2020 https://itpcru.org/2019/07/29/rezultaty-monitoringa-zakupok-preparatov-dlya-lecheniya-gepatita-s-v-rossii-v-2018-godu/
Высокие устойчивые показатели вирусологического ответа на схемы на основе софосбувира у китайских пациентов с инфекцией ВГС генотипа 3a в реальных условиях | Журнал вирусологии
ВГС. Глобальная распространенность и распределение генотипов инфекции, вызванной вирусом гепатита С, в 2015 году: модельное исследование. Ланцет Гастроэнтерол Гепатол. 2017; 2 (3): 161–76.
Ланцет Гастроэнтерол Гепатол. 2017; 2 (3): 161–76.
Артикул
Google ученый
Петруцциелло А., Марильяно С., Локерсио Г., Коццолино А., Каччапуоти К.Глобальная эпидемиология вирусной инфекции гепатита С: последние данные о распространении и циркуляции генотипов вируса гепатита С. Мир Дж. Гастроэнтерол. 2016; 22 (34): 7824–40.
Артикул
Google ученый
Xia GL, Liu CB, Cao HL, Bia SL, Zhan MY, Su CA, Nan JH, Qi XQ. Распространенность вирусных инфекций гепатита B и C среди населения Китая в целом. Результаты общенационального поперечного сероэпидемиологического исследования вирусных инфекций гепатита A, B, C, D и E в Китае, 1992 г.Int Hepatol Commun. 1996. 5 (1): 62–73.
Артикул
Google ученый
Беннетт Х., Вазер Н., Джонстон К., Као Дж. Х., Лим Ю.С., Дуан З.П., Ли Й.Дж., Вей Л., Чен С.Дж., Сиверт В. и др. Обзор бремени инфицирования вирусом гепатита С в Китае, Японии, Южной Корее и Тайване. Hepatol Int. 2015; 9 (3): 378–90.
Артикул
Google ученый
Смит Д.Б., Бух Дж., Куикен К., Муэрхофф А.С., Райс С.М., Стэплтон Дж. Т., Симмондс П.Расширенная классификация вируса гепатита С на 7 генотипов и 67 подтипов: обновленные критерии и веб-ресурс назначения генотипов. Гепатология. 2014; 59 (1): 318–27.
Артикул
Google ученый
Zhang Y, Chen LM, He M. Вирус гепатита C в материковом Китае с акцентом на распределение генотипов и подтипов. Вирол Дж.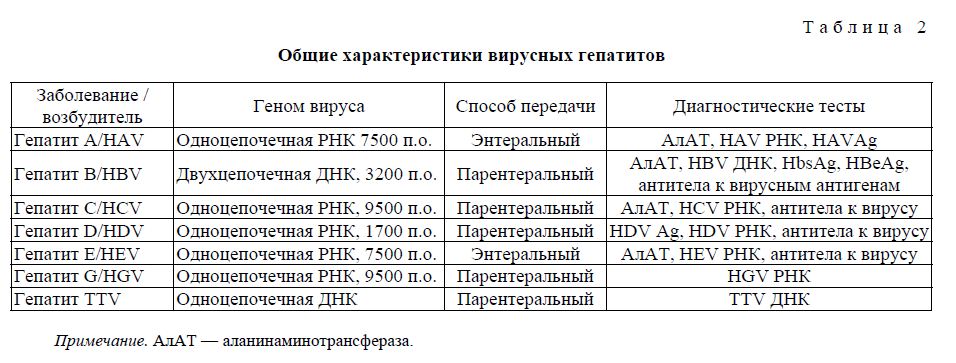 2017; 14 (1): 41.
2017; 14 (1): 41.
CAS
Статья
Google ученый
Chen Y, Yu C, Yin X, Guo X, Wu S, Hou J. Генотипы и подтипы вируса гепатита C, циркулирующие в материковом Китае. Emerg Microbes Infect. 2017; 6 (11): e95.
PubMed
PubMed Central
Google ученый
Хуанг К., Чен Дж., Сюй Р., Цзян Х, Ма Х, Цзя М., Ван М., Хуанг Дж., Ляо К., Шань З. и др. Молекулярная эволюция вируса гепатита С в Китае: общенациональное исследование. Вирусология. 2018; 516: 210–8.
CAS
Статья
Google ученый
Цзяо И, Чжан Икс, Ван Ц., Ли Л., Лю Дж., Бар К. Дж., Вэй Х, Ху И, Хуан П, Цзэн З. и др. Подтип вируса гепатита С и характер эволюции среди потребителей наркотиков, мужчин, практикующих секс с мужчинами, и населения в целом в Пекине, Китай. Медицина (Балтимор). 2016; 95 (6): e2688.
Дж., Вэй Х, Ху И, Хуан П, Цзэн З. и др. Подтип вируса гепатита С и характер эволюции среди потребителей наркотиков, мужчин, практикующих секс с мужчинами, и населения в целом в Пекине, Китай. Медицина (Балтимор). 2016; 95 (6): e2688.
Артикул
Google ученый
Ju W, Yang S, Feng S, Wang Q, Liu S, Xing H, Xie W, Zhu L, Cheng J. Распространение вируса гепатита C и подтипа у пациентов с хроническим гепатитом C в Китае: общенациональное распространение Генотипы 3 и 6 HCV.Вирол Дж. 2015; 12: 109.
Артикул
Google ученый
Лу Дж., Сян Х, Цао З., Ван В., Чжао Дж., Тан В., Чен Л., Го С., Чжуан Ю., Ши Д. и др. Более молодая тенденция заболеваемости циррозом у пациентов с HCV генотипа 3 в восточном Китае. J Med Virol. 2017; 89 (11): 1973–80.
J Med Virol. 2017; 89 (11): 1973–80.
CAS
Статья
Google ученый
Ge D, Fellay J, Thompson AJ, Simon JS, Shianna KV, Urban TJ, Heinzen EL, Qiu P, Bertelsen AH, Muir AJ, et al.Генетическая изменчивость IL28B позволяет прогнозировать клиренс вируса, вызванный лечением гепатита С. Природа. 2009. 461 (7262): 399–401.
CAS
Статья
Google ученый
Зарин СК, Кумар СК. Лечение пациентов с хроническим гепатитом С генотипа 3 — современные и будущие методы лечения. Liver Int. 2012; 32 (Дополнение 1): 141–5.
CAS
Статья
Google ученый

МакКомбс Дж., Мацуда Т., Тонну-Михара И., Сааб С., Хайнс П., Л’италиен Дж., Джудей Т., Юань Ю.Риск долгосрочной заболеваемости и смертности у пациентов с хроническим гепатитом С: результаты анализа данных Клинического реестра Департамента по делам ветеранов. JAMA Intern Med. 2014. 174 (2): 204–12.
Артикул
Google ученый
Шахназарян В., Рамай Д., Редди М., Моханти С. Генотип 3 вируса гепатита С: клинические особенности, текущие и новые вирусные ингибиторы, проблемы будущего. Энн Гастроэнтерол. 2018; 31 (5): 541–51.
PubMed
PubMed Central
Google ученый
Пробст А., Данг Т., Бохуд М., Эггер М., Негр Ф., Бохуд П.Й. Роль генотипа 3 вируса гепатита С в прогрессировании фиброза печени — систематический обзор и метаанализ. J Viral Hepat. 2011. 18 (11): 745–59.
CAS
Статья
Google ученый
Гондо C, Пейдж, GP, Ларри Д. Инфекция вирусом гепатита С: есть ли еще специфические проблемы с генотипом 3? Мир Дж. Гастроэнтерол.2015; 21 (42): 12101–13.
CAS
Статья
Google ученый
Nkontchou G, Ziol M, Aout M, Lhabadie M, Baazia Y, Mahmoudi A., Roulot D, Ganne-Carrie N, Grando-Lemaire V, Trinchet JC, et al. Генотип 3 HCV связан с более высокой заболеваемостью гепатоцеллюлярной карциномой у пациентов с продолжающимся вирусным циррозом C. J Viral Hepat. 2011; 18 (10): e516–22. https://doi.org/10.1111/j.1365-2893.2011.01441.x.
CAS
Статья
PubMed
Google ученый
Идрис М., Рафик С., Рехман И., Акбар Х., Юсуф М.З., Батт С., Аван З., Манзур С., Акрам М., Афтаб М. и др. Инфекция вируса гепатита C генотипа 3a и гепатоцеллюлярная карцинома: опыт Пакистана. Мир Дж. Гастроэнтерол. 2009. 15 (40): 5080–5.
CAS
Статья
Google ученый
Панель управления AASLD-IDSA HCV. Обновление руководства по гепатиту C 2018: рекомендации AASLD-IDSA по тестированию, контролю и лечению вирусной инфекции гепатита C.Clin Infect Dis. 2018; 67 (10): 1477–92.
Артикул
Google ученый
Европейская ассоциация изучения печени. Электронный адрес: [email protected]; Европейская ассоциация изучения печени. Рекомендации EASL по лечению гепатита C 2018. J Hepatol. 2018; 69 (2): 461–511.
Артикул
Google ученый
Омата М., Канда Т., Вей Л., Ю М.Л., Чуанг В.Л., Ибрагим А., Лесмана С.Р., Соллано Дж., Кумар М., Джиндал А. и др.Консенсусные заявления APASL и рекомендации по лечению гепатита C. Hepatol Int. 2016; 10 (5): 702–26.
Артикул
Google ученый
Wei L, Lim SG, Xie Q, Văn KN, Piratvisuth T., Huang Y, Wu S., Xu M, Tang H, Cheng J, et al. Софосбувир-велпатасвир для лечения хронической вирусной инфекции гепатита С в Азии: открытое исследование фазы 3 в одной группе. Ланцет Гастроэнтерол Гепатол. 2018; (18): 30343–1. https://doi.org/10.1016 / S2468-1253.
Tao YC, Deng R, Wang ML, Lv DD, Yuan M, Wang YH, Chen EQ, Tang H. Удовлетворительный вирусологический ответ и улучшение фиброза схем на основе софосбувира для китайских пациентов с генотипом вируса гепатита C 3 инфекция: результаты реального когортного исследования. Вирол Дж. 2018; 15 (1): 150.
Артикул
Google ученый
Нельсон Д. Р., Купер Дж. Н., Лалезари Дж. П., Лавиц Э., Покрос П. Дж., Гитлин Н., Фрейлих Б. Ф., Юнес З. Х., Харлан В., Галиб Р. и др.Полностью пероральное 12-недельное лечение даклатасвиром и софосбувиром у пациентов с инфекцией вируса гепатита С генотипа 3: исследование III фазы ALLY-3. Гепатология. 2015; 61 (4): 1127–35.
CAS
Статья
Google ученый
Belperio PS, Shahoumian TA, Loomis TP, Mole LA, Backus LI. Реальная эффективность комбинации даклатасвир плюс софосбувир и велпатасвир / софосбувир при гепатите C генотипа 2 и 3. J Hepatol. 2019; 70 (1): 15–23.
CAS
Статья
Google ученый
Del Rio-Valencia JC, Asensi-Diez R, Madera-Pajin R, Yunquera-Romero L, Muñoz-Castillo I. Лечение пациентов с гепатитом C генотипа 3 в стационаре третичного уровня без интерферона. Преподобный Эсп Кимиотер. 2018; 31 (1): 35–42.
PubMed
PubMed Central
Google ученый
Хуанг Р., Рао Х., Се Кью, Гао З, Ли В., Цзян Д., Мо Х., Массетто Б., Штамм Л.М., Брейнард Д.М. и др. Сравнение эффективности софосбувира и рибавирина у китайских пациентов с генотипом 3a или 3b инфекции HCV.J Med Virol. 2019. https://doi.org/10.1002/jmv.25454.
CAS
Статья
Google ученый
Moshyk A, Martel MJ, Tahami Monfared AA, Goeree R. Экономическая эффективность схемы на основе даклатасвира и софосбувира для лечения инфекции вируса гепатита C генотипа 3 в Канаде. J Med Econ. 2016; 19 (2): 181–92.
Артикул
Google ученый
Парк Х, Чен С., Ван В., Генри Л., Кук Р.Л., Нельсон Д.Р.Вирус хронического гепатита С (ВГС) увеличивает риск хронической болезни почек (ХБП), в то время как эффективное лечение ВГС снижает частоту возникновения ХБП. Гепатология. 2018; 67 (2): 492–504.
CAS
Статья
Google ученый
Сперл Дж., Франкова С., Крейдлова М., Мерта Д., Тотова М., Спикак Дж. Комбинация софосбувира и даклатасвира в лечении хронической инфекции вируса гепатита С генотипа 3 у пациентов, находящихся на поддерживающем гемодиализе.Ther Clin Risk Manag. 2017; 13: 733–8.
CAS
Статья
Google ученый
Beinhardt S, Al Zoairy R, Ferenci P, Kozbial K, Freissmuth C, Stern R, Stättermayer AF, Stauber R, Strasser M, Zoller H, et al. Противовирусное лечение пациентов с хроническим гепатитом С на основе ПППД в условиях до и после трансплантации почки. Transpl Int. 2016; 29 (9): 999–1007.
CAS
Статья
Google ученый
Бурра П., Родригес-Кастро К.И., Марчини Ф., Бонфанте Л., Фуриан Л., Феррарез А., Занетто А., Джермани Г., Руссо Ф. П., Сензоло М. Инфекция вируса гепатита С при терминальной стадии почечной недостаточности и трансплантации почки. Transpl Int. 2014; 27 (9): 877–91.
Артикул
Google ученый
Desnoyer A, Pospai D, Lê MP, Gervais A, Heurgué-Berlot A, Laradi A, Harent S, Pinto A, Salmon D, Hillaire S, et al. Фармакокинетика, безопасность и эффективность ежедневного приема полной дозы софосбувира у гемодиализных пациентов с хроническим гепатитом С.J Hepatol. 2016; 65 (1): 40–7.
CAS
Статья
Google ученый
Бартолини Б., Джомбини Э, Тайби К., Лионетти Р., Монтальбано М., Виско-Командини Ю., Д’Оффици Г., Капобианки М. Р., Макфи Ф., Гарбулия АР. Характеристика встречающихся в природе полиморфизмов NS5A и NS5B у пациентов, инфицированных HCV генотипа 3a, получавших противовирусные препараты прямого действия. Вирусы. 2017; 9 (8). https://doi.org/10.3390/v
12.
Артикул
Google ученый
Qiao B, Tong YQ, Wang M, Gong WJ, Li Y. Распространенность мутации S282T в различных генотипах вируса гепатита C у наивных китайских пациентов, получавших DAA, которые были хронически инфицированы HCV. Eur Rev Med Pharmacol Sci. 2018; 22 (16): 5305–11.
CAS
PubMed
Google ученый
Ramirez S, Mikkelsen LS, Gottwein JM, Bukh J. Надежная система культивирования инфекционных клеток с генотипом 3a HCV позволяет идентифицировать варианты ускользания с устойчивостью к софосбувиру.Гастроэнтерология. 2016; 151 (5): 973–985.e2.
CAS
Статья
Google ученый
Генотипирование РНК ВГС показывает, что 3a является наиболее распространенным генотипом в Мардане, Пакистан
Клинические исходы у пациентов, инфицированных вирусом гепатита С (ВГС), варьируются от острого разрешенного гепатита до хронических заболеваний печени, таких как цирроз печени или гепатоцеллюлярная карцинома . Идентификация генотипа инфекционного вируса необходима для изучения многих аспектов инфекции ВГС, включая эпидемиологию, патогенез и ответ на противовирусную терапию.В этом исследовании 1419 человек прошли скрининг на анти-ВГС, из которых 166 (11,7%) были признаны реактивными с помощью ИКТ (иммунохроматографический тест). Эти 166 анти-HCV-положительных и 26 нормальных людей были дополнительно проанализированы. РНК была извлечена из сыворотки и подвергнута обратной транскрипции в кДНК, а центральная область генома HCV была нацелена и амплифицирована с помощью мультиплексной ПЦР. РНК ВГС была обнаружена у 121 человека, из которых 87 были мужчинами и 34 женщинами. Генотип 3a был наиболее распространенным среди всех наблюдаемых генотипов, за которым следовал 3b.Генотипы 1a, 2a и 2b были обнаружены у 10,89%, 13,22% и 6,61% пациентов соответственно. 25,41% образцов, положительных по РНК ВГС, не были типированы. У 6,05% пациентов были обнаружены смешанные генотипы. Эти результаты не только помогут врачам назначить более подходящее лечение инфекции ВГС, но также привлекут внимание политиков, связанных со здоровьем, к разработке стратегий для более эффективного сдерживания болезни.
1. Введение
Вирус гепатита С (ВГС) является наиболее частой причиной хронического вирусного гепатита во всем мире.В последние годы инфекция HCV стала одной из наиболее частых причин острых и хронических заболеваний печени во всем мире [1]. HCV является членом семейства Flaviviridae , которое несет геном положительной смысловой одноцепочечной РНК (оцРНК) длиной примерно 10 т.п.н. Поскольку одно только тестирование на анти-ВГС не позволяет дифференцировать острую, хроническую или разрешенную инфекцию, необходимо также провести дополнительный тест, включающий измерение индекса активности иммуноглобулина G против ВГС [2] или реактивности антител к конкретным структурным и неструктурным белкам ВГС [2]. 3], чтобы подтвердить положительный результат анти-ВГС [1].Известно, что HCV имеет высокую степень генетической гетерогенности [4]. Это позволило разделить штаммы ВГС на ряд генетически отличных групп, известных как генотипы, подтипы, изоляты и квазивиды [5]. Генетическая изменчивость среди штаммов ВГС составляет 65,8–68,7% идентичности нуклеотидных последовательностей полноразмерных последовательностей для типов, 76,9–80,1% идентичностей нуклеотидных последовательностей полноразмерных последовательностей для подтипов и 90,8–99% идентичностей нуклеотидных последовательностей полных -длины последовательностей для изолятов и квазивидов [6].На данный момент идентифицировано шесть основных генотипов, то есть с 1 по 6 и более 50 подтипов. Эти генотипы различаются на 31–34% по нуклеотидным последовательностям, тогда как подтипы различаются на 20–23% по своим полноразмерным геномным последовательностям. Эта обширная генетическая гетерогенность, а также склонность к мутациям препятствовали разработке вакцины против этого вируса [5]. Поскольку пациенты, инфицированные разными генотипами, по-разному реагируют на терапию противовирусными препаратами, идентификация инфекционного генотипа неизбежна для определения правильной дозы и продолжительности текущей комбинированной терапии (пегилированный альфа-интерферон плюс рибавирин) [7].
Гепатит С также распространен в Пакистане, но точная эпидемиологическая информация весьма ограничена. На окраинах городов и в отдаленных районах неквалифицированные практикующие врачи и стоматологи, дамы-медсестры, акушерки и парикмахеры часто используют нестерилизованные инструменты, которые являются основными потенциальными источниками распространения инфекции ВГС среди городского и сельского населения Пакистана [8] . Хотя точное соотношение этого хронического заболевания неизвестно, различные исследования показали, что 3–7% населения Пакистана инфицировано [9].В более раннем исследовании сообщалось, что 8,9% населения инфицировано ВГС в Мардане [10], втором по величине городе в провинции Хайбер-Пахтунхва в Пакистане. Очень важно проверить степень и распределение генотипов ВГС в районе Мардан, Хайбер-Пахтунхва, где выявление и определение генотипа до начала лечения носят спорадический характер. Следовательно, соответствующая информация для индивидуального лечения необходима для того, чтобы максимизировать вероятность успешного исхода лечения для каждого отдельного пациента, что делает анализ генотипирования ВГС важным и полезным инструментом для оптимизации типа, продолжительности и дозы лечения.Это исследование было разработано, чтобы определить активную РНК-инфекцию ВГС, а также узнать о генотипах ВГС, циркулирующих в районе исследования.
2. Материалы и метод
Все пробы крови были собраны из разных районов (больниц и клинических лабораторий) Мардана. В пробирку Vacutainer отбирали 5 см3 крови и выделяли сыворотку или хранили цельную кровь при -80 ° C для дальнейшего анализа в Департаменте биотехнологии KUST. При сборе образцов крови заполнялась проформа для сбора медицинской / клинической информации от всех людей и получения их согласия.Отмечались анамнез пациента, функциональные тесты печени (LFT), желтуха, переливание крови и другие различные тесты, такие как HBs Ag и анти-HCV, если они проводились. Это исследование было проведено с одобрения этического комитета Кохатского университета науки и технологий (KUST), Кохат, Пакистан.
2.1. Иммунохроматографический тест (ICT)
Первоначально все образцы были проверены на антитела к HCV с использованием набора устройств ICT (Accurate Diagnostic, Канада), как описано в соответствии с инструкциями производителя.
2.2. Экстракция РНК и синтез кДНК (для обнаружения 5’UTR)
РНК экстрагировали из 300 мкл л образца крови с использованием набора для экстракции РНК (набор для очистки РНК, Ultrascript, Anagen Technologies, Inc., США). кДНК синтезировали из области 5’UTR экстрагированной РНК с использованием праймеров.
2.3. Регулярная ПЦР (для обнаружения 5’UTR)
Синтезированная кДНК
затем была амплифицирована в следующем раунде регулярной ПЦР с использованием смыслового и антисмыслового праймера, специфичного для 5’UTR [11].кДНК использовали из предыдущего раунда и обрабатывали в термоциклере. Условия цикла для регулярной ПЦР состояли из 25 циклов в три этапа I, II и III.
2.4. Вложенная ПЦР (для обнаружения 5’UTR ВГС)
После обычной ПЦР была проведена вложенная ПЦР с использованием следующей пары праймеров, внутренних по отношению к первому [11]. Смесь готовили так же, как для обычной ПЦР, за исключением праймеров. Условия цикла ПЦР были такими же, как и для обычной ПЦР.
2,5. Электрофорез
12 мкл мкл амплифицированной кДНК разделяли на 2% агарозном геле.Полосы кДНК (230 п.н.) идентифицировали путем сравнения с лестничным маркером ДНК 100 п.н. (Fermentas, США) и визуализировали при УФ-освещении с использованием системы гель-документации.
2.6. Генотипирование ВГС
2.6.1. Синтез кДНК для области ядра
кДНК
синтезировали из области ядра экстрагированной РНК со специфическими праймерами [11]. Реакцию проводили в термоциклере (Techne Inc., США) по той же программе, что и для 5’UTR.
2.6.2. 1-й раунд ПЦР HCV для генотипирования
Для амплификации кДНК в термоциклере (Techne Inc.) использовали два праймера (один обратный и один прямой) [11], специфичных для области ядра HCV., США) с ДНК-полимеразой Taq (Fermentas, США).
2.6.3. ПЦР, специфичная для генотипа HCV
Генотипирование с помощью типоспецифичных праймеров [11] для центральной области генома HCV было выполнено для девяти наиболее распространенных подтипов и типов HCV (1a, 1b, 2a, 2b, 3a, 3b, 4, 5а и 6а). Для различения различных продуктов амплифицированных генотипов HCV типоспецифическая смесь ПЦР была разделена на смесь A и смесь B. Для смеси B все реагенты были одинаковыми, за исключением антисмысловых праймеров.ПЦР, специфичная для генотипа HCV / мультиплексная ПЦР, выполнялась с использованием той же программы, что и для 1-го раунда ПЦР.
2.6.4. Электрофорез
ПЦР-продуктов разделяли на 2% агарозном геле, приготовили в 0,5X буфере TBE и визуализировали в ультрафиолетовом свете. Генотипы HCV определяли путем сравнения амплифицированного продукта (полос кДНК) определенного генотипа с лестничным маркером ДНК 100 п.н. (Fermentas, США).
3. Результаты
Всего 1419 субъектов прошли скрининг на анти-HCV, из которых 166 оказались положительными на антитела к HCV, включая 11.7% обследованного населения (Рисунок 1 и Таблица 1). Из общего числа прошедших скрининг лиц 192 были отобраны для дальнейшего исследования, из них 166 были анти-HCV-положительными и 26 были анти-HCV-отрицательными (нормальные люди) в качестве контроля, без явного анамнеза или симптомов гепатита C. 103 мужчины и 63 женщины были анти-ВГС-положительными, тогда как в общей популяции 17 мужчин и 9 женщин были анти-ВГС-отрицательными (Таблица 1).
| |||||||||||||||||||||||||||||||||||||||||
| Roy’s | ||||||||||||||||||||||||||||||||||||||||
4. Обсуждение
Вирус гепатита С (ВГС) имеет различные клинические исходы у разных инфицированных пациентов, от острого разрешающегося гепатита до хронических заболеваний печени, включая цирроз печени и гепатоцеллюлярную карциному (ГЦК) [12]. Идентификация генотипа инфекционного вируса важна для изучения многих аспектов инфекции ВГС, включая эпидемиологию, патогенез и ответ на противовирусную терапию [13, 14]. Подходящий и надежный метод генотипирования ВГС неизбежен для крупномасштабных эпидемиологических и экспериментальных исследований [11].Описан ряд лабораторных процедур, направленных на определение генотипов ВГС [15]. Определение генотипа HCV с помощью анализа полноразмерной геномной последовательности с последующим филогенетическим анализом по-прежнему является золотым стандартом. Хотя эта система дорогая и требует много времени, и ее нельзя адаптировать для клинических исследований или широкого стандартного использования [15]. ПЦР широко используется для генотипирования [13], которое основано на амплификации вирусных последовательностей в клинических образцах с использованием типоспецифичных праймеров, которые специфически амплифицируют различные генотипы [11, 16].Информация, полученная из различных частей мира, сосредоточена на возрастающем значении генотипирования ВГС и подчеркивает необходимость простых, надежных, экономичных и быстрых методов массового скрининга.
Точное и чувствительное измерение РНК ВГС важно для лечения инфицированных пациентов и изучения биологии ВГС и инфекций ВГС в исследованиях [17]. Клинические причины, факторы риска и тяжесть инфекций ВГС и генотипов ВГС в Марданском районе, как и в других районах Хайбер-Пахтунхва, все еще плохо определены.Антитела против ВГС наблюдались у 11,70% исследуемой популяции, что показывает высокую распространенность по сравнению с 4,57%, о которых сообщили Мухаммад и Ян в районе Бунер [18].
Наши данные показали, что генотип 3a (26,44%), за которым следует генотип 3b (16,52%), преобладает в районе Мардан и в исследовании Идрис и Риазуддин [19], где генотипы 3a и 3b доминировали среди исследуемой популяции [19] . Также в другом исследовании, проведенном Идрисом и Риазуддином, генотип 3a HCV оказался преобладающим в общей популяции [19].Что касается встречаемости генотипов ВГС в других странах, таких как Аргентина, генотип 2 более распространен [20]. Аналогичным образом, Alfonso et al. (2001) наблюдали генотип 1 у 61,4% и генотип 3 у 23,7% инфицированных пациентов в регионе Латинской Америки [21]. В недавнем обзоре мы сообщили, что на генотип 3a приходится 68,94% инфекций ВГС в Пенджабе, 76,88% в Синде, 58% в КПК и 60,71% в провинциях Белуджистан в Пакистане [22].
Анализ эпидемиологических данных показал заметные различия между пациентами с одиночными инфекциями и пациентами с явно смешанными инфекциями, проиллюстрированные типоспецифической ПЦР [13].Смешанная инфекция наблюдалась в нашем исследовании в 4,13% образцов (рис. 2). Смешанные генотипы могут быть связаны с инфицированием разными типами ВГС в результате повторного воздействия ВГС [23]. Кроме того, 17,35% индивидуумов, которые были подтверждены вложенной ПЦР на РНК ВГС, не были типизированы с помощью ПЦР по типу. Это не согласуется с нашими предыдущими выводами, которые показали, что 20,16% пациентов с ВГС в КПК были нетипируемыми [22].
ВГС известен как «тихий убийца», потому что в большинстве случаев на ранних стадиях инфекции не проявляются надлежащие признаки или симптомы, а когда симптомы появляются, лечение затруднено.Во-вторых, в большинстве развивающихся стран диагностика не является правильной из-за отсутствия оборудования. Людей проверяют на анти-HCV с помощью полосок или с помощью ELISA-теста на анти-HCV на инфекцию HCV, но эти методы более ошибочны и не чувствительны [24]. Следовательно, молекулярное обнаружение ВГС с помощью методов, основанных на ПЦР, неизбежно из-за более высоких уровней чувствительности и специфичности, чем у серологических методов. Инфекция ВГС является типичным примером заболеваний, при которых прямое обнаружение вируса имеет важное значение для постановки правильного диагноза.По сравнению с другими существующими анализами in vitro, ОТ-ПЦР имеет дополнительные перспективы для диагностики, поскольку она предлагает окончательное обнаружение ВГС [25].
Настоящее исследование показывает, что распределение генотипа 3 ВГС в Мардане сходно с таковым в других районах Пакистана. В этой области преобладают ВГС 2 и 3 типов, которые лучше реагируют на терапию интерфероном, но также циркулируют типы 1 и 4, которые требуют более длительного лечения. В этой области следует начать надлежащие эпидемиологические исследования и стратегии лечения.Следует также принять во внимание соответствующие превентивные меры, чтобы контролировать распространение этой ужасной болезни.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов в отношении публикации данной статьи.
Благодарности
Авторы выражают благодарность Университету Мардана Абдул Вали Хана (AWKUM), Университету науки и технологий Кохат (KUST), Университету Пешавара и Комиссии по высшему образованию (HEC) Пакистана за финансирование проекта.
Генотип вируса гепатита С 3: генотип, который нелегко поддается лечению
Предпосылки:
Необходимы эффективные пангенотипические методы лечения инфекции, вызванной вирусом гепатита С (ВГС).
Цель:
Оценить безопасность и эффективность софосбувира с велпатасвиром у пациентов, инфицированных генотипами 1-6 ВГС.
Дизайн:
Рандомизированное открытое исследование фазы 2. (ClinicalTrials.gov: NCT01858766).
Параметр:
48 сайтов в США.
Пациенты:
377 пациентов без цирроза, не получавших лечения. В части А пациентам, инфицированным генотипами 1–6 ВГС, случайным образом назначали софосбувир в дозе 400 мг и велпатасвир в дозе 25 или 100 мг в течение 12 недель.В части B пациентам с генотипом 1 или 2 инфекции HCV случайным образом назначали софосбувир в дозе 400 мг и велпатасвир в дозе 25 или 100 мг с рибавирином или без него в течение 8 недель.
Размеры:
Устойчивый вирусологический ответ через 12 недель (УВО12).
Полученные результаты:
В части A частота УВО12 составила 96% (26 из 27) при приеме 25 мг велпатасвира и 100% (28 из 28) при приеме 100 мг велпатасвира для генотипа 1; 93% (25 из 27) в обеих группах для генотипа 3; и 96% (22 из 23) с велпатасвиром, 25 мг, и 95% (21 из 22) с велпатасвиром, 100 мг, для генотипов 2, 4, 5 и 6.В части B для генотипа 1 частота УВО12 составила 87% (26 из 30) при приеме 25 мг велпатасвира; 83% (25 из 30) с велпатасвиром, 25 мг, плюс рибавирин; 90% (26 из 29) с велпатасвиром, 100 мг; и 81% (25 из 31) с велпатасвиром, 100 мг, плюс рибавирин. Для генотипа 2 частота УВО12 составила 77% (20 из 26) при приеме 25 мг велпатасвира; 88% (22 из 25) с велпатасвиром, 25 мг, плюс рибавирин; 88% (23 из 26) с велпатасвиром, 100 мг; и 88% (23 из 26) с велпатасвиром, 100 мг, плюс рибавирин. Побочные эффекты включали усталость (21%), головную боль (20%) и тошноту (12%).Один пациент покончил жизнь самоубийством.
Ограничение:
Исследование носило открытый характер, никаких выводов статистики не планировалось, а размеры выборки были небольшими.
Вывод:
Двенадцатинедельный курс софосбувира в дозе 400 мг и велпатасвира в дозе 100 мг хорошо переносился и приводил к высокому УВО у пациентов, инфицированных генотипами 1–6 ВГС.
Основной источник финансирования:
Gilead Sciences.
Эпидемический анамнез генотипов и подтипов вируса гепатита С в Португалии
Всемирная организация здравоохранения. Глобальный доклад о гепатите, 2017 г. .ISBN 978-92-4-156545-5 (2017).
Смит Д. Б. и др. . Расширенная классификация вируса гепатита С на 7 генотипов и 67 подтипов: обновленные критерии и веб-ресурс назначения генотипов. Гепатология 59 , 318–327 (2014).
Артикул
PubMed
Google ученый
Simmonds, P. et al . Классификация вируса гепатита С на шесть основных генотипов и ряд подтипов с помощью филогенетического анализа области NS-5. J. Gen. Virol. 74 , 2391–2399 (1993).
Артикул
PubMed
CAS
Google ученый
Смит Д. Б. и др. . Международный комитет по таксономии вирусов (ICTV). Классификация ВПЦ. Веб-ресурс для управления классификацией и присвоением генотипов и подтипов вируса гепатита С. на https://talk.ictvonline.org/ictv_wikis/flaviviridae/w/sg_flavi/56/hcv-classification (2017).
Пибус, О. Г. и Тезе, Дж. Межвидовая передача гепацивируса и происхождение вируса гепатита С. Curr. Opin. Virol. 16 , 1–7 (2016).
Артикул
PubMed
CAS
Google ученый
Blach, S. et al. . Глобальная распространенность и распределение генотипов инфекции, вызванной вирусом гепатита С, в 2015 году: модельное исследование. Ланцет Гастроэнтерол. Гепатол. 2 , 161–176 (2017).
Артикул
Google ученый
Jeannel, D. et al. . Доказательства высокого генетического разнообразия и долгосрочной эндемичности генотипов 1 и 2 вируса гепатита С в Западной Африке. J. Med. Virol. 55 , 92–97 (1998).
Артикул
PubMed
CAS
Google ученый
Марков П.В. и др. . Филогеография и молекулярная эпидемиология генотипа 2 вируса гепатита С в Африке. J. Gen. Virol. 90 , 2086–2096 (2009).
Артикул
PubMed
CAS
Google ученый
Simmonds, P. et al . Консенсусные предложения по единой системе номенклатуры генотипов вируса гепатита С. Гепатология 42 , 962–973 (2005).
Артикул
PubMed
CAS
Google ученый
Ур Рехман, И. и др. . Генетическая история вируса гепатита С в Пакистане. Заражение. Genet. Evol. 27 , 318–324 (2014).
Артикул
PubMed
Google ученый
Илес, Дж. К. и др. . Филогеография и эпидемическая история генотипа 4 вируса гепатита С в Африке. Вирусология 464–465 , 233–243 (2014).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Pybus, О. Г. и др. . Генетическая история вируса гепатита С в Восточной Азии. J. Virol. 83 , 1071–1082 (2009).
Артикул
PubMed
CAS
Google ученый
Мерфи Д. Г. и др. . Генотип 7 вируса гепатита С, новый генотип, происходящий из Центральной Африки. J. Clin. Microbiol. 53 , 967–972 (2015).
Артикул
PubMed
PubMed Central
Google ученый
Макнотон, А. Л. и др. . Пространственно-временная реконструкция проникновения вируса гепатита С в Шотландию и его последующей региональной передачи. J. Virol. 89 , 11223–11232 (2015).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Пибус, О. Г., Кокрейн, А., Холмс, Э. К. и Симмондс, П. Эпидемия вируса гепатита С среди потребителей инъекционных наркотиков. Заражение. Genet. Evol. 5 , 131–139 (2005).
Артикул
PubMed
Google ученый
Эстебан, Дж. И., Сауледа, С. и Квер, Дж. Изменяющаяся эпидемиология вирусной инфекции гепатита С в Европе. J. Hepatol. 48 , 148–162 (2008).
Артикул
PubMed
Google ученый
Альтер М. Дж. Эпидемиология вирусной инфекции гепатита С. World J. Gastroenterol. 13 , 2436–2441 (2007).
Артикул
PubMed
PubMed Central
Google ученый
Тимм Дж. И Роггендорф М. Разнообразие последовательностей вируса гепатита С: значение для иммунного контроля и терапии. World J. Gastroenterol. 13 , 4808–4817 (2007).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Пренто, Дж., Веласкес-Моктесума, Р., Фунг, С. К. Х., Лоу, М. и Бух, Дж. Гипервариабельное экранирование области 1 вируса гепатита С является основным фактором генотипических различий в чувствительности к нейтрализации. 64 , 1881–1892 (2016).
Педерсен, Дж. и др. . Устойчивость к нейтрализации вируса гепатита С можно преодолеть с помощью рекомбинантных человеческих моноклональных антител. Гепатология 58 , 1587–1597 (2013).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Фрид М., Шиффман М. Л. и Редди К. Пегинтерферон альфа-2а плюс рибавирин при хронической инфекции вируса гепатита С. N. Engl. J. Med. 347 , 975–982 (2002).
Артикул
PubMed
CAS
Google ученый
Hadziyannis, S. et al . Комбинированная терапия пегинтерфероном-α2a и рибавирином при хроническом гепатите c: рандомизированное исследование продолжительности лечения и дозы рибавирина. Ann.Междунар. Med. 140 , 346–355 (2004).
Артикул
PubMed
CAS
Google ученый
Маннс М. П. и др. . Пегинтерферон альфа-2b плюс рибавирин в сравнении с интерфероном альфа-2b плюс рибавирин для начального лечения хронического гепатита С: рандомизированное исследование. Ланцет 358 , 958–965 (2001).
Артикул
PubMed
CAS
Google ученый
Mangia, A. et al . Пегинтерферон альфа-2а и рибавирин в течение 16 или 24 недель при генотипе 2 или 3 ВГС. N. Engl. J. Med. 357 , 124–134 (2005).
Google ученый
Камал С. М. и др. . Терапия пегинтерфероном α − 2b и рибавирином при хроническом гепатите C генотипа 4: влияние продолжительности лечения и вирусной кинетики на устойчивый вирусологический ответ. Кишечник 54 , 858–866 (2005).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Павлоцкий, Дж. М. Новые методы лечения гепатита С: инструментарий, стратегии и проблемы. Гастроэнтерология 146 , 1176–1192 (2014).
Артикул
PubMed
CAS
Google ученый
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA). Лечение гепатита B и C.Полный список одобренных в настоящее время методов лечения гепатита B и C FDA см. По адресу http://www.fda.gov/ForPatients/Illness/HepatitisBC/ucm408658.htm (2017).
Европейское агентство по лекарственным средствам (EMA). Европейские общественные оценочные отчеты. на http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/landing/epar_search.jsp&mid=WC0b01ac058001d124&startLetter=Просмотреть все & searchTab = & keyword = Введите ключевые слова & searchType = name & alreadyLoadedTy == (2017).
Götte, M. & Feld, J. J. Противовирусные агенты прямого действия для гепатита C: структурные и механистические идеи. Nat. Publ. Gr. 13 , 338–351 (2016).
Google ученый
Лавиц, Э. и др. . Софосбувир для лечения хронического гепатита С. N Engl J Med 368 , 1878–1887 (2013).
Артикул
PubMed
CAS
Google ученый
Якобсон, И. и др. . Софосбувир для лечения гепатита С 2 или 3 генотипа у пациентов без вариантов лечения. N Engl J Med 368 , 1867–1877 (2013).
Артикул
PubMed
CAS
Google ученый
Zeuzem, S. et al . Софосбувир и рибавирин в генотипах 2 и 3 ВГС. N. Engl. J. Med. 370 , 1993–2001 (2014).
Артикул
PubMed
CAS
Google ученый
Sulkowski, M. S. et al . Софосбувир и рибавирин для лечения гепатита С у пациентов с коинфекцией ВИЧ. JAMA 312 , 353–61 (2014).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Лавиц, Э. и др. . Симепревир плюс софосбувир, с рибавирином или без него, для лечения хронической инфекции вирусом гепатита С генотипа 1 у лиц, не ответивших на пегилированный интерферон и рибавирин, и пациентов, не получавших лечение: рандомизированное исследование COSMOS. Ланцет 384 , 1756–1765 (2017).
Артикул
CAS
Google ученый
Кво, П. и др. . Симепревир плюс софосбувир (12 и 8 недель) у инфицированных вирусом гепатита С генотипа 1 пациентов без цирроза: ОПТИМИСТ-1, фаза 3, рандомизированное исследование. Гепатология 64 , 370–380 (2016).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Афдал, Н. и др. . Ледипасвир и софосбувир при нелеченой инфекции HCV генотипа 1. N. Engl. J. Med. 370 , 1889–1898 (2014).
Артикул
PubMed
CAS
Google ученый
Afdhal, N. et al . Ледипасвир и софосбувир для лечения ранее пролеченной инфекции HCV генотипа 1. N. Engl. J. Med. 370 , 1483–93 (2014).
Артикул
PubMed
CAS
Google ученый
Каудли, К. В. и др. . Ледипасвир и софосбувир в течение 8 или 12 недель при хроническом гепатите С без цирроза печени. N. Engl. J. Med. 370 , 1879–88 (2014).
Артикул
PubMed
CAS
Google ученый
Bourlière, M. et al. . Ледипасвир-софосбувир с рибавирином или без него для лечения пациентов с инфекцией HCV генотипа 1 и циррозом, не отвечающим на предыдущую терапию ингибиторами протеазы: рандомизированное двойное слепое исследование фазы 2 (SIRIUS). Lancet Infect. Дис. 15 , 397–404 (2015).
Артикул
PubMed
CAS
Google ученый
Feld, J. J. et al. . Софосбувир и Велпатасвир для инфекций генотипа 1, 2, 4, 5 и 6 ВГС. N. Engl. J. Med. 373 , 2599–2607 (2015).
Артикул
PubMed
CAS
Google ученый
Gilead Sciences, I.Основные сведения о назначении: Харвони (ледипасвир и софосбувир). Фостер-Сити, Калифорния . 1–41 на http://www.gilead.com/~/media/Files/pdfs/medicines/liver-disease/harvoni/harvoni_pi.pdf. (2016).
Фостер, Г. Р. и др. . Софосбувир и Велпатасвир для инфекции генотипа 2 и 3 ВГС. N. Engl. J. Med. 373 , 2599–2607 (2015).
Артикул
CAS
Google ученый
Карри, М. П. и др. . Софосбувир и Велпатасвир для лечения гепатита С у пациентов с декомпенсированным циррозом печени. N. Engl. J. Med . 151116123036000, https://doi.org/10.1056/NEJMoa1512614 (2015).
Основные положения предписывающей информации для VIEKIRA PAK. 1–51 (2016).
Ди Майо, В. К. и др. . Генетическая изменчивость вируса гепатита С и наличие мутаций, связанных с устойчивостью к ns5b, в качестве естественных полиморфизмов в выбранных генотипах могут повлиять на реакцию на ингибиторы ns5b. Антимикробный. Агенты Chemother. 58 , 2781–2797 (2014).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Костантино А. и др. . Встречающиеся в природе мутации, связанные с устойчивостью к полимеразе NS5B и ингибиторам протеазы NS3 HCV у не получавших лечения пациентов с хроническим гепатитом C. Virol. J. 12 , 186 (2015).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Чхатвал, Дж. и др. . Проекция пациентов, не прошедших лечение в эпоху противовирусных препаратов прямого действия. J. Hepatol. 66 , S512 – S513 (2017).
Артикул
Google ученый
Мартин, Т. С. и др. . Частота повторного инфицирования вирусом гепатита С и результаты лечения среди ВИЧ-инфицированных МСМ. СПИД 27 , 2551–2557 (2013).
Артикул
PubMed
Google ученый
Ингилиз, П. и др. . Частота повторного инфицирования ВГС и показатели спонтанного выздоровления у ВИЧ-инфицированных мужчин, практикующих секс с мужчинами, в Западной Европе. J. Hepatol. 66 , 282–287 (2017).
Артикул
PubMed
Google ученый
Ingiliz, P. et al . Высокая частота повторной инфекции ВГС у ВИЧ-положительных МСМ в эпоху ПППД. в 16-й Европейской конференции по СПИДу; 2017 25-27 октября; Милан, Италия, , http: // mediatheque.cyim.com/mediatheque/media.aspx?mediaId=34876&channel=28172 (2017).
Европейский центр мониторинга наркотиков и наркомании (EMCDDA). Статистический бюллетень 2017 . на http://www.emcdda.europa.eu/data/stats2017 (2017 г.).
Fundação Francisco Manuel dos Santos. PORDATA, Base de Dados de Portugal Contemporâneo. на http://www.pordata.pt/Portugal (2017).
Карвалхана, С. К., Лейтао, Дж., Алвес, А. К., Бурбон, М.И Кортез-Пинто, H. Распространенность гепатита B и C в Португалии. Eur. J. Gastroenterol. Гепатол. 28 , 640–644 (2016).
Артикул
PubMed
Google ученый
Anjo, J. et al. . О воздействии гепатита в Португалию. GE J. Port. Гастрентерология 21 , 44–54 (2014).
Артикул
Google ученый
Мариньо, Р. Т., Моура, М. К., Гириа, Дж. А. и Ферриньо, П. Эпидемиологические аспекты гепатита С в Португалии. J. Gastroenterol. Гепатол. 16 , 1076–1079 (2001).
Артикул
PubMed
CAS
Google ученый
Всемирная организация здравоохранения. Глобальная стратегия сектора здравоохранения по вирусному гепатиту на 2016-2021 гг. Glob. Hepat. Программа. Деп. ВИЧ / СПИД 56, WHO / HIV / 2016.06 (2016).
Ministério da Saúde. Direção-Geral da Saúde. Programa nacional para as hepatites virais 2017 . на https://www.dgs.pt/documentos-e-publicacoes/relatorio-do-programa-nacional-para-as-hepatites-virais-2017.aspx (2017).
Rodrigues, A. et al. . Генотипы вируса гепатита С и влияние индукции иммуносупрессии антитимоцитарным глобулином (АТГ) на хронический гепатит у реципиентов почечного трансплантата. Transpl. Int. 11 (1), S115–8 (1998).
Артикул
PubMed
Google ученый
Сарменто-Кастро, Р. и др. . Влияние лечения пегинтерфероном альфа-2b и рибавирином на ткань печени у пациентов с сочетанной инфекцией ВГС или ВГС-ВИЧ. J. Infect. 54 , 609–616 (2007).
Артикул
PubMed
Google ученый
Ramalho, F. et al. . Корреляция генотипов и пути передачи с гистологической активностью и стадией заболевания при хроническом гепатите С. Dig. Дис. Sci. 45 , 182–187 (2000).
Артикул
PubMed
CAS
Google ученый
Calado, R.A. et al. . Подтипы вируса гепатита С, циркулирующие среди потребителей инъекционных наркотиков в Лиссабоне, Португалия. J. Med. Virol. 83 , 608–615 (2011).
Артикул
PubMed
Google ученый
Padua, E., Avo, AP, Almeida, C., Agua Doce, I. & Cortes Martins, H. Оценка разнообразия вируса гепатита C в дополнение к частоте генотипов в образцах, проанализированных в период с 2009 по 2014 год в справочной лаборатории Национального института здравоохранения. Рикардо Хорхе. Acta Med. Порт. 28 , 695–701 (2015).
Артикул
PubMed
Google ученый
Мессина, Дж. П. и др. . Глобальное распространение и распространенность генотипов вируса гепатита С. Гепатология 61 , 77–87 (2015).
Артикул
PubMed
Google ученый
Кати, W. и др. . In vitro профиль активности и устойчивости дасабувира, ненуклеозидного ингибитора полимеразы вируса гепатита С. Антимикробный. Агенты Chemother. 59 , 1505–1511 (2015).
Артикул
PubMed
PubMed Central
Google ученый
Карташев, В. и др. . Новые данные о распределении генотипов HCV в отдельных регионах Западной Европы, России и Израиля. J. Clin. Virol. 81 , 82–89 (2016).
Артикул
PubMed
Google ученый
Petruzziello, A., Marigliano, S., Loquercio, G., Cozzolino, A. & Cacciapuoti, C. Глобальная эпидемиология вирусной инфекции гепатита C: обновленная информация о распространении и циркуляции гепатита C. генотипы вирусов. Всемирный журнал гастроэнтерологии , https://doi.org/10.3748/wjg.v22.i34.7824 (2016).
Чу, К. Л. и др. . Выделение клона кДНК, полученного из генома передающегося с кровью вирусного гепатита не-A, не-B. Наука (80-.). 244 , 359 LP – 362 (1989).
ADS
Статья
Google ученый
Куо, Г. и др. . Анализ циркулирующих антител к главному этиологическому вирусу гепатита человека не-A, не-B. Наука (80-.). 244 , 362 LP – 364 (1989).
ADS
Статья
Google ученый
Морейра, М., Хьюз, Б., Коста Сторти, К. и Зобель, Ф. EMCDDA. Профиль наркополитики: Португалия. Профиль наркополитики 26 стр., Https://doi.org/10.2810/41390 (2011).
Европейский центр мониторинга наркотиков и наркомании (EMCDDA). Тенденции употребления инъекционных наркотиков в Европе . Выбранный выпуск 3 4 , (2010).
Csete, J. et al. . Общественное здравоохранение и международная наркополитика. Ланцет 387 , 1427–1480 (2016).
Артикул
PubMed
PubMed Central
Google ученый
Колецки, Д. и др. . Полная последовательность генома трех изолятов вируса гепатита С подтипа 4b из Португалии. Arch. Virol. 154 , 127–132 (2009).
Артикул
PubMed
CAS
Google ученый
De Bruijne, J. et al. . Появление генотипа 4 вируса гепатита С: филогенетический анализ показывает три различных эпидемиологических профиля. J. Clin. Microbiol. 47 , 3832–3838 (2009).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Wiessing, L. et al. . Эпидемиология вирусной инфекции гепатита С среди потребителей инъекционных наркотиков в Европе: систематический обзор данных для расширения масштабов лечения и профилактики. PLoS One 9 (2014 г.).
Пибус, О. Г., Драммонд, А. Дж., Накано, Т., Робертсон, Б. Х. и Рамбаут, А. Эпидемиология и ятрогенная передача вируса гепатита С в Египте: объединяющий байесовский подход. Мол. Биол. Evol. 20 , 381–387 (2003).
Артикул
PubMed
CAS
Google ученый
Feucht, H.H. et al. . Влияние возраста на распространенность вируса гепатита C подтипов 1a и 1b. J Infect Dis 175 , 685–688 (1997).
Артикул
PubMed
CAS
Google ученый
Брачо, Ма и др. . Полный геном изолята европейского вируса гепатита С подтипа 1g: филогенетический и генетический анализы. Virol. J. 5 , 72 (2008).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Пикетт, Б. Э., Страйкер, Р. и Лефковиц, Э. Дж. Доказательства разделения подтипа 1а ВГС на две отдельные клады. J. Viral Hepat. 18 , 608–618 (2011).
Артикул
PubMed
CAS
Google ученый
Де Лука, А. и др. . Две разные клады вируса гепатита С генотипа 1а имеют разное географическое распространение и ассоциацию с естественной устойчивостью к ингибиторам протеазы NS3. Заражение открытого форума. Дис. 2 , оф043 (2015).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Santos, A. F. et al. . Углубленный филогенетический анализ вируса гепатита С подтипа 1а и наличие 80К и связанных полиморфизмов в протеазе NS3. Sci. Отчет 6 , 1–6 (2016).
Артикул
CAS
Google ученый
Палладино, К. и др. . Низкая частота замен, связанных с резистентностью к NS5A, на Эльбасвир среди вируса гепатита С генотипа 1a в Испании: перекрестное исследование. Sci. Отчет 7 , 3–8 (2017).
Артикул
Google ученый
Сваровская, Е.С. и др. . Редкое развитие резистентности у инфицированных вирусом гепатита с генотипов 1-6 субъектов, получавших софосбувир во 2 и 3 фазах клинических испытаний. Clin. Заразить. Dis . 59 (2014).
Сваровская Е.С. и др. . Замены NS5B вируса гепатита C, ассоциированного с софосбувиром L159F и V321A. J. Infect. Дис. 213 , 1240–1247 (2016).
Артикул
PubMed
CAS
Google ученый
Чен, З. В., Ли, Х., Рен, Х. и Ху, П. Глобальная распространенность уже существующих вариантов ВГС, устойчивых к противовирусным агентам прямого действия (ПППД): анализ данных генома ВГС GenBank. Sci. Отчет 6 , 4–12 (2016).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Ди Майо, В. К. и др. . Мультиклассовая резистентность вируса гепатита C к противовирусной недостаточности прямого действия у реальных пациентов выступает за индивидуализированную терапию второй линии. Liver Int. 37 , 514–528 (2017).
Артикул
PubMed
CAS
Google ученый
Susser, S. et al. . Европейская база данных RAV: частота и характеристики RAV у пациентов, ранее не получавших лечения, и пациентов, получавших ПППД [Аннотация PS007]. Международный конгресс по печени TMEASL — Европейская ассоциация по изучению печени 64 , S139 (2016).
Google ученый
Кришнан, П. и др. . Анализ устойчивости исходных и новых вариантов лечения генотипа 1 вируса гепатита С в исследовании AVIATOR с паритапревиром-ритонавиром, омбитасвиром и дасабувиром. Антимикробный. Агенты Chemother. 59 , 5445–5454 (2015).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Brandão, R. et al. . Характеристика замен, связанных с резистентностью к NS5A и NS5B, у пациентов, инфицированных вирусом гепатита С генотипа 1, в португальской когорте. Вирусы 2018 10 , 223 (2018).
Google ученый
Bartolini, B. et al. . Динамика вариантов, связанных с устойчивостью к генотипу 4 HCV, во время вирусологического ускользания с pIFN / RBV + даклатасвир: тематическое исследование с использованием сверхглубокого пиросеквенирования. J. Clin. Вирол . 66 (2015).
фон Эльм, Э. и др. . Заявление об усилении отчетности по обсервационным исследованиям в эпидемиологии (STROBE): Руководство по отчетности по обсервационным исследованиям. Внутр. J. Surg. 61 , 344–349 (2014).
Google ученый
Leitner, T. et al. . Анализ гетерогенных вирусных популяций прямым секвенированием ДНК. Biotechniques 15 , 120–127 (1993).
PubMed
CAS
Google ученый
Kuiken, C. et al. . Комплексная система последовательной нумерации последовательностей, белков и эпитопов ВГС. Гепатология 44 , 1355–1361 (2006).
Артикул
PubMed
CAS
Google ученый
Като, К. и Стэндли, Д. М. Программа множественного выравнивания последовательностей MAFFT, версия 7: Повышение производительности и удобства использования. Мол. Биол. Evol. 30 , 772–780 (2013).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Gouy, M., Guindon, S. & Gascuel, O. SeaView, версия 4: мультиплатформенный графический пользовательский интерфейс для выравнивания последовательностей и построения филогенетического дерева. Мол. Биол. Evol. 27 , 221–224 (2010).
Артикул
PubMed
CAS
Google ученый
Струк, Д., Юрист, Г., Тернес, А. М., Шмит, Дж. К. и Беркофф, Д. П. КОМЕТ: Адаптивное контекстное моделирование для сверхбыстрой идентификации подтипа ВИЧ-1. Nucleic Acids Res. 42 , 1–11 (2014).
Артикул
CAS
Google ученый
de Oliveira, T. et al . Автоматическая система генотипирования для анализа ВИЧ-1 и других микробных последовательностей. Биоинформатика 21 , 3797–3800 (2005).
Артикул
PubMed
CAS
Google ученый
Алькантара, L.С. J. и др. . Стандартизированная структура для точного и высокопроизводительного генотипирования рекомбинантных и нерекомбинантных вирусных последовательностей. Nucleic Acids Res. 37 , 634–642 (2009).
Артикул
CAS
Google ученый
Сильвестро, Д. и Михалак, И. RaxmlGUI: графический интерфейс для RAxML. Org. Дайверы. Evol. 12 , 335–337 (2012).
Артикул
Google ученый
Letunic, I. & Bork, P. Интерактивное древо жизни (iTOL) v3: онлайн-инструмент для отображения и аннотации филогенетических и других деревьев. Nucleic Acids Res. 44 , W242 – W245 (2016).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Ragonnet-Cronin, M. et al. . Автоматический анализ филогенетических кластеров. BMC Bioinformatics 14 , 317 (2013).
Артикул
PubMed
PubMed Central
Google ученый
Пинеда-Пенья, А.С. и др. . Тенденции и предикторы передачи лекарственной устойчивости (TDR) и кластеров с TDR в местной бельгийской эпидемии ВИЧ-1. PLoS One 9 , e101738 (2014).
ADS
Статья
PubMed
PubMed Central
CAS
Google ученый
Роуз, Р. и др. . Идентификация кластеров передачи с помощью средства выбора кластеров и HIV-TRACE . Исследования СПИДа и человеческие ретровирусы 33 (2017).
Драммонд, А. Дж., Сушард, М. А., Се, Д. и Рамбо, А. Байесовская филогенетика с BEAUti и ЗВЕРЬОМ 1.7. Мол. Биол. Evol. 29 , 1969–1973 (2012).
Артикул
PubMed
PubMed Central
CAS
Google ученый
Шапиро Б., Рамбаут А. и Драммонд А. Дж. Выбор подходящих моделей замены для филогенетического анализа последовательностей, кодирующих белок. Мол. Биол. Evol. 23 , 7–9 (2006).
Артикул
PubMed
CAS
Google ученый
Грей Р. Р. и др. . Способ и темп эволюции вируса гепатита С внутри и среди хозяев. BMC Evol. Биол. 11 , 131 (2011).
Артикул
PubMed
PubMed Central
Google ученый
Аль-Катани, А.А. и др. . Эпидемическая динамика вирусов гепатита C подтипов 4a и 4d в Саудовской Аравии. Sci. Отчет 7 , 44947 (2017).
ADS
Статья
PubMed
PubMed Central
CAS
Google ученый
Павлоцкий, Дж. М. Устойчивость вируса гепатита С к противовирусным препаратам прямого действия в режимах без интерферона. Гастроэнтерология 151 , 70–86 (2016).
Артикул
PubMed
CAS
Google ученый
EASL. Рекомендации EASL по лечению гепатита C Европейская ассоциация изучения печени. J Hepatol. 66 , 1–23 (2016).
Google ученый
Американская ассоциация по изучению заболеваний печени и Американское общество инфекционных болезней.Руководство по ВГС: Рекомендации по тестированию, ведению и лечению гепатита C . на www.hcvguidelines.org (2017).
Сорбо, М. К. и др. . Замещения, связанные с лекарственной устойчивостью вируса гепатита С, и их клиническая значимость: Обновление 2018 г. Drug Resist. Updat. 37 , 17–39 (2018).
Артикул
PubMed
Google ученый
Генотип 4 ВГС; Краткий обзор | Афзал
Мухаммад Сохаил Афзал, Амани Абд Эльрехим, Ахмед Рагаа, Ахмед Вахид
Мухаммад Сохаил Афзал, Школа прикладных биологических наук Атта ур Рахман (ASAB), Национальный университет науки и технологий (NUST), Исламабад, Пакистан
Амани Абд Эльрехим, Ахмед Рагаа, Ахмед Вахид, кафедра биохимии, фармацевтический факультет, университет Миниа, Египет
Для корреспонденции: Ахмед Вахид, кафедра биохимии, фармацевтический факультет, университет Миниа, Египет.
Эмиаль: [email protected]
Телефон: + 2-03-5742435
Поступила: 30 сентября 2013 г.
Доработана: 25 ноября 2013 г.
Принята в печать: 30 ноября 2013 г.
Опубликовано онлайн: 21 февраля 2014 г.
РЕФЕРАТ
Вирус гепатита С (ВГС) — известная ведущая причина хронических заболеваний печени и гепатоцеллюлярной карциномы (ГЦК). Текущее доступное лечение зависит от одновременного приема пегинтерферона и рибавирина.Современные лечебные препараты чрезвычайно дороги, эффективны не для всех пациентов с разными генотипами и связаны с серьезными побочными эффектами, которые в некоторых случаях могут привести даже к смерти. Филогенетический анализ привел к классификации вируса гепатита С (ВГС) на более чем 7 генотипов в зависимости от нескольких критериев, среди которых — их всемирное распространение, передача и прогрессирование заболевания. Отсутствие эффективной вакцины позволило образовательным программам стать наиболее подходящими мерами борьбы с распространением ВГС.Здесь, в этом обзоре, мы обсудим передовые инструменты для изучения генотипа 4 ВГС, а также современные методы лечения и испытания вакцинации против ВГС и, наконец, превращение ВГС в гепатоцеллюлярную карциному.
Ключевые слова: ВПЦ; Генотип 4; Уход; Испытания вакцины
© 2014 Авторы. Опубликовано ACT Publishing Group Ltd.
Афзал М.С., Элрехим А.А., Рагаа А., Вахид А. Генотип 4 ВГС; Краткий обзор. Журнал исследований гастроэнтерологии и гепатологии 2014; 3 (2): 968-976 Доступно по адресу: URL: http: // www.ghrnet.org/index.php/joghr/article/view/606
Введение
Вирус гепатита С (ВГС) — сложное заболевание печени. Его медицинское значение и необходимость быстрого определения новых терапевтических подходов привели к интенсивным исследованиям его возбудителя. Инфекция ВГС является серьезной проблемой общественного здравоохранения, во всем мире инфицировано более 160 миллионов человек, эта цифра составляет почти 3% от общей численности населения мира по оценкам Всемирной организации здравоохранения (ВОЗ), и 2–3 миллиона новых случаев заболевания ежегодно. [1,2].
ВГС — одна из основных проблем со здоровьем, особенно в Египте, где преобладает 4-й генотип ВГС, поскольку, по оценкам ВОЗ, он поражает более 20% населения в целом. Самая высокая распространенность антител к вирусу гепатита С (ВГС) в мире зарегистрирована в Египте, где преобладает генотип 4 ВГС [3].
Существует множество возможных причин широкого распространения ВГС в Египте. Среди них — стоматологическое лечение как возможный источник передачи инфекции ВГС [4].Было обнаружено, что пациенты, находящиеся на гемодиализе, также подвержены высокому риску передачи ВГС [5]. Более того, ранее сообщалось, что использование стеклянных шприцев на юге Италии является одним из старых способов передачи инфекции [6]. И, наконец, основные факторы риска инфицирования ВГС в Корее в основном связаны с несоответствующими медицинскими процедурами, такими как переливание крови, травма от укола иглой, хирургия, стоматологические процедуры и нанесение татуировок [7].
ЧАСТИЦА ВГС
HCV — это небольшой вирус с оболочкой, относящийся к роду Hepacivirus в семействе Flaviviridae.5′-UTR генома HCV содержит большой структурированный домен, который служит внутренним сайтом входа в рибосомы (IRES) [1,8,9]. При инфицировании вирусом гепатита C нормальный процесс трансляции, зависящий от кэпа, сильно ингибируется, и инфицированные клетки вместо этого переключают большую часть своей способности синтеза белка на продукцию вирусных полипротеинов. Элемент IRES HCV рекрутирует рибосомную субъединицу 40S непосредственно для инициации трансляции вирусной РНК, минуя потребность в нескольких факторах инициации трансляции [10,11]. Геном РНК с положительной цепью HCV затем кодирует один полипротеин, который процессируется клеточными и вирусными протеазами в 10 зрелых белков (4 структурных и 6 неструктурных белков) [12].
Наше понимание процесса морфогенеза ВГС все еще находится в зачаточном состоянии. Различные вирусные компоненты были идентифицированы как участники процесса морфогенеза. Как и ожидалось, структурные белки необходимы в составе вируса. Среди этих компонентов гликопротеины оболочки HCV, E1 и E2, представляют особый интерес, поскольку в дополнение к их роли в сборке, они также являются основными игроками во время процесса входа. Гликопротеины оболочки HCV E1 и E2 представляют собой трансмембранные белки I типа, которые состоят из C-концевого трансмембранного домена и большого N-концевого эктодомена, который сильно модифицирован N-связанными гликанами [13].Важно отметить, что функции входа и сборки должны строго контролироваться, чтобы происходить в подходящем месте и в нужное время [14]. Эти два белка собираются как нековалентный гетеродимер внутри эндоплазматического ретикулума (ER) инфицированных клеток, тогда как они образуют большие дисульфидно-связанные комплексы на поверхности вириона [15]. Они действительно участвуют в связывании рецепторов и опосредуют процесс слияния между вирусной оболочкой и мембраной эндосомной клетки-хозяина. Гликопротеины E1 и E2 активно участвуют в испытаниях вакцинации против HCV.
ГЕНОТИПЫ ВГС
HCV далее классифицируется как минимум на семь основных генотипов, которые различаются примерно на 30 процентов по своей нуклеотидной последовательности. Эти генотипы (1, 2, 3, 4, 5, 6 и 7) демонстрируют различия, основанные на их распространении по всему миру, передаче и прогрессировании заболевания (как упоминалось выше). Между этими генотипами существует множество различий в их нуклеотидных заменах в вирусном геноме (разница нуклеотидных последовательностей 31-33% между разными генотипами) и более 100 подтипов (разница 20-25% между разными подтипами одного и того же генотипа), присутствующих в геноме вируса. разные регионы мира [16].
Существует большая дискуссия о классификации различных генотипов ВГС. Некоторые исследователи предложили до 11 различных генотипов ВГС, а согласно другим ВГС делится только на 6 основных генотипов, причем генотипы 6-11 являются вариантами генотипа 6. Согласно этой теории, генотипы 6-11 следует классифицировать как один генотип, т. Е. тип 6 [17]. Как показано недавно, генотипы 1-3 распространены по всему миру, а типы 1a и 1b являются наиболее распространенными в мире. Генотип 1b наиболее распространен в Японии (70%) [18-20].Генотип 1 более распространен в Европе [21,22]. В Юго-Восточной Азии генотип 3 наиболее часто встречается у 90% пациентов [23-25]. В то время как генотип 4 наиболее распространен в Центральной Африке, Египте и на Ближнем Востоке [26]. Примечательно, что генотип 4 является квазиисключительным (91%) в Египте [27]. Вьетнамское население имеет географически изолированные генотипы 7, 8 и 9, и эти генотипы пока идентифицированы только из этого региона [28]. Генотипы 10 и 11 идентифицируются только у индонезийских пациентов, инфицированных ВГС [29].
РАЗРАБОТКА ИНСТРУМЕНТОВ РАСШИРЕННЫХ ИССЛЕДОВАНИЙ ДЛЯ ИЗУЧЕНИЯ ГЕНОТИПА 4 ВГС
HCV циркулирует у инфицированных пациентов с относительно низкими титрами и образует комплексы с такими компонентами сыворотки, как липопротеины [30,31].По причинам, которые частично остаются неизвестными, вирус гепатита С, полученный из сыворотки крови, не может размножаться в культуре клеток. Эти ограничения затрудняют исследования ВГС, и они в значительной степени зависят от суррогатных систем. Например, ретровирусы с дефицитом репликации, псевдотипы гликопротеинов оболочки HCV (HCVpp) [32], были использованы для изучения проникновения HCV [33]. Точно так же системы репликонов позволили исследовать репликацию HCV (см. Обзор [34]). Однако до 2005 года не существовало системы для воспроизведения сборки и секреции HCV, что оставалось в основном неуловимым.Точно так же через 21 год после открытия ВГС его структура остается неизвестной. Тем не менее, в 2005 г. нескольким командам наконец удалось размножить ВГС в культуре клеток (ВГС, ВГС, культивируемые в клетках) [35–37], что позволило подтвердить большую часть предыдущих данных о проникновении вирусов и облегчило тестирование противовирусных препаратов. Более того, эта система впервые позволила исследовать сборку вирусов.
После его идентификации было много попыток определить генотип 4 HCV путем анализа частичных последовательностей вариантов.Варианты генотипа 4 HCV амплифицировали из сывороток пациентов. Были секвенированы и проанализированы области 5 ’UTR, core, E1, E2, NS3, NS4, NS5 и 3’UTR [38-41]. В 1997 г. Чемберлен и др. Сообщили о полной нуклеотидной последовательности египетского варианта генотипа 4a HCV, ED43 (номер доступа в GenBank Y11604) [42]. Кроме того, в 2007 году Тимм и др. Описали полноразмерную последовательность генотипа 4d HCV, наиболее распространенного подтипа при инфекциях в Африке к югу от Сахары [43]. Эталонные последовательности генотипа 4 HCV и его подтипов можно найти в (базе данных LosAlamos HCV) (http: // hcv.lanl.gov/content/hcv-db/classification/genotable.html).
ПОДГЕНОМНЫЙ РЕПЛИКОН
В 1999 г. была разработана система репликона HCV для генотипа 1b. Эта система была разработана путем обрезки вирусного генома, необходимого для репликации вируса, то есть NS3-NS5B вместе с 3 ’, 5’ UTR-областями [44]. Из-за меньшего размера, чем у аутентичного вирусного генома, было возможно вставить гетерологичный доминантный селектируемый маркер (например, неомицинфосфотрансферазу, neo), не превышая естественную длину генома HCV.Репликоны часто представляли собой бицистронные конструкции с трансляцией неомицин-фосфотрансферазы, управляемой IRES HCV, за которой следует HCV NS3-3 ‘UTR под контролем второго IRES, полученного из вируса энцефаломиокардита (EMCV).
Ранее системы репликона HCV были успешно созданы только для дикого типа или адаптированного генотипа 1a [44-56]. Совсем недавно лаборатория Чарльза Райса разработала репиликоновые системы для генотипов 3a и 4a [57]. Штамм-прототип ED43 (4a) был использован для создания G418-селектируемых субгеномных репликонов.Чтобы сделать эти репликоны более полезными для высокопроизводительного скрининга и оценки противовирусных соединений, они были модифицированы для экспрессии химерного слитого белка люциферазы светлячка и неомицинфосфотрансферазы с получением стабильных экспрессирующих репликон клеток.
ПСЕВДОТИПНЫЕ РЕТРОВИРУСНЫЕ ЧАСТИЦЫ
В отсутствие системы культивирования клеток HCV для изучения всего жизненного цикла вируса были разработаны суррогатные модели для изучения роли гликопротеинов HCV в проникновении вируса.Наиболее успешной моделью для исследования ранних стадий инфицирования ВГС было выявление ретровирусных псевдотипов, несущих немодифицированные гликопротеины ВГС (HCVpp) [58,59]. HCVpp основан на котрансфекции почечных клеток 293T векторами экспрессии, кодирующими E1 и E2 HCV, белками gag-pol вируса лейкемии мышей (MLV) или вируса иммунодефицита человека (ВИЧ) и, наконец, геномом ретровируса, кодирующим репортерный ген люцифераза). HCVpp можно использовать для исследований нейтрализации антител, поскольку связывание и рецепторное взаимодействие этих ретровирусных псевдотипов регулируется функциональным белковым комплексом E1-E2 HCV, включенным в оболочку этих частиц.Стоит отметить, что система HCVpp для генотипа 4 HCV была разработана тремя независимыми группами [60–62], которые широко использовались для исследований проникновения вирусов и связывания рецепторов.
МОДЕЛИ ДЛЯ ИССЛЕДОВАНИЯ ИНДИВИДУАЛЬНЫХ БЕЛКОВ ГЕНОТИПА 4 ВГС В КОНТЕКСТЕ ПОЛНОЙ ДЛИНЫ ВИРУСА
Разработка эффективных систем культивирования для изучения важных противовирусных мишеней NS3, NS5A, специфичных для генотипа, в контексте полного вируса, позволила исследовать небольшие противовирусные соединения прямого действия.Действительно, NS5A считается одной из многообещающих мишеней для небольших соединений против HCV, которые уже проходят клинические испытания [63]. Еще многое предстоит узнать о роли очень разнообразных функций NS5A в генотипе 2a; и; кроме того, для большинства других генотипов NS5A вообще не изучался. Недавно были разработаны системы культивирования инфекционных генотипов NS5A HCV для генотипа 4 HCV наряду с другими генотипами HCV путем замены полного NS5A рекомбинантного J6 / JFh2 [64] на NS5A из ED43 (4a) [65].Другой очень важной мишенью является неструктурный белок NS3 HCV. Недавно разработанный полноразмерный компетентный к репликации клон Jc1 (pFK JFh2 / J6 / C-846), который показал очень высокую эффективность репликации в клетках Huh7.5, был использован для разработки рекомбинантного вируса, экспрессирующего протеазу NS3 генотипа 4 HCV и всех остальных. другие генотипы [66]. Этот рекомбинантный вирус позволял осуществлять прямой мониторинг ингибирования противовирусными препаратами конкретных протеаз путем оценки снижения как инфективности супернатанта, так и кинетики репликации.Эта генотип-специфическая протеазная система также обеспечивала фенотипический анализ для быстрой оценки возникающей резистентности во время терапии и влияния конкретных мутаций на результат лечения.
РЕКОМБИНАНТНЫЙ ВИРУС (4a / JFh2)
2005 год стал важной вехой в исследованиях ВГС, когда Вакита и др. [67] разработали систему культивирования клеток генотипа 2a JFh2 у японского пациента с фулиминантным гепатитом. JFh2 — это эффективная система in vitro, позволяющая исследовать полный жизненный цикл инфекционного вируса.JFh2 обладает уникальной способностью к репликации в клетках Huh7. В том же году Lindenbach et al [64] разработали более эффективную систему культивирования клеток HCV 2a (J6 / JFh2), заменив область Core-NS2 из другого изолята 2a. Недавно были разработаны системы межгенотипных рекомбинантов (4a / JFh2) клеточных культур, содержащие структурные гены (Core, E1 и E2), p7 и все или часть NS2 прототипного штамма 4a ED43. Эти химерные вирусы позволили провести специфичный для генотипа функциональный анализ Core-NS2 и скрининг нейтрализующих антител и ингибиторов, нацеленных на эту область [68].
Совсем недавно Gottwein et al (2011) разработали репортерные вирусы с использованием рекомбинантов на основе JFh2, экспрессирующих core-NS2 изолятов-прототипов генотипов 1-7. Область Core-NS2 ED43 была использована для создания репортерной рекомбинантной системы. Усиленный GFP (EGFP) или RLuc вставляли в C-концевой домен III JFh2 NS5A в сайте, описанном ранее Moradpour et al 2004 (ниже аминокислотных остатков 2356 или 2390, нумерация относится к H77, генотип 1b). Эти репортерные вирусы можно использовать для высокопроизводительных генотип-специфических функциональных исследований взаимодействий рецептора HCV, сывороточных нейтрализующих антител и терапевтических средств, препятствующих проникновению или сборке HCV, на основе флуоресценции и люминесценции.
МОДЕЛЬ ШИМПАНЗЕ КАК ЕДИНСТВЕННАЯ НАДЕЖНАЯ МОДЕЛЬ ДЛЯ ИССЛЕДОВАНИЯ ГЕНОТИПА 4 ВГС
Шимпанзе — единственная модель для изучения инфекции ВГС, отражающая иммунопатогенез и вирусную устойчивость, наблюдаемую при инфекциях человека. Шимпанзе можно инфицировать с помощью внутривенной инокуляции частиц HCV и внутрипеченочной трансфекции транскриптами РНК из полноразмерных клонов кДНК HCV. Молекулярные инфекционные клоны генотипов 1a (штаммы H77, HCV-1, HC-TN), 1b (HC-J4, Con1, HCV-N) и 2a (HC-J6 и JFh2) были использованы для инициации моноклональных инфекций у шимпанзе ( рассмотрено в Gottwein et al [69]), чтобы изучить функцию определенных участков генома с помощью обратных генетических исследований, а также изучить естественное течение ВГС и защитный иммунитет.Кроме того, пулы плазмы моноклонально инфицированных шимпанзе использовали для заражения вирусом в исследованиях вакцин и противовирусных препаратов у шимпанзе [70] или мышей SCID-uPA, привитых гепатоцитами человека [71]. В 2010 году Gottwein и Scheel et al создали консенсусные клоны кДНК штаммов ED43 (генотип 4a), которые были полностью функциональны у шимпанзе [70]. С разработкой модели шимпанзе с генотипом 4 ВГС стало возможным анализировать определенные участки вирусного генома с помощью обратной генетики, иммунных ответов хозяина во время острой инфекции, включая периферические и внутрипеченочные Т-клеточные ответы, вакцины и исследования противовирусных препаратов, особенно для этого важного вирусного генотипа. .
МОДЕЛЬ ХИМЕРНЫХ МЫШЕЙ ПЕЧЕНИ ЧЕЛОВЕКА
Гепатоциты человека трансплантировали мышам uPA / scid; у трансгенных мышей, у которых ген урокиназы управляется промотором / энхансером человеческого альбумина, эти трансплантированные человеческие клетки пролиферировали и заменили апоптозные клетки печени мышей [72]. Было показано, что эти химерные мыши восприимчивы к инфекции HCV. Уровни репликации вируса пропорциональны индексу репопуляции гуманизированных клеток [73].У этих химерных мышей достигается успешная репликация вирусов HCV генотипа 2a [74], 1a [75], 1b [76] и межгенотипных химерных вирусов JFh2 [74]. Показано, что в недавно разработанной модифицированной форме химерных мышей (Fah — / — Rag2 — / — Il2rg — / — мышь) ВГС сохраняется более полугода и, скорее всего, не оказывает никакого влияния на здоровье животного. HCV также может передаваться от одной химерной мыши к другой с вирусными титрами и динамикой, аналогичными тем, которые достигаются при инокуляции сывороткой пациента.Эти химерные животные использовались для тестирования противовирусных препаратов, таких как интерфероны [74].
ПРОГРЕСС В ЛЕЧЕНИИ И ВАКЦИНАЦИИ ВГС 4a
Лечение ВГС пегилированным интерфероном (ПЕГ-ИФН) и рибавирином (РБВ) становится стандартом лечения (SOC) для лечения большинства генотипов ВГС, где двойная терапия является современным только для инфекций, не относящихся к генотипу 1. [77]. Однако несколько факторов влияют на эффективность комбинированных схем PEG-INF / RBV.Подобно вариации эффективности лечения в зависимости от вирусного генотипа, предикторы устойчивого вирусологического ответа (УВО) варьируются в зависимости от генотипа. Сравнительно высокая стоимость лечения комбинациями ПЭГ-ИФН / рибавирин и серьезные побочные эффекты усиливают важность оценки и оптимизации факторов, влияющих на лечение, до его начала. На сегодняшний день мало что известно о факторах, влияющих на исход лечения PEG-INF / RBV при HCV-4. Некоторые из этих факторов связаны с вирусами, а другие — с факторами, связанными с хозяином.Факторами, связанными с вирусом, являются генотип ВГС, исходная вирусная нагрузка и квазивиды ВГС [78]. Факторами, связанными с хозяином, являются однонуклеотидные полиморфизмы (SNP) в генах интерлейкина (IL) -28B и NS5A, сывороточный анти-E1E2 до лечения и индуцируемый интерферон-гамма белок-10 кДа (IP-10 или CXCL10), этническая принадлежность и гистопатология печени. .
ВИРУСНЫЕ ФАКТОРЫ
HCV-4 — это трудноизлечимый генотип [78]. Более того, высокая исходная вирусная нагрузка увеличивает устойчивость к терапии.Пороговое значение 400 000 МЕ / мл используется в большинстве исследований [79,80]. Другой важной причиной трудностей лечения является наличие нескольких видов HCV-4 [81]. Видовое разнообразие позволяет вирусу избежать противовирусной терапии.
ХОЗЯЙСТВЕННЫЕ ФАКТОРЫ
Недавнее когортное исследование выявило связь полиморфизма IL-28B и ответа на лечение интерфероном [82]. В это исследование вошли 129 пациентов с HCV-4 из трех медицинских центров Саудовской Аравии. У этих пациентов были идентифицированы пять однонуклеотидных полиморфизмов (SNP), которые коррелировали с SVR.Эти данные показали, что генотип IL-28B rs12979860 CC и rs12980275AA были связаны с УВО. Более того, определяющая устойчивость к IFN / RBV область (IRRDR) была идентифицирована как новая область, расположенная рядом с С-концом гена NS5A. SNP в этом регионе показали корреляцию с результатами лечения PEG-IFN / RBV при инфекциях HCV-2a и -2b. Недавно полиморфизм в этой области показал корреляцию с результатами лечения PEG-IFN / RBV у египетских пациентов, инфицированных HCV-4 [83].
Недавний отчет Shaker et al из Египта показал, что SNP в IL-28B (rs8099917 T / G и rs12979860 C / T) и сывороточные уровни IL-10 и IL-28 могут быть многообещающими предикторами пегилированного генотипа 4 HCV. исход терапии интерфероном / рибавирином [84].Недавно опубликованный мета-анализ влияния полиморфизмов IL-28B (rs12979860 и rs8099917) на спонтанный и связанный с лечением клиренс у пациентов с гепатитом C показал, что эти полиморфизмы имеют сильную прогностическую связь с ответом на терапию для генотипа 4 HCV [85]. Fortunato et al (2008) [86] сообщили, что генетические варианты в генах IRF-1 и Stat1 пути IFN также связаны с инфекцией HCV.
Анти-E1E2 и IP-10 в сыворотке до лечения также являются другими факторами, влияющими на реакцию на лечение.Ответ анти-E1E2 в сыворотке до лечения прогнозирует лучший клиренс РНК HCV и результат лечения. Комбинация анти-E1E2 и IP-10 значительно улучшает прогноз ответа на лечение. Это требует дальнейшего исследования и проверки на более широких когортах пациентов в контексте новых терапевтических стратегий. Данные о корреляции между этнической принадлежностью и результатами лечения ПЭГ-ИФН / рибавирином у пациентов с ВГС-4 все еще противоречивы. Два исследования оценивали влияние этнической принадлежности между египтянами и европейцами на терапевтический результат лечения PEG-IFN / RBV и не показали значительных различий между двумя разными этническими группами [87,88].Напротив, недавнее исследование пришло к выводу, что египетская этническая принадлежность является благоприятным фактором для клинического исхода [77,89]. В Египте исследование показало, что тяжелый фиброз, тяжелый стеатоз, лечение стандартным интерфероном являются прогностическими факторами низкого УВО [90]. Это исследование предполагает, что при рутинной оценке факторов, предсказывающих ответ на лечение, следует учитывать уровень альфа-фетопротеина (AFP) в сыворотке до начала лечения.
В настоящее время пациентов с гепатитом С лечат интерфероном альфа (IFN-a) отдельно или в комбинации с аналогом нуклеозидов рибавирином.Сообщается, что система IFN опосредует противовирусные, антипролиферативные, иммунные и другие клеточные эффекты [91]. Отличительной чертой всех IFN является их способность усиливать экспрессию множества генов. Некоторые из этих генов кодируют эффекторные белки, такие как белок PKR, с замечательной противовирусной активностью. У человека противовирусное действие IFN опосредуется индукцией по крайней мере двух основных белков, протеинкиназы R и MxA [92]. PKR (протеинкиназа, регулируемая РНК) участвует в патогенезе ГЦК, связанного с генотипом 4 HCV, путем ингибирования вирусных и клеточных белков, связанных с ростом и пролиферацией клеток.Экспрессия гена PKR считается надежным маркером для прогнозирования ГЦК с высокой чувствительностью, специфичностью и диагностической точностью [93].
ИССЛЕДОВАНИЯ ПО ВАКЦИНАЦИИ ОТ ВГС
Разработка защитной вакцины против ВГС оказалась чрезвычайно сложной задачей. Обширные исследования в этой области показывают, что успешная вакцина против ВГС должна стимулировать выработку нейтрализующих антител (возможно, против гликопротеинов оболочки ВГС E1 и / или E2) и мощных Т-клеточных ответов, специфичных для ВГС.
белков E1 и E2 присутствуют на поверхности вирусных частиц и, таким образом, распознаются нейтрализующими антителами. Гликопротеин E2 считается основной мишенью нейтрализующих антител против вируса гепатита C. Он также является белком, связывающим рецептор вируса гепатита C, который, как было показано, взаимодействует с тетраспанином CD81 и рецептором скавенджера BI (SRB1), двумя корецепторами вируса гепатита C.
Большинство антител, идентифицированных на сегодняшний день, нацелены на рецептор-связывающие эпитопы в гликопротеине E2. Нацеливание на факторы хозяина может представлять собой альтернативный подход к предотвращению проникновения ВГС.Эти антитела не нацелены на саму вирусную частицу, а скорее блокируют взаимодействие вирус-хозяин. Действительно, было показано, что ряд антирецепторных антител, нацеленных на CD81 и SR-BI, блокируют проникновение вируса.
НЕЙТРАЛИРУЮЩИЕ ЭПИТОПЫ ВГС И АНТИТЕЛЫ
Идентификация механизмов иммунной защиты — важный шаг в разработке вакцины против ВГС. Действительно, идентификация клонов человеческих антител с широкой нейтрализующей активностью важна для разработки эффективной вакцины против большинства известных человеческих вирусов.Ранее было показано, что индукция нейтрализующих антител после вакцинации составляет главный компонент защиты, обеспечиваемой адаптивным иммунным ответом, против ряда вирусов. Однако в случае вируса гепатита С инфекция может сохраняться даже в присутствии широко нейтрализующих антител в более чем 50% случаев, когда многие пациенты не могут избавиться от вируса и вместо этого у них развивается хроническая инфекция в присутствии нейтрализующих антител к вирусу гепатита C. которые обычно выявляются в течение 1-3 месяцев после инфицирования ВГС.Это может привести к различным формам хронического гепатита, цирроза печени и в конечном итоге может привести к гепатоцеллюлярной карциноме и смерти. Были предложены различные механизмы, лежащие в основе этого явления, и одним из самых последних предложенных является присутствие мешающих антител, которые останавливают ответы нейтрализации антител. Ранее сообщалось, что у большинства хронически инфицированных пациентов в сыворотке крови обнаруживаются перекрестно-реактивные нейтрализующие антитела. Нейтрализующие антитела не были обнаружены в нескольких случаях острых излечивающихся инфекций, и обнаружение нейтрализующих антител у остро инфицированных лиц, по-видимому, не было связано с клиренсом вируса.Напротив, в другом исследовании сообщалось, что у некоторых пациентов наблюдалось прогрессирующее появление относительно сильного нейтрализующего ответа в корреляции со снижением вирусной нагрузки в крови. В рамках этого исследования было также продемонстрировано, что нейтрализующие антитела с высоким титром сыворотки были обнаружены у лиц, излечившихся от инфекции. Более того, у большинства людей, прогрессирующих до хронической инфекции, обнаруживались нейтрализующие антитела с низким титром во время ранней острой инфекции, когда вирус мог ускользнуть.Вместе эти наблюдения предполагают клиническую важность нейтрализующих антител.
БЕЛКИ Е1 И Е2 ЯВЛЯЮТСЯ ДВУМЯ ГЛАВНЫМИ ЦЕЛЯМИ СИНТЕЗА ВАКЦИНЫ ОТ ВГС
Гликопротеин E1 HCV демонстрирует относительно высокую степень консервативности, чем E2. Было доказано, что это трудная мишень для нейтрализации моноклональных антител. Это можно объяснить предполагаемой низкой иммуногенностью, сравнимой с белком E2 [94,95]. Несмотря на эту проблему, были идентифицированы два моноклональных антитела, направленных против гликопротеина E1 HCV (IGH 505 и IGH 526) [96].Эти антитела сильно нейтрализуют HCVpp, несущий гликопротеин оболочки E1 различных генотипов, таких как 1a, 2a, 1b, 4a, 5a и 6a, тогда как они не смогли нейтрализовать генотип 3a HCV. Эпитопы для обоих моноклональных антител были картированы в области, охватывающей аминокислоты с 313 по 327. Однако механизм, с помощью которого эти E1-направленные моноклональные антитела нейтрализуют инфекцию HCV, остается неясным [96]. В дополнение к этим двум антителам, антитело H-111, как сообщалось, реагировало в ELISA с экспрессируемыми белками E1 из генотипов 1a, 1b, 2b и 3a.Сообщалось, что H-111 связывается с 192YEVRNVSGVYh311 областью E1. Кроме того, другая идентифицированная эпитопная область E1 рассматривалась как универсально консервативная область E1, содержащая аминокислоты 315-328.
E2 кодирует кластеры высокоиммуногенных перекрывающихся эпитопов. Ранее был идентифицирован эпитоп, участвующий в нейтрализации вируса HCV, расположенный в белке E2 HCV и содержащий аминокислоты 412-419. Другой основной мишенью нейтрализующих антител является гипервариабельная область (HVR1) в белке оболочки E2 HCV [97].Очевидная вариабельность гипервариабельной области E2 (HVR1), первых 27 аминокислот эктодомена E2, по-видимому, обусловлена отбором антителом вариантов иммунного ускользания. Несмотря на вариабельность последовательности HVR1, физико-химические свойства остатков в каждом положении и конформация HVR1 высоко консервативны среди различных видов. Сообщается также, что E2 HVR1 отвечает за связывание и проникновение вируса. Было высказано предположение, что HVR1 играет роль нейтрализующего эпитопа, поскольку эта область демонстрирует заметную изменчивость последовательности.Ранее также сообщалось, что разрешенная инфекция связана со стабильными последовательностями HVR1, тогда как стойкая инфекция HCV связана с изменением последовательности HVR1. В целом это говорит о том, что HVR1 играет важную роль в нацеливании реакции антител на гликопротеин E2 HCV. К сожалению, иммуногенные эпитопы HVR1 имеют тенденцию быть изолят-специфичными без распознавания других генотипов, что приводит к ускользанию от вируса. В литературе сообщалось о нескольких мутантах, ускользающих от ВГС, в том числе о Q412H у хронических носителей ВГС.Недавно было показано, что последовательности гликопротеинов E1 и E2 управляются нейтрализующими ответами антител, где ускользающие мутантные штаммы вскоре становятся доминирующими.
ПРОГРЕСС ПАЦИЕНТОВ С ГЕНОТИПОМ 4 ВГС ДО ГЕПАТОЦЕЛЛЮЛОЗНОЙ Карциномы
ВГС часто первоначально диагностируется на поздней стадии, когда возможности лечения уже ограничены. Из-за медленного и незаметного начала многие пациенты не знают о своей инфекции, и около 50% случаев остаются невыявленными [98]. В частности, все большее внимание уделяется ВГС из-за его широкого и глубокого проникновения в общество в сочетании с очень высокой частотой ГЦК у пациентов, инфицированных хоническим ВГС.Действительно, гепатоцеллюлярная карцинома (ГЦК) стала основной причиной смерти людей, постоянно инфицированных ВГС [99]). После установления цирроза печени у хозяев, инфицированных ВГС, ежегодная скорость ГЦК составляет около 6% [91]). ГЦК составляет около 2% от общего числа раковых заболеваний и является самой смертельной формой рака, и его заболеваемость росла за последние 30 лет [1100]. В соответствии с этими сообщениями, индийское исследование показало, что инфекция ВГС (генотип 4) увеличивает риск развития ГЦК в три раза по сравнению с другими генотипами [101].Напротив, в Египте, где преобладает генотип 4 HCV, сообщалось об отсутствии связи между инфицированием генотипом 4 и развитием HCC [102].
МЕХАНИЗМЫ ПРОГРЕССИИ ВГС К ГЦК
Механизм канцерогенеза до конца не изучен. Некоторые исследования демонстрируют, что когда воспаление индуцируется в печени в присутствии корового белка HCV, производство окислительного стресса запускается до такой степени, что не может быть остановлено нормальным физиологическим антагонистическим агентом [103].Более того, стеатоз печени, частый и серьезный признак инфекции вируса гепатита С (ВГС), может усиливать гиперпродукцию оксидативного стресса [104]. Другими возможными путями с участием корового белка вируса ВГС могут быть изменение экспрессии некоторых клеточных генов и модуляция внутриклеточных сигнальных путей. Например, было обнаружено, что фактор некроза опухоли (TNF) -α и интерлейкин-1β транскрипционно активируются на уровне белка и мРНК у мышей, инфицированных HCV [105]. Более того, ранее сообщалось, что прогрессирование заболевания печени от хронического заболевания печени до HCC из-за инфекции HCV генотипа 4 связано с дисбалансом между определенными типами цитокинов [106].В дополнение к этим причинам, коровый белок HCV, как сообщается, модулирует внутриклеточные сигнальные пути некоторых белков, таких как ретиноидный рецептор X (RXR) -α, которые играют важную роль в пролиферации и метаболизме клеток [107].
КОНФЛИКТ ИНТЕРЕСОВ
В отношении настоящего исследования нет конфликта интересов.
ССЫЛКИ
1
Бальдо В., Балдовин Т., Тривелло Р., Флореани А. Эпидемиология инфекции ВГС.Curr Pharm Des 2008 14: 1646-1654
2
Паркин ДМ. Глобальная статистика рака в 2000 году. Lancet Oncol 2001; 2: 533-543
3
Миллер FD, Абу-Раддад LJ. Доказательства интенсивной продолжающейся эндемической передачи вируса гепатита С в Египте. Proc Natl Acad Sci U S A 2009; 107: 14757-14762
4
Махбуби Н., Портер С.Р., Караяннис П., Алавян С.М. Стоматологическое лечение как фактор риска вирусной инфекции гепатита В и С. Обзор новейшей литературы.J Gastrointestin Liver Dis 2013; 22: 79-86
5
Gentile I, Di Flumeri G, Scarica S, Frangiosa A, Foggia M, Reynaud L, Borgia G. Острый гепатит C у пациентов, находящихся на гемодиализе: опыт терапии высокими дозами интерферона. Минерва Урол Нефрол 2013; 65: 83-84
6
Guadagnino V, Stroffolini T, Caroleo B, Menniti Ippolito F, Rapicetta M, Ciccaglione AR, Chionne P, Madonna E, Costantino A, De Sarro G et al. Инфекция вирусом гепатита С в эндемичном районе на юге Италии 14 лет спустя: свидетельства исчезновения инфекции.Dig Liver Dis 2013; 45 403-407
7
Kim JY, Cho J, Hwang SH, Kil H, Bae SH, Kim YS, Lee HC, Jeong SH Поведенческие и связанные со здоровьем факторы риска хронической инфекции вируса гепатита C в Корее. J Korean Med Sci 2012; 27 1371-1377
8
Вайнбаум К., Лайерла Р., Марголис Х.С. Профилактика и борьба с инфекциями вирусами гепатита в исправительных учреждениях. Центры по контролю и профилактике заболеваний. MMWR Recomm Rep 2003; 52 1-36; викторина CE31-34
9
Гурцевич В.Е.Онкогенные вирусы человека: вирусы гепатита В и С и их роль в гепатоканцерогенезе. Биохимия (Моск) 2008; 73: 504-513
10
Пестова Т.В., Колупаева В.Г., Ломакин И.Б., Пилипенко Е.В., Шацкий И.Н., Агол В.И. и Эллен К.Р. Молекулярные механизмы инициации трансляции у эукариот. Proc Natl Acad Sci U S A 2001; 98: 7029-7036
11
Отто GA, Puglisi JD. Путь инициации трансляции, опосредованной IRES HCV. Cell 2004; 119: 369-380
12
Морадпур Д., Пенин Ф., Райс К.М.Репликация вируса гепатита С. Nat Rev Microbiol 2007; 5: 453-463
13
Goffard A, Dubuisson J. Гликозилирование белков оболочки вируса гепатита С. Biochimie 2003; 85: 295-301
14
Deleersnyder V, Pillez A, Wychowski C, Blight K, Xu J, Hahn YS, Rice CM, Dubuisson J. Формирование нативных гликопротеиновых комплексов вируса гепатита С. J Virol 1997; 71: 697-704
15
Виерес Дж., Томас Х, Декамп В., Дюверли Дж., Патель А. Х., Дюбюиссон Дж. Характеристика гликопротеинов оболочки, связанных с инфекционным вирусом гепатита С 2010; Дж. Вирол 84: 10159-10168
16
Куикен Ч., Симмондс П.Номенклатура и нумерация вируса гепатита С. Методы Мол Биол 2009; 510: 33-53
17
Мерфи Д.Г., Виллемс Б., Дешен М., Хилзенрат Н., Муссо Р., Саббах С. Использование анализа последовательности области NS5B для рутинного генотипирования вируса гепатита С со ссылкой на последовательности нетранслируемой области С / Е1 и 5 ’. J Clin Microbiol 2007; 45: 1102-1112
18
Ву С., Канда Т., Накамото С., Цзян Х, Миямура Т., Накатани С.М., Оно С.К., Такахаши-Накагути А., Гоной Т., Ёкосука О.Распространенность субгенотипов 1a и 1b вируса гепатита C у японских пациентов: сверхглубокий анализ секвенирования области, специфичной для генотипа NS5B HCV. PLoS One, 8, e73615
19
Негр Ф., Альберти А. Бремя заражения вирусом гепатита С в мире. Liver Int 2011; 31: Дополнение 2, 1-3
20
Чжао Л., Фэн И, Ся XS. Различные эпидемии и эволюция генотипов ВГС. И Чуань 2012; 34: 666-672
21
Liberto MC, Marascio N, Zicca E, Matera G. Эпидемиологические особенности и особенности инфекции HCV: когортное исследование на базе больниц в университетском медицинском центре региона Калабрия.BMC Infect Dis 2012; 12: Дополнение 2, S4.
22
Панасюк А., Флисиак Р., Мозер-Лисевска I, Адамек А., Тычино М., Халота В., Павловска М., Станьчак Ю., Берак Н., Вавжинович-Сычевска М., Боронь-Качмарска А., Лапиньска Ажесчашич Т.В. , Jabłkowski M, Kryczka W, Zarebska-Michaluk D, Stepień P, Garlicki AM, Kozłowska J, Wiercińska-Drapało A, Zasik E, Mazur W, Dobracka B, Dobracki W, Simon K, Ryzkogratzan J, Pawłzowska J K, Янушкевич-Левандовска Д., Сзенборн Л., Залеска I, Рокитка М., Стравинска Э, Балиновска К., Смиатач Т., Сталке П., Сикорска К., Лакомы А., Здроевски М., Лахович А.Распространение генотипов ВГС в Польше. Przegl Epidemiol 2013; 67, 11-16, 99-103
23
Афзал М.С., Анджум С., Заиди Н.У. Влияние функционального полиморфизма интерлейкина-10 на ответ на терапию пегилированным интерфероном-альфа и рибавирином у пациентов с хроническим гепатитом С, инфицированных генотипом 3a, в популяции Пакистана.Hepat Mon 2014; 13: e10274
24
Анджум С., Али С., Ахмад Т., Афзал М.С., Вахид Ю., Шафи Т., Ашраф М., Андлиб С. Последовательный и структурный анализ 3 ’нетранслируемой области вируса гепатита С, генотип 3а, из пакистанских изолятов.Hepat Mon 2013; 13: e8390
25
Вахид Ю., Саид У., Анджум С., Афзал М.С., Ашраф М. Разработка глобальной согласованной последовательности и анализ высококонсервативных доменов протеина NS5B HCV в Hepat Mon 2012; 12: e6142
26
Сиверт В., Альтраиф I, Разави Х.А., Абдо А., Ахмед Э.А., Аломайр А, Амарапуркар Д., Чен С.Х., Доу Х, Эль-Хаят Х., Эльшазли М., Эсмат Г., Гуан Р., Хан К.Х., Койке К., Ларген А., МакКоган G, Mogawer S, Monis A, Nawaz A, Piratvisuth T, Sanai FM, Sharara AI, Sibbel S, Sood A, Suh DJ, Wallace C, Young K, Negro F.Систематический обзор эпидемиологии вируса гепатита С в Азии, Австралии и Египте. Liver Int 2011; 31: Дополнение 2, 61-80
27
Рэй Р., Мейер К., Банерджи А., Басу А., Коутс С., Абриньяни С., Хоутон М., Фрей С. Е., Белше РБ. Характеристика антител, индуцированных вакцинацией гликопротеинами оболочки вируса гепатита С. J Infect Dis 2010; 202: 862-866
28
Токита Х., Шреста С.М., Окамото Х., Сакамото М., Хорикита М., Иидзука Х, Шреста С., Миякава Ю., Маюми М. Варианты вируса гепатита С из Непала с новыми генотипами и их классификация в третью основную группу.J Gen Virol 1994; 75 (Pt 4): 931-936
29
Tokita H, Okamoto H, Iizuka H, Kishimoto J, Tsuda F, Lesmana LA, Miyakawa Y, Mayumi M. Варианты вируса гепатита C из Джакарты, Индонезия, классифицируются на новые генотипы во втором (2e и 2f), десятом (10a) и одиннадцатая (11а) генетическая группа. J Gen Virol 1996; 77 (Пт 2): 293-301
30
Andre P, Komurian-Pradel F, Deforges S, Perret M, Berland JL, Sodoyer M, Pol S, Brechot C, Paranhos-Baccala G, Lotteau V. Характеристика РНК-содержащих вирусов гепатита C низкой и очень низкой плотности Частицы.J Virol 2002; 76: 6919-6928
31
Нильсен С.У., Бассендин М.Ф., Берт А.Д., Мартин С., Пумихокчай В., Томс Г.Л. Связь между вирусом гепатита С и липопротеинами очень низкой плотности (ЛПОНП) / ЛПНП проанализирована в градиентах плотности йодиксанола. J Virol 2006; 80: 2418-2428
32
Бартош Б., Бух Дж., Менье Дж. К., Гранье С., Энгл Р. Э., Блэквелдер В. С., Эмерсон С. С., Коссет Флорида, Перселл Р. Х. Анализ нейтрализующих антител к вирусу гепатита С in vitro: данные о широко консервативных эпитопах нейтрализации.Proc Natl Acad Sci U S A 2003; 100: 14199-14204
33
Bartosch B, Cosset FL. Поступление в клетки вируса гепатита С. Вирусология 2006; 348: 1-12
34
Бартеншлагер Р. Система репликонов вируса гепатита С: от фундаментальных исследований до клинического применения. J Hepatol 2005; 43: 210-216
35
Lindenbach BD, Evans MJ, Syder AJ, Wölk B, Tellinghuisen TL, Liu CC, Maruyama T., Hynes RO, Burton DR, McKeating JA, Rice CM. Полная репликация вируса гепатита С в культуре клеток.Наука 2005; 309: 623-626
36
Вакита Т., Пичманн Т., Като Т., Дате Т., Миямото М., Чжао З., Мурти К., Хаберманн А., Краусслих Г. Г., Мизоками М., Бартеншлагер Р., Лян Т. Дж.. Производство вируса инфекционного гепатита С в культуре ткани из клонированного вирусного генома. Nat Med 2005; 11: 791-796
37
Чжун Дж., Гастаминза П., Ченг Дж., Кападиа С., Като Т., Бертон Д.Р., Виланд С.Ф., Апричард С.Л., Вакита Т., Чисари Ф.В. Устойчивое заражение вирусом гепатита С in vitro. Proc Natl Acad Sci U S A 2005; 102: 9294-9299
38
Bhattacherjee V, Prescott LE, Pike I, Rodgers B, Bell H, El-Zayadi AR, Kew MC, Conradie J, Lin CK, Marsden H et al.Использование пептидов NS-4 для идентификации типоспецифических антител к генотипам вируса гепатита С 1, 2, 3, 4, 5 и 6. J Gen Virol 1995; 76 (Pt 7): 1737-1748
39
Rapicetta M, Argentini C, Dettori S, Spada E, Pellizzer G, Gandin C. Молекулярная гетерогенность и новые подтипы генотипа 4 HCV. Res Virol 1998; 149: 293-297
40
Симмондс П., Холмс Е.С., Ча Т.А., Чан С.В., Макомиш Ф., Ирвин Б., Билл Е., Яп П.Л., Колберг Дж., Урдя М.С. Классификация вируса гепатита С на шесть основных генотипов и ряд подтипов с помощью филогенетического анализа области NS-5.J Gen Virol 1993; 74 (Пт 11): 2391-2399
41
Симмондс П., Макомиш Ф., Яп П.Л., Чан С.В., Лин С.К., Душейко Г., Саид А.А., Холмс Э.С. Вариабельность последовательностей в 5’-некодирующей области вируса гепатита С: идентификация нового типа вируса и ограничения на разнообразие последовательностей. J Gen Virol 1993; 74 (Пт 4): 661-668
42
Чемберлен Р. У., Адамс Н., Саид А. А., Симмондс П., Эллиотт Р. М.. Полная нуклеотидная последовательность варианта вируса гепатита С 4 типа, преобладающего генотипа на Ближнем Востоке.J Gen Virol 1997; 78 (Pt 6): 1341-1347
43
Тимм Дж., Нойкамм М., Кунцен Т., Ким А.Ю., Чанг Р.Т., Брандер С., Лауэр Г.М., Уокер Б.Д., Аллен Т.М. Характеристика полноразмерных последовательностей генотипа 4 вируса гепатита С. J Viral Hepat 2007; 14: 330-337
44
Ломанн В., Корнер Ф., Кох Дж., Хериан Ю., Тейлманн Л., Бартеншлагер Р. Репликация субгеномных РНК вируса гепатита С в клеточной линии гепатомы. Science 1999; 285: 110-113
45
Блайт К.Дж., Маккитинг Д.А., Маркотриджиано Дж., Райс К.М.Эффективная репликация РНК вируса гепатита С генотипа 1a в культуре клеток. J Virol 2003; 77: 3181-3190
46
Grobler JA, Markel EJ, Fay JF, Graham DJ, Simcoe AL, Ludmerer SW, Murray, EM, Migliaccio G, Flores OA. Идентификация ключевой детерминанты адаптации культуры клеток вируса гепатита С в домене II геликазы NS3. J Biol Chem 2003; 278: 16741-16746
47
Черне DM, Джонс CT, Эванс MJ, Lindenbach BD, McKeating JA, Rice CM. Зависимая от времени и температуры активация вируса гепатита С при низком уровне pH.J Virol 2006; 80: 1734-1741
48
Абе К., Икеда М., Дансако Х., Нака К., Като Н. Адаптивные мутации NS3 в культуре клеток, необходимые для надежной репликации РНК вируса гепатита С длиной генома. Virus Res 2007; 125: 88-97
49
Блайт К.Дж., Колыхалов А.А., Райс СМ. Эффективное инициирование репликации РНК HCV в культуре клеток. Science 2000; 290: 1972-1974
50
Гуо Дж. Т., Бичко В. В., Сигер С. Влияние альфа-интерферона на репликон вируса гепатита С. J Virol 2001; 75: 8516-8523
51
Икеда М, Йи М, Ли К., Лимон С.М.Селектируемые дицистронные РНК субгеномной длины и длины генома, полученные из инфекционного молекулярного клона штамма HCV-N вируса гепатита C, эффективно реплицируются в культивируемых клетках Huh7. J Virol 2002; 76, 2997-3006.
52
Като Т., Дате Т., Миямото М., Фурусака А., Токусиге К., Мизоками М., Вакита Т. Эффективная репликация субгеномного репликона вируса гепатита С генотипа 2а. Гастроэнтерология 2003; 125: 1808-1817
53
Кригер Н., Ломанн В., Бартеншлагер Р. Усиление репликации РНК вируса гепатита С с помощью адаптивных мутаций в культуре клеток.J Virol 2001; 75: 4614-4624
54
Maekawa S, Enomoto N, Sakamoto N, Kurosaki M, Ueda E, Kohashi T., Watanabe H, Chen CH, Yamashiro T., Tanabe Y, Kanazawa N, Nakagawa M, Sato C, Watanabe M. Введение мутаций NS5A позволяет создавать субгеномные репликоны HCV. полученный из изолята HC-J4, инфицированного шимпанзе, для эффективной репликации в клетках Huh-7. J Viral Hepat 2004; 11: 394-403
55
Mori K, Abe K, Dansako H, Ariumi Y, Ikeda M, Kato N. Новая эффективная система репликации с геномом вируса гепатита C, полученным от пациента с острым гепатитом C.Biochem Biophys Res Commun 2008; 371: 104-109
56
Йи М, Бодола Ф, Лимон С.М. Субгеномные репликоны вируса гепатита С, индуцирующие экспрессию секретируемого ферментативного репортерного белка. Вирусология 2002; 304: 197-210
57
Саид М., Шил Т.К., Готвейн Дж. М., Марукиан С., Дастин Л. Б., Бух Дж., Райс К. М.. Эффективная репликация репликонов вируса гепатита C генотипов 3a и 4a в клетках гепатомы человека. Противомикробные агенты Chemother 2012; 56: 5365-5373
58
Bartosch B, Dubuisson J, Cosset FL.Псевдочастицы вируса инфекционного гепатита С, содержащие функциональные комплексы белков оболочки E1-E2. J Exp Med 2003; 197: 633-642
59
Сюй М., Чжан Дж., Флинт М., Логвинов К., Ченг-Майер К., Райс С.М., Маккитинг Дж. Гликопротеины вируса гепатита С опосредуют pH-зависимое проникновение в клетку ретровирусных частиц, обладающих определенным значением. Proc Natl Acad Sci U S A 2003; 100: 7271-7276
60
Lavillette D, Tarr AW, Voisset C, Donot P, Bartosch B, Bain C, Patel AH, Dubuisson J, Ball JK, Cosset FL.Характеристика диапазона хозяев и свойств входа в клетки основных генотипов и подтипов вируса гепатита С. Гепатология 2005; 41: 265-274
61
McKeating JA, Zhang LQ, Logvinoff C, Flint M, Zhang J, Yu J, Butera D, Ho DD, Dustin LB, Rice CM, Balfe P. Различные гликопротеины вируса гепатита C опосредуют вирусную инфекцию CD81-зависимым образом. J Virol 2004; 78: 8496-8505
62
Meunier JC, Engle RE, Faulk K, Zhao M, Bartosch B, Alter H, Emerson SU, Cosset FL, Purcell RH, Bukh J.Доказательства кросс-генотипической нейтрализации псевдочастиц вируса гепатита С и повышения инфекционности аполипопротеином C1. Proc Natl Acad Sci U S A 2005; 102: 4560-4565
63
Гао М., Крапива Р.Э., Белема М., Снайдер Л. Б., Нгуен В. Н., Фриделл Р. А., Серрано-Ву М. Х., Лэнгли Д. Р., Сан Дж. Х., О’Бойл Д. Р. 2-й, Лемм Дж. А., Ван С., Книп Дж. Грасела Д.М., Меанвелл Н.А., Хаманн Л.Г. Стратегия химической генетики определяет ингибитор NS5A HCV с сильным клиническим эффектом. Природа 2010; 465: 96-100
64
Lindenbach BD, Evans MJ, Syder AJ, Wölk B, Tellinghuisen TL, Liu CC, Maruyama T., Hynes RO, Burton DR, McKeating JA, Rice CM.Полная репликация вируса гепатита С в культуре клеток. Наука 2005; 309: 623-626
65
Scheel TK, Gottwein JM, Mikkelsen LS, Jensen TB, Bukh J. Рекомбинантные варианты HCV с NS5A генотипов 1-7 имеют разную чувствительность к ингибитору NS5A, но не к интерферону-альфа. Гастроэнтерология 2011; 140: 1032-1042
66
Имхоф I, Симмондс П. Разработка метода культивирования межгенотипных клеток вируса гепатита С (ВГС) для оценки противовирусной чувствительности и развития устойчивости генов протеазы ВГС NS3 из генотипов 1-6 ВГС.J Virol 2010; 84: 4597-4610.
67
Вакита Т., Пичманн Т., Като Т., Дате Т., Миямото М., Чжао З., Мурти К., Хаберманн А., Краусслих Г. Г., Мизоками М., Бартеншлагер Р., Лян Т. Дж.. Производство вируса инфекционного гепатита С в культуре ткани из клонированного вирусного генома. Nat Med 2005; 11: 791-796.
68
Scheel TK, Gottwein JM, Jensen TB, Prentoe JC, Hoegh AM, Alter HJ, Eugen, Olsen J, Bukh J. Разработка систем культивирования клеток на основе JFh2 для генотипа 4a вируса гепатита С и доказательства нейтрализации перекрестного генотипа.Proc Natl Acad Sci U S A 2008; 105: 997-1002
69
Gottwein JM, Jensen TB, Mathiesen CK, Meuleman P, Serre SB, Lademann JB, Ghanem L, Scheel TK, Leroux-Roels G, Bukh J. Разработка и применение репортерных вирусов гепатита C с генотипом 1-7, неструктурный белок 2 (NS2), экспрессирующие флуоресцентные белки или люциферазу в модифицированном JFh2 NS5A. J Virol 2011; 85: 8913-8928
70
Боуэн Д.Г., Уокер СМ. Мутационный уход от CD8 + Т-клеточного иммунитета: эволюция ВГС от шимпанзе к человеку.J Exp Med 2005; 201: 1709-1714
71
Meuleman P, Libbrecht L, De Vos R, de Hemptinne B, Gevaert K, Vandekerckhove J, Roskams T. и Leroux-Roels G. Морфологическая и биохимическая характеристика печени человека в химере мышей uPA-SCID. Гепатология 2005; 41: 847-856
72
Рим Дж. А., Сандгрен Е. П., Пальмитер Р. Д., Бринстер Р. Л.. Полное восстановление печени мыши ксеногенными гепатоцитами. Proc Natl Acad Sci U S A 1995 92: 4942-4946
73
Мерсер Д.Ф., Шиллер Д.Ф., Эллиотт Дж. Ф., Дуглас Д. Н., Хао С., Ринфрет А., Аддисон В. Р., Фишер К. П., Черчилль Т. А., Лейки Дж. Р., Тиррелл Д. Л., Кнетеман Н. М..Репликация вируса гепатита С у мышей с химерной печенью человека. Nat Med 2001; 7: 927-933
74
Биссиг К.Д., Виланд С.Ф., Тран П., Исогава М., Ле Т.Т., Чисари Ф.В., Верма И.М. Химерные мыши с печенью человека представляют собой модель инфицирования и лечения вирусами гепатита B и C. J Clin Invest 2010; 120: 924-930
75
Хирага Н., Имамура М., Цуге М., Ногучи К., Такахаши С., Ивао Е., Фудзимото Ю., Абэ Х, Маэкава Т., Очи Х, Татено С., Йошизато К., Сакаи А., Сакаи Й, Хонда М, Канеко С., Вакита Т. , Чаяма К.Заражение химерных гепатоцитов мыши вирусом гепатита С, созданным методами генной инженерии, и его чувствительность к интерферону. FEBS Lett 2007; 581: 1983–1987
76
Кимура Т., Имамура М., Хирага Н., Хатакеяма Т., Мики Д., Ногучи К., Мори Н., Цуге М., Такахаши С., Фудзимото И., Ивао Е., Очи Х., Абэ Х, Маэкава Т., Аратаки К., Татено К., Йошизато К. , Вакита Т., Окамото Т., Мацуура Ю., Чаяма К. Создание клона вируса гепатита С инфекционного генотипа 1b у химерных мышей с гепатоцитами человека.J Gen Virol 2008; 89: 2108-2113
77
Moucari R, Ripault MP, Martinot-Peignoux M, Voitot H, Cardoso AC, Stern C, Boyer N, Maylin S, Nicolas-Chanoine MH, Vidaud M, Valla D, Bedossa P, Marcellin P. Инсулинорезистентность и географическое происхождение: основные предикторы фиброза печени и ответа на пегинтерферон и рибавирин при ВГС-4. Gut 2009; 58: 1662-1669
78
Эсмат Г., Эль-Кассас М., Хассани М., Гамил М.Э., Эль-Разики М. Как оптимизировать терапию ВГС у пациентов с генотипом 4.Liver Int 2013; 33 Дополнение 1: 41-45
79
Камаль С.М., Эль Камари С.С., Шарделл, доктор медицины, Хашем М., Ахмед И.Н., Мухаммади М., Сайед К., Мустафа А., Хакем С.А., Ибрахием А., Монием М., Мансур Н., Абдельазиз М. Пегилированный интерферон альфа 2b плюс рибавирин у пациентов с генотипом 4 хронический гепатит C: роль быстрого и раннего вирусологического ответа. Гепатология 2007; 46: 1732-1740
80
Salomon JA, Weinstein MC, Hammitt JK и Goldie SJ. Экономическая эффективность лечения хронической инфекции гепатита С у меняющейся популяции пациентов.JAMA 2003; 290: 228-237
81
Fan X, Mao Q, Zhou D, Lu Y, Xing J, Xu Y, Ray SC, Di Bisceglie AM. Высокое разнообразие квазивидов вируса гепатита С связано с ранним вирусологическим ответом у пациентов, получающих противовирусную терапию. Гепатология 2009; 50: 1765-1772
82
Абдо А.А., Аль-Ахдал М.Н., Халид С.С., Хельми А., Санаи Ф.М., Альсват К., Аль-Хамуди В., Али С.М., Аль-Ашгар Н.И., Аль-Мдани А. и др. Полиморфизм IL28B позволяет прогнозировать вирусологический ответ на стандартную терапию у пациентов с хронической инфекцией вируса гепатита С генотипа 4.Hepatol Int 2013; 7: 533-538
83
Эль-Шами А, Шоджи I, Эль-Акель В., Биласи С.Е., Денг Л., Эль-Разики М., Цзян Д.П., Эсмат Г., Хотта Х. Гетерогенность последовательности NS5A вируса гепатита С генотипа 4а предсказывает клинический исход пегилированного интерферона. лечение рибавирином у египетских пациентов. J Clin Microbiol 2012; 50: 3886-3892
84
Шейкер О.Г., Садик Н.А. Полиморфизмы генов интерлейкина-10 и интерлейкина-28B у египетских пациентов с генотипом 4 вируса хронического гепатита С и их влияние на ответ на терапию пегилированным интерфероном / рибавирином.J Gastroenterol Hepatol, 2012; 27: 1842-1849
85
Хименес-Соуза М.А., Фернандес-Родригес А., Гусман-Фульхенсио М., Гарсия-Альварес М., Ресино С. Мета-анализ: влияние полиморфизма интерлейкина-28B на спонтанный и связанный с лечением клиренс у пациентов с гепатитом С. BMC Med 2013; 11: 6.
86
Fortunato G, Calcagno G, Bresciamorra V, Salvatore E, Filla A, Capone S, Liguori R, Borelli S, Gentile I, Borrelli F, Borgia G, Sacchetti L. Множественный склероз и вирусная инфекция гепатита С связаны с однонуклеотидными полиморфизмами в гены пути интерферона.J Interferon Cytokine Res 2008; 28: 141-152
87
Папастергиу В., Димитроулопулос Д., Скорда Л., Лисгос П., Кетикоглу И., Костас Н., Каратапанис С. Предикторы устойчивого вирусологического ответа у греческих и египетских пациентов с генотипом 4 гепатита С: имеет ли значение этническая принадлежность? J Med Virol 2012; 84: 1217-1223
88
Димитроулопулос Д., Элефсиниотис I, Павлидис С., Ксинопулос Д., Цамакидис К., Пацавела С., Кипреос Д., Фердеригу А., Корколис Д., Кутсунас С. и др. Европейский vs.Пациенты из Египта с HCV-4 с повышенным исходным уровнем РНК HCV, получавшие PEG-IFN-alpha2a и рибавирин: роль быстрого и раннего вирусологического ответа. Гепат Пн 10: 193-198
89
Roulot D, Bourcier V, Grando V, Deny P, Baazia Y, Fontaine H, Bailly F, Castera L, De Ledinghen V, Marcellin P, Poupon R, Bourlière M, Zarski JP, Roudot-Thoraval F; Наблюдательная исследовательская группа VHC4. Эпидемиологические характеристики и ответ на лечение пегинтерфероном и рибавирином инфекции вируса гепатита С генотипа 4.J Viral Hepat 2007; 14: 460-467
90
Gad RR, Males S, El Makhzangy H, Shouman S, Hasan A, Attala M, El Hoseiny M, Zalata K, Abdel-Hamid M, Fontanet A, Mohamed MK, Esmat G. Предикторы устойчивого вирусологического ответа у пациентов с генотипом 4 хронический гепатит C. Liver Int 2008; 28: 1112-1119
91
Икеда К., Сайто С., Сузуки И., Кобаяши М., Цубота А., Койда И., Арасе Y, Фукуда М., Чайама К., Мурашима Н., Кумада Х. Прогрессирование заболевания и гепатоцеллюлярный канцерогенез у пациентов с хроническим вирусным гепатитом: проспективное наблюдение за 2215 пациенты.J Hepatol 1998; 28: 930-938
92
Haller O, Frese M, Kochs G. Mx белки: медиаторы врожденной устойчивости к РНК-вирусам. Rev Sci Tech 1998; 17: 220-230
93
Мохамед А.А., Нада Огайо, Эль-Десуки Массачусетс. Роль количественной оценки гена протеинкиназы R в гепатоканцерогенезе, индуцированном генотипом 4 вируса гепатита С. Diagn Pathol 2012; 7: 103
94
Пичманн Т., Кауль А., Кутсудакис Г., Шавинская А., Каллис С., Штайнманн Э., Абид К., Негр Ф., Дре М., Коссет Ф., Бартеншлагер Р.Конструирование и характеристика инфекционных внутригенотипических и межгенотипических химер вируса гепатита С. Proc Natl Acad Sci U S A 2006; 103: 7408-7413
95
Dreux M, Pietschmann T, Granier C, Voisset C, Ricard-Blum S, Mangeot PE, Keck Z, Foung S, Vu-Dac N, Dubuisson J, Bartenschlager R, Lavillette D, Cosset FL. Липопротеин высокой плотности подавляет антитела, нейтрализующие вирус гепатита С, за счет стимуляции проникновения клеток через активацию рецептора скавенджера BI. J Biol Chem 2006; 281: 18285-18295
96
Менье Дж. К., Рассел Р. С., Гуссенс В., Прием С., Уолтер Х., Депла Е., Юнион А., Фолк К. Н., Бух Дж., Эмерсон С. С., Перселл Р. Х.Выделение и характеристика широко нейтрализующих человеческих моноклональных антител к гликопротеину e1 вируса гепатита С. J Virol 2008; 82: 966-973
97
Фарси П., Шимода А., Вонг Д., Кабезон Т., Де Джиоаннис Д., Страззера А., Симидзу Ю., Шапиро М., Альтер Х.Дж., Перселл Р.Х. Профилактика заражения вирусом гепатита С у шимпанзе с помощью гипериммунной сыворотки против гипервариабельной области 1 белка оболочки 2. Proc Natl Acad Sci U S. A 1996; 93 15394-15399
98
Халик С., Латиф Н., Джахан С.Роль различных участков генома вируса гепатита С в терапевтическом ответе на лечение интерфероном. Arch Virol 2014; 159 (1): 1-15
99
Койке К. Вирус гепатита С участвует в гепатоканцерогенезе, модулируя метаболические и внутриклеточные сигнальные пути. J Gastroenterol Hepatol 2007; 22 Приложение 1: S108-111.
100
Абу-Альфа ГК. Гепатоцеллюлярная карцинома: молекулярная биология и терапия. Семин Онкол 2006; 33: S79-83
101
Ryu SH, Fan X, Xu Y, Elbaz T, Zekri AR, Abdelaziz AO, Di Bisceglie AM.Отсутствие связи между генотипами и подтипами ВГС и возникновением гепатоцеллюлярной карциномы в Египте. J Med Virol 2009; 81: 844-847
102
Сарма М.П., Асим М., Медхи С., Бхарати Т., Кар П. Гепатоцеллюлярная карцинома, связанная с вирусом гепатита С: исследование случай-контроль из Индии. J Med Virol 2012; 84: 1009-1017
103
Мория К., Накагава К., Санта Т, Синтани И, Фуджи Х, Миёси Х, Цуцуми Т, Миядзава Т, Ишибаши К., Хори Т, Имаи К., Тодороки Т, Кимура С., Коике К.Окислительный стресс в отсутствие воспаления на мышиной модели гепатоканцерогенеза, связанного с вирусом гепатита С. Cancer Res 2001; 61: 4365-4370
104
Койке К., Мория К. Метаболические аспекты вирусной инфекции гепатита С: стеатогепатит, напоминающий НАСГ, но отличающийся от него. J Gastroenterol 2005; 40: 329-336
105
Tsutsumi T, Suzuki T, Moriya K, Yotsuyanagi H, Shintani Y, Fujie H, Matsuura, Y, Kimura S, Koike K, Miyamura T. Изменение внутрипеченочной экспрессии цитокинов и активация AP-1 у трансгенных мышей, экспрессирующих ядерный белок вируса гепатита C. .Вирусология 2002; 304: 415-424
106
Зекри А.Р., Ашур М.С., Хассан А., Алам Эль-Дин Х.М., Эль-Шехаби А.М., Абу Шади М.А. Цитокиновый профиль египетского вируса гепатита С генотипа-4 в зависимости от прогрессирования заболевания печени. World J Gastroenterol 2005; 11: 6624-6630
107
Цуцуми Т., Сузуки Т., Шимоике Т., Сузуки Р., Мория К., Шинтани И., Фуджи Х, Мацуура Ю., Койке К., Миямура Т. Взаимодействие основного белка вируса гепатита С с ретиноидным рецептором Х-альфа модулирует его транскрипционную активность.Гепатология 2002; 35: 937-946
Рецензенты: Муначика Эндодзи, доктор медицинских наук, Центр здравоохранения, Университет Фукуока, 8-19-1 Нанакума, Джонан-ку, Фукуока 814-0180, Япония; Иван Джентиле, Департамент общественной медицины и социального обеспечения — Отдел инфекционных болезней (изд. 18), Неаполитанский университет «Федерико II», через С. Пансини, 5- I-80131 Неаполь Италия.
проблем в лечении вируса гепатита C генотипа 3
В Соединенных Штатах от 3 до 4 миллионов человек страдают хронической инфекцией вируса гепатита С (ВГС). 1 Среди 6 известных генотипов ВГС генотип 1 (GT1) является наиболее распространенным и составляет три четверти случаев. 1 От 13% до 15% случаев ВГС относятся к генотипу 2 (GT2) и примерно 10% — к генотипу 3 (GT3). 2,3 В глобальном масштабе распределение отличается: на ВГС GT3 приходится 75% инфекций ВГС в Южной Азии, 25% в Западной Европе и от 10% до 20% всех инфекций ВГС в Северной Америке. 4
Ранние клинические испытания монотерапии интерфероном (IFN) или IFN плюс рибавирин показали, что пациентов с GT2 и GT3 легче вылечить, чем пациентов с GT1. 5-7 Однако в этих ранних испытаниях схем на основе ИФН пациенты с GT2 и GT3 были сгруппированы вместе и представлены объединенные данные об исходах. 4 Когда в клинических испытаниях новых противовирусных препаратов прямого действия (DAA), не содержащих IFN, результаты оценивались по генотипам, результаты опровергли общепринятые представления и показали, что GT3 на самом деле было труднее вылечить, чем другие генотипы. 2,4
Устойчивый вирусологический ответ (УВО), определяемый как «уровень РНК ВГС ниже порога количественной оценки» 4 , сохраняющийся в течение 12–24 недель после окончания лечения, считается прогностическим фактором излечения.В клинических испытаниях препарата ПППД софосбувир плюс рибавирин только от 30% до 60% пациентов с GT3 имели УВО после 12–16 недель терапии по сравнению с 95% пациентов с GT2. 2,3 Данные показали, что пациенты с ВГС GT3 имеют более быстрое прогрессирование фиброза и более высокие показатели цирроза, тяжелого стеатоза и гепатоцеллюлярной карциномы. 2,4 Стеатоз связан с более высокой вирусной нагрузкой, а цирроз указывает на более низкую вероятность излечения у пациентов, не получавших лечение, что может помочь объяснить более низкие показатели УВО у пациентов с GT3 по сравнению с другими генотипами HCV. 4 Действительно, когда УВО у пациентов с GT3 стратифицирован в соответствии с наличием компенсированного цирроза или предшествующей неудачи лечения, ранее нелеченные пациенты и пациенты без цирроза с гораздо большей вероятностью достигают УВО при терапии ПППД. 4
Обновленные инструкции для GT3 HCV
Наивные пациенты без цирроза печени
Для не лечившихся пациентов с GT3, у которых нет цирроза, недавно обновленные совместные рекомендации Американского общества инфекционных болезней (IDSA) и Американской ассоциации по изучению заболеваний печени (AASLD) рекомендуют начинать с 8-недельного курса. Мавырет (глекапревир 300 мг / сут + пибрентасвир 120 мг / сут) или 12-недельным курсом эпклуса (софосбувир 400 мг / сут + велпатасвир 100 мг / сут). 8 Mavyret и Epclusa представляют собой комбинированные пероральные таблетки с фиксированной дозой.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США одобрило Mavyret в августе 2017 года для лечения ВГС GT1 — GT6 на основании положительных результатов ENDURANCE-3, рандомизированного исследования фазы 3 с участием не получавших лечения пациентов с ВГС GT3, у которых на момент включения не было цирроза. 9 Пациенты были случайным образом распределены 2: 1 на группу Mavyret (n = 233) или на софосбувир / даклатасвир (n = 115) в течение 12 недель. Позже в исследование была добавлена открытая группа, в которую вошли 157 пациентов, получавших Mavyret в течение 8 недель. 9 Частота УВО12 составила 95% (95% ДИ, 93-98%) в группе 12-недельного Мавырета, 97% (95% ДИ, 91-99%) в группе софосбувира / даклатасвира и 95%. % (95% ДИ, 91% -99%) в 8-недельной группе Mavyret, которые были статистически эквивалентны. 9 Обратите внимание, что результаты исследования ENDURANCE-3 еще не опубликованы в рецензируемом журнале. Хотя показатели УВО в ENDURANCE-3 намного лучше, чем показатели УВО, наблюдавшиеся в более ранних исследованиях софосбувира / рибавирина у пациентов с GT3, они все еще отстают от показателей SVR12 для пациентов с HCV с GT1 или GT2.В исследованиях Mavyret фазы 2 SURVEYOR-I и SURVEYOR-II, SVR12 варьировался от 97% до 100% у пациентов с GT1 и от 96% до 100% у пациентов с GT2 по сравнению с 83% до 94% у пациентов с GT3. 10
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США одобрило Epclusa в июне 2016 года для пациентов с ВГС GT3 с циррозом или без него на основе результатов рандомизированного контролируемого исследования ASTRAL-3 фазы 3 (N = 558). 11 Примерно 75% пациентов не получали лечения, а остальные пациенты ранее получали схему на основе ИФН.Пациентам случайным образом назначали Epclusa в течение 12 недель или софосбувир / рибавирин в течение 24 недель. 11 Частота УВО12 составила 95% (95% ДИ, 92–98%) в группе Epclusa по сравнению с 80% (95% ДИ, 75–85%) в группе софосбувира / рибавирина. 11 В исследование ASTRAL-2 были включены пациенты с GT2 и сообщалось о частоте УВО12 99% (95% ДИ, 96–100%). 11
Показатель излечения от гепатита С превышает 90% среди пациентов с трудно поддающимся лечению генотипом 3
Пациенты с гепатитом С с трудно поддающимся лечению генотипом 3 показали устойчивый вирусологический ответ (УВО) более 90% в реальных условиях. исследование жизни терапии, основанной на противовирусном препарате прямого действия (DAA) софосбувир (Sovaldi, Gilead Sciences Inc.)
Генотип 3 HCV был связан с повышенным риском развития цирроза и гепатоцеллюлярной карциномы (HCC) по сравнению с другими версиями вируса, как показали предыдущие исследования.
«Инфекция вируса хронического гепатита С (HCV) генотипа 3 с запущенной болезнью печени оказалась наиболее сложной для лечения», — исследователи под руководством Олава Далгарда (на фото), доктора медицины, доктора философии. в больнице Университета Акерсхус в Осло, Норвегия, — отмечается в их исследовании.
Группа исследователей из Норвегии, Дании, Финляндии и Швеции выбрала пациентов из этих четырех стран для ретроспективного когортного исследования.Согласно исследованию, около 100 000 человек в Скандинавии инфицированы ВГС, и половина из них имеет генотип 3.
«Генотип 3 распространен по всей Скандинавии и в Великобритании», — сказал Далгард в электронном письме журналу MD Magazine. «Мы не знаем почему, но генотип 3 берет свое начало в Южной Азии, а в Великобритании, Норвегии и Дании есть большие популяции иммигрантов из Пакистана».
Лишь в нескольких исследованиях сообщалось об эффекте лечения на основе софосбувира у пациентов с генотипом 3 с прогрессирующим заболеванием печени в реальных условиях, говорят авторы.
«Наша статья важна во всем мире, потому что она показывает, что очень хорошие показатели УВО могут быть достигнуты с помощью доступных лекарств даже у пациентов с декомпенсированным циррозом печени и инфекцией генотипа 3», — сказал Далгард.
Команда выбрала для исследования пациентов в возрасте 18 лет и старше, получивших по крайней мере одну дозу софосбувира. Те, кто перенесли трансплантацию органов или были инфицированы гепатитом B (HBV) или вирусом иммунодефицита человека (ВИЧ), были исключены. Всего было отобрано 316 пациентов, и 311 были включены в популяцию с модифицированным намерением лечить (miTT).
Группе давали софосбувир в различных комбинациях с другими препаратами. Комбинации включали софосбувир с рибавирином, даклатасвир (Daklinza, Bristol-Myers Squibb), ледипасвир (Harvoni, Gilead) или пегилированный интерферон альфа (peg-IFN-α). Назначенное лечение зависело от национальных рекомендаций и доступности.
Показатели УВО через 12 недель были одинаковыми для всех схем лечения, как показало исследование. У мужчин показатель излечения был ниже (89%), чем у женщин (97%). Пациенты с циррозом печени оказались хуже, чем те, у кого не было рубцевания печени, на 90% против 96%.У пациентов с декомпенсированным циррозом была более низкая частота УВО12, чем у лиц с компенсированным заболеванием печени — 82% по сравнению с 94%. Точно так же увеличение жесткости печени было связано со снижением шансов достижения УВО, пишут авторы.
Однако результаты следует интерпретировать с осторожностью, поскольку, согласно документу, внешний мониторинг данных не проводился. Даже в этом случае данные, полученные в реальных условиях, дополняют информацию, полученную в результате рандомизированных клинических испытаний, говорят исследователи.

 м. н., профессор, специализация – лечение вирусных гепатитов, автор более 70 публикаций, в том числе 7 учебно-методических пособий и 56 научных работ. Член Международного общества по изучению инфекционных болезней (International Society for Infectious Diseases (ISID)).
м. н., профессор, специализация – лечение вирусных гепатитов, автор более 70 публикаций, в том числе 7 учебно-методических пособий и 56 научных работ. Член Международного общества по изучению инфекционных болезней (International Society for Infectious Diseases (ISID)).
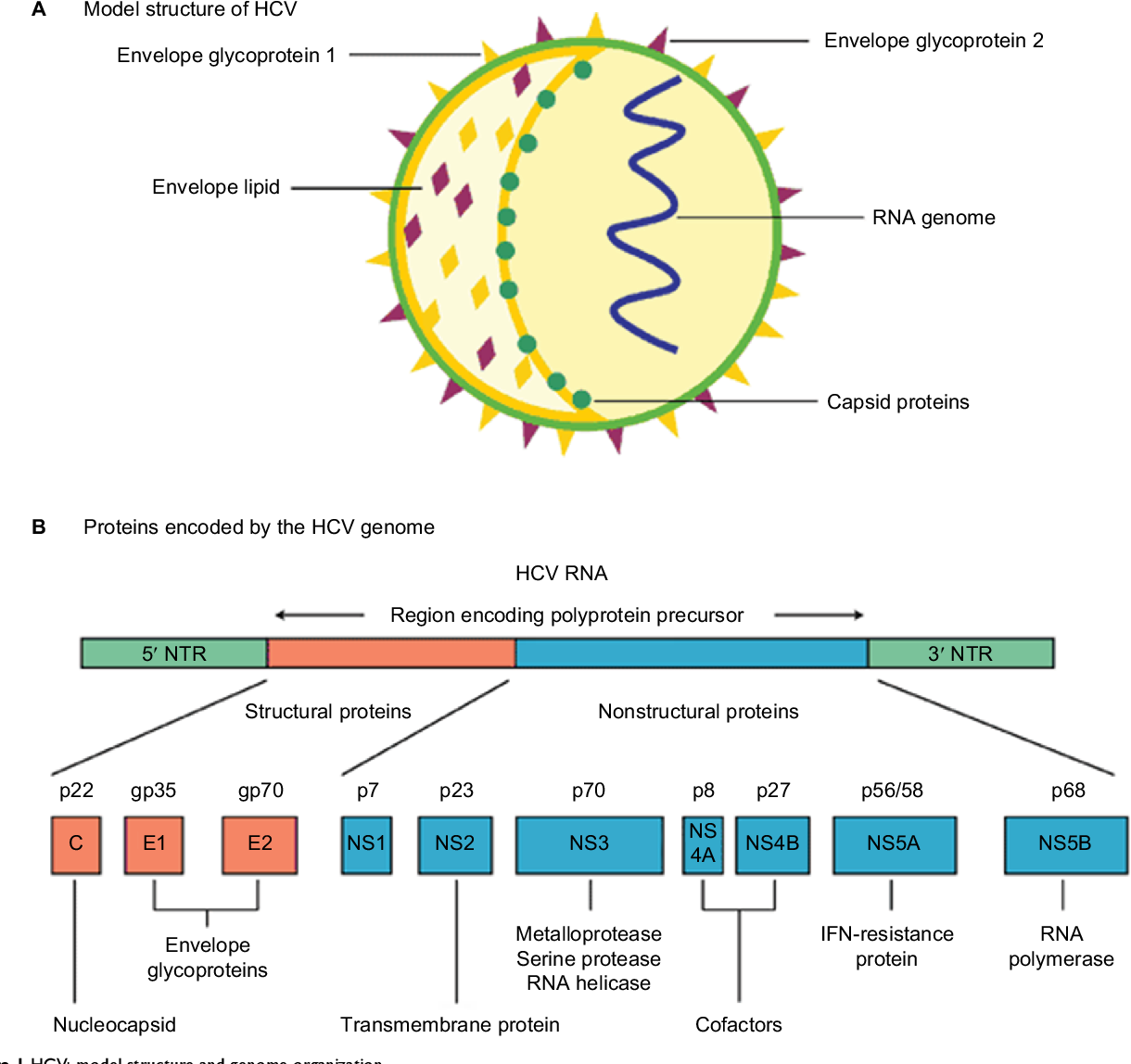 Санкт-Петербурга, член-корреспондент РАН Константин Жданов. – Он поражает не только печень, но и другие органы и системы организма, нередко являясь причиной таких серьезных патологий, как сахарный диабет, злокачественные новообразования, сердечно-сосудистые заболевания и другие. Поэтому сегодня во всем мире подчеркивается важность раннего начала лечения хронического гепатита С для предотвращения развития этих заболеваний».
Санкт-Петербурга, член-корреспондент РАН Константин Жданов. – Он поражает не только печень, но и другие органы и системы организма, нередко являясь причиной таких серьезных патологий, как сахарный диабет, злокачественные новообразования, сердечно-сосудистые заболевания и другие. Поэтому сегодня во всем мире подчеркивается важность раннего начала лечения хронического гепатита С для предотвращения развития этих заболеваний».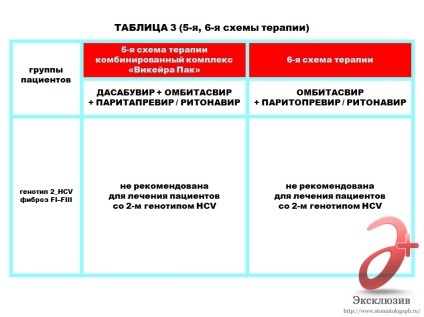 При этом во время лечения пациентам уже не приходится часто обращаться к специалисту для контроля процесса терапии, как раньше. Дополнительное преимущество пангенотипных схем – упрощение диагностики. Короткий 8-недельный курс позволяет вылечить больше пациентов при сокращении нагрузки на систему здравоохранения».
При этом во время лечения пациентам уже не приходится часто обращаться к специалисту для контроля процесса терапии, как раньше. Дополнительное преимущество пангенотипных схем – упрощение диагностики. Короткий 8-недельный курс позволяет вылечить больше пациентов при сокращении нагрузки на систему здравоохранения». Для этого компания разработала препараты, направленные на ускорение элиминации ХГС.
Для этого компания разработала препараты, направленные на ускорение элиминации ХГС.