Микоз туловища — симптомы (признаки), лечение, лекарства
Раздел предназначен исключительно для медицинских и фармацевтических работников! Если Вы не являетесь медицинским и фармацевтическим работником — покиньте раздел! Условия использования
- Номер класса:
- I
- Наименование класса:
- Некоторые инфекционные и паразитарные болезни
- Номер блока:
- B35-B49
- Наименование блока:
- Микозы
- Код заболевания:
- B35.4
МИКРОСПОРИЯ — грибковое заболевание кожи и волос. Болеют главным образом дети. Различают антропонозную и зооантропонозную микроспорию. Антропонозная микроспория в нашей стране очень редка. Возбудители — антропофильные микроспорумы (Microsporon fen-ugineum) — поражают роговой спой эпидермиса и волосы; отличаются высокой контагиозностью.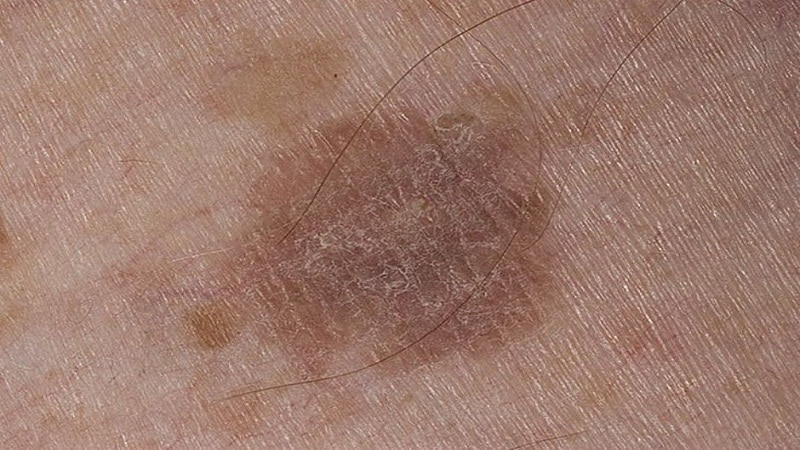 Источник — больной человек. Пути передачи — прямой и опосредованный (через головные уборы, щетки, расчески, одежду, игрушки и другие предметы).
Источник — больной человек. Пути передачи — прямой и опосредованный (через головные уборы, щетки, расчески, одежду, игрушки и другие предметы).
Зооантропонозная микроспория-частый микоз. Возбудители — зоофильные микроспорумы (в нашей стране М. canis) — поражают роговой слой и волосы; по контагиознос-ти уступают антропофильным. Источники — кошки (особенно котята), реже собаки. Пути передачи — прямой (основной) и опосредованный (через предметы, загрязненные волосами или чешуйками, содержащими М. canis). Относительно редко инфицирование происходит от больного человека.
Клиническая картина. Проявления антропонозной и зооантропонозной микроспории однотипны и сходны с поверхностной трихофитией, в отличие от которой для нее характерны: более четкие границы, округлые очертания, крупные размеры очагов поражения на волосистой части головы;
обламывание (обычно сплошное) волос на уровне 6-8 мм;
наличие вокруг «пеньков» беловатых чехлов; отсутствие черных точек; на гладкой коже — множественные очаги; почти постоянное вовлечение пушковых волос, нередкое увеличение заушных, затылочных и шейных лимфатических узлов. Возможны изменения по типу инфильтративно-нагноительной трихофитии.
Возможны изменения по типу инфильтративно-нагноительной трихофитии.
Диагноз микроспории всегда должен быть подтвержден лабораторными исследованиями (микроскопия, посев пораженных волос или чешуек кожи). Важное значение имеет люминесцентная диагностика (осмотр под лампой Вуда).
Лечение проводят в стационаре. Внутрь — гризеофульвин, низорал; местно-йодно-мазевая терапия, микозолон.
Прогноз благоприятный.
Профилактика. Изоляция больных детей; осмотр всех контактировавших с больным (включая домашних животных) с использованием лампы Вуда; отлов бездомных кошек и собак.
Администрация сайта не осуществляет деятельность в сфере медицинских услуг. Консультации и рекомендации носят лишь информационный характер и не являются полноценной медицинской помощью. Любая медицинская помощь осуществляется только в специализированных медицинских учреждениях. При любых недомоганиях обратитесь к врачу.
Микозы кистей, стоп и туловища
Микозы кистей, стоп и туловища — Клинические рекомендации
Этиология и эпидемиология
Наиболее частыми возбудителями дерматофитий являются патогенные грибы Trichophyton rubrum (90%) и Trichophyton mentagrophytes, interdigitale. Реже эти заболевания вызываются Epidermophyton floccosum и грибами рода Candida
interdigitale. Реже эти заболевания вызываются Epidermophyton floccosum и грибами рода Candida
Заражение патогенными грибами может происходить при непосредственном контакте с больным,
межпальцевых складок,
кровообращения
при сосудистых заболеваниях конечностей и др.
Микозы могут приобретать распространенный характер при наличии сопутствующих заболеваний — эндокринных,
крови,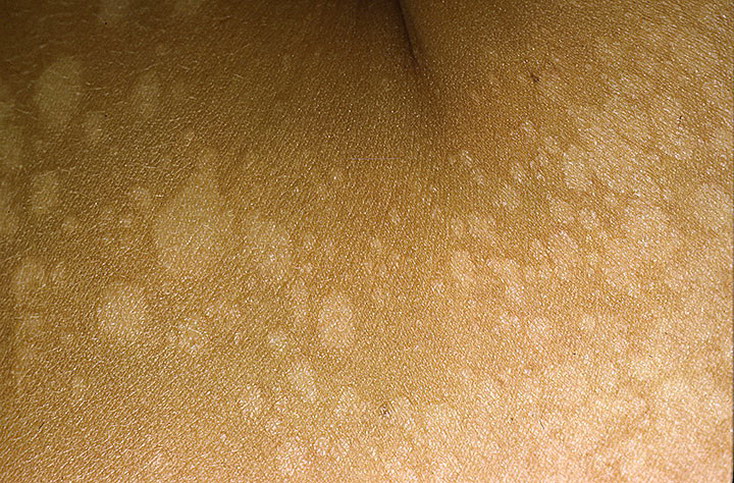
В настоящее время микоз стоп,
Классификация
- В35.1 Микоз ногтей
- В35.2 Микоз кистей
- В35.3 Микоз стоп
- В35.4 Микоз туловища
- В35.6 Эпидермофития паховая
- В37.2 Кандидоз кожи и ногтей
Микоз стоп
Сквамозно-гиперкератотическая форма микоза стоп
Известна таже как мокасиновый тип микоза стоп (Tinea Pedis Moccasin Type).Характеризуется наличием шелушения на коже межпальцевых складок, Обычно пораженные участки
Обычно пораженные участки
кожи имеют
слабовыраженную воспалительную
окраску и покрыты мелкими отрубевидными или муковидными чешуйками. Шелушение в кожных бороздах создает утрированный рисунок,
Интертригинозная форма микоза стоп
Известна также как межпальцевый тип микоза стоп ( Tinea Pedis Interdigital Type).Для этой формы характерно появление мацерации и трещин в межпальцевых складках,
В межпальцевых складках на фоне отека и гиперемии формируется четко отграниченный участок мацерированной и эрозированной кожи. Высыпания в виде эрозий и глубоких трещин, В ряде случаев наблюдаются пузырьковые высыпания.Субъективно отмечаются зуд,
В ряде случаев наблюдаются пузырьковые высыпания.Субъективно отмечаются зуд,
Дисгидротическая форма микоза стоп
Известна также как воспалительный тип микоза стоп ( Tinea Pedis Inflammatory Type).Проявляется многочисленными пузырьками с толстой покрышкой,
розово-красного
цвета. Обычно пузырьки располагаются на неизмененной коже; при нарастании воспалительных явлений присоединяются гиперемия и отечность кожи,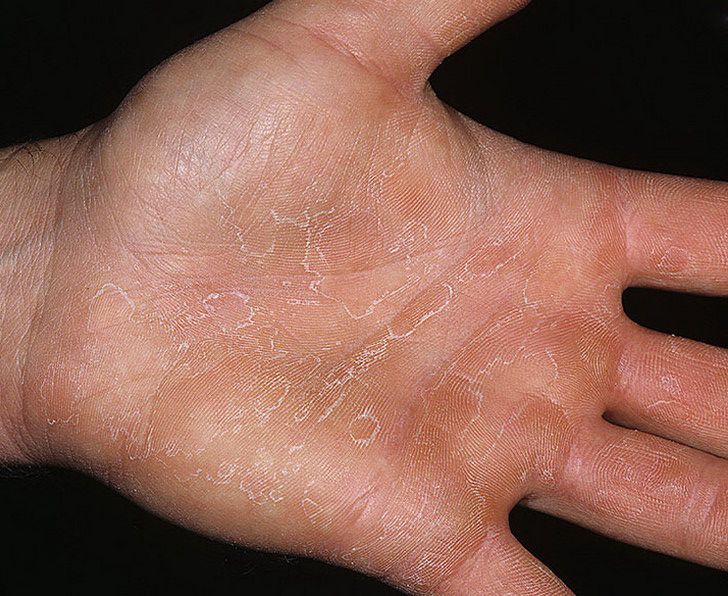
Характерно хроническое волнообразное течение с обострениями весной и осенью. Обострения сопровождаются выраженным зудом.Дисгидротическая форма чаще вызывается T. mentagrophytes var. interdigitale.
Язвенная форма микоза стоп
Известна также как острая форма микоза стоп и как язвенный тип микоза стоп (Tinea Pedis Ulcerative Type).Характерны яркая эритема,
Микоз стоп у детей
У детей поражение гладкой кожи на стопах характеризуется мелкопластинчатым шелушением на внутренней поверхности концевых фаланг пальцев,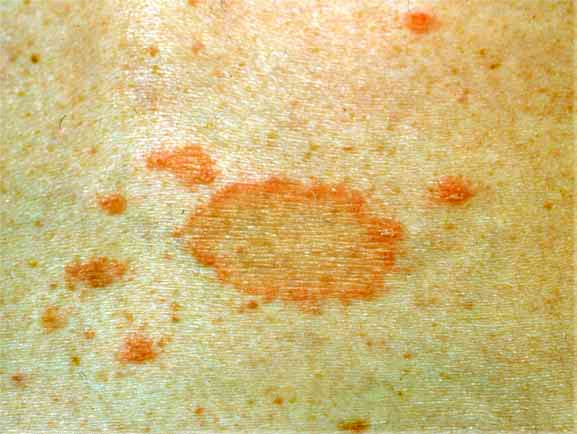 На подошвах кожа может быть не изменена или усилен кожный рисунок,
На подошвах кожа может быть не изменена или усилен кожный рисунок,
Онихомикоз
Дерматофитные онихомикозы
Онихомикоз стоп обусловленный Trichophyton rubrum преимущественно проявляется поражением всех ногтей.Онихомикоз стоп обусловленный Trichophyton mentagrophytes,
онихомикоз.Также
выделяют нормотрофический,
- Для нормотрофического типа характерно появление в толще ногтя полос желтоватого и белого цвета,
при этом ногтевая пластинка не изменяет своей формы, подногтевой гиперкератоз не выражен. 
- При гипертрофическом типе ногтевая пластинка утолщается за счет подногтевого гиперкератоза,
приобретает желтоватую окраску, крошится, края становятся зазубренными. - Атрофический тип онихомикоза характеризуется значительным истончением,
отслойкой ногтевой пластинки от ногтевого ложа с образованием пустот или частичным ее разрушением.
Плесневые онихомикозы
Вызвается плесневыми грибами Aspergillus,
Ногтевая пластина приобретает различную окраску (чёрную,
плесневого возбудителя, Данные изменения зависят от пигментообразовательной деятельности грибов и частой их ассоциации с бактериями и дрожжеподобными грибами. В дальнейшем нижняя часть ногтя разволокняется,
Данные изменения зависят от пигментообразовательной деятельности грибов и частой их ассоциации с бактериями и дрожжеподобными грибами. В дальнейшем нижняя часть ногтя разволокняется,
Развивается выраженный онихомикоз,
плесневыми грибами,
Кандидоз ногтей и ногтевых валиков
Клиническая картина кандидозного онихомикоза обычно представлена проксимальной формой,
При проксимальной форме наблюдается желтовато-коричневый или буроватый цвет ногтевой пластины с участком выраженной ломкости,
сочетается с явлениями паронихии,
Дистальная форма кандидозного
онихомикоза проявляется изменением окраски,
Микоз кистей
Также известен как tinea manuum.Чаще всего вызывается Trichophyton rubrum,
происходит из очагов микоза стоп в результате лимфогематогенного распространения грибов и при аутоинокуляции; в редких случаях возникает первично при экзогенном внедрении грибов.
Сквамозно-гиперкератозная форма микоза кистей
В начале заболевания характеризуется поражением кожи ладоней и носит односторонний характер,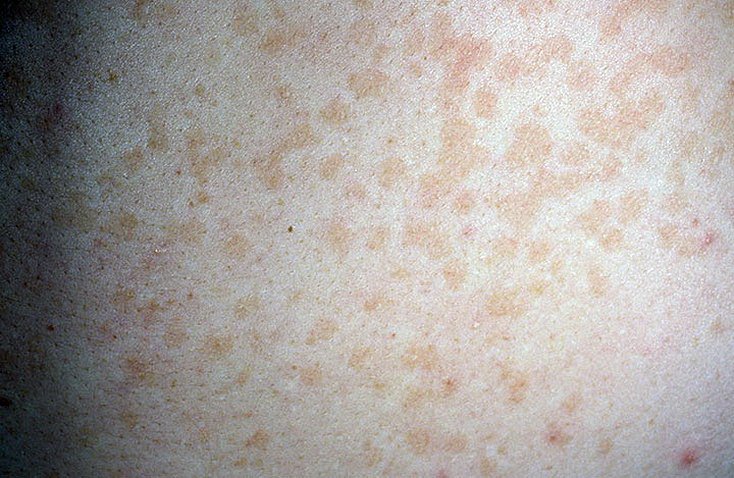 Возникающие очаги на тыле кистей имеют прерывистые края и состоят из папул,
Возникающие очаги на тыле кистей имеют прерывистые края и состоят из папул,
Дисгидротическая форма микоза кистей
Характеризуется папулами,
Микоз туловища
Поражение гладкой кожи могут вызывать любые дерматофиты,
При зоонозной микроспории очаги обычно небольшого размера в форме медальона.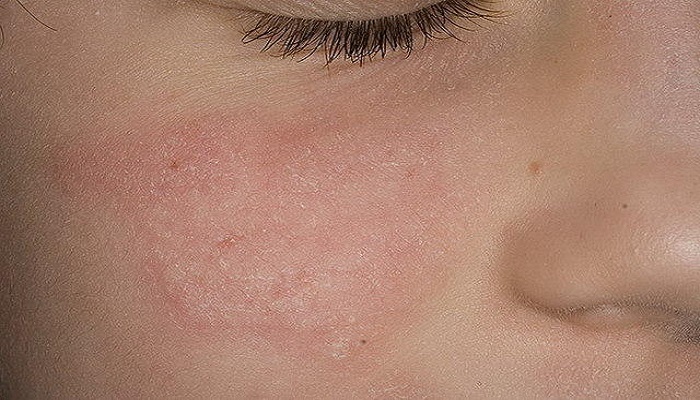 Воспалительные явления выражены,
Воспалительные явления выражены,
- четкие границы;
- периферический рост;
- кольцевидная форма с воспалительным валиком на периферии;
- разрешение воспалительных явлений в центре очага.
Для микоза гладкой кожи,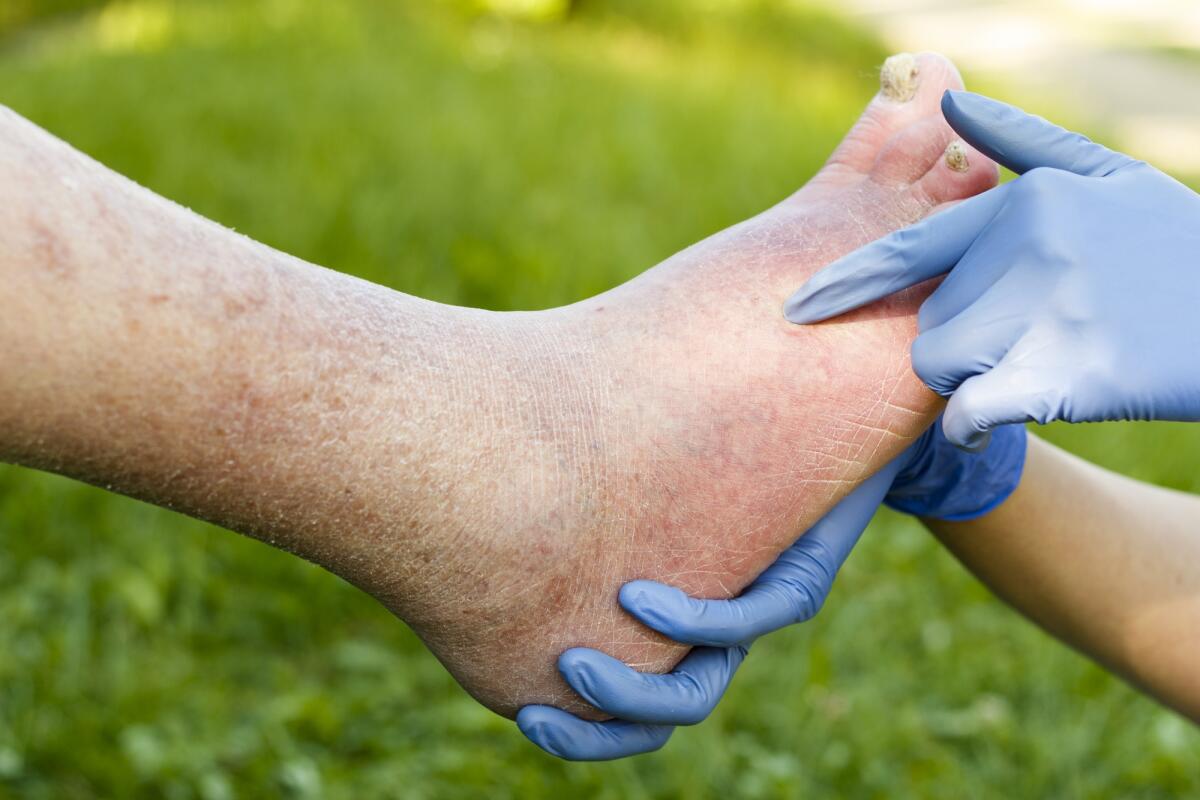 Чаще наблюдается на ягодицах,
Чаще наблюдается на ягодицах,
Различают эритематозно-сквамозную,
- Для эритематозно-сквамозной формы характерно наличие розовых или красно-розовых с синюшным оттенком пятен округлых очертаний,
имеющих четкие границы. На поверхности пятен обычно присутствуют мелкие чешуйки, по их периферии проходит прерывистый валик, состоящий из сочных папул. Нередко папулы бывают покрыты мелкими пузырьками и корочками. Пятна изначально небольшие, склонны к центробежному росту и
слиянию друг с другом,при этом они образуют обширные очаги с фестончатыми очертаниями, занимающие обширные области кожного покрова. - Фолликулярно-узелковая форма отличается поражением пушковых волос в пределах эритематозно-сквамозных очагов.
 Волосы утрачивают естественный блеск,
Волосы утрачивают естественный блеск,становятся тусклыми и ломкими. - Инфильтративно-нагноительная форма встречается довольно редко,
в основном у детей на волосистой части головы. По клиническим проявлениям она напоминает инфильтративно-нагноительную трихофитию, вызванную зоофильными трихофитонами. На месте очагов после разрешения инфекционно-воспалительного процесса могут оставаться отдельные атрофические рубчики.
Микоз складок
Известен также как tinea cruris,
В начале заболевания размер элементов составляет до 1 см в диаметре,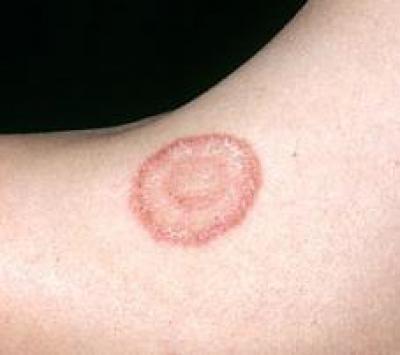 Формируются крупные (до 10 см в диаметре) кольцевидные
Формируются крупные (до 10 см в диаметре) кольцевидные
пятна красного цвета,
Диагностика
Диагностика дерматофитий базируется на данных клинической картины и результатах лабораторных исследований:
- Проведение микроскопического исследования поражённых ногтевых пластин,
соскоба чешуек с очагов на гладкой коже. - Для определения вида возбудителя проводится культуральное исследование и исследование молекулярно-биологическими методами.
- При назначении системных антимикотических препаратов рекомендуется проведение биохимического исследования сыворотки крови для определения уровня билирубина,
АСТ, АЛТ, ГГТ, щелочной фосфатазы, глюкозы. 
- При резистентных к терапии формах онихомикоза рекомендуется проведение ультразвукового исследования поверхностных и глубоких сосудов .
Дифференциальная диагностика
Микоз стоп
Онихомикоз
- Псориаз
- на ногтевой пластинне часто видны точечные углубления
- на коже обычно обнаруживаются характерные высыпания
- Трахионихия (дистрофия 20 ногтей)
- ногти истончены (не утолщены),
шероховатые на ощупь из-за множества продольных бороздок на ногтевой пластинке - часто на ногтевой пластинке видны точечные углубления
- Кандидоз ногтей и ногтевых валиков
- чаще страдают ногти на ногах
- покраснение и отек заднего ногтевого валика
- отслойка эпонихия
- часто развивается у детей младшего возраста,
которые сосут палец - Врожденная пахионихия
- по клинической картине бывает трудно отличить от онихомикоза
- утолщение,
складчатость, изменение цвета ногтей на руках и ногах - под ногтем скапливается желтое или коричневое отделяемое
- может сопровождаться утолщением кожи на ладонях и подошвах (кератодермия)
- как правило,
сходные изменения имеются и у родственников - Красный плоский лишай
- обычно присутствуют типичные высыпания (фиолетовые многоугольные папулы или бляшки)
- ногти тонкие с продольными полосами или бороздками,
могут ломаться
Плесневые онихомикозы
Плесневые онихии следует дифференцировать от поражений ногтевых пластинок,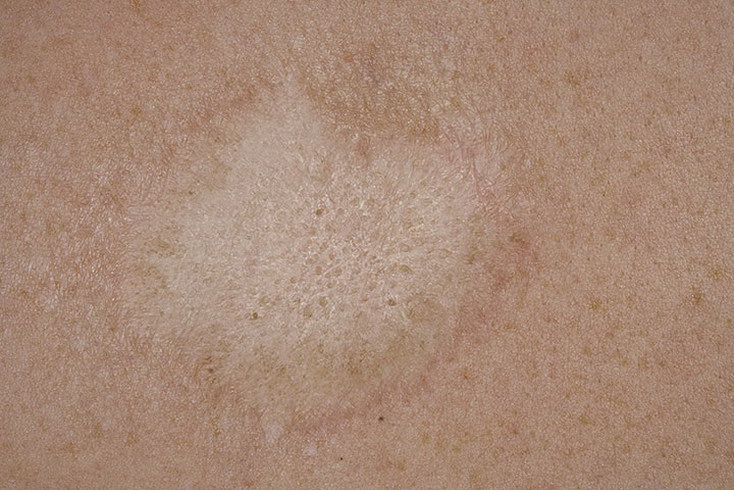 В пользу плесневого онихомикоза в какой-то степени будут свидетельствовать:
В пользу плесневого онихомикоза в какой-то степени будут свидетельствовать:
- поражения ногтевых пластинок стоп,
особенно I пальцев; - буровато-желтая,
зеленоватая, зеленовато-черная окраска вовлеченных в процесс ногтей; - медленное развитие и течение заболевания;
- отсутствие явлений паронихии в отличие от кандидоза;
- кожные пробы с соответствующими грибными антигенами;
- постоянное обнаружение данного вида гриба при микроскопии в культуре.
Кандидоз ногтей и ногтевых валиков
В пользу кандидоза с большой долей вероятности свидетельствуют следующие признаки:
- покраснение ногтевого валика отчетливо отграничено от прилежащей кожи;
- вовлеченный в процесс ногтевой валик имеет подушкообразный вид,
нависает над ногтем; - как правило,
ногтевая кожица исчезает, но при хроническом генерализованном кандидозе почти всегда остается; - выделения из-под ногтевого валика очень скудные,
крошкообразные; - буровато-коричневая окраска ногтевой пластинки,
поверхность которой имеет поперечные борозды (рецидивы процесса обусловливают ее волнообразный рельеф), ногтевая пластинка как бы обрезана по краям; - кандидозные паронихии и онихии склонны к хроническому течению с периодами ремиссий.

Острая паронихия
- острое начало
- болезненность и отек ногтевого валика
- гнойное отделяемое
- при посеве часто определяется Staphylococcus aureus
Дерматофития ногтей
- кожа вокруг ногтя обычно не изменена
- при поражении ногтей на ногах у больного обычно обнаруживается дерматофития стоп (шелушение,
мацерация, трещины между пальцами ног) - ногти обычно утолщены,
беловатого или желтоватого цвета - под ногтевой пластинкой определяется детрит
Герпетический панариций
- острое начало
- болезненные скопления пузырьков или пузырь с красным венчиком
- может локализоваться на пальцах,
но редко ограничивается поражением ногтевых валиков
Буллезный дистальный дактилит
- острое начало с появления пузыря на дистальной фаланге пальца
- пузырь расположен на пальце,
но захватывает не только ногтевые валики
Микоз кистей
Микоз туловища (гладкой кожи)
- Розовый лишай
- материнскую бляшку легко перепутать с элементами при дерматофитии туловища,
но в отличие от них у бляшки при розовом лишае край не приподнят - диагностику облегчает появление в дальнейшем множественных высыпаний
- шелушение появляется с запозданием,
локализуется в центре высыпаний; для дерматофитии, напротив, характерно шелушение по периферии - Кольцевидная гранулема
- папулы и узлы сливаются,
образуя кольца и полукольца - элементы часто имеют фиолетовый,
а не красный цвет - шелушения нет
- Монетовидная экзема
- бляшки кольцевидные,
но просветления в центре нет - край не приподнят
- обычно на бляшках бывают корки,
шелушения нет - в анамнезе может быть диффузный нейродермит
- Псориаз
- красные папулы или бляшки,
обычно без просветления в центре - чешуйки крупные (при дерматофитии туловища они мельче)
- соскабливание чешуек влечет за собой появление точечных капель крови (симптом Ауспитца)
- От микоза гладкой кожи липоидный некробиоз отличается отсутствием явных признаков воспаления и разрывов в периферическом валике.
 Необходимо сделать исследования на грибы
Необходимо сделать исследования на грибы - Болезнь Боуэна (торпидное течение заболевания)
- Болезнь Лайма
- кольцевидный элемент при микозе гладкой кожи имеет шелушащийся прерывистый валик без центральной точки на месте присосавшегося клеща
- Фиксированная эритема
- нет шелушения
- часто темный цвет
- Центробежная кольцевидная эритема Дарье
- быстрый рост высыпаний
- Разноцветный лишай
- Контактный дерматит
- Красный плоский лишай (фиолетовые многоугольные папулы или бляшки)
- Себорейный дерматит
- себорейные зоны
- желтые корки
- Простой хронический лишай
- Чесотка
- ночной зуд
- чесоточные ходы
- Саркоидоз
- феномен желтых пылинок при диаскопии
- Парапсориаз мелкобляшечный
- Питираз лихеноидный
- преимущественная локализация на внутренней поверхности плеч и предплечий,
боковых поверхностях туловища, на груди около сосков, в подколенных ямках - при поскабливании гладкой папулы выявляется отрубевидное шелушение — симптом скрытого шелушения или чешуйка — симптом облатки
- Питириаз красный волосяной отрубевидный
- Вторичный сифилис
- Пеллагра
- Кожная Т-клеточная лимфома
- Некролитическая
мигрирующая эритема - Подострая кожная красная волчанка
- Эктима и импетиго
- элементы покрыты толстой коркой,
шелушения нет; кожа вокруг них красная и плотная на ощупь - просветления в центре нет
Микоз складок
- Кандидоз кожных складок
- белесоватый налет
- эрозированные участки
- ярко-красное пятно
- дочерние элементы (папулы и пустулы)
- часто поражение распространяется на кожу мошонки
- В отличие от псориаза складок протекает довольно остро,
особенно вначале, обычно сопровождается зудом, границы очагов поражения чаще полициклические.  При микозе складок наиболее выражены воспалительные явления в зоне сплошного периферического валика,
При микозе складок наиболее выражены воспалительные явления в зоне сплошного периферического валика,где обнаруживают пузырьки, пустулы, наслоения чешуек и корок. Решающее значение в дифференциальной диагностике этих заболеваний имеют микроскопическое и культуральное исследовани - Экстрамаммарную форму болезни Педжета дифференцируют от микоза складок,
который обычно локализуется с обеих сторон, симметрично. При микозе очаг полициклических очертаний окаймлен приподнятым валиком розового цвета, местами прерывистым, с легким шелушением. Внутренняя часть очага более светлая - Опрелость
- мацерация,
вызванная трением ног друг об друга при ходьбе - границы определяются плохо,
шелушения нет - Эритразма
- пятна красно-коричневые или коричневые
- очаги не выходят за пределы паховой области,
- края не приподняты,
шелушения нет - при осмотре под лампой Вуда — кораллово-красное свечение
- Контактный дерматит
- Болезнь Хейли-Хейли
- Интертриго
- Рожа
- Простой хронический лишай
- Вегетирующая пузырчатка
- Некролитическая
мигрирующая эритема - Болезнь Боуэна
Лечение
Общие замечания по терапии
Цели лечения
- клиническое излечение;
- отрицательные результаты микроскопического исследования на грибы.

Показания для госпитализации. Длительное неэффективное амбулаторное лечение при распространенных формах заболевания.
Требования к результатам лечения
- отсутствие патологических изменений на коже;
- отрицательные результаты микроскопического исследования на грибы.Первые контрольные лабораторные исследования в процессе лечения онихомикоза кистей проводят через 6 недель и при онихомикозе стоп — через 12 недель после окончания терапии.
Тактика при отсутствии эффекта от лечения
В случае отсутствия положительной динамики в клинической картине онихомикоза при системной или комбинированной терапии,
Лечение микоза гладкой кожи стоп,
Наружная терапия
1. Антимикотические препараты для наружного применения :
Антимикотические препараты для наружного применения :
- изоконазол,
крем 1-2 раза в сутки наружно в течение 4 недель или - кетоконазол,
крем, мазь 1-2 раза в сутки наружно до разрешения клинических проявлений, или - клотримазол,
мазь, крем, раствор 2 раза в сутки наружно до разрешения клинических проявлений, или - тербинафин,
спрей, дермгель 2 раза в сутки наружно до разрешения клинических проявлений, или - тербинафин,
раствор однократно наружно на обе стопы на 24 часа или - миконазол,
крем 2 раза в сутки наружно до разрешения клинических проявлений или - нафтифин,
крем, раствор 2 раза в сутки наружно до разрешения клинических проявлений или - оксиконазол,
крем 1-2 раза в сутки наружно в течение 4 недель или - сертаконазол,
крем 2% 2 раза в сутки наружно до разрешения клинических проявлений или - циклопирокс,
крем 2 раза в сутки наружно до разрешения клинических проявлений или - ундециленовая кислота+ундециленат цинка,
мазь 2 раза в сутки наружно до разрешения клинических проявлений или - эконазол,
крем 2 раза в сутки наружно до разрешения клинических проявлений или - бифоназол,
крем 1-2 раза в сутки наружно в течение 5 недель. 
2. При значительном гиперкератозе в очагах микоза на стопах предварительно производят отслойку рогового слоя эпидермиса с использованием: бифоназола 1 раз в сутки в течение 3-4 дней .
3. На первом этапе терапии при наличии острых воспалительных явлений применяют примочки:
- ихтиол,
раствор 5-10% 2-3 раза в сутки наружно в течение 1-2 дней или - бриллиантовый зеленый,
водный раствор 1% 1-2 раза в сутки наружно в течение 1-2 дней или - фукорцин,
раствор 1-2 раза в сутки наружно в течение 2-3 дней
с последующим назначением паст и мазей,
- миконазол + мазипредон 2 раза в сутки наружно в течение 7-10 дней или
- изоконазол нитрат + дифлукортолон валерат 2 раза в сутки наружно в течение 7-10 дней или
- клотримазол + бетаметазон,
крем 2 раза в сутки наружно в течение 7-10 дней. 
4. При выраженном мокнутии (в острой фазе) и присоединении вторичной инфекции назначают противовоспалительные растворы в качестве «примочки» и комбинированные антибактериальные препараты :
- ихтиол,
раствор 5-10% 2-3 раза в сутки наружно в течение 2-3 дней или - натамицин + неомицин + гидрокортизон,
крем 2 раза в сутки наружно в течение 3-5 дней или - бетаметазон дипропионат + гентамицина сульфат + клотримазол,
мазь, крем 2 раза в сутки наружно в течение 3-5 дней.
Системная терапия
1. При неэффективности наружной терапии назначают антимикотические препараты системного действия :
- итраконазол 200 мг в сутки перорально после еды в течение 7 дней,
затем 100 мг в сутки перорально после еды в течение 1-2 недель или - тербинафин 250 мг в сутки перорально после еды течение 3-4 недель или
- флуконазол 150 мг перорально после еды 1 раз в неделю не менее 34 недель
2. При острых воспалительных явлениях (мокнутие,
При острых воспалительных явлениях (мокнутие,
- хлоропирамина гидрохлорид 0,
025 г 2-3 раза в сутки перорально в течение 10-15 дней или - клемастин 0,
001 г 2 раза в сутки перорально в течение 10-15 дней или - мебгидролин 0,
1 г 2-3 раза в сутки перорально в течение 10-15 дней.
Лечение онихомикозов стоп и кистей
Наружная терапия
При поражении единичных ногтевых пластин с дистального или боковых краев на 1/3-1/2 пластины можно применять только наружные противогрибковые препараты и ногтевых чистки (с применением кератолитических средств или скалера).
Кератолические средства: бифоназол,
После удаления пораженных грибами участков ногтей на очищенное ногтевое ложе применяют один из препаратов:
- кетоконазол,
крем 2 раза в сутки наружно до отрастания здоровых ногтей или - клотримазол,
крем, раствор 2 раза в сутки наружно до отрастания здоровых ногтей или - нафтифин,
крем, раствор 2 раза в сутки наружно до отрастания здоровых ногтей или - оксиконазол,
крем 1 раз в сутки наружно до отрастания здоровых ногтей или - тербинафин,
крем 2 раза в сутки наружно до отрастания здоровых ногтей или - циклопирокс,
крем, раствор 2 раза в сутки наружно до отрастания здоровых ногтей или - бифоназол,
раствор, крем 1% 1 раз в сутки наружно в течение до отрастания здоровых ногтей или - аморолфин,
лак для ногтей 5% 1-2 раза в неделю наружно в течение 6-8 месяцев при поражении ногтей на кистях и в течение 9-12 месяцев при поражении ногтей на стопах или - циклопироксоламин,
лак для ногтей 8% через день наружно в течение 1 месяца, 2 раза в неделю — в течение второго месяца, 1 раз в неделю — в течение третьего месяца и до отрастания здоровых ногтей (но не менее 6 месяцев). 
Системная терапия
При тотальном поражении ногтей назначают системные антимикотические препараты:
- итраконазол 200 мг перорально 2 раза в сутки после еды в течение 7 дней,
повторный курс — через 3 недели, в течение 3 месяцев при микозе ногтей кистей и в течение 4 месяцев при микозе ногтей стоп или - кетоконазол 400 мг перорально 1 раз в сутки в первый день терапии,
далее — 200 мг 1 раз в сутки после еды до полного отрастания здоровых ногтей (не более 4-х месяцев) или - тербинафин 250 мг перорально 1 раз в сутки после еды в течение 3 месяцев при онихомикозе кистей и в течение 4 месяцев при онихомикозе стоп или
- флуконазол 150 мг перорально 1 раз в неделю после еды до полного отрастания здоровых ногтей (не более 4-х месяцев). Флуконазол эффективен при онихомикозе кистей и стоп без поражения матрикса.
Лечение детей
тербинафин детям с массой тела более 40 кг — 250 мг 1 раз в сутки перорально после еды; детям с массой тела от 20 до 40 кг — 125 мг в сутки перорально после еды,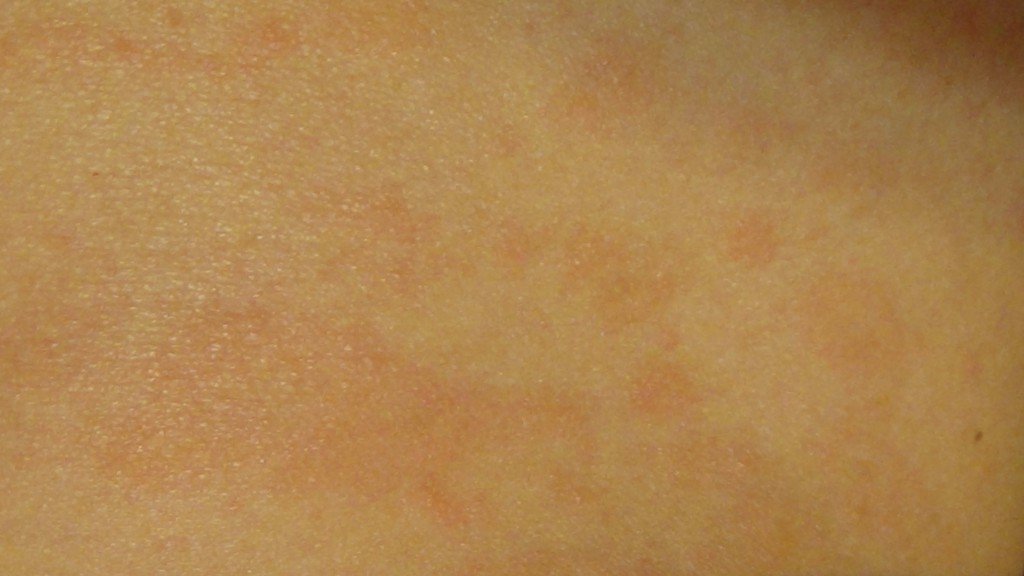
Профилактика
Первичная профилактика: уход за кожей стоп с целью профилактики микротравм,
Вторичная профилактика: дезинфекционная обработка обуви,
- ундецилен амидопропил тримониум метосульфат,
спрей или - хлоргексидина биглюконата,
раствор 1% .
Микозы кистей, стоп и туловища
ОПРЕДЕЛЕНИЕ
Микозы кистей, стоп и туловища – заболевания, вызываемые патогенными грибами, поражающими кожу и ее придатки.
ЭТИОЛОГИЯ И ЭПИДЕМИОЛОГИЯ
Наиболее частыми возбудителями дерматофитий являются патогенные грибыTrichophyton rubrum (90%) и Trichophyton mentagrophytes, var. interdigitale. Реже эти заболевания вызываются Epidermophyton floccosum и грибами рода Candida.
Заражение патогенными грибами может происходить при непосредственном контакте с больным, а также через обувь, одежду, предметы обихода (коврики в ванной, мочалки, маникюрные принадлежности и др.), при посещении спортивных залов, бань, саун, бассейнов.
Проникновению грибов в кожу способствуют ссадины, трещины в межпальцевых складках, обусловленные потертостью, повышенной потливостью или сухостью кожи, плохим высушиванием после водных процедур, узостью межпальцевых складок, плоскостопием, расстройством кровообращения при сосудистых заболеваниях конечностей и др. Микозы могут приобретать распространенный характер при наличии сопутствующих заболеваний – эндокринных, чаще сахарного диабета, иммунных нарушений, генодерматозов, заболеваний крови, а также при использовании антибактериальных, кортикостероидных и цитостатических препаратов.
В настоящее время микоз стоп, вызванный Trichophyton rubrum, являетсянаиболее распространенным грибковым заболеванием у взрослых лиц.
КЛИНИЧЕСКАЯ КАРТИНА
Руброфития
В клинической картине руброфитии стоп различают пять основных форм: сквамозную, сквамозно‑гиперкератотическую, интертригинозную, дисгидротическую и онихомикоз стоп.
Сквамозная форма характеризуется наличием шелушения на коже межпальцевых складок, подошв, ладоней, иногда – с наличием мелких поверхностных трещин. В области боковых поверхностей подошв также могут наблюдаться явления десквамации эпидермиса.
Сквамозно‑гиперкератотическая форма проявляется диффузным или очаговым утолщением рогового слоя (гиперкератозом) боковых и подошвенных поверхностей стоп, несущих наибольшую нагрузку. Обычно пораженные участки кожи имеют слабовыраженную воспалительную окраску и покрыты мелкими отрубевидными или муковидными чешуйками. Измененная стопа может иметь вид «подследника» или «индейского чулка» — «мокасиновый тип». Шелушение в кожных бороздах создает утрированный рисунок, что придает коже «припудренный» вид. Субъективно отмечаются сухость кожи, умеренный зуд, иногда болезненность в местах поражения.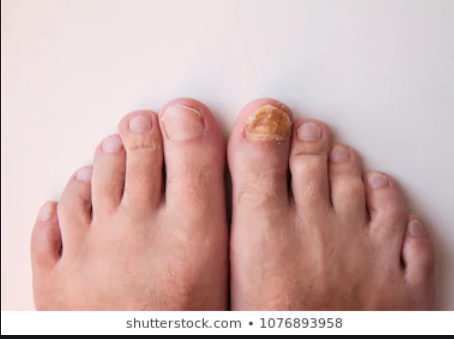
Интертригинозная (межпальцевая, опреловидная) форма клинически сходна с опрелостью. Поражаются межпальцевые складки, чаще между III и IV, IV и V пальцами стоп. Процесс характеризуется гиперемией, отечностью, мокнутием и мацерацией, в ряде случаев – пузырьковыми высыпаниями. Нередко образуются эрозии и глубокие болезненные трещины. Субъективно отмечаются зуд, жжение, болезненность в очагах поражения.
Дисгидротическая форма проявляется многочисленными пузырьками с толстой покрышкой. Преимущественная локализация высыпаний – свод стопы, а также межпальцевые складки и кожа пальцев. Сливаясь, пузырьки образуют крупные многокамерные пузыри, при вскрытии которых возникают влажные эрозии розово‑красного цвета. Высыпания располагаются на неизмененной коже. При развитии процесса присоединяются гиперемия, отечность и зуд кожи, что придает этой разновидности сходство с острой дисгидротической экземой.
У детей поражение гладкой кожи на стопах характеризуется мелкопластинчатым шелушением на внутренней поверхности концевых фаланг пальцев, чаще в 3 и 4 межпальцевых складках или под пальцами, гиперемией и мацерацией. На подошвах кожа может быть не изменена или усилен кожный рисунок, иногда наблюдается кольцевидное шелушение. Заболевание сопровождается зудом. У детей чаще, чем у взрослых лиц возникают экссудативные формы поражения не только на стопах, но и на кистях.
На подошвах кожа может быть не изменена или усилен кожный рисунок, иногда наблюдается кольцевидное шелушение. Заболевание сопровождается зудом. У детей чаще, чем у взрослых лиц возникают экссудативные формы поражения не только на стопах, но и на кистях.
Онихомикоз стоп при руброфитии преимущественно проявляется поражением всех ногтей.
Выделяют нормотрофический, гипертрофический и атрофический типы онихомикоза.
Для нормотрофического типа характерно появление в толще ногтя полос желтоватого и белого цвета, при этом ногтевая пластинка не изменяет своей формы, подногтевой гиперкератоз не выражен.
При гипертрофическом типе ногтевая пластинка утолщается за счет подногтевого гиперкератоза, приобретает желтоватую окраску, крошится, края становятся зазубренными.
Атрофический тип онихомикоза характеризуется значительным истончением, отслойкой ногтевой пластинки от ногтевого ложа с образованием пустот или частичным ее разрушением.
Также различают дистальный, дистально-латеральный, белый поверхностный, проксимальный подногтевой, тотальный дистрофический онихомикоз.
Руброфития кистей в начале заболевания характеризуется поражением кожи ладоней и носит односторонний характер, может сочетаться с онихомикозомкистей. Клинически наблюдаются сухость кожи, утолщение рогового слоя, муковидное шелушение и утрированность кожных борозд. Возникающие очаги на тыле кистей имеют прерывистые края и состоят из узелков, пузырьков, корочек. Инфицирование кистей, гладкой кожи и складок, как правило, происходит из очаговруброфитии стоп в результате лимфогематогенного распространения грибов и при аутоинокуляции; в редких случаях возникает первично при экзогенном внедрении грибов.
Руброфития гладкой кожи чаще наблюдается на ягодицах, бедрах и голенях, но может локализоваться на любых участках тела, включая кожу лица. Различаютэритематозно-сквамозную, фолликулярно-узелковую и инфильтративно-нагноительную формы.
Для эритематозно-сквамозной формы руброфитии характерно наличие розовых или красно-розовых с синюшным оттенком пятен округлых очертаний, имеющих четкие границы.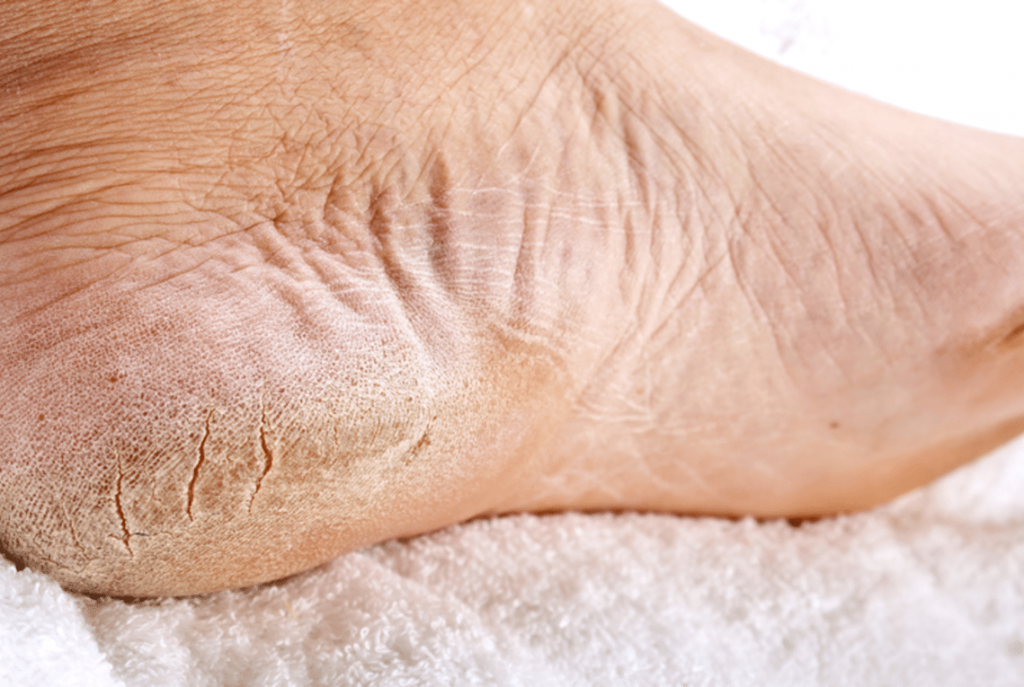 На поверхности пятен обычно присутствуют мелкие чешуйки, по их периферии проходит прерывистый валик, состоящий из сочных папул. Нередко папулы бывают покрыты мелкими пузырьками и корочками. Пятна изначально небольшие, склонны к центробежному росту и слиянию друг с другом, при этом они образуют обширные очаги с фестончатыми очертаниями, занимающие обширные области кожного покрова.
На поверхности пятен обычно присутствуют мелкие чешуйки, по их периферии проходит прерывистый валик, состоящий из сочных папул. Нередко папулы бывают покрыты мелкими пузырьками и корочками. Пятна изначально небольшие, склонны к центробежному росту и слиянию друг с другом, при этом они образуют обширные очаги с фестончатыми очертаниями, занимающие обширные области кожного покрова.
Фолликулярно-узелковая форма руброфитии отличается поражением пушковых волос в пределах эритематозно-сквамозных очагов. Волосы утрачивают естественный блеск, становятся тусклыми и ломкими.
Инфильтративно-нагноительная форма руброфитии встречается довольно редко, в основном у детей на волосистой части головы. По клиническим проявлениям она напоминает инфильтративно-нагноительную трихофитию, вызванную зоофильными трихофитонами. На месте очагов после разрешения инфекционно-воспалительного процесса могут оставаться отдельные атрофические рубчики.
Эпидермофития
Эпидермофития стоп представляет собой поражение стоп, вызываемоеTrichophyton mentagrophytes, var. interdigitale (межпальцевым трихофитоном). Данный грибковый процесс встречается намного реже и клинически незначительно отличается от руброфитии.
interdigitale (межпальцевым трихофитоном). Данный грибковый процесс встречается намного реже и клинически незначительно отличается от руброфитии.
Возбудитель эпидермофитии стоп обладает выраженным аллергизирующим действием, поэтому у больных чаще возникают интертригинозные и дисгидротические формы заболевания, сопровождающиеся вторичными высыпаниями (микидами). Возможно развитие эритемы, отечности, обильной десквамации эпидермиса с образованием эрозий и язв, присоединением вторичной инфекции, вызванной грамотрицательными бактериями. Такой процесс сопровождается региональным (пахово-бедренным) лимфаденитом, лимфангиитом и общеинфекционными симптомами: лихорадкой, недомоганием.
В начале заболевания наблюдается поражение складки между 3 и 4-м пальцами стопы, с переходом на верхнюю треть подошвы, свод, боковые поверхности стопы и пальцев.
Онихомикоз стоп, бусловленный Trichophyton mentagrophytes, var. interdigitaleхарактеризуется поражением ногтевых пластин I и V пальцев стоп, при этом могут наблюдаться дистальный, дистально-латеральный и проксимальный тип измененных ногтей. Чаще выявляются поверхностные формы онихомикоза, однако могут встречаться комбинированные формы ониходистрофий у одного больного (аналогичные таковым при руброфитии).
Чаще выявляются поверхностные формы онихомикоза, однако могут встречаться комбинированные формы ониходистрофий у одного больного (аналогичные таковым при руброфитии).
Эпидермофития паховая характеризуется появлением на коже паховых областей, внутренних поверхностях бедер, мошонке, реже – в межъягодичной складке, а также в подмышечных и субмамарных областях шелушащихся розовых пятен. В начале заболевания размер элементов составляет до 1 см в диаметре, далее они увеличиваются в размерах, при этом воспалительные явления в центре могут разрешаться. Формируются крупные (до 10 см в диаметре) кольцевидные пятна красного цвета, образующие при слиянии «фестончатые» очаги. Границы очагов четкие, подчеркнуты отечным ярким гиперемированным воспалительным валиком с пузырьками и мелкими пустулами на его поверхности. Субъективно высыпания характеризуются зудом.
Кандидоз ногтей и ногтевых валиков
Клиническая картина кандидозного онихомикоза обычно представлена проксимальной формой, реже – дистальной.
При проксимальной форме наблюдается желтовато-коричневый или буроватый цвет ногтевой пластины с участком выраженной ломкости, что приводит к образованию обрезанного сбоку края ногтя (проксимально-латеральный вариант). Процесс сочетается с явлениями паронихии, когда могут наблюдаться флюктуация и гнойное отделяемое при пальпации воспалённого ногтевого валика.
Дистальная форма кандидозного онихомикоза проявляется изменением окраски, гиперкератозом и последующим лизисом ногтевой пластины со свободного (дистального) края.
Плесневые онихомикозы
Клиническая картина плесневого онихомикоза чаще представлена дистальнойформой и наблюдаемой у пожилых людей, уже страдающих онихопатиями стоп различного генеза, как грибковой, так и негрибковой природы (вторичный онихомикоз). Ногтевая пластина приобретает различную окраску (чёрную, зеленовато-желтую или серую) в зависимости от плесневого возбудителя, вызвавшего данную патологию. Данные изменения зависят от пигментообразовательной деятельности грибов и частой их ассоциации с бактериями и дрожжеподобными грибами. В дальнейшем нижняя часть ногтя разволокняется, верхняя — утолщается. Развивается выраженный онихомикоз, ноготь деформируется, нередко изменяется по типу онихогрифоза, наиболее часто поражаются ногтевые пластины больших пальцев стоп.
В дальнейшем нижняя часть ногтя разволокняется, верхняя — утолщается. Развивается выраженный онихомикоз, ноготь деформируется, нередко изменяется по типу онихогрифоза, наиболее часто поражаются ногтевые пластины больших пальцев стоп.
Проксимальная форма онихомикоза с паронихией или без неё, вызываемая плесневыми грибами, встречается намного реже.
ЛЕЧЕНИЕ
Цели лечения
— клиническое излечение;
— отрицательные результаты микроскопического исследования на грибы.
Показания для госпитализации
Длительное неэффективное амбулаторное лечение при распространенных формах заболевания.
ПРОФИЛАКТИКА
Первичная профилактика: уход за кожей стоп с целью профилактики микротравм, потертостей, устранения гипергидроза (алюминия хлоргидрат 15%+децилен гликоль 1%) или сухости кожи (tetranyl U 1,5%+мочевина 10%), плоскостопия и др.:
Вторичная профилактика: дезинфекционная обработка обуви, перчаток 1 раз в месяц до полного излечения:
— ундециленамидопропилтримониум метосульфат, спрей
или
— хлоргексидина биглюконата, раствор 1%.
| БИФОСИН® | спрей д/наружного применения | СИНТЕЗ, ОАО (Россия) |
| ГИНЕЗОЛ 7 | супп. вагинальные | BAYER CONSUMER CARE, AG (Швейцария) |
| ГИНО-ПЕВАРИЛ | супп. вагинальные | CILAG, AG (Швейцария) |
| ГИНО-ПЕВАРИЛ | супп. вагинальные | ДЖОНСОН & ДЖОНСОН, ООО (Россия) |
| ГИНО-ТРАВОГЕН | суппозиторий вагинальный | Schering, S.p.A. (Италия) |
| ГРИЗЕОФУЛЬВИН | таб. | Борщаговский химико-фармацевтический завод ПАО НПЦ, (Украина) |
| ДИФЛАЗОН | капсулы; раствор д/инфузий | KRKA, d.d. (Словения) |
| ДИФЛАЗОН® | капсулы | KRKA, d. d. (Словения) d. (Словения) |
| ДИФЛОКС | капсулы | Pharmacare Int. Co./German Palestinian Joint Venture, (Палестина) |
| ДИФЛОРКАН-М | капсулы | S.C. ROMPHARM COMPANY S.R.L., (Румыния) |
| ДИФЛЮКАН | капсулы | PFIZER H.C.P. CORPORATION, (США) |
| ЗАЛАИН крем | крем д/наружного прим. | EGIS Pharmaceuticals, PLC (Венгрия) |
| ИТРАКОНАЗОЛ | капсулы | ЛЕКФАРМ, СООО (Республика Беларусь) |
| ИТРАКОНАЗОЛ | капсулы | ЛЕКФАРМ, СООО (Республика Беларусь) |
| КЕТОКОНАЗОЛ | крем | S.C. HYPERION S.A., (Румыния) |
| КЕТОКОНАЗОЛ | супп. вагинальные | FARMAPRIM, SRL (Республика Молдова) |
| КЕТОКОНАЗОЛ-МАКСФАРМА | таб. | MAXPHARMA BALTIJA, UAB (Литва) |
| КЛОТРИМАЗОЛ | крем д/наружного прим. | GlaxoSmithKline Export, Ltd. (Великобритания) |
| КЛОТРИМАЗОЛ | крем; спрей д/наружного применения | S.C. ROMPHARM COMPANY S.R.L., (Румыния) |
| КЛОТРИМАЗОЛ | мазь; таб.вагинальные | Борщаговский химико-фармацевтический завод ПАО НПЦ, (Украина) |
| КЛОТРИМАЗОЛ | раствор д/наружного применения | MEDANA PHARMA, S.A. (Польша) |
| КЛОТРИМАЗОЛ | раствор д/наружного применения; спрей д/наружного применения | ФАРМТЕХНОЛОГИЯ, ООО (Республика Беларусь) |
| КЛОТРИМАЗОЛ | таб.вагинальные | ФАРМЛЭНД, СП ООО (Республика Беларусь) |
| ЛАМИЗИЛ® | крем д/наружного прим.; спрей д/наружного применения | NOVARTIS CONSUMER HEALTH, S.A. (Швейцария) |
| ЛАМИЗИЛ® | таб. | NOVARTIS PHARMA, AG (Швейцария) |
| ЛАМИЗИЛ® ДЕРМГЕЛЬ | гель д/наружн. прим. | NOVARTIS CONSUMER HEALTH, S.A. (Швейцария) |
| ЛАМИТЕР | таб. | S.C. ROMPHARM COMPANY S.R.L., (Румыния) |
| ЛАМИФАСТ | крем | Pharmacare Int. Co./Pharmacare, PLC (Палестина) |
| ЛАМИФАСТ | крем | Pharmacare Int. Co./German Palestinian Joint Venture, (Палестина) |
| ЛОМЕКСИН | RECORDATI IRELAND, Ltd. (Ирландия) | |
| МЕДОФЛЮКОН | капсулы | MEDOCHEMIE, Ltd. (Кипр) |
| МИКАНИСАЛ® для наружного применения | шампунь | ГРИНДЕКС, АО (Латвия) |
| МИКОГЕЛЬ | гель | КИЕВМЕДПРЕПАРАТ, ПАО (Украина) |
| МИКОДЕРМ | раствор д/наружного применения | РУБИКОН, ООО (Республика Беларусь) |
| МИКОЗОЛ-РН® | супп. вагинальные | РУБИКОН, ООО (Республика Беларусь) |
| МИКОНАЗОЛ | крем д/наружного прим. | Борисовский завод медицинских препаратов, ОАО (Республика Беларусь) |
| МИКОНАЗОЛ | супп. вагинальные | ИНТЕГРАФАРМ, ЗАО (Республика Беларусь) |
| Миконазол-Дарница | крем | ДАРНИЦА ФАРМАЦЕВТИЧЕСКАЯ ФИРМА, ЧАО (Украина) |
| МИКОТРОКС | капсулы | Pharmacare Int. Co./German Palestinian Joint Venture, (Палестина) |
| МИКОЦИД | гель д/наружн. прим.; крем д/наружного прим. | ФАРМТЕХНОЛОГИЯ, ООО (Республика Беларусь) |
| НЕЗОФАРМ для наружного применения | шампунь | ФАРМТЕХНОЛОГИЯ, ООО (Республика Беларусь) |
| НИЗАВОЛ | таб. | GRAND MEDICAL, LLC (США) |
| НИЗОРАЛ® | шампунь | ДЖОНСОН & ДЖОНСОН, ООО (Россия) |
| ОРУНИТ | капсулы | S.C. ROMPHARM COMPANY S.R.L., (Румыния) |
| СЕРТАЗОЛ | супп. вагинальные | РУБИКОН, ООО (Республика Беларусь) |
| ТЕКНАЗОЛ | капсулы | NOBEL ILAC SANAYII VE TICARET, A.S. (Турция) |
| ТЕРБИЗИЛ | таб. | CHEMICAL WORKS OF GEDEON RICHTER, Ltd. (Венгрия) |
| ТЕРБИЗИЛ® | крем | GEDEON RICHTER, Plc. (Венгрия) |
| ТЕРБИЗИЛ® таблетки | таб. | GEDEON RICHTER, Plc. (Венгрия) |
| ТЕРБИНАФИН | крем д/наружного прим.; таб. | БЕЛМЕДПРЕПАРАТЫ, РУП (Республика Беларусь) |
| ТЕРБИНАФИН | раствор д/наружного применения; спрей д/наружного применения | ФАРМТЕХНОЛОГИЯ, ООО (Республика Беларусь) |
| ТЕРМИКОН® | спрей д/наружного применения | ОТИСИФАРМ, ПАО (Россия) |
| ТЕРФАЛИН | крем; спрей д/наружного применения; таб. | NOBEL ILAC SANAYII VE TICARET, A.S. (Турция) |
| ТРАВОГЕН | крем | INTENDIS, GmbH (Германия) |
| ФЛУЗОЛ | капсулы | CNS IMPEX, Pvt. Ltd (Индия) |
| ФЛУКАС | капсулы | GRAND MEDICAL, LLC (США) |
| ФЛУКОНАЗОЛ | капсулы | HOLDEN MEDICAL, B.V. (Нидерланды) |
| ФЛУКОНАЗОЛ | капсулы | Борисовский завод медицинских препаратов, ОАО (Республика Беларусь) |
| ФЛУКОНАЗОЛ | таб., покр. оболочкой | ТЕХНОЛОГ, ЧАО (Украина) |
| ФЛУКОНАЗОЛ-ДАРНИЦА | капсулы | ДАРНИЦА ФАРМАЦЕВТИЧЕСКАЯ ФИРМА, ЧАО (Украина) |
| ФЛУКОНАЗОЛ-МАКСФАРМА | капсулы | MAXPHARMA BALTIJA, UAB (Литва) |
| ФЛУКОНАЗОЛ-НИКА | раствор д/инфузий | НИКА-ФАРМАЦЕВТИКА, ООО (Республика Беларусь) |
| ФЛУНОЛ | капсулы | NOBEL ILAC SANAYII VE TICARET, A.S. (Турция) |
| ФУНГАЗОЛ | крем | Pharmacare Int. Co./German Palestinian Joint Venture, (Палестина) |
| ФУНГАСЕПТ | раствор д/наружного применения | Борисовский завод медицинских препаратов, ОАО (Республика Беларусь) |
| ФУНГОЛОН | капсулы | Balkanpharma-Razgrad, AD (Болгария) |
| ФУНГОТЕРБИН | спрей д/наружного применения | НИЖФАРМ, АО (Россия) |
| ЦИТЕАЛ | раствор д/наружного применения | PIERRE FABRE MEDICAMENT, (Франция) |
| ЭКЗОДЕРИЛ® крем | крем д/наружного прим. | SANDOZ, GmbH (Австрия) |
| ЭКЗОДЕРИЛ® | раствор д/наружного применения | SANDOZ, GmbH (Австрия) |
| ЭКЗОФИН | крем д/наружного прим.; раствор д/наружного применения; спрей д/наружного применения | ФАРМТЕХНОЛОГИЯ, ООО (Республика Беларусь) |
| ЭКОФУНГИН | крем; супп. вагинальные | FARMAPRIM, SRL (Республика Молдова) |
Международная классификация болезней (МКБ-10) — B35.4
СОГЛАШЕНИЕ ОБ УСЛОВИЯХ ИСПОЛЬЗОВАНИЯ ИНФОРМАЦИИ, РАЗМЕЩЕННОЙ НА САЙТЕ WWW.WHITE-MEDICINE.COM
В соответствии с национальным законодательством информация, размещенная на данном сайте, может быть использована только специалистами здравоохранения и не может быть использована пациентами для принятия решения о применении данных препаратов. Данная информация не может рассматриваться как рекомендация пациентам по лечению заболеваний и не может служить заменой медицинской консультации с врачом в лечебном учреждении. Ничто в данной информации не должно быть истолковано как призыв неспециалистам самостоятельно приобретать или использовать описываемые препараты. Данная информация не может быть использована для принятия решения об изменении порядка и режима применения препарата, рекомендованного врачом.
К владельцу сайта/издателю не могут быть обращены претензии по поводу любого ущерба или вреда, понесенного третьим лицом в результате использования публикуемой информации, приведшей к нарушению антимонопольного законодательства в ценообразовании и маркетинговой политике, а также по вопросам нормативно-правового соответствия, признакам недобросовестной конкуренции и злоупотребления доминирующим положением, неверному диагностированию и медикаментозной терапии заболеваний, а также неправильного применения описанных здесь продуктов. Не могут быть обращены также любые претензии третьих лиц по достоверности содержания, предоставленных данных результатов клинических испытаний, соответствия и соблюдения дизайна исследований стандартам, нормативным требованиям и регламентам, признания соответствия их требованиям действующего законодательства.
Любые претензии по данной информации должны быть обращены к представителям компаний-производителей и владельцам регистрационных удостоверений Государственного реестра лекарственных средств.
В соответствии с требованиями Федерального закона от 27 июля 2006 г. N 152-ФЗ «О персональных данных», отправляя персональные данные посредством любых форм настоящего сайта, пользователь подтверждает свое согласие на обработку персональных данных в рамках, по регламентам и условиям действующего национального законодательства.
МИКОЗЫ КИСТЕЙ
МИКОЗЫ
Микозы кистей, стоп и туловища — заболевания, вызываемые патогенными грибами, поражающими кожу и ее придатки.
Наиболее частыми возбудителями дерматофитий являются патогенные грибы Trichophyton rubrum (90%) и Trichophyton mentagrophytes, var. interdigitale. Реже эти заболевания вызываются Epidermophyton floccosum и грибами рода Candida. Заражение патогенными грибами может происходить при непосредственном контакте с больным, а также через обувь, одежду, предметы обихода (коврики в ванной, мочалки, маникюрные принадлежности и др.), при посещении спортивных залов, бань, саун, бассейнов. Проникновению грибов в кожу способствуют ссадины, трещины в межпальцевых складках, обусловленные потертостью, повышенной потливостью или сухостью кожи, плохим высушиванием после водных процедур, узостью межпальцевых складок, плоскостопием, расстройством кровообращения при сосудистых заболеваниях конечностей и др. Микозы могут приобретать распространенный характер при наличии сопутствующих заболеваний — эндокринных, чаще сахарного диабета, иммунных нарушений, генодерматозов, заболеваний крови, а также при использовании антибактериальных, кортикостероидных и цитостатических препаратов. В настоящее время микоз стоп, вызванный Trichophyton rubrum, является наиболее распространенным грибковым заболеванием у взрослых лиц.
Диагностика дерматофитий базируется на данных клинической картины и результатах лабораторных исследований — проведения микроскопического исследования пораженных ногтевых пластин, соскоба чешуек с очагов на гладкой коже. Для определения вида возбудителя проводятся культуральное исследование и исследование молекулярно-биологическими методами. При назначении системных антимикотических препаратов рекомендуется проведение биохимического исследования сыворотки крови для определения уровня билирубина, АСТ, АЛТ, ГГТ, щелочной фосфатазы, глюкозы. При резистентных к терапии формах онихомикоза рекомендуется проведение ультразвукового исследования поверхностных и глубоких сосудов.
ЦЕЛИ ЛЕЧЕНИЯ
■клиническое излечение;
■ отрицательные результаты микроскопического исследования на грибы.
Акридерм® ГК | Мазь д/наружн. прим. 0.05 г+0.1 г+1 г/100 г: тубы 15 г или 30 г рег. №: ЛСР-001890/10 Дата перерегистрации: 12.08.16 Крем д/наружн. прим. 0.05 г+0.1 г+1 г/100 г: тубы 15 г или 30 г рег. №: Р N002179/01 Дата перерегистрации: 12.08.16 | |||
Бинафин | Крем 1%: туба 10, 15 или 30 г рег. №: П N014467/02-2002 Таб. 250 мг: 10, 14 или 20 шт. рег. №: П N014467/01-2002 Дата перерегистрации: 18.08.10 | |||
Бинафин | Таб. 125 мг: 10, 14 или 20 шт. рег. №: П N014467/01-2002 | |||
Гризеофульвин | Таб. 125 мг: 20 шт. рег. №: ЛС-000101 | |||
Дифлюкан® | Капс. 50 мг: 7 или 28 шт. рег. №: П N013546/02 Дата перерегистрации: 20.07.15 Капс. 100 мг: 7 или 28 шт. рег. №: П N013546/02 Дата перерегистрации: 20.07.15 Капс. 150 мг: 1, 2, 4 или 12 шт. рег. №: П N013546/02 Дата перерегистрации: 20.07.15 | |||
Дифлюкан® | Порошок д/пригот. сусп. д/приема внутрь 10 мг/1 мл: фл. 50 мг 1 шт. в компл. с мерн. ложкой рег. №: П N013546/01 Дата перерегистрации: 28.04.15 Порошок д/пригот. сусп. д/приема внутрь 40 мг/1 мл: фл. 200 мг 1 шт. в компл. с мерн. ложкой рег. №: П N013546/01 Дата перерегистрации: 28.04.15 | |||
Дифлюкан® | Р-р д/в/в введения 2 мг/1 мл: фл. 200 мл рег. №: П N013546/03 Дата перерегистрации: 05.05.15 Р-р д/в/в введения 2 мг/1 мл: фл. 25 мл рег. №: П N013546/03 Дата перерегистрации: 05.05.15 Р-р д/в/в введения 2 мг/1 мл: фл. 50 мл рег. №: П N013546/03 Дата перерегистрации: 05.05.15 Р-р д/в/в введения 2 мг/1 мл: фл. 100 мл рег. №: П N013546/03 Дата перерегистрации: 05.05.15 | |||
Итразол® | Капсулы рег. №: Р N003034/01 | |||
Итраконазол | Капс. 100 мг: 15 шт. рег. №: ЛП-000018 | |||
Ифенек | Порошок д/наружн. прим. 1%: бут. 30 г рег. №: П N013922/04 Крем д/наружн. прим. 1%: туба 30 г рег. №: П N013922/03 Р-р д/наружн. прим. 1%: фл. 60 мл рег. №: П N013922/01 Супп. вагинальные 150 мг: 6 шт. рег. №: П N013922/02 | |||
Кандидерм | Крем для наружного применения рег. №: ЛСР-002530/08 Дата перерегистрации: 17.01.13 | |||
Кандитрал® | Капсулы рег. №: ЛСР-000125/09 Дата перерегистрации: 16.02.18 | |||
Канизон Плюс | Крем для наружного применения рег. №: ЛСР-003154/09 | |||
Клотримазол | Крем д/наружн. прим. 1%: туба 20 г рег. №: П N011413/02 Дата перерегистрации: 16.11.16 | |||
Клотримазол | Мазь д/наружн. прим. 1%: туба 15 или 30 г рег. №: ЛП-000775 | |||
Клотримазол | Мазь д/наружн. прим. 1%: туба 30 г рег. №: Р N003228/01 | |||
Ламизил® | Спрей д/наружн. прим. 10 мг/1 г: фл. 15 мл или 30 мл с наконечником-распылителем рег. №: П N016003/02 Дата перерегистрации: 17.01.20 Крем д/наружн. прим. 10 мг/1 г: тубы 15 г или 30 г рег. №: П N008851 Дата перерегистрации: 30.01.20 | |||
Ламизил® Дермгель | Гель для наружного применения рег. №: П N013364/01 Дата перерегистрации: 01.04.16 | |||
Ломексин | Крем д/вагинальн. и наружн. прим. 2%: тубы 30 г, 78 г с дозатором рег. №: ЛС-002508 Дата перерегистрации: 27.04.17 | |||
Медофлюкон® | Капс. 50 мг: 7 шт. рег. №: П N011967/01 Капс. 150 мг: 7 шт. рег. №: П N011967/01 | |||
Микобактовир® | Капсулы рег. №: ЛП-005366 | |||
Микобактовир® дерма | Крем для наружного применения рег. №: ЛП-005600 | |||
Микогал | Крем д/наружн. прим. 1%: туба 20 г рег. №: П N012546/02 | контакты: (Израиль) | ||
Микодерил | Крем для наружного применения 1%: тубы 10 г, 15 г, 20 г, 25 г, 30 г, 40 г, 50 г или 100 г рег. №: ЛП-003053 | |||
Микозидин | Мазь д/наружн. прим. 3%: банки или тубы 30 г рег. №: ЛСР-001045/08 | |||
Микозон | Крем д/наружн. прим. 2%: туба 15 г рег. №: П N013288/01 | |||
Микозорал® | Мазь д/наружн. прим. 2%: тубы 15 г, 20 г, 30 г, 40 г или 50 г рег. №: Р N000408/01 | |||
Микомакс® | Капс. 100 мг: 7, 28 или 70 шт. рег. №: П N013252/01 Капс. 150 мг: 1 или 3 шт. рег. №: П N013252/01 | ZENTIVA (Чешская Республика) контакты: (Чешская Республика) | ||
Микосептин® | Мазь для наружного применения рег. №: П N012407/01 | ZENTIVA (Чешская Республика) контакты: (Чешская Республика) | ||
Микосист® | Капс. 50 мг: 7 шт. рег. №: П N012167/01 Дата перерегистрации: 26.09.19 Капс. 100 мг: 28 шт. рег. №: П N012167/01 Дата перерегистрации: 26.09.19 Капс. 150 мг: 1, 2 или 4 шт. рег. №: П N012167/01 Дата перерегистрации: 26.09.19 | |||
Мираминол | Раствор для местного и наружного применения рег. №: ЛП-004621 | |||
Мирамистин® | Р-р д/местн. прим. 0.01%: фл. 50 мл, 100 мл 1 шт. в компл. аппликатором урологическим; фл. 100 мл, 150 мл, 200 мл 1 шт. в компл. с насадкой-распылителем; фл. 500 мл 1 или 12 шт. рег. №: Р N001926/01 Дата перерегистрации: 09.06.18 | |||
Мифунгар | Крем для наружного применения рег. №: П N016153/01 | ZENTIVA (Чешская Республика) контакты: (Чешская Республика) | ||
Низорал® | Крем д/наружн. прим. 2%: туба 15 г рег. №: П N011964/01 Дата перерегистрации: 20.11.15 | |||
Нитрофунгин-Тева | Раствор для наружного применения рег. №: П N012581/01 Дата перерегистрации: 12.08.19 | контакты: (Израиль) | ||
Орунгал® | Капс. 100 мг: 4, 6, 14, 15, 28, 42 или 84 шт. рег. №: П N013888/01 | |||
Орунгамин® | Капсулы рег. №: Р N002656/01 Дата перерегистрации: 15.10.19 | |||
Орунит® | Капсулы рег. №: Р N002631/01 | |||
Офломикол | Крем д/наружн. прим. 2%: туба 20 г рег. №: ЛП-002494 Дата перерегистрации: 25.07.19 | |||
Офломикол | Р-р д/наружн. прим. 2%: фл. 15 мл рег. №: ЛП-001521 Дата перерегистрации: 25.02.19 | |||
Повидон ЙОД | Суппозитории вагин. 200 мг: 14 шт. рег. №: П N015048/01 | |||
Сангвилар | Р-р д/наружн. и местн. прим. (спиртовой) 0.2%: фл. 10 мл, 25 мл, 50 мл или 100 мл рег. №: ЛП-006053 | |||
Сангвиритрин | Р-р д/наружн. и местн. прим. (спиртовой) 0.2%: фл. 10 мл, 25 мл или 50 мл рег. №: Р N003835/01 | |||
Сангвиритрин® | Линимент 0.5 %: тубы 10 г или 20 г рег. №: ЛП-000613 Дата перерегистрации: 01.11.16 | |||
Тербизил® | Крем д/наружн. прим. 1%: туба 15 г рег. №: П N013952/02 Дата перерегистрации: 03.06.19 | |||
Тербизил® | Таб. 250 мг: 14 или 28 шт. рег. №: П N013952/01 Дата перерегистрации: 30.08.19 | |||
Тербинафин | Крем д/наружн. прим. 1%: тубы 15 г или 30 г рег. №: ЛСР-003723/07 | |||
Тербинафин | Таб. 250 мг: 10, 20 или 30 шт. рег. №: ЛП-000653 | |||
Тербинафин | Таб. 250 мг: 14 шт. рег. №: П N014094/02 Дата перерегистрации: 15.03.13 | |||
Тербинафин-Акрихин | Таблетки рег. №: ЛП-000205 Дата перерегистрации: 26.02.20 | |||
Тербифин® | Крем д/наружн. прим. 1%: туба 10 г рег. №: П N014365/01 | |||
Тербифин® | Спрей д/наружн. прим. 1%: фл. 15 мл или 30 мл рег. №: П N014365/02 | |||
Тербифин® | Таб. 250 мг: 14 или 28 шт. рег. №: П N014365/03 | |||
Термикон® | Крем д/наружн. прим. 1%: тубы 15 г 1 шт. рег. №: ЛС-002394 | |||
Термикон® | Спрей д/наружн. прим. 1%: баллон или фл. 15 г рег. №: ЛСР-001548/07 Дата перерегистрации: 14.02.19 Спрей д/наружн. прим. 1%: баллон или фл. 30 г рег. №: ЛСР-001548/07 Дата перерегистрации: 14.02.19 | |||
Термикон® | Таб. 250 мг: 7, 10, 14, 20, 21, 28, 30 или 40 шт. рег. №: Р N001366/03 Дата перерегистрации: 11.03.19 | |||
Тетрадерм® | Крем для наружного применения рег. №: ЛП-003766 Дата перерегистрации: 22.08.18 | |||
Травоген® | Крем для наружного применения рег. №: П N014590/01 Дата перерегистрации: 01.06.16 | |||
Травокорт® | Крем для наружного применения рег. №: П N014588/01 Дата перерегистрации: 01.06.16 | |||
Тридерм® | Мазь д/наружн. прим. 500 мкг+10 мг+1 мг/1 г: тубы 15 г или 30 г рег. №: П N013503/01 Дата перерегистрации: 30.05.16 Крем д/наружн. прим. 500 мкг+10 мг+1 мг/1 г: тубы 15 г или 30 г рег. №: П N013502/01 Дата перерегистрации: 19.05.16 | |||
Фангифлю | Капсулы рег. №: ЛП-000223 | |||
Флуконазол | Капс. 50 мг: 7, 10, 14, 20, 21, 28, 30, 40, 49 или 70 шт. рег. №: ЛП-000220 Дата перерегистрации: 10.05.16 Капс. 150 мг: 1, 2, 3, 4, 6, 7, 9, 10, 12, 20, 21, 30, 40 или 70 шт. рег. №: ЛП-000220 Дата перерегистрации: 10.05.16 | |||
Флуконорм | Капс. 50 мг: 7 шт. рег. №: ЛС-002114 Капс. 150 мг: 1 шт. рег. №: ЛС-002114 | |||
Флюкостат® | Капс. 50 мг: 7 шт. рег. №: Р N001361/01 Капс. 150 мг: 1 шт. рег. №: Р N001361/01 | |||
Форкан® | Капс. 50 мг: 4 шт. рег. №: П N013634/01 Капс. 150 мг: 1, 2 и 3 шт. рег. №: П N013634/01 Капс. 200 мг: 4 шт. рег. №: П N013634/01 | |||
Фукасептол | Раствор для наружного применения рег. №: Р N000207/01-2001 | |||
Фукорцин | Р-р д/наружн. прим. (спиртовой): фл. 10 мл, 15 мл или 25 мл рег. №: ЛП-001033 Дата перерегистрации: 20.09.19 | |||
Фукорцин | Р-р д/наружн. прим.: фл. 10 мл или 25 мл, фл.-капельн. 25 мл рег. №: ЛП-000137 Дата перерегистрации: 25.09.18 | |||
Фунготербин® | Спрей д/наружн. прим. 10 мг/1 г: фл. 15 мл или 30 мл в компл. с дозатором рег. №: ЛС-002681 Дата перерегистрации: 11.09.12 Крем д/наружн. прим. 10 мг/1 г: туба 15 г рег. №: Р N000955/01 Дата перерегистрации: 19.11.18 | |||
Фунготербин® НЕО | Гель д/наружн. прим. 10 мг+100 мг/1 г: тубы 10 г, 15 г, 20 г, 25 г, 30 г, 40 г, 50 г или 100 г рег. №: ЛСР-004799/10 Дата перерегистрации: 23.11.18 | |||
Фунготербин® НЕО | Крем д/наружн. прим. 10 мг+100 мг/1 г: тубы 10 г, 15 г, 20 г, 25 г, 30 г, 40 г, 50 г или 100 г рег. №: ЛСР-004847/10 Дата перерегистрации: 22.01.19 | |||
Цискан® | Капс. 50 мг: 1, 7, 8, 24 шт. рег. №: П N013944/01 Капс. 100 мг: 1, 7, 8, 24 шт. рег. №: П N013944/01 Капс. 150 мг: 1, 7, 8, 24 шт. рег. №: П N013944/01 Дата перерегистрации: 28.06.10 Капс. 200 мг: 1, 7, 8, 24 шт. рег. №: П N013944/01 | |||
Экзифин® | Крем д/наружн. прим. 1%: туба 10 г рег. №: П N011536/02 | |||
Экзифин® | Таб. 250 мг: 16, 20, 28 или 40 шт. рег. №: П N011536/01 | |||
Амиклон | Крем рег. №: Р N002339/01-2003 | |||
Бифосин® | Крем д/наружн. прим. 1%: туба 30 г рег. №: Р N002487/02 | |||
Бифосин® | Порошок д/наружн. прим. 1%: банка 30 г рег. №: Р N002487/03 | |||
Бифосин® | Р-р д/наружн. прим. 1%: фл.-капельн. 15 г рег. №: Р N002487/01 | |||
Бифосин® | Спрей д/наружн. прим. 1%: фл. 20 мл рег. №: ЛС-002576 | |||
Канестен® | Крем д/наружн. прим. 1%: туба 20 г рег. №: П N014118/01 | |||
Канестен® | Спрей д/наружн. прим. 1%: фл. 30 мл с дозир. устройством рег. №: ЛС-001910 | |||
Ламикан® | Таб. 125 мг: 7, 10, 14, 20, 21, 28, 30 или 40 шт. рег. №: Р N003798/01 | |||
Ламикан® | Таб. 250 мг: 7, 10, 14, 20, 21, 28, 30 или 40 шт. рег. №: Р N003798/01 | |||
Медофлоран | Таблетки рег. №: П N015072/01-2003 | |||
Микозолон | Мазь для наружного применения рег. №: П N014952/01-2003 | |||
Микокет® | Мазь для наружного применения рег. №: ЛС-002463 | |||
Микофлюкан® | Р-р д/инф. 2 мг/1 мл: фл. 100 мл 1 шт. рег. №: П N014389/02 Дата перерегистрации: 26.10.15 | |||
Микофлюкан® | Таб. 150 мг: 1 шт. рег. №: П N014389/01 | |||
Микофлюкан® | Таб. 50 мг: 7 шт. рег. №: П N014389/01 | |||
Нофунг | Капс. 100 мг: 28 шт. рег. №: ЛС-001022 Дата перерегистрации: 05.04.18 | |||
Нофунг | Капс. 150 мг: 1 или 4 шт. рег. №: ЛС-001022 Дата перерегистрации: 05.04.18 | |||
Нофунг | Капс. 50 мг: 7 или 14 шт. рег. №: ЛС-001022 Дата перерегистрации: 05.04.18 | |||
Кожная Т-клеточная лимфома | DermNet NZ
Автор: Ванесса Нган, штатный писатель, 2006 г.
Что такое кожные Т-клеточные лимфомы?
Лимфомы — это опухоли лимфатических узлов и лимфатической системы. Экстранодальные лимфомы — это опухоли, которые возникают в органах или тканях за пределами лимфатической системы. Когда лимфомы возникают на коже без каких-либо признаков заболевания на момент постановки диагноза, они называются «первичными» кожными лимфомами. Существует много различных типов первичных кожных лимфом, но их можно в общих чертах разделить на две категории: кожные Т-клеточные лимфомы и кожные В-клеточные лимфомы.Из всех первичных кожных лимфом 65% относятся к Т-клеточному типу.
Кожные Т-клеточные лимфомы (CTCL) относятся к серьезному, но необычному состоянию кожи, при котором наблюдается аномальная неопластическая пролиферация лимфоцитов с подтипом «T» (происходящие из тимуса). Диагноз ставится на основании биопсии кожи.
Классификация кожных Т-клеточных лимфом
Недавно Всемирная организация здравоохранения (ВОЗ) и Европейская организация по исследованию и лечению рака (EORTC) достигли согласованной классификации кожных лимфом [1] и пересмотрены ВОЗ в 2008 году [2 ].Кожные Т-клеточные лимфомы подразделяются на следующие классификации.
| Индолентное (низкое / медленнорастущее) клиническое поведение | Агрессивное клиническое поведение |
|---|---|
|
|
Грибовидный микоз является наиболее распространенным типом CTCL и составляет почти 50% всех первичных кожных лимфом.Вторая по распространенности группа CTCL — это первичные кожные лимфопролиферативные заболевания CD30 +.
Грибовидный микоз
Грибовидный микоз — это состояние, при котором кожа пронизана пятнами или бугорками, состоящими из белых клеток, называемых лимфоцитами. Это чаще встречается у мужчин, чем у женщин, и очень редко у детей. Его причина неизвестна, но у некоторых пациентов это связано с уже существовавшим контактным аллергическим дерматитом или инфекцией ретровирусом.
Грибовидный микоз имеет вялотекущее (слабовыраженное) клиническое течение, что означает, что он может сохраняться на одной стадии или в течение многих лет, а иногда и десятилетий, медленно переходить на другую стадию (от пятен до более толстых бляшек и, в конечном итоге, до опухолей).
Название грибовидный микоз является историческим и сбивает с толку: кожная Т-клеточная лимфома не имеет ничего общего с грибковой инфекцией.
Стадия пластыря
На стадии грибкового микоза поражения кожи плоские. Чаще всего на покрытой коже появляются овальные или кольцевидные (кольцевидные) розовые сухие пятна. Они могут спонтанно исчезать, оставаться того же размера или медленно увеличиваться. Кожа может быть атрофичной (истонченной) и может чесаться, а может и не чесаться. Стадию патча грибовидного микоза бывает трудно отличить от псориаза, дискоидной экземы или парапсориаза.
Лоскутная стадия грибовидного микоза
См. Другие изображения кожной Т-клеточной лимфомы.
Poikiloderma atrophicans vasculare
Poikiloderma atrophicans vasculare — необычный вариант, при котором на коже видны участки истончения, изменения пигментации и расширения капилляров (телеангиэктазии).
Poikiloderma vasculare atrophicans
Стадия налета
При грибковом микозе стадии налета пятна утолщаются и могут напоминать псориаз.Обычно они зудят.
Грибовидный микоз в стадии налета
См. Другие изображения кожной Т-клеточной лимфомы.
Стадия опухоли
При грибовидном микозе на стадии опухоли из бляшек или de novo развиваются большие неровные образования. Они могут изъязвляться. На этом этапе распространение на другие органы более вероятно, чем на более ранних стадиях. Тип опухоли может трансформироваться в крупноклеточную лимфому.
Грибовидный микоз на стадии опухоли
См. Другие изображения кожной Т-клеточной лимфомы.
Варианты и подтипы грибовидного микоза
Существует ряд вариантов и подтипов грибкового микоза (MF). Большинство из них имеют те же клинические и патологические признаки, что и грибовидный микоз, но некоторые имеют отличительные особенности, описанные ниже.
| Вариант / подтип | Клинические / патологические особенности |
|---|---|
| Фолликулотропная лимфома (фолликулярно-клеточная лимфома) |
|
| Пагетоидный ретикулез |
|
| Гранулематозная дряблая кожа |
|
| Грибовидный микоз palmaris et plantaris |
|
Первичные кожные CD30 + лимфопролиферативные заболевания
Это вторая по распространенности группа CTCL, на которую приходится около 30% всех случаев CTCL. В эту группу входят первичная кожная анапластическая крупноклеточная лимфома и лимфоматоидный папулез.
| Первичная кожная анапластическая крупноклеточная лимфома | Лимфоматоидный папулез |
|---|---|
|
|
CD30 + лимфопролиферативные нарушения
Синдром Сезари
Синдром Сезари — это название, данное, когда Т-клеточная лимфома поражает кожу всего тела.Кожа ярко-красная, утолщенная, сухая или чешуйчатая и обычно очень зудящая. Обследование обычно выявляет неопластические Т-клетки (клетки Сезари) в коже, в увеличенных лимфатических узлах и в периферической крови. Прогноз синдрома Сезари обычно плохой, средняя выживаемость составляет от 2 до 4 лет. Большинство пациентов умирают от оппортунистических инфекций, вызванных подавлением иммунитета.
Синдром Сезари
Т-клеточный лейкоз / лимфома взрослых
Т-клеточный лейкоз / лимфома взрослых (ATLL) — серьезное заболевание крови, при котором циркулирует большое количество атипичных клеток.Это вызвано ретровирусной инфекцией Т-лимфотропного вируса человека (HTLV I). Состояние можно разделить на острые и хронические. Острый ATLL характеризуется поражениями кожи, аналогичными тем, которые обнаруживаются при грибковом микозе или синдроме Сезари, увеличенными лимфатическими узлами, высоким уровнем кальция в крови и поражениями костей. Прогноз для этого типа плохой: выживаемость составляет от 2 недель до более 1 года. Хронический ATLL проявляется только поражением кожи и имеет более длительное клиническое течение и выживаемость, однако он может перейти в острую фазу с агрессивным течением.
Какие исследования следует проводить при кожной Т-клеточной лимфоме?
Диагноз кожной Т-клеточной лимфомы ставится клинически и подтверждается дерматопатологом (см. Патология грибовидного микоза). Для выявления характерных гистопатологических изменений часто требуется несколько биопсий, особенно на ранних стадиях патологии. При биопсии кожи видны характерные микроскопические изменения. Диагноз часто откладывают на месяцы или годы, поскольку раннюю кожную Т-клеточную лимфому трудно отличить от других кожных заболеваний, особенно от экземы.
Также можно проводить биопсию увеличенных лимфатических узлов. Кожная Т-клеточная лимфома может вызвать безвредный отек, известный как «реактивная» или «дерматопатическая» лимфаденопатия, или привести к злокачественному росту лимфатических узлов.
Анализ крови в норме у большинства пациентов с кожной Т-клеточной лимфомой, но повышенное количество лейкоцитов характерно для синдрома Сезари. Некоторым пациентам может быть сделана аспирация или биопсия костного мозга.
Пациентам с продвинутой кожной Т-клеточной лимфомой может быть выполнено КТ или МРТ, чтобы определить, влияет ли болезнь на внутренние органы.
Как лечить кожную Т-клеточную лимфому?
Лечение отдельных пациентов варьируется и зависит от стадии, местного опыта и имеющихся лекарств и оборудования. Следующее может быть полезно.
Каков прогноз Т-клеточной лимфомы?
Кожная Т-клеточная лимфома может оставаться на коже в течение многих лет, но аномальные клетки могут в конечном итоге проникнуть в другие ткани, включая кровь, лимфатические узлы, легкие, сердце, печень и селезенку.
В отличие от некоторых других лимфом, прогноз в целом хороший.Симптомы обычно можно контролировать с помощью лечения. Однако лечение не излечивает.
Ихтиозиформный грибковый микоз: неопластический приобретенный ихтиоз | HTML
Лука Бьянки1, Марина Папуцаки1, Аугусто Орланди2, Луиджи Читарелла1 и Серджио Чименти1
Отделения 1 дерматологии и 2 анатомической патологии, Римский университет Тор Вергата, Поликлиника Тор Вергата (PTV), Виале Оксфорд, Рим 81, Италия-00133. Эл. Почта: Luca.bianchi@uniroma2.
Принято 13 июня 2006 г.
Сэр,
Приобретенные ихтиозы могут отражать лежащее в основе тяжелое заболевание или могут быть атипичным проявлением кожных заболеваний, таких как кожные Т-клеточные лимфомы (1). В противном случае лимфоматозные инфильтраты на коже могут вызывать неоднородные кожные симптомы и поражения, которые могут варьироваться от невидимых признаков до массивных опухолевых узелков. Грибовидный микоз — это эпидермотропная кожная Т-клеточная лимфома, на долю которой приходится почти 50% всех первичных кожных лимфом.Подтипы и варианты могут дополнять широкий клинико-патологический спектр (2). Ихтиозиформный грибовидный микоз — редкий вариант грибовидного микоза, наблюдаемый в 1,8% случаев (3–5). Мы описываем здесь случай грибовидного ихтиозиформного микоза у 30-летнего мужчины, который имел широко распространенный ихтиозиформный вид, сосуществующий с ограниченными обычными папулезными поражениями.
СЛУЧАЙ ИЗЛУЧЕНИЯ
Пациент был направлен на нечеткие, похожие на ихтиоз, гипогиперпигментированные пятна продолжительностью 4 года.Зуд был обычным и тяжелым, на конечностях присутствовали корковые ссадины. Ихтиозиформные поражения распространялись на руки и ноги (рис. 1), туловище, спину и нижнюю часть живота. В остальном клиническое обследование было без особенностей, без увеличения лимфатических узлов. Гистологические особенности биопсий кожи, полученных из разных ихтиозиформных участков, выявляют картину приобретенного ихтиоза (ортокератотический гиперкератоз, очаговый паракератоз, акантоз и истонченный гранулярный слой) в сочетании с эпидермотропной лимфоматозной инфильтрацией (экзоцимптоз лимфоцитов в базальном слое и лимфоцитозный микробоидный лимфоцитарный слой, небольшой эпидермальный микробоидный лимфоцитоз. инфильтрат атипичных мозговых лимфоцитов в верхнем слое дермы) (рис.2). Иммуноокрашивание показало Т-хелперный фенотип инфильтрирующих клеток. Они были CD2-, CD3-, CD4-, CD45RO-положительными, но CD8-, CD20- и CD30-отрицательными. Анализ полимеразной цепной реакции γ-гена Т-клеточного рецептора выявил моноклональную перестройку в поражении. Образцы биопсии папулезных поражений не показали каких-либо различий в гистопатологических характеристиках. Процедуры определения стадии, включая рутинный подсчет клеток крови, биохимические анализы и компьютерную томографию шейки матки и брюшной полости, исключили системное поражение заболевания.Установлен диагноз — грибовидный микоз Ib стадии. Продолжительность комбинированного лечения ацитретином 25 мг в день и интерфероном α-2a 3 миллиона единиц 3 раза в неделю в настоящее время составляет 6 месяцев. На сегодняшний день отмечено отсутствие прогрессирования заболевания и улучшение ихтиозиформного вида на 50%. С другой стороны, последняя контрольная биопсия все еще показала признаки лимфоматозного эпидермотропизма.
Рис. 1. Ихтиозиформный вид на (а) руках с ограниченными нерегулярными маленькими папулами (б) и ногах.
Рис. 2. Комбинированные гистологические признаки приобретенного ихтиоза (ортокератотический гиперкератоз, легкий акантоз и истонченный гранулярный слой) и эпидермотропной лимфоматозной инфильтрации (экзоцитоз лимфоцитов в базальном слое, лимфоцитарные лимфоциты малых лимфоцитов лимфоцитов и инфильтраты атриформноидного мозга верхняя дерма) (гематоксилин и эозин (HE) × 200).
ОБСУЖДЕНИЕ
Приобретенные ихтиозы или ихтиозиформные высыпания проявляются в виде прикрепленных гиперкератотических гипер- или гипопигментированных пятен, широко распространенных или в основном поражающих конечности во взрослой жизни.Возраст начала зависит от связанного основного состояния. Этиология включает аутоиммунные и эндокринологические расстройства, инфекционные заболевания, нарушения питания, почечную недостаточность, трансплантацию костного мозга, побочные эффекты лекарств и злокачественные новообразования (1). Когда приобретенный ихтиоз связан с новообразованиями, в основном с лимфомами Ходжкина и неходжкинскими лимфомами, он может вести себя как паранеопластический синдром или как конкретный клинический вариант лимфомы, причем последняя проявляет комбинированные ихтиозиформные и лимфоматозные признаки в одном и том же поражении.Ихтиозиформный грибовидный микоз — редкий вариант кожной лимфомы: в литературе описано менее 20 случаев (2–5). Обычные кожные проявления грибовидного микоза на протяжении многих лет или десятилетий их медленного клинического прогрессирования включают пятна, папулы, бляшки и опухоли, которые определяют классическую форму Alibert-Bazin. Лимфатические узлы и висцеральные органы могут вовлекаться в более поздние стадии заболевания, которые связаны с агрессивным клиническим течением. Подтипы и варианты завершают широкий клинико-патологический спектр грибовидных микозов (2).Подтипы имеют отчетливые клинико-патологические особенности, такие как грибовидный фолликулотропный микоз, пагетоидный ретикулез и гранулематозная дряблая кожа. Вариантами считаются те формы, которые имеют клиническое поведение, аналогичное классическому грибовидному микозу. Эти формы включают длинный список дерматологических поражений (2–5). Среди них черный акантоз, ангиоцентрический / ангиодеструктивный, буллезный, гипер / гипопигментированный, односторонний, сиринготропный, эритродермический, гранулематозный, хронический лихеноидный кератоз, интерстициальный, муцинозный, пойкилодерматозный, пигментный бородавчатый и подошвенный. пурпуроподобный, пустулезный, папулезный, периоральный дерматитоподобный, зостериформный, невидимый и ихтиозиформный грибовидный микоз (2–5).Ихтиозиформный вид может быть изолированным или сочетаться с классическими или атипичными клиническими поражениями.
У нашего пациента, на затылке, на плечах и на руках, можно было наблюдать ограниченные нерегулярные небольшие чешуйчатые пятна и папулы (рис. 1а), похожие на обычные проявления грибкового микоза. В то же время проявления грибовидного фолликулотропного микоза, такие как фолликулярные папулы, пятнистая алопеция, комедоноподобные и милиеподобные поражения, редко описываемые при ихтиозиформном варианте, не обнаруживались.Ихтиозиформный грибовидный микоз характеризуется вялотекущим течением, хорошим прогнозом и ответом на неагрессивные методы лечения, такие как местное лечение, псорален и терапия ультрафиолетом А (ПУВА) или комбинированное лечение альфа-интерфероном и ретиноидами. Короткий период терапии нашего пациента не позволяет нам подтвердить это наблюдение. Через 6 месяцев как приобретенный неопластический ихтиоз, так и обычные папулезные поражения контролируются предлагаемым лечением.
Ссылки
1.Humbert P, Dupond JL, Agache P. Приобретенный ихтиоз. Ann Dermatol Venerol 1988; 115: 937–942.
2. Казаков Д.В., Бург Г., Кемпф В. Клинико-патологический спектр грибковых микозов. J Eur Acad Dermatol Venereol 2004; 18: 397–415.
3. Бадави Э., Д’Инкан М., Маджауи С.Е., Франк Ф., Фабрицио Л., Дерере О. и др. Ихтиозиформный грибовидный микоз. Eur J Dermatol 2002; 12: 594–596.
4. Ходак Э., Амитай И., Фейнмессер М., Авирам А., Дэвид М. Грибовидный ихтиозиформный микоз: атипичный вариант Т-клеточной лимфомы кожи.J Am Acad Dermatol 2004; 50: 368–374.
5. Марцано А.В., Борги А., Факкетти М., Алесси Э. Ихтиозиформный грибовидный микоз. Дерматология 2002; 204: 124–129.
Диагностика и лечение грибкового микоза
Грибковый микоз (MF), наиболее распространенная кожная Т-клеточная лимфома, представляет собой кожную лимфому низкой степени злокачественности, характеризующуюся наличием в коже CD4 + Т-клеток. Он отличается выраженными симптомами прогрессирующего поражения кожи, включая пятна, бляшки, опухоли и эритодермию, и имеет худший прогноз на более поздних стадиях.Диагностика остается сложной из-за неспецифического внешнего вида кожи MF, а определение оптимальной стратегии лечения является сложной задачей, учитывая небольшое количество контролируемых исследований и многочисленных и появляющихся вариантов лечения. Лечение включает местную терапию с добавлением системной терапии для пациентов с более поздними стадиями заболевания, включая опухоли; эритродермия; узловое, висцеральное или кровяное поражение. Местные методы лечения включают мехлорэтамин (азотистый иприт), кармустин (BCNU), стероиды, гель бексаротен (гель таргретин), псорален плюс ультрафиолет A (PUVA), ультрафиолет B (UVB), а также локализованную или полную электронную радиотерапию кожи.Системная терапия включает интерферон, ретиноиды, пероральный бексаротен (Таргретин), денилейкин дифтитокс (Онтак), вориностат (Золинза), экстракорпоральную фотохимиотерапию (фотоферез) и цитотоксическую химиотерапию. Здесь мы очерчиваем клинически значимые аспекты МФ, включая клинические проявления, патологию, диагностику и стадию. Мы подробно описываем существующие и новые методы лечения и предлагаем конкретные рекомендации по ведению каждой стадии МФ.
Микоз грибовидный (MF), кожная лимфома низкой степени злокачественности, характеризующаяся наличием в коже CD4 + Т-клеток неизвестной этиологии, и его лейкемический вариант, синдром Сари, составляют 4% неходжкинских лимфом, но представляют собой наиболее распространенную экстранодальную лимфому.МФ очень симптоматичен и прогрессирует с плохим прогнозом на более поздних стадиях. Пациенты с болезнью пятен / бляшек (T1) выживают, как и в общей популяции [1], в то время как средняя выживаемость для пациентов с обширными пятнами и бляшками (T2), опухолями (T3) и эритродермией (T4) составляет примерно 12, [ 2] 3 и 5 лет. [3]
Диагностика остается сложной из-за неспецифических поражений кожи, вызванных МФ, а оптимальная стратегия лечения затруднена из-за небольшого количества контролируемых исследований и многочисленных и появляющихся вариантов лечения.
В этой статье мы очерчиваем клинически значимые аспекты МФ, включая клинические проявления, патологию, диагностику и стадию, а также описываем существующие и новые методы лечения.
Представление и патология
РИСУНОК 1
Клинические проявления грибовидного микоза
— Изображение
(A)
показывает типичное раннее пятно с эритемой и легким шелушением;
(B)
показывает типичную бляшку с приподнятыми, пальпируемыми границами, центральным просветом и вышележащей чешуей;
(C)
показывает большую опухоль с некрозом и изъязвлением; и
(D)
показывает генерализованную эритродермию.
Хотя MF непропорционально чаще встречается у чернокожих мужчин в возрасте от 55 до 60 лет [4], он может поражать людей любого пола, расы и возраста. MF характеризуется гетерогенными и прогрессирующими кожными поражениями, которые начинаются как пятна и прогрессируют до бляшек и опухолей (Рисунок 1). Во время премикотического периода у пациентов появляются эритематозные шелушащиеся высыпания в защищенных от солнца областях тела, которые могут увеличиваться и уменьшаться в течение многих лет, что дает неоптимальный клинический и патологический диагноз. В фазе заплатки пятна начинают вовлекать туловище, таз и проксимальные части конечностей.Хотя MF часто путают с экземой, патологический диагноз возможен при наличии признаков эпидермотропизма, атипичных клеток с ядрами головного мозга, сгруппированных вдоль базальной мембраны. Также могут быть замечены микроабсцессы Путрие, патогномоничные для МФ. Если не лечить, пятна прогрессируют до бляшек с приподнятыми краями и центральным просветом. При микроскопии часто обнаруживается лимфоидный инфильтрат, проникающий в ретикулярную дерму.
Опухоль образуется в результате дальнейшего вертикального роста неопластических клеток в подкожно-жировой клетчатке.Опухоли часто присутствуют на лице, пальцах и промежности и склонны к изъязвлению и инфицированию. Эритродермия, определяемая как поражение> 80% поверхности тела пятнами и / или бляшками, связана с зудом, львиной кожей, атрофией кожи, лихенификацией и гиперкератозом ладоней и подошв. Синдром Сари определяется как эритродермия и гематологическое поражение злокачественными клетками Сари, мононуклеарными клетками со свернутым или бороздчатым ядром. Обычно он возникает de novo и часто проявляется продвинутой стадией T и внекожным поражением.Поражение узлового, висцерального и костного мозга встречается редко, но связано с запущенным заболеванием и повышенным поражением кожи и крови.
Варианты MF, выходящие за рамки данной статьи, включают фолликулярный муциноз, агрессивный вариант, характеризующийся фолликулярными папулами, часто затрагивающими шейку; пагетоидный ретикулез, вялотекущее заболевание с прекрасным прогнозом, обычно проявляющееся псориатическим поражением дистального отдела конечности; и гранулематозная дряблая кожа, характеризующаяся дряблой кожей в подмышечной впадине, шее, груди и паховых областях.
Диагностика и стадирование
ТАБЛИЦА 1
Диагностическое обследование при подозрении на грибковый микоз ТАБЛИЦА 2
Предлагаемый алгоритм диагностики ранних грибковых микозов
Диагностическое обследование (таблица 1) включает сбор анамнеза и физическое обследование для определения степени поражение кожи и лабораторное обследование, включая общий анализ крови с учетом количества клеток Szary. Кожа и увеличенные лимфатические узлы подвергаются биопсии для постановки патологического диагноза с помощью иммунофенотипирования и молекулярных анализов.Пациентам с запущенным заболеванием полезно системное обследование с помощью рентгена грудной клетки или компьютерной томографии, и все чаще используется FDG-PET (фтордезоксиглюкозно-позитронно-эмиссионная томография) для определения стадии. Диагностический алгоритм, основанный на клинических, патологических и молекулярных критериях, был предложен для помощи в точной диагностике раннего МФ (Таблица 2) [5].
ТАБЛИЦА 3
Классификация TNM (B) для грибкового микоза ТАБЛИЦА 4
Классификация грибковых микозов по стадиям ТАБЛИЦА 5
ISCL / EORTC Пересмотр классификации микозов-грибков и синдромов Szary 9000 / 6ORTC 9000 / 6ORTC Определение стадии грибкового микоза и синдрома Сари
Определение стадии MF традиционно проводилось Американским объединенным комитетом по раку (AJCC), который определяет степень и характер поражений кожи, внекожное заболевание и лейкемическую трансформацию как прогностические факторы (таблицы 3 и 4). ).[6] Недавно Международное общество кожной лимфомы и Европейская организация по исследованию и лечению рака (ISCL / EORTC) предложили изменения к этой системе (таблицы 5 и 6), в том числе: 1) добавлен дескриптор «a / b». к заболеванию Т1 и Т2, где «а» обозначает только пятна, а «b» обозначает пятна и / или бляшки; 2) N2 указывает на ограниченное поражение узлов и N3 указывает на частичное или полное сглаживание узлов; 3) B0 представляет <5% лимфоцитов, вовлеченных в клетки Szary, ограниченное участие B1 в крови и значительное участие B2 в крови; 4) дескриптор «a / b», обозначающий отсутствие («a») или присутствие («b») популяции клональных Т-клеток в лимфатическом узле или крови, обнаруженных с помощью ПЦР (полимеразная цепная реакция) или саузерн-блоттинга.[7]
Обзор лечения
Кожно-направленная терапия является краеугольным камнем лечения МФ. У пациентов с кожно-ограниченным заболеванием только местная терапия может привести к ремиссии и даже излечению. Для пациентов с локализованным односторонним МФ только местные методы лечения обеспечивают долгосрочную выживаемость без признаков заболевания, превышающую 85% [8]. Для тех, у кого более одного пластыря или бляшки, но с поражением площади поверхности тела менее 10% (T1, N0 и T1, N1), только местные методы лечения обеспечивают долгосрочную выживаемость без заболевания в диапазоне от 30% до 50%.У пациентов с обширными пятнами или бляшками местная терапия нечасто приводит к длительной ремиссии. Такие пациенты должны получать интенсивную местную терапию для достижения полной ремиссии с последующей менее интенсивной адъювантной местной терапией для поддержания ремиссии. Существует несколько вариантов лечения для пациентов с опухолями, эритродермией, узловыми, висцеральными заболеваниями или заболеваниями крови. Следовательно, цели лечения включают смягчение кожных симптомов и контроль системного заболевания. Среди местных методов лечения тотальная электронно-лучевая терапия кожи (TSEBT) имеет самые высокие показатели полного ответа.[9,10] Для поддержания ремиссии следует назначать адъювантную системную и / или местную терапию. Трансплантация аллогенных стволовых клеток может стать излечивающим фактором для избранной группы населения. [11]
ТАБЛИЦА 7
Рекомендации по лечению грибкового микоза по стадиям
Далее следует полное обсуждение местных, системных и новых методов лечения, а в таблице 7 представлен полный список вариантов лечения.
Кожно-направленная терапия
Мехлорэтамин
Местный мехлорэтамин гидрохлорид (HN2), также известный как азотный иприт, представляет собой алкилирующий агент, используемый в качестве начальной терапии для лечения пятен и бляшек MF.Данные Стэнфордского университета демонстрируют 65% -ную частоту полного ответа, 45% 10-летнюю безрецидивную выживаемость и 95% 10-летнюю специфическую выживаемость у пациентов с болезнью T1, а также 34% -ную частоту полного ответа и 20% 10-летнюю выживаемость. лет безрецидивной выживаемости у пациентов с Т2 [12].
Ирритантный дерматит встречается примерно у 50% пациентов, получавших водный HN2, но его можно уменьшить, если азотистый иприт растворить в мази. [12] Другие токсические эффекты могут включать ксероз, гиперпигментацию и, в редких случаях, буллезные реакции и синдром Стивенса-Джонсона.Подавление костного мозга не вызывает беспокойства из-за минимальной системной абсорбции. Канцерогенность HN2 остается предметом дискуссий: в одной серии сообщается об отсутствии повышенного риска [12], а в другой — о восьмикратном увеличении риска немеланомного рака кожи [13]. HN2 может усиливать канцерогенность других методов лечения, включая TSEBT или псорален и ультрафиолетовое излучение A (PUVA). [14]
Кармустин
Кармустин для местного применения (BCNU), еще один алкилирующий агент, ассоциируется с частотой полного ответа 86% и 47% и 5-летней безрецидивной выживаемостью 35% и 10% для пациентов с T1 и T2, соответственно.[15] Поскольку кармустин системно всасывается и может вызывать угнетение костного мозга, его следует применять на
<10% тела, продолжительность лечения должна быть ограничена до 4 месяцев, а общий анализ крови пациентов следует контролировать, пока они находятся на приеме. терапия. Кожная гиперчувствительность встречается редко, но могут возникать телеангиэктазии и гиперпигментация.
Стероиды для местного применения
Высокоэффективные стероиды для местного применения, часто используемые в качестве терапии первой линии при заболеваниях T1 и T2, обеспечивают эффективное паллиативное лечение и могут вызвать регрессию поражения с полной степенью ответа 63% и 25% для пациентов с T1 и T2.[16] Применение ограничено активными поражениями, так как широкое применение может привести к снижению уровня кортизола в сыворотке крови. [16] Длительное использование может привести к атрофии кожи и телеангиэктазиям.
Рексиноиды для местного применения
Бексаротен — это рексиноид, производное витамина А, которое связывается с рецепторами ретиноидов X, что приводит к транскрипции генов, которые контролируют клеточную дифференцировку и пролиферацию. Гель Bexarotene был одобрен после того, как исследования фазы I / II продемонстрировали 44–54% ответ на лечение у пациентов с рефрактерным кожным МФ.[17,18] Может возникнуть ирритантный дерматит; поэтому бексаротен следует назначать пациентам с поражением поверхности тела менее 15%. Как и системные ретиноиды, бексаротен не рекомендуется во время беременности из-за его возможной тератогенности.
Светотерапия
Ультрафиолетовый свет, в том числе UVB (длина волны 320–290 нм), узкополосный UVB (длина волны 311 нм) и псорален плюс UVA (PUVA, длина волны 400–320 нм) используется в MF-терапии. Фотохимиотерапевтический агент 8-метоксипсорален (8-MOP) проглатывается до воздействия УФА.UVA активирует 8-MOP, что приводит к сшиванию ДНК и гибели клеток в результате апоптоза. Из-за ограниченного проникновения через кожу УФ-В предназначен для лечения тонких пятен и дает полный ответ примерно на 80% и среднюю продолжительность ответа 2 года [19]. ПУВА, проникая более глубоко, эффективно лечит некоторые поражения бляшками, обеспечивая полную реакцию на 80–100% для болезни T1 N0 и 60–100% для болезни T2, N0. [16,20] Хотя рецидивы являются обычным явлением, обычно требуется повторное лечение. успешный.Комбинированная терапия интерфероном-β является безопасной и связана с увеличением частоты полного ответа и продолжительности ответа при лечении болезни Т2. [21]
PUVA и UVB вводятся 2–3 дня в неделю. После достижения полного ответа частота лечения снижается до одного раза в 2-4 недели, а затем каждые 4-8 недель в течение нескольких лет. Острая токсичность включает эритему кожи, гиперпигментацию, ксероз, зуд, образование пузырей, фотостарение и повышенный риск рака кожи. Очки для глаз, которые носят во время сеансов лечения, могут снизить риск образования катаракты.Побочные эффекты терапии 8-MOP включают тошноту, рвоту и повышение уровня трансаминаз. Для пациентов с непереносимостью 8-MOP разумной альтернативой является местная «псораленовая ванна».
Лучевая терапия
Лучевая терапия может применяться локально к отдельному поражению или группе поражений или ко всей поверхности кожи через TSEBT. Частота полного ответа и долгосрочная выживаемость без признаков заболевания для локализованной лучевой терапии достигают 91% и 85%, соответственно. [22-24] Существует зависимость доза-реакция, с наилучшим успехом при дозах от 20 до 30 Гр.[22,23] Запас поля 1-2 см для местной лучевой терапии и низкая доза на фракцию, от 1,2 до 2,0 Гр в день, рекомендуется для минимизации поздних эффектов и сохранения переносимости кожи на случай дальнейшего дальнейшего облучения. требуется. Предпочтительно использовать одно поле излучения, хотя прилегающие поля часто требуются для обработки выпуклых поверхностей, таких как кожа головы, грудь, рука или ступня.
ЦЭБТ — комплексное лучевое лечение, эффективно лечящее МФ Т1–4 стадии. Для пациентов с ограниченным количеством пятен и бляшек TSEBT дает примерно 90% полного ответа.[1,25] TSEBT дает полный ответ примерно на 70–90% у пациентов с заболеванием T2 и от 50% до 100% у пациентов с заболеванием T3. [9,25,26] Для пациентов с обширными пятнами и бляшками. (T2, N0) и опухоли (T3, N0), TSEBT, по-видимому, предлагает лучшее искоренение заболевания и паллиативное лечение, но для пациентов с болезнью T3 следует рассмотреть возможность повышения. Одно исследование показало, что TSEBT приводит к более высокой частоте полных ответов, чем HN2 (76% против 39% для T2 и 44% против 8% для T3, соответственно), но не влияет на общую выживаемость.[9] У пациентов с эритродермией (T4, N0) TSEBT может вызвать полные ответы и может привести к увеличению продолжительности безрецидивной выживаемости у этих пациентов без вовлечения крови. [10] Рецидивы можно успешно спасти с помощью второго курса TSEBT. [27]
Длительная ремиссия не характерна для монотерапии ЦЭБТ. Однако адъювантная поддерживающая терапия HN2 или PUVA улучшает исходы при заболеваниях T1 и T2. В Стэнфорде 10-летний риск рецидива был 60% среди пациентов, получавших TSEBT с последующим HN2, по сравнению с 90% 10-летним риском рецидива среди пациентов, получавших только TSEBT.[9] Аналогичным образом, в Йельском университете у 7% пациентов с МФ T1 или T2, получавших поддерживающую ПУВА-терапию, наблюдался трехлетний рецидив, по сравнению с 43% пациентов, получавших только TSEBT. В то время как существуют ограниченные данные относительно адъювантной терапии заболевания T3 или T4, поддерживающая терапия с использованием HN2, [9] фотофореза, [28] интерферона-β, бексаротена или денилейкина дифтитокса является разумной. [29] Продолжительность адъювантной терапии точно не установлена.
РИСУНОК 2
Позиции для лечения тотальной электронно-лучевой терапии кожи
• TSEBT Technique- В Йельской программе TSEBT линейный ускоритель производит электроны с энергией 6 МэВ, когда пациент стоит 3.8 метров от портала. Пациенты размещаются в шести лечебных положениях, которые максимально раскрывают кожу и улучшают однородность дозы (рис. 2). Переднезадняя, правая задняя косая и левая задняя косые позиции обрабатываются в первый день лечения, а задне-передняя, правая передняя косая и левая передняя косая позиции обрабатываются той же дозой на второй день лечения. В течение 2-дневного цикла 2 Гр доставляется на всю поверхность кожи. Пациенты получают лечение 4 дня в неделю в течение 9 недель с общей дозой 36 Гр.
Процедура «Boost» для областей с недостаточной дозировкой включает подошвы ступней и промежность. Электронный отражатель над головой пациента обеспечивает соответствующую дозу на кожу головы. Другие недодозированные области, которые могут потребовать повышения, включают вентральный половой член, верхнюю часть медиальной части бедер, инфрамаммарные складки, панникулярные складки, а также боковые и более плоские области лица и туловища, а также опухоли толщиной более 4 мм. «Предварительные повышения» могут применяться для паллиативного облегчения болезненных или кровоточащих поражений, а дополнительные повышения могут применяться при стойких поражениях.И наоборот, руки, запястья, уши, лодыжки и дорсальный половой член могут быть передозированы и, следовательно, требуют экранирования, чтобы ограничить их дозу до ≤ 36 Гр. Также предусмотрена защита глаз и ногтей.
• TSEBT Toxicity — TSEBT обычно вызывает зуд, сухое шелушение, гиперпигментацию, алопецию, ксероз, пузыри или отек рук и ног, снижение потоотделения и потерю ногтей на руках и ногах. Долгосрочные осложнения, как правило, легкие и имеют курс из 36 фракций, но они могут включать стойкую дистрофию ногтей, ксероз, телеангиэктазии, частичную алопецию волосистой части головы и дизестезию кончиков пальцев.Возможно мужское бесплодие из-за поверхностного расположения яичек. Сообщалось о вторичном раке кожи, особенно у пациентов, подвергавшихся дополнительным потенциально канцерогенным препаратам, таким как PUVA или HN2. [14]
Системная терапия
Интерферон
Интерферон-± -2a (IFN-±; Альферон, роферон-А) является эффективным средством лечения пятен и бляшек благодаря его прямому противоопухолевому и иммуномодулирующему действию. [30] IFN-β ± можно использовать отдельно [31], но он обеспечивает более длительный ответ в сочетании с ретиноидами, PUVA [21] или экстракорпоральным фотоферезом.[32] Рандомизированное исследование с участием 82 пациентов показало, что IFN-β ± плюс PUVA дает полный ответ на 70% по сравнению с 38% у пациентов, получавших ацитретин (этретин, сориатан) плюс PUVA. [33] IFN-β может вызывать симптомы гриппа, психические расстройства, включая депрессию, трансаминит, миелосупрессию, протеинурию и миелопатию.
Ретиноиды
Пероральные ретиноиды, такие как изотретиноин и ацитретин, влияют на клеточную дифференцировку и могут безопасно комбинироваться с другими методами лечения, такими как PUVA, [34] IFN-β ± и TSEBT.[35] Частота ответов приближается к 60%, хотя процент полных ответов составляет менее 20%. [36] Побочные эффекты включают светочувствительность, ксероз, миалгию, головные боли, нарушение ночного зрения, помутнение роговицы, тератогенность, повышение уровня трансаминаз, гиперлипидемию и панкреатит.
Рексиноиды: Bexarotene
Пероральный бексаротен одобрен для всех стадий рефрактерной МФ и может безопасно сочетаться с другими методами лечения. [36] Фазы II и III испытаний перорального приема бексаротена пациентам с рефрактерным заболеванием в дозах 300 мг / м2 / день или выше показали 45% и 55% ответов и снижение как поражения кожи, так и зуда.[37] Комбинирование бексаротена с PUVA, фотофорезом или IFN-β может повысить частоту ответа до 69%. [38] До 80% пациентов страдают гипертриглицеридемией, что увеличивает риск панкреатита и атеросклероза. Центральный гипотиреоз поражает примерно 75% пролеченных пациентов. Следовательно, необходимо контролировать уровни холестерина и функции щитовидной железы. Другие побочные эффекты включают головные боли, легкую нейтропению и повышение уровня трансаминаз, шелушение кожи и зуд. Перед лучевой терапией прием бексаротена следует прекратить, поскольку комбинированная терапия может обострить кожные реакции.
Денилейкин Дифтитокс
Денилейкин дифтитокс — это внутривенный рекомбинантный гибридный белок, который объединяет дифтерийный токсин с рецептор-связывающей частью интерлейкина-2 (ИЛ-2) и одобрен для пациентов с МФ с рефрактерным заболеванием, клетки которых экспрессируют CD25. [39] Однако недавнее исследование показало частоту ответа и у CD25-отрицательных пациентов [40]. Связывание с рецептором IL-2 приводит к эндоцитозу дифтерийного токсина, ингибированию синтеза белка и гибели клеток. Введение денилейкина дифтитокса происходит в дни 1–5 каждые 3 недели до восьми циклов.Некоторые данные свидетельствуют о взаимосвязи доза-реакция: одно исследование фазы III показало частоту ответа 38% при 18 мкг / кг / день по сравнению с 10% при 9 мкг / кг / день и улучшение зуда на 68% [39]. ] Его можно комбинировать и иметь возможный синергетический эффект с бексаротином [41] и различными кожно-направленными препаратами для обеспечения долгосрочного контроля над заболеванием. [36]
В ранее упомянутом исследовании 21% пациентов выбыли из исследования из-за побочных эффектов: у 60% возникла реакция гиперчувствительности, у 25% — синдром утечки сосудов и у 11% — событие тромбоза.[39] Другие токсические эффекты включают конституциональные симптомы, инфекции, повышение уровня трансаминаз, почечную недостаточность, тиреоидит и лимфопению. Однако предварительная обработка кортикостероидами снижает риск острой токсичности [42].
Ингибиторы гистон-деацетилазы (HDAC)
Вориностат (Zolinza), ингибитор гистон-деацетилазы (HDAC), также известный как субероиланилидгидроксамовая кислота, увеличивает ацетилирование гистонов, что приводит к снижению доступности ядерной ДНК для связывания с факторами транскрипции.Снижение транскрипции снижает уровни внутриклеточного белка, что в конечном итоге приводит к остановке клеточного цикла и апоптозу. Вориностат одобрен для лечения прогрессирующего, стойкого или рецидивирующего МФ после лечения как минимум двумя предшествующими системными терапиями. Первое опубликованное исследование вориностата фазы II показало, что дозировка 400 мг в день является наилучшей переносимой дозой [43]. В этом исследовании у 24% пациентов был частичный ответ, и почти половина сообщила об улучшении зуда. Второе испытание фазы II у рефрактерных пациентов с МФ, стадия IB – IVA, показало общую частоту ответа 36% и продолжительность ответа 26 недель.[44] Кроме того, 32% испытали облегчение зуда. Некоторые данные предполагают синергетический эффект с денилейкином дифтитоксом или ингибиторами метилирования. [36] Ромидепсин (Istodax), новый многообещающий ингибитор HDAC, дал общий ответ 34% и продолжительность ответа 13,7 месяца у 71 пациента с рефрактерным заболеванием> IIB [45]. Ромидепсин одобрен для лечения кожной Т-клеточной лимфомы, резистентной по крайней мере к одной предшествующей системной терапии. Побочные эффекты включают диарею, тошноту, усталость и тромбоцитопению, а также возможную прологацию QTc.В вышеупомянутом исследовании у нескольких пациентов наблюдалась токсичность> 3 степени на вориностате, однако у 5% наблюдалась легочная эмболия [43].
Экстракорпоральная фотохимиотерапия
Экстракорпоральный фотофорез — это иммунная терапия, используемая при лечении эритродермического МФ и / или синдрома Сари, при которой лейкоциты удаляются с помощью лейкафереза в сочетании с 8-МОП, подвергаются воздействию ультрафиолета А и повторно вводятся пациенту через два последовательных дней каждые 2–4 недели или чаще, если у пациента обширное заболевание.[46,47] Этот процесс, как полагают, приводит к перекрестному связыванию ДНК Т-клеток и, в конечном итоге, к апоптозу собранных Т-клеток MF. Общая доля ответов составляет около 50%, а доля полных ответов — около 15%. [36] Как правило, перенос жидкости переносится хорошо, но он может привести к гипотонии, аритмии и сердечной недостаточности. Экстракорпоральный фотофорез безопасно комбинируется с IFN-β, бексаротеном и TSEBT. [28,32,36]
Системная химиотерапия
Системная химиотерапия предназначена для прогрессирующих или рефрактерных МФ.Частота ответа обычно высока для монотерапии или комбинированной терапии, однако ответы кратковременны и могут быть связаны со значительной токсичностью, включая миелосупрессию и бактериемию. [36,48] При запущенном заболевании исследование фазы II показало общую скорость ответа. 80%, но имелся высокий профиль токсичности: 61% испытывали нейтропению> 3 степени и 40% испытывали бактериемию. [48] Кроме того, в рандомизированном исследовании, сравнивающем одновременную терапию TSEBT и системную химиотерапию с последовательной местной терапией, 23% пациентов, получавших химиотерапию, требовали госпитализации.[49] Нет данных, свидетельствующих о том, что комбинированная химиотерапия превосходит последовательную терапию, а комбинированная терапия имеет повышенную токсичность.
Типичные химиотерапевтические агенты включают пероральные агенты, такие как метотрексат, этопозид (Toposar, VePesid) или хлорамбуцил, которые позволяют избежать необходимости в центральных венозных линиях и связанного с этим риска бактериемии, но несут нейтропению как риск. Пегилированный липосомальный доксорубицин (Доксил) связан с более низким риском миелосупрессии и кардиотоксичности, чем традиционный доксорубицин, и в исследованиях он дает 88% -ный общий ответ без каких-либо серьезных побочных эффектов.[50] Гемцитабин (Gemzar), аналог нуклеозидов, продемонстрировал частоту полного ответа до 23% и общую частоту ответа около 70% при ограниченной миелосупрессии 3-4 степени. [51] Гемцитабин связан с обратимой гепатотоксичностью. Пентостатин (Нипент), аналог пурина, продемонстрировал частоту ответа 54%, но он более эффективен у пациентов с синдромом Сари, чем у пациентов с прогрессирующим МФ [52]. Флударабин (Флудара), аналог пиримидина, не показал таких перспектив.
Высокодозная химиотерапия с последующей трансплантацией костного мозга
Справочное руководство
Терапевтические агенты
Упомянутые в этой статье
Ацитретин (этретин, сориатан)
Алемтузумаб (кампат)
Таргретин, гель (
Таргаротин, гель) )
Кармустин
Денилейкин дифтитокс (Онтак)
Этопозид (Топосар, Вепесид)
Флударабин (Флудара)
Гемцитабин (Гемзар)
Интерферон-Î ±
Интерферон-±
Интерферон-Î ± ± -2a (Ленферон-Револимид) 90 (Алонферон-Рофферон) Револимид 90 (Аленферон-Рофферон, Револимид)
Мехлорэтамин [азотный горчичный]
Пероральный бексаротен (таргретин)
Пегилированный липосомальный доксорубицин
(Доксил)
Пентостатин (Нипент)
Пралатрексат (Фолотин)
Ромидепсин (
-вородинстат) Торговые марки указываются в скобках только в том случае, если лекарство не доступно в общем виде и продается не более чем как два товарных знака или зарегистрированных продуктов.В скобках также могут быть включены более знакомые альтернативные общие обозначения.
Хотя существуют ограниченные данные относительно использования высоких доз химиотерапии с аутологичным или аллогенным трансплантатом для лечения прогрессирующего рефрактерного МФ, аллогенный трансплантат может быть целесообразным для избранных более молодых пациентов. Хотя трансплантация аутологичных стволовых клеток дает высокий уровень полного ответа, рецидив в течение 1 года является обычным явлением. [53] Напротив, аллогенные трансплантаты могут привести к продолжительному безрезультатному выживанию.Онкологический центр «Город надежды» сообщил о восьми пациентах с рефрактерным МФ, которые прошли предварительное лечение и перенесли аллогенную трансплантацию [11]. Однако два пациента умерли, остальные шесть были живы без признаков лимфомы в среднем через 56 месяцев после трансплантации.
Emerging Therapies
Пралатрексат (Folotyn), аналог фолиевой кислоты, такой как метотрексат, обладает большей цитотоксичностью, чем метотрексат, из-за более высокого сродства к пониженному переносчику фолиевой кислоты и повышенной полиглутамации. [54] В исследовании с участием 11 пациентов общая частота ответа составила 45% с несколькими ответами только после одного цикла приема пралатрексата.Отмечено несколько случаев гематологической токсичности. [55] Цитокины, в том числе интерлейкин-12, интерлейкин-2, перспективны при лечении МФ. [29,56] В предварительном исследовании фазы II леналидомид (Ревлимид), усилитель клеточного иммунитета Т-хелпера 1, одобрен для лечения миелодиспластического синдрома. и множественная миелома, показали многообещающие результаты у трех из восьми пациентов с кожной Т-клеточной лимфомой. [57] Ингибитор протеосом бортезомиб (Велкейд) является многообещающим, с показателем ответа, приближающимся к 67%, и отсутствием токсичности 4 степени в исследовании фазы II у 12 пациентов с рецидивирующей рефрактерной кожной Т-клеточной лимфомой или периферической Т-клеточной лимфомой.[58] Фородезин (также известный как иммуциллин-H), ингибитор пуриновой нуклеозидфосфорилазы, приводит к истощению Т-клеток и апоптозу, и он дал многообещающие результаты с ограниченной токсичностью у пациентов с рефрактерным заболеванием. [59] Алемтузумаб (Campath), моноклональное антитело, нацеленное на CD52, проявляет активность в этой популяции пациентов, но несет в себе риск оппортунистической инфекции. [60,61] Занолимумаб (HuMax-CD4), моноклональное антитело к CD4, приводит к меньшему количеству инфекций и ранние исследования были связаны с частотой ответа 50% и средней продолжительностью ответа 81 неделя.[62]
Резюме
Диагностика и лечение грибовидных микозов представляют собой серьезную проблему из-за различных клинических проявлений грибовидных микозов и многочисленных доступных терапевтических методов. Следовательно, необходим междисциплинарный подход. Последнее десятилетие принесло значительные успехи в области диагностики и классификации патологий, что привело к разработке новой, целевой и биологической терапии. Будущее обещает дальнейшие клинические успехи, которые в конечном итоге должны привести к улучшению контроля над заболеванием и повышению качества жизни пациентов с грибовидным микозом.
Раскрытие финансовой информации: Авторы не имеют значительных финансовых интересов или других отношений с производителями каких-либо продуктов или поставщиками каких-либо услуг, упомянутых в этой статье.
Ссылки:
Ссылки
1. Kim YH, Jensen RA, Watanabe GL, et al: Клиническая стадия Ia (ограниченное пятно и бляшка) грибовидный микоз. Анализ долгосрочных результатов. Arch Dermatol 132: 1309-1313, 1996.
2.Kim YH, Chow S, Varghese A, et al: Клинические характеристики и долгосрочные исходы пациентов с грибовидным микозом генерализованных пятен и / или бляшек (T2). Arch Dermatol 135: 26-32, 1999.
3. Ким YH, Hoppe RT: грибовидный микоз и синдром Сезари. Semin Oncol 26: 276-289, 1999.
4. Criscione VD, Weinstock MA: Заболеваемость кожной Т-клеточной лимфомой в США, 1973-2002. Arch Dermatol 143: 854-859, 2007.
5.Пимпинелли Н., Олсен Е.А., Сантуччи М. и др.: Определение ранних грибовидных микозов. J Am Acad Dermatol 53: 1053-1063, 2005.
6. Грин, Флорида, Пейдж DL, Флеминг И.Д. и др.: Руководство по стадированию рака AJCC, 6-е изд. New York, Springer, 2002.
7. Olsen E, Vonderheid E, Pimpinelli N и др.: Изменения в постановке и классификации грибовидного микоза и синдрома Сезари: предложение Международного общества кожных лимфом (ISCL) и Целевая группа по кожной лимфоме Европейской организации исследования и лечения рака (EORTC). Кровь 110: 1713-1722, 2007.
8. Heald PW, Glusac EJ: Однородная кожная Т-клеточная лимфома: клинические особенности, терапия и последующее наблюдение за 10 пациентами с чувствительным к лечению вариантом грибовидного микоза. J Am Acad Dermatol 42: 283-285, 2000.
9. Chinn DM, Chow S, Kim YH, et al: Тотальная электронно-лучевая терапия кожи с или без адъювантного местного азотного иприта или только азотистого иприта в качестве начального лечения Грибовидный микоз Т2 и Т3. Int J Radiat Oncol Biol Phys 43: 951-958, 1999.
10. Джонс Г. В., Розенталь Д., Уилсон Л. Д.: Общее электронное излучение кожи для пациентов с эритродермической кожной Т-клеточной лимфомой (грибовидный микоз и синдром Сезари). Cancer 85: 1985-1995, 1999.
11. Молина А., Заин Дж., Арбер Д.А. и др.: Устойчивые клинические, цитогенетические и молекулярные ремиссии после трансплантации аллогенных гемопоэтических клеток при рефрактерном синдроме Сезари и грибовидном микозе. J Clin Oncol 23: 6163-6171, 2005.
12.Kim YH, Martinez G, Varghese A, et al: Актуальный азотный иприт в лечении грибкового микоза: обновление опыта Стэнфордского университета. Arch Dermatol 139: 165-173, 2003.
13. Vonderheid EC, Tan ET, Kantor AF и др.: Долгосрочная эффективность, лечебный потенциал и канцерогенность местной химиотерапии мехлорэтамином при кожной Т-клеточной лимфоме. J Am Acad Dermatol 20: 416-428, 1989.
14. Licata AG, Wilson LD, Braverman IM, et al: Злокачественная меланома и другие вторичные кожные злокачественные новообразования при Т-клеточной лимфоме кожи.Влияние дополнительной терапии после тотального облучения кожи электронным пучком. Arch Dermatol , 131: 432-435 1995.
15. Zackheim HS, Epstein EH, Jr., Crain WR: Местный кармустин (BCNU) при кожной Т-клеточной лимфоме: 15-летний опыт лечения 143 пациентами. J Am Acad Dermatol 22: 802-810, 1990.
16. Zackheim HS, Kashani-Sabet M, Amin S: Актуальные кортикостероиды для лечения грибкового микоза. Опыт у 79 пациентов. Arch Dermatol 134: 949-954, 1998.
17. Бренеман Д., Дувик М., Кузель Т. и др.: Фазы 1 и 2 испытания геля бексаротена для кожно-направленного лечения пациентов с кожной Т-клеточной лимфомой. Arch Dermatol 138: 325-332, 2002.
18. Heald P, Mehlmauer M, Martin AG и др.: Местная терапия бексаротином для пациентов с рефрактерной или стойкой кожной Т-клеточной лимфомой на ранней стадии: результаты фазы III клиническое испытание. J Am Acad Dermatol 49: 801-815, 2003.
19. Diederen PV, van Weelden H, Sanders CJ, et al: Узкополосный УФB и псорален-УФA в лечении грибкового микоза на ранних стадиях: ретроспективное исследование . J Am Acad Dermatol 48: 215-219, 2003.
20. Herrmann JJ, Roenigk HH, Jr., Hurria A, et al: Лечение грибовидного микоза фотохимиотерапией (PUVA): долгосрочное наблюдение. J Am Acad Dermatol 33: 234-242, 1995.
21. Chiarion-Sileni V, Bononi A, Fornasa CV и др.: Испытание фазы II интерферона-альфа-2a плюс псоларен с ультрафиолетовым светом A у пациентов с кожная Т-клеточная лимфома. Cancer 95: 569-575, 2002.
22. Wilson LD, Kacinski BM, Jones GW: Местная поверхностная лучевая терапия в лечении кожной Т-клеточной лимфомы минимальной стадии IA (грибовидный микоз). Int J Radiat Oncol Biol Phys 40: 109-115, 1998.
23. Микали Б., Миямото С., Кантор Г. и др.: Лучевая терапия при одностороннем грибковом микозе. Int J Radiat Oncol Biol Phys 42: 361-364, 1998.
24. Wong R, Jones G, Farrar N, et al: Местная поверхностная лучевая терапия (LSRT) для недавно диагностированной стадии ia грибовидного микоза пятен-бляшек (MF ) только с одним, двумя или тремя поражениями. Int J Radiat Oncol Biol Phys 57 Приложение 1: S289-S290, 2003.
25. Джонс Г.В., Хоппе Р.Т., Глатштейн Э.: Электронно-лучевое лечение кожной Т-клеточной лимфомы. Hematol Oncol Clin North Am 9: 1057-1076, 1995.
26. Quiros PA, Kacinski BM, Wilson LD: Степень поражения кожи как прогностический индикатор отсутствия болезни и общей выживаемости пациентов с T3 кожными Т-клетками лимфома лечится с помощью тотальной лучевой терапии кожи электронным пучком. Cancer 77: 1912-1917, 1996.
27. Wilson LD, Quiros PA, Kolenik SA и др.: Дополнительные курсы тотальной электронно-лучевой терапии кожи при лечении пациентов с рецидивирующей кожной Т-клеточной лимфомой. J Am Acad Dermatol 35: 69-73, 1996.
28. Wilson LD, Jones GW, Kim D, et al: Опыт тотальной электронно-лучевой терапии кожи в сочетании с экстракорпоральным фотоферезом при ведении пациентов с эритродермией ( Т4) грибовидный микоз. J Am Acad Dermatol 43: 54-60, 2000.
29. Rook AH, Kuzel TM, Olsen EA: Цитокиновая терапия кожной Т-клеточной лимфомы: интерфероны, интерлейкин-12 и интерлейкин-2. Hematol Oncol Clin North Am 17: 1435-1448, 2003.
30. Росс К., Тингсгаард П., Йоргенсен Х. и др.: Лечение кожной Т-клеточной лимфомы интерфероном. Eur J Haematol 51: 63-72, 1993.
31. Jumbou O, N’Guyen JM, Tessier MH, et al: Долгосрочное наблюдение за 51 пациентом с грибовидным микозом и синдромом Сезари, получавшим лечение интерферон-альфа. Br J Dermatol 1999; 140: 427-431.
32. Wollina U, Looks A, Meyer J, et al: Лечение кожной Т-клеточной лимфомы II стадии интерфероном альфа-2a и экстракорпоральной фотохимиотерапией: проспективное контролируемое исследование. J Am Acad Dermatol 44: 253-260, 2001.
33. Stadler R, Otte HG, Luger T и др.: Проспективное рандомизированное многоцентровое клиническое исследование использования интерферона-2а плюс ацитретин по сравнению с интерфероном-2а и ПУВА у пациентов с кожной Т-клеточной лимфомой I и II стадии. Кровь 92: 3578-3581, 1998.
34. Томсен К., Хаммар Н., Молин Л. и др.: Ретиноиды плюс ПУВА (RePUVA) и ПУВА при грибовидном микозе, стадия налета. Отчет Скандинавской группы грибковых микозов. Acta Derm Venereol 69: 536-538, 1989.
35. Jones G, McLean J, Rosenthal D, et al: Комбинированное лечение пероральным этретинатом и электронно-лучевой терапией у пациентов с кожной Т-клеточной лимфомой (грибовидный микоз и др.). Синдром Сезары). J Am Acad Dermatol 26: 960-967, 1992.
36. Duvic M: Системная монотерапия против комбинированной терапии для CTCL: Обоснование и будущие стратегии. Oncology (Williston Park) 21: 33-40, 2007.
37. Duvic M, Martin AG, Kim Y, et al: Фаза 2 и 3 клинических испытаний перорального бексаротена (капсул таргретина) для лечения рефрактерных или персистирующая кожная Т-клеточная лимфома на ранней стадии. Arch Dermatol 137: 581-593, 2001.
38. Talpur R, Ward S, Apisarnthanarax N, et al: Оптимизация терапии бексаротеном для кожной Т-клеточной лимфомы. J Am Acad Dermato l 47: 672-684, 2002.
39. Olsen E, Duvic M, Frankel A, et al: Основное испытание фазы III двух уровней доз денилейкина дифтитокса для лечения кожных Т-лимфоцитов. лимфома. J Clin Oncol 19: 376-388, 2001.
40. Negro-Vilar A: Эффективность и безопасность денилютоксина дифититокса (DD) в фазе III двойного слепого плацебо-контролируемого исследования CD25 + пациентов с кожным T- клеточная лимфома (CTCL). J Clin Oncol 25: 447s, 2007.
41. Foss F, Demierre MF, DiVenuti G: испытание фазы 1 бексаротена и денилейкина дифтитокса у пациентов с рецидивирующей или рефрактерной кожной Т-клеточной лимфомой. Blood 106: 454-457, 2005.
42. Foss FM, Bacha P, Osann KE, et al: Биологические корреляты событий острой гиперчувствительности с DAB (389) IL-2 (denileukin diftitox, Ontak) в кожном T -клеточная лимфома: снижение частоты и тяжести при премедикации стероидами. Clin Lymphoma 1: 298-302, 2001.
43. Duvic M, Talpur R, Ni X и др.: Испытание фазы 2 перорального вориностата (субероиланилид гидроксамовая кислота, SAHA) при резистентной кожной Т-клеточной лимфоме (CTCL). Blood 109: 31-39, 2007.
44. Olsen EA, Kim YH, Kuzel TM, et al: Фаза IIb многоцентрового исследования вориностата у пациентов с персистирующей, прогрессирующей или резистентной к лечению кожной Т-клеточной лимфомой. J Clin Oncol 25: 3109-3115, 2007.
45. Piekarz RL, Frye R, Turner M, et al: Фаза II мультиинституционального испытания ингибитора гистондеацетилазы ромедепсина в качестве монотерапии для пациентов с кожными Т-клетками лимфома. J Clin Oncol 27: 5410-5417, 2009.
46. Лим Х.В., Эдельсон Р.Л .: Фотоферез для лечения кожной Т-клеточной лимфомы. Hematol Oncol Clin North Am 9: 1117-1126, 1995.
47. Хилд П., Рук А., Перес М. и др.: Лечение эритродермической кожной Т-клеточной лимфомы экстракорпоральной фотохимиотерапией. J Am Acad Dermatol 27: 427-433, 1992.
48. Akpek G, Koh HK, Bogen S, et al: Химиотерапия этопозидом, винкристином, доксорубицином, болюсным циклофосфамидом и пероральным преднизоном у пациентов с рефрактерным кожным тестостероном. -клеточная лимфома. Cancer 86: 1368-1376, 1999.
49. Kaye FJ, Bunn PA, Jr., Steinberg SM, et al: рандомизированное исследование, сравнивающее комбинацию электронно-лучевой радиации и химиотерапии с местной терапией при начальном лечении микоза. фунгоиды. N Engl J Med 321: 1784-1790, 1989.
50. Wollina U, Dummer R, Brockmeyer NH, et al: Многоцентровое исследование пегилированного липосомального доксорубицина у пациентов с Т-клеточной лимфомой кожи. Рак 98: 993-1001, 2003.
51.Марчи Э., Алинари Л., Тани М. и др.: Гемцитабин в качестве переднего лечения кожной Т-клеточной лимфомы: исследование фазы II с участием 32 пациентов. Cancer 104: 2437-2441 2005.
52. Tsimberidou AM, Giles F, Duvic M, et al: Фаза II исследования пентостатина при распространенных злокачественных опухолях Т-клеточного лимфоида: обновление серии онкологических центров M.D. Anderson. Cancer 100: 342-349, 2004.
53. Russell-Jones R, Child F, Olavarria E, et al: Трансплантация аутологичных стволовых клеток периферической крови при грибовидном микозе на стадии опухоли: предикторы выживаемости без болезней. Ann NY Acad Sci 941: 147-154, 2001.
54. Wang ES, O’Connor O, She Y, et al: Активность нового антифолата (PDX, 10-пропаргил 10-дезазааминоптерин) против лимфома человека превосходит метотрексат и коррелирует с экспрессией гена RFC-1 в опухоли. Leuk Lymphoma 44: 1027-1035, 2003.
55. Horwitz S, Duvic M, Kim Y, et al: Низкие дозы пралатрексата (PDX) активны при кожных Т-клеточных лимфомах: предварительные результаты мульти- исследование центра по подбору дозы (аннотация 261). Ann Oncol 19 (приложение 4): iv162, 2008.
56. Querfeld C, Rosen ST, Guitart J, et al: Испытание фазы II подкожных инъекций человеческого рекомбинантного интерлейкина-2 для лечения грибкового микоза и Sosis © Жарский синдром. J Am Acad Dermatol 56: 580-583, 2007.
57. Querfeld C, Kuzel TM, Guitart J, et al: Предварительные результаты исследования фазы II CC-5013 (леналидомид, Ревлимид) у пациентов с кожным T -клеточная лимфома (аннотация 3351). Кровь 106: 936A-937A, 2005.
58. Зинзани П.Л., Мусурака Г., Тани М. и др.: Фаза II испытания ингибитора протеасом бортезомиба у пациентов с рецидивирующей или резистентной кожной Т-клеточной лимфомой. J Clin Oncol 25: 4293-4297, 2007.
59. Duvic M, Foss F, Olsen E, et al: Ответ на пероральный прием фородезина при резистентной кожной Т-клеточной лимфоме: промежуточные результаты исследования фазы I / II. (аннотация 122). Кровь 110: 2007.
60. Ruuls SR, Lammerts van Bueren JJ, van de Winkel JG, et al: Новые терапевтические препараты с человеческими антителами: эпоха Umabs. Biotechnol J 3: 1157-1171, 2008.
61. Берненго М.Г., Куаглино П., Комессатти А. и др.: Периодический прием низких доз алемтузумаба в лечении синдрома Сезари: клинические и иммунологические результаты у 14 пациентов. Haematologica 92: 784-794, 2007.
62. Kim YH, Duvic M, Obitz E, et al: Клиническая эффективность занолимумаба (HuMax-CD4): два исследования фазы 2 при резистентной кожной Т-клеточной лимфоме. Кровь 109: 4655-4662, 2007.
63. Смит Б.Д., Уилсон Л.Д.: Управление грибковыми микозами.Часть 1. Диагностика, стадия и прогноз. Онкология (Уиллистон Парк) 17: 1281-1288, 2003.
64. Смит Б.Д., Уилсон Л.Д.: Управление грибовидным микозом: Часть 2. Лечение. Oncology (Williston Park) 17: 1419-1428, 2003.
Какова клиническая история классического грибовидного микоза кожной Т-клеточной лимфомы (CTCL)?
Виллемзе Р., Яффе Э.С., Бург Г. и др. Классификация ВОЗ-EORTC для кожных лимфом. Кровь . 2005 15 мая. 105 (10): 3768-85.[Медлайн].
Виллемзе Р., Серрони Л., Кемпф В., Берти Е., Факкетти Ф., Свердлов С.Х. и др. Обновление 2018 г. классификации ВОЗ-EORTC для первичных кожных лимфом. Кровь . 2019 18 апреля. 133 (16): 1703-1714. [Медлайн]. [Полный текст].
Ливингстон И., Рамамурти С., Драммонд С., Кемп Э., Робертс Ф. Перфорация роговицы из-за лимбального поражения при синдроме Сезари. Офтальмол Грэфес Арч Клин Экспер . 2011 Июль 249 (7): 1091-4.[Медлайн].
Vonderheid EC, Bernengo MG, Burg G, et al. Обновленная информация о эритродермической кожной Т-клеточной лимфоме: отчет Международного общества кожных лимфом. J Am Acad Dermatol . 2002, январь, 46 (1): 95-106. [Медлайн].
Karube K, Aoki R, Nomura Y, et al. Полезность проточной цитометрии для дифференциальной диагностики предшественников и периферических Т-клеточных и NK-клеточных лимфом: анализ 490 случаев. Патол Инт .2008 Февраль 58 (2): 89-97. [Медлайн].
Olsen E, Vonderheid E, Pimpinelli N, et al. Изменения в постановке и классификации грибовидного микоза и синдрома Сезари: предложение Международного общества кожных лимфом (ISCL) и целевой группы по кожным лимфомам Европейской организации исследования и лечения рака (EORTC). Кровь . 2007 сентябрь 15. 110 (6): 1713-22. [Медлайн].
Kaye FJ, Bunn PA Jr, Steinberg SM, et al.Рандомизированное исследование, сравнивающее комбинацию электронно-лучевой радиации и химиотерапии с местной терапией при начальном лечении грибовидного микоза. N Engl J Med . 1989, 28 декабря. 321 (26): 1784-90. [Медлайн].
Хофф Н.П., Гроффик А., Мота Р. и др. [Успешное использование трансплантации аллогенных стволовых клеток для лечения резистентных к лечению грибовидных микозов]. Hautarzt . 2008 Октябрь 59 (10): 779-82. [Медлайн].
Rook AH, Yoo EK, Grossman DJ, Kao DM, Fox FE, Niu Z.Использование модификаторов биологического ответа при лечении кожной Т-клеточной лимфомы. Curr Opin Oncol . 1998 марта 10 (2): 170-4. [Медлайн].
Querfeld C, Rosen ST, Guitart J, Kuzel TM. Спектр кожных Т-клеточных лимфом: новые взгляды на биологию и терапию. Curr Opin Hematol . 2005 июл.12 (4): 273-8. [Медлайн].
Duvic M, Cather JC. Новые методы лечения кожной Т-клеточной лимфомы. Дерматол Клин .2000 января 18 (1): 147-56. [Медлайн].
Foss FM, Kuzel TM. Новые подходы к лечению кожной Т-клеточной лимфомы. Резолюция по лечению рака . 1999. 99: 227-40. [Медлайн].
Herrmann JJ, Roenigk HH Jr, Hönigsmann H. Ультрафиолетовое излучение для лечения кожной Т-клеточной лимфомы. Гематол Онкол Клин Норт Ам . 1995 октября, 9 (5): 1077-88. [Медлайн].
Zackheim HS. Кожная Т-клеточная лимфома: обновление лечения. Дерматология . 1999. 199 (2): 102-5. [Медлайн].
Синха А.А., Хилд П. Успехи в лечении кожной Т-клеточной лимфомы. Дерматол Клин . 1998 16 апреля (2): 301-11. [Медлайн].
Гарднер JM, Эванс KG, Musiek A, Rook AH, Kim EJ. Обновленная информация о лечении кожной Т-клеточной лимфомы. Curr Opin Oncol . 2009 21 марта (2): 131-7. [Медлайн].
Prince HM, Whittaker S, Hoppe RT.Как лечить грибовидный микоз и синдром Сезари. Кровь . 2009, 12 ноября. 114 (20): 4337-53. [Медлайн].
Ramsay DL, Meller JA, Zackheim HS. Местное лечение ранней кожной Т-клеточной лимфомы. Гематол Онкол Клин Норт Ам . 1995 Октябрь 9 (5): 1031-56. [Медлайн].
Рассел-Джонс Р. Экстракорпоральный фотоферез при кожной Т-клеточной лимфоме. Несогласованные данные подчеркивают необходимость рандомизированных исследований. Br J Дерматол .2000, январь, 142 (1): 16-21. [Медлайн].
Fukushima T, Horio K, Matsuo E, et al. Успешная трансплантация пуповинной крови при грибковом микозе. Инт Дж. Гематол . 2008 декабрь 88 (5): 596-8. [Медлайн].
Olsen EA, Rook AH, Zic J, et al. Синдром Сезари: иммунопатогенез, обзор литературы о вариантах лечения и рекомендации по терапии Консорциума кожных лимфом США (USCLC). J Am Acad Dermatol .2011 Февраль 64 (2): 352-404. [Медлайн].
Diamandidou E, Cohen PR, Kurzrock R. грибовидный микоз и синдром Сезари. Кровь . 1 октября 1996 г. 88 (7): 2385-409. [Медлайн].
Koh HK, Charif M, Weinstock MA. Эпидемиология и клинические проявления кожной Т-клеточной лимфомы. Гематол Онкол Клин Норт Ам . 1995 Октябрь 9 (5): 943-60. [Медлайн].
Carbone A, Bernardini L, Valenzano F, et al.Сравнительная геномная гибридизация на основе массивов при грибовидных микозах на ранних стадиях: повторяющаяся делеция генов-супрессоров опухолей BCL7A, SMAC / DIABLO и RHOF. Гены Хромосомы Рака . 2008 декабрь 47 (12): 1067-75. [Медлайн].
ван Дорн Р., ван Кестер М.С., Дейкман Р. и др. Онкогеномный анализ грибовидного микоза показывает основные отличия от синдрома Сезари. Кровь . 2009 г. 1. 113 (1): 127-36. [Медлайн].
Виллемзе Р., Керл Н., Стерри В. и др.Классификация первичных кожных лимфом по EORTC: предложение Исследовательской группы кожных лимфом Европейской организации по исследованию и лечению рака. Кровь . 1 июля 1997 г. 90 (1): 354-71. [Медлайн].
Виллемзе Р., Мейер С.Дж. Классификация первичных кожных лимфом EORTC: сравнение с R.E.A.L. Классификация и предлагаемая классификация ВОЗ. Энн Онкол . 2000. 11 Прил. 1: 11-5. [Медлайн].
Ким Й.Х., Виллемзе Р., Пимпинелли Н., Уиттакер С., Олсен Э.А., Ранки А. и др.Система классификации TNM для первичных кожных лимфом, отличных от грибовидного микоза и синдрома Сезари: предложение Международного общества кожных лимфом (ISCL) и Целевой группы по кожным лимфомам Европейской организации исследования и лечения рака (EORTC). Кровь . 2007 15 июля. 110 (2): 479-84. [Медлайн].
Hoque SR, Child FJ, Whittaker SJ, et al. Подкожная панникулитоподобная Т-клеточная лимфома: клинико-патологический, иммунофенотипический и молекулярный анализ шести пациентов. Br J Дерматол . 2003 Март 148 (3): 516-25. [Медлайн].
Massone C, Chott A, Metze D, Kerl K, Citarella L, Vale E, et al. Подкожные, бластные естественные киллеры (NK), NK / T-клетки и другие цитотоксические лимфомы кожи: морфологическое, иммунофенотипическое и молекулярное исследование 50 пациентов. Am J Surg Pathol . 2004, 28 июня (6): 719-35. [Медлайн].
Burg G, Kempf W. Этиология и патогенез кожных лимфом.Burg G, Kempf W. Кожные лимфомы . Лондон: Тейлор и Фрэнсис; 2005.
Burg G, Dummer R, Wilhelm M, et al. Подкожная дельта-положительная Т-клеточная лимфома, продуцирующая гамма-интерферон. N Engl J Med . 1991, 10 октября. 325 (15): 1078-81. [Медлайн].
Burg G, Kempf W., Cozzio A, et al. Кожные злокачественные лимфомы: обновление 2006 г. J Dtsch Dermatol Ges . 2006 г., 4 (11): 914-33. [Медлайн].
Beltzung F, Ortonne N, Pelletier L, Beylot-Barry M, Ingen-Housz-Oro S, Franck F, et al.Первичные кожные CD4 + малые / средние Т-клеточные лимфопролиферативные заболевания: клиническое, патологическое и молекулярное исследование 60 случаев с единичным поражением: многоцентровое исследование Французской группы изучения кожной лимфомы. Am J Surg Pathol . 2020 7 апреля [Medline].
Jaffe ES, Krenacs L, Raffeld M. Классификация лимфом цитотоксических Т-клеток и естественных киллерных клеток. Семин Гематол . 2003 июл. 40 (3): 175-84. [Медлайн].
Эль-Шабрави-Каэлен Л., Серрони Л., Керл Х.Клинико-патологический спектр цитотоксических лимфом кожи. Семин Кутан Мед Сург . 2000 июн.19 (2): 118-23. [Медлайн].
Миямото Т., Йошино Т., Такехиса Т., Хагари Ю., Михара М. Кожные проявления носовой / назальной лимфомы Т / NK-клеток: клинико-патологические данные четырех случаев. Br J Дерматол . 1998 сентябрь 139 (3): 481-7. [Медлайн].
Колер С. Экстранодальная NK / Т-клеточная лимфома носового типа. LeBoit P, Burg G, Weedon D, Lyon SA. Книги ВОЗ: Опухоли кожи . Женева: Всемирная организация здравоохранения МАИР; X. 2006. 191-2.
Kim ST, Sim HJ, Jeon YS, Lee JW, Roh HJ, Choi SY, et al. Клинико-патологические особенности и данные о перестройке генов Т-клеточных рецепторов грибовидного микоза у пациентов моложе 20 лет. Дж Дерматол . 2009 Июль 36 (7): 392-402. [Медлайн].
Берти Е., Томазини Д., Вермеер М. Х., Мейер С. Дж., Алесси Е., Виллемзе Р. Первичные кожные CD8-положительные эпидермотропные цитотоксические Т-клеточные лимфомы.Выраженная клинико-патологическая сущность с агрессивным клиническим поведением. Ам Дж. Патол . 1999, август, 155 (2): 483-92. [Медлайн]. [Полный текст].
Кемпф В., Остхерен-Михаэлис С., Паулли М. и др. Гранулематозный грибовидный микоз и гранулематозная дряблая кожа: многоцентровое исследование Целевой группы по гистопатологии кожных лимфом Европейской организации по исследованию и лечению рака (EORTC). Дерматол Арки . 2008 декабрь 144 (12): 1609-17.[Медлайн].
Юмин С., Жирарди М. Взгляд на молекулярные и клеточные основы кожной Т-клеточной лимфомы. Йельский университет, биол. Медицина . 2020 Март 93 (1): 111-121. [Медлайн]. [Полный текст].
Girardi M, Heald PW, Wilson LD. Патогенез грибовидного микоза. N Engl J Med . 2004 May 6. 350 (19): 1978-88. [Медлайн].
Väisänen E, Fu Y, Koskenmies S, Fyhrquist N, Wang Y, Keinonen A, et al.ДНК кутавируса в злокачественной и незлокачественной коже кожной Т-клеточной лимфомы и у пациентов с трансплантацией органов, но не у здоровых взрослых. Клин Инфекция Дис . 2019 17 мая. 68 (11): 1904-1910. [Медлайн].
Criscione VD, Weinstock MA. Заболеваемость кожной Т-клеточной лимфомой в США, 1973–2002 гг. Дерматол Арки . 2007 июл.143 (7): 854-9. [Медлайн].
Сетояма М., Катахира Ю., Канзаки Т. Клинико-патологический анализ 124 случаев Т-клеточной лейкемии / лимфомы у взрослых с кожными проявлениями: тлеющий тип с кожными проявлениями имеет худший прогноз, чем считалось ранее. Дж Дерматол . 1999 26 декабря (12): 785-90. [Медлайн].
Альсале К.А., Нанда А., Аль-Аджми Х., Аль-Сабах Х., Элькашлан М., Аль-Шеммари С. и др. Клинико-эпидемиологические особенности грибкового микоза в Кувейте, 1991-2006 гг. Инт Дж Дерматол . 2010 декабрь 49 (12): 1393-8. [Медлайн].
Agar NS, Wedgeworth E, Crichton S, et al. Результаты выживаемости и прогностические факторы при грибовидном микозе / синдроме Сезари: проверка пересмотренного предложения Международного общества кожных лимфом / Европейской организации по исследованию и лечению рака. Дж. Клин Онкол . 2010, 1. 28 (31): 4730-9. [Медлайн].
Tancrède-Bohin E, Ionescu MA, de La Salmonière P, et al. Прогностическое значение эозинофилии крови при первичных кожных Т-клеточных лимфомах. Дерматол Арки . 2004 сентябрь 140 (9): 1057-61. [Медлайн].
Weinstock MA, Gardstein B. Двадцатилетние тенденции зарегистрированной заболеваемости грибковыми микозами и связанной с ними смертности. Am J Public Health . 1999 Август.89 (8): 1240-4. [Медлайн]. [Полный текст].
Kim YH, Hoppe RT. Грибовидный микоз и синдром Сезари. Семин Онкол . 1999, июнь, 26 (3): 276-89. [Медлайн].
Финк-Пучс Р., Вольф П., Керл Н., Серрони Л. Золотистый лишай: клинико-патологические особенности, естественное течение и связь с грибовидным микозом. Дерматол Арки . 2008 сентябрь 144 (9): 1169-73. [Медлайн].
Скарисбрик Дж. Дж., Уиттакер С., Эванс А. В. и др.Прогностическое значение опухолевой нагрузки в крови больных первичной кожной Т-клеточной лимфомой. Кровь . 2001 г. 1. 97 (3): 624-30. [Медлайн].
van Doorn R, Scheffer E, Willemze R. Фолликулярный грибовидный микоз, отдельное заболевание с ассоциированным фолликулярным муцинозом или без него: клинико-патологическое и последующее исследование 51 пациента. Дерматол Арки . 2002 Февраль 138 (2): 191-8. [Медлайн].
Симояма М.Диагностические критерии и классификация клинических подтипов Т-клеточной лейкемии-лимфомы взрослых. Отчет Исследовательской группы лимфомы (1984-87). Br J Haematol . 1991 ноябрь 79 (3): 428-37. [Медлайн].
Fink-Puches R, Zenahlik P, Bäck B, Smolle J, Kerl H, Cerroni L. Первичные кожные лимфомы: применимость существующих схем классификации (Европейская организация по исследованию и лечению рака, Всемирная организация здравоохранения) на основе наблюдаемых клинико-патологических особенностей в большой группе пациентов. Кровь . 2002 г. 1. 99 (3): 800-5. [Медлайн].
Bekkenk MW, Vermeer MH, Jansen PM и др. Периферические Т-клеточные лимфомы на коже неуточненные: анализ прогностических факторов в группе из 82 пациентов. Кровь . 2003 15 сентября. 102 (6): 2213-9. [Медлайн].
Чан Дж. К., Син В. К., Вонг К. Ф., Нг С. С., Цанг Вайоминг, Чан Ч. и др. Неназальные лимфомы, экспрессирующие естественный маркер клеток-киллеров CD56: клинико-патологическое исследование 49 случаев необычного агрессивного новообразования. Кровь . 1997 15 июня. 89 (12): 4501-13. [Медлайн].
Bekkenk MW, Jansen PM, Meijer CJ, Willemze R. Гематологические новообразования в коже CD56 +: ретроспективный анализ 23 новых случаев и 130 случаев из литературы. Энн Онкол . 2004 июл.15 (7): 1097-108. [Медлайн].
Mraz-Gernhard S, Natkunam Y, Hoppe RT, LeBoit P, Kohler S, Kim YH. Природная киллерная / природная киллероподобная Т-клеточная лимфома, CD56 +, проявляющаяся в коже: все более узнаваемая сущность с агрессивным течением. Дж. Клин Онкол . 2001 15 апреля. 19 (8): 2179-88. [Медлайн].
Toro JR, Liewehr DJ, Pabby N, Sorbara L, Raffeld M, Steinberg SM, et al. Гамма-дельта-Т-клеточный фенотип связан со значительным снижением выживаемости при кожной Т-клеточной лимфоме. Кровь . 1 мая 2003 г. 101 (9): 3407-12. [Медлайн].
Quaglino P, Pimpinelli N, Berti E, et al. Тенденции развития заболевания у пациентов с классическим грибовидным микозом с течением времени, клиническими путями и долгосрочными опасностями: многоцентровое ретроспективное последующее исследование итальянской группы кожных лимфом. Рак . 6 июня 2012 г. [Medline].
Pope E, Weitzman S, Ngan B, et al. Грибовидный микоз в педиатрической популяции: отчет международного детского реестра кожных лимфом. Дж. Cutan Med Surg . 2010 янв-фев. 14 (1): 1-6. [Медлайн].
Шимаути Т., Сугита К., Накамура М., Токура Ю. Папулоэритродермия, проявляющаяся лейкемической кожной Т-клеточной лимфомой с фенотипом CD3 (-) CD4 (+). Acta Derm Venereol .2010. 90 (1): 68-72. [Медлайн].
Herrmann JL, Hughey LC. Распознавание крупноклеточной трансформации грибовидного микоза. J Am Acad Dermatol . 2012 18 января [Medline].
Рошм А., Шлейер В., Ландталер М., Фогт Т. Фолликулярный грибовидный микоз: изменчивость редкой формы. Обрезанный кожей . 2005 янв-фев. 4 (1): 12-7. [Медлайн].
Muniesa C, Estrach T, Pujol RM, Gallardo F, Garcia-Muret P, Climent J, et al.Фолликулотропный грибовидный микоз: клинико-патологические особенности и исходы в серии из 20 случаев. J Am Acad Dermatol . 2010 Март 62 (3): 418-26. [Медлайн].
Pileri A, Facchetti F, Rütten A, Zumiani G, Boi S, Fink-Puches R, et al. Грибовидный сиринготропный микоз: редкий вариант заболевания с своеобразными клинико-патологическими особенностями. Am J Surg Pathol . 2011 января, 35 (1): 100-9. [Медлайн].
Bi MY, Curry JL, Christiano AM, Hordinsky MK, Norris DA, Price VH, et al.Спектр облысения у больных грибовидным микозом и синдромом Сезари. J Am Acad Dermatol . 2011 Январь 64 (1): 53-63. [Медлайн].
Clarijs M, Poot F, Laka A, Pirard C, Bourlond A. Гранулематозная дряблая кожа: лечение с обширным хирургическим вмешательством и обзор литературы. Дерматология . 2003. 206 (4): 393-7. [Медлайн].
Марцано А.В., Берти Э., Паулли М., Капуто Р. Цитофагический гистиоцитарный панникулит и подкожная панникулитоподобная Т-клеточная лимфома: отчет о 7 случаях. Дерматол Арки . 2000 июл.136 (7): 889-96. [Медлайн].
Török L, Gurbity TP, Kirschner A, Krenács L. Панникулитоподобная Т-клеточная лимфома клинически проявляется как алопеция. Br J Дерматол . 2002 Октябрь 147 (4): 785-8. [Медлайн].
Сантуччи М., Пимпинелли Н., Масси Д. и др. Цитотоксические кожные лимфомы / лимфомы из естественных клеток-киллеров. Отчет рабочей группы EORTC по кожной лимфоме. Рак . 2003 г. 1. 97 (3): 610-27.[Медлайн].
von den Driesch P, Coors EA. Локализованная кожная плеоморфная Т-клеточная лимфома малого и среднего размера: сообщение о 3 случаях, стабильных в течение многих лет. J Am Acad Dermatol . 2002 Апрель 46 (4): 531-5. [Медлайн].
Barrionuevo C, Андерсон В.М., Зеваллос-Джампьетри Э. и др. Гидроа-подобная кожная Т-клеточная лимфома: клинико-патологическое и молекулярно-генетическое исследование 16 педиатрических случаев из Перу. Appl Immunohistochem Mol Morphol .2002 10 марта (1): 7-14. [Медлайн].
Chen HH, Hsiao CH, Chiu HC. Первичная кожная CD8-положительная Т-клеточная лимфома, подобная Hydroa вакциниформной. Br J Дерматол . 2002 Сентябрь 147 (3): 587-91. [Медлайн].
Гутте Р., Харкар В., Махаджан С., Чихалкар С., Хопкар У. Гранулематозный грибовидный микоз с гипогидрозом, имитирующим лепроматозную лепру. Indian J Dermatol Venereol Leprol . 2010 ноябрь-декабрь. 76 (6): 686-90. [Медлайн].
Рассел-Джонс Р.Диагностика эритродермической кожной Т-клеточной лимфомы. Br J Дерматол . 2005 июль 153 (1): 1-5. [Медлайн].
Lange-Asschenfeldt S, Babilli J, Beyer M, Ríus-Diaz F, González S, Stockfleth E, et al. Согласованность и распределение характеристик отражательной конфокальной микроскопии для диагностики кожной Т-клеточной лимфомы. Дж. Биомед Опт . 2012 17 января (1): 016001. [Медлайн].
Петрелла Т., Комо М.Р., Майнади М. и др. Агранулярное CD4 + CD56 + гематодермическое новообразование (бластная NK-клеточная лимфома) происходит из популяции клеток-предшественников CD56 +, связанных с плазматическими моноцитами. Am J Surg Pathol . 2002 26 июля (7): 852-62. [Медлайн].
Smoller BR, Santucci M, Wood GS, Whittaker SJ. Гистопатология и генетика кожной Т-клеточной лимфомы. Гематол Онкол Клин Норт Ам . 2003 г., 17 (6): 1277-311. [Медлайн].
Haghighi B, Smoller BR, LeBoit PE, Warnke RA, Sander CA, Kohler S. Пагетоидный ретикулез (болезнь Ворингера-Колоппа): иммунофенотипическое, молекулярное и клинико-патологическое исследование. Мод Патол .2000 Май. 13 (5): 502-10. [Медлайн].
Мао X, Лиллингтон Д., Скарисбрик Дж. Дж. И др. Молекулярно-цитогенетический анализ кожных Т-клеточных лимфом: определение общих генетических изменений при синдроме Сезари и грибовидном микозе. Br J Дерматол . 2002 Сентябрь 147 (3): 464-75. [Медлайн].
Пай РК, Маллинс FM, Ким Й.Х., Конг CS. Цитологическая оценка лимфаденопатии, связанной с грибовидным микозом и синдромом Сезари: роль иммунофенотипических и дополнительных молекулярных исследований. Рак . 2008, 25 октября. 114 (5): 323-32. [Медлайн].
Burg G, Zwingers T, Staegemeir E, Santucci M. Межисследовательская и внутриэкологическая вариабельность при оценке кожных лимфопролиферативных Т-клеточных инфильтратов. Проектная группа по кожной лимфоме EORTC. Дерматол Клин . 1994 г., 12 (2): 311-4. [Медлайн].
Santucci M, Biggeri A, Feller AC, Massi D, Burg G. Эффективность гистологических критериев для диагностики ранних грибковых микозов: исследование группы исследования кожной лимфомы EORTC.Европейская организация по исследованию и лечению рака. Am J Surg Pathol . 2000 24 января (1): 40-50. [Медлайн].
Сантуччи М., Смоллер Б. Исследование ISCL по ранней диагностике грибовидного микоза. (в процессе подготовки).
Pimpinelli N, Olsen EA, Santucci M, et al. Определение ранних грибовидных микозов. J Am Acad Dermatol . 2005 декабрь 53 (6): 1053-63. [Медлайн].
Фурманчик П.С., Волгамот Г.М., Куссик С.Дж., Сабат Д.Е., Олеруд Ю.Е., Аргений З.Б.Диагностика грибовидных микозов с использованием различных алгоритмических подходов. Дж. Кутан Патол . 2010 Январь 37 (1): 8-14. [Медлайн].
Zelger B, Sepp N, Weyrer K, Grünewald K, Zelger B. Сиринготропная кожная Т-клеточная лимфома: вариант грибовидного микоза ?. Br J Дерматол . 1994 июн. 130 (6): 765-9. [Медлайн].
Герами П., Гитарт Дж. Базалоидная фолликулолимфоидная гиперплазия: отличительная находка при грибовидном фолликулярном микозе. Дж. Кутан Патол . 2007 декабрь 34 Дополнение 1: 29-32. [Медлайн].
Имаи С., Бург Дж., Браун-Фалько О. Грибовидный микоз и синдром Сезари демонстрируют различные гистоморфологические особенности. Дерматология . 1986. 173 (3): 131-5. [Медлайн].
Камарашев Дж., Бург Дж., Кемпф В., Хесс Шмид М., Даммер Р. Сравнительный анализ гистологических и иммуногистологических особенностей грибовидного микоза и синдрома Сезари. Дж. Кутан Патол .1998 25 сентября (8): 407-12. [Медлайн].
Sibaud V, Beylot-Barry M, Thiébaut R, et al. Гистопатологическая и молекулярная стадия костного мозга при эпидермотропных Т-клеточных лимфомах. Ам Дж. Клин Патол . 2003 Март, 119 (3): 414-23. [Медлайн].
Такешита М., Окамура С., Оширо Ю. и др. Клинико-патологические различия между 22 случаями CD56-отрицательной и CD56-положительной подкожной панникулитоподобной лимфомы в Японии. Хум Патол .2004 Февраль 35 (2): 231-9. [Медлайн].
de Wolf-Peeters C, Achten R. gammadelta Т-клеточные лимфомы: однородное образование ?. Гистопатология . 2000 апр. 36 (4): 294-305. [Медлайн].
Джонс Д., Вега Ф, Саррис А. Х., Медейрос Л. Дж.. CD4-CD8- «дважды отрицательные» кожные Т-клеточные лимфомы имеют общие гистологические особенности и агрессивное клиническое течение. Am J Surg Pathol . 2002 26 февраля (2): 225-31. [Медлайн].
Beljaards RC, Meijer CJ, Van der Putte SC, Hollema H, Geerts ML, Bezemer PD, et al.Первичная кожная Т-клеточная лимфома: клинико-патологические особенности и прогностические параметры 35 случаев, кроме грибовидного микоза и CD30-положительной крупноклеточной лимфомы. Дж. Патол . 1994, январь 172 (1): 53-60. [Медлайн].
Наткунам Ю., Смоллер Б.Р., Зендер Ю.Л., Дорфман Р.Ф., Варнке Р.А. Агрессивные NK- и NK-подобные Т-клеточные лимфомы кожи: клинико-патологический, иммуногистохимический и молекулярный анализ 12 случаев. Am J Surg Pathol . 1999 Май. 23 (5): 571-81.[Медлайн].
Lambert WC, Cohen PJ, Schwartz RA. Хирургическое лечение грибовидного микоза. J Med . 1997. 28 (3-4): 211-22. [Медлайн].
Thomas TO, Agrawal P, Guitart J, et al. Исход пациентов, получавших однофракционную дозу паллиативного излучения при кожной Т-клеточной лимфоме. Int J Radiat Oncol Biol Phys . 2012 17 июля [Medline].
Tsuji H, Wada T., Murakami M, et al.Два случая грибкового микоза, леченные трансплантацией пуповинной крови пониженной интенсивности. Дж Дерматол . 2010 декабрь 37 (12): 1040-5. [Медлайн].
Wu PA, Kim YH, Lavori PW, Hoppe RT, Stockerl-Goldstein KE. Метаанализ пациентов, получающих аллогенную или аутологичную трансплантацию гемопоэтических стволовых клеток при грибовидном микозе и синдроме Сезари. Пересадка костного мозга Biol . 2009 15 августа (8): 982-90. [Медлайн].
D’Acunto C, Gurioli C, Neri I.Зубной налет на стадии грибовидного микоза лечили бексаротином в низких дозах и УФB-NB. J Dermatolog Treat . 2010 21 января (1): 45-8. [Медлайн].
Chustecka Z. Первый запатентованный гель для лечения лимфомы кожи. Медицинские новости Medscape. 27 августа 2013 г. Доступно по адресу http://www.medscape.com/viewarticle/810067. Доступ: 3 сентября 2013 г.
Ceptaris получил одобрение FDA на гель валхлор (мехлорэтамин) для лечения кожной Т-клеточной лимфомы грибовидного типа на стадии IA и IB у пациентов, которые ранее получали терапию, направленную на кожу [пресс-релиз].Ceptaris Therapeutics Inc. Доступно по адресу https://www.actelion.com/media/media-releases?newsId=1724720. 26 августа 2013 г .; Дата обращения: 9 августа 2018 г.
Lessin SR, Duvic M, Guitart J, Pandya AG, Strober BE, Olsen EA и др. Местная химиотерапия при кожной Т-клеточной лимфоме: положительные результаты рандомизированного контролируемого многоцентрового исследования эффективности и безопасности нового 0,02% геля мехлоретамина при грибовидном микозе. Дерматол JAMA . 2013 Январь 149 (1): 25-32.[Медлайн]. [Полный текст].
Хорвиц С.М., Ким Ю.Х., Фосс Ф. и др. Определение активной, хорошо переносимой дозы пралатрексата у пациентов с рецидивирующей или резистентной кожной Т-клеточной лимфомой. Кровь . 2012 3 мая. 119 (18): 4115-22. [Медлайн]. [Полный текст].
Kim YH, Bagot M, Rook AH, Whittaker S, Duvic M. Моноклональные антитела против CCR4, могамулизумаб (Moga), демонстрируют более высокую эффективность по сравнению с вориностатом (Vor) у пациентов с ранее леченной кожной Т-клеточной лимфомой (CTCL) : Результаты исследования фазы 3 MAVORIC (аннотация).J Invest Dermatol. 2018; 138 (5) приложение 1 (S78). Представлено на Ежегодном собрании Международной исследовательской дерматологии 2018 г., IID 2018, 16-19 мая 2018 г. Орландо, Флорида.
Knobler E. Современные стратегии лечения кожной Т-клеточной лимфомы. Клин Дерматол . 2004 май-июнь. 22 (3): 197-208. [Медлайн].
Lundin J, Hagberg H, Repp R, et al. Фаза 2 исследования алемтузумаба (моноклональное антитело против CD52) у пациентов с запущенным грибовидным микозом / синдромом Сезари. Кровь . 1 июня 2003 г. 101 (11): 4267-72. [Медлайн].
Kanokrungsee S, Rajatanavin N, Rutnin S, Vachiramon V. Эффективность узкополосного ультрафиолета B два раза в неделю для гипопигментированных грибовидных микозов у азиатов. Клин Экспер Дерматол . 2012 марта 37 (2): 149-52. [Медлайн].
Ysebaert L, Truc G, Dalac S, et al. Окончательные результаты лучевой терапии грибовидного микоза Т1-Т2 (включая повторное облучение). Int J Radiat Oncol Biol Phys .2004 15 марта. 58 (4): 1128-34. [Медлайн].
Onozuka T, Yokota K, Kawashima T., Shimada H, Kodama K, Kobayashi H и др. Пожилой пациент с грибовидным микозом успешно пролечен хронической пероральной терапией низкими дозами этопозида. Клин Экспер Дерматол . 2004 29 января (1): 91-2. [Медлайн].
Даммер Р., Уросевич М., Кемпф В., Казаков Д., Бург Г. Имиквимод вызывает полное удаление PUVA-устойчивой бляшки при грибовидном микозе. Дерматология .2003. 207 (1): 116-8. [Медлайн].
Apisarnthanarax N, Talpur R, Ward S, Ni X, Kim HW, Duvic M. Tazarotene 0,1% гель для резистентных поражений грибовидного микоза: открытое пилотное исследование. J Am Acad Dermatol . 2004 апр. 50 (4): 600-7. [Медлайн].
Сингх Ф, Лебволь МГ. Лечение кожной Т-клеточной лимфомы с использованием бексаротена и ПУВА: серия случаев. J Am Acad Dermatol . 2004 Октябрь, 51 (4): 570-3. [Медлайн].
Fujimura T, Sato Y, Tanita K, Amagai R, Shimauchi T., Ogata D, et al.Серия случаев кожных Т-клеточных лимфом, получавших терапию на основе бексаротена. Дж Дерматол . 2020 24 марта. [Medline].
Hüsken AC, Tsianakas A, Hensen P, Nashan D, Loquai C, Beissert S и др. Сравнение пегилированного интерферона α-2b плюс псорален PUVA и стандартного интерферона α-2a плюс PUVA у пациентов с кожной Т-клеточной лимфомой. J Eur Acad Dermatol Venereol . 2012 26 января (1): 71-8. [Медлайн].
Чунг К.Г., Полигон Б.Другие химиотерапевтические агенты при кожной Т-клеточной лимфоме. Дерматол Клин . 2015 Октябрь, 33 (4): 787-805. [Медлайн]. [Полный текст].
Ли В.С., Хван Дж. Х., Ким М. Дж., Го С. И., Ли А., Сон Г. Н. и др. Циклоспорин А как первичное лечение панникулитоподобной Т-клеточной лимфомы: случай с длительной ремиссией. Лечение рака . 2014 Июль 46 (3): 312-6. [Медлайн].
Guenova E, Schanz S, Hoetzenecker W, Desimone JA, Mehra T, Voykov B, et al.Системные кортикостероиды при подкожной панникулитоподобной Т-клеточной лимфоме. Br J Дерматол . 2014 г., 12 апреля [Medline].
Ахерн К., Гилмор Е.С., Полигон Б. Зуд при кожной Т-клеточной лимфоме: обзор. J Am Acad Dermatol . 2012 26 января. [Medline].
Джонс Г.В., Хоппе Р.Т., Глатштейн Э. Электронно-лучевое лечение кожной Т-клеточной лимфомы. Гематол Онкол Клин Норт Ам . 1995 Октябрь 9 (5): 1057-76. [Медлайн].
Leverkus M, Rose C, Bröcker EB, Goebeler M. Фолликулярная кожная Т-клеточная лимфома: благотворное влияние изотретиноина на стойкие кисты и комедоны. Br J Дерматол . 2005, январь 152 (1): 193-4. [Медлайн].
Джейкоб Р., Скала М., Фунг М.А. Случай сиринготропной кожной Т-клеточной лимфомы, леченный местной лучевой терапией. J Am Acad Dermatol . 2009 Январь 60 (1): 152-4. [Медлайн].
Del Guzzo CA, Jariwala NN, Haun PL, MacArthur KM, Mowad CM, Richard EG, et al.Экспериментальное исследование нового терапевтического подхода к рефрактерным фолликулотропным грибковым микозам на поздней стадии. Acta Derm Venereol . 2020 4 марта. [Medline].
Национальный институт рака спонсировал исследование классификаций неходжкинских лимфом: краткое изложение и описание рабочего препарата для клинического использования. Проект патологической классификации неходжкинских лимфом. Рак . 1982 15 мая. 49 (10): 2112-35. [Медлайн].
Харрис Н.Л., Яффе Э.С., Стейн Х., Бэнкс П.М., Чан Дж. К., Клири М.Л. и др.Пересмотренная европейско-американская классификация лимфоидных новообразований: предложение Международной исследовательской группы лимфомы. Кровь . 1994 Сентябрь 1. 84 (5): 1361-92. [Медлайн]. [Полный текст].
Swerdlow SH, Campo E, Harris NL, et al, eds. Классификация опухолей кроветворных и лимфоидных тканей ВОЗ . Издание 4-е, переработанное. Лион, Франция: Международное агентство по изучению рака; 2017.
[Руководство] NCCN Руководство по клинической практике в онкологии.Первичные кожные лимфомы. Национальная всеобъемлющая онкологическая сеть. Доступно на https://www.nccn.org/professionals/physician_gls/pdf/primary_cutaneous.pdf. Версия 2.2020 — 10 апреля 2020 г .; Дата обращения: 10 апреля 2020 г.
[Рекомендации] Траутингер Ф., Эдер Дж., Ассаф С., Багот М., Коццио А., Даммер Р. и др. Консенсусные рекомендации Европейской организации по исследованию и лечению рака по лечению грибовидного микоза / синдрома Сезари — обновление 2017 г. Eur J Cancer .2017 май. 77: 57-74. [Медлайн]. [Полный текст].
[Рекомендации] Виллемзе Р., Ходак Э., Зинзани П.Л., Шпехт Л., Ладетто М., Комитет по руководствам ESMO. Электронный адрес: [email protected]. Первичные кожные лимфомы: Руководство ESMO по клинической практике по диагностике, лечению и последующему наблюдению. Энн Онкол . 2018 29 октября Дополнение 4: iv30-iv40. [Медлайн]. [Полный текст].
[Рекомендации] Kempf W, Pfaltz K, Vermeer MH, et al. Консенсусные рекомендации EORTC, ISCL и USCLC по лечению первичных кожных CD30-положительных лимфопролиферативных заболеваний: лимфоматоидного папулеза и первичной кожной анапластической крупноклеточной лимфомы. Кровь . 2011 Октябрь 13, 118 (15): 4024-35. [Медлайн]. [Полный текст].
[Рекомендации] Стейнторп А., Флиман Н., Хаутен Р., Чаплин М., Боланд А., Бил С. и др. Брентуксимаб Ведотин для лечения рецидивирующей или рефрактерной CD30-положительной кожной Т-клеточной лимфомы: взгляд группы обзора доказательств на оценку единой технологии NICE. Pharmacoecon Open . 2020 23 марта. [Medline]. [Полный текст].
Wilcox RA. Кожная Т-клеточная лимфома: Обновленная информация о диагностике, стратификации риска и лечении, 2014 г. Ам Дж. Гематол . 2014 августа 89 (8): 837-51. [Медлайн].
Pellegrini C, Stefoni V, Casadei B, Maglie R, Argnani L, Zinzani PL. Отдаленные результаты лечения пациентов с Т-клеточной лимфомой на поздней стадии, получавших гемцитабин. Энн Гематол . 2014 г. 8 июня [Medline].
Coiffier B, Pro B, Prince HM, Foss F, Sokol L, Greenwood M, et al. Ромидепсин для лечения рецидивирующей / рефрактерной периферической Т-клеточной лимфомы: обновление основного исследования демонстрирует устойчивый ответ. Дж Гематол Онкол . 2014 23 января. 7 (1): 11. [Медлайн]. [Полный текст].
Даммер Р., Дувик М., Скарисбрик Дж., Олсен Э.А., Розати С., Эггманн Н. и др. Окончательные результаты многоцентрового исследования фазы II ингибитора пуриновой нуклеозидфосфорилазы (PNP) фородезина у пациентов с распространенными кожными Т-клеточными лимфомами (CTCL) (грибовидный микоз и синдром Сезари). Энн Онкол . 2014 июн 19. [Medline].
[Рекомендации] Olsen EA, Whittaker S, Kim YH, et al.Клинические конечные точки и критерии ответа при грибовидном микозе и синдроме Сезари: согласованное заявление Международного общества кожных лимфом, Консорциума кожных лимфом США и Целевой группы по кожным лимфомам Европейской организации по исследованию и лечению рака. Дж. Клин Онкол . 2011. 20 июня. 29 (18): 2598-607. [Медлайн]. [Полный текст].
Ким Й.Х., Таваллаи М., Сундрам У., Сальва К.А., Вуд Г.С., Ли С. и др. Фаза II инициированного исследователем исследования брентуксимаба ведотина при грибковом микозе и синдроме Сезари с переменным уровнем экспрессии CD30: совместный проект с несколькими учреждениями. Дж. Клин Онкол . 2015 10 ноября. 33 (32): 3750-8. [Медлайн].
Fungoides фолликулярного микоза, явное заболевание с ассоциированным фолликулярным муцинозом или без него: клинико-патологическое и последующее исследование с участием 51 пациента | Аллергия и клиническая иммунология | JAMA дерматология
Цель
Определить клинико-патологические особенности и течение заболевания у больных грибовидным фолликулярным микозом (МФ).
Проект
Многоцентровый 14-летний ретроспективный когортный анализ.
Настройка
Голландская группа кожных лимфом.
Пациенты
51 пациент с клинико-патологическими особенностями фолликулярного МФ с (n = 49) или без (n = 2) ассоциированным фолликулярным муцинозом. Данные наблюдения сравнивались с данными 158 пациентов с классическим эпидермотропным типом МФ, включая 122 пациента с МФ на стадии генерализованной бляшки (T2 N0 M0) и 36 пациентов с МФ на стадии опухоли (T3 N0 M0).
Наблюдения
Характерными клиническими признаками, которые не наблюдались или редко наблюдались при классическом МФ, были преимущественная локализация кожных поражений в области головы и шеи (45 из 51 пациента), наличие фолликулярных папул, алопеция, угревые образования, муцинорея и часто сильный зуд. Характерными гистологическими данными были наличие перифолликулярных неопластических инфильтратов с различной степенью фолликулотропизма, но в целом отсутствие эпидермотропизма, фолликулярный муциноз (49 из 51 случая) и часто значительная примесь эозинофилов и плазматических клеток.Ответ на начальное лечение, риск прогрессирования заболевания (развитие внекожного заболевания и / или смерть от лимфомы), специфическая для заболевания и общая выживаемость пациентов с фолликулярным МФ были хуже, чем у пациентов с классическим МФ. Актуарная выживаемость по конкретному заболеванию составила 68% через 5 лет и 26% через 10 лет.
Выводы
Фолликулярный МФ демонстрирует отличительные клинико-патологические особенности, более устойчив к лечению и имеет худший прогноз, чем классический тип МФ; его следует рассматривать как отдельный тип кожной Т-клеточной лимфомы.Основываясь на этих результатах и результатах других исследований, мы предлагаем термин фолликулярный MF для случаев с ассоциированным фолликулярным муцинозом или без него.
грибовидный микоз (MF) — это наиболее распространенный тип кожной Т-клеточной лимфомы, клинически характеризующийся вялотекущим клиническим течением с последующим развитием пятен, бляшек и опухолей, а гистологически — инфильтрацией эпидермиса от среднего до среднего размера. большие атипичные Т-клетки с мозговыми ядрами. 1
В первые 10 лет после постановки диагноза прогрессирование заболевания, включая развитие внекожных заболеваний и связанных с ними смертей, происходит только у меньшинства пациентов. 2 Помимо этого так называемого классического типа МФ по Алиберту-Базину, сообщалось о многих клинических и гистологических подтипах, включая гипопигментированные, везикулярные, пустулезные, гранулематозные и другие типы МФ. Поскольку эти вариантные типы MF имеют такое же клиническое течение и клиническое поведение и требуют того же терапевтического подхода, что и классический тип MF, они, как правило, не считаются отдельными объектами.И в классификации EORTC (Европейская организация исследований по лечению рака) 1 для первичных кожных лимфом, и в классификации ВОЗ (Всемирная организация здравоохранения) 3 только пагетоидный ретикулез и фолликулярный муциноз, связанный с МФ, были отнесены к категории отдельные сущности. В дальнейшем последнее состояние будет обозначаться как фолликулярный MF , термин, также используемый в классификации ВОЗ для случаев с ассоциированным фолликулярным муцинозом или без него.
Фолликулярный МФ был классифицирован как отдельная форма, поскольку он имеет отличительные клинические и гистологические особенности, более устойчив к стандартному лечению и имеет худший прогноз, чем классический МФ. Однако это наблюдение основано, в частности, на клиническом опыте членов классификационного комитета группы кожных лимфом EORTC и недостаточно обосновано в литературе. Фактически, опубликованные отчеты о фолликулярном МФ относительно немногочисленны, обычно касаются сообщений о случаях заболевания или небольших серий пациентов и в основном сосредоточены на дифференциации фолликулярного муциноза, ассоциированного с МФ, и муцинозной алопеции, доброкачественной идиопатической формы фолликулярного муциноза. 4 -9
В недавнем исследовании, проведенном членами нашей группы 2 на 309 пациентах с МФ, 32 пациента с фолликулярным МФ, по-видимому, имели значительно более высокие показатели прогрессирования заболевания и смертности, чем 277 пациентов без фолликулярного муциноза. Эти наблюдения побудили нас рассмотреть все случаи фолликулярного МФ, зарегистрированные в Голландской группе кожных лимфом в период с 1985 по 1998 год.
С октября 1985 г. по декабрь 1998 г. 57 пациентов с фолликулярным МФ были включены в регистр Голландской группы кожных лимфом.Трое из 57 были исключены из настоящего исследования, 1 из-за неполных данных последующего наблюдения и 2 из-за отсутствия репрезентативных образцов биопсии кожи. Еще 3 пациента были исключены, потому что у них в анамнезе был классический эпидермотропный МФ в течение 4-7 лет до того, как у них развились кожные опухоли на лице с гистологическими признаками фолликулярного муциноза, ассоциированного с МФ. В последнюю исследуемую группу вошел 51 пациент. Каждому пациенту диагноз был поставлен группой экспертов дерматологов и патологов на одном из ежеквартальных собраний Голландской группы кожных лимфом.Основными критериями для диагностики и включения в исследование были наличие перифолликулярных и диффузных дермальных инфильтратов с различным количеством атипичных Т-клеток с мозговыми ядрами, инфильтрирующими фолликулярный эпителий, и наличие муцинозной дегенерации фолликулярного эпителия, что подтверждается данными исследования. Окрашивание Альциановым синим первых образцов диагностической биопсии (диагностических образцов). 6 , 7 Сорок девять пациентов соответствовали обоим критериям. Также были включены два случая с одинаковыми цитоархитектурными особенностями в диагностическом образце, но без ассоциированного фолликулярного муциноза.Время оценки первого диагностического образца считалось временем постановки диагноза.
Во всех случаях диагностическая оценка на момент постановки диагноза состояла из тщательного медицинского осмотра, полного подсчета клеток крови, химического исследования сыворотки и оценки образца кожи. Биопсия лимфатических узлов и компьютерная томография грудной клетки и брюшной полости выполнялись только у пациентов с увеличенными периферическими лимфатическими узлами. Поражение лимфатических узлов оценивалось с использованием критериев, описанных ранее. 10 При наличии клинических показаний были проведены дополнительные исследования для определения поражения внутренних органов.
Во всех случаях оценивались истории болезни и данные последующего наблюдения, которые собирались ежегодно. Были зарегистрированы следующие переменные: возраст; секс; продолжительность поражения кожи до постановки диагноза; вид начальной терапии; была ли полная ремиссия после начальной терапии; дата прогрессирования заболевания, если применимо; и дату последнего контакта (или смерти, если применимо).Из-за трудностей определения стадии кожи у пациентов с фолликулярным МФ, прогрессирование заболевания определялось развитием гистологически задокументированного поражения узлов у пациентов с ранее ограниченным кожным заболеванием, развитием висцерального поражения у пациентов с предшествующим поражением кожи и / или лимфатических узлов. и смерть от лимфомы. Во всех случаях были проанализированы один или несколько образцов биопсии кожи, полученных во время постановки диагноза, а в большинстве случаев также полученных во время последующего наблюдения.
Чтобы оценить различия в клиническом поведении между фолликулярным МФ и классическим МФ, 49 пациентов с фолликулярным МФ с заболеванием, ограниченным кожным покровом, сравнивали со 158 пациентами с классическим МФ, включенными в более раннее исследование. 2 В эту последнюю группу вошли 122 пациента с MF на стадии генерализованной бляшки (T2 N0 M0) и 36 пациентов с MF на стадии опухоли (T3 N0 M0) без признаков внекожного заболевания и без ассоциированного фолликулярного муциноза на момент постановки диагноза.
Актуарные кривые выживаемости были рассчитаны с даты постановки диагноза до даты последнего контакта (или даты смерти) с использованием метода Каплана-Мейера. Различия между кривыми выживаемости и прогрессирования заболевания анализировали с использованием лог-рангового критерия. Одномерный анализ возможных прогностических факторов проводился с использованием лог-рангового критерия и регрессионного анализа пропорциональных рисков Кокса. Пациенты, потерянные для последующего наблюдения, считались подвергнутыми цензуре на момент последнего контакта. Анализы выполняли с использованием статистического программного обеспечения SPSS (SPSS Inc, Чикаго, Иллинойс).
Основные клинические особенности и соответствующие данные наблюдения были обобщены в таблице 1. В это исследование был включен 51 пациент, в том числе 42 мужчины и 9 женщин. Четыре (8%) из 51 пациента были моложе 40 лет на момент постановки диагноза. На момент постановки диагноза 49 пациентов (96%) имели заболевание, ограниченное кожей, в том числе 4 пациента с увеличенными, но гистологически не пораженными лимфатическими узлами, тогда как у 1 пациента было одновременное поражение лимфатических узлов, а у другого — сопутствующее поражение внутренних органов.
На момент постановки диагноза у 34 из 51 пациента были только пятна, бляшки или (сгруппированные) фолликулярные папулы, часто связанные с алопецией; У 14 были (сопутствующие) узелки или опухоли; и у 3 была эритродермия (рис. 1). Угреобразные поражения, включая комедоподобные поражения и эпидермальные кисты, были характерной особенностью у 4 пациентов. Муцинорея (т. Е. Выделение муцинозного вещества из устьев фолликулов) отмечалось у 3 пациентов. Во время болезни у 2 пациентов появилось львиное лицо (рис. 2).У 45 из 51 пациента поражения кожи на момент постановки диагноза были преимущественно локализованы в области головы и шеи. Характерной находкой у 25 из этих 45 пациентов было наличие бляшек или опухолей на голове или шее, тогда как на туловище и конечностях наблюдались только пятна или слегка инфильтрованные бляшки и / или сгруппированные фолликулярные папулы (рис. 1A-B). Часто обнаруживались инфильтрованные бляшки в бровях с сопутствующей алопецией. У большинства пациентов был зуд от умеренного до сильного.
Было изучено 74 репрезентативных образца биопсии кожи от 51 пациента.В их число вошли 51 диагностический образец, 8 преддиагностических образцов, полученных от 4 до 30 месяцев (медиана, 12 месяцев) до постановки диагноза, и 15 образцов, полученных во время последующего наблюдения во время рецидива или прогрессирования заболевания. Характерно, что диагностические образцы показали перифолликулярные и периваскулярно-диффузные дермальные инфильтраты с различной инфильтрацией фолликулярного эпителия атипичными Т-клетками среднего и большого размера с мозговыми ядрами (рис. 3). Микроабсцессы Путрие проявились лишь в небольшом количестве образцов.Инфильтрация межфолликулярного эпидермиса (атипичными) Т-клетками, как и при классическом МФ, была редкой. Только 5 из 51 образца показали инфильтрацию как эпидермиса (эпидермотропизм), так и фолликулярного эпителия (фолликулотропизм). Выраженная инфильтрация эккринных потовых желез наблюдалась в 3 образцах. Во всех случаях, кроме двух, образцы кожи показали муцинозную дегенерацию волосяных фолликулов, варьировавшую от очагов отложения муцина (которые нужно было искать на серийных срезах) до озер муцина (Рисунок 3B).
Количество атипичных Т-клеток, инфильтрирующих фолликулярный эпителий, обычно было низким и не коррелировало с количеством отложений муцина. Перифолликулярные инфильтраты состояли из различного количества атипичных Т-клеток среднего и большого размера с ядрами мозга и бластными клетками, а также небольшими лимфоцитами, гистиоцитами, эозинофилами (которых было много в 13 из 51 образца) и плазматическими клетками, особенно у пациентов с вторичная бактериальная инфекция (рис. 3С).Параллельные пятна на туловище демонстрировали по существу те же гистологические особенности, хотя количество атипичных Т-клеток часто было меньше, чем в более инфильтрированных поражениях на голове и шее, что делало точный диагноз на этих образцах более трудным или даже невозможным.
Иммуногистохимический анализ продемонстрировал фенотип CD3 + -CD4 + -CD8 — неопластических Т-клеток во всех изученных случаях. Регулярно наблюдали небольшое количество разбросанных бластных клеток CD30 + , а также небольшие кластеры смешанных В-клеток.В первичных диагностических образцах 7 из 51 пациента мы обнаружили значительное количество бластных клеток (> 15%; как правило, смесь бластных клеток CD30 + и CD30 — ). Шесть из этих 7 пациентов умерли от лимфомы от 11 до 100 месяцев (в среднем 40 месяцев) после постановки диагноза.
В образцах для последующего наблюдения, взятых во время прогрессирования заболевания, дермальные инфильтраты имели тенденцию становиться более диффузными, иногда обнаруживалось полное стирание фолликулярных структур и неизменно обнаруживалось увеличение количества бластных клеток CD30 — и / или CD30 + .В 8 преддиагностических образцах дермальные инфильтраты были в основном ограничены перифолликулярными областями. Хотя некоторые из этих образцов уже содержали небольшое количество атипичных Т-клеток в фолликулярном эпителии и перифолликулярных инфильтратах, размер и морфологические характеристики инфильтрирующих Т-клеток не требовали точного диагноза фолликулярного МФ.
Начальная терапия включала лечение псораленом и УФ-А (PUVA) у 22 пациентов и полное облучение кожи электронным пучком (TSEBI) у 11 пациентов (таблица 1).Семь пациентов первоначально лечили местной лучевой терапией в сочетании с другими методами лечения, включая ПУВА с ретиноидами или без них, УФ-В, местный мехлорэтамин или местные стероиды. Для остальных пациентов лечение включало местные стероиды (3 пациента), местный мехлорэтамин (1 пациент), УФ-B (1 пациент), PUVA в сочетании с ретиноидами (1 пациент), преднизон (1 пациент), азатиоприн в сочетании с местным мехлорэтамином (1 пациент) или полихимиотерапия (2 пациента).Один пациент отказался от лечения.
Только 8 (16%) из 51 пациента, каждый с заболеванием, ограниченным кожным покровом, достигли полной ремиссии при начальном лечении. Шесть из них получали TSEBI, 1 — PUVA и 1 — комбинацию PUVA, ретиноидов и местной лучевой терапии. Двое из этих 7 пациентов все еще находились в полной ремиссии после 38 и 192 месяцев наблюдения, соответственно, и могут считаться вылеченными.
Срок наблюдения варьировал от 8 до 239 месяцев (в среднем 48 месяцев; в среднем 58 месяцев).Развитие лимфатических узлов или внутренних органов было зарегистрировано у 14 и 7 пациентов соответственно. Прогрессирование заболевания, определяемое как развитие внекожного заболевания или смерть от лимфомы, произошло у 20 (39%) из 51 пациента и произошло через 11–168 месяцев (в среднем 45 месяцев) после постановки диагноза. Расчетный риск прогрессирования заболевания в течение первых 5 лет после постановки диагноза составил 37%; в 10 лет — 66%. По завершении исследования 26 пациентов умерли, 20 — от лимфомы. 5- и 10-летняя выживаемость при конкретном заболевании составила 68% и 26% соответственно.Соответствующие общие показатели выживаемости через 5 и 10 лет составили 64% и 14%. Одномерный анализ не продемонстрировал связи между выживаемостью при конкретном заболевании и возрастом на момент постановки диагноза, полом, продолжительностью кожных повреждений до постановки диагноза или ответом на начальное лечение.
Фолликулярные мф против классических мф
Чтобы оценить различия в клиническом поведении и прогнозе между фолликулярным МФ и классическим МФ, мы сравнили соответствующие клинические характеристики 49 пациентов с фолликулярным МФ, у которых болезнь ограничивалась кожей, с особенностями 122 пациентов с МФ на стадии генерализованной бляшки и 36 пациентов. с МФ на стадии опухоли без признаков внекожного заболевания и без ассоциированного фолликулярного муциноза (Таблица 2).Пациенты с фолликулярным МФ показали значительно более высокое соотношение мужчин и женщин и реже достигали полной ремиссии на начальном этапе лечения. Расчетный риск прогрессирования заболевания, как определено в этом исследовании, в течение первых 5 лет после постановки диагноза составил 36% для фолликулярного MF против 12% для MF на классической стадии бляшки и 24% для MF на стадии опухоли. Специфическая для заболевания и общая выживаемость у пациентов с фолликулярным МФ были значительно ниже, чем у пациентов с генерализованным МФ на стадии бляшки, и были примерно аналогичны пациентам с МФ на стадии опухоли без ассоциированного фолликулярного муциноза (рис. 4).
Результаты настоящего исследования ясно демонстрируют, что фолликулярный МФ имеет отличительные клинико-патологические особенности и должен рассматриваться как отдельное заболевание. Характерные гистологические особенности включают первичную перифолликулярную локализацию дермальных инфильтратов с различной инфильтрацией фолликулярного эпителия атипичными Т-клетками среднего и большого размера с ядрами мозгового вещества. В большинстве случаев эпидермис сохраняется (фолликулотропизм вместо эпидермотропизма).В большинстве случаев происходит муцинозная дегенерация фолликулярного эпителия, часто присутствует значительная примесь эозинофилов и плазматических клеток.
Клинические характеристики включают преимущественную локализацию кожных поражений в области головы и шеи (45 из 51 пациента), наличие папул (часто сгруппированных), алопецию, частую вторичную бактериальную инфекцию и, реже, наличие угревой сыпи. и муцинорея. В отличие от классического МФ, зуд часто бывает тяжелым и может представлять собой хороший показатель активности заболевания: у некоторых пациентов рецидиву после начальной терапии предшествовало повторное появление зуда.Кроме того, пациенты с фолликулярным МФ в целом оказались более невосприимчивыми к стандартной классической терапии МФ, показали более частое прогрессирование заболевания и имели менее благоприятный прогноз (Таблица 2).
Этот более неблагоприятный прогноз предполагает истинное биологическое различие в клиническом поведении пациентов с фолликулярным МФ и пациентов с классическим эпидермотропным типом МФ, что согласуется с выводом недавнего исследования. 11 Сходная продолжительность кожных поражений до постановки диагноза у пациентов с фолликулярным МФ и пациентов с МФ классического типа указывает на то, что разница в выживаемости не является просто результатом отбора пациентов с более запущенным заболеванием в настоящем исследовании (Таблица 2) .Сравнение данных по конкретной болезни и общей выживаемости показывает, что пациенты с фолликулярным МФ имеют аналогичную (через 5 лет) или худшую (через 10 лет) выживаемость, чем пациенты с МФ на стадии опухоли (таблица 2). Тем не менее, согласно классической системе классификации MF, 12 , 13 большинство наших пациентов с фолликулярным MF были бы классифицированы как стадия IA (T1 N0 M0) или IB (T2 N0 M0), и только у 14 из них были узелки. или опухоли на момент постановки диагноза. Это подтверждает наше мнение о том, что эти системы клинического определения МФ не очень полезны у пациентов с фолликулярным МФ.Например, пациенты с единичным пятном или бляшкой на лице не имеют стадии IA или T1 N0 M0 стадии. Из-за перифолликулярной локализации дермальных инфильтратов такие пациенты всегда должны считаться страдающими опухолевой стадией, независимо от клинических проявлений поражения кожи, и их следует лечить соответствующим образом.
Mf-ассоциированный фолликулярный муциноз по сравнению с фолликулярным mf
В последние годы термин фолликулярная MF или кожная Т-клеточная лимфома (также фолликулоцентрическая MF или пилотропная MF ) был введен для редкого клинического варианта MF, характеризующегося фолликулярными папулами, фолликулярными кератозами, комедоличными образованиями. и эпидермальные кисты.Гистологически присутствуют перифолликулярные инфильтраты с выраженным фолликулотропизмом, но, как правило, нет эпидермотропизма или фолликулярного муциноза. 14 -22 Оценка опубликованных отчетов о «фолликулярном МФ» демонстрирует значительную клиническую неоднородность и предполагает, что этот термин использовался для диагнозов по крайней мере 3 различных групп пациентов.
Самую большую группу составляют пациенты с клинически и гистологически классическими МФ до или, реже, одновременно с развитием фолликулярных поражений. 17 , 21 , 22 В настоящем исследовании 3 пациента с 4-7-летней историей классических эпидермотропных МФ, развивающихся опухолей кожи с гистологическими особенностями фолликулярного МФ, были исключены, поскольку такие случаи демонстрируют клиническое поведение классический МФ, развивающийся в опухолевой стадии.
Во вторую группу входят пациенты, у которых угревые образования являются преобладающим или единственным проявлением заболевания. 17 , 19 , 21 , 22 Однако аналогичная клиническая картина может также наблюдаться у пациентов с ассоциированным фолликулярным муцинозом 23 , 24 и преобладала у 4 из 51 пациента в настоящее время. изучение.Одним из наших пациентов был 16-летний мальчик, у которого в анамнезе были сильные зудящие акнеформные поражения и алопеция более 5 лет до того, как был поставлен диагноз фолликулярного муциноза, связанного с МФ. Несмотря на лучевую терапию и мультиагентную химиотерапию, он умер через 5 лет после постановки диагноза системной лимфомы. Интересно, что в то время как на некоторых из его акнеиформных поражений наблюдались отложения муцина, на других его не было даже после дальнейшего разделения.
Наконец, некоторые из зарегистрированных случаев демонстрируют все характерные клинические и гистологические особенности случаев, описанных здесь, за исключением наличия фолликулярного муциноза. 18 , 20 Настоящее исследование включает 2 таких случая у пациентов, которые в остальном не отличались ни клинически, ни гистологически от 49 пациентов с ассоциированным фолликулярным муцинозом. Основываясь на этих наблюдениях, мы не считаем, что полезно различать фолликулярный МФ с ассоциированным фолликулярным муцинозом и без него в этих двух последних группах. С биологической точки зрения наиболее важной особенностью фолликулярного МФ с фолликулярным муцинозом или без него является глубокая перифолликулярная локализация неопластических инфильтратов, что делает их менее доступными для терапии, нацеленной на кожу.На основании наших собственных наблюдений и доступной литературы, 11 , мы склонны полагать, что фолликулярный МФ с фолликулярным муцинозом или без него не следует рассматривать отдельно, и что случаи с преимущественным (пери) фолликулярным распределением неопластических инфильтратов, независимо от наличия муцинозной дегенерации, фолликулярный MF следует обозначать как .
Хотя отличительные клинические и гистологические особенности должны способствовать ранней и правильной диагностике, по нашему опыту за последние 15 лет, диагностике фолликулярных МФ часто не уделяют должного внимания.Из-за преимущественного поражения области головы и шеи, отсутствия пятен и бляшек на туловище или ягодицах и отсутствия эпидермотропных атипичных Т-клеток диагноз МФ или кожной Т-клеточной лимфомы часто не рассматривается. Следующие неверные диагнозы были поставлены более чем один раз до направления к специалисту: себорейный дерматит у пациентов с эритематозными высыпаниями на коже черепа и бровей; атопический дерматит из-за сильного зуда; и гранулема лица с эозинофилией у пациентов с единичным налетом на лице и инфильтратом, богатым эозинофилами.Наконец, следует отметить, что даже при подозрении на фолликулярный МФ может потребоваться несколько биопсий для постановки точного диагноза. Важно брать образцы биопсии из наиболее инфильтрированных кожных поражений, как правило, на лице или шее, а не только из участков с фолликулярными папулами или без них на туловище.
Результаты настоящего исследования подтверждают наше клиническое мнение и разрозненные данные в литературе о том, что пациенты с фолликулярным МФ, как правило, менее чувствительны к стандартным методам лечения, используемым у пациентов с классическим МФ. 11 , 20 , 25 Наше ретроспективное исследование не позволяет провести достоверное сравнение эффектов различных методов лечения, поскольку пациенты лечились в разных учреждениях, и на выбор лечения могла повлиять тяжесть заболевания.
Из-за перифолликулярной локализации дермальных инфильтратов пациенты с фолликулярным МФ всегда должны считаться страдающими опухолевой стадией, независимо от клинических проявлений кожных поражений.Следовательно, у пациентов с единичной бляшкой или опухолью или несколькими кластерами кожных поражений, но без пятен или фолликулярных папул на других участках, лучевая терапия является первым выбором для лечения. В отдельных случаях с поверхностными поражениями, представленными на нескольких участках, сначала может быть предпринято лечение PUVA. Однако в большинстве случаев такой подход не приводит к полной ремиссии. В настоящей серии полная ремиссия была достигнута с помощью ПУВА-терапии только у 1 из 22 пациентов. У пациентов с более инфильтрированными кожными поражениями, особенно у тех, кто не отвечает только на PUVA-терапию, TSEBI является предпочтительным методом лечения.Однако только 6 из 11 пациентов, получавших TSEBI, достигли полной ремиссии, а у 3 из 6 пациентов, полностью ответивших на лечение, случился рецидив в течение 6 месяцев.
Сообщалось об относительной невосприимчивости фолликулярного MF к TSEBI. 18 У некоторых пациентов рецидивное кожное заболевание можно эффективно контролировать с помощью поддерживающего лечения с применением местного азотного иприта. Если TSEBI недоступен, альтернативой может быть PUVA в сочетании с альфа-интерфероном или ретиноидами и местная лучевая терапия для толстых опухолей.Такой же подход можно использовать при рецидиве заболевания после TSEBI. По нашему опыту, мультиагентная химиотерапия обычно не приводит к полной ремиссии у пациентов с кожно-ограниченным заболеванием, поэтому ее следует применять только для пациентов, у которых развивается внекожное заболевание.
Принята к публикации 2 июля 2001 г.
Автор для переписки и оттиски: Рейн Виллемзе, доктор медицины, отделение дерматологии, B1-Q-93, Медицинский центр Лейденского университета, Albinusdreef 2, 2333 ZA Leiden, Нидерланды (электронная почта: [email protected]).
1. Виллемзе
RKerl
HSterry
W
и другие. Классификация первичных кожных лимфом по EORTC: предложение Исследовательской группы кожных лимфом Европейской организации по исследованию и лечению рака. Кровь. 1997;
-371Google Scholar2.Van Doorn
Рван Хаселен
CWvan Voorst Vader
ПК
и другие. Грибовидный микоз: развитие болезни и прогноз 309 голландских пациентов. Arch Dermatol. 2000; 136504-510Google ScholarCrossref 3.Harris
NLJaffe
ESDiebold
J
и другие. Классификация неопластических заболеваний кроветворной и лимфоидной ткани Всемирной организации здравоохранения: отчет совещания клинического консультативного комитета, Эйрли-Хаус, Вирджиния, ноябрь 1997 г. J Clin Oncol. 1999; 173835–3849 Google Scholar4.Pinkus
H Связь муцинозной алопеции со злокачественной лимфомой. Dermatologica. 1964; 129266-270Google ScholarCrossref 6.Николофф
BJWood
C Доброкачественный идиопатический по сравнению с фолликулярным муцинозом, ассоциированным с грибовидным микозом. Pediatr Dermatol. 1985; 2201-206Google ScholarCrossref 7.Sentis
HJWillemze
RScheffer
E Муцинозная алопеция, прогрессирующая в грибовидный микоз: долгосрочное катамнестическое исследование двух пациентов. Am J Dermatopathol. 1988; 10478-486Google ScholarCrossref 8. Гибсон
ЛЕМюллер
С.А.Лейферман
KMPeters
MS Фолликулярный муциноз: клинико-гистопатологическое исследование. J Am Acad Dermatol. 1989; 20441-446Google ScholarCrossref 9. Mehregan
Д.А.Гибсон
ЛЕМюллер
SA Фолликулярный муциноз: гистопатологический обзор 33 случаев. Mayo Clin Proc. 1991; 66387-390Google ScholarCrossref 10.Scheffer
EMeijer
CJVan Vloten
WA Дерматопатическая лимфаденопатия и поражение лимфатических узлов при грибковом микозе. Рак. 1980; 45137-148Google ScholarCrossref 11.Bonta
MDTannous
ZSDemierre
MFGonzalez
EHarris
НЛДункан
LM Быстро прогрессирующий грибовидный микоз, проявляющийся в виде фолликулярного муциноза. J Am Acad Dermatol. 2000; 43635–640Google ScholarCrossref 12.Bunn
PLamberg
S Отчет Комитета по стадированию и классификации кожных Т-клеточных лимфом. Cancer Treat Rep. 1979; 63725-728Google Scholar13.Fuks
ZBagshaw
MFarber
E Прогностические признаки и лечение грибовидного микоза. Рак. 1973; 321385–1395Google ScholarCrossref 15.Lacour
JPCastanet
JPerrin
COrtonne
JP Фолликулярный грибовидный микоз — клинический и гистологический вариант кожной Т-клеточной лимфомы: сообщение о двух случаях. J Am Acad Dermatol. 1993; 29330-334Google ScholarCrossref 16. Goldhersh
МАЗлотогорский
ARosenmann
E Фолликулярный грибовидный микоз. Am J Dermatopathol. 1994; 1652-55Google ScholarCrossref 17.Vergier
BBeylot-Barry
МБейлот
C
и другие. Пилотропная кожная Т-клеточная лимфома без муциноза: вариант грибовидного микоза? Arch Dermatol. 1996; 132683-687Google ScholarCrossref 18.Pereyo
NGRequena
LGalloway
JSangueza
OP Фолликулярный грибовидный микоз: клинико-гистопатологическое исследование. J Am Acad Dermatol. 1997; 36563-568Google ScholarCrossref 19. Фрейзер-Эндрюс
EAshton
Р.Рассел-Джонс
R Пилотропный грибовидный микоз, проявляющийся множественными кистами, комедонами и алопецией. Br J Dermatol. 1999; 140141-1444Google ScholarCrossref 20.Klemke
CDDippel
EAssaf
C
и другие. Фолликулярный грибовидный микоз. Br J Dermatol. 1999; 141137-140Google ScholarCrossref 21.Hodak
EFeinmesser
MSegal
Т
и другие.Фолликулярная кожная Т-клеточная лимфома: клинико-патологическое исследование девяти случаев. Br J Dermatol. 1999; 141315-322Google ScholarCrossref 22.Grau
CPont
Вматарредона
JFortea
JMAliaga
Фолликулярный грибовидный микоз: описание случая и обзор литературы. J Eur Acad Dermatol Venereol. 1999; 13131-136Google ScholarCrossref 23. Wilkinson
JDBlack
MMChu
Фолликулярный муциноз, связанный с грибовидным микозом, проявляющийся грубыми кистозными изменениями на лице. Clin Exp Dermatol. 1982; 7333-339Google ScholarCrossref 24.Wittenberg
GPGibson
Л.Е. Питтельков
МРел-Ажары
RA Фолликулярный муциноз в виде угревой сыпи: сообщение о четырех случаях. J Am Acad Dermatol. 1998; 38849-851Google ScholarCrossref 25.Gilliam
ACLessin
SRWilson
Д.М.Салхани
KR Фолликулотропный грибовидный микоз с крупноклеточной трансформацией, проявляющийся в виде расслаивающего целлюлита волосистой части головы. J Cutan Pathol. 1997; 24169-175Google ScholarCrossref
Гипопигментация: замаскированный грибовидный микоз
Описание
45-летний мужчина индийского происхождения поступил в дерматологическую клинику с историей кожных изменений за последние 2 года. При осмотре были обнаружены многочисленные гипопигментированные пятна на руках и туловище (рисунок 1). Атопии в анамнезе не было.
Рисунок 1
Гипопигментированные поражения на предплечье и туловище.
Первоначальное подозрение было на разноцветный лишай, распространенное заболевание кожи, вызванное инфекцией дрожжевыми грибками Malassezia .Разноцветный лишай характеризуется хорошо разграниченными, гиперпигментированными или гипопигментированными пятнами, которые чаще всего встречаются на туловище. Пациент лечился от этого в первичной медико-санитарной помощи; улучшения не наблюдалось.
Белый отрубевидный лишай, хотя чаще встречается у детей, также рассматривался. Однако для этого состояния характерны гипопигментированные пятна, которые обычно поражают лицо. Обратите внимание, что витилиго вызывает депигментацию кожи и не должно рассматриваться как дифференциал для гипопигментированных поражений (рисунок 2).
Рисунок 2
Крупным планом — гипопигментированные поражения предплечья.
Поскольку указанные выше различия не соответствовали клинической картине пациента, была рассмотрена необычная причина гипопигментации: кожная Т-клеточная лимфома, известная как грибовидный микоз. Гипопигментированные поражения сами по себе являются редким проявлением этого заболевания, обычно наблюдаемым у пациентов с более темным типом кожи.1
Грибовидный микоз обычно проявляется в возрасте от 45 до 60 лет. Он имеет три клинических стадии, начиная с фазы пластыря, стадии, на которой обратился этот пациент, прогрессирующей до стадии бляшки и, в конечном счете, до стадии опухоли, что имеет наихудший прогноз.2 Заболевание на ранней стадии легко принять за множественные доброкачественные дерматозы3
Биопсия кожи и исследования перестройки генов Т-клеток подтвердили диагноз, и фототерапия была начата в качестве начальной терапии.
Очков обучения
Существует ряд дифференциальных диагнозов гипопигментации, включая разноцветный лишай, белый лишай и грибовидный микоз.
Витилиго не следует включать в дифференциал, поскольку оно вызывает депигментацию, а не гипопигментацию.
Грибовидный микоз может имитировать многие кожные заболевания; Системный подход к анамнезу и дерматологическому обследованию может помочь диагностировать более редкие состояния, такие как грибовидный микоз.
Грибовидный микоз — Консультант по терапии рака
Грибковый микоз
I. Что нужно знать каждому врачу.
Грибовидный микоз (MF) — наиболее распространенный тип кожной Т-клеточной лимфомы, которая проявляется в виде пятен, бляшек или узелков на участках кожи, не подвергающихся воздействию солнца.Эти поражения кожи могут медленно перерасти в опухоли. В тяжелых случаях МФ также поражает внекожные ткани, такие как лимфатические узлы, легкие, печень, селезенку и желудочно-кишечный тракт. Классический МФ считается вялотекущим заболеванием, которое медленно прогрессирует от лет до десятилетий.
Синдром Сезари — это агрессивный и лейкемический вариант кожной Т-клеточной лимфомы, характеризующийся циркулирующими атипичными Т-клетками (клетки Сезари), диффузной эритемой (эритродермия) и серьезным нарушением функции зуда с лимфаденопатией или без нее.
Пациенты с МФ и синдромом Сезари имеют значительно повышенный риск развития второй лимфомы, особенно лимфомы Ходжкина и лимфоматоидного папулеза подтипа Т-клеточной лимфомы кожи, а также негематологических злокачественных новообразований.
II. Диагностическое подтверждение: Вы уверены, что у вашего пациента МФ?
Во многих отчетах документально подтверждено, что MF имитирует другие дерматозы, что привело к тому, что некоторые врачи назвали MF «великим имитатором».
MF диагностируется на основании клинических, гистологических и иммунопатологических оснований, поддерживаемых молекулярно-биологическими критериями, основанными на рекомендациях Международного общества кожных лимфом (ISCL) и целевой группы по кожным лимфомам Европейской организации исследований и лечения рака (EORTC). ).
Для диагностики грибкового микоза требуется всего 4 балла на основе любой комбинации баллов из клинических, гистопатологических, молекулярных и иммунопатологических критериев. Клинические и гистопатологические разделы далее делятся на основные и дополнительные критерии:
Если соблюдены основные критерии и два дополнительных балла, дается 2 балла.
Если соблюдены основные критерии и один дополнительный критерий, дается 1 балл.
1) Клиническая
Основной критерий — наличие стойких пятен на коже / тонких бляшек.
Дополнительные клинические критерии включают:
Наличие этих поражений на участках, не подверженных воздействию солнца
Изменения размера и формы этих поражений и
Пойкилодермия (участки повышенной и пониженной пигментации, выступающие кровеносные сосуды и истончение кожи).
2) Гистопатологический
Основной критерий — наличие поверхностных лимфоидных инфильтратов при биопсии кожи.
Дополнительные критерии включают:
Эпидермотропизм без спонгиоз (подробнее см. Ниже)
Наличие увеличенных гиперхроматических ядер с неправильными контурами ядер на биоптате
Поскольку показатели согласованности среди патологов низки для диагностики раннего МФ, для постановки окончательного диагноза необходимы серийные образцы биопсии из различных клинических учреждений.
3) Молекулярно-биологический
Клональная реаранжировка гена Т-клеточного рецептора с помощью ПЦР оценивается в 1 балл.Это отсутствует в 50% случаев.
4) Иммунопатологический
Присутствие любого из нижеприведенных иммунопатологических критериев дает право на получение 1 балла:
Менее 50% Т-клеток инфильтратов поражений экспрессируют CD2, CD3 и / или CD5.
Для полных инфильтратов поражения менее 10% Т-клеток экспрессируют CD7.
Несоответствие дермальных и эпидермальных клеток (дефицит эпидермиса) в экспрессии CD2, CD3, CD5 или CD7.
В прошлом диагноз синдрома Сезари (агрессивная лейкемическая фаза грибкового микоза) ставился, когда в крови было обнаружено большое количество клеток Сезари (аномальные лимфоциты с мозговыми ядрами и уникальной морфологической внешностью). Однако ее в значительной степени заменили проточной цитометрией из-за высокой вариабельности количества клеток у разных наблюдателей.
A. История, часть I: Распознавание образов:
Обычно пациенты обращаются с жалобами на хронические, зудящие и шелушащиеся участки кожи или бляшки на участках, не подверженных воздействию солнца, или участках кожи, напоминающих «купальный костюм».Это включает грудь, ягодицы, нижнюю часть туловища и пах. Зуд присутствует часто, но не всегда, и может быть настолько серьезным, что может повлиять на качество жизни.
Диагностика может быть осложнена премикотической фазой (наличие неспецифических поражений кожи и недиагностических результатов биопсии). Эта фаза может предшествовать диагностике и длиться месяцами. Иногда эти поражения кожи прогрессируют до инфильтрированных бляшек, за которыми следуют язвенные поражения или многочисленные новообразования. Пациенты могут также иметь кожные пятна, бляшки, опухоли и язвы одновременно.
Госпитализация может быть следствием генерализованной эритродермии, которая может быть основной жалобой у пациентов с более поздними стадиями заболевания. Редко у некоторых пациентов МФ ассоциируется с алопецией или пигментными пурпуроподобными поражениями кожи. Жалобой может быть множественная рецидивирующая кожная инфекция. У некоторых пациентов жалобой могут быть множественные рецидивирующие кожные инфекции. В литературе также представлены случаи пациентов с запущенным заболеванием с обширными некротизированными участками кожи, кожными инфекциями и бактериальными инфекциями кровотока.
Б. История, часть 2: Распространенность:
MF обычно проявляется в возрасте 55-60 лет, но также может наблюдаться у более молодых людей. Он поражает мужчин больше, чем женщин, и чернокожих больше, чем белых. Приблизительно заболеваемость МФ составляет 3,6 на 100 000 человеко-лет. Считается, что MF возникает в результате хронической антигенной стимуляции, которая приводит к неконтролируемой клональной экспансии и накоплению в коже хелперных клеток памяти Т-клеток. Генетические аномалии и триггеры окружающей среды считаются предрасполагающими факторами.Было высказано предположение, что существует связь между MF и человеческим Т-лимфотропным вирусом типа I (HTLV-I). Однако на сегодняшний день эта связь не подтверждена.
C. История, часть 3: Конкурирующие диагнозы, которые могут имитировать MF.
MF может проявляться аналогично другим папулосквамозным и экзематозным кожным заболеваниям. Следующие патологические процессы могут имитировать МФ: экзема, псориаз, красный плоский лишай, фотодерматит, лекарственные реакции, первичная кожная лимфома и фолликулотропные МФ. Для постановки правильного диагноза необходимы тщательный сбор анамнеза, физикальное обследование, гистология и иммунопатология кожи.Сообщалось, что даже tinea corporis имитирует МФ.
D. Результаты физикального осмотра.
Типичные физические признаки включают хронические, зудящие и шелушащиеся пятна на коже, в основном на участках, не подвергающихся воздействию солнца, таких как ягодицы и грудь. Поражения кожи также могут быть обнаружены в виде бляшек, язвенных или опухолевых новообразований. Эти поражения кожи могут быть гипо- или гиперпигментированными и / или атрофированными. Другие находки включают очаговую или генерализованную эритиродермию. Облысение также можно обнаружить при клиническом обследовании.Чаще всего возникает алопеция, но в редких случаях также может наблюдаться полное облысение на теле.
В запущенных случаях при клиническом обследовании также могут быть обнаружены лимфаденопатия и органомегалия (например, гепатоспленомегалия).
E. Какие диагностические тесты следует провести?
Отсутствуют результаты физикального обследования или приемы осмотра, которые могли бы подтвердить диагноз МФ. Диагноз МФ ставится на основании комбинации клинических, гистопатологических, биологических и иммунопатологических критериев (см. Выше).
1. Какие лабораторные исследования (если таковые имеются) следует заказать для установления диагноза? Как следует интерпретировать результаты?
Сначала должны быть получены базовые лабораторные исследования, такие как общий анализ крови (ОАК) с мазком периферической крови (для оценки синдрома Сезари), полная метаболическая панель и лактатдегидрогеназа (ЛДГ).
Для установления диагноза необходимы биопсия кожи и гистология. Для подтверждения диагноза рекомендуется провести множественную биопсию кожи.Присутствие агрегатов мононуклеарных клеток с мозговыми ядрами в эпидермисе, окружающем клетки Лангерганса, также известных как микроабсцессы Паутье, является редким, но диагностическим признаком. В основном биопсия кожи выявляет атипичные лимфоциты в эпидермисе или поверхностной дерме. Биопсия лимфатических узлов может быть получена и имеет прогностическое значение.
Иммунофенотипирование проводится по гистопатологии кожи. Подробное обсуждение иммунофенотипирования выходит за рамки этой главы, но вкратце, отсутствие одного или нескольких маркеров зрелых Т-клеток на лимфоцитах способствует диагностике лимфомы.
ПЦР или саузерн-блот используется затем для оценки перестройки гена Т-клеточного рецептора для подтверждения диагноза грибовидного микоза.
2. Какие визуализационные исследования (если таковые имеются) следует заказать для установления диагноза? Как следует интерпретировать результаты?
Для установления диагноза МФ не требуется визуализирующего исследования, но можно выполнить рентген грудной клетки, компьютерную томографию (КТ) грудной клетки, брюшной полости и таза, чтобы оценить поражение внутренних органов. ВНИМАНИЕ !!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!Известно, что позитронно-эмиссионная томография (ПЭТ) имеет более высокую чувствительность. Пациентам, которым нельзя пройти ПЭТ-сканирование, могут потребоваться исследования магнитно-резонансной томографии (МРТ).
F. Чрезмерно используемые или «потраченные впустую» диагностические тесты, связанные с этим диагнозом.
NA
III. Управление по умолчанию.
После постановки диагноза необходимо определить стадию опухоли. Это включает в себя тщательное обследование кожных поражений и оценку поражения лимфатических узлов и других органов с помощью визуализационных исследований.В запущенных случаях также можно получить биопсию лимфатического узла и, в редких случаях, костного мозга.
Лечение впоследствии зависит от степени поражения болезни.
A. Непосредственное управление.
MF представляет собой вялотекущую неходжкинскую Т-клеточную лимфому, обычно не требующую немедленного лечения. Перед началом лечения необходимо провести подробное обследование. Решения о лечении и лечении МФ следует принимать после консультации со специалистами в области гематологии / онкологии и дерматологии.
Редко МФ может сопровождаться такими осложнениями, как пневмония или сепсис (от кожных инфекций, связанных с иммунодефицитом) или сердечно-сосудистой недостаточностью. Лечение осложнений следует начинать немедленно.
B. Советы медицинского осмотра для руководства.
Врачи должны контролировать изменения кожных поражений и лимфаденопатии после начала лечения. Если при постановке диагноза было установлено поражение внутренних органов, за ними следует внимательно следить с помощью визуализационных исследований.
Важно знать, что местная терапия, например азотистым ипритом и кортикостероидами, может усилить зуд после начала лечения.
Гистоновая деацетилаза (ромедепсис и вориностат), как известно, вызывает изменения ST / T и QT на ЭКГ и требует частого мониторинга ЭКГ при инфузии.
C. Лабораторные тесты для отслеживания реакции и корректировок в управлении.
Во время лечения системными ретиноидами следует тщательно контролировать липидную панель и тесты функции щитовидной железы.Гемфиброзила следует избегать из-за известных побочных эффектов комбинированной терапии; Вместо этого можно использовать таблетки рыбьего жира. Некоторые авторы также задокументировали токсичность для печени, связанную с введением ретинодиса, и у этих пациентов также следует контролировать функциональные тесты печени (LFT).
Известно, что ромедепсис и вориностат, гистондеацетилаза вызывают дискразию крови, изменения ST / T и QT на ЭКГ и побочные эффекты со стороны желудочно-кишечного тракта. У этих пациентов перед началом инфузии необходимо получить исходную ЭКГ, полную метаболическую панель (CMP) и общий анализ крови.
Во время лечения метотрексатом следует контролировать легочные функциональные пробы и комплексную метаболическую панель (включая функцию печени и почек).
D. Долгосрочное управление.
Подробные сведения о лечении МФ выходят за рамки данной главы и должны быть разработаны вместе с экспертом по гематологии / онкологии. Вкратце, локализованное заболевание можно лечить с помощью местной химиотерапии (азотистый иприт или кармустин), местных кортикостероидов (обычно используемых в качестве дополнительного лечения), тотальной электронно-лучевой терапии кожи (TSEBT) для локализованной области и фототерапии (UVB или PUVA).
Обширное заболевание лечат одним или комбинацией любого из следующих: тотальная кожная электронно-лучевая терапия (TSEBT), системный ретиноид, интерферон, ингибиторы гистондеацетилазы, денилейкин дифтитокс, экстракорпоральная фотохимиотерапия (ECP, фотоферез) и системная химиотерапия. Лечение обычно продолжается до исчезновения кожных поражений. В некоторых случаях в литературе задокументирована продолжительность лечения от 3-5 лет до неопределенного срока.
E. Общие ловушки и побочные эффекты управления.
Со временем лимфоциты могут потерять свою склонность к эпидермису и могут нацеливаться на дерму, лимфатические узлы и другие органы, превращая МФ в более агрессивный и устойчивый лейкоз. Иногда MF может подвергаться крупной трансформации клеток (анапластические клетки или иммунобласты), что связано с худшим прогнозом.
Ромедепсис и вориностат являются мощными ингибиторами ферментной системы CYP и могут вызывать серьезную токсичность лекарств, которые метаболизируются аналогичными ферментами CYP.
Лечение системными ретиноидами связано с гипертриглицеридемией, гиперхолестеринемией, аномалиями щитовидной железы и печени, требующими замены гормонов щитовидной железы и гиполипидемической терапии во время лечения.
Сверхактивные глюкокортикоиды нельзя наносить на лицо и шею, так как эти области подвержены осложнениям, вызванным стероидами. Кроме того, использование стероидов в течение длительного периода времени связано с повреждением кожи и кожными инфекциями.
Азотный горчица обычно вызывает аллергические кожные реакции, а кармустин может привести к гиперпигментации кожи.
Фототерапия связана с острым ожогом кожи и, как было показано, увеличивает вероятность других видов рака кожи, если используется в течение более длительных периодов времени.
Хорошо известно, что лечение интерфероном связано с гриппоподобными симптомами.
Денилейкин дифтитокс связан с множественными побочными эффектами, включая сердечную аритмию, дисфункцию печени, миалгию, симптомы гриппа и синдром утечки капилляров (редкое заболевание, при котором экстравазация жидкости через капилляры из крови в межклеточное пространство приводит к гипотонии, отек и полиорганная недостаточность).
Наконец, системная химиотерапия связана с побочными эффектами со стороны желудочно-кишечного тракта и миелосупрессией; метотрексат может вызвать легочную, печеночную и почечную токсичность. Во время лечения следует контролировать легочные функциональные пробы, функциональные пробы печени и почечную панель.
Пегилированный липосомальный доксорубицин связан с заболеваниями крови и ладонно-подошвенной эритродизестезией (болезненное ощущение в ладонях и подошвах, связанное с болезненностью или отеком).
IV.Лечение сопутствующих заболеваний.
A. Почечная недостаточность.
Дозу метотрексата необходимо уменьшить у пациентов с почечной недостаточностью.
B. Печеночная недостаточность.
Дозу метотрексата необходимо уменьшить у пациентов с нарушением функции печени.
C. Систолическая и диастолическая сердечная недостаточность.
Ромедепсис и вориностат могут удлинять QTc; их следует вводить осторожно пациентам с сердечной недостаточностью.
D. Заболевание коронарной артерии или заболевание периферических сосудов.
Без изменений в стандартном управлении.
E. Диабет или другие эндокринные проблемы.
Без изменений в стандартном управлении.
F. Злокачественность.
Без изменений в стандартном управлении.
G. Иммуносупрессия (ВИЧ, хронические стероиды и т. Д.).
Без изменений в стандартном управлении.
H. Первичное заболевание легких (ХОБЛ, астма, ILD).
Без изменений в стандартном управлении.
I. Проблемы с желудочно-кишечным трактом или питанием.
Без изменений в стандартном управлении.
J. Проблемы гематологии или коагуляции.
Без изменений в стандартном управлении.
K. Деменция или психическое заболевание / Лечение.
Без изменений в стандартном управлении.
V. Переходы опеки.
A. Рекомендации по выходу из системы во время госпитализации.
Зависит от сопутствующих заболеваний. Пациенты с МФ обычно не нуждаются в госпитализации. Редко MF может проявляться такими осложнениями, как пневмония или сепсис (от кожных инфекций, связанных с иммунодефицитом) или сердечно-сосудистой недостаточностью, и требует госпитализации.В этих случаях необходим соответствующий диагноз.
B. Ожидаемая продолжительность пребывания.
Зависит от сопутствующих заболеваний.
C. Когда пациент готов к выписке.
Зависит от сопутствующих заболеваний. Пациенты с МФ обычно не нуждаются в госпитализации. Редко MF может проявляться такими осложнениями, как пневмония или сепсис (от кожных инфекций, связанных с иммунодефицитом) или сердечно-сосудистой недостаточностью. От лечения этих осложнений зависит дата выписки.
D. Организация последующего наблюдения в клинике.
1. Когда и с кем следует организовать наблюдение в клинике?
Помимо наблюдения у врачей первичной медико-санитарной помощи, пациенты с диагнозом МФ также должны находиться под наблюдением онколога и дерматолога. В некоторых случаях лечение может занять годы, прежде чем будет достигнута ремиссия. Точные сроки наблюдения варьируются от случая к случаю и должны определяться в индивидуальном порядке.
2. Какие анализы следует провести перед выпиской, чтобы лучше всего пройти первый визит в клинику?
Пациентам с МФ не требуется госпитализация.В случае госпитализации пациента можно провести такие процедуры, как биопсия кожи, а также гистопатологические и иммунопатологические тесты и тестирование биологических маркеров, чтобы ускорить процесс диагностики и лечения до того, как пациент появится в клинике. При необходимости могут потребоваться визуализирующие исследования, такие как рентген грудной клетки и компьютерная томография, для определения стадии заболевания.
3. Какие анализы следует заказать амбулаторно до или в день посещения клиники?
Basic CBC, CMP и LDH следует заказать до посещения клиники.
E. Соображения по размещению.
NA
F. Прогноз и консультирование пациентов.
Прогноз МФ зависит от степени поражения и типа поражения кожи. Пациенты с запущенным заболеванием с поражением нескольких органов имеют худший прогноз. Пациенты с эритродермией и опухолевым ростом кожи имеют худшие результаты по сравнению с пациентами с локализованным пятнистым поражением кожи.
Пациенты, у которых МФ переходит в более агрессивные формы, также имеют худший прогноз.
Другие факторы, такие как высокий уровень лактатдегидрогеназы (ЛДГ), фолликулотропные МФ, пожилой возраст, мужской пол, пойкилодерматозные МФ и МФ с крупноклеточной трансформацией, также связаны с худшими результатами.
VI. Безопасность пациентов и меры качества.
A. Стандарты и документация по основным показателям.
NA
B. Соответствующая профилактика и другие меры по предотвращению реадмиссии.
Пациенты должны быть обучены наблюдать за участками кожи при любом прогрессировании или новом возникновении лимфаденопатии.Пациенту следует описать появление новых симптомов, связанных с поражением внутренних органов. Раннее обнаружение этих симптомов может помочь в ранней диагностике и лечении и, таким образом, избежать поздних осложнений заболевания, предотвращающих попадание в больницу.
VII. Какие доказательства?
Виллемзе, Р., Яффе, Э.С., Бург, Дж., Черрони, Л., Берти, Э, Свердлов, Ш. «Классификация ВОЗ-EORTC для кожных лимфом». Кровь. об. 105. 2005. pp. 3768-3785.
Джавед, С.И., Мысковски, П.Л., Хорвиц, С., Московиц, А., Кверфельд, К. «Первичная кожная Т-клеточная лимфома (грибовидный микоз и синдром Сезари)». J Am Acad Dermatol. об. 70. 2014. С. e1-17.
Zackheim, HS, McCalmont, TH. «Грибовидный микоз: великий имитатор». J Am Acad Dermatol. об. 47. 2002. pp. 914-918.
Vonderheid, EC, Pena, J, Nowell, P. «Подсчет клеток Сезари в эритродермической кожной Т-клеточной лимфоме: значение для прогноза и определения стадии». Leuk Лимфома. об. 47. 2006. pp. 1841-1856.
Хуанг, К.П., Вайншток, Массачусетс, Кларк, Калифорния, Макмиллан, А., Хоппе, Р.Т., Ким, Ю.Х. «Вторичные лимфомы и другие злокачественные новообразования у пациентов с грибовидным микозом и синдромом Сезари: данные популяционных и клинических когорт». Arch Dermatol. об. 143. 2007. С. 45-50.
Girardi, M, Heald, PW, Wilson, LD. «Патогенез грибовидного микоза». N Engl J Med. об. 350. 2004. С. 1978–1988.
Copyright © 2017, 2013 ООО «Поддержка принятия решений в медицине». Все права защищены.

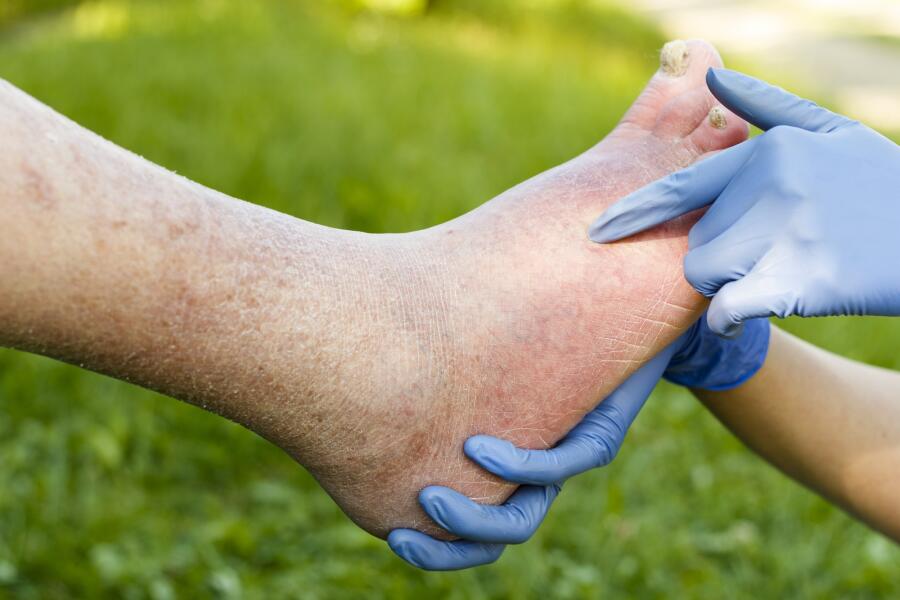
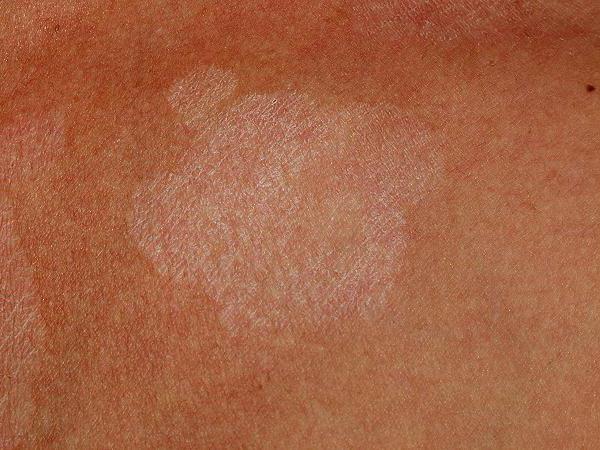 Волосы утрачивают естественный блеск,
Волосы утрачивают естественный блеск,
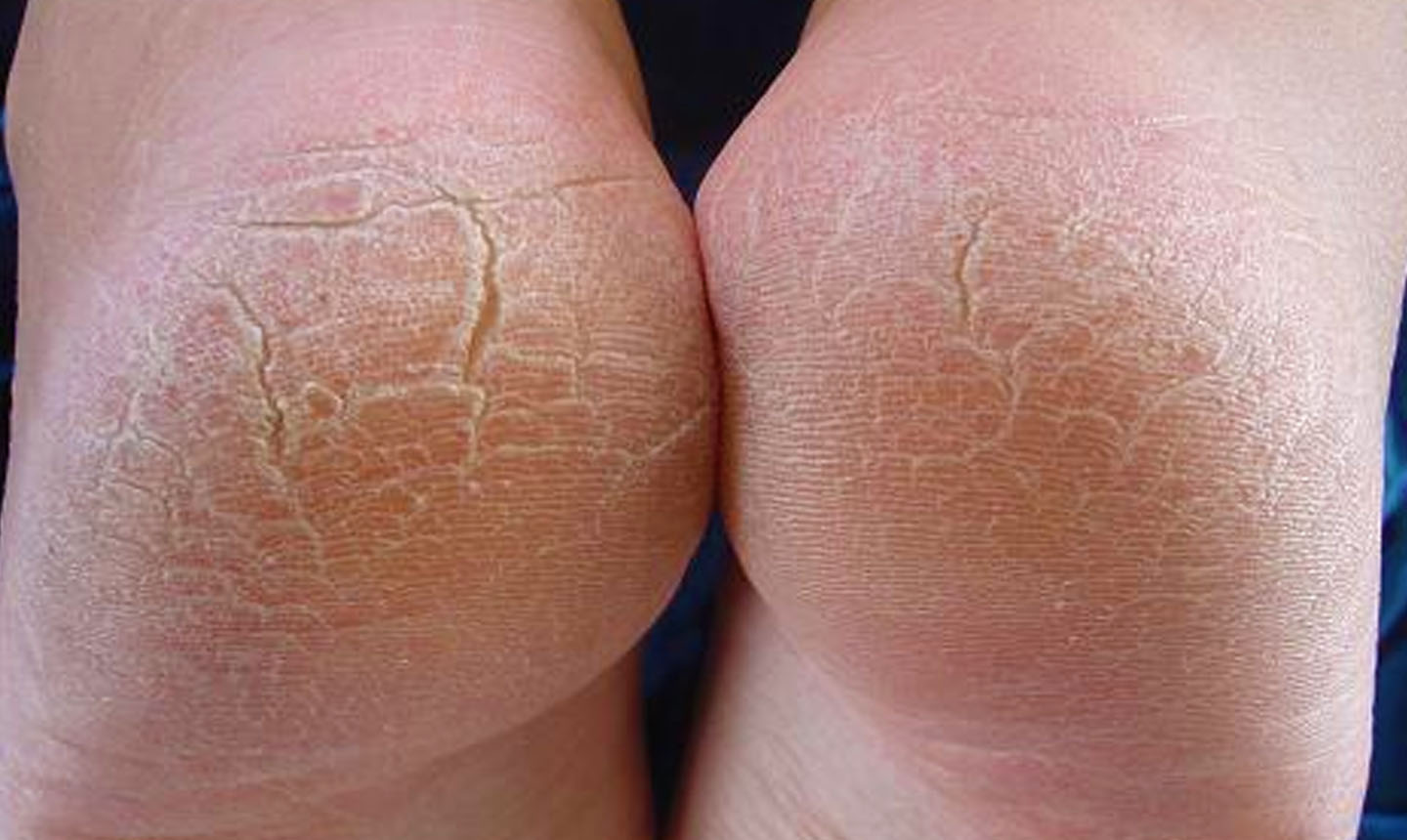
 Необходимо сделать исследования на грибы
Необходимо сделать исследования на грибы При микозе складок наиболее выражены воспалительные явления в зоне сплошного периферического валика,
При микозе складок наиболее выражены воспалительные явления в зоне сплошного периферического валика,


:max_bytes(150000):strip_icc()/GettyImages-823679170-5b092265a474be0037cc1dba.jpg)