При лечении дисбактериоза у детей назначают эубиотик — КиберПедия
а) бисептол
б) бифидумбактерин
в) димедрол
г) панзинорм
Задание 2.Продемонстрировать технику обработки кожных складок при опрелости у грудного ребенка по чек-листу, оформить фотоотчёт выполнения данной манипуляции.
Перед выполнением манипуляции посмотрите видео сюжет манипуляции «Обработка складок у малыша» по указанной ниже ссылке. Сравните действия медицинской сестры с алгоритмом манипуляции по чек-листу, найдите нарушения в технике выполнения манипуляции, и опишите их при ответе.
https://www.youtube.com/watch?v=Sikb6PLbr3s
Подготовка пациента:
— положить ребёнка на пеленальный стол, обработанный одним из дез средств (ближе к источнику света) ираспеленать его.
— успокоить ребенка
Оснащение:
— Ёмкость (мензурка) со стерильным вазелиновым или растительным маслом
— Бикс со стерильными ватными шариками
— Стерильный лоток
— Стерильный пинцет
— Стерильные перчатки
— Лоток для сброса, использованного материала
— Ёмкость с дез. раствором и чистая ветошь
раствором и чистая ветошь
— Ёмкость для использованной ветоши
— 2 чистые пелёнки
— Комплект для пеленания или комплект чистого нательного белья: подгузник
(памперс), ползунки, распашонки, кофточка)
Последовательность действий:
1.Вымойте руки гигиеническим способом
2.Осмотрите кожные покровы ребенка,
3.Подмойте ребенка проточной водой (37-38 0 С) при загрязнении кожных покровов каловыми массами или мочой,
4. Подсушите кожные покровы чистой пелёнкой,
5.Уложите ребенка на спину на чистую пеленку,
6.Помойте руки, наденьте стерильные перчатки,
7.Возьмите ватный шарик стерильным пинцетом из бикса, опустите его в мензурку со стерильным маслом комнатной температуры,
8.Достаньте рукой его рукой и слегка отожмите,
9.Осторожными движениями протрите кожные складки в следующей последовательности: заушные, шейные, подмышечные, локтевые, подколенные, паховые, ягодичные, межягодичная,
10. Сбросьте использованный ватный шарик в лоток, для сброса, использованного материала,
Сбросьте использованный ватный шарик в лоток, для сброса, использованного материала,
11. При необходимости ватный шарик можно поменять.
12. Сбросьте использованный ватный шарик и перчатки в лоток для сброса, использованного материала,
13. Запеленайте ребенка, согласно алгоритму манипуляции или оденьте его.
Ошибки: манипуляция выполнена без перчаток, а должна проводиться в стерильных перчатках, стерильными ватными шариками, которые достаются из стерильного лотка стерильным пинцетом. Нарушена последовательность обработки кожных складок, по чек-листу следующая последовательность — заушные, шейные, подмышечные, локтевые, подколенные, паховые, ягодичные, межягодичная. При обработке межягодичной складки движение должно быть спереди назад, особенно это важно при обработки межягодичной складки у девочек
Здания 3.Решить профессиональные задачи.
Задача № 1
Ребенок 6-ти месяцев находится на приеме в поликлинике в день здорового ребенка.
Диагноз: экссудативно-катаральный диатез.
Ребенок с 3-х месяцев на искусственном вскармливании. Вес при рождении 3200, в последующие месяцы прибавка массы 1000-1100 гр. С 2 месячного возраста у ребенка часто возникают опрелости, несмотря на хороший уход.
Кожа на щеках сухая, гиперемированная. На волосистой части головы себорея. Мать отмечает усиление кожных высыпаний после употребления ребенком в пищу яичного желтка, виноградного сока. Опрелости I-II ст. в паховых складках, в подмышечных областях, на складках шеи. Из носа слизистые выделения.
Задания
1. Определите проблемы пациента; сформулируйте цели и составьте план сестринского ухода по приоритетной проблеме с мотивацией каждого сестринского вмешательства.
2. Объясните матери необходимость соблюдения диеты и обучите мать правилам ведения «Пищевого дневника».
3. Продемонстрируйте обработку кожи и слизистых ребенка (в электронном отчете).
Проблемы пациента:
— изменения кожных покровов в результате нарушения обмена веществ и неправильного питания;
— ребенок неправильно питается из-за незнания мамы правил кормления малышей;
- затруднение носового дыхания из-за выделений из носа.
Приоритетная проблема: неправильное питание ребенка из-за дефицита знаний матери о рациональном вскармливании.
Цель: мать через 1-2 дня расскажет об особенностях питания своего ребенка.
| План | Мотивация |
| 1. М/с проведет с матерью беседу о заболевании. | 1. Для ликвидации дефицита знаний матери о заболевании. |
| 2. М/с расскажет матери о причинах заболевания и значении соблюдения диеты. | 2. Для ликвидации дефицита знаний матери о заболевании. |
| 3. М/с научит мать ведению «Пищевого дневника». | 3. Для выявления непереносимости продуктов. Для выявления непереносимости продуктов.
|
| 4. М/с обучит мать уходу за полостью носа. | 4. Для улучшения носового дыхания и облегчения приема пищи. |
| 5. М/с организует консультацию врачей-специалистов (аллерголога, ЛОРа, дерматолога). | 5. Для ранней диагностики. |
- Пищевой дневник – это блокнот или тетрадь, в которой мама ведет учет продуктов, съеденных малышом в течение дня, и отражает все необычные реакции и проявления, которые возникают у ребенка в этот период
Какие разделы должны быть в пищевом дневнике?
- дата и время кормления,
- вид продуктов,
- примерное количество съеденной пищи,
- все необычные реакции и изменения в самочувствии ребенка (кожные проявления, изменение характера стула или эмоционального состояния ребенка),
- время их возникновения.
Правила ведения пищевого дневника:
Ведение этого учетного документа – дело ответственное и требует от мамы самодисциплины и терпения. В течение периода времени, определенного педиатром или врачом-аллергологом, ей необходимо точно и методично заносить в дневник все употребленные за день продукты, а также фиксировать все изменения в самочувствии малыша на протяжении суток. Удобнее отвести для заполнения дневника определенное время, например, вечерние часы, когда малыш спит.
В течение периода времени, определенного педиатром или врачом-аллергологом, ей необходимо точно и методично заносить в дневник все употребленные за день продукты, а также фиксировать все изменения в самочувствии малыша на протяжении суток. Удобнее отвести для заполнения дневника определенное время, например, вечерние часы, когда малыш спит.
3.
Задача № 2
Ребенку 1 мес. Мать жалуется на беспокойство ребенка, плохой сон. Ребенок от первой беременности, нормально протекавшей. Масса при рождении 3400 г, длина 51 см. Находится на естественном вскармливании, но кормления проводятся беспорядочно. После кормления беспокоен. Стул 1 раз в день, кашицеобразный, без примесей.
Температура нормальная, масса 3500, длина 54 см, кожа бледная, тургор тканей снижен. При контрольном взвешивании выяснено, что за кормление ребенок высасывает по 60-80 мл. Молока в молочной железе матери после кормления не остается. Ребенку был поставлен диагноз: дистрофия по типу гипотрофии 1 степени.
Ребенку был поставлен диагноз: дистрофия по типу гипотрофии 1 степени.
Задания:
1. Определите проблемы пациента; сформулируйте цели и составьте план сестринского ухода по приоритетной проблеме с мотивацией каждого сестринского вмешательства. Объясните родителям необходимость соблюдения режима питания.
2. Объясните матери необходимость соблюдение режима питания и обучите ее правилам введения докорма.
3. Продемонстрируйте технику контрольного взвешивания (в электронном отчете).
Эталон ответа на ПСЗ.
Нарушенные потребности: спать, есть
| ПРОБЛЕМЫ
ПАЦИЕНТА | ЦЕЛЬ
| ПЛАН | Вид действия | ОЦЕНКА действий |
| Настоящие – нарушение питания, нарушение сна, низкая прибавка массы, нерациональное вскармливание, недокорм.
Потенциальные – отставание в физ.  развитии, отставание в нервно – психическом развитии, развитие иммунодефицита. развитии, отставание в нервно – психическом развитии, развитие иммунодефицита.
Приоритетная- нерациональное вскармливание, недокорм. Приоритетная проблема – нерациональное вскармливание. | Краткосрочная- нормализовать питание ребенка к концу недели
Долгосрочная – ребенок даст хорошую прибавку массы тела к концу месяца | 1. Мед. Сестра проведет контрольное взвешивание. Для определения дозы высасываемого молока, выяснение дефицита массы.
2. Мед. Сестра определит возрастную суточную и разовую дозу молока, дозу докорма. Для выявления дефицита питания и его устранения. 3. Мед. Сестра даст рекомендации матери по режиму кормления ребенка. Для выработки условного рефлекса у малыша на кормление. 4. Мед сестра по назначению врача порекомендует введение докорма( в виде адаптированной смеси). Для устранения недостающего объема питания. 5. Мед. Сестра по назначению врача, расскажет и порекомендует кормящей женщине увеличить объем употребляемой жидкости до 3-х литров, употреблятьв пищу продукты, стимулирующие лактацию.  Для устранения гипогалактин Для устранения гипогалактин
6. Мед. Сестра будет выполнять назначения врача. |
2. Правила введения докорма:
1. Докорм даётся после кормления грудью;
2. В зависимости от количества грудного молока докорм назначают после каждого кормления, после 2-х – 3-х кормлений, в виде самостоятельного кормления.
3. Прикладывать ребёнка к груди следует не менее 3-4 раз в сутки (иначе снижается лактация).
4. В сутки в качестве докорма ребёнок должен получать не более 2-х разных смесей.
5. Если объём докорма невелик (30-50 мл), его нужно давать с ложечки, если объём больше 50 мл – из бутылочки с соской.
6. Докорм даётся после кормления сразу (если ребёнок не съел, не следует давать докорм повторно через некоторое время).
7. В качестве докорма рекомендуется применение адаптированных молочных смесей.
8. При нарушении процессов пищеварения предпочтение отдается кисломолочным смесям. Их количество не должно превышать ½ суточного объёма питания.
Их количество не должно превышать ½ суточного объёма питания.
9. Смесь готовится непосредственно перед употреблением.
3.
Здания 4. Продемонстрировать технику проведения туалета пупочной ранки при омфалите по чек-листу, оформить фотоотчёт выполнения данной манипуляции.
Особенности применения препаратов для микробиологической коррекции дисбактериоза кишечника у детей | #05-06/00
Ю. А. Копанев
НИИ эпидемиологии и микробиологии им. Г. Н. Габричевского, Москва
Л. Г. Кузьменко, доктор медицинских наук, профессор
РУДН, Москва
В комплексной терапии дисбактериоза кишечника у детей выделяют следующие направления: иммунокоррекция, микробиологическая коррекция, коррекция нарушений функций желудочно-кишечного тракта (ЖКТ), лечение сопутствующих заболеваний (прежде всего паразитарных и хронических инфекционных) [1, 3, 4].

Использование комплексных схем лечения, включающих препараты этих направлений, дают более
выраженный и стойкий клинический и микробиологический эффект, нежели лечение, охватывающее лишь одно из данных направлений
В результате наблюдений в течение трех лет за детьми, получавшими лечение по поводу дисбактериоза кишечника (1-1,5 тысячи пациентов в год), мы выделили некоторые особенности микробиологической коррекции у детей.
Микробиологическая коррекция включает в себя антимикробные препараты и препараты бактерий нормальной кишечной флоры (эубиотики).
Антимикробные препараты при лечении дисбактериоза назначаются для селективной деконтаминации, т. е. целенаправленного снижения количества условно-патогенных микроорганизмов. Для этой цели используются бактериофаги, кишечные антисептики (фуразолидон, интетрикс, энтерол и др.), растительные антисептики (хлорофиллипт, ротокан), противогрибковые препараты [1]. Доказано прямое антимикробное действие комплексного иммуноглобулинового препарата (КИП) [2]. Применение антибиотиков для коррекции дисбактериоза нежелательно, так как эти препараты часто приводят к усугублению микробиологических нарушений аутофлоры. Тем не менее применение антибиотиков оправданно, когда дисбактериоз является следствием хронического инфекционного заболевания (хламидиоз, йерсиниоз).
Доказано прямое антимикробное действие комплексного иммуноглобулинового препарата (КИП) [2]. Применение антибиотиков для коррекции дисбактериоза нежелательно, так как эти препараты часто приводят к усугублению микробиологических нарушений аутофлоры. Тем не менее применение антибиотиков оправданно, когда дисбактериоз является следствием хронического инфекционного заболевания (хламидиоз, йерсиниоз).
Особенности применения антимикробных препаратов
1. Применение любых препаратов для селективной деконтаминации может привести к ухудшению состояния. Это связано с токсическим действием продуктов распада условно-патогенных микроорганизмов. Если в составе микробиоценоза кишечника снижено количество бактерий аутофлоры, выполняющих барьерную функцию, вероятность осложнений увеличивается. При ухудшении состояния, которое может быть существенным, следует подключить симптоматическую терапию или приостановить проведение деконтаминации.
2. Антимикробная терапия может оказаться неэффективной без сопутствующей иммунокоррекции.
3. Длительное непрерывное (более двух недель) применение антимикробных препаратов, в том числе бактериофагов, не оправданно, так как в этом случае происходят нарушения состава аутофлоры кишечника. В частности, угнетается кишечная палочка с нормальной ферментативной активностью, а также лактобактерии.
4. В случае когда дисбактериоз кишечника вызван очагом хронической инфекции (хламидии, йерсинии), антибактериальная терапия будет более эффективна, если ее начать в стадии обострения, и менее эффективна, если ее начинать в фазе ремиссии.
Эубиотики (пробиотики) — препараты живых бактерий нормальной кишечной флоры — применяются при коррекции дисбактериоза кишечника с дефицитом этих микробов в составе микробиоценоза кишечника [5]. Препараты данной группы применяются также в ситуациях, когда требуется поддержание микробиоценоза при каких-либо неблагоприятных факторах: кишечные или респираторные инфекции, применение антибактериальных препаратов, в качестве профилактики поствакцинальных осложнений, при прорезывании зубов и др.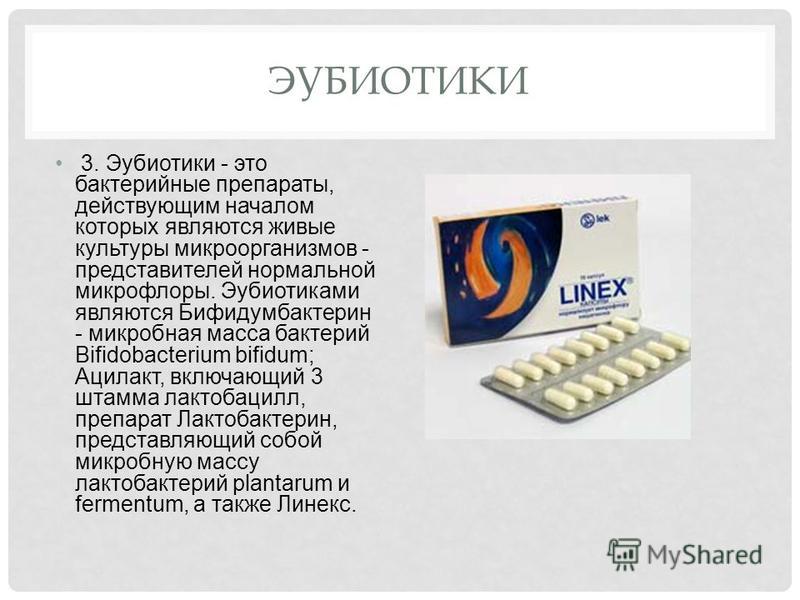
Наиболее широко известные эубиотики: отечественные — сухие бифидумбактерин, лактобактерин, ацилакт, аципол, бификол, колибактерин; импортные — примадофилюс, флорадофилюс, линекс. Относительно недавно появились и хорошо себя зарекомендовали жидкие формы: жидкий бифидумбактерин (жидкий концентрат бифидобактерий, ЖКБ), жидкий лактобактерин (жидкий концентрат лактобактерий, ЖКЛ). Препараты примадофилус и фермент лактаза применяются в различных возрастных группах с целью коррекции нарушенной микрофлоры и уменьшения брожения в пищеварительном тракте. Иногда метеоризм и нарушения стула бывают даже у находящихся на естественном вскармливании детей. Для коррекции подобных нарушений, часто связанных с возрастной ферментативной недостаточностью, возможно назначение ферментного препарата лактозы. Можно добавлять содержимое капсулы непосредственно в молоко или молочные продукты.
Примадофилус применяется для коррекции дисбактериоза в любой возрастной группе, поскольку в каждую из четырех форм выпуска препарата включены специально отобранные те виды бифидо- и лактобактерий, которые встречаются в норме в данном возрасте. Препарат выпускается в кишечнорастворимых капсулах и в порошке — для младенцев.
Препарат выпускается в кишечнорастворимых капсулах и в порошке — для младенцев.
Рекомендуется: обычная доза приема — одна капсула, в порошке — один раз в день по чайной ложке во время еды.
Порошок может добавляться к любым видам пищи, включая детское питание.
Особенности применения эубиотиков
1. Лечебные дозы для восстановления бифидо- и лактофлоры при очень существенном снижении количества этих бактерий (бифидобактерии менее 107, лактобактерии менее 105) — по 5 доз каждого из препаратов два раза в день при курсе лечения не менее трех недель. Применение меньших доз или короткие курсы лечения в этой ситуации часто оказываются недостаточно эффективными.
2. При умеренном снижении бифидо- и лактофлоры (бифидобактерии не менее 107, лактобактерии не менее 105) эффективно использование эубиотиков по 5 доз один раз в сутки. Как поддерживающие препараты эубиотики могут успешно использоваться короткими курсами (7-10 дней).
3. Аутофлора восстанавливается лучше при совместном применении эубиотиков и ферментативных препаратов (абомин, мезим-форте, креон и др.) [4]. Препараты ЖКБ и ЖКЛ содержат ферменты.
4. Во время применения эубиотиков возможно кратковременное ухудшение самочувствия ребенка, не требующее отмены препаратов. Чем активнее препарат, тем более вероятно ухудшение в процессе лечения. Лечение самыми активными из современных эубиотиков — ЖКБ и ЖКЛ — нередко приводит к появлению болей в животе, обострению или появлению кожных высыпаний, изменению характера стула. Все эти явления практически всегда проходят в течение недели, не требуя коррекции терапии.
5. При длительном использовании с лечебной целью однокомпонентных препаратов (например, включающих только бифидофлору) желательно совместно применять в поддерживающей дозе препараты других бактерий аутофлоры. В противном случае, по нашим наблюдениям, может развиться нежелательный перекос микробиоценоза в сторону одной из трех главных групп (бифидофлора, лактофлора, кишечная палочка с нормальной ферментативной активностью) с угнетением остальных.
Знание этих особенностей может помочь более грамотно назначать терапию и правильно оценивать происходящие во время микробиологической коррекции изменения состояния.
Литература
1. Коровина Н. А., Вихирева З. Н., Захарова И. Н., Заплатников А. Л. Профилактика и коррекция нарушений микробиоценоза кишечника у детей раннего возраста. М., 1995.
2. Копанев Ю. А., Соколов А. Л., Алешкин В. А., Пожалостина Л. В., Ефимова О. Г. Действие комплексного иммуноглобулинового препарата на условно-патогенную флору // Врач. 1998. № 5. С. 38.
3. Мухина Ю. Г. Диагностика и коррекция дисбактериоза у детей // Русский медицинский журнал. 1999. №11. С. 487-494.
4. Таболин В. А., Бельмер С. В. и др. Рациональная терапия дисбактериоза кишечника у детей. М., 1998.
5. Применение бактерийных биологических препаратов в практике лечения больных кишечными инфекциями. Диагностика и лечение дисбактериоза кишечника. Методические рекомендации. М., 1986.
Методические рекомендации. М., 1986.
Дисбактериоз у новорожденных и грудных детей | Bifiform ru
В норме микрофлора кишечника состоит в среднем из 1 млн микробов на 1 мл содержимого. Нормальную микрофлору составляют 15-20 представителей анаэробных (бактерии, которые не могут жить в присутствии кислорода) и аэробных (способных существовать в присутствии кислорода) бактерий основных родов: бактероиды, бифидобактерии, лактобактерии и другие. Бифидобактерии относятся к доминирующей микрофлоре (Ig10-11)1,2
Здоровая микрофлора участвует в пищеварительных процессах организма, усиливает активность пищеварительных ферментов, действует на моторику желудочно-кишечного тракта, способствует выработке витаминов, гормонов, аминокислот и повышает иммунитет.
Также микрофлора выполняет детоксикационную и антиаллергенную функции. Защитные функции кишечника сводятся к созданию барьера для размножения болезнетворных бактерий и разрушения аллергенов. Нормальная микрофлора также обладает антиоксидантными, антимутагенными и противораковыми функциями1,2
Нормальная микрофлора также обладает антиоксидантными, антимутагенными и противораковыми функциями1,2
Формирование микрофлоры
Формирование и функционирование иммунной системы происходит в 2 этапа. Первый заключается в формировании клонов Т- и В-лимфоцитов на основе генетического материала, который был представлен в период раннего эмбриогенеза (ранние этапы беременности).
Второй этап — начинается после рождения человека и заселения микробами слизистых оболочек, в том числе и ЖКТ. Кишечник – представляет собой не только часть пищеварительной системы, но и является иммунным органом, до 80% иммунных клеток располагаются именно в кишечнике. Таким образом, формирование собственного кишечного иммунитета у грудного ребенка происходит с период ранней микробной колонизации и начинается сразу после рождения ребенка. Поэтому момент появления на свет является одним из ключевых этапов в формировании здорового ЖКТ3.
В становлении нормальной микрофлоры ребенка особенно важную роль играют бифидобактерии. Количество бифидобактерий в кишечнике ребенка, находящегося на грудном вскармливании, быстро нарастает в первые недели его жизни. В течение первого года жизни меняется видовой состав кишечной микрофлоры, что связано с различными периодами в жизни ребенка: периодом грудного вскармливания до введения прикорма, после введения прикорма, после появления в рационе твердой пищи, после прекращения грудного вскармливания. Беременность мамы, микрофлора родовых путей, течение родов, рождение раньше срока, наличие и продолжительность грудного вскармливания, раннее введение прикорма, частые простудные заболевания определяют становление этого процесса.
Количество бифидобактерий в кишечнике ребенка, находящегося на грудном вскармливании, быстро нарастает в первые недели его жизни. В течение первого года жизни меняется видовой состав кишечной микрофлоры, что связано с различными периодами в жизни ребенка: периодом грудного вскармливания до введения прикорма, после введения прикорма, после появления в рационе твердой пищи, после прекращения грудного вскармливания. Беременность мамы, микрофлора родовых путей, течение родов, рождение раньше срока, наличие и продолжительность грудного вскармливания, раннее введение прикорма, частые простудные заболевания определяют становление этого процесса.
Нормальная микрофлора ребенка
Микрофлора обусловливает защиту слизистой кишечника от внедрения патогенных микроорганизмов, поддерживает и активирует иммунную систему, участвует в обмене белков, липидов, углеводов, выполняет антиаллергическую функцию, участвует в синтезе аминокислот, витаминов, гормонов, влияет на пищеварительные функции желудочно-кишечного тракта 1.
Пробиотический комплекс Бифиформ Бэби можно давать даже новорожденным с первых дней жизни. Его основное назначение – формирование сбалансированной микрофлоры кишечника, в том числе, при различных проблемах, связанных с кормлением. Особый комплекс бактерий может способствовать профилактикекишечных расстройств различного характера, включая колики 4.
Нормальную микрофлору кишечника составляют множество видов микроорганизмов. Одни из значимых и изученных на сегодняшний день:
Бифидобактерии
Представители рода Bifidobacterium являются наиболее важным компонентом нормальной микробиоты желудочно-кишечного тракта человека. Большая часть бифидобактерий находится в толстой кишке, составляя у детей более 90% всех микроорганизмов 5 Начинают доминировать в кишечной микрофлоре младенцев к концу первой недели жизни. Синтезируют аминокислоты и белки, витамин К, пантотеновую кислоту, витамины группы В: B1 — тиамин, B2 — рибофлавин, B3 — никотиновую кислоту, фолиевую кислоту, B6 — пиридоксин. Способствуют усилению процессов всасывания через стенки кишечника ионов кальция, железа, витамина D 6.
Способствуют усилению процессов всасывания через стенки кишечника ионов кальция, железа, витамина D 6.
Лактобактерии
Уменьшают активность пероксидазы, оказывая антиоксидантный эффект, обладают противоопухолевой активностью, стимулируют продукцию иммуноглобулина А (IgA), подавляют рост патогенной микрофлоры и стимулируют рост лакто- и бифидофлоры, оказывают противовирусное действие 6
Нарушения микрофлоры
Дисбактериоз является нарушением качественного и количественного состава микрофлоры кишечника. Это означает, что патогенных микроорганизмов может стать значительно больше, чем полезных. Иногда сам организм может справиться с временно возникшими изменениями в кишечной микрофлоре, но при определенных ситуациях для лечения дисбактериоза используются пробиотики, содержащие полезные микроорганизмы 2.
Дисбактериоз у грудных детей может проявляться в виде изменения частоты, состава и цвета стула, нарушения процессов переваривания пищи, повышенного газообразования, беспокойного поведения ребенка, плача, повышенной раздражительности, плохого аппетита и сна, ухудшение состояния кожного покрова и даже аллергических реакций 3.
Причины возникновения дисбактериоза у новорожденных и грудничков
В группе риска по нарушению баланса микрофлоры находятся дети, мамы которых имели различные осложнения в период беременности и родах, а также дети, находящиеся на искусственном вскармливании, недоношенные. Простудные заболевания, прием некоторых лекарственных препаратов (лечение антибиотиками) могут приводить к нарушениям баланса микрофлоры кишечника. Внешними проявлениями этого состояния могут быть нарушения сна, плаксивость, нарушение аппетита, аллергические высыпания, колики и постоянное бурчание в животе после кормления 1,3.
Сдача анализов
При возникновении симптомов недомогания у Вашего ребенка, обязательно проконсультируйтесь с врачом. Для постановки диагноза дисбактериоза врач может порекомендовать сдать анализ кала на дисбактериоз.
Как правильно собрать кал для анализа на дисбактериоз:
Кал собирается в стерильную баночку, предварительно прокипяченную вместе с крышкой в течение 20 минут. Посуда для анализа, на основании результатов которого будет проводиться лечение дисбактериоза у грудных детей, должна храниться в холодильнике не более суток. Собранный в стерильную емкость анализ доставляется в лабораторию в течение 2 часов (не позднее). Результаты подготавливаются через 7-10 дней.
Посуда для анализа, на основании результатов которого будет проводиться лечение дисбактериоза у грудных детей, должна храниться в холодильнике не более суток. Собранный в стерильную емкость анализ доставляется в лабораторию в течение 2 часов (не позднее). Результаты подготавливаются через 7-10 дней.
Для получения информации о том, где можно приобрести Бифиформ Бэби , посетите раздел «Где купить».
БАД. НЕ ЯВЛЯЕТСЯ ЛЕКАРСТВЕННЫМ СРЕДСТВОМ
- Донских Е.Е. Микрофлора — Дисбактериоз у детей http://lekmed.ru/info/literatyra/disbakterioz-y-detei.html
- Корниенко Е.А., Мазанкова Л.Н., Горелов А.В. Применение пробиотиков в педиатрии: анализ лечебного и профилактического действия с позиций доказательной медицины. Лечащий врач 2015.
- И.А. Беляева. Пробиотические добавки для коррекции младенческих колик: перспективы использоавния.
- Беляева И.А., Митиш М.Д., Катосова Л.К. Эффективность использования пробиотиков у недоношенных детей.
 РМЖ 2009.
РМЖ 2009. - Рыбальченко О.В., Бондаренко В.М. Оценка микробиоты и пробиотических штаммов с позиций новых научных технологий. Фарматека №11, 2016
- Бельмер С.В., Малкоч А.В. Кишечная микрофлора и значение пребиотиков для ее функционирования. Лечащий врач 2006, 4
PP-BIB-RUS-0082
Задания тестовые задания по циклу «Сестринское дело в педиатрии: организация и управление» с ответами
содержание ..
2
3
4
5 ..
300.
Профилактическая доза витамина D ребенку составляет (МЕ)
а) 200
б) 400
в) 600
г) 800
301. Характерное проявление нервно-артритического диатеза у детей
а) приступ рвоты
б) приступ удушья
в) отеки
г) желтуха
302.
Причина экссудативно-катарального диатеза у детей
а) грудное вскармливание
б) перегревание
в) переохлаждение
г) ферментативная
недостаточность
303. При
аллергическом диатезе у ребенка из питания исключают
а) цитрусовые
б) кефир
в) яблочный сок
304.Лимфатико-гипопластический
диатез у детей характеризуется увеличением лимфатических узлов и
а) сердца
б) щитовидной железы
в) вилочковой железы
г) почек
305.
Причина внезапной смерти у детей с лимфатико-гипопластическим диатезом —
недостаточность
а) дыхательная
б) сердечная
в) почечная
г) надпочечниковая
306. Аскаридозом заражаются:
а) воздушно-капельным путем
б) при употреблении недоброкачественной пищи
в) при употреблении недостаточно обработанной рыбы
г) через грязные руки, воду, овощи
307.
Недомогание, снижение аппетита, анемия, аллергические реакции, эозинофилия у
детей характерны для
а) энтеробиоза
б) аскаридоза
в) описторхоза
г) большинства гельминтозов
308. У
детей отмечаются боли в животе, тошнота, рвота, периодический неустойчивый
стул, если гельминты паразитируют в
а) печени
б) кишечнике
в) легких
г) коже
309. Для лечения
лямблиоза ребенку назначают
а) антибиотики и сульфаниламиды
б) нитрофурановые препараты и
метронидазол
в) спазмолитики и сульфаниламиды
г) холекинетики и сульфаниламиды
310.
Энтеробиоз у детей вызывается
а) аскаридами
б) острицами
в) лямблиями
г) кошачьей двуусткой
311. Зуд в
перианальной области, как основной симптом гельминтоза у детей, характерен для
а) энтеробиоза
б) описторхоза
в) аскаридоза
г) трихоцефалеза
312. Для
Для
специфической терапии энтеробиоза у детей применяют
а) димедрол
б) декарис
в) баралгин
г) фуросемид
313. Для
дегельминтизации у детей применяют
а) бисептол
б) пирантел
в) левомицетин
г) супрастин
314.
Особое значение в развитии вторичных дискинезий желчевыводящих путей у детей
придается
а) лямблиозу кишечника
б) перенесенной дизентерии
в) перенесенному сальмонеллезу
г) хроническому тонзиллиту
315. Для
улучшения обменных процессов гепатоцитов ребенку с хроническим гепатитом
назначают мембраностабилизатор
а) интерферон
б) преднизолон
в) эссенциале форте
г) левамизол
316. В
лечении детей с острым панкреатитом применяют ингибиторы протеаз
а) но-шпу или платифилин
б) контрикал или трасилол
в) фестал или панзинорм
г) баралгин или триган
317. Симптомами гастрита с пониженной
Симптомами гастрита с пониженной
секрецией являются:
а) » голодные», ночные
боли
б) отрыжка, тяжесть в области
желудка после еды
в) изжога, боль в эпигастрии через
1,5 часа после еды
г) запоры, метеоризм
318.
Существенную роль в язвообразовании у детей отводят
а) кишечной палочке
б) протею
в) хеликобактерным
микроорганизмам
г) палочке молочно-кислого брожения
319.
Осложнение язвенной болезни у детей, требующее немедленного оказания помощи
а) пенетрация
б) малигнизация
в) кровотечение
г) деформация луковицы
двенадцатиперстной кишки
320. Боли
опоясывающего характера с иррадиацией в левую половину грудной клетки у ребенка
характерны для
а) острого панкреатита
б) острого холецистохолангита
в) хронического активного гепатита
г) желчной колики
321. В
В
биохимическом анализе крови у детей с острым панкреатитом характерно повышение
уровня
а) глюкозы
б) холестерина
в) билирубина
г) амилазы
322. При
лечении дисбактериоза у детей назначают эубиотик:
а) бисептол
б) бифидумбактерин
в) димедрол
г) панзинорм
323. Для
лучшего отхождения мокроты ребенку с острым бронхитом применяют
а) вибрационный массаж,
постуральный дренаж
б) банки, горчичники
в) оксигенотерапию, УФО
г) строгий постельный режим, диету
№ 15
324.
Ведущий клинический симптом обструктивного бронхита у детей
а) боль в грудной клетке
б) лихорадка
в) одышка
г) слабость
325. Для
определения этиологического фактора пневмонии у ребенка следует провести
а) общий анализ крови
б) общий анализ мочи
в) рентгенографию легких
г) посев мокроты
326. Лихорадка, одышка, кашель, локальное
Лихорадка, одышка, кашель, локальное
укорочение перкуторного звука у детей характерны для:
а) острого бронхита
б) хронического бронхита
в) острой пневмонии
г) бронхиальной астмы
327.
Этиотропная терапия пневмонии у детей — применение препаратов
а) противомикробных
б) десенсибилизирующих
в) отхаркивающих
г) бронхолитических
328. При остром бронхиолите у детей
развивается выраженная недостаточность
а) дыхательная,
сердечно-сосудистая
б) дыхательная, почечная
в) печеночная, почечная
г) печеночная, надпочечниковая
329. При
приступе бронхиальной астмы ребенок садится, опираясь руками на край сидения
для
а) облегчения кашля
б) облегчения дыхания
в) снижения АД
г) снижения температуры тела
330. При
При
приступе бронхиальной астмы у ребенка над легкими аускультативно определяется
а) крепитация
б) сухие, свистящие хрипы
в) шум трения плевры
г) шум трения перикарда
331. Для купирования приступа бронхиальной
астмы у детей используют b-адреномиметик
а) димедрол
б) интал
в) преднизолон
г) сальбутамол
332.
Пикфлоуметрия проводится ребенку для
а) мониторинга бронхиальной
астмы
б) лечения бронхиальной астмы
в) улучшения выделения мокроты
г) снижения температуры тела
333. Для
профилактики приступов бронхиальной астмы у детей применяют
а) пипольфен
б) интал
в) эуфиллин
г) эфедрин
334.
Поражение нервной системы при ревматизме у детей проявляется развитием:
а) анулярной эритемы
б) спазмофилии
в) эклампсии
г) хореи
335. При
При
ревматизме у детей преимущественно поражается система
а) сердечно-сосудистая
б) дыхательная
в) пищеварительная
г) костно-мышечная
336. Исход
ревматического эндокардита у детей
а) гипотрофия
б) рахит
в) порок сердца
г) спазмофилия
337. В
качестве диуретических препаратов используются:
а) курантил, трентал
б) вольтарен, бруфен
в) верошпирон, гипотиазид
г) резерпин, раунатин
338. При
лечении вегетососудистой дистонии у детей применяется растение, обладающее
седативным действием
а) алтей
б) багульник
в) валериана
г) толокнянка
339.
Повышенная кровоточивость при гемофилии связана с
а) недостатком некоторых
факторов свертывающей системы крови
б) уменьшением количества
тромбоцитов
в) изменением качества тромбоцитов
г) недостатком эритроцитов
340.
Кровотечение у детей с гемофилией — показание к немедленному введению
а) анальгетических средств
б) кровезаменителей
в) кальцийсодержащих препаратов
г) концентрированных
антигемофильных препаратов
341. Для
местного гемостаза при гемофилии применяют:
а) тромбин
б) холод
в) гидрокортизон
г) хлористый кальций
342.
Больным с гемофилией разрешается:
а) плавание
б) езда на велосипеде
в) футбол
г) гимнастика
343. Болезнь Верльгофа возникает в
результате:
а) снижения факторов свертывания
крови
б) уменьшения количества
эритроцитов
в) уменьшения количества
тромбоцитов
г) снижения гемоглобина
344. Цвет
кровоизлияний при тромбоцитопенической пурпуре у детей
а) розовый
б) красно-багровый
в) ярко-красный
г) от ярко-красного до
сине-зеленоватого
345.
Уровень гемоглобина в крови у детей при легкой форме железодефицитной анемии
снижается ниже (г/л)
а) 110
б) 80
в) 66
г) 50
346.
Уровень гемоглобина в крови у детей при тяжелой форме железодефицитной анемии
снижается ниже (г/л)
а) 110
б) 80
в) 70
г) 90
347. Препараты железа рекомендуется
запивать:
а) кислыми разбавленными соками
б) сладким чаем
в) молоком
г) киселем
348. При
лечении тяжелой формы анемии назначают железо в виде:
а) драже (ферроплекс)
б) инъекции (эктофер)
в) суспензий (урферрон)
г) сиропа (сироп алоэ с железом)
349.
Наиболее частый путь инфицирования у девочек при цистите
а) гематогенный
б) нисходящий
в) контактный
г) восходящий
350. У ребенка раннего возраста цистит
У ребенка раннего возраста цистит
возникает при несоблюдении
а) правил гигиены промежности
б) режима кормления
в) режима сна
г) температурного режима в
помещении
351.
Бактериальное воспаление почечной ткани и слизистой оболочки лоханок у детей,
сопровождающееся поражением канальцев — это
а) гломерулонефрит
б) цистит
в) пиелонефрит
г) нефроптоз
352.
Симптомы интоксикации, боли в животе и поясничной области, положительный
симптом Пастернацкого у детей старшего возраста наблюдаются при
а) дисметаболической нефропатии
б) цистите
в) пиелонефрите
г) вульвовагините
353.
Высокая лейкоцитурия и бактериурия у детей характерны для
а) пиелонефрита
б) гломерулонефрита
в) опухоли почек
г) дисметаболической нефропатии
354. Для
Для
выявления лейкоцитурии проводят:
а) пробу Зимницкого
б) пробу Нечипоренко
в) анализ мочи на кетоновые тела
г) общий анализ крови
355.
Этиотропной терапией при остром пиелонефрите у детей является
а) антибактериальная терапия
б) фитотерапия
в) физиотерапия
г) витаминотерапия
356.
Лечебное питание ребенка с пиелонефритом строится по принципу
а) молочно-растительной диеты с
умеренным ограничением белка и соли
б) усиленного белкового питания
в) бессолевой диеты
г) молочно-растительной диеты с
ограничением сахара
357. В
основе развития гломерулонефрита у детей лежат
а) иммунные реакции
б) гиподинамия
в) гормональный фон
г) стрессовый фактор
358.
Повышение АД у детей, особенно диастолического, характерно для:
а) острого периода
гломерулонефрита
б) острого периода пиелонефрита
в) латентного течения
гломерулонефрита
г) латентного течения пиелонефрита
359. Для
Для
протеинурического варианта мочевого синдрома у детей характерно преобладание в
моче
а) лейкоцитов
б) эритроцитов
в) сахара
г) белка
360.Ребенку
с любой формой гломерулонефрита в первую очередь назначают
а) антибактериальную терапию
б) строгий постельный режим и диету
в) гипотензивные и диуретические
препараты
г) препараты цитостатического
действия
361. Для
улучшения почечного кровотока при гломерулонефрите назначают:
а) кортикостероиды
б) вольтарен, бруфен
в) курантил, трентал
г) иммунодепрессанты
362. Дети, больные гломерулонефритом, должны
наблюдаться окулистом, так как длительное повышение АД вызывает
а) астигматизм
б) миопию
в) изменения на глазном дне
г) дальнозоркость
363. При
При
лечении ребенка, больного гломерулонефритом, синдром отмены развивается при
внезапной отмене
а) метилурацила
б) фуросемида
в) делагила
г) преднизолона
364. Данные о функциональном состоянии почки
у детей получают при
а) обзорной урографии
б) пробе Зимницкого
в) общем анализе мочи
г) пробе Нечипоренко
365. Для определения уровня глюкозы в крови
ребенка следует направить в лабораторию
а) через 10мин после еды
б) через 20мин после еды
в) через 30мин после еды
г) натощак
366.
Клинические симптомы сахарного диабета у детей
а) полифагия, полидипсия,
полиурия
б) лихорадка, кашель с мокротой
в) боль в пояснице, отеки
г) тахикардия, тремор, зкзофтальм
367. При сахарном
диабете у детей в общем анализе мочи наблюдаются
а) высокая относительная плотность,
гематурия
б) высокая относительная
плотность, глюкозурия
в) низкая относительная плотность,
бактериурия
г) низкая относительная плотность,
лейкоцитурия
368. При лечении
При лечении
сахарного диабета у детей сахар заменяют
а) сорбитом
б) медом
в) вареньем
г) конфетами
369. Ведущим в лечении гипотиреоза являются:
а) пирацетам, церебролизин
б) витамины группы В
в) тироксин, тиреотом
г) антиструмин
370.
Основной препарат, применяемый для лечения диффузного токсического зоба у детей
а) тиреотом
б) антиструмин
в) L — тироксин
г) мерказолил
371.
Выраженной нейротропностью обладают
а) аденовирусы
б) вирусы гриппа
в) риновирусы
г) респираторно-синцитиальные
вирусы
372. Ведущим признаком крупа у детей
является
а) лихорадка
б) гиперемия лица
в) инспираторная одышка
г) экспираторная одышка
373.
Осложнение ларинготрахеита
а) пилоростеноз
б) стеноз гортани
в) головная боль
г) воспаление плевры
374. Обструктивный синдром при ОРВИ у детей
характеризуется
а) упорным кашлем, одышкой
б) слабостью, повышением
температуры
в) недомоганием, отеками
г) желтухой, болью в животе
375. При
ОРВИ детям назначают противовирусный препарат
а) амоксициллин
б) глауцин
в) лейкоцитарный интерферон
г) сульфален
376. При
лечении менингококковой инфекции у детей с этиотропной целью применяют
а) антибиотики
б) диуретики
в) сердечные гликозиды
г) плазмозамещающие растворы
377. Для
краснухи характерно:
а) поэтапное появление сыпи
б) увеличение затылочных и
заднешейных лимфатических узлов
в) выраженные катаральные явления
верхних дыхательных путей
г) везикулярная сыпь
378. Антитоксическая сыворотка применяется у детей при лечении
Антитоксическая сыворотка применяется у детей при лечении
а) гриппа
б) ветряной оспы
в) кори
г) дифтерии
379.Увеличение околоушных слюнных желез у детей характерно для
а) кори
б) краснухи
в) ветряной оспы
г) эпидемического паротита
380.
Больной коклюшем заразен в течение:
а) 7 дней
б) 14 дней
в) 25-30 дней
г) 35-40 дней от начала заболевания
381. Пятна
Бельского-Филатова-Коплика появляются у детей на
а) лице
б) туловище
в) конечностях
г) слизистой оболочке щек
382.
Первые элементы сыпи при кори у детей появляются на
а) лице
б)
туловище
в) руках г)
ногах
383.
Ангина у детей является постоянным симптомом
а) гриппа
б) ветряной оспы
в) скарлатины
г) риновирусной инфекции
384.
Частое развитие токсикозов у детей при различных заболеваниях обусловлено
а) слабой детоксицирующей
функцией печени
б) слабой секреторной функцией
желудка
в) высокой детоксицирующей функцией
печени
г) высокой секреторной функцией
желудка
385.
Частые рецидивирующие гнойные и грибковые заболевания, инфекции верхних
дыхательных путей у детей – это проявления
а) гиповитаминоза
б) избыточного питания
в) иммунодефицита
г) перегревания
386.
Прививка против туберкулеза проводится в родильном доме
а)
недоношенным
б)
ослабленным
в) всем
здоровым
г) только
контактным по туберкулезу
387. Стул характерный для дизентерии:
а) в виде «болотной тины»
б) оранжевый брызжущий, водянистый
в) скудный с примесью крови, гноя и слизи
г) кашецообразный с непереваренными комочками
388. Оральная регидратация при кишечных инфекциях проводится:
а) регидрон, оралит
б) 2% раствор бикарбоната натрия
в) минеральная вода с газом
г) яблочный сок
389. Стул характерный для сальмонеллеза
а) в виде «болотной тины»
б) в виде ректального плевка
в) в виде рисового отвара
г) кашецообразный с непереваренными комочками
390. Что следует ограничить в питании детей, страдающих нервно –
артритическим диатезом?
А). молочные продукты
Б). картофельное пюре
В). сладости
Г). мясные продукты
391. Судороги при спазмофилии купируются:
А)Седуксен
Б).Глюкоза
В). хлорид кальция
Г). Аммония хлорид
392. Лабораторным показателем эффективнолсти лечения ЖДА служит:
А). ЦП
Б). уровень гемоглобина
В). размер эритроцитов
Г). количество эритроцитов
393. Для лимфатического диатеза характерно:
А). снижение МТ
Б). повышение МТ
В). сыпь на коже
Г). рвота
394. С прорфилактической целью вит. Д не назначается при кормлении
ребенка:
А). грудью
Б). адаптированной молочной смесью
В). кашей
395. При рахите у ребенка отмечается:
А). краниотабес
Б). раннее закрытие малого родничка
В). кефалогематома
396. Наиболее вероятный возраст появления признаков рахита:
А). 1 мес.
Б). 3 мес.
В). 6 мес.
Г), 12 мес.
397. Различают следующие
формы рахита:
А). латентная
Б), судорожная
В). Смешанная
Г), Рецидивирующая
398. Спазмофилия проявляется
преимущественно:
А), в первом полугодии
жизни
Б), во втором полугодии жизни
В), на втором году жизни
Г). у детей старше 3 лет
399. Большой родничок у
здоровых детей закрывается к:
А). 2 – 3 мес.
Б). к 5 – 6 мес.
В). к 12 мес.
Г). к 2 годам
содержание ..
2
3
4
5 ..
Аципол — инструкция по применению
Торговое наименование: Аципол®
Международное непатентованное или группировочное наименование: лактобактерии ацидофильные + грибки кефирные.
Лекарственная форма: капсулы
Состав на одну капсулу.
Действующие вещества: Лактобактерии ацидофильные живые* – не менее 107 КОЕ
Биомасса кефирного грибка инактивированная – 0,4 мг**
Вспомогательные вещества:
Капсулы твердые желатиновые № 3 — 48,0 мг
Корпус и крышечка:
Титана диоксид (Е 171) – 1,0 %
Оксид железа красный (Е 172) – 0,3 %
Оксид железа желтый (Е 172) – 0,1 %
Желатин – до 100 %
* — действующее вещество представляет собой лиофилизат, содержащий лактобактерии Lactobacillus acidophilus;
** — определение проводят по содержанию полисахарида кефирных грибков; «биомасса кефирного грибка инактивированная» представляет собой лиофилизат с расчетной массой 2,0 мг»;
Описание: капсулы твердые желатиновые № 3 оранжевого цвета. Содержимое капсулы – порошок от светло-кремового до светло-коричневого цвета с кисломолочным запахом.
Фармакотерапевтическая группа: эубиотик
Код АТХ: A07FA51
Фармакологические свойства
Фармакодинамика
Терапевтический эффект Аципола® определяют содержащиеся в нем живые ацидофильные лактобациллы и полисахарид кефирных грибков. По механизму действия Аципол® является многофакторным лечебным средством, обладает антагонистической активностью в отношении патогенных и условно-патогенных микроорганизмов, оказывает корригирующее действие на микрофлору кишечника, повышает иммунологическую реактивность организма.
Фармакокинетика
Компоненты препарата не всасываются из желудочно-кишечного тракта (ЖКТ) и не оказывают системного действия.
Показания к применению
Аципол применяют у взрослых и детей с 3 месяцев в комплексном лечении дисбактериоза кишечника на фоне:
- острых кишечных инфекций;
- хронических заболеваний желудочно-кишечного тракта, таких как колит, энтероколит инфекционного и неинфекционного происхождения;
- длительной антибактериальной терапии.
Профилактика дисбактериоза:
- повышение общей резистентности организма.
Противопоказания
Повышенная чувствительность к компонентам препарата, детский возраст до 3 месяцев.
Применение при беременности и в период грудного вскармливания
Компоненты препарата действуют в просвете ЖКТ и не всасываются в системный кровоток, поэтому применение препарата в период беременности и грудного вскармливания не противопоказано и возможно по согласованию с лечащим врачом.
Способ применения и дозы
Внутрь.
Взрослым и детям старше 3-х лет – капсулы следует принимать, не разжевывая, запивать кипяченой водой.
Детям в возрасте от 3-х месяцев до 3-х лет Аципол® следует принимать вместе с пищей, предварительно вскрыв капсулу и растворив ее содержимое в молоке или кипяченой воде.
Для лечения дисбактериоза Аципол® назначают:
- Детям в возрасте от 3-х месяцев до 3-х лет — по 1 капсуле 2-3 раза в сутки, вместе с пищей.
- Детям старше 3-х лет и взрослым — по 1 капсуле 3-4 раза в сутки, за 30 минут до приема пиши.
Продолжительность курса терапии дисбактериоза при острых кишечных инфекциях — 5-8 дней. Более длительные курсы возможны по назначению врача при хроническом течении заболеваний, сопровождающихся дисбактериозом.
Для профилактики дисбактериоза Аципол® назначают: по 1 капсуле 1 раз в сутки в течение 10-15 дней.
Повторные курсы терапии и профилактики проводят не ранее 1 месяца после окончания предыдущего курса.
Если после лечения улучшения не наступает или симптомы усугубляются, или появляются новые симптомы, необходимо проконсультироваться с врачом. Применяйте препарат только согласно тем показаниям, тому способу применения и тех дозах, которые указаны в инструкции.
Побочное действие
Возможны аллергические реакции.
Если у Вас отмечаются побочные эффекты, указанные в инструкции или они усугубляются, или вы заметили любые другие побочные эффекты, не указанные в инструкции, сообщите об этом врачу.
Передозировка
Случаев передозировки не зарегистрировано.
Взаимодействие с другими лекарственными препаратами
Возможно одновременное применение с антибактериальными, противовирусными и иммуномодулирующими препаратами.
Особые указания
Необходимо соблюдать рекомендованную в инструкции схему и длительность приема препарата. Изменение суточной дозы и продолжительности лечения возможно по назначению врача, в зависимости от возраста пациента, тяжести и длительности заболевания.
При сохранении симптомов заболевания или ухудшении состояния на фоне применения препарата в течение 3-х дней следует сообщить об этом лечащему врачу.
Влияние на способность управлять транспортными средствами, механизмами
Препарат не оказывает влияния на способность к выполнению потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций (в том числе, управление транспортными средствами, работа с движущимися механизмами).
Форма выпуска
Капсулы.
По 20 или 30 капсул во флакон полипропиленовый, укупоренный крышкой из полиэтилена высокого давления с силикагелем и контролем первого вскрытия или в банку полипропиленовую выдувную с натягиваемой крышкой из полиэтилена высокого давления с силикагелем и картонным вкладышем с контролем первого вскрытия.
На флакон или банку наклеивают этикетку самоклеящуюся.
1 флакон или банку вместе с инструкцией по применению помещают в пачку из картона.
Условия хранения
При температуре от 2 до 8 °С.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности.
Условия отпуска
Отпускают без рецепта.
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей
АО «Отисифарм», Россия,
123112, г. Москва, ул. Тестовская,
д. 10, эт. 12, пом. II, ком. 29
Тел.: +7 (800) 775-98-19
Факс: +7 (495) 221-18-02
www.otcpharm.ru
Производитель
ЗАО «ЛЕККО», Россия
601125, Владимирская обл., Петушинский район, пос. Вольгинский ул. Заводская, стр. 277,
601125, Владимирская обл., Петушинский район, пос. Вольгинский ул. Заводская, стр. 279,
тел./факс (49 243) 71 5 52.
Немного о роли микрофлоры кишечника в жизни человека
Кудин А.П., к.м.н., доцент, зав. инфекционным отделением № 5 УЗ «Городская детская инфекционная больница г. Минска»
Организм человека населяет большое количество микроорганизмов (по приблизительным подсчетам — около 1000 видов), основную массу которых составляют бактерии. В значительно меньшем количестве представлены другие микроорганизмы (вирусы, археи, простейшие). В норме все они находятся в состоянии равновесия между собой и с организмом человека.
Микроорганизмы попадают к человеку из внешней среды и заселяют (с рождения и пожизненно) те области, которые непосредственно контактируют с внешней средой: кожа, дыхательные пути, мочевыводящие пути, желудочно-кишечный тракт (ЖКТ). Внутренняя среда макроорганизма, а также альвеолы, внутреннее и среднее ухо, матка, почки и мочеточники в норме стерильны. Очевидно, самые благоприятные условия для пребывания микробов в организме человека создаются в ЖКТ.
Заселение кишечника ребенка начинается примерно с середины периода внутриутробного развития (единичные микробы), но основное заселение происходит с момента рождения. При прохождении через родовые пути начинается интенсивная колонизация кожных покровов и слизистых оболочек, соприкасающихся с внешней средой. Эпидермальные стафилококки заселяют кожу α-стрептококки – носоглотку. Массивная колонизация кишечника здорового новорожденного происходит гетерогенной флорой (аэробной и анаэробной) в первые сутки. Однако с 3-5 дня основной (резидентной) флорой становятся бифидобактерии, которые вытесняют другие микроорганизмы из местного биотопа. Это связано с тем, что лактоза грудного молока активно метаболизируется в первую очередь бифидо- и лактобактериями. Кроме того, содержащийся в женском (но не коровьем) молоке N-ацетилглюкозамин стимулирует рост бифидобактерий.
При родоразрешении путем кесарева сечения состав микробов, колонизирующих организм новорожденного, отличается в сторону дефицита лактобацилл, энтеробактерий и дифтероидов.
Некоторые факторы (течение беременности, способ родоразрешения, особенности выхаживания ребенка после рождения и др.) могут нарушать этапность заселения и видовой состав микрофлоры кишечника.
Состав микробного пейзажа во многом определяется характером питания. У грудных детей, находящихся на естественном вскамливании, доминируют бифидо- и лактобактерии. У грудных детей на искусственном вскармливании микрофлора кишечника более гетерогенна, и преобладание молочно-кислых микробов над другими выражено в значительно меньшей степени. У более старших детей по мере уменьшения в питании доли молочных продуктов и включения мяса и мясных продуктов увеличивается удельный вес протеолитических микробов.
Нормальная микрофлора человека представлена облигатными микроорганизмами (которые присутствуют, практически, постоянно) и транзиторными (факультативными), на долю которых приходится не более 1-2%.
В зависимости от особенностей метаболизма все микробы кишечника можно условно разделить на протеолитические (кишечная палочка и другие грамм-отрицательные энтеробактерии, бакероиды, клостридии) и сахаролитические (бифидо- и лактобактерии, энтерококки).
По отношению к кислороду бактерии делят на облигатные аэробы, растущие только в присутствии кислорода, облигатные анаэробы рост которых подавляется кислородом (бактероиды, бифидобактерии, клостридии) и факультативные анаэробы, способные к росту как в присутствии кислорода, так и без него (лактобактерии, кишечная палочка и др. грамм-отрицательные энтеробактерии, стафилококки, стрептококки, энтерококки). На долю облигатных анаэробов (бактероиды и бифидобактерии) приходится 95-99% всех микробов кишечника (причем, бактероидов больше).
По локализации в кишечнике выделяют пристеночную и полостную микрофлору. В тонкой кишке содержание пристеночной флоры на несколько порядков превышает численность полостной. В толстой кишке это соотношение меняется на противоположное.
Общее колическтво микробных клеток в организме человека по расчетам составляет около 1014, что превышает число собственных клеток человека.
Распределение нормальной микрофлоры вдоль желудочно-кишечного тракта (ЖКТ) неоднородно по качественному и количественному составу.
В ротовой полости анаэробов примерно на порядок больше, чем аэробов, т.к. первые, находясь в труднодоступных местах (десневые карманы, щели между зубами и т.д.), лучше защищены от действия лизоцима и других протективных факторов слюны. Среди бактерий здесь преобладают стрептококки (до 60% всех микробов ротовой полости). Из других частых представителей микрофлоры следует упомянуть фузобактерии, вейонеллы, бактероиды, спирохеты, актиномицеты. Здесь же обитают микоплазмы (M.salivarium), грибы рода Candida, простейшие (Entamoeba buccalis, Entamoeba dentalis, Trichomonas buccalis). Данная микробиота представляет собой первый барьер, препятствующий проникновению болезнетворных микроорганизмов, попадающих в полость рта из внешней среды, дальше в ЖКТ.
В желудке здорового человека микробов, практически, нет из-за действия желудочного сока, имеющего низкое значение рН. В небольшом количестве здесь могут существовать некоторые лактобактерии и грамотрицательные энтеробактерии. Содержание Helicobacter pylori обычно не превышает 103 бактерий в 1 мл содержимого желудка.
Верхние отделы тонкой кишки относительно мало заселены микроорганизмами. В физиологических условиях в тощей кишке содержится 104-5/мл микробов (в основном, лакто- и бифидобактерии), и по мере приближения к илеоцекальному клапану количество микробов в подвздошной кишке увеличивается до 107/мл (в основном за счет бактероидов, энтерококков, кишечной палочки).
Толстая кишка отличается самой высокой плотностью заселения микроорганизмами, количество которых достигает 109-1012/мл, из которых анаэробы составляют 95-99%. К ним относятся грамположительные палочки (бифидо-, лакто- и эубактерии), грамотрицательные палочки (бактероиды), грамположительные спорообразующие палочки (клостридии). Из других частых представителей нормальной микрофлоры следует назвать энтерококки, грамотрицательные факультативно-анаэробные палочки (кишечная палочка, клебсиелла, энтеробактер и др.). в меньших количествах обнаруживаются стафилококки, дрожжевые грибы, простейшие и вирусы.
Сохранению относительного постоянства нормальной микрофлоры способствуют различные факторы, к которым относятся нормальная перистальтика кишечника (прежде всего, тонкой кишки), герметичность эпителиального слоя, компоненты пищеварительных соков (соляная кислота, желчные кислоты, протеолитические ферменты и т.д.), сохранная функция илеоцекального клапана, факторы местного иммунитета (секреторные IgA, лизоцим, лимфоидные образования кишечника, состояние перманентного физиологического воспаления в стенке кишки).
Значение кишечной микробиоты для организма человека трудно переоценить. К основным функциям нормальной микрофлоры относятся:
- Защитная функция, суть которой заключается в обеспечении колонизационной резистентности, т.е. предотвращении колонизации ЖКТ патогенными микроорганизмами. Это осуществляется за счет конкуренции за питательные вещества, за места адгезии (рецепторы), за счет выработки бактериоцинов, короткоцепочечных жирных кислот, а также за счет стимуляции местных защитных факторов (в виде состояния легкого воспаления).
- Пищеварительная функция. Микрофлора обеспечивает конечный гидролиз белков, омыление жиров, сбраживание высокомолекулрных углеводов, которые не метаболизировались в тонкой кишке. Кроме того, некоторые вещества, поступающие с пищей, могут расщепляться только кишечной микрофлорой (например, целлюлоза). Под действием нормальной микрофлоры в подвздошной кишке происходит деконъюгация 90% желчный кислот с последующим обратным всасыванием и повторным участием в пищеварении. Оставшиеся в кале желчные кислоты обеспечивают нормальную гидратацию каловых масс.
- Двигательная функция. На перистальтику кишечника микрофлора может влиять по-разному. С одной стороны, за счет стимуляции синтеза окиси азота и активации L-клеток кишечника может замедлять моторику в тонкой кишке и проксимальных отделах толстой кишки. С другой стороны, короткоцепочечные жирные кислоты, синтезирующиеся микрофлорой, в дистальных отделах толстой кишки стимулируют усиление моторики.
- Способствует всасыванию воды (с помощью некоторых продуктов микробного метаболизма).
- Нормальная микрофлора способна обезвреживать многие токсические вещества как путем их химической обработки, так и за счет сорбции на своей поверхности и выведения с каловыми массами. По антитоксической функции некоторые авторы приравнивают кишечных микробов к печени.
- Участвуют в синтезе некоторых необходимых веществ: витаминов группы В (В1,В2,В6,В12), фолиевой кислоты, витамина К и др. и хотя большинство из этих синтезирующихся веществ не всасываются, они могут оказаться важными и полезными для собственно слизистой кишечника. Например, было показано, что недостаточное поступление к эпителию слизистой толстой кишки витаминов В6, В12 и фолиевой кислоты связано с повышенным риском развития рака толстой кишки.
Стоит отметить, что геном человека содержит около 23 тыс генов, а количество генов микробов и вирусов, содержащихся только в ЖКТ, составляет более 3 млн, и, возможно, часть из них участвует в синтезе необходимых человеку веществ. В эксперименте показано, например, что у стерильных («гнотобиологических») животных отмечается недоразвитие лимфоидной и гемопоэтической ткани, отмечаются нарушения со стороны головного мозга, истончается стенка кишечника, ослабляется реактивность фагоцитов, развивается гипогаммаглобулинемия.
- Иммуномодулирующая функция связана с воздействием на факторы врожденного и адаптивного иммунитета как на местном, так и на системном уровне. И это влияние, возможно, является главным во взаимодействии микрофлоры и макроорганизма. Влияние нормальной микрофлоры на систему иммунитета складывается из нескольких моментов. Во-первых, слизистая кишечника, особенно толстой кишки (вследствие наиболее массивного заселения бактериями), обильно инфильтрирована макрофагами, лимфоцитами, плазматическими клетками, т.е., фактически, находится в состоянии постоянного хронического воспаления. Это перманентное воспаление обеспечивает пребывание иммунокомпетентных клеток в состоянии субактивации и, как следствие, — более быстрый и эффективный ответ на попадание агрессивной (патогенной) флоры. Во-вторых, под действием нормальной микрофлоры синтезируются «естественные» («нормальные») антитела, реагирующие на наиболее распространенные в природе антигенные детерминанты (паттерны). Это обеспечивает протективную функцию в отношении многих патогенов. И наконец, в-третьих, не вдаваясь в подробности, следует напомнить, что в кишечнике постоянно находится около 60-70% всех лимфоцитов человека, которые рециркулируют по всему организму. Контакт с микробами кишечника может приводить к активации различных клонов лимфоцитов. Это влияние сохраняется при попадании этих лимфоцитов в кровеносное русло. И в зависимости от того, какие свойства приобрели иммунные клетки, будет определяться их влияние на весь организм. Кроме того, системное действие могут оказывать и вырабатывающиеся в кишечнике под действием микрофлоры различные биологически активные вещества, прежде всего, цитокины. Итогом такого влияния может оказаться как иммуностимуляция, так и иммуносупрессия. Эти процессы могут лежать в основе развития различных заболеваний, в т.ч. и аутоиммунных.
Различные виды и штаммы представителей нормальной микрофлоры слизистых могут оказывать разнонаправленное влияние на активность иммунной системы. Поэтому существует потенциальная возможность целенаправленно влиять на функционирование иммунной системы человека посредством воздействия с помощью микроорганизмов на факторы врожденного и адаптивного иммунитета. Здесь будет уместно процитировать статью Андреевой И.В. и Стецюк О.У., в которой суммированы данные литературы о влиянии различных пробиотиков на организм человека (табл.).
Влияние пробиотиков на макроорганизм (И.В. Андреева и О.У. Стецюк, 2010),
|
Штамм пробиотика
|
Положительное влияние на макроорганизм
|
|
L.rhamnosus GG
|
Усиление иммунного ответа, профилактика и лечение инфекций дыхательных путей у детей, профилактика и лечение инфекционной диареи у детей, профилактика антибиотик-ассоциированной диареи, профилактика возникновения атопического дерматита у детей, улучшение эрадикации H.pylori
|
|
L.reuteri SD2112
|
Усиление иммунного ответа, профилактика инфекций дыхательных путей у взрослых, лечение ротавирусной диареи
|
|
L.casei DN-114001
|
Усиление иммунного ответа, лечение диареи
|
|
L.acidophilus NCFM
|
Снижение непереносимости лактозы, уменьшение выраженности синдрома избыточного бактериального роста, лечение и профилактика урогенитальных инфекций у женщин, лечение инфекций дыхательных путей у детей, лечение диареи у детей, улучшение эрадикации H.pylori
|
|
L.plantarum 299V
|
Нейтрализация проявлений синдрома раздраженного кишечника, применяется в восстановительном периоде после хирургических вмешательств
|
|
L.casei Shirota YIT9029
|
Профилактика рецидивов поверхностного рака мочевого пузыря, усиление иммунного ответа
|
|
L.salivarius UCC118
|
Нейтрализация проявлений воспалительных заболеваний кишечника
|
|
B.lactis BB-12
|
Профилактика инфекций дыхательных путей у детей, профилактика и лечение инфекционной диареи и желудочно-кишечных расстройств у детей, профилактика антибиотик-ассоциированной диареи
|
|
B.infantis 35624
|
Нейтрализация проявлений синдрома раздраженного кишечника
|
|
B.longum BB536
|
Лечение атопической экземы, улучшение эрадикации H.pylori, лечение язвенного колита
|
|
B.lactis HN019 (DR10)
|
Усиление иммунного ответа, особенного у пожилых
|
|
B.animalis DN173-010
|
Нормализация времени прохождения пищи по кишечнику
|
|
L.johnsonii La1 (Lj1)
|
Улучшение эрадикации H.pylori, усиление иммунного ответа
|
|
S.boulardii
|
Профилактика антибиотик-ассоциированной диареи
|
|
S.thermophilus (большинство штаммов)
|
Профилактика проявлений лактазной недостаточности
|
Взаимодействие макроорганизма с кишечной микрофлорой может осуществляться несколькими путями: в виде комменсализма, паразитизма, симбиоза.
По современным представлениям, провести четкую границу между комменсалами и условно-патогенной микрофлорой невозможно. В определенных случаях заболевание могут вызвать различные микробы, входящие в состав нормальной микрофлоры.
В настоящее время в печати (в том числе, и медицинской) нередко говорится о дисбактериозе, как о несуществующей проблеме. Аргументируется это разными доводами.
- Под «дисбактериозом» обычно обозначают изменения соотношений и состава нормальной микрофлоры организма, а также места их обитания. Однако до настоящего времени во всем мире нет понятия нормы кишечного биоценоза. И нет «золотого стандарта» диагностики дисбактериоза.
- Наиболее часто для диагностики дисбактериоза используют посев кала. Однако результаты этого анализа непоказательны. Во-первых, анализ показывает состояние микробов, обитающих только в просвете толстой кишки, причем в ее дистальном (конечном) отделе. Состав микробиоты тонкой кишки остается неизвестным. Во-вторых, при таком исследовании выделяют 8-12 видов микробов, в то время как их количество в кишечнике более 1000 (причем не учитывается содержание даже бактериодов, которые составляют более 50% массы всех кишечных микробов). В-третьих, для достоверной диагностики требуется собрать содержимое кишечника в стерильных условиях, транспортировать материал при определенной температуре и доставить его в лабораторию в течение 2 часов. Иначе результаты будут искажены.
Существует другая методика: посев аспирата тонкокишечного содержимого или биоптата стенки тонкой кишки. В этом случае мы получаем данные о состоянии флоры в тонком кишечнике. Но такая диагностика применяется крайне редко.
Есть также косвенные методы, которые позволяют судить о состоянии микрофлоры кишечника. К ним относятся химические методы: газожидкостная хроматография и масс-спектрометрия.
Для анализа используется содержимое кишечника, в котором определяется концентрация веществ — продуктов жизнедеятельности микрофлоры, а затем делается вывод о ее качественном и количественном составе.
Используются также дыхательные тесты, когда продукты жизнедеятельности бактерий определяют в выдыхаемом воздухе. Однако эти методы можно использовать только в качестве предварительной диагностики, так как велика доля ложных результатов.
- Даже современные молекулярные методики не дают исчерпывающего результата: до 75% разновидностей микробов остаются не классифицируемыми. Содержание микробов в кале не отражает реальной ситуации в просвете тонкой и толстой кишок, а тем более в пристеночных биотопах, где состав микробов может заметно отличаться от состава просветной флоры.
- И, кроме того, диагноз «дисбактериоз кишечника» не имеет четкой клинической составляющей — иными словами, такой болезни просто не существует.
Все перечисленное верно. Однако говорить об отсутствии проблемы нарушенного, аномального, избыточного и т.д. роста кишечных микробов, очевидно, неверно. Небольшие возможности современной диагностики этого состояния не исключают существование самой проблемы. В зарубежной литературе вместо термина «дисбактериоз кишечника» для обозначения нарушений качественного и количественного состава кишечной микрофлоры применяют термин «синдром избыточного роста бактерий» в тонкой кишке (bacterial overgrowth syndrome). Под этим синдромом понимают клинически и/или лабораторно подтвержденный синдром мальдигестии/мальабсорбции, связанный с качественными или количественными изменениями микробиоты тонкой кишки.
В этой статье, говоря о проблеме влияния измененноймикробиоты на организм человека, мы будем пользоваться привычным нам термином «дисбактериоз».
При дисбактериозе происходит перераспределение флоры на протяжении кишечника: малонаселенная в норме тонкая кишка оказывается заполненной огромным количеством бактерий, а в толстой кишке меняется их видовой состав. Вместо полезных и привычных видов появляются патогенные (чаще это условно-патогенные микробы, которые при определенных условиях начинают проявлять свойства патогенных).
Причин нарушения видового состава и количества микроорганизмов в кишечнике очень много, и обычно действуют они в комплексе.
«Полезные» бактерии гибнут:
- если им нечего есть. Такое случается, когда рацион несбалансирован, беден растительной клетчаткой и кисломолочными продуктами.
- если им некомфортно. При различных заболеваниях (колит, панкреатит, холецистит, гастрит, гепатит и др.) в кишечнике меняется pH. В изменившихся условиях нарушается обмен веществ и целостность клеток кишечных микробов.
- если их место занимают агрессивные «собратья» — патогенные бактерии, микроорганизмы, гельминты, грибы.
Не секрет, что облигатнопатогенные микробы (сальмонеллы, шигеллы, иерсинии, кампилобактерии и др.) вызывают соответствующие заболевания. При дисбактериозе же часто обнаруживаются, так называемые, условно-патогенные микробы, но в большом количестве. И здесь будет уместно напомнить о таком феномене, как «чувство кворума» (quorum sensing) – способность ощущать плотность собствнной популяции микробов. Оказалось, что микроорганизмы обладают способностью к самостимуляции собственного размножения. При благоприятных условиях они начинают продуцировать специальные автоиндукторы, стимулирующие соседние и недалеко расположенные микробные клетки данного вида. При превышении определенной пороговой концентрации биологические свойства этих микробов изменяются: у них экспрессируются заторможенные до этого гены, в которых закодированы биологически активные вещества, повышающие патогенность микробов (различные токсины, ферменты и т.д.). Таким образом, вроде бы безобидные микроорганизмы приобретают свойства патогенных. И в этом случае они уже способны оказывать повреждающее действие на организм человека и вызывать заболевание. (Если немного отвлечься от микробов, то можно сказать, что этот феномен, наверное, имеет универсальное действие. Например, люди в офисе, на стройке или производстве обычно ведут себя адекватно, но собираясь большой группой, например, на стадионе могут становиться агрессивными). Следует отметить, что предпринимаются попытки использовать «чувство кворума» в лечебных целях для увеличения метаболической и антагонистической активности представителей нормальной микрофлоры с целью защиты макроорганизма от действия патогенных агентов.
Поэтому лечение дисбактериоза может потребовать применения антимикробных препаратов, включая антибиотики. Однако следует помнить, что принципиально важным является то, что нужно лечить не плохой анализ на дисбактериоз, а клинически выраженное патологическое состояние, в основе которого лежит дисбактериоз. В немногочисленных данных содержимого тонкой кишки было показано, что до 20% здоровых людей могут иметь отклонения в микробном пейзаже (при патологии этот показатель составляет до 64%).
И, конечно же, говоря о лечении дисбактериоза, нельзя не сказать о применении биопрепаратов. Все они делятся на:
- Пребиотики (лаклулоза, инулин, фруктозо- и галактозоолигосахариды и др.) — это препараты, которые подготавливают кишечник к заселению нормальной микрофлорой, создают для нее комфортные условия. К пребиотикам относятся также продукты питания, такие как: кукурузные, овсяные каши, ржаной хлеб, бобовые, соки с мякотью, отруби, молочные продукты и др.
- Пробиотики (эубиотики) — это препараты, содержащие нормальную микрофлору кишечника и способные благоприятно воздействовать на кишечную микробиоту и общее состояние огранизма. Свойствами пробиотиков также обладают кисломолочные продукты, обогащенные лакто- и бифидобактериями.
- Синбиотики— комбинированные препараты про- и пребиотиков.
Практика показывает, что хорошо работающие «в пробирке» препараты не всегда оказывают должный эффект в организме. Введенная с пробиотиками флора часто пропадает после окончания курса терапии. Дело в том, что дисбактериоз — это скорее следствие, нежели причина болезней. В больном организме «полезные» бактерии просто не приживаются, сколько их не «сажай». Дисбактериоз развивается под влиянием множества факторов. И вылечить его только лишь приемом лекарств невозможно.
Отдельно необходимо сказать о применении биопреаратов после приема антибиотиков. Многие считают, что это является обязательным. На самом деле, при отсутствии каких-либо клинических проявлений антибиотик-ассоциированной диареи в применении биопрепаратов нет необходимости. (Так же, как и при наличии изменений в анализе на дисбактериоз при отсутствии соответствующей симптоматики).
Прежде чем заниматься микрофлорой, необходимо лечение хронических заболеваний, особенно желудочно-кишечного тракта. Важно избавиться от очагов инфекции во рту, ЛОР-органах. Огромное значение имеет сбалансированный рацион питания. То есть, нужно создать самые благоприятные условия для колонизации кишечника, и только после этого рассчитывать на благоприятный эффект от лечения.
И наконец, следует сказать о еще одном заблуждении, которое довольно широко распространено. Многие считают что живые пробиотики колонизируют кишечник и, тем самым, излечивают дисбактериоз. Однако оказалось, что профилактические и лечебные эффекты пробиотиков могут быть воспроизведены с убитыми бактериями и продуктами их разрушения. Это служит подтверждением мысли о том, что основной механизм действия биопрепаратов связан с их влиянием на систему местной защиты организма ребенка (местного врожденного и адаптивного иммунитета кишечника).
Использование пробиотиков в медицине теоретически имеет большие перспективы. К настоящему времени доказана их эффективность при различных заболеваниях ЖКТ как инфекционных (ротавирусная инфекция, диарея путешественников, хеликобактерных хронических гастритах), так и – неинфекционных (некротизирующий энтероколит, неспецифический язвенный колит). Кроме того, показана терапевтическая эффективность пробиотиков при атопических заболеваниях, снижение частоты и тяжести эпизодов ОРИ у детей на фоне применения пробиотиков, и даже – усиление иммунного ответа на вакцинацию. Существуют работы, в которых показана возможная эффективность определенных пробиотиков в лечении воспалительных заболеваний кишечника (болезни Крона, неспецифического язвенного колита).
Если пофантазировать, то при определенном уровне знаний можно с помощью пробиотиков вызывать вполне определенные, необходимые данному конкретному пациенту иммунные реакции, способные помочь человеку справиться с различными по патогенезу заболеваниями (инфекционными, иммунными, неоплазменными). Но, как легко понять, это дело не близкого будущего.
И, в заключение, несколько ключевых моментов этой статьи:
- При отсутствии клинических признаков поражения ЖКТ (неустойчивый стул, боли в животе, беспокойство, плохая прибавка массы тела и т.д.) обнаруженные в анализе кала признаки дисбактериоза не требуют лечения (!),
- Проведение АБ-терапии не означает, что детям обязательно необходимо назначать биопрепараты. В подавляющем большинстве случаев достаточно правильного полноценного питания, с включением продуктов, содержащих растительную клетчатку, и, если нет противопоказаний в виде лактазной недостаточности или непереносимости белка коровьего молока, — кисломолочных продуктов.
- Развитие АБ-ассоциированной диареи обычно купируется после отмены причинно-значимого препарата. Хотя в этом случае может возникнуть потребность в медикаментозном лечении, что в каждом случае решается индивидуально. Однако роль правильного питания и в этом случае также является решающей. (Исключением является псевдомембранозный колит клостридиозной этиологии, лечение которого довольно сложное и может быть не всегда эффективным).
- У детей первых 4-6 месяцев жизни расстройство стула часто трудно поддаются лечению, но в большинстве случаев быстро исчезают после введения прикорма (в первую очередь, фруктов и овощей).
- Необходимо понимать, что проблема дисбактериоза – это проблема местной защиты. Поэтому, даже если путем героических усилий добиться нормализации состава микрофлоры кишечника (по анализу кала на дисбактериоз, что само по себе ни о чемне говорит, как уже упоминалось ранее), то при сохранении плохой местной защиты попадание в кишечник достаточно агрессивных возбудителей вновь приведет развитию дисбактериоза.
- Микробы, содержащиеся в биопрепаратах, хоть и могут участвовать в заселении кишечника, но их роль в этом процессе невелика. Основная их функции – стимуляция местного иммунитета. (Косвенным подтверждением этого тезиса является убедительно доказанный факт защитного действия L.rhamnosus GG при ротавирусном энтерите).
Диатез или атопический дерматит. Статьи
1.Что такое диатез? Это только особенная детская аллергия, или пока лишь предрасположенность к аллергии? Почему она возникает?
Итак, что такое диатез? На сегодня под термином диатез подразумевают состояния предрасположенности организма к развитию аллергических болезней. Клиническими проявлениями предрасположенности ребенка к аллергическим заболеваниям являются легкие транзиторные аллергические реакции на пищу или бытовые аллергены, вакцины или укусы насекомых, химические вещества и другое — єто и есть ответ на вопрос «Что такое диатез». Также к таким проявлениям стоит отнести изменения стула со слизью, эпизоды насморка с водянистыми выделениями, повторные явления бронхообструкции и стеноз гортани при ОРВИ, эозинофилию.
2.Может ли диатез проявлять себя в виде опрелости у крошки, потнички при любом, даже самом легком перегревании? А серо-желтые сальные корочки на волосяной части головы и бровях тоже от этого? Каковы его первые признаки?
Да, действительно частыми проявлениями диатеза у детей есть повторные транзиторные кожные высыпания, опрелости при отсутствии дефектов ухода за малышом, а также гнейсы. Это и является первыми признаками, которые должны насторожить маму.
3.Является диатез своеобразным сигналом для мамы, что в будущем ребенок будет склонен к аллергиям?
Діатез является сигналом, но при соблюдении всех рекомендаций и организации правильного питания прогноз вполне благоприятный — про слово диатез забудете навсегда. Неадекватная лечебная тактика, примененная к ребенку в раннем детском возрасте, может привести к реализации в атопические заболевания различных органов и систем с хроническим течением.
4.С какого возраста у крошки может возникнуть настоящая аллергия в случае, если он на грудном вскармливании? А на искусственном? Существуют ли группы аллергенов, которые могут вызывать аллергии или діатез в раннем возрасте?
Сроки реализации диатеза в настоящую аллергию зависит от различных факторов, таких как генетическая предрасположенность, реактивность организма, правильность питания и ухода за кожей малыша.
Начало симптомов аллергического дерматита отмечается: в возрасте до 6 месяцев — в 60% случаев, до 1 года- в 75%, до 7 лет-80-90%.На грудном вскармливании риск развития аллергии меньший. Наиболее опасные аллергены коровье молоко, яйца, злаки, соя, рыба, овощи и фрукты красного или оранжевого цвета.
5.Какими методами можно выяснить аллергия ли это?
Диагностика аллергии базируется главным образом на анализе клинических проявлений . Существующие лабораторные исследования являются вспомогательными и имеют значение только при наличии клинической картины.
6.Могут ли аллергии быть последствием каких -либо очагов хронической инфекции, например, наличием глистов в организме у ребенка, лямблий, хламидий, дисбактериоза кишечника?
Может, ведь часто ликвидация хронических очагов инфекции, избавление от глистов и здоровый желудочно-кишечный тракт – все эти факторы способствуют избавлению от аллергии.
7.Почему надо лечить аллергии? К каким последствиям могут привести не вылеченные аллергии?
Лечить аллергии необходимо, так как это может привести к развитию бронхиальной астмы, аллергического ринита, рецидивирующего ларинготрахеита а также поллиноза.
8.Какие методы лечения аллергии существуют сегодня?
В детском, особенно грудном возрасте, необходима диета. Большое значение имеет лечение патологии пищеварительного тракта, дисбактериоза. Назначают эубиотики, ферментные препараты, гепатопротекторы. Длительно болеющим детям целесообразно периодически рекомендовать седативные препараты В период обострения применяют непродолжительными курсами антигистаминные препараты. Иммуномодуляторы- по показаниям. Кортикостероиды при атопическом дерматите использовать нежелательно, поскольку формируется гормонорезистентность, отмена же приводит к утяжелению процесса. При осложнении вторичным инфицированием назначают наружно кремы с антибактериальными препаратами. Большое внимание следует уделять процедурам, способствующих увлажнению кожи. Это должны быть ежедневные ванны(можно с поваренной, морской солью, отрубями), последующее нанесение увлажняющих кремов. Хороший результат дает назначение конституционно подобранных гомеопатических препаратов.
9.Что такое прививка от аллергии?
Прививка от аллергии это метод специфической иммунотерапии. Метод заключается во введении в организм взрослых доз аллергенов, к которому у больного повышенная чувствительность, с целью синтеза защитных антител, что приводит к уменьшению или полному исчезновению симптомов. У детей раннего возраста не используется, так как тяжело выявить аллерген.
10.С какого возраста можно вводить прикорм ребенку страдающему диатезом или аллергиями ?Лучше использовать готовые смеси и консервы, или натуральные продукты?
Прикорм , как здоровым так и ребенку с диатезом следует начинать не ранее с 6 месяцев. Овощи или каши ,в каком обьеме, в какое время определяет непосредственно ваш доктор, который учитывает уровень физического развития ребенка, состояния желудочно-кишечного тракта, переносимость или непереносимость определенных продуктов родителями, наличия у ребенка сопутствующих заболеваний.
Обычно грудным детям начинают вводить прикормы по 1/4 чайной ложке, по капельке, по несколько грамм, между едой или докармливая, после грудного молока. И даже если не совершается грубых ошибок, когда ребенку дают сразу большой объем новой пищи или вводят продукт не по возрасту .Можно выделить три основных правила осторожного введения прикормов.
1.НЕ БОЛЕЕ ОДНОГО НОВОГО ПРОДУКТА В 1 — 2 НЕДЕЛИ
2.НОВУЮ ЕДУ ДАВАТЬ В КОНЦЕ КОРМЛЕНИЯ, ПО ВОЗМОЖНОСТИ СМЕШИВАЯ СО «СТАРОЙ» (ЗНАКОМОЙ РЕБЕНКУ) ПИЩЕЙ
3.ЧЕМ МЕНЬШЕ ПЕРВОНАЧАЛЬНАЯ ДОЗА, ЧЕМ МЕДЛЕННЕЕ ОНА УВЕЛИЧИВАЕТСЯ, ТЕМ МЕНЬШЕ ВЕРОЯТНОСТЬ ВОЗНИКНОВЕНИЯ ДИАТЕЗА
Для ребенка с аллергией лучше использовать адоптированные лечебные смеси, которые не только способствуют гормоничному развитию малыша, но и оздоравливают желудочно-кишечный тракт. Натуральные продукты конечно же полезны, если вы уверенны в их безопасности. Я бы советовала начинать прикорм с натуральных овощей и фруктов, если ребенок среагировал плохо- пробуйте готовые консервы.
11.Если у ребенка старшего возраста уже есть пищевая аллергия на какие либо продукты, иногда возникает даже отек Квинке, есть ли надежда, что с возрастом это заболевание у него пройдет? Какие методы лечения существуют?
Прогноз лечения зависит от многих факторов, но надежда на выздоровление всегда есть. Каждому ребенку нужен индивидуальный подход к лечению и залогом успешной терапии атопического дерматита является комплексное лечение ,направленное на коррекцию разнообразных звеньев патогенеза данного заболевания под системным наблюдением врача.
Статью подготовила врач педиатр медицинского центра «MDclinic» Коломиец Людмила Александровна.
Вмешательство при дисбактериозе у детей, рожденных кесаревым сечением — FullText — Annals of Nutrition and Metabolism 2018, Vol. 73, Прил. 3
Аннотация
Симбиотические отношения между микробами и человеком имеют фундаментальное значение для физиологического развития и здоровья. Микробиом новорожденного претерпевает кардинальные изменения в процессе рождения и в первую тысячу дней жизни. Мать-природа предоставила нам наилучший возможный старт для достижения эубиоза: вагинальные роды для получения микробиома нашей матери и грудного молока, которое способствует созданию полезных бактерий.Младенцы, лишенные одного или обоих этих эволюционных дарований, подвергаются серьезной модификации микробных сообществ, ведущей к состоянию дисбактериоза, что увеличивает вероятность возникновения различных иммунных, воспалительных и метаболических нарушений. Умеем ли мы подражать природе? Есть ли какое-либо вмешательство при дисбактериозе у детей, рожденных путем кесарева сечения? В этом обзоре мы постараемся ответить на этот интригующий вопрос на основе самых последних научных данных.
© 2018 С.Karger AG, Базель
Введение
Люди эволюционировали, чтобы жить и развиваться в среде, плотно населенной микробами. Недавно стало очевидно, что наше существование в микробном мире, а не просто сожительство, можно определить как взаимовыгодный симбиоз [1].
Состоящая из 10 11 –10 12 микроорганизмов на грамм фекалий и укрывающая более 500 видов, микробиота кишечника является важным посредником в здоровье и болезнях и взаимодействует с различными органами и системами организма. включая мозг, печень, кости и сердечно-сосудистую систему.Это сложная экосистема, сформированная эволюцией, с ассоциациями хозяин-бактерия, которые способствуют хрупкому равновесию, эволюционировавшему для модуляции иммунных ответов и укрепления здоровья [2].
Микробная колонизация желудочно-кишечного тракта — важный процесс, определяющий физиологию и иммунитет хозяина, который начинается на раннем этапе развития и претерпевает глубокие изменения в течение жизни.
Этот деликатный процесс, разработанный в ходе эволюции и характеризующийся высокой численностью различных видов бактерий, может претерпевать несколько модификаций, вторичных по отношению к различным условиям окружающей среды, которые в конечном итоге могут нанести ущерб хозяину.Эти факторы могут включать способ родоразрешения, гестационный возраст при рождении, использование антибиотиков в раннем возрасте, вскармливание младенцев, чрезмерную гигиену и воздействие окружающей среды, а также другие медицинские вмешательства.
В течение десятилетий считалось, что диада плод-мать свободна от микробов до момента родов и первого контакта с микробным сообществом влагалища и фекалий матери. Однако недавние данные свидетельствуют о том, что колонизация начинается в утробе матери; действительно, микробы были идентифицированы в околоплодных водах, пуповинной крови, плодных оболочках, меконии и плаценте [3].Недавние исследования с использованием комбинации культуральных и некультуральных методов показывают, что новорожденные могут подвергаться воздействию микробов, которые достигают околоплодных вод, даже при наличии неповрежденных мембран или хориоамнионита с положительным посевом [4]. Следует помнить, что в течение последнего триместра беременности плод проглатывает большие количества околоплодных вод, которые достигают высоко иммуно-реактивного кишечника плода, который подвергается воздействию большого количества микробов и микробных компонентов / продуктов.
Однако оживление — это первое и самое важное окно воздействия микробов: это критическая и уникальная возможность начать создание стабильной микробиоты сердцевины кишечника. Процесс вагинальных родов позволяет микробиому матери служить «закваской» для микробиома младенца: во время родов и вскоре после этого бактерии матери и окружающей среды колонизируют кишечник младенца.
Вагинальные роды — это способ, которым природа устроила рождение млекопитающих, и эволюция диады мать-плод развивалась вокруг этой особенности, и это продолжалось миллионы лет.Однако природа не могла предвидеть появления других модальностей рождения. Кесарево сечение (кесарево сечение) спасло очень большое количество жизней; однако в последние десятилетия это стало стандартной и иногда ненужной или, что еще хуже, удобной практикой. За последние два десятилетия частота кесарева сечения в некоторых странах приблизилась к 50%, что не демонстрирует особого интереса к тому, как «способ родоразрешения» может повлиять на здоровье в долгосрочной перспективе.
За последние несколько столетий, особенно в промышленно развитых странах, рост рождаемости из-за кесарева сечения, преждевременных родов и использования антибиотиков во время беременности, в дополнение к изменениям в кормлении младенцев, условиях жизни, диете, образе жизни и общей гигиене могут изменили способы приобретения кишечных микробных сообществ.Модификация микробных сообществ может привести к состоянию дисбактериоза, увеличивая вероятность возникновения различных иммунных (например, астма), воспалительных (воспалительное заболевание кишечника) и метаболических (например, детское ожирение) расстройств.
В настоящее время известно, что микробная колонизация после вагинальных родов отличается от того, что происходит после кесарева сечения [5]; во время родов через естественные родовые пути контакт с микрофлорой влагалища и кишечника матери является наиболее важным источником микробной колонизации младенцев, способствующей колонизации, главным образом, Lactobacilli, Prevotella и Bifidobacteria [6].Напротив, во время кесарева сечения колонизация новорожденного пилотируется бактериями окружающей среды нематериального происхождения, что приводит к менее разнообразной флоре и бактериальному сообществу, напоминающему микробиоту поверхности кожи (Staphylococcus), и задерживает колонизацию кишечника Lactobacillus, Bifidobacterium и Bacteroides. [7]. Последние данные показывают, что младенцы, рожденные в результате планового кесарева сечения, имеют особенно низкое бактериальное богатство и разнообразие, задержку колонизации типа Bacteroidetes и снижение ответов Th2 в течение первых 2 лет жизни [8, 9].Имеющиеся эпидемиологические данные показывают, что атопические заболевания, астма, диабет 1 типа и пищевая аллергия более распространены у младенцев после кесарева сечения, чем после родов через естественные родовые пути [10].
Хотя все данные, кажется, указывают на одно и то же направление, недавнее многоцентровое исследование в Европе, в котором были проанализированы 606 младенцев, показало, что способ родоразрешения не влияет на относительную долю бифидобактерий в 6-недельных младенцах. Тем не менее, вагинальные роды были связаны с более высокой средней долей Bacteroides и членов кластера Atopobium и более низкой долей членов группы Coccoides и группы Streptococcus.Младенцы, рожденные естественным путем, имели более разнообразную и богатую микробиоту с большей долей по сумме выявленных групп по сравнению с другими младенцами [11].
В недавнем исследовании Sakwinska et al. [12] исследовали роль способа родов и кормления на материнском вкладе в микробиоту кишечника и носа младенца. Используя секвенирование 16S рРНК и специфическую количественную полимеразную цепную реакцию, авторы смогли профилировать микробиоту 42 матери и ребенка на участках тела (влагалище матери, прямая кишка и кожа, стул и нос младенца) и продемонстрировать перекрытие между влагалищем матери и младенцем. фекальная микробиота (минимальная) и материнская ректальная и младенческая микробиота (высокая).
Montoya-Williams et al. недавно опубликовал систематический обзор влияния способа родоразрешения на развитие микробиома младенца с учетом доступной литературы, опубликованной с 2010 по 2015 год, с единственным ограничением на английском языке. Они сообщили, что микробиом кишечника новорожденных, рожденных через естественные родовые пути, более похож на микробиом влагалища их матерей и, таким образом, чаще состоит из потенциально полезной микробиоты, такой как Lactobacillus, Bifidobacterium и Bacteroides.Напротив, микробиом младенцев, рожденных посредством кесарева сечения, показывает повышенное преобладание либо кожной флоры, либо потенциально патогенных микробных сообществ, таких как Klebsiella, Enterococcus и Clostridium [13].
Смешивающие факторы
Данные по этой теме имеют серьезный недостаток, связанный с несколькими ошибками. Первоначальная медицинская причина кесарева сечения, независимо от того, проводится ли процедура во время выборов или в экстренной ситуации, получали ли матери антибиотики в дородовой или послеродовой период, а также время кормления грудью или смесью — это факторы, которые все еще нуждаются в полном понимании и исследовании. в будущих исследованиях.Наконец, немедицинские переменные, такие как социально-экономический статус матери и семьи, также могут играть важную роль в выборе между кесаревым сечением и вагинальными родами.
Формирование кишечной микробиоты после C-Section
Зная важность «здорового» состава желудочно-кишечного микробиома, становится очевидным, что микробные вмешательства во время беременности и в течение первых 1000 дней жизни могут представлять собой эффективные стратегии и окно возможностей для целевых вмешательств, направленных на улучшение здоровья детей в будущем.
Эти стратегии могут быть сосредоточены на матери, новорожденном или на обоих сразу. Улучшение окружающей среды с помощью различных «гигиенических» привычек и методов охраны здоровья может повлиять на формирование микробиоты. В качестве альтернативы вмешательство может быть сосредоточено на матери путем использования пробиотиков, и / или пребиотиков, и / или полиненасыщенных жирных кислот во время беременности. Наконец, вмешательство может быть сосредоточено на новорожденном с использованием различных подходов: микробный «посев», грудное вскармливание в отличие от кормления смесью или использование пробиотиков / пребиотиков.В этом обзоре мы обобщаем возможное биологическое объяснение текущих возможных стратегий, направленных на предотвращение / коррекцию дисбактериоза «Когда аист идет за скальпелем» [14].
Окружающая среда
Эпидемиологические исследования показывают, что проживание в непосредственной близости от естественной сельской или прибрежной среды, часто обозначаемой «зеленым пространством» или «синим пространством» соответственно, может быть полезно для здоровья человека как за счет снижения распространенности болезней, так и за счет увеличения выживаемости. «Дарвиновский» синтез гипотезы гигиены (или «старых друзей») предполагает, что рост хронических воспалительных заболеваний, который начался в Европе в середине 19 века и все еще продолжается, может быть, по крайней мере, частично отнесен к иммунной дерегуляции.Сниженное или несоответствующее воздействие конкретных микроорганизмов, с которыми мы эволюционно участвовали в процессах созревания, ведущих к установлению физиологической иммунной регуляции, может быть результатом нынешней эпидемии «современных болезней». Биоразнообразие среды, в которой находится ребенок, включая членов семьи, контактирующих с младенцами, различный образ жизни и гигиенические методы, может напрямую влиять на разнообразие микробов, которые передаются младенцу.
Например, в 2013 году Azad et al.оценили различные микробы, присутствующие в 24 образцах фекалий, собранных в период с 2008 по 2009 год у 4-месячных младенцев; Из 24 младенцев 15 жили в домах как минимум с 1 собакой или кошкой. Исследователи обнаружили, что проживание с домашними животными приводит к большему разнообразию микробов в кишечнике младенца (по данным их фекалий) [15].
Вмешательства во время беременности
Диета матери до и во время беременности может влиять на развитие кишечной микробиоты ребенка [16]. Было показано, что чрезмерное потребление трансжирной кислоты (ТЖК) у крыс вызывает у младенцев слабое воспаление, в то время как Юссара (Euterpe edulis Mart.) добавление во время беременности и кормления грудью отменяет эффекты трансжирных кислот и увеличивает количество Lactobacillus spp. в потомстве [17].
Исследования на мышах показывают, что безглютеновая диета матери увеличивает количество Akkermansia, Proteobacteria, в микробиоте кишечника потомства и снижает частоту диабета и воспалений низкой степени [18]. На людях также было показано, что «нездоровая» диета матери во время беременности или плохое питание в раннем детстве может привести к формированию дефектной кишечной микробиоты [19].
Введение пробиотиков будущим матерям, особенно на поздних сроках беременности, может представлять собой эффективную стратегию по обеспечению здорового микробного состава у младенцев. Было продемонстрировано, что лечение будущих матерей с помощью L. rhamnosus GG способно передать и сохранить этот штамм новорожденному от 6 до 24 месяцев. Кроме того, младенцы, матери которых получали L. rhamnosus GG на поздних сроках беременности, демонстрируют более высокие показатели колонизации бифидобактериями по сравнению с младенцами, рожденными от матерей, получавших плацебо [20].Однако во втором исследовании L. rhamnosus GG не удалось положительно изменить микробное разнообразие, несмотря на то, что он способствовал положительному профилю Bifidobacterium [21].
Различные рандомизированные контролируемые испытания продемонстрировали, что вмешательство матери с пробиотиками во время беременности и грудного вскармливания может эффективно снизить частоту атопического дерматита у ребенка [22]; этот эффект был недавно подтвержден в метаанализе, подтверждающем, что введение пробиотиков во время беременности предотвращает атопический дерматит у детей [23].Возможное объяснение этого открытия заключается в том, что введение пробиотиков матерям во время беременности и / или грудного вскармливания может положительно влиять на цитокиновый профиль материнского молока и увеличивать sIgA в фекалиях младенцев, тем самым способствуя ответу Th2 [24].
Помимо пробиотиков, пребиотики также показали многообещающие эффекты в улучшении состояния иммунной системы и здоровья, вызванного микробиотой. Пребиотики — это «неперевариваемые вещества, которые оказывают положительный физиологический эффект на хозяина, избирательно стимулируя рост или активность ограниченного числа местных бактерий.Пребиотики естественным образом содержатся в пищевых продуктах, таких как овощи, пшеница и соевые бобы, и обычно представляют собой олигосахариды или более сложные сахариды. Пока что наиболее часто изучаемыми соединениями являются инулин, фруктоолигосахариды и галактоолигосахариды. Исследования на животных показали, что добавление пребиотиков во время беременности и кормления грудью приносит потомству пользу, включая модуляцию набора веса независимо от приема, увеличение длины толстой кишки, мышечной массы, костной массы и снижение частоты симптомов аллергии / астмы [25].Исследования на людях ограничены, но добавление неперевариваемых олигосахаридных пребиотиков (особенно фруктоолигосахаридов и / или галактоолигосахаридов) значительно увеличивает количество материнских фекальных Bifidobacterium spp. И, что наиболее важно, Bifidobacterium longum; однако этот бифидогенный эффект может не передаваться потомству [26].
Вагинальный посев
Прививка новорожденного материнской вагинальной микробиотой сразу после родов кесарева сечения называется вагинальным посевом.Это представляет собой потенциальный способ колонизации младенцев с кесаревым сечением микробами, которые они получили бы при естественных родах. Вагинальный посев не является технически сложной процедурой. В первой опубликованной статье стерильная марля, пропитанная физиологическим раствором, вводилась во влагалище за 1 час до кесарева сечения. Его удалили перед операцией и хранили в стерильном контейнере до рождения ребенка, после чего марлевым тампоном протирали ребенка, начиная со рта и лица, а затем со всей остальной части тела [27].Это новаторское исследование имеет некоторые существенные ограничения: во-первых, были изучены только 4 ребенка, а анализ микробиома проводился только в течение 30 дней после рождения. Однако этот эксперимент, подтверждающий принцип действия, должен быть подтвержден в более широкой когорте с более длительным периодом наблюдения.
Вагинальный посев постоянно вызывает интерес в научном мире как в средствах массовой информации, так и среди беременных женщин. Под растущим давлением со стороны акушеров и будущих мам в ноябре 2016 года Американский колледж акушеров и гинекологов выпустил практические рекомендации по процедуре вагинального посева.Их вывод заключался в том, что, хотя преимущества вагинального посева биологически вероятны, до сих пор нет подтверждающих доказательств его использования из-за отсутствия данных о безопасности, связанных с рисками и потенциальным вредом для ребенка. Теоретически передача некоторых патогенов, протекающая бессимптомно у матери («стрептококк группы B, вирус простого герпеса, Chlamydia trachomatis и Neisseria gonorrhea), может быть причиной серьезных неблагоприятных последствий для младенцев. Об аналогичных предупреждениях педиатры из Соединенного Королевства сообщили в редакционной статье BMJ в феврале 2016 г. [28].
Грудное вскармливание
Грудное вскармливание — идеальное питание для новорожденных, и примерно десять лет назад оно считалось бесплодным; в 2003 г. молочнокислые бактерии были впервые описаны в материнском молоке здоровых женщин [29].
В настоящее время в материнском молоке описано более 200 различных видов (принадлежащих к 50 различным родам) с большими индивидуальными вариациями [30]. Грудное молоко здоровой матери содержит 10 9 микроорганизмов на литр, и здоровое питание матери имеет решающее значение для достижения «нормального» состава молока и правильной микробиоты кишечника у младенца [31].
Грудное молоко сегодня признано источником комменсальных и потенциально пробиотических бактерий, выступающих пионерами на решающем этапе начальной колонизации кишечника новорожденных и играющих ключевую роль в здоровье младенцев, способствуя созреванию иммунной системы и конкурентному исключению патогенов. . В период грудного вскармливания начинается колонизация актинобактериями и фирмами [32]; актинобактерии представлены в основном Bifidobacterium (В.), B. breve, B. longum, B. dentium, B.Infantis, B. Pseudocatenulatum и Firmicutes, вызываемые Lactobacillus, Enterococcus и Clostridia [33].
Помимо бактерий, грудное молоко характеризуется уникальным присутствием олигосахаридов грудного молока (HMOs), которые представляют собой гетерогенную смесь неконъюгированных гликанов, не перевариваемых хозяином, и основного источника углерода для кишечных бактерий: a, изменение профиля олигосахаридов в молоке влияет на микробный состав кишечника младенца [34]. Грудное молоко также содержит множество антимикробных факторов, таких как лизоцим, лактоферрин и секреторный иммуноглобулин A (IgA), которые накладывают дополнительный отбор на микробное сообщество кишечника [35].
Было обнаружено, что ранний контакт кожа к коже способствует грудному вскармливанию, косвенно способствуя созданию здоровой микробиоты кишечника.
Пребиотики / добавки с пробиотиками
Пробиотики — это живые микроорганизмы, которые при введении в адекватных количествах приносят пользу здоровью хозяина [36]. Как можно раньше вмешательство с пробиотиками может дать потомству большее преимущество в формировании эубиотической микробиоты кишечника. Механизмы, с помощью которых пробиотики оказывают эти положительные эффекты на хозяина, находятся в центре внимания ряда доклинических и клинических исследований и включают все следующее: (а) улучшение микробного состава кишечника, (б) сохранение его стабильности, (в) конкуренция с патогены на питательные вещества, рост и адгезию, (d) укрепление барьера слизистой оболочки кишечника, (e) противовоспалительный эффект и (f) модуляция иммунной системы.Было установлено, что определенные штаммы пробиотиков обладают способностью изменять состав микробиоты кишечника: у здоровых младенцев, получавших смесь с добавлением Lactobacillus rhamnosus GG, было повышенное количество лактобацилл по сравнению с теми, кто получал обычную смесь [37]. Добавление пробиотиков Bifidobacterium breve Bb12 младенцам с очень низкой массой тела при рождении приводило к колонизации кишечника, а также к быстрому росту Lactobacillus по сравнению с плацебо.
Гарсия Роденас и др.[38] были направлены на оценку реакции детской микробиоты, полученной кесаревым сечением, на смесь, содержащую Lactobacillus reuteri DSM 17938. Младенцы, доставленные путем кесарева сечения и вагинально, были рандомизированы для получения либо контрольной смеси, либо той же смеси, содержащей Lactobacillus reuteri, в течение 72 часов после при рождении и образцы стула были собраны в возрасте 2 недель и 4 месяцев. Авторам удалось продемонстрировать, что L reuteri DSM 17938 у младенцев, рожденных посредством кесарева сечения, играет ключевую роль в модуляции раннего развития микробиоты в сторону состава, обнаруженного после вагинальных родов.
Однако продолжительность приема добавки для обеспечения длительного положительного эффекта неизвестна.
Пребиотики — это «субстрат, который избирательно используется микроорганизмами-хозяевами, принося пользу для здоровья». Это определение расширяет понятие пребиотиков, возможно, включая (а) неуглеводные вещества (например, полиненасыщенные жирные кислоты), (б) применение на участках тела, отличных от желудочно-кишечного тракта, и (в) различные категории помимо продуктов питания [39].
Есть многообещающие результаты исследований, в которых оценивалось влияние смесей с пребиотиками на кишечную флору младенцев.В целом, смесь с пребиотиками по сравнению с смесью без добавок увеличивает мягкость стула и может снизить частоту кишечных инфекций и диареи, уменьшить экзему, снизить потребность в лечении антибиотиками и увеличить количество бифидобактерий [40]. К результатам следует относиться с осторожностью, поскольку эти исходы не были представлены или продемонстрированы во всех испытаниях, включенных в обзор, а другие авторы в предыдущей систематической статье не смогли продемонстрировать увеличение количества бифидобактерий или лактобацилл или снижение уровня патогенов ( Bacteriodes , Escherichia coli ) у младенцев, получающих смесь с пребиотиками [41].
Новые исследования показали важность ОПЗ в усилении развития кишечной микробиоты и поддержке иммунной защиты. Puccio et al. [42] оценили влияние детской смеси с добавлением ОПЗ на рост, переносимость и заболеваемость здоровых детей. Здоровые младенцы были рандомизированы на получение стандартной детской смеси или той же смеси с 1,0 г / л 2’-фукозиллактозы (2’FL) и 0,5 г / л лакто-N-неотетраозы (LNnT) в течение 6 месяцев. Они пришли к выводу, что детские смеси с 2’FL и LNnT безопасны, хорошо переносятся и поддерживают соответствующий возрасту рост; добавление ОПЗ было связано с более низкими показателями заболеваемости, о которой сообщали родители (особенно бронхита), и с использованием лекарств, что позволяет предположить, что ОПЗ могут оказывать влияние за пределами желудочно-кишечного тракта.
Наконец, еще предстоит доказать, могут ли младенцы, рожденные с помощью кесарева сечения, по сравнению с младенцами, рожденными естественным путем, получить большее преимущество от смеси с пребиотиками.
Выводы
Первая тысяча дней формирует здоровье будущего человека. Мать-природа предоставила нам наилучший старт двумя разными способами: вагинальные роды для получения микробиома нашей матери, сформированного вокруг нашего генома, и грудное молоко, которое способствует созданию полезных бактерий для защиты ребенка от колонизации патогенными бактериями и предотвращение неонатального поноса. и инфекции дыхательных путей.Иногда младенцы лишены одного или обоих этих эволюционных даров, что приводит к резким изменениям состава и формы микробиоты с возможным негативным воздействием на здоровье взрослых в будущем. «Новые микробы», приобретенные сразу после рождения посредством кесарева сечения, могут способствовать дисбалансу иммунной системы, играющему роль как в раннем постнатальном периоде жизни, так и на протяжении всей жизни человека. Умеем ли мы подражать природе? Конечно, нет, но разработка стратегий для достижения золотого стандарта должна основываться на результатах хорошо спланированных и проведенных клинических испытаний, которые мы надеемся провести в ближайшем будущем.Надеясь на лучшее, мы «никогда не думаем о будущем — оно наступит достаточно скоро» (Альберт Эйнштейн).
Заявление о раскрытии информации
Все авторы не имеют финансовых отношений, имеющих отношение к этой статье, которые следует раскрывать. Все авторы не сообщают о конфликте интересов.
Источник финансирования
Не указывается.
Список литературы
- Backhed F, Ley RE, Sonnenburg JL и др.: Бактериальный мутуализм хозяина в кишечнике человека.Наука 2005; 307: 1915–1920.
- Guarner F, Malagelada JR: Кишечная флора в состоянии здоровья и болезней. Lancet 2003; 361: 512–519.
- Neu J Микробиом во время беременности и в раннем послеродовом периоде.Semin Fetal Neonatal Med 2016; 21: 373–379.
- DiGiulio DB, Romero R, Amogan HP и др.: Распространенность, разнообразие и изобилие микробов в околоплодных водах во время преждевременных родов: исследование на основе молекулярных и посевов. PLoS One 2008; 3: 33056.
- Neu J, Rushing J: Кесарево сечение по сравнению с вагинальными родами: долгосрочные исходы для новорожденных и гипотеза гигиены.Clin Perinatol 2011; 38: 321–331.
- Домингес-Белло М.Г., Костелло Е.К., Контрерас М. и др.: Способ доставки формирует приобретение и структуру исходной микробиоты в различных средах обитания новорожденных. Proc Natl Acad Sci USA 2010; 107: 11971–11975.
- Биасуччи Г., Бененати Б., Морелли Л. и др.: Кесарево сечение может повлиять на раннее биоразнообразие кишечных бактерий.J Nutr 2008; 138: 1796–1800 гг.
- Azad MB, Konya T, Maughan H et al: Микробиота кишечника здоровых канадских младенцев: профили по способам родоразрешения и питанию младенцев в 4 месяца. CMAJ 2013; 185: 385–394.
- Jakobsson HE, Abrahamsson TR, Jenmalm MC и др.: Уменьшение разнообразия кишечной микробиоты, задержка колонизации Bacteroidetes и снижение ответа Th2 у младенцев, рожденных с помощью кесарева сечения.Gut 2014; 63: 559–566.
- Eggesbø M, Botten G, Stigum H и др.: Является ли кесарево сечение фактором риска пищевой аллергии? J Allergy Clin Immunol 2003; 112: 420–426.
- Фаллани М., Янг Д., Скотт Дж. И др.: Кишечная микробиота 6-недельных младенцев по всей Европе: географическое влияние за пределами родовспоможения, грудного вскармливания и антибиотиков.J Pediatr Gastroenterol Nutr 2010; 51: 77–84.
- Саквинска О., Фоата Ф, Бергер Б. и др.: Играет ли материнская вагинальная микробиота роль в посеве микробиоты кишечника и носа новорожденных? Benef Microbes 2017; 8: 763–778.
- Montoya-Williams D, Lemas DJ, Spiryda L, et al: Микробиом новорожденного и его частичная роль в опосредовании связи между рождением путем кесарева сечения и неблагоприятными педиатрическими исходами.Неонатология 2018; 114: 103–111.
- Миньелло В.Л., Коласанто А., Кристофори Ф. и др.: Биомодуляторы кишечной микробиоты, когда аист проникает через скальпель. Clin Chim Acta 2015; 451: 88–96.
- Азад МБ, Конья Т., Моган Х. и др.: Микробиота кишечника младенца и гигиеническая гипотеза аллергического заболевания: влияние домашних животных и братьев и сестер на состав и разнообразие микробиоты.Allergy Asthma Clin Immunol 2013; 9:15.
- Майлс И.А., Пинкус Н.Б., Фонтекилла Н.М. и др.: Влияние родительского потребления омега-3 жирных кислот на микробиом и иммунитет потомства. PLoS One 2014; 9: e87181.
- Алмейда Мораис К., Ояма Л. М., де Оливейра Дж. Л. и др .: Юссара (Euterpe edulis Mart.) добавление во время беременности и кормления грудью модулирует экспрессию генов и белков биомаркеров воспаления, индуцированных трансжирными кислотами в толстой кишке потомства. Медиаторы Inflamm 2014; 2014: 987927.
- Hansen CH, Krych L, Buschard K и др. Безглютеновая диета по материнской линии снижает воспаление и заболеваемость диабетом у потомства мышей NOD.Диабет 2014; 63: 2821–2832.
- Салазар Н., Арболея С., Вальдес Л. и др.: Микробиом кишечника человека в экстремальном возрасте. Диетическое вмешательство как способ противодействия изменениям. Front Genet 2014; 5: 406.
- Schultz M, Gottl C, Young RJ, et al: Введение оральных пробиотических бактерий беременным женщинам вызывает временную инфантильную колонизацию.J Pediatr Gastroenterol Nutr 2004; 38: 293–297.
- Исмаил И.Х., Оппедисано Ф., Джозеф С.Дж. и др.: Пренатальное введение Lactobacillus rhamnosus не влияет на разнообразие микробиоты кишечника новорожденных. Pediatr Allergy Immunol 2012; 23: 255–258.
- Раутава С., Кайнонен Э., Салминен С. и др.: Прием материнских пробиотиков во время беременности и кормления грудью снижает риск экземы у младенца.J Allergy Clin Immunol 2012; 130: 1355–1360.
- Zuccotti G, Meneghin F, Aceti A, et al: Пробиотики для профилактики атопических заболеваний у младенцев: систематический обзор и метаанализ. Аллергия 2015; 70: 1356–1371.
- Луото Р., Каллиомаки М., Лайтинен К. и др.: Влияние перинатального пробиотического вмешательства на развитие избыточного веса и ожирения: последующее исследование от рождения до 10 лет.Int J Obes 2010; 34: 1531–1537.
- Буэно-Варгас П., Манзано М., Диас-Кастро Дж. И др.: Пищевая добавка для матери с инулином, обогащенным олигофруктозой, у беременных / кормящих крыс сохраняет материнскую кость и улучшает микроархитектуру костей у их потомства. PLoS One 2016; 11: e0154120.
- Джинно С., Тошимицу Т., Накамура Ю. и др.: Прием пребиотиков матери увеличивает количество фекальных бифидобактерий у беременных женщин, но не у новорожденных в возрасте одного месяца. Питательные вещества 2017; 9: e196.
- Домингес-Белло М.Г., Де Хесус-Лабой К.М., Шен Н. и др.: Частичное восстановление микробиоты младенцев, рожденных после кесарева сечения, посредством вагинального микробного переноса.Nat Med 2016; 22: 250–253.
- Каннингтон А.Дж., Сим К., Дейерл А. и др. «Вагинальный посев» младенцев, рожденных с помощью кесарева сечения. BMJ 2016; 352: i227.
- Мартин Р., Ланга С., Ревириего С. и др.: Грудное молоко является источником молочнокислых бактерий для кишечника младенца.J Pediatr 2003; 143: 754–758.
- Хант К.М., Фостер Дж. А., Форни Л. Дж. И др.: Характеристика разнообразия и временной стабильности бактериальных сообществ в материнском молоке. PLoS One 2011; 6: e21313.
- Кабрера-Рубио Р., Колладо М.К., Лайтинен К. и др.: Микробиом грудного молока изменяется в течение лактации и определяется весом матери и способом родоразрешения.Am J Clin Nutr 2012; 96: 544–551.
- Turroni F, Peano C, Pass DA и др.: Разнообразие бифидобактерий в микробиоте кишечника младенца. PLoS One 2012; 7: e36957.
- Harmsen HJ, Wildeboer-Veloo AC, Raangs GC, et al: Анализ развития кишечной флоры у детей, находящихся на грудном вскармливании и вскармливании смеси, с использованием методов молекулярной идентификации и обнаружения.J Pediatr Gastroenterol Nutr 2000; 30: 61–67.
- Knol J, Scholtens P, Kafka C и др.: Микрофлора толстой кишки у младенцев, вскармливаемых смесями с галакто- и фруктоолигосахаридами: больше похожа на младенцев на грудном вскармливании. J Pediatr Gastroenterol Nutr 2005; 40: 36–42.
- Planer JD, Peng Y, Kau AL, et al: Развитие кишечной микробиоты и IgA-ответов слизистых оболочек у близнецов и мышей-гнотобиотов.Природа 2016; 534: 263–266.
- Hill C, Guarner F, Reid G и др.: Документ о консенсусе экспертов. Консенсусное заявление Международной научной ассоциации пробиотиков и пребиотиков относительно области применения и надлежащего использования термина пробиотик. Нат Рев Гастроэнтерол Гепатол 2014; 11: 506–514.
- Вендт Н., Грюнберг Х., Тууре Т. и др.: Рост в течение первых 6 месяцев жизни у младенцев с использованием смеси, обогащенной Lactobacillus rhamnosus GG: двойное слепое рандомизированное испытание. J Hum Nutr Diet 2006; 19: 51–58.
- Гарсия Роденас С.Л., Лепаж М., Нгом-Брю С. и др.: Влияние смеси, содержащей лактобациллу реутери DSM 17938, на фекальную микробиоту младенцев, рожденных с помощью кесарева сечения.J Педиатр Гастроэнтерол Нутр 2016; 63: 681–687.
- Гибсон Г.Р., Хаткинс Р., Сандерс М.Э. и др.: Консенсусный документ экспертов: консенсусное заявление Международной научной ассоциации пробиотиков и пребиотиков (ISAPP) по определению и сфере применения пребиотиков. Нат Рев Гастроэнтерол Гепатол.2017; 14: 491–502.
- Skórka A, Piescik-Lech M, Kolodziej M, et al: Детские смеси с пребиотиками: лучше ли они, чем без добавок? Обновленный систематический обзор. Br J Nutr 2018; 119: 810–825.
- Mugambi MN, Musekiwa A, Lombard M, et al: Синбиотики, пробиотики или пребиотики в детских смесях для доношенных детей: систематический обзор.Nutr J 2012; 11: 81.
- Пуччо Дж., Аллиет П., Кахоззо С. и др.: Влияние детской дормулы с олигосахаридами грудного молока на рост и заболеваемость: рандомизированное многоцентровое исследование. J Педиатр Гастроэнтерол Нутр 2017; 64: 624–631.
Автор Контакты
Флавия Индрио
«Б.Трамбусти »Больница Джованни XXIII
Виа Амендола 270 Бари
IT – 70124 (Италия)
Эл. Почта [email protected]
Подробности статьи / публикации
Предварительный просмотр первой страницы
Опубликовано онлайн: 24 июля 2018 г.
Дата выпуска: июль 2018 г.
Количество страниц для печати: 6
Количество рисунков: 0
Количество столов: 0
ISSN: 0250-6807 (печатный)
eISSN: 1421-9697 (онлайн)
Для дополнительной информации: https: // www.karger.com/ANM
Авторские права / Дозировка лекарства / Заявление об ограничении ответственности
Авторские права: Все права защищены. Никакая часть данной публикации не может быть переведена на другие языки, воспроизведена или использована в любой форме или любыми средствами, электронными или механическими, включая фотокопирование, запись, микрокопирование, или с помощью какой-либо системы хранения и поиска информации, без письменного разрешения издателя. .
Дозировка лекарства: авторы и издатель приложили все усилия, чтобы гарантировать, что выбор и дозировка лекарства, указанные в этом тексте, соответствуют текущим рекомендациям и практике на момент публикации.Тем не менее, ввиду продолжающихся исследований, изменений в правительственных постановлениях и постоянного потока информации, касающейся лекарственной терапии и реакций на них, читателю настоятельно рекомендуется проверять листок-вкладыш для каждого препарата на предмет любых изменений показаний и дозировки, а также дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендованным агентом является новый и / или редко применяемый препарат.
Отказ от ответственности: утверждения, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и соавторам, а не издателям и редакторам.Появление в публикации рекламы и / или ссылок на продукты не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности. Издатель и редактор (-ы) не несут ответственности за любой ущерб, причиненный людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в контенте или рекламе.
% PDF-1.7
%
2888 0 объект
>
эндобдж
xref
2888 80
0000000016 00000 н.
0000005361 00000 п.
0000005613 00000 н.
0000005650 00000 н.
0000006231 00000 п.
0000006918 00000 н.
0000007352 00000 н.
0000007949 00000 п.
0000008350 00000 н.
0000008389 00000 н.
0000008504 00000 н.
0000008617 00000 н.
0000008986 00000 н.
0000009457 00000 н.
0000009734 00000 н.
0000009847 00000 н.
0000010465 00000 п.
0000011859 00000 п.
0000012276 00000 п.
0000012729 00000 п.
0000012815 00000 п.
0000013163 00000 п.
0000014482 00000 п.
0000015770 00000 п.
0000016996 00000 н.
0000017783 00000 п.
0000018224 00000 п.
0000018706 00000 п.
0000019388 00000 п.
0000019645 00000 п.
0000019896 00000 п.
0000021083 00000 п.
0000022101 00000 п.
0000022236 00000 п.
0000022388 00000 п.
0000022417 00000 п.
0000023030 00000 н.
0000024517 00000 п.
0000031067 00000 п.
0000032253 00000 п.
0000034904 00000 п.
0000034975 00000 п.
0000035083 00000 п.
0000066944 00000 п.
0000076002 00000 п.
0000076251 00000 п.
0000100524 00000 н.
0000105078 00000 н.
0000109472 00000 п.
0000149854 00000 н.
0000158645 00000 н.
0000159115 00000 н.
0000159264 00000 н.
0000159390 00000 н.
0000159621 00000 н.
0000160012 00000 н.
0000160053 00000 н.
0000195992 00000 н.
0000196377 00000 н.
0000196873 00000 н.
0000197274 00000 н.
0000197668 00000 н.
0000197939 00000 н.
0000220349 00000 н.
0000220615 00000 н.
0000221003 00000 н.
0000243239 00000 н.
0000243733 00000 н.
0000243985 00000 н.
0000244366 00000 н.
0000253537 00000 н.
0000253603 00000 н.
0000253696 00000 н.
0000256124 00000 н.
0000256420 00000 н.
0000256683 00000 н.
0000256712 00000 н.
0000257107 00000 н.
0000005133 00000 п.
0000001939 00000 н.
трейлер
] / Назад 1336048 / XRefStm 5133 >>
startxref
0
%% EOF
2967 0 объект
> поток
h {fP! fIcTch $ \ «ajSQ-Qv-H * lGΞT {s} s {|
Дисбиотическая микробиота у аутичных детей и их матерей: сохранение в крови вариантов L-формы грибков и бактерий с дефицитом стенок
Накопленные знания о вариантах микробной клеточной стенки или так называемом феномене L-формы дают основание полагать, что сообщество L-форм может составлять микробиоту в крови человека 3,4,5,6 .Отсутствие клеточных стенок и необычные биологические свойства делают возможным выживание L-форм в бактериостатической среде в крови 17,18,19,20,21,22,23,24 . Мэттман предоставляет собственные данные и данные других авторов и считает, что в различных ситуациях бактерии и грибки существуют и растут как организмы с дефицитом стенок, иногда как естественное явление, иногда вызываемое антимикробными агентами 25 . Доминг предполагает, что L-формы обладают потенциалом неограниченного роста и, в зависимости от полученного стимула, развиваются по разным маршрутам 8 .Итак, L-формы характеризуются как недифференцированные и мультипотентные клетки. Переход L-форм в более дифференцированные клетки был хорошо продемонстрирован электронной микроскопией в наших предыдущих исследованиях 3,4,5,6 . Как было обнаружено в текущем исследовании, популяция сферических L-форм развивалась из крови здоровых людей, а также из крови аутичных детей и их матерей. В отличие от здоровой контрольной группы, L-формы крови аутичных детей и их матерей преобразовывались при соответствующих условиях культивирования в обнаруживаемые бактерии и грибки.Таким образом, было продемонстрировано, что изолированные условно-патогенные бактерии, дрожжи и мицелиальные грибы способны не только существовать как варианты с дефицитом клеточной стенки (CWD) в крови, но также возвращаться к нормальным воспроизводящим клеткам путем синтеза новой клеточной стенки. Извлечение бактериальных и грибковых культур из крови, как правило, особенно сложно, особенно когда они находятся в состоянии дефицита клеточной стенки и не может быть достигнуто обычными методами, которые используются в стандартных микробиологических лабораториях. Однако использование новаторской методологии позволило их эффективно наблюдать, культивировать, возвращать, изолировать и идентифицировать.Из результатов становится ясно, что общей важной характеристикой для детей с РАС было сохранение в их крови вариантов грибковых и бактериальных клеточных стенок. Подобное явление было обнаружено в крови их матерей. Как показано на рис. 2–6, убедительные доказательства превращения CWD в обнаруживаемые бактерии и грибы были получены с помощью светового микроскопа и наблюдений с помощью ПЭМ во время фаз их культивирования.
Основываясь на гипотезе о существующей микробиоте вариантов с дефицитом клеточной стенки в крови человека, ее можно разделить на два типа состояний: (i) «эубиотическое» или сбалансированное состояние микробиоты крови у здоровых людей и (ii) «дисбиотическое». , или дестабилизированная микробиота крови у аутичных детей и их матерей.При анализе микробиоты детей и матерей следует отметить наиболее очевидную и объединяющую находку для них — наличие в крови безстеночных вариантов жизненного цикла мицелиальных грибов. Как было продемонстрировано в настоящем исследовании, культивирование в адаптированных для грибов жидких средах и дальнейшее субкультивирование на полутвердых средах привело к развитию колоний плесени, напоминающих колонии Aspergillus. Положительный тест на сывороточные антитела, соответственно повышенный титр специфических IgG, IgM, IgA, обнаруженный почти у всех детей, был решающим аргументом в пользу доказанного Aspergillus fumigatus .Не менее удивительным было наличие в крови обследованных детей с РАС и некоторых их матерей безстеночных вариантов Candida parapsilosis , Cryptococcus albidus и Rhodotorula mucilaginosa . В поддержку наших результатов исследования других авторов подтвердили, что дрожжи и мицелиальные грибы способны существовать как формы с дефицитом клеточной стенки при определенных условиях 26,27,28,29,30,31 .
Возникает вопрос, может ли присутствие и сохранение в крови вариантов с дефицитом клеточной стенки (условно-патогенные бактерии, дрожжи и мицелиальные грибы) в крови способствовать развитию аутизма.Когда, как и из каких источников может возникнуть это явление у детей с РАС. Различные факторы риска, такие как пренатальные, перинатальные и послеродовые инфекции или воздействие токсинов окружающей среды после рождения, обсуждались для развития аутизма. 32 . Исследование случаев аутизма обнаружило связь с материнскими бактериальными инфекциями во втором триместре беременности 33 . При анализе микробиоты крови матерей в настоящем исследовании прежде всего выделяется тот факт, что все матери являются носителями разновидностей мицелиальных грибов без стенок.Из их крови были также выделены культуры Candida parapsilosis и Rhodotorula mucilaginosa , а также культуры условно-патогенных бактерий, которые часто встречаются как причины урогенитальных инфекций. Таким образом, микробиоту крови матери можно рассматривать как «дисбиотик». Вероятно, что матери во взрослом возрасте приобретают и сохраняют длительные хронические бактериальные инфекции, а также вторичное вмешательство грибковых агентов. Из локальных очагов хронических инфекций в кровоток могут проникать бактерии и грибки в виде дефектных стенок, преодолевая анатомические барьеры.Взаимоотношения между аутичными детьми и их матерями следует искать во время беременности. Беременность может стать важной вехой для проникновения в эмбрион материнских бактериальных и грибковых L-форм. Недавно мы сообщили, что сохраняющиеся в крови человека самовоспроизводящиеся L-тельца размером 100 нм способны преодолевать барьер матери и плода, проникать в кровоток плода и колонизировать новорожденных 3,4,6 . Представляется, что дисбиотическая микробиота крови матери может быть приобретена эмбрионом уже в процессе онтогенетического развития.Это объясняет, почему дети этих матерей могут демонстрировать практически врожденную толерантность к свободным от стенок вариантам условно-патогенных бактерий и грибов.
Candida spp . являются наиболее часто диагностируемым возбудителем дрожжевых инфекций кровотока у детей, в то время как Aspergillus spp являются ведущими причинами системных инфекций плесени 34,35,36 . Диагноз грибковой инфекции всегда сложно установить, потому что в большинстве случаев посевы отрицательные 25 .Врожденные грибковые инфекции часто упускаются из виду, и их влияние на здоровье новорожденных не распознается. 37 . Результаты текущего исследования дают основание полагать, что как у аутичных детей, так и у их матерей можно заподозрить феномен «грибковой колонизации» или «тихой инфекции», когда «носители» не испытывают симптомов, необходимых для клинического диагноза. Однако стандартные критерии, позволяющие отличить колонизацию от активной инфекции, еще не установлены. Важно, чтобы в случае с матерями инвазия и колонизация грибов происходили в период их взросления и обычно являются вторичными событиями после бактериальных инфекций или других причин.У аутичных детей варианты без стенки грибка могут быть получены от матери вертикальным путем до рождения, и, таким образом, новорожденный может родиться уже колонизированным грибами. Как упоминалось выше, фильтруемые L-формы способны проходить через плацентарный барьер и колонизировать плод 4,6 . В поддержку этого предположения были продемонстрированы фильтруемые формы ТЕА в бульонной культуре аутичного ребенка.
В отличие от матерей, у аутичных детей «грибковая колонизация» или «тихая грибковая инфекция» является основным ведущим состоянием в раннем детстве и может сильно влиять на развитие иммунной и нервной систем.Персистирующие грибы остаются метаболически активными и могут производить микотоксины и другие побочные продукты. Метаболиты грибов часто обнаруживаются в моче аутичных детей и служат маркерами присутствия грибов 38 . Известно, что для преодоления защитных сил организма Aspergillus fumigatus выделяет глиотоксин для подавления иммунной системы. Глиотоксин является ингибитором активации Т-клеток и фагоцитоза макрофагов, а также индуцирует апоптоз в моноцитах и дендритных клетках, происходящих из моноцитов 39,40 .Очевидно, что первичное подавление иммунитета, вызванное Aspergillus, у детей может привести к вторичной полимикробной инвазии условно-патогенных бактерий и других видов грибов, таких как Candida parapsilosis или Cryptococcus albidus , как было обнаружено здесь. Побочные продукты метаболизма плесени отрицательно влияют на структурную или функциональную целостность развивающейся нервной системы 41 . Известно, что Aspergillus секретирует ферменты и белки в больших количествах и может генерировать наночастицы внеклеточно. 42 .Как было продемонстрировано ПЭМ в текущем исследовании, обилие наночастиц было обнаружено у ребенка с РАС, но не у здорового человека из контрольной группы. Наночастицы грибов могут быть эффективным сорбентом токсичных металлов, таких как Al, Sb, Ba, Hg, Pb, Cd и Tl 43 . Более того, наночастицы обладают свойством проникать в огромное количество органов и тем самым усиливать токсическое действие тяжелых металлов. Повышенный уровень тяжелых металлов часто обнаруживается у аутичных детей 44 .Следует отметить, что обнаруженные наночастицы у обследованного с помощью ТЕА аутичного ребенка (1/156) совпадали с обнаруженными высокими уровнями Pb, Al, Ba и Sb в его моче (данные предоставлены родителями). Согласно информации, предоставленной некоторыми из родителей (2/158; 6/178, 7/180, 11/190), повышенный уровень тяжелых металлов (Al, Sb, Ba, Pb, Cd, As, Tin, W, Sn) были обнаружены в моче их детей. Взаимосвязь между производством наночастиц (из Aspegillus fumigatus) и обнаруженными высокими уровнями тяжелых металлов у аутичных детей — это явление, которое заслуживает дальнейшего и более глубокого исследования, чтобы расшифровать патогенез и найти правильный путь к лечению.
Спектр эффектов и нарушений, вызываемых A. fumigatus , в первую очередь зависит от реакции иммунной системы хозяина и может варьироваться от бессимптомного до критического состояния. Однако весь спектр этих состояний находится под одним и тем же диагнозом — аспергиллез, аналогично спектру нарушений психического развития у аутичных детей.
В заключение, варианты условно-патогенных бактерий и грибов с дефицитом клеточной стенки были выделены из крови аутичных детей и их матерей.CWD превращается в подходящих условиях культивирования в обнаруживаемые бактерии и грибы. Объединяющим открытием для детей-аутистов и их матерей стало присутствие в крови вариантов без стенки из жизненного цикла Aspergillus fumigatus , феномена грибковой «колонизации» или «тихой инфекции». Можно предположить, что дети с аутизмом могут рождаться с грибковой колонией, полученной от матери трансплацентарным путем. «Тихий аспергиллез» может сильно влиять на развитие иммунной и нервной систем в раннем детстве и быть основной причиной нарушений развития нервной системы.
Перспективным направлением будущих исследований является разработка критериев для персонализированной оценки микробиоты крови и раннего скрининга микробной колонизации у новорожденных и их матерей, а также выборочного подхода к лечению и уходу за этими новорожденными с целью предотвращения развития аутизма.
Антибиотики | Бесплатный полнотекстовый | Важный вопрос в отношении риска рака и терапии: положительные или отрицательные эффекты антибиотиков? Текущие ответы и возможные альтернативы
1.Вклад бактерий в эукариотическое происхождение и биологию человека
В ходе непрерывного процесса, в ходе которого живые существа постепенно достигали уровней возрастающей структурной и функциональной сложности, бактерии появились в биосфере Земли намного раньше человека. Первоначально популяции бактерий взаимодействовали между собой посредством механизмов, которые способствовали увеличению их собственного разнообразия, а также их способности колонизировать широкий спектр сред. Затем, как утверждается в теории эндосимбиоза [1,2], именно стабильное симбиотическое слияние различных типов бактерий привело к появлению нового типа более сложных организмов, таких как самые ранние одноклеточные эукариоты.С момента своего первого официального предложения более 50 лет назад, хотя теория эндосимбиоза эукариогенеза была подвергнута сомнению [3,4], переоценена [5,6,7] и расширена [8,9,10], ее обоснованность получила широкую поддержку [ 11,12]. Сегодня широко признано, что симбиотический вклад различных структурных и функциональных характеристик специализированных прокариотических организмов, особенно митохондрий и предшественников хлоропластов, представляет собой фундаментальный переход, который позволил эукариотам реструктурировать свои геномы и приобрести огромный биоэнергетический потенциал для значительного более широкое расширение ниши, адаптация к окружающей среде, колонизация и диверсификация, что в конечном итоге приведет к постоянному установлению многоклеточности организма.Помимо создания основы для развития огромного разнообразия и сложности, достигнутого эукариотическими организмами, прокариотические организмы в целом и бактерии в частности сыграли еще одну ключевую полезную роль, сосуществуя с различными организмами-хозяевами, включая человека, и установили мутуалистическое взаимодействие с ними. У человека большое количество бактерий сосуществует почти в каждом органе и на всех поверхностях, непосредственно подвергающихся воздействию компонентов внешней среды (например,д., кожа, носоглотка и полости рта, легкие) или к побочным продуктам, полученным в результате переваривания пищевых соединений (например, желудочно-кишечная система). Эндогенная популяция комменсальных бактерий человека наиболее часто изучается и, следовательно, лучше всего охарактеризована, это то, что раньше называлось «кишечной флорой», а в последнее время нечетко именуется кишечной «микробиотой» или «микробиомом», хотя эти термины часто путают и неправильно используют [13,14]. Термин «микробиота» является правильным, когда он используется для обозначения репертуара штаммов микроорганизмов в данной экосистеме [15].Принято считать, что термин «микробиом» был придуман Джошуа Ледербергом в начале 2000-х годов [16]. Фактически, первое понятие микробиома было введено в 1800-х годах Сергеем Виноградским с точки зрения микробной экологии для обозначения микробной экосистемы («микроб» плюс «биом») в целом. Тем не менее, его нынешнее значение отличается от такого понятия и относится исключительно к геномам видов микробов, населяющих конкретную экосистему [17,18]. За последние 10 лет произошло впечатляющее возрождение фундаментальных и клинических исследований, связанных с микробиота и микробиом человека.Доступность улучшенных методологий культивирования и секвенирования [19,20,21], наряду с достижениями, достигнутыми в результате функциональных исследований, предоставили обширные знания о роли микробиоты как сложного «органа», который выполняет важную роль в поддержании баланса здоровья. и болезненные состояния у людей [22,23,24,25]. Микробиота кишечника, как известно, устанавливает сеть органов кишечника [26], которая поддерживает взаимодействие с микробиотой неколонической кишки [27] и с центральными регуляторами гомеостаза, такими как иммунная система [28,29,30], эндокринная система. [31], метаболизм [32,33], внутренние циркадные часы [34], функция мозга [35] и другие.Через эту сеть микробиота кишечника влияет на начало, тяжесть и исход заболеваний, вызывающих высокие уровни заболеваемости и смертности среди людей, включая сердечно-сосудистые [36,37], печеночные [38], аутоиммунные [39] или инфекционные заболевания [40]. , а также рак [41]. Хотя всегда есть номенклатурные недовольства [42], термины эубиотик и дисбиотик, особенно последний, обычно использовались, чтобы различать «хорошее» (сбалансированное само по себе и с хозяином) и «плохое» (несбалансированное) состояние организма. микробиота кишечника [43,44].Хотя было показано, что различие между этими двумя состояниями не является чисто черно-белым [45,46], общепризнано, что полезная и способствующая развитию болезни роль микробиоты связана с ее эубиотической и дисбиотической стадиями. соответственно [47, 48]. Некоторые микробы сосуществовали и эволюционировали вместе с людьми посредством мутуалистических взаимодействий и выполняли фундаментальные роли в поддержании нашего физиологического и метаболического гомеостаза в ответ на изменения в нашей внутренней и внешней среде.Однако другие микроорганизмы взяли на себя крайне инвазивные роли и стали патогенными для человека, создавая риск для здоровья и угрожая выживанию человека. В конечном итоге результат конкурентных взаимодействий между комменсальными членами нашей микробиоты и потенциальными патогенами станет ключевым фактором, определяющим жизнь / смерть человека [49]. Недавние методологические достижения (например, высокопроизводительное секвенирование ДНК) в палеомикробиологии [50,51,52] позволили существенно расширить наше понимание появления инфекционных микроорганизмов человека, их совместной эволюции с людьми, состояния здоровья человека в прошлом. популяции и общие глобальные экологические взаимодействия во времени.Соответственно, теперь мы знаем, что микробные патогены, особенно бактерии, инфицировали людей в течение тысяч лет [53,54,55]. В настоящее время считается, что самые недавние общие предки Helicobacter pylori, инфицирующие желудки человека, относятся ко времени появления анатомически современных людей [53]; Mycobacterium tuberculosis, этиологический агент туберкулеза, существует менее 6000 лет [53,54], а Yersinia pestis, вызвавшая чуму, распространилась по всему миру не менее 5000 лет [53,55].Данные, полученные из палеомикробиологии, наряду с письменными историческими записями ясно показали, что иногда определенные патогенные бактерии распространяются с высокой скоростью, и их передача приобретает масштабы эпидемии или даже пандемии (таблица 1). Однако стало также ясно, что развитие человеческой цивилизации к более оседлому образу жизни (например, переход от сообществ охотников-собирателей к обществам с земледельческой и скотоводческой экономикой), сопровождаемое созданием все более крупных городов и установлением лучших пути сообщения между городами привели к появлению устойчивых инфекций, вызванных адаптированными к человеку бактериальными патогенами [56,57], многие из которых имели зоонозное происхождение и передавались от животных различными путями [58,59,60].Информация о лечении бактериальных инфекций в первые годы 20-го века была зафиксирована в трудах Древней Греции, где Гиппократ стал основоположником современной медицины [61,62]. С его концепцией болезни как дисбаланса, влияющего на четыре основных телесных жидкости (или «юмора»), и лечения как способов помочь природе восстановить утраченный баланс, Гиппократ повлиял на то, как клиническая практика осуществлялась на протяжении веков [63] по существу во всем мире. и вплоть до современного мира.Контроль и лечение заболеваний включало использование таких процедур, как кровопускание, диетические вмешательства, потребление слабительных, обеспечение отдыха и физических упражнений и другие. Бактериальные инфекции не были исключением и, с включением ампутаций в крайних случаях, лечились в соответствии с принципами «теории юмора» до открытия пенициллина Александром Флемингом в 1928 году и его клинической доступности в конце 1930-х годов [64,65 ]. Благоприятные эффекты пенициллина были немедленно оценены, поскольку его использование спасло тысячи жизней во время Второй мировой войны и привело к значительному увеличению продолжительности жизни человека за довольно короткое время.Однако уже в 1945 году уже были предупреждения о необходимости разумного использования пенициллина как пациентами (чтобы избежать самолечения), так и врачами (для использования соответствующих протоколов дозирования), поскольку уже были некоторые признаки развития пенициллина. устойчивость к пенициллину. К сожалению, реакция многих врачей и ученых на решение проблемы резистентности заключалась в том, чтобы сосредоточиться на выявлении и выделении новых антибиотиков, а не на введении корректирующих поведенческих мер.Хотя первоначально использование дополнительных новых антибиотиков вылечило многие бактериальные инфекции, устойчивость к антибиотикам продолжала расти, и в какой-то момент не было доступных антибиотиков для лечения некоторых инфекций (например, MRSA, метициллин-резистентный Staphylococcus aureus; МЛУ-ТБ, множественный лекарственный туберкулез). -резистентные Mycobacterium tuberculosis) [66]. После многих лет отсутствия новых антибиотиков в настоящее время предпринимаются попытки открыть соединения, которые могут проявлять свою антибиотическую активность через пути, менее благоприятные для развития механизмов устойчивости у целевых популяций бактерий [67,68].Внедрение других видов соединений (например, бактериофагов, энзибиотиков и др.) В качестве альтернативы применению антибиотиков, не вызывающих эффектов лекарственной устойчивости, будет обсуждаться позже в этом обзоре.
2. Бактерии и рак
Существует ряд сходных ассоциаций между прокариотическими микроорганизмами, особенно бактериями, и заболеваемостью раком в животном мире, включая людей [69,70]. Как и в случае с инфекционными заболеваниями, письменные записи из разных культур [71,72,73,74] и данные палеоонкологии / патологии [75,76,77,78] ясно показывают, что рак действительно является древней болезнью (Таблица 2 ).Фактически, самый ранний рак гоминида, описанный на сегодняшний день, соответствует случаю остеосаркомы возрастом 1,7 миллиона лет, описанному в Южной Африке [79]. Интересно, что, как и в случае с бактериальными инфекциями, лечение рака также основывалось на «теории юмора» до середины 19 века с постепенным внедрением улучшенных хирургических методов [80,81]. Только в 1890-х годах рентгеновские лучи стали использоваться в качестве первой формы лучевой терапии [82], примерно в 1940 году для начала химиотерапии [83], после 1970 года для использования антител [84] и гораздо позже для лечения использование протоколов, нацеленных на иммунные контрольные точки [85], в результате чего иммунотерапия стала первой линией доступных в настоящее время противоопухолевых методов лечения.Стоит упомянуть, что термин «химиотерапия» был впервые введен в начале 1900-х годов немецким биохимиком Полем Эрлихом для обозначения использования химических веществ для лечения заболеваний, в частности инфекционных [83]. В настоящее время под термином «химиотерапия» чаще всего понимают использование химических веществ для лечения рака. Тем не менее, эта концепция кажется взаимозаменяемой между противоопухолевым и противомикробным лечением, потому что различные антибиотики с активностью как ДНК-алкилирующие агенты (например,g., адриамицин, также называемый доксорубицином, и другие антрациклины, продуцируемые Streptomyces spp.), используются в противоопухолевых режимах [83], а также различные препараты, используемые в химиотерапии рака (например, цисплатин, который до сих пор используется в качестве стандарта лечения раковые заболевания человека, такие как опухоли яичек), также обладают антимикробной активностью [86]. Наиболее вероятно, что наиболее прямая связь между бактериями и раком человека проистекает из того факта, что определенные бактериальные инфекции вызывают рак [87]. Бактерии вызывают канцерогенез посредством двух основных механизмов: (а) индукция хронических воспалительных процессов, приводящих к раку в различных органах человека, или (б) выработка канцерогенных метаболитов, что часто имеет место при раке толстой кишки [87].Возможно, наиболее известным примером рака, вызванного бактериями, является Helicobacter pylori, который вызывает лимфому желудка MALT (лимфоидная ткань, связанная со слизистой оболочкой). Поскольку инфекция H. pylori может распространяться через зараженную пищу или воду и передается через контакт изо рта в рот, она часто передается в детстве и, по оценкам, присутствует более чем у 60% населения мира, причем особенно часто. в развивающихся странах [87]. Длительная инфекция H. pylori в конечном итоге приводит к хроническому воспалению, процессу, который резко изменяет слизистую оболочку желудка и стимулирует пролиферацию регенеративных клеток, а также производство активных форм кислорода (ROS) и активных форм азота (RNOS), что вместе может привести к точечные мутации, делеции и / или транслокации в ДНК клеток-хозяев, запускающие начало канцерогенного процесса [88].Также сообщалось о возможной ассоциации H. pylori с другими типами рака, такими как рак толстой кишки [89], легких [90,91] и поджелудочной железы [90,92]. К счастью, лечение антибиотиками по отдельности или в сочетании с агентами, которые могут предотвратить развитие устойчивости к антибиотикам, может искоренить инфекцию H. pylori и, следовательно, предотвратить развитие рака [93,94,95]. Третья точка сходства между бактериями и рак относится к упомянутой выше роли микробиоты человека как глобального регулятора гомеостаза, с помощью которого она обеспечивает защиту от ряда заболеваний, включая рак.После канцерогенного воздействия хорошо сбалансированная микробиота, с учетом как разнообразия штаммов, так и относительного размера различных бактериальных компонентов, может быть ключевым фактором, определяющим исход проканцерогенного процесса, позволяя или не допуская начало образования опухоли. . В этом сценарии, хотя небольшой процент случаев рака имеет генетический компонент [96], важно учитывать тот факт, что рак является экологическим заболеванием [97,98], и на риск рака, возможно, могут влиять внешние факторы (e .ж., диета, загрязнители, канцерогены или образ жизни), а также внутренние факторы (например, эпигенетическая сигнализация, состав микробиоты, способность к детоксикации или иммунная компетентность). В этом контексте антибиотики — это те соединения, которые могут изменять риск рака из-за их способности действовать как внешние химические канцерогенные факторы окружающей среды (прямое действие) и изменять нормальный баланс микробиоты в сторону более проканцерогенного состава. (непрямое действие). Таким образом, очевидно положительное действие антибиотиков против бактериальных патогенов может быть перевешено возможностью вызвать параллельное увеличение риска рака.Важность этой проблемы подчеркивается (а) чрезмерным воздействием антибиотиков на людей в результате самолечения или обмена рецептами с друзьями или родственниками во многих сообществах, регионах и странах, где антибиотики можно получить без рецепта [99], а социальная проблема, которую легко решить при соответствующем руководстве [100]; и (b) ошибочными показаниями и несоответствующими схемами дозирования, предписанными врачами и медицинскими учреждениями [101,102] для лечения клинических случаев, даже не связанных с бактериальными инфекциями, во многих случаях просто для удовлетворения требований пациентов, чтобы им прописали «все», чтобы ощутить что о них должным образом заботятся.В дополнение к этим случаям неосведомленного, ненужного, необоснованного и неадекватного использования антибиотиков, которые все еще заставляют нас сомневаться в безопасности антибиотиков в 21 веке [103,104], больные раком часто подвергаются воздействию антибиотиков в качестве профилактических или терапевтических компонентов их протоколов противоопухолевого лечения. , особенно в послеоперационный период после операции [105,106,107], а также когда пациенты подавлены действием химиотерапевтических препаратов [108,109]. Кроме того, возможно, что либо из-за их собственного прямого канцерогенного действия, либо путем косвенного изменения микробиоты воздействие антибиотиков может изменить реакцию онкологических больных на терапию, снизив ее эффективность, что приведет к появлению вторичного рака, прогрессированию до запущенные стадии, включая метастазирование или рецидив опухоли.Эти два аспекта возможного влияния антибиотиков на риск рака и терапевтические результаты изучались с двух основных точек зрения: эпидемиологический анализ, непосредственно изучающий связь между воздействием антибиотиков и заболеваемостью раком, и оценки возможного влияния непрямого воздействия антибиотиков на микробиота способствует возникновению и развитию рака. Как свидетельствуют публикации за последние 10 лет (рис. 1), результаты исследований последнего типа сообщались и продолжают сообщаться с большей частотой, чем эпидемиологические данные.В следующих разделах будет изучена связь между воздействием антибиотиков и риском рака, а также его влияние на эффективность лечения и результаты для онкологических больных.
3. Антибиотики и риск рака
Как правильно выразили Маккормак и Боффетта в названии одной из своих статей («Образ жизни сегодня, рак завтрашнего дня: тенденции в образе жизни факторов риска развития рака в странах с низким и средним уровнем дохода») [110 ], реальность такова, что именно в тех странах, где не только нерегулируемое потребление антибиотиков происходит чаще, но и где, в отличие от того, что происходит в развитых странах [111], точные данные о заболеваемости раком периодически не обновляются или даже не обновляются. поддерживается вообще.В этой ситуации очень ценны эпидемиологические оценки воздействия антибиотиков и риска рака. В течение последних пятнадцати лет исследования возможных эффектов воздействия антибиотиков на риск рака были сосредоточены в первую очередь на типах рака, более часто встречающихся у людей, и, как правило, были разработаны для включения когорт больных раком и случайно выбранных пациентов, не страдающих раком. В исследованиях, связанных с раком груди, данные свидетельствуют о связи между потреблением антибиотиков и риском рака.Хотя в некоторых исследованиях связь была квалифицирована как слабая [112,113], в других исследованиях сообщалось о явно положительной взаимосвязи с количеством назначенных рецептов и кумулятивным количеством дней приема антибиотиков [114,115]. В то время как в некоторых исследованиях одинаковые модели ассоциации наблюдались со всеми классами протестированных антибиотиков [114,115], лучшая ассоциация была отмечена для разных классов антибиотиков [112,116]. Ситуация в отношении рака легких была неясной, поскольку данные не предоставили достаточных доказательств, чтобы поддержать или опровергнуть возможное канцерогенное действие антибиотиков [117].Информация из исследований колоректального рака (CRC) кажется более убедительной, скорее всего, из-за того, что большее количество исследований публикуется гораздо чаще из-за общей тенденции повышения научного интереса к микробиоте кишечника. Большинство исследований, связанных с CRC, сообщают о связи, даже на стадии аденомы, как со временем, так и с продолжительностью воздействия антибиотиков [118,119,120]. Кроме того, что более важно, некоторые из этих исследований позволили разделить влияние использования антибиотиков на риск рака толстой кишки ирак прямой кишки, поскольку данные неизменно демонстрируют положительную связь между применением антибиотиков и раком толстой кишки, но не было никакой связи или отрицательной корреляции с раком прямой кишки [121, 122, 123]. В более общих исследованиях других видов рака пищеварительной системы (пищевода, желудка, тонкий кишечник, гепатобилиар и поджелудочная железа), были обнаружены положительные ассоциации между определенными классами антибиотиков и определенными типами опухолей, количество которых увеличивалось с увеличением дозы [124, 125]. Положительные ассоциации были обнаружены между использованием пенициллинов и раком пищевода, желудка и поджелудочной железы, с более четкими эффектами доза-реакция у последнего типа [124].Нитроимидазолы и хинолоны показали более скромную связь со всеми исследованными типами пищеварительных опухолей [125]. Исследования немеланомного рака кожи показали, что существует повышенный риск развития рака кожи, связанный с использованием светочувствительных антибиотиков [126,127,128,129,130]. Воздействие антибиотиков, таких как ципрофлоксацин, кетоконазол и сульфаметоксазол, увеличивало риск развития базальноклеточной карциномы (BCC), тогда как использование доксициклина и сульфаметоксазола увеличивало риск плоскоклеточного рака (SCC) [126, 127, 129].Хотя некоторые исследования связывали использование тетрациклина с риском BCC [126,127], также сообщалось, что использование тетрациклина продемонстрировало положительное взаимодействие в отношении одновременного воздействия УФ-света и риска SCC [129]. Также наблюдалась связь между применением моксифлоксацина и повышенным риском развития ПКР в течение первого года после трансплантации легкого [128]. Кроме того, использование математической модели также предсказало и каким-то образом подтвердило, что риск развития рака кожи положительно связан с использованием антибиотиков [130].Наконец, стоит упомянуть два крупных исследования нескольких типов опухолей [131, 132]. В первом [131] исследователи в течение шести лет отслеживали количество случаев рака, диагностированных в выборке из 3 112 624 человек, не имевших в анамнезе онкологических заболеваний, и анализировали эту информацию в отношении моделей использования антибиотиков в исследуемой популяции. . Данные этого исследования показали, что заболеваемость раком увеличивалась с увеличением количества назначений, и что степень связи относительного риска с воздействием антибиотиков варьировалась в зависимости от типа опухоли, наибольшая в опухолях эндокринных желез, за которой в порядке убывания следовали раковые образования простата, грудь, легкое, толстая кишка и яичник [131].Второе исследование с множественными опухолями [132], крупнейшее на сегодняшний день, сообщило о результатах системного обзора около 7,9 миллионов человек, показывающих, что в среднем использование антибиотиков увеличивает риск рака примерно на 18%, хотя эффект варьируется в зависимости от опухоли. тип: увеличение на 30% случаев рака легких, поджелудочной железы и мочеполовой системы; меньшее увеличение риска (6-8%) для CRC, рака желудка и меланомы; и не было обнаружено никакой связи с раком пищевода или шейки матки. Что касается типов антибиотиков, наибольший риск был связан с использованием β-лактамов, цефалоспоринов и фторхинолонов [132].
5. Центральная регулирующая роль микробиоты
Как указывалось выше, в последние десять лет наблюдается чрезвычайный интерес к человеческой микробиоте, в частности, в отношении ее критической способности поддерживать баланс здоровья / болезни на протяжении всей нашей жизни. Теперь ясно, что микробиота играет ряд центральных регулирующих ролей, связанных с экологическими рисками [146], ответом на антибиотики [147], прогрессированием опухоли [148] или ответом на терапию рака [149, 150, 151]. Основные механизмы, с помощью которых дисбаланс микробиоты стимулирует развитие рака, можно разделить на два основных типа: генетические и эпигенетические.Генетические механизмы связаны с индуцированием повреждения ДНК, вмешательством в реакцию на повреждение ДНК и, следовательно, с накоплением и передачей мутаций в ДНК хозяина. Кроме того, дисбиоз микробиоты имеет существенные эпигенетические эффекты, включая изменения глобального метилирования ДНК, ацетилирование гистонов, ремоделирование хроматина и другие эпигенетические аномалии [152]. Дисбаланс микробиоты вызывает некоторые из этих генетических и эпигенетических проканцерогенных эффектов через ферменты, токсины, метаболиты, такие как короткоцепочечные жирные кислоты (SCFA), или другие продукты, либо секретируемые кишечными микробами, либо образующиеся в качестве побочных продуктов в результате их метаболического преобразования пищевых компонентов и другие принятые внутрь ксенобиотики [152].Именно посредством взаимодействия с клеточными рецепторами и каскадами клеточных сигналов секретируемые или метаболические продукты микробного происхождения опосредуют положительный или отрицательный результат микробиоты, модулируя терапевтический ответ больных раком. В качестве мишени для действия антибиотиков [153] весьма вероятно, что различные уровни дисбиоза микробиоты могут усилить негативные эффекты воздействия антибиотиков как на повышение риска рака, так и на снижение эффективности протоколов химиотерапии, иммунотерапии и лучевой терапии.В этом контексте кажется совершенно очевидным, что внедрение в клинику стратегий, которые могут позволить модуляцию микробиоты, может быть ключевым шагом на пути к обеспечению оптимальной биологической основы для облегчения профилактики и лечения рака [154]. Уменьшение заболеваемости раком желудка, достигаемое за счет искоренения H. pylori, является ярким примером противоракового потенциала модуляции микробиоты [155]. Поэтому представляется возможным, что учет состояния их микробиома может улучшить использование противомикробных препаратов, а также результаты лечения онкологических больных [156].Протоколы модуляции микробиоты могут предоставить инструменты для получения прогностической информации о результатах лечения рака [157,158,159].
6. Альтернативные подходы
На основании информации, представленной выше, наиболее актуальной задачей является содействие изменению моделей использования антител [160] как способ снижения не только риска рака, но и повышенного риска для всех. причины смертности, связанные с длительным применением антибиотиков в позднем взрослом возрасте [161], а также возможные риски, передаваемые потомству на разных этапах беременности [162].В качестве альтернативы следует предпринять усилия для выявления или разработки новых антибиотиков, которые могут обладать как антимикробной, так и противоопухолевой активностью [163, 164]. Выбор антибиотиков с противоопухолевой активностью может осуществляться с учетом: (а) их механизма действия, использования таких свойств, как их генотоксичность [165, 166], их потенциал индуцирования апоптоза [167, 168], их способность к блокировать опухолеспецифические сигнальные пути [169], их эпигенетические модулирующие эффекты [170,171] или другие соответствующие молекулярные механизмы [172,173]; и (b) минимально возможное вредное воздействие на микробиоту, как в случае рифаксимина [174, 175], который имеет широкий спектр действия против грамположительных и грамотрицательных бактерий и, на основе его уникальной абсорбционной способности, растворимости и фармакокинетические свойства могут фактически исправить дисбиотический дисбаланс микробиоты [176].Методы модификации микробиоты предоставили очевидную вторую основную альтернативу, которая может быть достигнута путем использования пробиотиков, пребиотиков или симбиотических добавок [177,178] или, точнее, трансплантации фекальной микробиоты (FMT) [179,180]. Доступные в настоящее время методы FMT [181] позволяют обратить вспять дисбиотические процессы микробиоты [182], а также предоставляют, в то же время, новые возможности для улучшенных протоколов лечения рака [183]. Наконец, есть также возможность замены антибиотики для других агентов, которые могут иметь аналогичные преимущества в отношении их антимикробной активности, но не создают побочных проблем, связанных с резистентностью, дисбактериозом микробиоты или снижением ответа на противоопухолевую терапию.Хотя агенты с двойной антимикробной и противоопухолевой активностями были бы идеальными, комбинированное применение монотерапевтических агентов может легко обеспечить тот же эффект. Два типа агентов, которые следует рассматривать в этом классе, — это бактериофаги [184,185,186,187] и энзибиотики [188,189,190,191], которые привлекли значительное внимание в последнее время и могут использоваться в профилактических и терапевтических целях в протоколах противомикробных и противоопухолевых препаратов. Бактериофаги были разработаны для медицинских применений [192] таким образом, чтобы они могли сохранять свою антибактериальную активность [185], и использовались в качестве систем доставки противораковых лекарств [186, 192], их возможное влияние на противоопухолевый иммунитет и ответ на противоопухолевую терапию должны подлежат дальнейшей оценке.То же самое еще более необходимо в отношении ферментов, слабоиммуногенных ферментов бактериофагов или другого природного происхождения, способных очень специфично действовать как противомикробные агенты [187], поскольку наши текущие знания об их потенциальном использовании в противоопухолевых стратегиях крайне ограничены.
7. Выводы и новые перспективы
Взаимодействие между антибиотиками и микробиотой регулирует их соответствующий вклад в канцерогенный процесс (путем модуляции риска рака и возникновения опухоли) и в реакцию больных раком на различные противоопухолевые методы лечения, ведущие к эффективному лечению или прогрессированию опухолей до запущенных, метастатических стадий.Рисунок 2 иллюстрирует это двойное регуляторное взаимодействие. Альтернативы использованию антибиотиков, которые либо не вызывают, либо вызывают лишь незначительные уровни дисбиоза микробиоты, предоставляют потенциально полезные стратегии для удержания канцерогенного процесса под контролем. Однако есть еще один фактор, который необходимо учитывать: микробиом опухоли человека. Тот факт, что бактерии, обнаруженные в опухолях человека, не были результатом заражения, был установлен около 100 лет назад, и только недавно технический прогресс позволил установление сигнатур опухолевого микробиома в отличие от сигнатур, полученных из геномных анализов нормальной микробиоты.Тем не менее, подробное описание микробиоты опухоли не продвигалось быстрыми темпами из-за ограничений, налагаемых очень низкой бактериальной биомассой, присутствующей в опухолях. Несмотря на эту ситуацию, совсем недавно было опубликовано [193] очень захватывающее открытие, демонстрирующее, что разные типы опухолей имеют разные микробиомные сигнатуры, что имеет важное значение с диагностической точки зрения, и, что еще более важно, микробиота опухоли состоит из внутриклеточных бактерий. .Понимание вклада внутриклеточных бактерий, специфичных к типу опухоли, в баланс нормальной микробиоты и эффектов антибиотиков в контексте риска рака и эффективности терапии, безусловно, потребует применения подходов системной биологии [194]. Интересно, что это открытие приносит Мы возвращаемся в мир прокариот, которые выполняют определенные функции, будучи внутриклеточными резидентами, как возможный случай того, что можно было бы назвать «онкологическим симбиозом». Более того, внутриклеточное расположение опухолевой микробиоты связывает ее с некоторыми из самых последних теорий происхождения опухолей [195,196].Одно из этих представлений видит корни этиологии рака в двух переходах (от прокариотических к эукариотическим и от одноклеточных к многоклеточным существам), которые в конечном итоге приводят к появлению высших организмов [195]. Другая, так называемая «Системно-эволюционная теория рака (SETOC)», предполагает, что как следствие длительных травм, вызванных факторами, способствующими развитию рака, рак возникает в результате процесса регрессии эукариотических клеток в сторону ситуация, в которой его прокариотический компонент принимает нескоординированное поведение, что в конечном итоге нарушает интеграцию компонентов эндосимбиотической клеточной системы [196].Будет чрезвычайно интересно посмотреть, играют ли недавно идентифицированные внутриклеточные прокариотические клетки опухолевой микробиоты какую-либо роль в этих предполагаемых регрессионных процессах.
границ | Профилактика низкими дозами антибиотиков вызывает быстрые модификации кишечной микробиоты у младенцев с пузырно-мочеточниковым рефлюксом
Введение
Кишечная микробиота (ГМ) — это индивидуально-специфическое множество микроорганизмов, живущих в желудочно-кишечном тракте в мутуалистических отношениях с хозяином и способствующих его гомеостазу (1, 2).ГМ важен для метаболических, иммунологических и неврологических функций (3).
Установленный вскоре после рождения, GM описывает траекторию развития в младенчестве, достигая почти стабильного взрослого профиля примерно к 3 годам (4, 5). В частности, первые месяцы жизни являются критическим временным окном для созревания ГМ, в течение которого различные факторы могут влиять на его эубиотическое состояние и траекторию, такие как способ доставки, смесь или грудное молоко и, что более важно, прием лекарств (6 –8).Эти изменения могут иметь краткосрочные и долгосрочные последствия для здоровья, что подтверждается обширной литературой (1, 2, 6, 7). В частности, изменения ГМ, вызванные ранним воздействием антибиотиков, были связаны с увеличением веса и последующим развитием астмы, аллергии, экземы, атопии и воспалительного заболевания кишечника (6, 7, 9, 10). Более того, ГМ младенцев, подвергшихся воздействию антибиотиков, может стать важным резервуаром генов устойчивости к антибиотикам, потенциально приводя к опасным для жизни осложнениям (9, 11).
Несмотря на противоречивость, непрерывная антибиотикопрофилактика (ВП), назначаемая в субтерапевтической суточной дозе, в настоящее время считается стандартом лечения младенцев с пузырно-мочеточниковым рефлюксом высокой степени (ПМР) для предотвращения рецидивирующих инфекций мочевыводящих путей (ИМП), почек. рубцевание и хроническое поражение почек (12–14). Кроме того, антибиотикопрофилактика рекомендуется при различных клинических состояниях, и в целом на нее может приходиться до 28,6% назначенных антибиотиков госпитализированным детям (15).
Текущее рандомизированное исследование PREDICT было разработано в контексте спорного соотношения затрат и результатов CAP (EudraCT 2013-000309-21) с целью прояснить эффективность CAP в предотвращении первых симптоматических ИМП у младенцев с высокой степенью ПМР. Планировалось вложенное исследование для оценки траектории GM в течение первых лет жизни, сравнивая пациентов, рандомизированных на ВП или нет.
Здесь мы представляем поперечный анализ образцов стула, взятых у 87 младенцев на этапе предварительного обследования, чтобы оценить влияние воздействия субтерапевтической дозы антибиотиков на состав ГМ у очень маленьких детей.
Методы
Выбор пациентов
Мы провели кросс-секционное исследование, проанализировав состав ГМ и уровни жирных кислот с короткой и разветвленной цепью (SCFAs и BCFAs, соответственно) в кале в когорте пациентов, прошедших скрининг для исследования PREDICT с октября 2014 года по ноябрь 2018 года. В исследование включены младенцы в возрасте <5 месяцев с ПМР высокой степени (III-V), без перенесенных ИМП и с гестационным возрастом ≥ 35 недель, которые рандомизированы для профилактики или нет и наблюдаются в течение 5 лет.Перед рандомизацией мы идентифицировали всех прошедших скрининг пациентов с жизнеспособным образцом стула и доступными данными о воздействии ВП. Отобранные пациенты были разделены на две группы: пациенты без ВП и пациенты без ВП (дополнительный рисунок 1). Использование ВП перед сбором стула было связано только с местной практикой и не мешало последующей рандомизации пациентов. Долгосрочное влияние ВП на траектории ГМ или ИМП не является предметом данного исследования.
Исследование было одобрено экспертным советом всех участвующих центров, и письменное информированное согласие было предоставлено всеми родителями или законными опекунами (этический кодекс одобрения координационного центра: 106/2013 / O / Sper).
Образцы и сбор данных
Для каждого пациента было собрано
образцов стула и немедленно заморожено при -80 ° C без обработки. Образцы были отправлены в сухом льду в Департамент фармации и биотехнологии Болонского университета (Болонья, Италия) для анализа на ГМ и SCFA / BCFA.
Из базы данных исследования PREDICT, данные о пациентах (возраст, пол, ПМР), предыдущей профилактике антибиотиками (агент, доза и продолжительность) и других потенциальных факторах, влияющих на ГМ (способ кормления, способ доставки, гестационный возраст, потребление лекарств и использование пробиотиков).
Экстракция микробной ДНК, подготовка библиотеки и секвенирование
Микробная ДНК была извлечена из фекалий с использованием метода повторного взбивания шариков плюс колонка, как описано ранее (16). Концентрацию и качество ДНК оценивали с помощью NanoDrop ND-100 (NanoDrop Technologies, Wilmington, DE, USA).
Для подготовки библиотеки гипервариабельная область V3-V4 гена 16S рРНК была амплифицирована с использованием праймеров 341F и 785R, как сообщалось ранее (16). Продукты ПЦР очищали с использованием системы очистки на основе магнитных шариков (Agencourt AMPure XP, Beckman Coulter, Бреа, Калифорния, США).ПЦР с ограниченным циклом была проведена для получения индексированной библиотеки с использованием технологии Nextera. Конечные библиотеки секвенировали на платформе Illumina MiSeq с протоколом парных концов 2 x 250 п.н. в соответствии с инструкциями производителя (Illumina, San Diego, CA, USA). Считанные данные секвенирования были депонированы в Национальном центре биотехнологической информации в архиве считывания последовательностей (NCBI SRA; BioProject ID PRJNA706153).
Определение SCFAs и BCFAs в фекалиях с помощью ГХ-МС
Примерно 0.25 г фекалий анализировали на уровни SCFA (уксусная, пропионовая, масляная и валериановая кислоты) и BCFA (изомасляная и изовалериановая кислоты). Подготовка проб выполнялась методом твердофазной микроэкстракции в свободном пространстве (HS-SPME) с последующим анализом методом газовой хроматографии и масс-спектрометрии (GC-MS), как описано ранее (17). Получение хроматограммы было получено в режимах сканирования полного ионного тока (TIC) и мониторинга одиночных ионов (SIM).
Биоинформатика и статистика
Различия между группами в характеристиках пациентов оценивались с помощью критерия хи-квадрат или критерия Вилкоксона, чтобы исключить потенциальные искажающие факторы в анализе GM.
Для GM необработанные последовательности обрабатывали с помощью QIIME 2 (18). Отфильтрованные по длине и качеству чтения были объединены в варианты последовательности ампликона (ASV) с использованием DADA2 (19). Таксономическое отнесение было выполнено с использованием базы данных Greengenes (выпуск от мая 2013 г.). Химеры были отброшены во время анализа. Альфа-разнообразие было рассчитано с использованием количества наблюдаемых ASV и филогенетического разнообразия Фэйт, в то время как бета-разнообразие было оценено путем вычисления расстояний UniFrac, которые использовались в качестве входных данных для анализа главных координат (PCoA).Весь статистический анализ проводился с использованием R (https://www.r-project.org/). Графики PCoA были созданы с использованием пакетов «vegan» и «Made4», а разделение данных было проверено с помощью теста перестановки с отношениями псевдо-F (функция «Adonis» в «веган»). Роды бактерий, которые вносят наибольший вклад в пространство ординации, были идентифицированы с использованием функции «envfit» от «веган». Тест Вилкоксона использовался для оценки значительных различий в альфа-разнообразии, относительной численности таксонов и уровнях SCFA / BCFA между группами.Значение p ≤ 0,05 считалось статистически значимым, а значение p между 0,05 и 0,1 как тренд.
Результаты
Население
Было включено 87 пациентов в возрасте от 1 до 5 месяцев с ПМР III-V степени. Шестьдесят семь (77%) были мужчинами, ни один из них не был обрезан. Все пациенты были европеоидной расы из семи стран Европы (Турция 32, Италия 25, Польша 14, Литва 11, Бельгия 3, Португалия 1, Франция 1). Основные демографические и клинические характеристики приведены в таблице 1.
Таблица 1 . Клиническая характеристика включенных в исследование пациентов.
Что касается воздействия ВП, на момент анализа 51 из 87 пациентов не получали ВП (группа без ВП), в то время как 36 из 87 пациентов принимали ВП (группа ВП). Средняя продолжительность ВП составляла 47 дней (диапазон: 16–140 дней). Использование разных классов антибиотиков в группе CAP было следующим: амоксициллин или амоксициллин + клавулановая кислота 21 (58,3%), триметоприм 7 (19,4%), пероральные цефалоспорины 6 (16.7%) и нитрофурантоин 2 (5,5%).
Сравнение потенциальных смешивающих факторов
Не сообщалось о коротких курсах антибиотиков при острой инфекции. Группы не различались по полу, способам кормления, гестационному возрасту и потреблению пробиотиков (таблица 1). В соответствии с их возрастом от 1 до 5 месяцев, все пациенты находились в стадии развития ГМ созревания, как было недавно установлено (4). Способы родоразрешения различались между группами, с большей долей детей, рожденных посредством кесарева сечения в группе без ВП, чем в группе ВП ( p = 0.001, критерий хи-квадрат). Как упоминалось ранее, все пациенты были европейцами, и все мужчины были необрезанными, независимо от группы.
Микробиота кишечника детей с ВП и без ВП
Секвенирование на основе гена 16S рРНК дало в общей сложности 908 524 считывания высокого качества, в среднем 10 443 ± 2 920 последовательностей на образец, разделенных на 3075 ASV. Никаких различий в альфа-разнообразии между пациентами с ВП и без ВП не наблюдалось ( p ≥ 0,2, критерий Вилкоксона) (рис. 1А). Анализ главных координат (PCoA) межличностных вариаций, основанный на взвешенных расстояниях UniFrac, выявил значительное разделение между группами ( p = 0.015, тест перестановки с отношениями псевдо-F — рис. 1B). Напротив, по невзвешенным показателям UniFrac не было обнаружено никаких существенных различий (дополнительный рисунок 2). Интересно, что не наблюдалось разделения ни по одному из оцениваемых потенциальных факторов, таких как пол, возрастная группа, способ кормления, гестационный возраст, потребление пробиотиков, способ доставки, степень VUR, класс антибиотиков и географическое происхождение (Рисунок 2).
Рисунок 1 . Микробиота кишечника младенцев, подвергшихся воздействию ВП, отделяется от микробиоты детей без ВП. (A) Альфа-разнообразие оценивается в соответствии с филогенетическим разнообразием Фейт и количеством наблюдаемых ASV. Существенных различий обнаружено не было ( p ≥ 0,2, критерий Вилкоксона). (B) Анализ главных координат (PCoA) на основе взвешенных расстояний UniFrac между образцами фекалий. Наблюдалось значительное разделение между группами ( p = 0,015, тест перестановки с отношениями псевдо-F). Эллипсы включают 95% доверительную область, основанную на стандартной ошибке средневзвешенного значения координат выборки.Роды бактерий с наибольшим вкладом в пространство ординации показаны синими стрелками ( p ≤ 0,05, тест пермутационной корреляции, функция «envfit»).
Рисунок 2 . ГМ-дисбиоз у младенцев с ВП не зависит от возможных факторов. Анализ основных координат (PCoA) на основе взвешенных расстояний UniFrac между образцами кала от детей с ВП и без ВП, стратифицированных по полу (мужчины и женщины, A ), возрастной группе (1-5 месяцев, B ), способ кормления (грудное вскармливание vs.смесь против смеси, C ), гестационный возраст (доношенный против недоношенного против переношенного, D ), потребление пробиотиков (да против нет, E ), способ родоразрешения (кесарево сечение против спонтанных родов, F ) степень VUR (степень III по сравнению с IV по сравнению с V, G ), класс антибиотиков (амоксициллин или амоксициллин + клавулановая кислота, триметоприм, пероральные цефалоспорины и нитрофурантоин, H ) и географическое происхождение (итальянский, бельгийский , Французский, литовский, польский, португальский и турецкий, I ).Не было обнаружено значительного разделения ( p ≥ 0,118, тест перестановки с отношениями псевдо-F). Эллипсы включают 95% доверительную область, основанную на стандартной ошибке средневзвешенного значения координат выборки. См. Также рисунок 1.
В ГМ младенцев с ВП и без ВП преобладали типы Actinobacteria, Proteobacteria и Firmicutes. Однако пациенты с ВП были значительно обогащены Bacteroidetes ( p = 0,03, критерий Вилкоксона) (рис. 3A). Хотя структура ГМ на уровне семьи в обеих группах в целом характеризовалась преобладанием Bifidobacteriaceae и Enterobacteriaceae (рис. 3B), выявились значительные различия.В частности, по сравнению с младенцами без ВП у детей, подвергшихся воздействию ВП, было обнаружено значительное обогащение Bacteroidaceae ( p = 0,03) и Enterobacteriaceae ( p = 0,05), а также тенденция к уменьшению доли Bifidobacteriaceae. ( p = 0,09). Как и ожидалось, соотношение Enterobacteriaceae к Bifidobacteriaceae , подтвержденного индекса для измерения здоровья кишечника и устойчивости к микробной колонизации, с более высоким значением, отражающим скомпрометированную экосистему (20), было значительно выше в группе CAP, чем в группе без CAP. группа ( p = 0.05) (Рисунок 3C).
Рисунок 3 . Структура кишечной микробиоты у детей с ВП и без ВП. (A, B) Столбчатые диаграммы, представляющие относительную численность основного типа (A) и семей (B) в ГМ детей с ВП и без ВП. (C, D) Коробчатые диаграммы, показывающие распределение относительной численности бактериальных семейств (C) и родов (D) со значительным различием ( p ≤ 0,05, критерий Вилкоксона; звездочка) или тенденцией (0 .05 < p ≤ 0,1; хэштег) между двумя группами. Учитывались только таксоны с относительной численностью> 0,1% как минимум в двух выборках.
Чтобы идентифицировать роды, ответственные за разделение между младенцами с ВП и без ВП, векторы относительной численности со статистически значимым вкладом были наложены на взвешенное пространство ординации UniFrac на Рисунке 1В ( p ≤ 0,05, функция «envfit») . Bacteroides и неклассифицированные роды Enterobacteriaceae были связаны с ВП, в то время как Bifidobacterium, Haemophilus и Streptococcus были связаны с группой без ВП ( p ≤ 0.05) (Рисунок 3D). Кроме того, профиль GM у пациентов с ВП характеризовался увеличением доли Parabacteroides ( p = 0,05), а также тенденцией к увеличению количества Klebsiella и Prevotella и уменьшению количества Lactobacillus ( p ≤ 0,1) (Рисунок 3D).
Большая часть различий в разнообразии и составе ГМ между детьми с ВП и без ВП сохранялась или имела тенденцию сохраняться даже после исключения пациентов, получавших пробиотики (дополнительный рисунок 3), что еще раз подтверждает, что ГМ-дисбиоз у детей с ВП не зависит от потенциальной помехи. факторы, такие как прием пробиотиков.
Уровни SCFA и BCFA в кале
Уровни кала
SCFA и BCFA были определены у 52/87 младенцев, из которых 29 не получали профилактику, а 23 находились в группе CAP. Не было обнаружено значительных различий между группами в общем количестве SCFA, а также в индивидуальных количествах уксусной, масляной, пропионовой и валериановой кислоты ( p > 0,05). Точно так же общие уровни BCFA и уровни изомасляной и изовалериановой кислоты не различались в зависимости от воздействия CAP ( p > 0.05) (дополнительный рисунок 4).
Обсуждение
Созревание
GM — это тонкий процесс, определяемый различными факторами окружающей среды (21). Первые месяцы жизни — это критическое временное окно, в течение которого общение с GM-хозяином закладывает основы будущего здоровья (8). Растут опасения по поводу влияния антибиотиков на высокодинамичный детский ГМ (7).
Младенцы с ПМР часто получают пролонгированную ВП для предотвращения ИМП, но потенциальные преимущества должны быть сопоставлены с долгосрочными побочными эффектами.
Сравнивая младенцев с ПМР, ранее получавших ВП, и тех, кто ранее не лечился, наше исследование показало изменение состава ГМ даже после короткого (47 дней) воздействия субтерапевтической дозировки антибиотиков. Изменения ГМ включали потерю типичных черт экосистемы эубиотического детского типа с уменьшением пропорций Bifidobacterium , ключевого таксона в младенческом ГМ, который доминирует в экосистеме, по крайней мере, до тех пор, пока не прекратится грудное вскармливание (4). Bifidobacterium spp.действительно способны развиваться на олигосахаридах грудного молока и связаны со многими функциями, способствующими укреплению здоровья, включая развитие иммунной системы (22). Напротив, по сравнению с пациентами без ВП, ГМ новорожденных с ВП был обогащен Bacteroides и Parabacteroides и продемонстрировал тенденцию к увеличению доли Prevotella . Согласно исследованию TEDDY, которое отслеживало траекторию ГМ у 903 детей в возрасте от 3 до 46 месяцев (4), Bacteroides связаны с повышенным разнообразием ГМ и более быстрым созреванием в раннем возрасте, независимо от способа рождения.Аналогично, Prevotella — еще один хорошо известный маркер взрослого ГМ, хотя он связан с переменными хозяина, включая диету и географию (17). Стоит отметить, что три энтеротипоподобных кластера, в которых доминируют Bacteroides, Prevotella и Bifidobacterium , недавно были обнаружены в микробиоте детей школьного возраста и предложены для представления стратифицированных тенденций развития ГМ по направлению к взрослой конфигурации, с энтеротип Bifidobacterium является менее зрелым (23).Поэтому есть соблазн предположить, что воздействие CAP может вызвать неэубиотическое ускоренное созревание ГМ младенца до профиля, подобного взрослому.
Кроме того, ГМ пациентов с ВП был обогащен Enterobacteriaceae , в частности Klebsiella (хотя и с низкой значимостью), хорошо известным клинически значимым нозокомиальным патогеном, связанным с системными инфекциями, включая устойчивые к антибиотикам ИМП (24). Помимо указания на неэффективность профилактики в борьбе с ее распространением, высокие количества Klebsiella в группе ВП могут представлять собой немаловажный фактор риска развития более трудно поддающихся лечению ИМП в этой крайне уязвимой группе населения.
В то время как несколько потенциальных факторов, влияющих на факторы, такие как способ кормления, возраст, пол, степень VUR, класс антибиотиков и географическое происхождение, не различались между группами, большее количество младенцев без ВП подверглось кесареву сечению. Хотя это могло частично смещать наши результаты, особенно в отношении Bacteroides , который иногда обнаруживался обогащенным у младенцев, рожденных вагинально (25), мы не обнаружили значительного влияния способа доставки на состав ГМ, когда мы выполняли суб- анализ согласно всем оцененным вмешивающимся факторам.Точно так же мы не наблюдали значительного разделения в структурах ГМ при приеме пробиотиков и даже исключая пациентов, которые их получали, мы получили те же результаты разнообразия и восстановили основные различающие таксоны (хотя иногда только тенденции из-за уменьшения размера выборки) . Это подтверждает специфическое влияние антибиотиков на дисбактериоз, связанный с ВП.
В предыдущих отчетах анализировалось влияние антибиотиков на ГМ у младенцев, но в других условиях, с менее однородными популяциями.В 2014 году исследование недоношенных детей продемонстрировало снижение разнообразия после 5-7 дней эмпирической антибиотикотерапии ампициллином или гентамицином, что привело к композиционному дисбалансу, например, к увеличению количества Enterobacter (26). В 2016 году Бокулич и его коллеги показали на 43 здоровых младенцах, что пренатальное и послеродовое воздействие антибиотиков разных классов и доз антибиотиков задерживает созревание ГМ и подавляет важные патобионты (8). В исследовании с участием 39 детей в возрасте 0–3 лет было обнаружено меньшее разнообразие и пик генов устойчивости после нескольких курсов (9–15) полной антибактериальной терапии (27).Устойчивые различия ГМ, не предотвращаемые употреблением пробиотиков, были продемонстрированы у 149 новорожденных, получавших перинатальные (пренатальные и / или послеродовые) антибиотики, по сравнению с контрольной группой (28). С другой стороны, Akagawa et al. показали незначительное влияние длительной ВП (до 6 месяцев) на ГМ у 35 пациентов младше 3 лет (29). Однако ВП назначали детям старшего возраста, которые ранее получали лечение антибиотиками от ИМП, что делает любые сравнения с нашими данными бессмысленными.
Наш анализ проливает дополнительный свет на влияние антибиотиков на ГМ у младенцев, показывая, что даже кратковременное воздействие субтерапевтической дозы антибиотиков при отсутствии предшествующих инфекций приводит к обнаруживаемой модификации ГМ в такой деликатный момент для ГМ. созревание.Наблюдаемое отклонение, вероятно, подразумевает нарушение барьерного эффекта, что подтверждается почти значительным увеличением количества Klebsiella . Хотя CAP-ассоциированный дисбиоз не привел к несбалансированному производству SCFA и BCFA, нельзя исключить отсроченный эффект в следующие месяцы / годы жизни, когда создается более ферментативная экосистема. В самом деле, было продемонстрировано, что ранние отклонения от компоновки эубиотических ГМ могут создавать долгосрочные патофизиологические проблемы в результате скомпрометированного диалога ГМ-хозяин, который терпит неудачу в зависимом от ГМ иммунологическом и метаболическом программировании (6, 9).
ГМ-дисбиоз, наблюдаемый после кратковременного воздействия ВП, указывает на потенциально еще более глубокие изменения, которые могут быть вызваны длительными, обычно двухлетними курсами, обычно назначаемыми пациентам с ПМР. Некоторые авторы предполагают, что нарушение ГМ в критическом возрасте способствует увеличению риска таких заболеваний, как астма, ожирение и аллергия (6, 7, 30, 31). Два различных исследования с участием более 23000 детей доказали, что воздействие антибиотиков до 6 месяцев связано с увеличением массы тела в более позднем младенчестве (32, 33).Считается, что эта ассоциация связана с модификациями GM (8). Мышиные модели предоставили четкие доказательства роли ГМ в регуляции роста, метаболизма и накопления жира (9, 34). Кроме того, ГМ-дисбиоз был связан с сердечно-сосудистыми заболеваниями у детей с хроническим заболеванием почек (35). Наконец, давление антибиотиков увеличивает гены лекарственной устойчивости у ГМ-микроорганизмов («резистом») с потенциальным горизонтальным переносом (7).
Исследование имеет некоторые ограничения. Относительно небольшой размер выборки мог недооценивать различия между группами, особенно это касается Klebsiella, Prevotella и Lactobacillus .Тем не менее, количество включенных пациентов сопоставимо с имеющейся литературой, а другие наблюдаемые различия в составе ГМ подтверждаются статистическим анализом. Кроме того, распределение пациентов, рожденных путем кесарева сечения, было несбалансированным, ВП состояла из разных типов антибиотиков, а некоторые пациенты получали пробиотики. Эти факторы (способ рождения, тип антибиотика и использование пробиотиков), как известно, связаны с вариациями ГМ. Тем не менее, соответствующие поданализы не показали значительного влияния на структуру ГМ, как и для всех других рассмотренных потенциальных факторов, что позволяет предположить, что наблюдаемые изменения, вероятно, связаны с профилактикой per se .
С учетом наблюдательного и перекрестного дизайна потребуются дальнейшие проспективные исследования в более крупных когортах, чтобы подтвердить стойкость ГМ-изменений и их влияние на здоровье детей в более позднем возрасте. В связи с этим ожидается, что текущее рандомизированное контролируемое исследование PREDICT, предполагающее проспективный мониторинг траекторий ГМ новорожденных, подвергшихся и не подвергавшихся воздействию ВП, вместе с клинической информацией относительно ожирения, аллергии или инфекций с множественной лекарственной устойчивостью, как ожидается, определит реальное долгосрочное влияние ВП. .
Заявление о доступности данных
Наборы данных, представленные в этом исследовании, можно найти в онлайн-репозиториях. Названия репозитория / репозиториев и номера доступа можно найти ниже: https://www.ncbi.nlm.nih.gov/bioproject/706153, PRJNA706153.
Заявление об этике
Исследование с участием людей было рассмотрено и одобрено Comitato etico Milano Area 2. Письменное информированное согласие на участие в этом исследовании было предоставлено законным опекуном / ближайшими родственниками участников.
Авторские взносы
WM, ST, JF, GM и MC разработали исследование, выполнили анализ образцов, интерпретацию данных, статистический анализ и рисунки, составили первоначальную рукопись, а также рассмотрели и исправили рукопись. FDA, JS и IA выполнили анализ образцов, интерпретацию данных, статистический анализ и рисунки, составили первоначальную рукопись, а также рассмотрели и исправили рукопись. EB, FY, AJ, MP, AZ, FB, DD, DM, GK, CL и KT-J собрали биологические образцы, предоставили клинические данные, проанализировали результаты и внесли свой вклад в интерпретацию.OM и FS внесли свой вклад в интерпретацию данных и критически рассмотрели рукопись. Все авторы участвовали в доработке рукописи и одобрили окончательную версию.
Финансирование
Работа была поддержана Министерством здравоохранения Италии. Номер гранта РФ2016-02363563. Спонсор не принимал участия в разработке и проведении исследования.
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Дополнительные материалы
Дополнительные материалы к этой статье можно найти в Интернете по адресу: https://www.frontiersin.org/articles/10.3389/fped.2021.674716/full#supplementary-material
Дополнительный рисунок 1. Блок-схема проверенного и зарегистрированного населения.
Дополнительный рисунок 2. Анализ основных координат (PCoA), основанный на невзвешенных расстояниях UniFrac между образцами кала от ВП и младенцев без ВП. Не было обнаружено значительного разделения между группами ( p = 0.346, тест перестановки с отношениями псевдо-F). Эллипсы включают 95% доверительную область, основанную на стандартной ошибке средневзвешенного значения координат выборки.
Дополнительный рисунок 3. ГМ-дисбиоз у младенцев с ВП не зависит от приема пробиотиков. (A) Альфа-разнообразие оценивается в соответствии с филогенетическим разнообразием Фейт и количеством наблюдаемых ASV. Существенных различий обнаружено не было ( p ≥ 0,1, критерий Вилкоксона). (B) Анализ главных координат (PCoA) на основе взвешенных расстояний UniFrac между образцами фекалий.Наблюдалось значительное разделение между группами ( p = 0,05, тест перестановки с отношениями псевдо-F). Эллипсы включают 95% доверительную область, основанную на стандартной ошибке средневзвешенного значения координат выборки. Роды бактерий с наибольшим вкладом в пространство ординации показаны синими стрелками ( p ≤ 0,05, тест пермутационной корреляции, функция «envfit»). (C) Коробчатые диаграммы, показывающие распределение относительной численности бактериальных таксонов, которые, как правило, по-разному представлены между двумя группами (0.05 < p ≤ 0,1, критерий Вилкоксона). Учитывались только таксоны с относительной численностью> 0,1% как минимум в двух выборках. Для этого анализа были включены только пациенты, которые не получали пробиотики (т.е. 32 против 43 в группе ВП по сравнению с группой без ВП). См. Также таблицу 1.
Дополнительный рисунок 4. Уровни SCFA и BCFA в кале у младенцев, подвергшихся или не подвергавшихся воздействию ВП. Коробчатые диаграммы, показывающие распределение абсолютных количеств SCFA (уксусная, пропионовая, масляная и валериановая кислоты) и BCFA (изомасляная и изовалериановая кислоты), измеренных в мкмоль / г.Существенных различий обнаружено не было ( p > 0,05, критерий Вилкоксона).
Список литературы
1. Кандела М., Бьяджи Э., Туррони С., Маккаферри С., Фигини П., Бриджиди П. Динамическая эффективность кишечной микробиоты человека. Crit Rev Microbiol. (2015) 41: 165–71. DOI: 10.3109 / 1040841X.2013.813900
PubMed Аннотация | CrossRef Полный текст | Google Scholar
2. Гилберт Дж., Блазер М. Дж., Капорасо Дж. Дж., Янссон Дж., Сьюзан В. Современное понимание микробиома человека. Nat Med. (2020) 24: 392–400. DOI: 10,1038 / нм.4517
CrossRef Полный текст | Google Scholar
3. Туррони С., Бриджиди П., Кавалли А., Кандела М. Трансгеномный метаболизм микробиоты и хозяина, биоактивные молекулы изнутри. J Med Chem. (2018) 61: 47-61. DOI: 10.1021 / acs.jmedchem.7b00244
PubMed Аннотация | CrossRef Полный текст | Google Scholar
4. Стюарт С.Дж., Аджами Н.Дж., О’Брайен Д.Л., Хатчинсон Д.С., Смит Д.П., Вонг М.К. и др. Временное развитие микробиома кишечника в раннем детстве по данным исследования TEDDY. Природа. (2018) 562: 583-8. DOI: 10.1038 / s41586-018-0617-x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
5. Бэкхед Ф., Розвалл Дж., Дальгрен Дж., Ван Дж. Динамика и стабилизация микробиома кишечника человека в течение первого года жизни. Клеточный микроб-хозяин. (2015) 17: 690-703. DOI: 10.1016 / j.chom.2015.04.004
PubMed Аннотация | CrossRef Полный текст | Google Scholar
8. Бокулич Н.А., Чанг Дж., Батталья Т., Хендерсон Н., Джей М., Ли Х и др.Антибиотики, способ родов и диета влияют на созревание микробиома в молодом возрасте. Sci Transl Med. (2016) 8: 343ra82. DOI: 10.1126 / scitranslmed.aad7121
PubMed Аннотация | CrossRef Полный текст | Google Scholar
9. Кокс Л.М., Яманиши С., Сон Дж., Алексеенко А.В., Леунг Дж. М., Чо И. и др. Изменение кишечной микробиоты во время критического периода развития имеет долгосрочные метаболические последствия. Cell. (2014) 158: 705–21. DOI: 10.1016 / j.cell.2014.05.052
PubMed Аннотация | CrossRef Полный текст | Google Scholar
10.Ким DH, Хан К., Ким SW. Влияние антибиотиков на развитие астмы и других аллергических заболеваний у детей и подростков. Allergy, Asthma Immunol Res. (2018) 10: 457–65. DOI: 10.4168 / aair.2018.10.5.457
PubMed Аннотация | CrossRef Полный текст | Google Scholar
11. Гаспаррини А.Дж., Ван Б., Сун Х, Кеннеди Е.А., Эрнандес-Лейва А., Ндао И.М. и др. Устойчивые метагеномные признаки госпитализации в раннем возрасте и лечения антибиотиками в микробиоте и резистоме кишечника младенца. Nat Microbiol. (2019) 4: 2285-97. DOI: 10.1038 / s41564-019-0550-2
PubMed Аннотация | CrossRef Полный текст | Google Scholar
13. Морелло В., Ла Скола С., Альберичи И., Монтини Г. Острый пиелонефрит у детей. Педиатр Нефрол . (2015) 31: 1253-65. DOI: 10.1007 / s00467-015-3168-5
CrossRef Полный текст | Google Scholar
14. Montini G, Tullus K, Hewitt I. Фебрильные инфекции мочевыводящих путей у детей. N Engl J Med. (2011) 365: 239–50.DOI: 10.1056 / NEJMra1007755
CrossRef Полный текст | Google Scholar
15. Hufnagel M, Versporten A, Bielicki J, Drapier N, Sharland M, Goossens H. Высокие показатели назначения противомикробных препаратов для профилактики у детей и новорожденных: результаты исследования устойчивости к антибиотикам и назначения в европейском исследовании точечной распространенности среди детей. J Pediatric Infect Dis Soc. (2019) 8: 143–51. DOI: 10.1093 / jpids / piy019
PubMed Аннотация | CrossRef Полный текст | Google Scholar
16.Д’Амико Ф., Бьяджи Э., Рампелли С., Фиори Дж., Зама Д., Соверини М. и др. Энтеральное питание у педиатрических пациентов, перенесших ТСК кроветворения, способствует восстановлению гомеостаза кишечного микробиома. Питательные вещества. (2019) 11: 2958. DOI: 10.3390 / nu11122958
PubMed Аннотация | CrossRef Полный текст | Google Scholar
17. Шнорр С.Л., Кандела М., Рампелли С., Чентанни М., Консоланди С., Басалья Дж. И др. Микробиом кишечника охотников-собирателей хадза. Nat Commun. (2014) 5: 3654.DOI: 10.1038 / ncomms4654
CrossRef Полный текст
18. Болиен Э., Райдаут Дж. Р., Диллон М. Р., Бокулич Н. А., Абнет СС. Воспроизводимые, интерактивные, масштабируемые и расширяемые данные микробиома с использованием QIIME 2. Nat Biotechnol. (2019) 37: 852–7. DOI: 10.1038 / s41587-019-0209-9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
19. Каллахан Б.Дж., Макмерди П.Дж., Розен М.Дж., Хан А.В., Джонсон А.Дж., Холмс С.П. DADA2: вывод образца с высоким разрешением из данных ампликона иллюминации. Нат. Методы. (2016) 13: 581-3. DOI: 10.1038 / nmeth.3869
PubMed Аннотация | CrossRef Полный текст | Google Scholar
20. Мулевичен А., Д’Амико Ф., Туррони С., Кандела М., Янкаускене А. Дисбиоз кишечной микробиоты, связанный с железодефицитной анемией, у младенцев и детей раннего возраста: пилотное исследование. Acta Microbiol Immunol Hung. (2018) 65: 551–64. DOI: 10.1556 / 030.65.2018.045
PubMed Аннотация | CrossRef Полный текст | Google Scholar
21.Форсгрен М., Изолаури Э., Салминен С., Раутава С. Поздние преждевременные роды имеют прямое и косвенное влияние на развитие кишечной микробиоты младенца в течение первых шести месяцев жизни. Acta Paediatr. (2017) 106: 1103–9. DOI: 10.1111 / apa.13837
PubMed Аннотация | CrossRef Полный текст | Google Scholar
22. Laforest-Lapointe I, Arrieta M. Модели колонизации кишечных микробов в раннем возрасте во время иммунного развития человека: экологическая перспектива. Front Immunol. (2017) 8: 788.DOI: 10.3389 / fimmu.2017.00788
PubMed Аннотация | CrossRef Полный текст | Google Scholar
23. Чжун Х., Пендерс Дж., Ши З., Рен Х., Цай К., Фанг С. и др. Влияние ранних событий и образа жизни на микробиоту кишечника и метаболические фенотипы у детей младшего школьного возраста. Микробиом. (2019) 7: 2. DOI: 10.1186 / s40168-018-0608-z
PubMed Аннотация | CrossRef Полный текст | Google Scholar
24. Холт К.Э., Вертхайм Х., Задокс Р.Н., Бейкер С., Уайтхаус, Калифорния, Дэнс Д.Геномный анализ разнообразия, популяционной структуры, вирулентности и устойчивости к противомикробным препаратам Klebsiella pneumoniae , неотложной угрозы общественному здоровью. Proc Natl Acad Sci USA. (2015) 112: E3574-81. DOI: 10.1073 / pnas.1501049112
PubMed Аннотация | CrossRef Полный текст | Google Scholar
25. Стинсон Л.Ф., Пейн М.С., Килан Дж. А. Критический обзор гипотезы бактериального крещения и влияния кесарева сечения на микробиом младенца. Front Med. (2018) 5: 135. DOI: 10.3389 / fmed.2018.00135
PubMed Аннотация | CrossRef Полный текст | Google Scholar
26. Гринвуд К., Морроу А.Л., Лагомарчино А.Дж., Алтай М., Тафт Д.Х., Ю. З. и др. Раннее эмпирическое применение антибиотиков у недоношенных детей связано с меньшим бактериальным разнообразием и более высоким относительным количеством энтеробактер. J Pediatr. (2014) 165: 23-9. DOI: 10.1016 / j.jpeds.2014.01.010
PubMed Аннотация | CrossRef Полный текст | Google Scholar
27.Яссур М., Ватанен Т., Сильяндер Х., Хямяляйнен А., Херконен Т., Рюханен С.Дж. и др. Естественная история микробиома кишечника младенца и влияние лечения антибиотиками на разнообразие и стабильность бактериальных штаммов. Sci Transl Med. (2016) 8: 343ra81. DOI: 10.1126 / scitranslmed.aad0917
PubMed Аннотация | CrossRef Полный текст | Google Scholar
28. Тапиайнен Т., Койвусаари П., Бринкач Л., Лоренци Х.А., Сало Дж., Ренко М. и др. Влияние интранатальных и послеродовых антибиотиков на микробиом кишечника и появление устойчивости к противомикробным препаратам у младенцев. Научная публикация (2019) 9: 10635. DOI: 10.1038 / s41598-019-46964-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
29. Акагава Ю., Кимата Т., Акагава С., Ямагути Т., Като С., Яманучи С. и др. Влияние долгосрочной профилактики низкими дозами антибиотиков на микробиоту кишечника у детей. J Urol. (2020) 204: 1320-5. DOI: 10.1097 / JU.0000000000001227
PubMed Аннотация | CrossRef Полный текст | Google Scholar
30. Ногацкая А.М., Салазар Н., Арболея С., Суарес М., Фернандес Н., Солис Г. и др.Ранняя микробиота, антибиотики и здоровье. Cell Mol Life Sci. (2018) 75: 83–91. DOI: 10.1007 / s00018-017-2670-2
CrossRef Полный текст | Google Scholar
31. Reinhardt C, Reigstad CS, Bäckhed F. Кишечная микробиота в младенчестве и ее значение для ожирения. Дж Педиатр Гастроэнтерол Нутр . (2009) 48: 249-56. DOI: 10.1097 / MPG.0b013e318183187c
PubMed Аннотация | CrossRef Полный текст | Google Scholar
33. Саари А., Вирта Л. Дж., Санкилампи Ю., Дункель Л., Саксен Х.Воздействие антибиотиков в младенчестве и риск ожирения в первые 24 месяца жизни. Педиатрия. (2015) 135: 617–26. DOI: 10.1542 / peds.2014-3407
PubMed Аннотация | CrossRef Полный текст | Google Scholar
34. Ридаура В.К., Фейт Дж. Дж., Рей Ф. Е., Ченг Дж., Дункан А. Э., Кау А. Л. и др. Микробиота кишечника близнецов, не согласных с ожирением, модулирует метаболизм у мышей. Наука. (2013) 341: 1241214. DOI: 10.1126 / science.1241214
PubMed Аннотация | CrossRef Полный текст | Google Scholar
35.Hsu CN, Lu PC, Hou CY, Tain YL. Нарушения артериального давления, связанные с короткоцепочечными жирными кислотами кишечной микробиоты у детей с врожденными аномалиями почек и мочевыводящих путей. J Clin Med. (2019) 8: 1090. DOI: 10.3390 / jcm8081090
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ранняя сигнатура кишечной микробиоты aGvHD у детей, перенесших аллогенную трансплантацию гемопоэтических клеток по поводу гематологических нарушений | BMC Medical Genomics
Филогенетический состав ГМ на основе гена 16S рРНК был получен путем секвенирования Illumina в общей сложности 78 образцов фекалий, взятых у 26 субъектов, зарегистрированных в четырех итальянских больницах.Было получено в среднем 11325 ± 4480 последовательностей высокого качества на образец. Пятьдесят три образца от 10 субъектов, зарегистрированных в больнице Сант’Орсола-Мальпиги в Болонье, секвенированные в нашем предыдущем исследовании по той же теме [7], также были включены в анализ, получив конечную когорту из 131 образца от 36 пациентов. Клинические характеристики и характеристики трансплантата обобщены в таблице 1. Образцы были сгруппированы как «до» (т. Е. Образцы, взятые перед ТГСК), «приживления» (т. Е. Первый образец, взятый после ТГСК для всех субъектов, приблизительно соответствующий времени приживления кроветворения, в диапазоне от 12 до 28 дней после ТГСК) и «пост» (все другие образцы, взятые после ТГСК) (рис.1).
Таблица 1 Анаграфические и клинические информационные характеристики включенных пациентов
Исследование смешивающих переменных
Анализ главных координат (PCoA), основанный на расстояниях Брея-Кертиса между микробными профилями на уровне рода, не показал разделения между образцами, секвенированными в настоящей работе. и те из нашего предыдущего исследования [7] (тест Адониса, P > 0,05) (дополнительный файл 1: Рисунок S1). Однако, согласно анализу случайного леса, относительная численность некоторых родов бактерий была дискриминационной между исследованиями ( P <0.01, частота ошибок 4,6%), а именно Streptococcus (в среднем 0,7 и 6,2% в исследовании 2015 г. и в настоящем исследовании, соответственно), Erwinia (0 и 6,8%), [Eubacterium] (6,1 и 0,8%). %) и [Ruminococcus] (6,3 и 3,8%). Упомянутые таксоны не были исключены из последующего анализа, но были приняты меры предосторожности при связывании их с другими переменными из-за их возможной связи с различными методами секвенирования, используемыми в двух исследованиях (пиросеквенирование Roche 454 гипервариабельной области V4 гена 16S рРНК в 2015 г. исследование, и Illumina секвенирование гипервариабельных областей V3-V4 гена 16S рРНК в настоящем исследовании).
Согласно анализу случайного леса, профиль ГМ на уровне родов существенно не различает возрастные группы, т. Е. «Младенец» (<2 лет), «педиатр» (2–12 лет) и «подросток» (> 12 лет). лет) (частота ошибок 37%). Анализ PCoA подтвердил перекрытие между образцами из педиатрической и подростковой групп во всех рассмотренных группах образцов (до, приживления и после). Однако разделение образцов, взятых у субъектов в группе «младенец», было выявлено в группах до и после взятия образцов (тест адониса, P = 0.002 и P = 0,006 соответственно) (Дополнительный файл 1: Рисунок S2). Последние результаты подчеркивают потерю и последующее восстановление возрастных характеристик ГМ после ТГСК.
Анализ случайного леса также подтвердил, что больница, в которую набирались пациенты, была важной переменной, влияющей на профиль ГМ на уровне рода, при этом больница Болоньи была более легко различимой (частота ошибок 16%). Анализ PCoA подтвердил влияние центра госпитализации на всю рассматриваемую группу образцов (до, приживления и после) (тест адониса, P = 0.003, P = 0,001 и P = 0,001 соответственно) (Дополнительный файл 1: Рисунок S3). Относительное содержание Enterococcus, Citrobacter, Erwinia , а также неклассифицированных представителей Aerococcaceae и Clostridiales было дискриминационным для образцов, взятых в различных больницах ( P <0,01). Как упоминалось выше, эти таксоны не были исключены из последующего анализа, но были приняты меры предосторожности при связывании их с другими переменными из-за их возможной связи с различными центрами регистрации.Действительно, подробный анализ (дополнительный файл 1: рисунок S4) показал, что OTU, назначенные для Enterococcus , были относительно многочисленны в GM субъектов, зарегистрированных в больницах Павии, Вероны и Рима, по сравнению с больницей Болоньи, особенно в образцах. взяты примерно при приживлении. Все олиготипы, полученные из OTU, присвоенных Enterococcus , показали одинаковый балл идентичности с различными видами Enterococcus (т.е. Enterococcus hirae, Enterococcus faecium, Enterococcus ratti, Enterococcus villorum ), как и ожидалось на основании очень высокого сходства между 16S рРНК. генные последовательности видов, принадлежащих к этому роду [24].Образцы из больниц Вероны и Рима также показали самое высокое относительное содержание Citrobacter (в частности, в образцах, взятых до трансплантации и после приживления) и Erwinia OTU. И Citrobacter , и Erwinia являются членами семейства Enterobacteriaceae. Erwinia обычно не упоминается как компонент ГМ человека. Известно, что секвенирование гена 16S рРНК, хотя оно и эффективно для филогенетической реконструкции на уровне семьи, может быть недостаточно эффективным для филогенетического анализа на уровне рода у Enterobacteriaceae [25], предполагая, что обнаружение высокого процента ОТЕ, относимых к этим родам в некоторых образцах, может указывают на гиперпролиферацию ряда общих кишечных патогенов.Таким образом, был проведен анализ олиготипирования последовательностей, отнесенных к этим родам, и репрезентативные последовательности были повторно назначены с использованием базы данных последовательностей генов NCBI 16S рРНК. Олиготипы, полученные из OTU, присвоенных Citrobacter , показали наивысший балл идентичности одному из трех обычно регистрируемых внутрибольничных патогенов, то есть Citrobacter murliniae, Klebsiella pneumoniae, и Enterobacter cloacae [26,27,28,29]. Ни один из этих видов не был связан с конкретной больницей или одной из трех рассматриваемых временных точек (до, приживления и после).Напротив, большинство олиготипов, полученных из OTU, присвоенных Erwinia , показали наивысший балл идентичности с E. cloacae (72% последовательностей) и меньшую фракцию с K. pneumoniae . В частности, во всех выборках, где был обнаружен высокий процент ОТЕ, назначенных Erwinia (> 10% всей микробиоты, все из больниц Вероны и Рима), олиготипы, отнесенные к E. cloacae , были доминирующими (93% последовательностей в среднем).
Наконец, исследовали возможное влияние основного заболевания на состав ГМ перед ТГСК. Согласно нашим выводам, анализ случайного леса не различал субъектов, страдающих различными гематологическими заболеваниями, на основе состава ГМ до ТГСК (частота ошибок 66,7%).
Анализ изменчивости микробиоты перед ТГСК в отношении развития рТПХ
Анализ PCoA, основанный на относительной численности на уровне рода, не показал разделения между образцами, взятыми перед ТГСК от субъектов, у которых впоследствии либо развился, либо не развился РТПХ (тест adonis, P > 0.05) (рис. 2а). Однако образцы до ТГСК от субъектов, у которых не развился оРТПХ, имели тенденцию демонстрировать более высокую относительную численность ОТЕ, отнесенных к роду Blautia (в основном относящемуся к виду кишечника человека Blautia wexlerae , согласно нашему анализу олиготипирования) по сравнению с испытуемыми. у которых развился оРТПХ любой степени (в среднем 8,7% при оРТПХ I-II степени, 4,0% при оРТПХ I-II степени и 1,4% при оРТПХ II-IV степени кишечника; тест Вилкоксона, P = 0,046) (рис. 2c) . Напротив, у субъектов, у которых развилась более тяжелая форма aGvHD с поражением желудочно-кишечного тракта, было выявлено значительно более высокое относительное количество выделенных Fusobacterium OTU по сравнению с другими образцами (медиана 0% для aGvHD без aGvHD и для aGvHD степени I-II кожи, 0.05% при оРТПХ II-IV степени кишечника; Тест Краскела-Уоллиса, P = 0,01) (рис. 2b), а также более высокая распространенность, то есть процент образцов, в которых ОТЕ, отнесенные к Fusobacterium , были обнаружены выше предела обнаружения (19% в не-aGvHD, 14 % при aGvHD I-II степени и 83% при aGvHD II-IV степени кишечника). На основании анализа олиготипирования и последующего сопоставления с базой данных генов 16S рРНК NCBI все OTU, отнесенные к этому роду, принадлежали к виду Fusobacterium nucleatum .Положительная и отрицательная связь Fusobacterium и Blautia с развитием и локализацией aGvHD была подтверждена анализом случайного леса ( P = 0,006 и P = 0,046, соответственно). Тот же анализ позволил идентифицировать несколько высокодоминирующих родов, которые были обнаружены, даже при очень низкой относительной численности, исключительно в образцах до ТГСК субъектов, у которых не развился РТПХ (т. Е. Leptotrichia и неклассифицированные представители Barnesiellaceae, средняя относительная численность 0.02% только для пациентов без aGvHD, P = 0,035 и P = 0,042 соответственно).
Рис. 2
Изменчивость кишечной микробиоты до ТГСК в связи с развитием оРТПХ. a PCoA на основе расстояний Брея-Кертиса профилей относительной численности на уровне рода в образцах, собранных до ТГСК у пациентов, у которых не развился aGvHD (зеленый), у которых развился aGvHD (I-II степени) только с поражением кожи (золото), и у которых развился желудочно-кишечный aGvHD (II-IV степени) (темно-красный).Образцы обозначены закрашенными кружками. На графике нанесены первый и второй основные компоненты (MDS1 и MDS2), на которые приходится 22,1 и 13,3% дисперсии в наборе данных, соответственно. Распределение прямоугольников и усов относительной численности (%) ОТЕ, отнесенных к родам Fusobacterium ( b ) и Blautia ( c ) в образцах, собранных перед ТГСК у субъектов, у которых не развился aGvHD (зеленый), у которых развился aGvHD (I-II степени) только с поражением кожи (золото), и у которых развился желудочно-кишечный aGvHD (II-IV степени) (темно-красный)
Было обнаружено, что биоразнообразие ГМ до HSCT ниже в кишечнике II-IV степени. aGvHD (индекс Симпсона, среднее ± SD = 0.70 ± 0,28) и группы пациентов aGvHD I-II степени (0,75 ± 0,16) по отношению к тем, у которых не развилось aGvHD (0,79 ± 0,16) (дополнительный файл 1: Рисунок S5), хотя это различие не было статистически значимым. . Что касается межиндивидуальной вариабельности, то разнообразие между образцами до ТГСК, аппроксимированное расчетом расстояний Брея-Кертиса, было выше у субъектов, у которых развивалась кишечная aGvHD (расстояния Брея-Кертиса, среднее ± SD = 0,86 ± 0,15), чем в обоих случаях. Субъекты без РТПХ (0,72 ± 0.15, тест Уилкоксона P = 0,001) и субъектов, у которых развивается aGvHD только кожи более низкой степени тяжести (0,77 ± 0,15, P = 0,02) (дополнительный файл 1: рисунок S6).
Анализ изменчивости микробиоты при приживлении в зависимости от развития aGvHD
Анализ PCoA, основанный на относительной численности на уровне рода, в образцах, собранных при приживлении, показал, что образцы от субъектов, у которых развился aGvHD степени II-IV с поражением желудочно-кишечного тракта, имели тенденцию отделяться от все остальные образцы (тест Адониса, P = 0.049) (рис. 3а). Два образца кишечника aGvHD от двух детей, поступивших в больницу Вероны (код объекта, V2 и V3, рис.1), характеризовались> 80% OTU, отнесенных к роду Erwinia , и повторно отнесенных к олиготипическому анализу и NCBI. База данных генов 16S рРНК для видов E. cloacae , и они были нанесены на график вдали друг от друга. Однако, поскольку OTU, отнесенные к роду Erwinia , были среди тех, которые были перечислены как возможно подверженные влиянию как метода секвенирования, так и больницы, в которую были включены пациенты (дополнительный файл 1: рисунок S4), эти данные могли быть предвзятыми и не исследовались в дальнейшем. .Образцы приживления кишечника у пациентов с aGvHD II-IV степени имели тенденцию демонстрировать более высокую относительную численность Bacteroides (в среднем 0,7% для aGvHD без aGvHD, 0,8% для aGvHD I-II степени и 23,7% для aGvHD II-IV степени кишечника. ; Критерий Краскала-Уоллиса, P = 0,050) (рис. 3б). Согласно нашему олиготипическому анализу, видовой состав Bacteroides показал высокую вариабельность среди людей с различной долей наиболее распространенных видов кишечника человека Bacteroides , таких как Bacteroides ovatus, Bacteroides vulgatus, Bacteroides uniformis, и Bacteroides dorei .Мы не смогли наблюдать никакой связи между обнаружением определенного вида Bacteroides и началом aGvHD II-IV степени кишечника.
Рис. 3
Изменчивость кишечной микробиоты при приживлении в зависимости от развития aGvHD. a PCoA на основе расстояний Брея-Кертиса профилей относительной численности на уровне рода образцов, собранных при приживлении трансплантата у пациентов, у которых не развился aGvHD (зеленый), у которых развился aGvHD (I-II степени) только с поражением кожи (золото) , и у которых развился желудочно-кишечный aGvHD (II-IV степени) (темно-красный).Образцы обозначены закрашенными кружками. Первый и второй главные компоненты (MDS1 и MDS2) нанесены на график, что составляет 26,2 и 10,4% дисперсии в наборе данных, соответственно. Двукратный график средних бактериальных координат, взвешенных по соответствующей относительной численности бактерий на образец, был наложен на график PCoA для двух родов бактерий, вносящих вклад в пространство ординации (стрелки). b Распределение коробок и усов относительной численности (%) OTU, отнесенных к роду Bacteroides , в образцах, собранных до ТГСК у субъектов, у которых не развился aGvHD (зеленый), у которых развился aGvHD (I-II степени) только с вовлечением кожа (золото), и у кого развился желудочно-кишечный aGvHD (II-IV степени) (темно-красный).Log2-кратные изменения основных родов дискриминанта между образцами пре-ТГСК и приживления у субъектов, у которых не развился aGvHD ( c ), у которых развился aGvHD (I-II степени) только с поражением кожи ( d ) и у которых развился желудочно-кишечный aGvHD (II-IV степени) ( e ). Показаны роды, для которых P ≤ 0,05 был получен по крайней мере для одной из трех групп субъектов (см. Дополнительный файл 2: Таблица S1) ( O., Oscillospira; F., Faecalibacterium; [Ru.], [Ruminococcus] ; Ro., Roseburia; L., Lachnospira; Д., Дореа; C., Coprococcus; Bl., Blautia; Bi., Bifidobacterium ). Средние значения отношений log2 представлены в виде столбиков, тогда как точки обозначают отдельные значения, полученные для каждого субъекта, включенного в каждую группу. Закрашенные черные точки и названия бактерий, выделенные жирным шрифтом, используются, когда численность ОТЕ, отнесенных к этому роду, значительно различалась между образцами до ТГСК и приживлением (парный тест Вилкоксона, P <0,05), тогда как пустые кружки используются, когда разница не имеет значения
Сравнение образцов пре-ТГСК и приживления от одних и тех же субъектов показало, что событие ТГСК привело к снижению относительной численности нескольких родов, важных для симбиотических, способствующих укреплению здоровья отношений между ГМ и хозяином, а именно Faecalibacterium, [Ruminococcus], Roseburia, Lachnospira, Dorea, Coprococcus, Blautia (парный тест Вилкоксона, P <0.05) (рис. 3в, г, д). Что касается последующего развития aGvHD, мы обнаружили, что у субъектов, у которых развивается aGvHD II-IV степени кишечника (рис. 3e), изменения, происходящие после HSCT, были менее очевидными, чем у всех других субъектов (рис. 3c и d), и незначительными, это намекает на то, что эти хорошо известные группы полезных для здоровья бактерий уже были относительно менее многочисленными в среднем до ТГСК, даже если сравнение с другими образцами до ТГСК показало значительные различия только для Blautia (рис.2c, Дополнительный файл 2: Таблица S1). Это может быть связано с более высокой вариабельностью до ТГСК у субъектов, у которых развился aGvHD кишечника (дополнительный файл 1: рис. S6), что могло помешать выявлению общих дисбиотических особенностей.
Анализ изменчивости микробиоты> 30 дней после HSCT
Анализ PCoA, основанный на относительной численности на уровне рода, показал отсутствие разделения между образцами, взятыми> 30 дней после HSCT от субъектов, у которых впоследствии либо развился, либо не развился aGvHD (тест adonis, P > 0.05) (Дополнительный файл 1: Рисунок S7). Анализ случайного леса подтвердил отсутствие значительных различий в профиле GM после ТГСК среди пациентов, у которых развивается aGvHD как на коже, так и в кишечнике (частота ошибок 55%).
Ранняя сигнатура кишечной микробиоты aGvHD у детей, перенесших аллогенную трансплантацию гемопоэтических клеток при гематологических нарушениях
TY — JOUR
T1 — Ранняя сигнатура кишечной микробиоты aGvHD у детей, перенесших аллогенную трансплантацию гемопоэтических клеток при гематологических нарушениях 9000 — A
AU — Zama, Daniele
AU — Rampelli, Simone
AU — Turroni, Silvia
AU — Brigidi, Patrizia
AU — Consolandi, Clarissa
AU — Severgnini
AU — Gasperini, Pietro
AU — Merli, Pietro
AU — Decembrino, Nunzia
AU — Zecca, Marco
AU — Cesaro, Simone
AU — Faraci
00040005 — AUlo AU — Locatelli, Franco
AU — Pession, Andrea
AU — Candela, Marco
AU — Masetti, Riccardo
PY — 2019/3/7
Y1 — 2019/3/7
N2 — Предпосылки: Начало острой болезни трансплантат против хозяина (aGvHD) коррелировало с составом кишечной микробиоты (GM), но экспериментально Наблюдений пока немного, в основном с участием групп взрослых пациентов.В текущем сценарии, когда трансплантация фекальной микробиоты использовалась в качестве новаторского терапевтического подхода для лечения стероидорезистентного aGvHD, существует острая необходимость в расширении существующих наблюдательных исследований динамики ГМ при трансплантации гемопоэтических стволовых клеток (HSCT). Целью настоящего исследования является изучение траектории ГМ у 36 педиатрических реципиентов ТГСК в связи с началом оРТПХ. Методы. В исследование были включены тридцать шесть педиатрических пациентов из четырех центров трансплантации, перенесших ТГСК.Стул собирали в трех временных точках: перед ТГСК, во время приживления и> 30 дней после ТГСК. Изменения филогенетической структуры ГМ изучали с помощью секвенирования гена 16S рРНК Illumina и филогенетического отнесения. Результаты. Дети с развивающимся кишечником aGvHD имели дисбиотическую структуру ГМ до того, как произошла ТГСК. Это предполагаемое предрасполагающее к aGvHD состояние экосистемы характеризовалось (i) уменьшенным разнообразием, (ii) более низким содержанием Blautia, (iii) увеличением численности Fusobacterium. Во время приживления структура GM претерпела глубокую перестройку у всех пациентов, но, независимо от возникновения aGvHD и его лечения, она снова приобрела эубиотическую конфигурацию с 30-го дня.Выводы: мы обнаружили специфическую сигнатуру GM перед HSCT, которая может прогнозировать последующее возникновение aGvHD в кишечнике. Наши данные могут открыть путь к основанной на ГМ стратификации риска развития aGvHD у детей, перенесших ТГСК, что потенциально полезно также для выявления пациентов, получающих пользу от профилактической трансплантации фекалий.
AB — Предпосылки: Начало острого заболевания «трансплантат против хозяина» (aGvHD) коррелировало с составом кишечной микробиоты (GM), но экспериментальных наблюдений все еще мало, в основном с участием когорт взрослых пациентов.В текущем сценарии, когда трансплантация фекальной микробиоты использовалась в качестве новаторского терапевтического подхода для лечения стероидорезистентного aGvHD, существует острая необходимость в расширении существующих наблюдательных исследований динамики ГМ при трансплантации гемопоэтических стволовых клеток (HSCT). Целью настоящего исследования является изучение траектории ГМ у 36 педиатрических реципиентов ТГСК в связи с началом оРТПХ. Методы. В исследование были включены тридцать шесть педиатрических пациентов из четырех центров трансплантации, перенесших ТГСК.Стул собирали в трех временных точках: перед ТГСК, во время приживления и> 30 дней после ТГСК. Изменения филогенетической структуры ГМ изучали с помощью секвенирования гена 16S рРНК Illumina и филогенетического отнесения. Результаты. Дети с развивающимся кишечником aGvHD имели дисбиотическую структуру ГМ до того, как произошла ТГСК. Это предполагаемое предрасполагающее к aGvHD состояние экосистемы характеризовалось (i) уменьшенным разнообразием, (ii) более низким содержанием Blautia, (iii) увеличением численности Fusobacterium. Во время приживления структура GM претерпела глубокую перестройку у всех пациентов, но, независимо от возникновения aGvHD и его лечения, она снова приобрела эубиотическую конфигурацию с 30-го дня.Выводы: мы обнаружили специфическую сигнатуру GM перед HSCT, которая может прогнозировать последующее возникновение aGvHD в кишечнике.

 РМЖ 2009.
РМЖ 2009.