что это такое у взрослых и детей, причины, признаки, диагностика и лечение
За этим длинным названием «гепатоспленомегалия» скрывается не конкретное заболевание. Это синдром, сопровождающий несколько патологий. Все они достаточно серьезные и нуждаются в обязательном излечении.
Содержание материала:
Что такое гепатоспленомегалия
Животрепещущий вопрос: если выявлена у детей или у взрослых гепатоспленомегалия – что это такое, чего ожидать. Так названо увеличение печени и селезенки, если это происходит одновременно. Первое именуется гепатомегалией, второе – спленомегалией. Врачи объединяют их в понятие «гепатолиенальный синдром».
Начало болезненных изменений иногда характеризуется большими размерами одного органа: селезенки – при патологиях крови, печени – при повреждении ее тканей. В итоге в процесс вовлекаются оба органа: они снабжаются кровью из единой системы
Чаще всего эта патология встречается у малышей в первые 3 года жизни. Но некоторые заболевания провоцируют его и у взрослых .
Но некоторые заболевания провоцируют его и у взрослых .
Причины развития у взрослого и ребенка
Причины синдрома разнообразны, но почти всегда гепатоспленомегалия – следствие какого-то недуга или порока развития.
Во взрослом возрасте это:
- различные заболевания печени (90 %) – воспаления любой природы, фиброз, когда между гепатоцитами разрастается соединительная ткань, кисты – образование полостей в органе, опухоли;
- заболевания сердца – недостаточность, пороки, воспаление перикарда;
- заражение инфекциями – бруцеллезом, мононуклеозом, малярией;
- болезни кровеносной системы – лейкозы, лимфогранулематоз, выраженная анемия, особенно злокачественная;
- заражение паразитами.
Гепатоспленомегалия у ребенка провоцируется онкологией или внутриутробной инфекцией. У новорожденных гепатолиенальный синдром возникает из-за гемолитической болезни. Часто его причиной в старшем детском возрасте является несбалансированное питание с высоким содержанием жиров.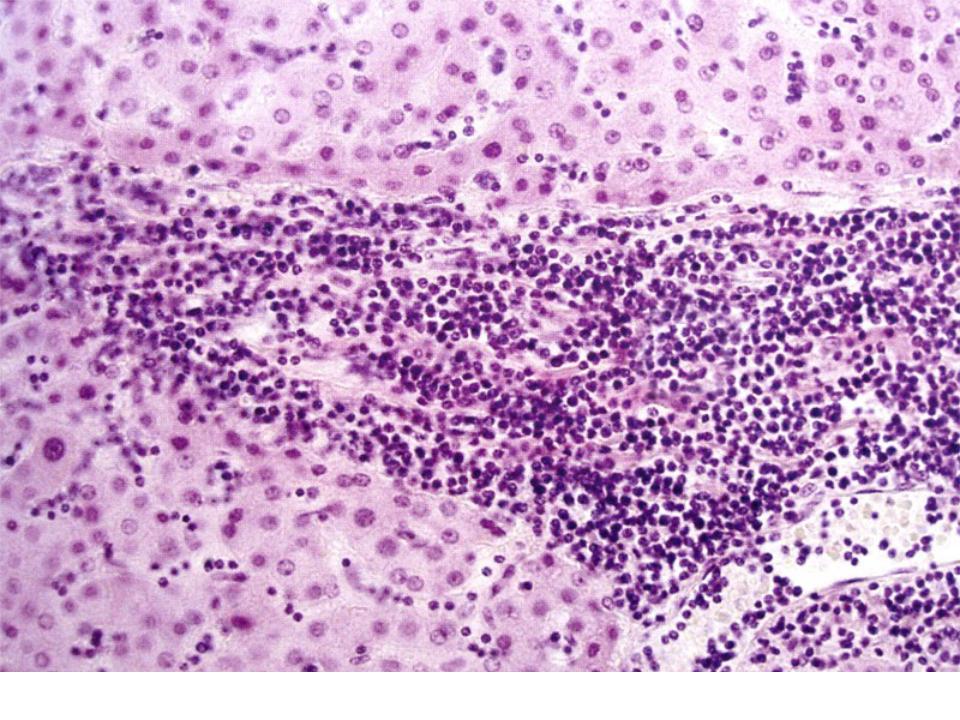
Симптоматика проявления
При изолированной гепатоспленомегалии больной отмечает следующие симптомы:
- тяжесть и распирание под ребрами слева или справа;
- плохое самочувствие;
- горечь во рту;
- тошноту;
- желтуху;
- асцит.
К этому присоединяются и симптомы недуга, ставшего причиной увеличения органов.
Быстро растут размеры печени при онкологии и гепатитах, вызванных вирусами. При пальпации край печени дает сильную боль. Если у пациента диагностирован цирроз или тромб в селезеночной вене, у него быстрее растут размеры селезенки. При таких тромбах частый симптомом – кровотечение из кишечника или желудка.
На заметку! Умеренная гепатоспленомегалия встречается чаще, чем выраженная.
Диагностика
Даже при полном здоровье у людей иногда под ребром пальпируется край печени. Но имеет ровную структуру, острую форму, он эластичный, не дает болезненных ощущений.
При гепатоспленомегалии органы иногда увеличены настолько, что это видно визуально. Часто бывает, что увеличение органов выявляется при профилактическом осмотре. Чтобы определить размеры печени и селезенки, их возможное отклонение от нормы, медики используют пальпацию (прощупывание) и перкуссию (выстукивание). Перкуссия помогает легко различить здоровые, но опущенные органы брюшной полости и патологически увеличенные.
Здоровая печень располагается по краю реберной дуги. Пальпация позволяет лучше определить ее размеры. Сложнее пальпируется здоровая селезенка.
При диагностике с помощью пальпации нужно отличать печень, увеличенную в размерах, от других патологий:
- опухолей в близлежащих органах – это толстая кишка, почка или желчный пузырь;
- гепатоптоза из-за эмфиземы, плеврита или поддиафрагмального абсцесса.
Увеличенную селезенку при пальпации можно спутать с опухолью в почке или поджелудочной железе, либо кистой в ней.
Но просто диагностировать гепатолиенальный синдром недостаточно, нужно выявить причины, его вызвавшие.
Для этого потребуются консультация врача гастроэнтеролога и проведение ряда анализов, исследований:
- общий анализ крови, в котором может обнаружиться гиперспленизм – снижение количества тромбоцитов, лейкоцитов и эритроцитов, а это достоверный признак гепатоспленомегалии;
- увеличенные показатели «печеночных проб» в биохимическом анализе свидетельствуют о поражении гепатоцитов или сердечной патологии;
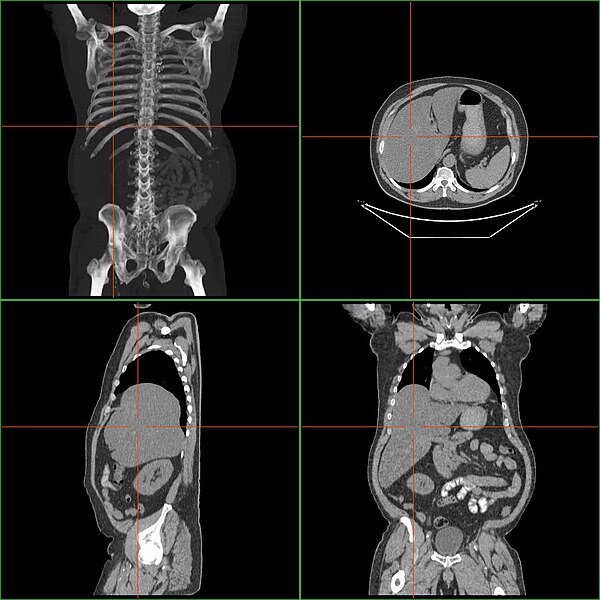
- УЗИ, а при необходимости КТ органов брюшной полости позволяет не только определить то, насколько увеличены печень и селезенка, но и выявить болезненное состояние других органов.
В сомнительных случаях проводят пункцию печени и исследуют полученный пунктат.
Как лечить заболевание
Когда обнаружена изолированная гепатоспленомегалия, а симптомов основного заболевания, ее вызвавшего, нет, первые 3 месяца за больным ведется пассивное наблюдение. Если улучшения нет, требуются госпитализация и углубленное обследование.
Терапию гепатолиенального синдрома проводят комплексно:
- ликвидируют его причину;
- улучшают состояние вовлеченных в патологический процесс селезенки и печени.

Основное заболевание лечат по принятой в каждом конкретном случае схеме.
Для улучшения состояния печени и селезенки при обнаружении вирусной инфекции применяют дезинтоксикационную терапию в дополнении к следующим препаратам:
- желчегонные – для лучшей эвакуации желчи;
- спазмолитики – для снятия спазмов и уменьшения боли;
- гепатопротекторы – восстанавливают гепатоциты и улучшают функцию печени;
- противовоспалительные средства.
При лечении детей учитывают, что гепатолиенальный синдром у них иногда проходит самостоятельно при исчезновении причины, его вызвавшей. В остальном назначают те же препараты, что и для взрослых, но в дозировках, соответствующих возрасту.
Диета при болезнях печени
Поврежденная печеночная ткань не в состоянии вырабатывать достаточное количество желчи, это сказывается на пищеварении. Щадящая диета поможет органам ЖКТ правильно функционировать.
Какие продукты рекомендованы:
- предпочтение отдают кисломолочным продуктам с низкой жирностью, свежее молоко можно добавить в блюдо при приготовлении в небольшом количестве;
- рыба и мясо – постные, в отварном или запеченном виде;
- для каш выбирают крупы из цельного зерна;
- вегетарианские супы на бульоне из овощей;
- свежие, запеченные и отварные овощи, не содержащие раздражающих печень веществ – тыква, кабачки, морковь;
- несладкое желе из фруктов, кисели, печеные яблоки;
- фрукты, не содержащие большое количество кислот.

Из рациона исключают все, что содержит пряности и экстрактивные вещества, красители и консерванты.
Жарить ничего нельзя.
Последствия гепатоспленомегалии
Если выявлено заболевание, вызвавшее гепатолиенальный синдром, его последствия зависят от полного излечения болезни. После этого органы могут вернуться к первоначальному состоянию, но это происходит не всегда. Если изменения в них необратимы, возможно развитие функциональной недостаточности печени или селезенки.
Прогноз и профилактика
Прогноз напрямую зависит от причины, вызвавшей состояние. Развитие гепатоспленомегалии зависит от множества факторов и происходит индивидуально в каждом конкретном случае. Но общим является необходимость обязательного лечения.
Выявленная гепатоспленомегалия – повод для обращения за медицинской помощью и выполнения всех рекомендаций врача.
Гепатоспленомегалия — лечение, причины, признаки, симптомы
Гепатоспленомегалия – это одновременное увеличение параметров селезенки и печени, имеющих общий путь оттока лимфатической жидкости, венозной крови и иннервацию. На самом деле в своей практической деятельности врачи не применяют диагноз «гепатоспленомегалия», так как увеличение метрических параметров печени и селезенки является лишь проявлением основной патологии. Таким образом, целесообразно применять термин «синдром гепатоспленомегалии», включающий целый спектр клинических и патоморфологических признаков.
На самом деле в своей практической деятельности врачи не применяют диагноз «гепатоспленомегалия», так как увеличение метрических параметров печени и селезенки является лишь проявлением основной патологии. Таким образом, целесообразно применять термин «синдром гепатоспленомегалии», включающий целый спектр клинических и патоморфологических признаков.
Причины гепатоспленомегалии
Гепатоспленомегалия у взрослых может провоцироваться различными патологическими изменениями в организме человека и каждое из них относится к одной из основных этиопатогенетических категорий. Первую и основную категорию патологических состояний, приводящих к нарушению оттока венозной крови по неизмененной системе воротной вены, составляют диффузные заболевания печени в виде цирроза, гепатита, жирового гепатоза. Также на процесс венозного кровообращения может оказывать негативное влияние любая кардиальная патология, сопровождающаяся хронической застойной сердечной недостаточностью.
Не так часто встречается инфекционная природа гепатоспленомегалии, однако при наличии инфекционного поражения организма возбудителями малярии, бруцеллеза, лейшманиоза и инфекционного мононуклеоза возрастает риск развития диффузных изменений в паренхиме печени и селезенки, неизбежно провоцирующие увеличение их размеров. Изолированная гепатоспленомегалия печени имеет место при заболеваниях, сопровождающихся метаболическими нарушениями в виде амилоидоза и гемохроматоза.
Изолированная гепатоспленомегалия печени имеет место при заболеваниях, сопровождающихся метаболическими нарушениями в виде амилоидоза и гемохроматоза.
Симптомы и признаки гепатоспленомегалии
Несмотря на все многообразие клинических проявлений гепатоспленомегалии, существует единственный абсолютный диагностический критерий, подтверждающий наличие данного патологического состояния у пациента – значительное или умеренное увеличение параметров селезенки и печени.
Пациенты, страдающие гепатоспленомегалией, чаще всего жалуются на наличие постоянного дискомфорта, тянущие боли в проекции подреберья справа, а также усиление этих болевых ощущений при резкой смене положения тела. Следует учитывать, что умеренная гепатоспленомегалия в большинстве случаев не сопровождается появлением специфических клинических симптомов, и обнаружение факта наличия увеличенных размеров селезенки и печени у пациента приходится на момент инструментального обследования больного (ультразвуковое сканирование брюшной полости, компьютерная томография).
При рассмотрении патогенеза развития гепатоспленомегалии устанавливается закономерность в упорядоченности увеличения размеров печени и селезенки. Практически в 80% случаев у пациента отмечается первичное увеличение размеров печени (в первую очередь левой ее доли), так как основную категорию больных с гепатоспленомегалией составляют лица, страдающие хроническими диффузными изменениями органов гепатобилиарной системы. В этой ситуации развитие гепатоспленомегалии носит вторичный реактивный характер. Единственной ситуацией, при которой отмечается первичное и даже изолированное увеличение параметров селезенки являются имеющиеся у больного системные заболевания крови в виде лейкоза, лимфогранулематоза и гемолитической анемии, так как селезенка относится к главным структурам ретикулоэндотелиальной системы.
В клинической симптоматике гепатоспленомегалии у больных на первый план выступают не симптомы, связанные с увеличением размеров печени и селезенки, а проявления фонового заболевания, являющегося провокатором развития данных изменений. Так, при хронической сердечной недостаточности застойного характера гепатоспленомегалия часто сочетается с асцитом. Наличие свободной жидкости в брюшной полости, кстати, затрудняет проведение инструментального обследования пациента и негативно влияет на определение достоверных размеров селезенки и печени.
Так, при хронической сердечной недостаточности застойного характера гепатоспленомегалия часто сочетается с асцитом. Наличие свободной жидкости в брюшной полости, кстати, затрудняет проведение инструментального обследования пациента и негативно влияет на определение достоверных размеров селезенки и печени.
В ситуации, когда гепатоспленомегалия развивается на фоне диффузного поражения паренхимы печени, клиническая симптоматика зависит от интенсивности холестатического и цитолитического синдромов. Чаще всего в этих случаях у пациентов отмечается выраженный желтушный синдром, а также астеновегетативный симптомокомплекс.
Синдром гепатоспленомегалии, возникающий на фоне имеющейся у больного патологии крови, сопровождается развитием геморрагического симптомокомплекса, главным проявлением которого является повышенная кровоточивость.
Выявление у пациента косвенных признаков гепатоспленомегалии в виде обнаружения увеличения размеров печени при проведении пальпации или перкуссии, наличие визуальных изменений кожных покровов и других клинических проявлений, должно сопровождаться дальнейшим обследованием пациента. Для уточнения этиологии возникновения гепатоспленомегалии наибольшей информативностью обладают лабораторные методы диагностики (биохимический анализ крови с определением показателей функции печени, анализ крови с подсчетом основных кровяных клеток и миелограмма, позволяющие исключить или подтвердить наличие патологии кроветворной системы, определение специфических вирусных и онкологических маркеров в крови).
Для уточнения этиологии возникновения гепатоспленомегалии наибольшей информативностью обладают лабораторные методы диагностики (биохимический анализ крови с определением показателей функции печени, анализ крови с подсчетом основных кровяных клеток и миелограмма, позволяющие исключить или подтвердить наличие патологии кроветворной системы, определение специфических вирусных и онкологических маркеров в крови).
С целью уточнения наличия изменений структуры увеличенных органов целесообразно применять инструментальные методы визуализации. Так, при проведении ультразвукового сканирования удается обнаружить объемные новообразования в увеличенных органах, изменения диффузного характера, а также оценить наличие повреждения общей архитектоники не только печени и селезенки, но и других органов брюшной полости. Для более точного исследования структуры увеличенного органа целесообразно применять лучевые методы визуализации (компьютерная томография). Контрастная ангиография позволяет исследовать причины нарушения венозного кровообращения в печени и селезенке, в частности в системе воротной вены.
В ситуациях, когда после применения инструментальных и лабораторных методов у лечащего врача остаются вопросы и сомнения по поводу природы возникновения гепатоспленомегалии, необходимым является выполнение чрескожной тонкоигольной биопсии увеличенных органов с дальнейшей морфологической верификацией диагноза.
Гепатоспленомегалия у ребенка
Развитие гепатолиенального синдрома в детском возрасте может быть спровоцировано как острой патологией, так и являться проявлением какого-либо хронического заболевания. При обнаружении факта наличия у ребенка увеличенных размеров селезенки и печени большинство врачей затрудняются в выборе правильной тактики ведения данной категории пациентов. Этот факт объясняется недостаточной информированностью лечащих специалистов-педиатров, а также малым количеством научных исследований в этой области. Основную группу риска по развитию гепатоспленомегалии в педиатрии составляют пациенты в возрасте до трех лет, так как в этот период у ребенка отмечается максимальный контакт с инфекционными агентами, которые являются самой частой причиной развития данной патологии.
Для того чтобы оценить увеличены ли печень и селезенка у ребенка, необходимо иметь нормативную базу в отношении нормальных размеров данных органов, но до настоящего времени таких четких нормативных данных не имеется. Среди этиологических факторов, провоцирующих развитие гепатоспленомегалии у детей в период новорожденности и ранний грудной период, чаще всего встречаются различные врожденные аномалии в виде врожденных кист, объемных новообразований, а также врожденного фиброза. На развитие гепатоспленомегалии у детей в меньшей степени оказывает влияние изменения холестатического характера. Частым провокаторами гепатолиенального синдрома в детском возрасте являются иммуноопосредованные заболевания и в этой ситуации первично увеличиваются размеры селезенки, как главной составляющей ретикулоэндотелиальной системы.
Отдельную категорию пациентов в педиатрической практике составляют дети, у которых наблюдается так называемая «реактивная гепатоспленомегалия», развивающаяся остро в качестве макрофагальной реакции в ответ на острые воспалительные процессы, происходящие в организме. В этой ситуации синдром гепатоспленомегалии имеет преходящий характер и самостоятельно нивелируется после устранения воспалительного очага. В случае длительного течения гепатолиенального синдрома, у ребенка формируются необратимые изменения структуры печеночной и селезеночной паренхимы в виде разрастания интерстициального матрикса, что неизбежно провоцирует нарушение основных функций органов.
В этой ситуации синдром гепатоспленомегалии имеет преходящий характер и самостоятельно нивелируется после устранения воспалительного очага. В случае длительного течения гепатолиенального синдрома, у ребенка формируются необратимые изменения структуры печеночной и селезеночной паренхимы в виде разрастания интерстициального матрикса, что неизбежно провоцирует нарушение основных функций органов.
Несмотря на то, что сам по себе факт увеличения печени и селезенки не является угрожающим для жизни ребенка состоянием, обнаружение гепатоспленомегалии является основанием для дальнейшей верификации основной патологии. Уже при первичном рутинном осмотре в арсенале каждого врача есть методики, применяя которые можно определить наличие гепатоспленомегалии у ребенка. Для этого достаточно овладеть правилами проведения пальпационного и перкуссионного обследования брюшной полости пациента. Для уточнения гепатоспленомегалии применения данных методик недостаточно и необходимо использовать инструментальные методы визуализации.
Лечение гепатоспленомегалии
Залогом успешного лечения синдрома гепатоспленомегалии является проведение адекватного курса этиопатогенетической терапии, то есть нормализация метрических параметров печени и селезенки возможна только после устранения причин их возникновения. Так, при гепатоспленомегалии, возникающей на фоне вирусного поражения печени, основополагающим звеном в лечении является применение курса противовирусной терапии, как основы лечения гепатита вирусной этиологии. При застойной сердечной недостаточности, одним из проявлений которой считается гепатоспленомегалия, основополагающее лечение заключается в применении диуретических средств (Фуросемид по 40 мг 1 раз в сутки), лапароцентеза при массивном асците.
Медикаментозное лечение синдрома гепатоспленомегалии заключается в применении средств дезинтоксикационного, глюкокортикостероидного ряда, а также симптоматической терапии. Дезинтоксикационная терапия при гепатоспленомегалии заключается в применении парентерального введения Реополиглюкина в объеме 400 мл или Гемодеза в объеме 300 мл. Лечение основного фонового заболевания, которое спровоцировало развитие гепатоспленомегалии должно дополняться средствами базальной терапии в виде иммуномодуляторов (ингаляционное введение Интерферона, 1 ампулу которого необходимо растворить в 10 мл воды). Следует учитывать, что при аутоиммунной природе гепатоспленомегалии напротив следует применять терапию иммунодепрессантами (пероральный прием Имурана в расчетной дозе 2 мг на 1 кг веса пациента).
Лечение основного фонового заболевания, которое спровоцировало развитие гепатоспленомегалии должно дополняться средствами базальной терапии в виде иммуномодуляторов (ингаляционное введение Интерферона, 1 ампулу которого необходимо растворить в 10 мл воды). Следует учитывать, что при аутоиммунной природе гепатоспленомегалии напротив следует применять терапию иммунодепрессантами (пероральный прием Имурана в расчетной дозе 2 мг на 1 кг веса пациента).
С целью устранения холестатических проявлений у больного, страдающего гепатоспленомегалией, рекомендуется непродолжительное применение средств группы холеспазмолитиков (Но-шпа в суточной дозе 0,08 г), а также желчегонных средств (Холосас по 5 мл 3 раза в сутки), при условии отсутствия конкрементов в просвете желчного пузыря и желчных протоках. В качестве дополнительных средств в лечении синдрома гепатоспленомегалии активно применяется гепатопротекторные средства (Гептрал по 0,8 г в сутки перорально), восстанавливающие архитектонику печени, в сочетании с пробиотическими лекарственными средствами (Лацидофил по 2 капсулы трижды в сутки).
Гепатоспленомегалия – какой врач поможет? При наличии или подозрении на развитие гепатоспленомегалии следует незамедлительно обратиться за консультацией к таким врачам как терапевт, гастроэнтеролог, гематолог и инфекционист.
Информация, представленная в данной статье, предназначена исключительно для ознакомления и не может заменить профессиональную консультацию и квалифицированную медицинскую помощь. При малейшем подозрении о наличии данного заболевания обязательно проконсультируйтесь с врачом!
Внутриутробный метод лечения плода
Гемолитическая болезнь (ГБ) плода и новорожденного (фетальный эритробластоз) – патология, связанная с иммуноконфликтной реакцией между организмами матери и плода, являющаяся одной из причин гибели плода и новорожденного.
По статистическим данным резус-несовместимость встречается в 9,5-13% всех браков, частота гемолитической болезни составляет около 1,5%. Из всех резус-сенсибилизированных женщин у 40-50% плод будет иметь легкую ГБ, или не иметь ее вообще, 25-30% будут иметь ГБ, требующую лечения в раннем неонатальном периоде и только у 20-25% развивается тяжелая анемия, требующая инвазивных методов терапии и досрочного родоразрешения. Для супружеской пары, имеющей в анамнезе потерю плода с тяжелой формой гемолитической болезни, современные методы лечения ГБ, в том числе внутриутробное переливание донорской крови плоду, по сути, являются единственной возможность доносить и родить ребенка.
Для супружеской пары, имеющей в анамнезе потерю плода с тяжелой формой гемолитической болезни, современные методы лечения ГБ, в том числе внутриутробное переливание донорской крови плоду, по сути, являются единственной возможность доносить и родить ребенка.
К сенсибилизации организма к резус-фактору могут вести не только роды. Причиной ее нередко являются самопроизвольное либо искусственное прерывание беременности, переливания крови без учета резус-принадлежности, кровотечения или инвазивные манипуляции во время беременности (в т.ч. инвазивная пренатальная диагностика).
При лечении ГБ любого генеза необходимо решать две основные задачи: недопущение токсических концентраций непрямого билирубина в крови, чтобы избежать поражения ядер головного мозга плода, т.е. ядерной желтухи, приводящей к тяжелой инвалидности, и своевременную коррекцию анемии. На сегодня одним из самых эффективных методов лечения непрямой гипербилирубинэмии, обусловленной ГБ у плода, является внутриутробное переливание (ВУП) крови.
ВУП донорской крови плоду проводится в связи с наличием тяжелой гемолитической болезни (отечной или тяжелой желтушно-анемической формы) у плода. Оценка тяжести гемолитической болезни у плода осуществляется по данным титра антирезусных антител в крови у матери, данным УЗИ (признаками развития тяжелой гемолитической болезни у плода являются: увеличение толщины и объема плаценты, гепатоспленомегалия, кардиомегалия, подкожный отек мягких тканей плода, асцит, двойной контур головки, а также изменения доплерометрических показателей скорости кровотока в средней мозговой артерии, пуповине, маточных артериях).
У таких беременных для диагностики состояния плода в ряде случаев необходимо использование кордоцентеза, который позволяет определить в крови плода группу крови, резус-фактор, гематокрит, гемоглобин, а также исследовать газовый состав и кислотно-основное состояние крови. Это позволяет судить не только о степени тяжести заболевания, но и при необходимости проводить коррекцию анемии у плода при помощи ВУП.
ВУП проводится после 30 недель беременности на базе стационара.
ВУП заключается в пункции полости матки и плодного пузыря иглой через переднюю брюшную стенку под контролем УЗИ и последующей пункции вены пуповины (кордоцентез). С целью обездвиживания плода в вену пуповины вводится миорелаксант (ардуан) и производится переливание рассчитанного, с учетом тяжести анемии и срока беременности, количества донорских эритроцитов и 10% раствора альбумина. Операция проводится под постоянным мониторным контролем за сердечной деятельностью плода (КТГ), который продолжается и в течение 30 минут после процедуры.
Трансфузии крови проводятся с интервалом в 2-3 недели. Между переливаниями крови необходим ежедневный контроль состояния плода (КТГ, доплеровское исследование средней мозговой артерии).
Для снижения частоты младенческой смертности и заболеваемости от гемолитической болезни плода на базе КМГК ГАУЗ ККЦСВМП внедрен метод внутриутробного переливания крови, который позволит оказывать помощь при тяжелых формах гемолитической болезни у плода и является важным этапом развития пренатальной диагностики в Приморском крае.
При появлении у беременной признаков резус-конфликта (изменений на УЗИ, роста титра антител к резус-фактору) для решения вопроса о целесообразности проведения ВУП у плода необходимо направление пациента на прием к акушеру-гинекологу по пренатальной диагностике Краевой медико-генетической консультации ГАУЗ «Краевой клинический центр специализированных методов медицинской помощи » Смирновой Анжелике Юрьевне.
Запись на прием осуществляется по адресу:
г. Владивосток, ул. Уборевича 30/37, телефон регистратуры: (423)242-98-83, 242-84-57.
По вопросам проведения процедуры Вы также можете обращаться к заведующему КМГК ГАУЗ ККЦСВМП Воронину Сергею Владимировичу, тел.: 8 (423)242-84-92.
Симптомы поликистоза почек — причины возникновения, описание болезни, симптомы
Поликистоз почек – наследственное заболевание новорождённых или детей раннего возраста, характеризующееся развитием множественных кист в обеих почках и перипортального фиброза (избыточное количество соединительной ткани). Это серьезное заболевание, требующее немедленного лечения. Поликистоз почек у детей встречается с частотой 1 случай на 250-1000 новорожденных.
Это серьезное заболевание, требующее немедленного лечения. Поликистоз почек у детей встречается с частотой 1 случай на 250-1000 новорожденных.
Выделяют 4 группы: перинатальную, неонатальную, раннего детского возраста и ювенильную.
Причины
- Генетическая предрасположенность.
- Возникновение мутации генов во время эмбрионального развития.
- Воздействие химических и лекарственных веществ (консервантов продуктов, инсектицидов, препаратов лития, цитостатиков и пр.), вирусов (цитомегаловируса и т. д.) на плод.
Симптомы
При перинатальном и неонатальном развитии болезни:
- 90% ткани почек замещается кистами.
- Резкое увеличение почек и объёма живота.
- Прогрессирующая почечная недостаточность.
- Респираторный дистресс-синдром.
У детей в раннем детском и ювенильном возрасте:
- Признаки патологии печени.

- Увеличение размеров почек, печени, гепатоспленомегалия.
- Стойкая высокая артериальная гипертензия.
- Инфекция мочевых путей.
- Почечная недостаточность.
- Анемия, остеодистрофия, отставание ребёнка в росте.
- Печёночный фиброз.
- Эзофагальное и желудочно-кишечное кровотечения.
Причины смерти при поликистозе почек детей — почечная недостаточность или осложнения печёночной недостаточности.
Диагностика поликистоза почек детей основана данных инструментального обследования — УЗИ, сцинтиграфии и КТ почек и печени. Нередко для уточнения печёночной патологии используют пункционную биопсию печени.
Профилактика
При наличии генетической предрасположенности к заболеванию профилактика поликистоза почек не может повлиять на возникновение болезни.
При поликистозе почек питание ребенок должен придерживаться диеты. Это низкосолевое и нежирное питание, употребление цельной здоровой пищи, клетчатки, нежирных молочных продуктов.
Это низкосолевое и нежирное питание, употребление цельной здоровой пищи, клетчатки, нежирных молочных продуктов.
Важен также мониторинг потребления жидкости, чтобы не перегружать почки.
Подробнее о детской урологии в клинике «ЮгМед»
Неходжкинская лимфома почки
Неходжкинские лимфомы представляют собой группы заболеваний, характеризующихся первичным локальным, преимущественно внекостномозговым, опухолевым ростом лимфатической ткани. Особого внимания заслуживают первичные экстранодальные неходжкинские лимфомы. Экстранодальные лимфомы, по данным разных исследователей, составляют 24–48% всех неходжкинских лимфом. Спектр поражения весьма широк: наиболее частая локализация — желудок, кольцо Вальдейера, кожа, крайне редко — почки, плевра, надпочечники и печень. Частота поражения почек составляет около 0,3%. Представляем случай установления диагноза при гистологическом изучении удаленной почки. Недооценка данных истории заболевания, жалоб больного привели к ошибочному диагнозу.
Пациент М. (23 года) ургентно поступил в урологическое отделение ОБМ с направительным диагнозом «Острый паранефрит слева, гепатоспленомегалия, асцит, сепсис». Заболел за 3 дня до поступления, когда через час после еды появились тошнота, рвота. В день госпитализации по месту жительства возникла схваткообразная боль в левой поясничной области. Госпитализирован в терапевтическое отделение по месту жительства. При обследовании выявлено увеличение печени +3 см, увеличение селезенки +1 см, в общем анализе крови — лимфопения (3,6×10×9 л), в анализе мочи — эритроциты 1–3 в поле зрения, соли ураты. По данным ультразвукового исследования (УЗИ) — острый паранефрит, асцит, гепатоспленомегалия. Назначено лечение: аргинин глутамат; метамизол натрий + питофенона гидрохлорид + фенпивериния бромид; физиологический раствор; меглюмина натрия сукцинат + натрия хлорид + калия хлорид + магния хлорида гексагидрат; панкреатин + экстракт желчи + гемицеллюлаза; обезжиренные обогащенные соевые фосфолипиды. Состояние больного не улучшалось, направлен в урологическое отделение областной больницы. Для уточнения диагноза применены основные и дополнительные методы исследования. По результатам УЗИ: эхопризнаки паранефральной гематомы справа. Гепатоспленомегалия.
Состояние больного не улучшалось, направлен в урологическое отделение областной больницы. Для уточнения диагноза применены основные и дополнительные методы исследования. По результатам УЗИ: эхопризнаки паранефральной гематомы справа. Гепатоспленомегалия.
Выявлены КТ-признаки ушиба почки, кровь в паранефральной клетчатке и подкапсульная гематома. Принято решение выполнить диагностическую люмботомию (признаки околопочечной гематомы, паранефрита). В ходе операции выявлено: капсула Герота спаяна с подлежащими тканями, выраженная сеть венозных сосудов. Почку со всех сторон охватывает опухолевидное образование желто-серого цвета, распространяющееся в ворота почки, сосудистую ножку. Выполнена нефрэктомия справа. Результат гистологического исследования: неходжкинская лимфома.
Недооценка жалоб и анамнеза больного (отсутствие указаний на травму), результатов УЗИ, КТ (гепатоспленомегалия), лабораторных данных (лимфопения) не дали возможности правильно установить диагноз.
Иерсиниоз и псевдотуберкулез — Кабинет инфекционных заболеваний — Отделения
Иерсиниоз и псевдотуберкулез – это кишечные сапрозоонозы, вызываемые иерсиниями, характеризующиеся поражением желудочно-кишечного тракта, выраженной токсико-вазарной симптоматикой и наклонностью (наиболее выраженной при псевдотуберкулезе) к генерализованному течению.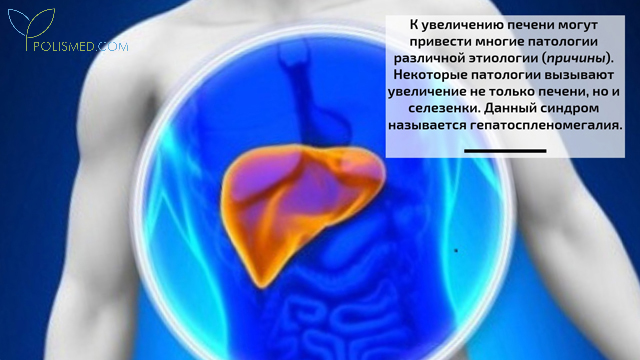 Оба заболевания имеют отчетливо выраженную тенденцию индуцировать развитие иммунопатологии.
Оба заболевания имеют отчетливо выраженную тенденцию индуцировать развитие иммунопатологии.
Этиология
Возбудители иерсиниоза (Y. enterocolitica) и псевдотуберкулеза (Y. pseudotuberculosis) относятся к семейству кишечных бактерий. Иерсинии представляют собой грамотрицательные палочки, которые растут как на обычных, так и на обедненных питательными веществами средах. Последние используются при бактериологическом исследовании по методу Петерсона и Кука (1963).
Иерсинии содержат О- и Н-антигены. Различия в строении 0-антигенов позволили выделить более 50 сероваров Y. enterocolitica. Наибольшее значение в патологии человека имеют серовары 03; 05,27; 07,8 и 09. У возбудителя псевдотуберкулеза — установлено наличие 8 сероваров. Наиболее часто заболевания у людей вызываются 1-м сероваром.
Многие штаммы иерсиний продуцируют экзотоксин (термостабильный энтеротоксин). При разрушении бактерий выделяется эндотоксин. Иерсинии обладают также способностью кадгезии, инвазии и внутриклеточному размножению. Инвазивные свойства у Y. pseudotuberculosis выражены в большей степени, чем у Y. entero-colitica.
Инвазивные свойства у Y. pseudotuberculosis выражены в большей степени, чем у Y. entero-colitica.
Иерсинии относятся к психрофилам. При температуре холодильника (4-8 °С) они способны длительно сохраняться и размножаться на овощах, корнеплодах и других пищевых продуктах. В то же время, некоторые из штаммов бактерий обладают повышенной термоустойчивостью к высокой температуре и способны выдержать режим пастеризации. При кипячении (100°С) все штаммы иерсиний погибают через несколько секунд. Чувствительны к действию обычных дезинфектантов.
Эпидемиология
Иерсинии (Y. enterocolitica и Y. pseudotuberculosis) широко распространены в природе. Их обнаруживали в почве, воде, выделяли из организма многих видов животных. Однако основным резервуаром возбудителя в природе, очевидно, являются мелкие грызуны, которые, обсеменяя различные объекты внешней среды, пищевые продукты, воду, способствуют распространению инфекции среди других животных. Другим резервуаром иерсиний является почва. Частое обнаружение в ней возбудителей болезней связано не только с загрязнением испражнениями животных, но и с наличием у иерсиний сапрофитических свойств. На основании этого заболевание может быть отнесено к сапрозоонозам.
Частое обнаружение в ней возбудителей болезней связано не только с загрязнением испражнениями животных, но и с наличием у иерсиний сапрофитических свойств. На основании этого заболевание может быть отнесено к сапрозоонозам.
Основным источником инфекции для человека при иерсиниозе являются сельскохозяйственные животные, реже – синантропные грызуны. Больной человек как источник инфекции имеет несравненно меньшее значение. При псевдотуберкулезе основными источниками инфекции являются синантропные и дикие грызуны. Человек, как правило, источником псевдотуберкулеза не является.
Основной путь распространения обеих инфекций – пищевой. Факторами передачи Y. enterocolitica чаще всего являются инфицированные мясные продукты, молоко, овощи, корнеплоды, вода. К факторам передачи Y. pseudotuberculosis относятся овощные блюда (салаты из капусты, моркови и др.) и молочные продукты, употребляемые в пищу без предварительной термической обработки. Водный путь передачи имеет при обеих инфекциях несравненно меньшее значение. Он обычно реализуется при употреблении воды из открытых водоемов. Другие пути передачи не имеют существенного значения в эпидемиологии иерсиниозов.
Он обычно реализуется при употреблении воды из открытых водоемов. Другие пути передачи не имеют существенного значения в эпидемиологии иерсиниозов.
Заболевание встречается во всех возрастных группах, но чаще у детей первых лет жизни. Сезонный подъем заболеваемости иерсиниозом отмечается в холодное время года с пиком в ноябре. В некоторых регионах наблюдается два сезонных подъема — осенью и весной. Пик заболеваемости псевдотуберкулезом приходится на весенние месяцы (март-май). Иерсиниоз и псевдотуберкулез протекают в виде спорадических и групповых заболеваний.
Патогенез
Входными воротами для возбудителей иерсиниоза и псевдотуберкулеза служит желудочно-кишечный тракт. Максимально выраженная местная реакция в ответ на инвазию иерсиний регистрируется со стороны слизистой оболочки подвздошной кишки и ее лимфоидных образований. В подвздошной кишке развивается различной выраженности воспалительный процесс – терминальный илеит. По лимфатическим сосудам иерсиний проникают в мезентериальные лимфатические узлы и вызывают мезаденит. В патологический процесс могут быть вовлечены червеобразный отросток и слепая кишка.
В патологический процесс могут быть вовлечены червеобразный отросток и слепая кишка.
На фоне инфекционно-воспалительных изменений развиваются токсический и токсико-вазарный (парез вазамоторов) процессы, связанные с токсинемией. На этом этапе инфекционный процесс, приобретая черты локализованной формы, может завершиться.
В случае прорыва лимфатического барьера кишечника, возникает бактериемия, обусловливающая развитие генерализованных форм заболевания. Наблюдается бактериально-токсическое поражение многих органов и систем, в первую очередь печени и селезенки, возможно развитие полилимфаденита, полиартрита, миозита, нефрита, уретрита, менингита и др.
При длительном нахождении иерсиний и их токсинов в крови и органах больного происходит сенсибилизация организма. У части больных, как правило, с фенотипом HLA-B27, иерсиниоз и псевдотуберкулез могут явиться толчком к возникновению иммунопатологических реакций и состояний.
Заключительное звено патогенеза – освобождение организма от возбудителя, ведущее к выздоровлению.
Развитие специфического иммунитета при иерсиниозе и псевдотуберкулезе происходит медленно и он не является достаточно прочным, с чем связано нередкое развитие обострений и рецидивов болезни.
Клиника
Продолжительность инкубационного периода при иерсиниозе колеблется от 1 до 7 дней, а псевдотуберкулезе – от 3 до 21 дня.
На основе общих патогенетических закономерностей кишечных зоонозов и клинико-патогенетических особенностей иерсиниоза и псевдотуберкулеза могут быть выделены локализованная (гастро-интестиномезентериальная) и генерал и зеванная формы. Они могут иметьманифестноеили (реже) бессимптомное течение.
Локализованная (гастроинтестиномезентериальная) форма манифестного течения включает следующие варианты: гастроэнтеро-колит, гастроэнтерит, энтероколит, энтерит, острый терминальный илеит, мезаденит, аппендицит. Бессимптомное течение локализованной (гастроинтестиномезентериальной) формы включает субклинический и реконвалесцентный варианты. Последний не характерен для псевдотуберкулеза.
Последний не характерен для псевдотуберкулеза.
Генерализованная форма манифестного течения может иметь две разновидности: токсикобактериемическая и септическая. В зависимости от преобладания той или иной симптоматики токсикобактериемическая разновидность генерализованной формы может протекать в следующих вариантах: экзантематозном, артритическом, желтушном (иерсиниозный гепатит), менингеальном, катаральном, смешанном и в виде иерсиниоза (псевдотуберкулеза) редких локализаций. В редких случаях (например, у иммунокомпрометированных лиц с хронической патологией печени и признаками тезауризмоза железа) развивается иерсиниозный сепсис. Бессимптомное течение при генерализованной форме может быть представлено реконвалесцентным вариантом. Последний обычно не характерен для псевдотуберкулеза.
По тяжести манифестного течения заболевания выделяют легкое, среднетяжелое и тяжелое течение. По характеру течения — гладкое и осложненное, в том числе с обострениями и рецидивами. По продолжительности заболевания и его исходам – острое (до 3 мес. ), хроническое (более 3 мес.) и клиника последствий (резидуальная фаза).
), хроническое (более 3 мес.) и клиника последствий (резидуальная фаза).
Локализованная (застроинтестиномезентериальная) форма встречается в 70% случаев иерсиниоза и почти 30% псевдотуберкулеза. Наиболее частыми проявлениями данной формы являются гастроэнтероколитический, гастроэнтеритический, энтероколитический и энтеритический варианты течения болезни. Они регистрируются во всех возрастных группах, но в основном у детей в возрасте до 10 лет.
Клиническая картина указанных вариантов характеризуется наличием интоксикационного синдрома и симптомов поражения желудочно-кишечного тракта на том или ином его уровне. Заболевание начинается остро: возникают озноб, повышение температуры тела до 38-38,5°С. Больных беспокоит головная боль, слабость, миалгии и артралгии. Одновременно с интоксикационным синдромом возникают тошнота, у части больных — рвота, боли в животе, которые носят схваткообразный или постоянный характер. Локализация болей – в эпигастрии, вокруг пупка, в правой подвздошной области, иногда в правом подреберье. Стул жидкий, вязкий, с резким запахом. У некоторых больных при вовлечении в патологический процесс толстой кишки в стуле обнаруживают примесь слизи, реже крови. Частота стула от 2-3 до 15 раз в сутки. Продолжительность заболевания от 2 до 15 сут. Наряду с доброкачественным течением встречаются тяжелые формы болезни с резко выраженной интоксикацией, обезвоживанием организма.
Локализация болей – в эпигастрии, вокруг пупка, в правой подвздошной области, иногда в правом подреберье. Стул жидкий, вязкий, с резким запахом. У некоторых больных при вовлечении в патологический процесс толстой кишки в стуле обнаруживают примесь слизи, реже крови. Частота стула от 2-3 до 15 раз в сутки. Продолжительность заболевания от 2 до 15 сут. Наряду с доброкачественным течением встречаются тяжелые формы болезни с резко выраженной интоксикацией, обезвоживанием организма.
Острый терминальный илеит сопровождается повышением температуры тела до 38-39°С, интенсивными болями в илеоцекальной области и диареей. Больные, как правило, описывают два вида болей: постоянного и на их фоне – схваткообразного типов. При рентгенологическом исследовании пораженная часть подвздошной кишки резко сужена и имеет сглаженный рельеф слизистой оболочки («симптом шнура»). Терминальный илеит имеет длительное и нередко осложненное течение. Среди возможных осложнений: инфарцирование и некроз слизистой оболочки с последующим ограниченным или (редко) разлитым перитонитом, спаечный процессе развитием кишечной непроходимости и др.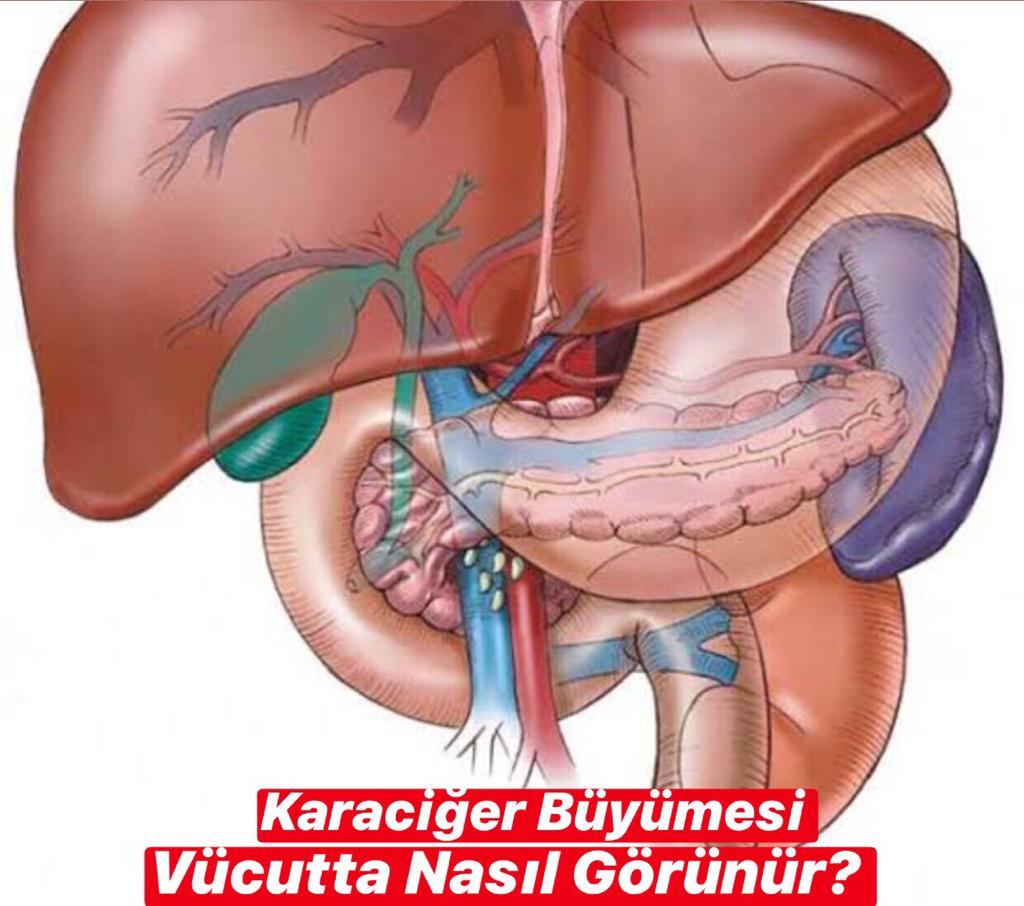 Возможно развитие клиники последствий в виде хронического гранулематозно-язвенного поражения подвздошной кишки, морфологически не отличимого от болезни Крона.
Возможно развитие клиники последствий в виде хронического гранулематозно-язвенного поражения подвздошной кишки, морфологически не отличимого от болезни Крона.
Острый мезаденит характеризуется умеренно выраженной интоксикацией, субфебрильной температурой, меньшей, чем при терминальном илеите силой схваткообразных и постоянного типа болей. В дебюте заболевания может иметь место тошнота, рвота, жидкий стул до 3-5 раз за сутки. В дальнейшем у значительной части больных наблюдается развитие (за 4-6 дней) «инфильтрата» в илеоцекальной области, представляющего собой группу увеличенных мезентериальных узлов, и перитонеальной симптоматики. Выявляют положительные симптомы Мак-Фаддена, Клейна, Падалки, «перекрестный» симптом Штернберга. Течение острого мезаденита нередко сопровождается обострениями и рецидивами. Возможен переход заболевания в затяжное и хроническое течение. Часть больных подвергаются оперативному вмешательству.
Острый иерсиниозный (псевдотуберкулезный) аппендицит в отличие от вульгарного имеет более медленный темп развития от катаральной до деструктивной форм. Как следствие этого – большая частота обнаружения катарально измененного червеобразного отростка в ходе оперативного вмешательства, чем при вульгарном аппендиците. Однако и этот вариант не отличается гладким течением. Нередко после хирургического вмешательства развиваются признаки генерализации: высокая лихорадка, полилимфаденит, гепатоспленомегалия, экзантема.
Как следствие этого – большая частота обнаружения катарально измененного червеобразного отростка в ходе оперативного вмешательства, чем при вульгарном аппендиците. Однако и этот вариант не отличается гладким течением. Нередко после хирургического вмешательства развиваются признаки генерализации: высокая лихорадка, полилимфаденит, гепатоспленомегалия, экзантема.
Всем вариантам локализованной формы свойственна не только абдоминальная (желудочно-кишечная), но и внеабдоминальная симптоматика, обусловленная действием токсина и избыточной продукцией простагландинов на вазомоторы и эндотелий сосудов: инъекция сосудов склер и гиперемия конъюнктив, «малиновый» язык, гиперемия мягкого неба, артралгии, миалгии и др.
В периферической крови наблюдается лейкоцитоз, нейтрофилез, палочкоядерный сдвиг, увеличение СОЭ, иногда эозинофилия.
Генерализованная форма встречается примерно в 30% случаев манифестного течения иерсиниозаи 70% случаев псевдотуберкулеза. Она имеет две разновидности течения :токсикобактериемическая и септическая. Как при иерсиниозе, так и при псевдотуберкулезе обычно наблюдается токсикобактериемическое течение генерализованной формы. Септическое течение при обоих заболеваниях встречается крайне редко.
Как при иерсиниозе, так и при псевдотуберкулезе обычно наблюдается токсикобактериемическое течение генерализованной формы. Септическое течение при обоих заболеваниях встречается крайне редко.
Токсикобактериемическое течение генерализованной формы наиболее хорошо изучено при экзантем атозном варианте псевдотуберкулеза, описанном ранее как дальневосточная скарлати неподобная лихорадка. Заболевание характеризуется острым началом. Больные жалуются на озноб, головную боль, миалгии и артралгии. Температура тела повышается до 38-40°С и держится на этом уровне в течение 5-7 сут, а при тяжелой форме и дольше. В первые дни болезни отмечаются тошнота, иногда рвота, жидкий стул, боли в животе. Нередко наблюдаются катаральные симптомы со стороны верхних дыхательных путей: першениеи умеренные боли при глотании, покашливание, насморк.
При объективном обследовании в 1-ю неделю заболевания кожа больных сухая, горячая, лицо одутловатое. Отмечается гиперемия конъюнктив, инъекция сосудов склер. Нередко, особенно у детей, определяется бледный носогубный треугольник. Слизистая оболочка ротоглотки диффузно гиперемирована. У части больных на мягком небе обнаруживается точечная энантема. К числу кардинальных признаков этого заболевания относятся точечная скарлатиноподобная экзантема в сочетании с симптомами «капюшона» (гиперемия лица и шеи), «перчаток» и «носков» (ограниченная гиперемия кистей и стоп). Эти кардинальные симптомы появляются чаще всего на 2-4-й день болезни. Продолжительность существования сыпи – 1-7 дней. После ее исчезновения, со 2-й недели болезни, у большинства больных появляется отрубевидное шелушение кожи туловища, лица и шеи и пластинчатое (листовидное) – кожи ладоней и стоп.
Нередко, особенно у детей, определяется бледный носогубный треугольник. Слизистая оболочка ротоглотки диффузно гиперемирована. У части больных на мягком небе обнаруживается точечная энантема. К числу кардинальных признаков этого заболевания относятся точечная скарлатиноподобная экзантема в сочетании с симптомами «капюшона» (гиперемия лица и шеи), «перчаток» и «носков» (ограниченная гиперемия кистей и стоп). Эти кардинальные симптомы появляются чаще всего на 2-4-й день болезни. Продолжительность существования сыпи – 1-7 дней. После ее исчезновения, со 2-й недели болезни, у большинства больных появляется отрубевидное шелушение кожи туловища, лица и шеи и пластинчатое (листовидное) – кожи ладоней и стоп.
Следует заметить, что подобный тип экзантемы практически не встречается при иерсиниозе. Для него более характерна мелкопятнистая сыпь на симметричных участках кожи туловища и/или конечностей, которая исчезает в срок от нескольких часов до 3-4 сут.
При пальпации находят умеренно увеличенные и болезненные периферические лимфоузлы.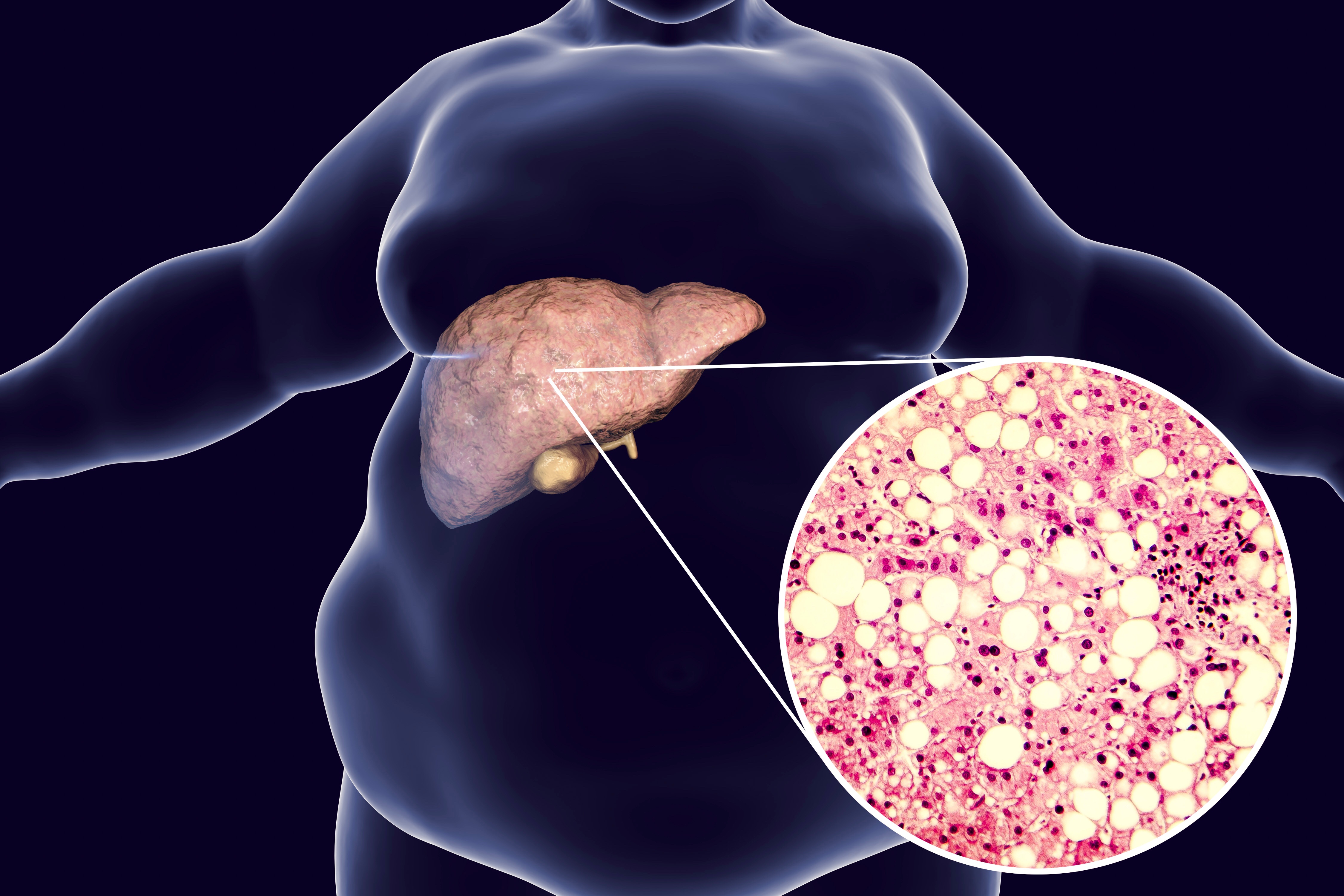 Определяются лабильность и учащение пульса, соответствующее температуре тела. Артериальное давление несколько снижено.
Определяются лабильность и учащение пульса, соответствующее температуре тела. Артериальное давление несколько снижено.
Органы пищеварительной системы закономерно вовлекаются в патологический процесс. Язык, обложенный в первые дни болезни белым налетом, часто к 5-7-му дню очищается и становится «малиновым». При пальпации живота отмечают болезненность и урчание в илеоцекальной области, с меньшим постоянством в эпи- и мезогастрии. Выявляются положительные симптомы Падалки, «перекрестный» Штернберга. У больных с пониженным питанием можно прощупать увеличенные и болезненные мезентериальные лимфатические узлы. Обычно в патологический процесс вовлекается печень. Она увеличивается, становится доступной для пальпации к концу 1-й недели заболевания. У некоторых больных поражение паренхимы печени приводит к появлению иктеричности склер и кожи, гипербилирубинемии, уробилин- и билирубинурии, умеренно выраженной гипертрансаминаземии.
В части случаев имеет место спленомегалия. В периферической крови – нейтрофильный лейкоцитоз Ю-ЗОхЮ^л, палочкоядерный сдвиг, иногда эозинофилия, увеличение СОЭ до 25-50 мм/ч.
Заболевание нередко сопровождается развитием признаков инфекционно-токсического интерстициального нефрита. В некоторых случаях тяжелого течения болезни наблюдаются признаки серозного менингита.
У части больных 2-я и 3-я недели болезни характеризуются появлением симптомов, свидетельствующих об иммунопатологической перестройке. В это тпериод нередко появляются уртикарные, макулезные и макулопапулезные высыпания с локализацией на туловище и конечностях, чаще в области крупных суставов. Возникает узловатая эритема. У некоторых больных развивается реактивный полиартрит, болезнь Рейтера.
Иногда в этот период заболевания выявляют миокардит, нефрит, уретрит, цистит, конъюнктивит, иридоциклит и другие поражения внутренних органов.
По преобладанию той или иной симптоматики в пределахтокси-кобактериемического течения генерализованной формы заболевания выделяют следующие варианты: экзантематозный, артритический, желтушный (иерсиниозный/псевдотуберкулезный гепатит), менингеальный, катаральный и иерсиниоз (псевдотуберкулез) редких локализаций.
Обострения и рецидивы часто осложняют течение иерсиниоза и псевдотуберкулеза. Они встречаются у 1/ больных и характеризуются повторной волной лихорадки и симптомами локальных поражений.
В период реконвалесценции температура тела снижается до нормальной, симптомы интоксикации исчезают, нормализуются функции внутренних органов.
Тяжесть течения иерсиниоза и псевдотуберкулеза определяется выраженностью интоксикационного синдрома и степенью вовлечения в патологический процесс внутренних органов. Чаще заболевание протекает в легкой и среднетяжелой формах.
Септическое течение генерализованной формы иерсиниоза и псевдотуберкулеза встречается очень редко. Оно, как правило, развивается при выраженном иммунодефиците, у лиц с хронической патологией печени и признаками тезауризмоза железа. Течение заболевания характеризуется тяжелой интоксикацией, микроабсцедированием внутренних органов, гепатоспленомегалией, нередко диареей, длительным рецидивирующим течением и, несмотря на лечение, высокой летальностью.
При всех формах манифестного течения иерсиниозной инфекции продолжительность заболевания обычно не превышает 1,5 мес. Однако иногда встречается затяжное течение болезни (от 1,5 до 3 мес) и в редких случаях хроническое (более 3 мес). Наличие заболевания, этиологически связанного с перенесенным иерсиниозом, но при доказанном бактериологически и серологически отсутствии возбудителя в организме больного должно расцениваться как клиника последствий иерсиниоза (резидуальная фаза).
Бессимптомное течение может быть острым (до 3 мес) и хроническим (более 3 мес). Последнее не характерно для псевдотуберкулеза. Кроме того, при иерсиниозев отличие от псевдотуберкулеза наблюдается не только субклиническое, но и реконвалесцентное бактериовыделение возбудителей болезни. Лица, имеющие бессимптомное течение заболевания, выявляются активно при обследовании работников пищевых предприятий и контактных – в очагах.
Прогноз в большинстве случаев, за исключением септического течения болезни, благоприятный.
Диагностика
Из клинических признаков наибольшее диагностическое значение имеет сочетание синдрома поражения желудочно-кишечного тракта и «внекишечной» токсико-вазарной симптоматики. Данные эпидемиологического анамнеза, особенно при групповом характере заболеваемости, также имеют большое значение в распознавании иерсиниоза и псевдотуберкулеза. Однако решающим в установлении окончательного диагноза являются специфические методы диагностики – бактериологический и серологический.
Основными материалам и для бактериологического исследования служат испражнения, кровь, цереброспинальная жидкость, резецированные лимфатические узлы и червеобразный отросток. Для определения присутствия псевдотуберкулезных антигенов в фекалиях и другом материале используют иммуноферментный анализ (ИФА).
Серологическая диагностика имеет большое значение для подтверждения не только клинического диагноза, но и этиологической роли выделенных иерсиний. Она осуществляется с помощью РА и РНГА методом парных сывороток. Исследуют сыворотки крови, взятые в начале и на 3-й неделе болезни. Диагностическим для РА считается титр антител 1:80 и выше, а для РНГА-1:160 и выше.
Исследуют сыворотки крови, взятые в начале и на 3-й неделе болезни. Диагностическим для РА считается титр антител 1:80 и выше, а для РНГА-1:160 и выше.
В экспресс-диагностике иерсиниоза используют РНГА с иммуноглобулиновыми диагностикумами и МФА.
Определенное значение в диагностике имеет также гистологическое исследование биоптатов лимфатических узлов и других органов.
Дифференциальная диагностика иерсиниоза и псевдотуберкулеза зависит от клинического варианта болезни. Наиболее часто возникает необходимость дифференцировать эти заболевания с острыми кишечными инфекциями, аппендицитом, различными заболеваниями суставов, вирусным гепатитом, сепсисом иной этиологии и др.
Лечение
В качестве этиотропных средств применяют антибиотики, сульфаниламиды и химиопрепараты. К препаратам выбора при генерализованной форме заболеваний относятся фторхинолоны. К препаратам резерва — цефалоспорины 3-го поколения, тетрациклины и левомицетин. Аминогликозиды обычно используют при лечении больных с иерсиниозным (псевдотуберкулезным) гепатитом. Для лечения больных с гастроинтестиномезентериальной формой (варианты: гастроэнтероколит, гастроэнтерит, энтероколит, энтерит) могут быть использованы препараты из группы котримоксазола и нитрофурана. Продолжительность этиотропной терапии зависит от формы заболевания. При локализованной форме она составляет 7-10 дней, при генерализованной – не менее 12-14 дней.
Для лечения больных с гастроинтестиномезентериальной формой (варианты: гастроэнтероколит, гастроэнтерит, энтероколит, энтерит) могут быть использованы препараты из группы котримоксазола и нитрофурана. Продолжительность этиотропной терапии зависит от формы заболевания. При локализованной форме она составляет 7-10 дней, при генерализованной – не менее 12-14 дней.
Патогенетическая терапия предусматривает назначение дезинтоксикационных, общеукрепляющих и стимулирующих, а также десенсибилизирующих средств. В некоторых случаях используют глюкозоэлектролитныеи полиионные растворы для регидратации.
Больных с септическим течением заболевания лечат в соответствие с принципами лечения сепсиса, используя 2-3 антибиотика (фторхинолоны, аминогликозиды, цефалоспорины) внутривенно в сочетании с интенсивной патогенетической терапией.
Больные с бессимптомным течением получают терапию в зависимости от варианта (субклинический или реконвалесцентный) и продолжительности бактериовыделения. Лечение острого субклинического варианта соответствует терапии легкого течения локализованной формы. В терапии хронического субклинического и реконвалесцентного вариантов используют фторхинолоны, аминогликозиды, рифампицин в комплексе с иммуноориентированными средствами.
Лечение острого субклинического варианта соответствует терапии легкого течения локализованной формы. В терапии хронического субклинического и реконвалесцентного вариантов используют фторхинолоны, аминогликозиды, рифампицин в комплексе с иммуноориентированными средствами.
По показаниям проводится оперативное лечение.
Профилактика
Контроль за состоянием овощехранилищ, борьба с грызунами.
Флюорография в Барнауле – Пациентам
Малярия
Синонимы: перемежающаяся лихорадка, болотная лихорадка, палюдизм.
Это острая протозойная трансмиссивная (кровяная) болезнь, проявляющаяся приступами лихорадки, гемолитической анемией, увеличением печени и селезенки, склонная к рецидивирующему течению. Болезнь распространена в странах с теплым и жарким климатом.
В СССР малярия практически ликвидирована в 1960 году. В последние годы в Российской Федерации отмечаются случаи завоза малярии из стран с тропическим и субтропическим климатом, чаще всего из стран Африки, Индии, Афганистана, Таиланда, а также Республик Таджикистан и Азербайджан.
Возбудители болезни малярийные плазмодии 4 видов, которые передаются самками комаров рода Anopheles.
Источником инфекции служит инвазированный человек, больные, паразитоносители. В естественных условиях возможно заражение человека от некоторых животных (ящерицы, птицы, грызуны, обезьяны). Механизм заражения трансмиссивный, через укус инфицированной самки комаров,. Заражение возможно также парентеральным путем — при гемотрансфузиях от донора-паразитоносителя, при проведении парентеральных манипуляций, а также в редких случаях — трансплацентарно или в родах.
Восприимчивость к малярии высокая, особенно у детей. Наряду с этим сохраняется естественная резистентность к малярии.
Виды малярии: 1.трехдневная
2. четырехдневная
3. тропическая
4. ovale — малярия Периоды течения болезни:
1. инкубации
2. первичных (острых) проявлений
3. латентный
4. период рецидивов
5. период реконвалесценции.
Диагностика
Распознавание малярии основывается на данных эпидемиологического анамнеза и ведущих клинических признаков — приступообразной лихорадки, гепатоспленомегалии, гемолитической анемии. Что подтвеждается результатом анализа крови.
Клиника
Клиническая картина болезни характеризуется пароксизмами: приступами лихорадки, развивающимися стадийно с ознобом, жаром и потоотделением. Начало болезни острое. Могут быть продромальные признаки в виде общего недомогания, слабости.
Инкубационный период малярии составляет от 10 дней до 14 месяцев в зависимости от вида возбудителя. На фоне химиопрофилактики продолжительность периода инкубации увеличивается.
Малярийный пароксизм делится на фазы: «озноб» (1-3 ч), «жар» (6-8 ч), и «пот». Общая продолжительность приступа составляет от 1 до 14 ч, при тропической малярии до 36 ч. Развиваются общетоксические явления: температура тела повышается до 40-41°С, отмечается головная боль, миалгии, головокружение, часто рвота, поясничные боли.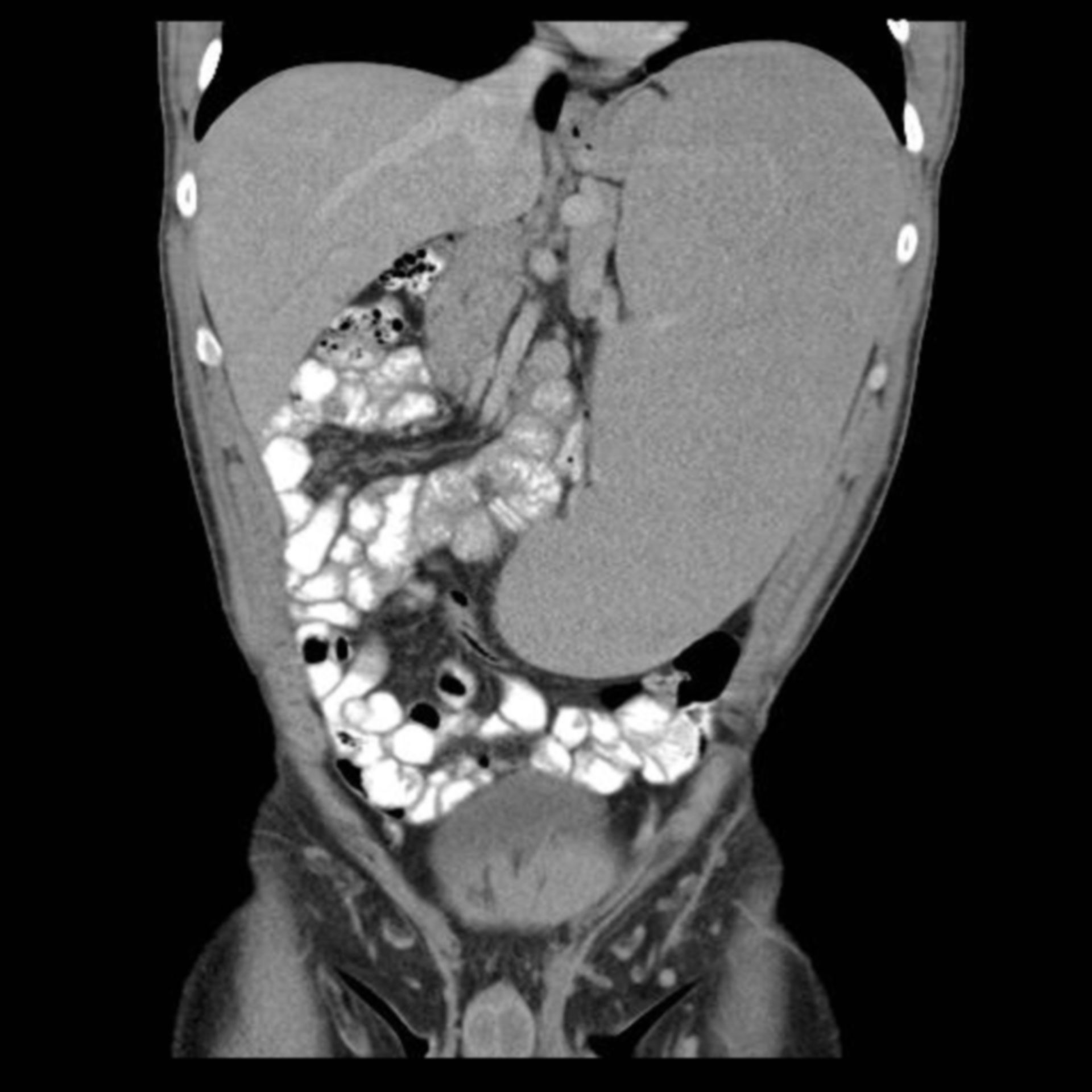
Окончание приступа сопровождается потливостью, уменьшением явлений интоксикации.
При отсутствии адекватной терапии спустя 1-3 мес. развиваются рецидивы болезни.
Тропическая малярия — тяжелая форма малярийной инфекции.
Осложнениями малярии могут быть малярийная кома, гемоглобинурийная лихорадка, геморрагический и отечный синдром, алгид, психозы, почечная недостаточность, разрыв селезенки. Малярия у беременных часто является причиной абортов, преждевременных родов, приводит к послеродовым осложнениям и летальным исходам.
Лечение
Больным малярией проводят этиотропную и патогенетическую терапию. Лечение проводят в условиях стационара.
Профилактика
Борьба с переносчиками является основным способом профилактики и уменьшения передач малярии:
-обработка территорий инсектицидами;
-осушение болот и улучшение санитарных условий территорий.
Для персональной защиты:
-использование закрытой одежды;
-использование репеллентов;
-использование противомоскитных сеток, обработанных инсектицидами;
-проведение специфической химиопрофилактики лицам, выезжающим в страны с тропическим климатом.
Гепатоспленомегалия: причины, осложнения и лечение
Гепатоспленомегалия — это состояние, которое вызывает отек и увеличение печени и селезенки.
Заболевания, связанные с печенью, часто начинаются с приставки «гепат-» (например, гепатит), а «селезенка» обозначает селезенку. Термин «мегалия» указывает на то, что что-то необычно большое.
Поскольку и селезенка, и печень играют важную роль в организме, очень важно выявить и исправить любые основные причины гепатоспленомегалии.
Гепатоспленомегалию могут вызывать несколько состояний. Примеры включают:
- инфекция, такая как гепатит С, сифилис или сепсис в результате значительной бактериальной инфекции
- хроническое заболевание печени с портальной гипертензией
- раковые заболевания, такие как амилоидоз или саркоидоз
- ВИЧ
- лейкемия
- лимфома
- злокачественная анемия
- акромегалия
- серповидно-клеточная анемия
- системная красная волчанка
- талассемия
- тиреотоксикоз
- травма, например автомобильная авария, повлиявшая на селезенку и печень
Увеличение печени также может вызвать увеличение селезенки потому что эти два органа расположены близко друг к другу.
Когда печень увеличивается в размерах, она оказывает дополнительное давление на селезенку. Это давление влияет на приток крови к селезенке, что может вызвать ее набухание и увеличение.
Также селезенка отвечает за фильтрацию бактерий и вирусов. Когда они вызывают проблемы с печенью, они также могут повлиять на селезенку.
Врачи могут легче диагностировать гепатоспленомегалию, если у человека есть следующие факторы риска:
- диабет
- высокий холестерин
- употребление алкоголя или наркомания
- история совместного использования игл
- избыточный вес
A Человек с этими факторами риска должен поговорить со своим врачом о том, как он может улучшить здоровье своей печени и снизить риск развития гепатоспленомегалии.
Гепатоспленомегалия возникает, когда печень и селезенка намного больше, чем их типичный размер. Обычно человек не чувствует границ своей печени или селезенки в желудке. Но если у них гепатоспленомегалия, они обычно чувствуют эти органы.
В среднем селезенка взрослого человека весит от 100 до 250 граммов (г). Длина селезенки сверху вниз составляет около 11 сантиметров (см).
Однако, когда у человека увеличена селезенка, она может весить более 400 г и иметь длину более 13 см.Если у человека очень выраженная спленомегалия, селезенка может весить от 500 до 1000 г.
Вес здоровой печени у мужчин составляет от 1,4 до 1,5 кг, а у женщин — от 1,2 до 1,4 кг. Длина печени обычно составляет 16 см или меньше, но увеличенная печень может быть значительно больше.
Когда печень и селезенка увеличены, они не могут функционировать так же хорошо, как обычно. Это может вызвать симптомы, которые могут включать:
- коричневая моча
- испражнения цвета глины
- увеличенный или вздутый живот
- лихорадка
- зуд
- желтуха или пожелтение глаз и кожи
- тошнота
- боль, особенно в верхней правой части желудка
- необъяснимая усталость
- рвота
Симптомы могут варьироваться от легких до тяжелых в зависимости от их первопричины.
Дети тоже могут страдать от гепатоспленомегалии. Некоторые из возможных причин гепатоспленомегалии у детей включают:
- лизосомные болезни накопления, которые представляют собой дисфункции ферментов печени, такие как неспособность обрабатывать глюкоцереброзид
- малярия
- сепсис или тяжелая бактериальная инфекция
- талассемия
Врач будет Начните диагностику гепатоспленомегалии с оценки истории болезни человека и текущих симптомов.
Врач проведет физический осмотр, уделяя особое внимание животу на предмет признаков увеличения органов.Они могут прощупать живот на предмет опухолей и проверить, легко ли они прощупывают печень и селезенку.
Врач, скорее всего, назначит много диагностических тестов, чтобы определить наиболее вероятную причину гепатоспленомегалии. Эти тесты включают:
- Анализы крови : Анализы крови на гепатоспленомегалию включают функциональный тест печени, общий анализ крови и тесты на факторы свертывания крови.

- Сканирование изображений : Компьютерная томография (КТ) или УЗИ могут помочь врачу определить, является ли опухоль причиной опухоли опухоль или абсцесс.Визуальные тесты также могут показать, насколько велики печень и селезенка.
- Биопсия : Врач может хирургическим путем удалить небольшой кусочек ткани печени, чтобы определить наличие раковых клеток.
Лечение гепатоспленомегалии широко варьируется в зависимости от причины увеличения органа. Лечение основной причины обычно помогает уменьшить размер органов.
Специальные лекарства могут использоваться для лечения многих причин гепатоспленомегалии, включая анемию, ВИЧ, заболевания печени и инфекции.Человеку также может потребоваться внести коррективы в свой рацион.
Если у человека злокачественная опухоль, поражающая печень или селезенку, врач может порекомендовать удалить опухоль и использовать химиотерапию или лучевую терапию, чтобы предотвратить возвращение рака.
В редких случаях врач может порекомендовать хирургическое удаление селезенки и части печени.
Хотя человек может жить без селезенки, он не может жить без своей печени. Людям с тяжелыми и опасными для жизни состояниями, связанными с гепатоспленомегалией, может потребоваться пересадка печени.
Гепатоспленомегалия может быть результатом многих заболеваний, связанных с печенью и селезенкой.
Врачи оценивают симптомы человека и используют диагностические тесты, чтобы определить лучший курс лечения. В редких случаях может потребоваться хирургическое вмешательство и трансплантация.
Гепатоспленомегалия: причины, осложнения и лечение
Гепатоспленомегалия — это состояние, которое вызывает отек и увеличение печени и селезенки.
Заболевания, связанные с печенью, часто начинаются с приставки «гепат-» (например, гепатит), а «селезенка» обозначает селезенку.Термин «мегалия» указывает на то, что что-то необычно большое.
Поскольку и селезенка, и печень играют важную роль в организме, очень важно выявить и исправить любые основные причины гепатоспленомегалии.
Гепатоспленомегалию могут вызывать несколько состояний. Примеры включают:
- инфекция, такая как гепатит С, сифилис или сепсис в результате значительной бактериальной инфекции
- хроническое заболевание печени с портальной гипертензией
- раковые заболевания, такие как амилоидоз или саркоидоз
- ВИЧ
- лейкемия
- лимфома
- злокачественная анемия
- акромегалия
- серповидно-клеточная анемия
- системная красная волчанка
- талассемия
- тиреотоксикоз
- травма, например автомобильная авария, повлиявшая на селезенку и печень
Увеличение печени также может вызвать увеличение селезенки потому что эти два органа расположены близко друг к другу.
Когда печень увеличивается в размерах, она оказывает дополнительное давление на селезенку. Это давление влияет на приток крови к селезенке, что может вызвать ее набухание и увеличение.
Также селезенка отвечает за фильтрацию бактерий и вирусов. Когда они вызывают проблемы с печенью, они также могут повлиять на селезенку.
Врачи могут легче диагностировать гепатоспленомегалию, если у человека есть следующие факторы риска:
- диабет
- высокий холестерин
- употребление алкоголя или наркомания
- история совместного использования игл
- избыточный вес
A Человек с этими факторами риска должен поговорить со своим врачом о том, как он может улучшить здоровье своей печени и снизить риск развития гепатоспленомегалии.
Гепатоспленомегалия возникает, когда печень и селезенка намного больше, чем их типичный размер. Обычно человек не чувствует границ своей печени или селезенки в желудке. Но если у них гепатоспленомегалия, они обычно чувствуют эти органы.
В среднем селезенка взрослого человека весит от 100 до 250 граммов (г). Длина селезенки сверху вниз составляет около 11 сантиметров (см).
Однако, когда у человека увеличена селезенка, она может весить более 400 г и иметь длину более 13 см.Если у человека очень выраженная спленомегалия, селезенка может весить от 500 до 1000 г.
Вес здоровой печени у мужчин составляет от 1,4 до 1,5 кг, а у женщин — от 1,2 до 1,4 кг. Длина печени обычно составляет 16 см или меньше, но увеличенная печень может быть значительно больше.
Когда печень и селезенка увеличены, они не могут функционировать так же хорошо, как обычно. Это может вызвать симптомы, которые могут включать:
- коричневая моча
- испражнения цвета глины
- увеличенный или вздутый живот
- лихорадка
- зуд
- желтуха или пожелтение глаз и кожи
- тошнота
- боль, особенно в верхней правой части желудка
- необъяснимая усталость
- рвота
Симптомы могут варьироваться от легких до тяжелых в зависимости от их первопричины.
Дети тоже могут страдать от гепатоспленомегалии. Некоторые из возможных причин гепатоспленомегалии у детей включают:
- лизосомные болезни накопления, которые представляют собой дисфункции ферментов печени, такие как неспособность обрабатывать глюкоцереброзид
- малярия
- сепсис или тяжелая бактериальная инфекция
- талассемия
Врач будет Начните диагностику гепатоспленомегалии с оценки истории болезни человека и текущих симптомов.
Врач проведет физический осмотр, уделяя особое внимание животу на предмет признаков увеличения органов.Они могут прощупать живот на предмет опухолей и проверить, легко ли они прощупывают печень и селезенку.
Врач, скорее всего, назначит много диагностических тестов, чтобы определить наиболее вероятную причину гепатоспленомегалии. Эти тесты включают:
- Анализы крови : Анализы крови на гепатоспленомегалию включают функциональный тест печени, общий анализ крови и тесты на факторы свертывания крови.
- Сканирование изображений : Компьютерная томография (КТ) или УЗИ могут помочь врачу определить, является ли опухоль причиной опухоли опухоль или абсцесс.Визуальные тесты также могут показать, насколько велики печень и селезенка.
- Биопсия : Врач может хирургическим путем удалить небольшой кусочек ткани печени, чтобы определить наличие раковых клеток.
Лечение гепатоспленомегалии широко варьируется в зависимости от причины увеличения органа. Лечение основной причины обычно помогает уменьшить размер органов.
Специальные лекарства могут использоваться для лечения многих причин гепатоспленомегалии, включая анемию, ВИЧ, заболевания печени и инфекции.Человеку также может потребоваться внести коррективы в свой рацион.
Если у человека злокачественная опухоль, поражающая печень или селезенку, врач может порекомендовать удалить опухоль и использовать химиотерапию или лучевую терапию, чтобы предотвратить возвращение рака.
В редких случаях врач может порекомендовать хирургическое удаление селезенки и части печени.
Хотя человек может жить без селезенки, он не может жить без своей печени. Людям с тяжелыми и опасными для жизни состояниями, связанными с гепатоспленомегалией, может потребоваться пересадка печени.
Гепатоспленомегалия может быть результатом многих заболеваний, связанных с печенью и селезенкой.
Врачи оценивают симптомы человека и используют диагностические тесты, чтобы определить лучший курс лечения. В редких случаях может потребоваться хирургическое вмешательство и трансплантация.
Гепатоспленомегалия: причины, осложнения и лечение
Гепатоспленомегалия — это состояние, которое вызывает отек и увеличение печени и селезенки.
Заболевания, связанные с печенью, часто начинаются с приставки «гепат-» (например, гепатит), а «селезенка» обозначает селезенку.Термин «мегалия» указывает на то, что что-то необычно большое.
Поскольку и селезенка, и печень играют важную роль в организме, очень важно выявить и исправить любые основные причины гепатоспленомегалии.
Гепатоспленомегалию могут вызывать несколько состояний. Примеры включают:
- инфекция, такая как гепатит С, сифилис или сепсис в результате значительной бактериальной инфекции
- хроническое заболевание печени с портальной гипертензией
- раковые заболевания, такие как амилоидоз или саркоидоз
- ВИЧ
- лейкемия
- лимфома
- злокачественная анемия
- акромегалия
- серповидно-клеточная анемия
- системная красная волчанка
- талассемия
- тиреотоксикоз
- травма, например автомобильная авария, повлиявшая на селезенку и печень
Увеличение печени также может вызвать увеличение селезенки потому что эти два органа расположены близко друг к другу.
Когда печень увеличивается в размерах, она оказывает дополнительное давление на селезенку. Это давление влияет на приток крови к селезенке, что может вызвать ее набухание и увеличение.
Также селезенка отвечает за фильтрацию бактерий и вирусов. Когда они вызывают проблемы с печенью, они также могут повлиять на селезенку.
Врачи могут легче диагностировать гепатоспленомегалию, если у человека есть следующие факторы риска:
- диабет
- высокий холестерин
- употребление алкоголя или наркомания
- история совместного использования игл
- избыточный вес
A Человек с этими факторами риска должен поговорить со своим врачом о том, как он может улучшить здоровье своей печени и снизить риск развития гепатоспленомегалии.
Гепатоспленомегалия возникает, когда печень и селезенка намного больше, чем их типичный размер. Обычно человек не чувствует границ своей печени или селезенки в желудке. Но если у них гепатоспленомегалия, они обычно чувствуют эти органы.
В среднем селезенка взрослого человека весит от 100 до 250 граммов (г). Длина селезенки сверху вниз составляет около 11 сантиметров (см).
Однако, когда у человека увеличена селезенка, она может весить более 400 г и иметь длину более 13 см.Если у человека очень выраженная спленомегалия, селезенка может весить от 500 до 1000 г.
Вес здоровой печени у мужчин составляет от 1,4 до 1,5 кг, а у женщин — от 1,2 до 1,4 кг. Длина печени обычно составляет 16 см или меньше, но увеличенная печень может быть значительно больше.
Когда печень и селезенка увеличены, они не могут функционировать так же хорошо, как обычно. Это может вызвать симптомы, которые могут включать:
- коричневая моча
- испражнения цвета глины
- увеличенный или вздутый живот
- лихорадка
- зуд
- желтуха или пожелтение глаз и кожи
- тошнота
- боль, особенно в верхней правой части желудка
- необъяснимая усталость
- рвота
Симптомы могут варьироваться от легких до тяжелых в зависимости от их первопричины.
Дети тоже могут страдать от гепатоспленомегалии. Некоторые из возможных причин гепатоспленомегалии у детей включают:
- лизосомные болезни накопления, которые представляют собой дисфункции ферментов печени, такие как неспособность обрабатывать глюкоцереброзид
- малярия
- сепсис или тяжелая бактериальная инфекция
- талассемия
Врач будет Начните диагностику гепатоспленомегалии с оценки истории болезни человека и текущих симптомов.
Врач проведет физический осмотр, уделяя особое внимание животу на предмет признаков увеличения органов.Они могут прощупать живот на предмет опухолей и проверить, легко ли они прощупывают печень и селезенку.
Врач, скорее всего, назначит много диагностических тестов, чтобы определить наиболее вероятную причину гепатоспленомегалии. Эти тесты включают:
- Анализы крови : Анализы крови на гепатоспленомегалию включают функциональный тест печени, общий анализ крови и тесты на факторы свертывания крови.
- Сканирование изображений : Компьютерная томография (КТ) или УЗИ могут помочь врачу определить, является ли опухоль причиной опухоли опухоль или абсцесс.Визуальные тесты также могут показать, насколько велики печень и селезенка.
- Биопсия : Врач может хирургическим путем удалить небольшой кусочек ткани печени, чтобы определить наличие раковых клеток.
Лечение гепатоспленомегалии широко варьируется в зависимости от причины увеличения органа. Лечение основной причины обычно помогает уменьшить размер органов.
Специальные лекарства могут использоваться для лечения многих причин гепатоспленомегалии, включая анемию, ВИЧ, заболевания печени и инфекции.Человеку также может потребоваться внести коррективы в свой рацион.
Если у человека злокачественная опухоль, поражающая печень или селезенку, врач может порекомендовать удалить опухоль и использовать химиотерапию или лучевую терапию, чтобы предотвратить возвращение рака.
В редких случаях врач может порекомендовать хирургическое удаление селезенки и части печени.
Хотя человек может жить без селезенки, он не может жить без своей печени. Людям с тяжелыми и опасными для жизни состояниями, связанными с гепатоспленомегалией, может потребоваться пересадка печени.
Гепатоспленомегалия может быть результатом многих заболеваний, связанных с печенью и селезенкой.
Врачи оценивают симптомы человека и используют диагностические тесты, чтобы определить лучший курс лечения. В редких случаях может потребоваться хирургическое вмешательство и трансплантация.
Гепатоспленомегалия: причины, осложнения и лечение
Гепатоспленомегалия — это состояние, которое вызывает отек и увеличение печени и селезенки.
Заболевания, связанные с печенью, часто начинаются с приставки «гепат-» (например, гепатит), а «селезенка» обозначает селезенку.Термин «мегалия» указывает на то, что что-то необычно большое.
Поскольку и селезенка, и печень играют важную роль в организме, очень важно выявить и исправить любые основные причины гепатоспленомегалии.
Гепатоспленомегалию могут вызывать несколько состояний. Примеры включают:
- инфекция, такая как гепатит С, сифилис или сепсис в результате значительной бактериальной инфекции
- хроническое заболевание печени с портальной гипертензией
- раковые заболевания, такие как амилоидоз или саркоидоз
- ВИЧ
- лейкемия
- лимфома
- злокачественная анемия
- акромегалия
- серповидно-клеточная анемия
- системная красная волчанка
- талассемия
- тиреотоксикоз
- травма, например автомобильная авария, повлиявшая на селезенку и печень
Увеличение печени также может вызвать увеличение селезенки потому что эти два органа расположены близко друг к другу.
Когда печень увеличивается в размерах, она оказывает дополнительное давление на селезенку. Это давление влияет на приток крови к селезенке, что может вызвать ее набухание и увеличение.
Также селезенка отвечает за фильтрацию бактерий и вирусов. Когда они вызывают проблемы с печенью, они также могут повлиять на селезенку.
Врачи могут легче диагностировать гепатоспленомегалию, если у человека есть следующие факторы риска:
- диабет
- высокий холестерин
- употребление алкоголя или наркомания
- история совместного использования игл
- избыточный вес
A Человек с этими факторами риска должен поговорить со своим врачом о том, как он может улучшить здоровье своей печени и снизить риск развития гепатоспленомегалии.
Гепатоспленомегалия возникает, когда печень и селезенка намного больше, чем их типичный размер. Обычно человек не чувствует границ своей печени или селезенки в желудке. Но если у них гепатоспленомегалия, они обычно чувствуют эти органы.
В среднем селезенка взрослого человека весит от 100 до 250 граммов (г). Длина селезенки сверху вниз составляет около 11 сантиметров (см).
Однако, когда у человека увеличена селезенка, она может весить более 400 г и иметь длину более 13 см.Если у человека очень выраженная спленомегалия, селезенка может весить от 500 до 1000 г.
Вес здоровой печени у мужчин составляет от 1,4 до 1,5 кг, а у женщин — от 1,2 до 1,4 кг. Длина печени обычно составляет 16 см или меньше, но увеличенная печень может быть значительно больше.
Когда печень и селезенка увеличены, они не могут функционировать так же хорошо, как обычно. Это может вызвать симптомы, которые могут включать:
- коричневая моча
- испражнения цвета глины
- увеличенный или вздутый живот
- лихорадка
- зуд
- желтуха или пожелтение глаз и кожи
- тошнота
- боль, особенно в верхней правой части желудка
- необъяснимая усталость
- рвота
Симптомы могут варьироваться от легких до тяжелых в зависимости от их первопричины.
Дети тоже могут страдать от гепатоспленомегалии. Некоторые из возможных причин гепатоспленомегалии у детей включают:
- лизосомные болезни накопления, которые представляют собой дисфункции ферментов печени, такие как неспособность обрабатывать глюкоцереброзид
- малярия
- сепсис или тяжелая бактериальная инфекция
- талассемия
Врач будет Начните диагностику гепатоспленомегалии с оценки истории болезни человека и текущих симптомов.
Врач проведет физический осмотр, уделяя особое внимание животу на предмет признаков увеличения органов.Они могут прощупать живот на предмет опухолей и проверить, легко ли они прощупывают печень и селезенку.
Врач, скорее всего, назначит много диагностических тестов, чтобы определить наиболее вероятную причину гепатоспленомегалии. Эти тесты включают:
- Анализы крови : Анализы крови на гепатоспленомегалию включают функциональный тест печени, общий анализ крови и тесты на факторы свертывания крови.
- Сканирование изображений : Компьютерная томография (КТ) или УЗИ могут помочь врачу определить, является ли опухоль причиной опухоли опухоль или абсцесс.Визуальные тесты также могут показать, насколько велики печень и селезенка.
- Биопсия : Врач может хирургическим путем удалить небольшой кусочек ткани печени, чтобы определить наличие раковых клеток.
Лечение гепатоспленомегалии широко варьируется в зависимости от причины увеличения органа. Лечение основной причины обычно помогает уменьшить размер органов.
Специальные лекарства могут использоваться для лечения многих причин гепатоспленомегалии, включая анемию, ВИЧ, заболевания печени и инфекции.Человеку также может потребоваться внести коррективы в свой рацион.
Если у человека злокачественная опухоль, поражающая печень или селезенку, врач может порекомендовать удалить опухоль и использовать химиотерапию или лучевую терапию, чтобы предотвратить возвращение рака.
В редких случаях врач может порекомендовать хирургическое удаление селезенки и части печени.
Хотя человек может жить без селезенки, он не может жить без своей печени. Людям с тяжелыми и опасными для жизни состояниями, связанными с гепатоспленомегалией, может потребоваться пересадка печени.
Гепатоспленомегалия может быть результатом многих заболеваний, связанных с печенью и селезенкой.
Врачи оценивают симптомы человека и используют диагностические тесты, чтобы определить лучший курс лечения. В редких случаях может потребоваться хирургическое вмешательство и трансплантация.
Длительная лихорадка, гепатоспленомегалия и панцитопения у 46-летней женщины
PLoS Med. 2009 Apr; 6 (4): e1000053.
,
1
,
*
,
2
,
1
,
3
,
3
и
3
Лиран Леви
1 Отделение внутренней медицины, Медицинский центр Еврейского университета Хадасса, Иерусалим, Израиль
Абедельмаджид Насереддин
2 Отделение паразитологии, Медицинский центр Еврейского университета Хадасса, Иерусалим, Израиль
, Иерусалим, Израиль 9 Рав-Ача
1 Отделение внутренней медицины, Медицинский центр Хадасса-Еврейского университета, Иерусалим, Израиль
Мейрав Кедми
3 Отделение гематологии, Медицинский центр Хадасса-Еврейского университета, Иерусалим, Израиль
Дебора Рунд
3 Отделение гематологии, Медицинский центр Хадасса-Еврейского университета, Иерусалим, Израиль
Моше Э.Гатт
3 Отделение гематологии Медицинского центра Еврейского университета Хадасса, Иерусалим, Израиль
Рональд К.В. Ма, редактор
1 Отделение внутренних болезней Медицинского центра Еврейского университета Хадасса, Иерусалим, Израиль
2 Кафедра паразитологии, Медицинский центр Хадасса-Еврейского университета, Иерусалим, Израиль
3 Кафедра гематологии, Медицинский центр Хадасса-Еврейского университета, Иерусалим, Израиль
Китайский университет Гонконга, Китай
Критерии авторства ICMJE прочитаны и выполнены: LL AN MR-A MK DR MEG.Согласны с результатами и выводами рукописи: LL AN MR-A MK DR MEG. Проанализированы результаты расследования дела: МЭГ. Собранные результаты испытаний: AN DR MEG. Написал первый черновик статьи: LL MEG. Участвовал в написании статьи: AN MR-A MK DR MEG. Проведен серологический анализ Leishmania , ПЦР, посев и видовой зимодемальный анализ: AN. Участвовал в диагностике и лечении больного: ДР.
Учебный форум обсуждает важную клиническую проблему, актуальную для широкой медицинской аудитории.
Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии надлежащего указания автора и источника.
Эта статья цитируется в других статьях в PMC.
Описание случая
46-летняя женщина была госпитализирована из-за лихорадки до 39 ° C в течение одной недели. Пациент жаловался на слабость, ночную потливость и похудание за две недели до поступления.Пациент не имел истории болезни и не принимал никаких лекарств, пищевых добавок или запрещенных препаратов. Она родилась и всю жизнь прожила в сельской местности. Она косвенно контактировала с сельскохозяйственными животными и домашними животными, но не имела с ними тесного контакта, а ее семья не занималась сельскохозяйственными работами. Она отрицала, что ее укусили клещи или блохи. Не было истории недавних зарубежных поездок или употребления сырого мяса или непастеризованного молока. Она не сообщила об отсутствии высыпаний, артралгии, сухости глаз, язв во рту или кожно-слизистых кровотечений.
При осмотре она выглядела бледной и потной. Кардиореспираторное обследование без особенностей. Были отмечены заметно болезненные и увеличенные печень и селезенка, на 3 см и 10 см ниже края ребер соответственно, без пальпируемых лимфатических узлов. Также присутствовал отек периорбитальных и периферических конечностей.
Каковы вероятные этиологии высокой температуры и органомегалии у этого пациента?
Врачи обычно принимают пациентов с продолжительной лихорадкой. Существует множество возможных этиологий, чаще всего инфекционные, но также возможны неопластические, воспалительные или аутоиммунные заболевания.К менее распространенным состояниям относятся лихорадка, связанная с приемом лекарств, искусственная (т. Е. Самоиндуцированная) лихорадка и другие редкие заболевания. Некоторым пациентам с продолжительной лихорадкой не удается диагностировать, несмотря на интенсивное диагностическое обследование.
Диагностический подход должен основываться на любых потенциальных подсказках в анамнезе пациента, физическом осмотре и рутинных скрининговых анализах крови и посевах. В этом случае история не дает очевидных ключей; поэтому органегалия должна быть основой для оценки.Массивная спленомегалия сужает дифференциальный диагноз, поскольку только несколько состояний обычно вызывают такую степень увеличения селезенки (вставка 1). К ним относятся инфекционные причины, такие как бактериальные (брюшной тиф, Mycobacterium tuberculosis или СПИД с комплексом M. avium ) и грибковые агенты (гистоплазмоз), но чаще спленомегалия возникает в результате паразитарных заболеваний, таких как малярия и лейшманиоз. Вирусы, вызывающие инфекционный мононуклеоз, например, вирус Эпштейна-Барра (EBV) и цитомегаловирус (CMV), или вирусы гепатита, редко вызывают такую степень органомегалии.Также следует учитывать гематологические нарушения, такие как миелопролиферативные заболевания, лимфома или хронический лимфолейкоз и волосатоклеточный лейкоз, а также промежуточная талассемия и аутоиммунная гемолитическая анемия. Инфильтративные заболевания, такие как болезнь Гоше, саркоидоз и амилоидоз, потенциально могут вызывать массивную спленомегалию. Полное здоровье в анамнезе, болезненность селезенки и резкое начало высокой температуры — все это свидетельствует в пользу острого, а не хронического тлеющего заболевания (например, инфильтративного, аутоиммунного или хронического гематологического неопластического заболевания).Тем не менее нельзя исключать хроническое заболевание, и его следует исследовать как основное заболевание, предшествующее более частой причине продолжительной лихорадки.
Вставка 1: Заболевания, связанные с массивной спленомегалией
Массивная спленомегалия определяется как селезенка, расширенная более чем на 8 см ниже левого края реберной кости и / или весом более 1000 г.
Гематологический
Инфекционный
Паразитарный
Бактериальный
Вирусный
Грибковый
Грибковый
Моча
Моча , и посев стула были отрицательными.Лабораторные результаты пациента выявили панцитопению с 2800 лейкоцитами / мм 3 (2200 нейтрофилов, 400 лимфоцитов, 200 моноцитов и отсутствие эозинофилов или базофилов / мм 3 ). Уровень гемоглобина 98 г / л, количество тромбоцитов 59 000 / мм 3 . Количество ретикулоцитов составляло 1,5%. Скорость оседания эритроцитов увеличивалась до 104 мм / ч. Протромбиновое время и частичное тромбопластиновое время были увеличены (41,5% и 46,6 секунды соответственно), а уровень фибриногена был низким — 82 мг / дл.Мазок периферической крови показал зрелые лейкоциты с легким сдвигом влево и несколько шистоцитов эритроцитов. Уровни сывороточного креатинина, мочевины и электролиты были в норме. Функциональные пробы печени (LFT) были в три-четыре раза выше нормальных значений, с гипербилирубинемией 27 ммоль / л (0-17 ммоль / л). Уровень лактатдегидрогеназы был заметно повышен до 4 245 Ед / л (300–620 Ед / л). Антиядерные антитела, ревматоидный фактор, антинейтрофильные цитоплазматические антитела, антикардиолипин и циркулирующие антикоагулянты были отрицательными, как и прямые тесты Кумбса.Серология на Mycoplasma , Brucella , Legionella , Q-лихорадку, пятнистую лихорадку, мышиный сыпной тиф, ВИЧ, EBV, CMV, гепатиты A, B и C, парвовирус B19 и лейшманиоз ( Leishmania infantum , Leishmania infantum , Leishmania infantum , Leishmania infantum , . donovani и L. chagasi ) были отрицательными. Кислотостойкие окрашивания мокроты и посевов крови на туберкулез отрицательны. Мазки толстой крови на малярию и Borrelia, были отрицательными. Компьютерная томография грудной клетки, брюшной полости и таза показала однородно увеличенные печень и селезенку (длинная ось селезенки, 24 см).Эхокардиография показала нормальную функцию желудочков и отсутствие клапанных аномалий. У пациентки продолжались ежедневные пиковые температуры и потоотделение, а ее цитопения, нарушения свертывания крови и LFT ухудшались.
Что делать дальше при отсутствии лабораторной диагностики признаков и симптомов этого пациента?
Основной наблюдаемый лабораторный признак — панцитопения. Однако большая часть, если не весь дифференциальный диагноз продолжительной лихорадки и спленомегалии может в некоторой степени включать в себя цитопении крови.Гематологические злокачественные новообразования могут поражать костный мозг и, следовательно, приводить к цитопении. Отсутствие эозинофилов, базофилов или ядросодержащих эритроцитов и морфологически нормальных циркулирующих лейкоцитов делает миелопролиферативное заболевание маловероятным. Отсутствие увеличенных лимфатических узлов и отсутствие атипичных клеток в периферической крови снижает вероятность другого гематологического злокачественного новообразования. Кроме того, спленомегалия сама может вызывать гиперспленизм и цитопении периферической крови. Нарушения коагуляции как протромбинового времени, так и частичного тромбопластинового времени с низким фибриногеном (который является реагентом острой фазы, который, как ожидается, будет повышаться при любом воспалительном состоянии) и циркулирующими шистоцитами, подразумевают наличие диссеминированного внутрисосудистого свертывания (ДВС) и заметно повышенные LFT. указывают на более тяжелое заболевание.Ничем не примечательные аутоиммунные серологии также выступают против такого продолжающегося процесса. Инфекции, вызывающие иммунную гиперплазию или инфильтрацию органов, могут поражать костный мозг, вызывая также цитопении. Поскольку все вышеперечисленные тесты не выявляют этиологию тяжелого заболевания этого пациента, необходима биопсия ткани. Поскольку печень и селезенка кажутся радиологически однородными без очаговых поражений для биопсии, следующим шагом должна быть биопсия костного мозга и аспирация, включая несколько культур для различных обсуждаемых инфекционных заболеваний.
Была проведена биопсия костного мозга, выявившая гиперклеточный костный мозг без признаков злокачественности. Аспират показал наличие большого количества моноцитов и выраженный гемофагоцитоз () без признаков незрелых клеток. Цитогенетическое исследование не выявило аномалий, иммунофенотипирование показало моноцитоз без избытка бластов. Трепан-биопсия окрашивалась на CD3, CD20, CD30, CD68 и общий антиген лейкоцитов без признаков лимфомы. Перестройка гена рецептора Т-клеток была отрицательной.ПЦР-исследования костного мозга на ВЭБ, ЦМВ, вирус герпеса-6 человека и Leishmania оказались отрицательными, и не было обнаружено явного возбудителя или заболевания. Культивированный костный мозг на бактерии и грибки оказался отрицательным. Повторное исследование костного мозга дало результаты, аналогичные результатам первого проведенного исследования.
Аспират костного мозга показывает моноциты (красные стрелки), поглощающие предшественников красных кровяных телец (черные стрелки).
(окраска по Гимзе)
По мере того, как симптомы пациента продолжали прогрессировать, была проведена трансъюгулярная биопсия печени, выявляющая гемофагоцитоз без патогенов или злокачественных новообразований.Дополнительные анализы крови показали уровень ферритина 15 614 нг / мл, триглицеридов 4,35 ммоль / л (0–2,3) и уровень растворимого рецептора интерлейкина 2 9 577 Ед / мл (<1000).
Пациентка была сочтена слишком больной для спленэктомии, и у нее был диагностирован гемофагоцитарный синдром. Эмпирическое лечение высокими дозами иммуноглобулина (2 г / кг) и 300 мг гидрокортизона ежедневно не вызывало клинического ответа. Были начаты высокие дозы дексаметазона (20 мг в день), затем циклоспорин А с быстрым и существенным улучшением в течение следующих нескольких дней.Температура спала, показатели крови поднялись, ДВС-синдром разрешился. Чувствовала себя хорошо, выписана в отличном состоянии с нормальными анализами крови. Она продолжила лечение, постепенно снижая дозу стероидов до завершения, и продолжала принимать циклоспорин А в дозе 5 мг / кг в день. При ежемесячном наблюдении у пациента не было симптомов, и в течение трех месяцев показатели крови оставались нормальными. УЗИ брюшной полости показало уменьшение печени и селезенки почти до нормы (15 см). Аспирация костного мозга и биопсия были выполнены еще два раза и оказались морфологически нормальными.Повторная ПЦР для EBV, который тесно связан с гемофагоцитарным лимфогистиоцитозом, также была отрицательной. Никаких других ПЦР или серологий в то время не прислали.
Как диагностировать и лечить гемофагоцитарный синдром? Это реальный случай первичного гемофагоцитарного синдрома?
Гемофагоцитарный синдром является клинико-патологическим заболеванием. Его диагноз определяется набором основных признаков и симптомов (вставка 2). Заболевание может быть семейным или первичным и наблюдается в основном у детей, хотя оно может быть вторичным по отношению к злокачественным новообразованиям (в основном Т-клеточные лимфомы), инфекциям (чаще всего связанным с ВЭБ), аутоиммунным заболеваниям или лекарствам.В этом случае критерии полностью выполнены, но, учитывая ее возраст и отсутствие соответствующего семейного анамнеза, главный вопрос, который следует задавать неоднократно: каков основной процесс, из-за которого возникает этот гемофагоцитоз? Первичный гемофагоцитоз в этом возрасте встречается настолько редко, что практически отсутствует. Следует продолжить поиск злокачественного новообразования или инфекционного организма и рассмотреть возможность спленэктомии.
Вставка 2: Критерии диагностики HLH
Должны присутствовать пять из восьми.
Основные клинические критерии (необходимо оценить все пять):
Лихорадка
Спленомегалия
Цитопения с участием двух или более клеточных линий
Гипертриглицеридемия или гипофибриногенемия
Гемофагоцитоз
Низкая или отсутствующая активность естественных клеток-киллеров.
Высокий уровень ферритина в сыворотке (> 500 мкг / л)
Высокорастворимый CD25 [рецептор растворимого интерлейкина 2] (> 2400 Ед / мл)
Гемофагоцитарный синдром — тяжелое заболевание с множеством причин, в основном вторичное по отношению к инфекционным организмам, а также к Т-клеточным лимфомам и аутоиммунным заболеваниям. Это также может быть (редко и чаще всего у детей) первичным идиопатическим заболеванием или наследственным заболеванием.
Причину HLH следует искать повторно.Если диагноз установить нелегко, следует провести повторный забор образцов тканей, серологические исследования и посевы.
Лечение HLH не следует откладывать, поскольку болезнь быстро прогрессирует и может быть необратимой.
Висцеральный лейшманиоз — это заболевание, которое может поражать несколько органов. В эндемичных районах следует активно искать диагноз, особенно у хозяев с ослабленным иммунитетом.
Иммуносупрессивная терапия, такая как лечение высокими дозами стероидов, — это палка о двух концах.Хотя это может облегчить симптомы, оно может скрыть диагноз.
- Вздутие живота (увеличение селезенки и печени)
- Легкое образование синяков (низкое количество тромбоцитов)
- Кровотечение, которое трудно остановить
- Анемия (низкий уровень эритроцитов)
- Усталость (чрезмерная усталость)
- Боль в костях / легко ломающиеся кости
- В некоторых случаях респираторные проблемы
- Увеличенная селезенка и печень: Когда клетки Гоше накапливаются в селезенке и / или печени, эти органы увеличиваются в размерах и могут вызвать опухание и болезненность живота.
- Низкое количество тромбоцитов: Нормально функционирующая селезенка избавляется от старых клеток крови. Селезенка, увеличенная болезнью Гоше, слишком быстро разрушает клетки крови, в том числе тромбоциты, которые отвечают за свертывание крови даже после незначительных травм.
- Проблемы с кровотечением и свертыванием: При меньшем количестве тромбоцитов у пациентов с болезнью Гоше могут возникнуть проблемы с кровотечением. Низкое количество тромбоцитов может вызвать такие проблемы, как частые кровотечения из носа, кровотечение десен и легкие синяки. Низкий уровень тромбоцитов также может привести к более серьезным проблемам с кровотечением, особенно после стоматологической работы, хирургических вмешательств, травм и родов.
- Анемия: Клетки Гоше в костном мозге снижают выработку клеток крови, а селезенка быстро разрушает клетки крови, которые производит организм.Эти процессы могут вызвать анемию или низкий уровень красных кровяных телец, которые переносят производящий энергию кислород ко всем частям тела. Пациенты также могут страдать анемией по другим причинам, таким как дефицит железа или витамина B12. Специалист Гоше может помочь вам разобраться в проблемах с анемией и решить их.
- Усталость: Анемия вызывает усталость, и пациенты с болезнью Гоше часто испытывают чрезмерную усталость. Однако не вся усталость при болезни Гоше возникает из-за анемии.
- Легкие: В некоторых случаях глюкоцереброзид может накапливаться в легких, вызывая респираторные проблемы.
- Боль в костях и перелом костей: Пациенты часто испытывают боль в костях, включая тяжелые эпизоды, называемые «кризом костей», возникающие из-за снижения притока крови к костям.
- Инфаркт кости или аваскулярный некроз (АВН): Это состояние возникает, когда части кости не получают достаточно кислорода, что приводит к разрушению костной ткани и ее гибели. Инфаркт кости часто приводит к проблемам с бедром или плечом, тяжелому артриту и повышенному риску переломов.
- Остеопения и остеопороз: Болезнь Гоше вызывает потерю кальция и минералов в костях (остеопения и остеопороз) у пациентов мужского и женского пола любого возраста. Курение, чрезмерное употребление алкоголя, недостаток физической активности и прием некоторых лекарств могут увеличить риск остеопороза у пациентов с болезнью Гоше.
- Самопроизвольные переломы: Остеопения (потеря костной массы) и остеопороз ослабляют кости, повышая вероятность их перелома. Переломы костей у пациентов с болезнью Гоше могут возникать даже без травм.
- Боль в суставах, артрит и повреждение суставов: Боли в суставах часто возникают у пациентов с болезнью Гоше. Болезнь Гоше может вызвать тяжелый артрит и повреждение суставов, которое может быть необратимым, если болезнь не лечить.
(без признаков злокачественности)
Новые критерии
(адаптировано из рекомендаций Общества гистиоцитов [2 ], [17].)
Лечение первичного гемофагоцитарного синдрома у детей состоит из высоких доз дексаметазона, циклоспорина А и химиотерапии на основе этопозида. У этой пациентки использование этого метода лечения казалось целесообразным, учитывая ее серьезное клиническое ухудшение без выявления основной этиологии.До сих пор остается загадкой, что основная причина болезни этого пациента не установлена. Реакция пациента на иммуносупрессивную терапию не является чем-то необычным. Следует иметь в виду, что Т-клеточные лимфомы имеют тенденцию проявляться гемофагоцитозом даже при минимальном заболевании, и что этот тип новообразований может реагировать на лимфолитические стероиды и циклоспорин А, которые являются депрессантами Т-клеток.
К концу трехмесячного периода, в течение которого иммуносупрессия продолжалась, но дозы постепенно снижались (), начальные симптомы лихорадки и слабости вернулись.Она была в срочном порядке госпитализирована с быстро прогрессирующей панцитопенией, ДВС-синдромом и повышенными ФПВ. Другая аспирация костного мозга, шестая по величине, впервые выявила макрофаги, заполненные организмами, внешний вид которых соответствовал таковому у Leishmania amastigotes (). Через несколько дней серологический анализ и посев костного мозга подтвердили диагноз Leishmania . Кроме того, ПЦР подтвердила идентификацию видов L. infantum . Эта форма лейшманиоза чаще всего встречается у детей или людей с ослабленным иммунитетом в эндемичных регионах мира.Это возбудитель кожной и висцеральной форм лейшманиоза; собака — его главный резервуар.
Диагностика и лечение пациента с течением времени ( x — ось в днях).
На оси и показаны уровни лактатдегидрогеназы (ЛДГ) синим цветом, количество лейкоцитов (WBC) — красным. Черные стрелки обозначают начало госпитализации. Зеленые стрелки обозначают биопсию костного мозга (BM) или аспирацию, красные — биопсию печени (LB).
Аспират костного мозга с множественными паразитами (черные стрелки) внутри и высвобожденными из моноцита, что соответствует присутствию амастигот Leishmania .
(окраска по Гимзе)
Начато лечение липосомальным амфотерицином B. Симптомы пациентки исчезли в течение нескольких дней, и ее лабораторные отклонения исчезли. Она была выписана, и при плановом наблюдении в течение двух дополнительных лет симптомы не проявлялись. Все прошлые патологические препараты были тщательно изучены, включая исследования костного мозга и биопсию печени, ни одна из которых не выявила паразитов Leishmania до заключительного диагностического обследования.Пациентка дала согласие на публикацию этого описания случая.
Обсуждение
Термин гемофагоцитоз описывает патологическое обнаружение активированных макрофагов и поглощения эритроцитов, лейкоцитов, тромбоцитов и их клеток-предшественников [1], [2], как показано у этого пациента. Его также можно более правильно назвать гемофагоцитарным лимфогистиоцитозом (ГЛГ). Наиболее типичными признаками и симптомами являются лихорадка, гепатоспленомегалия и цитопения. Менее часто наблюдаемые клинические проявления — неврологические симптомы, лимфаденопатия, отек, кожная сыпь и желтуха [1], [3], [4].Общие лабораторные данные включают гипертриглицеридемию, коагулопатию с гипофибриногемией и повышенные LFT.
Сущность включает два разных состояния, которые может быть трудно отличить друг от друга [2], [5], [6]: первичный и вторичный HLH. Первичный HLH, чаще всего обнаруживаемый у детей раннего возраста, представляет собой наследственное передающееся заболевание, которое считается аутосомно-рецессивным заболеванием, влияющим на иммунную регуляцию. Недавно было обнаружено, что мутации в одном из двух генов лежат в основе 40-50% случаев: ген, кодирующий перфорин, главный иммунный цитотоксический белок, и ген, кодирующий MUNC 13-4, белок, участвующий в экзоцитозе перфорин-несущих белков. цитотоксические гранулы при апоптозе [7].Вторичный HLH, который обнаруживается как у детей, так и у взрослых, включает лимфогистиоцитарную пролиферацию с гемофагоцитозом. Он также развивается как следствие сильной иммунологической активации.
Эта вторичная форма чаще всего встречается при тяжелой инфекции. Вирусно-ассоциированная [8], чаще всего связанная с ВЭБ форма также называется фатальным или молниеносным инфекционным мононуклеозом, но при этом замешаны и другие вирусы. Следует предпринять попытки скрининга на инфекцию EBV, CMV и парвовирусом B19 либо с помощью серологического тестирования, либо с помощью ПЦР, гибридизации in-situ или (в случае CMV) иммунофлуоресцентного тестирования антигена.Также следует рассмотреть возможность серологического тестирования на ВИЧ и инфекцию вируса герпеса-6 человека [9]. Сообщалось, что бактериальные инфекции, такие как бруцеллез, сальмонеллез, туберкулез и риккетсиоз, вызывают этот редкий синдром. Паразитарные заболевания, такие как малярия и лейшманиоз, также могут вызывать вторичный HLH [7]. Проявление висцерального лейшманиоза с гемофагоцитарным синдромом редко во всех возрастных группах, особенно у взрослых [10], [11], [12]. Кроме того, серологический тест Leishmania и исследование костного мозга, включенные в обследование, могут быть изначально отрицательными, что требует повторных процедур костного мозга для диагностики [10].Действительно, диагностика Leishmania у этого пациента на шестом аспирате костного мозга (после пяти предыдущих отрицательных исследований) является крайним примером. HLH может также развиваться после других форм иммунологического стресса и активации, как при расстройстве активации макрофагов при ревматических заболеваниях, но чаще всего наблюдается при злокачественных новообразованиях [13]. Он был описан во время активной лимфомы, а также у пациентов в полной ремиссии [14]. Даже если подтверждена инфекция, связанная с HLH, тесты на иммунофенотип и перестройку генов Т-клеточного рецептора должны проводиться на образцах костного мозга или других тканях, чтобы определить, присутствует ли лежащая в основе Т-клеточная лимфома [9].Чтобы еще больше усложнить диагностику, перестройки Т-клеточного рецептора также могут быть обнаружены как в EBV-ассоциированных HLH, так и в EBV-положительных Т-клеточных лимфомах [15], но еще не были продемонстрированы при других вторичных формах HLH.
ГЛГ считается последним общим путем распространения различных инфекционных организмов, а также аутоиммунных заболеваний и лимфом, возникающих в результате одного и того же процесса, вызывающего активацию иммунной системы. Патофизиология, стоящая за этой чрезмерной активацией, хотя и проявляется в основном в моноцитарном клоне, включает взаимодействия Т-клеток и макрофагов.На основную патогенную роль гиперактивации Th2 указывают высокие уровни цитокинов, таких как интерферон-γ, фактор некроза опухоли-α и интерлейкины 1 и 6, все из которых секретируются активированными клетками Th2 [10]. Эти цитокины вызывают усиленный фагоцитоз in vitro. Основная роль Th2 дополнительно подтверждается сосуществованием HLH Th2-связанных инфекций, таких как туберкулез и лейшманиоз, а также терапевтическим применением циклоспорина, депрессанта Т-клеток. Все они подтверждают гипотетическую роль Т-клеток как ключевого элемента в патофизиологии HLH.Имеются сообщения [10], описывающие пациентов с вторичным HLH, вызванным лейшманиозом, которые лечились иммунодепрессантами, что привело к временной долгосрочной ремиссии, что еще раз подчеркивает иммунологическую реактивность как основу этиологии HLH, а не возбудителя инфекции. Тем не менее, не у всех пациентов со вторичными заболеваниями, связанными с ГЛГ, появляются настоящие симптомы ГЛГ. Таким образом, основной дефицит иммунной модуляции, который отличает пациента, склонного к развитию HLH, от его или ее коллеги, у которого не развивается этот синдром, еще предстоит определить.
Хорошо известно, что иммунокомпетентные, иммунодефицитные, иммуносупрессивные и ВИЧ-инфицированные пациенты более склонны к заражению или реактивации паразитов Leishmania , в основном в эндемичных районах, как это видно в районе Средиземноморья [16], [17]. Таким образом, можно утверждать, что при подавлении иммунитета пациент приобрел оппортунистическую инфекцию или активировал спящую [18].
Этот аргумент нельзя полностью опровергнуть, поскольку факты неоднозначны. Предварительный отрицательный серологический анализ подтверждает возможность того, что сероконверсия, появившаяся позже в ходе заболевания, была новой оппортунистической инфекцией, вызванной иммуносупрессивным лечением.Согласно этой гипотезе, у пациентки был идиопатический HLH, который исчез после лечения стероидами и циклоспорином A. При иммуносупрессии она приобрела Leishmania , второе оппортунистическое заболевание. Точно так же можно утверждать, что в прошлом пациент был инфицирован бессимптомно и, таким образом, антитела к Leishmania не были обнаружены [18], [19].
Хотя это кажется разумным альтернативным объяснением, есть несколько причин в пользу гипотезы Leishmania как начального события, вызывающего весь синдром.Во-первых, изначально отрицательный анализ на Leishmania не подтверждает наличие скрытой инфекции, а скорее указывает на острую инфекцию с ложноотрицательными результатами. В предыдущих сообщениях о HLH и лейшманиозе описывались пациенты, получавшие иммуносупрессивные препараты для лечения HLH, вплоть до постановки окончательного диагноза через несколько месяцев [10]. Во-вторых, вероятность того, что у пациента было два сопутствующих очень редких заболевания — идиопатический HLH и оппортунистический лейшманиоз, — маловероятна. В-третьих, тот факт, что окончательно диагностированная инфекция Leishmania проявлялась точно такими же признаками и симптомами, что и первичный HLH, а также факт быстрого разрешения всего синдрома при соответствующей терапии (липосомальный амфотерицин B) и излечении. (в настоящее время пациент находится в ремиссии более двух лет), также поддерживает эту теорию.
Чтобы определить заболевание как первичное или идиопатическое, необходимо исключить все явные или редкие причины. Важно повторить анализы крови и повторить биопсию предполагаемых органов. Повторная аспирация костного мозга, обычно безопасная процедура [20], кажется наиболее эффективным методом последующего наблюдения. При обнаружении гемофагоцитоза могут потребоваться последовательные повторные аспирации, чтобы выявить его вторичную этиологию [10], [21], [22].
У всех взрослых пациентов может не быть четкого диагноза ГЛГ.В большой серии случаев у 20 из 34 пациентов с HLH не было выявлено основной этиологии [23]. Специфической особенности HLH нет, но болезнь часто заканчивается летальным исходом, поэтому своевременная диагностика обязательна. Диагностические рекомендации были разработаны исследовательской группой HLH в 1991 г. [6], включая клинические, лабораторные и гистопатологические данные (вставка 1). Заболевание может быть недооценено, поскольку лечащие врачи не часто учитывают его при дифференциальной диагностике пациентов-кандидатов [2], [6].Некоторые пациенты могут выражать один или несколько диагностических критериев на поздних стадиях заболевания. Таким образом, при отсутствии какого-либо специфического маркера заболевания у педиатрических пациентов лечение может быть начато на основании сильного клинического подозрения на первичный HLH, прежде чем подавляющая активность болезни вызовет необратимые повреждения и вероятность ответа на лечение будет меньше [2 ], [9], [21]. Можно ли применить это правило к взрослым пациентам, у которых ГЛГ почти всегда вторичен, следует рассматривать индивидуально.
Следовательно, лечение HLH зависит от его причины. Инфекционные, неопластические или аутоиммунные причины следует лечить незамедлительно, а также проводить поддерживающую терапию. Рандомизированных исследований первичного ГЛГ нет из-за редкости этого заболевания. Лечение основано на комбинации подавления иммунитета (например, циклоспорина А) и химиотерапии (например, этопозида) [22], [23]. Также могут быть полезны внутривенные иммуноглобулины. План комбинированного лечения (например, протокол HLH-2004) описан на странице протокола веб-сайта Общества гистиоцитов [23].
Выводы
Гемофагоцитоз, будучи редким сам по себе, является диагнозом, который обычно ставится тяжелобольным госпитализированным пациентам. Лейшманиоз, эндемичный в определенных регионах, но редко встречающийся в большинстве промышленно развитых стран, поэтому может быть слишком редким для лечащего врача в стационаре. Таким образом, в этой настройке диагноз может быть отложен. У описанной выше пациентки предварительный диагноз первичного или семейного HLH вместе с предполагаемым клиническим улучшением при иммуносупрессивной терапии, возможно, первоначально спас ей жизнь.Тем не менее, это лечение внесло большой вклад в отсрочку постановки правильного диагноза. Возможно, спленэктомия или биопсия селезенки (обе из которых имеют значительный риск у пациентов с панцитопенией) могли бы выявить правильный диагноз раньше.
Необходимо извлечь несколько уроков (см. Основные обучающие моменты). ГЛГ — это тяжелое заболевание, которое необходимо выявлять и лечить в кратчайшие сроки. Диагноз может быть трудоемким и труднодостижимым, но следует постоянно искать первоисточник, особенно для неизвестных патогенов.Лечение следует начинать без промедления, однако следует иметь в виду, что использование иммуносупрессии может еще больше отсрочить постановку диагноза и окончательное лечение.
Ключевые моменты обучения
Сокращения
| CMV | цитомегаловирус |
| DIC | диссеминированного внутрисосудистого свертывания крови вируса |
| EBV | Эпштейна-Барр |
| HLH | гемофагоцитарный лимфогистиоцитоз |
| LFT | функциональный тест печени |
Сноски
Авторы заявили, что не существует конкурирующих интересов.
У этой рукописи не было специального финансирования, и ни один финансирующий агент не участвовал в подготовке статьи.
Источник: Не сдан в эксплуатацию; внешняя экспертная оценка
Ссылки
1. Фавара Б. Гемофагоцитарный лимфогистиоцитоз: гемофагоцитарный синдром. Semin Diagn Pathol. 1992; 9: 63–74. [PubMed] [Google Scholar] 2. Henter JI, Aricò M, Egeler RM, Elinder G, Favara BE и др. HLH-94: протокол лечения гемофагоцитарного лимфогистиоцитоза. Группа изучения HLH Общества гистиоцитов.Med Pediatr Oncol. 1997. 28: 342–347. [PubMed] [Google Scholar] 3. Арико М., Янка Дж., Фишер А., Хентер Дж. И., Бланш С. и др. Гемофагоцитарный лимфогистиоцитоз: диагностика, лечение и факторы прогноза. Отчет о 122 детях из международного реестра. Лейкемия. 1983; 10: 197–203. [PubMed] [Google Scholar] 4. Янка Г.Е. Семейный гемофагоцитарный лимфогистиоцитоз. Eur J Pediatr. 1983; 140: 221–230. [PubMed] [Google Scholar] 5. [Авторы не указаны] Синдромы гистиоцитоза у детей. Группа писателей Общества гистиоцитов.Ланцет. 1987; 1: 208–209. [PubMed] [Google Scholar] 6. Henter J-I, Elinder G, Ost Å. Рекомендации по диагностике гемофагоцитарного лимфогистиоцитоза. Группа изучения FHL Общества гистиоцитов. Семин Онкол. 1991; 18: 29–33. [PubMed] [Google Scholar] 7. Филипович АХ. Гемофагоцитарный лимфогистиоцитоз и связанные с ним нарушения. Curr Opin Allerg Clin Immunol. 2006; 6: 410–415. [PubMed] [Google Scholar] 8. Имашуку С., Курияма К., Сакаи Р., Накао Ю., Масуда С. и др. Лечение гемофагоцитарного лимфогистиоцитоза, связанного с вирусом Эпштейна-Барра (EBV-HLH), у молодых людей: отчет центра исследований HLH.Med Pediatr Oncol. 2003. 41: 103–109. [PubMed] [Google Scholar] 10. Gagnaire MH, Galambrun C, Stephan JL. Гемофагоцитарный синдром: вводящее в заблуждение осложнение висцерального лейшманиоза у детей — серия из 12 случаев. Педиатрия. 2000; 106: E58. [PubMed] [Google Scholar] 11. Мацнер Ю., Бехар А., Бери Э, Гундерс А. Е., Хершко С. Системный лейшманиоз, имитирующий злокачественный гистиоцитоз. Рак. 1979; 43: 398–402. [PubMed] [Google Scholar] 12. Бутани В., Датта Ю., Дас Р., Сингх К. Гемофагоцитарный синдром как проявление висцерального лейшманиоза.J Assoc Physitors Индия. 2002; 50: 838–839. [PubMed] [Google Scholar] 13. Kaito K, Kobayashi M, Katayama T, Otsubo H, Ogasawara Y и др. Факторы прогноза гемофагоцитарного синдрома у взрослых: Анализ 34 случаев. Eur J Haematol. 1997. 59: 247–253. [PubMed] [Google Scholar] 14. Goldschmidt N, Amir G, Krieger M, Gilead L, Paltiel O. Фатальный гемофагоцитарный синдром у пациента с панникулитоподобной Т-клеточной лимфомой и без клинических признаков заболевания. Лимфома лейка. 2003; 44: 1803–1806. [PubMed] [Google Scholar] 15.Крейг Ф., Клэр Н., Склар Дж., Бэнкс П. Т-клеточная лимфома и вирус-ассоциированный гемофагоцитарный синдром. Am J Clin Pathol. 1991; 97: 189–194. [PubMed] [Google Scholar] 16. Хименес М., Феррер-Дюфол М., Канявате С., Гутьеррес-Солар Б., Молина Р. и др. Вариабельность Leishmania (Leishmania) infantu m среди стада от иммунокомпетентных пациентов и собак в Испании. FEMS Microbiol Lett. 1995; 131: 197–204. [PubMed] [Google Scholar] 17. Вайссер М., Ханлари Б., Терраччиано Л., Арбер С., Гратволь А. и др.Висцеральный лейшманиоз: угроза для пациентов с ослабленным иммунитетом в неэндемичных регионах? Clin Microbiol Infect. 2007. 13: 751–753. [PubMed] [Google Scholar] 18. Castellino G, Govoni M, Lo Monaco A, Montecucco C, Colombo F и др. Висцеральный лейшманиоз, осложняющий заболевание соединительной ткани: три клинических случая из Италии. Волчанка. 2004. 13: 201–203. [PubMed] [Google Scholar] 20. Bain BJ. Заболеваемость, связанная с аспирацией костного мозга и трепанобиопсией — обзор данных Великобритании за 2004 г. Haematologica. 2006. 91: 1295–1296.[PubMed] [Google Scholar] 21. Гольдшмидт Н., Гурал А., Корнберг А., Спектр Г., Шопен А. и др. Длительная лихорадка неизвестного происхождения и гемофагоцитоз, переходящий в острый лимфобластный лейкоз. Am J Hematol. 2004. 76: 364–367. [PubMed] [Google Scholar] 22. Хентер Дж. И., Хорн А., Арико М., Эгелер Р. М., Филипович А. Х. и др. HLH-2004: Руководство по диагностике и лечению гемофагоцитарного лимфогистиоцитоза. Педиатр Рак крови. 2007. 48: 124–131. [PubMed] [Google Scholar]
Проявления печени при гематологических заболеваниях
Abstract
Поражение печени часто наблюдается при нескольких гематологических заболеваниях, что приводит к аномальным функциональным тестам, отклонениям в исследованиях изображений печени или клиническим симптомам, проявляющимся в печени.При гемолитической анемии желтуха и гепатоспленомегалия часто напоминают заболевания печени. При гематологических злокачественных новообразованиях злокачественные клетки часто инфильтрируют печень и могут демонстрировать аномальные результаты тестов функции печени, сопровождающиеся гепатоспленомегалией или образованием множественных узелков в печени и / или селезенке. В дальнейшем эти случаи могут перерасти в фульминантную печеночную недостаточность.
1. Введение
Гепатологи или терапевты иногда сталкиваются с печеночными проявлениями различных гематологических нарушений в повседневной практике, включая различные отклонения в тестах функции печени или визуализирующих исследованиях печени.Некоторые гематологические нарушения также имитируют заболевания печени. Хотя обзорные статьи о гематологических нарушениях и заболеваниях печени публиковались ранее [1–3], мы также рассматриваем более свежие темы в этой статье.
2. Нарушения эритроцитов (эритроцитов)
2.1. Гемолитическая анемия (HA)
2.1.1. Классификация по сайту разрушения эритроцитов
При серьезном повреждении мембраны эритроцитов в кровотоке происходит немедленный лизис (внутрисосудистый гемолиз).В случаях менее серьезного повреждения клетки могут разрушаться внутри моноцитарно-макрофагальной системы в селезенке, печени, костном мозге и лимфатических узлах (внесосудистый гемолиз) [4–6].
2.1.2. Клиническая картина
Пациенты с ГК обычно обращаются со следующими признаками: быстрое начало анемии, желтуха, пигментные (билирубиновые) желчные камни в анамнезе и спленомегалия. Также может возникнуть легкая гепатомегалия [4].
2.1.3. Тесты функции печени на HA
При гемолизе уровни сывороточной лактатдегидрогеназы (ЛДГ) (особенно изоформ ЛДх2 и ЛДх3) повышаются из-за лизированных эритроцитов [4].Уровни аспартаттрансаминазы (AST) в сыворотке также слегка повышаются при гемолизе, причем соотношение LDH / AST в большинстве случаев превышает 30 [7]. Уровень общего билирубина редко может превышать 5 мг / дл при нормальной функции печени, за исключением случаев острого гемолиза, вызванного серповидно-клеточным кризом. Дисфункция печени также может быть вызвана переливанием крови при анемии при серповидно-клеточной анемии (ВСС) и талассемии [1, 3].
2.1.4. Гемолиз при заболевании печени
Гемолиз может быть вызван либо аномалиями мембран эритроцитов (внутренними), либо факторами окружающей среды (внешними).Большинство внутренних причин являются наследственными, за исключением пароксизмальной ночной гемоглобинурии (ПНГ) или редких состояний приобретенной альфа-талассемии [4].
Внешний HA вызывается иммунными или неиммунными механизмами. Внешний неиммунный HA вызывается системными заболеваниями, включая некоторые инфекционные заболевания и заболевания печени или почек. Различные заболевания печени могут индуцировать HA, и две основные причины внешнего HA у пациентов с заболеванием печени — это разрушение эритроцитов в увеличенной селезенке (гиперспленизм) и приобретенные изменения в мембране красных клеток (например,g., клетки-мишени, акантоциты, эхиноциты и стоматоциты). Заболевания печени, особенно вызванные алкогольной интоксикацией, вызывают тяжелую гипофосфатемию [8–10], которая, предположительно, приводит к снижению уровня аденозинтрифосфата в эритроцитах, что ведет к хрупкости и сфероидности мембран эритроцитов. Эти эритроциты легко захватываются селезенкой из-за их пониженной деформируемости. Когда преобладающей причиной является чрезмерное употребление алкоголя, состояние быстро улучшается после прекращения употребления алкоголя.
Синдром Зиве — плохо изученное заболевание, характеризующееся ожирением печени / циррозом, сильной болью в верхней части живота и правом подреберье, желтухой, гиперлипидемией и HA [11–13].
2.2. Аутоиммунный HA (AIHA)
AIHA характеризуется повышенным разрушением эритроцитов за счет аутоантител с активацией комплемента или без нее. Диагностика АИГА включает сочетание клинических и лабораторных признаков гемолиза эритроцитов вместе с обнаружением аутоантител и / или отложением комплемента на эритроцитах, обнаруживаемых с помощью прямого антиглобулинового теста, также известного как прямой тест Кумбса [14].Более чем у половины пораженных пациентов АИГА связан с основным заболеванием, включая какой-либо тип инфекционного заболевания, иммунного расстройства или лимфопролиферативного заболевания (вторичный АИГА), тогда как у других пациентов отсутствуют какие-либо признаки основного заболевания (идиопатического или первичного АИГА). [15].
2.2.1. Тесты функции печени в AIHA
Лабораторные данные AIHA не отличаются от результатов других причин гемолиза, то есть снижения уровня гаптоглобина в сыворотке, непрямой билирубинемии и повышенных уровней ЛДГ в сыворотке (преобладание I> II) и АСТ (в основном ЛДГ). / AST> 30).Общий билирубин в сыворотке редко превышает 5 мг / дл, часто наблюдается поликлональная гипергаммаглобулинемия.
2.2.2. Печеночная недостаточность в AIHA
Иммуноглобулин (Ig) G-антитела (редко антитела IgM) обычно реагируют с антигенами на поверхности эритроцитов при температуре тела и поэтому называются «теплыми агглютининами», тогда как антитела IgM (редко типа IgG) реагируют с антигенами. на поверхности эритроцитов ниже температуры тела и поэтому называются «холодовыми агглютининами». Тепло реагирующие антитела IgM могут приводить к печеночной недостаточности in vivo аутоагглютинации [16].Сообщалось о летальном случае, когда первичный АИГА проявлялся острой печеночной недостаточностью [16]. У пациента наблюдались повторяющиеся эпизоды внутрисосудистого гемолиза. Несмотря на терапию кортикостероидами, спленэктомию и многократные переливания крови, пациент в конечном итоге скончался от печеночной недостаточности.
2.3. PNH
PNH — это необычный тип приобретенного гемолиза, который встречается у взрослых людей среднего возраста [17, 18]. Пациенты обращаются с темной мочой (гемоглобинурия), обычно это утренние пробы. Было доказано, что ПНГ является приобретенным клональным генетическим заболеванием, вызванным соматической мутацией X-сцепленного гена PIG-A в гемопоэтических стволовых клетках [19].
2.3.1. Клиническая картина
Клинические проявления ПНГ в первую очередь связаны с нарушениями функции кроветворения, ГК, состоянием гиперкоагуляции, гипоплазией или аплазией костного мозга и прогрессированием до миелодиспластического синдрома или острого лейкоза [18].
2.3.2. Диагноз ПНГ
ПНГ ранее ставился косвенно на основании чувствительности эритроцитов ПНГ к лизированию комплементом. Тест на лизис сахарозы используется в качестве скринингового теста, а диагноз подтверждается тестом на кислотный гемолиз Хэма [20–22].Однако обнаружение дефицита гликозилинозитолфосфолипидного белка при ПНГ с помощью проточного цитометрического анализа было разработано для диагностики [23].
2.3.3. ПНГ-ассоциированное заболевание печени
Одним из серьезных осложнений ПНГ является развитие состояния гиперкоагуляции и образование тромбов. Тромбоз при ПНГ обычно возникает во внутричерепных, печеночных или воротных сосудах. ПНГ является одной из наиболее частых причин появления тромбоза воротной вены de novo и редкой причиной синдрома Бадда-Киари [24].
2.4. Серповидноклеточная болезнь (SCD)
SCD — это аутосомно-рецессивное генетическое заболевание, возникающее в результате наследования варианта гемоглобина S (Hb S) цепи β -глобина. Наиболее тяжелая форма с гомозиготностью по Hb S (Hb SS) называется серповидноклеточной анемией (SCA). Менее тяжелые формы обладают гетерозиготностью по Hb S и C (Hb SC) или Hb β -талассемия (Hb β -thal). Эритроциты деформируются до серповидной формы, склонны к гемолизу, часто образуя скопления в сосудистой сети (вазоокклюзионный криз), вызывая повреждение органов [25].
2.4.1. Проявление печени при SCD
Печень может быть поражена заболеванием с сосудистыми осложнениями от серповидного процесса. Более того, многократные переливания крови, необходимые для лечения, могут увеличить риск вирусного гепатита, перегрузки железом и развития пигментированных желчных камней, все из которых может способствовать развитию заболевания печени, называемого «серповидноклеточная гепатопатия» [26–28]. Острая боль в животе и аномальные тесты функции печени, а также желтуха могут быть вызваны острым серповидно-печеночным кризом, серповидноклеточным внутрипеченочным холестазом, холециститом и холедохолитиазом с обструкцией общего желчного протока.
2.4.2. Функциональные тесты печени при ВСС
Нарушения функциональных тестов печени часто встречаются у пациентов с ВСС. Повышение непрямого билирубина, ЛДГ и АСТ без других признаков заболевания печени обнаруживается у 72% пациентов с ВКА, что связано с гемолизом и / или неэффективным эритропоэзом [29]. Концентрация общего билирубина обычно <6 мг / дл, но может удвоиться (<15 мг / л) во время серповидно-печеночного криза [30]. Уровни АЛТ в сыворотке могут более точно отражать повреждение гепатоцитов [29].Щелочная фосфатаза (ЩФ) в сыворотке крови, преимущественно костного происхождения, обычно повышена [31].
Острое повышение сывороточной аминотрансферазы может наблюдаться при ишемии печени при вазоокклюзионном кризе, тогда как хронические нарушения функции печени обнаруживаются у 9–25% пациентов [29, 32], обычно вызванные сопутствующими заболеваниями печени, такими как хронические гепатит B или C, непроходимость общего желчного протока или употребление алкоголя.
2.4.3. Гипераммониемия из-за дефицита цинка при SCD
Низкие уровни цинка в плазме наблюдаются у 44% пациентов с SCD [33], что может привести к развитию энцефалопатии из-за гипераммонемии у пациентов с циррозом и SCA, которую можно исправить введением цинка [34] .
2.4.4. Визуализирующие исследования печени при SCD
Результаты компьютерной томографии пациентов с гомозиготной SCA выявляют диффузную гепатомегалию. Селезенка обычно небольшая, атрофическая и может иметь плотные кальцификаты из-за повторного инфаркта селезенки. Двойные гетерозиготы (Hb SC и Hb S β -thal) обычно имеют спленомегалию и могут проявлять инфаркт, разрыв, кровотечение или абсцесс селезенки.
МРТ может показывать снижение интенсивности сигнала в печени и поджелудочной железе [35] из-за отложения железа у пациентов с ВСС, получающих хронические переливания крови [36–39].УЗИ брюшной полости может выявить камни в желчном пузыре или повышенную эхогенность печени и поджелудочной железы из-за отложений железа [37].
3. Нарушения свертывания крови
3.1. Диссеминированная внутрисосудистая коагуляция (ДВС)
ДВС — системный процесс, вызывающий как тромбоз, так и кровотечение. Патогенез ДВС-синдрома обусловлен, прежде всего, чрезмерной выработкой тромбина, что приводит к широко распространенному и системному внутрисосудистому образованию тромбов. Основными инициирующими факторами являются высвобождение или экспрессия тканевого фактора, вторичного по отношению к обширному повреждению эндотелия сосудов, или усиленная экспрессия моноцитами в ответ на эндотоксин и различные цитокины.Наиболее частыми причинами ДВС-синдрома являются сепсис, травмы и разрушение тканей, рак и акушерские осложнения.
3.1.1. Диагностика ДВС-синдрома
Диагноз ДВС-синдрома предполагает наличие анамнеза и симптомов, тромбоцитопении и наличия микроангиопатических изменений в мазке крови. Диагноз подтверждается лабораторными тестами, которые демонстрируют доказательства как увеличения образования тромбов (например, снижение фибриногена), так и увеличения фибринолиза (например, повышение количества продуктов распада фибрина или D-димера).
3.1.2. Проявление печени в DIC
Желтуха часто встречается у пациентов с ДВС-синдромом и может быть вызвана повреждением печени и повышенным продуцированием билирубина вследствие гемолиза. Кроме того, гепатоцеллюлярное повреждение может быть вызвано сепсисом и гипотонией. Общие проявления острого ДВС-синдрома, помимо кровотечения, включают тромбоэмболию и дисфункцию почек, печени, легких и центральной нервной системы. В серии из 118 пациентов с острым ДВС-синдромом нарушение функции печени было обнаружено у 19% [38].Тяжелое заболевание печени включает снижение синтеза факторов и ингибиторов свертывания крови [39], фибринолиз, фибриногенолиз и повышенные уровни продуктов распада фибрина. Тромбоцитопения может быть вызвана гиперспленизмом, вторичным по отношению к портальной гипертензии.
3.2. Синдром антифосфолипидных антител (APS)
Синдром антифосфолипидных антител (APS) или синдром APLA характеризуется присутствием одного из антифосфолипидных антител (aPL) в плазме и возникновением любых клинических проявлений, включая венозные или артериальные тромбозы или заболеваемость беременностью. .
3.2.1. Клиническая картина
APS возникает как первичный или вторичный из основных заболеваний, таких как системная красная волчанка (СКВ). В серии первичных или вторичных АФС, тромбоз глубоких вен (ТГВ) (32%), тромбоцитопения (22%), ретикулярная ливедо (20%), инсульт (13%), поверхностный тромбофлебит (9%), тромбоэмболия легочной артерии (9%) , потеря плода (8%), транзиторная ишемическая атака (7%) и гемолитическая анемия (7%) часто наблюдаются [40], а венозные тромбозы встречаются чаще, чем артериальные тромбозы [41, 42].Хотя наиболее частыми участками, где возникает ТГВ, являются икры и почечные вены, также могут быть поражены печеночные, подмышечные, подключичные и сетчатые вены, пазухи головного мозга и полая вена.
3.2.2. Проявление печени в APS
Поражение печени может включать тромбоз печени или воротной вены, который может приводить к синдрому Бадда-Киари, веноокклюзионной болезни печени, инфаркту печени, портальной гипертензии и циррозу. [40, 43].
3.3. Синдром HELLP
Синдром HELLP определяется гемолизом с микроангиопатическим мазком крови, повышенными ферментами печени и низким количеством тромбоцитов [44].HELLP-синдром встречается примерно у 1-2 на 1000 беременностей и у 10-20 процентов женщин с тяжелой преэклампсией / эклампсией.
3.3.1. Клиническая картина
Наиболее частыми клиническими проявлениями являются боль в животе [45], тошнота, рвота и недомогание, которые могут напоминать вирусный гепатит, особенно если уровни АСТ и ЛДГ в сыворотке заметно повышены [46]. Гипертония и протеинурия присутствуют примерно в 85 процентах случаев. Дифференциальный диагноз включает острую жировую болезнь печени при беременности (ОЖП).Увеличение протромбинового времени, активируемое частичным тромбопластиновым временем (АЧТВ), низкие концентрации глюкозы и повышенные концентрации креатинина чаще встречаются у женщин с AFLP, чем у женщин с HELLP.
3.3.2. Печеночные проявления при HELLP-синдроме
HELLP-синдром и тяжелая преэклампсия могут быть связаны с печеночными проявлениями, включая инфаркт, кровотечение и разрыв.
4. Криоглобулинемия
4.1. Определение и классификация
Осадки в сыворотке при температуре ниже 37 ° C относятся к криоглобулину (CG).ХГ состоит из иммуноглобулина (Ig) и компонентов комплемента [47], а криоглобулинемия относится к наличию ХГ в сыворотке крови пациента. Согласно классификации Бруэ, основанной на клональности Ig [48], существует три типа ХГ. Тип I CG (моноклональный Ig) обычно связан с гематологическим злокачественным новообразованием, таким как макроглобулинемия Вальденстрема или множественная миелома. CG типа II (поликлональный и моноклональный Ig) часто является вторичным по отношению к хроническим инфекциям, таким как гепатит C или инфекция вируса иммунодефицита человека.CG типа III (поликлональный Ig) часто является вторичным по отношению к системным ревматическим заболеваниям.
4.2. Клиническая презентация
Клинические признаки ХГ типа I (моноклональные Ig) включают синдром повышенной вязкости, вызванный гематологическими злокачественными новообразованиями. В то время как CG типа II и III (смешанный и поликлональный Ig, соответственно) присутствуют с «триадой Мельцера» пальпируемой пурпуры, артралгии и миалгии, вызванной васкулитом в сосудах малого и среднего размера [49].
Вторичные лимфопролиферативные расстройства встречаются менее чем у 5–10 процентов пациентов с ХГ типа II через 5–10 лет после постановки диагноза [50–52].Первичные злокачественные новообразования включают В-клеточную неходжкинскую лимфому, лимфому средней и высокой степени злокачественности и лимфому низкой степени злокачественности, такую как иммуноцитома, лимфоидные опухоли, связанные со слизистой оболочкой, и центроцитарную фолликулярную лимфому. Среди пациентов с криоглобулинемией II типа, связанной с гепатитом С, частота неходжкинской лимфомы оценивается в 35 раз выше, чем в общей популяции.
4.3. Криоглобулинемия при инфекции ВГС
Патогенез ХГ наиболее изучен при хронической инфекции ВГС.Гиперактивация В-клеток может быть результатом инфицирования В-клеток вирусом гепатита С через белок клеточной поверхности CD81 [53], хронической антиген-неспецифической стимуляции макромолекулярными комплексами сыворотки, содержащими ВГС, включая ВГС-IgG и ВГС-липопротеин [54, 55], или от антиген-специфический механизм HCV [56], приводящий к размножению специфических клонов B-клеток, экспрессирующих идиотип WA [57] или V (H) 1-69 [58]. Частицы HCV часто обнаруживаются в комплексах CG, но развитие CG при инфекции гепатита C не обязательно требует вириона HCV или его компонентов [59].
Среди пациентов с инфекцией ВГС количество циркулирующих регуляторных Т-клеток сравнивали между пациентами с симптоматической и бессимптомной ХГ [60], и было обнаружено, что средние уровни регуляторных Т-клеток были значительно ниже у пациентов с симптоматической ХГС-ассоциированной ХГ чем бессимптомные предметы.
4.4. Печеночная манифестация криоглобулинемии
Сообщалось о печеночных проявлениях в виде гепатомегалии, аномальных функциональных тестов печени или аномальной биопсии печени, до 90 процентов которых, возможно, были вызваны самим хроническим гепатитом [61].
5. Гематологические новообразования
5.1. Классификация новообразований кроветворного происхождения
Новообразования, происходящие из кроветворных и лимфоидных тканей, классифицируются в соответствии с их морфологическими, иммунофенотипическими, генетическими и клиническими особенностями, а также по типу происхождения клеток и стадии дифференцировки в соответствии с широко используемыми и принятыми Всемирной организацией здравоохранения система классификации 2001 г., обновленная в 2008 г. [62].
Миелоидные новообразования включают хронические миелопролиферативные новообразования (MPN), MDS или острые лейкемии с миелоидными линиями.Лимфоидные новообразования подразделяются на острый лимфобластный лейкоз / лимфому, происходящие от предшественников В- или Т-лимфоидов, или на опухоли, происходящие из зрелых Т- или В-лимфоцитов, включая плазматические клетки. Новообразования гистиоцитарных / дендритных клеток происходят из антигенпрезентирующих клеток или тканевых макрофагов. Редкие случаи не поддаются классификации по миелоидной или лимфоидной линии [62].
6. Миелоидные новообразования
Хронические MPN, также называемые миелопролиферативными заболеваниями, классически включают хронический миелоидный лейкоз (CML), истинную полицитемию (PV), эссенциальную тромбоцитемию и первичный идиопатический миелофиброз.
6.1. CML
CML — это MPN, характеризующийся нарушением регуляции продукции и неконтролируемой пролиферацией зрелых и незрелых гранулоцитов с нормальной морфологией. Опухолевые клетки происходят из плюрипотентной гемопоэтической стволовой клетки, имеющей приобретенный гибридный ген BCR-ABL1 , обычно посредством транслокации между хромосомами 9 и 22, t (9; 22) (q34; q11), именуемой филадельфийской (Ph ) хромосома. BCR-ABL1 индуцирует лейкемогенез через киназозависимые и независимые пути передачи сигналов.Естественное течение ХМЛ варьируется от хронической фазы до ускоренной фазы или взрывного кризиса, но процесс прогрессирования полностью не изучен [62].
6.1.1. Клинические симптомы и проявление ХМЛ в печени
На момент обращения у 20–50% пациентов симптомы отсутствуют. Лабораторные данные включают лейкоцитоз с незрелыми клетками гранулоцитарного ряда и базофилию, легкую анемию и тромбоцитоз. Симптомы включают усталость, недомогание, потливость и потерю веса.Боль в животе и дискомфорт могут возникать в левом верхнем квадранте (иногда относящемся к левому плечу), а также может присутствовать раннее насыщение из-за спленомегалии с периспленитом и / или инфарктом селезенки или без него. Также наблюдаются различные степени гепатомегалии. Болезненность в нижней части грудины иногда возникает из-за разрастания костного мозга, и часто встречаются эпизоды кровотечения из-за дисфункции тромбоцитов [63, 64].
В хронической фазе примерно у 50% пациентов с ХМЛ при поступлении наблюдается гепатомегалия от легкой до умеренной степени без нарушений функции печени [65].Однако во время бластного криза инфильтрация синусоид печени незрелыми клетками может привести к увеличению печени и повышению уровня ЩФ в сыворотке [66].
6.2. PV
PV является одним из хронических MPN, и клинические признаки включают повышенное количество эритроцитов, спленомегалию, тромбоцитоз и / или лейкоцитоз, тромботические осложнения, эритромелалгию или зуд. При физикальном обследовании спленомегалия, полнокровие лица (красный цианоз) и гепатомегалия выявляются у 70%, 67% и 40% пациентов соответственно [67].Непальпируемая спленомегалия распознается у большинства пациентов при визуализирующих исследованиях [68, 69].
Жалобы со стороны желудочно-кишечного тракта часто встречаются при ПВ, с высокой частотой эпигастрального дистресса, пептических язв и гастродуоденальных эрозий при эндоскопии верхних отделов желудка [70]. Они были приписаны изменениям кровотока в слизистой оболочке желудка из-за изменения вязкости крови и / или повышенного высвобождения гистамина из тканевых базофилов, хотя одно исследование показало высокую частоту положительного ответа на инфекцию Helicobacter pylori [70].Хотя прямое поражение печени встречается редко, у некоторых пациентов может развиваться острый или хронический синдром Бадда-Киари [71].
6.3. Первичный миелофиброз (PMF)
Первичный миелофиброз (PMF) — хроническое злокачественное гематологическое заболевание, характеризующееся спленомегалией, лейкоэритробластозом, фиброзом костного мозга и экстрамедуллярным гематопоэзом.
6.3.1. Проявление PMF в печени
На момент постановки диагноза PMF гепатомегалия наблюдается у 40–70% пациентов, а спленомегалия — как минимум у 90% [72–74].Гепатоспленомегалия вызывается выраженным экстрамедуллярным кроветворением, которое может развиться после спленэктомии, особенно в печени [75, 76]. В отчете о 10 пациентах с PMF значительное увеличение размера печени и сывороточных концентраций ALP, билирубина и / или γ -GTP было замечено у всех пациентов, у которых впоследствии развилась острая печеночная недостаточность, что привело к смерти 3 -4 недели после спленэктомии [76].
6.3.2. Аномальные функциональные тесты печени в PMF
Пациенты с PMF могут иметь неспецифические отклонения лабораторных тестов, включая повышение сывороточных концентраций ALP, LDH, мочевой кислоты, лейкоцитарной ALP и витамина B12 [77, 78].Повышение ЩФ может быть связано с поражением печени или костей, в то время как повышение ЛДГ может быть результатом неэффективного кроветворения.
6.4. MPN и тромбоз воротной вены
MPN могут быть нечастой причиной тромбоза тирозинкиназы воротной вены (V617F) неясной этиологии [79–81]. В таких случаях может быть обнаружена мутация JAK2 [82, 83].
6.5. MPN и синдром Бадда-Киари
Мутация JAK2 может быть обнаружена почти у всех пациентов с PV и примерно у 50 процентов пациентов с эссенциальной тромбоцитемией (ET) или PMF. JAK2 Мутации (V617F) были описаны у 26-59 процентов пациентов с синдромом Бадда-Киари без видимых обнаружений MPN [84–87]. Эти данные предполагают наличие скрытых MPN у некоторых пациентов с так называемым «идиопатическим» синдромом Бадда-Киари.
7. Лимфоидные новообразования
7.1. Лимфома Ходжкина (HL)
HL, ранее называвшаяся болезнью Ходжкина, является первой выявленной лимфоидной опухолью, которая обычно возникает в лимфатических узлах и распространяется непрерывно через лимфатическую систему.HL гистологически характеризуется гигантскими клетками, называемыми клетками Ходжкина / Рида-Штернберга (H / RS), большинство из которых представляют собой трансформированные вирус-положительные В-клетки Эпштейна-Барра, присутствующие в реактивном клеточном фоне, состоящем из гранулоцитов, плазматических клеток и лимфоцитов.
7.1.1. Печеночные проявления HL
Инфильтрация злокачественных клеток в печени наблюдалась у 14% пациентов с HL. Гепатомегалия обнаруживается у 9% пациентов с I-II стадиями заболевания и у 45% пациентов с III-IV стадиями [88].Легкое повышение аминотрансферазы и умеренное повышение ЩФ может происходить из-за инфильтрации опухолью или обструкции внепеченочных желчных протоков [88]. Холестаз может быть вызван прямой инфильтрацией клеток лимфомы, обструкцией внепеченочных желчных путей, вирусным гепатитом, гепатотоксичностью лекарств или синдромом исчезающих желчных протоков [89–91]. Приблизительно у 3–13% пациентов с HL наблюдается желтуха [90]. Острая печеночная недостаточность может быть вызвана ишемией, вторичной по отношению к сдавлению синусоидов печени инфильтрирующими клетками лимфомы [92, 93].
7.2. Неходжкинская лимфома (NHL)
NHL классифицируется по клеточной морфологии как мелкоклеточный тип, а также как крупноклеточный, а в соответствии с естественным течением клинической агрессивности заболевания — как низкий, средний или высокий.
7.2.1. Печеночная манифестация NHL
Инфильтрация лимфомными клетками печени с гепатомегалией чаще встречается в НХЛ, чем в HL, при этом в 16–43% случаев наблюдается поражение печени [88]. Внепеченочная обструкция также чаще встречается при НХЛ, чем при HL, а инфильтрация печени чаще встречается при B-клеточных лимфомах низкой степени, чем при лимфомах высокой степени [94].Острая печеночная недостаточность может возникать при НХЛ, как видно из HL [95], что вызвано внезапной ишемией, связанной с массивной инфильтрацией синусоидов или замещением паренхимы печени злокачественными клетками [95]. Хотя вовлечение печени в HL и NHL может проявляться как острая печеночная недостаточность [96–101], трансплантации печени следует избегать [102].
Острую печеночную недостаточность из-за лимфомы можно заподозрить в случаях острого начала увеличения печени и лактоацидоза, отличных от других причин печеночной недостаточности [2, 103].
7.2.2. Тесты на отклонение от нормы функции печени в NHL
Тесты функции печени у пациентов с NHL показывают повышение уровня ЩФ в сыворотке от легкого до умеренного [88]. Повышенный уровень ЛДГ в сыворотке также часто наблюдается у пациентов с НХЛ, особенно при высокоагрессивном типе, таком как лимфома Беркитта или лимфобластная лимфома, что отражает высокую опухолевую нагрузку, обширную инфильтрацию печени и сопутствующую иммуноопосредованную ГК, которые связаны с плохим прогнозом. .
7.2.3. Визуализирующие исследования печени в NHL
Хотя диффузная гепатоспленомегалия обычно наблюдается у пациентов с вялотекущими лимфомами, функция печени при НХЛ обычно сохраняется.С другой стороны, дискретные образования печени чаще встречаются у высокоагрессивных подтипов [104, 105]. Однако не все очаговые поражения печени у пациентов с НХЛ связаны с лимфомой. В отчете о 414 последовательных пациентах с НХЛ, только 39% очаговых поражений печени, обнаруженных в начале заболевания, были вызваны НХЛ и 58% были доброкачественными [106], тогда как 74% поражений, обнаруженных во время наблюдения, были вызваны НХЛ и 15% были связаны с НХЛ. из-за злокачественного новообразования, отличного от НХЛ (например, гепатоцеллюлярная карцинома, метастатическая опухоль из другого вторичного злокачественного образования).Асцит может присутствовать и может быть хилезным в случае лимфатической обструкции.
7.3. Первичная НХЛ печени
Первичная НХЛ печени — редкое заболевание, составляющее <1% всех экстранодальных лимфом. Две трети случаев возникают у мужчин в возрасте приблизительно 50 лет. Симптомы включают боль в животе, лихорадку, гепатомегалию и аномальные тесты функции печени с повышением уровня ЛДГ выше, чем у АЛТ [107, 108]. Наиболее распространенным гистологическим подтипом первичной НХЛ печени является диффузная В-крупноклеточная лимфома, составляющая 80–90% случаев.Это заболевание может проявляться узелками в печени или диффузной портальной инфильтрацией и синусоидальным распространением [109].
Острая печеночная недостаточность, вызванная первичной лимфомой печени, лечится с помощью трансплантации печени и последующей химиотерапии [110]. Хотя первичная лимфома печени встречается редко, стойкие воспалительные процессы, связанные с инфекцией ВГС или аутоиммунным заболеванием, могут играть роль в лимфомагенезе В-клеток печени [111].
7.4. Primary Hepatosplenic NHL
Сообщалось о первичной гепатоспленочной диффузной крупноклеточной B-лимфоме, ассоциированной с HCV [112], также может развиться острая печеночная недостаточность плода [113].Хотя этиологическая роль ВГС в лимфоме неизвестна, ВГС-положительные лимфомы, как правило, возникают в экстранодальных участках, особенно в печени, селезенке или слюнных железах, где находится ВГС и происходит хроническая инфильтрация лимфоцитов.
7,5. Внутрисосудистая диффузная крупноклеточная лимфома
Внутрисосудистая диффузная крупноклеточная лимфома или внутрисосудистая лимфома — редкое, но важное состояние у пациентов с быстро проявляющейся лихорадкой, сыпью или ишемическими, неврологическими или респираторными симптомами.При этом состоянии опухолевые клетки обычно развиваются исключительно в мелких сосудах кожи, головного мозга, печени или легких. Биопсия из этих органов необходима для гистологического диагноза.
Симптомы лихорадки, ночного потоотделения и потери веса наблюдаются у 55–85% пациентов с В-клеточной лимфомой [114, 115]. Пораженные органы различаются в зависимости от области. В западных странах чаще всего встречаются симптомы, связанные с центральной нервной системой (39%) и кожей (39%) [114, 116, 117], тогда как симптомы, связанные с костным мозгом (32%), печенью (26%), и селезенка (26%) встречаются реже.В Азии чаще встречаются симптомы, связанные с поражением костного мозга (75%), селезенки (67%) и печени (55%) [118–121], тогда как симптомы, связанные с поражением центральной нервной системы (27%) и кожи. поражения (15%) встречаются реже [122]. Гемофагоцитарный синдром также описан в японской серии (азиатский вариант) [120].
Диагноз внутрисосудистой крупноклеточной лимфомы может быть установлен путем случайной биопсии кожи [123] или биопсии органов, предположительно пораженных; например, биопсия печени, если наблюдаются необъяснимые нарушения функции печени, легкого, если присутствуют необъяснимые легочные симптомы, и мозга, если существуют необъяснимые неврологические симптомы [124–127].
7.6. Гепатоспленочная Т-клеточная лимфома
7.6.1. Клиническая презентация
Гепатоспленочная Т-клеточная лимфома — это редкий тип агрессивной НХЛ, связанный с пациентами, получающими терапию противоопухолевым фактором некроза альфа и аналогами пурина для лечения воспалительного заболевания кишечника [128].
7.6.2. Проявление гепатоспленической Т-клеточной лимфомы в печени
Клинические признаки включают гепатоспленомегалию, лихорадку, потерю веса, ночную потливость, панцитопению и периферический лимфоцитоз.Функциональные пробы печени повышены примерно у 50% пациентов с небольшим повышением АСТ, АЛТ или ЩФ. Уровни ЛДГ в сыворотке крови также повышены примерно у 50% пациентов, от умеренных до чрезвычайно высоких. Иммуносупрессия, особенно Т-лимфоцитов, с помощью терапии противоопухолевым фактором некроза альфа и аналогами пурина может увеличить риск этого заболевания [129].
7.7. Гемофагоцитарный синдром (ГПС)
7.7.1. Клиническая картина
HPS — это состояние, проявляющееся системными воспалительными симптомами, такими как лихорадка, гепатоспленомегалия, цитопения и гемофагоцитоз в костном мозге, селезенке и лимфатических узлах [130, 131].ГПС вызывается гиперцитокинемией, которая запускается сильно стимулированными естественными киллерами и цитотоксическими Т-клетками. Основные расстройства включают вирусные инфекции, обычно вирус Эпштейна-Барра у молодых пациентов, ревматические расстройства, синдромы иммунодефицита и агрессивные лимфомы [132]. Сообщалось, что агрессивная форма NK-клеточной лимфомы или внутрисосудистой лимфомы азиатского варианта осложняется HPS [133]. ГФС следует подозревать, если пациенты соответствуют по крайней мере пяти из следующих восьми критериев: лихорадка, спленомегалия, цитопения, гипертриглицеридемия, низкий уровень фибриногена, гемофагоцитоз при биопсии костного мозга, низкая или отсутствующая активность NK-клеток или повышенный уровень ферритина или растворимого рецептора IL2. [130].
7.7.2. Проявление HPS в печени
HPS может вызывать гепатомегалию, желтуху с холестазом, умеренное повышение уровня трансаминаз, гиперферритинемию, снижение синтетической функции печени и молниеносную печеночную недостаточность. Гепатотоксичность вызывается гемофагоцитозом синусоидов печени и воротных трактов или очаговым гепатоцеллюлярным некрозом [132].
8. Лейкемия
8.1. Острый лейкоз
8.1.1. Клиническая картина
Острые лейкозы — это новообразования, происходящие от предшественников миелоидной или лимфоидной линии (редко — неоднозначной).Хотя ОЛЛ является наиболее распространенным злокачественным новообразованием у детей, заболеваемость увеличивается также и у пожилых людей. Заболеваемость ОМЛ увеличивается с возрастом, и ОМЛ является наиболее распространенным типом лейкозов у взрослых.
8.1.2. Печеночные манифестации острого лейкоза
Хотя вовлечение печени при остром лейкозе обычно мягкое и бессимптомное на момент постановки диагноза [134], патологоанатомическое исследование показало инфильтрацию печени в> 95% случаев острого лимфобластного лейкоза (ОЛЛ) и до 75%. случаев острого миелоидного лейкоза (ОМЛ) [135].При ОЛЛ инфильтрация была ограничена воротными трактами, тогда как при ОМЛ инфильтрация наблюдалась как в воротных трактах, так и в синусоидах. Массивная инфильтрация печени лейкозными клетками может проявляться как фульминантная печеночная недостаточность [136]. У пациентов с острым лейкозом поражение печени, вызванное лекарственными препаратами, а также бактериальные или грибковые инфекции могут также влиять на печень.
8.1.3. ОМЛ и гепатоспленомегалия
Пальпируемая органегалия как проявление ОМЛ встречается редко, а значительное увеличение лимфатических узлов редко встречается у пациентов с ОМЛ.Заметная гепатоспленомегалия также встречается редко; однако, если он присутствует, у пациента скорее всего будет ОЛЛ или развитие ОМЛ в результате предшествующего миелопролиферативного расстройства (бластный кризис ХМЛ).
8.2. ОЛЛ у детей
При поступлении у детей с ОЛЛ могут быть отмечены несколько аномалий, включая дисфункцию печени, нарушения свертывания крови, гиперкальциемию, гипокальциемию, гиперкалиемию и гиперфосфатемию [137].
8.3. Предшественник B-ALL / лимфобластная лимфома (LBL) у взрослых
Предшественник B-клеточного ALL связан с уменьшением количества нормальных клеток крови, вызванным замещением костного мозга опухолевыми клетками.Клинические проявления пациентов включают анемию, склонность к кровотечениям или предрасположенность к инфекциям. Часто присутствуют B-симптомы, такие как лихорадка, ночная потливость и потеря веса, но могут быть легкими. Гепатомегалия, спленомегалия или лимфаденопатия могут наблюдаться почти у половины взрослых пациентов при поступлении.
8.4. Предшественник T-ALL / LBL
Предшественник T-ALL / LBL, происходящий из Т-клеток-предшественников тимуса, обычно встречается у мужчин в возрасте приблизительно 20 лет. Клиническая картина включает лимфаденопатию (50%) или объемное новообразование в переднем средостении (50–75%) [138].Поражение брюшной полости встречается редко, но может быть обнаружено в основном в печени и селезенке. Более 80% пациентов имеют III или IV стадию заболевания, и почти 50% имеют B-симптомы, а уровни ЛДГ в сыворотке обычно повышены. Несмотря на то, что костный мозг при обращении часто бывает нормальным, примерно у 60% пациентов развивается инфильтрация костного мозга и последующая лейкемическая фаза, неотличимая от Т-клеточного ОЛЛ [139].
8,5. Хронический лимфоидный лейкоз (ХЛЛ)
8.5.1.Клиническая презентация
Хронический лимфолейкоз (ХЛЛ) — одно из хронических лимфопролиферативных заболеваний, характеризующихся прогрессирующим накоплением моноклональных лимфоидных клеток. Считается, что ХЛЛ идентична малой лимфоцитарной лимфоме (SLL), которая является одной из вялотекущих неходжкинских лимфом [62, 140]. ХЛЛ — наиболее распространенная лейкемия в западных странах, на которую приходится примерно 30 процентов всех лейкозов в Соединенных Штатах. Хотя ХЛЛ-лимфоциты по морфологии напоминают нормальные маленькие лимфоциты, они являются активированными клональными В-клетками на стадии между пре-В и зрелыми В-клетками.[141–143]. Лимфоциты B-CLL положительны в отношении антигенов, связанных с B-клетками (CD19, CD20, CD21 и CD23) и CD5, и экспрессируют чрезвычайно низкие уровни поверхностных мембранных иммуноглобулинов (IgM или как IgM, так и IgD).
8.5.2. Клиническая стадия ХЛЛ
Естественное течение ХЛЛ неоднородно. Системами стадирования, которые широко используются для прогнозирования прогноза пациента и определения терапевтических стратегий, являются система Раи [144] и система Бине [145].
8.5.3. Клинические особенности CLL
Наиболее частым физическим признаком является лимфаденопатия, которая присутствует у 50–90 процентов пациентов.Другой лимфоидный орган, часто увеличивающийся при ХЛЛ, — это селезенка, которая пальпируется в 25–55% случаев.
8.5.4. Печеночные проявления ХЛЛ
Пациенты с ХЛЛ часто показывают увеличение печени от легкой до умеренной степени во время первоначального диагноза в 15–25% случаев [145, 146]. Печень обычно увеличена незначительно, от 2 до 6 см ниже правого реберного края, с диапазоном тупости до перкуссии примерно 10–16 см. При пальпации печень обычно безболезненная, твердая, с гладкой поверхностью.Увеличенная печень у пациентов с ХЛЛ часто проявляется обширной лимфоцитарной инфильтрацией в портальных трактах с функциональным нарушением печени на поздних стадиях [147, 148].
8.6. Волосатоклеточный лейкоз (HCL)
8.6.1. Клиническая картина
Клиническая картина HCL включает следующее [144, 149]: (1) переполнение живота из-за спленомегалии, которое может вызвать спонтанный разрыв селезенки [150], (2) системные симптомы, такие как усталость, слабость и потеря веса. без лихорадки или ночного потоотделения, (3) склонность к кровотечениям, вызванная тяжелой тромбоцитопенией или рецидивирующими инфекциями, и (4) бессимптомная спленомегалия или цитопения, которые могут быть обнаружены случайно, и наиболее частым физическим признаком HCL является пальпируемая спленомегалия (80–90%) случаев).Массивная спленомегалия, простирающаяся более чем на 8 см ниже левого реберного края, наблюдается в 25% случаев.
8.6.2. Проявление HCL в печени
Гепатомегалия и лимфаденопатия при HCL не характерны и проявляются примерно у 20% и 10% пациентов соответственно.
8.6.3. Результаты лабораторных исследований
У большинства пациентов с HCL наблюдаются панцитопения (60–80%), анемия (85%), тромбоцитопения и нейтропения (80%). Лейкоцитоз может присутствовать в 10–20% случаев.Аномальные функциональные пробы печени и гипергаммаглобулинемия наблюдаются в 20% случаев. Клетки лейкемии часто инфильтрируют печень как в портальных трактах, так и в синусоидах, а увеличение печени наблюдается у 40% пациентов [151].
Список литературы
1. Гитлин Н. Печень и системные заболевания . Нью-Йорк, Нью-Йорк, США: Черчилль Ливингстон; 1997. [Google Scholar] 3. Сингх М.М., Покрос П.Дж. Гематологические и онкологические заболевания и печени. Клиники болезней печени .2011; 15 (1): 69–87. [PubMed] [Google Scholar]
4. Актуальность. Подход к диагностике гемолитической анемии у взрослого. 2012.
5. Cazzola M, Beguin Y. Новые инструменты для клинической оценки функции эритрона у человека. Британский гематологический журнал . 1992. 80 (3): 278–284. [PubMed] [Google Scholar] 6. Босси Д., Джардина Б. Физиология красных клеток. Молекулярные аспекты медицины . 1996. 17 (2): 117–128. [PubMed] [Google Scholar]
7. Клинические справочники по идиопатическим гемопоэтическим нарушениям.при поддержке Министерства здравоохранения, труда и социального обеспечения Японии.
8. Актуальность. Внешняя неиммунная гемолитическая анемия, вызванная системным заболеванием. 2012.
9. Якоб HS, Амсден Т. Острая гемолитическая анемия с ригидными эритроцитами при гипофосфатемии. Медицинский журнал Новой Англии . 1971. 285 (26): 1446–1450. [PubMed] [Google Scholar] 10. Шило С., Вернер Д., Хершко С. Острая гемолитическая анемия, вызванная тяжелой гипофосфатемией при диабетическом кетоацидозе. Acta Haematologica .1985. 73 (1): 55–57. [PubMed] [Google Scholar] 11. Зиве Л. Желтуха, гиперлипемия и гемолитическая анемия: ранее нераспознанный синдром, связанный с алкогольной жировой дистрофией печени и циррозом. Анналы внутренней медицины . 1958; 48 (3): 471–496. [PubMed] [Google Scholar] 12. Мелроуз У.Д., Белл П.А., Юп ДМЛ, Байки МДж. Алкогольный гемолиз при синдроме Зиева: клиническое и лабораторное исследование пяти случаев. Клиническая и лабораторная гематология . 1990. 12 (2): 159–167. [PubMed] [Google Scholar] 13.Пиччини Дж., Халдар С., Джефферсон Б. Случаи из медицинской службы Ослера в университете Джона Хопкинса. Американский медицинский журнал . 2003. 115 (9): 729–731. [PubMed] [Google Scholar] 14. Zeerleder S. Аутоиммунная гемолитическая анемия — практическое руководство для решения диагностических и терапевтических задач. Нидерландский медицинский журнал . 2011. 69 (4): 177–184. [PubMed] [Google Scholar] 15. Engelfriet CP, Van’t Veer MB, Maas N, Ouwehand WH, Beckers D, Von dem Borne Kr. A.E.G. AEG. Аутоиммунные гемолитические анемии. Клиническая иммунология и аллергия Байера . 1987. 1 (2): 251–267. [Google Scholar] 16. Шири Р.С., Киклер Т.С., Белл В., Литтл Б., Смит Б., Несс П.М. Смертельная иммунная гемолитическая анемия и печеночная недостаточность, связанные с аутоантителами IgM, реагирующими на тепло. Vox Sanguinis . 1987. 52 (3): 219–222. [PubMed] [Google Scholar] 17. Socié G, Mary JY, De Gramont A и др. Пароксизмальная ночная гемоглобинурия: отдаленное наблюдение и прогностические факторы. Ланцет . 1996. 348 (9027): 573–577.[PubMed] [Google Scholar] 18. Де Латур Р.П., Мэри Дж. Ю., Саланубат С. и др. Пароксизмальная ночная гемоглобинурия: естественное течение подкатегорий болезней. Кровь . 2008. 112 (8): 3099–3106. [PubMed] [Google Scholar] 19. Росс ВФ. Пароксизмальная ночная гемоглобинурия как молекулярное заболевание. Медицина . 1997. 76 (2): 63–93. [PubMed] [Google Scholar] 20. Hartmann RC, Jenkins DE. Тест «сахар-вода» при пароксизмальной ночной гемоглобинурии. Медицинский журнал Новой Англии .1966. 275 (3): 155–157. [PubMed] [Google Scholar] 21. Хэм TH, Дингл JH. Исследования по разрушению красных кровяных телец. II. Хроническая гемолитическая анемия с пароксизмальной ночной гемоглобинурией: некоторые иммунологические аспекты гемолитического механизма с особым упором на сывороточный комплемент. Журнал клинических исследований . 1939. 18 (6): 657–672. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23. Актуально. Диагностика и лечение пароксизмальной ночной гемоглобинурии. 2012.
24.Шах А. Приобретенная гемолитическая анемия. Индийский журнал медицинских наук . 2004. 58 (12): 533–536. [PubMed] [Google Scholar]
25. Актуально. Обзор клинических проявлений серповидноклеточной анемии. 2012.
26. Банерджи С., Оуэн С., Чопра С. Серповидноклеточная гепатопатия. Гепатология . 2001. 33 (5): 1021–1028. [PubMed] [Google Scholar] 27. Берри PA, Cross TJS, Thein SL, et al. Нарушение функции печени при серповидно-клеточной анемии: новая система классификации
на основе глобальной оценки. Клиническая гастроэнтерология и гепатология . 2007. 5 (12): 1469–1476. [PubMed] [Google Scholar] 28. Эберт Э.С., Нагар М., Хагшпиль К.Д. Желудочно-кишечные и печеночные осложнения серповидноклеточной анемии. Клиническая гастроэнтерология и гепатология . 2010. 8 (6): 483–489. [PubMed] [Google Scholar] 29. Джонсон С.С., Омата М., Тонг М.Дж. Поражение печени при серповидно-клеточной анемии. Медицина . 1985. 64 (5): 349–356. [PubMed] [Google Scholar] 30. Sheehy TW. Серповидно-клеточная гепатопатия. Южный медицинский журнал .1977; 70 (5): 533–538. [PubMed] [Google Scholar] 31. Броуди Д.И., Райан В.Н., Хайдар М.А. Изоферменты щелочной фосфатазы сыворотки при серповидно-клеточной анемии. Журнал Американской медицинской ассоциации . 1975. 232 (7): 738–741. [PubMed] [Google Scholar] 32. ДеВолт К.Р., Фридман Л.С., Вестерберг С., Мартин П., Хосейн Б., Баллас СК. Гепатит С при серповидно-клеточной анемии. Журнал клинической гастроэнтерологии . 1994. 18 (3): 206–209. [PubMed] [Google Scholar] 33. Леонард МБ, Земель Б.С., Кавчак Д.А., Охене-Фремпонг К., Столлингс В.А.Статус цинка в плазме, рост и созревание у детей с серповидно-клеточной анемией. Педиатрический журнал . 1998. 132 (3): 467–471. [PubMed] [Google Scholar] 34. Прасад А.С., Раббани П., Варт Дж. Влияние цинка на гипераммониемию у субъектов с серповидно-клеточной анемией. Американский журнал гематологии . 1979. 7 (4): 323–327. [PubMed] [Google Scholar] 35. Гугре Н.Р., Вуд Дж.С. Калибровка релаксации-железа при перегрузке железом в печени: исследование основных биофизических механизмов с использованием модели Монте-Карло. Магнитный резонанс в медицине . 2011. 65 (3): 837–847. [Бесплатная статья PMC] [PubMed] [Google Scholar] 36. Hankins JS, Smeltzer MP, McCarville MB, et al. Особенности накопления железа в печени у пациентов с серповидноклеточной анемией и талассемией с перегрузкой железом. Европейский гематологический журнал . 2010. 85 (1): 51–57. [Бесплатная статья PMC] [PubMed] [Google Scholar] 37. Siegelman ES, Outwater E, Hanau CA, et al. Распределение железа в брюшной полости при серповидно-клеточной анемии: результаты МРТ у пациентов с переливанием и нетрансфузионной зависимостью. Журнал компьютерной томографии . 1994. 18 (1): 63–67. [PubMed] [Google Scholar] 38. Сигал Т., Селигсон У., Агай Э., Модан М. Клинические и лабораторные аспекты диссеминированного внутрисосудистого свертывания (ДВС): исследование 118 случаев. Тромбоз и гемостаз . 1978. 39 (1): 122–134. [PubMed] [Google Scholar] 39. Штейн С.Ф., Харкер Л.А. Кинетические и функциональные исследования тромбоцитов, фибриногена и плазминогена у пациентов с циррозом печени. Журнал лабораторной и клинической медицины .1982. 99 (2): 217–230. [PubMed] [Google Scholar] 40. Сервера Р., Пьетте Дж. К., Фонт Дж. И др. Антифосфолипидный синдром: клинические и иммунологические проявления и паттерны проявления заболевания в когорте из 1000 пациентов. Артрит и ревматизм . 2002. 46 (4): 1019–1027. [PubMed] [Google Scholar] 41. Ашерсон Р.А., Хамашта М.А., Орди-Рос Дж. И др. «Первичный» антифосфолипидный синдром: основные клинические и серологические признаки. Медицина . 1989. 68 (6): 366–374. [PubMed] [Google Scholar] 42.Gromnica-Ihle E, Schossler W. Антифосфолипидный синдром. Международный архив аллергии и иммунологии . 2000; 123: с. 67. [PubMed] [Google Scholar] 43. Усман I, Хамашта М. Абдоминальные проявления антифосфолипидного синдрома. Ревматология . 2007. 46 (11): 1641–1647. [PubMed] [Google Scholar] 44. Stone JH. HELLP-синдром: гемолиз, повышенные ферменты печени и низкие тромбоциты. Журнал Американской медицинской ассоциации . 1998. 280 (6): 559–562. [PubMed] [Google Scholar] 45.Сибай Б.М., Рамадан МК, Уста I, Салама М., Мерсер Б.М., Фридман С.А. Материнская заболеваемость и смертность при 442 беременностях с гемолизом, повышенными ферментами печени и низким уровнем тромбоцитов (синдром HELLP) Американский журнал акушерства и гинекологии . 1993. 169 (4): 1000–1006. [PubMed] [Google Scholar] 46. Катанзарит В.А., Стейнберг С.М., Мосли К.А., Ландерс К.Ф., Казинс Л.М., Шнайдер Дж.М. Тяжелая преэклампсия с молниеносным и резким повышением уровней аспартатаминотрансферазы и лактатдегидрогеназы: высокий риск материнской смерти. Американский журнал перинатологии . 1995. 12 (5): 310–313. [PubMed] [Google Scholar] 47. Рамос-Казальс М., Стоун Дж. Х., Сид М.К., Бош X. Криоглобулинемии. Ланцет . 2012. 379 (9813): 348–360. [PubMed] [Google Scholar] 48. Brouet JC, Clauvel JP, Danon F. Биологическое и клиническое значение криоглобулинов. Отчет о 86 случаях. Американский медицинский журнал . 1974. 57 (5): 775–788. [PubMed] [Google Scholar] 49. Росса А.Д., Тревизани Г., Бомбардиери С. Криоглобулины и криоглобулинемия: диагностические и терапевтические соображения. Клинические обзоры по аллергии и иммунологии . 1998. 16 (3): 249–264. [PubMed] [Google Scholar] 50. Инверницци Ф., Пиолтелли П., Каттанео Р. Долгосрочное последующее исследование эссенциальной криоглобулинемии. Acta Haematologica . 1979; 61 (2): 93–99. [PubMed] [Google Scholar] 51. La Civita L, Zignego AL, Monti M, Longombardo G, Pasero G, Ferri C. Смешанная криоглобулинемия как возможное предопухолевое заболевание. Артрит и ревматизм . 1995. 38 (12): 1859–1860. [PubMed] [Google Scholar] 52.Саадун Д., Селлам Дж., Гиллани-Далбин П., Кресель Р., Пьетте Дж. К., Какуб П. Повышенный риск лимфомы и смерти среди пациентов с смешанной криоглобулинемией, не связанной с вирусом гепатита С. Архив внутренней медицины . 2006. 166 (19): 2101–2108. [PubMed] [Google Scholar] 53. Пилери П., Уэмацу Й., Кампаньоли С. и др. Связывание вируса гепатита С с CD81. Наука . 1998. 282 (5390): 938–941. [PubMed] [Google Scholar] 54. Аньелло В., Чунг Р. Т., Каплан Л. М.. Роль инфекции вируса гепатита С в криоглобулинемии II типа. Медицинский журнал Новой Англии . 1992. 327 (21): 1490–1495. [PubMed] [Google Scholar] 55. Аньелло В. Этиология и патофизиология смешанной криоглобулинемии, вызванной вирусной инфекцией гепатита С. Семинары Springer по иммунопатологии . 1997. 19 (1): 111–129. [PubMed] [Google Scholar] 56. Чарльз ЭД, Грин Р.М., Марукиан С. и др. Клональная экспансия иммуноглобулина M + CD27 + B-клеток при HCV-ассоциированной смешанной криоглобулинемии. Кровь .2008. 111 (3): 1344–1356. [Бесплатная статья PMC] [PubMed] [Google Scholar] 57. Knight GB, Gao L, Gragnani L, et al. Обнаружение В-клеток WA при вирусной инфекции гепатита С: потенциальный прогностический маркер криоглобулинемического васкулита и В-клеточных злокачественных новообразований. Артрит и ревматизм . 2010. 62 (7): 2152–2159. [PubMed] [Google Scholar] 58. Чарльз Э.Д., Брунетти С., Марукиан С. и др. Клональные В-клетки у пациентов со смешанной криоглобулинемией, ассоциированной с вирусом гепатита С, содержат расширенное подмножество анергических В-клеток CD21low. Кровь . 2011. 117 (20): 5425–5437. [Бесплатная статья PMC] [PubMed] [Google Scholar] 59. Шотт П., Пользен Ф., Мюллер-Иссбернер А., Рамадори Г., Хартманн Х.
In vitro Реактивность криоглобулина IgM и IgG при смешанной криоглобулинемии, связанной с вирусом гепатита С. Гепатологический журнал . 1998. 28 (1): 17–26. [PubMed] [Google Scholar] 60. Бойер О., Саадун Д., Абриол Дж. И др. CD4 + CD25 + дефицит регуляторных Т-клеток у пациентов с гепатитом С-смешанным криоглобулинемическим васкулитом. Кровь . 2004. 103 (9): 3428–3430. [PubMed] [Google Scholar] 61. Монтаньино Г. Переоценка клинических проявлений смешанной криоглобулинемии. Семинары Springer по иммунопатологии . 1988. 10 (1): 1–19. [PubMed] [Google Scholar] 62. Swerdlow SH, Campo E, Harris NL, et al., Редакторы. Классификация опухолей кроветворных и лимфоидных тканей Всемирной организации здравоохранения . Лион, Франция: IARC Press; 2008. [Google Scholar] 63. Faderl S, Talpaz M, Estrov Z, O’Brien S, Kurzrock R, Kantarjian HM.Биология хронического миелолейкоза. Медицинский журнал Новой Англии . 1999. 341 (3): 164–172. [PubMed] [Google Scholar] 64. Savage DG, Szydlo RM, Goldman JM. Клинические особенности при постановке диагноза у 430 пациентов с хроническим миелоидным лейкозом, наблюдавшихся в специализированном центре в течение 16 лет. Британский гематологический журнал . 1997. 96 (1): 111–116. [PubMed] [Google Scholar] 65. Сервантес Ф., Розман С. Многофакторный анализ прогностических факторов при хроническом миелоидном лейкозе. Кровь .1982. 60 (6): 1298–1304. [PubMed] [Google Scholar] 66. Ондрейко SM, Кьельдсберг CR, Fineman RM. Монобластная трансформация при хроническом миелолейкозе: проявление массивного поражения печени. Рак . 1981. 48 (4): 957–963. [PubMed] [Google Scholar] 67. Berlin NI. Диагностика и классификация полицитемий. Семинары по гематологии . 1975. 12 (4): 339–351. [PubMed] [Google Scholar] 68. Пирсон Т.С., Мессинези М. Диагностические критерии красноватой полицитемии. Лейкемия и лимфома .1996; 22 (приложение 1): 87–93. [PubMed] [Google Scholar] 69. Michiels JJ, Juvonen E. Предложение по пересмотру диагностических критериев эссенциальной тромбоцитемии и истинной полицитемии Исследовательской группой Thrombocythemia Vera. Семинары по тромбозам и гемостазу . 1997. 23 (4): 339–347. [PubMed] [Google Scholar] 70. Торгано Дж., Манделли С., Массаро П. и др. Гастродуоденальные поражения при истинной полицитемии: частота и роль Helicobacter pylori
. Британский гематологический журнал .2002. 117 (1): 198–202. [PubMed] [Google Scholar] 71. Валла Д., Касадеваль Н., Лакомб С. Первичное миелопролиферативное заболевание и тромбоз печеночной вены. Проспективное исследование образования эритроидных колоний in vitro у 20 пациентов с синдромом Бадда-Киари. Анналы внутренней медицины . 1985. 103 (3): 329–334. [PubMed] [Google Scholar] 72. Visani G, Finelli C, Castelli U и др. Миелофиброз с миелоидной метаплазией: клинико-гематологические параметры, предсказывающие выживаемость у 133 пациентов. Британский гематологический журнал . 1990; 75 (1): 4–9. [PubMed] [Google Scholar] 73. Сильверштейн MN. Агногенная миелоидная метаплазия . Актон, Массачусетс, США: Publishing Sciences Group; 1975. [Google Scholar] 74. Варки А., Лоттенберг Р., Гриффит Р., Рейнхард Э. Синдром идиопатического миелофиброза. Клинико-патологический обзор с акцентом на прогностические переменные, предсказывающие выживаемость. Медицина . 1983; 62 (6): 353–371. [PubMed] [Google Scholar] 75. Лиоте Ф., Йени П., Тейе-Тибо Ф. и др.Асцит, выявляющий перитонеальное и печеночное экстрамедуллярное кроветворение с пелиозом при агногенной миелоидной метаплазии: клинический случай и обзор литературы. Американский медицинский журнал . 1991. 90 (1): 111–117. [PubMed] [Google Scholar] 76. Лопес-Гильермо А., Сервантес Ф., Бругера М., Перейра А., Фелиу Е., Розман С. Дисфункция печени после спленэктомии при идиопатическом миелофиброзе: исследование с участием 10 пациентов. Acta Haematologica . 1991. 85 (4): 184–188. [PubMed] [Google Scholar] 77.Thiele J, Kvasnicka HM, Werden C, Zankovich R, Diehl V, Fischer R. Идиопатический первичный остео-миелофиброз: клинико-патологическое исследование с участием 208 пациентов с особым упором на эволюцию особенностей заболевания, дифференциацию от эссенциальной тромбоцитемии и переменные прогностического воздействия . Лейкемия и лимфома . 1996. 22 (3-4): 303–317. [PubMed] [Google Scholar] 78. Пиво ПА, Кэмпбелл П.Дж., Грин Ар. Сравнение различных критериев диагностики первичного миелофиброза показывает ограниченную клиническую применимость для измерения сывороточной лактатдегидрогеназы. Haematologica . 2010; 95 (11): 1960–1963. [Бесплатная статья PMC] [PubMed] [Google Scholar] 79. Приминьяни М., Мартинелли И., Буччарелли П. и др. Факторы риска тромбофилии при обструкции внепеченочной воротной вены. Гепатология . 2005. 41 (3): 603–608. [PubMed] [Google Scholar] 80. Валла Д., Касадеваль Н., Хьюисс М.Г. и др. Этиология тромбоза воротной вены у взрослых. Проспективная оценка первичных миелопролиферативных заболеваний. Гастроэнтерология . 1988. 94 (4): 1063–1069.[PubMed] [Google Scholar] 81. Хукстра Дж., Брессер Е.Л., Смальберг Дж. Х., Спаандер М.С., Либик Ф.В., Янссен Х.Л. Длительное наблюдение за пациентами с тромбозом воротной вены и миелопролиферативными новообразованиями. Журнал тромбоза и гемостаза . 9 (11): 2208–2214. [PubMed] [Google Scholar] 82. P’ng S, Carnley B, Baker R, Kontorinis N, Cheng W. Недиагностированное миелопролиферативное заболевание в случаях внутрибрюшного тромбоза: полезность мутации JAK2 617F. Клиническая гастроэнтерология и гепатология .2008. 6 (4): 472–475. [PubMed] [Google Scholar] 83. Qi X, Yang Z, Bai M, Shi X, Han G, Fan D. Мета-анализ: значение скрининга мутации JAK2V617F при синдроме Бадда-Киари и тромбозе системы воротной вены. Пищевая фармакология и терапия . 2011. 33 (10): 1087–1103. [PubMed] [Google Scholar] 84. Мурад С.Д., Плессье А., Эрнандес-Герра М. и др. Этиология, лечение и исход синдрома Бадда-Киари. Анналы внутренней медицины . 2009. 151 (3): 167–175.[PubMed] [Google Scholar] 85. Primignani M, Barosi G, Bergamaschi G, et al. Роль мутации JAK2 в диагностике хронических миелопролиферативных заболеваний при тромбозе внутренних вен. Гепатология . 2006. 44 (6): 1528–1534. [PubMed] [Google Scholar] 86. Патель Р.К., Ли Н.К., Хенеган М.А. и др. Распространенность активирующей мутации тирозинкиназы JAK2 V617F при синдроме Бадда-Киари. Гастроэнтерология . 2006. 130 (7): 2031–2038. [PubMed] [Google Scholar]
87. Актуально.Эпидемиология, патологические особенности и диагностика классической лимфомы Ходжкина. 2012.
88. Росс А., Фридман Л.С. Печень при системном заболевании. В: Bacon BR, O’Grady JG JG, Di Bisceglie AM, Lake JR, редакторы. Комплексная клиническая гепатология . 2-е издание. Филадельфия, Пенсильвания, США: Мосби Эльзевьер; 2006. с. п. 537. [Google Scholar] 89. Хабшер С.Г., Ламли М.А., Элиас Э. Синдром исчезающего желчного протока: возможный механизм внутрипеченочного холестаза при лимфоме Ходжкина. Гепатология .1993. 17 (1): 70–77. [PubMed] [Google Scholar] 90. Гулитер С., Эрдем О., Исик М., Ямак К., Улуоглу О. Холестатическая болезнь печени с дуктопенией (синдром исчезающего желчного протока) при болезни Ходжкина: отчет о случае. Тумори . 2004. 90 (5): 517–520. [PubMed] [Google Scholar] 91. Леувенбург I, Lugtenburg EPJ, Van Buuren HR, Zondervan PE, De Man RA. Тяжелая желтуха, вызванная синдромом исчезающего желчного протока, как симптом лимфомы Ходжкина, полностью обратимая после химиотерапии. Европейский журнал гастроэнтерологии и гепатологии .2008. 20 (2): 145–147. [PubMed] [Google Scholar] 92. Роуботэм Д., Вендон Дж., Уильямс Р. Острая печеночная недостаточность, вторичная по отношению к инфильтрации печени: опыт одного центра из 18 случаев. Кишечник . 1998. 42 (4): 576–580. [Бесплатная статья PMC] [PubMed] [Google Scholar] 93. Шехаб Т.М., Камински М.С., Лок АСФ. Острая печеночная недостаточность из-за поражения печени гематологическими злокачественными новообразованиями. Болезни пищеварения и науки . 1997. 42 (7): 1400–1405. [PubMed] [Google Scholar] 94. Jaffe ES. Злокачественные лимфомы: патология поражения печени. Семинары по болезням печени . 1987. 7 (3): 257–268. [PubMed] [Google Scholar] 95. Сало Дж., Номдеду Б., Бругера М. и др. Острая печеночная недостаточность из-за неходжкинской лимфомы. Американский журнал гастроэнтерологии . 1993. 88 (5): 774–776. [PubMed] [Google Scholar] 96. Вардарели Э., Дундар Э., Аслан В., Гулбас З. Острая печеночная недостаточность из-за лимфомы Ходжкина. Медицинские принципы и практика . 2004. 13 (6): 372–374. [PubMed] [Google Scholar] 97. Dourakis SP, Tzemanakis E, Deutsch M, Kafiri G, Hadziyannis SJ.Фульминантная печеночная недостаточность как паранеопластическое проявление болезни Ходжкина. Европейский журнал гастроэнтерологии и гепатологии . 1999. 11 (9): 1055–1058. [PubMed] [Google Scholar] 98. Роуботэм Д., Вендон Дж., Уильямс Р. Острая печеночная недостаточность, вторичная по отношению к инфильтрации печени: опыт одного центра из 18 случаев. Кишечник . 1998. 42 (4): 576–580. [Бесплатная статья PMC] [PubMed] [Google Scholar] 99. Эмиль Дж. Ф., Азулай Д., Горнет Дж. М. и др. Первичные неходжкинские лимфомы печени с узловатой и диффузной инфильтрацией имеют разные прогнозы. Анналы онкологии . 2001. 12 (7): 1005–1010. [PubMed] [Google Scholar] 100. Морали Г.А., Розенманн Э., Ашкенази Дж., Мюнтер Г., Браверман Д.З. Острая печеночная недостаточность как единственное проявление рецидивирующей неходжкинской лимфомы. Европейский журнал гастроэнтерологии и гепатологии . 2001. 13 (10): 1241–1243. [PubMed] [Google Scholar] 101. Йешурун М., Иснард Ф., Гардерет Л. и др. Острая печеночная недостаточность как начальное проявление трансформации неходжкинской лимфомы низкой степени в крупноклеточную лимфому. Лейкемия и лимфома . 2001. 42 (3): 555–559. [PubMed] [Google Scholar] 102. Вульф Г.М., Петрович Л.М., Ройтер С.Е. и др. Острая печеночная недостаточность из-за лимфомы. Диагностическая проблема при рассмотрении трансплантации печени. Болезни пищеварения и науки . 1994. 39 (6): 1351–1358. [PubMed] [Google Scholar] 103. Бругера М., Микель Р. Влияние гематологических и лимфатических заболеваний на печень. В: Rodés J, Benhaumou JP, Blei AT, Reichen J, Rizzetto M, редакторы. Учебник гепатологии .3-е издание. Оксфорд, Великобритания: Блэквелл; 2007. с. п. 1662. [Google Scholar] 104. Гоффине Д.Р., Кастеллино Р.А., Ким Х. Стадия лапаротомии у неотобранных ранее нелеченных пациентов с неходжкинскими лимфомами. Рак . 1973; 32 (3): 672–681. [PubMed] [Google Scholar] 105. Рисдалл Р., Хоппе Т., Варнке Р. Лимфома неходжкина. Исследование эволюции болезни на основе 92 вскрытых случаев. Рак . 1979; 44 (2): 529–542. [PubMed] [Google Scholar] 106. Civardi G, Vallisa D, Bertè R, Lazzaro A, Moroni CF, Cavanna L.Очаговые поражения печени при неходжкинской лимфоме: исследование их распространенности, клинического значения и роли инфекции вируса гепатита С. Европейский журнал рака . 2002. 38 (18): 2382–2387. [PubMed] [Google Scholar] 107. Масуд А., Кайруз С., Худхуд К. Х., Хегази А.З., Бану А., Гупта, Северная Каролина. Первичная неходжкинская лимфома печени. Современная онкология . 2009. 16 (4): 74–77. [Бесплатная статья PMC] [PubMed] [Google Scholar] 108. Хайдер Ф.С., Смит Р., Хан С. Первичная лимфома печени, проявляющаяся как фульминантная печеночная недостаточность с гиперферритинемией: отчет о болезни. Журнал медицинских историй болезни . 2008; 2, статья № 279 [Бесплатная статья PMC] [PubMed] [Google Scholar] 109. Баумхор Д., Цанков А., Дирнхофер С., Торнилло Л., Терраччано Л. М.. Особенности инфильтрации печени при лимфопролиферативном заболевании. Гистопатология . 2008. 53 (1): 81–90. [PubMed] [Google Scholar] 110. Кэмерон А.М., Трути Дж., Труэлл Дж. И др. Фульминантная печеночная недостаточность от первичной лимфомы печени: успешное лечение ортотопической трансплантацией печени и химиотерапией. Трансплантация .2005. 80 (7): 993–996. [PubMed] [Google Scholar] 111. Кикума К., Ватанабе Дж., Оширо Ю. и др. Этиологические факторы первичной В-клеточной лимфомы печени. Вирховский архив . 2012. 460 (4): 379–387. [Бесплатная статья PMC] [PubMed] [Google Scholar] 112. Идзуми Т., Сасаки Р., Миура Ю., Окамото Х. Первичная гепатоспленочная лимфома: связь с инфекцией вируса гепатита С. Кровь . 1996. 87 (12): 5380–5381. [PubMed] [Google Scholar] 113. Йошикава М., Ямане Ю., Йонеда С. и др. Острая печеночная недостаточность из-за гепатоспленочной B-клеточной неходжкинской лимфомы у пациента, инфицированного вирусом гепатита С. Гастроэнтерологический журнал . 1998. 33 (6): 880–885. [PubMed] [Google Scholar] 114. Феррери А.Дж., Кампо Э., Сеймур Дж. Ф. и др. Внутрисосудистая лимфома: клинические проявления, естественное течение, лечение и прогностические факторы в серии из 38 случаев, с особым акцентом на «кожный вариант» British Journal of Hematology . 2004. 127 (2): 173–183. [PubMed] [Google Scholar] 115. Шимада К., Мацуэ К., Ямамото К. и др. Ретроспективный анализ внутрисосудистой крупноклеточной В-клеточной лимфомы, получавшей химиотерапию, содержащую ритуксимаб, по данным исследовательской группы IVL в Японии. Журнал клинической онкологии . 2008. 26 (19): 3189–3195. [PubMed] [Google Scholar] 116. Чапин Дж. Э., Дэвис Л. Е., Корнфельд М., Мандлер Р. Н.. Неврологические проявления внутрисосудистого лимфоматоза. Acta Neurologica Scandinavica . 1995. 91 (6): 494–499. [PubMed] [Google Scholar] 117. Детский М.Э., Чиу Л., Шандлинг М.Р., Спроул М.Э., Урселл М.Р. На неправильном пути. Медицинский журнал Новой Англии . 2006; 355 (1): 67–74. [PubMed] [Google Scholar] 118. Мурасе Т., Ямагути М., Сузуки Р. и др.Внутрисосудистая крупноклеточная B-лимфома (IVLBCL): клинико-патологическое исследование 96 случаев с уделением особого внимания иммунофенотипической гетерогенности CD5. Кровь . 2007. 109 (2): 478–485. [PubMed] [Google Scholar] 119. Мурасе Т., Накамура С., Каваути К. и др. Азиатский вариант внутрисосудистой крупной B-клеточной лимфомы: клинические, патологические и цитогенетические подходы к диффузной большой B-клеточной лимфоме, связанной с гемофагоцитарным синдромом. Британский гематологический журнал . 2000. 111 (3): 826–834.[PubMed] [Google Scholar] 120. Кодзима К., Канеда К., Ясукава М. и др. Специфичность анализа клональности перестройки гена тяжелой цепи иммуноглобулина на основе полимеразной цепной реакции для выявления инфильтрата костного мозга при гемофагоцитарном синдроме, ассоциированном с В-клеточной лимфомой. Британский гематологический журнал . 2002. 119 (3): 616–621. [PubMed] [Google Scholar] 121. Наримацу Х., Моришита Й., Сайто С. и др. Полезность аспирации костного мозга для точной диагностики азиатского варианта внутрисосудистой лимфомы: четыре вскрытия. Лейкемия и лимфома . 2004. 45 (8): 1611–1616. [PubMed] [Google Scholar] 122. Шимада К., Мурасе Т., Мацуэ К. и др. Поражение центральной нервной системы при внутрисосудистой В-крупноклеточной лимфоме: ретроспективный анализ 109 пациентов. Наука о раке . 2010. 101 (6): 1480–1486. [PubMed] [Google Scholar] 123. Röglin J, Böer A. Кожные проявления внутрисосудистой лимфомы имитируют воспалительные заболевания кожи. Британский дерматологический журнал . 2007. 157 (1): 16–25. [PubMed] [Google Scholar] 124.Понзони М., Феррери А.Дж., Кампо Э. и др. Определение, диагностика и лечение внутрисосудистой крупноклеточной В-клеточной лимфомы: предложения и перспективы международного консенсусного совещания. Журнал клинической онкологии . 2007. 25 (21): 3168–3173. [PubMed] [Google Scholar] 125. Гангули С. Острое внутримозговое кровоизлияние при внутрисосудистой лимфоме: серьезное побочное действие ритуксимаба, связанное с инфузией. Американский журнал клинической онкологии . 2007. 30 (2): 211–212. [PubMed] [Google Scholar] 126.Мартусевич-Борос М., Виатр Э., Радзиковска Э., Рошковски-Слиз К., Лангфорт Р. Легочная внутрисосудистая крупноклеточная B-лимфома как причина тяжелой гипоксемии. Журнал клинической онкологии . 2007. 25 (15): 2137–2139. [PubMed] [Google Scholar] 127. Ямада С., Ниший Р., Ока С. и др. FDG-PET — основной метод визуализации для диагностики внутрисосудистой лимфомы с началом инсульта. Архив неврологии . 2010. 67 (3): 366–367. [PubMed] [Google Scholar] 128. Рош Дж. Р., Гросс Т., Мамула П., Гриффитс А., Хьямс Дж.Т-клеточная лимфома печени и селезенки у подростков и молодых людей с болезнью Крона: поучительный рассказ? Воспалительные заболевания кишечника . 2007. 13 (8): 1024–1030. [PubMed] [Google Scholar] 129. Бейгель Ф., Юргенс М., Тиллак С. и др. Т-клеточная лимфома печени и селезенки у пациента с болезнью Крона. Nature Reviews Гастроэнтерология и гепатология . 2009. 6: 433–436. [PubMed] [Google Scholar] 130. Créput C, Galicier L, Buyse S, Azoulay E. Понимание органной дисфункции при гемофагоцитарном лимфогистиоцитозе. Медицина интенсивной терапии . 2008. 34 (7): 1177–1187. [PubMed] [Google Scholar] 131. Янка Г.Е. Гемофагоцитарные синдромы. Обзоры крови . 2007. 21: 245–253. [PubMed] [Google Scholar] 132. Де Кергенек С., Хиллер С., Молиние В. и др. Печеночные проявления гемофагоцитарного синдрома: исследование 30 случаев. Американский журнал гастроэнтерологии . 2001. 96 (3): 852–857. [PubMed] [Google Scholar] 133. Аркаини Л., Лаццарино М., Коломбо Н. и др. Лимфома маргинальной зоны селезенки: прогностическая модель для клинического использования. Кровь . 2006. 107 (12): 4643–4649. [PubMed] [Google Scholar] 134. Бругера М., Микель Р. Влияние гематологических и лимфатических заболеваний на печень. В: Rodés J, Benhaumou JP, Blei AT, Reichen J, Rizzetto M, редакторы. Учебник гепатологии . 3-е издание. Оксфорд, Великобритания: Блэквелл; 2007. с. п. 1662. [Google Scholar] 135. Thiele DL. Печеночные проявления системных заболеваний и других заболеваний печени. В: Feldman M, Friedman LS, Sleisenger MH, редакторы. Болезни желудочно-кишечного тракта и печени Sleisenger & Fordtran .7-е издание. Филадельфия, Пенсильвания, США: Elsevier Science; 2002. с. п. 1603. [Google Scholar] 136. Litten JB, Rodríguez MM, Maniaci V. Острый лимфобластный лейкоз, проявляющийся фульминантной печеночной недостаточностью. Кровь у детей и рак . 2006. 47 (6): 842–845. [PubMed] [Google Scholar] 137. Марголин JF, Steuber CP, Poplack DG. Острый лимфобластный лейкоз. В: Pizzo PA, Poplack DG, ред. Принципы и практика детской онкологии . 4-е издание. Филадельфия, Пенсильвания, США: Липпинкотт-Рэйвен; 2001 г.п. п. 489. [Google Scholar] 138. Streuli RA, Kaneko Y, Variakojis D. Лимфобластная лимфома у взрослых. Рак . 1981; 47 (10): 2510–2516. [PubMed] [Google Scholar] 139. Копелан Э.А., Макгуайр Э.А.. Биология и лечение острого лимфобластного лейкоза у взрослых. Кровь . 1995. 85 (5): 1151–1168. [PubMed] [Google Scholar] 140. Цимбериду А.М., Вен С., О’Брайен С. и др. Оценка хронического лимфолейкоза и малой лимфоцитарной лимфомы по абсолютному количеству лимфоцитов у 2126 пациентов: 20-летний опыт работы в Техасском университете М.Онкологический центр Д. Андерсона. Журнал клинической онкологии . 2007. 25 (29): 4648–4656. [PubMed] [Google Scholar] 141. Фейс Ф., Гиотто Ф., Хашимото С. и др. В-клетки хронического лимфоцитарного лейкоза экспрессируют ограниченные наборы мутированных и немутантных рецепторов антигена. Журнал клинических исследований . 1998. 102 (8): 1515–1525. [Бесплатная статья PMC] [PubMed] [Google Scholar] 142. Дамле Р.Н., Гиотто Ф., Валетто А. и др. Клетки В-клеточного хронического лимфоцитарного лейкоза выражают фенотип поверхностной мембраны активированных, испытанных антигеном В-лимфоцитов. Кровь . 2002. 99 (11): 4087–4093. [PubMed] [Google Scholar] 143. Стивенсон Ф.К., Калигарис-Каппио Ф. Хронический лимфоцитарный лейкоз: откровения от рецептора В-клеток. Кровь . 2004. 103 (12): 4389–4395. [PubMed] [Google Scholar] 144. Катовский Д. Волосато-клеточный лейкоз и пролимфоцитарный лейкоз. Клиники гематологии . 1977; 6 (1): 245–268. [PubMed] [Google Scholar] 145. Бине Дж. Л., Окуье А., Дигьеро Дж. И др. Новая прогностическая классификация хронического лимфолейкоза, полученная на основе многомерного анализа выживаемости. Рак . 1981. 48 (1): 198–206. [PubMed] [Google Scholar] 146. Рай KR, Савицкий A, Cronkite EP. Клиническая стадия хронического лимфолейкоза. Кровь . 1975. 46 (2): 219–234. [PubMed] [Google Scholar] 147. Шварц Дж. Б., Шамсуддин А. М.. Эффекты лейкозных инфильтратов в различных органах при хроническом лимфолейкозе. Патология человека . 1981. 12 (5): 432–440. [PubMed] [Google Scholar] 148. Wilputte JY, Martinet JP, Nguyen P, Damoiseaux P, Rahier J, Geubel A. Хронический лимфоцитарный лейкоз с портальной гипертензией и без поражения печени: клинический случай, подчеркивающий роль усиленного сплено-портального кровотока и «защитной» синусоидальной вазоконстрикции. Acta Gastro-Enterologica Belgica . 2003. 66 (4): 303–306. [PubMed] [Google Scholar] 149. Голомб HM, Катовский D, Golde DW. Волосатоклеточный лейкоз. Клинический обзор 71 случая. Анналы внутренней медицины . 1978. 89 (5): 677–683. [PubMed] [Google Scholar] 151. Yam LT, Janckila AJ, Chan CH, Li CY. Поражение печени при лейкемии волосатых клеток. Рак . 1983. 51 (8): 1497–1504. [PubMed] [Google Scholar] 152. Кайл Р.А., Герц М.А., Витциг Т.Э. и др. Обзор 1027 пациентов с впервые диагностированной множественной миеломой. Труды клиники Мэйо . 2003. 78 (1): 21–33. [PubMed] [Google Scholar] 153. Перес-Солер Р., Эстебан Р., Альенде Э. Участие печени во множественной миеломе. Американский журнал гематологии . 1985. 20 (1): 25–29. [PubMed] [Google Scholar] 154. Чанг Х., Бартлетт Э.С., Паттерсон Б., Чен К.И., Йи QL. Отсутствие CD56 на злокачественных плазматических клетках спинномозговой жидкости является признаком множественной миеломы с поражением центральной нервной системы. Британский гематологический журнал . 2005. 129 (4): 539–541.[PubMed] [Google Scholar]
155. Актуально. Обзор амилоидоза. 2012.
156. Бак Ф.С., Косс МН. Амилоидоз печени: морфологические различия между системными типами AL и AA. Патология человека . 1991. 22 (9): 904–907. [PubMed] [Google Scholar] 157. Ивата Т., Хошии Ю., Кавано Х. и др. Амилоидоз печени в Японии: гистологический и морфометрический анализ на основе амилоидных белков. Патология человека . 1995. 26 (10): 1148–1153. [PubMed] [Google Scholar] 158. Левин Р.А.Амилоидная болезнь печени. Корреляция клинических, функциональных и морфологических признаков у 47 пациентов. Американский медицинский журнал . 1962. 33 (3): 349–357. [PubMed] [Google Scholar] 159. Sarsik B, Sen S, Kirdok FS, Akarca US, Toz H, Yilmaz F. Амилоидоз печени: морфологический спектр гистопатологических изменений при амилоидозе AA и nonAA. Патология — исследования и практика . 2012. 208 (12): 713–718. [PubMed] [Google Scholar] 160. Ван Ю.Д., Чжао С.Ю., Инь Х.З. Первичный амилоидоз печени: небольшой обзор литературы и отчеты о пяти случаях. Анналы гепатологии . 2012; 11: 721–727. [PubMed] [Google Scholar]
симптомов болезни Гоше | Национальный фонд Гоше
Симптомы болезни Гоше (произносится как go-SHAY) часто варьируются от человека к человеку. Несмотря на то, что вы можете испытывать серьезные симптомы болезни Гоше, возможно, что у вас вообще не будет симптомов или признаков. Лечение может уменьшить симптомы и предотвратить необратимое повреждение вашего тела.
Каковы симптомы болезни Гоше?
Наиболее частые симптомы болезни Гоше включают:
Ниже приводится подробное объяснение всех признаков и симптомов болезни Гоше.
Симптомы болезни Гоше крови и органов
Симптомы болезни Гоше, затрагивающие кровь и органы, включают:
Костные симптомы болезни Гоше
Проблемы с костями часто встречаются у людей с болезнью Гоше. При своевременном лечении вы можете свести к минимуму любой необратимый вред для ваших костей и суставов.
Симптомы болезни Гоше, поражающие кости, включают:
Лечение болезни Гоше — ключ к предотвращению необратимых повреждений вашего тела.Тестирование на болезнь Гоше включает в себя анализ крови, называемый тестом на лейкоциты бета-глюкозидазы (BGL), для определения уровня ферментов в вашем организме. Если вы подвержены риску или испытываете симптомы, спросите своего врача о прохождении анализа.
Неврологические признаки и симптомы болезни Гоше
Неврологические (стволовые) симптомы и признаки болезни Гоше присутствуют только у пациентов с болезнью Гоше 2 или 3 типа. Эти признаки и симптомы болезни Гоше могут быть серьезными и вызывать преждевременную смерть.Узнайте больше о 2 и 3 типах болезни Гоше.
Заболевания, связанные с болезнью Гоше
Исследования показывают, что пациенты с болезнью Гоше могут подвергаться повышенному риску развития других заболеваний в более позднем возрасте, обычно после 50 лет.