Рак легких 4 степени и сколько с ним живут при должном лечении?
Формирование злокачественного новообразования легких происходит достаточно медленно. Диагностика порою бывает затруднительна, поскольку многие симптомы неспецифичны и принимаются специалистами за проявления иных легочных патологий. Нередко до обращения в специализированную клинику ситуация доходит до крайности – у пациента диагностируют уже рак легких 4 степени, что существенно затрудняет лечение и ухудшает прогноз выживаемости.
Проблеме продолжительности жизни при раке легких 4 стадии уделяется большое внимание онкологами всех стран мира. К сожалению, даже при использовании самых современных методик терапии, значительно отсрочить дату смерти удается в 12-15 % случаев на 4-5 лет, а полное излечение составляет лишь 1-2 %.
Характерные особенности
Отсутствие явных признаков расстройств деятельности дыхательной системы существенно затрудняет адекватную диагностику рака легких 4 стадии – пациентом слабость и малопродуктивный кашель воспринимаются, как симптомы иных легочных патологий, к примеру, хронического бронхита.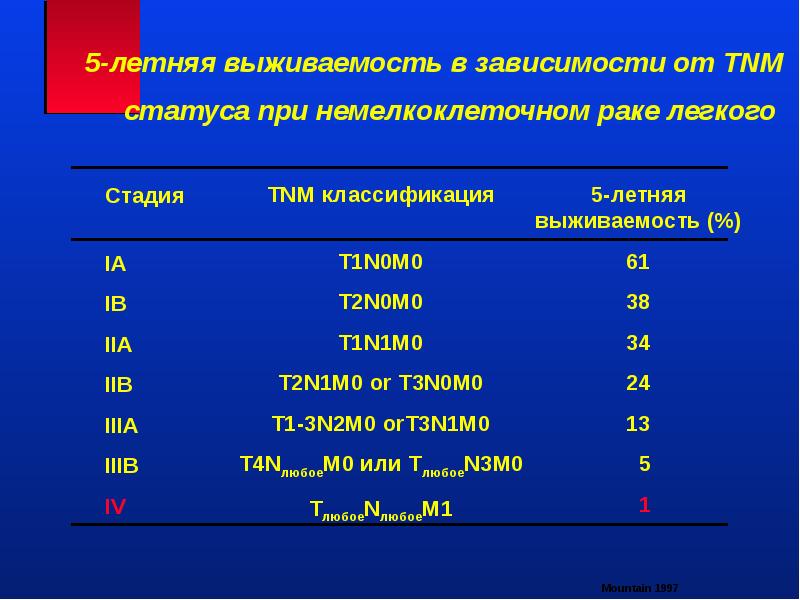
Нередко человека в медицинское учреждение приводит значительное ухудшение самочувствия, вызванное поражением иных органов, к примеру, со стороны желудка, печени, метастазами, продуцируемыми из первичного легочного очага.
Изменения в органах человека в этом случае практически не обратимы – последняя стадия рака легких для многих больных звучит, как смертельный приговор. Все симптомы рака, присущие именно 4 стадии заболевания, можно подразделить на общие, взаимосвязанные с раковой интоксикацией, и специфические, появившиеся именно из-за метастазирования.
Общие проявления рака легкого:
- нехарактерная ранее слабость и крайне быстрая утомляемость;
- ознобы и беспричинное колебание температуры;
- депрессивные расстройства и апатия;
- необоснованная утрата аппетита и быстрое понижение массы тела.
Рак легких 4 стадии имеет и специфические проявления – дыхательные расстройства. На 2-3 этапе формирования патологии они не столь показательны, но к моменту выхода метастазов в иных органы, степень их интенсивности такова, что постановка адекватного диагноза не вызывает у специалистов затруднений.
Специфические симптомы:
- Малопродуктивный кашель – имеет надсадный, мучительный характер, беспокоит пациента в горизонтальном положении. Легочный периферический вариант патологии и вовсе может протекать без кашля.
- Болевой синдром отличается вариабельностью проявлений – от локальных и маловыраженных, при нижнедолевой локализации. До нестерпимых ощущений – сильные боли отличают верхушечный вариант 4 стадии рака.
- Прогрессирующая одышка – захват опухолевым процессом все большего количества паренхимы органа провоцирует затруднение с дыхательной деятельностью у пациентов. Часто комбинируется с расстройством в сердечнососудистой системе – приступы стенокардии напряжения, что еще более усугубляет положение, продолжительность жизни сокращается.
- Кровохарканье – выделяемая при кашле мокрота может быть окрашена лишь в едва заметный розовый цвет в начале появления заболевания, в дальнейшем, когда наблюдается финальный этап патологии, она напоминает «ягодное желе».
 При прорастании опухоли в крупный сосуд у пациента остро возникает массивное легочное кровотечение, вплоть до летального исхода.
При прорастании опухоли в крупный сосуд у пациента остро возникает массивное легочное кровотечение, вплоть до летального исхода.
Симптомы, сопровождающие метастазирование онкопроцесса, напрямую зависят от его локализации. При переносе с током крови раковых клеток в головной мозг, пациента будут беспокоить приступы эпилепсии, судорог, расстройство зрительной, двигательной деятельности.
Тактика лечения
Крайне непростая задача – лечение 4 стадии рака легкого, поскольку к этому моменту пораженными оказывается большинство систем организма пациента. Онкологи подчеркивают – абсолютного восстановления параметров здоровья ожидать не стоит. Основная цель лечебных мероприятий – максимальное продление полноценной жизни онкобольного.
Как правило, рак легких последней стадии – это сильнейшие боли и значительные нарушения деятельности многих органов. Поэтому проводятся лишь паллиативные лечебные мероприятия, направленные на оптимальное восстановление угнетенных функций, максимальное облегчение болевого синдрома у пациента.
Для предотвращения дальнейшего разрастания онкологического образования специалистами, как правило, используется комбинация из лучевой и химиотерапии.
Важно! Вопрос об оперативном вмешательстве решается в индивидуальном порядке, поскольку новообразование в четвертый период заболевания может достигать гигантских размеров и удалить его безопасно не представляется возможным.
Прожить не менее 5 лет пациентам помогают различные комбинации вышеописанной терапии, а также симптоматические методы облегчения самочувствия – подбираются специалистами для каждого больного отдельно. В случае накопления патологического секрета в легких – будет показано проведение торакоцентеза.
Подбор адекватных обезболивающих препаратов – основная задача специалиста при раке 4 стадии. Боли постепенно усиливаются, и пациент не может обходиться без сильных препаратов для обезболивания. В крайне тяжелых случаях требуются наркотические медикаменты.
Прогноз
Узнав предположительный диагноз, многие люди тут же стараются узнать больше информации, набирают в поисковой строке вопросы о том сколько живут люди на 4 стадии рака легких, но онкологи не рекомендуют этого делать – ведь каждый человек уникален, и особенности его организма значительно отличаются от тех, что были присущи пациентам, обсуждающим свои симптомы на форумах. Кто-то максимально использует свои возможности и продолжает жить и трудиться, несмотря ни на что. А другой тут же опускает руки и не доживает даже до годовщины выставления диагноза.
Кто-то максимально использует свои возможности и продолжает жить и трудиться, несмотря ни на что. А другой тут же опускает руки и не доживает даже до годовщины выставления диагноза.
Случаи абсолютного излечения при онкопоражении структур легкого 4 стадии крайне редки. Медицинская статистика убедительно доказывает, что 5-летняя выживаемость при немелкоклеточном варианте заболевания составляет 8-12 %, в то время, как при мелкоклеточном виде ракового образования – лишь 1-2 %. Огромное значение имеет своевременность выявления заболевания и начало лечебных мероприятий.
лечение химиотерапией, прогноз жизни, симптомы и стадии
Плоскоклеточный рак легких относится к немелкоклеточному раку легких (НМРЛ). На его долю приходится около 40-50% всех случаев злокачественных новообразований бронхолегочной системы. Как правило, он развивается из эпителия крупных бронхов 2-4 порядка.
Основные формы плоскоклеточного рака легких:
- Центральный рак — это новообразование, которое разрастается из эпителия крупных бронхов 1-4 порядка.

- Периферический рак — эта форма рака легкого поражает мелкие периферические бронхи и альвеолы. Особенностью данной локализации является поздняя симптоматика. Первые признаки заболевания проявляются, когда опухоль начинает прорастать соседние ткани и достигает просвета крупных бронхов, или альвеол. Из-за этого опухоль поздно диагностируется, что неблагоприятно сказывается на прогнозе.
Второстепенные формы злокачественных новообразований легкого:
- Диссеминированный рак — диагностируется несколько опухолевых очагов, которые могут располагаться по всему легкому. Заболевание очень быстро прогрессирует.
- Медиастинальная форма — изначально опухоль имеет внелегочную локализацию, и поражает легкие при метастазировании в медиастинальные лимфатические узлы.
Факторы развития плоскоклеточного рака легких
Главным фактором развития плоскоклеточного рака легкого является курение. В целом у курильщиков риск развития рака легких составляет 17-20%. При отказе от курения, этот показатель снижается, поскольку ткань бронхов восстанавливается. Особенно опасно курение для женщин, принимающих гормональную терапию, у них риск погибнуть от рака легкого на 60% выше, чем у женщин, не принимающих гормоны. Помимо этого, рак легкого, развившийся у курильщика, имеет более неблагоприятное и агрессивное течение, чем аналогичное заболевание у некурящего человека.
При отказе от курения, этот показатель снижается, поскольку ткань бронхов восстанавливается. Особенно опасно курение для женщин, принимающих гормональную терапию, у них риск погибнуть от рака легкого на 60% выше, чем у женщин, не принимающих гормоны. Помимо этого, рак легкого, развившийся у курильщика, имеет более неблагоприятное и агрессивное течение, чем аналогичное заболевание у некурящего человека.
Также канцерогенным эффектом в отношении рака легких обладают:
- Радон. Является вторым по значимости фактором риска рака легкого. Радон – это природный газ, который образуется при распаде урана, который в тех или иных концентрациях присутствует в земной коре. Концентрация радона зависит от природных особенностей почвы. В целом 100 Бк/м3 увеличивает риск рака легких на 16%.
- Асбест. Данное вещество повышает риск развития многих видов злокачественных новообразований дыхательной системы, в том числе рака легких.
- Некоторые вирусы. Сюда относят вирус папилломы человека, обезьяний вирус, цитомегаловирус и др.
 Они влияют на жизненный цикл клетки, блокируют апоптоз (запрограммированную гибель клетки), что провоцирует неконтролируемое деление и рост эпителия.
Они влияют на жизненный цикл клетки, блокируют апоптоз (запрограммированную гибель клетки), что провоцирует неконтролируемое деление и рост эпителия. - Пыль. Исследования, проведенные Американским обществом рака, доказали, что увеличение содержания пыли во вдыхаемом воздухе на 1% увеличивает риск развития рака легкого на 14%.
Из эндогенных причин выделяют следующие факторы риска рака легкого:
- Хронические заболевания легких.
- Гормональные нарушения.
- Возраст старше 50 лет.
- Наследственная предрасположенность.
Симптомы плоскоклеточного рака легких
Клиническая картина рака легких зависит от локализации опухоли и стадии заболевания. Симптоматика неспецифична, т. е. все признаки могут обнаруживаться при других заболеваниях органов дыхательной системы.
Все симптомы рака легких делят на 4 группы:
- Первичные. Эти симптомы развиваются из-за воздействия опухоли на бронхи и альвеолы.
- Симптомы, которые развиваются при прорастании опухоли легких на соседние органы.
- Симптомы, развивающиеся, когда опухоль дает отдаленные метастазы. Например, метастазирование в головной мозг может проявляться признаками инсульта или менингита, при обширном поражении печени может развиваться желтуха.
- Симптомы, возникающие из-за системного воздействия рака легких на организм. Сюда относят повышение температуры тела, похудание и истощение, общую слабость и упадок сил.
Первичные признаки
Наличие и проявление первичной симптоматики будет определяться локализацией и/или размерами опухоли. Раньше всего проявляются эндофитные (растущие в просвет бронха) опухоли плоскоклеточного центрального рака легкого. Первым симптомом является кашель. Сначала он сухой, возникает из-за рефлекторного раздражения стенки бронха. Затем из-за нарушения дренирования неизбежно присоединяется инфекция, и кашель становится влажным. На этом фоне может развиться пневмония. Антибактериальная терапия приносит облегчение, но неизбежно развивается рецидив.
В ряде случаев обнаруживается кровохаркание. При этом мокрота либо полностью пропитана кровью («малиновое желе»), либо кровь присутствует в виде прожилок. Кровохаркание развивается из-за распада опухоли или изъязвления поверхности бронха. Если опухоль проросла в кровеносные сосуды, может развиться серьезное кровотечение.
При закупорке просвета бронха возникает чувство нехватки воздуха. Если поражен крупный бронх, может возникнуть ателектаз (спадение доли легкого).
Вторичные симптомы
- Боль. Бронхи и альвеолы не имеют болевых рецепторов, поэтому болезненные ощущения возникают при прорастании опухоли в соседние ткани, например, плевру. Также причиной развития боли может стать смещение органов грудной клетки и ателектаз.
- Одышка. Развивается из-за спадения легкого или его доли, при опухолевой обтурации просвета бронха, а также при развитии опухолевого плеврита, гемоторакса и др.
- Также вторичными симптомами является осиплость голоса из-за поражения возвратного нерва, нарушение глотания из-за врастания опухоли в пищевод и др.
Стадии заболевания
При первой стадии, опухоль не превышает 3 см. Отсутствуют признаки поражения лимфатических узлов и плевры. Эта стадия бессимптомна, новообразование диагностируется случайно, при обследовании по поводу другого заболевания.
При второй стадии опухоль достигает размеров в 5 см, могут иметься единичные метастазы в регионарные лимфатические узлы. На этой стадии уже появляются клинические симптомы.
3 стадия делится на 3а и 3b. При 3а стадии размеры новообразования превышают 5 см, опухоль прорастает плевру и грудную стенку. Имеются метастазы в регионарные лимфатические узлы. На этой стадии диагностируется более половины всех случаев плоскоклеточного рака легкого.
При 3b стадии опухоль прорастает кровеносные сосуды, плевру, пищевод, перикард (может поражаться сердце). Размер опухоли может быть любым.
При выставлении 4 стадии размер опухоли не имеет значения. Ключевым моментом является наличие отдаленных метастазов.
Диагностика плоскоклеточного рака
Для диагностики плоскоклеточного рака легких необходимо специальное обследование, поскольку ни анамнез, ни симптомы, ни данные физикального осмотра не позволяют заподозрить диагноз. Могут использоваться следующие методы:
- Рентгенологическое исследование. Не является точным методом диагностики рака легкого, поскольку чаще всего не позволяет визуализировать опухоль. Тем не менее, ее наличие можно заподозрить по ряду специфических признаков, характерных для нарушения вентиляции легочной ткани. Проводится рентгенография в переднезадней и боковой проекциях. Более информативным методом рентгендиагностики является компьютерная томография. Она позволяет выявить даже начальные формы новообразования до возникновения симптомов нарушения вентиляции, а также обнаружить перибронхиальный плоскоклеточный рак.
- УЗИ проводится для обнаружения отдаленных метастазов.
- Биопсия. Для того чтобы определить морфологический и молекулярно-генетический тип опухоли, необходимо исследовать ее фрагмент в лаборатории. Эти данные влияют на тактику лечения пациента и прогноз течения заболевания. Для проведения биопсии, используются различные методы, некоторые опухоли можно пропунктировать через грудную стенку, другие – во время бронхоскопии, биопсию более глубоколежащих новообразований проводят после хирургического удаления опухоли.
Лечение плоскоклеточного рака легкого
Хирургический метод
Основным методом лечения плоскоклеточного рака легкого является хирургическая операция. Ее объем будет определяться размером опухоли и ее взаимоотношением с окружающими тканями.
При периферической локализации плоскоклеточного рака удаляется доля легкого (лобэктомия), при центральном раке — все легкое (пневмонэктомия). Ингода при центральном раке есть возможность сохранить долю пораженного легкого с помощью бронхопластических операций, когда накладываются межбронхиальные анастамозы.
Современное развитие торакальной онкохирургии и анестезиологии позволяет проводить сложные обширные вмешательства при распространенных формах плоскоклеточного рака легких. Например, при прорастании опухоли в грудную стенку, пищевод и одновременно с удалением новообразования проводится резекция пораженных органов.
Также есть технологии, которые позволяют провести стандартные вмешательства с минимальной травматичностью. Например, лобэктомия проводится посредством видеоассистированной торакоскопии — все манипуляции выполняются через небольшие проколы в грудной стенке. Для того чтобы видеть, что происходит внутри, в грудную полость вводится миниатюрная видеокамера.
После удаления опухоли, ее отправляют в лабораторию для гистологического и молекулярно-генетического исследования. В зависимости от полученных результатов, будет решаться вопрос о назначении послеоперационной адъювантной химиотерапии.
Химиотерапия плоскоклеточного рака легких
К сожалению, у подавляющего большинства больных на момент постановки диагноза имеется местнораспространенная или метастатическая форма заболевания, поэтому такие пациенты нуждаются в химиотерапии. Ее применяют в следующих случаях:
- Как паллиативное лечение плоскоклеточной формы рака 3b-4 стадии.
- Предоперационная химиотерапия.
- Адъювантная (послеоперационная) химиотерапия.
- Совместно с лучевой терапией для лечения местнораспространенных форм опухоли.
Для химиотерапии плоскоклеточного рака легкого используются следующие двухкомпонентные платиносодержащие режимы:
- Гемзар + цисплатин.
- Таксотер+цисплатин.
- Навельбин + цисплатин.
На второй линии ХТ применяются алимта, доцетаксел, эрлотиниб, этопозид, гемцитабин. В качестве препаратов 3 линии используется эрлотиниб (тарцева).
Иммунотерапия
Иммунотерапия применяется при лечении распространенных стадий заболевания у пациентов, не имеющих драйверных молекулярно-генетических нарушений. Используются препараты пембролизумаб (китруда) при положительной экспрессии PD-LI, и ниволумаб. При назначении ниволумаба в рамках терапии второй линии определение PD-LI не требуется.
Суть действия данных препаратов заключается в следующем:
злокачественные клетки блокируют противоопухолевое действие Т-лимфоцитов путем связывания рецептора PD с его лигандами. Пембролизумаб является моноклональным телом, которое блокирует эту связь, тем самым делая раковые клетки заметными для иммунной системы.
Радиотерапия
Долгое время лучевая терапия была основным методом лечения плоскоклеточного рака легких 3-4 стадии. Однако его результаты были неудовлетворительными — медиана выживаемости составляла около 10 месяцев, пятилетняя выживаемость не превышала 5%. В настоящее время используется комбинированное лечение, включающее лучевую терапию в СОД 60-65Гр и двухкомпонентную платиносодержащую химиотерапию. Такое лечение позволило в 2 раза увеличить пятилетнюю выживаемость и медиану жизни.
Симптоматическая терапия плоскоклеточного рака легких
Симптоматическая терапия направлена на облегчение состояния больного и устранение тягостных симптомов заболевания:
- В первую очередь необходимо адекватное обезболивание. Для этого используется паллиативная лучевая терапия, химиотерапия, анальгетики (в том числе наркотические) и другие методы.
- Паллиативная лучевая терапия проводится при кровохаркании и обструкции бронхов.
- Для лечения экссудативного плеврита, который сопровождается одышкой, проводят плевроцентез с эвакуацией выпота и введением в плевральную полость цитостатиков. При массивной экссудате решается вопрос об установке дренажа.
- При развитии легочного кровотечения показано оперативное вмешательство, если его проведение невозможно, выполняют консервативный гемостаз.
- При массивном распаде опухоли встает вопрос о паллиативной операции.
Выживаемость при раке легких
Прогноз выживаемости определяется стадией заболевания. При радикальном хирургическом лечении на начальных стадиях удается добиться 5-летней выживаемости у 50-70% больных. При распространенных формах болезни при отсутствии лечения, средняя продолжительность жизни колеблется в пределах 9 месяцев. Специальное лечение позволяет увеличить этот показатель до 2-х лет.
Рак легких 3 стадия с метастазами: прогноз выживаемости и лечение
Лечится ли рак лёгких?
Ответ скорее положительный, чем отрицательный, но это справедливо лишь на первых стадиях заболевания.
Возможно, всё равно придётся делать операцию, но даже с одним легким можно жить, и при желании полноценно.
Конечно, стометровку пробежать будет сложновато, но работать вполне возможно.
На данный момент критерием излечения в онкологии служит пятилетняя выживаемость.
Лучшие результаты достигаются при 1-2 стадиях заболевания.
Рак лёгких 3 стадии – это значительно худшие отдаленные результаты.
К тому же после лечения на третьей стадии часто бывают рецидивы. Почему это происходит?
Рак лёгкого 3 степени
Как известно, рак лёгких подразделяется на несколько стадий: от 0 до 4, в каждой стадии могут быть ещё и степени.
Стадия рака определяет размер опухоли и её распространённость, а степень – скорость развития заболевания, то есть скорость размножения опухолевых клеток.
Выделяют три степени: первая, вторая и третья. Чем выше степень, тем быстрее идёт болезненный процесс.
Рак лёгкого 3 степени – это значит, что клетки размножаются очень быстро, поэтому и скорость распространения велика.
Рак в нулевой стадии – это самое начало процесса, 1 стадия рака легких означает, что опухоль ещё небольшая, не более 5 см в диаметре, и распространения ни на лимфатические узлы, ни на другие органы нет.
Если не приняты меры по лечению, то процесс расширяется и ускоряется, приводя к следующим стадиям.
Рак легких 3 стадии с метастазами
- Размер опухоли более 7 см;
- Затронуты лимфатические узлы;
- В онкологический процесс включаются окружающие органы.
Третья стадия рака легких может быть первой и второй степени.
В первой степени опухоль распространяется на близлежащие лимфатические узлы и окружающие образования: диафрагма, плевра, трахея, бронхи.
Опухоль начинает прорастать в соседнюю долю лёгкого, может захватить соседний бронх, главный бронх.
В случае прорастания рака в дыхательные пути опухоль начинает препятствовать прохождению воздуха.
Рак легких 3 стадия: прогноз
На этой стадии пятилетняя выживаемость при мелкоклеточном раке – около 13%, при других видах – 19-24%.
Во второй степени распространение опухоли увеличивается. Она уже переходит на лимфоузлы с противоположной стороны грудной клетки.
Поражается не только диафрагма, но и средостение, оболочки сердца. В этом случае пятилетняя выживаемость не более 9%.
Таким образом, раковая опухоль в третьей стадии приводит к повреждению органов или нарушениям в их работе.
Поэтому и лечение не всегда может дать желаемые результаты.
Лечение третьей стадии рака лёгких
Выбор метода лечения рака лёгких во многом зависит от стадии заболевания, его степени.
Рак третьей стадии лечат комплексно, используя все три основных метода: операция, химиотерапия, лучевая терапия.
Хирургическое операция представляет собой удаление опухоли, доли легкого, может быть, и целого легкого. Всё зависит от степени распространения рака.
Хирургическое лечение, как правило, назначается при немелкоклеточном раке.
Мелкоклеточный рак протекает более агрессивно, для его лечения применяют радиотерапию, химиотерапию.
Операция также не рекомендуется и в тех случаях, когда опухоль распространилась на другие органы или затронула трахею, либо в случае сопутствующих заболеваний, которые могут быть противопоказаниями к хирургическому вмешательству.
Лучевая, или радиотерапия, — это облучение опухоли, в результате которого раковые клетки погибают.
Такой же эффект оказывает и химиотерапия, зачастую эти методы сочетают в лечении пациентов в 3 стадии рака лёгких.
Лечение на этой стадии не всегда приводит к успеху, чаще всего удаётся лишь продлить жизнь пациенту.
Чтобы избежать страшных последствий, необходимо быть внимательным к себе, не следует пренебрегать регулярным флюорографическим обследованием.
Многие бессимптомные формы рака лёгких или заболевание на самых ранних стадиях выявляются при обращении к участковому терапевту по поводу простуды, и происходит это именно во время флюорографии.
Рак легких: сколько можно прожить?
При постановке проблемы: «Рак легких: сколько можно прожить?» важное значение имеет конкретный подтип заболевания и его распространенность. Он может быть локализованным на одном участке или расширится на лимфосистему и другие органы.
Прогноз выживаемости также зависит от таких аспектов:
- этапа заболевания на момент постановки диагноза;
- быстроты роста злокачественного заболевания;
- возраста и общего состояния здоровья;
- реагирования болезни на варианты лечения;
- первичное или вторичное это заболевание;
- присутствуют ли метастазы.
Виды злокачественных заболеваний легких
Определено два основных типа легочного онкопроцесса:
1. Немелкоклеточное злокачественное заболевание легких:
На его долю приходится от 85% до 90% всех случаев. Подвиды представлены:
- аденокарциномой ‒ форма опухоли легких, которая встречается наиболее часто;
- плоскоклеточное онкообразование, что локализуется в подкладке легких;
- большие карциномы, или недифференцированные ‒ промежуточный вариант между аденокарциномой и эпидермоидным раком. Они представляют только 5% всех случаев;
2. Рак легких небольших клеток:
Как правило, вызван курением и составляет 10-15 % от всего злокачественного процесса легких. Он возникает очень редко и может быстро распространятся.
3. Мезотелиомы:
Мезотелиома – это очень опасный вид рака, который возникает в результате воздействия асбеста.
Важно знать: Правильная диагностика рака легких. Список анализов, процедур, тестов
Сколько можно прожить с центральным раком легкого?
Установление выживаемости учитывает процент людей с определенным типом злокачественного процесса и его стадией, а также время, на протяжении которого пациент остается жив. Статистические данные основываются на исследовании больших групп людей. Однако следует учитывать, что прогноз для каждого человека сугубо индивидуален.
- Мелкоклеточный рак легких (ограниченный и обширный) представляет общую 5-летнюю выживаемость только в 6%. Без лечения при этом раке легких человек может прожить от 2-х до 4-х месяцев. При лечении ‒ 6-12.
- Общая 5-летняя выживаемость при немелкоклеточном раке на всех этапах заболевания становит примерно 18%.
- Бронхиолоальвеолярная карцинома репрезентирует гораздо высшую 5-летнюю выживаемость, нежели другие подвиды. Так, например, если опухоль находится на ранней стадии (меньше 3 см в диаметре), выживаемость после проведения операции составляет 100%. На более продвинутых этапах прогноз варьируется.
Пятилетняя выживаемость при немелкоклеточном раке легких в зависимости от стадии
Следует понимать, что не все пациенты с одинаковой стадией будут живы одно и то же количество времени или только 5 лет. Ниже наведены только общие характеристики выживаемости:
Этап I. Болезнь локализируется непосредственно в органе и не покинула его границы. Общий уровень выживаемости составляет от 45% до 49%.
Этап II. Опухолевые клетки наблюдаются в лимфоузлах возле легких. Общая статистическая выживаемость представляет 30-31% людей, которые будут живы по истечению пяти лет.
Этап III. Рак легких 3 стадии: сколько можно прожить? На этом этапе опухоль довольно больших размеров и уже переместилась в лимфоузлы грудной клетки. В зависимости от конкретного места расположения метастазов, различают подэтапы:
3А: злокачественные клетки сосредоточены в лимфоузлах на той же стороне грудной клетки, в которой начался рак. В среднем, выживаемость становит 14%;
3В: онкологические повреждения наблюдаются на противоположной от груди стороне, ниже или выше ключицы. Ңа таком продвинутом этапе статистические данные представляют очень низкие показатели ‒ всего 5%. При этом средняя продолжительность жизни при лечении составляет 13 месяцев.
Этап IV. Рак легких (сколько можно прожить) 4 стадии. Общий уровень 5-летней длительности жизни для людей с 4-ой стадией становит только 1%. Медиана выживаемости составляет около 8 месяцев.
К сожалению, большинство рака обнаруживается на 3-ей или 4-ой стадии. В связи с этим, общая выживаемость с момента диагностирования заболевания составляет всего 16%.
Сколько можно прожить после операции?
Раковая выживаемость пациентов после хирургического вмешательства в большинстве случаев зависит от стадии и последующей терапии. Во время проведения операции удаляются все пораженные раковым процессом ткани. Однако врач не может гарантировать, что их больше не осталось в организме.
Для продления жизни врачи применяют такие методы:
- Химиотерапия, что позволяет уничтожить раковые клетки. Препараты представлены “Циспластин”(-ом) и “Паклитаксел”(-ом).
- Радиация, влияющая на онкологические ткани с помощью интенсивной энергии.
- Целевая лекарственная терапия ‒ один из новейших методов борьбы с раковым процессом. При этом способе лечения применяются медикаментозные средства, нацелены на конкретные аномалии в злокачественных клетках. Среди них выделяются:
- бевацизумаб («Авастин»), останавливающий опухоль от создания нового кровоснабжения;
- эрлотиниб («Тарцева»), блокирующий размножение опухолевых клеток.
Рак легких: сколько можно прожить с метастазами?
Исследования свидетельствуют, что пациенты, принимающие дополнительную терапию после операции, остаются жить значительно дольше нежели те, кто не использует все методы лечения.
Поэтому человек с метастазами при адекватном лечении может прожить намного дольше статистических данных для 4 стадии рака, если кроме традиционных способов воспользуется еще и альтернативным лечением, в частности стимуляцией иммунной системы организма. Для этого используются средства, которые восстанавливают человеческие защитные силы, их способность к сопротивлению злокачественному процессу, а также препятствуют образованию нового кровотока опухоли.
Учитывая все современные способы лечения рака, можно сказать, что вопрос «Рак легких: сколько можно прожить?» носит сугубо индивидуальный характер и зависит от конкретного случая. Ни статистические данные, ни наилучшие специалисты не способны дать однозначного и точного ответа. Бывают лишь предположения.
Отдаленные результаты операций немелкоклеточного рака легкого
Продолжительность жизни больных является вторым основным критерием оценки эффективности хирургического лечения больных с опухолями легких.
При злокачественных опухолях отдаленные результаты хирургического лечения мало удовлетворяют хирургов.
Пятилетняя выживаемость больных немелкоклеточным раком легкого составляет в среднем 30% и не имеет заметной тенденции к повышению.
Аналогичная ситуация, хотя несколько лучшая, при злокачественных неэпителиальных и метастатических опухолях. Удовлетворительные отдаленные результаты хирургического лечения отмечаются при карциноидных опухолях, особенно высокодифференцированных и умеренно дифференцированных, хорошие — при доброкачественных опухолях легких.
Постоянное совершенствование методов хирургического лечения больных раком легкого существенно не отразилось на 5-летней выживаемости. Так, в 1962 г. В. В. Родионов обобщил данные 30 авторов, согласно которым за периоде 1947 по 1958 г. из 2803 радикально оперированных больных более 5 лет прожили 608 (21,3%).
По сводной статистике А.С. Павлова и соавт. (1979), основанной на данных 46 публикаций (1960-1976 гг.), этот процент составил 24,8: из 12 223 больных, перенесших радикальные операции, более 5 лет прожил 3031 (24,8%).
По материалам 17 торакальных клиник мира, опубликованным в 1979-1985 гг., после 8815 операций 5-летняя выживаемость больных составила 29,9%. Этот показатель варьирует в довольно значительных пределах — от 22 до 38% (Трахтенберг А.Х., 1987). Более высокие показатели обычно обусловлены сужением показаний к хирургическому лечению (более низким удельным весом расширенных и комбинированных пневмонэктомии).
В публикациях 90-х годов отдельные авторы приводят почти аналогичные показатели 5-летней выживаемости больных немелкоклеточным раком легкого. Так, поданным В.П. Харченко и И.В. Кузьмина (1994), после хирургического лечения 504 больных плоскоклеточным и железистым раком легкого этот срок пережили 39,2%, а при крупноклеточном и диморфном раке ни один пациент не прожил более 5 лет. По материалам В.И. Зырянова и соавт. (1997), из 190 радикально оперированных больных 5 лет и более жили 45 (23,7%).
По нашим данным (рис. 5.72), более 1 года после хирургического лечения прожили 78,4% (1491 из 1902) больных немелкоклеточным раком легкого, более 3 лет — 47,2% (766 из 1624) и 5 лет — 33,6% (509 из 1514). Таким образом, первые 3 года после операции являются критическим сроком, поскольку более 70% больных, переживших этот срок, живут более 5 лет.
Рис. 5.72. Продолжительность жизни больных раком легкого после хирургического лечения (данные МНИОИ им П.А.Герцена).
Продолжительность жизни больных
Продолжительность жизни больных после хирургического лечения зависит от многих факторов. Основными факторами, определяющими прогноз после радикальной операции, являются размер первичной опухоли, особенности вовлечения в опухолевый процесс соседних органов и структур, состояние внутригрудных лимфатических узлов, т.е. стадия заболевания, гистологическая структура и степень дифференцировки опухоли, радикальность выполненной операции.
По данным Б.Е. Петерсона (1976), после радикальных операций по поводу рака легкого I стадии более 5 лет прожили 48,5% больных, II — 41,3%, III — 18,4% больных.
Аналогичные результаты приводят G. Braghieri и соавт. (1982) — 52,36 и 14%, Н. Thorarinson и соавт. (1983) — 50, 33 и 15%, Ohta Mitsuo и соавт. (1985) — 61, 27 и 10,5% соответственно.
В публикациях последнего десятилетия отдаленные результаты приведены в зависимости от стадии опухоли согласно Международной классификации по системе TNM (1986).
Так, по материалам В.П. Харченко и И.В. Кузьмина (1994), после хирургического лечения больных раком легкого I стадии 5-летняя выживаемость составила 69,9%, II — 29,8%, IIIA — 22,2% (р
Таким образом, удовлетворительные отдаленные результаты удается получить лишь при I стадии. Пятилетняя выживаемость при IIIА стадии почти в 3 раза ниже, чем при I стадии.
По материалам МНИОИ им. П.А. Герцена, 5-летняя выживаемость больных раком легкого I стадии в 1,5 раза выше, чем II стадии, и в 3 раза выше, чем IIIА стадии (табл. 5.11).
Таблица 5.11. Выживаемость (в процентах) больных раком легкого после хирургического лечения в зависимости от стадии заболевания
Таким образом, одним из реальных путей улучшения отдаленных результатов хирургического лечения рака легкого остается совершенствование организационных мероприятий по активному выявлению заболевания в ранних стадиях.
Опубликованные результаты хирургического лечения больных первичным внутриэпителиальным раком легкого показывают, что 5-летняя выживаемость составляет 90%. Значительно больше сведений о микроинвазивном раке легкого без распространения опухолевой инфильтрации до уровня бронхиальных хрящей. Отдаленные результаты хирургического лечения таких больных удовлетворительные: 5-летняя выживаемость достигает 75% (Cortese D. et al., 1983).
Достоверные данные о выживаемости больных раком легкого в стадии Т1N0M0 уже не редкость. Описано более 1500 наблюдений с анализом отдаленных результатов хирургического лечения. По материалам М.Л. Шулутко и соавт. (1983), Р.И. Вагнера (1983), М. Mezzetti и соавт. (1982) и V. Baltrami (1994), более 5 лет после лобэктомии прожили соответственно 68,1, 72,2, 76 и 68,2% больных. Другие авторы приводят более низкие показатели 5-летней выживаемости: Б.Н. Зырянов и соавт. (1997) — 42,8%, В. Krause (1987) — 50%, G. Spreafico и соавт. (1995) — 50%.
В МНИОИ им. П.А. Герцена хирургическое лечение при раке легкого в стадии T1N0M0 проведено 236 больным; у 96% из них выполнены органосохраняющие операции, преимущественно лобэктомия и реже экономная резекция. У большинства больных операция оказалась радикальной не только в клиническом, но и в биологическом отношении: более 5 лет прожили 76%, более 10 лет — 52% (рис. 5.73).
Рис. 5.73. Выживаемость больных (236) немелкоклеточным раком легкого II стадии ТIN0M0 после хирургического лечения.
I — больные, подвергшиеся хирургическому лечению; II — нелеченые больные.
Чрезвычайно важно, что у 96% больных центральным раком и у 65% больных периферическим раком легкого диагноз был морфологически верифицирован до операции, что свидетельствует о реальных возможностях современной клинической онкологии в диагностике рака легкого в стадии T1N0M0.
Увеличение числа больных с начальными формами рака легкого, несомненно, будет способствовать улучшению результатов хирургического лечения этого заболевания. Только своевременно выполненное оперативное вмешательство позволяет рассчитывать на стойкое излечение рака легкого и продление жизни больного на длительный срок.
При раке легкого I стадии возникла проблема выбора адекватного объема операции: обсуждается возможность осуществления экономной сублобарной резекции (атипичной типа клиновидной или краевой, сегментэктомии). В последние годы наметилась тенденция к увеличению частоты выполнения таких вмешательств: их удельный вес составляет в среднем 5% (с колебаниями от 1,3 до 19,3%) общего количества операций, произведенных при раке легкого (Зырянов Б.Н. и др., 1997; McCaughan В., 1991; Pastorino U. et al., 1991; Mazzetti M. et al., 1994; Ginsberg R.J., 1998).
Вместе с тем следует отметить, что в литературе отсутствуют единое мнение и научно обоснованные показания к выполнению экономных сублобарных резекций при раке легкого.
Вначале эти операции выполняли при низких показателях функции внешнего дыхания и сердечно-сосудистой системы, т.е. в тех случаях, когда невозможно выполнить стандартную лобэктомию, и их называли «компромиссными». После «компромиссных» экономных сублобарных резекций, выполняемых и при внутригрудных метастазах, 5-летняя выживаемость составляет 15-36% (McCormack P.M., 1980; Temeck В.К. et al., 1992).
R.J. Ginsberg (1998) суммировал данные литературы о 763 экономных сублобарных резекциях при периферическом раке легкого в стадии Т1N0M0. Пятилетняя выживаемость составила от 50% (Wain J.С. et al., 1991) до 70% (Read R.C. et al., 1990), а частота локорегионарного рецидива колеблется от 12% (Jensik R.J., 1986), 18,9% (Ginsberg R.J., Rubinstein L.V., 1995) до 22,7% (Warren W.H., Faber L.P., 1994).
При раке легкого I стадии (T1-2N0M0) 5-летняя выживаемость наблюдаемых нами больных после лобэктомии равняется 72%, классической сегментэктомии — 60,4% и атипичной экономной резекции — 42,9%. Локорегионарный рецидив констатирован после лобэктомии в 5% и экономной сублобарной резекции в 22%. Аналогичные показатели приводят М.И. Давыдов и соавт. (1996), Б.Н. Зырянов и соавт. (1997), L.H. Faber (1993), RJ. Ginsberg (1998).
По материалам М. Mazzetti и соавт. (1994), после хирургического лечения 263 больных раком легкого I стадии (T1N0M0, T2N0M0) более 5 лет прожили 51,4%: после лобэктомии (217) — 62%, после экономной резекции — 47,8%. При T1N0M0 5-летняя выживаемость после лобэктомии составила 52,5%, после экономной резекции — 53,8%, а при T2N0M0 — 51,8 и 40% соответственно. Авторы показали значение гистологической структуры и приданной стадии заболевания (табл. 5.12).
Таблица 5.12. Зависимость 5-летней выживаемости (в процентах) больных немелкоклеточным раком легкого I стадии (T1N0M0, T2N0M0) от гистологической структуры опухоли
Как видно из данных табл. 5.12, лучшие результаты при T1N0M0 и T2N0M0 отмечаются у больных плоскоклеточным раком, при железистом паке в стадии T2N0M0 экономная резекция — неадекватная операция, а при крупноклеточном раке не относится к лечебным, после лобэктомий 5-летняя выживаемость низкая.
Причины неудовлетворительных отдельных результатов экономных сублобарных резекций
Основной причиной неудовлетворительных отдельных результатов экономных сублобарных резекций при периферическом раке I стадии является нерадикальность операции. Так, Т. Ishida и соавт. (1994) установили, что при опухоли диаметром менее 1 см регионарные метастазы отсутствуют, 1,1-2 см их обнаруживают у 17%, 2,1-3см — у 38% больных.
Аналогичные данные приводят Y. Ichinose и соавт. (1994) и Н. Asamura и соавт. (1996), согласно которым при периферическом раке диаметром менее 3 см метастазы в регионарных лимфатических узлах были выявлены у 22,3% больных. Следовательно, экономная (клиновидная) резекция легкого при опухоли, соответствующей Т1, не всегда является радикальной, онкологически оправданной операцией.
Не являясь абсолютными противниками выполнения экономной резекции у больных периферическим раком легкого при диаметре опухоли до 3 см, мы все же считаем, что с онкологических позиций минимальным объемом радикального оперативного вмешательства может быть лишь классическая сегментэктомия с раздельной обработкой элементов корня сегмента и срочным интраоперационным морфологическим исследованием регионарных (пульмональные, бронхопульмональные)лимфатических узлов.
При выявлении метастазов оптимальным объемом оперативного вмешательства у функционально операбельных больных должна быть органосохраняющая и функционально щадящая операция типа лобэктомий.
Вместе с тем при локализации опухоли небольших размеров (до 3 см) субплеврально, в плащевой зоне легкого, особенно у больных с низкими резервами дыхательной и сердечно-сосудистой систем, в последние голы привлекает внимание торакоскопическая хирургия, открывающая возможность выполнения экономной резекции при минимальном доступе (Сигал Е.И., Хамидуллин Р.Г., 1998; Casadio С. et al., 1993; McKneally M.F., 1993; Miller J.I., 1993; Landreneau R.J. et al., 1996; Asamura H. et al., 1996).
У больных с ранними формами центрального рака легкого все чаше выявляют рак in situ и микроинвазивный рак, при которых альтернативным методом радикального лечения становится эндоскопический (электрокоагуляция и лазерная коагуляция, фотолинамическая терапия и ее сочетание с лучевой терапией), позволяющий получать удовлетворительные непосредственные и отдаленные результаты (Соколов В.В., 1996).
Вместе с тем необходим поиск более эффективных методов лечения больных раком легкого II-IIIА стадии, составляющих большинство оперированных. Выявление во время операции метастазов во внутригрудных лимфатических узлах, особенно корня легкого и средостения, значительно ухудшает прогноз.
Так, по данным Б.Е. Петерсона (1976), в отсутствие метастазов в регионарных лимфатических узлах 5-летняя выживаемость больных после операций составила 39,5%, а при наличии метастазов — лишь 22,3%. Аналогичные результаты приводят М.Л. Шулутко и соавт. (1983) — 43,4 и 20%, D. Stevenson и соавт. (1983) — 39,2 и 19,3%, Н. Seydel (1984) — 55 и 20%, Ohta Mitsuo и соавт. (1985) — 49,8 и 27,1%.
Установлена прямая зависимость результатов хирургического лечения от характера и обширности метастатического процесса. При поражении бронхолегочных лимфатических узлов (N1) более 5 лет прожили 24,4% больных, а при метастазах в лимфатических узлах средостения (N2) — 8% (Шулутко М.Л. и др., 1982).
По данным S.Serrano и соавт. (1981), эти показатели равны соответственно 30 и 8%, В.П. Харченко и соавт. (1994) — 26,8 и 5,4%. По нашим данным, эти показатели составляют 30,1 и 16,2%.
По материалам МНИОИ им. П.А. Герцена (рис. 5.74), 3- и 5-летняя выживаемость больных раком легкого с поражением внутригрудных лимфатических узлов соответственно в 2,1 и 2,3 раза ниже, чем больных без регионарных метастазов (табл. 5.13).
Рис. 5.74. Продолжительность жизни больных немелкоклеточным раком легкого после хирургического лечения в зависимости от состояния внутригрудных лимфатических узлов.
Таблица 5.13. Продолжительность жизни больных раком легкого после хирургического лечения в зависимости от состояния внутригрудных лимфатических узлов
По материалам М.И. Давыдова и Б.Е. Полоцкого (1994), 5-летняя выживаемость больных раком легкого с поражением бронхопульмональных и корневых лимфатических узлов (N1) составила 38%, а при метастазах в средостенных узлах (N2) — 19,3%. Аналогичная закономерность отмечалась при плоскоклеточном раке и аденокарциноме.
В публикациях последних лет по сути подтверждаются данные о плохом прогнозе при N2 (McCormack P.M., 1995; Naruke Т., 1995; Keller S.M., 1996; Warren W.H., Faber L.P., 1996).
Зависимость отдаленных результатов хирургического лечения рака легкого от гистологической структуры опухоли общеизвестна. По данным большинства хирургов, из трех основных гистологических форм наилучшие результаты отмечаются при плоскоклеточном раке.
Результаты операций изкодифференцированных форм рака легкого
Неблагоприятны отдаленные результаты у больных с низкодифференцированными формами рака легкого. Различие взглядов относительно прогноза объясняется отсутствием унификации гистологических вариантов низко- и недифференцированного рака.
В МНИОИ им. П.А. Герцена из 1902 больных, у которых изучены отдаленные результаты хирургического лечения, у 65% подтвержден плоскоклеточный рак, у 25,1% — железистый рак и у 9,9% — крупноклеточный рак легкого. Пятилетняя выживаемость составила 39,8, 29,6 и 16,6% соответственно (рис. 5.75).
Рис. 5.75. Отдаленные результаты хирургического лечения больных немелкоклеточным раком легкого в зависимости от гистологической структуры опухоли. I — плоскоклеточный рак; II — аденокарцинома; III — крупноклеточный рак.
На продолжительность жизни больных оказывает влияние степень дифференцировки опухолевых клеток внутри каждой гистологической структуры рака легкого. Изучение данных о продолжительности жизни больных железистым раком легкого после хирургического лечения в МНИОИ им. П.А. Герцена показало, что наилучшие отдаленные результаты достигаются при высокодифференцированном и умеренно дифференцированном вариантах, плохие отмечаются при малодифференцированной аденокарциноме: более 3 лет прожили 54,1, 47,3 и 18,1% больных соответственно, более 5 лет — 40,4 и 27,2%, но ни один больной мало-дифференцированной аденокарциномой не пережил этот срок.
Приведенные материалы обусловливают необходимость изучения прогностической роли степени дифференцировки опухолевых клеток и при других гистологических структурах опухоли, что, позволит конкретизировать показания к хирургическому лечению рака легкого.
Детальное изучение особенностей гисто- и ультраструктуры бронхиолоальвеолярного рака, частоты внутригрудного метастазирования при одинаковой первичной опухоли, результатов хирургического лечения позволяет считать, что его последнее место в ряду деления аденокарцином по степени дифференцировки, т.е. степени злокачественности, не соответствует действительности (Трахтенберг А.Х. и др., 1988).
Согласно нашим данным, при бронхиолоальвеолярном раке с первичной опухолью Т1-2 частота поражения внутригрудных лимфатических узлов метастазами у оперированных больных была статистически достоверно ниже (р
Пятилетняя выживаемость больных бронхиолоальвеолярным раком I-II стадии после хирургического лечения равнялась 68,8±7,9%, а больных с высокодифференцированной аденокарциномой — 42,3±6,2%, при IIIА стадии этот срок пережили 28,6 и 22,5% больных соответственно.
В связи с этим представляется более оправданным следующий вариант градации аденокарцином в зависимости от степени их злокачественности и прогноза после хирургического лечения:
• бронхиолоальвеолярный рак;
• высокодифференцированная аденокарцинома;
• умеренно дифференцированная аденокарцинома;
• малодифференцированная аденокарцинома.
Необходимо отметить, что у больных раком легкого I и II стадии гистологическая структура опухоли также играет важную роль в прогнозе результатов хирургического лечения. При плоскоклеточном раке более 5 лет прожили 52,2% больных, аденокарциноме — 42,8%, низкодифференцированных формах рака — 22,2%.
Установлены различия в показателях 5-летней выживаемости больных раком легкого IIIА стадии. Этот срок пережили 28,3, 18,3 и 4% больных соответственно (рис. 5.76). Такие же результаты получены при анализе продолжительности жизни больных в зависимости от состояния регионарных лимфатических узлов.
Рис. 5.76. Отдаленные результаты хирургического лечения больных немелкоклеточным раком легкого в зависимости от стадии заболевания и гистологической структуры опухоли.
а — I-II стадия: б — IIIА стадия; I — плоскоклеточный рак; II — аденокарцинома; III — крупноклеточный рак.
Почти аналогичные показатели 5-летней выживаемости приводят М.И. Давыдов и Б. Е. Полоцкий (1994). В отсутствие регионарных метастазов эти показатели у больных плоскоклеточным раком и с аденокарциномой достоверно не различались — 56,5 и 46,4% соответственно (р>0,05).
При поражении бронхопульмональных и корневых лимфатических узлов (N1) более 5 лет прожили 44,8 и 15,3% больных соответственно, а при метастазах в средостенных лимфатических узлах гистологическая структура опухоли теряет свое значение: этот срок пережили только 20,3 и 12,7% больных.
При глубоком анализе с учетом стратификации не выявлено статистически достоверных различий в продолжительности жизни оперированных больных раком легкого в зависимости от клинико-анатомической формы и локализации опухоли в долях легкого.
Продолжительность жизни больных с центральным и периферическим раком
Большая продолжительность жизни больных центральным раком и при локализации опухоли в верхней доле правого легкого объясняется различиями в гистологической структуре опухолей. При периферическом раке, например, чаше наблюдаются менее благоприятные в прогностическом отношении гистологические формы: малодифференцированная аденокарцинома и недифференцированный рак.
При учете гистологической структуры и стадии заболевания продолжительность жизни больных центральным и периферическим раком одинакова. Большая продолжительность жизни больных после операций на правом легком объясняется особенностями левой половины средостения и закономерностями лимфооттока слева, а также лучшими условиями для удаления трахеобронхиальных и паратрахеальных лимфатических узлов справа.
Согласно результатам кооперированных рандомизированных исследований, осуществленных в ведущих хирургических клиниках США, клинико-анатомическая форма рака легкого, локализация опухоли, иммунный статус больных, сопутствующие воспалительные осложнения, объем оперативного вмешательства и результаты биохимических тестов не оказывают выраженного влияния на отдаленные результаты хирургического лечения (Gail М. et al., 1985; Ginsberg R., 1998).
По данным литературы, к факторам, влияющим на продолжительность жизни больных, оперированных по поводу рака легкого, относят пол и возраст. Преобладает мнение о наилучших показателях выживаемости у женщин и больных старше 50 лет, что принято объяснять биологическими особенностями женского организма, в частности защитными свойствами эстрогенов.
Нами не выявлено статистически достоверных различий в продолжительности жизни больных в зависимости от их пола и возраста. Более низкие показатели выживаемости у мужчин и больных в возрасте до 50 лет также объясняются в основном различиями в гистологической структуре опухолей и стадиях заболевания.
Таким образом, основными факторами прогноза при хирургическом лечении больных раком легкого являются распространенность опухолевого процесса (стадия заболевания, наличие метастазов в регионарных лимфатических узлах), гистологическая структура опухоли и степень анаплазии клеток. Пол и возраст больных, клинико-анатомическая форма и локализация опухоли имеют второстепенное значение в прогнозе и связаны с основными факторами.
Ряд авторов отметили достоверные различия в показателях 5-лстней выживаемости у больных, выявленных при профессиональных осмотрах, и оперированных больных, не предъявлявших жалоб (доклиническая форма рака), по сравнению с больными, у которых заболевание сопровождалось различными клиническими проявлениям
Выживаемость при раке легких
Ежегодно от рака легких в Соединенных Штатах умирает больше людей, чем от рака груди, рака простаты и рака прямой кишки вместе взятых. В 2005 году в Соединенных Штатах было зарегистрировано 159 217 смертей от рака легких. Хотя распространенность рака легких во всем мире ниже, чем в США, рак легких также является ведущей причиной смерти от рака во всем мире. Ежегодно от этой болезни умирает около 1,3 миллиона человек.
Высокий уровень смертности, связанный с раком легких, частично связан с тем, что его очень трудно лечить.По этой причине показатели выживаемости при раке легких довольно низкие. Ниже приводится обзор выживаемости при раке легких в разбивке по времени, уровню прогрессирования рака и типу рака легких.
Общая статистика выживаемости при раке легких
Показатели выживаемости при раке легких зависят от типа диагностированного рака и от того, насколько рано диагностируется болезнь. Расчетная общая выживаемость для всех пациентов с раком легких (независимо от типа рака и стадии рака) составляет:
| Срок службы после диагностики | |
|---|---|
| Годы после диагностики | Выживаемость |
| 5 | 15% |
| 10 | 5% |
В зависимости от стадии рака на момент постановки диагноза выживаемость оценивается в:
| Выживаемость по стадиям рака при диагнозе | |
|---|---|
| Этап | Выживаемость |
| Этап 0 | 70-80% |
| I этап | 50% |
| II этап | 30% |
| III этап | 15% |
| IV этап | Менее 2% |
Немелкоклеточный рак легкого vs.Мелкоклеточный рак легкого
В целом, у пациентов с диагнозом немелкоклеточный рак легкого (НМРЛ) прогноз лучше, чем у пациентов с более агрессивным мелкоклеточным раком легкого (МРЛ). На НМРЛ приходится примерно 85 процентов всех случаев рака легких. Пятилетняя выживаемость при НМРЛ оценивается в:
.
| Пятилетняя выживаемость пациентов с НМРЛ | |
|---|---|
| Этап | Выживаемость |
| Этап IA | 49% |
| Стадия IB | 45% |
| Стадия IIA | 30% |
| IIB этап | 31% |
| этап IIIA | 14% |
| Стадия IIIB | 5% (средняя выживаемость 13 месяцев) |
| IV этап | 1% (средняя выживаемость восемь месяцев) |
Для сравнения, общая 5-летняя выживаемость людей с диагнозом мелкоклеточный рак легкого оценивается примерно в шесть процентов.При лечении среднее время выживания для пациентов с МРЛ составляет от шести до 12 месяцев. Пациенты, диагностированные на более ранней ограниченной стадии, обычно имеют лучший прогноз.
Выживаемость при раке легких: данные в США и во всем мире
Пациенты с раком легких в Соединенных Штатах имеют более длительное среднее время выживания, чем пациенты в других странах. Пятилетняя выживаемость в Европе составляет всего около 8 процентов. Расчетный уровень выживаемости для всего мира также оценивается примерно в восемь процентов.
Информация о компенсации
доступна для тех, у кого диагностирован рак легких, в нашем БЕСПЛАТНОМ информационном пакете по раку легкого или по бесплатному телефону 1-800-988-9729.
Подробнее о:
» Помощь пациентам с раком легких
»Как понять показатели выживаемости
Рак легкого
Среди наиболее распространенных форм рака — рак легких.Более 50 000 женщин и 100 000 мужчин в Соединенных Штатах страдают от рака легких. Курение — самая серьезная причина рака легких. Если человек курит две пачки в день в течение двадцати лет, вероятность возникновения рака легких увеличивается более чем в 70 раз. В случае пассивного воздействия дыма вероятность возникновения рака легких увеличивается на 50 процентов. Если человек подвергается воздействию промышленных металлов, загрязнений и асбеста, вероятность возникновения рака легких возрастает.Также дефицит витамина А, туберкулез и употребление марихуаны могут увеличить риск рака легких.
Мазь для ногтей
Лучшее, 100% натуральное средство для ежедневного ухода за ногтями в идеальной форме.
Основными симптомами рака легких являются охриплость голоса, мокрота (с кровью или ржавчиной), кашель и хрипы. Некоторые пациенты страдают от боли в груди, в руках, плечах, от жара, а также от потери аппетита, одышки и потери веса. Симптомы часто появляются на более поздних стадиях болезни.Рак легких принимает одну из следующих форм: овсяные клетки или мелкие клетки, крупноклеточные, аденокарциномы и плоскоклеточные. Иногда рак, возникающий из других частей тела, также распространяется на легкие. Рентген грудной клетки может обнаружить рак легких. Иногда компьютерная томография требуется для обнаружения небольших опухолей. Далее требуется биопсия, которая окончательно подтверждает рак легких. Классификация рака зависит от размера опухоли и степени ее распространения. В число методов лечения рака легких входят операции по поводу небольших опухолей.В большинстве случаев рак легких распространяется до того, как его обнаруживают. Химиотерапия — основной метод лечения рака легких. Другие методы лечения включают лекарства и лучевую терапию.
Пищевые добавки и травы
Сок алоэ останавливает процесс превращения химических веществ табака в канцерогены. Ежедневно следует принимать 60 мл, то есть 1/4 стакана сока алоэ. Однако если вы страдаете диареей, вам следует избегать сока алоэ вера.
Капсулы астрагала стимулируют Т- и LAK-клетки (активированные имфокином киллеры), эти клетки атакуют рак легких.Принимайте по 1000 мг три раза в день.
Пациенту следует трижды в день принимать 2 мл настойки астрагала в 1/4 стакана воды. Если у вас кожная инфекция или жар, не используйте астрагал.
Пациенту следует принимать 2 мл настойки женьшеня Panax, смешанные с 1/4 стакана воды, трижды в день. Это стимулирует иммунную систему и увеличивает продолжительность жизни, если человек проходит курс химиотерапии.
Настойка кошачьего когтя: назначенную дозу лекарства смешать с 1/2 стакана воды и 1 чайной ложкой лимонного сока.Лекарство стимулирует иммунную систему. Пациентам с сахарным диабетом, принимающим инсулин, не следует принимать этот препарат. Беременным женщинам также следует избегать приема этого лекарства. Это лекарство нельзя назначать детям младше шести лет.
Кайенский порошок: 1 столовую ложку кайенского порошка следует использовать ежедневно. Это останавливает превращение табачных химикатов в канцерогенную форму.
Настойка Санта-Клауса Эспинхейра: Принимать в соответствии с инструкцией. Лекарство токсично для различных видов клеток рака легких.
Лентинан внутримышечно: Инъекция проводится в соответствии с рекомендациями врача. Это увеличивает время выживания при вторичном раке легких.
Мазь от прыщей
Акне мешает? Попробуйте эту 100% натуральную мазь и навсегда измените свою жизнь.
Таблетки полисахарида куреха: 6000 мг таблеток PSK следует принимать ежедневно. Эти таблетки продлевают срок жизни пациента при лучевой терапии.
Капсулы с семенами бугу чжи или псоралеи: капсулы следует принимать трижды в день, доза не должна превышать 1000 мг.Лекарство следует принимать под наблюдением врача. В лекарстве есть соединения, подавляющие рак легких. Однако семя псоралеи увеличивает чувствительность пациента к солнечному свету. Следует избегать воздействия солнца или использовать солнцезащитный крем.
Капсулы
Scutellaria: капсулы следует принимать трижды в день, дозировка должна находиться в пределах 1 000–2 000 мг. В составе лекарства есть соединения, которые останавливают воспалительные процессы и облегчают кашель. Не применяйте лекарство, если вы страдаете диареей.
Таблетки концентрата изофлавона сои следует принимать один раз в день, и доза не должна превышать 3000 мг. Эти таблетки помогают в уничтожении клеток рака легких.
Таблетки куркумы и куркумина: эти таблетки следует принимать трижды в день, и дозировка не должна превышать 250 мг. Эти травяные таблетки активируют p53, ген, отключающий рак, для борьбы с мелкоклеточным раком легких.
Ароматерапия
Эфирные масла, обычно используемые при раке легких:
Гомеопатия
Гомеопатические препараты действуют как паллиативное средство при лечении пациентов, страдающих раком легких.Гомеопатические препараты уменьшают тяжесть и интенсивность симптомов, облегчая тем самым пациентов, страдающих раком легких. Бедствие и боль пациентов можно уменьшить с помощью гомеопатических средств. Эти лекарства не имеют каких-либо побочных эффектов, и когда гомеопатические лекарства используются с химиотерапией, они делают химиотерапию более переносимой, контролируя отрицательные эффекты химиотерапевтических препаратов.
Гомеопатические препараты помогают повысить иммунитет пациента, что приводит к увеличению способности человека к самовосстановлению.Повышенный иммунитет пациента помогает ему сопротивляться вторичным инфекциям и предотвращает дальнейшее распространение болезни. После операции гомеопатические препараты помогают быстрее выздороветь и снижают вероятность рецидива заболевания. Таким образом, гомеопатические лекарства улучшают жизнь пациента и помогают ему вести более здоровый образ жизни. Ниже приведены распространенные гомеопатические средства, используемые для лечения рака легких: Euphorbium officinarum, Bryonia, Chelidonium majus, Arsenicum iodatum, Acalypha indica, Phosphorous, Sulphuricum acidum, Bromium, Methylene blue, Crotalus horridus, Conium maculatum и Aranea diadema.
Дополнительные действия, которые вы можете сделать
Лучший способ избежать рака легких — это бросить курить и избегать табачного дыма как из активных, так и из пассивных источников. В случае, если пациент постоянно подвергается воздействию табачного дыма, ему становится трудно преодолеть рак, вместо этого это может привести к другим заболеваниям легких, что приведет к снижению емкости легких. Пациенту следует регулярно принимать петрушку. Петрушка богата миристицином, который, как обнаружено, активирует детоксифицирующий фермент GST, тем самым уменьшая образование опухолей легких.
Добавки фолиевой кислоты следует принимать ежедневно в соответствии с рекомендациями врача. Если пациент проходит химиотерапию МТА, тегафур или фторурацил и UFT, ему следует избегать приема фолиевой кислоты. Недавнее исследование, проведенное в Медицинском центре Новой Англии, показало, что пациенты с раком легких, которые принимали добавки фолиевой кислоты, имели период без рака в течение сорока одного месяца. Для сравнения, пациенты, которые не принимали добавки фолиевой кислоты, имели период без рака одиннадцать месяцев.Потребление витамина B12 (500 миллиграммов) принесет пациентам дополнительную пользу. Витамин B12 помогает предотвратить повреждение легких.
GLA, то есть гамма-линоленовая кислота, способствует росту здоровых клеток и замедляет рост клеток рака легких. GLA работает вместе с цисплатином и убивает клетки рака легких. Употребление натуральных источников, богатых ГЛК, таких как масло примулы вечерней или масло семян бурачника, помогает улучшить состояние пациента. Однако GLA не следует принимать в случае химиотерапии цисплатином.
Воздействие солнечного света помогает пациенту получить необходимый витамин D. Витамин D вырабатывается кожей из ультрафиолетовых (УФ) лучей, присутствующих в солнечном свете. В случае достаточного количества витамина А это приводит к клеточному самоубийству или апоптозу раковых клеток в легких. Таким образом, пациент должен сидеть на солнечном свете так, чтобы руки и лицо смотрели на солнечный свет около двадцати минут, и это должно быть повседневной практикой. Пациентам следует избегать использования солнцезащитного крема, так как он блокирует необходимые УФ-лучи солнечного света.
Когда пациент проходит курс химиотерапии, ему следует избегать приема витамина Е, поскольку он защищает раковые клетки и делает их чувствительными к адриамицину (доксорубицин гидрохлорид) и Велбану (винбластин сульфат). Диета, богатая овощами и фруктами, помогает снизить вероятность возникновения рака легких.
Диета должна быть богата черным чаем, яблоками, морковью и помидорами, так как они помогают предотвратить рак легких. Исследование, проведенное в Швеции, показало, что морковь помогает избежать рака легких у людей, которые никогда не курили.Для женщин помидоры — лучшая пища для предотвращения рака легких, поскольку в них есть химическое вещество под названием ликопин, которое снижает риск рака легких. Черный чай также снижает риск развития рака легких; Легкие курильщики должны выпить не менее двух чашек черного чая. Употребление яблок также снижает риск развития рака легких на 50 процентов.
Женщинам особенно следует избегать жареного красного мяса. Согласно исследованию, проведенному Национальным институтом рака, каждая 1/3 унции жареного красного мяса увеличивает вероятность рака легких примерно на 9 процентов.Увеличение потребления жареного красного мяса в рационе увеличивает риск рака легких.
Диета может помочь снизить риск развития рака легких. Также это может повлиять на то, где происходит развитие рака. В нижней части легких лечить рак легче, в то время как в верхней части легких лечить рак очень сложно. Рекомендуется как минимум пять приемов пищи с оранжевыми и желтыми овощами, что снижает вероятность развития раковых клеток в верхней части легких.
Для постоянных курильщиков очень полезно ежедневное потребление 150 мкг селена. Сочетание низкого уровня витамина Е, тяжелого курения и селена увеличивает риск возникновения рака легких. Однако курильщикам следует избегать приема добавок бета-каротина. Исследования показали, что добавки бета-каротина не помогают предотвратить рак легких, а наоборот, увеличивают вероятность возникновения рака легких у курильщиков. Это связано с тем, что бета-каротин приводит к превращению табачного дыма в канцерогенную форму.Ситуация ухудшается, если потребление бета-каротина не сбалансировано использованием других каротинов, содержащихся в овощах и фруктах. Рекомендуется употреблять больше овощей и фруктов, а не принимать добавки с бета-каротином.
Другие полезные травы
Мазь от грибка
Вся сила фармацевтических фунгицидов — но без агрессивных химикатов.
Комментарии
Последние новости о раке легких | Информация о лечении NSCLC / SCLC
Новости рака легких
BiTE, нацеленный на DLL3, демонстрирует противоопухолевую активность при SCLC
Дата публикации
BiTE, нацеленный на DLL3, продемонстрировал противоопухолевую активность — но высокие показатели СВК — среди пациентов с ранее пролеченным SCLC.
Экспрессия PD-L1 во внеклеточных везикулах как прогностический биомаркер
Дата публикации
Внеклеточные везикулы, несущие PD-L1 в качестве груза, могут функционировать как прогностический биомаркер иммунотерапевтического ответа при НМРЛ.
Адъювант Осимертиниб: новый стандарт в EGFR — Мутант NSCLC
Дата публикации
Через 2 года в группе осимертиниба в два раза больше пациентов со стадией II – IIIA были живы и заболели. бесплатно, как в группе плацебо.
Эффективность ALK TKI согласно статусу опухоли ALK
Дата публикации
В этом анализе сравнивались результаты эффективности подгрупп пациентов с НМРЛ, получавших алектиниб, и кризотиниба в соответствии со статусом опухоли ALK.
Таргетная терапия, иммунотерапия, иммуномодуляторы: краткое руководство по описанию терапии рака
Дата публикации
Иногда различия между группами лечения рака нечеткие.Вот руководство по их определениям и происхождению.
Больше понижения стадии НМРЛ с помощью неоадъювантной химиотерапии плюс ICI
Дата публикации
Неоадъювантное лечение химиотерапией плюс ниволумаб привело к более высокой частоте снижения стадии НМРЛ по сравнению с химиотерапией или только лечением ICI.
Ингибитор AXL плюс пембролизумаб проявляет активность в отношении ранее пролеченных NSCLC
Дата публикации
Бемсентиниб, ингибитор AXL, был переносимым и продемонстрировал противоопухолевую активность в комбинации с пембролизумабом при AXL-положительном NSCLC.
Телемедицина и качество жизни пациентов с раком легких
Дата публикации
В связи с продолжающейся пандемией COVID-19 телемедицина стала как никогда важной.Исследования Центров по контролю и профилактике заболеваний США (CDC) показали, что в первом квартале 2020 года использование услуг телемедицины увеличилось на 50% по сравнению с 2019 годом, а на 13 неделе 2020 года — на 154%…
Характеристики Детская мезотелиома
Дата публикации
Детская мезотелиома продемонстрировала отличные характеристики от болезни взрослых, включая хороший прогноз.
Статистический индекс
показывает, что многие исследования ICI демонстрируют неопределенную клиническую пользу демонстрируют сильную клиническую пользу. Утверждение FoundationOne Liquid CDx расширено до PIK3CA , BRCA и ALK Изменения
Дата публикации
FDA одобрило FoundationOne CDxis в качестве вспомогательного средства диагностики рака молочной железы , рукапариб при некоторых гинекологических формах рака и алектиниб при раке легких.
Реальные результаты для пациентов, получавших лечение с помощью ингибиторов иммунных контрольных точек
Дата публикации
Пациенты, получавшие ингибиторы иммунных контрольных точек в реальном мире, как правило, имели лучшие результаты, чем пациенты, получившие стандартную помощь.
Использование специальной паллиативной помощи у пациентов с метастатическим немелкоклеточным раком легкого
Дата публикации
Анализ данных из базы данных SEER-Medicare продемонстрировал преимущества специализированной паллиативной помощи для Medicare с течением времени бенефициары с НМРЛ.
Добавление цетуксимаба к афатинибу не увеличивает выживаемость при EGFR — мутантный NSCLC
Дата публикации
Добавление цетуксимаба к афатинибу не показало клинической пользы и привело к увеличению токсичности для лечения пациенты с НМРЛ с мутантным EGFR.
Оценка влияния клинических и патологических характеристик на ОС при злокачественной мезотелиоме брюшной полости
Дата публикации
Результаты этого ретроспективного когортного исследования подтверждают «сложное взаимодействие клинических и патологических факторов», способствующих развитию болезни. прогноз этих пациентов.
Группа вопросов Рекомендации по устранению различий в скрининге рака легких
Дата публикации
Стратегии должны учитывать расовые, этнические, социально-экономические и гендерные различия.
Осимертиниб проходит приоритетную проверку для ранней стадии EGFR -Мутантный НМРЛ
Дата публикации
sNDA подтверждается данными фазы 3 исследования ADAURA, в котором осимертиниб оценивался по сравнению с плацебо у 682 пациентов с ранним -стадия EGFRm NSCLC после полной резекции опухоли с адъювантной химиотерапией или без нее.
Opdivo Plus Yervoy одобрен для лечения злокачественной мезотелиомы плевры
Дата публикации
Одобрение было основано на предварительно определенном промежуточном анализе открытого исследования CheckMate-743 фазы 3.
Тепотиниб дает высокие показатели частичного ответа при НМРЛ с MET Изменениями
Дата публикации
Изменение MET встречается у 3–4% пациентов с этим заболеванием.
Преимущество ОС для атезолизумаба первой линии при метастатическом НМРЛ с высокой экспрессией PD-L1
Дата публикации

 При прорастании опухоли в крупный сосуд у пациента остро возникает массивное легочное кровотечение, вплоть до летального исхода.
При прорастании опухоли в крупный сосуд у пациента остро возникает массивное легочное кровотечение, вплоть до летального исхода.
 Они влияют на жизненный цикл клетки, блокируют апоптоз (запрограммированную гибель клетки), что провоцирует неконтролируемое деление и рост эпителия.
Они влияют на жизненный цикл клетки, блокируют апоптоз (запрограммированную гибель клетки), что провоцирует неконтролируемое деление и рост эпителия.