Колоректальный рак с синхронными метастазами в легких: клинические характеристики, лечение, прогноз | Расулов
1. Steele G. Jr. Natural History Studies and the Evolution of Regional Treatment Modalities for Patients With Isolated Liver Metastases From Primary Colon and Rectum Carcinoma. Cancer Control 1996;3(1):34–41.
2. Kanas G.P., Taylor A., Primrose J.N. et al. Survival after liver resection in metastatic colorectal cancer: review and meta-analysis of prognostic factors. Clin Epidemiol 2012;4:283–301.
3. Saltz L.B., Clarke S., Diaz-Rubio E. et al. Bevacizumab in combination with oxaliplatinbased chemotherapy as first-line therapy in metastatic colorectal cancer: a randomized phase III study. J Clin Oncol 2008;26(12):2013–9.
4. Stathopoulos G.P., Batziou C., Trafalis D. et al. Treatment of colorectal cancer with and without bevacizumab: a phase III study. Oncology 2010;78(5–6):376–81.
Stathopoulos G.P., Batziou C., Trafalis D. et al. Treatment of colorectal cancer with and without bevacizumab: a phase III study. Oncology 2010;78(5–6):376–81.
5. Langenbuch C. Ein Fall von Resection eines linksseitigen Schurlappens der Leber. Berl Klin Wochenschr 1888;25:37–9.
6. Kemeny N.E. Treatment of metastatic colon cancer: “the times they are A-changing”. J Clin Oncol 2013;31(16):1913–6.
7. Tan K.K., Lopes Gde L. Jr, Sim R. How uncommon are isolated lung metastases in colorectal cancer? A review from database of 754 patients over 4 years. J Gastrointest Surg 2009;13(4):642–8.
8. Blalock A. Recent advances in surgery. New Engl J Med 1944;231:261–7.
9. National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology: rectal cancer 1.2016. Available at: http://www.nccn.org/professionals/physician_gls/pdf/rectal.pdf 2015.
National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology: rectal cancer 1.2016. Available at: http://www.nccn.org/professionals/physician_gls/pdf/rectal.pdf 2015.
10. National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology: colon cancer 2.2016. Available at: http://www.nccn.org/professionals/physician_gls/pdf/colon.pdf 2015.
11. Poston G.J., Tait D., O’Connell S. et al. Diagnosis and management of colorectal cancer: summary of NICE guidance. BMJ 2011;343:d6751.
12. Gonzalez M., Gervaz P. Risk factors for survival after lung metastasectomy in colorectal cancer patients: systematic review and meta-analysis. Future Oncol 2015;11(2 Suppl):31–3.
13. Aberg T., Malmberg K.A., Nilsson B., Nöu E. The effect of metastasectomy: fact or fiction? Ann Thorac Surg 1980;30(4):378–84.
Aberg T., Malmberg K.A., Nilsson B., Nöu E. The effect of metastasectomy: fact or fiction? Ann Thorac Surg 1980;30(4):378–84.
14. Penna C., Nordlinger B. Colorectal metastasis (liver and lung). Surg Clin North Am 2002;82(5):1075–90.
15. Mitry E., Guiu B., Cosconea S. et al. Epidemiology, management and prognosis of colorectal cancer with lung metastases: a 30-year population-based study. Gut 2010;59(10):1383–8.
16. Nozawa H., Sunami E., Nakajima J. et al. Synchronous and metachronous lung metastases in patients with colorectal cancer: A 20-year monocentric experience. Exp Ther Med 2012;3(3):449–56.
17. Poultsides G.A., Paty P.B. Reassessing the need for primary tumor surgery in unresectable metastatic colorectal cancer: overview and perspective. Ther Adv Med Oncol 2011;3(1):35–42.
Ther Adv Med Oncol 2011;3(1):35–42.
18. Yedibela S., Klein P., Feuchter K. et al. Surgical management of pulmonary metastases from colorectal cancer in 153 patients. Ann Surg Oncol 2006;13(11):1538–44.
19. Watanabe K., Nagai K., Kobayashi A. et al. Factors influencing survival after complete resection of pulmonary metastases from colorectal cancer. Br J Surg 2009;96(9): 1058–65.
20. Onaitis M.W., Petersen R.P., Haney J.C. et al. Prognostic factors for recurrence after pulmonary resection of colorectal cancer metastases. Ann Thorac Surg 2009;87(6): 1684–8.
21. Rama N., Monteiro A., Bernardo J.E. et al. Lung metastases from colorectal cancer: surgical resection and prognostic factors. Eur J Cardiothorac Surg 2009;35(3):444–9.
Eur J Cardiothorac Surg 2009;35(3):444–9.
22. Hattori N., Kanemitsu Y., Komori K. et al. Outcomes after hepatic and pulmonary metastasectomies compared with pulmonary metastasectomy alone in patients with colorectal cancer metastasis to liver and lungs. World J Surg 2013;37(6):1315–21.
Прогноз выживаемости при раке толстой кишки
Большинство пациентов беспокоятся по поводу прогноза своего заболевания. В настоящее время существует несколько разных способов оценки прогноза пациентов, наиболее важный из которых основывается на анализе стадии развития заболевания.
Выделают 4 стадии рака толстой кишки:
- Опухоль не проросла через стенку кишки
- Опухоль охватывает всю толщину стенки кишки
- Опухоль распространилась на лимфоузлы
- Имеются отдаленные метастазы опухоли
Навигация по статье
Как пройти дистанционное лечение рака в Израиле во время эпидемии коронавируса?
youtube.com/embed/k5a7EpIOUZs» frameborder=»0″ allow=»accelerometer; autoplay; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»»/>
Каков прогноз на различных стадиях рака толстой кишки?
Само собой, при раке на первой стадии удаление совсем небольшой опухоли ведет к дальнейшему благоприятному прогнозу. В данном случае почти все пациенты полностью излечиваются. Однако если опухоль вырастает в размере или распространяется в лимфатические узлы, прогноз ухудшается. Сегодня онкологи применяют разнообразные способы лечения в целях улучшения итогового результата с помощью адъювантной химиотерапии. При метастатическом заболевании речь идет об активно развивающемся, смертельно опасном раке, и химиотерапия необходима для увеличения общей выживаемости.
За последние 10 лет общая выживаемость превысила показатель в 30 месяцев, то есть 2,5 с половиной года. Это небывалый успех. При отсутствии лечения выживаемость составит примерно 6 или 8 месяцев.
Изменения касаются не только данного показателя – значительно улучшилось и качество жизни пациентов. Медицина постоянно совершенствуется, врачи теперь владеют некоторыми клиническими патологическими критериями, и при изучении биоматериалов с помощью микроскопа специалисты могут определить потенциальную степень агрессивности опухолей – такие новообразования обычно низкодифференцированны. Чем больше у опухоли метастазов, тем хуже конечный прогноз. Если рак проник в печень, легкое, кость или головной мозг, болезнь хуже поддается лечению и прогноз не так благоприятен, как в случае обнаружения одиночных очагов в печени или легком.
Как новые методы диагностики помогают уточнить прогноз заболевания?
В настоящее время врачи овладевают все большим объемом информации о молекулярных маркерах, и пациенты могут пройти соответствующее обследование. Обнаружение мутации в гене BRAF свидетельствует о неблагоприятном прогнозе. Об этом врачу всегда тяжело говорить пациенту. Однако он имеет право знать о наличии у него такой генной мутации и о плохом прогнозе; хорошая новость заключается в том, что современная наука разработала медикаменты с таргетным воздействием именно на этот прогностический маркер.
Однако он имеет право знать о наличии у него такой генной мутации и о плохом прогнозе; хорошая новость заключается в том, что современная наука разработала медикаменты с таргетным воздействием именно на этот прогностический маркер.
Вероятно, в будущем ученые обнаружат еще больше прогностических маркеров, позволяющих выбрать оптимальный метод лечения рака в Израиле и лучше понять, как подобрать химиотерапию в индивидуальном порядке для каждого пациента, используя таргетные препараты, разработанные специально для этой мутации.
Понадобится более тщательный мониторинг состояния таких пациентов, потому что у них могут рано образоваться метастазы – в том числе в таких необычных областях, как головной мозг. Поэтому по мере внедрения новых технологий в клиническую практику врачи смогут разрабатывать максимально индивидуализированные схемы лечения и наблюдения за состоянием пациентов. Эти инновации будут полезными для всех онкобольных, так как чем больше врачи знают о заболевании, тем ответственнее они подходят к терапии.
В сентябре 2015 года я почувствовала комок в левой груди. Я не паникер, но я знала, что это может значить. У меня была назначена встреча через месяц с моим акушером-гинекологом, поэтому сначала я подумала, что подожду и поговорю об этом со своим врачом.
У меня была маммография всего шесть месяцев назад. Но после изучения информации в интернете, я поняла, что для безопасности нужно встретиться с врачом раньше.
Читать далее…
За пять лет до того, как мне поставили диагноз, я тренировалась четыре раза в неделю и была в отличной форме. Друзья заметили, что я сильно похудела, но я просто думала, что это связано с моим активным образом жизни. В это время у меня постоянно были проблемы с желудком. Мои врачи рекомендовали безрецептурные препараты.
В течение месяца у меня также была постоянная диарея. Мои врачи не нашли ничего плохого.
Читать далее…
В начале 2016 года я воспользовалась советом врача и сделала колоноскопию. Я никогда этого не делала до этого. Мой доктор показал мужу, и мне изображение толстой кишки. На изображении были видны два полипа. Врач указал на первое место на моей толстой кишке, заверив нас, что беспокоиться не о чем. Затем он указал на другое место и сказал нам, что, по его мнению, есть подозрение на рак. Во время процедуры он сделал биопсию, и ткань была проанализирована.
Мой доктор показал мужу, и мне изображение толстой кишки. На изображении были видны два полипа. Врач указал на первое место на моей толстой кишке, заверив нас, что беспокоиться не о чем. Затем он указал на другое место и сказал нам, что, по его мнению, есть подозрение на рак. Во время процедуры он сделал биопсию, и ткань была проанализирована.
Читать далее…
В 2011 году у меня начался кислотный рефлюкс. Это было неудобно и тревожно, поэтому я пошел к нашему семейному врачу для обследования. Во время визита он спросил меня, когда я в последний раз проверял свой антиген пса, рутинный тест, который многие мужчины делают, чтобы проверить возможные признаки рака простаты. Прошло около трех лет с тех пор, как я делал этот тест, поэтому он добавил его к моему визиту в тот день.
Читать далее…
Моя история начинается с онемения. Однажды в 2012 году три пальца на моей левой руке внезапно потеряли чувствительность. Я сразу же записался на прием к врачу. К тому времени, когда врач меня смог принять, уже все прошло, но жена убедила меня все-таки пойти на консультацию. У меня был рентген, чтобы увидеть, есть ли какие-либо признаки повреждения позвоночника, возможно, от вождения грузовика. Когда на пленке появились какие-то…
У меня был рентген, чтобы увидеть, есть ли какие-либо признаки повреждения позвоночника, возможно, от вождения грузовика. Когда на пленке появились какие-то…
Читать далее…
Зимой 2010 года, когда мне было 30 лет, я почувствовала внезапную боль в правом боку. Боль была резкой и началась без предупреждения. Я сразу же отправилась в ближайшую больницу.
Врач получил результаты моего анализа крови, и он увидел, что мой уровень лейкоцитов был чрезвычайно повышен. Врач и другие, кто видел эти результаты, были встревожены и попросили гинеколога по вызову приехать ко мне сразу же.
Читать далее…
Около трех лет я боролся с прерывистым кашлем. Он появлялся зимой и исчезал к весне, а потом я забывал о нем. Но осенью 2014 года это произошло раньше. В октябре моя жена позвонила местному пульмонологу. Первая встреча нам назначили через три месяца.
… В онкоцентре Ихилов мы встретились с торакальным хирургом. Решили полностью удалить узелок. Читать далее…
Читать далее…
Лечение в онкоцентре Ихилов.
Как специалисты клиники лечат пациентов во время коронавируса.
Узнать подробности
Лікування в онкоцентрі Іхілов.
Як фахівці клініки лікують пацієнтів під час коронавируса.
Дізнатися подробиці
Стоимость диагностики рака толстой кишки в онкоцентре Ихилов
| Вид диагностики или лечения | Стоимость |
|---|---|
| ПЭТ-КТ (для определения возможных метастазов) | $1714 |
| Анализы крови (включая онкомаркеры) | $870 |
| Консультация онколога | $563 |
Первый шаг к выздоровлению вы можете сделать прямо сейчас. Для этого заполните заявку – и в течение 2 часов с вами свяжется один из наших врачей. Либо позвоните по телефону:+972-3-376-03-58 в Израиле и +7-495-777-6953 в России.
Эта консультация ни к чему вас не обязывает и является совершенно бесплатной. Мы гарантируем вам полную конфиденциальность и сохранение медицинской тайны. Мы поможем вам, как помогли и другим пациентам.
Мы поможем вам, как помогли и другим пациентам.
НЕПОСРЕДСТВЕННЫЕ РЕЗУЛЬТАТЫ РАДИКАЛЬНЫХ ОПЕРАЦИЙ В УСЛОВИЯХ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ РАКА ПРЯМОЙ КИШКИ | Афанасьев
1. Авдеев С.В., Афанасьев С.Г., Савосина С.И., Фальтин В.В., Гердт Л.В., Стахеева М.Н., Тузиков С.А. Оценка эффективности эпидуральной анестезии при комбинированном и хирургическом лечении рака прямой кишки // Сибирский онкологический журнал. 2015. № 2. С. 39–45.
2. Афанасьев С.Г., Старцева Ж.А., Тарасова А.С., Усова А.В., Самцов Е.Н. Результаты комбинированного лечения рака прямой кишки с применением пролонгированной предоперационной химиолучевой терапии // Сибирский онкологический журнал. 2012. № 6. С. 5–12.
3. Барсуков Ю.А., Кузьмичев Д.В., Ткачев С.И., Алиев В.А., Тамразов Р. И., Малихов А.Г., Мамедли З.З., Татаев И.Ш., Власов О.А., Гордеев С.С. Комплексное лечение больных раком прямой кишки с использованием неоадъювантной термохимиолучевой терапии // Онкологическая колопроктология. 2014. № 3. С. 23–28.
И., Малихов А.Г., Мамедли З.З., Татаев И.Ш., Власов О.А., Гордеев С.С. Комплексное лечение больных раком прямой кишки с использованием неоадъювантной термохимиолучевой терапии // Онкологическая колопроктология. 2014. № 3. С. 23–28.
4. Давыдов М.И., Аксель Е.М. Статистика злокачественных новообразований в России и странах СНГ в 2009 г. // Вестник РОНЦ им. Н.Н. Блохина РАМН. 2010. Т. 23, № 3 (85). Прил. 1.
5. Злокачественные новообразования в России в 2014 году / Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М., 2016, 250 с.
6. Одарюк Т.С., Воробьев Г.И., Шелыгин Ю.А. Хирургия рака прямой кишки. М., 2005. 256 с.
7. Правосудов И.В., Алиев И.И., Шулепов А.В., Крживицкий П. И. Мультидисциплинарный подход к лечению больных раком прямой кишки: оценка клинического и патологического ответа у больных, получавших предоперационную химиолучевую терапию // Онкологическая колопроктология. 2012. № 1. С. 7–11.
И. Мультидисциплинарный подход к лечению больных раком прямой кишки: оценка клинического и патологического ответа у больных, получавших предоперационную химиолучевую терапию // Онкологическая колопроктология. 2012. № 1. С. 7–11.
8. Черниченко М.А., Сидоров Д.В., Бойко А.В. Лечение рака нижнеампулярного отдела прямой кишки: современное состояние проблемы // Онкология. Журнал им. П.А. Герцена. 2015. Т. 4, № 1. С. 84–90.
9. Чойнзонов Е.Л., Старцева Ж.А., Мухамедов М.Р., Спивакова И.О., Черемисина О.В., Грибова О.В., Кульбакин Д.Е., Суркова П.В. Локальная гипертермия в комбинированном лечении рака гортани и гортаноглотки // Сибирский онкологический журнал. 2014. № 5. С. 5–9.
10. Юдин А.А., Кохнюк В.Т., Колядич Г.И. Непосредственные результаты комбинированного и комплексного лечения пациентов с низколокализованным раком прямой кишки // Онкологическая колопроктология. 2015. Т. 5, № 4. С. 19–23.
2015. Т. 5, № 4. С. 19–23.
11. Folkessen J., Birgesson H., Pahlman L., Cedermark B., Glimelius B., Gunnarsson U. Swedish rectal cancer trial: long lasting benefits from radiotherapy on survival and local recurrence rate // J. Clin. Oncol. 2005. Vol. 23 (24). P. 5644–5650.
12. Maluta S., Romano M., Dall’oglio S., Genna M., Oliani C., Pioli F., Gabbani M., Marciai N., Palazzi M. Regional hyperthermia added to intensified preoperative chemo-radiation in locally advanced adenocarcinoma of middle and lower rectum // Int. J. Hyperthermia. 2010. Vol. 26 (2). P. 108–117. doi: 10.3109/02656730903333958.
13. Musters G.D., Buskens C.J., Bemelman W.A., Tanis P.J. Perineal wound healing after abdominoperineal resection for rectal cancer: a systematic review and meta-analysis // Di. s Colon Rectum. 2014. Vol. 57 (9). P. 1129–1139. doi: 10.1097/DCR.0000000000000182.
s Colon Rectum. 2014. Vol. 57 (9). P. 1129–1139. doi: 10.1097/DCR.0000000000000182.
14. Schroeder C., Gani C., Lamprecht U., von Weyhern C.H., Weinmann M., Bamberg M., Berger B. Pathological complete response and sphincter-sparing surgery after neoadjuvant radiochemotherapy with regional hyperthermia for locally advanced rectal cancer compared with radiochemotherapy alone // Int. J. Hyperthermia. 2012. Vol. 28 (8). P. 707–714. doi: 10.3109/02656736.2012.722263.
15. Zengel B., Uslu A., Adıbelli Z., Yetiş H., Cengiz F., Aykas A., Şimşek C., Akpınar G., Eliyatkın N., Duran A.Adjuvant versus neoadjuvant chemoradiotherapy in distal rectal cancer: Comparison of two decades in a single center // Ulus Cerrahi Derg. 2015. Vol. 31 (4). P. 218–223. doi: 10.5152/UCD.2015.3015.
Рак толстой кишки, опухоли — Медицинский центр
Жалобы (симптомы): При начальных стадиях рака кишечника, жалоб практически нет (главная опасность). Вот почему ВОЗ рекомендует с 40 лет проводить планово без всяких жалоб проходить колоноскопию. Первые симптомы это запор, понос или неустойчивый стул. Выделение крови и слизи также являются грозными симптомами рака толстой кишки, но почему то большинство людей связывают эти жалобы с геморроем и порой обращаются слишком поздно. Анемия (малокровие) одна из частых симптомов рака правой половины толстой кишки В настоящее время если соединить статистику рака прямой и ободочной кишки, то рак кишечник выходит на первое место среди онкологических заболеваний.
Вот почему ВОЗ рекомендует с 40 лет проводить планово без всяких жалоб проходить колоноскопию. Первые симптомы это запор, понос или неустойчивый стул. Выделение крови и слизи также являются грозными симптомами рака толстой кишки, но почему то большинство людей связывают эти жалобы с геморроем и порой обращаются слишком поздно. Анемия (малокровие) одна из частых симптомов рака правой половины толстой кишки В настоящее время если соединить статистику рака прямой и ободочной кишки, то рак кишечник выходит на первое место среди онкологических заболеваний.
Рак толстой кишки: причины
- Одна из причин рафинированная пища – низкое содержание растительной клетчатки и увеличение в рационе мяса , сладостей, выпечки
- Последние годы ученые выяснили, что одной из причин является запор.
- Полипы которые часто перерождаются рак кишечника
- Наследственность
Рак толстой кишки: диагностика
Как мы уже сказали, симптомов может не быть и если появились запор понос или неустойчивый стул с выделение крови при стуле то первое, что нужно сделать обратиться на прием к проктологу.
Благодаря мобильности персонала и хорошего оборудования мы можем за два дня провести обследование и выставить предварительный диагноз. Проводится первичный осмотр проктологом, выполняется ректороманоскопия (инструментальный осмотр прямой кишки) и на следующий день выполняется колоноскопия. Если доктор что то заподозрил берется материал на гистологическое исследование и через 5-7 дней диагноз выставлен. Необходимо также выполнить дополнительные исследования для выяснения вопроса о распространенности опухолевого процесса.
Лечение рака толстой кишки: методы и перспективы
Лечение в настоящее время комбинированное включает химиотерапию, лучевую терапию и оперативное лечение.
Есть одно заветное правило, чем раньше выставлен диагноз, тем лучше прогноз. К сожалению ранние стадии рака толстой кишки ставятся лишь 15-20% случаев. Основная проблема это нежелание людей сделать колоноскопию после 40 лет при отсутствии жалоб.
Рак толстой кишки: прогноз
Вовремя проведенная операция, химиотерапия при раке толстой кишки позволяет давать положительные прогнозы и чем больше стадия тем хуже прогноз.
Медцентр ведет прием жителей городов: Иркутск, Шелехов, Ангарск, Братск, Усолье-сибирское, Черемхово и других городов Иркутской области.
ВЛИЯНИЕ НАЦИОНАЛЬНЫХ ПРОЕКТОВ В ОБЛАСТИ ОНКОЛОГИИ НА ВЫЖИВАЕМОСТЬ БОЛЬНЫХ РАКОМ ПРЯМОЙ КИШКИ: ПОПУЛЯЦИОННЫЙ АНАЛИЗ | Дубовиченко
1. GLOBOCAN 2018: estimated cancer incidence, mortality and prevalence worldwide in 2012 [accessed 03.11.2018]. Available at: http://gco.iarc.fr/today/online-analysis-pie
2. Winawer S, Classen M, Lambert R, Fried M. Colorectal cancer screening. URL: http://www.worldgastroenterology.org/assets/downloads/en/pdf/guidelines/06_colorectal_cancer_screening.pdf (ACCESSED 21.07.2018).
3. GLOBOCAN 2012: estimated cancer incidence, mortality and prevalence worldwide in 2012 [accessed 15. 04.2017]. Available at: http://globocan.iarc.fr/Default.aspx
04.2017]. Available at: http://globocan.iarc.fr/Default.aspx
4. Murray SA, Grant E, Grant A, Kendall M. Dying from cancer in developed and developing countries: lessons from two qualitative interview studies of patients and their carers. BMJ. 2003 Feb 15;326 (7385):368.
5. Navarro M, Nicolas A, Ferrandez A, Lanas A. Colorectal cancer population screening programs worldwide in 2016: An update. World Journal of Gastroenterology. 2017;23 (20):3632–3642. DOI: 10.3748/wjg.v23.i20.3632
6. Saha AK, Smith KJ, Sue-Ling H, Sagar PM, Burke D, Finan PJ. Prognostic factors for survival after curative resection of Dukes’ B colonic cancer. Colorectal Dis. 2011 Dec;13 (12):1390–4. DOI: 10.1111/j.1463–1318.2010.02507.x
7. Laohavinij S, Maneechavakajorn J, Techatanol P. Prognostic factors for survival in colorectal cancer patients. J Med Assoc Thai. 2010 Oct;93 (10):1156–66.
Laohavinij S, Maneechavakajorn J, Techatanol P. Prognostic factors for survival in colorectal cancer patients. J Med Assoc Thai. 2010 Oct;93 (10):1156–66.
8. Zhang S, Gao F, Luo J, Yang J. Prognostic factors in survival of colorectal cancer patients with synchronous liver metastasis. Colorectal Dis. 2010;12:754–761
9. Каприн А. Д., Старинский В. В., Петрова Г. В. Злокачественные новообразования в России в 2016 году (заболеваемость и смертность). М.: МНИОИ им. П. А. Герцена филиал ФГБУ «НМИРЦ» Минздрава России. 2018. Доступно: http://www.oncology.ru/service/statistics/malignant_tumors/2016.pdf [дата обращения 28.07.2018].
10. Указ Президента РФ № 204 от 7.05.2018 г. «О национальных целях и стратегических задачах развития Российской Федерации на период до 2024 года» (Москва, Кремль, 7 мая 2018 г. ). Доступно по: http://www.kremlin.ru/acts/bank/43027
). Доступно по: http://www.kremlin.ru/acts/bank/43027
11. Мерабишвили В. М. Злокачественные новообразования в Северо-Западном федеральном округе России (заболеваемость, смертность, контингенты, выживаемость больных). Экспресс-информация. Выпуск IV. Под ред. проф. А. М. Беляева. СПб., 2018, 444 с.
12. Дубовиченко Д. М., Вальков М. Ю., Карпунов А. А., Панкратьева А. Ю. Популяционная оценка динамики заболеваемости и стадийной структуры рака прямой кишки в условиях реализации мероприятий Национального проекта «Здоровье» и диспансеризации определенных групп взрослого населения в Архангельской области (итоги предварительного исследования). Исследования и практика в медицине. 2017;4 (3):23–32. DOI: 10.17709/2409–2231–2017–4-3–3
13. Allemani C, Coleman MP. Public health surveillance of cancer survival in the United States and worldwide: The contribution of the CONCORD programme. Cancer. 2017 Dec 15;123 Suppl 24:4977–4981. DOI: 10.1002/cncr.30854
Cancer. 2017 Dec 15;123 Suppl 24:4977–4981. DOI: 10.1002/cncr.30854
14. Coleman MP. Cancer survival: global surveillance will stimulate health policy and improve equity. Lancet. 2014 Feb 8;383 (9916):564–73. DOI: 10.1016/S0140–6736 (13)62225–4
15. Allemani C, Matsuda T, Di Carlo V, Harewood R, Matz M, Nikšić M, et al. Global surveillance of trends in cancer survival 2000–14 (CONCORD-3): analysis of individual records for 37 513 025 patients diagnosed with one of 18 cancers from 322 population-based registries in 71 countries. Lancet. 2018 Mar 17;391 (10125):1023–1075. DOI: 10.1016/S0140–6736 (17)33326–3
16. Moghimi-Dehkordi B, Safaee A, Zali MR. Comparison of colorectal and gastric cancer: survival and prognostic factors. Saudi J Gastroenterol. 2009 Jan;15 (1):18–23. DOI: 10.4103/1319–3767.43284.
DOI: 10.4103/1319–3767.43284.
17. Morris EJ, Sandin F, Lambert PC, Bray F, Klint A, Linklater K, et al. A population-based comparison of the survival of patients with colorectal cancer in England, Norway and Sweden between 1996 and 2004. Gut. 2011 Aug;60 (8):1087–93. DOI: 10.1136/gut.2010.229575.
18. Hoseini S, Moaddabshoar L, Hemati S, et al. An overview of clinical and pathological characteristics and survival rate of colorectal cancer in Iran. Ann Colorectal Res 2014;2: e17264.
19. Geiger TM, Ricciardi R. Screening Options and Recommendations for Colorectal Cancer. Clin Colon Rectal Surg. 2009 Nov;22 (4):209–17. DOI: 10.1055/s-0029–1242460
20. Doubeni CA, Weinmann S, Adams K, Kamineni A, Buist DS, Ash AS, et al Screening colonoscopy and risk of incident latestage colorectal cancer diagnosis in average-risk adults: a nested case-control study. Ann Intern Med. 2013 Mar 5;158 (5 Pt 1):312–20. DOI: 10.7326/0003–4819–158–5-201303050–00003.
Ann Intern Med. 2013 Mar 5;158 (5 Pt 1):312–20. DOI: 10.7326/0003–4819–158–5-201303050–00003.
21. Bretthauer M. Evidence for colorectal cancer screening. Best Pract Res Clin Gastroenterol. 2010 Aug;24 (4):417–25. DOI: 10.1016/j.bpg.2010.06.005.
22. El Zoghbi M, Cummings LC. New era of colorectal cancer screening. World J Gastrointest Endosc. 2016 Mar 10;8 (5):252–8. DOI: 10.4253/wjge.v8.i5.252
23. Levin TR, Corley DA, Jensen CD, Schonger JE, Quinn VP, Zauber AG, et al. Eff ects of Organized Colorectal Cancer Screening on Cancer Incidence and Mortality in a Large Community-Based Population. Gastroenterology. 2018 Nov;155 (5):1383–1391.e5. DOI: 10.1053/j.gastro.2018.07.017
24. Sormani MP. The Will Rogers phenomenon: the eff ect of diff erent diagnostic criteria. J Neurol Sci. 2009 Dec;287 Suppl 1: S46–9. DOI: 10.1016/S0022–510X (09)71300–0
Sormani MP. The Will Rogers phenomenon: the eff ect of diff erent diagnostic criteria. J Neurol Sci. 2009 Dec;287 Suppl 1: S46–9. DOI: 10.1016/S0022–510X (09)71300–0
25. Ng O, Watts E, Bull C, Morris R, Acheson A, Banerjea A. Colorectal cancer outcomes in patients aged over 85 years. Ann R Coll Surg Engl. 2016 Mar;98 (3):216–21. DOI: 10.1308/rcsann.2016.0085.
26. Millan M, Merino S, Caro A, Feliu F, Escuder J, Francesch T. Treatment of colorectal cancer in the elderly. World J Gastrointest Oncol. 2015 Oct 15;7 (10):204–20. DOI: 10.4251/wjgo.v7.i10.204.
Рак толстой кишки
Ежегодно в мире регистрируются 600 000 новых случаев заболеваний раком толстой кишки (РТК). Проблема очень актуальна для США, Европы, России, причем, для обоих полов.
Рак ободочной кишки встречается в 2 раза чаще, чем рак прямой кишки.
В связи с отсутствием диспансеризации, как правило выявляются 3 или 4 стадии заболевания.
Рак толстой кишки длительное время может протекать бессимптомно. Затем в зависимости от величины и локализации опухоли возникают различные нарушения: коликообразные боли, кишечный дискомфорт (вздутие живота, задержка стула, сменяющаяся поносами со слизью и кровью, рвота), повышение температуры тела, слабость, утомляемость, похудание, анемия. Наиболее частым проявлением далеко зашедшего рака толстой кишки служит хроническая или острая непроходимость кишечника.
Симптоматика рака толстой кишки проявляется по-разному при поражении правых (слепая, восходящая ободочная) и левых (нисходящая ободочная, сигмовидная кишка) отделов.
При локализации рака толстой кишки в правых отделах основными симптомами являются боли в животе (ноющие постоянные или приступообразные), нередко длительное время заболевание проявляется только анемией (плохо корректирующийся приемом железосодержащих препаратов) или лихорадкой неясного генеза. По мере роста новообразования, опухоль может прощупываться самим больным.
По мере роста новообразования, опухоль может прощупываться самим больным.
Для рака толстой кишки, локализующегося в ее левых отделах, основным проявлением являются симптомы кишечной непроходимости. По мере роста опухоли, запоры начинают носить более выраженный характер, не поддаются медикаментозному лечению и чередуются с поносами (из-за усиления процессов брожения при задержке каловых масс). При травматизации слизистой кишечника в кале часто обнаруживается примесь крови, при присоединении инфекции – гной. Могут возникать боли в левой половине живота. При дальнейшем прогрессировании процесса возникает острая или хроническая кишечная непроходимость. Также рак толстой кишки может осложняться перфорацией стенки кишки, кровотечением, возникновением абсцессов как в кишечной стенке, так и в брюшной полости. Основными методами обследования, кроме клинического являются рентгенологический и эндоскопический.
Основной метод лечения злокачественных новообразований – оперативный. Радикальная операция включает удаление опухоли и регионарных лимфоузлов. При своевременно проведенном лечении (опухоль прорастает только слизистую оболочку кишки) 5-ти летняя выживаемость составляет почти 100%.
Радикальная операция включает удаление опухоли и регионарных лимфоузлов. При своевременно проведенном лечении (опухоль прорастает только слизистую оболочку кишки) 5-ти летняя выживаемость составляет почти 100%.
Нами прооперировано 8 пациентов с различной локализацией опухоли в толстой кишке. Двум пациентам по поводу рака ободочной кишки выполнены операции из лапароскопического доступа.
Четвертая стадия рака кишки: прогнозы
Четвертая стадия рака кишки — каковы прогнозы?
О четвертой стадии рака говорят тогда, когда рак распространяется или метастазирует в другие ткани и органы. Четвертая стадия рака кишки чаще всего означает, что рак распространился на печень, но он также может достигать легких, лимфатических узлов или слизистой оболочки брюшной полости.
Тем не менее все люди разные, и многие факторы могут способствовать ремиссии.
Диагностика
Врач может порекомендовать несколько тестов для точной диагностики рака толстой кишки.
Правильный диагноз рака толстой кишки может потребовать терпения, так как врачи используют множество тестов для выявления и локализации рака.
Если доктора идентифицируют рак определенного органа, они расширяют спектр тестов, чтобы увидеть, распространился ли он на другие органы.
Тесты и процессы, которые могут помочь в диагностике рака толстой кишки, включают в себя:
- физическое обследование
- анализы крови
- колоноскопию прямой кишки
- биопсию, при которой врач берет образец ткани и отправляет его в лабораторию для анализа
- молекулярное тестирование, чтобы помочь определить специфические характеристики опухоли, которые могут быть важны для лечения
- визуальные тесты, такие как КТ, ПЭТ-КТ, УЗИ и МРТ, чтобы увидеть, распространился ли рак на другие органы
- рентген грудной клетки, чтобы проверить, распространился ли рак на легкие
После выполнения всех необходимых тестов, врач обсудит диагноз с пациентом.
Решения
Любой пациент, кому поставили диагноз рака толстой кишки 4-й стадии, должен будет принять некоторые решения относительно дальнейших действий, особенно в отношении вариантов лечения.
Важно обсудить все варианты с врачом и понять конечную цель каждого метода лечения.
Четвертая стадия рака кишки: варианты лечения
Варианты лечения, доступные пациентам с раком толстой кишки стадии 4, более ограничены, чем те, которые подходят для ранних стадий этого рака. Тем не менее есть еще несколько вариантов лечения, которые необходимо учитывать, а также другие факторы, которые следует рассмотреть.
Хирургия
Когда раковые клетки распространились на отдаленные органы и ткани, одно хирургическое вмешательство вряд ли поможет. Однако в некоторых случаях операция все еще может быть возможна.
Если сканирование показывает, что рак распространился только на несколько небольших близлежащих областей, операция все еще может быть возможна.
Эти операции будут включать удаление части толстой кишки, а также близлежащих лимфатических узлов. Дополнительная операция может удалить области ткани, на которые распространился рак. Врачи обычно также рекомендуют химиотерапию до или после операции.
Если опухолевые клетки слишком велики, чтобы их можно было удалить, или их слишком много, врачи порекомендуют химиотерапию до того, как человек подвергнется каким-либо хирургическим процедурам. Если это в итоге позволит уменьшить опухоль, тогда можно будет провести операцию.
Врачам также может потребоваться выполнить дополнительные хирургические процедуры, если рост раковых клеток сужает кишку или уже блокирует ее. В некоторых случаях возможна минимально инвазивная хирургия, такая как установка стента.
Хирурги могут поместить во время колоноскопии в толстую кишку стент, который представляет собой полую трубку, состоящую, обычно из металлической или пластиковой сетки. В случае успеха, стент может помочь сохранить проем кишки открытым и исключить более инвазивные операции.
Врачи могут также порекомендовать отводящую колостому, которая по существу разрезает толстую кишку над раковой тканью и отводит отходы из организма через небольшое отверстие в коже.
Химиотерапия
Химиотерапия является основным методом лечения метастазирующего рака.
В случае, если рак толстой кишки распространился слишком далеко, и есть сомнения в эффективности операции, основным вариантом лечения является химиотерапия.
Большинство пациентов с раком толстой кишки 4-й стадии будут получать химиотерапию или специальную целевую (таргетную) терапию, чтобы помочь контролировать прогрессирование рака или его симптомы.
Врачи могут порекомендовать некоторые схемы лечения, которые включают избирательное лекарственное средство, нацеленное либо на путь сосудистого эндотелиального фактора роста (VEGF), либо на путь рецептора эпителиального фактора роста (EGFR).
Выбор между режимами будет варьироваться в каждой ситуации. Выбор наиболее подходящего варианта будет зависеть от типов лечения, которые человек проходил раньше, от его общего состояния здоровья и от его восприимчивости к лечению.
Для врачей весьма распространено пробовать разные варианты. Если рак не реагирует на первичное лечение, они могут прекратить его и назначить другое.
Радиационная терапия (облучение)
Врачи также могут порекомендовать лучевую терапию при поздней стадии рака толстой кишки, чтобы уменьшить симптомы, такие как боль и дискомфорт. Это лечение может даже уменьшить опухоль на некоторое время, но обычно не излечивает рак полностью.
Инфузия печеночной артерии
Инфузия печеночной артерии может быть вариантом лечения для людей с раком толстой кишки, который распространился на печень. Инфузия печеночной артерии представляет собой тип региональной химиотерапии (эндоваскулярная химиотерапия), которая включает доставку химиотерапевтического препарата непосредственно в печеночную артерию в печени. Это лечение может помочь уничтожить раковые клетки, не нанося вреда здоровым клеткам печени.
Абляция или эмболизация
Абляция или эмболизация могут быть подходящими для людей, у которых есть метастатический или рецидивирующий колоректальный рак, вызывающий несколько опухолей в легких или печени, объемом менее 4 сантиметров.
Абляция использует радиочастоты, микроволны или алкоголь — которые люди также называют подкожной инъекцией этанола (PEI) — для уничтожения раковых клеток, оставляя при этом окружающие ткани относительно невредимыми.
Во время эмболизации врач вводит вещества в кровеносные сосуды, пытаясь заблокировать или уменьшить приток крови к раковым клеткам.
Паллиативная помощь
Если рак прогрессирует во многие отдаленные органы и ткани, хирургическое вмешательство может оказаться бесполезным. Другие варианты лечения могут вызывать дискомфорт и вызывать дополнительные симптомы, ухудшающие качество жизни человека.
В этих случаях люди могут отказаться от медицинской помощи, которая направлена на излечение от рака, и вместо этого выбрать паллиативную помощь, чтобы попытаться сделать жизнь более комфортной.
Паллиативная помощь, как правило, включает в себя поиск способов справиться с болью и уменьшить симптомы от рака, чтобы человек смог комфортно прожить как можно дольше.
Прогнозы
Чувствительность пациента к лечению будет зависеть от ряда факторов, таких как возраст и общее состояние здоровья.
Рак толстой кишки является третьим наиболее часто диагностируемым раком у мужчин и женщин. В среднем один из каждых 22 мужчин и одна из каждых 24 женщин в течение жизни получают диагноз рака толстой кишки.
Четвертая стадия рака кишки — это рак поздней стадии, при котором заболевание распространилось на другие ткани или органы в организме и, следовательно, почти не поддается лечению. Лечение может быть только частично успешным, и рак с большой вероятностью может вернуться после лечения (рецидивировать).
Относительная выживаемость в течение 5 лет при раке толстой кишки 4 стадии составляет 14%. Однако это не учитывает другие факторы, которые могут повлиять на индивидуальную выживаемость.
Например, успех отдельных методов лечения может отличаться у разных людей, при этом лечение, которое очень хорошо работает для одних пациентов, неэффективно для других.
Кроме того, эксперты основывают статистику прогнозов на прошлых случаях. Поскольку методы лечения имеют тенденцию улучшаться с течением времени, показатели выживаемости также могут расти по мере появления более эффективных методов лечения.
Отдельные факторы могут также играть важную роль. Например, возраст и общее состояние здоровья пациента могут влиять на его восприимчивость к лечению.
Скорость прогрессирования рака также может изменить прогноз. Если рак вызывает осложнения, такие как закупорка толстой кишки или дыра в стенке кишечника, взгляды пациента на свой образ жизни и питания могут измениться.
Эта статистика выживаемости применима только к раку толстой кишки 4 стадии, когда врачи диагностируют его впервые. Коэффициент выживаемости будет отличаться для тех, у кого рак распространился дальше или вернулся (рецидивировал) после лечения.
Выводы
Четвертая стадия рака кишки — рак поздней стадии.
Ожидаемая продолжительность жизни ниже, чем на более ранних стадиях этого рака.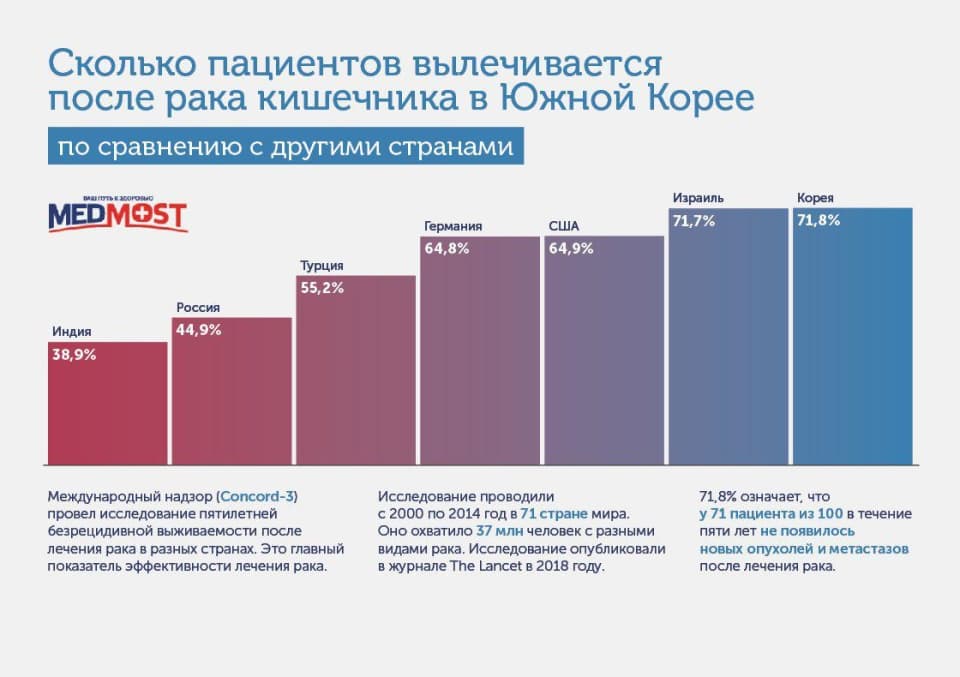 Пятилетняя относительная выживаемость при раке толстой кишки 4-й стадии, который распространился на другие части тела, составляет около 14%.
Пятилетняя относительная выживаемость при раке толстой кишки 4-й стадии, который распространился на другие части тела, составляет около 14%.
Однако другие факторы, такие как выбранные методы лечения и общее состояние здоровья человека, по-разному влияют на продолжительность жизни.
Хотя зачастую существует несколько вариантов лечения, включая хирургию и химиотерапию, некоторые пациенты с поздней стадией рака предпочитают не получать медицинскую помощь и вместо этого обращаются за паллиативной помощью.
Любой пациент, у которого диагностировали рак толстой кишки 4 стадии, должен плотно взаимодействовать со своим лечащим врачом, чтобы узнать все возможные варианты лечения и решить, какой из них лучше всего подойдет в его случае.
Южная Корея — одна из лидирующих стран в мире по лечению рака толстой кишки поздних стадий. Подробнее о лечении рака толстой кишки в Корее вы можете почитать по этой ссылке.
Какие факторы влияют на выживаемость при раке прямой кишки?
Какие факторы влияют на выживаемость при раке прямой кишки и какова текущая продолжительность жизни на основе этой статистики?
СТИВ ГШМЕЙССНЕР / Getty Images
Выживаемость при раке прямой кишки и ожидаемая продолжительность жизни
Столкнувшись с неуверенностью в отношении рака, человеческая природа желает узнать как можно больше о болезни и попытаться понять, как все это будет развиваться. Представленные здесь показатели выживаемости при раке прямой кишки помогут вам понять суть проблемы, но важно помнить, что показатели выживаемости являются обобщениями, и индивидуальные шансы на выживание могут быть совершенно разными.
Представленные здесь показатели выживаемости при раке прямой кишки помогут вам понять суть проблемы, но важно помнить, что показатели выживаемости являются обобщениями, и индивидуальные шансы на выживание могут быть совершенно разными.
Имейте в виду, что эти цифры — статистика, основанная на прошлой выживаемости. Например, пятилетняя выживаемость, зафиксированная в 2017 году, будет применяться к людям, которым был поставлен диагноз, начиная с 2012 года или ранее. Поскольку в последние несколько лет стали доступны новые методы лечения, эти показатели могут не отражать то, как человек с раком прямой кишки будет делать это сегодня, используя методы лечения, которые у нас есть сейчас.
Переменные, которыми нельзя управлять
Вот несколько переменных, которые мы не можем контролировать, но они могут сыграть важную роль в прогнозе.
Где вы живете
Согласно исследованию 2018 года, опубликованному в журнале CA: A Cancer Journal для клиницистов, показатели выживаемости при раке прямой кишки различаются в зависимости от страны. В то время как общая пятилетняя выживаемость при раке прямой кишки в Америке составляет 67 процентов, в Европе этот показатель составляет 61 процент. . Одним из факторов может быть качество медицинской помощи, но другим может быть использование программ скрининга колоректального рака. Как правило, чем раньше обнаружен рак прямой кишки, тем легче его лечить.
В то время как общая пятилетняя выживаемость при раке прямой кишки в Америке составляет 67 процентов, в Европе этот показатель составляет 61 процент. . Одним из факторов может быть качество медицинской помощи, но другим может быть использование программ скрининга колоректального рака. Как правило, чем раньше обнаружен рак прямой кишки, тем легче его лечить.
Этап при диагностике
Стадия постановки диагноза сильно влияет на выживаемость при раке прямой кишки.Средняя продолжительность жизни в зависимости от стадии приведена ниже, но опять же, имейте в виду, что некоторые другие переменные играют роль.
Раса и пол
В целом выживаемость афроамериканцев с раком прямой кишки ниже, чем у белых, страдающих этим заболеванием. Среди переменных, которые могут способствовать этому несоответствию, — наличие медицинской страховки.
Ваш пол — еще один фактор, влияющий на выживаемость при раке прямой кишки. Исследования показали, что, в отличие от многих других видов рака, у женщин выживаемость рака прямой кишки ниже, чем у мужчин. Взаимодействие с другими людьми
Взаимодействие с другими людьми
Онкомаркеры
Тесты, обнаруживающие в крови так называемые онкомаркеры, могут предоставить более подробную информацию о прогнозе рака прямой кишки. Мы не будем вдаваться в эти конкретные меры, но полезно понимать, что молекулярный состав вашей опухоли может играть роль в выживание. Определение этих молекулярных характеристик, вероятно, улучшит прогнозы, и они определяют агрессивность и типы лечения отдельного рака.
Управляемые переменные
Факторы, которые мы обсуждали до сих пор, в основном находятся вне вашего контроля.Вы живете там, где живете
, и у вас развился рак, когда он у вас развился. Итак, что можно сделать с , чтобы повысить свои шансы на выживание? Сосредоточение внимания на следующих переменных и их корректировке может не только помочь вам справиться с болезнью, но и повлиять на ваш результат.
Упражнение
Исследователи из Института рака Дана-Фарбер в Бостоне обнаружили, что умеренные упражнения могут значительно увеличить выживаемость пациентов с колоректальным раком. Узнайте больше о влиянии физических упражнений на выживаемость при колоректальном раке.
Узнайте больше о влиянии физических упражнений на выживаемость при колоректальном раке.
Страховая защита
Те, у кого есть медицинская страховка, как правило, имеют лучшие результаты, чем те, кто не застрахован, отчасти потому, что люди без страховки, как правило, не получают профилактической медицинской помощи и могут избегать необходимой медицинской помощи при серьезных проблемах со здоровьем из-за стоимости. Это не переменная, которая может быть изменена в зависимости от страхового покрытия в начале лечения, но тем, кто не застрахован или застрахован недостаточно во время лечения, следует рассмотреть свои варианты.Ваш социальный работник онкологического центра может стать хорошей отправной точкой для определения ваших возможностей.
Аспирин
Некоторые исследования показывают, что прием аспирина увеличивает выживаемость при колоректальном раке. Однако очень важно поговорить со своим врачом: аспирин может помешать вашему плану лечения рака.
Витамин D
Как и в случае с аспирином, некоторые исследования показывают, что витамин D может играть роль в увеличении выживаемости при колоректальном раке.Добавьте к этому тот факт, что большинство американцев испытывают дефицит витамина D, и ваш врач может обнаружить, что ваш уровень также низкий. Ваш врач может назначить простой анализ крови, чтобы определить, так ли это, и при необходимости он может порекомендовать добавки витамина D3. Всегда консультируйтесь со своим врачом перед тем, как принимать какие-либо пищевые добавки, продаваемые без рецепта. Некоторые витаминные и минеральные препараты могут мешать лечению рака.
Сообщество поддержки
Хотя это специально не изучалось для пациентов с раком прямой кишки, было обнаружено, что люди с прогрессирующим раком легких, как правило, живут значительно дольше, когда у них больше социальной поддержки.Имейте в виду, что вы можете получить поддержку, даже если чувствуете себя недостаточно хорошо, чтобы покинуть дом. Многие онлайн-сообщества по раку прямой кишки не только предлагают профессиональную поддержку, но и позволяют вам общаться с людьми, которые сталкиваются с аналогичными проблемами.
Многие онлайн-сообщества по раку прямой кишки не только предлагают профессиональную поддержку, но и позволяют вам общаться с людьми, которые сталкиваются с аналогичными проблемами.
Сгустки крови
Сгустки крови в ногах (тромбоз глубоких вен), которые могут оторваться и попасть в легкие (тромбоэмболия легочной артерии), являются важной причиной болезней и смерти для людей, живущих с любым видом рака. Узнайте о симптомах сгустков крови а также то, что вы можете сделать, чтобы снизить риск образования тромбов при раке.
Другие условия, влияющие на выживаемость
В дополнение к указанным выше переменным, на выживаемость человека с колоректальным раком могут влиять и другие факторы. Они могут включать:
- Ваш возраст: В целом молодые люди, как правило, справляются с этим заболеванием лучше, чем пожилые люди, хотя это может идти в обоих направлениях. У молодых людей может быть больше шансов иметь генетическую предрасположенность и, следовательно, более агрессивные опухоли, но их общее состояние здоровья может быть лучше, и, таким образом, они могут переносить наиболее агрессивные планы лечения.

- Ваш статус работоспособности: Статус работоспособности — это способ определить, насколько хорошо пациент может вести нормальную повседневную деятельность. Хотя его чаще всего используют для определения того, соответствует ли человек критериям для участия в клиническом исследовании, он также связан с прогнозом.
- Ваше общее состояние здоровья: От того, насколько вы здоровы, помимо рака, может зависеть, какие виды лечения вы можете переносить, а также на то, можете ли вы заниматься физическими упражнениями — привычка, улучшающая выживаемость.
- Полученные лечения и то, как ваша опухоль реагирует на лечение.
- Молекулярный профиль и степень (агрессивность) вашего рака.
- Перфорация или непроходимость кишечника , вызванная раком, снижает выживаемость.
Почему статистика не является предсказателем
Даже принимая во внимание все вышеперечисленные переменные, трудно сказать, как долго хоть один человек проживет с колоректальным раком.
Статистика может давать средние значения, но люди — это не числа. В целом статистика говорит нам, как пациенты переносили колоректальный рак в недавнем прошлом. Самая последняя исчерпывающая статистика, которая у нас есть, часто насчитывает четыре или пять лет, но с тех пор медицина добилась значительного прогресса в лечении рака. Таким образом, по сути, показатели выживаемости могут сказать вам, как поступил человек с аналогичным диагнозом при более старом лечении болезни, но результаты лечения, одобренного с того времени, могут быть неизвестны еще несколько лет.Взаимодействие с другими людьми
Статистика ожидаемой продолжительности жизни при раке толстой и прямой кишки
Рак прямой кишки часто связывают с раком толстой кишки в статистике выживания рака; однако у них разная выживаемость.
Согласно программе наблюдения, эпидемиологии и конечных результатов Национального института рака (SEER), пятилетняя выживаемость при раке толстой кишки (на основе людей, диагностированных в период с 2009 по 2015 год) составляет:
- Локализовано: 90%
- Регионально: 71%,
- Удаленное: 14%
- Все этапы объединены: 63%
Пятилетняя выживаемость при раке прямой кишки составляет:
- Локализовано: 89%
- Регионально: 71%,
- Удаленное: 15%
- Все этапы объединены: 67%
Обратите внимание, что статистика SEER применима только к стадии рака, когда он впервые диагностирован, а не к тому, растет ли рак, распространяется или возвращается после лечения. Также имейте в виду, что показатели выживаемости сгруппированы в зависимости от того, насколько далеко распространился рак, но ваш возраст, общее состояние здоровья, реакция рака на лечение и другие факторы также будут влиять на ваш прогноз. И еще раз помните, что люди, у которых сейчас диагностирован рак толстой или прямой кишки, могут иметь более благоприятные перспективы, чем показывают эти цифры, потому что со временем методы лечения улучшаются.
Также имейте в виду, что показатели выживаемости сгруппированы в зависимости от того, насколько далеко распространился рак, но ваш возраст, общее состояние здоровья, реакция рака на лечение и другие факторы также будут влиять на ваш прогноз. И еще раз помните, что люди, у которых сейчас диагностирован рак толстой или прямой кишки, могут иметь более благоприятные перспективы, чем показывают эти цифры, потому что со временем методы лечения улучшаются.
Выводы о выживаемости при раке толстой и прямой кишки
Многие исследования указывают на множество факторов, влияющих на выживаемость при раке.В последние годы были одобрены новые методы лечения, а другие проходят клинические испытания. Варианты лечения в клинических испытаниях необходимо оценить, прежде чем они станут общедоступными. Национальный институт рака предлагает пациентам подумать о том, будет ли клиническое испытание вариантом их лечения. О клинических испытаниях существует много мифов, но правда в том, что многие из лучших методов лечения, доступных через пять лет, могут быть доступны только в клинические испытания сегодня.
Показатели, статистика и результаты выживших после рака прямой кишки
В Центрах лечения рака Америки ® (CTCA) мы понимаем, что вы можете захотеть получить информацию о результатах выживаемости пациентов с отдаленным (также называемым метастатическим) раком прямой кишки, которым был поставлен диагноз и / или, по крайней мере, первоначально частично лечиться в наших больницах, чтобы помочь вам и вашей семье решить, куда обратиться за лечением, в рамках многих других факторов, которые вы можете учитывать.Поэтому мы попросили независимого биостатиста проанализировать результаты выживаемости пациентов с CTCA ® .
Статистическая методология и ограничения
Квалификация независимых исследователей
В приведенной ниже таблице отражены коэффициенты выживаемости CTCA и SEER для пациентов с раком прямой кишки с отдаленным (метастатическим) заболеванием, которые были диагностированы в период с 2000 по 2015 гг. Он включает оценки процента пациентов с раком прямой кишки с отдаленным (метастатическим) заболеванием, которые выжили в течение шести месяцев. до пяти лет после первоначального диагноза, как указано в базах данных CTCA и SEER.
до пяти лет после первоначального диагноза, как указано в базах данных CTCA и SEER.
- В этот анализ были включены пациенты с раком прямой кишки из CTCA, у которых были первичные очаги опухоли (по кодировке C209 в МКБ-O-2 (1973+), были диагностированы с 2000 по 2015 г. (включая 2000 и 2015 гг.) начальный курс лечения в CTCA. Все пациенты, включенные в анализ, считались аналитическими пациентами по CTCA.
- больных раком прямой кишки с отдаленным (метастатическим) заболеванием из базы данных SEER и пациенты с раком прямой кишки с отдаленным (метастатическим) заболеванием из базы данных CTCA.Кроме того, из анализа были исключены пациенты, в медицинских записях которых отсутствовала какая-либо из следующих сведений:
- SEER Сводные этапы
- Первичные очаги опухоли
- Гистологические типы рака
- Дата первичного диагноза
- Возраст при первоначальном диагнозе
- Пол
- Гонка
В анализ были включены
* Данные SEER представляют собой национальные результаты по большому количеству учреждений и были включены в иллюстративных целях. Они не предназначены для представления контролируемого исследования и / или идеального анализа данных CTCA из-за различий в размерах выборки двух баз данных, клиническом состоянии (-ях) пролеченных пациентов и других факторах.
Они не предназначены для представления контролируемого исследования и / или идеального анализа данных CTCA из-за различий в размерах выборки двух баз данных, клиническом состоянии (-ях) пролеченных пациентов и других факторах.
Выборка CTCA относительно мала, потому что в нее были включены только пациенты с метастатическим раком прямой кишки, которые были первоначально диагностированы в CTCA и / или прошли по крайней мере часть своего первоначального курса лечения в CTCA. Эти факторы значительно уменьшили размер выборки CTCA, а это означает, что оценки, отраженные в диаграмме выживаемости, могут сильно отличаться и не могут быть воспроизведены в будущем, когда у нас будет более крупная выборка CTCA для анализа.
Чтобы получить полное техническое объяснение методологии, использованной в анализе, и подробное описание включенных групп пациентов CTCA и SEER, щелкните здесь, чтобы просмотреть статистическую методологию, а для получения дополнительной информации о программе SEER перейдите на seer. cancer.gov
cancer.gov
Мы также хотим быть уверены, что вы понимаете, что рак — это сложное заболевание, и состояние здоровья каждого человека индивидуально; поэтому CTCA не делает заявлений ни об эффективности конкретных методов лечения, оказании помощи, ни о значении анализов CTCA и SEER.Не все больные раком, проходящие лечение в больнице CTCA, могут получить такие же результаты.
Узнайте о выживаемости при раке толстой кишки
Следующая тема: Какие вопросы чаще всего возникают о колоректальном раке?
Лечение рака прямой кишки (PDQ®) — версия для пациента
О PDQ
Запрос данных врача (PDQ) — это обширная база данных по раку Национального института рака (NCI). База данных PDQ содержит резюме последней опубликованной информации о профилактике, обнаружении, генетике, лечении, поддерживающей терапии, а также дополнительной и альтернативной медицине.Большинство резюме представлено в двух версиях. Версии для медицинских работников содержат подробную информацию на техническом языке. Версии для пациентов написаны понятным, нетехническим языком. Обе версии содержат точную и актуальную информацию о раке, и большинство версий также доступно на испанском языке.
Версии для пациентов написаны понятным, нетехническим языком. Обе версии содержат точную и актуальную информацию о раке, и большинство версий также доступно на испанском языке.
PDQ — это услуга NCI. NCI входит в состав Национальных институтов здравоохранения (NIH). NIH — это центр биомедицинских исследований при федеральном правительстве. Обзоры PDQ основаны на независимом обзоре медицинской литературы.Это не политические заявления NCI или NIH.
Цель этого обзора
В этом обзоре информации о раке PDQ содержится текущая информация о лечении рака прямой кишки. Он предназначен для информирования и помощи пациентам, семьям и лицам, осуществляющим уход. Он не дает официальных руководящих принципов или рекомендаций для принятия решений в отношении здравоохранения.
Рецензенты и обновления
Редакционные коллегии составляют сводки информации о раке PDQ и поддерживают их в актуальном состоянии. Эти советы состоят из экспертов в области лечения рака и других специальностей, связанных с раком. Резюме регулярно пересматриваются, и в них вносятся изменения при появлении новой информации. Дата в каждой сводке («Обновлено») — это дата самого последнего изменения.
Резюме регулярно пересматриваются, и в них вносятся изменения при появлении новой информации. Дата в каждой сводке («Обновлено») — это дата самого последнего изменения.
Информация в этом обзоре пациентов была взята из версии для медицинских работников, которая регулярно проверяется и обновляется по мере необходимости редакционной коллегией PDQ по лечению взрослых.
Информация о клиническом испытании
Клиническое испытание — это исследование, призванное ответить на научный вопрос, например, лучше ли одно лечение, чем другое.Испытания основаны на прошлых исследованиях и на том, что было изучено в лаборатории. Каждое испытание отвечает на определенные научные вопросы, чтобы найти новые и лучшие способы помочь больным раком. Во время клинических испытаний лечения собирается информация об эффектах нового лечения и о том, насколько хорошо оно работает. Если клинические испытания покажут, что новое лечение лучше, чем то, что используется в настоящее время, новое лечение может стать «стандартным». Пациенты могут захотеть принять участие в клиническом исследовании.Некоторые клинические испытания открыты только для пациентов, которые еще не начали лечение.
Пациенты могут захотеть принять участие в клиническом исследовании.Некоторые клинические испытания открыты только для пациентов, которые еще не начали лечение.
Клинические испытания можно найти в Интернете на сайте NCI. Для получения дополнительной информации позвоните в Информационную службу рака (CIS), контактный центр NCI, по телефону 1-800-4-CANCER (1-800-422-6237).
Разрешение на использование данного обзора
PDQ является зарегистрированным товарным знаком. Содержимое документов PDQ можно свободно использовать как текст. Его нельзя идентифицировать как сводку информации о раке NCI PDQ, если не отображается вся сводка и не обновляется регулярно.Тем не менее, пользователю будет разрешено написать такое предложение, как «Сводка информации о раке PDQ NCI о профилактике рака груди указывает риски следующим образом: [включить выдержку из резюме]».
Лучший способ процитировать это резюме PDQ:
Редакционная коллегия PDQ® Adult Treatment. PDQ Лечение рака прямой кишки. Bethesda, MD: Национальный институт рака. Обновлено <ММ / ДД / ГГГГ>. Доступно по адресу: https://www.cancer.gov/types/colorectal/patient/rectal-treatment-pdq. Дата обращения <ММ / ДД / ГГГГ>.[PMID: 26389378]
PDQ Лечение рака прямой кишки. Bethesda, MD: Национальный институт рака. Обновлено <ММ / ДД / ГГГГ>. Доступно по адресу: https://www.cancer.gov/types/colorectal/patient/rectal-treatment-pdq. Дата обращения <ММ / ДД / ГГГГ>.[PMID: 26389378]
Изображения в этом резюме используются с разрешения автора (ов), художника и / или издателя только для использования в резюме PDQ. Если вы хотите использовать изображение из сводки PDQ и не используете все сводки, вы должны получить разрешение от владельца. Он не может быть предоставлен Национальным институтом рака. Информацию об использовании изображений в этом обзоре, а также многих других изображений, связанных с раком, можно найти в Visuals Online. Visuals Online — это коллекция из более чем 3000 научных изображений.
Заявление об ограничении ответственности
Информация, содержащаяся в этом резюме, не должна использоваться для принятия решений о страховом возмещении. Более подробная информация о страховом покрытии доступна на сайте Cancer. gov на странице «Управление онкологическими услугами».
gov на странице «Управление онкологическими услугами».
Свяжитесь с нами
Дополнительную информацию о том, как связаться с нами или получить помощь на веб-сайте Cancer.gov, можно найти на нашей странице «Свяжитесь с нами для получения помощи». Вопросы также можно отправить на Cancer.gov через электронную почту веб-сайта.
Рак прямой кишки: основы практики, история вопроса, анатомия
Американское онкологическое общество.Онкологические факты и цифры, 2020. Американское онкологическое общество. Доступно по адресу https://www.cancer.org/content/dam/cancer-org/research/cancer-facts-and-statistics/annual-cancer-facts-and-figures/2020/cancer-facts-and-figures- 2020.pdf. Дата обращения: 11 марта 2020 г.
Джованнуччи Э, Ву К. Рак толстой и прямой кишки. Schottenfeld D, Fraumeni J, ред. Рак. Эпидемиология и профилактика . 3-е изд. Издательство Оксфордского университета; 2006.
Anagnostopoulos G, Sakorafas GH, Kostopoulos P, et al.Плоскоклеточный рак прямой кишки: описание случая и обзор литературы. Eur J Cancer Care (Engl) . 2005 14 марта (1): 70-4. [Медлайн].
[Рекомендации] Национальная комплексная онкологическая сеть. Руководство NCCN по клинической практике в онкологии. Рак прямой кишки. Доступно на http://www.nccn.org/professionals/physician_gls/PDF/rectal.pdf. Версия 1.2021 — 22 декабря 20200 г .; Дата обращения: 5 января 2021 г.
Kapiteijn E, Marijnen CA, Nagtegaal ID, Putter H, Steup WH, Wiggers T.Предоперационная лучевая терапия в сочетании с полным мезоректальным иссечением резектабельного рака прямой кишки. N Engl J Med . 2001 30 августа. 345 (9): 638-46. [Медлайн].
DʼSouza N, de Neree Tot Babberich MPM, d’Hoore A, et al. Определение прямой кишки: международный экспертный консенсус Delphi. Энн Сург . 2019 Декабрь 270 (6): 955-959. [Медлайн].
Определение прямой кишки: международный экспертный консенсус Delphi. Энн Сург . 2019 Декабрь 270 (6): 955-959. [Медлайн].
Heald RJ. «Священный план» ректальной хирургии. J R Soc Med .1988 сентябрь 81 (9): 503-8. [Медлайн]. [Полный текст].
Leggett BA, Devereaux B, Biden K, Searle J, Young J, Jass J. Гиперпластический полипоз: связь с колоректальным раком. Ам Дж. Сург Патол . 2001 25 февраля (2): 177-84. [Медлайн].
Wheeler JM, Bodmer WF, Mortensen NJ. Гены репарации несоответствия ДНК и колоректальный рак. Кишечник . 2000 июл. 47 (1): 148-53. [Медлайн]. [Полный текст].
Сигель Р.Л., Федева С.А., Андерсон В.Ф., Миллер К.Д., Ма Дж., Розенберг П.С. и др.Паттерны заболеваемости колоректальным раком в США, 1974–2013 гг. Национальный институт рака . 28 февраля 2017 г. 109: [Полный текст].
Национальный институт рака . 28 февраля 2017 г. 109: [Полный текст].
Siegel RL, Miller KD, Goding Sauer A, Fedewa SA, Butterly LF, Anderson JC и др. Статистика колоректального рака, 2020. CA Cancer J Clin . 2020 5 марта. [Medline]. [Полный текст].
Всемирная организация здравоохранения. Колоректальный рак. ВОЗ. Доступно на http://gco.iarc.fr/today/data/factsheets/cancers/10_8_9-Colorectum-fact-sheet.pdf. 2018; Дата обращения: 11 марта 2020 г.
Программа эпиднадзора, эпидемиологии и конечных результатов. Факты статистики рака: колоректальный рак. Национальный институт рака. Доступно по адресу http://seer.cancer.gov/statfacts/html/colorect.html. Дата обращения: 5 января 2021 г.
Yothers G, Sargent DJ, Wolmark N и др. Результаты среди чернокожих пациентов со стадией II и III рака толстой кишки, получающих химиотерапию: анализ испытаний адъюванта ACCENT. Национальный институт рака .19 октября 2011 г. 103 (20): 1498-1506. [Медлайн]. [Полный текст].
Национальный институт рака .19 октября 2011 г. 103 (20): 1498-1506. [Медлайн]. [Полный текст].
Роббинс А.С., Сигель Р.Л., Джемал А. Расовые различия в показателях смертности от колоректального рака в зависимости от стадии с 1985 по 2008 год. J Clin Oncol . 2012 1 февраля. 30 (4): 401-5. [Медлайн].
Ротвелл П.М., Фаукс Г.Р., Белч Дж.Ф., Огава Х., Варлоу С.П., Мид ТВ. Влияние ежедневного приема аспирина на долгосрочный риск смерти от рака: анализ данных отдельных пациентов из рандомизированных исследований. Ланцет . 7 декабря 2010 г .; Ранняя онлайн-публикация. [Полный текст].
Burn J, Gerdes AM, Macrae F, et al. Долгосрочное влияние аспирина на риск рака у носителей наследственного колоректального рака: анализ рандомизированного контролируемого исследования CAPP2. Ланцет . 2011 17 декабря. 378 (9809): 2081-7. [Медлайн]. [Полный текст].
2011 17 декабря. 378 (9809): 2081-7. [Медлайн]. [Полный текст].
Rothwell PM, Price JF, Fowkes FG, Zanchetti A, Roncaglioni MC, Tognoni G, et al. Краткосрочные эффекты ежедневного приема аспирина на заболеваемость раком, смертность и смертность от несосудистых заболеваний: анализ динамики рисков и преимуществ в 51 рандомизированном контролируемом исследовании. Ланцет . 2012 28 апреля. 379 (9826): 1602-12. [Медлайн].
Stitzenberg KB, Sanoff HK, Penn DC, Meyers MO, Tepper JE. Практические шаблоны и долгосрочное выживание при ранней стадии рака прямой кишки. Дж Клин Онкол . 13 декабря 2013 г. 31 (34): 4276-82. [Медлайн]. [Полный текст].
Eu KW, Seow-Choen F, Ho JM, Ho YH, Leong AF. Местный рецидив после резекции прямой кишки по поводу рака. J R Coll Surg Edinb . 1998 декабрь 43 (6): 393-6. [Медлайн]. [Полный текст].
[Медлайн]. [Полный текст].
Thong MS, Mols F, Lemmens VE, et al. Влияние предоперационной лучевой терапии на общее и конкретное заболевание состояние здоровья выживших после рака прямой кишки: популяционное исследование. Int J Radiat Oncol Biol Phys . 2011 г. 1. 81 (3): e49-58. [Медлайн].
Харрисон П. Провоспалительная диета способствует риску CRC у обоих полов. Медицинские новости Medscape. Доступно на https://www.medscape.com/viewarticle/891665.23 января 2018 г .; Доступ: 30 января 2018 г.
Табунг Ф.К., Лю Л., Ван В., Фунг Т.Т., Ву К., Смит-Уорнер С.А. и др. Ассоциация диетического воспалительного потенциала с риском колоректального рака у мужчин и женщин. JAMA Онкол . 18 января 2018 г. [Medline].
Джанфреди В., Нуччи Д., Сальватори Т. , Даллагиакома Г., Фатигони С., Моретти М. и др. Рак прямой кишки: снижение риска на 20% благодаря потреблению пищевых волокон. Систематический обзор и метаанализ. Питательные вещества . 2019 12 июля. 11 (7): 916-32. [Медлайн]. [Полный текст].
, Даллагиакома Г., Фатигони С., Моретти М. и др. Рак прямой кишки: снижение риска на 20% благодаря потреблению пищевых волокон. Систематический обзор и метаанализ. Питательные вещества . 2019 12 июля. 11 (7): 916-32. [Медлайн]. [Полный текст].
Чао А., Тун М.Дж., Коннелл С.Дж. и др. Потребление мяса и риск колоректального рака. ЯМА . 2005 12 января 293 (2): 172-82. [Медлайн].
Baron JA, Beach M, Mandel JS, van Stolk RU, Haile RW, Sandler RS и др. Добавки кальция для профилактики колоректальных аденом. Исследовательская группа по профилактике полипов кальция. N Engl J Med . 1999 14 января.340 (2): 101-7. [Медлайн].
Феррари П, Дженаб М, Норат Т., Москаль А., Слимани Н., Олсен А. и др. Пожизненное и исходное потребление алкоголя и риск рака толстой и прямой кишки в Европейском проспективном исследовании рака и питания (EPIC). Инт Дж. Рак . 2007 г. 1. 121 (9): 2065-72. [Медлайн].
Инт Дж. Рак . 2007 г. 1. 121 (9): 2065-72. [Медлайн].
Kabat GC, Howson CP, Wynder EL. Потребление пива и рак прямой кишки. Int J Epidemiol . 1986, 15 декабря (4): 494-501.[Медлайн].
Цой К.К., Пау С.Й., Ву В.К., Чан Ф.К., Гриффитс С., Сун Дж.Дж. Курение сигарет и риск колоректального рака: метаанализ проспективных когортных исследований. Клин Гастроэнтерол Гепатол . 2009 июн. 7 (6): 682-688.e1-5. [Медлайн].
Фиппс А.И., Барон Дж., Ньюкомб, Пенсильвания. Предиагностический анамнез курения, потребление алкоголя и выживаемость при колоректальном раке: Семейный реестр рака толстой кишки. Рак . 2011 1 ноя.117 (21): 4948-57. [Медлайн]. [Полный текст].
Johns LE, Houlston RS. Систематический обзор и метаанализ риска семейного колоректального рака. Ам Дж. Гастроэнтерол . 2001 Октябрь 96 (10): 2992-3003. [Медлайн].
Ам Дж. Гастроэнтерол . 2001 Октябрь 96 (10): 2992-3003. [Медлайн].
Берт RW. Семейный риск и колоректальный рак. Гастроэнтерол Clin North Am . 1996 25 декабря (4): 793-803. [Медлайн].
[Рекомендации] Национальная комплексная онкологическая сеть. NCCN Clinical Practice Guidelines in Oncology: Genetic / Familial High Risk Assessment: Colorectal.NCCN. Доступно на http://www.nccn.org/professionals/physician_gls/pdf/genetics_colon.pdf. Версия 2.2021 — 20 ноября 2020 г .; Дата обращения: 5 января 2021 г.
Хендерсон Д. Домашний тест стула выявляет 79% колоректального рака. Медицинские новости Medscape. Доступно на http://www.medscape.com/viewarticle/820194. Доступ: 10 февраля 2014 г.
Ли Дж. К., Лайлс Э. Г., Бент С., Левин Т. Р., Корли Д. А.. Точность иммунохимических тестов кала на колоректальный рак: систематический обзор и метаанализ. Энн Интерн Мед. . 2014 Февраль 4. 160 (3): 171. [Медлайн]. [Полный текст].
А.. Точность иммунохимических тестов кала на колоректальный рак: систематический обзор и метаанализ. Энн Интерн Мед. . 2014 Февраль 4. 160 (3): 171. [Медлайн]. [Полный текст].
de Wijkerslooth TR, Stoop EM, Bossuyt PM, Meijer GA, van Ballegooijen M, van Roon AH, et al. Иммунохимический анализ кала на скрытую кровь одинаково чувствителен для проксимальных и дистальных продвинутых неоплазий. Ам Дж. Гастроэнтерол . 2012 31 июля. [Medline].
Нельсон Х, Петрелли Н, Карлин А, Кутюр Дж, Флешман Дж, Гиллем Дж и др. Рекомендации 2000 г. по хирургии рака прямой и толстой кишки. Национальный институт рака . 2001, 18 апреля. 93 (8): 583-96. [Медлайн].
Schoen RE, Pinsky PF, Weissfeld JL, Yokochi LA, Church T, Laiyemo AO и др. Заболеваемость и смертность от рака прямой и прямой кишки при скрининговой гибкой сигмоидоскопии. N Engl J Med . 2012 21 мая. [Medline].
N Engl J Med . 2012 21 мая. [Medline].
[Рекомендации] Целевая группа превентивных служб США, Биббинс-Доминго К., Гроссман Д.К., Карри С.Дж., Дэвидсон К.В., Эплинг Дж. У. мл. И др. Скрининг колоректального рака: Рекомендация рабочей группы США по профилактическим услугам. ЯМА . 2016, 21 июня. 315 (23): 2564-75. [Медлайн]. [Полный текст].
Макнамара Д. Доказательства в пользу скрининга молодых людей на колоректальный рак. Медицинские новости Medscape. Доступно на https://www.medscape.com/viewarticle/887768. 30 октября 2017 г .; Доступ: 15 ноября 2017 г.
Браунс Л. Р., Леманн Р. К., Лесперанс К. Э., Браун Т. А., Стил С. Р.. Повышение показателей скрининга на колоректальный рак среди населения с равным доступом. Am J Surg .2009 Май. 197 (5): 609-12; обсуждение 612-3. [Медлайн].
Келлер Д.С., Берхо М., Перес Р.О., Векснер С.Д., Чанд М. Междисциплинарное лечение рака прямой кишки. Нат Рев Гастроэнтерол Гепатол . 2020 Июл.17 (7): 414-429. [Медлайн].
Бакстер Н.Н., Гарсия-Агилар Дж. Консервация органов при раке прямой кишки. Дж Клин Онкол . 2007 10 марта. 25 (8): 1014-20. [Медлайн].
Hospers G, Bahadoer RR, Dijkstra EA, et al.Краткосрочная лучевая терапия с последующей химиотерапией перед ТМЕ при местнораспространенном раке прямой кишки: рандомизированное исследование RAPIDO. Дж Клин Онкол . 2020. 38 (Suppl; abstr 4006): [Полный текст].
Cercek A, Roxburgh CSD, Strombom P, Smith JJ, Temple LKF, Nash GM и др. Принятие тотальной неоадъювантной терапии местнораспространенного рака прямой кишки. JAMA Онкол . 14 июня 2018 г. 4 (6): e180071. [Медлайн]. [Полный текст].
JAMA Онкол . 14 июня 2018 г. 4 (6): e180071. [Медлайн]. [Полный текст].
Rothenberger D, Garcia-Aquilar J.Рак прямой кишки, местное лечение. Современная терапия в хирургии толстой кишки и прямой кишки . 2-е изд. Филадельфия, Пенсильвания: Мосби; 2005.
Пэн Дж., Чен В., Венук А. П. и др. Отдаленный исход рака прямой кишки на ранней стадии после стандартной резекции и местного иссечения. Клинический колоректальный рак . 2011 г. 1. 10 (1): 37-41. [Медлайн].
Брукс М. Местное иссечение рака прямой кишки увеличивается, но неэффективно. Медицинские новости Medscape. Доступно по адресу http: // www.medscape.com/viewarticle/815376. 4 декабря 2013 г .; Дата обращения: 5 января 2021 г.
Weiser MR, Landmann RG, Wong WD, Shia J, Guillem JG, Temple LK, et al. Хирургическое лечение рецидива рака прямой кишки после трансанального иссечения. Диск прямой кишки . 2005 июн. 48 (6): 1169-75. [Медлайн].
Хирургическое лечение рецидива рака прямой кишки после трансанального иссечения. Диск прямой кишки . 2005 июн. 48 (6): 1169-75. [Медлайн].
Кваан MR, Стюарт старший DB, Данн KB. Толстая кишка, прямая кишка и анус. Brunicardi FC, Andersen DK, Billiar TR, et al, eds. Принципы хирургии Шварца .11 изд. Нью-Йорк, Нью-Йорк: образование Макгроу-Хилл; 2019. Vol 2: 1259-1330.
Li S, Chi P, Lin H, Lu X, Huang Y. Долгосрочные результаты лапароскопической хирургии по сравнению с открытой резекцией при раке средней и нижней прямой кишки: исследование NTCLES. Эндоскопическая хирургия . 2011 25 октября (10): 3175-82. [Медлайн].
Green BL, Marshall HC, Collinson F, Quirke P, Guillou P, Jayne DG и др. Долгосрочное наблюдение за результатами исследования CLASICC, проведенного Советом по медицинским исследованиям, по сравнению традиционной и лапароскопической резекции при колоректальном раке. Br J Surg . 2012 6 ноября [Medline].
Br J Surg . 2012 6 ноября [Medline].
Bonjer HJ, Deijen CL, Abis GA, Cuesta MA, van der Pas MH, de Lange-de Klerk ES, et al. Рандомизированное исследование лапароскопической и открытой хирургии рака прямой кишки. N Engl J Med . 2015 Апрель 2. 372 (14): 1324-32. [Медлайн].
Augestad KM, Crawshaw B, Delany CP. Рак прямой кишки: оперативное лечение. Fazio VW, Church JM, Delaney CP, Kiran RP, ред. Современная терапия в хирургии толстой кишки и прямой кишки .3-е изд. Филадельфия, Пенсильвания: Эльзевьер; 2017. 146-151.
Maurer CA, Renzulli P, Kull C, et al. Влияние введения тотального мезоректального иссечения на частоту местных рецидивов и выживаемость при раке прямой кишки: отдаленные результаты. Энн Сург Онкол . 2011 июл.18 (7): 1899-906. [Медлайн].
Хан Ю.Д., Ким В.Р., Парк С.В., Чо М.С., Хур Х., Мин Б.С. и др. Предикторы патологического полного ответа у пациентов с раком прямой кишки, подвергающихся тотальному иссечению мезоректальной кишки после предоперационной химиолучевой терапии. Медицина (Балтимор) . Ноябрь 2015. 94 (45): e1971. [Медлайн]. [Полный текст].
Якобс М., Вердея Дж. С., Гольдштейн HS. Минимально инвазивная резекция толстой кишки (лапароскопическая колэктомия). Хирургическая лапароскопическая эндоскопия . 1991 Сентябрь 1 (3): 144-50. [Медлайн].
Хирургическая лапароскопическая эндоскопия . 1991 Сентябрь 1 (3): 144-50. [Медлайн].
Trastulli S, Cirocchi R, Listorti C, Cavaliere D, Avenia N, Gullà N и др. Лапароскопическая и открытая резекция рака прямой кишки: метаанализ рандомизированных клинических исследований. Колоректальный диск . 14 июня 2012 г. (6): e277-96. [Медлайн].
van der Pas MH, Haglind E, Cuesta MA, Fürst A, Lacy AM, Hop WC, et al. Сравнение лапароскопической и открытой хирургии рака прямой кишки (ЦВЕТ II): краткосрочные результаты рандомизированного исследования фазы 3. Ланцет Онкол . 2013 14 марта (3): 210-8. [Медлайн].
Fleshman J, Branda M, Sargent DJ и др. Влияние лапароскопической резекции и открытой резекции рака прямой кишки II или III стадии на патологические исходы: рандомизированное клиническое испытание ACOSOG Z6051. ЯМА . 2015 Октябрь 6. 314 (13): 1346-55. [Медлайн]. [Полный текст].
ЯМА . 2015 Октябрь 6. 314 (13): 1346-55. [Медлайн]. [Полный текст].
Bujko K, Rutkowski A, Chang GJ, Michalski W., Chmielik E, Kusnierz J. Основано ли правило резекции дистального отдела кишечника на расстоянии 1 см при раке прямой кишки на основании клинических данных? Систематический обзор. Индийский J Surg Oncol . 2012 июн. 3 (2): 139-46. [Медлайн]. [Полный текст].
Quan D, Gallinger S, Nhan C., Auer RA, Biagi JJ, Fletcher GG, et al. Роль резекции печени при метастазах колоректального рака в эпоху мультимодального лечения: систематический обзор. Хирургия . 2012 июнь 151 (6): 860-70. [Медлайн].
Дхир М., Лайден Э.Р., Ван А. и др. Влияние границ на общую выживаемость после резекции печени по поводу колоректального метастаза: метаанализ. Энн Сург . 2011 Август 254 (2): 234-42. [Медлайн].
[Медлайн].
Маргалит Д. Н., Мамон Х. Дж., Анчукевич М. и др. Переносимость комбинированной терапии рака прямой кишки у пожилых пациентов в возрасте 75 лет и старше. Int J Radiat Oncol Biol Phys . 2011 декабрь 1. 81 (5): e735-41. [Медлайн].
Ceelen WP, Van Nieuwenhove Y, Fierens K. Предоперационная химиолучевая терапия в сравнении с одной только радиацией при резектабельном раке прямой кишки II и III стадии. Кокрановская база данных Syst Rev . 2009 21 января. CD006041. [Медлайн].
Якобсен А., Плоен Дж., Вуонг Т., Аппельт А., Линдебьерг Дж., Рафаэльсен С.Р. Зависимость доза-эффект в химиолучевой терапии для местнораспространенного рака прямой кишки: рандомизированное испытание, сравнивающее две дозы облучения. Int J Radiat Oncol Biol Phys . 2012 15 мая. [Medline].
Кэссиди Р.Дж., Лю Й., Патель К., Чжун Дж., Стойер С.Е., Куби Д.А. и др. Можем ли мы отменить неоадъювантную химиолучевую терапию в пользу неоадъювантной мультиагентной химиотерапии для некоторых ректальных аденокарцином II / III стадии: анализ национальной базы данных по раку. Рак . Март 2017. 123 (5): 783-793. [Медлайн]. [Полный текст].
Ng K, Ogino S, Meyerhardt JA и др.Взаимосвязь между использованием статинов и рецидивом рака толстой кишки и выживаемостью: результаты исследования CALGB 89803. J Natl Cancer Inst . 2011 Октябрь 19, 103 (20): 1540-51. [Медлайн]. [Полный текст].
Цао С., Бхаттачарья А., Дуррани Ф.А., Факих М. Иринотекан, оксалиплатин и ралтитрексед для лечения распространенного колоректального рака. Экспертное мнение Фармаколог . 2006 г., 7 (6): 687-703. [Медлайн].
Моган Т.С., Адамс Р.А., Смит К.Г. и др. Добавление цетуксимаба к комбинированной химиотерапии первой линии на основе оксалиплатина для лечения распространенного колоректального рака: результаты рандомизированного исследования MRC COIN фазы 3. Ланцет . 2011, 18 июня. 377 (9783): 2103-14. [Медлайн].
[Медлайн].
Douillard JY, Siena S, Cassidy J, Tabernero J, Burkes R, Barugel M и др. Рандомизированное исследование фазы III панитумумаба с инфузией фторурацила, лейковорина и оксалиплатина (FOLFOX4) по сравнению с одним только FOLFOX4 в качестве терапии первой линии у пациентов с ранее нелеченным метастатическим колоректальным раком: исследование PRIME. Дж Клин Онкол . 2010 г., 1. 28 (31): 4697-705. [Медлайн].
Peeters M, Price TJ, Cervantes A, Sobrero AF, Ducreux M, Hotko Y.Рандомизированное исследование III фазы панитумумаба с фторурацилом, лейковорином и иринотеканом (FOLFIRI) по сравнению с одним только FOLFIRI в качестве лечения второй линии у пациентов с метастатическим колоректальным раком. Дж Клин Онкол . 2010 г., 1. 28 (31): 4706-13. [Медлайн].
Simkens LH, Koopman M, Mol L, et al. Влияние индекса массы тела на исход у пациентов с запущенным колоректальным раком, получающих химиотерапию с таргетной терапией или без нее. евро J Рак .2011 ноябрь 47 (17): 2560-7. [Медлайн].
Влияние индекса массы тела на исход у пациентов с запущенным колоректальным раком, получающих химиотерапию с таргетной терапией или без нее. евро J Рак .2011 ноябрь 47 (17): 2560-7. [Медлайн].
Boisen MK, Johansen JS, Dehlendorff C, Larsen JS, Osterlind K, Hansen J и др. Первичная локализация опухоли и эффективность бевацизумаба у пациентов с метастатическим колоректальным раком. Энн Онкол . 17 июля 2013 г. [Medline].
Nelson R. Pembro Одобрено для использования 1-й линии при колоректальном раке MSI-H / dMMR. Медицинские новости Medscape. Доступно на https://www.medscape.com/viewarticle/933172. 30 июня 2020 г .; Доступ: 8 июля 2020 г.
Райан ЭДЖ, О’Салливан Д.П., Келли М.Э., Сайед А.З., Нири ПК, О’Коннелл П.Р. и др. Метаанализ эффекта увеличения интервала после длительного курса химиолучевой терапии перед операцией при местнораспространенном раке прямой кишки. Br J Surg . 2019 июн 19, 10 (9): e0138720. [Медлайн].
Br J Surg . 2019 июн 19, 10 (9): e0138720. [Медлайн].
Эберт М.П., Танцер М., Баллафф Б. и др. TFAP2E-DKK4 и химиорезистентность при колоректальном раке. N Engl J Med . 2012, 5 января, 366 (1): 44-53. [Медлайн].
Hendlisz A, Van den Eynde M, Peeters M, Maleux G, Lambert B, Vannoote J, et al. Испытание фазы III, сравнивающее длительную внутривенную инфузию фторурацила отдельно или с радиоэмболизацией микросфер иттрия-90 при метастатическом колоректальном раке, рефрактерном к стандартной химиотерапии. Дж Клин Онкол . 2010 10 августа. 28 (23): 3687-94. [Медлайн].
Wasan HS, et al; Исследователи испытаний FOXFIRE., Исследователи испытаний SIRFLOX., Исследователи FOXFIRE-Global, Ван Хейзел Г., Шарма Р.А. Селективная внутренняя лучевая терапия первой линии плюс химиотерапия по сравнению с одной химиотерапией у пациентов с метастазами в печень от колоректального рака (FOXFIRE, SIRFLOX и FOXFIRE-Global): комбинированный анализ трех многоцентровых рандомизированных исследований фазы 3. Ланцет Онкол . 2017 сентября 18 (9): 1159-1171. [Медлайн]. [Полный текст].
Ланцет Онкол . 2017 сентября 18 (9): 1159-1171. [Медлайн]. [Полный текст].
Сантьяго I, Барата М., Фигейредо Н., Пареш О, Энрикес В., Галцерано А. и др.Признак расщепленного рубца как показатель устойчивого полного ответа на неоадъювантную терапию рака прямой кишки. евро Радиол . 26 июля 2019 г. [Medline].
Song M, Wu K, Meyerhardt JA, Ogino S, Wang M, Fuchs CS и др. Потребление клетчатки и выживаемость после диагностики колоректального рака. JAMA Онкол . 2 ноября 2017 г. [Medline]. [Полный текст].
Давенпорт Л. Высокое потребление клетчатки связано с улучшением выживаемости при раке толстой кишки. Медицинские новости Medscape.Доступно на https://www.medscape.com/viewarticle/888006. 3 ноября 2017 г .; Доступ: 8 ноября 2017 г.
[Рекомендации] Левин Б., Либерман Д.А., МакФарланд Б. и др.Скрининг и наблюдение для раннего выявления колоректального рака и аденоматозных полипов, 2008 г .: совместное руководство Американского онкологического общества, Целевой группы многих обществ США по колоректальному раку и Американского колледжа радиологии. CA Cancer J Clin . 2008 май-июнь. 58 (3): 130-60. [Медлайн].
[Рекомендации] Рекомендации Американского онкологического общества по скринингу колоректального рака. Американское онкологическое общество. Доступно по адресу https://www. cancer.org/cancer/colon-rectal-cancer/detection-diagnosis-staging/acs-recommendations.html. 30 мая 2018 г .; Дата обращения: 11 марта 2020 г.
cancer.org/cancer/colon-rectal-cancer/detection-diagnosis-staging/acs-recommendations.html. 30 мая 2018 г .; Дата обращения: 11 марта 2020 г.
Уилт Т.Дж., Харрис Р.П., Касим А., Целевая группа по высокому уходу Американского колледжа врачей. Скрининг на рак: рекомендации Американского колледжа врачей по оказанию высококачественной помощи. Энн Интерн Мед. . 2015 19 мая. 162 (10): 718-25. [Медлайн].
[Рекомендации] Рекс Д.К., Джонсон Д.А., Андерсон Дж.С., Шонфельд П.С., Берк Калифорния, Инадоми Дж. М. и др. Рекомендации Американского колледжа гастроэнтерологии по скринингу на колоректальный рак, 2009 г. [исправлено]. Ам Дж. Гастроэнтерол . 2009 Март 104 (3): 739-50. [Медлайн].
[Рекомендации] Национальная комплексная онкологическая сеть. NCCN Clinical Practice Guidelines in Oncology: Colorectal Cancer Screening. NCCN. Доступно на http://www.nccn.org/professionals/physician_gls/pdf/colorectal_screening.pdf. Версия 2.2019 — 2 августа 2019 г .; Дата обращения: 11 марта 2020 г.
NCCN. Доступно на http://www.nccn.org/professionals/physician_gls/pdf/colorectal_screening.pdf. Версия 2.2019 — 2 августа 2019 г .; Дата обращения: 11 марта 2020 г.
[Рекомендации] Рубинштейн Дж. Х., Эннс Р., Хайдельбо Дж., Баркун А., Комитет по клиническим руководствам.Руководство Института Американской гастроэнтерологической ассоциации по диагностике и лечению синдрома Линча. Гастроэнтерология . 2015 сентябрь 149 (3): 777-82; викторина e16-7. [Медлайн]. [Полный текст].
[Рекомендации] Бальманья Дж., Балагер Ф., Сервантес А., Арнольд Д., Рабочая группа по рекомендациям ESMO. Семейный риск колоректального рака: Руководство по клинической практике ESMO. Энн Онкол . 2013 24 октября Дополнение 6: vi73-80. [Медлайн]. [Полный текст].
[Рекомендации] Стоффель Е.М., Мангу ПБ, Грубер С.Б., Гамильтон С. Р., Калади М.Ф., Лау М.В. и др.Синдромы наследственного колоректального рака: Американское общество клинической онкологии. Подтверждение рекомендаций по клинической практике семейного риска — колоректального рака: Руководства по клинической практике Европейского общества медицинской онкологии. Дж Клин Онкол . 2015 10 января. 33 (2): 209-17. [Медлайн]. [Полный текст].
Р., Калади М.Ф., Лау М.В. и др.Синдромы наследственного колоректального рака: Американское общество клинической онкологии. Подтверждение рекомендаций по клинической практике семейного риска — колоректального рака: Руководства по клинической практике Европейского общества медицинской онкологии. Дж Клин Онкол . 2015 10 января. 33 (2): 209-17. [Медлайн]. [Полный текст].
[Рекомендации] Syngal S, Brand RE, Church JM, Giardiello FM, Hampel HL, Burt RW и др. Клинические рекомендации ACG: Генетическое тестирование и лечение синдромов наследственного рака желудочно-кишечного тракта. Ам Дж. Гастроэнтерол . 2015 февраль 110 (2): 223-62; викторина 263. [Medline]. [Полный текст].
Umar A, Boland CR, Terdiman JP, et al. Пересмотренные рекомендации Bethesda по наследственному неполипозному колоректальному раку (синдром Линча) и микросателлитной нестабильности. Национальный институт рака . 2004 18 февраля. 96 (4): 261-8. [Медлайн].
Национальный институт рака . 2004 18 февраля. 96 (4): 261-8. [Медлайн].
[Директива] Гупта С., Либерман Д., Андерсон Дж. К., Берк Калифорния, Доминиц Дж. А., Кальтенбах Т. и др. Рекомендации по дальнейшему наблюдению после колоноскопии и полипэктомии: обновленный консенсус Целевой группы США по колоректальному раку. Гастроэнтерология . 2020 Март 158 (4): 1131-1153.e5. [Медлайн].
[Рекомендации] Раттер, доктор медицины, Ист Дж., Рис CJ, Криппс Н., Дочерти Дж., Долвани С. и др. Британское общество гастроэнтерологов / Ассоциация колопроктологов Великобритании и Ирландии / Управление общественного здравоохранения Англии после полипэктомии и постколоректальной резекции рака. Кишечник . 2020 Февраль 69 (2): 201-223. [Медлайн]. [Полный текст].
[Рекомендации] Черч Дж., Симманг С. Целевая группа по стандартам, Американское общество хирургов толстой и прямой кишки, Совместная группа Америк по наследственному колоректальному раку и Комитет по стандартам Американского общества хирургов толстой и прямой кишки. Параметры практики лечения пациентов с доминантно наследственным колоректальным раком (семейный аденоматозный полипоз и наследственный неполипозный колоректальный рак). Диск прямой кишки . 2003 августа 46 (8): 1001-12. [Медлайн].
Параметры практики лечения пациентов с доминантно наследственным колоректальным раком (семейный аденоматозный полипоз и наследственный неполипозный колоректальный рак). Диск прямой кишки . 2003 августа 46 (8): 1001-12. [Медлайн].
[Рекомендации] Монсон Дж. Р., Вайзер М. Р., Буйе В. Д., Чанг Дж. Дж., Рафферти Дж. Ф., Буйе В. Д. и др. Параметры практики лечения рака прямой кишки (пересмотренная). Диск прямой кишки . 2013 май. 56 (5): 535-50. [Медлайн].
[Рекомендации] Глинн-Джонс Р., Вирвиц Л., Тирет Э., Браун Г., Рёдел С., Сервантес А. и др.Рак прямой кишки: Руководство ESMO по клинической практике по диагностике, лечению и последующему наблюдению. Энн Онкол . 2018, 1. 29 октября (Приложение_4): iv263. [Медлайн]. [Полный текст].
[Рекомендации] Meyerhardt JA, Mangu PB, Flynn PJ, Korde L, Loprinzi CL, Minsky BD, et al. Последующее наблюдение, протокол наблюдения и меры вторичной профилактики для переживших колоректальный рак: одобрение руководства по клинической практике Американского общества клинической онкологии. Дж Клин Онкол .2013 декабрь 10. 31 (35): 4465-70. [Медлайн].
Последующее наблюдение, протокол наблюдения и меры вторичной профилактики для переживших колоректальный рак: одобрение руководства по клинической практике Американского общества клинической онкологии. Дж Клин Онкол .2013 декабрь 10. 31 (35): 4465-70. [Медлайн].
[Рекомендации] Лабианка Р., Нордлингер Б., Беретта Г.Д., Москони С., Мандала М., Сервантес А. и др. Ранний рак толстой кишки: Руководство ESMO по клинической практике по диагностике, лечению и последующему наблюдению. Энн Онкол . 2013 24 октября Дополнение 6: vi64-72. [Медлайн].
[Рекомендации] Стил С.Р., Чанг Г.Дж., Хендрен С., Вайзер М., Ирани Дж., Буйе В.Д. и др. Практическое руководство по наблюдению за пациентами после лечебного лечения рака прямой и толстой кишки. Диск прямой кишки . 2015 Август 58 (8): 713-25. [Медлайн]. [Полный текст].
[Рекомендации] Ван Катсем Э., Сервантес А., Адам Р. и др. Консенсусное руководство ESMO по ведению пациентов с метастатическим колоректальным раком. Энн Онкол . 2016 27 августа (8): 1386-422. [Медлайн]. [Полный текст].
выживаемости при раке толстой кишки | Моффит
Показатель выживаемости при раке толстой кишки обнадеживающе высок; более 92 процентов пациентов, у которых диагностирован рак толстой кишки 1 стадии, живут не менее пяти лет после постановки диагноза. Показатели выживаемости на более поздних стадиях также неуклонно повышаются, в первую очередь благодаря доступности более эффективных вариантов лечения и все более глубокому пониманию болезни с течением времени.
Показатели выживаемости на более поздних стадиях также неуклонно повышаются, в первую очередь благодаря доступности более эффективных вариантов лечения и все более глубокому пониманию болезни с течением времени.
Хотя информация о выживаемости при раке толстой кишки может помочь людям узнать больше об опыте других пациентов, статистика не принимает во внимание личные факторы, которые могут улучшить шансы человека на выживание. Например:
- У людей, которые участвуют в регулярных обследованиях, больше шансов на раннее выявление — и, следовательно, больше шансов на выживание.Подсчитано, что до 60 процентов всех смертей, связанных с раком толстой кишки, можно было бы предотвратить, если бы каждый выполнял соответствующие рекомендации по скринингу.
- Люди, которые не считаются подходящими кандидатами на традиционные методы лечения, могут расширить свой диапазон возможностей, рассматривая клинические испытания. Хотя участие в клинических испытаниях не гарантирует более высоких шансов на выживание, оно дает пациентам возможность одними из первых получить пользу от нового многообещающего лечения рака толстой кишки.

- Людям, которые обращаются за помощью к онкологу — или, предпочтительно, к группе онкологов, — которые имеют большой опыт лечения различных форм колоректального рака, часто полезно более индивидуализированное лечение. Например, некоторые методы лечения, которые эффективны при раке прямой кишки, менее эффективны при раке толстой кишки, и онкологи, которые лечат многих пациентов с этими состояниями, имеют более широкий опыт применения этих методов лечения и могут разработать более индивидуальные планы лечения.
В онкологическом центре Моффитта мы стремимся постоянно повышать выживаемость больных раком толстой кишки.Мы являемся лидерами в разработке и оценке новых методов лечения, предлагая нашим пациентам доступ к обширному портфелю клинических испытаний. Кроме того, у нас есть многопрофильная команда хирургов, медицинских онкологов, лучевых терапевтов и специалистов по поддерживающей терапии, которые лечат исключительно пациентов с колоректальным раком, и для консультации с любым из этих экспертов не требуется направления. Чтобы узнать больше, позвоните по телефону 1-888-663-3488 или отправьте новую форму регистрации пациента онлайн.
Чтобы узнать больше, позвоните по телефону 1-888-663-3488 или отправьте новую форму регистрации пациента онлайн.
Лечение метастатического рака прямой кишки
Метастаз означает, что рак распространился за пределы прямой кишки на другие части тела.Это часто называют распространенным раком прямой кишки.
Варианты лечения будут зависеть от нескольких факторов, в том числе от степени рака и места его распространения. Колоректальный рак обычно распространяется на печень. Он также может распространяться на легкие, слизистую оболочку брюшной полости, яичники, мозг и другие органы.
Последние достижения в области лечения улучшили перспективы для людей с метастатическим раком прямой кишки, включая рак IV стадии.
Варианты лечения метастатического рака прямой кишки
Рак прямой кишки, распространившийся на другие органы, часто требует комбинированного лечения. Сюда могут входить:
Сюда могут входить:
- хирургия
- химиотерапия
- методы лечения под визуальным контролем, такие как МРТ и КТ
- лучевая терапия
- Таргетная терапия и иммунотерапия
- клинические испытания
Варианты лечения рака прямой кишки, распространившегося на печень
Рак прямой кишки чаще всего распространяется на печень. Отчасти это происходит потому, что кровоснабжение толстой кишки, в том числе прямой кишки, связано с печенью через большой кровеносный сосуд.
Для лечения рака прямой кишки, распространившегося на печень, специалисты MSK могут использовать несколько вариантов, часто в комбинации. К ним относятся:
Хирургия опухолей прямой кишки и печени
Хирурги
MSK часто могут удалять опухоли прямой кишки и печени во время одной и той же процедуры. Это может уменьшить боль и сократить время восстановления. Химиотерапия и лучевая терапия иногда используются для уменьшения опухоли перед операцией. Хирурги MSK ежегодно оперируют несколько сотен человек с метастазами в печень.
Хирурги MSK ежегодно оперируют несколько сотен человек с метастазами в печень.
Некоторым людям понадобится колостома. Для этой процедуры хирург разрезает прямую кишку выше уровня рака и прикрепляет конец к хирургическому отверстию на животе. Отходы собираются через это отверстие и хранятся в прикрепленном к коже мешке.
Узнайте больше о метастазах в печени.
Химиотерапия
Химиотерапия часто сочетается с хирургическим вмешательством и другими видами лечения. Это можно делать в разное время во время лечения:
Неоадъювантная терапия проводится перед операцией, чтобы уменьшить опухоли или остановить их рост.
Адъювантная терапия проводится после операции. Это может помочь уничтожить оставшиеся раковые клетки, снижая риск повторного появления опухолей.
Инфузия печеночной артерии (HAI) — это разновидность химиотерапии, которая проводится внутривенно.
 HAI доставляет химиотерапевтические препараты непосредственно в печень через крошечный насос, который имплантируется под кожу в нижней части живота.HAI оказывает лечение непосредственно там, где находится опухоль.
HAI доставляет химиотерапевтические препараты непосредственно в печень через крошечный насос, который имплантируется под кожу в нижней части живота.HAI оказывает лечение непосредственно там, где находится опухоль.
Интервенционная радиология
При интервенционной радиологии, например абляции, для уменьшения или разрушения опухолей используются несколько форм высокофокусированной энергии. Это можно сделать до или после операции или вместо операции, если это невозможно. Эти методы чрезвычайно точны. Сложные инструменты визуализации, такие как КТ и ПЭТ / КТ, позволяют специалистам видеть, что происходит внутри тела во время лечения.
Эти методы иногда сочетаются с процедурой, называемой эмболизацией. Это включает введение крошечных частиц, чтобы заблокировать или уменьшить приток крови к раковым клеткам, перекрывая их питание.
Таргетная терапия
Целенаправленная терапия атакует определенные гены и белки в раковых клетках.
Некоторые лекарства нацелены на белок, называемый VEGF. Этот белок помогает опухолям образовывать новые кровеносные сосуды, чтобы получать питательные вещества, необходимые для роста.;
Другие препараты нацелены на EGFR. Этот белок способствует росту раковых клеток.
Третий тип лекарств известен как ингибитор киназ. Он нацелен на белок, который передает важные сигналы в центр управления раковыми клетками. Блокирование этого белка может помочь остановить рост раковых клеток.
Таргетная терапия эффективна для относительно небольшого числа людей с колоректальным раком, в зависимости от множества генетических факторов.
Иммунотерапия
Иммунотерапия использует собственную иммунную систему организма для атаки раковых клеток.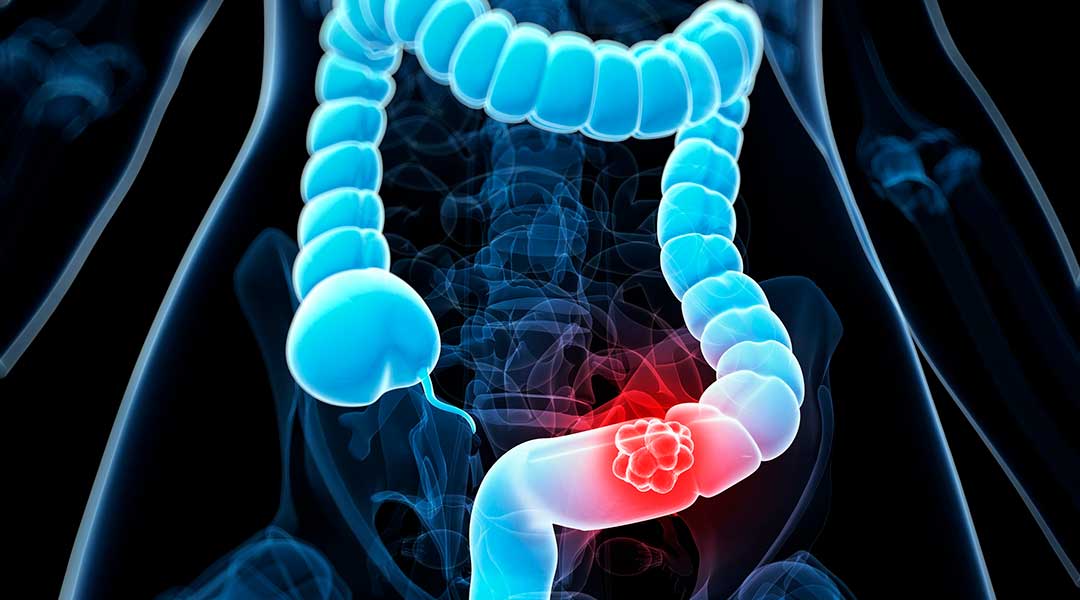
Ингибиторы контрольных точек — это лекарства, которые высвобождают мощные Т-клетки иммунной системы для борьбы с раком. Некоторые раковые клетки становятся невидимыми для иммунной системы, сигнализируя о том, что они не вредны. Ингибиторы КПП предотвращают этот обман. Эти препараты позволяют Т-клеткам видеть и атаковать опухоль.
Иммунотерапия — это захватывающее новое достижение, но она помогает лишь небольшому количеству людей с колоректальным раком с определенным генетическим набором.
Узнайте больше об иммунотерапии.
Клинические испытания
Являясь одним из ведущих в мире онкологических институтов, MSK может предоставить вам доступ к клиническим испытаниям новых методов лечения, которые нельзя найти где-либо еще. Поговорите со своей группой по уходу, чтобы узнать, может ли клиническое испытание быть для вас вариантом.
Исход и прогностические факторы у 593 пациентов с неметастатическим раком прямой кишки: монофункциональное исследование
Характеристики пациентов
Были проанализированы данные 593 последовательных пациентов без метастазов, прошедших лучевую терапию в период с 2004 по 2015 год для доказанного РЦ. На момент лучевой терапии средний возраст составлял 68,8 года (диапазон: 27–96), с 362 мужчинами и 231 женщинами. Пациенты были в хорошем состоянии, 549 пациентов (92,6%) имели статус эффективности ECOG 0–1. Недоедание (ИМТ <18,5) было зарегистрировано у 21 пациента (3,5%). Большинство РЦ (n = 507, 85,5%) были диагностированы в местно-распространенных условиях (II-III стадии). Опухоли располагались в нижней (n = 252, 42,5%), средней (n = 249, 42%) или верхней (88, 14,8%) прямой кишке. Наиболее частой гистологией была аденокарцинома (n = 587, 99%) с умеренной дифференцировкой (n = 278, 46.9%). Операция на прямой кишке выполнена 552 пациентам (93,1%). Характеристики пациента и опухоли представлены в таблице 1.
На момент лучевой терапии средний возраст составлял 68,8 года (диапазон: 27–96), с 362 мужчинами и 231 женщинами. Пациенты были в хорошем состоянии, 549 пациентов (92,6%) имели статус эффективности ECOG 0–1. Недоедание (ИМТ <18,5) было зарегистрировано у 21 пациента (3,5%). Большинство РЦ (n = 507, 85,5%) были диагностированы в местно-распространенных условиях (II-III стадии). Опухоли располагались в нижней (n = 252, 42,5%), средней (n = 249, 42%) или верхней (88, 14,8%) прямой кишке. Наиболее частой гистологией была аденокарцинома (n = 587, 99%) с умеренной дифференцировкой (n = 278, 46.9%). Операция на прямой кишке выполнена 552 пациентам (93,1%). Характеристики пациента и опухоли представлены в таблице 1.
Таблица 1 Характеристики пациента и опухоли.
Характеристики лечения
Характеристики лучевой терапии
Лучевая терапия проводилась в предоперационном (n = 477, 80,5%), послеоперационном (n = 75, 12,6%) или эксклюзивном (n = 41, 6,9%) режимах. У пациентов, перенесших предоперационную лучевую терапию, медиана EQD2 прямой кишки составила 49,2 Гр (Q1-Q3 = 44–50) при средней продолжительности 4.9 недель. При послеоперационной и эксклюзивной лучевой терапии медиана EQD2 прямой кишки составляла 47,7 Гр (Q1-Q3 = 43,9–50) в обеих программах, при средней продолжительности 4,6 и 4,4 недели соответственно. Средняя доза на фракцию составляла 2 Гр для до- и послеоперационной лучевой терапии и 2,5 Гр для эксклюзивной лучевой терапии. В предоперационных условиях среднее время от лучевой терапии до операции составляло 6,7 недели (Q1-Q3: 6–7,5). Для пациентов, прошедших послеоперационную лучевую терапию, среднее время от операции до лучевой терапии составило 10.3 недели (Q1 – Q3: 7,8–14,9). Характеристики лучевой терапии подробно описаны в таблице 2.
У пациентов, перенесших предоперационную лучевую терапию, медиана EQD2 прямой кишки составила 49,2 Гр (Q1-Q3 = 44–50) при средней продолжительности 4.9 недель. При послеоперационной и эксклюзивной лучевой терапии медиана EQD2 прямой кишки составляла 47,7 Гр (Q1-Q3 = 43,9–50) в обеих программах, при средней продолжительности 4,6 и 4,4 недели соответственно. Средняя доза на фракцию составляла 2 Гр для до- и послеоперационной лучевой терапии и 2,5 Гр для эксклюзивной лучевой терапии. В предоперационных условиях среднее время от лучевой терапии до операции составляло 6,7 недели (Q1-Q3: 6–7,5). Для пациентов, прошедших послеоперационную лучевую терапию, среднее время от операции до лучевой терапии составило 10.3 недели (Q1 – Q3: 7,8–14,9). Характеристики лучевой терапии подробно описаны в таблице 2.
Таблица 2 Характеристики лучевой терапии (n = 593 пациента).
Характеристики химиотерапии
Химиотерапия ассоциировалась с лучевой терапией у большинства пациентов (n = 414, 69,8%) либо одновременно (n = 409, 69%), либо последовательно (n = 5, 0,8%). Пациенты, подвергавшиеся последовательному химиолучевому лечению, были либо послеоперационными пациентами RC с тяжелыми хирургическими осложнениями, либо пожилыми послеоперационными пациентами.Сопутствующая химиотерапия была связана с 74,6% дооперационной (n = 356/477), 52% послеоперационной (n = 39/75) и 31,7% эксклюзивной (n = 13/41) лучевой терапии. Пероральный или внутривенный 5-ФУ использовался в основном в сопутствующих условиях (n = 331/409, 81%). Характеристики химиотерапии представлены в таблице 3.
Пациенты, подвергавшиеся последовательному химиолучевому лечению, были либо послеоперационными пациентами RC с тяжелыми хирургическими осложнениями, либо пожилыми послеоперационными пациентами.Сопутствующая химиотерапия была связана с 74,6% дооперационной (n = 356/477), 52% послеоперационной (n = 39/75) и 31,7% эксклюзивной (n = 13/41) лучевой терапии. Пероральный или внутривенный 5-ФУ использовался в основном в сопутствующих условиях (n = 331/409, 81%). Характеристики химиотерапии представлены в таблице 3.
Таблица 3 Характеристики химиотерапии.
Острая и поздняя токсичность
Из-за острой токсичности 4 пациента (0,7%) не завершили заранее запланированную программу лучевой терапии.Сообщалось об одной острой токсичности 5 степени: пациент прошел эксклюзивную лучевую терапию по поводу опухоли Т4 и прошел химиотерапию миеломы за месяц до начала радиоактивного облучения. Перед лучевой терапией опухоль прямой кишки превратилась в абсцесс, что привело к летальному исходу после 4 курсов облучения. Сообщалось об одной острой токсичности 4 степени, при этом пациент, проходивший исключительно лучевую терапию, страдал обструктивным лучевым проктитом. Об острой интоксикации в полевых условиях сообщалось у 57,9% дооперационных (262 степени 1-2, 14 степени 3), 53.3% послеоперационных (35 степени 1-2, 5 степени 3) и 63,4% эксклюзивных (20 степени 1-2, 4 степени 3, 2 степени 4-5) лучевой терапии. Острые побочные эффекты 3 степени были желудочно-кишечными (11 пациентов, 10 из которых получали сопутствующую химиотерапию), кожными (7 пациентов, 6 из которых получали сопутствующую химиотерапию) и мочевыми (1 пациент, получавшими сопутствующую химиотерапию) токсичностью.
Сообщалось об одной острой токсичности 4 степени, при этом пациент, проходивший исключительно лучевую терапию, страдал обструктивным лучевым проктитом. Об острой интоксикации в полевых условиях сообщалось у 57,9% дооперационных (262 степени 1-2, 14 степени 3), 53.3% послеоперационных (35 степени 1-2, 5 степени 3) и 63,4% эксклюзивных (20 степени 1-2, 4 степени 3, 2 степени 4-5) лучевой терапии. Острые побочные эффекты 3 степени были желудочно-кишечными (11 пациентов, 10 из которых получали сопутствующую химиотерапию), кожными (7 пациентов, 6 из которых получали сопутствующую химиотерапию) и мочевыми (1 пациент, получавшими сопутствующую химиотерапию) токсичностью.
О поздней токсичности 5 степени не сообщалось. Сообщалось о двух поздних интоксикациях 4 степени, со стенозом мочеточника, вызывающим хроническую почечную недостаточность.Двум пациентам была проведена предоперационная гипофракционированная лучевая терапия с дозой 2,5–2,7 Гр / фракция. Один пациент перенес одновременную химиотерапию с внутривенным введением 5-ФУ. Поздняя токсичность была отмечена в 13,8% дооперационных (59 степени 1-2, 7 степени 3), 12% послеоперационных (9 степень 1-2) и 2,4% эксклюзивных (одна степень 2) лучевой терапии. Поздняя токсичность 3 степени была желудочно-кишечной (6 пациентов с фистулой и стенозом, 5 одновременных химиолучевых препаратов) и мочевой (1 пациент с дизурией, который подвергся одновременной химиотерапии).
Поздняя токсичность была отмечена в 13,8% дооперационных (59 степени 1-2, 7 степени 3), 12% послеоперационных (9 степень 1-2) и 2,4% эксклюзивных (одна степень 2) лучевой терапии. Поздняя токсичность 3 степени была желудочно-кишечной (6 пациентов с фистулой и стенозом, 5 одновременных химиолучевых препаратов) и мочевой (1 пациент с дизурией, который подвергся одновременной химиотерапии).
Эффективность
Общий результат
Средний период наблюдения составил 3,4 года. На момент анализа 21,9% (n = 130) из 593 включенных пациентов испытали метастатическое прогрессирование, а 33% (n = 196) умерли. В подгруппе из 552 пациентов, перенесших ректальную операцию, 29,2% (n = 161) умерли в конце периода наблюдения. В конце периода наблюдения 397 пациентов были живы (то есть без зарегистрированной даты смерти) во всей группе пациентов, из них 391 — в подгруппе пациентов, перенесших ректальную операцию.Из всего набора пациентов 126 смертей были конкретно вызваны RC. Медиана ОВ составила 9,04 года (ДИ 95%: 7-нет данных). Медиана ВБП составила 6,7 года (ДИ 95%: 4-нет данных). Из 552 пациентов, перенесших лечебную операцию, у 54 был полный регресс патологии (9,8%).
Медиана ВБП составила 6,7 года (ДИ 95%: 4-нет данных). Из 552 пациентов, перенесших лечебную операцию, у 54 был полный регресс патологии (9,8%).
Прогностические факторы ОВ у всей группы пациентов: однофакторный и многомерный анализ
Что касается характеристик лучевой терапии, предоперационные или послеоперационные параметры облучения не коррелировали со значительно различающимися результатами, при медиане ОВ 9.1 год (ДИ 95%: 9-нет данных) против . 6,7 года (ДИ 95%: 4,2-NA), p = 0,065 соответственно (рис.1 ) . Эксклюзивная лучевая терапия была значимо связана с уменьшением выживаемости по сравнению с предоперационной лучевой терапией, со средней выживаемостью 1 год (ДИ 95%: 0,36–1,7), p <0,001 (рис. 1). Пороговые значения дозы облучения в прямой кишке или тазу не были достоверно коррелированы с ОВ при одномерном анализе. Однофакторный анализ предоставил потенциальные (p <0,2) прогностические факторы ОС, представленные в таблице 4.Несмотря на значимость при одномерном анализе, полная резекция опухоли, количество подтвержденных патологией пораженных лимфатических узлов, сосудистая инвазия и эксклюзивная лучевая терапия не могли быть включены в многомерный анализ, поскольку они были коррелированы по конструкции с резекцией опухоли. Таким образом, влияние выбранных факторов на ОС было изучено с использованием многомерного анализа Кокса (, таблица 4, ) . Что касается характеристик пациентов, возраст (> 70 лет) был независимым фактором риска смерти (HR = 3.54 ДИ 95% (2,28–5,48), p <0,001) и правильное состояние питания (ИМТ> 18,5) были независимым защитным фактором смерти (HR = 0,37 ДИ 95% (0,16–0,85), p = 0,02). Что касается характеристик опухоли, стадия III и низкодифференцированные опухоли были независимыми факторами риска смерти, с HR = 1,78 CI 95% (1,17–2,70), p = 0,007 и HR = 2,98 CI 95% (1,52-5,72), p = 0,001 соответственно. . Наконец, резекция опухоли была наиболее важным независимым защитным фактором с HR = 0,08 CI 95% (0,04-0.15), p <0,001.
Рисунок 1
Общая выживаемость пациентов, перенесших предоперационную, послеоперационную или эксклюзивную лучевую терапию.
Таблица 4 Прогностические факторы общей выживаемости для всей группы пациентов (n = 593 пациента).
Факторы прогноза OS у пациентов, перенесших резекцию опухоли: одномерный и многомерный анализ
Одномерный анализ предоставил потенциальные (p <0,2) прогностические факторы OS. Несмотря на то, что в однофакторном анализе значимы, сосудистая инвазия, неполная резекция опухоли, сопутствующая химиотерапия, ypCR и статус производительности не могут быть включены в многомерный анализ из-за корреляции с другими переменными.Плохая дифференцировка опухоли была независимым фактором прогноза укороченной OS (HR = 3,43 CI 95% (1,65–7,15), p <0,001). Степень поражения узлов также была независимым фактором риска смерти, поскольку стадия N1 была связана с HR = 2,11 ДИ 95% (1,39–3,22), p <0,001 и стадия N2 с HR = 3,04 ДИ 95% (1,86–4,97). ), p <0,001. Наконец, наиболее важным независимым прогностическим фактором смерти был возраст с HR = 4,66 CI 95% (3,04–7,14), p <0,001 для пациентов старше 70 лет.Результаты однофакторного и многомерного анализов представлены в таблице 5.
Таблица 5 Прогностические факторы общей выживаемости пациентов, перенесших резекцию опухоли (n = 552 пациента).


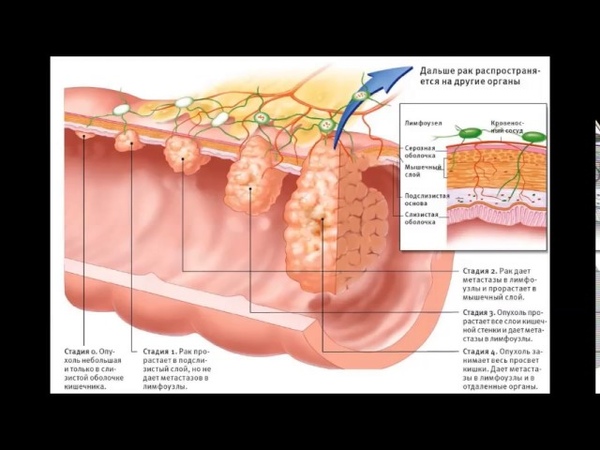
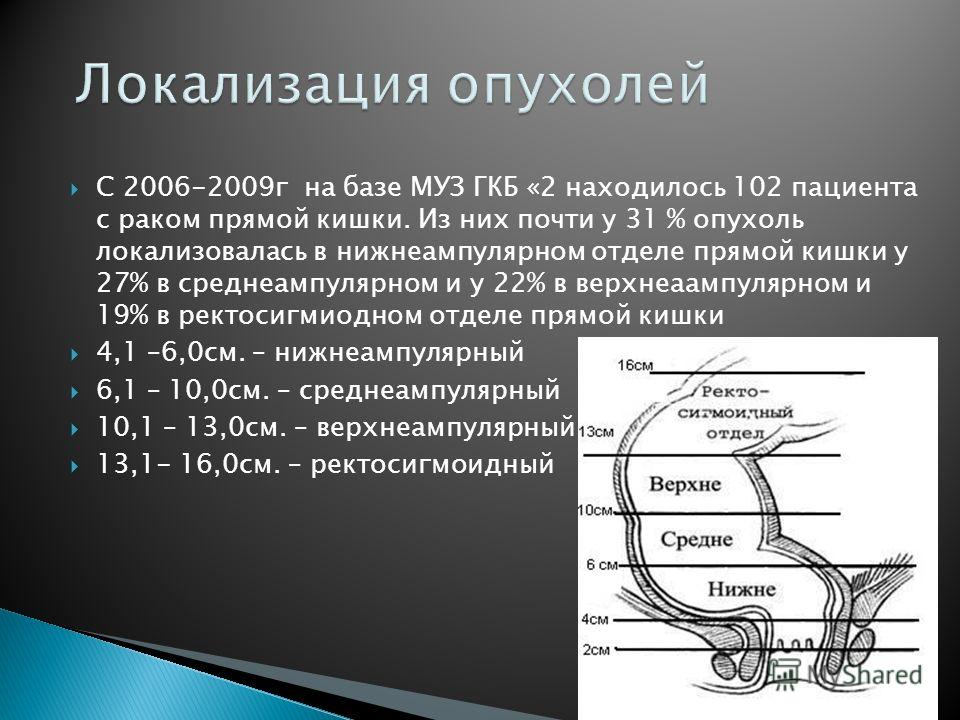 HAI доставляет химиотерапевтические препараты непосредственно в печень через крошечный насос, который имплантируется под кожу в нижней части живота.HAI оказывает лечение непосредственно там, где находится опухоль.
HAI доставляет химиотерапевтические препараты непосредственно в печень через крошечный насос, который имплантируется под кожу в нижней части живота.HAI оказывает лечение непосредственно там, где находится опухоль.