Поздние рецидивы у лиц с остаточными туберкулезными изменениями в легких | Гусейнов
1. Азаматова М. М., Аминов Х. К., Фаттахова Л. З. и др. Рецидивы туберкулеза в Республике Башкортостан // Туберкулез в России, год 2007. М., 2007. — С. 5.
2. Андрианова А. Ю., Мишин В. Ю. Результаты отдаленных наблюдений за лицами с остаточными туберкулезными изменениями в легких, состоящими на учете в поликлиниках общей медицинской сети // Туб. — 2011. — № 4. — С. 34-35.
3. Асхабалиев М. Г., Адзиев А. А., Пахиева Х. Ю. и др. Эпидемиологические аспекты туберкулеза с множественной лекарственной устойчивостью возбудителя в Республике Дагестан // Матер. 7-й Науч.-практ. конференции Республики Дагестан. — Махачкала, 2015. — С. 46-49.
4. Васильева И. А. Стратегия борьбы с туберкулезом в РФ в период до 2020 г. // Доклад на X съезде фтизиатров Российской Федерации. 26.05.2015 г. Интернет.
5. Мамаева П. М. Факторы риска и алгоритм выявления женщин с повышенным риском заболевания туберкулезом в Дагестане: Автореф. дис. … канд. мед. наук. — Махачкала, 2000. — 29 с.
6. Скачкова Е. И., Шестаков М. Г., Темирджанова С. Ю. Динамика и социально-демографическая структура туберкулеза в Российской Федерации, его зависимость от уровня жизни // Туб. — 2009. — № 7. — С. 4-8.
7. Тахтоходжаева Г. Р., Смайлова Д. А. Рецидивы и причины их развития у лиц, излеченных от туберкулеза различной локализации // Туберкулез в России, год 2007. — М., 2007. — С. 37-38.
— С. 37-38.
8. Isikhan V., Balbay O., Annakkaya A. et al. The beliefs ofpatients about the causes of tuberculosis // Europ. Resp. J. — 2005. — Vol. 29. — P. 4358.
9. Mc. Donald H. P., Garg A. X., Haunes R. B. Interventions to enhance patients adherence to medication prescriptions // J. Amer. Med. Assoc. — 2002. — Vol. 288, № 22. — P. 2868-2879.
10. Morisky D. E., Ebin V. S., Malotte C. K. et al. Assesment of tuberculosis treatment completion in an ethically diverse population using two data sources // Evoluat. Health Profes. — 2003. — Vol. 26, № 1. — P. 43-58.
Результаты лечения рецидивов туберкулеза легких Текст научной статьи по специальности «Клиническая медицина»
Оригинальные исследования УДК 616.24-002.5-036.87-08
РЕЗУЛЬТАТЫ ЛЕЧЕНИЯ РЕЦИДИВОВ ТУБЕРКУЛЕЗА ЛЕГКИХ
Пустовой Ю.Г, Гриб ЕЮ. Манохина ОЮ.
ДУ «Луганский государственный медицинский университет», Луганск
Целью работы было сравнение клинической картины и результатов лечения рецидивов туберкулёза легких с бактериовыделением и без бактериовыделения. Были обследованы 156 пациентов с рецидивом туберкулёза лёгких. Установлено, что клинические проявления рецидивов туберкулёза легких c бактериовыделением тяжелее: больше сопутствующих заболеваний, деструктивных изменений легочной ткани, высокий уровень резистентности к противотуберкулёзным препаратам. Количество положительных результатов лечения («излечен»+»лечение завершено») абациллярных рецидивов туберкулёза легких составляет 68%, а у пациентов с бактериовыделением только 39%. Таким образом, экономически и эпидемиологически выгоднее выявление и лечение рецидивов туберкулёза легких без бактериовыделения.
Таким образом, экономически и эпидемиологически выгоднее выявление и лечение рецидивов туберкулёза легких без бактериовыделения.
Ключевые слова: рецидивы туберкулёза лёгких, клиническая картина, результаты лечения.
Общеизвестным является тот факт, что клиническая картина рецидивов туберкулёза легких значительно тяжелее, чем при впервые выявленных процессах [1, 5, 6]. Зачастую исследователи акцентируют внимание на рецидивах с бактериовыделением, что, несомненно, важно в эру мультирезистентного туберкулёза. Так, при повторных процессах уровень резистентности составляет от 68% до 86% [5, 6], уровень мультирезистентности среди рецидивов в 6 раз больше, чем у пациентов с впервые выявленными заболеваниями [6]. Учитывая высокий удельный вес случаев с резистентностью M. tuberculisis, эффективность лечения таких пациентов остаётся, к сожалению, низкой: количество пациентов с успешными результатами лечения («излеченные»+ «лечение завершено») составляет от 34% до 46% в странах Восточной Европы [3, 4, 7] и до 75% в странах Африки и Индии [10, 11, 12]. Значительно лучше результаты лечения у пациентов с рецидивом туберкулёза легких без бактериовыделения: удельный вес случаев с успешными результатами лечения составляет от 65% до 80% [2, 12]. В отечественной литературе крайне мало работ, посвященных рецидивам туберкулёза МБТ-, зарубежные авторы рассматривают такие процессы чаще всего только с позиции ко-инфекции с ВИЧ/СПИД [11], клиническая картина процессов без сопутствующего иммунодефицита в настоящее время освещена недостаточно. Учитывая все вышеизложенное, изучение особенностей клинической картины и результатов лечения рецидивов туберкулёза без бактериовыделения позволит повысить эффективность лечения таких пациентов и предупредить развитие форм с наличием МБТ+ в мокроте.
Цель исследования: изучить разницу в клинической картине и результатах лечения рецидивов туберкулёза легких с бактериовыделением и без бакте-риовыделения.
Материалы и методы. Было проведено ретроспективное исследование среди 156 пациентов, которые получали лечение по поводу рецидива туберкулёза лёгких. Все исследуемые были разделены на 2 группы. 1 группу составили пациенты с бактериовыделением (n=80), 2 группа — пациенты без бакте-риовыделения (n=76). Все пациенты были обследованы следующим образом: изучение анамнестических данных; осмотр и физикальное обследование; рентгенологическое обследование; клинический анализ крови, общий анализ мочи, биохомическое исследование крови с определением билирубина, АлАТ, АсАТ, сахара крови, остаточного азота, креатинина, мочевины; исследование мокроты на M. tuberculosis методом микроскопии мазка по Циль-Нильсену,
методом посева на плотную питательную среду Ле-венштейна-Йенсена, определение чувствительности МБТ к противотуберкулёзным препаратам методом посева на питательную среду Левенштейна-Йенсена (методика регламентирована Приказом МОЗ Украины №45 от 06 февраля 2002 г.), электрокардиография, спирография. Все обследования проводились в начале лечения, в конце интенсивной фазы, перед выпиской из стационара.
Для статистической обработки данных использовался метод доверительных интервалов, t-критерий Стьюдента, метод углового преобразования Фишера, определялось стандартное отклонение.
Результаты и обсуждение. В структуре пациентов с бактериовыделением преобладали пациенты с массивным выделением МБТ (n=44, 55%, CI=35,8…57,1). Количество бактериовыде-лителей, которые были подтверждены только методом посева на среду Левенштейна-Йенсена, было 1/3 всех пациентов 1 группы (n=27, 33,8%, CI=24,3…44,7 ). У пациентов 2 группы выделение МБТ отсутствовало по результатам бактериоско-пического исследования мокроты по Циль-Ниль-сену и посева на среду Левенштейна-Йенсена.
Из 80 обследованных 1 группы 18,7% (n=15) тест медикаментозной чувствительности не проводился, у 6,3% (n=5) чувствительность к противотуберкулёзным препаратам сохранена, пациентов с разным уровнем резистентности было 75% (n=60, 75%, CI=64,5.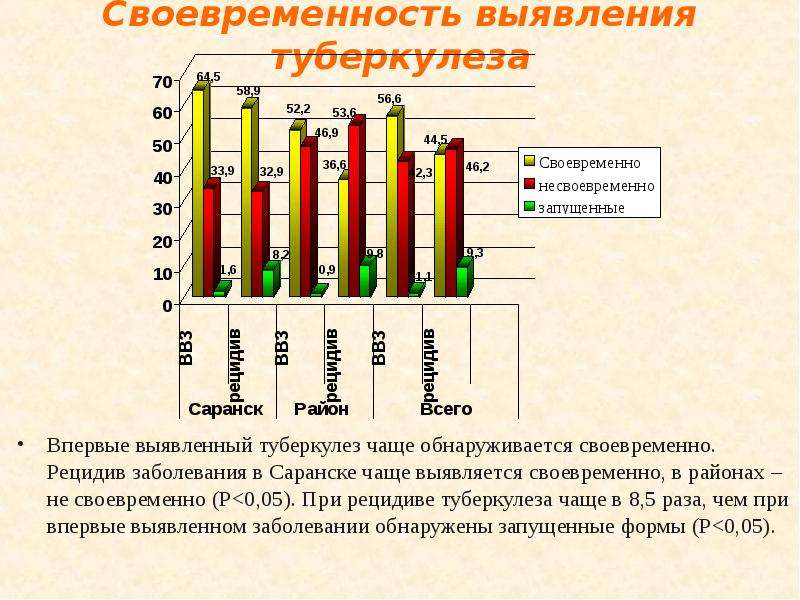 ..83,3). Распределение по видам резистентности среди пациентов 1 группы: монорезистентность — 8,8%, (CI=4,0…17,2), полирезистентность — 31%, (CI=14,7…32,9), мультирезистентность — 36,2%, (CI=17,8…36,9), расширенная резистентность — 20,8% (CI=8,6…24,6). Таким образом, более чем у половины пациентов с рецидивом туберкулёза легких уже в начале лечения имелась устойчивость к противотуберкулёзным препаратам 1 ряда, чаще это самые эффективные: стрептомицин у 83,3%, изони-азид — 80%, рифампицин — 58,3%, этамбутол — 40%.
..83,3). Распределение по видам резистентности среди пациентов 1 группы: монорезистентность — 8,8%, (CI=4,0…17,2), полирезистентность — 31%, (CI=14,7…32,9), мультирезистентность — 36,2%, (CI=17,8…36,9), расширенная резистентность — 20,8% (CI=8,6…24,6). Таким образом, более чем у половины пациентов с рецидивом туберкулёза легких уже в начале лечения имелась устойчивость к противотуберкулёзным препаратам 1 ряда, чаще это самые эффективные: стрептомицин у 83,3%, изони-азид — 80%, рифампицин — 58,3%, этамбутол — 40%.
По форме процесса в обеих группах у преобладающего большинства пациентов имел место инфильтративный туберкулёз: в 1 группе у 77,5% (n=62, CI=67,1…85,4), во 2 группе у 88,2% (n=67, 0=78,8…93,9), статистического различия между группами нет (p>0,05).
По локализации процесса группы не различались (p>0,05). Правое легкое было поражено больше: 43,7% и 44,7% в 1 и 2 группах, соответственно. Поражение обоих легких встречается в 23,8% случаев (n=19) 1 группы и 15,8% случаев (n=12) 2 группы.
В 1 группе количество пациентов с деструк-
104 Журнал Гродненского государственного медицинского университета № 3, 2014 г.
Оригинальные исслсдоини
цией легочной ткани составило 82,5% (n=66, Cl= 72,6…89,4), во 2 группе лишь 39,5% (n=30, CI=29,2…50,7), разница достоверная (р<0,05). Для оценки размера все полости распада были разделены на малые ( до 2 см в диаметре), середние (2-5 см), большие ( 5-7см) и гигантские (больше 7 см). Установлено, что у пациентов 1 группы деструктивные процессы представлены шире: имели место большие размеры полостей и большее их количество у 1 пациента (до 5 полостей), тогда как у пациентов 2 группы максимальное количество полостей составило 2, к тому же размер варьировал от малого к среднему, гигантские и большие полости у пациентов второй группы отсуствовали. При анализе жалоб пациентов
При анализе жалоб пациентов
1 и 2 групп было установлено, что при выявлении рецидива процесса у пациентов 1 группы жалобы наблюдались в 63,8% случаев (n=51, CI=52,8…73,5), тогда как у пациентов 2 группы только в 34,2% (n=26, CI=24,5…45,4), разница между группами достоверна (p<0,05). Среди жалоб при выявлении у пациентов 1 группы доминировали: кашель с мокротой, субфебрильная температура, одышка, слабость. Сопутствующие заболевания были выявлены у половины пациентов 1 группы (n=37, 46,3%, CI=35,8…57,1) и только в 18,4% (n=14, Cl=11,18…28,7) у пациентов с рецидивом туберкулёза легких без бактериовыделения, разница между группами достоверна (р<0,05). Доминирующую позицию занимали пациенты с алкоголизмом, сахарным диабетом.
Средние сроки пребывания пациента в стационаре в 1 группе составляли (учитывая то, что пациенты, переведенные с неэффективным лечением в кат. 4 продолжали лечение в стационаре) 5,6±3,6 мес., для 2 группы средние сроки составляли- 3,3±1,7 мес., разница между группами достоверна (p<0,05).
На момент выписки из стационара прекращение бактериовыделения по мазку мокроты в 1 группе наблюдалось у 68,8% пациентов, тогда как во
2 группе у 4 человек (3,9%) наблюдалось появление бактериовыделения в конце интенсивной фазы.
Инфильтративные изменения уменьшились в 1 группе в 66,3% случаев в среднем за 5,5 месяцев, во 2 группе — в 63,1% случаев за 3 месяца, 1\4 пациентов в 1 группе и 1\5 — во 2 группе были выписаны из стационара без изменений со стороны инфильтрации, статистически достоверной разницы между группами не было (p>0,05), деструктивные изменения исчезли у 36,7% пациентов во 2 группе и только у 16,7% в 1 группе, без изменений в данной категории было около половины пациентов 1 группы и 1\4 2 группы, разница между группами статистически достоверная (p<0,05).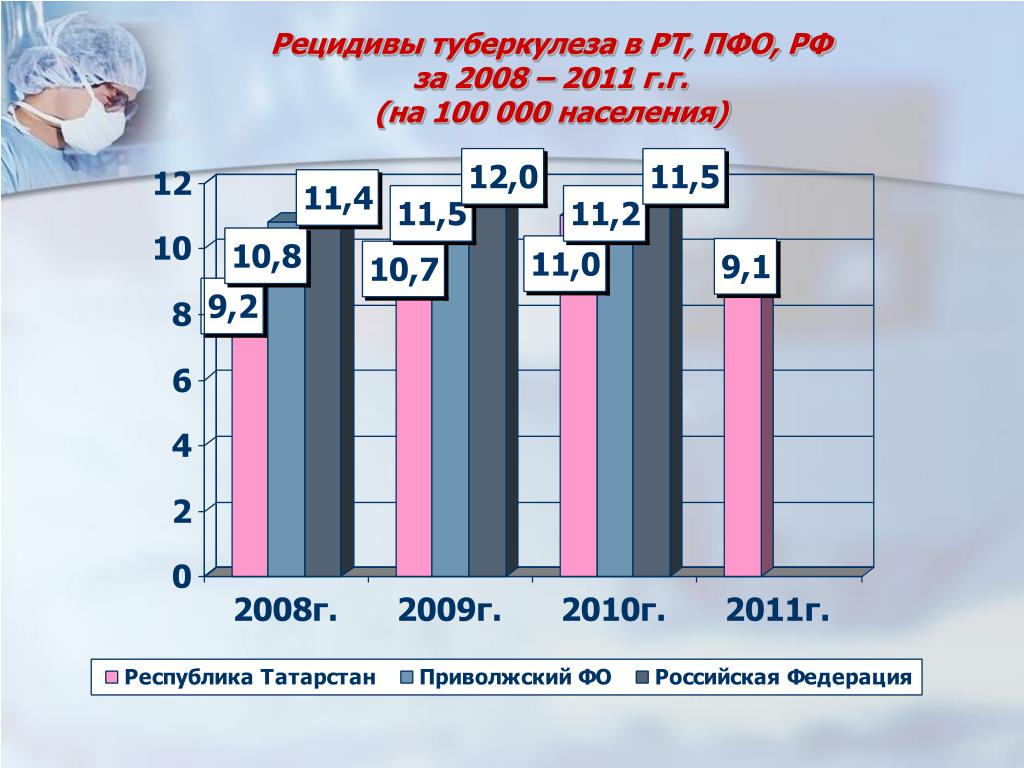
На момент выписки клинические проявления исчезли у большинства пациентов 1 группы (58,7%) и 2 группы (78,9%), но в 1 группе у 15% данный показатель остался неизменным по сравнению с началом лечения, разница между группами достоверна (p<0,05).
Оценка результатов лечения по когортному анализу проводилась согласно Приказу МОЗ Украины № 1091 от 21.12.12, и осуществлялась в конце курса лечения.
Сравнение результатов когортного анализа проводилось по суммам положительных («лечение завер-шено+ излечено») и отрицательных («лечение прер-вано+ неудача лечения+умер») результатов лечения Так, в 1 группе количество пациентов с положительными результатами лечения составило 38,8%, тогда как во 2 группе — 68,4%, разница между группами достоверна (p<0,05). Во 2 группе к концу интенсивной
Таблица 1 — Результаты лечения на момент выписки больного из стационара
Показатель Результат 1CTMU и-и 1 1 [>уИ1Ы 2 группа
збс’слнос. количество .% Средина сровн. жес. □оо’относ. количеств о,% С реяние сроки, мес. Р
Мазок аоьротыпо Цжть- Нильсвну* прекращение 42-68гВ% 4?б±3,1
уменьшение Ъ33% «±1.4 » ■
продолжение 1616?% —
появление 3 — —
Культура по ТТотШЦ 1 ITI ifcuuy -Нансену* преьрашенне 32\4(fii 5,0±3,3 — —
уменьшение 5Ч6:ЗГп 2,5±1,1> — —
продолжение 42У52.53* 4±2,4 — —
пгиштпэттст-а 3 4 3. ti 3:9/3,1 2,1\0:9
ti 3:9/3,1 2,1\0:9
Примечания: *за 100% в каждой группе считалось количество пациентов у которых был анализируемый признак.
Таблица 2 — Результат когортного анализа для 1 и 2 группы
Результат ПС ьатортном у анализу 1 трупа n=S0 2 j руна п=7б
АБс. кд-лнчк тво(п) Относ ИТ. ЕЛ-юЧБ стна (%) □ Абс. ьюлнчес ТБО Относит. количеств oC’i) □
Излечение 31 ЗВ,В 28,В-49,7 и 14,3 Е,1-24,3
Лечение •завершено 41 53,9 42, В-64.7
Лечение inarm 9 1U 5,8-20,2 11 14,5 Е,1-24,3
Неудача ттагаатз-и’з 37 46.3 33.8-37,1 12 15,8 9,1-25,8
Умер 3 3,8 0,8-10,9 1 1:3 0.2-7.1
фазы количество пациентов, у которых появилось бактериовыделение, составляло 4, но к концу основного курса лечения (на момент проведения когортно-го анализа) количество пациентов с неэффективным лечением составляло 12 человек: у 10 пациентов отмечалось бактериовыделение к концу основного курса лечения и 2 чел. были переведены на паллиативное лечение по решению врачебной комиссии в связи с непереносимостью противотуберкулёзных препаратов.
Выводы. В структуре пациентов с МБТ+ преобладали массивные бактериовыделители, что в сочетании с высоким уровнем резистентности среди рецидивов туберкулёза представляет высокую эпидемиологическую опасность и способствует распространению резистентных штаммов M. tuberculosis.
Журнал Гродненского государственного медицинского университета № 3, 2014 г. 105
Оригинальные исследования
Кроме того, у пациентов с бактериовыделением достоверно больше деструктивных процессов с большим размером полостей и большим их количеством. Такие формы значительно сложнее поддаются лечению, об этом свидетельствует низкий уровень положительных результатов лечения у пациентов с рецидивами туберкулёза лёгких с бактериовыделением.
Такие формы значительно сложнее поддаются лечению, об этом свидетельствует низкий уровень положительных результатов лечения у пациентов с рецидивами туберкулёза лёгких с бактериовыделением.
Литература
1. Будрицкий, А.М. Некоторые характеристики больных с рецидивом туберкулёза органов дыхания в Витебской области / А.М. Будрицкий, В.А. Серёгина, И.В. Кучко // Проблемы туберкулёза. — 2011. — №12. — С.32-34.
2. Ильина, Т.Я. Абациллярные рецидивы туберкулёза органов дыхания / Т.Я. Ильина, А.А. Жигарев, О.А. Сидоренко // Туберкулёз и болезни лёгких. — 2004. — №2. -С.33-35.
3. Копылова, И.Ф. Исходы туберкулёза лёгких у больных без бактериовыделения (по данным микроскопии мокроты) / И.Ф. Копылова, Л.А. Ломова // Туберкулёз и болезни лёгких. — 2009. — №9. — С.12-15.
4. Петренко, В.М. Оцшка результата лжування хворих на вперше д1агностований туберкульоз легень та з рецидивами захворювання за показниками когортного аналгзу/ В.М. Петренко, С.О. Черенько, Н.А. Литвиненко, Л.М. Циганкова // Украшський пульмонолопчний журнал. -2011. — №3. — С.5-10.
5. Петренко, В.М. Проблеми рецидив1в туберкульозу легень/ Петренко В.М., Черенько С.О., Литвиненко Н.А., Сенько Ю.О. // Укр. пульмонол. журн. — 2008. — №2. — С.60-64.
6. Плиева, С.Л. Особенности ранних и поздних рецидивов туберкулёза органов дыхания./ Плиева С.Л., Сельцовский П.П. // Туберкулёз и болезни лёгких. — 2011.
— №6. — С.23-27.
7. Рукосуева, О.В. Клинические и микробиологические особенности рецидивов туберкулёза органов дыхания /
O. В. Рукосуева, И.А. Васильева, В.А. Пузанов // Проблемы туберкулёза. — 2008. — №10. — С.28-31.
В. Рукосуева, И.А. Васильева, В.А. Пузанов // Проблемы туберкулёза. — 2008. — №10. — С.28-31.
8. Сливка В.1. Ефектившсть лжування хворих з рецидивами деструктивного туберкульозу з невщомою чутливгстю збудника до антимжобактер1альних препарата/ В.1. Сливка, В.П. Шаповалов, В.О. Степаненко, Б.1. Квасницький // Клшчна та експериментальна патолопя. — 2009. — Т.8. — №1.
— С.80-84.
9. Dobler C.C. Recurrence of tuberculosis in a low-incidence setting / C.C. Dobler, A.B.H. Crawford, P.J. // Eur. Respir J.- 2009.-№33.- P.150-167.
10. Harries A.D. High early death rate in tuberculosis patients in Malawi./A.D. Harries, N.J.Hargreaves // International journal tuberculosis lung dis. — 2001. — № 5(11). — P.1000-1005.
11. Salaniponi F.M. Characteristics, management and outcome of patients with recurrent tuberculosis under routine programme conditions in Malawi / F.M. Salaniponi, T.E. Nyirenda, J.R. Kemp //International journal tuberculosis lung dis. — 2003. — №7(10). — P.948-952.
12. Sevim T. Treatment outcome of relapse and defaulter pulmonary tuberculosis patients / T. Sevim, G. Atac, G. Gungor // International journal tuberculosis lung dis. — №6(4). — 2002.-
P. 320-325.
Таким образом, экономически и эпидемиологически более выгодно своевременно выявлять и лечить рецидивы туберкулёза лёгких без бактериовыделения, что возможно при условии дальнейшего исследования причин, клинической картины и условий возникновения рецидивов туберкулёза легких МБТ+ и МБТ-.
Literatura
1. Budrickij, A.M. Nekotorye harakteristiki bol’nyh s recidivom tuberkuljoza organov dyhanija v Vitebskoj oblasti/ A.M. Budrickij, V.A. Serjogina, I.V. Kuchko // Problemy tuberkuljoza.-2011.-№12.-S.32-34.
Budrickij, A.M. Nekotorye harakteristiki bol’nyh s recidivom tuberkuljoza organov dyhanija v Vitebskoj oblasti/ A.M. Budrickij, V.A. Serjogina, I.V. Kuchko // Problemy tuberkuljoza.-2011.-№12.-S.32-34.
2. Il’ina, T.Ja. Abacilljarnye recidivy tuberkuljoza organov dyhanija / T.Ja.Il’ina, A.A. Zhigarev, O.A. Sidorenko// Tuberkuljoz i bolezni ljogkih. -2004.- №2.- S.33-35.
3. Kopylova, I.F. Ishody tuberkuljoza ljogkih u bol’nyh bez bakteriovydelenija (po dannym mikroskopii mokroty)/I.F. Kopylova, L.A. Lomova // Tuberkuljoz i bolezni ljogkih.-2009. — №9. — S.12-15.
4. Petrenko, V.M. Ocinka rezul’tativ likuvannja hvorih na vpershe diagnostovanij tuberkul’oz legen’ ta z recidivami zahvorjuvannja za pokaznikami kogortnogo analizu/ V.M. Petrenko, S.O. Cheren’ko, N.A. Litvinenko, L.M. Cigankova // Ukrains’kij pul’monologichnij zhurnal. — 2011. — №3. — S.5-10.
5. Petrenko, V.M. Problemi recidiviv tuberkul’ozu legen’/ Petrenko V.M., Cheren’ko S.O., Litvinenko N.A., Sen’ko Ju.O. // Ukr. pul’monol. zhurn. — 2008. -№2. — S.60- 64.
6. Plieva, S.L Osobennosti rannih i pozdnih recidivov tuberkuljoza organov dyhanija / Plieva S.L., Sel’covskij P.P. // Tuberkuljoz i bolezni ljogkih. — 2011. — №6. — S.23-27.
7. Rukosueva, O.V. Klinicheskie i mikrobiologicheskie osobennosti recidivov tuberkuljoza organov dyhanija /
O. V. Rukosueva, I.A. Vasil’eva, V.A. Puzanov // Problemy tuberkuljoza. — 2008. — №10. — S.28-31.
8. Slivka V.I. Efektivnist’ likuvannja hvorih z recidivami destruktivnogo tuberkul’ozu z nevidomoju chutlivistju zbudnika do antimikobakterial’nih preparativ / V. I. Slivka, V.P. Shapovalov, V.O. Stepanenko, B.I. Kvasnic’kij // Klinichna ta eksperimental’na patologija. — 2009. — T.8. — №1.- S.80-84.
I. Slivka, V.P. Shapovalov, V.O. Stepanenko, B.I. Kvasnic’kij // Klinichna ta eksperimental’na patologija. — 2009. — T.8. — №1.- S.80-84.
9. Dobler C.C. Recurrence of tuberculosis in a low-incidence setting / C.C. Dobler, A.B.H. Crawford, P.J. // Eur. Respir J. — 2009. — №33.- P.150-167.
10. Harries A.D. High early death rate in tuberculosis patients in Malawi /A.D. Harries, N.J.Hargreaves // International journal tuberculosis lung dis. — 2001. — № 5(11). — P.1000-1005.
11. Salaniponi F.M. Characteristics, management and outcome of patients with recurrent tuberculosis under routine programme conditions in Malawi./ F.M. Salaniponi, T.E. Nyirenda, J.R. Kemp //International journal tuberculosis lung dis. — 2003. — №7(10). — P.948-952.
12. Sevim T. Treatment outcome of relapse and defaulter pulmonary tuberculosis patients / T. Sevim, G. Atac, G. Gungor // International journal tuberculosis lung dis. — №6(4). — 2002.-
P. 320-325.
106 Журнал Гродненского государственного медицинского университета № 3, 2014 г.
Оригинальные исследования
TREATMENT OUTCOMES OF PULMONARY TUBERCULOSIS RELAPSES
Pustovoy Yu. G., Grib E . Yu., Manokhina O . Yu.
Educational Establishment «Lugansk State Medical University», Lugansk
Comparison of pulmonary tuberculosis clinical picture and treatment outcomes of relapses was the purpose of the investigation. 156 patients with pulmonary tuberculosis relapse were examined. Clinical picture of smear-positive relapses was more severe than in case of smear-negative relapses: a lot of concomitant diseases, lung tissue disintegration, high level of drug resistance. The total number of treatment positive results of smear-negative relapses was 68%, and that of smearpositive relapses only 39%. Thus it is more economically and epidemiologically profitable to detect and treat pulmonary tuberculosis with smear-negative relapses.
Clinical picture of smear-positive relapses was more severe than in case of smear-negative relapses: a lot of concomitant diseases, lung tissue disintegration, high level of drug resistance. The total number of treatment positive results of smear-negative relapses was 68%, and that of smearpositive relapses only 39%. Thus it is more economically and epidemiologically profitable to detect and treat pulmonary tuberculosis with smear-negative relapses.
Key words: relapse of pulmonary tuberculosis, clinical picture, treatment outcomes.
Адрес для корреспонденции: е-mail: [email protected]
Поступила 25.05.2014
Журнал Гродненского государственного медицинского университета № 3, 2014 г. 107
Причины рецидивов у больных туберкулезом легких в Ивановской области
1. Агзамова, Р.А. Факторы риска рецидивов туберкулёза / Р.А. Агзамова // III (XII) съезд врачей-фтизиатров. Екатеринбург,!997. — С.24.
2. Агзамова, Р.А. Пути снижения туберкулёзной эндемии на эпидемиологически и эпизоотически неблагополучных территориях / Р.А. Агзамова: Автореф. дис. . д-ра.мед.наук. Алматы, 1997. — С.45.
3. Азаматова, М.М. Рецидивы туберкулёза в республике Башкортостан / М.М. Азаматова, Х.К. Аминев, Л.З. Фаттахова, Г.М. Сидоренко // Туберкулёз в России: материалы VIII Российского съезда фтизиатров. -М., 2007. С.5.
4. Алексеева, Т.В. Клинико-эпидемиологическая характеристика и совершенствование своевременного выявления рецидивов туберкулёза органов дыхания в современных условиях / Т.В. Алексеева: Автореф. дис. .канд.мед.наук. Новосибирск, 2001. — С.24.
5. Алексеева, Т.В. Новые подходы к своевременному выявлению рецидивов туберкулёза органов дыхания / Т.В. Алексеева // Пробл. туб.- 2003. №2. — С.14-16.
№2. — С.14-16.
6. Анастасьев, B.C. Причины рецидивов туберкулёза лёгких / B.C. Анастасьев // Пробл. туб.-1985. №2. — С.14-18.
7. Андреева, Т.Н. Рецидивы туберкулёза органов дыхания / Т.Н. Андреева, М.Н. Кириллов // Туберкулёз сегодня: материалы VII Российского съезда фтизиатров. М., 2003. — С.6.
8. Березовский, Б.А. Влияние социальных факторов на заболеваемость туберкулёзом / Б.А. Березовский, Г.Ю. Солобай, В.В. Марчак, В.А. Кучер, В.У. Василюк, Л.В. Михей // Пробл. туб.-1991. №12. — С.3-5.
9. Бирон, М.Г. Характер и значение посттуберкулёзных изменений у больных некоторыми общесоматическими заболеваниями / М.Г. Бирон: Автореф. дис. . .канд. мед. наук. М, 1988. — С.22.
10. Бобарыкин, B.C. Отдалённые результаты лечения больных очаговым туберкулёзом / B.C. Бобарыкин // III Съезд врачей-фтизиатров. -Екатеринбург, 1997. С.24-25.
11. Богородская, Е.М. Проблемы формирования эпидемиологических показателей по туберкулезу / Е.М. Богородская, С.А. Стерликов, С.А. Попов // Пробл. туб.- 2008. №7. — С.3-6.
12. Босенко, Т.Я. Особенности рецидивов туберкулёза органов дыхания в современных условиях / Т.Я. Босенко, Е.А. Горяинова, И.О. Дубовицкая, Н.А. Володько // Туберкулёз в России: материалы VIII Российского съезда фтизиатров. М., 2007. — С.14-15.
13. Бубочкин, Б.Н. Экономический кризис в обществе как причина реверсии туберкулеза / Б.Н. Бубочкин, П.Н. Новоселов // Тезисы докладов 4 съезда научно-медицинской ассоциации фтизиатров. М.-Йошкар-Ола, 1999.- С.1
14. Бурухина, JI.B. Причины рецидивов туберкулеза легких, ближайшие и отдаленные результаты лечения / JI.B. Бурухина, Е.А. Золотовская, З.А. Прудникова, А.Н. Вершинин, Н.П. Колмакова // Пробл. туб.-1995.-№3.-С.29-31.
15. Буткене, П.П. К вопросу о причинах рецидива туберкулёза у лиц VII А группы диспансерного учета / Буткене П.П. // Актуальные вопросы эпидемиологии и клиники туберкулёза и других заболеваний лёгких: тез. докл. Вильнюс, 1988 — №1. — С.69-71.
16. Василенко, Т. И. Анализ причин обострений и рецидивов туберкулёза органов дыхания. / Т.И. Василенко, B.C. Одинец, В.И. Жукова //
И. Анализ причин обострений и рецидивов туберкулёза органов дыхания. / Т.И. Василенко, B.C. Одинец, В.И. Жукова //
17. Тезисы докладов 4 съезда научно-медицинской ассоциации фтизиатров. М — Йошкар-Ола, 1999. — С.168.
18. Васильев, А.В. Современные проблемы туберкулёза в регионе Северо-запада России / А.В. Васильев // Пробл. туб.- 1999. №3. — С.3-5.
19. Визель, А.А. Туберкулез / А.А. Визель, М.Э. Гурылева Издательство Гоэтар. Медицина. Москва,1999.
20. Волковинская, JI.C. Роль социально-гигиенических факторов в возникновении туберкулёза органов дыхания и развитии его рецидивов/ JI.C. Волковинская: Дис.канд.мед.наук. -М.,1990.
21. Волошина, Е.П. Совершенствование формирования диспансерных контингентов с излеченным туберкулёзом лёгких у взрослых и наблюдения за ними / Е.П. Волошина: Автореф. дис. .канд.мед.наук. -МД991.-С.24.
22. Вязкова, Н.Н. Значение динамического диспансерного наблюдения для предупреждения развития рецидива туберкулёза органов дыхания из III группы диспансерного учёта / Н.Н. Вязкова: Автореф. дис. . канд. мед. наук. М., 2008. — 28 с.
23. Гавриленко, B.C. Частота и сроки возникновения рецидива туберкулёза органов дыхания у взрослых / B.C. Гавриленко // Пробл. туб.- 1993. -№2. С.10-13.
24. Гавриленко, B.C. Современные аспекты рецидива туберкулёза органов дыхания у взрослых / B.C. Гавриленко, Т.С. Хрулёва // Пробл. туб.-1996. №4. — С.2-4.
25. Гиллер, Б.М. Повторные и этапные операции в лечении послеоперационных рецидивов туберкулёза лёгких / Б.М. Гиллер, Д.Б. Гиллер, Т.В. Гиллер // Тезисы докладов 4 съезда научно-медицинской ассоциации фтизиатров. Москва — Йошкар-Ола, 1999. — С.594.
26. Голубчиков, П.Н. Анализ рецидивов у больных туберкулёзом, пролеченных по протоколам ВОЗ / П.Н. Голубчиков, А.К. Стрелис,
27. B.Т. Голубчикова, Г.В. Янова // Туберкулёз сегодня: Материалы VII российского съезда фтизиатров. — М., 2003. С.11.
28. Григорьев, Ю.Г. Лечение хронического лёгочного сердца у больных туберкулёзом лёгких / Ю. Г. Григорьев // Тезисы докладов IV съезда научно-медицинской ассоциации фтизиатров. Москва-Иошкар-Ола, 1999.-С.200.
Г. Григорьев // Тезисы докладов IV съезда научно-медицинской ассоциации фтизиатров. Москва-Иошкар-Ола, 1999.-С.200.
29. Давыдовский, И.В. Патологическая анатомия и патогенез болезней.-Л., 1938. -189 с.
30. Державин, В.И. Некоторые аспекты реактивации туберкулёзного процесса. Кишинев, 1981. — С.33-39.
31. Державин, В.И. Усовершенствование диспансеризации и химиопрофилактики лиц повышенного риса рецидива и заболевания туберкулёзом лёгких / В.И. Державин: Автореф. дис. канд.мед.наук. -МД983.-24 с.
32. Дорожкова, И.Р. Формы персистирования микобактерий туберкулёза в организме человека / И.Р. Дорожкова: Автореф. дис. . .д-ра мед.наук. -М.,1974.
33. Дорожкова, И.Р. Эндогенная реактивация туберкулеза как результат реверсии персистирующих L-форм микобактерий / И.Р. Дорожкова, З.С. Земскова, В.Н. Круду, Е.Я. Кочеткова // Пробл. туб.-1995.- №3.1. C.43-45.
34. Дорошенкова, А.Е. К проблеме патогенеза и диагностики рецидива туберкулёза лёгких после хирургического и антибактериального лечения / А.Е. Дорошенкова // II съезд врачей фтизиатров. Саратов, 1994.-С.176.
35. Елькин, А.В. Хирургическое лечение послеоперационных рецидивов туберкулёза лёгких / А.В. Елькин, Ю.М. Репин // Тезисы докладов 4 съезда научно-медицинской ассоциации фтизиатров. М. — Йошкар-Ола, 1999.-С.602.
36. Елькин, А.В. Функция внешнего дыхания и капиллярный лёгочный кровоток у больных с послеоперационными рецидивами туберкулёза лёгких / А.В. Елькин, И.Б. Савин // Пробл. туб.- 1999. №3. — С. 16-19.
37. Елькин, А.В. Послеоперационные рецидивы туберкулёза лёгких: факторы риска, хирургическое лечение / А.В. Елькин: Дис. .д-ра.мед.наук. СПб, 2000.
38. Елькин, А.В. Отдалённые результаты хирургического лечения туберкулёза лёгких в зависимости от массивности бактериовыделения и лекарственной устойчивости возбудителя / А.В Елькин., Ю.М. Репин, Ю.Н. Левашев // Пробл. туб. 2003. — №5. — С28-31.
39. Ерохин, В.В. Морфологические признаки недостаточно эффективной химиотерапии экспериментального деструктивного туберкулёза лёгких / В. В. Ерохин // Пробл. туб. 1998. — №3. — С.61-66.
В. Ерохин // Пробл. туб. 1998. — №3. — С.61-66.
40. Ерохин, В.В. Актуальные проблемы организации борьбы с туберкулёзом в России / В.В. Ерохин // Материалы научной сессии, посвящённой 85-летию ЦНИИТ РАМН. М. — 2006. — С. 13-14.
41. Ерохин, В.В. Казеозная пневмония / В.В. Ерохин, В.Ю. Мишин, В.И. Чуканов, Д.Б. Гиллер М.,2008. — 192 с.
42. Жестовских, С.Н. Диагностика и течение рецидивов туберкулёза органов дыхания в период напряжённой эпидемической ситуации / С.Н. Жестовских: Дис. .канд. мед. наук. -М,- 2002.
43. Жестовских, С.Н. Особенности течения современных рецидивов туберкулёза лёгких / С.Н. Жестовских //Туберкулёз сегодня: Материалы VII российского съезда фтизиатров. М., 2003. — С. 127.
44. Жестовских, С.Н. Рецидив туберкулёза лёгких в период напряженной эпидемической ситуации / С.Н. Жестовских // Туберкулёз сегодня: Материалы VII российского съезда фтизиатров. — М., 2003. С.14.
45. Жукова, М.П. Основные источники формирования контингентов у больных туберкулёзом, выделяющих лекарственно-устойчивые и чувствительные микобактерии туберкулёза. ЦНИИТ / М.П. Жукова // Пробл. туб.- 1998. №4. — С.4-5.
46. Завалев, В.И. Пути повышения эффективности методов выявления туберкулёза в современных социально-экономических условиях / В.И. Завалев: Автореф. дис. .канд.мед наук. — М.,2000. — 30 с.
47. Закопайло, Г.Г. О причинах рецидива туберкулеза легких / Г.Г. Закопайло, A.M. Хошаба, В.Н. Примаковский, С.Н. Реган // Пробл. туб. 1991.- №8.- С.74-75.
48. Занкисова, И.Г. Характеристика обострений туберкулёза / И.Г. Занкисова: Дис. .канд.мед.наук. Москва, 1961.
49. Земскова, З.С. Скрыто протекающая туберкулёзная инфекция / З.С. Земскова, И.Р. Дорожкова. М.,1984.
50. Иванов, Е.А. Рецидивы туберкулёза лёгких у взрослых в улусах Якутии за последние 12 лет / Е.А. Иванов, О.Н. Максимова, Р.В. Попова // Пробл. туб. 1997. — №2. — С.5-8.
51. Ильина Т. Я., Курманбаев К.К., Головенко JI.C. Циррозы лёгких. — Алма-Аты, 1992.
52. Ильина, Т.Я. Резистентность микобактерий туберкулёза у впервые выявленных больных и при рецидивах заболевания / Т.Я Ильина, А.А. Жангиреев // Пробл. туб.- 2003. №5. — С. 19-21.
53. Ильина, Т.Я. Абациллярные рецидивы туберкулёза органов дыхания / Т.Я. Ильина, А.А. Жангиреев, О.А. Сидоренко // Пробл. туб. 2004. -№2. — С.33-35.
54. Ильина, Т.Я. Распространённость рецидивов туберкулёза органов дыхания при напряженной эпидемической ситуации / Т.Я. Ильина, А.А. Жангиреев // Пробл. туб. 2005. — №7.- С. 15-17.
55. Ильина, Т. Я. Особенности бактериовыделения и чувствительности микобактерий туберкулеза к химиопрепаратам у больных с рецидивами туберкулеза легких / Т. Я. Ильина, А. А. Жангиреев, О. А. Сидоренко // Пробл. туб. 2008. — №5. С 34-36.
56. Ильичёва, Е.Ю. Усовершенствование системы организации противотуберкулёзной помощи в современных социально-экономических условиях / Е.Ю.Ильичёва: Автореф. дис. .канд.мед.наук, 1996.-С. 18.
57. Какорина, Е.П. Социально-гигиенические особенности состояния здоровья населения в современных условиях / Е.П. Какорина // Проблемы социальной гигиены, здравоохранения и истории медицины. М., 2000. -№2. -С.12 -16.
58. Канетти, Г. Эндогенная реактивация и экзогенная реинфекция; их относительное значение в развитии непервичного туберкулёза / Г. Канетти // Труды XXI Международной конференции по туберкулёзу. -М., 1972. С.171-175.
59. Карабач, С.С. Поздние рецидивы туберкулёза органов дыхания / С.С. Карабач: Дис. .канд.мед.наук. Вильнюс, 1989. — 179 с.
60. Капков, Л.П. Значение показателей резервуара бациллярных больных туберкулёзом органов дыхания в оценке эпидемической ситуации по туберкулёзу / Капков Л.П. // Пробл. туб. 2007. — №1. — С. 17-22.
61. Карпов, А.В. Экономическая целесообразность и медицинская эффективность методов активного выявления туберкулёза / А.В. Карпов // Проблемы туберкулёза, 2000. №2. — С.3-5.
62. Кибрик, Б.С. К дискуссии «О группировке контингентов, обслуживаемых противотуберкулёзными диспансерными учреждениями» / Б. С. Кибрик, Е.О. Соловьев, Т.С. Шаброва // Пробл. туб. 1993.- №3.- С.-33-34.
С. Кибрик, Е.О. Соловьев, Т.С. Шаброва // Пробл. туб. 1993.- №3.- С.-33-34.
63. Кибрик, Б.С. Некоторые особенности современной клиники казеозной пневмонии / Б.С. Кибрик, О.Г. Челнокова // Пробл. туб. 1999. — №2. -С.5.
64. Ковалев, Г.К. О структуре рецидивов туберкулёза лёгких у лиц, находящихся в исправительно-трудовых учреждениях / Г.К. Ковалев // Пробл. туб. 1994. — №2. — С.56-57.
65. Ковалёва, С.И. Отдалённые результаты диспансерного наблюдения за впервые выявленными больными деструктивным туберкулёзом лёгких ЦНИИТ / С.И. Ковалёва, В.П. Колосовская, Е.П. Волошина- // Пробл. туб. 1995.-№3.-С.34-36.
66. Ковалёва С.И., Волошина Е.П., Шмакова Л.Н. Пробл. туб. 1996. — №6. — С.25-27.
67. Коваленко И.П. Реактивации туберкулеза легких. Кишинев. «Штиинца», 1989.
68. Колмаков, Н.М. Основные причины реактиваций и рцидивов туберкулёза в оперированном лёгком / Н.М. Колмаков, Г.А. Кавандина, О.В. Кузьмин // Туберкулёз сегодня: Материалы VII российского съезда фтизиатров. М., 2003. — С.280.
69. Колендо, С.Е. Некоторые аспекты диагностики туберкулёза лёгких в многопрофильной больнице / С.Е. Колендо, Ю.А. Антошина, Л.И. Дворецкий // Пульмонология, 2000. №1. — С.35-41.
70. Коломиец В.М. Реактивация туберкулёза лёгких и её профилактика при формировании групп повышенного риска / В.М. Коломиец: Автореф. дис. . .д-ра.мед.наук. Киев, 1982. — С.28.
71. Комисарова, О.Г. Особенности течения процесса и эффективность лечения рецидивов туберкулёза лёгких у больных с различным уровнем генерации оксида азота в мононуклеарах и нейтрофилах крови/ О.Г Комисарова: Автореф. дис. .канд.мед.наук. -М,2005. 24 с.
72. Кочеткова, Е.Я. Значение L форм в реактивации туберкулёза у больных пожилого возраста / Е.Я Кочеткова, И.Р. Дорожкова, М.А. Карачунский // Тезисы докладов 4 съезда научно-медицинской ассоциации фтизиатров. — М. — Йошкар-Ола, 1999. — С. 434.
73. Кравченко, О.А. Частота и причины развития рецидивов туберкулёза лёгких / О.А. Кравченко, В.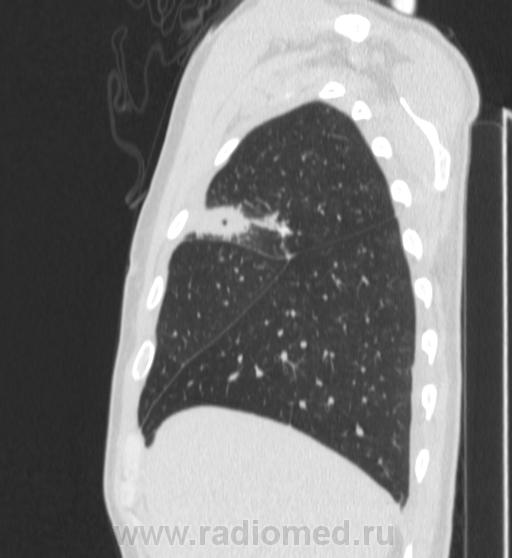 Б. Данилова, Е.Е. Полушнина // Тезисы докладов 4 съезда научно-медицинской ассоциации фтизиатров. Москва Йошкар-Ола, 1999. — С. 184.
Б. Данилова, Е.Е. Полушнина // Тезисы докладов 4 съезда научно-медицинской ассоциации фтизиатров. Москва Йошкар-Ола, 1999. — С. 184.
74. Краснов, В.А. Излечение рецидивов туберкулёза лёгких / В.А. Краснов: Дис. .канд. мед. наук, Новосибирск, 1985.
75. Краснов, В.А. Клиническое течение и исходы рецидива туберкулёза лёгких / В.А. Краснов // Пробл. туб. 1993. — №5. — С. 14-16.
76. Краснов, В.А. Количественная характеристика иммунитета у больных с реактивацией туберкулёза лёгких / В.А. Краснов // Пробл. туб. 1994. -№1. — С.17-19.
77. Краснов, В.А. Хирургическое лечение больных с деструктивными формами туберкулёза лёгких / В.А. Краснов: Дис. .д-ра мед.наук. -Новосибирск, 1994. С.242.
78. Краснов, В. А. Излечение рецидивов туберкулёза легких. -Новосибирск, 1995. 159 с.
79. Круду, В.Н. Характеристика микобактериальной популяции при реактивации процесса у лиц с ОТИ в лёгких / В.Н. Круду: Автореф. дис. . .канд.мед.наук. — М.,1990. — 25 с.
80. Кузнецова, З.А. Частота, клинические особенности и меры предупреждения рецидивов туберкулёза органов дыхания / З.А. Кузнецова: Автореф. дис. .канд.мед.наук. Киев, 1986. — 24 с.
81. Кучеров, A.JI. Туберкулёз среди социально-отягощенных лиц населения / А.Л. Кучеров // Пробл. туб,- 1990. №6. — С.20-23.
82. Лазарева, Я.В. Диагностическое значение носительства посттуберкулёзных кальцинированных внутригрудных аденопатий / Я.В. Лазарева // Клин. Медицина, 1998. №6. — с.48-51.
83. Левин, В.Р. Рецидивы туберкулёза лёгких по диспансерным данным / В.Р. Левин: Дис.канд.мед.наук. -М.,1962.
84. Левин, В.Р. Остаточные изменения при клиническом излечении туберкулёза лёгких и их прогностическое значение в клинико-диспансерной практике / В.Р. Левин: Дис. . .д-ра мед.наук. М., 1971.
85. Литвин, Л.М. Клинико-ренгенологическая характеристика больных с рецидивами туберкулёза лёгких в городских и сельских условиях / Л.М. Литвин // Пробл. туб. 1985. — №1. — С.39-42.
86. Литвинов, В.И. Эпидемическая ситуация и особенности эндемии туберкулёза в Москве / В.И. Литвинов, П.П. Сельцовский, Е.Я. Кочеткова, И.М. Сон, Г.Я. Андрюхина. // Туберкулёз сегодня: Материалы VII российского съезда фтизиатров. М., 2003. — С.20.
Эпидемическая ситуация и особенности эндемии туберкулёза в Москве / В.И. Литвинов, П.П. Сельцовский, Е.Я. Кочеткова, И.М. Сон, Г.Я. Андрюхина. // Туберкулёз сегодня: Материалы VII российского съезда фтизиатров. М., 2003. — С.20.
87. Максимова, О.Н. Особенности развития и течения рецидивов туберкулёза лёгких / О.Н. Максимова: Автореф. дис. .канд.мед.наук. -М., 2004.-22 с.
88. Малиновский, А.Ф. Отдалённые результаты повторного хирургического лечения больных с реактивациями туберкулёза послерезекции лёгких / А.Ф. Малиновский // Значение хирургии в излечении больных туберкулёзом лёгких. МД974. — С.221-224.
89. Мамонтов, О.А. Роль социального статуса впервые выявленного больного туберкулёзом в выборе организационного режима терапии / О.А. Мамонтов, В.Д. Ломаченков // Пробл. туб. 2000. — №2. — С 17-18.
90. Мишин, В.Ю. Диагностика и лечение остропрогрессирующих форм туберкулеза легких в современных условиях / В.Ю. Мишин, В.И. Чуканов // Российский медицинский вестник, 1998.- №4.- С.22-25.
91. Мишин, В.Ю. Казеозная пневмония: диагностика, клиника и лечение / В.Ю. Мишин, В.В. Ерохин, В.И. Чуканов, В.Н. Наумов, Ю.Г. Григорьев, И.А. Васильева // Методическое пособие для врачей. М.,2000.
92. Мишин, В.Ю. Разработка современных протоколов диагностики и лечения туберкулеза органов дыхания /В.Ю. Мишин, С.Е. Борисов, Г.Б. Соколова, И.А. Васильева, И.Р. Дорожкова, С.Г. Сафонова, С.В. Сидорова// Consilium medicum. 2001. -t.3.-№3.-C.148-154.
93. Мишин, В.Ю. Особенности диагностики рецидивов туберкулёза органов дыхания / В.Ю. Мишин, С.Н. Жестовских // Пробл. туб. -2005. №5. — С.39-43.
94. Мишин, В.Ю. Эффективность II Б стандартного режима химиотерапии при лечении больных рецидивами туберкулёза лёгких / О.Г. Комисарова, А.Н. Наумова, А.С. Кононец, Л.И. Голубева, Н.Е. Хорошилов, Т.В. Мякишева, А.И. Садовский, Е.Д. Нагорная, Е.Ю.
95. Шевчук // Туберкулёз в России: материалы VIII Российского съезда фтизиатров. М., 2007. — С.441
96. Мишкинис, К. Результаты лечения полорезистентного туберкулёза по данным республиканской туберкулёзной больницы Сантаришкес / К. Мишкинис, А. Каминскайте, Б. Пурванецкене // Пробл. туб. 2000. -№3. — С. 9-11.
Мишкинис, К. Результаты лечения полорезистентного туберкулёза по данным республиканской туберкулёзной больницы Сантаришкес / К. Мишкинис, А. Каминскайте, Б. Пурванецкене // Пробл. туб. 2000. -№3. — С. 9-11.
97. Муминов, Т.А. Диспансерное наблюдение за больными туберкулёзом органов дыхания и пути его совершенствования / Т.А. Муминов, Т.Я. Ильина, З.Д. Спримбитова, Л.Д. Синявская, Г.К. Алимбекова // Пробл. туб.- 1999. -№4.-С.49-52.
98. Недлинская, Н.Н. Определение степени риска рецидива туберкулёза лёгких и эффективность дифференцированных противотуберкулёзных мероприятий / Н.Н. Недлинская: Дис .канд.мед.наук. — Киев, 1989. — 159с.
99. Незлин С.Е. Противотуберкулёзный диспансер. — М.: Медицина, 1989. -224с.
100. Несис, А.И. Профилактика и своевременная диагностика туберкулёза у «угрожаемых» контингентов / А.И. Несис // Пробл. туб. 1994. — №2. -С.22-23.
101. Нефедов, В.Б. Динамика функции лёгких у больных с рецидивами туберкулёза и неудачами первичного лечения в интенсивную фазу контролируемой схемой химиотерапии / В.Б.Нефедов, Л.А. Попова, Е.А. Шергина//Пробл. туб.-2002.- №12.- С.29-32.
102. Нечаева, О. Б. Рецидивы туберкулёза в Свердловской области / О. Б.Нечаева, Э. В. Арефьева, Н. В. Кожекина // Пробл. туб. 2007. — №1. — С.42.
103. Нечаева, О. Б. Смертность от рецидивов туберкулёза в Свердловской области / О. Б.Нечаева, Э. В. Арефьева, Н. В. Кожекина // Пробл. туб. -2007. №3. — С.42.
104. Остаточные изменения на различных этапах излечения туберкулёза. // Сборник статей под ред. Кочновой И.Е. — Вып.8, 1976.
105. Перельман М.И. Туберкулёз сегодня. Материалы VII российского съезда фтизиатров. — М.: Бином, 2003. -352 с.
106. Петренко, В.М. Причины рецидивов туберкулеза легких у жителей города и села / В.М Петренко, JI.B. Гурченко, С.И. Пархоменко, B.C. Бабарыкин // Пробл. туб. 1990.-№10.- С.47-48.
107. Пироцкий, Н.Н. Характеристика котингентов больных в туберкулёзной клинической больнице №3 им. Г.А. Захарьина / Н.Н. Пироцкий // Проблемы туберкулёза и болезней лёгких, 2000. №1. — С. 12.
108. Приказ Минздрава РФ от 21 марта 2003 г. N109 «О совершенствовании противотуберкулезных мероприятий в Российской Федерации».
109. Рабухин А.Е. Туберкулёз органов дыхания у взрослых. -М. Медицина, 1976.
110. Репик, В.И. Актуальные проблемы туберкулеза органов дыхания: эпидемиология, диагностика, клиника и лечение / Репик, В.И., Чуканов В.И. / Пульмонология, 2000.-№1.- С.70-77.
111. Репин, Ю.М. Повторные органосохраняющие операции при рецидивах туберкулёза лёгких / Ю.М, Репин // Пробл. туб. 1991.-312. — С.27-31.
112. Репин, Ю.М. Отдалённые результаты сложных полисекментарных резекций лёгких по поводу туберкулёза с множественной локализацией / Ю.М. Репин, А.В. Елькин, Т.Ф. Оттен, Т.Б. Рлепянская, М.А. Трофимов // Пробл. туб. 1998. — №6. — С.26-29.
113. Риекстиня, В. Факторы риска ранних рецидивов туберкулёза в Латвии / В. Риекстиня, Л. Торп, В. Леймане // Пробл. туб. 2005. — №1. -Сс.43-46.
114. Рогожина, Н.А. Социально-клинические аспекты рецидивов туберкулёза лёгких / Н.А. Рогожина // Пробл. туб. 1993. — №1. — С.54-55.
115. Рудой, Н.М. Сроки и критерии прекращения основного курса химиотерапии больных туберкулёзом лёгких / Н.М. Рудой // Пробл. туб.- 1981. №12. — С.3-6.
116. Рудой Н.М., Чубаков Т.Ч. Туберкулёз лёгких и алкоголизм. -М.:Медицина, 1985. С. 42-44.
117. Рудой, Н.М. Рецидивы туберкулёза лёгких у больных, страдающих психическими заболеваниями и алкоголизмом / Н.М. Рудой, Т.Ч. Чубаков // Пробл. туб. 1991. — № 10. — С.44-45.
118. Рыбка, Л.Н. Опыт применения лечения по программам DOTS у бездомных и мигрантов, больных туберкулёзом / Л.Н. Рыбка, Л.П. Алексеева, К.М. Атамановская // Тезисы докладов IV съезда научно-медицинской ассоциации фтизиатров. М.- Йошкар-Ола, 1999. — С.87.
119. Рыжанков, А.К., Послеоперационная реактивация туберкулёза легких / А.К. Рыжанков, Н.А. Ким, Л.В. Четырина, И.С. Маруизак, А.А. Тупикин // Пробл. туб.-. 1994. №5. — С.53.
120. Салобай Р.Ю. Результаты наблюдения и эффективность лечения больных с рецидивами туберкулёза лёгких // Национальный конгресс по пульмонологии, 1997. С. 1507.
121. Скачкова, Е.И. Мониторинг рецидивов туберкулёза: причины и факторы, способствующие развитию рецидивов / Е.И. Скачкова, О.Б.Нечаева, Э.В.Арефьева, Н.В. Ясинецкая // Пробл. туб. 2008. — №8.
122. Соловьева А.С. Причины рецидивов туберкулёза лёгких. // Здравоохранение Белоруссии. 1987. — №9. — С.8-10.
123. Сон И.М. Значимость показателя заболеваемости для оценки эпидемиологической ситуации при разных уровнях распространенности туберкулёза.: Дис. .канд.мед.наук. — М. 1998.-с.22.
124. Сон, И.М., Андрюхина Г.Я., Пронина Т.В., Виноходова И.М. Смертность от туберкулёза в Москве в 2002 г. / И.М. Сон, Г.Я. Андрюхина, Т.В. Пронина, И.М. Виноходова // Туберкулёз сегодня: Материалы VII российского съезда фтизиатров. М., 2003. — С.26-27.
125. Струтинский М.И. Деструктивные формы рецидива туберкулёза лёгких у жителей села // Пробл. туб. 1988. — №4. — С.3-4.
126. Тоичкина, Т.В. Эффективность лечения больных с рецидивами туберкулёза / Т.В. Тоичкина, Н.И. Низовцева, А.О. Марьяндышев // Туберкулёз сегодня: Материалы VII российского съезда фтизиатров. — М., 2003.-С.264.
127. Топчиев Ш.Р. Рецидивы туберкулёза лёгких и факторы, способствующие их возникновению // Пробл. туб. 1988. — №11. -С.60-62.
128. Туберкулёз в Российской Федерации. Аналитический обзор основных статистических показателей по туберкулёзу, используемых в РФ. М. -«Триада», 2007. С.31-32.
129. Урсов, И.Г. К вопросу о рецидивах туберкулеза органов дыхания / И.Г. Урсов, О.Г. Леонов // Пробл. туб. 1999.-№2.-С.43.
130. Урсов И.Г. Современные проблемы экзогенных реинфекций человека микобактериями бычьего типа. Новосибирск, 2000. — С.94.
131. Фишер, Ю.Я. Формирование и медико-социальная характеристика контингента больных IA гр. ДУ ПТД / Ю.Я. Фишер, Н.Д.Терехова, И.Н. Мовродин // Пробл. туб. 1998. — №2. — С.4-6.
132. Фридман Д.Я. Влияние отягощающих факторов в реактивации туберкулёза в отдалённые сроки после резекции лёгких: Дис. .канд.мед.наук. -М, 1982. 154 с.
133. Фтизиатрия: Национальное руководство / под. ред. М.И. Перельмана. -М.: ГЭОТАР Медиа, 2007. — С.51-59.
134. Хоменко А.Г. Туберкулез как международная и национальная проблема // Пробл. туб.- 1994.- N 2. С.2-4.
135. Хоменко, А.Г. Эффективность химиотерапии туберкулёза лёгких с лекарственной устойчивостью микобактерий / А.Г. Хоменко,
136. B.И.Чуканов, А.А. Корнеев // Пробл. туб. 1996. — №6. — С.42-44.
137. Хоменко А.Г. Туберкулёз вчера, сегодня и завтра//Пробл. туб. 1997. — №6, — С.9-12.
138. Хоменко А.Г. Современные тенденции распространения туберкулёза в России // Русский медицинский журнал, 1998. Т.6. — №17. — С.1121-1125.
139. Хоменко А.Г. Концепция организации борьбы с туберкулёзом в конце XX и начале XXI века // Тезисы докладов IV съезда научно-медицинской ассоциации фтизиатров. Москва Йошкар-Ола, 1999.1. C.5-6.
140. Хоменко, А. Г. Диагностика, клиника и тактика лечения остропрогрессирующих форм туберкулеза легких в современных эпидемических условиях / А. Г.Хоменко, В. Ю.Мишин, В. И. Чуканов // Пробл. туб. — 1999. — N 1 . — С. 22-27.
141. Хрулёва Т.С. К проблеме рецидивов туберкулёза // Туберкулёз сегодня: проблемы и перспективы Научные труды и материалы конференции, посвященной памяти М.М. Авербаха (к 75-летию со дня рождения). Москва, 2000. С. 222-224.
142. Худушина, Т.А. Лекарственная устойчивость микобактерий туберкулёза у впервые выявленных больных туберкулёзом лёгких / Т.А.Худушина, Е.П.Волошина, Н.В.Адамович, М.Г.Маслакова, Н.Д. Терехова // Пробл. туб. 2005. — №12. — С.37-39.
143. Челнокова, О.Г. Эпидемиология остропрогрессирующего деструктивного туберкулёза лёгких / О.Г.Челнокова, Б.С. Кибрик, Ю.В. Маковей Туберкулёз сегодня: материалы VII Российского съезда фтизиатров. М. — 2003. — С.29.
144. Чуканов, В.И. Лекарственная устойчивость микобактерий туберкулёза проблема современной фтизиатрии / В.И. Чуканов, В.И. Голышевская,
145. A.А. Корнеев, Н.В. Кузьмина // 2 национальный конгресс «Человек и лекарство». Москва. — 1995. — С.251.
146. Чуканов, В.И. Особенности лечения лекарственно-устойчивого туберкулёза лёгких / В.И. Чуканов, В.Ю. Мишин, В.Н. Наумов // Кубанский научный мед. вестник. 2001. — №4(58). — С.23-25.
147. Чуканов, В. И. Эффективность нового стандартного режима химиотерапии при лечении больных с рецидивами туберкулеза легких /
148. B. И.Чуканов, О. Г. Комиссарова, В. Ю. Мишин, Р. Ю. Абдуллаев, А.
149. C. Кононец // Пробл. туб. 2006. — №8.- С.9-13.
150. Шилова М.В. Итоги оказания противотуберкулёзной помощи населению России в 2003г//Пробл. туб 2005. — №6. — С.3-10.
151. Шилова, М.В. Эффективность лечения больных туберкулёзом легких на современном этапе / М.В. Шилова, Т.С. Хрулёва // Пробл. туб -2005. №3. — С.3-11.
152. Шилова М.В. Туберкулез в России в 2007 году. М., 2008. 151с.
153. Шихалиев, Я.Ш. Нетрадиционные методы предупреждения развития рецидива туберкулёза / Шихалиев Я.Ш. // Пробл. туб. 1997. — №3. = С.14-17.
154. Шихалиев, Я.Ш. Рецидивы туберкулёза лёгких и факторы, способствующие их возникновению / Шихалиев Я.Ш. // Тезисы докладов IV съезда научно-медицинской ассоциации фтизиатров. — Москва Йошкар-Ола, 1999. — С.214.
155. Шихалиев, Я.Ш. Совершенствование методов выявления и лечения рецидивов туберкулеза / Я.Ш. Шихалиев: Дис. . д-ра мед. наук. М., 2001.
156. Эйсаев, Б.А. Результаты лечения больных с рецидивами туберкулёза лёгких при различных типах гаптоглобина / Б.А. Эйсаев // Пробл. туб. -1995. №6. — С.20-21.
157. Эйсмонт, Н.В. Рецидивы туберкулёза у психически больных, проживавших в психоневрологических интернатах Свердловской области / Эйсмонт Н.В. // Туберкулёз сегодня: Материалы VII российского съезда фтизиатров. М., 2003. — С.31.
158. Ященко, Б.П. Рецидивы туберкулёза органов клинически излеченныхот туберкулёза лиц пожилого и старческого возраста / Б.П. Ященко, i
159. Л.В. Турченко // Пробл. туб. 1987. — №3. — С.3-5.
160. Banavalicer J., Bose М. Relaps of Tuberculosis // Int. J. Tuber. Lung Dis. -2001.-V. 5.- Nll.-Suppl.l.-P.82.
161. Bernard E., Thibier R., Pretet S. Relapse in pulmonary tuberculosis after chemotherapeutic treatment // Bull. Union Int. Tuberc. 1955. — V.25. — N 3.- P.248-253.
162. Bothamley G.N., Rudd R.M. Clinical evaluation of a sesological assay using a monoclonal antibody (ТВ 72) to the 38 kDa antigen of Mycobacterium of tuberculosis // Eur. Resp. T. 1994. — V.7. — P.240-246.
163. Boushey H.A. Current concepts in the treatment of tuberculosis // West. J. Med., 1987. V.146. — N4. — P. 461-465.
164. Brennan P.Y. Tuberculosis in the context of emerging diseases. F. EMS // Immunol. Med. Microbiol. 1997. — V.18. — N4. — P.263-269.
165. Bruce M.C., Ronez L., Klingez Y.D. et al. Biochemical and pathologic evidence for proteolytic destruction of lung connective tissue in cystic fibroses // Am. Rev. respires. Dis. 1985. — V.132. — P.529-535.
166. Caminero J.A. Management of multidrag-resistant tuberculosis andpatient in retreatment // Eur. Respir. J., May 2005. V.25. — P.928-936.
167. Chan E.D., Laurel V., Chan J.F., Hyunh M.L., Goble M., Iserman M.D. Retrospective analysis of 1973 to 1983 abstract. // Am J Respir. Crit. Care Med. 2001. V. 163. — P. 4497.
168. Cline J.C., Davis S.M. Risk of infection or reactivation of tuberculosis associated with chronic corticosteroid therapy // Ann-Pharmacother, 1997. -V.31. — N6. P.775-6.
169. Crofton J. The prevention and management of drug-resistant tuberculosis // Bull. Int. Un. Tuberc. 1987. — V.62. — N12. — P.6-12.
170. Davidson P.T. Drag resistance and the selection of therapy for tuberculosis // Amer. Rev. Resp. Dis., 1987. V.136. — N2. — P.255-257.
171. Donald P.R., Beyers N., Rook G.A.W. Adolescent tuberculosis // African. Med. U. 1995. -V.86. -P.231-233.
172. Dye Ch., Scheele S., Dolin P., Pathania V., Raviglione M. Global Burden of Tuberculosis. Estimated Incidence, Prevalence, and mortality by Country // JAMA, August 18, 1999. Vol.282. — N 7. — P.677-686.
173. Faustini A., Hall A.J, and C.A. Perucci. Risk factors for multidrag-resistant tuberculosis in Europe: a systematic review // Thorax, Feb 2006. — V.61. -P.158-163.
174. Gosling R.D., Uiso L.O., Sam N.E., Bongard E., Kanduma E.G., Nyindo M., Morris R.W., Gillespie S.H. The bactericidal activity of moxifloxacin in patient with pulmonary tuberculosis // Am. J. of Resp. and Crit. Care Med. 2003. — V.168. — P. 1342-1345.
175. Goldman S. Die Tuberculose in Yugoslawien Gegeuwart und Zurunft // Prax. Pneum. 1977. Bd. 31, f5. — P.322-324.
176. Haanaes O.C., Bjatveit K. Late relaps of tuberculosis after earlier medical treatment in an industrialized country // Bull. Int. UN. Tuberc. — 1982. — Y.57. -Nl.-P.69.
177. Inderlied C.D., Murray P.R., Baron E.J., et al. // Manual of Clinical Microbiology. Washington, 1999. — P. 1601-1623.
178. Junker E. Der tuberkuloserkranke Auslander // Mitt, oster. Sanitatsverwalt, 1989. -Bd.90, N5. -P.177-181.
179. Lilleback T. Molecular evidence of endogenous reactivation of M. tuberculosis // Intern. J. Tuberc. And Lung. Dis. 2001. — Vv.5, N11. -P.35.
180. Liu X.R. A stady on the relapse and its potential causes in pulmonary tuberculosis // Beijing Institute of Thoracic Tumor and Tuberculosis. -Chung-Hua-Chien-Ho-Ho-Hu-Tsa-Chih, 1993. V.16 — N2. — P.69-72, 122.
181. Mikhailov M., Mamedov M., Semenenko T. Immunologic parameters of patients with malignant tumors infected hepatits B. Abst. IX ynt. // Congr: Immunology and liver. Falk Symp. 1992. — V.70.— P.46.
182. Mitchison D. Seminars in Resp. and Critic. Care Med. 2004. — V. 25, N3. — P.307-315.
183. Moser H. Der Tuberkuloschilfeempfanger und seine soziales Schicksal // Mitt, osterr. Sanitatsverwalt. 1989. — Bd. 90, N5. — P. 164-175.
184. Nakhosten Y. Prophylaxe und Therapie der Tuberculose // Atemw. Zandenrrank. 1990. V.16.-P.123-125.
185. O’Brien R.J. Development of fluoroquinolones as first-line drugs for tuberculosis: at long last! // Am. J. of Resp. and Crit. Care Med. 2003. -V.168. —P.1266-1268.
186. Ormerod L.P. Multidrug-resistant tuberculosis (MDR-TB): epidemiology, prevention and treatment // Br.Med.Bull., June 2005. V73. — P. 17-24.
187. Perry G., Bonora S. Which agents should we use for the treatment of multidrug-resistant Mycobacterium tuberculosis? // J. Antimicrob. Chemother. 2004. — V. 54. — P. 593-602.
188. Petit jean R. Etude epidemiologue du risque de Bas-Rhin: 1967-1977 // Rev. Malad. Resp. 1984. — V.l. — N2. -P.93-97.
189. Ravlgllone M.S., Rieder H.L., Styblo K., Khomenko A.G., Esteves K., Kochi A. Tuberculosis treand in Eastern Europe and the former USSR // Tuberc. Lung. Dis. 1994. — V.75. — N6. — P.400-416.
190. Saloman N., Perlman D.C., Friedmann P., Buchstein S., Kreiswirth B.N., Mildvan D. Predictors and outcome of multidrug-resistant tuberculosis // Clin Infect Dis 1995. V.21. — P. 1245-1252.
191. Seaworth B.J. Multidrug-resistant tuberculosis // Infect Dis Clin North Am 2002.- V.16. — P.73-105.
192. Scharkof H. Tuberkulose Ruckfallerkrankungen in der DDR — eine kommunitatsbesogene retrograde Analyse der Janre 1984-1986 // Pneumologie. — 1990. — Bd. 44, N1. — P.449-450.
193. Schluger N.W. Tuberculosis drug resistance in Europe: sunny days, but clouds on the horizon? // Eur. Respir. J., Nov 2007. V.30. — P.825-827.
194. Steinbruck P. Die Entwicklung der tuberculose be Kampfung und der tuberculose epidemiologie in der DDR. Y. Erkr. Atm. Org. 1983. -Bd.161, f.l. -P.36-45.
195. Styblo K. Epidemiology of tuberculosis // Bullint in Tuberc. 1978. — V.55. — N.3. — P.141-152.
196. Tahaoglu K., Torun Т., Sevin T.,Atac G., Kir A., Karasulu L., Ozmen I., Karakli N. The treatment of of multidrug-resistant tuberculosis in Turkey // N. Engl. J. Med. 2001.- V.345. — P. 170-171.
197. Tmka G., Trefni Y. Tuberculosis control and its prospects in Czechoslovakia // Bui. in UN. 1981. — V.56. — N2. — P.5-9.
198. Tripathy S.P. Relapse in tuberculosis // Indian. J. Tuberc., 1981. V.28. -N2.-P. 45-56.
199. Yareldzis B.P., Grosset J., Kantori D., Crofton J., Laszlo A., Felten M., Raviglione M.S., Koshi A. Drug-resistant tuberculosis: laboratory issues World Health Organization recommendation // Tubercle and Lung. Dis. — 1994. — V.75. N1. — P. 1-7.
200. Wada M., Seita A., Mori Т., Ogata H., Sugie Т., Sugita H. Retreatment of pulmonary tuberculosis duration of chemotherapy // Research Institute of Tuberculosis, Japan Anti-tuberculosis, Association, Tokyo, Kekkaku. -1993.-V.68 — N7. — P.469-78.
201. Walls T. and Shingadia Delane. The epidemiology of tuberculosis in Europe // Arch. Dis. Child. 2007.-V.92. — P.726-729.
202. Weis S.E., Slocum P. C., Blais F.X., King В., Nunn M., Matney G.B., Gomez E., Foresman B.N. The effect of directly observed therapy on therates of drag resistance in tuberculosis see comments. // N-Engl-J-Med. -1994. V.330. — N17. — P.l 179-1184.
203. Yamamoto M. Relaps of Tuberculosis // Kekkaku, 1982. V.57. — N10. -P.537-555.
204. Yoshida F. Prognosis of isoniasid-resistant patient of pulmonary tuberculosis // Kekkaku, 1987. V.62. — N1. — P. 17-24.
205. Zakoska M. Risk factors for relapses of tuberculosis // Eur. Resp. J. 2003. -V. 22. — suppl. 45. -P.2172.
206. Zellweger J.P., Coulon P. Outcome of patients treated for tuberculosis in Vand County // Switzerland. Int.J.Tuberc.Lung.Dis — 1998. — V.2. — N5. -P.372-377.
Особенности развития и течения рецидивов туберкулёза легких
Библиографическое описание:
Ходжаева, М. И. Особенности развития и течения рецидивов туберкулёза легких / М. И. Ходжаева, Б. Н. Сирожов. — Текст : непосредственный // Молодой ученый. — 2018. — № 10.1 (196.1). — С. 57-59. — URL: https://moluch.ru/archive/196/49426/ (дата обращения: 25.03.2021).
Рецидивы туберкулеза имеют тенденцию к росту в связи распространенность МЛУ ТБ. Больные с рецидивами туберкулеза органов дыхания ежегодно пополняют контингенты противотуберкулезных диспансеров, в качестве основного источника формирования хронических деструктивных форм туберкулеза, а также распространения МЛУ штаммов микобактерий туберкулеза, и являются основным резервуаром туберкулезной инфекции.
Несмотря на значительные успехи, достигнутые в борьбе с туберкулезом, проблема этой инфекционной и социальной болезни сохраняет свою актуальность[1,с.45].
Показатель частоты ранних рецидивов отражает наличие дефектов в лечении и качестве обследования при переводе больных туберкулезом в неактивные группы диспансерного учета. Показатель частоты поздних рецидивов свидетельствует о распространенности туберкулезной инфекции, неблагоприятных медико-биологических и социальных факторах[2,с.26;3,с.6]
Одной из главных задач при оказании противотуберкулезной помощи населению в настоящее время является своевременность выявления туберкулеза. Другой первостепенной задачей является укрепление приверженности к лечению больных туберкулезом.
Республика Узбекистан обладает завидной инфраструктурой противотуберкулёзной службы и долгой историей эффективной борьбы с туберкулёзом. Программа борьбы с туберкулёзом имеет вертикальную структуру с широкой сетью учреждений. Несмотря на организационные изменения в системе здравоохранения,наличие различных факторов, влияющих на развитие устойчивых форм туберкулёза наблюдается увеличение количество больных с МЛУ туберкулёзом в связи, с чем увеличиваются рецидивы туберкулёзного процесса.
По данным ВОЗ в Республике Узбекистан среди впервые выявленных больных МЛУ ТБ встречается в 23%, а среди ранее леченных в 62 % случаев (Отчет ВОЗ за 2015). Причины рецидивов остаются недостаточно изученными. Взгляды исследователей относительно влияния тех или иных факторов на развитие рецидивов туберкулёза совпадают.
Так, среди рецидивов уровень резистентности МБТ к противотуберкулезным препаратам составляет от 68% до 86% [4], уровень мультирезистентности – в 6 раз выше, чем у больных, впервые заболевших туберкулезом [4], что резко снижает эффективность лечения таких пациентов. Количество случаев успешного лечения в этой категории больных («излечение» + лечение завершено») составляет, по данным разных источников, от 34% до 75% [4,с.65,]. Значительно лучше результаты лечения у больных с рецидивом туберкулеза легких без бактериовыделения – удельный вес случаев эффективного лечения среди них составляет от 65% до 80%., что также ниже показателей ВОЗ. С другой стороны, отсутствие бактериовыделения у данной категории пациентов, невозможность своевременно получить тестна лекарственную чувствительность существенно осложняют выбор оптимальной врачебной тактики.
Следует предположить, что активизация усилий по выявлению и лечению туберкулеза легких на этапе до появления бактериовыделения более оправданна как с экономической, так и с эпидемиологической точки зрения.
В отечественной литературе недостаточно работ, посвященных изучению механизмов повышения качества выявления, особенностей течения и эффективности лечения рецидивов туберкулеза легких. Установлено, что клинико-рентгенологические проявления рецидивов туберкулеза легких, сопровождающегося бактериовыделением, значительно более выражены: типичны множественные крупные деструкции легочной ткани, высокий уровень резистентности к противотуберкулезным препаратам, характеризуется возникновением более распространенных форм туберкулеза, с возникновением деструкций и наличием сопутствующих заболеваний.
Нами было обследовано 50 больных, из которых впервые выявленные составили- 33, и рецидивы туберкулёзного процесса- 17. По клиническим формам распределение больных представлено в таблице.
№ | Клиническая форма | Впервые выявленные | Рецидив ТБ |
1 | Инфильтративные ТБ | 67,5 | 43,9 |
2 | Фиброзно-кавернозный ТБ | 3,75 | 36,6 |
3 | Очаговый ТБ | 13,7 | 4,5 |
4 | Кавернозный ТБ | 2,5 | 4,5 |
5 | Диссеминированный ТБ | 6,9 | 4,5 |
6 | Цирротический ТБ | 1,9 | 3 |
7 | Туберкуломы | 1,25 | 3 |
8 | Внутригруд. ЛУ ТБ | 1 | |
9 | Казеозная пневмония | 1,25 |
У больных с рецидивами туберкулезного процесса отмечались сопутствующие заболевание, осложнения основного заболевания и преобладание социального фактора.
В эпидемиологическом плане у 18 (54,5%) впервые выявленных больных МБТ обнаружены методом бактериоскопии, у 27 (81,8%) МБТ выявленные бактериологическим методом. Среди больных с рецидивами туберкулёзного процесса бактериовыделение обнаружено у 9 (53%), из них 4 (44,4%) МБТ выявлены методом бактериоскопии и 6 (66,7%) бактериологическим методом. Чувствительность к противотуберкулезным препаратам у 4 (23,5%) больных с рецидивами отмечено наличие устойчивых штаммов МБТ.
Клиническая картина рецидивов туберкулеза легких протекает значительно тяжелее, чем при впервые выявленных процессах. Случаи рецидивов, которые сопровождаются бактериовыделением, несомненно важны в эру химиорезистентного туберкулеза, так как позволяют, прежде всего, изучить спектр чувствительности микобактерий туберкулеза(МБТ) к противотуберкулезным препаратам, оптимизировать сроки и схемы лечения, а также решить многие другие проблемы, связанные с выявлением, диагностикой и профилактикой туберкулеза.
Контроль и лечение химиорезистентного туберкулёза является одним из важных приоритетов благодаря осознанию проблемы, росту материально – технической базы и распространению принципов современной медицины. Для того, чтобы взять под контроль химиорезистентный туберкулёз и, связанные с ним рецидивы, необходимо интенсивное внедрение альтернативных и вспомогательных методов современной диагностики и лечения с учетом сложившейся ситуации.
Своевременная диагностика дополнительными методами химиорезистентности у лиц с рецидивом туберкулеза легких при наличии МБТ и без бактериовыделения, определение значения социального статуса больных, осложнений основного заболевания в возникновении рецидивов туберкулеза – наиболее важная и трудно решаемая задача в стратегии борьбы с лекарственно устойчивыми формами заболевания.
Таким образом, поиск путей улучшения качества работы по своевременному выявлению, в том числе и посредством использования методов современной лабораторной диагностики, рецидивов туберкулеза легких в учреждениях первичного звена совместно с фтизиатрами остается приоритетным направлением деятельности современной медицины.
Литература:
- Гриб Е.Ю, Грицова Н.А. Результаты лечения рецидивов туберкулеза легких// Семейная Медицина -№4 -(60), 2015.с.45
- Петренко В.М, Черенько С.О., Литвиненко Н.А., Циганкова Л.М. Рецидивами захворювання за показникамикогортногоаналізу//Український пульмонологічний журнал. 2011.№ 3. С. 5–10.
- Плиева С.Л. Особенности ранних и поздних рецидивов туберкулеза органов дыхания//Туберкулез и болезни легких. 2011. № 6. С. 23-27.
- Рустамова С.Р. Изучение причин и факторов, способствующих развитию рецидивов туберкулеза органов дыхания// Конгресс Национальной Ассоциации Фтизиатров,Санкт-Петербург, 2014. С.65
Основные термины (генерируются автоматически): туберкулезный процесс, больной, рецидив, рецидив туберкулеза легких, бактериологический метод, метод бактериоскопии, основное заболевание, современная медицина, туберкулезная инфекция, Узбекистан.
Сибирские ученые разработали способ определения риска рецидива туберкулеза легких
Одна из ключевых задач в области здравоохранения, поставленная ВОЗ, – положить конец эпидемии туберкулеза к 2030 году. Для этого необходимы методы ранней диагностики и эффективной терапии этого заболевания. Ученые ТГУ совместно со специалистами СибГМУ, Томского областного туберкулезного диспансера и НИИ туберкулеза (Новосибирск) разработали новый подход к выявлению лекарственно-устойчивых форм туберкулеза легких. Исследователи создали компьютерную модель, которая прошла машинное обучение и может с точностью более 95 процентов определять пациентов группы риска.
– Ситуация с ростом заболеваемости туберкулезом, который сейчас отмечается во всем мире, осложняется не только увеличением количества первичных больных, но и тем, что становится больше пациентов с лекарственно-устойчивыми формами, – говорит заместитель проректора ТГУ по научной работе Юрий Кистенев. – В таких случаях терапия не дает нужного эффекта, у человека происходит рецидив заболевания, что приводит к заражению других людей. Лечение таких пациентов требует больших финансовых затрат и времени. Чтобы снизить количество подобных случаев, необходимо в начале лечения оценивать риск рецидива при лечении пациента стандартными лекарственными препаратами.
Медики предоставили базу данных с клиническими показателями 850 больных туберкулезом и информацией о рецидивах. В ходе разработки компьютерной модели были апробированы разные методы классификации информации. Используя методы машинного обучения, из 120 исходных параметров ученые выявили около 30, на их основе была простроена модель, способная с очень высокой вероятностью прогнозировать рецидив, то есть выделять группу риска с лекарственной устойчивостью.
Верификация созданной прогнозной модели была проведена на данных, которые не участвовали в процессе обучения. Она показала высокую точность выявления риска рецидивов, достигающую на отдельных вариантах модели почти 100 процентов.
Применение этой программы на практике поможет фтизиатру определять степень риска рецидива и подбирать для пациента тот набор препаратов, который будет эффективен при его форме заболевания.
По данным ВОЗ в 2016 году в мире заболело туберкулезом больше 10 000 000 человек. На Индию, Китай и РФ пришлось 47 процентов случаев. В России за последние 10 лет доля впервые выявленных больных туберкулезом с лекарственной устойчивостью увеличилась в два раза. На территории Томской области доля впервые выявленных больных за этот же период увеличилась в полтора раза.
Компьютерную модель научили прогнозировать рецидивы туберкулеза легких
Одна из ключевых задач в области здравоохранения, поставленная ВОЗ, –
положить конец эпидемии туберкулеза к 2030 году. Для этого необходимы
методы ранней диагностики и эффективной терапии этого заболевания.
Ученые ТГУ совместно со специалистами СибГМУ, Томского областного
туберкулезного диспансера и НИИ туберкулеза (Новосибирск) разработали
новый подход к выявлению лекарственно-устойчивых форм туберкулеза
легких. Исследователи создали компьютерную модель, которая прошла
машинное обучение и может с точностью более 95 процентов определять
пациентов группы риска.
– Ситуация с ростом заболеваемости туберкулезом, который сейчас
отмечается во всем мире, осложняется не только увеличением количества
первичных больных, но и тем, что становится больше пациентов с
лекарственно-устойчивыми формами, – говорит заместитель проректора ТГУ
по научной работе Юрий Кистенев. – В таких случаях терапия не
дает нужного эффекта, у человека происходит рецидив заболевания, что
приводит к заражению других людей. Лечение таких пациентов требует
больших финансовых затрат и времени. Чтобы снизить количество подобных
случаев, необходимо в начале лечения оценивать риск рецидива при лечении
пациента стандартными лекарственными препаратами.
Медики предоставили базу данных с клиническими показателями 850
больных туберкулезом и информацией о рецидивах. В ходе разработки
компьютерной модели были апробированы разные методы классификации
информации. Используя методы машинного обучения, из 120 исходных
параметров ученые выявили около 30, на их основе была простроена модель,
способная с очень высокой вероятностью прогнозировать рецидив, то есть
выделять группу риска с лекарственной устойчивостью.
Верификация созданной прогнозной модели была проведена на данных,
которые не участвовали в процессе обучения. Она показала высокую
точность выявления риска рецидивов, достигающую на отдельных вариантах
модели почти 100 процентов.
Применение этой программы на практике поможет фтизиатру определять
степень риска рецидива и подбирать для пациента тот набор препаратов,
который будет эффективен при его форме заболевания.
По данным ВОЗ в 2016 году в мире заболело туберкулезом больше
10 000 000 человек. На Индию, Китай и РФ пришлось 47 процентов случаев. В
России за последние 10 лет доля впервые выявленных больных туберкулезом
с лекарственной устойчивостью увеличилась в два раза. На территории
Томской области доля впервые выявленных больных за этот же период
увеличилась в полтора раза.
Фтизиатр Тарас Ворончихин: «Туберкулез чаще всего возникает из-за ослабленного иммунитета»
О том, как снизить риски встречи с туберкулезом, и кто более других подвержен этой болезни рассказал врач-фтизиатр, практикующий торакальный хирург, оперирующий данный недуг, Тарас Ворончихин.
Тарас, скажите, пожалуйста, какие главные риски заражения туберкулезом можно выделить?
Главная причина заболевания туберкулезом – это ослабление иммунитета. Отсюда и риски – причины, которые ослабляют иммунную систему: стресс, неправильное и недостаточное питание, курение, злоупотребление алкоголем, наркомания и так далее.
Издавна детям делаю пробу Манту. Ваше мнение, как специалиста, правда ли это помогает снизить риски заболевания туберкулезом?
Реакция Манту – это диагностическая проба, позволяющая выявить детей, у которых произошло инфицирование невакцинным штаммом микобактерии и отнести их в группу риска по заболеванию туберкулезом. Выявив с помощью пробы Манту, туберкулин положительных детей, им проводят Диаскин тест (тоже кожный диагностический тест) и, если он положительный, то таким детям назначают химио-профилактику, чтобы у них инфицирование не переросло в настоящий туберкулезный процесс. Причем, проявится заболевание может через несколько лет. Вовремя проведенная химио-профилактика значительно снижает риски заболевания туберкулезом.
Какие обследования человеку нужно пройти, чтобы понять, что у него туберкулез?
Основной метод позволяющий установить диагноз туберкулеза является клинико-рентгенологический. При подозрении на туберкулезный процесс больному проводят рентгенологическое обследование, в то числе и компьютерную томографию, исследуют мокроту для выявления туберкулезных микобактерий.
Кроме того, для подтверждения диагноза возможно проведение диагностических операций: биопсии легких, лимфоузлов, плевры. Это бывает необходимо, если невозможно получить мокроту. Также, бывает, необходимо проведение бронхоскопии, на которой выявляют специфические для туберкулеза изменения, а так же берут смывы с бронхов для выявления туберкулезной палочки. При выявлении в мокроте и промывных водах бронхов туберкулезных микобактерий позволяет выставить диагноз туберкулеза легких в 100%.
Поставлен диагноз «туберкулез». Что дальше? Всех ли больных необходимо изолировать?
После того, как диагноз «туберкулез» выставлен, необходимо начинать лечение. Основной метод лечения – это прием противотуберкулезных препаратов. Лечение должно быть длительным, непрерывным, комплексным. Конечно, изоляция больных необходима, так как основной путь передачи туберкулеза в любом случае воздушно-капельный.
Тарас,как быстро можно избавиться от туберкулеза, если вовремя начать лечение?
Лечение туберкулеза процесс в принципе длительный и зависит от формы туберкулеза легких, иногда занимает до 18-24 месяцев. Если больной принимает препараты правильно, не пропускает дозы, полностью излечиться можно за 10-12 месяцев.
В каких случаях туберкулез легких все-таки нужно оперировать?
Туберкулез легких бесследно не проходит, и часто формируются крупные ограниченные очаги туберкулезной инфекции – туберкуломы. Их необходимо убирать хирургическом путем, так как они могут быть «минами замедленного действия», и в любой момент могут «рвануть», вследствие чего туберкулез вернется – возникнет рецидив.
Второе показание к оперативному лечению, даже более важное, чем первое, это наличие полостей распада в легком, которые, несмотря на проводимое лечение не ликвидируются. В любом случае показание к операции определяет торакальный хирург. После операции лечение не заканчивается, и курс терапии противотуберкулезными препаратами необходимо продолжать еще до 6-8 месяцев. Только в этом случает можно достичь стойкого положительного эффекта и выздороветь.
Как же заметить болезнь на ранней стадии? Какие признаки говорят о том, что человек, вероятно, болен?
Обследованию на туберкулез легких подлежат больные с затяжными пневмониями, длительным кашлем (более 4 недель), длительным субфибрилитетом. На ранних стадиях туберкулез протекает бессимптомно, жалобы начинают предъявлять зачастую в запущенных стадиях. Чтобы «захватить» болезнь на ранних стадиях, необходимо регулярно проходить флюорографическое обследование.
А есть ли способы профилактики туберкулеза?
Главное правило профилактики туберкулеза легких это – здоровый образ жизни.
Говорят, что туберкулез чаще встречается у взрослых, чем у детей. Так ли это?
Действительно, заболеваемость туберкулезом легких у взрослых выше, чем у детей. Детей после рождения вакцинируют, и иммунитет предохраняет детей от генерализованных, наиболее опасных форм туберкулеза. В подростковом возрасте в связи с гормональной перестройкой заболеваемость растет. У взрослых поствакцинальный иммунитет уже не работает, и любые факторы, ослабляющие иммунную систему, приводят к болезни.
Тарас, важна ли в этом вопросе наследственность?
Вопрос наследственной предрасположенности при туберкулезе открыт, есть много исследований, но однозначного ответа нет. Бесспорно, есть генетическая предрасположенность к реакции организма на инфекционный процесс. Но однозначно говорить о наследственности нельзя.
Автор: Татьяна Зайцева эксклюзивно для ПрессОрг24. Фото: личный архив Тараса Ворончихина.
Какова частота рецидивов у пациентов, завершивших курс лечения туберкулеза (ТБ)?
Автор
Томас Э. Херклайн, доктор медицины Профессор медицины, Государственный университет Райта, Медицинская школа Буншофт; Медицинский консультант, Общественное здравоохранение, Туберкулезная клиника округа Дейтон и Монтгомери (Огайо)
Томас Э. Херклайн, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американского общества инфекционных болезней, Общества инфекционных болезней Огайо
Раскрытие информации: Нечего раскрывать.
Соавтор (ы)
Джудит К. Амороса, доктор медицины, FACR Клинический профессор радиологии и заместитель председателя по развитию профессорско-преподавательского состава и медицинского образования, Медицинская школа Рутгерса Роберта Вуда Джонсона
Джудит К. Амороса, доктор медицины, FACR является членом следующих медицинских обществ: Американский колледж радиологии, Американское общество рентгеновских лучей, Ассоциация университетских радиологов, Радиологическое общество Северной Америки, Общество торакальной радиологии
Раскрытие: Ничего не разглашать.
Главный редактор
Майкл Стюарт Бронз, доктор медицины Дэвид Росс Бойд Профессор и председатель медицинского факультета, кафедра внутренней медицины, кафедра медицины, Научный центр здравоохранения Университета Оклахомы; Магистр Американского колледжа врачей; Научный сотрудник Американского общества инфекционных болезней; Член Королевского колледжа врачей, Лондон
Майкл Стюарт Бронз, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американский колледж врачей, Американская медицинская ассоциация, Ассоциация профессоров медицины, Общество инфекционных болезней Америки, Государственная медицинская ассоциация штата Оклахома, Южное общество клинических исследований
Раскрытие информации: нечего раскрывать.
Благодарности
Эрика Банг Медицинский центр государственного университета Нью-Йорка Медицинский колледж
Раскрытие: Ничего не раскрывать.
Диана Брейнард, MD Консультант, Отделение инфекционных заболеваний, Массачусетская больница общего профиля
Раскрытие: Ничего не раскрывать.
Памела С. Чавис, доктор медицины Профессор кафедры офтальмологии и неврологии Медицинского университета Южной Каролины, Медицинский колледж
Памела С. Чавис, доктор медицины, является членом следующих медицинских обществ: Американской академии неврологии, Американской академии офтальмологии и Североамериканского нейроофтальмологического общества
Раскрытие: Ничего не раскрывать.
Дирк М. Элстон, доктор медицины Директор, Академия дерматопатологии Акермана, Нью-Йорк,
Дирк М. Элстон, доктор медицины, является членом следующих медицинских обществ: Американская академия дерматологии
Раскрытие: Ничего не раскрывать.
Теодор Дж. Гаэта, DO, MPH, FACEP Доцент кафедры неотложной медицины, Медицинский колледж Вейл Корнелл; Заместитель председателя и директор программы резидентуры по неотложной медицине, Департамент неотложной медицины, Методистская больница Нью-Йорка; Научный руководитель, адъюнкт-профессор кафедры неотложной медицины, медицинский факультет Университета Святого Георгия
Теодор Дж. Гаэта, DO, MPH, FACEP является членом следующих медицинских обществ: Альянса клинического образования, Американского колледжа врачей неотложной помощи, руководителей отделов неотложной медицины, Совета директоров резиденций неотложной медицины, Нью-Йоркской медицинской академии и Общество академической неотложной медицины
Раскрытие: Ничего не раскрывать.
Аарон Глатт, доктор медицины Профессор клинической медицины Нью-Йоркского медицинского колледжа; Президент и генеральный директор, бывший главный врач отделения медицины и инфекционных заболеваний больницы Святого Иосифа (ранее — больница Нью-Айленд)
Аарон Глатт, доктор медицины, является членом следующих медицинских обществ: Американского колледжа грудных врачей, Американского колледжа врачей, Американского колледжа врачей, Американского колледжа врачей-Американского общества внутренней медицины, Американской медицинской ассоциации, Американского общества микробиологов. , Американское торакальное общество, Американская ассоциация венерических заболеваний, Американское общество инфекционных заболеваний, Международное общество по СПИДу и Общество здравоохранения и эпидемиологии Америки
Раскрытие: Ничего не раскрывать.
Саймон К. Лоу, доктор медицинских наук, фармацевт Клинический профессор медицинских наук, кафедра офтальмологии, Глазной институт Жюля Штейна, Калифорнийский университет, Лос-Анджелес, медицинская школа Дэвида Геффена
Саймон К. Лоу, доктор медицинских наук, фармацевт является членом следующих медицинских обществ: Американской академии офтальмологии, Американского общества глаукомы и Ассоциации исследований в области зрения и офтальмологии
Раскрытие: Ничего не раскрывать.
Джон М. Лидом, доктор медицины Заслуженный профессор медицины Медицинской школы им. Кека Университета Южной Калифорнии
Джон М. Лидом, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американский колледж врачей — Американское общество внутренней медицины, Американское общество микробиологии, Американское общество инфекционных болезней, Международное общество по СПИДу и Phi Beta Kappa
.
Раскрытие: Ничего не раскрывать.
Джеймс Ли, доктор медицины Бывший доцент отделения неотложной медицины Гарвардской медицинской школы; Совет директоров Remote Medicine
Раскрытие: Ничего не раскрывать.
Джеффри Мефферт, доктор медицины Ассистент клинического профессора дерматологии, Школа медицины Техасского университета в Сан-Антонио
Джеффри Мефферт, доктор медицины, является членом следующих медицинских обществ: Американской академии дерматологии, Американской медицинской ассоциации, Ассоциации военных дерматологов и Техасского дерматологического общества
Раскрытие: Ничего не раскрывать.
Монте С. Мельцер, доктор медицины , начальник дерматологической службы, госпиталь Юнион Мемориал
Монте С. Мельцер, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha и Американской академии дерматологии
Раскрытие: Ничего не раскрывать.
Susannah K Mistr, MD Врач-резидент, отделение офтальмологии, Медицинский центр Университета Мэриленда
Сюзанна К. Мистр, доктор медицины, является членом следующих медицинских обществ: Американской академии офтальмологии, Американского колледжа хирургов, Американской медицинской ассоциации, Американской ассоциации студентов-медиков / Фонда, Американского общества катарактальной и рефракционной хирургии и Медицинской ассоциации Южной Каролины
.
Раскрытие: Ничего не раскрывать.
Кэрол Нэйси, доктор философии Адъюнкт-профессор, факультет биологии, Католический университет Америки; Адъюнкт-профессор кафедры тропической медицины и микробиологии, Университет Джорджа Вашингтона
Кэрол Нейси, доктор философии, является членом следующих медицинских обществ: Американской академии микробиологии и Американского общества микробиологии
Раскрытие информации: Sequella, Inc. Доля собственности Занятость; Sequella, Inc. Инвестор долевого участия
Джей Джеймс Роуси, доктор медицины Бывший директор службы роговицы, Институт катаракты и лазера Св. Луки
Джеймс Роуси, доктор медицины, является членом следующих медицинских обществ: Американской академии офтальмологии, Американской ассоциации развития науки, Американской медицинской ассоциации, Ассоциации исследований в области зрения и офтальмологии, Флоридской медицинской ассоциации, Панамериканской ассоциации офтальмологов. , Sigma Xi и Южная медицинская ассоциация
Раскрытие: Ничего не раскрывать.
Хэмптон Рой старший, доктор медицины Доцент кафедры офтальмологии Медицинского университета Арканзаса
Хэмптон Рой-старший, доктор медицинских наук, является членом следующих медицинских обществ: Американской академии офтальмологии, Американского колледжа хирургов и Панамериканской ассоциации офтальмологов
Раскрытие: Ничего не раскрывать.
Джон Д. Шеппард-младший, доктор медицины, MMSc Профессор офтальмологии, микробиологии и молекулярной биологии, клинический директор Центра глазной фармакологии Томаса Р. Ли, директор исследовательской программы резидентуры по офтальмологии Медицинской школы Восточной Вирджинии; Президент, Virginia Eye Consultants
Джон Д. Шеппард-младший, доктор медицины, MMSc является членом следующих медицинских обществ: Американской академии офтальмологии, Американского общества микробиологов, Американского общества катарактальной и рефракционной хирургии, Американского общества увеитов и Ассоциации исследований в области зрения и офтальмологии
Раскрытие: Ничего не раскрывать.
Ричард Х. Синерт, DO Профессор неотложной медицины, клинический доцент медицины, директор по исследованиям Медицинского колледжа Государственного университета Нью-Йорка; Консультанты, отделение неотложной медицины, госпиталь округа Кингс
Ричард Синерт, доктор медицинских наук, является членом следующих медицинских обществ: Американского колледжа врачей и Общества академической неотложной медицины
Раскрытие: Ничего не раскрывать.
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Medscape Salary Employment
Кейт Цанг, врач-резидент , клинический ассистент инструктора, отделение неотложной медицины, Государственный университет Нью-Йорка, нижний штат Нью-Йорк, больница округа Кингс
Кейт Цанг, доктор медицины, является членом следующих медицинских обществ: Американского колледжа врачей неотложной помощи, Ассоциации резидентов неотложной медицины и Общества академической неотложной медицины
Раскрытие: Ничего не раскрывать.
Шьям Верма, MBBS, DVD, FAAD Доцент кафедры дерматологии Университета Вирджинии; Адъюнкт-профессор кафедры дерматологии Государственного университета Нью-Йорка в Стоунибруке, адъюнкт-профессор кафедры дерматологии Пенсильванского университета
Шьям Верма, MBBS, DVD, FAAD является членом следующих медицинских обществ: Американская академия дерматологии
Раскрытие: Ничего не раскрывать.
Ричард П. Винсон, доктор медицины Ассистент клинического профессора, кафедра дерматологии, Центр медицинских наук Техасского технологического университета, Медицинская школа Пола Л. Фостера; Консультант, Дерматология Маунтин-Вью, PA
Ричард П. Винсон, доктор медицины, является членом следующих медицинских обществ: Американской академии дерматологии, Ассоциации военных дерматологов, Техасского дерматологического общества и Техасской медицинской ассоциации
.
Раскрытие: Ничего не раскрывать.
Эрик Л. Вайс, доктор медицины, DTM & H Медицинский директор, Управление непрерывности обслуживания и планирования на случай стихийных бедствий, директор по стипендии, Стипендия по медицине стихийных бедствий Медицинского центра Стэнфордского университета, председатель SUMC и LPCH Целевая группа по биотерроризму и готовности к чрезвычайным ситуациям, младший клинический консультант Департамента здравоохранения Хирургия (неотложная медицина), Медицинский центр Стэнфордского университета
Эрик Л. Вайс, доктор медицины, DTM & H является членом следующих медицинских обществ: Американского колледжа врачей неотложной помощи, Американского колледжа медицины труда и окружающей среды, Американской медицинской ассоциации, Американского общества тропической медицины и гигиены, Врачи за социальную ответственность, Юго-восточный хирургический Конгресс, Южная ассоциация онкологии, Южное клиническое неврологическое общество и Общество дикой медицины
Раскрытие: Ничего не раскрывать.
Рецидив туберкулеза среди пациентов с впервые выявленным положительным мазком мокроты, получавших лечение в рамках пересмотренной национальной программы борьбы с туберкулезом, Индия: многоцентровое проспективное исследование
Аннотация
Введение
Отсутствует информация о доле новых больных туберкулезом легких с положительным мазком (ЛТБ), получавших 6-месячную схему лечения трижды в неделю в рамках пересмотренной национальной программы по борьбе с туберкулезом (RNTCP), у которых после успешного исхода лечения развился рецидив ТБ.
Объектив
Для оценки рецидивов туберкулеза среди пациентов с впервые выявленным ПТБ, которые успешно завершили лечение, и для документирования эндогенной реактивации или повторного инфицирования. Определены факторы риска неблагоприятных исходов лечения и рецидива туберкулеза.
Методология
Взрослых (в возрасте ≥ 18 лет) новых пациентов с PTB с положительным мазком, начавших лечение в рамках RNTCP, были набраны из центров в Тамил Наду, Карнатаке, Дели, Махараштре, Мадхья-Прадеш и Керале.Пациенты, заявившие об «успешном лечении» в конце лечения, прошли по 2 исследования мокроты через 3, 6 и 12 месяцев после завершения лечения. Генотипирование MIRU-VNTR было выполнено для выявления эндогенной реактивации или экзогенной повторной инфекции при рецидиве ТБ. Рецидивы ТБ выражались как частота на 100 человеко-лет (с 95% доверительным интервалом [95% ДИ]). Для выявления факторов риска неблагоприятного ответа на лечение и рецидива туберкулеза использовались регрессионные модели.
Результаты
Из 1577 новых пациентов с положительным мазком мокроты, включенных в исследование, 1565 были проанализированы.Общий показатель излечения составил 77% (1207/1565), а успех лечения — 77% (1210/1565). Показатель излеченности варьировал от 65% до 86%. У 158 из 1210 пациентов был рецидив туберкулеза после успешного лечения. Общая оценка рецидивов ТБ составила 10,9% [95% ДИ: 0,2–21,6], а частота рецидивов ТБ на 100 человеко-лет составила 12,7 [95% ДИ: 0,4–25]. Частота рецидивов ТБ на 100 человеко-лет варьировала от 5,4 до 30,5. Эндогенная реактивация наблюдалась у 56 (93%) из 60 пациентов, которым проводилось генотипирование. Мужской пол был связан с рецидивом туберкулеза.
Заключение
У значительной части новых пациентов с ПТБ с положительным мазком мокроты, успешно пролеченных 6-месячным режимом трижды в неделю, наблюдается рецидив ТБ в соответствии с настройками программы.
Образец цитирования: Velayutham B, Chadha VK, Singla N, Narang P, Gangadhar Rao V, Nair S, et al. (2018) Рецидив туберкулеза среди пациентов с впервые выявленным положительным результатом мокроты туберкулеза легких, проходящих лечение в рамках пересмотренной национальной программы борьбы с туберкулезом, Индия: многоцентровое проспективное исследование.PLoS ONE 13 (7):
e0200150.
https://doi.org/10.1371/journal.pone.0200150
Редактор: Пере-Жоан Кардона, Fundació Institut d’Investigació en Ciències de la Salut Germans Trias i Pujol, Автономный университет Барселоны, Испания
Поступила: 25.01.2018 г .; Принята к печати: 20 июня 2018 г .; Опубликовано: 6 июля 2018 г.
Авторские права: © 2018 Velayutham et al. Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Доступность данных: Данные содержат потенциальные идентификаторы пациентов. В соответствии с нормами ICMR-Национального института исследований в области туберкулеза, запросы данных можно направлять директору Национального института исследований в области туберкулеза. Электронная почта: [email protected].
Финансирование: Исследование финансировалось Центральным противотуберкулезным отделением. Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Конкурирующие интересы: Авторы заявили, что никаких конкурирующих интересов не существует.
Введение
В 2016 г. на Индию приходилось почти 2,8 миллиона из 10,4 миллиона случаев заболевания туберкулезом во всем мире [1]. Правительство Индии внедрило Пересмотренную национальную программу борьбы с туберкулезом (RNTCP) с 1997 года, основанную на рекомендованной на международном уровне стратегии краткосрочного лечения под непосредственным наблюдением (DOTS). В рамках RNTCP пациенты с впервые выявленным туберкулезом легких с положительным мазком мокроты получали лечение по 6-месячной схеме лечения три раза в неделю, состоящей из начальной интенсивной фазы (IP) изониазида (H), рифампицина (R), пиразинамида (Z) и этамбутола ( E) в течение двух месяцев с последующей фазой продолжения (CP) H и R в течение четырех месяцев (2 H 3 R 3 Z 3 E 3 / 4H 3 R 3 ).Каждая доза во время IP должна вводиться под непосредственным наблюдением; во время ХП первая недельная доза вводилась под непосредственным наблюдением, а оставшиеся две недельные дозы вводились самостоятельно [2]. Результат лечения в первую очередь основывается на контрольной микроскопии мокроты по окончании лечения. Согласно рутинным данным эпиднадзора RNTCP, успех лечения среди новых микробиологически подтвержденных пациентов с легочным туберкулезом, зарегистрированных для лечения по этой схеме в 2015 году, составил 88%, вылеченные: 84% и завершенное лечение: 4% [3].
Ранее было проведено очень мало исследований, в основном в ограниченных географических районах, чтобы выяснить долю таких пациентов, у которых наблюдается рецидив ТБ, и которые обычно включали одноразовое наблюдение в переменный момент времени после завершения лечения и, таким образом, были ограничены в дизайне исследований [ 4,5]. Отсутствует информация о частоте рецидивов на национальном уровне и доле рецидивов, связанных с эндогенной реактивацией / экзогенной реинфекцией.Поэтому было проведено многоцентровое исследование с основной целью оценить частоту рецидивов ТБ среди успешно пролеченных новых пациентов с ТБ легких с положительным мазком мокроты в течение первого года после того, как они были объявлены вылеченными или лечение завершено. Ранее было продемонстрировано, что большинство рецидивов возникает в течение одного года после завершения лечения [5]. Вторичные цели включали выяснение (а) доли успешно пролеченных, (б) доли повторных случаев ТБ, связанных с эндогенной реактивацией, (в) факторов риска, связанных с неблагоприятным исходом лечения ТБ и рецидивом ТБ.
Методология
Рабочий кабинет
Исследование было проведено в 12 отчетных районах RNTCP шестью институтами-исполнителями, отобранными целенаправленно на основе соответствующего исследовательского потенциала и готовности участвовать, с Национальным институтом исследований туберкулеза (NIRT), Ченнаи, в качестве узлового центра. Три из этих институтов были расположены в южной части страны и по одному в северной, западной и центральной частях страны. Каждый внедряющий институт провел исследование в двух удобно выбранных районах (рис. 1).Распространенность ВИЧ среди взрослого населения в 2013–2014 годах в штатах, где проводилось исследование, была следующей: Мадхья-Прадеш (0,09%), Керала (0,12%), Дели (0,22%), Тамил Наду (0,28%), Махараштра (0,42%) и Карнатака (0,52%) [6]. Процент населения за чертой бедности (2011–2012 годы) составлял 7,1%, 9,9%, 11,3%, 17,4%, 20,9% и 31,6% в Керале, Дели, Тамил Наду, Махараштре, Карнатаке и Мадхья-Прадеше соответственно [7].
Популяция исследования и дизайн исследования
Исследуемая популяция состояла из новых взрослых пациентов с легочным туберкулезом (возраст ≥ 18 лет) с положительным мазком мокроты (ПОШ), проживающих в выбранном районе противотуберкулезного отделения (ТУ) и зарегистрированных для лечения по прерывистому режиму трижды в неделю в рамках RNTCP.Из них те, кто был объявлен успешно пролеченным, проспективно наблюдались в течение 12 месяцев после лечения.
Отбор проб
Размер выборки оценивался в 1200 новых больных туберкулезом легких с положительным мазком, зарегистрированных для лечения; параметры и значения, учитываемые для оценки размера выборки, были ниже —
Доля успешно пролеченных = 85%
Доля успешно пролеченных пациентов с ожидаемым рецидивом туберкулеза = 15%
Абсолютная точность = 2.5%
Уровень значимости = 5%
Ожидаемая потеря для последующего наблюдения в период после лечения = 20%.
Предполагаемый размер выборки был равномерно распределен между различными учреждениями-исполнителями, каждый из которых расположен в своем штате. Таким образом, размер выборки в 200 человек каждая была затем равномерно распределена на 2 района в соответствующем штате. В каждом районе было выбрано одно противотуберкулезное отделение (ТУ); критерием является регистрация в рамках RNTCP не менее 150 новых больных туберкулезом легких с положительным мазком мокроты за последние два квартала.В случае отсутствия такой ЕП выбирались две ЕП. ОП — это административная единица подрайонного уровня, ответственная за реализацию RNTCP в своей географической юрисдикции с населением около 250 000–500 000 человек. В пределах каждой ОП в исследование были включены последовательные пациенты, пока не был достигнут размер выборки, выделенный для района.
Процедуры исследования
Полевые следователи (FI), которые были специально наняты для исследования, прошли комплексную и единообразную подготовку в NIRT.Они посещали каждый Назначенный микроскопический центр (DMC) в соответствующих TU каждую неделю, и в строке перечислялись все диагностированные новые пациенты с легочным туберкулезом с положительным мазком мокроты. Обычно в каждой ТП 3–5 РСЧ. FI координировал свои действия со старшим терапевтом (STS), лаборантом (LT), фармацевтом и патронажным врачом (TB-HV) для связи с пациентом. Исключались лица, проживающие за пределами исследуемого района, и возраст <18 лет. FI проинформировал пациента об исследовании, его процедурах и получил подпись пациента в форме информированного согласия.У тех, кто дал согласие на участие, FI собрала два дополнительных образца мокроты для целей исследования до начала противотуберкулезного лечения (ATT) или в течение одной недели после начала лечения.
Те пациенты, которым не была начата АТТ, были исключены из дальнейших процедур исследования. Процедуры исследования включали сбор соответствующих данных из записей RNTCP, интервью с пациентами, сбор и исследование мокроты с помощью мазка и посева, тестирование лекарственной чувствительности (ТЛЧ), генотипирование культуральных изолятов, тестирование на ВИЧ и измерение уровня сахара в капиллярной крови.
Данные из карты лечения туберкулеза и интервью с пациентом.
Первоначальный опрос каждого пациента проводился FI — в течение 14 дней после начала лечения. Информация, собранная в ходе интервью и из карты лечения ТБ, включала возраст, пол, симптомы с продолжительностью, личные привычки — курение / употребление алкоголя, сопутствующие заболевания — ВИЧ / диабет, первоначальную оценку мазка мокроты, рост (см), масса тела (кг), дата начала лечения и временной интервал между появлением симптомов до обращения за медицинской помощью и началом АТТ.Данные записывались в заранее составленный график интервью.
В конце интенсивной фазы лечения информация, собранная из карты лечения туберкулеза, включала массу тела (кг), статус мазка мокроты, время, необходимое для завершения IP, количество пропущенных доз, изменение лечения, если таковое имеется, с указанием причины.
Во время объявления результата лечения из карты лечения ТБ и во время второго интервью с пациентом с использованием графика «Интервью по результатам лечения» была собрана следующая информация: масса тела (кг), тип результата лечения с указанием даты, количество пропущенные дозы, время, необходимое для завершения КП, модификация лечения, если таковая имеется по причине, симптомы, если таковые имеются, сопутствующее заболевание, личные привычки и тип лечения под непосредственным наблюдением (DOT) — на базе медицинского учреждения / на уровне общины.Для пациентов с исходом лечения «потеря для последующего наблюдения» были предприняты попытки опросить пациента, а также выяснить причины прерывания лечения. В отношении «умерших» пациентов соответствующая информация была получена путем опроса родственников погибших. Пациенты, не прошедшие оценку результатов лечения в связи с переводом, были исключены из интервью и дальнейшего наблюдения.
Для пациентов, признанных успешно пролеченными, было проведено третье интервью во время рецидива или в конце 12 месяцев после лечения.Собранная информация включала симптомы, если таковые были, проводилась ли ATT в период наблюдения после лечения, сопутствующие заболевания и личные привычки.
На каждом этапе исследования было предпринято минимум три попытки связаться с пациентом по телефону или посетить его на дому, чтобы завершить сбор данных.
Сбор и исследование мокроты.
Два образца мокроты (один пятнистый и один ранним утром) были собраны в течение 14 дней после начала лечения и на момент получения результата лечения.У пациентов, признанных успешно пролеченными, по два образца мокроты были взяты в конце 3 -х , 6 и 12 -х месяцев после лечения или во время рецидива ТБ, если он был обнаружен в промежуточные периоды. Информация об этом была получена благодаря тесной связи с персоналом RNTCP и периодическим телефонным звонкам с пациентом.
Каждый образец был подвергнут исследованию мазка мокроты и посеву на кислотоустойчивые бациллы (КУБ) в лаборатории микобактериологии, сертифицированной RNTCP соответствующего учреждения; три из которых были национальными справочными лабораториями (NRL), а остальные три были промежуточными справочными лабораториями (IRL).Микроскопию проводили с использованием метода окрашивания Циля Нильсена или флуоресцентной микроскопии в зависимости от наличия в соответствующем институте [8]. Посев мокроты проводился на твердой среде Lowenstein Jensen (LJ) в соответствии с Учебным руководством RNTCP для Mycobacterium tuberculosis Культура и тестирование лекарственной чувствительности (ТЛЧ) [9]. Результаты были классифицированы как: отсутствие роста — отрицательные, 1–9 колоний — скудные (указано фактическое количество колоний), от 10 до 100 колоний — 1+,> 100 колоний — 2+, сплошной рост -3+, контаминированные – Cont, атипичные рост — нетуберкулезные микобактерии (НТМ).Идентификационные тесты проводились с использованием ниацинового теста, теста восстановления нитратов и быстрого анализа бокового потока MPT64. Для роста обозначен как M . tuberculosis , Тестирование лекарственной чувствительности (DST) было проведено в соответствующих NRL для H, R и E методом пропорциональной чувствительности (PST) с использованием разовой концентрации 0,2, 40 и 2 мкг / мл соответственно [9]. Любой штамм, демонстрирующий 1% или более рост на склонах, не содержащих лекарств, по сравнению с соответствующими наклонами без лекарств, считался устойчивым.Для культур, выполненных в IRL, DST проводился в соответствующем NRL или в самом IRL, если он утвержден и сертифицирован. Результаты ТЛЧ были сообщены пациенту, медицинскому работнику (МО) медицинского центра, а также районному врачу по борьбе с туберкулезом для принятия соответствующих мер в соответствии с руководящими принципами RNTCP.
Генотипирование.
Положительные исходные культуры из всех центров были доставлены в НИРТ для хранения при -80 ° C для последующего генотипирования в случае рецидива ТБ. Генотипирование также было выполнено на росте культуры, обнаруженной положительным для M . туберкулез на момент рецидива.
Культуру микобактерий получали путем культивирования на среде LJ, а затем снова субкультивировали на среде LJ для экстракции геномной ДНК. Геномная ДНК была извлечена из M . tuberculosis культур стандартным методом экстракции цетилтриметиламмонийбромидом (CTAB) –NaCl.
MIRU-VNTR генотипирование выполняли путем разделения в 2% геле, при этом каждый локус амплифицировали отдельно с помощью симплексной ПЦР [10].Полученное таким образом изображение геля использовали для проклейки. Размер продукта ПЦР определяли путем сравнения с положением маркера стандарта размера. Затем этот размер был согласован с таблицей MIRU-VNTR. Следующее было проверено перед присвоением номера аллеля.
- Консистенция с обычным аллельным диапазоном.
- Аллель контроля h47Rv правильный.
- Согласованность результатов оценивали по возрастающему интервалу между продуктами ПЦР из разных изолятов
Если паттерны MIRU были идентичны во время постановки диагноза и при рецидиве, рецидив относили к эндогенной реактивации (рецидив) и экзогенной повторной инфекции, если они отличались на 2 или более MIRU-VNTR [10].
Анализы крови.
Если пациент еще не прошел тестирование на ВИЧ, его / ее направляют в Центр интегрированного консультирования и тестирования (ICTC) во время первоначального интервью, и результаты фиксируются. Если тест на ВИЧ был отрицательным, его повторяли в случае рецидива туберкулеза у пациента.
Измерение глюкозы в капиллярной крови (CBG) проводилось с помощью глюкометра после ночного голодания. Уровень сахара в крови регистрировался у участников исследования во время первоначального интервью и во время рецидива туберкулеза.В случае аномальных значений сахара в крови (уровень глюкозы в капиллярах натощак ≥ 110 мг / дл) пациентов направляли для дальнейшей оценки, чтобы подтвердить / исключить сахарный диабет [11].
Определения исследования.
Определения, использованные в исследовании для нового пациента с ТБ, исхода лечения, рецидива ТБ, сопутствующего заболевания, личных привычек, представлены в качестве вспомогательной информации (файл S1)
Этические соображения.
Исследование было одобрено комитетами по институциональной этике каждого участвующего института.
Каждый участник исследования был проинформирован о целях и процедурах исследования с использованием информационного листа для пациентов, напечатанного на местном языке, а также устно и письменного согласия. Никого не заставляли участвовать в исследовании. Все пациенты лечились по стандартизированной схеме в ближайшем государственном учреждении здравоохранения в соответствии с рекомендациями RNTCP.
Пациентам, у которых результаты ТЛЧ показали устойчивость к одному или нескольким препаратам, лечащему врачу была предоставлена информация для необходимого изменения лечения.
Все пациенты с положительным результатом посева в конце лечения были направлены к соответствующему районному специалисту по борьбе с туберкулезом (DTO) / MO-TU для дальнейшего необходимого лечения. Результаты ТЛЧ были сообщены лечащему МО-ТУ при первой возможности. Точно так же пациенты с рецидивом были направлены на соответствующее лечение вместе с результатами мазка, посева и ТЛЧ.
Были также предприняты попытки восстановить пациентов, потерянных для последующего наблюдения во время лечения, и перевести их на режим повторного лечения в зависимости от культуры и статуса ТЛЧ в соответствии с рекомендациями RNTCP.
Сумма в рупиях. 200 / — (3 $) были даны каждому участнику исследования во время каждого интервью, забор крови или мокроты в качестве компенсации транспортных расходов и потери заработной платы, если таковая имеется.
Анализ данных.
Данные были тщательно проверены на полноту и непротиворечивость и введены с помощью Microsoft Access, 2003/2007. Данные были проанализированы с помощью SPSS версии 20.0. Количественные переменные суммировались с использованием среднего и стандартного отклонения (SD) или медианы и межквартильного диапазона (IQR), если применимо.Пропорции были вычислены для категориальных переменных. Рецидивы туберкулеза среди новых пациентов с положительным мазком мокроты, у которых был успешный исход лечения, выражали как показатель на 100 человеко-лет с 95% доверительным интервалом (ДИ). Частота рецидивов ТБ на 100 человеко-лет рассчитывалась с помощью программы Epi-Info 7.0. Поскольку ежемесячного наблюдения не проводилось, предполагалось, что событие произошло в середине периода времени между периодами наблюдения в 3, 6 и 12 месяцев.
Объединенная доля рецидивов ТБ и объединенная частота рецидивов рассчитывались по следующей формуле:
Где w i — это вес, соответствующий i -му участку , и равен 1 / Дисперсия p i
p i — доля / частота повторения в каждом сайте, а P — объединенное значение .
Стандартная ошибка была рассчитана по формуле: —
Относительный риск (RR) и Скорректированный RR (ARR) с 95% доверительным интервалом были рассчитаны с использованием модели регрессии Пуассона для определения потенциальных факторов риска неблагоприятного ответа на лечение и рецидива ТБ. Переменные со значением p ≤ 0,10 в одномерном анализе рассматривались для модели множественной регрессии, которая выполнялась методом ввода, в котором все переменные вводились за один шаг; значение p <0.05 считался статистически значимым.
Результаты
Всего было перечислено 2384 пациента, из которых 1577 были включены в исследование, число которых варьировалось от 242 до 302 в разных центрах (рис. 2). Причины отказа в включении в исследование включали возраст <18 лет, проживание вне ТУ исследования, отказ в согласии и другие причины (наличие болезни и госпитализации, нестабильность по месту жительства, предыдущее лечение против туберкулеза). После исключения 12 пациентов [потеря до лечения для последующего наблюдения (n = 8), ранее леченных (n = 3), первоначальный мазок не доступен (n = 1)], 1565 пациентов были доступны для анализа [Тамил Наду (n = 249), Карнатака (n = 230), Дели (n = 302), Махараштра (n = 246), Керала (n = 297) и Мадхья-Прадеш (n = 241)].
Исходные характеристики
Исходные характеристики 1565 пациентов показаны в таблице 1. Большинство, 1125 (72%) были мужчинами. Средний возраст ± стандартное отклонение составлял 41 ± 15 лет (диапазон от 18 до 90 лет), а средний индекс массы тела (ИМТ) ± стандартное отклонение составлял 17 ± 3 кг / м 2 (диапазон от 10 до 38 кг / м 2 ) .
Всего 884 человека (56%) были в возрасте от 18 до 44 лет. ИМТ <18,5 (недостаточный вес) наблюдался у 1053 (67%) от общего числа пациентов. 807 (52%) никогда не курили, 672 (43%) курили в прошлом и 86 (5%) курили в настоящее время.Средняя продолжительность приема алкоголя составляла 15 лет [IQR: 7–25 лет]. Было 759 (48%) потребителей, не употреблявших / никогда не употреблявших алкоголь, 779 (50%) бывших потребителей и 27 (2%) нынешних потребителей.
Из 1565 пациентов 1506 (96%) не были реактивными на ВИЧ, 48 (3%) реактивными, а ВИЧ-статус оставшихся 11 был неизвестен. Из 48 ВИЧ-реактивных пациентов 38 (79%) были помещены на анти- ретровирусное лечение.
Двести девяносто три человека (19%) страдают диабетом. Подробная информация о противодиабетических препаратах была доступна для 276 (94%): 183 (65%) принимали пероральные препараты, 54 (19%) получали инсулин и 39 (14%) принимали как инсулин, так и пероральные препараты.
Исходный мазок мокроты, посев и профиль лекарственной чувствительности
Распределение исследуемой популяции по результатам мазка мокроты, посева и ТЛЧ представлено в таблице 2.
Из 1565 пациентов 860 (55%) имели оценку мазка мокроты 2 + / 3 +. В общей сложности 1368 (87%) имели по крайней мере одну положительную исходную культуру для M . туберкулез . Было 166 (11%) с отрицательными посевами мокроты, 8 (<1%) с положительными культурами на нетуберкулезных микобактерий , 18 (1%) с контаминацией культур и 5 (<1%) с недостаточностью образцов.
Информация о тесте на лекарственную чувствительность была доступна для 1304 (95%) из 1368 пациентов с положительным посевом. из них 1173 (90%) были восприимчивы к H, R и E, а остальные 131 (10%) имели устойчивость к одному или нескольким лекарствам. Монорезистентность к H наблюдалась у 77 (6%), монорезистентность к E — у 27 (2%), устойчивость к EH — у 6 (<1%), а устойчивость к R / HR - у 20 (1,5%).
Продолжительность от появления симптомов до начала противотуберкулезного лечения
Средняя продолжительность от появления симптомов до 1 -го обращения за помощью составила 2 недели [IQR: 1–6 недель].Средняя продолжительность лечения от 1 до начала противотуберкулезного лечения составила одну неделю [IQR: 1–5 недель]. В целом, средняя продолжительность от появления симптомов до начала противотуберкулезного лечения составила 6 недель [IQR: 3–12 недель].
Конверсия мазка мокроты в конце интенсивной фазы лечения
Статус мазка мокроты в конце IP был доступен у 1442 (92%) из 1565 пациентов. Из них 1241 (86%) имели отрицательный результат мазка мазка через 2 месяца IP, а еще 146 (10%) преобразовались через 3 месяца IP; информация о месяце конверсии отсутствовала для одного пациента; в то время как остальные 54 не обратились.
Результат лечения
Из 1565 пациентов 1210 (77%) были успешно вылечены (вылечены: 1207, лечение завершено: 3) [Таблица 3]. Неудача лечения наблюдалась у 126 (8%) и 93 (6%) пациентов умерли во время лечения туберкулеза. Период смерти от начала лечения имелся у 84 (90%) пациентов; 44 (52%) умерли в течение 60 дней после начала лечения. Девяносто шесть (6%) пациентов были потеряны из-за лечения. Причины потери лечения были получены от 82 (85%) пациентов; это были связанные с употреблением алкоголя у 29 (35%), исчезновение симптомов у 20 (24%), побочные эффекты наркотиков у 7 (8%), связанные с работой у 1 (1%) и другие 31 (38%), которые включал миграцию / отказ от приема лекарств.
18 (1%) из общего числа перешли на лечение МЛУ-ТБ. Лечение было изменено для 15 (1%) пациентов: по поводу диабета (n = 8), по клиническим показаниям (n = 6), у которых была продлена фаза продолжения, и у одного по медицинским показаниям (почечная недостаточность). Было 7 (<1%) пациентов, результаты лечения которых не оценивались.
Рецидив ТБ
Из 1210 успешно пролеченных пациентов 950 (79%) имели безрецидивную выживаемость через 12 месяцев наблюдения, 158 (13%) имели рецидивы в различные моменты времени в течение периода наблюдения, 73 (6%) были потеряны из-за наблюдение через 12 месяцев, 29 (2%) умерли [Таблица 4].Взвешенная доля пациентов, у которых был рецидив ТБ, составляла 10,9% [95% ДИ: 0,2–21,6], а частота рецидивов ТБ на 100 человеко-лет составляла 12,7 [95% ДИ: 0,4–25].
На долю легочного туберкулеза пришлось 155 (98%) из 158 рецидивов туберкулеза, и у 3 был туберкулезный лимфаденит. Из пациентов с ПТБ 150 были бактериологически положительными [Таблица 5].
В общей сложности 87 (55%) пациентов имели рецидив ТБ в течение 3 месяцев после лечения, и в общей сложности 122 (77%) пациентов произошли в течение 6 месяцев.
Из 150 пациентов, у которых был бактериологически подтвержденный рецидив ТБ, у 123 были доступные исходные и повторные посевы мокроты, положительные на M . tb и подходили для генотипирования. Детали генотипирования были доступны для 60 (49%) из 123 пациентов, в то время как ДНК не удалось извлечь у остальных 63 пациентов. Эндогенная реактивация наблюдалась у 56 (93%) пациентов. У двух ВИЧ-положительных пациентов с рецидивом произошла эндогенная реактивация. Генотипирование невозможно было провести у 63 пациентов, так как ДНК не удалось извлечь из-за недостаточного роста или загрязнения.
Факторы риска неблагоприятного исхода противотуберкулезного лечения
Факторы, проанализированные для неблагоприятного ответа в конце лечения, включали пол, возрастную группу, ИМТ, исходный уровень мазка мокроты, уровень культуры, профиль лекарственной чувствительности, диабет и антидиабетические препараты, статус ВИЧ и АРТ, курение, алкоголь, продолжительность фазы интенсивного лечения, места лечения, продолжительности от симптомов до начала лечения и пропущенных доз в интенсивной фазе (таблица 6).Ни один из проанализированных факторов не был связан с неблагоприятным ответом на лечение.
Факторы риска рецидива ТБ
Факторы, проанализированные на предмет рецидива ТБ, включали пол, возрастную группу, ИМТ, исходный уровень мазка мокроты, уровень посева, профиль лекарственной чувствительности, диабет и антидиабетические препараты, статус ВИЧ и АРТ, продолжительность интенсивной фазы лечения, тип DOT , курение и употребление алкоголя во время лечения и / или последующего наблюдения, респираторные симптомы в конце лечения, продолжительность противотуберкулезного лечения, увеличение веса во время лечения и пропущенные дозы в интенсивной фазе (таблица 7).Из всех факторов, проанализированных у 1108 пациентов с успешным лечением, мужской {ARR: 2,4 [95% ДИ: 1,3–4,6] (p = 0,006)} был связан с рецидивом ТБ.
Более высокая доля ВИЧ-реактивных пациентов имела рецидивы по сравнению с ВИЧ-реактивными пациентами; однако эта разница не была значимой из-за небольшого числа ВИЧ-реактивных пациентов.
Обсуждение
Это первое исследование, в котором была предпринята попытка определить частоту рецидивов ТБ при 6-месячной схеме лечения трижды в неделю в условиях программы в Индии среди новых пациентов с положительным мазком мокроты, распределенных в разных географических регионах.Мы наблюдали частоту рецидивов ТБ на уровне 12,7 на 100 человеко-лет в течение первого года после того, как они были объявлены успешно вылеченными. Что касается пропорций, 10,9% испытали рецидив, что было похоже на более ранние исследования, проведенные в разных географических точках страны в разные моменты времени. В систематическом обзоре сообщалось о 10% рецидивах после успешного лечения среди пациентов, получавших DOTS в Индии [12]. В более раннем исследовании, проведенном в штате Тамил Наду, Южная Индия, у 12% успешно пролеченных больных ТБ наблюдались рецидивы, когда образцы мокроты собирались через 6, 12 и 18 месяцев после лечения и исследовались посевом [5].Исследования в Гуджарате и Бангалоре сообщили о доле рецидивов на уровне 10,8% и 11,4% соответственно, когда пациенты проходили одноразовое интервью через 2 года и 2,5 года после успешного лечения; эти исследования были ограничены в подходе, включая систематическую ошибку воспоминаний [4, 13]. В нашем исследовании 77% наблюдаемых рецидивов произошли в течение 6 месяцев. В исследовании, проведенном в Тамил Наду, как указано выше, 77% всех рецидивов, наблюдаемых в течение 18 месяцев, произошли в течение 6 месяцев и 92% — в течение 12 месяцев [5].
В нашем исследовании вероятность рецидива туберкулеза была связана с большей вероятностью мужского пола.Наши результаты противоречили более раннему систематическому обзору, проведенному в Индии, в котором сообщалось, что секс не является фактором риска рецидива ТБ [12]. Факторы риска рецидива ТБ, о которых сообщалось в более ранних исследованиях, включали диабет, ВИЧ, курение, алкоголизм, исходную лекарственную устойчивость и нерегулярность приема лекарств [12,14,15]. Однако в настоящем исследовании такой связи не наблюдалось, что может быть связано с тем ограничением, что исследование, особенно размер выборки, не было специально разработано для этой цели. Поскольку хорошо известно, что легочный туберкулез гораздо чаще встречается у мужчин, чем у женщин, было бы разумно предположить, что рецидивы туберкулеза также могут иметь такую склонность.Однако мы хотели бы повторить, что исследование не было специально разработано для выявления факторов риска. Наблюдение о том, что у мужчин вероятность рецидива туберкулеза выше, необходимо изучить в будущих исследованиях.
рецидив туберкулеза произошел в основном из-за эндогенной реактивации, как предполагают результаты генотипирования в нашем исследовании. Это плохо отражается на эффективности режима в соответствии с настройками программы с точки зрения его способности предлагать безрецидивное лечение. Предыдущее молекулярное исследование, проведенное в Индии, документально подтвердило, что большинство (88%) рецидивов ТБ у ВИЧ-инфицированных пациентов были вызваны экзогенной повторной инфекцией, в то время как большинство (91%) рецидивов ТБ у неинфицированных ВИЧ были вызваны эндогенной реактивацией [16].Аналогичным образом, в нашем исследовании большинство (93%) повторных случаев туберкулеза у ВИЧ-инфицированных пациентов были вызваны эндогенной реактивацией.
Показатель излечения в нашем исследовании составил 77%. Это ниже по сравнению с целевым показателем RNTCP в 90% [17]. Возможная причина может быть связана с определением излечения в нашем исследовании, которое включало отрицательные результаты мазка и культуры, в то время как RNTCP учитывает только отрицательный результат мазка мокроты. Исследования, проведенные с участием новых пациентов с легочным туберкулезом с положительным мазком в различных частях Индии, показали уровень излечения 77% в Мангалоре (n = 212), 83.8% в Химачал-Прадеше (n = 130), 74% в округе Тируваллур, Тамил Наду (n = 295) [18–20]. Частота неудач в 8%, наблюдаемая в нашем исследовании, вдвое превышает ожидаемую цель RNTCP в 4%, в то время как общая доля смертей во время лечения и потерянных для последующего наблюдения за лечением была незначительно выше — по 6% в каждом случае, чем ожидаемая цель в 5% [17 ]. Предыдущие исследования документально подтвердили, что мужчины, возраст, алкоголизм, курение, туберкулез с множественной лекарственной устойчивостью, масса тела <35 кг и пропущенные дозы связаны с потерей лечения, неудачей или смертью [4, 20–23].Однако в настоящем исследовании не было обнаружено, что ни один из факторов связан с исходом лечения, что опять же может быть связано с тем, что исследование не было разработано для этой цели.
Конверсия мокроты 96% в конце интенсивной фазы лечения соответствует целевому показателю RNTCP> 90% [17]. Кроме того, мы заметили, что 89% из них обратились за 2 месяца. Исследование, проведенное в Гувахати, зафиксировало 84% конверсию мазка в конце 2 месяцев у 100 новых пациентов с ПТБ с положительным мазком [24].Напротив, ретроспективное исследование, проведенное в районе Тумкур в Индии, зафиксировало конверсию мазка мокроты на 66,7% в конце 2 месяцев лечения у 268 новых пациентов с ПТБ с положительным мазком [25]. Мы не пытались собирать мокроту в рамках процедур исследования в конце интенсивной фазы лечения и задокументировали статус мазка мокроты из карт лечения туберкулеза.
Мы наблюдали среднюю задержку в 6 недель от появления симптомов до начала лечения. В систематическом обзоре задержки в диагностике и лечении пациентов с легочным туберкулезом в Индии сообщается, что средняя задержка составляет 57.5 дней от появления симптомов до начала лечения [26]. Средняя задержка от появления симптомов до 1 обращений за помощью составила 19,4 дня в систематическом обзоре по сравнению с 2 неделями, наблюдаемыми в нашем исследовании [26]. Различия между учреждениями для средней задержки от появления симптомов до начала лечения в нашем исследовании, которая варьировалась от 3 недель до 12 недель, подчеркивают важность выявления причин, связанных с пациентом и поставщиком медицинских услуг, и разработки новых стратегий для уменьшения задержки.
Исследование имеет несколько присущих ему ограничений. Мы не собирали данные о радиологической степени заболевания. Подробности курения и алкоголя сообщались самостоятельно. Нам не удалось провести генотипирование всех положительных культур рецидивирующего ТБ из-за недостаточного роста.
Наши результаты показывают, что у значительной части новых пациентов с туберкулезом легких с положительным мазком мокроты, успешно пролеченных 6-месячным режимом трижды в неделю, в условиях программы наблюдается рецидив туберкулеза. В настоящее время RNTCP пересмотрела схему лечения, и в настоящее время рекомендуется 6-месячный ежедневный курс комбинированных препаратов с фиксированной дозой (FDC).
Благодарности
Мы благодарны доктору Сумье Сваминатан, бывшему директору NIRT и DG -ICMR, за ее поддержку. Мы признательны за вклад штатным фтизиатрам, медицинским работникам и сотрудникам RNTCP округов. Мы признательны за вклад полевых исследователей в набор участников исследования, последующее наблюдение и сбор данных. Благодарим сотрудников лаборатории за их поддержку. Мы высоко ценим вклад операторов ввода данных, участвующих в вводе и проверке данных.Мы благодарим зачисленных пациентов за их ценный вклад в исследование.
Список литературы
- 1.
Всемирная организация здоровья. Глобальный доклад о туберкулезе, 2017 г. Женева: 2017 г. http://apps.who.int/iris/bitstream/10665/259366/1/9789241565516-eng.pdf?ua=1. (Проверено 25 ноября 2017 г.) - 2.
Центральное противотуберкулезное отделение. Пересмотренная Национальная программа борьбы с туберкулезом. Управление RNTCP в вашем регионе — Учебный курс (Модуль 1–4). http://www.tbcindia.nic.in/showfile.php? lid = 2907 (последнее посещение — 4 июля 2017 г.) - 3.
TB India 2017. Отчет о статусе RNTCP. Центральное противотуберкулезное отделение, Главное управление здравоохранения. Министерство здравоохранения и благополучия семьи, Нирман Бхаван, Нью-Дели. http://tbcindia.gov.in/WriteReadData/TB%20India%202017.pdf (по состоянию на 4 июля 2017 г.) - 4.
Виджай С., Баласангамешвара В.Х., Джеганнатха П.С., Сароджа В.Н. и Кумар П. Результаты лечения и статус наблюдения в течение двух с половиной лет новых пациентов с положительным мазком мокроты, получавших лечение в рамках RNTCP.Ind J Tuberc 2004; 51: 199–208. - 5.
Томас А., Гопи П.Г., Сантха Т., Чандрасекаран В., Субрамани Р., Сельвакумар Н. и др. Предикторы рецидива среди пациентов с туберкулезом легких, проходящих лечение по программе DOTS в Южной Индии. Int J Tuberc Lung Dis 2005; 9 (5): 556–561 pmid: 15875929 - 6.
Государственные информационные бюллетени, март 2014 г. Департамент по борьбе со СПИДом, Министерство здравоохранения и благополучия семьи, Правительство Индии http://naco.gov.in/sites/default/files/State_Fact_Sheet_2013_14.pdf (доступ 10 апреля 2018 г.) - 7.
Сообщение для прессы об оценке бедности, 2011–2012 гг. Комиссия по планированию правительства Индии, июль 2013 г. http://planningcommission.nic.in/news/pre_pov2307.pdf (по состоянию на 10 апреля 2018 г.) - 8.
Пересмотренная Национальная программа борьбы с туберкулезом. Руководство по флуоресцентной микроскопии мазка мокроты. Центральный отдел туберкулеза Генеральный директорат службы здравоохранения Министерства здравоохранения и благополучия семьи, Нирман Бхаван, Нью-Дели. https://tbcindia.gov.в / showfile.php? lid = 2988. (Проверено 4 июля 2017 г.) - 9.
Пересмотренное Учебное пособие Национальной программы борьбы с туберкулезом по культуре Mycobacterium tuberculosis и тестированию на лекарственную чувствительность. Апрель 2009 г. Главное управление по борьбе с туберкулезом, Главное управление служб здравоохранения, Министерство здравоохранения и благополучия семьи, Нирман Бхаван, Нью-Дели. http://tbcindia.nic.in/WriteReadData/l892s/6995271860Training%20manual%20M%20tuberculosis%20C%20DST.pdf. (Проверено 4 июля 2017 г.) - 10.
Мультилокусное количество переменных Тандемное повторение.Техническое руководство по генотипированию Mycobacterium tuberculosis. Филип Снабжение. INSERM U629. Institut de Biologie / Institut Pasteur de Lille, май 2005 г. http://www.miru-vntrplus.org/MIRU/files/MIRU-VNTRtypingmanualv6.pdf - 11.
Диагностика диабета, преддиабета и метаболического синдрома. Показания к скринингу. Ведение сахарного диабета II типа. Академические рекомендации по клинической помощи 2009 г. (Часть 1). http://www.diabetesindia.com/diabetes/cons_pre-diabetes_metabolic.htm. (Проверено 4 июля 2017 г.) - 12.Ажар Г.С. ДОТС при рецидиве туберкулеза в Индии: систематический обзор. Lung India 2012; 29 (2): 147–53. pmid: 22628930
- 13.
Дэйв П., Раде К., Моди Б., Соланки Р., Патель П., Шах А., Вейд и др. Оценка долгосрочного результата среди новых пациентов с легочным туберкулезом с положительным мазком мазка, получавших прерывистый режим в рамках ретроспективного когортного исследования RNTCP – A. Natl J Community Med 2013; 4 (2): 189–194. - 14.
Trinh QM, Nguyen HL, Nguyen VN, Nguyen TV, Sintchenko V, Marais BJ.Сочетание туберкулеза и ВИЧ-инфекции в Азиатско-Тихоокеанском регионе. Int J Infect Dis. 2015; 32: 170–8. pmid: 25809776 - 15.
Бейкер М.А., Харрис А.Д., Чон С.Ю., Харт Дж. Э., Капур А., Лённрот К. и др. Влияние диабета на результаты лечения туберкулеза: систематический обзор. BMC Med. 2011; 9: 81. pmid: 21722362 - 16.
Нараянан С., Сваминатан С., Сапплай П., Шанмугам С., Нарендран Г., Хари Л. и др. Влияние ВИЧ-инфекции на рецидив туберкулеза в Южной Индии.J Infect Dis 2010; 201: 691–703. pmid: 20121433 - 17.
Центральное противотуберкулезное отделение. Пересмотренная Национальная программа борьбы с туберкулезом. Управление RNTCP в вашем районе — Учебный курс (Модуль 5–9) http://www.tbcindia.nic.in/showfile.php?lid=2911 (по состоянию на 4 июля 2017 г.) - 18.
Джозеф Н., Нагарадж К., Бхат Дж., Бабу Р., Котиан С., Ранганатха И. и др. Результаты лечения новых случаев туберкулеза с положительным мазком и повторного лечения туберкулеза в Мангалоре, Южная Индия — описательное исследование. Австралас Мед Дж.2011; 4 (4): 162–7 pmid: 23393507 - 19.
Sharama A, Kansal D, Katoch K, Sharma PK, Bansal R, Tarun Sharma T. Результат лечения новых пациентов с туберкулезом легких с положительным мазком мокроты, получавших лечение под непосредственным наблюдением, краткосрочный курс в сельской больнице третичного уровня в холмистой местности Int J Общественное здравоохранение. 2016; 3 (8): 2129–2132 - 20.
Сантха Т., Гарг Р., Фриден Т.Р., Чандрасекаран В., Субрамани Р., Гопи П.Г. и др. Факторы риска, связанные с невыполнением, неудачей и смертью среди больных туберкулезом, лечившихся по программе DOTS, в округе Тируваллур, Южная Индия, 2000 г.Int J Tuberc Lung Dis. 2002. 6 (9): 780–8. pmid: 12234133 - 21.
Рой Н., Басу М., Дас С., Мандал А., Датт Д., Дасгупта С. Факторы риска, связанные с невыполнением обязательств среди больных туберкулезом в районе Дарджилинг в Западной Бенгалии, Индия. J Family Med Prim Care. 2015; 4 (3): 388–94. pmid: 26288779 - 22.
Баса С., Венкатеш С. Исследование невыполнения обязательств и связанных с этим факторов среди больных туберкулезом, проходящих лечение по программе DOTS, в районе Маюрбхандж, Одиша. J Health Res Rev 2015; 2: 25–8. - 23.
Падмаприядарсини К., Шобана М., Лакшми М., Бина Т., Сваминатан С. Недоедание и туберкулез в Индии: анализ ситуации и путь вперед. Индийский J Med Res. 2016; 144 (1): 11–20. pmid: 27834321 - 24.
Bawri S, Ali S, Phukan C, Tayal B, Baruwa P. Изучение конверсии мокроты у новых случаев туберкулеза легких с положительным мазком с интервалом в 1, 2 и 3 месяца в режиме краткосрочного курса лечения под непосредственным наблюдением (DOTS).Легкая Индия. 2008. 25 (3): 118–23. pmid: 20165663 - 25.
Йеллаппа В., Кандпал В., Лалл Д., Табассум А. Детерминанты конверсии мокроты через два месяца лечения в рамках пересмотренной национальной программы борьбы с туберкулезом, Южная Индия. Int J Med Sci Public Health 2016; 5: 2416–2420 - 26.
Sreeramareddy CT, Qin ZZ, Satyanarayana S, Subbaraman R, Pai M. Задержки в диагностике и лечении туберкулеза легких в Индии: систематический обзор. Int J Tuberc Lung Dis. 2014. 18 (3): 255–66.pmid: 24670558
Новый метод прогнозирования риска рецидива туберкулеза
Поделиться
Статья
Вы можете поделиться этой статьей в соответствии с международной лицензией Attribution 4.0.
Тестирование Mycobacterium tuberculosis Согласно новому исследованию, бактерий, вызывающих туберкулез (ТБ), могут идентифицировать большинство людей с высоким риском рецидива заболевания до начала лечения.
«Самым важным признаком успешного лечения туберкулеза является частота рецидивов», — говорит Дэвид Алланд, профессор и заведующий кафедрой инфекционных заболеваний медицинского факультета Университета Рутгерса.
«Примерно у пяти процентов пациентов с лекарственно-чувствительным туберкулезом или туберкулезом, который поддается эффективному лечению, через шесть месяцев после первого лечения наблюдается рецидив. Примерно у 20 процентов пациентов через четыре месяца после терапии случается рецидив », — говорит Алланд.
Диапазон сопротивления
Исследование показывает текущий подход к разделению M.tuberculosis на «лекарственно-чувствительные» и «лекарственно-устойчивые» — это слишком упрощенно. Даже среди группы, чувствительной к лекарствам, существует диапазон устойчивости, который имеет решающее значение для прогнозирования результатов лечения туберкулеза.
Новые результаты, опубликованные в журнале New England Journal of Medicine , предполагают, что стандартные критерии, также называемые «контрольными точками», используемые для определения лекарственной устойчивости, могут нуждаться в обновлении.
«Свойства, присущие бактериям, в сочетании с легко доступной клинической информацией, относящейся к каждому инфицированному пациенту, можно использовать для прогнозирования результатов лечения», — говорит Роберто Коланджели, доцент кафедры медицины.«Это также говорит о том, что сила противотуберкулезного препарата так же важна, как и механизм действия при лечении туберкулеза».
Сокращение времени лечения
Исследователи
Insights, собранные в ходе исследования, раскрывают способ определить, какие пациенты могут лечиться от туберкулеза в течение четырех месяцев вместо шести. Они также определяют, какие пациенты должны получать лечение более шести месяцев, чтобы добиться излечения.
«Стандартная шестимесячная многокомпонентная терапия увеличивает риск токсических эффектов, несоблюдения режима лечения и развития лекарственной устойчивости, а также ложится бременем на системы здравоохранения», — говорит Алланд.
«Сокращение времени лечения даже на два месяца потенциально означало бы значительную экономию средств для программ общественного здравоохранения, а также лучшие результаты лечения людей, инфицированных туберкулезом», — объясняет он.
Источник: Университет Рутгерса
Когда туберкулезная инфекция возвращается — Туберкулезный центр
Туберкулез — потенциально опасная для жизни бактериальная инфекция, передающаяся по воздуху, которую можно найти во всем мире. Схема лечения длительная, но если вы будете ее придерживаться и принимать лекарства так, как вам следует, вы можете победить болезнь.Однако даже после лечения повторное заражение туберкулезом становится проблемой.
Длительный курс лечения туберкулеза
У людей, больных туберкулезом, очень часто возникают рецидивы во время лечения. Лечение симптомов туберкулеза может длиться от шести месяцев до года, а иногда и больше при лекарственно-устойчивом туберкулезе. Есть несколько таблеток, которые нужно принимать каждый день — в одно и то же время каждый день, — иначе лечение может не сработать.
Вы можете почувствовать себя лучше и подумать, что ваш туберкулез успешно вылечен, только для того, чтобы узнать, что он вернулся — сильнее и труднее лечить. Или вы, возможно, все сделали правильно и болезнь исчезла, только чтобы обнаружить, что вы снова инфицированы туберкулезом.
Как происходит повторное заражение туберкулезом
Существует много споров о том, вызван ли рецидив туберкулеза рецидивом — повторным заболеванием тем же штаммом туберкулеза даже после лечения — или повторным заражением туберкулезом новым штаммом бактерий.
В Соединенных Штатах и Канаде, похоже, что большинство рецидивирующих случаев туберкулеза являются рецидивом первоначальной инфекции, возможно, из-за недостаточного лечения, а не из-за повторного заражения туберкулезом новым штаммом бактерий.
В других частях мира ситуация иная. В исследовании, проведенном в Кейптауне, Южная Африка, где туберкулез очень распространен, 18 процентов из 612 участников исследования были повторно инфицированы туберкулезом. Четырнадцать процентов этих пациентов были успешно вылечены от своей болезни и снова были инфицированы другим штаммом туберкулеза.
Многие люди могут болеть так называемой латентной туберкулезной инфекцией, что означает, что у них нет симптомов туберкулеза, но бактерии все еще находятся в их организме. Как только бактерии становятся активными и вызывают симптомы туберкулеза, инфекция переходит в активный туберкулез.
Кто повторно заражается?
Основываясь на результатах исследования в Кейптауне, исследователи не обнаружили никаких факторов риска, которые повышали вероятность повторного заражения туберкулезом у людей.
Люди, которые болели туберкулезом раньше и заболели им снова, подвергаются гораздо более высокому риску развития туберкулеза, чем те, кто никогда не болел.Необходимо провести дополнительные исследования, но ученые подозревают, что некоторые люди могут быть более восприимчивы к туберкулезу, чем другие, по неизвестным пока причинам.
Другое исследование, проведенное на ВИЧ-положительных людях, инфицированных туберкулезом, предполагает, что ВИЧ делает их более восприимчивыми к повторному заражению туберкулезом, чем пациенты, не инфицированные ВИЧ.
Лечение реинфекции туберкулеза
Лечение рецидивирующего туберкулеза, вызванного рецидивом — лечение, которое было неэффективным или было неполным — сложно.Часто бактерии становятся устойчивыми к лечению, и рекомендуется использовать другую комбинацию лекарств в течение более длительного периода времени.
Одно исследование показало, что основной причиной лекарственно-устойчивого туберкулеза, который наиболее трудно поддается лечению, является повторное инфицирование. Даже когда повторное заражение туберкулезом происходит от другого штамма бактерий, рецидивирующий тип часто оказывается устойчивым к лекарствам, что означает, что какая-то мутация исходного штамма бактерий не реагирует на лекарства.
Если рецидивирующий случай поддается лечению, его можно успешно вылечить. Опять же, режим необходимо соблюдать в точности.
Предотвращение повторного заражения туберкулезом
Невозможно всегда предотвратить туберкулез, будь то первичная или рецидивирующая инфекция. Но вы можете предпринять шаги, чтобы снизить свой риск.
Для людей с ВИЧ одним из способов предотвращения повторного заражения туберкулезом является использование антибиотика изониазида (INH). После завершения лечения туберкулеза курс профилактических антибиотиков может стать вариантом снижения риска повторного заражения туберкулезом у ВИЧ-положительных людей.
Лучший способ предотвратить повторное появление туберкулеза — всегда принимать лекарства в точном соответствии с рекомендациями врача. И как бы очевидно это ни звучало, ограничение контакта с людьми, которые могут быть заражены туберкулезом, также снижает риск повторного заражения.
Предикторы рецидива среди пациентов с туберкулезом легких, проходящих лечение по программе DOTS в Южной Индии
Справочная информация: Туберкулез является серьезной проблемой общественного здравоохранения в Йемене. Рецидив туберкулеза еще больше усложняет ситуацию и имеет серьезные негативные последствия для экономики и здоровья.Это исследование оценило частоту рецидивов туберкулеза в течение 5-летнего периода наблюдения и выявило факторы риска, связанные с рецидивом.
Методы. Это было проспективное исследование с 5-летним периодом наблюдения, проведенное в медицинских центрах с противотуберкулезными отделениями в десяти провинциях. Участники были проспективно включены в исследование с июля 2007 года по июнь 2008 года, причем последний пациент завершил лечение 15 марта 2009 года.
Результаты: когорта из 814 пациентов с туберкулезом легких завершила лечение и находилась под наблюдением в течение пяти лет.В ходе последующего наблюдения 3,4% (n = 28) умерли, а 4,3% (n = 35) были потеряны для участия в исследовании, что дало окончательную когорту из 751 пациента. Средний возраст ± стандартное отклонение составил 32 ± 13 лет. Мужчины составляли 57,6% испытуемых. Общая частота рецидивов туберкулеза составила 9,5% (71/751) со значительными различиями между подгруппами пациентов (диапазон = 7–25,8%). Наибольшая частота рецидивов была обнаружена у пациентов с диабетом (25,8%, p <0,001), несоблюдавшихся пациентов (22%, p <0,001), курильщиков (16,1%, p =.010), пациенты с полостным заболеванием легких (14,4%, p = 0,004), пациенты с увеличением веса ≤5% во время интенсивной фазы (13,3%, p <0,001) и безработные пациенты (11,9%, p = 0,017) . В многомерном логистическом регрессионном анализе эти факторы риска были независимо связаны с рецидивирующим туберкулезом: диабет (скорректированное отношение шансов, AOR 3,78, 95% доверительный интервал, CI 1,84–7,80), несоблюдение (AOR 3,22, 95% CI 1,76–5,87). , прибавка в весе ≤5% (aOR 2,51, 95% CI 1,39–4,55), курение (aOR 2,18, 95% CI 1.07–4.47), наличие кавитации в легких (aOR 2,01, 95% CI 1,16–3,46) и безработицы (aOR 2,15, 95% CI 1,16–4,01).
Заключение: частота рецидивов туберкулеза в Йемене была высокой. Наличие факторов риска у вновь диагностированных пациентов должно насторожить медицинских работников. Поскольку большинство факторов риска можно изменить, модель Всемирной организации здравоохранения, ориентированная на пациента при лечении туберкулеза, должна продвигаться во всех туберкулезных центрах страны.
Краткий курс терапии под непосредственным наблюдением — плюс в сравнении с DOTS для повторного лечения рецидива легочного туберкулеза в Гуанчжоу — Полный текст
Цели: 1) Оценить эффективность и результаты повторного лечения легочного туберкулеза в Гуанчжоу с помощью предварительного лечения тесты на чувствительность при выборе схемы химиотерапии & 2) Изучить прогностические факторы неблагоприятных исходов при повторном лечении легочного туберкулеза в Гуанчжоу, где неблагоприятные исходы включают неудачи лечения и рецидивы.
Пациенты будут рандомизированы в одну из следующих категорий: а) стратегия DOTS, состоящая из следующих мер: политическая приверженность, выявление случаев посредством бактериологической оценки, стандартизованное лечение с наблюдением и поддержкой пациентов, эффективная система снабжения лекарствами, а также система отчетности и регистрации, которая позволяет оценка лечения; или b) Стратегия DOTS-Plus включает дополнительные меры, включая постоянный надзор за лекарственной устойчивостью, культивирование, тестирование лекарственной чувствительности для пациентов с ТБ и адаптацию индивидуальной схемы приема лекарств с использованием препаратов первого и второго ряда.
Первичной конечной точкой является 18-месячный комбинированный неэффективность лечения / рецидив (неблагоприятный исход) в группе, устойчивой к рифампицину. Вторичные конечные точки включают 30-месячный комбинированный неэффективность лечения / рецидив (неблагоприятный исход) в группе с устойчивостью к рифампицину, случаи туберкулеза с множественной лекарственной устойчивостью (МЛУ-ТБ) и все случаи повторного лечения; Мазок мокроты / коэффициент конверсии через 2, 3, 8, 12, 18 и 24 мес .; Показатели лекарственной устойчивости к различным лекарствам, в частности рифампицину, и заболеваемость МЛУ-ТБ.Будут проанализированы факторы прогнозирования неблагоприятных исходов лечения (включая неудачи и рецидивы).
Ведение случаев повторного лечения только с помощью DOTS часто бывает проблематичным, особенно когда имеется резистентность к рифампицину, и это может привести к неудаче / рецидиву лечения с дальнейшим сопротивлением. Благодаря реализации стратегии «ДОТС-плюс» Гонконг (Гонконг) добился низкого уровня распространенности МЛУ-ТБ — около 1%. Это исследование предоставит важные данные о предикторах неэффективности лечения / рецидива в случаях повторного лечения, а также о том, может ли стратегия DOTS-plus эффективно снизить частоту неудач / рецидивов и распространенность МЛУ-ТБ в Гуанчжоу.Проект предоставит полезные данные по надзору, эпидемиологии и контролю за туберкулезом со стороны общественного здравоохранения, имеющие региональное (трансграничное) значение.
Понимание диагностики, лечения и рецидивов внелегочного туберкулеза: туберкулез перикарда
28 -й Всемирный конгресс по кардиологии и болезням сердца
05-06 ноября 2018 | Амстердам, Нидерланды
Дженнифер Коллинз
Ливерпульская школа тропической медицины, Великобритания
Плакаты и принятые тезисы : J Clin Exp Cardiolog
Аннотация :
Общие сведения: внелегочный туберкулез — это множество проявлений туберкулеза, которые, как известно, опасны для жизни и,
в некоторых случаях вызвать пожизненную инвалидность.Ведение туберкулеза легких уже давно находится на переднем крае общественного здравоохранения.
стратегии, однако, внелегочному туберкулезу не уделялось такого же внимания. В настоящее время нет набора параметров для
диагностика, лечение и рецидив туберкулезного перикардита в медицинских или исследовательских кругах.
Цель: Целью этого исследования было понять текущие клинические рабочие параметры для диагностики, лечения и рецидива
внелегочный туберкулез; Туберкулезный перикардит в медицинских и научных кругах.
