симптомы, лечение пневмонии у взрослых — клиника «Добробут»
Воспаление легких – виды, симптомы, лечение
Пневмония (воспаление легких) – воспалительный процесс, который развивается в одном или одновременно двух легких. Как правило, пневмония имеет инфекционную этиологию: может быть спровоцирована вирусами, грибками или болезнетворными бактериями. Назначение лечения воспаления легких у взрослых всегда вариативно и зависит от того, какой конкретно вид заболевания диагностирован.
Рассматриваемая патология может быть следствием обычной простуды. Поэтому при возникновении характерных симптомов пневмонии необходимо в кратчайшее время обратиться к семейному доктору.
Виды и симптомы воспаления легких
Клинические проявления воспаления легких во многом определяются причиной заболевания, а также распространённостью инфильтративного процесса в легочной ткани. По объему поражения выделяют: очаговую, полисегментарную, долевую. Также процесс может быть односторонним, либо двусторонним. Обычными проявлениями пневмонии являются общая слабость, утомляемость, озноб, резкий подъем температуры тела до высоких цифр 38–40°C. Частым симптомом является сухой кашель, который со временем становится влажным с трудно отделяемой слизисто-гнойной мокротой. Когда при пневмонии вовлекается в процесс плевра – это сопровождается выраженным болевым синдромом, что усиливается при попытке сделать глубокий вдох. Тяжелое течение пневмонии часто сопровождается одышкой, бледностью или синюшностью кожи в области носогубного треугольника. У детей, лиц пожилого возраста симптомы интоксикации могут значительно преобладать в клинической картине. В зависимости от объема поражения легочной ткани выделяют очаговую, долевую и тотальную формы пневмонии. Очаговая пневмония развивается постепенно: повышается температура, появляется сухой кашель. Крупозная пневмония начинается с повышения температуры тела до 39-40°C, сильного озноба, появления боли в грудной клетке, кашля.
Также процесс может быть односторонним, либо двусторонним. Обычными проявлениями пневмонии являются общая слабость, утомляемость, озноб, резкий подъем температуры тела до высоких цифр 38–40°C. Частым симптомом является сухой кашель, который со временем становится влажным с трудно отделяемой слизисто-гнойной мокротой. Когда при пневмонии вовлекается в процесс плевра – это сопровождается выраженным болевым синдромом, что усиливается при попытке сделать глубокий вдох. Тяжелое течение пневмонии часто сопровождается одышкой, бледностью или синюшностью кожи в области носогубного треугольника. У детей, лиц пожилого возраста симптомы интоксикации могут значительно преобладать в клинической картине. В зависимости от объема поражения легочной ткани выделяют очаговую, долевую и тотальную формы пневмонии. Очаговая пневмония развивается постепенно: повышается температура, появляется сухой кашель. Крупозная пневмония начинается с повышения температуры тела до 39-40°C, сильного озноба, появления боли в грудной клетке, кашля. Заболевание может сопровождаться одышкой, лихорадочным румянцем щек, который более выражен на стороне поражения.
Заболевание может сопровождаться одышкой, лихорадочным румянцем щек, который более выражен на стороне поражения.
Суточные колебания температуры тела при пневмонии могут быть в пределах 1,5 градусов. Повышение наблюдается чаще всего к вечеру. Как правило скачки температуры тела при своевременном медицинском вмешательстве длятся до 3 дней.
При крупозной пневмонии у больного в мокроте могут появиться прожилки крови.
Врачи должны также провести полную диагностику и дифференцировать пневмонию от туберкулеза – симптомы этих заболеваний идентичны.
Виды по условию возникновения
Выделяют внебольничные пневмонии и внутрибольничную (госпитальную) пневмонию. Внутрибольничной считается форма, развивающаяся в условиях стационара, клиники спустя 48 часов после госпитализации пациента по иным показаниям. Выделяют данную разновидность воспаления легких по причине особенностей протекания и лечения, так как в условиях стационаров и больниц нередко развиваются штаммы инфекционных возбудителей, устойчивые к антибактериальной терапии.
Аспирационная форма, развивающаяся вследствие попадания в нижние дыхательные пути содержимого полости рта, носоглотки или желудка, а также инородных частиц в виде твердых тел. Бактериальные возбудители, находящиеся в аспирационных массах или предметах, развиваются и вызывают тяжелый вид воспаления с гнойными осложнениями: выработкой гнойной мокроты, затрудненностью ее транспортировки и значительными поражениями тканей легкого.
Существует еще несколько видов и форм рассматриваемого воспалительного процесса. Все данные об этом, а также информацию о том, как вылечить воспаление легких, можно найти на страницах нашего сайта: https://www.dobrobut.com/.
Общие правила лечения воспаления легких
Прежде чем начинать терапию, направленную на избавление от патологии, больной должен пройти полноценное обследование. Любые диагностические и терапевтические процедуры/манипуляции проводятся только в условиях стационара. Если диагностируется воспаление легких без температуры и кашля, специалисты должны исключить другие заболевания органов дыхания – например, туберкулез или онкологию.
Выбор схемы лечения и конкретный подбор лекарственных средств осуществляется в индивидуальном порядке. Но существует и общий принцип терапии при воспалительном процессе в легких:
- Антибактериальные препараты. Должны быть назначены в обязательном порядке. Если пневмония протекает типично и без осложнений, то антибиотики назначаются в таблетках/капсулах, во всех остальных случаях проводится внутривенное введение препаратов.
- Симптоматическая терапия. Используются такие препараты как муколитики, мукокинетики, жаропонижающие. Целью назначения данных препаратов является облегчение симптоматики, что улучшает течение заболевания.
- Физиотерапия. Если у больного присутствует одностороннее воспаление легких без кашля и критичного повышения температуры, то в условиях стационара ему могут быть назначены разнообразные физиотерапевтические процедуры.
- Также используются дополнительные методы, что включают в себя лечение травами и дыхательную гимнастику.

Обычно курс лечения длится от 10 дней до двух недель.
Как лечить воспаление легких, должен определить врач – самолечение чревато развитием серьезных осложнений. Своевременно и грамотно проведенный курс лечения позволяет избежать развития хронического воспаления легких и осложнений.
Связанные услуги:
Прием у педиатра
Терапевтический стационар
Главный пульмонолог России о коронавирусе, его последствиях и 20-летних пациентах на ИВЛ: Общество: Россия: Lenta.ru
В России уже более 60 тысяч человек заразились коронавирусом, и долгожданное плато, после которого специалисты ожидают спад эпидемии, до сих пор не наступило. О том, почему коронавирус так опасен, станет ли эффективным экспериментальное лечение, когда все закончится и что будет со здоровьем переболевших, — «Ленте.ру» рассказал профессор, заведующий кафедрой пульмонологии Первого Московского государственный медицинского университета имени И. М. Сеченова (Сеченовский университет), главный пульмонолог Минздрава России Сергей Авдеев.
М. Сеченова (Сеченовский университет), главный пульмонолог Минздрава России Сергей Авдеев.
«Лента.ру»: Есть ли для вас в поведении новой коронавирусной инфекции что-то неожиданное?
Сергей Авдеев: Это абсолютно новая болезнь для нас. Данная вирусная инфекция имеет огромный тропизм (свойство действовать на ткани и клетки определенного типа — прим. «Ленты.ру») к альвеолярному эпителию, то есть мишенью для вируса является легочная ткань. Таких вирусов мы раньше просто не видели и не знали. Сейчас в наших клиниках среди госпитализированных с ковидом пациентов почти у каждого есть пневмония — у 95 процентов! Это очень необычное явление.
Сама пневмония протекает по абсолютно разным сценариям. В ряде случаев — без единого симптома. Ни температуры, ни кашля, ни одышки. То есть человек просто не ощущает, что болеет.
Другой сценарий — пневмонии при COVID-19 часто быстро прогрессируют, у пациентов возникает острая дыхательная недостаточность. Это требует использования сложных методов респираторной поддержки, включая искусственную вентиляцию легких.
Разве пневмония может быть бессимптомной — без кашля и температуры?
Да, это одна из особенностей COVID-19. Самый действенный метод — увидеть пневмонию на компьютерной томографии. Чувствительность метода КТ достигает 97 процентов, поэтому он выходит на первый план при диагностике воспалительного процесса.
Реаниматологи отмечают, что при COVID-19 пациенты с «разрушенными» легкими, у которых пульсоксиметр показывает острую кислородную недостаточность, активны до последнего, удушья не замечают. Почему такая обманчивая картина?
Я бы не сказал, что эти пациенты так уж активны. Но человек действительно может не ощущать симптомов. Некоторые исследователи сегодня говорят, что развитие ковидного острого респираторного дистресс-синдрома (ОРДС, дыхательная недостаточность — прим.«Ленты.ру») очень сильно отличается от традиционного ОРДС.
Отличие состоит в некоторых патофизиологических характеристиках поражения легких. В частности, эластичность легочной ткани, или комплаенс, при ковиде почему-то особенно не нарушается. Основное нарушение с точки зрения патофизиологии — это гипоксемия и вентиляционно-перфузионный дисбаланс (нарушение газообмена в легких). Главные характеристики механики дыхания — это податливость и сопротивление. Если эластичность легких не нарушена, то у пациента нет трудностей при дыхании, нет одышки. Вот в этом необычность ситуации. То есть у многих тяжелых пациентов нет субъективного ощущения тяжести болезни.
Основное нарушение с точки зрения патофизиологии — это гипоксемия и вентиляционно-перфузионный дисбаланс (нарушение газообмена в легких). Главные характеристики механики дыхания — это податливость и сопротивление. Если эластичность легких не нарушена, то у пациента нет трудностей при дыхании, нет одышки. Вот в этом необычность ситуации. То есть у многих тяжелых пациентов нет субъективного ощущения тяжести болезни.
Некоторые ваши коллеги подозревают, что у пациентов не пневмония, а другое специфическое поражение легких, связанное с нарушением работы гемоглобина — белка-переносчика кислорода. Насколько это может соответствовать действительности?
Теория сегодня действительно часто обсуждается. Но ее происхождение, знаете, какое? Это китайская научная работа, выполненная на основе компьютерного моделирования. Там сделали модель гемоглобина, в ней есть альфа- и бета-цепи. И увидели, что у бета-цепи конфигурация вроде бы конгруэнтна [соразмерна] вирусу SARS-CoV-2. И на этом основании решили, что есть тропизм вируса к бета-цепи гемоглобина. Поэтому и поражается гемоглобин. Но этой научной работы в интернете вы уже не найдете, ее удалили как недоказанную. Тем не менее конспирологические гипотезы до сих пор живут и обсуждаются.
Поэтому и поражается гемоглобин. Но этой научной работы в интернете вы уже не найдете, ее удалили как недоказанную. Тем не менее конспирологические гипотезы до сих пор живут и обсуждаются.
Фото: Александр Авилов / АГН «Москва»
Нет никаких оснований говорить о том, что ковид-пневмония — это и не пневмония вовсе. К сожалению, у нас сегодня есть морфологическое подтверждение процесса. Почему к сожалению — потому что это аутопсия умерших пациентов.
Есть, конечно, определенные особенности новой вирусной пневмонии. Она вовсе не такая, как, скажем, вирусная пневмония, связанная с гриппом. Но это все-таки пневмония — воспалительная реакция, связанная с вирусной агрессией в ткани легких.
До ковида сколько вирусных пневмоний у нас было в стране?
Немного — в среднем 10-15 процентов. Раньше самой частой причиной вирусных пневмоний был грипп. При вирусе гриппа характерно поражение эпителия верхних дыхательных путей: рта, носа, горла и так далее. Если инфекция спускается вниз, то это все же не признак того, что она перерастет в пневмонию. Скорее всего — в бронхит. Поэтому, говоря сегодня о кардинальных отличиях других вирусов от вируса SARS-CoV-2, прежде всего отмечают огромное количество пневмоний. Почти у всех пациентов, попавших в стационар с COVID-19, поражены легкие.
Скорее всего — в бронхит. Поэтому, говоря сегодня о кардинальных отличиях других вирусов от вируса SARS-CoV-2, прежде всего отмечают огромное количество пневмоний. Почти у всех пациентов, попавших в стационар с COVID-19, поражены легкие.
До регистрации SARS-CoV-2 у нас уже были известны другие коронавирусы. Они становились причинами пневмоний?
Известны четыре коронавируса, которые входят в структуру острых респираторных заболеваний. Но болезнь при их участии протекала достаточно легко и обычно без поражений нижних дыхательных путей. Вирус SARS-CoV-2 — абсолютно новый. Китайцы с ним впервые встретились в конце 2019 года, а мы, европейцы и американцы, — в 2020 году.
Могла ли часть жителей России, особенно на Дальнем Востоке, граничащем с Китаем, в Сибири, переболеть COVID-19 еще прошлой осенью?
Исключено. Многие сейчас пытаются вспомнить, как они болели осенью и в начале зимы. В ноябре-декабре действительно отмечалось много пневмоний, но опять-таки они были связаны совсем с другими возбудителями.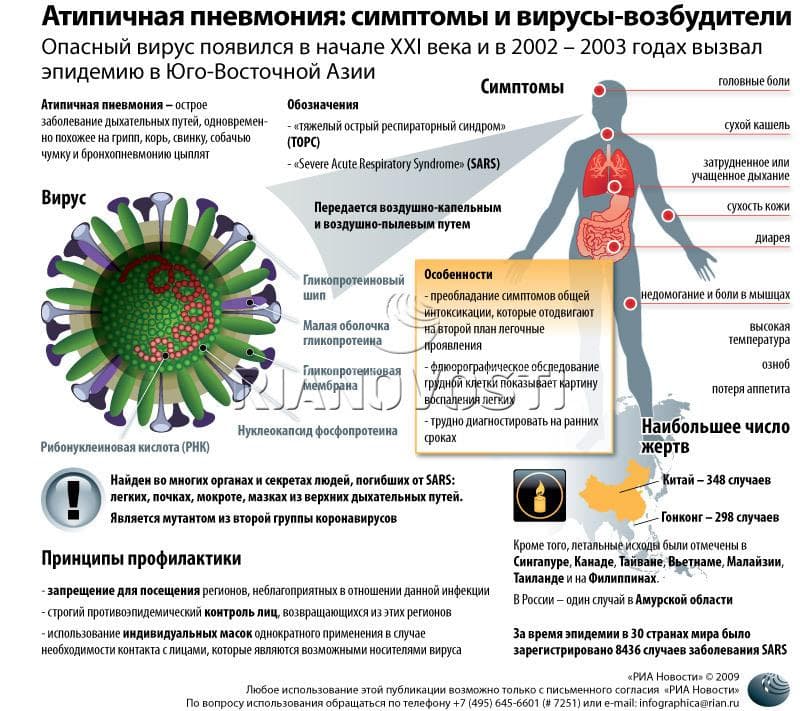 Один из самых частых возбудителей, которые тогда фиксировались, — микоплазма [mycoplasma pneumoniae — лат.]. А микоплазма — это также контагиозная инфекция, то есть может передаваться от одного человека к другому. Но сценарий протекания микоплазменных пневмоний — совсем другой. На снимках компьютерной томографии картина иная, чем то, что мы наблюдаем сегодня. И совсем другие лабораторные показатели. При COVID-19 — это абсолютно четкая особенная картина болезни.
Один из самых частых возбудителей, которые тогда фиксировались, — микоплазма [mycoplasma pneumoniae — лат.]. А микоплазма — это также контагиозная инфекция, то есть может передаваться от одного человека к другому. Но сценарий протекания микоплазменных пневмоний — совсем другой. На снимках компьютерной томографии картина иная, чем то, что мы наблюдаем сегодня. И совсем другие лабораторные показатели. При COVID-19 — это абсолютно четкая особенная картина болезни.
В чем особенность?
Если коротко, то при COVID-19 пневмония — двусторонняя, локализация — периферическая. Микоплазменные пневмонии чаще односторонние. Встречаются и двусторонние, однако в этом случае томографические снимки отличаются, изменения в легких иные.
Наши рентгенологи, описывая снимки легких при ковидных пневмониях, употребляют такие термины, как «булыжная мостовая», симптом «матового стекла». Именно так выглядят поражения
Считается, что новая болезнь опасна для пожилых. Но тяжело болеют и молодые. С чем это связано?
С чем это связано?
Действительно, молодых много. Под «молодыми» я имею в виду тех, кто моложе сорока.
Есть и двадцатилетние. Но, как правило, все эти молодые люди имеют определенные сопутствующие заболевания. Часто гипертензия, диабет, ожирение
Ситуация, когда условно здоровый молодой человек вдруг заболевает и оказывается на ИВЛ, исключена?
Почему исключена? В медицине редко бывает так, что либо единица, либо ноль. Исключения возможны. Но когда мы видим у молодого непростое течение болезни, то, скорее всего, у него все же есть сопутствующие патологии.
И плюс еще абсолютно свежая информация — генетики США опубликовали исследование, что к коронавирусу есть определенная генетическая предрасположенность индивидуумов с разным набором генов. Это достаточно интересно, речь идет о человеческих лейкоцитарных антигенах. В эту группу входят более 150 антигенов. Но, в частности, речь идет об антигене В 46:04. Выдвигается версия, что он ассоциирован с более тяжелым течением COVID-19.
Если версия подтвердится, то в практическом плане что это даст?
В ближайшем будущем генетическое исследование, которое достаточно недорогое, может дать информацию, кто из индивидуумов находится в группе риска по COVID-19. Эти люди в первую очередь будут являться кандидатами для вакцинации.
В тяжелых случаях пациентов переводят на искусственную вентиляцию легких. Сейчас на Западе врачи считают, что эта процедура не только неэффективна, но даже усугубляет состояние ковидных больных. У вас сложилось какое-то представление?
Во многих странах мы видим достаточно высокие показатели летальности на фоне ИВЛ. Но пациенты, которые находятся на искусственной вентиляции легких, имеют такую степень дыхательной недостаточности, что при помощи других методов терапии они, наверное, не смогли бы прожить не то что несколько часов, но даже и нескольких минут
Поэтому этот метод — жестокая необходимость. Но, как мы видим, иногда и он не спасает тяжелого пациента от неблагоприятного исхода.
Как я понимаю, лечения от коронавируса до сих пор нет. Какой из предложенных методов сегодня считается самым эффективным?
Это правда, все проводимое лечение сегодня — экспериментальное. Среди тех препаратов, которые мы используем, нет ни одного для прямого воздействия на эту вирусную инфекцию. Мы работаем с препаратами для лечения малярии, ВИЧ-инфекции. Но надеемся, что в ближайшее время будут зарегистрированы лекарства именно для COVID-19. Эти надежды не случайны, так как сейчас завершаются клинические исследования препаратов Ремдесивир и Фавипиравир.
Насколько перспективно лечение плазмой крови выздоровевших, нужно ли его срочно внедрять во всех больницах?
Метод начали в свое время использовать еще китайские коллеги. О безусловной эффективности метода говорить рано, так как история его применения достаточно короткая. Но сейчас по этой методике накапливается хороший позитивный опыт. В частности, в институте Склифосовского (НИИ скорой помощи им. Н. В. Склифосовского в Москве — прим. «Ленты.ру»). Есть надежда, что это действительно перспективно, так как с плазмой переболевшего вводятся другому болеющему нейтрализующие антитела. Они помогают бороться с инфекцией.
«Ленты.ру»). Есть надежда, что это действительно перспективно, так как с плазмой переболевшего вводятся другому болеющему нейтрализующие антитела. Они помогают бороться с инфекцией.
Фото: Kin Cheung / Reuters
Сегодня московские врачи заявили, что смысла разделять обычную пневмонию и коронавирусную нет. Это правильный подход?
Да, такая практика должна применяться по всей стране. В Москве мы видим, что на первом месте среди всех респираторных инфекций стоит COVID-19. В ближайшее время волна дойдет и в регионы. Это не значит, что все другие внебольничные пневмонии исчезли. Такие пациенты есть.
Если коронавирус был подтвержден только клинически и с помощью КТ, но не доказан тестами — эти случаи попадают в статистику заболевших и умерших?
Конечно, попадают. Все неподтвержденные диагнозы мы кодируем как вероятный случай COVID-19.
Почему смертность от этой инфекции в России сейчас одна из самых низких в мире?
Показатели смертности в России сравнимы с Южной Кореей, Германией. И говорить о том, что у нас какая-то особая статистика, я бы не стал.
И говорить о том, что у нас какая-то особая статистика, я бы не стал.
Наверное, все-таки вы спрашиваете об очень большой разнице в летальности со многими европейскими странами, той же Италией, Испанией. Объяснить это можно несколькими факторами. Первый — охват лабораторной диагностикой населения. Чем он шире — тем меньше процент летальности. А второй — это уровень подготовки системы здравоохранения к пандемии.
Все-таки Россия для этого получила большую фору. Если помните, то мы достаточно рано закрыли границы с Китаем. В Москве и других городах развернуты целые ковид-госпитали. В больницах организованы места для пациентов, сформированы бригады врачей, есть оборудование, в том числе аппараты для искусственной вентиляции легких. Организация процесса имеет очень большое значение для эффективного лечения этого недуга.
Много сейчас пишут и о том, что в той или иной стране началась вторая волна эпидемии. Может ли такое случиться и в России?
Официально о второй волне ни в одной стране не сообщается. Есть информация о новой вспышке в Китае, но в другом городе — Харбине (город в 500 километрах от Благовещенска — прим. «Ленты.ру»), там в январе-феврале больных почти не было. Вопрос о второй волне обсуждается, но фактов пока немного.
Есть информация о новой вспышке в Китае, но в другом городе — Харбине (город в 500 километрах от Благовещенска — прим. «Ленты.ру»), там в январе-феврале больных почти не было. Вопрос о второй волне обсуждается, но фактов пока немного.
Повторное заражение сразу же после выздоровления возможно?
В России и за рубежом таких пациентов нет. Скорее всего — невозможно. По крайней мере, не в этот сезон. Как долго может сохраняться иммунитет — говорить пока рано, очень маленький срок наблюдения. В 2002-2003 годах в мире была вспышка атипичной пневмонии, вызванной вирусом SARS. Это тоже коронавирус, он отличается от нового родственника. Однако на 80 процентов эти вирусы схожи.
Тестирование на антитела
Фото: Ddp Images / Globallookpress.com
После перенесенной атипичной пневмонии SARS у пациентов шло формирование гуморального иммунитета, наработка антител — иммуноглобулина G. Этот иммуноглобулин определялся примерно у 90 процентов людей, переболевших SARS. И его уровни были высокими на протяжении первых двух лет после выздоровления. Поскольку коронавирусы SARS и SARS-CoV-2 очень похожи, то такой же сценарий можно ожидать и сейчас.
И его уровни были высокими на протяжении первых двух лет после выздоровления. Поскольку коронавирусы SARS и SARS-CoV-2 очень похожи, то такой же сценарий можно ожидать и сейчас.
По динамике развития пандемии в России можно ли сказать, когда у нас будет пик?
Наверное, в первую-вторую недели мая. Если рассматривать китайский сценарий, то по нему на плато мы должны выйти примерно через месяц. Плато — это стабильное количество случаев, когда нет подъема заболеваемости и летальности. Будем надеяться, что плато может продлиться три-четыре недели. А дальше уже пойдет снижение. При хорошем сценарии в конце лета — начале осени можно будет ожидать конца эпидемии. Но хочу добавить — точного прогноза сегодня, наверное, не может дать никто!
Какие последствия могут быть у людей, переболевших коронавирусной пневмонией?
Говорить об обязательных последствиях, конечно же, сегодня нельзя. Вполне вероятно, что большинство переболевших COVID-19 не будут иметь проблем ни со стороны легких, ни со стороны почек, ни со стороны сердечно-сосудистой системы. То, что у некоторых возможны какие-то остаточные изменения, — это да. Но мы о масштабах проблем пока не знаем. Если пневмония прошла в легкой форме, без симптомов, то скорее всего она не оставит никаких изменений в легких.
То, что у некоторых возможны какие-то остаточные изменения, — это да. Но мы о масштабах проблем пока не знаем. Если пневмония прошла в легкой форме, без симптомов, то скорее всего она не оставит никаких изменений в легких.
Вашу работу коронавирус как-то изменил?
У меня сегодня в клинике находятся пациенты только с одним типом болезни — коронавирусная пневмония. Их ни много ни мало — 300 человек. Недавно открылась университетская клиническая больница №1 Сеченовского университета на 800 коек. Всего в клиниках университета развернуто 2000 коек для лечения ковида. Конечно, наша работа полностью изменилась. Будем надеяться, что временно. Чем быстрее это все закончится, тем лучше для всех нас.
Врач – о том, что нужно знать о пневмонии
Какие осложнения может дать вирусная пневмония? Правда ли, что пневмонии могут протекать бессимптомно? Станет ли летом меньше пневмоний? На эти и другие вопросы «АиФ» ответила заведующая кафедрой фтизиопульмонологии БГМУ, доктор медицинских наук, доцент Галина Бородина.
Фото: Александра Квиткевич
«Увидеть» болезнь
— Какие основные осложнения может дать вирусная пневмония?
— После любой перенесенной пневмонии могут развиться тяжелые осложнения (плеврит, абсцесс легких, сепсис, отек легких и т.д.), но при правильном и своевременном лечении легкие достаточно быстро восстанавливаются и по своей структуре, и по функции. Чтобы предотвратить их развитие или нивелировать последствия, важна реабилитация.
— Пневмонию можно увидеть только с помощью флюорографии?
— Издавна воспаление легких диагностировалось с помощью выслушивания (аускультации) и простукивания (перкуссии). Однако симптомы, которые врач может выявить, используя фонендоскоп, характеризуются достаточно низкой чувствительностью и специфичностью. И ориентироваться только на данный метод диагностики нельзя.
Поэтому врач должен назначить комплекс анализов, а также обязательно рентгенографию, которая позволяет «увидеть» пневмонию. В некоторых случаях может быть показана компьютерная томография (КТ). Целесообразность КТ определяет врач.
В некоторых случаях может быть показана компьютерная томография (КТ). Целесообразность КТ определяет врач.
В частности, при коронавирусной инфекции компьютерная томография обычно выполняется, так как позволяет выявить специфические характеристики, которые характерны для этой пневмонии.
Болел или нет?
— Правда ли, что пневмонии могут протекать бессимптомно: человек даже не заметит, что переболел?
— Типичная пневмония характеризуется резким подъемом температуры. Потом у пациента возникает кашель — вначале сухой, впоследствии с выделением мокроты. Появляется одышка, могут быть боли в груди, иногда кровохаркание.
Однако симптомы воспаления легких не проявляются столь ярко во всех случаях. В настоящее время врачи сталкиваются с малосимптомными пневмониями. Поэтому возможно, что человек даже не заметит, что переболел пневмонией, списывая небольшое недомогание на усталость или простуду.
Особенно это касается пожилых людей, пневмония у которых часто отличается неяркой клинической картиной.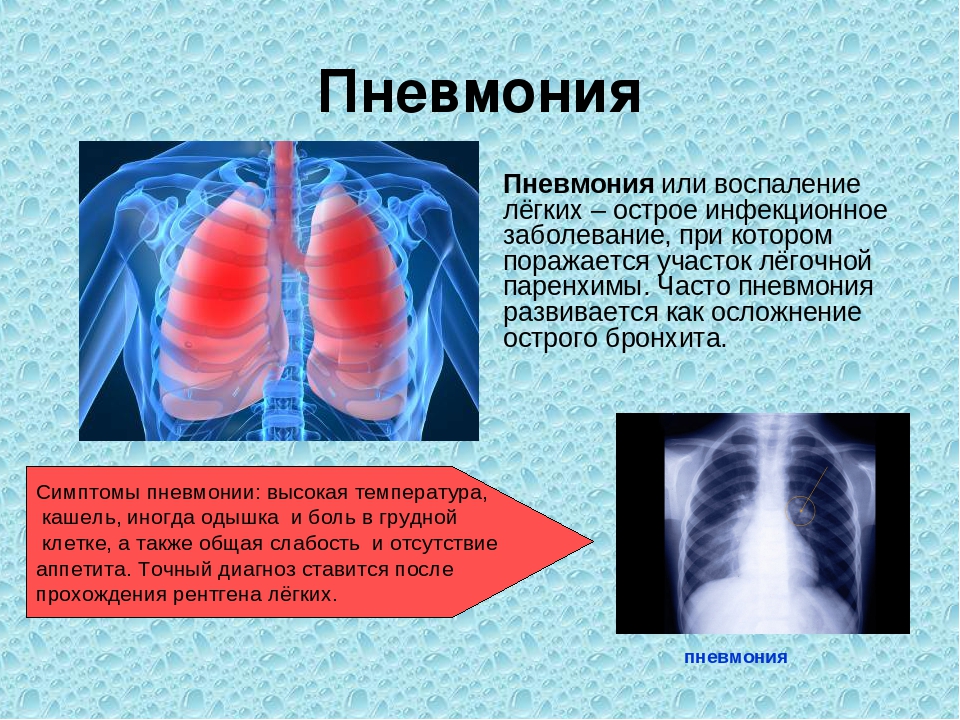 Кроме того, пневмония у пожилых протекает на фоне сопутствующих заболеваний, что еще больше затрудняет диагностику.
Кроме того, пневмония у пожилых протекает на фоне сопутствующих заболеваний, что еще больше затрудняет диагностику.
Поэтому нужно быть внимательным к своему здоровью и при появлении симптомов заболевания обратиться за медицинской помощью.
Когда вирус отступит
— Сколько раз человек может переболеть пневмонией? Летом станет меньше пневмоний? Или заболеваемость не зависит от сезона?
— Человек может болеть пневмонией много раз, иммунитет после этого заболевания не формируется.
Ежегодный подъем уровня заболеваемости пневмонией отмечается после всплеска вирусных инфекций. Чаще всего он выпадает на март. Поэтому летом пневмоний действительно становится меньше. Но это не относится к пневмониям, ассоциированным с коронавирусной инфекцией, — в данном случае заболеваемость будет определяться комплексом различных причин.
Настройтесь на здоровье
— Что вы думаете о народных методах лечения коронавируса: таких как чеснок, раствор соды, имбирь?
— Во-первых, никакие народные методы не прошли соответствующих испытаний, позволяющих считать их лекарственными средствами. Это не медицина доказательств, часто при их применении помогает только вера человека в действенность процедуры или вещества. Что касается терапии бактериальных пневмоний — тут нужны антибиотики, а над решением загадки эффективного лечения вирусных инфекций до сих пор бьется весь медицинский мир. Поэтому вылечиться этими методами от пневмонии не получится.
Это не медицина доказательств, часто при их применении помогает только вера человека в действенность процедуры или вещества. Что касается терапии бактериальных пневмоний — тут нужны антибиотики, а над решением загадки эффективного лечения вирусных инфекций до сих пор бьется весь медицинский мир. Поэтому вылечиться этими методами от пневмонии не получится.
Тем не менее, многие народные методы помогают справиться с определенными симптомами заболеваний. Так, ингаляции раствора соды создают щелочную среду и улучшают отхождение мокроты, чеснок содержит фитонциды, способствующие профилактике вирусных инфекций, имбирь используется преимущественно для лечения заболеваний верхних дыхательных путей.
— Как быстрее восстановиться после перенесенной пневмонии, в том числе коронавируса?
— Большое значение в выздоровлении имеют мотивация пациента и уход за ним. Важно соблюдать постельный режим и использовать положение пациента лежа на животе, чтобы облегчить дыхание в основных отделах легких, если беспокоит одышка.
Нахождение в комнате с температурой воздуха 18−20 градусов и определенным уровнем влажности, легкая диета (нежирные сорта рыбы и мяса, курица, куриный бульон, фрукты, овощи, молоко, кисломолочные продукты) также будут способствовать выздоровлению.
Постепенно следует приступать к тренировкам дыхания — например, методике «создания положительного давления на выдохе» путем надувания воздушных шариков или выдыхания в стакан с водой через соломинку.
Одним словом, адекватное лечение позволяет добиться благоприятного исхода пневмонии. Что подтверждает и нынешняя ситуация, когда большинство пациентов быстро восстанавливаются. Неблагоприятный же прогноз может быть при иммунодефицитном состоянии или декомпенсации других органов и систем организма.
Читайте также
Вакцинация против пневмонии
Пневмония является причиной смертности 15% детей до 5 лет во всем мире.
На сегодняшний день одна из основных причин детской смертности – это пневмония, вызванная пневмококком.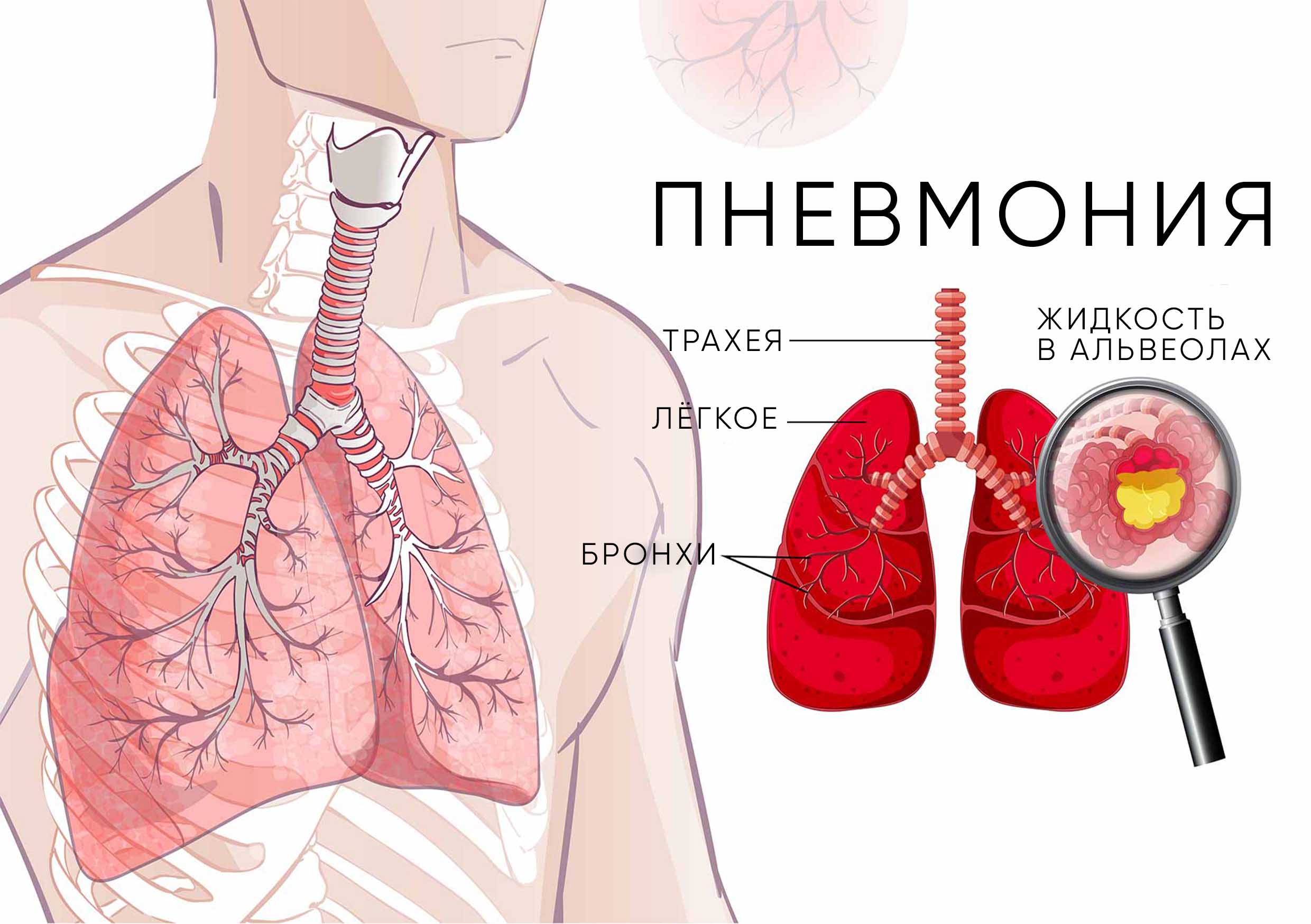
Пневмония — восполение легочной ткани, которое чаще всего вызывают бактерии, вирусы и грибки.
Среди всех видов пневмоний, пневмококковая занимает лидирующую позицию.
Возбудителем пневмококковой инфекции (ПИ) является пневмококк (Streptococcus pneumoniае) – представитель нормальной микрофлоры дыхательных путей.
Особенно опасна пневмококковая инфекция для маленьких в возрасте до 2 лет и взрослых старше 65 лет. Заболевший ребенок или пожилой человек (особо уязвимые лица, входящие в группу риска) с большой вероятностью рискуют получить такие осложнения как эндокардит, менингит, отит. Наиболее тяжело пневмонии протекают у пожилых людей, на фоне сопутствующих заболеваний (онкологические заболевания, болезни крови, сахарный
диабет, сердечно-сосудистые заболевания, заболевания почек и печени, хроническая обструктивная болезнь легких, алкоголизм, вирусные инфекции и другие). Большинство осложнений пневмококковой инфекции опасны для жизни.
Группы риска пневмококковой инфекции:
- недоношенные дети;
- дети до 2 лет;
- взрослые 65 лет и старше;
- дети и взрослые с хроническими заболеваниями ;
- люди с положительным ВИЧ-статусом;
- дети и взрослые с онкогематологическими заболеваниями;
- дети или взрослые, планирующие или уже подвергшиеся удалению селезенки.
Пневмонию, вызванную пневмококком (пневмококковая инфекция), сегодня успешно предупреждают путем вакцинации
Вакцинация — наиболее эффективный метод предупреждения пневмококковой инфекции.
Вакцинация детей проводится в плановом порядке, в соответствии с Национальным календарем профилактических прививок, в возрасте 2 месяца (первая вакцинация), 4,5 месяца (вторая вакцинация), 15 месяцев – ревакцинация (приказ Минздрава России от 21 марта 2014 г. № 125н), а также в рамках календаря профилактических прививок по эпидемическим показаниям — детей в возрасте от 2 до 5 лет. Также вакцинация против пневмококковой инфекции показана призывникам (во время осеннего призыва).
Также вакцинация против пневмококковой инфекции показана призывникам (во время осеннего призыва).
Важнейшим аргументом в пользу вакцинации против пневмококковых инфекций является растущая устойчивость возбудителей к антибиотикам. В связи с чем, при развитии заболевания, антибактериальные препараты будут просто неэффективны.
В настоящее время используются вакцины следующих типов:
- 23-валентная пневмококковая полисахаридная вакцина (вводится только с двухлетнего возраста, так как не обеспечивает защиту новорожденных детей и детей младшего возраста). Эта вакцина способна защитить организм от 23 типов возбудителя пневмонии. Вакцина используется у детей после достижения 2 лет, а также у пожилых (старше 65 лет).
- Конъюгированные 10- и 13-валентные пневмококковые вакцины (ПКВ-10 и ПКВ-13).
ПКВ-13 применяется у детей в возрасте 6 недель – 17 лет и для взрослых в возрасте 18 лет и старше.
Главным преимуществом пневмококковой конъюгированной вакцины является возможность ранней защиты детей от пневмококковой инфекции, (начиная с 2-х месячного возраста до 5 лет). Этот вид вакцины обеспечивает невосприимчивость организма к основным 13 разновидностям возбудителя пневмонии.
Этот вид вакцины обеспечивает невосприимчивость организма к основным 13 разновидностям возбудителя пневмонии.
Как действует вакцина против пневмонии?
Вакцина, вводимая в организм человека, имеет в своем составе компоненты возбудителя пневмококковой инфекции, в ответ на введение которых, организм вырабатывает антитела, защищающие организм привитого человека от этой инфекции на протяжении 5 лет. Если в течение этого времени в организм попадет пневмококк, а это практически неизбежно, – он будет уничтожен или минимизирован.
Какие осложнения могут возникать после введения пневмококковой вакцины?
- Покраснение и отек тканей в месте инъекции
- Повышение температуры тела до 39оС и выше, сонливость
- Увеличение лимфоузлов
- Диарея, рвота
Все осложнения носят временный характер.
Вакцина против пневмококковой инфекции крайне редко вызывает какие-либо осложнения, в том числе аллергическую реакцию.
Для того, чтобы избежать осложнений, необходимо наблюдать за состоянием ребенка, вакцинацию проводить только на фоне полного здоровья
Если ребенок заболел острой вирусной инфекцией или его хроническое заболевание находится в стадии обострения, вакцинацию откладывают на то время, пока ребенок не выздоровеет.
Если на момент вакцинации ребенок испытывает недомогание, течение основного заболевания может ухудшиться на фоне вакцинации.
Вопросы:
1. Если ребенку проводилось переливание крови, через какое время можно проводить вакцинацию?
Не ранее, чем через 3-4 месяца.
2. Ребенку в связи с обострением хронического аутоиммунного заболевания назначена иммуносупрессивная терапия. Когда правильно привить его против пневмококковой инфекции, т. к. такой ребенок входит в группу риска по развитию тяжелых форм пневмококковой инфекции?
к. такой ребенок входит в группу риска по развитию тяжелых форм пневмококковой инфекции?
Пациентам с хроническими воспалительными заболеваниями, нуждающимся в иммуносупрессивной терапии, вакцины следует вводить не менее, чем за 2 недели до начала иммуносупрессивной терапии.
3. Можно ли проводить вакцинацию против пневмококковой инфекции вместе с вакцинацией против гриппа?
Иммунизацию против ПИ можно проводить в течение всего года. Если планируется организация программы массовой вакцинации против гриппа, то удобно провести эту вакцинацию одновременно с иммунизацией против пневмококковой инфекции перед началом сезона ОРЗ и гриппа, что соответствует рекомендациям Всемирной организации здравоохранения.
КТ легких при коронавирусе: когда, зачем, как проводится?
Главная
статьи
КТ легких при коронавирусе: когда, зачем, как проводится?
Вспышка нового коронавируса COVID-19, впервые зарегистрированная в китайской провинции Хубэй, в кратчайшие сроки охватила весь мир и всего за 9 месяцев унесла жизни около 1 млн. человек.
человек.
Коронавирус — это острое респираторное заболевание дыхательных путей, ассоциированное с вирусом SARS-CoV-2.
Коронавирусная инфекция нового типа быстро распространяется и легко передается от человека человеку воздушно-капельным или контактно-бытовым путем. Если мы рассмотрим коронавирус под микроскопом, то обратим внимание, что на поверхности вириона расположены белковые шипы — с их помощью вирус прочно прикрепляется к белкам-рецепторам на поверхности клеток человека, в частности легких.
Коронавирус приводит к тяжелым осложнениям — воспалению и фиброзу легких, лихорадке, острой дыхательной и сердечной недостаточности. Компьютерная томография (КТ) легких на сегодняшний день признана основным методом диагностики коронавируса. Этот метод исследования достоверно и на ранних стадиях показывает паттерн поражения легких, то есть пневмонию, при которой альвеолы заполняются патологическим субстратом (жидкостью, фиброзной тканью), а не воздухом.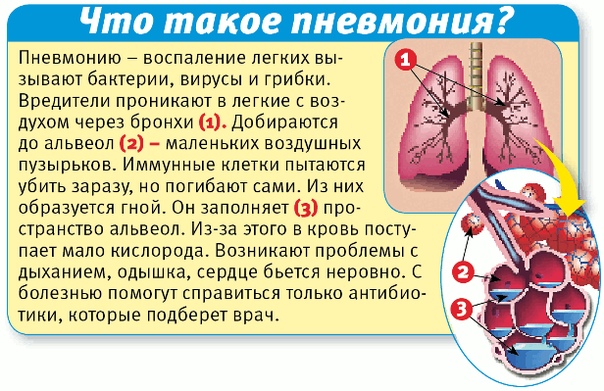
Под паттерном («моделью, схемой, узором») в медицине понимается совокупность признаков и симптомов, типичных для того или иного клинического состояния. Например, сочетание «матовых стекол» и их консолидация в определенных участках легких визуализируется на томограммах и трактуется как паттерн вирусной пневмонии COVID-19.
Поражение легких более чем на 50% считается опасным и требует госпитализации, особенно если пульсоксиметр показывает сатурацию (насыщение крови кислородом) менее 92-93%.
Нужно ли делать КТ легких при коронавирусе?
Во время первой волны эпидемии COVID-19 в апреле 2020 г. российские медики отмечали, что у 45,5% зараженных не отмечалось клинических проявлений заболевания — у таких пациентов коронавирусная инфекция развивалась бессимптомно. На сегодняшний день КТ легких считается основным методом диагностики вирусной пневмонии, главным последствием которой является частичное поражение легких.
Альвеолы представляют собой небольшие воздушные ячейки в легком. Когда их объем сокращается из-за фиброза или скопления жидкости, происходит критическое нарушение дыхательной функции. У человека возникает одышка, кашель с мокротой (иногда с кровью), повышается температура тела.
При пневмонии, вызванной COVID-19, чаще всего беспокоит:
- Боль и дискомфорт в груди;
- Одышка и нехватка воздуха;
- Сухой кашель;
- Потеря обоняния;
- Повышенная температура.
Лабораторные анализы крови, направленные на выявление и определение вирусного возбудителя, иногда дают ложноотрицательный результат. В этой связи медиками было принято конвенциональное решение, согласно которому наличие признаков поражение легких на томограммах, несмотря на отрицательный ПЦР, должны расцениваться как вероятная коронавирусная инфекция до тех пор, пока не будет поставлен альтернативный диагноз.
Другим методом лучевой диагностики пневмонии при коронавирусе является стандартная рентгенография грудной клетки. Рентген — более доступный по цене и распространенности метод обследования. Однако он существенно уступает компьютерной томографии по информативности. Дело в том, что рентген не показывает поражение легких I и II степени. У этого метода есть и другие недостатки, например, при наложении теней от крупных органов друг на друга возникают артефакты, которые могут быть истолкованы неверно.
Рентген — более доступный по цене и распространенности метод обследования. Однако он существенно уступает компьютерной томографии по информативности. Дело в том, что рентген не показывает поражение легких I и II степени. У этого метода есть и другие недостатки, например, при наложении теней от крупных органов друг на друга возникают артефакты, которые могут быть истолкованы неверно.
Согласно действующим клиническим рекомендациям, в условиях пандемии любые уплотнения (инфильтрации) легочной ткани и признаки воспалительных изменений на рентгенограммах должны рассматриваться как подозрительные в отношении COVID-19. Это значит, что после рентгена пациента направляют сделать КТ. Чтобы избежать лишней лучевой нагрузки при подозрении на коронавирус пациенту целесообразно сразу сделать КТ легких.
Поражение легких при коронавирусе на КТ
При подозрении на наличие коронавирусной инфекции пациентов чаще всего беспокоят вопросы: как определяют степень поражения легких, когда необходима госпитализация и можно ли восстановить легкие после пневмонии? Разберем подробнее эту тему и посмотрим, чем будет полезна компьютерная томография легких.
Проявления коронавируса
Согласно наблюдениям китайских ученых и медиков, обобщенным в «Справочнике по профилактике и лечению COVID-19», боль в груди при коронавирусе свидетельствует уже о прогрессирующем (около 10 дней) заболевании. При легком течении пневмонии на ранней стадии дискомфорт не беспокоит. Поэтому очень важно прислушиваться к своему организму (особенно дыханию), измерять температуру. А если вы контактировали с больным или людьми из эпидемиологически неблагоприятных стран, необходимо сделать тест на COVID-19 и КТ легких. Только томография выявляет начальные стадии поражения легких при коронавирусе, когда вылечить пневмонию и сохранить функцию дыхательного органа легче всего.
Легочная ткань не может сильно болеть, поскольку в ней совсем немного нервных рецепторов. Дискомфорт в легких при коронавирусе — следствие отека воспалительного характера. Когда альвеолы легких заполняются жидкостью или фиброзной тканью, растягивается плевральная оболочка. Это и вызывает боль тупого характера. Наряду с этим при коронавирусе пациент может ощущать:
Это и вызывает боль тупого характера. Наряду с этим при коронавирусе пациент может ощущать:
- Давление в груди, сильное распирание;
- Неприятные ощущения во время глубокого вдоха, при резком вдохе отмечается сильный продолжительный кашель;
- Дискомфорт в области шеи, ключиц, между ребер.
Однако похожие симптомы характерны и для других респираторных заболеваний. Тем не менее, чтобы исключить коронавирус или вовремя его обнаружить и предотвратить развитие дистресс-синдрома.
ОРДС (острый респираторный дистресс-синдром или «шоковое лёгкое» ) — это острое и тяжелое состояние, которое характеризуется двухсторонней инфильтрацией и отеком лёгких с выраженной гипоксемией. Обширный воспалительный процесс резко вызывает у больного дыхательную недостаточность, проблемы с сердцем, спазм легочных сосудов. У некоторых пациентов переходит в фиброз, после которого полное восстановление пораженных легких иногда невозможно. ОРДС — основная причина летальных исходов при коронавирусе.
ОРДС — основная причина летальных исходов при коронавирусе.
Как выглядит поражение легких на КТ
На поражение легких, вызванное коронавирусом нового типа, указывают так называемые «матовые стекла» — сравнительно светлые участки, напоминающие налет, которые свидетельствуют об уплотнении ткани. В норме «матовых стекол» быть не должно. Особенность компьютерной томографии заключается в том, что такие признаки коронавирусной пневмонии видны достаточно ясно, даже если легкие поражены на 5% и менее. Традиционная рентгенография и другие аппаратные методы диагностики обладают меньшей разрешающей способностью, поэтому могут дать неоднозначный результат.
При пневмонии, ассоциированной с COVID-19, участки «матового стекла» располагаются в обоих легких: в нижних и боковых отделах, вокруг бронхов или ближе к плевре. КТ позволяет определить степень поражения легких при коронавирусе. Менее трех «матовых стекол» соответствуют легкой степени заболевания, более трех свидетельствуют об умеренном поражении легких. Если наблюдается их консолидация, состояние пациента оценивают как среднетяжелое, с распространенными уплотнениями — тяжелое.
Если наблюдается их консолидация, состояние пациента оценивают как среднетяжелое, с распространенными уплотнениями — тяжелое.
Чтобы оценить степень поражения в процентах, легкие делят на 5 долей: три в правом и две в левом. Врач-рентгенолог осматривает каждую долю и оценивает, насколько повреждена каждая из них по пятибалльной шкале, где 1 балл соответствует 5% обструкции и менее, а 5 баллов — более 75%. Далее все баллы складывают и умножают на 4. Полученное число и будет выражать степень поражения легких при коронавирусе в процентах. Если дыхательный орган функционирует на 50% и менее, это уже является основанием для госпитализации.
Помимо «матовых стекол» на КТ легких у пациентов, больных коронавирусом, врач увидит и другие клинически значимые признаки пневмонии:
- Синдром «булыжной мостовой» или «лоскутного одеяла» — когда уплотнение распространяется и на перегородки между дольками легких (примерно на третий день воспаления легких), то текстура легочной ткани на КТ сканах приобретает сходство с брусчаткой.

- Консолидацию «матовых стекол» — по мере развития заболевания (обычно на 5-8 день), легочная ткань становится все более плотной и хуже пропускает рентгеновские лучи, при этом становится меньше ее функциональных участков, участвующих в газообмене.
- Симптом обратного гало или синдром ободка — участки уплотнения вокруг очага инфекции («матового стекла»), похожие на кольца. Встречается у более 50% больных коронавирусом.
- Симптом воздушной бронхограммы — наличие воздуха в просвете бронхов наряду с выраженной консолидацией «матовых стекол».
Когда при коронавирусе нужно делать КТ легких?
Согласно принятой классификации выявленных патологических изменений, стандарт «КТ1» соответствует менее 25% поражению легких, «КТ2» — 35-50%, «КТ3» — 50-75%, «КТ4» — 75% и более. Особенность пневмонии, вызванной новым коронавирусом COVID-19, заключается в том, что переход осложнения в более тяжелую форму происходит быстро.
В отличие от рентгена, КТ покажет поражение легких 5% и менее — врач-рентгенолог видит даже единичные участки инфильтрации диаметром от 4-5 мм. По рентгеновскому снимку не определить пневмонию, соответствующую КТ1, а иногда и КТ2. При наличии характерных симптомов, даже в легкой форме, и положительного теста на COVID-19, нет необходимости ждать, пока инфекция интенсивнее распространится и вызовет поражение больших участков легких.
КТ легких показана при:
- Температуре 38 градусов;
- Частоте дыхания > 22 в минуту;
- Одышке / кашле / боли в груди;
- Сатурации крови
КТ при коронавирусе делают даже в том случае, если тест на COVID-19 показывает отрицательный результат, а на рентгене не выявлены существенные изменения легочной ткани (очаги могут быть еще небольшими, на снимке могут быть артефакты и тени) — при этом пациента беспокоят вышеуказанные симптомы, не исключен контакт с больными в прошлом.
Какое КТ легких делают при коронавирусе?
Сегодня «золотым стандартом» КТ при коронавирусе считается посрезовое 1-2 мм сканирование на мультиспиральном томографе или МСКТ легких. Диагностика на таких современных аппаратах занимает всего минуту и позволяет получить снимки в максимально высоком разрешении. Процедура проходит в наиболее комфортных для пациента условиях, поэтому подходит даже больным, находящимся в тяжелом состоянии здоровья (при искусственной вентиляции легких). КТ легких при коронавирусе проводится без контраста, при этом диагностическая ценность превосходит рентген, МРТ, УЗИ.
В специализированном центре КТ «Ами» пациенты проходят КТ легких на мультиспиральном томографе нового поколения Siemens Somatom go.Now со сниженной лучевой нагрузкой и сразу получают запись исследования (КТ сканы) на DVD-диске.
Как делают КТ легких при коронавирусе
Специальная предварительная подготовка к исследованию не требуется. Перед процедурой пациенту необходимо снять все металлические предметы и украшения, поскольку они ослабляют рентгеновские лучи. Затем пациента приглашают в процедурную, тот ложится на диагностический стол. Медицинская сестра включает томограф, и стол постепенно движется к гентри — раме томографа, оснащенной чувствительными датчиками. Гентри сканера вращается вокруг грудной клетки и делает множество сканов (снимков). Все это время сохраняется обратная связь врача-рентгенолога с пациентом. КТ легких делают на вдохе, пациент на несколько секунд задерживает дыхание. Затем изображения обрабатываются на компьютере — программа делает объемную 3D-реконструкцию внутренних органов. Врач-рентгенолог изучает полученные данные, записывает томограмму на диск и готовит заключение.
Перед процедурой пациенту необходимо снять все металлические предметы и украшения, поскольку они ослабляют рентгеновские лучи. Затем пациента приглашают в процедурную, тот ложится на диагностический стол. Медицинская сестра включает томограф, и стол постепенно движется к гентри — раме томографа, оснащенной чувствительными датчиками. Гентри сканера вращается вокруг грудной клетки и делает множество сканов (снимков). Все это время сохраняется обратная связь врача-рентгенолога с пациентом. КТ легких делают на вдохе, пациент на несколько секунд задерживает дыхание. Затем изображения обрабатываются на компьютере — программа делает объемную 3D-реконструкцию внутренних органов. Врач-рентгенолог изучает полученные данные, записывает томограмму на диск и готовит заключение.
Что еще показывает КТ легких?
Помимо пневмоний, КТ грудной клетки показывает туберкулез, опухоли легких и средостения, заболевания (лимфоаденопатию) средостения, тимомы и другие новообразования средостения.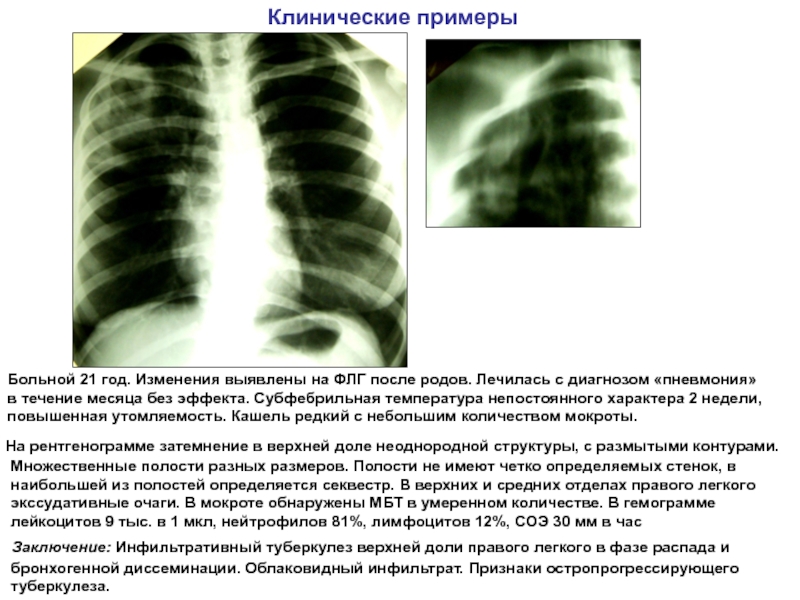 В этом случае диагностика мягких тканей с помощью компьютерной томографии даже предпочтительнее МРТ легких. Также КТ грудной клетки делают после травм, переломов ребер и грудного отдела позвоночника для оценки повреждений. КТ грудной клетки с контрастом позволяет дополнительно визуализировать сосуды. В рамках исследования с контрастным усилением врач может увидеть и детально оценить тромбоэмболии легочной артерии, опухоли легких, грудную аорту.
В этом случае диагностика мягких тканей с помощью компьютерной томографии даже предпочтительнее МРТ легких. Также КТ грудной клетки делают после травм, переломов ребер и грудного отдела позвоночника для оценки повреждений. КТ грудной клетки с контрастом позволяет дополнительно визуализировать сосуды. В рамках исследования с контрастным усилением врач может увидеть и детально оценить тромбоэмболии легочной артерии, опухоли легких, грудную аорту.
КТ легких после коронавируса
КТ легких при коронавирусе делают не только с целью оценки поражения легких, но и для мониторинга процесса восстановления в рамках терапии. Первую делают через три дня после начала лечения, если оно не дает результатов, и пациент не идет на поправку. Следующую томографию можно повторить через неделю, если состояние больного не улучшается.
При благоприятном лечении в реабилитационном периоде КТ легких можно пройти дважды (интервал — 2-3 недели), чтобы отслеживать динамику восстановления легких после коронавируса. Всего в год рекомендовано делать не более 5 КТ.
Всего в год рекомендовано делать не более 5 КТ.
Легочная ткань эластична и способна к регенерации. Если патология вовремя обнаружена, и предприняты меры лечения, то организм пациента может справиться с инфекцией за 1 месяц, а после реабилитации функциональность легких будет полностью восстановлена.
Если пациент поступил в медицинское учреждение с поражением легких более 50%, перенес тяжелую пневмонию или острый респираторный дистресс-синдром, то возможно формирование фиброза. Последствия фиброза легких напоминают рубцы, и такие патологические изменения могут быть необратимыми. Однако если поражены небольшие участки, то они с функциональной точки зрения легко компенсируются здоровыми и в течении жизни не ощущаются. Целесообразность и количество повторных компьютерных томографий в реабилитационном периоде определяется врачом.
МБУЗ «ЦГБ» г.Батайска РО | Всемирный день борьбы с пневмонией!
Профилактика пневмонии
Пневмония представляет собой инфекционное заболевание легких. Обычно поражает детей младше 2 лет, взрослых старше 65 лет и людей с ослабленной иммунной системой.
Обычно поражает детей младше 2 лет, взрослых старше 65 лет и людей с ослабленной иммунной системой.
Пневмония может развиваться как самостоятельно, так и на фоне различных патологических состояний: других болезней, травм, в послеоперационный период и др. К предрасполагающим факторам относятся переохлаждение (особенно в условиях повышенной влажности), острые респираторные вирусные инфекции, высокая загазованность, физическое и умственное переутомление, перенесенные заболевания легких, недостаточное питание, курение. У пожилых людей и тяжелобольных из-за низкой двигательной активности пневмонию могут вызвать застойные явления в легких.
В развитии пневмонии важную роль играют бактерии, такие, как пневмококки, стафилококки, стрептококки, гемофильная палочка и пр., а также вирусы, являющиеся ведущими факторами риска легочного воспаления.
Пневмония характеризуется острым, внезапным началом, как правило, связанным с переохлаждением, повышением температуры, слабостью, головной болью, ознобом, кашлем. В первые дни кашель бывает сухим, затем появляется мокрота. Могут возникать боли в грудной клетке при дыхании, одышка, интоксикация. При появлении таких симптомов необходимо незамедлительно обратиться к врачу или вызвать его на дом. Для подтверждения наличия пневмонии проводится рентгенологическое исследование органов грудной клетки.
В первые дни кашель бывает сухим, затем появляется мокрота. Могут возникать боли в грудной клетке при дыхании, одышка, интоксикация. При появлении таких симптомов необходимо незамедлительно обратиться к врачу или вызвать его на дом. Для подтверждения наличия пневмонии проводится рентгенологическое исследование органов грудной клетки.
Острые пневмонии не оставляют иммунитета: переболевший человек подвержен новому заражению в последующем. Учитывая то, что пневмония часто выступает осложнением после перенесенного заболевания ОРВИ и гриппом, то ежегодная вакцинация против гриппа является наиболее эффективным способом профилактики.
Чтобы не допустить болезнь, следует избегать переохлаждений и стрессовых факторов и внимательно относиться к своему здоровью: вовремя лечить другие заболевания, ведь даже кариозный зуб как источник болезнетворной флоры может привести к тяжелейшей пневмонии.
Необходимо поддерживать сопротивляемость организма с помощью закаливания, здорового питания, полноценного отдыха, прогулок на свежем воздухе, регулярной физической нагрузки, отказа от вредных привычек, в частности, курения, которое снижает естественную устойчивость бронхов и легких к респираторным инфекциям, и злоупотребления алкоголем. Укреплять иммунитет можно также с помощью иммуномодуляторов.
Укреплять иммунитет можно также с помощью иммуномодуляторов.
Как можно чаще мойте руки с мылом, чтобы удалить микроорганизмы, способные вызвать пневмонию, поддерживайте чистоту в доме, регулярно проветривайте помещения.
Выполняйте дыхательную гимнастику, направленную на улучшение вентиляции легких. С этой целью можно надувать воздушные шары или систематически делать глубокие вдохи и выдохи. Еще одним средством неспецифической профилактики воспаления легких является массаж, который рекомендуется в любом возрасте.
В период сезонного подъема заболеваемости острыми респираторными инфекциями нужно ограничить пребывание в местах массового скопления людей, сократить количество поездок в общественном транспорте, избегать контакта с больными.
Информация для родителей.
Профилактика внебольничной пневмонии Внебольничная пневмония — это острое заболевание, возникшее во внебольничных условиях (вне стационара) сопровождающееся симптомами инфекции нижних отделов дыхательных путей (лихорадка, кашель, выделение мокроты, боль в грудной клетке, одышка) и рентгенологическими признаками.
Острой пневмонией называют инфекционное заболевание, при котором в воспалительный процесс вовлекаются структурные единицы легкого — альвеолы и окружающая их соединительная ткань. В тяжелых случаях пневмония может привести к летальному исходу, когда поражаются практически оба легких. Внебольничная пневмония является достаточно распространенным заболеванием в нашей стране. За последние 2 года наблюдается рост количества заболеваний. Основная группа микроорганизмов, способных вызвать внебольничные пневмонии: пневмококк, гемофильная палочка, клебсиелла, хламидия, микоплазма, легионелла, респираторные вирусы. Источником инфекции является больной человек с признаками инфекций дыхательных путей, а также люди с бессимптомными и манифестными формами болезни; основной путь передачи — воздушно-капельный (при чихании, кашле, разговоре, дыхании). В типичных случаях острая пневмония проявляется следующими симптомами: повышение температуры тела, озноб, кашель, который сначала может быть сухим, а потом стать влажным с отделением мокроты, одышка — ощущение затруднения при дыхании, боли в грудной клетке при дыхании. Также больного могут беспокоить общие симптомы, особенно при тяжелых случаях: резкая слабость, отсутствие аппетита, боли в суставах, диарея, тошнота, рвота, тахикардия (частый пульс), снижение артериального давления. К сожалению, из-за особенностей самих микроорганизмов, а также и по причине безграмотного и неправильного бесконтрольного применения населением антибиотиков, например, при острых вирусных респираторных заболеваниях (ОРВИ или ОРЗ), многие бактерии приобрели устойчивость к ряду антибиотиков, поэтому применение этих препаратов в современных условиях не всегда бывает эффективным, что заставляет менять схемы лечения, или вместо одного антибиотика использовать несколько. Лечение назначает только врач.
Также больного могут беспокоить общие симптомы, особенно при тяжелых случаях: резкая слабость, отсутствие аппетита, боли в суставах, диарея, тошнота, рвота, тахикардия (частый пульс), снижение артериального давления. К сожалению, из-за особенностей самих микроорганизмов, а также и по причине безграмотного и неправильного бесконтрольного применения населением антибиотиков, например, при острых вирусных респираторных заболеваниях (ОРВИ или ОРЗ), многие бактерии приобрели устойчивость к ряду антибиотиков, поэтому применение этих препаратов в современных условиях не всегда бывает эффективным, что заставляет менять схемы лечения, или вместо одного антибиотика использовать несколько. Лечение назначает только врач.
Основные рекомендации по профилактике пневмонии:
1. Необходимо вести здоровый образ жизни: заниматься физкультурой и спортом, не курить и не употреблять алкоголь, совершать частые прогулки на свежем воздухе.
2. Необходимо здоровое полноценное питание с достаточным содержанием белков, микроэлементов и витаминов.
3. До наступления холодов и подъема заболеваемости респираторными инфекциями следует сделать прививку против гриппа, поскольку пневмония часто является осложнением гриппа, протекает очень тяжело и может привести к летальному исходу.
4. Для профилактики пневмонии у детей существуют вакцины против гемофильной и пневмококковой инфекций; необходимо также ежегодно прививать детей против гриппа.
5. В холодное время года нужно одеваться по погоде, избегать переохлаждений и сквозняков.
6. Следует соблюдать режимы проветривания и влажной уборки в помещениях.
7. Как можно чаще мыть руки и промывать носовые ходы.
8. В период подъема заболеваемости гриппом рекомендуется избегать контакта с больными ОРВИ и гриппом людьми, использовать маску для защиты органов дыхания, воздержаться от посещения мест с большим скоплением людей.
9. Принимать иммуностимулирующие препараты: препараты на основе эхинацеи (иммунал, иммунорм), экстракт корней элеутерококка.
Однако очень важно учитывать то, что имеющие растительное происхождение иммуностимуляторы не могут применяться бесконтрольно, так как существуют определенные противопоказания, о которых необходимо узнать перед приемом у врача. Очень полезный иммуностимулятор, который прекрасно подходит детям, это мед. В нем содержится очень большое количество полезных незаменимых витаминов и микроэлементов. Единственным противопоказанием в данном случае являются аллергические реакции на мед. Очень сильным иммуностимулятором является чеснок. Однако важно учесть, что детям до трех лет можно давать исключительно вареный чеснок.
Очень полезный иммуностимулятор, который прекрасно подходит детям, это мед. В нем содержится очень большое количество полезных незаменимых витаминов и микроэлементов. Единственным противопоказанием в данном случае являются аллергические реакции на мед. Очень сильным иммуностимулятором является чеснок. Однако важно учесть, что детям до трех лет можно давать исключительно вареный чеснок.
В заключении надо сказать: если заболели Вы или ваш ребенок, то не стоит идти на работу или вести ребенка в сад, школу, так как можете заразить людей находящихся с вами или вашим ребенком в контакте, а также не вызвать осложнение собственного заболевания. Вызовите врача на дом или обратитесь за медицинской помощью в поликлинику. Поставить диагноз, определить степень тяжести заболевания и прогноз может только врач. При наличии у Вас или вашего ребенка повышенной температуры тела, сухого кашля или кашля с отделением мокроты, одышки, боли в груди, немотивированной слабости, утомляемости, сильном потоотделении, особенно по ночам, обратитесь к врачу-терапевту, врачу-педиатру. Вам и вашему ребенку будет назначено своевременное лечение пневмонии, индивидуальное для каждого, с учетом тяжести заболевания, возраста, сопутствующих заболеваний. Врач-терапевт и врач-педиатр поможет Вам и вашему ребенку снова стать здоровыми!!!!!
Вам и вашему ребенку будет назначено своевременное лечение пневмонии, индивидуальное для каждого, с учетом тяжести заболевания, возраста, сопутствующих заболеваний. Врач-терапевт и врач-педиатр поможет Вам и вашему ребенку снова стать здоровыми!!!!!
Как легкие восстанавливаются после коронавируса?
https://ria.ru/20201201/legkie-1587071696.html
Как легкие восстанавливаются после коронавируса?
Как легкие восстанавливаются после коронавируса?
Легкие человека самостоятельно регенерируются после перенесенного коронавируса. Как ускорить этот процесс, рассказал в интервью радио Sputnik пульмонолог… РИА Новости, 01.12.2020
2020-12-01T02:12
2020-12-01T02:12
2020-12-01T02:12
распространение коронавируса
александр карабиненко
коронавирус в россии
коронавирус covid-19
россия
здоровье
медицина
общество
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdn21. img.ria.ru/images/07e4/0b/03/1582897357_0:135:3162:1914_1920x0_80_0_0_5bea142ef7ec8217bb7281e37751fb07.jpg
img.ria.ru/images/07e4/0b/03/1582897357_0:135:3162:1914_1920x0_80_0_0_5bea142ef7ec8217bb7281e37751fb07.jpg
МОСКВА, 1 дек — РИА Новости. Легкие человека самостоятельно регенерируются после перенесенного коронавируса. Как ускорить этот процесс, рассказал в интервью радио Sputnik пульмонолог Александр Карабиненко.Перенесенная коронавирусная пневмония оставляет последствия, с которыми придется бороться некоторое время. В легких переболевшего человека еще сохраняется обширная зона фиброзных изменений, кашель и одышка могут наблюдаться достаточно долго, до полутора месяцев, отметил Александр Карабиненко. Но если не мешать организму, пройдет полный процесс восстановления легких, пояснил врач.По его словам, человек, который курит, не дает легким возможности восстановиться. В данном случае это не просто вредная привычка, а медленное самоубийство, уверен Карабиненко. «Если человек курит, то у него легкие никогда не восстановятся после тяжелой пневмонии или коронавируса. Курить после этого – это просто медленное самоубийство. Без этого сами легкие восстановятся. Этот процесс происходит у всех по-разному», – уточнил врач.В среднем восстановление легких идет от трех месяцев до года. Многое зависит от состояния иммунитета и физической формы человека. «Все эти болезни, связанные с коронавирусом и другими инфекционными заболеваниями органов дыхания, говорят о слабости защитных сил. На первом месте иммунитет, потом физические кондиции человека. Человек, который занимается спортом, который следит за своим здоровьем, даже если заболевает, то болеет не так сильно, как тот, кто за собой не следил», – заключил Карабиненко.
Без этого сами легкие восстановятся. Этот процесс происходит у всех по-разному», – уточнил врач.В среднем восстановление легких идет от трех месяцев до года. Многое зависит от состояния иммунитета и физической формы человека. «Все эти болезни, связанные с коронавирусом и другими инфекционными заболеваниями органов дыхания, говорят о слабости защитных сил. На первом месте иммунитет, потом физические кондиции человека. Человек, который занимается спортом, который следит за своим здоровьем, даже если заболевает, то болеет не так сильно, как тот, кто за собой не следил», – заключил Карабиненко.
https://ria.ru/20201130/virusolog-1587003210.html
https://ria.ru/20201130/simptomy-1587010000.html
россия
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2020
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og. xn--p1ai/awards/
xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
https://cdn25.img.ria.ru/images/07e4/0b/03/1582897357_747:55:3150:1857_1920x0_80_0_0_9166f6a400da1761fee9331f1f518000.jpg
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
александр карабиненко, коронавирус в россии, коронавирус covid-19, россия, здоровье, медицина, общество
МОСКВА, 1 дек — РИА Новости. Легкие человека самостоятельно регенерируются после перенесенного коронавируса. Как ускорить этот процесс, рассказал в интервью радио Sputnik пульмонолог Александр Карабиненко.
Как ускорить этот процесс, рассказал в интервью радио Sputnik пульмонолог Александр Карабиненко.
Перенесенная коронавирусная пневмония оставляет последствия, с которыми придется бороться некоторое время. В легких переболевшего человека еще сохраняется обширная зона фиброзных изменений, кашель и одышка могут наблюдаться достаточно долго, до полутора месяцев, отметил Александр Карабиненко. Но если не мешать организму, пройдет полный процесс восстановления легких, пояснил врач.
«Есть процесс регенерации в нашем организме, когда одни клетки отмирают, а другие рождаются, при этом восстанавливается и структура легких, но в некоторых случаях это происходит не полностью, так бывает, если человек сам себя губит», – сказал пульмонолог.
По его словам, человек, который курит, не дает легким возможности восстановиться. В данном случае это не просто вредная привычка, а медленное самоубийство, уверен Карабиненко.
30 ноября 2020, 17:03Распространение коронавирусаВирусолог назвал условие завершения эпидемии COVID-19 в России
«Если человек курит, то у него легкие никогда не восстановятся после тяжелой пневмонии или коронавируса.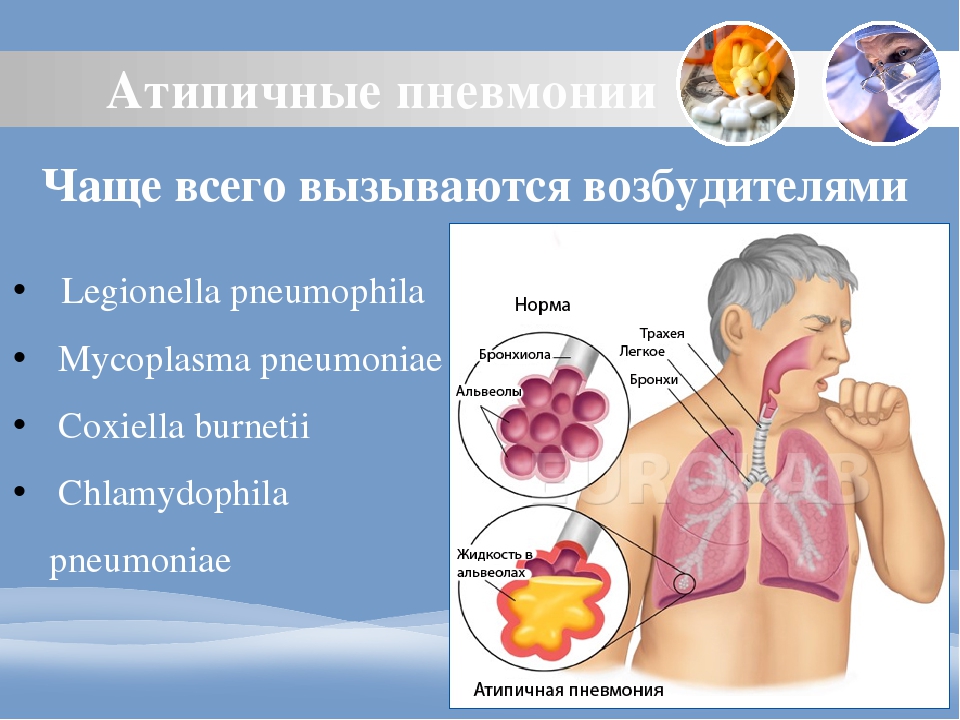 Курить после этого – это просто медленное самоубийство. Без этого сами легкие восстановятся. Этот процесс происходит у всех по-разному», – уточнил врач.
Курить после этого – это просто медленное самоубийство. Без этого сами легкие восстановятся. Этот процесс происходит у всех по-разному», – уточнил врач.
В среднем восстановление легких идет от трех месяцев до года. Многое зависит от состояния иммунитета и физической формы человека.
«Все эти болезни, связанные с коронавирусом и другими инфекционными заболеваниями органов дыхания, говорят о слабости защитных сил. На первом месте иммунитет, потом физические кондиции человека. Человек, который занимается спортом, который следит за своим здоровьем, даже если заболевает, то болеет не так сильно, как тот, кто за собой не следил», – заключил Карабиненко.
30 ноября 2020, 17:28Распространение коронавирусаМясников назвал наиболее опасные симптомы коронавируса
Пневмония — наш мир в данных
Институт показателей и оценки здоровья (IMHE). (2014). Ускоряя темп: прогресс и проблемы в борьбе с детской пневмонией.
Макаллистер, Д. А., Лю, Л., Ши, Т., Чу, Ю.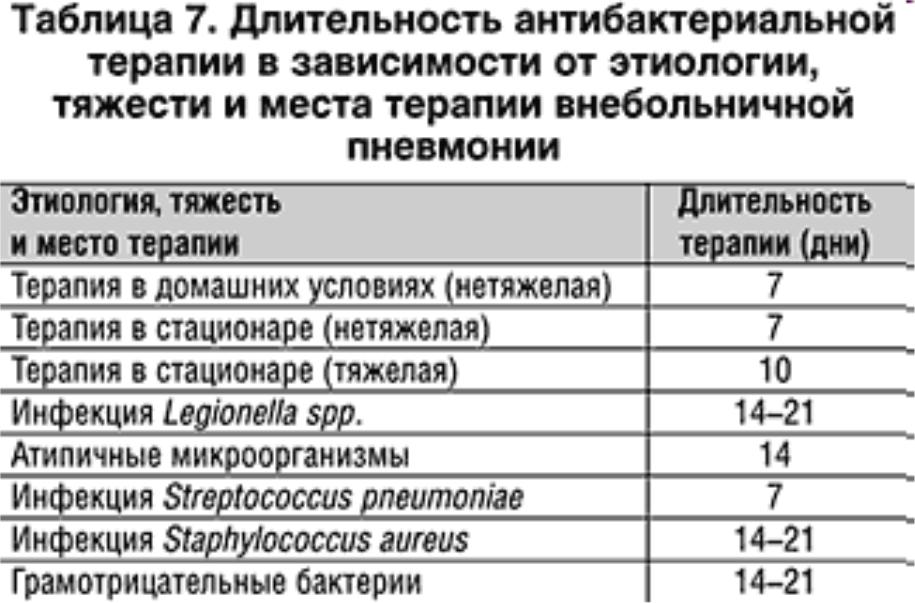 , Рид, К., Берроуз, Дж.,… И Наир, Х. (2019). Глобальные, региональные и национальные оценки заболеваемости и смертности от пневмонии у детей младше 5 лет в период с 2000 по 2015 год: систематический анализ. The Lancet Global Health , 7 (1), e47-e57.
, Рид, К., Берроуз, Дж.,… И Наир, Х. (2019). Глобальные, региональные и национальные оценки заболеваемости и смертности от пневмонии у детей младше 5 лет в период с 2000 по 2015 год: систематический анализ. The Lancet Global Health , 7 (1), e47-e57.
Мы используем термин пневмония здесь как широкий термин для обозначения инфекций нижних дыхательных путей. См. Этот раздел, чтобы узнать, как эти термины определены и почему они сгруппированы вместе.
(286.1-260.9) /286.1=0.09
Уоткинс, К., и Шридхар, Д. (2018). Пневмония: глобальная причина без чемпионов. Ланцет , 392 (10149), 718-719.
Редакция журнала Lancet Global Health (2018). Позорное пренебрежение детской пневмонией. Ланцет. Глобальное здравоохранение , 6 (12), e1253.
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг . : систематический анализ для исследования глобального бремени болезней, 2016 г. The Lancet Infectious Diseases , 18 ( 11), 1191-1210.
: систематический анализ для исследования глобального бремени болезней, 2016 г. The Lancet Infectious Diseases , 18 ( 11), 1191-1210.
Чисти, м.Дж., Тебрюгге, М., Ла Винсенте, С., Грэхем, С. М., и Дьюк, Т. (2009). Пневмония у детей с тяжелой недостаточностью питания в развивающихся странах — риск смертности, этиология и достоверность клинических признаков ВОЗ: систематический обзор. Тропическая медицина и международное здравоохранение , 14 (10), 1173-1189.
Дерани, М., Поуп, Д., Маскаренхас, М., Смит, К. Р., Вебер, М., и Брюс, Н. (2008). Загрязнение воздуха внутри помещений в результате использования необработанного твердого топлива и риск пневмонии у детей в возрасте до пяти лет: систематический обзор и метаанализ.
Бюллетень Всемирной организации здравоохранения (2006). Рекомендации по качеству воздуха: глобальное обновление, 2005 г., стр. 123-124.
Нел, А. (2005). Заболевания, связанные с загрязнением воздуха: воздействие частиц. Science , 308 (5723), 804-806.
Science , 308 (5723), 804-806.
Эберг, М., Яаккола, М. С., Вудворд, А., Перуга, А., и Прюсс-Устюн, А. (2011). Бремя болезней от воздействия вторичного табачного дыма во всем мире: ретроспективный анализ данных из 192 стран .Ланцет , 377 (9760), 139-146. Исследование показало, что пассивное курение привело к 165 000 смертей среди детей в возрасте до 5 лет от болезней нижних дыхательных путей.
Теодорату, Э., Макаллистер, Д. А., Рид, К., Аделой, Д. О., Рудан, И., Мухе, Л. М.,… и Наир, Х. (2014). Глобальные, региональные и национальные оценки бремени пневмонии у ВИЧ-инфицированных детей в 2010 г .: метаанализ и модельное исследование. The Lancet Infectious Diseases , 14 (12), 1250-1258.
Дополнение к: McAllister DA, Liu L, Shi T, et al. Глобальные, региональные и национальные оценки заболеваемости и смертности от пневмонии у детей младше 5 лет в период с 2000 по 2015 год: систематический анализ. Lancet Glob Health 2018; опубликовано онлайн 26 ноября.
Lancet Glob Health 2018; опубликовано онлайн 26 ноября.
Коэн, К., Фон Моллендорф, К., Де Гувейя, Л., Ленгана, С., Мейринг, С., Куан, В.,… и Мадхи, С. А. (2017). Эффективность 13-валентной пневмококковой конъюгированной вакцины против инвазивной пневмококковой инфекции у южноафриканских детей: исследование случай-контроль. The Lancet Global Health , 5 (3), e359-e369.
Лусеро, М. Г., Дулалия, В. Э., Ниллос, Л. Т., Уильямс, Г., Парреньо, Р. А. Н., Нохинек, Х.,… и Макела, Х. (2009). Пневмококковые конъюгированные вакцины для профилактики инвазивного пневмококкового заболевания вакцинного типа и пневмонии, определяемой с помощью рентгеновских лучей, у детей в возрасте до двух лет. Кокрановская база данных систематических обзоров , (4).
Мур, М. Р., Линк-Геллес, Р., Шаффнер, В., Линфилд, Р., Хольцман, К., Харрисон, Л. Х.,… и Томас, А. (2016). Эффективность 13-валентной пневмококковой конъюгированной вакцины для профилактики инвазивного пневмококкового заболевания у детей в США: исследование типа случай-контроль. Ланцет респираторной медицины , 4 (5), 399-406.
Ланцет респираторной медицины , 4 (5), 399-406.
Чен, К., Лисерас, Ф. К., Флаше, С., Сидхарта, С., Юн, Дж., Сундарам, Н., и Джит, М. (2019). Эффект и экономическая эффективность пневмококковой конъюгированной вакцинации: анализ глобального моделирования. The Lancet Global Health , 7 (1), e58-e67.
Подробнее о пневмококковых вакцинах см. В разделе ниже.
Кроме того, вакцинация детей PCV может защитить взрослых за счет эффекта стада, а это означает, что преимущества не ограничиваются одной возрастной группой населения — особенно важно, поскольку пневмония является значительным бременем для пожилых людей.
Chen, C., Liceras, F. C., Flasche, S., Sidharta, S., Yoong, J., Sundaram, N., & Jit, M.(2019). Эффект и экономическая эффективность пневмококковой конъюгированной вакцинации: анализ глобального моделирования. The Lancet Global Health , 7 (1), e58-e67.
Троегер, К. , Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования Global Burden of Disease Study 2016. The Lancet Infectious Diseases , 18 (11), 1191-1210.
, Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования Global Burden of Disease Study 2016. The Lancet Infectious Diseases , 18 (11), 1191-1210.
Ламберти, Л. М., Закария-Гркович, И., Уокер, К. Л. Ф., Теодорату, Э., Наир, Х., Кэмпбелл, Х. и Блэк, Р. Э. (2013). Грудное вскармливание для снижения риска заболеваемости и смертности от пневмонии у детей до двух лет: систематический обзор литературы и метаанализ. BMC общественное здравоохранение , 13 (3), S18.
41% число оценивается ЮНИСЕФ на основе самых последних данных, доступных для стран из опросов в период с 2013 по 2018 год.
ДАННЫЕ ЮНИСЕФ. (2019). Кормление детей грудного и раннего возраста . [онлайн] [доступ 4 сентября 2019 г. ].
].
ВОЗ, США (2006 г.). Рекомендации по качеству воздуха: глобальное обновление, 2005 г., стр. 123-124. Всемирная организация здравоохранения .
Фердоус, Ф., Ахмед, С., Дас, С. К., Чисти, М. Дж., Насрин, Д., Котлофф, К. Л.,… и Вагацума, Ю. (2018). Смертность от пневмонии и использование медицинских услуг у маленьких детей в сельских районах Бангладеш: проспективное вербальное вскрытие. Тропическая медицина и здоровье , 46 (1), 17.
ДАННЫЕ ЮНИСЕФ. (2018). Пневмония у детей . [онлайн] [Доступ 5 сентября 2019 г.]
Всемирная организация здравоохранения. (2014). Пересмотренная классификация ВОЗ и лечение пневмонии у детей в медицинских учреждениях: краткое справочное руководство (№ WHO / FWC / MCA / 14.9). Всемирная организация здоровья.
Unicef.org. (2018). Дисперсные таблетки амоксициллина: обновление рынка и предложения .[онлайн] [доступ 26 сентября 2019 г. ].
].
Unicef. (2016). Положение детей в мире, 2016 г. Нью-Йорк: Детский фонд Организации Объединенных Наций .
Лаззерини, М., Сонего, М., и Пеллегрин, М.С. (2015). Гипоксемия как фактор риска смертности от острых респираторных инфекций нижних дыхательных путей у детей в странах с низким и средним уровнем дохода: систематический обзор и метаанализ. PLoS One , 10 (9), e0136166.
Воздух, которым мы дышим, содержит 21% газообразного кислорода, но можно сконцентрировать этот газ с помощью специальных концентраторов кислорода.Затем обогащенный кислородом воздух может подаваться к человеку с пневмонией через дыхательную маску, таким образом компенсируя снижение кислородного обмена в легких.
Всемирная организация здравоохранения. (2016). Кислородная терапия для детей: пособие для медицинских работников.
Всемирная организация здравоохранения. (2019). Типовой список основных лекарственных средств ВОЗ: 7-й список, август 2019 г.
Делароза, Дж., Хейс, Дж., Пантюшенко, Э., Кейт, Б., Эмблер, Г.и Лоуренс К. (2017). Кислород необходим: учебник по политике и защите интересов . [онлайн] ПУТЬ. [Доступ 5 сентября 2019 г.].
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования глобального бремени болезней, 2016 г. The Lancet Infectious Diseases , 18 ( 11), 1191-1210.
Who.int. (2019) — Охват иммунизацией . [онлайн] [доступ 10 сентября 2019 г.]. http://view-hub.org/viz/ (Перейти к PCV -> PCV — Доступ к вакцинам -> Дети без доступа)
Hanada, S., Pirzadeh, M., Carver, KY, & Deng, JC (2018). Изменения микробиома, вызванные респираторной вирусной инфекцией, и вторичная бактериальная пневмония. Frontiers in иммунологии , 9 , 2640.
Frontiers in иммунологии , 9 , 2640.
Song, J. Y., Nahm, M.Х. и Мозли М.А. (2013). Клинические последствия пневмококковых серотипов: потенциал инвазивного заболевания, клинические проявления и устойчивость к антибиотикам. Журнал корейской медицины , 28 (1), 4-15.
Количество серотипов, включенных в вакцину, обычно указывается в ее названии, например PCV13 — пневмококковая конъюгированная вакцина, эффективная против 13 серотипов бактерий. Вакцины, включающие все больше серотипов, вводились с годами, ЦВС7 был представлен в 2000 году, а сегодня наиболее часто используемый ЦВС13 был представлен в 2010 году.
Хаусдорф, В. П., Фейкин, Д. Р., & Клугман, К. П. (2005). Эпидемиологические различия между серотипами пневмококков. Ланцет инфекционных болезней , 5 (2), 83-93.
Текущая неконъюгированная вакцина, PPSV23, обычно вводится только взрослым или в виде однократной дозы после двух иммунизаций PCV13 детям старше 2 лет.
Голос, М., Элиаким-Раз, Н., Стерн, А., Лейбович, Л., и Пол, М. (2016). Конъюгированная пневмококковая вакцина в сравнении с полисахаридной пневмококковой вакциной для профилактики пневмонии и инвазивной пневмококковой инфекции у иммунокомпетентных и ослабленных иммунитетом взрослых и детей. Кокрановская база данных систематических обзоров , (8).
27% относятся к рентгенологически определенным случаям пневмонии. Для клинически установленной пневмонии, менее точного диагноза, чем для случаев, определенных с помощью рентгеновского излучения, число составляет 6%. Оба этих показателя относятся к случаям пневмонии, вызванной любым возбудителем, а не только пневмококком. Лусеро, М. Г., Дулалия, В. Э., Ниллос, Л. Т., Уильямс, Г., Парреньо, Р. А. Н., Нохинек, Х.,… и Макела, Х. (2009). Пневмококковые конъюгированные вакцины для профилактики инвазивного пневмококкового заболевания вакцинного типа и пневмонии, определяемой с помощью рентгеновских лучей, у детей в возрасте до двух лет.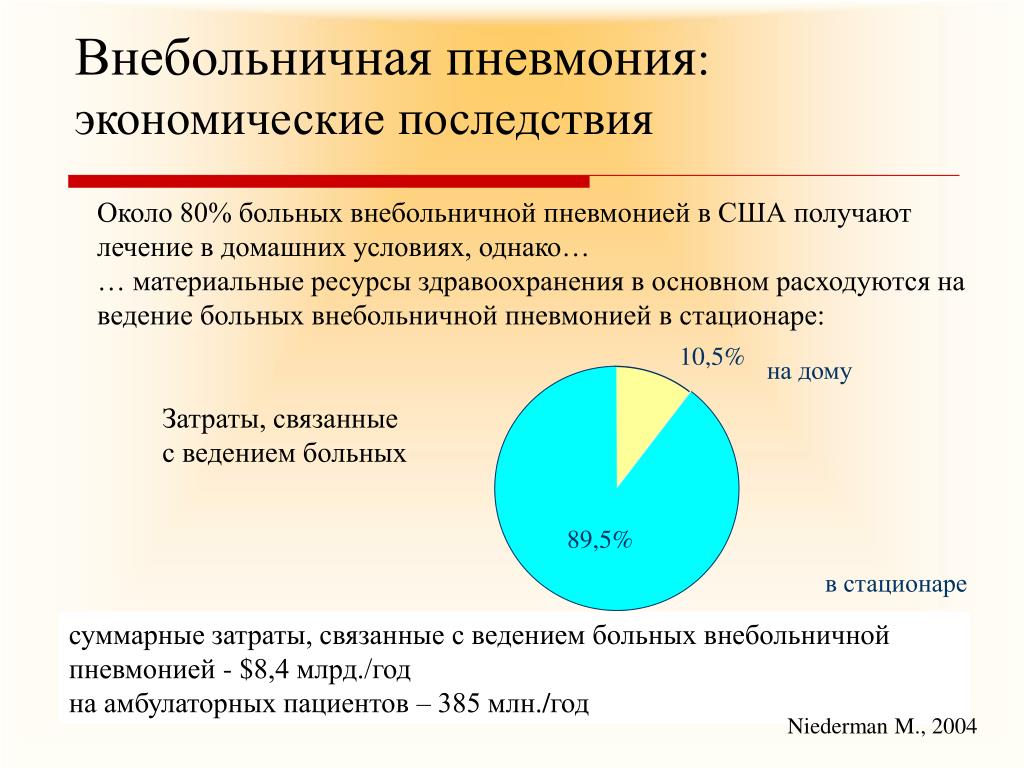 Кокрановская база данных систематических обзоров , (4).
Кокрановская база данных систематических обзоров , (4).
Вал Б., О’Брайен К. Л., Гринбаум А., Маджумдер А., Лю Л., Чу Ю.,… и Рудан И. (2018). Бремя болезней Streptococcus pneumoniae и Haemophilus influenzae типа b у детей в эпоху конъюгированных вакцин: глобальные, региональные и национальные оценки за 2000-15 гг. The Lancet Global Health , 6 (7), e744-e757.
Chen, C., Liceras, F. C., Flasche, S., Sidharta, S., Юн, Дж., Сундарам, Н., и Джит, М. (2019). Эффект и экономическая эффективность пневмококковой конъюгированной вакцинации: анализ глобального моделирования. The Lancet Global Health , 7 (1), e58-e67.
ГАВИ (Глобальный альянс по вакцинам и иммунизации) — это некоммерческая организация, которая обеспечивает доступ к программам вакцинации для стран с низким уровнем доходов, предоставляя финансовую поддержку и индивидуальный опыт.
О’Брайен, К. Л. (2018).Когда меньше значит больше: сколько доз ПКВ достаточно ?. The Lancet Infectious Diseases , 18 (2), 127-128.
The Lancet Infectious Diseases , 18 (2), 127-128.
Например, Кения недавно вступила в переходную фазу, во время которой она будет оплачивать все большую и большую часть стоимости вакцины PCV. К 2027 году Кения должна будет заплатить полную цену в размере 9 долларов за трехдозовый курс вакцинации детей. Расходы на здравоохранение на душу населения в Кении в 2016 году составили около 66 долларов (5% ВВП), очевидно, 9 долларов на ребенка — это нетривиальные затраты.
Симонсен, Л., ван Вейхе, М., и Тейлор, Р. (2019). Дорогие вакцины — лучшее вложение для стран с низким и средним доходом? The Lancet Global Health , 7 (5), e548-e549.
Оджал, Дж., Гриффитс, У., Хаммитт, Л. Л., Адетифа, И., Акеч, Д., Табу, К.,… и Флаше, С. (2019). Поддержание пневмококковой вакцинации после перехода от поддержки Гави: моделирование и исследование экономической эффективности в Кении. The Lancet Global Health , 7 (5), e644-e654.
Окупаемость инвестиций была оценена для прогнозируемого охвата отдельных стран на десятилетие с 2011 по 2020 годы. Это означает, что экономические выгоды (измеряемые затратами на программу вакцинации, вычтенными из сокращенных затрат на лечение и потери производительности ) использования вакцины в 3 раза выше, чем ее неиспользования.
Для снижения затрат некоторые страны могут также рассмотреть возможность перехода на схему иммунизации с двумя, а не с тремя дозами, однако необходимы дополнительные исследования эффективности этого графика в разных странах.См. O’Brien et al. (2018) ссылка.
Накамура М. М., Тасслими А., Лиу Т. А., Левин О., Нолл М. Д., Рассел Л. Б. и Синха А. (2011). Экономическая эффективность детской пневмококковой конъюгированной вакцинации в странах со средним уровнем дохода. Международное здравоохранение , 3 (4), 270-281.
Одзава, С., Кларк, С., Портной, А., Гревал, С., Брензель, Л., и Уокер, Д. Г. (2016). Рентабельность инвестиций в иммунизацию детей в странах с низким и средним уровнем доходов, 2011–2020 гг. Департамент здравоохранения , 35 (2), 199-207.
Г. (2016). Рентабельность инвестиций в иммунизацию детей в странах с низким и средним уровнем доходов, 2011–2020 гг. Департамент здравоохранения , 35 (2), 199-207.
Центр, И.В.А. (2017). Доказательная база для пневмококковых конъюгированных вакцин (ПКВ): данные для принятия решений относительно использования ПКВ в детстве. Балтимор (Мэриленд): Университет Джона Хопкинса .
Голдблатт, Д., Саузерн, Дж., Эндрюс, Н. Дж., Бербидж, П., Партингтон, Дж., Роалф, Л.,… и Снейп, М. Д. (2018). Пневмококковая конъюгированная вакцина 13 доставлялась в виде одной первичной и одной бустерной дозы (1+ 1) по сравнению с двумя первичными дозами и бустерной дозой (2+ 1) для младенцев в Великобритании: многоцентровое рандомизированное контролируемое исследование с параллельными группами. The Lancet Infectious Diseases , 18 (2), 171-179.
О’Брайен, К. Л. (2018). Когда меньше значит больше: сколько доз ПКВ достаточно ?. The Lancet Infectious Diseases , 18 (2), 127-128.
The Lancet Infectious Diseases , 18 (2), 127-128.
Адегбола Р. А., ДеАнтонио Р., Хилл П. К., Рока А., Усуф Э., Хут Б. и Гринвуд Б. М. (2014). Носительство Streptococcus pneumoniae и других респираторных бактериальных патогенов в странах с низким доходом и доходом ниже среднего: систематический обзор и метаанализ. PloS one , 9 (8), e103293.
Мегиддо, И., Кляйн, Э., и Лакшминараян, Р. (2018). Возможные последствия внедрения пневмококковой конъюгированной вакцины в национальные программы иммунизации: экономико-эпидемиологический анализ с использованием данных из Индии. BMJ global health , 3 (3), e000636.
Джонсон, Х. Л., Делориа-Нолл, М., Левин, О. С., Стошек, С. К., Ханс, Л. Ф., Райтингер, Р.,… и О’Брайен, К.Л. (2010). Систематическая оценка серотипов, вызывающих инвазивную пневмококковую болезнь у детей в возрасте до пяти лет: проект глобального серотипа пневмококков.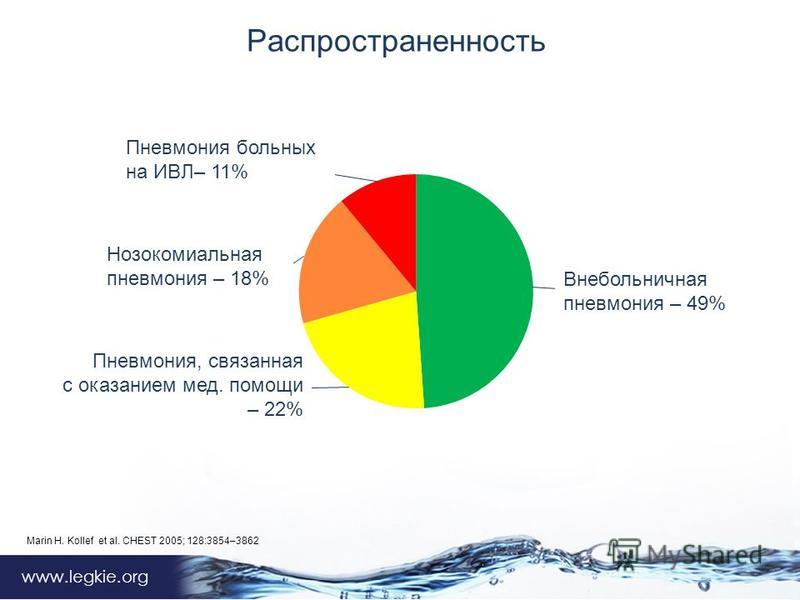 PLoS лекарство , 7 (10), e1000348.
PLoS лекарство , 7 (10), e1000348.
Всемирная организация здравоохранения. (2010). Изменение эпидемиологии пневмококковых серотипов после введения конъюгированной вакцины: отчет за июль 2010 г. Еженедельный эпидемиологический отчет [Relevé épidémiologique hebdomadaire ], 85 (43), 434-436.
Пичичеро, М.Е. (2017). Пневмококковые цельноклеточные и белковые вакцины: изменение парадигмы. Экспертиза вакцин , 16 (12), 1181-1190.
Гинзбург, А. С., Нах, М. Х., Хамбати, Ф. М., и Олдерсон, М. Р. (2012). Проблемы и вызовы разработки пневмококковых белковых вакцин. Экспертный обзор вакцин, 11 (3), 279-285
Troeger, C., Blacker, B., Khalil, I.A., Rao, P.C, Cao, J., Zimsen, S.R.,… & Adetifa, I.М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования глобального бремени болезней 2016 г. The Lancet Infectious Diseases , 18 (11), 1191-1210.
The Lancet Infectious Diseases , 18 (11), 1191-1210.
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования Global Burden of Disease Study 2016. The Lancet Infectious Diseases , 18 (11), 1191-1210.
О’Брайен, К. Л., Баггетт, Х. К., Брукс, В. А., Фейкин, Д. Р., Хаммитт, Л. Л., Хигдон, М. М.,… и Мадхи, С. А. (2019). Причины тяжелой пневмонии, требующей госпитализации у детей без ВИЧ-инфекции из Африки и Азии: многострановое исследование «случай-контроль» PERCH. Ланцет .
Например, когда происходит вторичная инфекция вирусом, которая может вызвать размножение обычно непатогенных бактерий.
Ханада, С., Пирзаде, М. , Карвер, К. Ю., и Дэн, Дж. К. (2018). Изменения микробиома, вызванные респираторной вирусной инфекцией, и вторичная бактериальная пневмония. Frontiers in Immunology , 9 , 2640.
, Карвер, К. Ю., и Дэн, Дж. К. (2018). Изменения микробиома, вызванные респираторной вирусной инфекцией, и вторичная бактериальная пневмония. Frontiers in Immunology , 9 , 2640.
Все визуализации, данные и код, произведенные «Нашим миром в данных», находятся в полностью открытом доступе по лицензии Creative Commons BY. У вас есть разрешение использовать, распространять и воспроизводить их на любом носителе при условии указания источника и авторов.
Данные, предоставленные третьими сторонами и предоставленные «Нашим миром в данных», регулируются условиями лицензии исходных сторонних авторов. Мы всегда будем указывать исходный источник данных в нашей документации, поэтому вы всегда должны проверять лицензию на любые такие сторонние данные перед использованием и распространением.
Наши статьи и визуализации данных основаны на работе множества разных людей и организаций. При цитировании этой записи просьба также указать основные источники данных. Эту запись можно цитировать:
Эту запись можно цитировать:
Пневмония — наш мир в данных
Институт показателей и оценки здоровья (IMHE). (2014). Ускоряя темп: прогресс и проблемы в борьбе с детской пневмонией.
Макаллистер, Д. А., Лю, Л., Ши, Т., Чу, Ю., Рид, К., Берроуз, Дж.,… И Наир, Х. (2019). Глобальные, региональные и национальные оценки заболеваемости и смертности от пневмонии у детей младше 5 лет в период с 2000 по 2015 год: систематический анализ. The Lancet Global Health , 7 (1), e47-e57.
Мы используем термин пневмония здесь как широкий термин для обозначения инфекций нижних дыхательных путей. См. Этот раздел, чтобы узнать, как эти термины определены и почему они сгруппированы вместе.
(286.1-260.9) /286.1=0.09
Уоткинс, К., и Шридхар, Д. (2018). Пневмония: глобальная причина без чемпионов. Ланцет , 392 (10149), 718-719.
Редакция журнала Lancet Global Health (2018).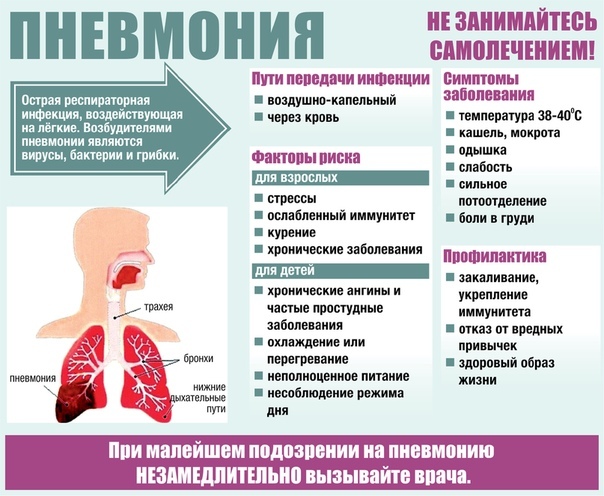 Позорное пренебрежение детской пневмонией. Ланцет. Глобальное здравоохранение , 6 (12), e1253.
Позорное пренебрежение детской пневмонией. Ланцет. Глобальное здравоохранение , 6 (12), e1253.
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования глобального бремени болезней, 2016 г. The Lancet Infectious Diseases , 18 ( 11), 1191-1210.
Чисти, М. Дж., Тебрюгге, М., Ла Винсенте, С., Грэхем, С. М., и Дюк, Т. (2009). Пневмония у детей с тяжелой недостаточностью питания в развивающихся странах — риск смертности, этиология и достоверность клинических признаков ВОЗ: систематический обзор. Тропическая медицина и международное здравоохранение , 14 (10), 1173-1189.
Дерани, М., Поуп, Д., Маскаренхас, М., Смит, К. Р., Вебер, М., и Брюс, Н.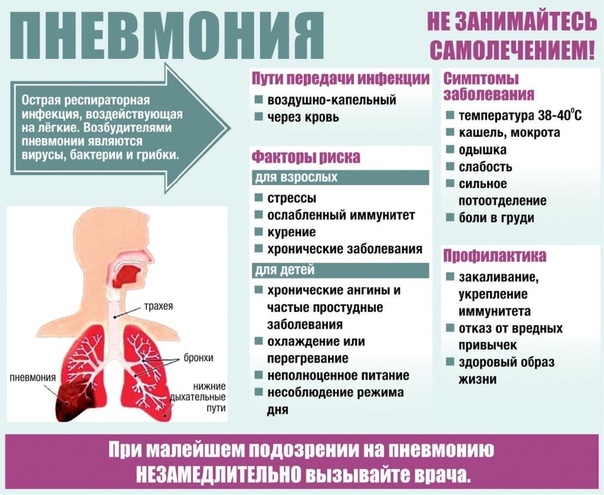 (2008). Загрязнение воздуха внутри помещений в результате использования необработанного твердого топлива и риск пневмонии у детей в возрасте до пяти лет: систематический обзор и метаанализ.
(2008). Загрязнение воздуха внутри помещений в результате использования необработанного твердого топлива и риск пневмонии у детей в возрасте до пяти лет: систематический обзор и метаанализ.
Бюллетень Всемирной организации здравоохранения (2006). Рекомендации по качеству воздуха: глобальное обновление, 2005 г., стр. 123-124.
Нел, А. (2005). Заболевания, связанные с загрязнением воздуха: воздействие частиц. Science , 308 (5723), 804-806.
Эберг, М., Яаккола, М. С., Вудворд, А., Перуга, А., и Прюсс-Устюн, А. (2011). Бремя болезней от воздействия вторичного табачного дыма во всем мире: ретроспективный анализ данных из 192 стран .Ланцет , 377 (9760), 139-146. Исследование показало, что пассивное курение привело к 165 000 смертей среди детей в возрасте до 5 лет от болезней нижних дыхательных путей.
Теодорату, Э., Макаллистер, Д. А., Рид, К., Аделой, Д. О., Рудан, И., Мухе, Л. М.,… и Наир, Х. (2014). Глобальные, региональные и национальные оценки бремени пневмонии у ВИЧ-инфицированных детей в 2010 г .: метаанализ и модельное исследование. The Lancet Infectious Diseases , 14 (12), 1250-1258.
М.,… и Наир, Х. (2014). Глобальные, региональные и национальные оценки бремени пневмонии у ВИЧ-инфицированных детей в 2010 г .: метаанализ и модельное исследование. The Lancet Infectious Diseases , 14 (12), 1250-1258.
Дополнение к: McAllister DA, Liu L, Shi T, et al. Глобальные, региональные и национальные оценки заболеваемости и смертности от пневмонии у детей младше 5 лет в период с 2000 по 2015 год: систематический анализ. Lancet Glob Health 2018; опубликовано онлайн 26 ноября.
Коэн, К., Фон Моллендорф, К., Де Гувейя, Л., Ленгана, С., Мейринг, С., Куан, В.,… и Мадхи, С. А. (2017). Эффективность 13-валентной пневмококковой конъюгированной вакцины против инвазивной пневмококковой инфекции у южноафриканских детей: исследование случай-контроль. The Lancet Global Health , 5 (3), e359-e369.
Лусеро, М. Г., Дулалия, В. Э., Ниллос, Л. Т., Уильямс, Г., Парреньо, Р. А. Н., Нохинек, Х.,… и Макела, Х.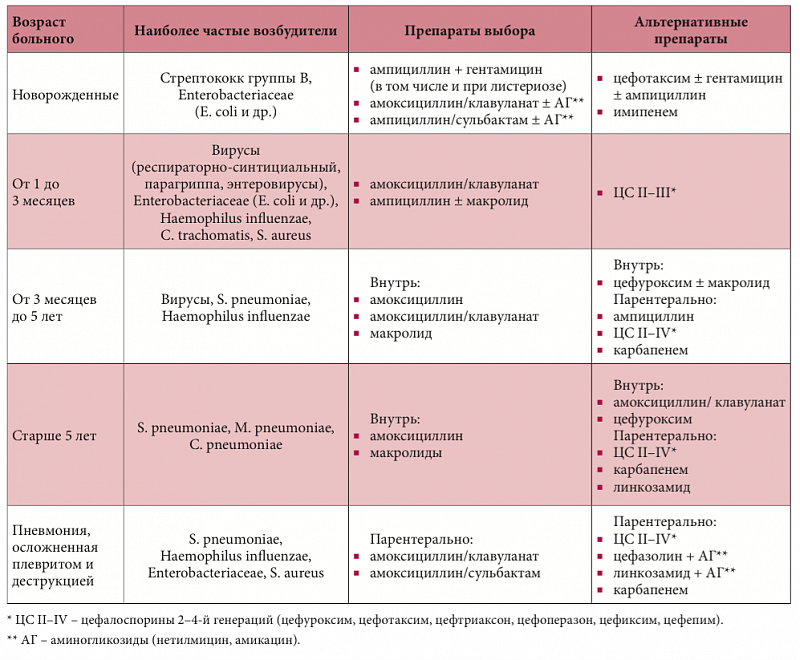 (2009). Пневмококковые конъюгированные вакцины для профилактики инвазивного пневмококкового заболевания вакцинного типа и пневмонии, определяемой с помощью рентгеновских лучей, у детей в возрасте до двух лет. Кокрановская база данных систематических обзоров , (4).
(2009). Пневмококковые конъюгированные вакцины для профилактики инвазивного пневмококкового заболевания вакцинного типа и пневмонии, определяемой с помощью рентгеновских лучей, у детей в возрасте до двух лет. Кокрановская база данных систематических обзоров , (4).
Мур, М. Р., Линк-Геллес, Р., Шаффнер, В., Линфилд, Р., Хольцман, К., Харрисон, Л. Х.,… и Томас, А. (2016). Эффективность 13-валентной пневмококковой конъюгированной вакцины для профилактики инвазивного пневмококкового заболевания у детей в США: исследование типа случай-контроль. Ланцет респираторной медицины , 4 (5), 399-406.
Чен, К., Лисерас, Ф. К., Флаше, С., Сидхарта, С., Юн, Дж., Сундарам, Н., и Джит, М. (2019). Эффект и экономическая эффективность пневмококковой конъюгированной вакцинации: анализ глобального моделирования. The Lancet Global Health , 7 (1), e58-e67.
Подробнее о пневмококковых вакцинах см. В разделе ниже.
Кроме того, вакцинация детей PCV может защитить взрослых за счет эффекта стада, а это означает, что преимущества не ограничиваются одной возрастной группой населения — особенно важно, поскольку пневмония является значительным бременем для пожилых людей.
Chen, C., Liceras, F. C., Flasche, S., Sidharta, S., Yoong, J., Sundaram, N., & Jit, M.(2019). Эффект и экономическая эффективность пневмококковой конъюгированной вакцинации: анализ глобального моделирования. The Lancet Global Health , 7 (1), e58-e67.
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования Global Burden of Disease Study 2016. The Lancet Infectious Diseases , 18 (11), 1191-1210.
Ламберти, Л. М., Закария-Гркович, И., Уокер, К. Л. Ф., Теодорату, Э., Наир, Х., Кэмпбелл, Х. и Блэк, Р. Э. (2013). Грудное вскармливание для снижения риска заболеваемости и смертности от пневмонии у детей до двух лет: систематический обзор литературы и метаанализ. BMC общественное здравоохранение , 13 (3), S18.
М., Закария-Гркович, И., Уокер, К. Л. Ф., Теодорату, Э., Наир, Х., Кэмпбелл, Х. и Блэк, Р. Э. (2013). Грудное вскармливание для снижения риска заболеваемости и смертности от пневмонии у детей до двух лет: систематический обзор литературы и метаанализ. BMC общественное здравоохранение , 13 (3), S18.
41% число оценивается ЮНИСЕФ на основе самых последних данных, доступных для стран из опросов в период с 2013 по 2018 год.
ДАННЫЕ ЮНИСЕФ. (2019). Кормление детей грудного и раннего возраста . [онлайн] [доступ 4 сентября 2019 г.].
ВОЗ, США (2006 г.). Рекомендации по качеству воздуха: глобальное обновление, 2005 г., стр. 123-124. Всемирная организация здравоохранения .
Фердоус, Ф., Ахмед, С., Дас, С. К., Чисти, М. Дж., Насрин, Д., Котлофф, К. Л.,… и Вагацума, Ю. (2018). Смертность от пневмонии и использование медицинских услуг у маленьких детей в сельских районах Бангладеш: проспективное вербальное вскрытие. Тропическая медицина и здоровье , 46 (1), 17.
Тропическая медицина и здоровье , 46 (1), 17.
ДАННЫЕ ЮНИСЕФ. (2018). Пневмония у детей . [онлайн] [Доступ 5 сентября 2019 г.]
Всемирная организация здравоохранения. (2014). Пересмотренная классификация ВОЗ и лечение пневмонии у детей в медицинских учреждениях: краткое справочное руководство (№ WHO / FWC / MCA / 14.9). Всемирная организация здоровья.
Unicef.org. (2018). Дисперсные таблетки амоксициллина: обновление рынка и предложения .[онлайн] [доступ 26 сентября 2019 г.].
Unicef. (2016). Положение детей в мире, 2016 г. Нью-Йорк: Детский фонд Организации Объединенных Наций .
Лаззерини, М., Сонего, М., и Пеллегрин, М.С. (2015). Гипоксемия как фактор риска смертности от острых респираторных инфекций нижних дыхательных путей у детей в странах с низким и средним уровнем дохода: систематический обзор и метаанализ. PLoS One , 10 (9), e0136166.
Воздух, которым мы дышим, содержит 21% газообразного кислорода, но можно сконцентрировать этот газ с помощью специальных концентраторов кислорода.Затем обогащенный кислородом воздух может подаваться к человеку с пневмонией через дыхательную маску, таким образом компенсируя снижение кислородного обмена в легких.
Всемирная организация здравоохранения. (2016). Кислородная терапия для детей: пособие для медицинских работников.
Всемирная организация здравоохранения. (2019). Типовой список основных лекарственных средств ВОЗ: 7-й список, август 2019 г.
Делароза, Дж., Хейс, Дж., Пантюшенко, Э., Кейт, Б., Эмблер, Г.и Лоуренс К. (2017). Кислород необходим: учебник по политике и защите интересов . [онлайн] ПУТЬ. [Доступ 5 сентября 2019 г.].
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования глобального бремени болезней, 2016 г. The Lancet Infectious Diseases , 18 ( 11), 1191-1210.
Who.int. (2019) — Охват иммунизацией . [онлайн] [доступ 10 сентября 2019 г.]. http://view-hub.org/viz/ (Перейти к PCV -> PCV — Доступ к вакцинам -> Дети без доступа)
Hanada, S., Pirzadeh, M., Carver, KY, & Deng, JC (2018). Изменения микробиома, вызванные респираторной вирусной инфекцией, и вторичная бактериальная пневмония. Frontiers in иммунологии , 9 , 2640.
Song, J. Y., Nahm, M.Х. и Мозли М.А. (2013). Клинические последствия пневмококковых серотипов: потенциал инвазивного заболевания, клинические проявления и устойчивость к антибиотикам. Журнал корейской медицины , 28 (1), 4-15.
Количество серотипов, включенных в вакцину, обычно указывается в ее названии, например PCV13 — пневмококковая конъюгированная вакцина, эффективная против 13 серотипов бактерий. Вакцины, включающие все больше серотипов, вводились с годами, ЦВС7 был представлен в 2000 году, а сегодня наиболее часто используемый ЦВС13 был представлен в 2010 году.
Хаусдорф, В. П., Фейкин, Д. Р., & Клугман, К. П. (2005). Эпидемиологические различия между серотипами пневмококков. Ланцет инфекционных болезней , 5 (2), 83-93.
Текущая неконъюгированная вакцина, PPSV23, обычно вводится только взрослым или в виде однократной дозы после двух иммунизаций PCV13 детям старше 2 лет.
Голос, М., Элиаким-Раз, Н., Стерн, А., Лейбович, Л., и Пол, М. (2016). Конъюгированная пневмококковая вакцина в сравнении с полисахаридной пневмококковой вакциной для профилактики пневмонии и инвазивной пневмококковой инфекции у иммунокомпетентных и ослабленных иммунитетом взрослых и детей. Кокрановская база данных систематических обзоров , (8).
27% относятся к рентгенологически определенным случаям пневмонии. Для клинически установленной пневмонии, менее точного диагноза, чем для случаев, определенных с помощью рентгеновского излучения, число составляет 6%. Оба этих показателя относятся к случаям пневмонии, вызванной любым возбудителем, а не только пневмококком. Лусеро, М. Г., Дулалия, В. Э., Ниллос, Л. Т., Уильямс, Г., Парреньо, Р. А. Н., Нохинек, Х.,… и Макела, Х. (2009). Пневмококковые конъюгированные вакцины для профилактики инвазивного пневмококкового заболевания вакцинного типа и пневмонии, определяемой с помощью рентгеновских лучей, у детей в возрасте до двух лет. Кокрановская база данных систематических обзоров , (4).
Вал Б., О’Брайен К. Л., Гринбаум А., Маджумдер А., Лю Л., Чу Ю.,… и Рудан И. (2018). Бремя болезней Streptococcus pneumoniae и Haemophilus influenzae типа b у детей в эпоху конъюгированных вакцин: глобальные, региональные и национальные оценки за 2000-15 гг. The Lancet Global Health , 6 (7), e744-e757.
Chen, C., Liceras, F. C., Flasche, S., Sidharta, S., Юн, Дж., Сундарам, Н., и Джит, М. (2019). Эффект и экономическая эффективность пневмококковой конъюгированной вакцинации: анализ глобального моделирования. The Lancet Global Health , 7 (1), e58-e67.
ГАВИ (Глобальный альянс по вакцинам и иммунизации) — это некоммерческая организация, которая обеспечивает доступ к программам вакцинации для стран с низким уровнем доходов, предоставляя финансовую поддержку и индивидуальный опыт.
О’Брайен, К. Л. (2018).Когда меньше значит больше: сколько доз ПКВ достаточно ?. The Lancet Infectious Diseases , 18 (2), 127-128.
Например, Кения недавно вступила в переходную фазу, во время которой она будет оплачивать все большую и большую часть стоимости вакцины PCV. К 2027 году Кения должна будет заплатить полную цену в размере 9 долларов за трехдозовый курс вакцинации детей. Расходы на здравоохранение на душу населения в Кении в 2016 году составили около 66 долларов (5% ВВП), очевидно, 9 долларов на ребенка — это нетривиальные затраты.
Симонсен, Л., ван Вейхе, М., и Тейлор, Р. (2019). Дорогие вакцины — лучшее вложение для стран с низким и средним доходом? The Lancet Global Health , 7 (5), e548-e549.
Оджал, Дж., Гриффитс, У., Хаммитт, Л. Л., Адетифа, И., Акеч, Д., Табу, К.,… и Флаше, С. (2019). Поддержание пневмококковой вакцинации после перехода от поддержки Гави: моделирование и исследование экономической эффективности в Кении. The Lancet Global Health , 7 (5), e644-e654.
Окупаемость инвестиций была оценена для прогнозируемого охвата отдельных стран на десятилетие с 2011 по 2020 годы. Это означает, что экономические выгоды (измеряемые затратами на программу вакцинации, вычтенными из сокращенных затрат на лечение и потери производительности ) использования вакцины в 3 раза выше, чем ее неиспользования.
Для снижения затрат некоторые страны могут также рассмотреть возможность перехода на схему иммунизации с двумя, а не с тремя дозами, однако необходимы дополнительные исследования эффективности этого графика в разных странах.См. O’Brien et al. (2018) ссылка.
Накамура М. М., Тасслими А., Лиу Т. А., Левин О., Нолл М. Д., Рассел Л. Б. и Синха А. (2011). Экономическая эффективность детской пневмококковой конъюгированной вакцинации в странах со средним уровнем дохода. Международное здравоохранение , 3 (4), 270-281.
Одзава, С., Кларк, С., Портной, А., Гревал, С., Брензель, Л., и Уокер, Д. Г. (2016). Рентабельность инвестиций в иммунизацию детей в странах с низким и средним уровнем доходов, 2011–2020 гг. Департамент здравоохранения , 35 (2), 199-207.
Центр, И.В.А. (2017). Доказательная база для пневмококковых конъюгированных вакцин (ПКВ): данные для принятия решений относительно использования ПКВ в детстве. Балтимор (Мэриленд): Университет Джона Хопкинса .
Голдблатт, Д., Саузерн, Дж., Эндрюс, Н. Дж., Бербидж, П., Партингтон, Дж., Роалф, Л.,… и Снейп, М. Д. (2018). Пневмококковая конъюгированная вакцина 13 доставлялась в виде одной первичной и одной бустерной дозы (1+ 1) по сравнению с двумя первичными дозами и бустерной дозой (2+ 1) для младенцев в Великобритании: многоцентровое рандомизированное контролируемое исследование с параллельными группами. The Lancet Infectious Diseases , 18 (2), 171-179.
О’Брайен, К. Л. (2018). Когда меньше значит больше: сколько доз ПКВ достаточно ?. The Lancet Infectious Diseases , 18 (2), 127-128.
Адегбола Р. А., ДеАнтонио Р., Хилл П. К., Рока А., Усуф Э., Хут Б. и Гринвуд Б. М. (2014). Носительство Streptococcus pneumoniae и других респираторных бактериальных патогенов в странах с низким доходом и доходом ниже среднего: систематический обзор и метаанализ. PloS one , 9 (8), e103293.
Мегиддо, И., Кляйн, Э., и Лакшминараян, Р. (2018). Возможные последствия внедрения пневмококковой конъюгированной вакцины в национальные программы иммунизации: экономико-эпидемиологический анализ с использованием данных из Индии. BMJ global health , 3 (3), e000636.
Джонсон, Х. Л., Делориа-Нолл, М., Левин, О. С., Стошек, С. К., Ханс, Л. Ф., Райтингер, Р.,… и О’Брайен, К.Л. (2010). Систематическая оценка серотипов, вызывающих инвазивную пневмококковую болезнь у детей в возрасте до пяти лет: проект глобального серотипа пневмококков. PLoS лекарство , 7 (10), e1000348.
Всемирная организация здравоохранения. (2010). Изменение эпидемиологии пневмококковых серотипов после введения конъюгированной вакцины: отчет за июль 2010 г. Еженедельный эпидемиологический отчет [Relevé épidémiologique hebdomadaire ], 85 (43), 434-436.
Пичичеро, М.Е. (2017). Пневмококковые цельноклеточные и белковые вакцины: изменение парадигмы. Экспертиза вакцин , 16 (12), 1181-1190.
Гинзбург, А. С., Нах, М. Х., Хамбати, Ф. М., и Олдерсон, М. Р. (2012). Проблемы и вызовы разработки пневмококковых белковых вакцин. Экспертный обзор вакцин, 11 (3), 279-285
Troeger, C., Blacker, B., Khalil, I.A., Rao, P.C, Cao, J., Zimsen, S.R.,… & Adetifa, I.М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования глобального бремени болезней 2016 г. The Lancet Infectious Diseases , 18 (11), 1191-1210.
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования Global Burden of Disease Study 2016. The Lancet Infectious Diseases , 18 (11), 1191-1210.
О’Брайен, К. Л., Баггетт, Х. К., Брукс, В. А., Фейкин, Д. Р., Хаммитт, Л. Л., Хигдон, М. М.,… и Мадхи, С. А. (2019). Причины тяжелой пневмонии, требующей госпитализации у детей без ВИЧ-инфекции из Африки и Азии: многострановое исследование «случай-контроль» PERCH. Ланцет .
Например, когда происходит вторичная инфекция вирусом, которая может вызвать размножение обычно непатогенных бактерий.
Ханада, С., Пирзаде, М., Карвер, К. Ю., и Дэн, Дж. К. (2018). Изменения микробиома, вызванные респираторной вирусной инфекцией, и вторичная бактериальная пневмония. Frontiers in Immunology , 9 , 2640.
Все визуализации, данные и код, произведенные «Нашим миром в данных», находятся в полностью открытом доступе по лицензии Creative Commons BY. У вас есть разрешение использовать, распространять и воспроизводить их на любом носителе при условии указания источника и авторов.
Данные, предоставленные третьими сторонами и предоставленные «Нашим миром в данных», регулируются условиями лицензии исходных сторонних авторов. Мы всегда будем указывать исходный источник данных в нашей документации, поэтому вы всегда должны проверять лицензию на любые такие сторонние данные перед использованием и распространением.
Наши статьи и визуализации данных основаны на работе множества разных людей и организаций. При цитировании этой записи просьба также указать основные источники данных.Эту запись можно цитировать:
Пневмония — наш мир в данных
Институт показателей и оценки здоровья (IMHE). (2014). Ускоряя темп: прогресс и проблемы в борьбе с детской пневмонией.
Макаллистер, Д. А., Лю, Л., Ши, Т., Чу, Ю., Рид, К., Берроуз, Дж.,… И Наир, Х. (2019). Глобальные, региональные и национальные оценки заболеваемости и смертности от пневмонии у детей младше 5 лет в период с 2000 по 2015 год: систематический анализ. The Lancet Global Health , 7 (1), e47-e57.
Мы используем термин пневмония здесь как широкий термин для обозначения инфекций нижних дыхательных путей. См. Этот раздел, чтобы узнать, как эти термины определены и почему они сгруппированы вместе.
(286.1-260.9) /286.1=0.09
Уоткинс, К., и Шридхар, Д. (2018). Пневмония: глобальная причина без чемпионов. Ланцет , 392 (10149), 718-719.
Редакция журнала Lancet Global Health (2018).Позорное пренебрежение детской пневмонией. Ланцет. Глобальное здравоохранение , 6 (12), e1253.
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования глобального бремени болезней, 2016 г. The Lancet Infectious Diseases , 18 ( 11), 1191-1210.
Чисти, М. Дж., Тебрюгге, М., Ла Винсенте, С., Грэхем, С. М., и Дюк, Т. (2009). Пневмония у детей с тяжелой недостаточностью питания в развивающихся странах — риск смертности, этиология и достоверность клинических признаков ВОЗ: систематический обзор. Тропическая медицина и международное здравоохранение , 14 (10), 1173-1189.
Дерани, М., Поуп, Д., Маскаренхас, М., Смит, К. Р., Вебер, М., и Брюс, Н. (2008). Загрязнение воздуха внутри помещений в результате использования необработанного твердого топлива и риск пневмонии у детей в возрасте до пяти лет: систематический обзор и метаанализ.
Бюллетень Всемирной организации здравоохранения (2006). Рекомендации по качеству воздуха: глобальное обновление, 2005 г., стр. 123-124.
Нел, А. (2005). Заболевания, связанные с загрязнением воздуха: воздействие частиц. Science , 308 (5723), 804-806.
Эберг, М., Яаккола, М. С., Вудворд, А., Перуга, А., и Прюсс-Устюн, А. (2011). Бремя болезней от воздействия вторичного табачного дыма во всем мире: ретроспективный анализ данных из 192 стран .Ланцет , 377 (9760), 139-146. Исследование показало, что пассивное курение привело к 165 000 смертей среди детей в возрасте до 5 лет от болезней нижних дыхательных путей.
Теодорату, Э., Макаллистер, Д. А., Рид, К., Аделой, Д. О., Рудан, И., Мухе, Л. М.,… и Наир, Х. (2014). Глобальные, региональные и национальные оценки бремени пневмонии у ВИЧ-инфицированных детей в 2010 г .: метаанализ и модельное исследование. The Lancet Infectious Diseases , 14 (12), 1250-1258.
Дополнение к: McAllister DA, Liu L, Shi T, et al. Глобальные, региональные и национальные оценки заболеваемости и смертности от пневмонии у детей младше 5 лет в период с 2000 по 2015 год: систематический анализ. Lancet Glob Health 2018; опубликовано онлайн 26 ноября.
Коэн, К., Фон Моллендорф, К., Де Гувейя, Л., Ленгана, С., Мейринг, С., Куан, В.,… и Мадхи, С. А. (2017). Эффективность 13-валентной пневмококковой конъюгированной вакцины против инвазивной пневмококковой инфекции у южноафриканских детей: исследование случай-контроль. The Lancet Global Health , 5 (3), e359-e369.
Лусеро, М. Г., Дулалия, В. Э., Ниллос, Л. Т., Уильямс, Г., Парреньо, Р. А. Н., Нохинек, Х.,… и Макела, Х. (2009). Пневмококковые конъюгированные вакцины для профилактики инвазивного пневмококкового заболевания вакцинного типа и пневмонии, определяемой с помощью рентгеновских лучей, у детей в возрасте до двух лет. Кокрановская база данных систематических обзоров , (4).
Мур, М. Р., Линк-Геллес, Р., Шаффнер, В., Линфилд, Р., Хольцман, К., Харрисон, Л. Х.,… и Томас, А. (2016). Эффективность 13-валентной пневмококковой конъюгированной вакцины для профилактики инвазивного пневмококкового заболевания у детей в США: исследование типа случай-контроль. Ланцет респираторной медицины , 4 (5), 399-406.
Чен, К., Лисерас, Ф. К., Флаше, С., Сидхарта, С., Юн, Дж., Сундарам, Н., и Джит, М. (2019). Эффект и экономическая эффективность пневмококковой конъюгированной вакцинации: анализ глобального моделирования. The Lancet Global Health , 7 (1), e58-e67.
Подробнее о пневмококковых вакцинах см. В разделе ниже.
Кроме того, вакцинация детей PCV может защитить взрослых за счет эффекта стада, а это означает, что преимущества не ограничиваются одной возрастной группой населения — особенно важно, поскольку пневмония является значительным бременем для пожилых людей.
Chen, C., Liceras, F. C., Flasche, S., Sidharta, S., Yoong, J., Sundaram, N., & Jit, M.(2019). Эффект и экономическая эффективность пневмококковой конъюгированной вакцинации: анализ глобального моделирования. The Lancet Global Health , 7 (1), e58-e67.
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования Global Burden of Disease Study 2016. The Lancet Infectious Diseases , 18 (11), 1191-1210.
Ламберти, Л. М., Закария-Гркович, И., Уокер, К. Л. Ф., Теодорату, Э., Наир, Х., Кэмпбелл, Х. и Блэк, Р. Э. (2013). Грудное вскармливание для снижения риска заболеваемости и смертности от пневмонии у детей до двух лет: систематический обзор литературы и метаанализ. BMC общественное здравоохранение , 13 (3), S18.
41% число оценивается ЮНИСЕФ на основе самых последних данных, доступных для стран из опросов в период с 2013 по 2018 год.
ДАННЫЕ ЮНИСЕФ. (2019). Кормление детей грудного и раннего возраста . [онлайн] [доступ 4 сентября 2019 г.].
ВОЗ, США (2006 г.). Рекомендации по качеству воздуха: глобальное обновление, 2005 г., стр. 123-124. Всемирная организация здравоохранения .
Фердоус, Ф., Ахмед, С., Дас, С. К., Чисти, М. Дж., Насрин, Д., Котлофф, К. Л.,… и Вагацума, Ю. (2018). Смертность от пневмонии и использование медицинских услуг у маленьких детей в сельских районах Бангладеш: проспективное вербальное вскрытие. Тропическая медицина и здоровье , 46 (1), 17.
ДАННЫЕ ЮНИСЕФ. (2018). Пневмония у детей . [онлайн] [Доступ 5 сентября 2019 г.]
Всемирная организация здравоохранения. (2014). Пересмотренная классификация ВОЗ и лечение пневмонии у детей в медицинских учреждениях: краткое справочное руководство (№ WHO / FWC / MCA / 14.9). Всемирная организация здоровья.
Unicef.org. (2018). Дисперсные таблетки амоксициллина: обновление рынка и предложения .[онлайн] [доступ 26 сентября 2019 г.].
Unicef. (2016). Положение детей в мире, 2016 г. Нью-Йорк: Детский фонд Организации Объединенных Наций .
Лаззерини, М., Сонего, М., и Пеллегрин, М.С. (2015). Гипоксемия как фактор риска смертности от острых респираторных инфекций нижних дыхательных путей у детей в странах с низким и средним уровнем дохода: систематический обзор и метаанализ. PLoS One , 10 (9), e0136166.
Воздух, которым мы дышим, содержит 21% газообразного кислорода, но можно сконцентрировать этот газ с помощью специальных концентраторов кислорода.Затем обогащенный кислородом воздух может подаваться к человеку с пневмонией через дыхательную маску, таким образом компенсируя снижение кислородного обмена в легких.
Всемирная организация здравоохранения. (2016). Кислородная терапия для детей: пособие для медицинских работников.
Всемирная организация здравоохранения. (2019). Типовой список основных лекарственных средств ВОЗ: 7-й список, август 2019 г.
Делароза, Дж., Хейс, Дж., Пантюшенко, Э., Кейт, Б., Эмблер, Г.и Лоуренс К. (2017). Кислород необходим: учебник по политике и защите интересов . [онлайн] ПУТЬ. [Доступ 5 сентября 2019 г.].
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования глобального бремени болезней, 2016 г. The Lancet Infectious Diseases , 18 ( 11), 1191-1210.
Who.int. (2019) — Охват иммунизацией . [онлайн] [доступ 10 сентября 2019 г.]. http://view-hub.org/viz/ (Перейти к PCV -> PCV — Доступ к вакцинам -> Дети без доступа)
Hanada, S., Pirzadeh, M., Carver, KY, & Deng, JC (2018). Изменения микробиома, вызванные респираторной вирусной инфекцией, и вторичная бактериальная пневмония. Frontiers in иммунологии , 9 , 2640.
Song, J. Y., Nahm, M.Х. и Мозли М.А. (2013). Клинические последствия пневмококковых серотипов: потенциал инвазивного заболевания, клинические проявления и устойчивость к антибиотикам. Журнал корейской медицины , 28 (1), 4-15.
Количество серотипов, включенных в вакцину, обычно указывается в ее названии, например PCV13 — пневмококковая конъюгированная вакцина, эффективная против 13 серотипов бактерий. Вакцины, включающие все больше серотипов, вводились с годами, ЦВС7 был представлен в 2000 году, а сегодня наиболее часто используемый ЦВС13 был представлен в 2010 году.
Хаусдорф, В. П., Фейкин, Д. Р., & Клугман, К. П. (2005). Эпидемиологические различия между серотипами пневмококков. Ланцет инфекционных болезней , 5 (2), 83-93.
Текущая неконъюгированная вакцина, PPSV23, обычно вводится только взрослым или в виде однократной дозы после двух иммунизаций PCV13 детям старше 2 лет.
Голос, М., Элиаким-Раз, Н., Стерн, А., Лейбович, Л., и Пол, М. (2016). Конъюгированная пневмококковая вакцина в сравнении с полисахаридной пневмококковой вакциной для профилактики пневмонии и инвазивной пневмококковой инфекции у иммунокомпетентных и ослабленных иммунитетом взрослых и детей. Кокрановская база данных систематических обзоров , (8).
27% относятся к рентгенологически определенным случаям пневмонии. Для клинически установленной пневмонии, менее точного диагноза, чем для случаев, определенных с помощью рентгеновского излучения, число составляет 6%. Оба этих показателя относятся к случаям пневмонии, вызванной любым возбудителем, а не только пневмококком. Лусеро, М. Г., Дулалия, В. Э., Ниллос, Л. Т., Уильямс, Г., Парреньо, Р. А. Н., Нохинек, Х.,… и Макела, Х. (2009). Пневмококковые конъюгированные вакцины для профилактики инвазивного пневмококкового заболевания вакцинного типа и пневмонии, определяемой с помощью рентгеновских лучей, у детей в возрасте до двух лет. Кокрановская база данных систематических обзоров , (4).
Вал Б., О’Брайен К. Л., Гринбаум А., Маджумдер А., Лю Л., Чу Ю.,… и Рудан И. (2018). Бремя болезней Streptococcus pneumoniae и Haemophilus influenzae типа b у детей в эпоху конъюгированных вакцин: глобальные, региональные и национальные оценки за 2000-15 гг. The Lancet Global Health , 6 (7), e744-e757.
Chen, C., Liceras, F. C., Flasche, S., Sidharta, S., Юн, Дж., Сундарам, Н., и Джит, М. (2019). Эффект и экономическая эффективность пневмококковой конъюгированной вакцинации: анализ глобального моделирования. The Lancet Global Health , 7 (1), e58-e67.
ГАВИ (Глобальный альянс по вакцинам и иммунизации) — это некоммерческая организация, которая обеспечивает доступ к программам вакцинации для стран с низким уровнем доходов, предоставляя финансовую поддержку и индивидуальный опыт.
О’Брайен, К. Л. (2018).Когда меньше значит больше: сколько доз ПКВ достаточно ?. The Lancet Infectious Diseases , 18 (2), 127-128.
Например, Кения недавно вступила в переходную фазу, во время которой она будет оплачивать все большую и большую часть стоимости вакцины PCV. К 2027 году Кения должна будет заплатить полную цену в размере 9 долларов за трехдозовый курс вакцинации детей. Расходы на здравоохранение на душу населения в Кении в 2016 году составили около 66 долларов (5% ВВП), очевидно, 9 долларов на ребенка — это нетривиальные затраты.
Симонсен, Л., ван Вейхе, М., и Тейлор, Р. (2019). Дорогие вакцины — лучшее вложение для стран с низким и средним доходом? The Lancet Global Health , 7 (5), e548-e549.
Оджал, Дж., Гриффитс, У., Хаммитт, Л. Л., Адетифа, И., Акеч, Д., Табу, К.,… и Флаше, С. (2019). Поддержание пневмококковой вакцинации после перехода от поддержки Гави: моделирование и исследование экономической эффективности в Кении. The Lancet Global Health , 7 (5), e644-e654.
Окупаемость инвестиций была оценена для прогнозируемого охвата отдельных стран на десятилетие с 2011 по 2020 годы. Это означает, что экономические выгоды (измеряемые затратами на программу вакцинации, вычтенными из сокращенных затрат на лечение и потери производительности ) использования вакцины в 3 раза выше, чем ее неиспользования.
Для снижения затрат некоторые страны могут также рассмотреть возможность перехода на схему иммунизации с двумя, а не с тремя дозами, однако необходимы дополнительные исследования эффективности этого графика в разных странах.См. O’Brien et al. (2018) ссылка.
Накамура М. М., Тасслими А., Лиу Т. А., Левин О., Нолл М. Д., Рассел Л. Б. и Синха А. (2011). Экономическая эффективность детской пневмококковой конъюгированной вакцинации в странах со средним уровнем дохода. Международное здравоохранение , 3 (4), 270-281.
Одзава, С., Кларк, С., Портной, А., Гревал, С., Брензель, Л., и Уокер, Д. Г. (2016). Рентабельность инвестиций в иммунизацию детей в странах с низким и средним уровнем доходов, 2011–2020 гг. Департамент здравоохранения , 35 (2), 199-207.
Центр, И.В.А. (2017). Доказательная база для пневмококковых конъюгированных вакцин (ПКВ): данные для принятия решений относительно использования ПКВ в детстве. Балтимор (Мэриленд): Университет Джона Хопкинса .
Голдблатт, Д., Саузерн, Дж., Эндрюс, Н. Дж., Бербидж, П., Партингтон, Дж., Роалф, Л.,… и Снейп, М. Д. (2018). Пневмококковая конъюгированная вакцина 13 доставлялась в виде одной первичной и одной бустерной дозы (1+ 1) по сравнению с двумя первичными дозами и бустерной дозой (2+ 1) для младенцев в Великобритании: многоцентровое рандомизированное контролируемое исследование с параллельными группами. The Lancet Infectious Diseases , 18 (2), 171-179.
О’Брайен, К. Л. (2018). Когда меньше значит больше: сколько доз ПКВ достаточно ?. The Lancet Infectious Diseases , 18 (2), 127-128.
Адегбола Р. А., ДеАнтонио Р., Хилл П. К., Рока А., Усуф Э., Хут Б. и Гринвуд Б. М. (2014). Носительство Streptococcus pneumoniae и других респираторных бактериальных патогенов в странах с низким доходом и доходом ниже среднего: систематический обзор и метаанализ. PloS one , 9 (8), e103293.
Мегиддо, И., Кляйн, Э., и Лакшминараян, Р. (2018). Возможные последствия внедрения пневмококковой конъюгированной вакцины в национальные программы иммунизации: экономико-эпидемиологический анализ с использованием данных из Индии. BMJ global health , 3 (3), e000636.
Джонсон, Х. Л., Делориа-Нолл, М., Левин, О. С., Стошек, С. К., Ханс, Л. Ф., Райтингер, Р.,… и О’Брайен, К.Л. (2010). Систематическая оценка серотипов, вызывающих инвазивную пневмококковую болезнь у детей в возрасте до пяти лет: проект глобального серотипа пневмококков. PLoS лекарство , 7 (10), e1000348.
Всемирная организация здравоохранения. (2010). Изменение эпидемиологии пневмококковых серотипов после введения конъюгированной вакцины: отчет за июль 2010 г. Еженедельный эпидемиологический отчет [Relevé épidémiologique hebdomadaire ], 85 (43), 434-436.
Пичичеро, М.Е. (2017). Пневмококковые цельноклеточные и белковые вакцины: изменение парадигмы. Экспертиза вакцин , 16 (12), 1181-1190.
Гинзбург, А. С., Нах, М. Х., Хамбати, Ф. М., и Олдерсон, М. Р. (2012). Проблемы и вызовы разработки пневмококковых белковых вакцин. Экспертный обзор вакцин, 11 (3), 279-285
Troeger, C., Blacker, B., Khalil, I.A., Rao, P.C, Cao, J., Zimsen, S.R.,… & Adetifa, I.М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования глобального бремени болезней 2016 г. The Lancet Infectious Diseases , 18 (11), 1191-1210.
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования Global Burden of Disease Study 2016. The Lancet Infectious Diseases , 18 (11), 1191-1210.
О’Брайен, К. Л., Баггетт, Х. К., Брукс, В. А., Фейкин, Д. Р., Хаммитт, Л. Л., Хигдон, М. М.,… и Мадхи, С. А. (2019). Причины тяжелой пневмонии, требующей госпитализации у детей без ВИЧ-инфекции из Африки и Азии: многострановое исследование «случай-контроль» PERCH. Ланцет .
Например, когда происходит вторичная инфекция вирусом, которая может вызвать размножение обычно непатогенных бактерий.
Ханада, С., Пирзаде, М., Карвер, К. Ю., и Дэн, Дж. К. (2018). Изменения микробиома, вызванные респираторной вирусной инфекцией, и вторичная бактериальная пневмония. Frontiers in Immunology , 9 , 2640.
Все визуализации, данные и код, произведенные «Нашим миром в данных», находятся в полностью открытом доступе по лицензии Creative Commons BY. У вас есть разрешение использовать, распространять и воспроизводить их на любом носителе при условии указания источника и авторов.
Данные, предоставленные третьими сторонами и предоставленные «Нашим миром в данных», регулируются условиями лицензии исходных сторонних авторов. Мы всегда будем указывать исходный источник данных в нашей документации, поэтому вы всегда должны проверять лицензию на любые такие сторонние данные перед использованием и распространением.
Наши статьи и визуализации данных основаны на работе множества разных людей и организаций. При цитировании этой записи просьба также указать основные источники данных.Эту запись можно цитировать:
Пневмония — наш мир в данных
Институт показателей и оценки здоровья (IMHE). (2014). Ускоряя темп: прогресс и проблемы в борьбе с детской пневмонией.
Макаллистер, Д. А., Лю, Л., Ши, Т., Чу, Ю., Рид, К., Берроуз, Дж.,… И Наир, Х. (2019). Глобальные, региональные и национальные оценки заболеваемости и смертности от пневмонии у детей младше 5 лет в период с 2000 по 2015 год: систематический анализ. The Lancet Global Health , 7 (1), e47-e57.
Мы используем термин пневмония здесь как широкий термин для обозначения инфекций нижних дыхательных путей. См. Этот раздел, чтобы узнать, как эти термины определены и почему они сгруппированы вместе.
(286.1-260.9) /286.1=0.09
Уоткинс, К., и Шридхар, Д. (2018). Пневмония: глобальная причина без чемпионов. Ланцет , 392 (10149), 718-719.
Редакция журнала Lancet Global Health (2018).Позорное пренебрежение детской пневмонией. Ланцет. Глобальное здравоохранение , 6 (12), e1253.
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования глобального бремени болезней, 2016 г. The Lancet Infectious Diseases , 18 ( 11), 1191-1210.
Чисти, М. Дж., Тебрюгге, М., Ла Винсенте, С., Грэхем, С. М., и Дюк, Т. (2009). Пневмония у детей с тяжелой недостаточностью питания в развивающихся странах — риск смертности, этиология и достоверность клинических признаков ВОЗ: систематический обзор. Тропическая медицина и международное здравоохранение , 14 (10), 1173-1189.
Дерани, М., Поуп, Д., Маскаренхас, М., Смит, К. Р., Вебер, М., и Брюс, Н. (2008). Загрязнение воздуха внутри помещений в результате использования необработанного твердого топлива и риск пневмонии у детей в возрасте до пяти лет: систематический обзор и метаанализ.
Бюллетень Всемирной организации здравоохранения (2006). Рекомендации по качеству воздуха: глобальное обновление, 2005 г., стр. 123-124.
Нел, А. (2005). Заболевания, связанные с загрязнением воздуха: воздействие частиц. Science , 308 (5723), 804-806.
Эберг, М., Яаккола, М. С., Вудворд, А., Перуга, А., и Прюсс-Устюн, А. (2011). Бремя болезней от воздействия вторичного табачного дыма во всем мире: ретроспективный анализ данных из 192 стран .Ланцет , 377 (9760), 139-146. Исследование показало, что пассивное курение привело к 165 000 смертей среди детей в возрасте до 5 лет от болезней нижних дыхательных путей.
Теодорату, Э., Макаллистер, Д. А., Рид, К., Аделой, Д. О., Рудан, И., Мухе, Л. М.,… и Наир, Х. (2014). Глобальные, региональные и национальные оценки бремени пневмонии у ВИЧ-инфицированных детей в 2010 г .: метаанализ и модельное исследование. The Lancet Infectious Diseases , 14 (12), 1250-1258.
Дополнение к: McAllister DA, Liu L, Shi T, et al. Глобальные, региональные и национальные оценки заболеваемости и смертности от пневмонии у детей младше 5 лет в период с 2000 по 2015 год: систематический анализ. Lancet Glob Health 2018; опубликовано онлайн 26 ноября.
Коэн, К., Фон Моллендорф, К., Де Гувейя, Л., Ленгана, С., Мейринг, С., Куан, В.,… и Мадхи, С. А. (2017). Эффективность 13-валентной пневмококковой конъюгированной вакцины против инвазивной пневмококковой инфекции у южноафриканских детей: исследование случай-контроль. The Lancet Global Health , 5 (3), e359-e369.
Лусеро, М. Г., Дулалия, В. Э., Ниллос, Л. Т., Уильямс, Г., Парреньо, Р. А. Н., Нохинек, Х.,… и Макела, Х. (2009). Пневмококковые конъюгированные вакцины для профилактики инвазивного пневмококкового заболевания вакцинного типа и пневмонии, определяемой с помощью рентгеновских лучей, у детей в возрасте до двух лет. Кокрановская база данных систематических обзоров , (4).
Мур, М. Р., Линк-Геллес, Р., Шаффнер, В., Линфилд, Р., Хольцман, К., Харрисон, Л. Х.,… и Томас, А. (2016). Эффективность 13-валентной пневмококковой конъюгированной вакцины для профилактики инвазивного пневмококкового заболевания у детей в США: исследование типа случай-контроль. Ланцет респираторной медицины , 4 (5), 399-406.
Чен, К., Лисерас, Ф. К., Флаше, С., Сидхарта, С., Юн, Дж., Сундарам, Н., и Джит, М. (2019). Эффект и экономическая эффективность пневмококковой конъюгированной вакцинации: анализ глобального моделирования. The Lancet Global Health , 7 (1), e58-e67.
Подробнее о пневмококковых вакцинах см. В разделе ниже.
Кроме того, вакцинация детей PCV может защитить взрослых за счет эффекта стада, а это означает, что преимущества не ограничиваются одной возрастной группой населения — особенно важно, поскольку пневмония является значительным бременем для пожилых людей.
Chen, C., Liceras, F. C., Flasche, S., Sidharta, S., Yoong, J., Sundaram, N., & Jit, M.(2019). Эффект и экономическая эффективность пневмококковой конъюгированной вакцинации: анализ глобального моделирования. The Lancet Global Health , 7 (1), e58-e67.
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования Global Burden of Disease Study 2016. The Lancet Infectious Diseases , 18 (11), 1191-1210.
Ламберти, Л. М., Закария-Гркович, И., Уокер, К. Л. Ф., Теодорату, Э., Наир, Х., Кэмпбелл, Х. и Блэк, Р. Э. (2013). Грудное вскармливание для снижения риска заболеваемости и смертности от пневмонии у детей до двух лет: систематический обзор литературы и метаанализ. BMC общественное здравоохранение , 13 (3), S18.
41% число оценивается ЮНИСЕФ на основе самых последних данных, доступных для стран из опросов в период с 2013 по 2018 год.
ДАННЫЕ ЮНИСЕФ. (2019). Кормление детей грудного и раннего возраста . [онлайн] [доступ 4 сентября 2019 г.].
ВОЗ, США (2006 г.). Рекомендации по качеству воздуха: глобальное обновление, 2005 г., стр. 123-124. Всемирная организация здравоохранения .
Фердоус, Ф., Ахмед, С., Дас, С. К., Чисти, М. Дж., Насрин, Д., Котлофф, К. Л.,… и Вагацума, Ю. (2018). Смертность от пневмонии и использование медицинских услуг у маленьких детей в сельских районах Бангладеш: проспективное вербальное вскрытие. Тропическая медицина и здоровье , 46 (1), 17.
ДАННЫЕ ЮНИСЕФ. (2018). Пневмония у детей . [онлайн] [Доступ 5 сентября 2019 г.]
Всемирная организация здравоохранения. (2014). Пересмотренная классификация ВОЗ и лечение пневмонии у детей в медицинских учреждениях: краткое справочное руководство (№ WHO / FWC / MCA / 14.9). Всемирная организация здоровья.
Unicef.org. (2018). Дисперсные таблетки амоксициллина: обновление рынка и предложения .[онлайн] [доступ 26 сентября 2019 г.].
Unicef. (2016). Положение детей в мире, 2016 г. Нью-Йорк: Детский фонд Организации Объединенных Наций .
Лаззерини, М., Сонего, М., и Пеллегрин, М.С. (2015). Гипоксемия как фактор риска смертности от острых респираторных инфекций нижних дыхательных путей у детей в странах с низким и средним уровнем дохода: систематический обзор и метаанализ. PLoS One , 10 (9), e0136166.
Воздух, которым мы дышим, содержит 21% газообразного кислорода, но можно сконцентрировать этот газ с помощью специальных концентраторов кислорода.Затем обогащенный кислородом воздух может подаваться к человеку с пневмонией через дыхательную маску, таким образом компенсируя снижение кислородного обмена в легких.
Всемирная организация здравоохранения. (2016). Кислородная терапия для детей: пособие для медицинских работников.
Всемирная организация здравоохранения. (2019). Типовой список основных лекарственных средств ВОЗ: 7-й список, август 2019 г.
Делароза, Дж., Хейс, Дж., Пантюшенко, Э., Кейт, Б., Эмблер, Г.и Лоуренс К. (2017). Кислород необходим: учебник по политике и защите интересов . [онлайн] ПУТЬ. [Доступ 5 сентября 2019 г.].
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования глобального бремени болезней, 2016 г. The Lancet Infectious Diseases , 18 ( 11), 1191-1210.
Who.int. (2019) — Охват иммунизацией . [онлайн] [доступ 10 сентября 2019 г.]. http://view-hub.org/viz/ (Перейти к PCV -> PCV — Доступ к вакцинам -> Дети без доступа)
Hanada, S., Pirzadeh, M., Carver, KY, & Deng, JC (2018). Изменения микробиома, вызванные респираторной вирусной инфекцией, и вторичная бактериальная пневмония. Frontiers in иммунологии , 9 , 2640.
Song, J. Y., Nahm, M.Х. и Мозли М.А. (2013). Клинические последствия пневмококковых серотипов: потенциал инвазивного заболевания, клинические проявления и устойчивость к антибиотикам. Журнал корейской медицины , 28 (1), 4-15.
Количество серотипов, включенных в вакцину, обычно указывается в ее названии, например PCV13 — пневмококковая конъюгированная вакцина, эффективная против 13 серотипов бактерий. Вакцины, включающие все больше серотипов, вводились с годами, ЦВС7 был представлен в 2000 году, а сегодня наиболее часто используемый ЦВС13 был представлен в 2010 году.
Хаусдорф, В. П., Фейкин, Д. Р., & Клугман, К. П. (2005). Эпидемиологические различия между серотипами пневмококков. Ланцет инфекционных болезней , 5 (2), 83-93.
Текущая неконъюгированная вакцина, PPSV23, обычно вводится только взрослым или в виде однократной дозы после двух иммунизаций PCV13 детям старше 2 лет.
Голос, М., Элиаким-Раз, Н., Стерн, А., Лейбович, Л., и Пол, М. (2016). Конъюгированная пневмококковая вакцина в сравнении с полисахаридной пневмококковой вакциной для профилактики пневмонии и инвазивной пневмококковой инфекции у иммунокомпетентных и ослабленных иммунитетом взрослых и детей. Кокрановская база данных систематических обзоров , (8).
27% относятся к рентгенологически определенным случаям пневмонии. Для клинически установленной пневмонии, менее точного диагноза, чем для случаев, определенных с помощью рентгеновского излучения, число составляет 6%. Оба этих показателя относятся к случаям пневмонии, вызванной любым возбудителем, а не только пневмококком. Лусеро, М. Г., Дулалия, В. Э., Ниллос, Л. Т., Уильямс, Г., Парреньо, Р. А. Н., Нохинек, Х.,… и Макела, Х. (2009). Пневмококковые конъюгированные вакцины для профилактики инвазивного пневмококкового заболевания вакцинного типа и пневмонии, определяемой с помощью рентгеновских лучей, у детей в возрасте до двух лет. Кокрановская база данных систематических обзоров , (4).
Вал Б., О’Брайен К. Л., Гринбаум А., Маджумдер А., Лю Л., Чу Ю.,… и Рудан И. (2018). Бремя болезней Streptococcus pneumoniae и Haemophilus influenzae типа b у детей в эпоху конъюгированных вакцин: глобальные, региональные и национальные оценки за 2000-15 гг. The Lancet Global Health , 6 (7), e744-e757.
Chen, C., Liceras, F. C., Flasche, S., Sidharta, S., Юн, Дж., Сундарам, Н., и Джит, М. (2019). Эффект и экономическая эффективность пневмококковой конъюгированной вакцинации: анализ глобального моделирования. The Lancet Global Health , 7 (1), e58-e67.
ГАВИ (Глобальный альянс по вакцинам и иммунизации) — это некоммерческая организация, которая обеспечивает доступ к программам вакцинации для стран с низким уровнем доходов, предоставляя финансовую поддержку и индивидуальный опыт.
О’Брайен, К. Л. (2018).Когда меньше значит больше: сколько доз ПКВ достаточно ?. The Lancet Infectious Diseases , 18 (2), 127-128.
Например, Кения недавно вступила в переходную фазу, во время которой она будет оплачивать все большую и большую часть стоимости вакцины PCV. К 2027 году Кения должна будет заплатить полную цену в размере 9 долларов за трехдозовый курс вакцинации детей. Расходы на здравоохранение на душу населения в Кении в 2016 году составили около 66 долларов (5% ВВП), очевидно, 9 долларов на ребенка — это нетривиальные затраты.
Симонсен, Л., ван Вейхе, М., и Тейлор, Р. (2019). Дорогие вакцины — лучшее вложение для стран с низким и средним доходом? The Lancet Global Health , 7 (5), e548-e549.
Оджал, Дж., Гриффитс, У., Хаммитт, Л. Л., Адетифа, И., Акеч, Д., Табу, К.,… и Флаше, С. (2019). Поддержание пневмококковой вакцинации после перехода от поддержки Гави: моделирование и исследование экономической эффективности в Кении. The Lancet Global Health , 7 (5), e644-e654.
Окупаемость инвестиций была оценена для прогнозируемого охвата отдельных стран на десятилетие с 2011 по 2020 годы. Это означает, что экономические выгоды (измеряемые затратами на программу вакцинации, вычтенными из сокращенных затрат на лечение и потери производительности ) использования вакцины в 3 раза выше, чем ее неиспользования.
Для снижения затрат некоторые страны могут также рассмотреть возможность перехода на схему иммунизации с двумя, а не с тремя дозами, однако необходимы дополнительные исследования эффективности этого графика в разных странах.См. O’Brien et al. (2018) ссылка.
Накамура М. М., Тасслими А., Лиу Т. А., Левин О., Нолл М. Д., Рассел Л. Б. и Синха А. (2011). Экономическая эффективность детской пневмококковой конъюгированной вакцинации в странах со средним уровнем дохода. Международное здравоохранение , 3 (4), 270-281.
Одзава, С., Кларк, С., Портной, А., Гревал, С., Брензель, Л., и Уокер, Д. Г. (2016). Рентабельность инвестиций в иммунизацию детей в странах с низким и средним уровнем доходов, 2011–2020 гг. Департамент здравоохранения , 35 (2), 199-207.
Центр, И.В.А. (2017). Доказательная база для пневмококковых конъюгированных вакцин (ПКВ): данные для принятия решений относительно использования ПКВ в детстве. Балтимор (Мэриленд): Университет Джона Хопкинса .
Голдблатт, Д., Саузерн, Дж., Эндрюс, Н. Дж., Бербидж, П., Партингтон, Дж., Роалф, Л.,… и Снейп, М. Д. (2018). Пневмококковая конъюгированная вакцина 13 доставлялась в виде одной первичной и одной бустерной дозы (1+ 1) по сравнению с двумя первичными дозами и бустерной дозой (2+ 1) для младенцев в Великобритании: многоцентровое рандомизированное контролируемое исследование с параллельными группами. The Lancet Infectious Diseases , 18 (2), 171-179.
О’Брайен, К. Л. (2018). Когда меньше значит больше: сколько доз ПКВ достаточно ?. The Lancet Infectious Diseases , 18 (2), 127-128.
Адегбола Р. А., ДеАнтонио Р., Хилл П. К., Рока А., Усуф Э., Хут Б. и Гринвуд Б. М. (2014). Носительство Streptococcus pneumoniae и других респираторных бактериальных патогенов в странах с низким доходом и доходом ниже среднего: систематический обзор и метаанализ. PloS one , 9 (8), e103293.
Мегиддо, И., Кляйн, Э., и Лакшминараян, Р. (2018). Возможные последствия внедрения пневмококковой конъюгированной вакцины в национальные программы иммунизации: экономико-эпидемиологический анализ с использованием данных из Индии. BMJ global health , 3 (3), e000636.
Джонсон, Х. Л., Делориа-Нолл, М., Левин, О. С., Стошек, С. К., Ханс, Л. Ф., Райтингер, Р.,… и О’Брайен, К.Л. (2010). Систематическая оценка серотипов, вызывающих инвазивную пневмококковую болезнь у детей в возрасте до пяти лет: проект глобального серотипа пневмококков. PLoS лекарство , 7 (10), e1000348.
Всемирная организация здравоохранения. (2010). Изменение эпидемиологии пневмококковых серотипов после введения конъюгированной вакцины: отчет за июль 2010 г. Еженедельный эпидемиологический отчет [Relevé épidémiologique hebdomadaire ], 85 (43), 434-436.
Пичичеро, М.Е. (2017). Пневмококковые цельноклеточные и белковые вакцины: изменение парадигмы. Экспертиза вакцин , 16 (12), 1181-1190.
Гинзбург, А. С., Нах, М. Х., Хамбати, Ф. М., и Олдерсон, М. Р. (2012). Проблемы и вызовы разработки пневмококковых белковых вакцин. Экспертный обзор вакцин, 11 (3), 279-285
Troeger, C., Blacker, B., Khalil, I.A., Rao, P.C, Cao, J., Zimsen, S.R.,… & Adetifa, I.М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования глобального бремени болезней 2016 г. The Lancet Infectious Diseases , 18 (11), 1191-1210.
Троегер, К., Блэкер, Б., Халил, И. А., Рао, П. К., Цао, Дж., Зимсен, С. Р.,… и Адетифа, И. М. О. (2018). Оценки глобальной, региональной и национальной заболеваемости, смертности и этиологии инфекций нижних дыхательных путей в 195 странах, 1990–2016 гг .: систематический анализ для исследования Global Burden of Disease Study 2016. The Lancet Infectious Diseases , 18 (11), 1191-1210.
О’Брайен, К. Л., Баггетт, Х. К., Брукс, В. А., Фейкин, Д. Р., Хаммитт, Л. Л., Хигдон, М. М.,… и Мадхи, С. А. (2019). Причины тяжелой пневмонии, требующей госпитализации у детей без ВИЧ-инфекции из Африки и Азии: многострановое исследование «случай-контроль» PERCH. Ланцет .
Например, когда происходит вторичная инфекция вирусом, которая может вызвать размножение обычно непатогенных бактерий.
Ханада, С., Пирзаде, М., Карвер, К. Ю., и Дэн, Дж. К. (2018). Изменения микробиома, вызванные респираторной вирусной инфекцией, и вторичная бактериальная пневмония. Frontiers in Immunology , 9 , 2640.
Все визуализации, данные и код, произведенные «Нашим миром в данных», находятся в полностью открытом доступе по лицензии Creative Commons BY. У вас есть разрешение использовать, распространять и воспроизводить их на любом носителе при условии указания источника и авторов.
Данные, предоставленные третьими сторонами и предоставленные «Нашим миром в данных», регулируются условиями лицензии исходных сторонних авторов. Мы всегда будем указывать исходный источник данных в нашей документации, поэтому вы всегда должны проверять лицензию на любые такие сторонние данные перед использованием и распространением.
Наши статьи и визуализации данных основаны на работе множества разных людей и организаций. При цитировании этой записи просьба также указать основные источники данных.Эту запись можно цитировать:
Каковы возрастные демографические характеристики и уровень смертности от бактериальной пневмонии?
Клавдий I, Бараф LJ. Неотложные состояния педиатрии, связанные с лихорадкой. Emerg Med Clin North Am . 2010 г., 28 (1): 67-84, vii-viii. [Медлайн].
Хуссейн А.Н., Кумар В. Легкое. В: Кумар В., Аббас А.К., Фаусто Н., ред. Роббинс и Котран: патологические основы болезни . 7-е изд. Филадельфия, Пенсильвания: Эльзевьер Сондерс; 2005 г.711-72.
[Руководство] Манделл Л.А., Вундеринк Р.Г., Анзуето А., Бартлетт Дж. Г., Кэмпбелл Г. Д., Дин Н. С. и др. Общество инфекционных болезней Америки / Американское торакальное общество согласовали руководящие принципы ведения внебольничной пневмонии у взрослых. Clin Infect Dis . 2007 г. 1. 44 Приложение 2: S27-72. [Медлайн].
Медицинский словарь Стедмана . 27 изд. Балтимор, Мэриленд: Липпинкотт, Уильямс и Уилкинс; 2003.
Brundage JF, Шэнкс GD.Смертность от бактериальной пневмонии во время пандемии гриппа 1918-19 гг. Emerg Infect Dis . 2008 14 августа (8): 1193-9. [Медлайн]. [Полный текст].
Anand N, Kollef MH. Алфавитный указатель пневмонии: CAP, HAP, HCAP, NHAP и VAP. Semin Respir Crit Care Med . 2009 30 февраля (1): 3-9. [Медлайн].
Эль Соль AA. Пневмония, перенесенная в домах престарелых. Semin Respir Crit Care Med . 2009 30 февраля (1): 16-25. [Медлайн].
Kuti JL, Shore E, Palter M, Nicolau DP.Проведение эмпирической антибактериальной терапии респираторно-ассоциированной пневмонии в отделении интенсивной терапии: руководство по применению рекомендаций. Semin Respir Crit Care Med . 2009 30 февраля (1): 102-15. [Медлайн].
Чако Р., Раджан А., Лайонел П., Тилагавати М., Ядав Б., Премкумар Дж. Методы деконтаминации полости рта и пневмония, связанная с вентилятором. Br J Nurs . 2017 июн 8. 26 (11): 594-599. [Медлайн].
Bouglé A, Foucrier A, Dupont H, Montravers P, Ouattara A, Kalfon P и др.Влияние продолжительности приема антибиотиков на клинические явления у пациентов с вентилятор-ассоциированной пневмонией Pseudomonas aeruginosa: протокол исследования для рандомизированного контролируемого исследования. Испытания . 2017 23 января. 18 (1): 37. [Медлайн]. [Полный текст].
Kollef MH, Ricard JD, Roux D и др. Рандомизированное испытание системы ингаляции амикацина фосфомицина для дополнительной терапии грамотрицательной пневмонии, связанной с вентилятором: испытание IASIS. Сундук . 2017 июн.151 (6): 1239-1246. [Медлайн].
Kalil AC, Metersky ML, Klompas M, Muscedere J, Sweeney DA, Palmer LB и др. Краткое резюме: Ведение взрослых с внутрибольничной пневмонией и пневмонией, связанной с искусственной вентиляцией легких: Руководство по клинической практике, 2016 г., Американское общество инфекционных болезней и Американское торакальное общество. Clin Infect Dis . 2016 Сентябрь 1. 63 (5): 575-82. [Медлайн].
Чалмерс Дж. Д., Ротер С., Салих В., Эвиг С.Пневмония, связанная со здравоохранением, не позволяет точно идентифицировать потенциально устойчивые патогены: систематический обзор и метаанализ. Clin Infect Dis . 2014 Февраль 58 (3): 330-9. [Медлайн].
Eggimann P, Pittet D. Инфекционный контроль в отделении интенсивной терапии. Сундук . 2001 декабрь 120 (6): 2059-93. [Медлайн].
Гейнес Р., Эдвардс-младший. Обзор нозокомиальных инфекций, вызванных грамотрицательными палочками. Clin Infect Dis .2005 15 сентября. 41 (6): 848-54. [Медлайн].
Пелег А.Ю., Хупер округ Колумбия. Внутрибольничные инфекции, вызванные грамотрицательными бактериями. N Engl J Med . 2010 13 мая. 362 (19): 1804-13. [Медлайн].
Марик ЧП. Аспирационный пневмонит и аспирационная пневмония. N Engl J Med . 2001 г., 1. 344 (9): 665-71. [Медлайн].
Mizgerd JP. Острая инфекция нижних дыхательных путей. N Engl J Med .2008 14 февраля. 358 (7): 716-27. [Медлайн]. [Полный текст].
Рубин Ю.Б., Янофф EN. Пневмолизин: многофункциональный фактор вирулентности пневмококков. Дж. Лаборатория Клин Мед. . 1998, январь, 131 (1): 21-7. [Медлайн].
Садикот РТ, Блэквелл Т.С., Кристман Дж. У., Принц А.С. Взаимодействие патоген-хозяин при пневмонии, вызванной Pseudomonas aeruginosa. Am J Respir Crit Care Med . 2005 г., 1. 171 (11): 1209-23. [Медлайн]. [Полный текст].
McCullers JA.Понимание взаимодействия вируса гриппа и пневмококка. Clin Microbiol Ред. . 2006 июл.19 (3): 571-82. [Медлайн]. [Полный текст].
Morens DM, Taubenberger JK, Fauci AS. Преобладающая роль бактериальной пневмонии как причины смерти при пандемическом гриппе: последствия для готовности к пандемическому гриппу. J Заразить Dis . 2008, 1 октября 198 (7): 962-70. [Медлайн]. [Полный текст].
Форги С., Марри Т.Дж. Атипичная пневмония, связанная со здоровьем. Semin Respir Crit Care Med . 2009 30 февраля (1): 67-85. [Медлайн].
Центры по контролю и профилактике заболеваний. Пневмония. Доступно на http://www.cdc.gov/Features/Pneumonia/. Доступ: 13 января 2011 г.
Restrepo MI, Anzueto A. Роль грамотрицательных бактерий при пневмонии, связанной с оказанием медицинской помощи. Semin Respir Crit Care Med . 2009 Февраль 30 (1): 61-6. [Медлайн].
Бактериальные коинфекции в образцах легочной ткани от смертельных случаев пандемического гриппа A (h2N1) 2009 г. — США, май-август 2009 г. MMWR Morb Mortal Wkly Rep . 2009 окт. 2. 58 (38): 1071-4. [Медлайн].
Пандемия гриппа A (h2N1), 2009 г. у беременных, нуждающихся в интенсивной терапии — Нью-Йорк, 2009 г. MMWR Morb Mortal Wkly Rep . 2010 26 марта. 59 (11): 321-6. [Медлайн].
Dennis DT, Inglesby TV, Henderson DA, Bartlett JG, Ascher MS, Eitzen E, et al. Туляремия как биологическое оружие: управление медициной и общественным здравоохранением. JAMA . 2001 6 июн.285 (21): 2763-73. [Медлайн].
Rello J, Ollendorf DA, Oster G, Vera-Llonch M, Bellm L, Redman R и др. Эпидемиология и исходы вентилятор-ассоциированной пневмонии в большой базе данных США. Сундук . 2002 Декабрь 122 (6): 2115-21. [Медлайн].
Американская ассоциация легких. Тенденции заболеваемости и смертности от пневмонии и гриппа. Сентябрь 2008 г. Американская ассоциация легких. Доступно на http://bit.ly/gwYJAE. Доступ: 13 января 2011 г.
Kung HC, Hoyert DL, Xu JQ, Murphy SL и Отдел статистики естественного движения населения. Смертность: окончательные данные за 2005 г. Национальные отчеты о статистике естественного движения населения. Хяттсвилл, Мэриленд: Национальный центр статистики здравоохранения, апрель 2008 г .: 56 (10). http://www.cdc.gov. Доступно на http://bit.ly/i3ATH5. Доступ: 13 января 2011 г.
Mufson MA, Stanek RJ. Бактериемическая пневмококковая пневмония в одном американском городе: 20-летнее продольное исследование, 1978–1997. Am J Med .1999 26 июля. 107 (1А): 34С-43С. [Медлайн].
Cillóniz C, Ewig S, Polverino E, Marcos MA, Esquinas C, Gabarrús A, et al. Микробная этиология внебольничной пневмонии и ее отношение к степени тяжести. Грудь . 2011 Апрель 66 (4): 340-6. [Медлайн].
van der Poll T, Opal SM. Патогенез, лечение и профилактика пневмококковой пневмонии. Ланцет . 2009 31 октября. 374 (9700): 1543-56. [Медлайн].
Slovis BS, Brigham KL.Сесил Основы медицины. : Андреоли Т., Карпентер CCJ, Григгс Р.С., Лоскальцо Дж. Подход к пациенту с респираторным заболеванием . 6-е изд. WB Saunders Co: Филадельфия, Пенсильвания; 2004. 177-80.
Brown SM, Jones BE, Jephson AR, Dean NC. Подтверждение рекомендаций Американского общества по инфекционным заболеваниям / Американского торакального общества 2007 г. по тяжелой внебольничной пневмонии. Crit Care Med . 2009 Декабрь 37 (12): 3010-6. [Медлайн]. [Полный текст].
Фанг У.Ф., Ян К.Ю., Ву К.Л., Ю.С.Дж., Чен С.В., Ту CY и др.Применение и сравнение показателей оценки для прогнозирования исходов у пациентов с пневмонией, связанной с оказанием медицинской помощи. Crit Care . 2011 19 января 15 (1): R32. [Медлайн].
Lim WS, van der Eerden MM, Laing R, Boersma WG, Karalus N, Town GI, et al. Определение степени тяжести внебольничной пневмонии при поступлении в больницу: международное исследование и валидация. Грудь . 2003 май. 58 (5): 377-82. [Медлайн]. [Полный текст].
Fine MJ, Auble TE, Yealy DM, Hanusa BH, Weissfeld LA, Singer DE, et al.Правило прогноза для выявления пациентов с внебольничной пневмонией из группы низкого риска. N Engl J Med . 1997 23 января. 336 (4): 243-50. [Медлайн].
Агентство медицинских исследований и качества. Калькулятор индекса тяжести пневмонии. Доступно на http://pda.ahrq.gov/clinic/psi/psicalc.asp. Доступ: 13 января 2011 г.
Sligl WI, Majumdar SR, Marrie TJ. Сортировка тяжелой пневмонии: какова «оценка» по правилам предсказания ?. Crit Care Med .2009 Декабрь 37 (12): 3166-8. [Медлайн].
Phua J, см. KC, Chan YH, Widjaja LS, Aung NW, Ngerng WJ, et al. Подтверждение и клиническое значение малых критериев IDSA / ATS для тяжелой внебольничной пневмонии. Грудь . 2009 Июль 64 (7): 598-603. [Медлайн].
Bloos F, Marshall JC, Dellinger RP и др. Многонациональное обсервационное исследование прокальцитонина у пациентов интенсивной терапии с пневмонией, требующих искусственной вентиляции легких: многоцентровое обсервационное исследование. Crit Care . 2011 7 марта. 15 (2): R88. [Медлайн].
Knaus WA, Draper EA, Wagner DP, Zimmerman JE. APACHE II: система классификации степени тяжести заболевания. Crit Care Med . 1985, 13 октября (10): 818-29. [Медлайн].
Le Gall JR, Lemeshow S, Saulnier F. Новая упрощенная оценка острой физиологии (SAPS II), основанная на многоцентровом исследовании в Европе / Северной Америке. JAMA . 1993 22-29 декабря. 270 (24): 2957-63. [Медлайн].
Винсент Дж. Л., Морено Р., Такала Дж., Уиллаттс С., Де Мендонса А., Брюнинг Х. и др. Шкала SOFA (оценка отказа органов, связанных с сепсисом) для описания дисфункции / отказа органа. От имени Рабочей группы по проблемам, связанным с сепсисом Европейского общества интенсивной терапии. Intensive Care Med . 1996 22 июля (7): 707-10. [Медлайн].
Эль-Солх А.А., Альхаджусаин А., Абу Джауд П., Дринка П. Достоверность оценок степени тяжести у госпитализированных пациентов с пневмонией, приобретенной в домах престарелых. Сундук . 2010 декабрь 138 (6): 1371-6. [Медлайн].
España PP, Capelastegui A, Gorordo I, Esteban C, Oribe M, Ortega M, et al. Разработка и проверка правила клинического прогноза тяжелой внебольничной пневмонии. Am J Respir Crit Care Med . 2006 декабрь 1. 174 (11): 1249-56. [Медлайн].
Rello J, Rodriguez A, Lisboa T, Gallego M, Lujan M, Wunderink R. Оценка PIRO для внебольничной пневмонии: новое правило прогноза для оценки степени тяжести внебольничной пневмонии у пациентов отделения интенсивной терапии. Crit Care Med . 2009 Февраль 37 (2): 456-62. [Медлайн].
Чарльз П.Г., Вулф Р., Уитби М., Файн М.Дж., Фуллер А.Дж., Стирлинг Р. и др. SMART-COP: инструмент для прогнозирования потребности в интенсивной респираторной или вазопрессорной поддержке при внебольничной пневмонии. Clin Infect Dis . 2008 г. 1. 47 (3): 375-84. [Медлайн].
Легкий RW. Клиническая практика. Плевральный выпот. N Engl J Med . 2002, 20 июня. 346 (25): 1971-7.[Медлайн].
Bafadhel M, Clark TW, Reid C, Medina MJ, Batham S, Barer MR, et al. Прокальцитонин и С-реактивный белок у госпитализированных взрослых пациентов с внебольничной пневмонией, обострением астмы и хронической обструктивной болезнью легких. Сундук . 28 октября 2010 г. [Medline].
Skerrett SJ. Диагностическое тестирование внебольничной пневмонии. Clin Chest Med . 1999 Сентябрь 20 (3): 531-48. [Медлайн].
Смит ПР.Какие диагностические тесты необходимы при внебольничной пневмонии ?. Med Clin North Am . 2001 ноябрь 85 (6): 1381-96. [Медлайн].
Ketai L, Jordan K, Marom EM. Визуализирующая инфекция. Clin Chest Med . 2008 29 марта (1): 77-105, vi. [Медлайн].
Купер М.С., Стюарт П.М. Кортикостероидная недостаточность у тяжелобольных. N Engl J Med . 2003 20 февраля. 348 (8): 727-34. [Медлайн].
Rivers E, Nguyen B, Havstad S, Ressler J, Muzzin A, Knoblich B и др.Ранняя целенаправленная терапия в лечении тяжелого сепсиса и септического шока. N Engl J Med . 2001, 8 ноября. 345 (19): 1368-77. [Медлайн].
Кан Я., Квон С.И., Юн Х.И., Ли Дж.Х., Ли CT. Роль С-реактивного белка и прокальцитонина в дифференциации туберкулеза от бактериальной внебольничной пневмонии. Korean J Intern Med . 2009 24 декабря (4): 337-42. [Медлайн]. [Полный текст].
Pirracchio R, Mateo J, Raskine L, Rigon MR, Lukaszewicz AC, Mebazaa A, et al.Могут ли бактериологические образцы верхних дыхательных путей, полученные при приеме в отделение интенсивной терапии, служить ориентиром для эмпирической антибиотикотерапии при ИВЛ-ассоциированной пневмонии? Crit Care Med . 2009 Сентябрь 37 (9): 2559-63. [Медлайн].
Гариб А.М., Стерн Э.Дж. Радиология пневмонии. Med Clin North Am . 2001 ноябрь 85 (6): 1461-91, x. [Медлайн].
Tarver RD, Teague SD, Heitkamp DE, Conces DJ Jr. Радиология внебольничной пневмонии. Radiol Clin North Am .2005 Май. 43 (3): 497-512, viii. [Медлайн].
Gotway MB, Reddy GP, Webb WR, Elicker BM, Leung JW. КТ легкого высокого разрешения: паттерны болезней и дифференциальные диагнозы. Radiol Clin North Am . 2005 Май. 43 (3): 513-42, viii. [Медлайн].
[Рекомендации] Деллинджер Р.П., Леви М.М., Карлет Дж. М. и др. Кампания по выживанию при сепсисе: международные рекомендации по ведению тяжелого сепсиса и септического шока: 2008 г. Intensive Care Med .2008, январь, 34 (1): 17-60. [Медлайн]. [Полный текст].
Семенюк Р.А., Мид М.О., Алонсо-Коэльо П., Бриэль М., Эванев Н., Прасад М. и др. Кортикостероидная терапия для пациентов, госпитализированных с внебольничной пневмонией: систематический обзор и метаанализ. Энн Интерн Мед. . 2015 Октябрь 6. 163 (7): 519-28. [Медлайн].
Арнольд Ф.В., ЛаДжой А.С., Брок Г.Н., Пейрани П., Релло Дж., Менендес Р. и др. Улучшение результатов у пожилых пациентов с внебольничной пневмонией путем соблюдения национальных рекомендаций: результаты международного когортного исследования организации внебольничной пневмонии. Arch Intern Med . 2009 14 сентября. 169 (16): 1515-24. [Медлайн].
МакКейб С., Киршнер С., Чжан Х., Дейли Дж., Фисман Д.Н. Согласованная с рекомендациями терапия и снижение смертности и продолжительности пребывания взрослых с внебольничной пневмонией: игра по правилам. Arch Intern Med . 2009 14 сентября. 169 (16): 1525-31. [Медлайн].
[Рекомендации] Центры услуг Medicare и Medicaid, Объединенная комиссия. Руководство по техническим условиям для национальных больничных мер качества стационарных пациентов.V. 2.6b. Ручная загрузка получена в апреле 2009 г.
Калил А.С., Мурти М.Х., Хермсен Э.Д., Нето Ф.К., Сан Дж., Рупп МЭ. Линезолид по сравнению с ванкомицином или тейкопланином при нозокомиальной пневмонии: систематический обзор и метаанализ. Crit Care Med . 2010 Сентябрь 38 (9): 1802-8. [Медлайн].
Лам А.П., Вундеринк РГ. Роль MRSA при пневмонии, связанной с оказанием медицинской помощи. Semin Respir Crit Care Med . 2009 30 февраля (1): 52-60. [Медлайн].
Центры по контролю и профилактике заболеваний.Грипп h2N1: обновленные оценки CDC случаев, госпитализаций и смертей от гриппа h2N1 в США в 2009 г. — 10 апреля 2010 г. Доступно по адресу http://www.cdc.gov/h2n1flu/estimates_2009_h2n1.htm. Доступ: 1 июня 2010 г.
Sullivan SJ, Jacobson RM, Dowdle WR, Poland GA. Грипп h2N1 2009 г. Mayo Clin Proc . 2010 январь 85 (1): 64-76. [Медлайн]. [Полный текст].
1. Филлипс Д. ACIP изменяет интервал вакцинации от пневмококка у пожилых людей из группы низкого риска. Medscape Medical News. WebMD Inc . 4 сентября 2015 г. Доступно по адресу http://www.medscape.com/viewarticle/850564.
Кобаяши М., Беннетт Н.М., Гирке Р., Альмендарес О., Мур М.Р., Уитни К.Г. и др. Интервалы между вакцинами против PCV13 и PPSV23: Рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Morb Mortal Wkly Rep . 2015 4 сентября. 64 (34): 944-7. [Медлайн].
Центры по контролю и профилактике заболеваний.Использование пневмококковой конъюгированной вакцины 13-Valent и пневмококковой полисахаридной вакцины 23-Valent для взрослых с иммунодефицитными состояниями: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Morb Mortal Wkly Rep . 2012 Октябрь 12, 61: 816-9. [Медлайн].
Tomczyk S, Bennett NM, Stoecker C, Gierke R, Moore MR, Whitney CG, et al. Использование пневмококковой конъюгированной вакцины 13-Valent и пневмококковой полисахаридной вакцины 23-Valent среди взрослых в возрасте 65 лет: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Morb Mortal Wkly Rep . 2014 сентябрь 19, 63 (37): 822-5. [Медлайн]. [Полный текст].
Bonten M, Bolkenbaas M, Huijts S, et al. Испытание иммунизации взрослых от пневмонии, приобретенной в сообществе (CAPiTA). № аннотации 0541. Пневмония 2014; 3: 95. Доступно по адресу https://pneumonia.org.au/public/journals/22/PublicFolder/ABSTRACTBOOKMASTERforwebupdated20-3-14.pdf.
Tang KL, Eurich DT, Minhas-Sandhu JK, Marrie TJ, Majumdar SR. Частота, корреляты и результаты рентгенографии грудной клетки нового диагноза рака легкого у 3398 пациентов с пневмонией. Arch Intern Med . 2011 г. 11 июля. 171 (13): 1193-8. [Медлайн].
FDA запрашивает упакованные в рамку предупреждения о фторхинолоновых противомикробных препаратах: стремится усилить предупреждения, касающиеся повышенного риска тендинита и разрыва сухожилий [пресс-релиз]. Сильвер-Спринг, Мэриленд: Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США; 8 июля 2008 г. FDA. Доступно на http://bit.ly/fkBFeA. Доступ: 14 января 2011 г.
Kollef M, et al. ASPECT-NP: рандомизированное двойное слепое исследование III фазы, сравнивающее эффективность и безопасность цефтолозана / тазобактама и меропенема у пациентов с вентилируемой нозокомиальной пневмонией (VNP).Представлен на Европейском конгрессе клинической микробиологии и инфекционных заболеваний (ECCMID) 2019 г. (P1917). Амстердам, Нидерланды. 13-16 апреля 2019 г.
предикторов смертности пациентов с COVID-19 пневмонией, вызванной SARS-CoV-2: проспективное когортное исследование
Резюме
Для определения факторов, связанных со смертью пациентов с COVID-19 пневмонией, вызванной новым коронавирусом SARS-CoV -2.
Все клинические и лабораторные параметры были проспективно собраны у когорты пациентов с пневмонией COVID-19, которые были госпитализированы в легочную больницу Ухань, город Ухань, провинция Хубэй, Китай, в период с 25 декабря 2019 года по 7 февраля 2020 года.Одномерная и многомерная логистическая регрессия была проведена для изучения взаимосвязи между каждой переменной и риском смерти пациентов с пневмонией COVID-19.
В настоящее проспективное исследование было включено 179 пациентов с пневмонией COVID-19 (97 мужчин и 82 женщины), 21 из которых умер. Однофакторный и многомерный логистический регрессионный анализ показал, что возраст ≥65 лет (отношение шансов, 3,765; 95% доверительный интервал, 1,146‒17,394; p = 0,023), ранее существовавшие сопутствующие сердечно-сосудистые или цереброваскулярные заболевания (2.464; 0,755‒8,044; p = 0,007), CD3 + CD8 + Т-лимфоциты ≤75 клеток · мкл -1 (3,982; 1,132.0014,006; p <0,001) и сердечного тропонина I ≥0,05 нг · мл -1 ( 4,077; 1,166 ± 14,253; р <0,001) были связаны с увеличением риска смертности от пневмонии COVID-19. В тематическом исследовании, соответствующем полу, возрасту и сопутствующим заболеваниям, CD3 + CD8 + Т-лимфоциты ≤75 клеток · мкл −1 и сердечный тропонин I ≥0,05 нг · мл −1 оставались до быть предикторами высокой смертности от пневмонии COVID-19.
Мы определили четыре фактора риска: возраст ≥65 лет, ранее существовавшие сопутствующие сердечно-сосудистые или цереброваскулярные заболевания, CD3 + CD8 + Т-клетки ≤75 клеток · мкл -1 и сердечный тропонин I ≥0,05 нг · мл −1 , особенно два последних фактора, были предикторами смертности пациентов с пневмонией COVID-19.
Abstract
Наши данные показали, что возраст ≥65 лет, ранее существовавшие сопутствующие сердечно-сосудистые или цереброваскулярные заболевания, CD3 + CD8 + Т-клетки ≤75 клеток · мкл − 1 и сердечный тропонин I≥0.05 нг · мл -1 были четырьмя факторами риска для прогнозирования высокой смертности пациентов с пневмонией COVID-19.
Введение
В декабре 2019 года новая инфекционная пневмония, названная COVID-19, вызванная новым коронавирусом (SARS-CoV-2), появилась в Ухане, провинция Хубэй, Китай, и теперь распространяется через международные границы [1–3]. По состоянию на 12 февраля 2020 г. 189 медицинских бригад в составе 21 569 врачей и медсестер из 29 провинций Китая были отправлены в Хубэй для лечения пневмонии COVID-19 [4].Продолжающаяся пандемия пневмонии COVID-19 в настоящее время не находится под контролем, с высоким риском распространения в Китае и во всем мире. По состоянию на 22 марта 2020 г. в общей сложности было зарегистрировано 307 297 подтвержденных случаев как минимум в 169 странах [5]. К сожалению, последствия вспышки пневмонии COVID-19 и ее конечный масштаб неясны, поскольку ситуация быстро развивается [6, 7]. На самом деле страх перед продолжающейся эпидемией COVID-19 был и играет важную роль в экономических и социальных последствиях.
В первой опубликованной когорте из 41 пациента с пневмонией COVID-19 из больницы Ухань Цзиньинтань у шести (14,6%) пациентов наступило ухудшение за короткий период времени и они умерли от полиорганной недостаточности [8]; когда размер когорты увеличился до 99 случаев, 11 (11,1%) пациентов умерли [9]. В другой когорте госпитализированных пациентов с пневмонией COVID-19 из Ухани общая смертность составила 4,3% (6/138) [10]. Результаты этих трех предыдущих исследований показали, что пожилой возраст и сопутствующие заболевания были связаны с тяжестью заболевания или смертью пациентов с пневмонией COVID-19 [8–10].В период с 25 декабря 2019 года по 7 февраля 2020 года в общей сложности 179 взрослых пациентов с пневмонией COVID-19 были госпитализированы в Уханьскую легочную больницу, специальную больницу для изоляции и лечения пациентов с инфекционными заболеваниями. По состоянию на 24 марта 2020 года 158 пациентов были выписаны, оставшийся 21 умер. В настоящем исследовании мы стремились определить клинические и лабораторные параметры, связанные со смертностью пациентов с пневмонией COVID-19.
Методы
Пациенты
Это исследование было проведено в соответствии с утвержденными рекомендациями Институционального наблюдательного совета Уханьской легочной больницы, город Ухань, провинция Хубэй, Китай (wufeilunli-2020-02).Письменное информированное согласие от каждого пациента было отклонено, поскольку мы проспективно собрали и проанализировали все данные от каждого пациента в соответствии с политикой расследования вспышек новых инфекционных заболеваний, разработанной Национальной комиссией здравоохранения Китайской Народной Республики.
В период с 25 декабря 2019 года по 7 февраля 2020 года в Уханьскую легочную больницу была госпитализирована одноцентровая когорта из 179 последовательных пациентов с подтвержденной и вероятной пневмонией COVID-19, и все они были включены в настоящее исследование.Вероятный и точный диагноз пневмонии COVID-19 был установлен в соответствии с определением случая, установленным временным руководством ВОЗ [11].
Сбор и анализ данных
Информация обо всех пациентах, включая демографические данные, клинические характеристики, лабораторные параметры и исходы, была собрана проспективно. Два исследователя независимо друг от друга изучили формы сбора данных, чтобы дважды проверить собранные данные.
Описательная статистика включала частотный анализ (проценты) для категориальных переменных и средние значения ± стандартное отклонение (sd) или медианы и межквартильные диапазоны (IQR) для непрерывных переменных.Сравнения проводились с помощью критерия Стьюдента t или U-критерия Манна-Уитни для непрерывных переменных в зависимости от ситуации и с использованием критерия χ 2 или точного критерия Фишера для категориальных переменных. Одномерная и многомерная логистическая регрессия была проведена для изучения ассоциации клинических характеристик и лабораторных параметров и риска смерти. Обратный условный метод использовался для выбора переменных визуализации, входящих в систему оценки. Уровень статистической значимости был установлен на 0.05 (двусторонний). Все анализы проводились с помощью статистического программного обеспечения MedCalc и SPSS версии 23.0.
Результаты
Клинические данные
В этом отчете описана когорта пациентов с пневмонией COVID-19, состоящая из 179 пациентов, госпитализированных в Уханьскую легочную больницу в период с 25 декабря 2019 г. по 7 февраля 2020 г., из которых 136 (76%) были поставлены точный диагноз имели пневмонию COVID-19 с положительным результатом теста на SARS-CoV-2, а остальные 43 (24%) были диагностированы клинически. Среднее время между появлением симптомов и госпитализацией составило 9.7 дней (сд, 4,3 дня). Средний возраст составил 57,6 года (стандартное отклонение 13,7 года; диапазон 18-87 лет), 97 (54,2%) составляли мужчины (таблица 1). Из 179 пациентов у 21 (11,7%) произошло ухудшение за короткий период времени и они умерли от полиорганной недостаточности, особенно от дыхательной недостаточности и сердечной недостаточности, а средняя продолжительность от поступления до смерти составила 13,7 дня (стандартное отклонение — 8,3 дня; ранг — 3). ‒33 дня) (дополнительная таблица 1).
ТАБЛИЦА 1
Демография и клинические проявления у пациентов с пневмонией COVID-19 #
Как показано в таблице 1, пациенты в группе умерших были намного старше, чем в группе выживших (70.2 ± 7,7 года против 56,0 ± 13,5 года, p <0,001). Мы отметили, что больше пациентов в группе умерших страдали артериальной гипертензией (61,9% против 28,5%, p = 0,005) и сердечно-сосудистыми или цереброваскулярными заболеваниями (57,1% против 10,8%, p <0,001), и что не было никакой разницы в заболеваемость диабетом, хроническими расстройствами пищеварения, туберкулезом, хронической печеночной или почечной недостаточностью, заболеванием периферических сосудов и злокачественными новообразованиями между двумя группами (все p> 0,05).
Очень похоже на результаты, полученные в предыдущих исследованиях [8–10, 12], мы отметили, что пять основных общих симптомов включали лихорадку (98.9% пациентов), сухой кашель (81,6%), одышка (49,7%), утомляемость (39,1%), выделение мокроты (30,7%) и др. При поступлении среди всего населения (таблица 1). За исключением одышки, утомляемости, выделения мокроты и головной боли, которые чаще присутствовали в группе умерших, чем в группе выживших (85,7% против 44,9%, p <0,001; 61,9% против 36,7%, p = 0,033; 57,1% против 27,2%, p = 0,010; 23,8% ( против 7,6%, p = 0,033), другие виды симптомов были схожими в двух группах.У пациентов из группы умерших частота дыхания была выше, чем у выживших (p = 0,016), разницы в частоте сердечных сокращений не было.
Результаты лабораторных исследований
Возможно, из-за наличия вторичной бактериальной инфекции, о чем свидетельствуют более высокие концентрации белка C-ответа и прокальцитонина, у умершего было больше лейкоцитов и нейтрофилов, чем у выживших (таблица 2). Фактически, вторичная бактериальная инфекция легких была задокументирована на поздней стадии заболевания у 10 из 21 умершего пациента, а этиологический спектр включал Klebsiella Pneumoniae, Staphylococcus, Acinetobacter Baumannii, и Escherichia Coli, и т. Д.Как и ожидалось, у умершего было меньше лимфоцитов по сравнению с выжившими. Одно примечательное открытие заключалось в том, что абсолютное количество CD3 + CD8 + Т-клеток, но не CD3 + Т-клеток, CD4 + , было значительно снижено у умерших по сравнению с выжившими.
ТАБЛИЦА 2
Лабораторные данные у пациентов с пневмонией COVID-19 #
По сравнению с пациентами в группе выживших, пациенты в группе умерших получали более частые и более тяжелые сердечные повреждения, поскольку все лабораторные параметры, отражающие функцию сердца, включая сердечный тропонин Уровень I, миоглобина и натрийуретического пептида мозга у умерших был значительно повышен (таблицы 2 и 3).Умершие были более подвержены печеночной или почечной недостаточности и дыхательной недостаточности, на что указывало повышение уровня аспартатаминотрансферазы или креатинина, а также снижение артериального парциального давления кислорода (PaO 2 ) и соотношение PaO 2 к фракции вдохновения O 2 (F I O 2 ).
ТАБЛИЦА 3
Одномерный анализ факторов риска смертности для пациентов с пневмонией COVID-19 #
Предикторы смертности
Для всех демографических данных, клинических проявлений и лабораторных данных, представленных в таблицах 1 и 2, мы первоначально оценили каждую переменную который показал статистическую значимость с p <0.05 в различии между выжившими и выжившими с использованием одномерного анализа. Наш анализ показал, что возраст ≥65 лет, гипертония, сердечно-сосудистые или цереброваскулярные заболевания, одышка, утомляемость, выделение мокроты, головная боль, количество лейкоцитов> 10 × 10 9 / л, нейтрофилов> 6,3 × 10 9 / л, CD3 + CD8 + Т-клетки ≤75 клеток · мкл −1 , сердечный тропонин I ≥0,05 нг · мл −1 , миоглобин> 100 нг · л −1 , креатинин ≥133 мкмоль · л -1 , D-димер ≥0.5 мг · л -1 и <60 мм рт. Ст. Было связано со смертью пациентов с пневмонией COVID-19 (таблица 3). Во всех исследуемых переменных РаО 2 ≥80 мм рт. Ст. Было единственным фактором, который был связан с выживаемостью пациентов (отношение шансов 0,233 [95% ДИ 0,065–0,840]; p = 0,026). Вышеуказанные 16 переменных были дополнительно обработаны с использованием модели многовариантной логистической регрессии, в которой были выбраны четыре переменных, которые прогнозировали смертность, включая возрастную группу ≥65 лет, сердечно-сосудистые или цереброваскулярные заболевания, CD3 + CD8 + Т-лимфоциты ≤75 клеток · мкл -1 , и сердечный тропонин I≥0.05 нг · мл -1 (таблица 4).
ТАБЛИЦА 4
Многомерный логистический регрессионный анализ факторов риска смертности для пациентов с пневмонией COVID-19
Чтобы лучше понять факторы, которые могут повлиять на выживаемость пациентов с пневмонией COVID-19 с аналогичным возрастом и основными заболеваниями, мы выбрали пол, возраст — и основное заболевание ‒ отобрали 42 пациента из выживших для проведения исследования случай-контроль в соотношении 2: 1. Как показано в Таблице 2 Приложения, не было различий по всем параметрам демографии и клинической картине между умершим и подобранным оставшиеся в живых после контроля.Учитывая, что многие выжившие были более молодыми, двое оставшихся в живых, возраст которых был одинаковым или ± 1 год, были сопоставлены с каждым умершим. По сравнению с выжившими, умершие имели значительно повышенные концентрации прокальцитонина, сердечного тропонина I, миоглобина и креатинина, а также значительное снижение количества CD3 + CD8 + Т-клеток (таблица 3 приложения). После исключения влияния возраста и основных заболеваний на смертность, одномерный анализ показал, что CD3 + CD8 + Т-лимфоциты ≤75 клеток · мкл -1 и сердечный тропонин I ≥0.05 нг · мл -1 были единственными двумя переменными, которые могли быть предикторами смертности пациентов с пневмонией COVID-19 (таблица 5).
ТАБЛИЦА 5
Одномерный анализ факторов риска смертности для пациентов с пневмонией COVID-19 в согласованном исследовании случай-контроль
Обсуждение
Продолжающаяся эпидемия SARS-CoV-2 стала третьим разом, когда зоонозный коронавирус скрестил виды и заразил человека. населения за последние 18 лет [13]. В ноябре 2002 года тяжелый острый респираторный синдром (SARS), вызванный SARS-CoV, был впервые обнаружен в провинции Гуандун, Китай, а количество случаев SARS значительно увеличилось в следующем году в Китае, а затем распространилось по всему миру [14], заразив 8098 человек. человек в 26 странах и убито 774 из них [15].В период с сентября 2012 г. по 20 января 2017 г. произошла вспышка 1879 лабораторно подтвержденных случаев ближневосточного респираторного синдрома (БВРС), вызванного БВРС-КоВ, в 27 странах, в результате чего произошло не менее 659 связанных смертей [16]. По состоянию на полночь 24 марта 2020 г. количество подтвержденных случаев пневмонии COVID-19 и смерти в Китае составило 81218 и 3281, соответственно, что указывает на общий уровень смертности от пневмонии COVID-19 в 4% [17].
В городе Ухань две крупные специальные больницы, Уханьская легочная больница и Уханьская больница Цзиньинтань, оказывают медицинские услуги пациентам с инфекционными заболеваниями.С момента вспышки пневмонии COVID-19 все пациенты в двух больницах были инфицированы пневмонией COVID-19. Обычно только пациенты с тяжелым заболеванием из больниц общего профиля переводились в специальные больницы на карантин и лечение. Вот почему общая смертность от пневмонии COVID-19 в специальных больницах (11,1% в когорте Уханьской больницы Цзиньинтань [9] и 11,7% [95% ДИ, 7,0–16,5%] в нашей текущей когорте) оказалась выше. чем в когорте больницы общего профиля (4.3%) [10]. К сожалению, не было доступных препаратов против SARS-CoV-2 для лечения пациентов с пневмонией COVID-19. Хотя ни один из антибиотиков, противогрибковых препаратов, кортикостероидов или иммунных глобулинов обычно не рекомендуется вводить при пневмонии COVID-19, в настоящем исследовании всем тяжелобольным пациентам назначали комбинацию из двух или более указанных выше препаратов.
Документально подтверждено, что, несмотря на некоторое сходство клинических признаков между SARS и MERS, MERS прогрессирует до респираторной недостаточности гораздо быстрее с гораздо большей смертностью, чем SARS, и что пожилой возраст и основное заболевание, вероятно, связаны со смертностью MERS [18].В настоящем исследовании пациенты в группе умерших были намного старше выживших, а одномерный и многомерный логистический регрессионный анализ показал, что возраст ≥65 лет является надежным предиктором смерти от пневмонии COVID-19. Фактически, из всей когорты из 179 пациентов с пневмонией COVID-19 не умерло ни одно лицо моложе 50 лет, тогда как 17 (81%) умерших пациентов были старше 65 лет. Как и ожидалось, наш анализ также показал, что основные сердечно-сосудистые или цереброваскулярные заболевания способствовали высокой смертности от пневмонии COVID-19.
Было продемонстрировано, что инактивированный SARS-CoV вызывает антиген-специфический ответ цитотоксических Т-лимфоцитов в мононуклеарных клетках периферической крови выздоровевших пациентов с SARS, но не у пациентов с критическим SARS или умерших от SARS, что позволяет предположить, что последние, по-видимому, не могут выработать достаточный защитный иммунитет для устранения SARS-CoV; их иммунные реакции на этот патоген на самом деле могли усугубить их болезнь [19]. В случае MERS несколько медиаторов воспаления, включая индуцибельный белок-10, хемоаттрактантный белок-1 моноцитов и концентрации интерлейкина-6, сильно связаны со смертностью [20].Учитывая, что пневмония COVID-19 является новым инфекционным заболеванием, механизмы, с помощью которых SARS-CoV-2 вызывает тяжелое заболевание и летальный исход у людей, неизвестны. Совсем недавно сообщалось, что количество CD8 + Т-лимфоцитов значительно снижено в периферической крови у пациентов с пневмонией COVID-19 [21]. Было показано, что несколько цитокинов и хемокинов, таких как интерлейкин-2, интерлейкин-7, интерлейкин-10, фактор, стимулирующий колонии макрофагов, индуцибельный белок-10, хемоаттрактантный белок-1 моноцитов, воспалительный белок макрофагов-1α и некроз опухоли. Концентрации фактора-α были выше у пациентов с тяжелой пневмонией COVID-19, чем у пациентов с легкой формой заболевания, что позволяет предположить, что инфекция SARS-CoV-2 повреждает иммунную систему человека и приводит к систематической воспалительной реакции [8].Одним из важных открытий в нашем исследовании было то, что CD3 + CD8 + Т-лимфоциты, но не CD3 + CD4 + Т-лимфоциты, в обращении были значительно сокращены у умерших пациентов по сравнению либо с общей выжившей популяцией, либо с теми, у кого был пол. -, возраст‒ и сопутствующие заболевания контрольные группы. Что еще более важно, CD3 + CD8 + Т-лимфоциты ≤75 клеток · мкл -1 , были надежным предиктором смертности пациента с пневмонией COVID-19. Эти данные показали, что прогрессирующее иммунно-ассоциированное повреждение и неадекватные адаптивные иммунные ответы могут быть возможными механизмами, с помощью которых SARS-CoV-2 вызывает тяжелое заболевание и летальный исход.
На 24 марта 2020 г. в Китае было зарегистрировано 4287 текущих случаев подтвержденной пневмонии COVID-19, из которых 1399 (32,6%) были очень тяжелыми случаями [17]. Как упоминалось выше, общий уровень смертности от пневмонии COVID-19 составлял 4% [17], и большинство умерших пациентов были пожилыми людьми с основным заболеванием [8–10]. Из более молодой когорты из 1716 китайских медицинских работников, возраст которых всегда был <65 лет по всей стране, умерли 6 (0,3%) [22]. Эти данные показывают, что большинство пациентов с пневмонией COVID-19 выздоровеют от болезни, особенно молодые люди.Наши текущие данные продемонстрировали, что пациенты в группе умерших были подвержены полиорганной недостаточности, особенно сердечной недостаточности и дыхательной недостаточности. Одним из лучших лабораторных параметров, влияющих на повреждение сердца для прогнозирования смертности от пневмонии COVID-19, был сердечный тропонин I, и этот параметр оставался действительным в контрольном анализе, сопоставленном с полом, возрастом и основным заболеванием. Наши результаты показывают, что при оказании помощи тяжелобольным пациентам с пневмонией COVID-19 следует уделять особое внимание стратегии защиты жизненно важных органов для их выживания.Следует отметить, что повышение уровня сердечного тропонина I у пациентов с COVID-19 было всего лишь признаком повреждения миокарда, которое, вероятно, было вторичным по отношению к тяжелой гипоксемии. Для пациентов с положительным результатом сердечного тропонина I мы могли выбрать подходящую стратегию респираторной поддержки для улучшения оксигенации и дождаться восстановления повреждения миокарда.
В заключение мы определили четыре предиктора: возраст ≥65 лет, ранее существовавшие сопутствующие сердечно-сосудистые или цереброваскулярные заболевания, CD3 + CD8 + Т-клетки ≤75 клеток · мкл -1 и сердечный тропонин I≥0.05 нг · мл −1 , для высокой смертности среди всего населения пациентов с пневмонией COVID-19. В исследовании случай-контроль с сопоставлением по полу, возрасту и сопутствующим заболеваниям мы также обнаружили CD3 + CD8 + Т-лимфоциты ≤75 клеток · мкл -1 и сердечный тропонин I ≥0,05 нг · мл −1 оставались предикторами высокой смертности пациентов с пневмонией COVID-19 с аналогичным возрастом и основными заболеваниями.
Сноски
Авторы: H.З.С. и П. задумал идею, разработал и руководил исследованием, имел полный доступ ко всем данным и взял на себя ответственность за их целостность. R.H.D, C.Q.Y., T.Z.C., M.L., G.Y.G., J.D., C.L.Z., Q.Z., M.H., X.Y.L. отвечали за диагностику и лечение пациентов, а также собирали клинические и лабораторные данные. L.R.L. и W.W. проанализировали данные и выполнили статистический анализ. Все авторы просмотрели и одобрили окончательную версию.
Заявление о поддержке: Эта работа была поддержана Планом миссии Пекинской городской администрации больниц, Китай (SML20150301), и программой талантов 1351 Пекинской больницы Чао-Ян, Китай (WXZXZ-2017-01).1351 Программа талантов Пекинской больницы Чао-Ян, Китай; Грант: WXZXZ-2017-01; Пекинское муниципальное управление больниц; DOI: http://dx.doi.org/10.13039/501100009601; Грант: SML20150301.
В этой статье есть дополнительные материалы, доступные на erj.ersjournals.com
Конфликт интересов: д-ру Ду нечего раскрывать.
Конфликт интересов: доктору Ляну нечего раскрывать.
Конфликт интересов: Dr.Ян нечего раскрывать.
Конфликт интересов: доктору Вангу нечего раскрывать.
Конфликт интересов: доктору Цао нечего раскрывать.
Конфликт интересов: доктору Ли нечего раскрывать.
Конфликт интересов: доктору Го нечего раскрывать.
Конфликт интересов: доктору Ду нечего раскрывать.
Конфликт интересов: доктору Чжэн нечего раскрывать.
Конфликт интересов: доктору Чжу нечего раскрывать.
Конфликт интересов: д-ру Ху нечего раскрывать.
Конфликт интересов: доктору Ли нечего раскрывать.
Конфликт интересов: доктору Пэну нечего раскрывать.
Конфликт интересов: доктору Ши нечего раскрывать.
- Поступила 2 марта 2020 г.
- Принята 30 марта 2020 г.
Статистика по детской пневмонии — ДАННЫЕ ЮНИСЕФ
Пневмония является наиболее серьезным исходом острой респираторной инфекции (ОРИ) и убивает больше детей, чем любое другое инфекционное заболевание, унося жизни более 800000 детей в возрасте до пяти лет каждый год, или около 2200 ежедневно. Это более 153 000 новорожденных. Для сравнения, в 2018 году 437000 детей в возрасте до пяти лет умерли от диареи и 272000 — от малярии. Во всем мире ежегодно регистрируется более 1400 случаев пневмонии на 100 000 детей или 1 случай на 71 ребенка, причем наибольшая заболеваемость приходится на Южную Азию (2500 случаев на 100 000 детей), а также в Западную и Центральную Африку (1620 случаев на 100 000 детей).
Прогресс в снижении смертности от пневмонии у детей в возрасте до пяти лет был значительно медленнее, чем в случае других инфекционных заболеваний. С 2000 года смертность детей в возрасте до пяти лет от пневмонии снизилась на 54 процента, а смертность от диареи снизилась на 64 процента и в настоящее время составляет почти половину случаев смерти от пневмонии.
Смертность от детской пневмонии тесно связана с факторами бедности, такими как недоедание, отсутствие безопасной питьевой воды и санитарии, загрязнение воздуха внутри и снаружи помещений, а также недостаточный доступ к медицинскому обслуживанию.По оценкам, к 2030 году потребуется еще около 18 миллионов медицинских работников для профилактики, диагностики и лечения пневмонии, а также для достижения целей ЦУР по всеобщему охвату услугами здравоохранения.
Около половины смертей от детской пневмонии связано с загрязнением воздуха. Последствия загрязнения воздуха внутри помещений убивают больше детей во всем мире, чем загрязнение атмосферного воздуха. В то же время около двух миллиардов детей в возрасте от 0 до 17 лет живут в районах, где уровень загрязнения атмосферного воздуха превышает установленные международные нормы.
Раннее обращение за медицинской помощью для детей с симптомами пневмонии от поставщика медицинских услуг снижает смертность, однако данные обследований населения показывают, что наблюдается медленный прогресс в поведении детей с ОРИ при обращении за помощью.За последнее десятилетие число обращающихся за помощью к поставщику медицинских услуг увеличилось всего на 8 процентов (60 против 68 процентов), при этом самый низкий уровень и практически отсутствие прогресса в Восточной и Южной Африке (54 процента).
Во всем мире примерно две трети (68 процентов) детей с симптомами пневмонии (ОРИ) направляются к врачу. Хотя нельзя предположить, что все дети с симптомами пневмонии болеют бактериальной пневмонией и должны получать антибиотики, данные указывают на большой разрыв между богатыми и бедными в лечении симптомов пневмонии: только 60 процентов детей из бедных семей по сравнению с 79 детьми на одного ребенка. процентов детей в богатых семьях, получающих помощь по поводу симптомов пневмонии у поставщика медицинских услуг.Кроме того, в странах Африки к югу от Сахары, где происходит большинство случаев смерти от пневмонии, только 57 процентов детей с симптомами пневмонии получают медицинскую помощь, причем самые низкие показатели наблюдаются в Восточной и Южной Африке.
Во время пандемии COVID-19 существуют дополнительные риски для здоровья и благополучия детей, поскольку пандемия вызывает нарушения во всей системе здравоохранения, а также в жизни семей. В районах, где медицинский персонал перегружен, становится нехватка основных товаров (например, кислородной терапии) или там, где поведение, связанное с обращением за медицинской помощью, снижается, усилия по смягчению передачи (например,грамм. карантин, ограничения на поездки), это может привести к более тяжелым заболеваниям и более высокой смертности от детской пневмонии.
Простые решения могут спасти жизнь детей
Комплексный глобальный план действий по профилактике пневмонии и диареи и борьбе с ними (GAPPD) представляет собой комплексную основу ключевых мероприятий, доказавших свою эффективность в защите здоровья детей, профилактике заболеваний и надлежащем лечении детей, которые действительно болеют диареей и пневмонией.
Protect: Защитные меры создают основу для сохранения здоровья детей и защиты от болезней
- Исключительное грудное вскармливание в течение первых 6 месяцев жизни (без дополнительных продуктов или жидкостей, включая воду) защищает младенцев от болезней и гарантирует им безопасный, чистый, доступный и полностью соответствующий их потребностям источник питания.Почти половину всех эпизодов диареи и одну треть всех респираторных инфекций можно предотвратить с помощью более широкого грудного вскармливания в странах с низким и средним уровнем доходов.
- Адекватный прикорм и продолжение грудного вскармливания: Обеспечивает полноценное питание, поддерживает сильную иммунную систему и обеспечивает защиту от болезней. В возрасте от 6 месяцев до 2 лет адекватный прикорм — предоставление детям достаточного количества безопасной, питательной и соответствующей возрасту пищи наряду с продолжением грудного вскармливания — может снизить детскую смертность, в том числе от пневмонии и диареи.
Профилактика: профилактические мероприятия помогают остановить передачу болезней и предотвратить заболевание детей
- Иммунизация: вакцины против Haemophilus influenzae типа b (Hib) и пневмококковые конъюгированные вакцины (PCV) эффективны для предотвращения двух наиболее распространенных бактериальных причин детской пневмонии. Кроме того, использование вакцин против кори и коклюша в национальных программах иммунизации существенно снижает заболеваемость пневмонией и смертность детей. В 2018 году 71 миллион детей не получили трех рекомендованных доз ПКВ, что подвергло их более высокому риску пневмонии.
- Снижение загрязнения воздуха в домашних условиях: более 40 процентов населения мира используют твердые виды топлива (древесина, уголь, навоз и отходы сельскохозяйственных культур) для приготовления пищи и обогрева своих домов, подвергая детей загрязнению воздуха в домашних условиях и почти вдвое увеличивая риск заболевания пневмонией. . Улучшение качества воздуха в домашних условиях может снизить количество случаев тяжелой пневмонии, а также предотвратить ожоги, сэкономить время и сократить расходы на топливо. Использование каминных печей может снизить загрязнение воздуха в домашних условиях наполовину, уменьшив тяжелую пневмонию почти на 30 процентов.
- Профилактика ВИЧ: Профилактика ВИЧ и лечение ВИЧ-инфекции с помощью антиретровирусных препаратов помогает поддерживать иммунную систему и снижает риск заражения пневмонией. Профилактика ко-тримоксазолом обеспечивает дополнительную защиту от пневмонии для ВИЧ-инфицированных и подвергшихся воздействию детей детей и может снизить смертность от СПИДа на 33 процента.
Диагностика и лечение: лечебные вмешательства — когда они своевременны и необходимы — могут вылечить детей от пневмонии и обеспечить выживание
Спасение детей от пневмонии требует неотложных действий, и распознавание признаков опасности, включая учащенное и затрудненное дыхание и кашель, является первым шагом.Для лечения большинства типов серьезной пневмонии часто используются антибиотики, которые обычно стоят менее 50 центов за полное лечение. Однако не все дети с симптомами пневмонии должны получать антибиотики: согласно рекомендациям ВОЗ и ЮНИСЕФ по комплексному ведению детских болезней, антибиотиками следует лечить только те случаи, которые медицинский работник классифицирует как пневмонию. Более того, не все дети, отнесенные к таковым, имеют настоящую пневмонию. Тем не менее, в условиях отсутствия адекватных диагностических инструментов рекомендации ВОЗ / ЮНИСЕФ предоставляют общий стандарт, по которому медицинские работники могут оценивать и классифицировать заболевания бактериальной пневмонии, требующие лечения антибиотиками.
Список литературы
ЮНИСЕФ, Одного слишком много: положить конец детской смертности от пневмонии и диареи , ЮНИСЕФ, Нью-Йорк, 2016.
ЮНИСЕФ, Очистите воздух для детей , ЮНИСЕФ, Нью-Йорк, 2016
ЮНИСЕФ, Стремление к выживанию детей: новое обещание — Отчет о ходе работы, 2015 г. , ЮНИСЕФ, Нью-Йорк, 2015 г.
Межучрежденческая группа Организации Объединенных Наций по оценке детской смертности (IGME), Уровни и тенденции детской смертности , ВОЗ и ЮНИСЕФ, Нью-Йорк, 2019
Прекращение предотвратимой детской смертности от пневмонии и диареи к 2025 году: Комплексный глобальный план действий по пневмонии и диарее (GAPPD) , ВОЗ, Женева, 2013 г.
ЮНИСЕФ, Пневмония и диарея: борьба с самыми смертоносными заболеваниями беднейших детей мира , ЮНИСЕФ, Нью-Йорк, 2012.
ВОЗ и ЮНИСЕФ, Глобальный план действий по профилактике пневмонии и борьбе с ней (GAPP) : Отчет неофициальной консультации , ВОЗ, Женева, 2008 г.
ВОЗ и ЮНИСЕФ, Комплексное ведение детских болезней , ВОЗ, Женева, 2008 г.
ЮНИСЕФ и ВОЗ, Пневмония: забытый убийца детей , ЮНИСЕФ, Нью-Йорк, 2006.
Рецензируемые публикации
Лю, Ли и др. (2016), «Глобальные, региональные и национальные причины смертности детей в возрасте до 5 лет в 2000–15 годах: обновленный систематический анализ с последствиями для целей в области устойчивого развития», Lancet, 388, 3027-3035.
Кэмпбелл, Х. и др., «Измерение охвата ЗМН: проблемы при мониторинге доли маленьких детей с пневмонией, получающих лечение антибиотиками», в PLOS Medicine : опубликовано 7 мая 2013 г., информация: doi / 10.1371 / journal.pmed.1001421 (см .: Коллекция PLOS: Измерение охвата в области охраны здоровья матери, новорожденного и ребенка).
.


