3.7. Гепатит С и туберкулез
Очень часто у людей, живущих с ВИЧ-инфекцией, обнаруживается вирус гепатита С и туберкулез. Такие сочетанные заражения одного организма разными по природе заболеваниями называются коинфекциями. Людям, которым поставлен диагноз ВИЧ-инфекция, рекомендуется пройти обследование на вирусные гепатиты и туберкулез.
Основные пути передачи гепатита С схожи с путями передачи ВИЧ — через кровь, в большинстве случаев при использовании нестерильного инструмента при употреблении инъекционных наркотиков. Также существуют единичные случаи передачи вируса при незащищенных половых контактах, но это скорее исключение, чем правило.
У людей, живущих с ВИЧ, наличие вирусного гепатита С может сопровождаться более серьезным поражением печени, поскольку организм ослаблен и существует иммунодефицит. Известно также, что ВИЧ ускоряет развитие гепатита С.
Если лечение ВИЧ в виде антиретровирусной терапии и лечение вирусного гепатита С проводятся одновременно, необходимо отслеживать состояние пациента, поскольку некоторые препараты повышают чувствительность организма к курсу лечения и вызвать побочные эффекты. Принцип лечения гепатита С как у людей с ВИЧ-инфекцией, так и без нее — один и тот же. В настоящее время для лечения вирусного гепатита С существует безинтерфероновая терапия, которая не дает побочных эффектов и увеличивает вероятность выздоровления до 100 %, в том числе у ВИЧ-позитивных людей.
Принцип лечения гепатита С как у людей с ВИЧ-инфекцией, так и без нее — один и тот же. В настоящее время для лечения вирусного гепатита С существует безинтерфероновая терапия, которая не дает побочных эффектов и увеличивает вероятность выздоровления до 100 %, в том числе у ВИЧ-позитивных людей.
Туберкулез у людей, которые живут с ВИЧ, так же, как и гепатит С, протекает в более острой форме и прогрессирует на фоне выраженного иммунодефицита.
Лечение туберкулеза у людей с ВИЧ-инфекцией ничем не отличается от режимов лечения людей без ВИЧ-инфекции и проводится по общим правилам. Лечение назначается сразу же после подтверждения диагноза и проводится под наблюдением врача, т. к. параллельно идет прием антиретровирусных препаратов. Химиотерапия туберкулеза у людей, живущих с ВИЧ, позволяет полностью излечиться от заболевания, несмотря на сниженный иммунитет.
Гепатит, туберкулез | Новая жизнь
Гепатит
Гепатит C («ц», hepatitis C) – это инфекционное заболевание печени, вызываемое вирусом. Инфекция, обусловленная вирусом гепатита C , может развиться у любого человека и наблюдается чаще у молодых людей. Заболеваемость гепатитом С растет.
Инфекция, обусловленная вирусом гепатита C , может развиться у любого человека и наблюдается чаще у молодых людей. Заболеваемость гепатитом С растет.
Вирус гепатита С передается через кровь. Большинство случаев гепатита С развивается незаметно и переходит в хроническую форму с многолетним течением без симптомов. Хронический гепатит С хорошо поддается лечению новыми препаратами. Действующей вакцины для профилактики гепатита С пока не существует, однако заражения можно избежать.
Полезные ресурсы
Туберкулёз
Основной фактор развития туберкулёза (если речь не идёт о контакте с больным с открытой формой) — ослабленный иммунитет. Упасть иммунитет может по самым разным причинам: из-за сильного стресса (развод, переезд, увольнение с работы или поступление в университет), из-за диет или бестолкового питания, из-за хронического недосыпа, переработок, алкоголя. Но есть как минимум одно состояние, когда иммунная система падает гарантированно, — это ВИЧ.
По данным ВОЗ, вероятность развития туберкулёза у людей с ВИЧ в 20–30 раз превышает аналогичный показатель среди неинфицированных людей.
Болеть в России не только страшно, но порой и стыдно — ряд диагнозов окружён стигмой такой силы, что вызывает у окружающих, включая и некоторых врачей, смесь ужаса и презрения. И если об одном из таких заболеваний — ВИЧ — постепенно начинают говорить более человечно и менее антинаучно, то о туберкулёзе, кажется, не говорят совсем.
Смертельная чахотка из классики русской литературы, болезнь бездомных и заключённых — вот примерно всё, что о нём принято знать. Мало кто подозревает, что в 2016 году это буквально может случиться с каждым: дремлющей формой заболевания в мире заражён каждый третий, а в России — практически каждый первый… Читать дальше
Полезные ресурсы
http://www.tbcentr.com/ — Центр специализированной медицнской помощи больным внелегокочной формой туберкулеза
Полностью побежденный вирус — Ведомости
Первая научная статья об открытии, благодаря которому был идентифицирован вирус гепатита C, была опубликована в журнале Science в 1989 г. С тех пор смертельную болезнь удалось досконально изучить и найти терапию, позволяющую полностью излечивать около 95% страдающих ею пациентов.
С тех пор смертельную болезнь удалось досконально изучить и найти терапию, позволяющую полностью излечивать около 95% страдающих ею пациентов.
Для заболевания, передающегося в основном через кровь, гепатит С впечатляет масштабами распространения. По данным ВОЗ, в мире хроническим гепатитом С страдает 71 млн человек. И 400 000 ежегодно умирают от гепатита этой разновидности и вызываемых им заболеваний. В России, по информации центра по мониторингу за вирусными гепатитами Роспотребнадзора, оценочное число случаев хронического вирусного гепатита С составляет от 3 млн до 5 млн. Частота регистрации хронического гепатита С в России в 2019 г. составила 31 случай на 100 000 населения, т. е. более 45 000 новых случаев.
ВОЗ считает гепатит настолько же опасным заболеванием, как туберкулез и ВИЧ. Не случайно успехи в борьбе с этой болезнью уже второй раз отмечаются Нобелевской премией – в 1976 г. награду получил доктор Барух Бламберг, который не только обнаружил и описал вирус гепатита В, но и разработал защищающую от него вакцину. А день рождения Бламберга – 28 июля – выбран ВОЗ в качестве Международного дня борьбы с гепатитом (World Hepatitis Day).
А день рождения Бламберга – 28 июля – выбран ВОЗ в качестве Международного дня борьбы с гепатитом (World Hepatitis Day).
В 1970-х гг. Харви Альтер и его коллеги изучали природу возникновения гепатита у пациентов, которым переливали кровь. Ее проверка на наличие вирусов гепатитов А и В не исключала случаев заражения. В 1978 г. Альтер опытным путем показал, что переливание плазмы от пациентов с не описанным тогда гепатитом может вызвать заболевание у шимпанзе. Это указывало на то, что болезнь вызвана именно возбудителем инфекции.
А в 1980-х гг. Майкл Хоутон и его коллеги, работавшие тогда в фармацевтической компании Chiron, искали возбудителя болезни, просеивая коллекции фрагментов ДНК, собранных у инфицированных шимпанзе. Они следили за тем, какие из ее фрагментов будут реагировать на антитела в крови людей, инфицированных гепатитом неизвестного тогда вида. Так команде Хоутона удалось идентифицировать возбудителя болезни – вирус гепатита С, РНК-вирус из семейства флавивирусов.
Затем исследователи разработали анализ крови и показали, что он может идентифицировать образцы, подозреваемые в передаче необъяснимых случаев гепатита. Это позволило провести скрининг донорской крови по всему миру, что резко сократило число вновь инфицированных людей. «До этих открытий переливание крови было похоже на русскую рулетку, – заявил изданию Science Нильс-Горан Ларссон, член Нобелевского комитета. – Эти ученые сделали переливание крови безопасным, и это предотвратило бесчисленное количество смертельных случаев».
Полностью излечимым гепатит С стал в последнее десятилетие. «В 1990-х этот вид гепатита считался неизлечимым, – говорит заведующая отделением трансплантации костного мозга и иммунотерапии университетской клиники «Хадасса» в Иерусалиме профессор Полина Степенски. – Безусловно, победа над таким заболеванием является великим достижением с точки зрения как науки, так и прикладной медицины. Вероятность полного излечения заболевания современными средствами составляет около 95%».
Прорыв случился благодаря разработке противовирусных препаратов прямого действия. Сегодня они стоят $10 000–20 000 на курс препаратов оригинального производства. Поскольку цена весьма высока, до полной победы над гепатитом во всем мире еще далеко. Но в научном, а не эпидемиологическом понимании болезнь уже побеждена, причем путь к этой победе занял не так много лет. И этот факт, вполне возможно, дал повод вспомнить тех, кто путь к этой победе начал, и отметить их главной наградой научного мира. Что особенно актуально сейчас, в разгар глобальной борьбы с другим смертельным вирусом.
На самом деле Харви Дж. Альтер, Майкл Хоутон и Чарльз Райс не считались основными претендентами на премию 2020 г. За неделю до решения Нобелевского комитета научный портал NewsWise опубликовал прогнозы членов совета Американского физиологического общества – всемирно признанных ученых. Большинство посчитало, что в этом году премию получит группа ученых за развитие технологии редактирования генома CRISPR. А по прогнозам компании Clarivate Analytics, подсчитывающей цитируемость в научной базе Web of Science, основными претендентами на награду по медицине и физиологии были биохимики из Гарварда Памела Бьоркман и Джек Стромингер, занимающиеся изучением структур и функций белков главного комплекса гистосовместимости человека, играющих основную роль в развитии иммунитета.
А по прогнозам компании Clarivate Analytics, подсчитывающей цитируемость в научной базе Web of Science, основными претендентами на награду по медицине и физиологии были биохимики из Гарварда Памела Бьоркман и Джек Стромингер, занимающиеся изучением структур и функций белков главного комплекса гистосовместимости человека, играющих основную роль в развитии иммунитета.
Из опрошенных NewsWise ученых премию за открытие гепатита С предсказал профессор физиологии Университета Монтаны Джейсон Картер. Но вот что интересно: среди номинантов он назвал Чарльза Райса и Ральфа Бартеншлагера из Университета Хейдельберга в Огайо. Однако последнего среди награжденных не оказалось. Так часто бывает: правила Нобелевской премии позволяют наградить не более трех человек, хотя в работе и достижении результата, как правило, участвуют большие научные коллективы.
Нобелевскую премию по медицине присудили первооткрывателям вируса гепатита C
5 октября в Стокгольме были объявлены лауреаты Нобелевской премии по физиологии или медицине 2020 года. Ими стали Харви Альтер (Harvey Alter), Майкл Хотон (Michael Houghton) и Чарльз Райс (Charles Rice). Премия присуждена учёным за открытие вируса гепатита С.
Ими стали Харви Альтер (Harvey Alter), Майкл Хотон (Michael Houghton) и Чарльз Райс (Charles Rice). Премия присуждена учёным за открытие вируса гепатита С.
Альтер и Райс родились в США, в этой же стране и работают в настоящий момент. Хотон родился в Великобритании, а сейчас работает в Канаде.
Каждый из трёх лауреатов получит треть призовой суммы.
Гепатит как глобальная проблема
Гепатит – это заболевание, сопровождающееся воспалением печени. Обычно он имеет инфекционную природу. Ещё в 1940-х годах стало ясно, что существует как минимум два вида этого недуга.
Гепатит А – это “болезнь грязных рук”, его возбудитель передаётся через пищу и воду или при непосредственном контакте с больным. Данная инфекция имеет ярко выраженные симптомы, например, пожелтение кожи и белков глаз. Специфического лечения от него не существует, но, как правило, организм пациента сам справляется с вирусом.
Другим видом гепатита (сейчас мы знаем, что его вызывают два разных возбудителя: вирусы гепатита B и С) можно заразиться через кровь и половым путём.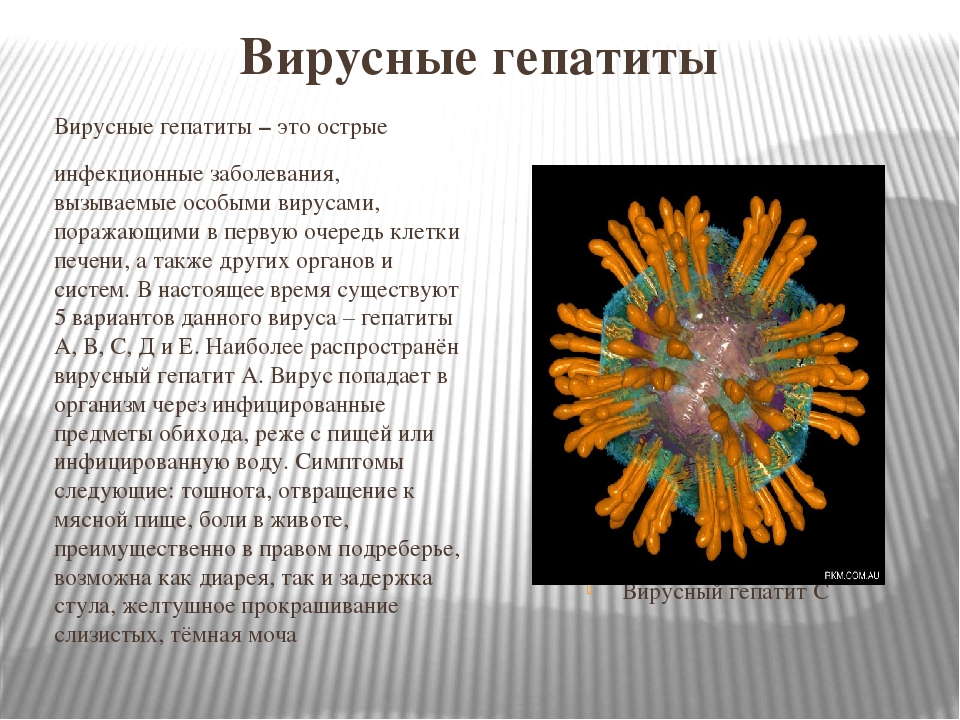 Такой гепатит гораздо более опасен, так как очень часто болезнь становится хронической и может перерасти в цирроз или рак печени. При этом больной человек может много лет не подозревать о своём недуге и заражать окружающих.
Такой гепатит гораздо более опасен, так как очень часто болезнь становится хронической и может перерасти в цирроз или рак печени. При этом больной человек может много лет не подозревать о своём недуге и заражать окружающих.
Даже сегодня от гепатита B и C в мире умирает более миллиона человек в год. Что делает его проблемой, сопоставимой по масштабам с ВИЧ и туберкулёзом.
Харви Альтер: заметить неладное
В 1960-х годах американский биолог Барух Бламберг выделил вирус гепатита B (за это он был удостоен Нобелевской премии по физиологии или медицине 1976 года). Учёные разработали диагностические тесты и эффективную вакцину. Радости медиков не было предела: наконец-то укрощён возбудитель опасного хронического гепатита!
Но благодаря исследованиям Альтера и его группы стало ясно: что-то о гепатите мы всё ещё не знаем. В организме многих пациентов, заразившихся гепатитом через кровь или половым путём, не обнаруживался вирус гепатита B. А значит, существует ещё какая-то причина опасной болезни.
Альтер показал, что кровь больного человека может заразить шимпанзе. После этого сомнений в инфекционной природе “гепатита не А и не B” не осталось. Дальнейшие изыскания привели Альтера и его коллег к заключению, что возбудитель болезни – не бактерия или другой микроорганизм, а вирус.
Майкл Хотон: в поисках убийцы
Многие учёные принялись искать новый вирус, но традиционные методы не дали результата. Тогда Хотон и его коллеги разработали и применили новый подход.
Они кропотливо выделяли из крови инфицированного шимпанзе фрагменты ДНК и РНК. Разумеется, почти все они принадлежали самому животному. Но биологи надеялись, что рано или поздно наткнутся на генетический след таинственного вируса.
Но как его опознать? Дело происходило в 1980-х годах, современных методов анализа ДНК и РНК, мощных компьютеров и обширных баз данных тогда не было.
Лауреат предположил, что в крови пациентов с “гепатитом не А и не B” должны быть антитела к вирусу. Учёные выделили из крови добровольцев разные антитела и принялись методично проверять, не среагирует ли какое-нибудь из них на фрагменты генома из крови шимпанзе. Это была очень трудоёмкая работа.
Учёные выделили из крови добровольцев разные антитела и принялись методично проверять, не среагирует ли какое-нибудь из них на фрагменты генома из крови шимпанзе. Это была очень трудоёмкая работа.
После долгих исследований команда Хотона действительно обнаружила антитело, которое реагировало на фрагмент РНК. Дальнейшие изыскания показали, что он принадлежит вирусу из рода флавивирусов. Его назвали вирусом гепатита C.
Чарльз Райс: окончательные доказательства
Но действительно ли именно этот вирус вызывает воспаление и гибель клеток печени? Да, мир теперь знал, что он обнаружился в крови больной гепатитом обезьяны, а антитела к нему – у больного гепатитом человека. Но, может быть, это случайность? Ведь и люди, и шимпанзе страдают от множества общих инфекций, например, от вируса герпеса. Его (и антитела к нему) вполне можно найти в крови животных и людей, в том числе и больных гепатитом. Но это же не значит, что гепатит вызывается герпесом!
Чтобы получить решающие доказательства, нужно было искусственно заразить животное новым вирусом и убедиться, что у него развился гепатит. Это и проделал Чарльз Райс и его команда.
Это и проделал Чарльз Райс и его команда.
Впрочем, сказать это проще, чем сделать. Ведь у биологов были только разрозненные фрагменты РНК вируса, а не он сам в целости и сохранности, с полным геномом и белковой оболочкой.
Райс выяснил, какие из обнаруженных фрагментов РНК, предположительно, важны для размножения вируса. Он также нашёл в образцах РНК генетические вариации, которые, вероятно, мешали патогену размножаться.
С помощью генной инженерии лауреат и его группа собрали РНК вируса, содержащую предположительно важные для размножения гены и не содержащую вредных. Эту РНК они ввели в печень обезьян.
Вскоре у подопытных животных развилось воспаление печени, а в крови стала обнаруживаться РНК вируса гепатита C. Так было окончательно доказано, что опасное заболевание вызывается именно этим возбудителем.
Таким образом, каждый из трёх лауреатов внёс важный вклад в открытие. Альтер выяснил, что существует неизвестный вирус гепатита, передающийся через кровь. Хотон обнаружил и исследовал генетический материал вируса, который, предположительно, и вызывал этот недуг. Райс доказал, что найденный Хотоном вирус действительно является возбудителем гепатита.
Хотон обнаружил и исследовал генетический материал вируса, который, предположительно, и вызывал этот недуг. Райс доказал, что найденный Хотоном вирус действительно является возбудителем гепатита.
Открытия лауреатов в дальнейшем позволили создать эффективные тесты на вирус гепатита C. Теперь предотвращая заражение при переливании крови, это тестирование спасает миллионы жизней. А в последние годы появились и эффективные препараты, подавляющие вирус. Это дарит человечеству надежду на полное искоренение опасной болезни.
Источник: https://www.vesti.ru/nauka/article/2467684
Стратегии по борьбе с вирусным гепатитом. ВИЧ и ИППП
C приближением 2030 года и подготовкой мирового сообщества к достижению амбициозного набора целей в области устойчивого развития ВОЗ разрабатывает три глобальные стратегии в области здравоохранения по ВИЧ/СПИДу, вирусному гепатиту и инфекциям, передаваемым половым путем (ИППП).
Эти стратегии охватят период 2016-2021 гг. и были рассмотрены на 69-й сессии Всемирной ассамблеи здравоохранения в 2016 году.
и были рассмотрены на 69-й сессии Всемирной ассамблеи здравоохранения в 2016 году.
Гепатит
Вирусный гепатит представляет серьезную проблему для междуна-родного здравоохранения. Настоящая стратегия является первым документом, который содействует реализации новым Устойчивым целям развития ООН на 2030 год. В стратегии описан вклад сектора здравоохранения в деятельность по ликвидации вирусного гепатита как угрозы общественному здравоохранению.
Проекты глобальных стратегий сектора здравоохранения Вирусный гепатит, 2016–2021 гг.
ВИЧ/СПИД
Международное сообщество обязалось к 2030 году положить конец эпи-демии СПИДа как одной из угроз для общественного здравоохранения — это одна из грандиозных целей Повестки дня в области устойчивого развития на период до 2030 года, принятой Генеральной Ассамблеей ООН в сентябре 2015 года. В настоящем проекте глобальной стратегии описывается вклад сектора здравоохранения в достижение этих целевых показателей. В ней изложены как задачи стран, так и направления действий ВОЗ. Если страны и ВОЗ осуществят эти действия в ускоренном порядке, то они будут способствовать более оперативному и активному принятию мер по борьбе с ВИЧ, направленных на то, чтобы цель «положить конец СПИДу» стала ре-альностью.
В ней изложены как задачи стран, так и направления действий ВОЗ. Если страны и ВОЗ осуществят эти действия в ускоренном порядке, то они будут способствовать более оперативному и активному принятию мер по борьбе с ВИЧ, направленных на то, чтобы цель «положить конец СПИДу» стала ре-альностью.
Проекты глобальных стратегий сектора здравоохранения ВИЧ, 2016–2021 гг.
Инфекции, передаваемые половым путем
В настоящем проекте стратегии для сектора здравоохранения по инфекци-ям, передаваемым половым путём, описывается один из важных компонентов того вклада, который сектор здравоохранения вносит в достижение этих целей. В нём сформулированы действия, которые следует предпринять странам и ВОЗ. Осуществление этих действий позволит ускорить и активизировать принятие мер борьбы с ИППП, направленных на то, чтобы продвижение к искоренению эпидемии ИППП стало реальностью.
Всемирный день борьбы со СПИДом
За период с 2000 года в мире была проделана большая работа по борьбе с ВИЧ-инфекцией во всем мире. Число новых случаев инфицирования снизилось на 35%, а число случаев смерти от СПИДа сократилось на 25%. Однако настало время для более решительных действий и принятия инновационных мер, что позволит положить конец этой эпидемии к 2030 году. Во Всемирный день борьбы со СПИДом, который отмечается каждый год 1 декабря, будут обнародованы новые рекомендации ВОЗ, которые помогут в достижении этих целей.
Число новых случаев инфицирования снизилось на 35%, а число случаев смерти от СПИДа сократилось на 25%. Однако настало время для более решительных действий и принятия инновационных мер, что позволит положить конец этой эпидемии к 2030 году. Во Всемирный день борьбы со СПИДом, который отмечается каждый год 1 декабря, будут обнародованы новые рекомендации ВОЗ, которые помогут в достижении этих целей.
ВИЧ среди потребителей наркотиков
Во всем мире около 16 миллионов людей употребляют инъекционные наркотики и 3 миллиона из них имеют ВИЧ. В среднем, причиной каждой десятой новой ВИЧ-инфекции является употребление инъекционных наркотиков, а в некоторых странах Восточной Европы и Средней Азии более 80% всех ВИЧ-инфекций связаны с употреблением наркотиков. ВОЗ твердо поддерживает уменьшение вреда в качестве основанного на фактических данных подхода к профилактике, лечению и уходу за людьми с ВИЧ, употребляющими инъекционные наркотики, и определила всесторонний пакет мероприятий.
Что такое ВИЧ?
Вирус иммунодефицита человека (ВИЧ) инфицирует клетки иммун-ной системы, разрушая или нарушая ее функции. Инфицирование вирусом приводит к прогрессирующей деградации иммунной системы и, в результате, к «иммунодефициту». Иммунная система считается дефектной тогда, когда она больше не может выполнять свою роль в борьбе с инфекциями и болезнями. Инфекции, связанные с тяжелым иммунодефицитом, известны как «оппортунистические инфекции», так как они «пользуются возможностями» ослабленной иммунной системы.
Инфицирование вирусом приводит к прогрессирующей деградации иммунной системы и, в результате, к «иммунодефициту». Иммунная система считается дефектной тогда, когда она больше не может выполнять свою роль в борьбе с инфекциями и болезнями. Инфекции, связанные с тяжелым иммунодефицитом, известны как «оппортунистические инфекции», так как они «пользуются возможностями» ослабленной иммунной системы.
Что такое СПИД?
Синдром приобретенного иммунодефицита (СПИД) — это термин, применяемый к самым последним стадиям ВИЧ-инфекции. Для него харак-терно появление каких-либо из более чем 20 оппортунистических инфекций или связанных с ВИЧ видов рака.
Как передается ВИЧ?
ВИЧ может передаваться при незащищенном сексуальном контакте (вагинальном или анальном) и оральном сексе с инфицированным челове-ком; при переливании зараженной крови; и при совместном использовании зараженных игл, шприцев или других острых инструментов. Он может также передаваться от матери ребенку во время беременности, родов и грудного вскармливания.
Сколько человек инфицированны ВИЧ?
По оценкам ВОЗ и ЮНЭЙДС, в конце 2014 года в мире насчитыва-лось 36,9 миллиона человек с ВИЧ. В этом же году около 2 миллионов человек приобрели инфекцию, а 1,2 миллиона человек умерли от причин, связанных с ВИЧ.
Как быстро у ВИЧ-инфицированного человека развивается СПИД?
Этот период времени у разных людей варьируется в широких пределах. При отсутствии лечения у большинства ВИЧ-инфицированных людей признаки связанной с ВИЧ болезни появляются в течение 5-10 лет, а, возможно, и раньше. После приобретения ВИЧ-инфекции до диагностирования СПИДа проходит обычно 10-15 лет, а иногда и больше. Антиретровирусная терапия (АРТ) может замедлить развитие болезни путем предотвращения репликации вируса и, следовательно, уменьшения количества вирусов (известного как «вирусная нагрузка») в крови инфицированного человека.
Какая угрожающая жизни оппортунистическая инфекция поражает людей с ВИЧ/СПИДом наиболее часто?
В 2014 году почти 390 тысяч людей с ВИЧ умерли от туберкулеза. Это основная причина смерти среди ВИЧ-инфицированных людей в Африке и одна из основных причин смерти среди этой группы населения во всем мире. Решающее значение для предотвращения и ведения инфекции туберкулеза у людей с ВИЧ имеют следующие основные стратегии здравоохранения:
Это основная причина смерти среди ВИЧ-инфицированных людей в Африке и одна из основных причин смерти среди этой группы населения во всем мире. Решающее значение для предотвращения и ведения инфекции туберкулеза у людей с ВИЧ имеют следующие основные стратегии здравоохранения:
— интенсивное выявление случаев заболевания активным ТБ;
— профилактическое лечение изониазидом;
— борьба с ТБ-инфекцией;
— раннее начало антиретровирусной терапии.
Как можно уменьшить риск передачи ВИЧ при сексуальных контактах?
— при каждом сексуальном контакте правильно использовать мужские или женские презервативы;
-заниматься только непроникающим сексом;
-сохранять верность в отношениях с неинфицированным и равным образом верным партнером и избегать каких-либо других форм рискованного поведения.
Предотвращает ли мужское обрезание от передачи ВИЧ?
Мужское обрезание способствует снижению риска приобретения ВИЧ во время сексуальных контактов между мужчиной и женщиной примерно на 60%. С 2007 года ВОЗ и ЮНЭЙДС рекомендуют проведение добровольного медицинского мужского обрезания в качестве дополнительной стратегии профилактики ВИЧ в условиях высокой распространенности ВИЧ и при низких уровнях мужского обрезания. 14 стран в Восточной и Южной Африке, соответствующих этим критериям, приступили к проведению программ по расширению масштабов мужского обрезания.
С 2007 года ВОЗ и ЮНЭЙДС рекомендуют проведение добровольного медицинского мужского обрезания в качестве дополнительной стратегии профилактики ВИЧ в условиях высокой распространенности ВИЧ и при низких уровнях мужского обрезания. 14 стран в Восточной и Южной Африке, соответствующих этим критериям, приступили к проведению программ по расширению масштабов мужского обрезания.
Одноразовая процедура медицинского мужского обрезания обеспечивает пожизненную частичную защиту от ВИЧ, а также от других инфекций, передаваемых половым путем. Мужское обрезание следует всегда рассматривать в качестве составной части общего пакета мер профилактики ВИЧ, которая ни в коей мере не заменяет другие известные способы профилактики, такие как мужские и женские презервативы.
Насколько эффективны презервативы в профилактике ВИЧ?
При правильном использовании во время каждого сексуального контакта презервативы являются надежным способом профилактики ВИЧ-инфекции у женщин и мужчин. Тем не менее, ни один способ защиты, кроме воздержания, не эффективен на 100%.
Тем не менее, ни один способ защиты, кроме воздержания, не эффективен на 100%.
Что такое женский презерватив?
Женский презерватив является единственным контролируемым жен-щиной контрацептивным барьерным методом, доступным в настоящее время на рынке. Женский презерватив представляет собой прочный, мягкий, прозрачный колпачок из полиуретана, вставляемый во влагалище перед сексуальным контактом. При его правильном использовании при каждом сексуальном контакте он полностью облегает влагалище и обеспечивает защиту, как от беременности, так и от инфекций, передаваемых половым путем, включая ВИЧ.
Каковы преимущества теста на ВИЧ?
Знание своего ВИЧ-статуса дает два важных преимущества:
1) узнав о том, что вы ВИЧ-позитивны, вы можете принять необходимые меры для того, чтобы получить доступ к лечению, уходу и поддержке до того, как появятся симптомы, и, тем самым, потенциально продлить свою жизнь и предотвратить развитие осложнений на протяжении многих лет.
2) узнав о том, что вы инфицированы, вы можете принять меры предосторожности, чтобы не допустить передачи ВИЧ другим людям.
Что такое антиретровирусные препараты?
Антиретровирусные препараты используются при лечении и профилактике ВИЧ-инфекции. Они борются с ВИЧ, останавливая или сдерживая репродукцию вируса и уменьшая его количество в организме.
Каков нынешний статус антиретровирусной терапии (АРТ)?
В середине 2015 года антиретровирусную терапию получали 15,8 миллиона человек во всем мире. До 2003 года высокая стоимость лекарств, слабая или неадекватная инфраструктура здравоохранения и нехватка финансовых средств препятствовали широкому использованию комбинированной антиретровирусной терапии в странах с низким и средним уровнем дохода. Но в последние годы благодаря возросшей политической и финансовой приверженности доступ к лечению был значительно расширен.
Имеется ли лекарство от ВИЧ?
Нет, лекарства от ВИЧ не существует. Но при надлежащем и непре-рывном соблюдении предписаний в отношении антиретровирусной терапии прогрессирование ВИЧ в организме можно замедлить почти до полной остановки. Все больше и больше людей с ВИЧ, даже в странах с низким уровнем дохода, могут сохранять хорошее самочувствие и продуктивность на протяжении длительного времени. ВОЗ рекомендует лечение для всех людей, инфицированных ВИЧ, а также для тех, кто подвергается значительному риску.
Но при надлежащем и непре-рывном соблюдении предписаний в отношении антиретровирусной терапии прогрессирование ВИЧ в организме можно замедлить почти до полной остановки. Все больше и больше людей с ВИЧ, даже в странах с низким уровнем дохода, могут сохранять хорошее самочувствие и продуктивность на протяжении длительного времени. ВОЗ рекомендует лечение для всех людей, инфицированных ВИЧ, а также для тех, кто подвергается значительному риску.
Какие другие виды помощи необходимы людям с ВИЧ?
Помимо антиретровирусной терапии людям с ВИЧ часто необходимо консультирование и психологическая поддержка. Доступ ВИЧ-инфицированных людей к надлежащему питанию, безопасной воде и основным гигиеническим средствам может также способствовать поддержанию высокого качества жизни.
ВИЧ/СПИД
Информационный бюллетень № 360 Июль 2016 г.
Основные факты
ВИЧ остается одной из основных проблем глобального общественного здравоохранения: на сегодняшний день он унес более 34 миллионов человеческих жизней. В 2014 году 1,2 [980000–1,6] миллиона людей в мире умерли от причин, связанных с ВИЧ.
В 2014 году 1,2 [980000–1,6] миллиона людей в мире умерли от причин, связанных с ВИЧ.
В конце 2014 года в мире насчитывалось примерно 36,9 [34,3–41,4] миллионов людей с ВИЧ-инфекцией, а 2 [1,9–2,2] миллиона человек в мире приобрели ВИЧ-инфекцию в 2014 году.
Наиболее пораженным регионом является Африка к югу от Сахары — здесь в 2014 году проживало 25,8 [24,0–28,7] миллиона человек с ВИЧ. На этот регион приходится также почти 70% глобального общего числа новых ВИЧ-инфекций.
ВИЧ-инфекцию часто диагностируют с помощью диагностических экспресс-тестов (ДЭТ), которые выявляют наличие или отсутствие антител к ВИЧ. В большинстве случаев результаты тестов можно получить в тот же день; это важно для постановки диагноза в тот же день и предоставления раннего лечения и ухода.
Лекарства, излечивающего от ВИЧ-инфекции, нет. Однако благодаря эффективному лечению антиретровирусными препаратами (АРВ) вирус можно контролировать и предотвращать его передачу, что позволяет людям с ВИЧ и тем, кто подвергается значительному риску иметь здоровую и продуктивную жизнь.
По оценкам, в настоящее время лишь 53% людей с ВИЧ знают о своем статусе. В 2014 году примерно 150 миллионов детей и взрослых в 129 странах с низким и средним уровнем дохода получили услуги по тестированию ВИЧ.
В 2014 году в глобальных масштабах антиретровирусную терапию (АРТ) получали 15,8 миллиона людей с ВИЧ.
За период с 2000 по 2015 гг. число новых ВИЧ-инфекций уменьши-лось на 35%, уровни смертности, связанной со СПИДом, снизились на 24%, то есть было спасено около 7,8 миллиона человеческих жизней в результате международных усилий, которые привели к выполнению в глобальных масштабах задач по ВИЧ в рамках Целей тысячелетия в области развития.
Расширение масштабов АРТ для охвата всех людей с ВИЧ и расширение выбора вариантов для профилактики может способствовать предотвращению 21 миллиона случаев смерти, связанной со СПИДом, и 28 миллионов новых инфекций к 2030 году.
Вирус иммунодефицита человека (ВИЧ) поражает иммунную систему и ослабляет системы контроля и защиты людей от инфекций и некоторых типов рака. Вирус разрушает и ослабляет функцию иммунных клеток, поэтому у инфицированных людей постепенно развивается иммунодефицит. Иммунная функция обычно измеряется числом клеток CD4. Иммунодефицит приводит к повышенной чувствительности к широкому ряду инфекций и болезней, которым могут противостоять люди со здоровыми иммунными системами. Самой поздней стадией ВИЧ-инфекции является Синдром приобретенного иммунодефицита (СПИД), который у разных людей может развиться через 2-15 лет. Для СПИДа характерно развитие некоторых типов рака, инфекций или других тяжелых клинических проявлений.
Вирус разрушает и ослабляет функцию иммунных клеток, поэтому у инфицированных людей постепенно развивается иммунодефицит. Иммунная функция обычно измеряется числом клеток CD4. Иммунодефицит приводит к повышенной чувствительности к широкому ряду инфекций и болезней, которым могут противостоять люди со здоровыми иммунными системами. Самой поздней стадией ВИЧ-инфекции является Синдром приобретенного иммунодефицита (СПИД), который у разных людей может развиться через 2-15 лет. Для СПИДа характерно развитие некоторых типов рака, инфекций или других тяжелых клинических проявлений.
Признаки и симптомы
Симптомы ВИЧ варьируются в зависимости от стадии инфекции. На протяжении нескольких первых месяцев люди с ВИЧ, как правило, наиболее заразны, но многие из них узнают о своем статусе лишь на более поздних стадиях. На протяжении нескольких первых недель после инфицирования у людей может не появляться никаких симптомов или развиться гриппоподобная болезнь, включая лихорадку, головную боль, сыпь или боль в горле.
По мере того как инфекция постепенно ослабляет иммунную систему, у людей могут развиваться другие признаки и симптомы, такие как опухшие лимфоузлы, потеря веса, лихорадка, диарея и кашель. При отсутствии лечения у них могут развиться такие тяжелые болезни, как туберкулез, криптококковый менингит, такие онкологические заболевания, как лимфомы и саркома Капоши, и другие.
Передача инфекции
ВИЧ может передаваться через разные жидкости организма инфицированных людей, такими как кровь, грудное молоко, семенная жидкость и вагинальные выделения. Люди не могут заразиться при обычных повседневных контактах, таких как поцелуи, объятия и пожатие рук, или при совместном пользовании личными предметами и употреблении продуктов питания или воды.
Факторы риска
Формы поведения и условия, повышающие риск заражения людей ВИЧ, включают следующие:
— незащищенный анальный или вагинальный секс;
— наличие другой инфекции, передаваемой половым путем, такой как сифилис, герпес, хламидиоз, гонорея и бактериальный вагиноз;
— совместное пользование зараженными иглами, шприцами и другим инъекционным оборудованием и растворами наркотиков при употреблении инъекционных наркотиков;
— небезопасные инъекции, переливания крови, медицинские процедуры, включающие нестерильные разрезы или прокалывание;
— случайные травмы от укола иглой, в том числе среди работников здравоохранения.
Диагностирование
Серологические тесты, такие как ДЭТ или иммуноферментный анализ (ИФА), выявляют наличие или отсутствие антител к антигенам ВИЧ-1/2 и/или ВИЧ-p24. Проведение таких тестов в рамках стратегии тестирования в соответствии с утвержденным алгоритмом тестирования позволяет выявлять ВИЧ-инфекцию с высокой степенью точности. Важно отметить, что серологические тесты не выявляют напрямую сам ВИЧ, а обнаруживают антитела, вырабатываемые организмом человека в процессе борьбы его иммунной системы с чужеродными патогенами.
У большинства людей антитела к ВИЧ-1/2 вырабатываются в течение 28 дней, и поэтому на ранней стадии инфекции, в течение так называемого периода серонегативного окна, антитела не выявляются. Этот ранний период инфекции является периодом наибольшей инфекционности, однако передача ВИЧ может происходить на всех стадиях инфекции.
Надлежащей практикой является проведение повторного тестирова-ния всех людей, первоначально диагностированных как ВИЧ-позитивные, до их включения в программы по уходу и/или лечению для исключения каких-либо потенциальных ошибок в тестировании или отчетности.
Тестирование и консультирование
Тестирование на ВИЧ должно быть добровольным, и право на отказ от тестирования должно быть признано. Обязательное или принудительное тестирование по инициативе медицинских работников, органа здравоохранения, партнера или члена семьи не допустимо, так как оно подрывает надлежащую практику общественного здравоохранения и нарушает права человека.
Некоторые страны ввели самотестирование или рассматривают во-прос о его введении в качестве дополнительного варианта. Самотестирование на ВИЧ — это процесс, в ходе которого человек, желающий знать свой ВИЧ-статус, собирает сперму, проводит тест и конфиденциально интерпретирует его результаты. Самотестирование на ВИЧ не позволяет поставить окончательный диагноз; это первоначальный тест, требующий дальнейшего тестирования, проводимого медработником на основе использования национального утвержденного алгоритма тестирования.
Все услуги по тестированию и консультированию должны учитывать пять компонентов, рекомендуемых ВОЗ: информированное согласие, конфиденциальность, консультирование, правильные результаты тестирования и связь со службами по уходу и лечению и другими службами.
Профилактика
Риск ВИЧ-инфицирования можно снизить путем ограничения воздействия факторов риска. Основные подходы к профилактике ВИЧ, используемые часто в сочетании, включают следующие:
1. Использование мужских и женских презервативов
Правильное и постоянное использование мужских и женских презервативов во время вагинального или анального секса может защитить от распространения инфекций, передаваемых половым путем, включая ВИЧ. Фактические данные свидетельствуют о том, что мужские латексные презервативы защищают на 85% или более от передачи ВИЧ и от других инфекций, передаваемых половым путем (ИППП).
2. Услуги по тестирование на ВИЧ и ИППП
Всем людям, подвергающимся воздействию каких-либо факторов риска, настоятельно рекомендуется тестирование на ВИЧ и другие ИППП с тем, чтобы они могли узнать о своем инфекционном статусе и незамедли-тельно получить доступ к необходимым услугам по профилактике и лече-нию. ВОЗ также рекомендует предлагать тестирование партнерам или парам.
ВОЗ также рекомендует предлагать тестирование партнерам или парам.
Туберкулез является самой распространенной болезнью среди людей с ВИЧ. Без выявления и лечения он приводит к смертельному исходу и является основной причиной смерти среди людей с ВИЧ — примерно каждый четвертый случай смерти, связанной с ВИЧ, происходит в результате туберкулеза. Раннее выявление этой инфекции и незамедлительное предоставление противотуберкулезных препаратов и АРТ могут предотвращать эти случаи смерти. Настоятельно рекомендуется включать скрининг на туберкулез в услуги по тестированию на ВИЧ и незамедлительно предоставлять АРТ всем людям, у которых диагностированы ВИЧ и активный туберкулез.
3. Добровольная медицинская мужская циркумцизия
Медицинская мужская циркумцизия (обрезание крайней плоти) в случае ее безопасного проведения специалистами здравоохранения, прошедшими надлежащую подготовку, снижает риск приобретения мужчинами ВИЧ-инфекции при гетеросексуальных контактах примерно на 60%. Это одна из основных мер вмешательства в условиях эпидемий с высокими уровнями распространенности ВИЧ и с низкими показателями мужской циркумцизии.
Это одна из основных мер вмешательства в условиях эпидемий с высокими уровнями распространенности ВИЧ и с низкими показателями мужской циркумцизии.
4. Использование антиретровирусной терапии (АРТ) для профилактики
4.1. Антиретровирусная терапия (АРТ) в качестве профилактики
Испытание, проведенное в 2011 году, показало, что в случае соблюдения ВИЧ-позитивным человеком эффективной схемы АРТ риск передачи вируса его неинфицированному сексуальному партнеру может быть снижен на 96%. Рекомендация ВОЗ в отношении АРТ для всех людей с ВИЧ будет способствовать значительному снижению уровней передачи ВИЧ.
4.2 Предэкспозиционная профилактика (ПрЭП) для ВИЧ-негативного партнера
Пероральная ПрЭП ВИЧ — это ежедневный прием людьми, неинфицированными ВИЧ, АРВ в целях предотвращения ВИЧ-инфицирования. Было проведено более 10 рандомизированных контролируемых исследований, продемонстрировавших эффективность ПрЭП в снижении уровней передачи ВИЧ среди целого ряда групп населения, включая серодискордантные гетеросексуальные пары (пары, в которых один партнер инфицирован, а другой — нет), мужчин, имеющих секс с мужчинами, женщин, изменивших половую принадлежность, гетеросексуальные пары высокого риска и потребителей инъекционных наркотиков.
В сентябре 2015 года ВОЗ опубликовала «Руководство в отношении начала антиретровирусной терапии и предэкспозиционной профилактики ВИЧ», в котором ПрЭП рекомендуется в качестве одного из вариантов профилактики для людей, подвергающихся значительному риску ВИЧ-инфицирования, в качестве составной части комбинированных подходов к профилактике.
4.3 Постэкспозиционная профилактика ВИЧ (ПЭП)
Постэкспозиционная профилактика (ПЭП) — это применение АРВ в течение 72 часов после воздействия ВИЧ для предотвращения инфекции. ПЭП включает консультирование, оказание первой помощи, тестирование на ВИЧ и проведение 28-дневного курса лечения АРВ с последующей медицинской помощью. В новом дополнении, выпущенном в декабре 2014 года, ВОЗ рекомендует проводить ПЭП в случае воздействия как связанного, так и не связанного с работой, а также для взрослых и детей. Новые рекомендации содержат упрощенные схемы приема АРВ, уже используемые для лечения. Осуществление новых руководящих принципов позволит упростить назначение лекарственных препаратов, улучшить соблюдение медицинских предписаний и повысить показатели полного завершения ПЭП для профилактики ВИЧ у людей, случайно подвергшихся воздействию ВИЧ, таких как работники здравоохранения, или у людей, подвергшихся воздействию ВИЧ в результате незащищенного секса или сексуальной агрессии.
5. Уменьшение вреда для потребителей инъекционных наркотиков
Люди, употребляющие инъекционные наркотики, могут соблюдать меры предосторожности для предотвращения ВИЧ-инфекции путем использования стерильного инъекционного оборудования, включая иглы и шприцы, для каждой инъекции. Полный пакет профилактики и лечения ВИЧ включает:
— программы по распространению игл и шприцев,
— опиоидную заместительную терапию для потребителей наркотиков и лечение зависимости от других психоактивных средств на основе фактических данных,
-тестирование и консультирование в отношении ВИЧ,
— лечение и уход при ВИЧ,
-обеспечение доступа к презервативам, и
— ведение ИППП, туберкулеза и вирусного гепатита.
6. Ликвидация передачи ВИЧ-инфекции от матери ребенку
Передача ВИЧ от ВИЧ-позитивной матери ее ребенку во время беременности, схваток, родов или грудного вскармливания называется вертикальной передачей инфекции, или передачей инфекции от матери ребенку (ПИМР). При отсутствии каких-либо мер вмешательства показатели передачи ВИЧ от метарие ребенку варьируются в пределах 15-45%. Такую передачу инфекции можно почти полностью предотвратить при условии, что и мать и ребенок получают АРВ на стадиях, когда может произойти инфицирование.
При отсутствии каких-либо мер вмешательства показатели передачи ВИЧ от метарие ребенку варьируются в пределах 15-45%. Такую передачу инфекции можно почти полностью предотвратить при условии, что и мать и ребенок получают АРВ на стадиях, когда может произойти инфицирование.
ВОЗ рекомендует ряд вариантов предотвращения передачи ВИЧ-инфекции от матери ребенку, которые включают предоставление АРВ матерям и детям во время беременности, родов и в послеродовой период или предложение пожизненного лечения для ВИЧ-позитивных беременных женщин независимо от их числа CD4.
В 2014 году 73% [68–79%] из предположительно 1,5 [1,3-1,6] миллиона беременных женщин с ВИЧ в странах с низким и средним уровнем дохода получали эффективные антиретровирусные препараты для предотвращения передачи инфекции их детям.
Лечение
ВИЧ можно ослаблять с помощью комбинированной антиретровирусной терапии (АРТ), состоящей из трех или более антиретровирусных препаратов (АРВ). АРТ не излечивает ВИЧ-инфекцию, но контролирует репликацию вируса в организме человека и содействует укреплению иммунной системы и восстановлению ее способностей бороться с инфекциями.
В 2015 году ВОЗ выпустила новое «Руководство в отношении начала антиретровирусной терапии и предэкспозиционной профилактики ВИЧ». Согласно его рекомендациям все люди, инфицированные ВИЧ, должны начинать антиретровирусную терапию как можно раньше после постановки диагноза.
К середине 2015 года 15,8 миллиона человек с ВИЧ в мире получали АРТ. К концу 2014 года 40% [37–45%] всех людей с ВИЧ получали АРТ.
С учетом новых рекомендаций ВОЗ в отношении лечения всех людей с ВИЧ и предложения антиретровирусных препаратов в качестве дополнительного варианта профилактики людям, подвергающимся «значительному» риску, число людей, отвечающих критериям антиретровирусной терапии, возрастает с 28 миллионов до 37 миллионов человек. Расширение доступа к лечению является одной из центральных задач, выдвинутых на 2020 год с целью ликвидации эпидемии СПИДа к 2030 году.
10 фактов о ВИЧ/СПИДе
1. ВИЧ (вирус иммунодефицита человека) инфицирует клетки иммунной системы.
Инфекция приводит к прогрессирующему истощению иммунной системы, разрушая способность организма давать отпор некоторым инфекциям и другим болезням. СПИД (синдром приобретенного иммунодефицита) относится к самым поздним стадиям ВИЧ-инфекции, на которых появляются какие-либо из более чем 20 оппортунистических инфекций или характерных для этой болезни раковых заболеваний.
2. ВИЧ передается несколькими путями
ВИЧ может передаваться следующими путями:
— незащищенный секс (вагинальный или анальный) или оральный секс с инфицированным человеком;
— переливание зараженной крови;
— использование зараженных игл, шприцев или других острых инструментов;
— передача от матери ребенку во время беременности, родов и грудного вскармливания.
3. Есть несколько способов предотвращения передачи ВИЧ
Основные способы предотвращения передачи ВИЧ:
— практика безопасного секса с использованием презервативов;
— тестирование и лечение инфекций, передаваемых половым путем, включая ВИЧ;
— воздержание от потребления инъекционных наркотиков или, в случае их потребления, использование всегда новых и одноразовых игл и шприцев;
— обеспечение того, чтобы кровь или продукты крови, которые могут быть необходимыми для вас, были протестированы на ВИЧ.
4. В мире 36,9 миллиона человек инфицированы ВИЧ
В 2014 году 36,9 [34,3–41,4] миллиона человек были инфицированы ВИЧ и 2,6 [2,4–2,8] миллиона из них — дети. По-давляющее большинство людей с ВИЧ живет в странах с низким и средним уровнем дохода. По оценкам, 2 [1,9–2,2] миллиона человек в мире приобрели ВИЧ-инфекцию в 2014 году. На сегодняшний день 34 миллиона человек умерли от причин, связанных с ВИЧ, из них 1,2 миллиона [1,0–1,5] в 2014 году.
5. Комбинированная антиретровирусная терапия (АРТ) предотвращает репликацию ВИЧ в организме
При прекращении репродукции вируса иммунные клетки организма способны жить в течение более длительного времени, обеспечивая защиту организма от инфекций. Если ВИЧ-позитивный партнер в паре получает АРТ, вероятность передачи ВИЧ сексуальным путем ВИЧ-негативному партнеру снижается на 96%.
6. В конце 2015 г. АРТ получали 17,0 миллионов человек в мире
Из них около 15,2 миллиона человек жили в странах с низким и средним уровнем дохода. В сентябре 2015 г. ВОЗ выпустила руководящие принципы, содержащие ключевые рекомендации по «лечению всех» людей с ВИЧ. Они также включают новые рекомендации по доставке услуг в отношении того, как расширить охват лечением ВИЧ для достижения всех людей с ВИЧ. Обеспечение охвата лечением всех людей, отвечающих критериям, остается сложной задачей.
В сентябре 2015 г. ВОЗ выпустила руководящие принципы, содержащие ключевые рекомендации по «лечению всех» людей с ВИЧ. Они также включают новые рекомендации по доставке услуг в отношении того, как расширить охват лечением ВИЧ для достижения всех людей с ВИЧ. Обеспечение охвата лечением всех людей, отвечающих критериям, остается сложной задачей.
7. Тестирование на ВИЧ является важнейшим условием для обеспечения лечения для нуждающихся людей
Для достижения цели по ликвидации СПИДа к 2030 году необхо-димо значительно активизировать усилия по обеспечению доступа к те-стированию на ВИЧ и к лекарственным препаратам. В 2014 году услуги по тестированию на ВИЧ получили примерно 150 миллионов детей и взрослых в 129 странах с низким и средним уровнем дохода. ВОЗ работает над обновлением в 2016 г. своих рекомендаций в отношении услуг по тестированию на ВИЧ на основе изучения таких инновационных подходов, как самотестирование на ВИЧ.
8. По оценкам, 2,6 миллиона детей инфицированы ВИЧ
По данным за 2014 год, большинство из этих детей живет в Африке к югу от Сахары и были инфицированы своими ВИЧ-позитивными матерями во время беременности, родов или грудного вскармливания. Около 220 000 [190 000 – 260 000] тысяч детей были инфицированы ВИЧ в 2013 году.
Около 220 000 [190 000 – 260 000] тысяч детей были инфицированы ВИЧ в 2013 году.
9. Ликвидация передачи ВИЧ от матери ребенку становится достижимой
Во многих странах с низким и средним уровнем дохода доступ к профилактическим мерам остается ограниченным. Но в некоторых областях, таких как предотвращение передачи ВИЧ от матери ребенку и сохранение жизни матерей, достигнут прогресс. В 2014 году антиретровирусные препараты получали немногим более 7 из 10 беременных женщин с ВИЧ, а именно 1 070 000 женщин в мире. В июне 2016 г. ликвидация передачи ВИЧ от матери ребенку была подтверждена еще в трех странах: Армении, Беларуси и Таиланде.
10. ВИЧ является важнейшим фактором риска развития активной формы ТБ
В 2014 г. среди людей с ВИЧ произошло примерно 390 000 случаев смерти от туберкулеза. В том же году предположительно 1,2 миллиона (12%) из 9,6 миллиона человек в мире, у которых развился ТБ, были ВИЧ-позитивными. 74% из предположительного числа ВИЧ-позитивных пациентов с ТБ пришлось на Африканский регион ВОЗ.
Прививки детям. Вакцинация в Кудрово.
В Национальном календаре прививок представлены такие болезни, как гепатит В, туберкулез, дифтерия, столбняк, коклюш, корь, эпидемический паротит. Могут ли дети в современном мире обойтись без вакцин из этого списка?
Вирусный гепатит В (ВГВ)
Прививку против гепатита В применяют во всех цивилизованных странах.
Всемирная организация здравоохранения установила, что приблизительно
2 млрд человек в мире заражены вирусом гепатита В. Это почти каждый третий житель нашей планеты. Число зараженных каждый год возрастает на 350 млн человек. Еще 1 млн ежегодно умирают. В России каждый год регистрируют около 50 тыс. заболевших ВГВ. Таким образом вероятность заражения остается высокой, т.к. переносчиком ВГВ является каждый десятый человек из окружения ребенка.
Туберкулез
Это так называемая социальная болезнь, которая возникает из-за неблагоприятных социально-экономических условий. В большинстве высокоразвитых стран это заболевание встречается очень редко, поэтому прививки от туберкулеза там не делаются. В России же заболеваемость стабильно высокая (120 заболевших на 100000 человек), и предпосылок к ее снижению пока нет.
В большинстве высокоразвитых стран это заболевание встречается очень редко, поэтому прививки от туберкулеза там не делаются. В России же заболеваемость стабильно высокая (120 заболевших на 100000 человек), и предпосылок к ее снижению пока нет.
Туберкулез поражает одного человека из тысячи. В течение года носитель болезни способен заразить 10-15 человек – в автобусе или метро, школе или супермаркете.
Очень опасен туберкулез для детей, которым еще нет года. При заражении, как правило, поражается центральная нервная система непривитых детей. Это приводит к развитию сепсиса и других серьёзных осложнений.
За год регистрируется около 200 осложнений после прививки БЦЖ. Половина из них — регионарные лимфадениты и «бцжиты». Это состояния, которые легко лечатся в амбулаторных условиях и не угрожают жизни.
Прививка от коклюша
Коклюш особенно опасен для малышей в первые три года их жизни. Длительные приступы кашля мешают малышу полноценно дышать, что может вызвать тяжелую гипоксию мозга, остановку дыхания. В такой ситуации помочь можно только в условиях детской реанимации.
В такой ситуации помочь можно только в условиях детской реанимации.
От коклюша лечат 4-6 месяцев. Максимально интенсивный кашель длится от двух недель до двух месяцев. ВОЗ рекомендует прививать от коклюша 3, 4, 5 и 6-месячных малышей. В 18 мес. проводится ревакцинация.
Прививка против дифтерии
Раньше эту болезнь называли «дифтеритом». Когда земский врач ставил такой диагноз, это означало для ребенка неминуемую смерть — либо от удушья из-за отека глотки, либо от осложнений, которые нарушали работу почек и сердца.
В 1990-х гг. многие родители отказывались прививать своих детей. Болезнь вернулась и поразила 120000 человек – взрослых и детей. Из них умерли 6 тысяч. Затем вакцинацию возобновили.
Сейчас дифтерия встречается редко, но поберечься от нее все же стоит. При заражении непривитый ребенок переносит токсическую форму дифтерии. Только экстренная медицинская помощь, зачастую в реанимационном отделении, поможет ему выжить. Если ребенок привит, он переболеет лишь легкой ангиной.
От дифтерии прививают миллионы детей во многих странах. Осложнения составляют всего 10-15 зарегистрированных случаев в год. Это может быть повышение температуры и фебрильные судороги у малышей. Поэтому после прививки необходимо контролировать температуру и своевременно снижать ее.
Прививка против полиомиелита
Это заболевание вызывает вялые параличи, в том числе дыхательной мускулатуры. Заболевший человек не сможет самостоятельно передвигаться, а затем и дышать.
Только вакцинация избавила человечество от полиомелита. Сейчас число привитых людей достаточно высоко, чтобы предотвратить распространение заболевания. Однако территории и социальные группы, где постоянно регистрируется полиомелит, сохраняются до сих пор. Поэтому если перестать прививаться, болезнь вернется.
Осложнения приема вакцины встречаются редко, до 10-15 случаев в год. Инактивированная вакцина, сделанная внутримышечно, почти не вызывает осложнений.
Прививка против столбняка
Вероятность заболеть невысока.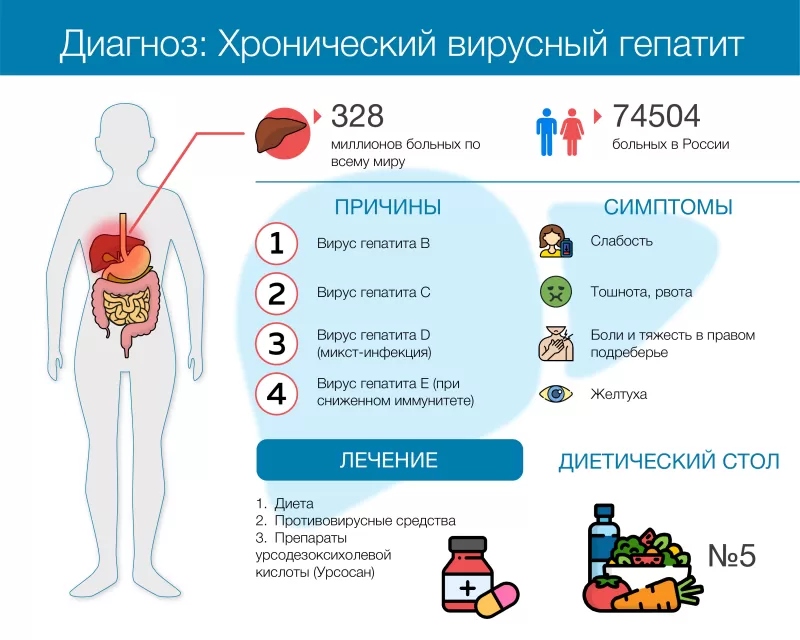 Но если болезнь разовьется, то никакая врачебная помощь не спасет ребенку жизнь и он умрет в мучениях. Родители должны знать, как поступить, если ребенок получил травму или рану, и своевременно обращаться в медицинские учреждения.
Но если болезнь разовьется, то никакая врачебная помощь не спасет ребенку жизнь и он умрет в мучениях. Родители должны знать, как поступить, если ребенок получил травму или рану, и своевременно обращаться в медицинские учреждения.
Прививка от кори, краснухи, паротита
Можно и не ставить вакцину, а переболеть ими в детстве. Однако инфицироваться можно и во взрослом возрасте. Но тогда болезнь будет проходить тяжело и даст осложнения на всю жизнь.
Родители боятся вакцин с самого начала их изобретения. Не подвергайте своих детей огромному риску заболеть инфекционными заболеваниями.
Специалисты «М+clinic» делают прививки детям в СПб, Кудрово и Новом Оккервиле высококачественными вакцинами в рамках Национального календаря прививок от всех вышеперечисленных инфекций.
Туберкулёз
Исследование микобактерии туберкулёза не относится к приоритетным
направлениям ГНЦ ВБ «Вектор», однако работы, начатые в 1999 году, продолжаются и
приносят свои результаты.
Микобактерии туберкулёза были открыты более 100 лет назад, однако до сих пор
эта болезнь остаётся одной из самой серьёзных социальных болезней. В отличие от
многих других опасных инфекций, туберкулёз особенно опасен ещё и тем, что
передаётся воздушно-капельным путём. Более того, на сегодняшний момент
совершенно точно доказано, что для инфицирования микобактериями туберкулёза
совсем не обязательно, чтобы имел место прямой контакт с больным человеком –
инфицирование может произойти, если вы посещаете одни и те же места с больным
туберкулезом – поликлиники, магазины, кинотеатры… Особенно «охотно» туберкулёз
поражает людей с ослабленной иммунной системой.
В 90-е годы в ряде регионов мира, таких как Африка, территория бывшего
Советского Союза, начался стремительный рост числа заболеваний туберкулёзом, но
не просто туберкулёзом, а туберкулёзом с множественной лекарственной
устойчивостью. Что это значит? Микобактериями туберкулеза с множественной
лекарственной устойчивостью называются штаммы, которые устойчивы как минимум к
изониазиду и рифампицину – двум самым мощным противотуберкулезным препаратам.
Противотуберкулёзные препараты делятся на два ряда, или линии. К первой линии
относят четыре препарата рутинного использования, которые назначают для лечения
в первую очередь. Такая комбинация позволяет резко уменьшить вероятность
возникновения мутаций, а значит, позволяет снизить вероятность появление
лекарственно устойчивых вариантов, и в то же время, эти препараты достаточно
доступны, дешёвы и т.д. Но когда оказывается больной, у которого лекарственно
устойчивый туберкулёз, то тогда препараты первого ряда уже не действуют, а
значит, приходится использовать резервные препараты второго ряда. Спектр
антимикробного действия у них шире, по цене они дороже и вызывают больше
побочных эффектов. И, соответственно, если они не помогают, то используют
препараты условно «третьего ряда», но у них спектр противомикробного действия
ещё шире, а это означает, что лечение становится всё менее и менее эффективным
против туберкулёза и начинает воздействовать на всю микрофлору организма. При
При
этом у ряда микобактерий туберкулёза возникает устойчивость не только к двум, а
к трём, четырём антибиотикам и эта проблема стала настолько острой, что в
октябре 2006 г., т.е. совсем недавно, ВОЗ ввела в обращение новый термин –
туберкулёз с широкой лекарственной устойчивостью. Такие формы туберкулеза
устойчивы не только к препаратам первой, но и второй линии, соответственно выбор
схем лечения туберкулеза с широкой лекарственной устойчивостью очень ограничен.
Лекарственно устойчивые штаммы туберкулёза возникают естественным путём в
ходе спонтанного мутагенеза как ответная реакция на введение антибиотиков. Они,
как правило, обладают слабым фитнесом, т.е. они медленнее растут, слабее
размножаются, у них нет других преимуществ, за исключением устойчивости к
антибиотикам. И, соответственно, первоначальная стратегия при столкновении с
лекарственно устойчивыми штаммами заключалась в том, чтобы, во-первых,
антибиотики, направленные на лечение туберкулёза, были изъяты из широкой сети
обращения и использовались только в специализированных учреждениях и, во-вторых,
курс лечения проводился особым образом: сначала больного лечили антибиотиками,
потом делали перерыв, за это время оставшиеся лекарственно чувствительные штаммы
начинали доминировать, соответственно вытесняя лекарственно устойчивые варианты,
затем опять проводили химиотерапию, достигали хороших результатов, что снова
приводило к появлению лекарственно устойчивых штаммов, снова делали перерыв и
так до полного излечения. Но потом оказалось, и обнаружили это, прежде всего в
Но потом оказалось, и обнаружили это, прежде всего в
Африке, что такие проблемы как СПИД, который поражает иммунную систему, приводят
к значительному росту числа лекарственно устойчивых штаммов. Причём если раньше
эти штаммы были в основном в лечебных учреждениях, то теперь они стали
обнаруживаться во всей популяции. И наиболее распространённая на сегодняшний
день теория, для которой находится всё больше и больше подтверждений,
заключается в том, что для того, чтобы лекарственно устойчивые штаммы вырвались
в популяцию, они должны пройти несколько циклов размножения в организме со
слабой иммунной системой, а именно такими объектами являются, прежде всего,
больные СПИДом. Далее обнаружилось, что в странах, где происходят колоссальные
социальные пертурбации, где всё рушится, возникает большая прослойка бедных,
социально дезориентированных людей, у которых доходы ниже прожиточного реального
минимума и иммунная система ослаблена, и такие люди тоже становятся тем
резервуаром, в котором лекарственно устойчивые штаммы могут адаптироваться и
приобрести такие преимущества, которые позволяют им конкурировать с лекарственно
чувствительными штаммами. Таким образом с появлением и распространением СПИДа в
Таким образом с появлением и распространением СПИДа в
мире, а также с началом таких крупных социальных потрясений, как в бывших
странах СНГ, появились две большие зоны, включающие Африку, Азию, страны СНГ,
где лекарственно устойчивые штаммы стали стремительно распространяться.
И тогда первыми забеспокоились международные организации, потому что эпидемия
любого заболевания, в том числе и туберкулёза, в одной стране, является
проблемой многих. В данном случае это было связано и усугублялось миграцией,
поскольку открылись все ворота, люди стали эмигрировать из бывшего Советского
Союза, и в Западной Европе вдруг стали обнаруживать те генотипы туберкулёза,
которые раньше там не регистрировались.
Ситуация ещё более осложнилась после того, как были обнаружены особые штаммы,
у которых очень специально устроен геном и которые мало того, что мутируют, как
и все микобактерии туберкулёза, но ещё и очень быстро адаптируются к новым
условиям. Эти штаммы получили название «пекинские», из-за того, что они впервые
Эти штаммы получили название «пекинские», из-за того, что они впервые
были идентифицированы голландскими учёными в изолятах, полученных от больных в
Пекинском национальном институте здоровья. Потом оказалось, что ареал
распространения этих штаммов очень широк, это не только Китай, но и Монголия, а
также территория бывшего Советского Союза вплоть до Прибалтики, и другие страны
и регионы, вплоть до Америки. Отслеживая эти штаммы, удалось установить пути их
распространения. В частности, в Германии, где ситуация по туберкулёзу очень
благополучная, заболеваемость составляет всего 5 случаев на 100 000 населения, а
медицина нацелена на быстрое выявление, лечение и изучение этого заболевания, на
основании эпидемиологического расследования с использованием
молекулярно-генетических методов были установлены случаи заболевания, источником
которых оказались иммигранты из Казахстана. Таким образом, проблема лекарственно
устойчивого туберкулёза касается не только России, но является международной.
Несмотря на то, что со дня открытия туберкулёза прошло уже больше ста лет,
микобактерия хорошо изучена, известен и расшифрован её геном, но, тем не менее,
мы пока не имеем надёжных средств вакцинации от туберкулёза. Спектр имеющихся
лекарственных препаратов из-за проблемы лекарственной устойчивости приходится
постоянно расширять и модифицировать, и ещё одна большая проблема – это проблема
ранней диагностики туберкулёза.
Кох, открыватель туберкулёза, получивший за это Нобелевскую премию, был
уверен, что можно быстро справиться с этой инфекцией. Но оказалось, что вакцина
Коха защиты не даёт. Тогда появилась другая вакцина, БЦЖ, но она защищает только
детей, а после 14 лет – что её вводи, что ни вводи – защиты нет. Кроме того,
эффективность использования этой вакцины значительно меняется в зависимости от
географического региона. В некоторых странах она обеспечивает высокую защиту
детей – до 80%, а в других – 0%. К этому могли привести очень многие факторы.
К этому могли привести очень многие факторы.
БЦЖ отличается от диких штаммов туберкулёза, у неё отсутствует фрагмент генома,
и соответственно, несколько десятков генов у БЦЖ нет. В каждой стране штаммы для
производства вакцины свои, единого мирового стандарта нет. По утверждениям
специалистов-фтизиатров, наблюдается неуклонный рост осложнений при вакцинации
БЦЖ. В чём причины? Они могут быть разнообразными. Может быть, сам ребёнок и его
состояние, потому что в последнее время возросло число патологий среди
новорождённых. Может быть, вакцинный штамм. Вакцинные штаммы строго контролируют
по всем стандартным микробиологическим параметрам, но эти параметры не позволяют
учитывать генотипические варианты. Так, во Франции на сегодняшний день
идентифицировано не менее четырех штаммов БЦЖ, которые используют для
вакцинации, в России – около двадцати. Поскольку при производстве штамм
контролируется не на генетическом уровне, то не исключено, что на генетическом
уровне могут происходить изменения и некоторые из них могут привести к не очень
хорошим свойствам, которые, в свою очередь, и приводят к осложнениям. Возможно.
Возможно.
Этого никто не проверял. Мы готовы принять участие в таких исследованиях, и мы
могли бы найти те нуклеотидные замены, которые не должны присутствовать в
исходном штамме, и создать устройство, с помощью которого можно было бы
контролировать штаммы в ходе производства. Это позволяло бы проводить более
глубокий независимый внутренний производственный контроль. Это в любом случае
необходимо делать и, безусловно, это будет сделано, потому что любые живые
вакцины требуют такого контроля. Всё в этом мире меняется, хотим мы или нет, это
естественный, неизбежный процесс, возникают мутации, приобретаются какие-то
селективные преимущества, иногда эти селективные преимущества срабатывают в
организме, и это может привести к осложнениям. Такие работы – составление
генетических портретов вакцинных штаммов — необходимы для практического
здравоохранения и весьма интересны с научной точки зрения.
Следующая проблема – диагностика. Для детей это – реакция Манту, для взрослых
Для детей это – реакция Манту, для взрослых
– флюорография или томография. В ходе наших исследований и в ходе общения с
коллегами, мы поняли, что реакция Манту имеет весьма условное диагностическое
значение. Во-первых, реакция Манту не однозначна и существенно зависит от
иммунного статуса человека. Во-вторых, она не всегда обладает высокой
специфичностью и чувствительностью и не может отличить иммунитет, полученный при
вакцинации БЦЖ, от дикой бактерии. Ведь реакция Манту – это суммарные белки от
БЦЖ, и если вы вакцинированы БЦЖ, то они пересекаются с белками, полученными при
прививке, появляется папула, на основании чего возникает подозрение, и надо
проводить исследования дальше, тщательно проверять, что же происходит в
организме. Чувствительность реакции Манту очень высока, а специфичность очень
низкая, по оценкам некоторых специалистов она составляет всего 8-20%. Если же
ещё накладывается коассоциированная инфекция – ВИЧ, или гепатит, или
респираторные заболевания, то это вносит ещё большую путаницу. Поэтому в случае
Поэтому в случае
положительной реакции Манту необходимо провести подтверждающие диагностические
анализы с помощью более совершенных методов. Если же говорить о флюорографии или
результатах томографических исследований, то они выдают уже патологию. Т.е. это,
безусловно, очень нужная, но уже не ранняя диагностика.
«Вектор» никогда не был каким-то микробиологическим центром, и исследования
туберкулёза не были магистральным направлением наших исследований, но, тем не
менее, когда мы этой проблемой занялись, и нас поддержали из разных фондов, в
том числе международных, то нам удалось занять своё, вполне достойное место.
«Вектор» нашёл свою нишу в использовании молекулярно-эпидемиологических методов
для изучения проблемы туберкулёза. И здесь он оказался полезен, потому что на
«Векторе» существовали и существуют кадры, которые в состоянии освоить самые
сложные молекулярно-биологические методики, была внешняя поддержка, и мы
оказались весьма полезными для партнёров, потому что мы могли и умели делать то,
чего не могли сделать они сами. Система фтизиатрической службы подразумевает
Система фтизиатрической службы подразумевает
наличие больниц, стационаров, которые работают по строго утверждённым методикам.
Головными кураторами фтизиатрической службы являются Центральный НИИ туберкулёза
и региональные НИИ туберкулёза, в частности, такой Институт есть и в
Новосибирске. Они обязаны курировать лечебные учреждения, следить за тем, как
они лечат, насколько адекватно утверждённым методикам. Сами они, конечно, тоже
разрабатывают новые схемы лечения. Основные задачи фтизиатрической службы – это
лечение и создание методов лечения, и кооперативное сотрудничество с любыми
учреждениями для изучения самого патогенеза этого заболевания. С молекулярными
биологами фтизиатрическая служба начала сотрудничать в 90-е годы и «Вектор»,
приступивший к этим работам в 1999 году, оказался на высоте.
В то время руководство «Вектора» искало источники внешнего финансирования, а
одним из приоритетных направлений международных фондов, которые финансировали
научные работы в России, был туберкулёз. Начиналось же всё с одного
Начиналось же всё с одного
«провального» дела: необходимо было собрать коллекцию штаммов для того, чтобы на
этих штаммах проверить новые биочиповые технологии – работают они или не
работают, но за это не собирались платить деньги, только материалы – реактивы,
пипетки и т.д., и получилось так, что подвизались на это дело многие, а
исхитрились и выполнили эту работу только мы. Набрали несколько десятков штаммов
и как позже оказалось, это было как раз то, что нужно – ключевые штаммы. Дальше
начались совместные исследования с Институтом молекулярной биологии им.
В.А.Энгельгардта. И тогда возникла тема, которая была энергично поддержана –
использование биочиповой технологии при ранней диагностике лекарственно
устойчивого туберкулёза. Мы оказались в соисполнителях, нам были выделены
средства, благодаря которым лаборатория и пережила наиболее трудные годы. Здесь
нам удалось получить хорошие результаты: мы адаптировали новую биочиповую
технологию к массовому применению. Например, мы научились эти биочипы
Например, мы научились эти биочипы
регенирировать, т.е. использовать несколько (до 7 раз) раз без снижения качества
результата, что снижает стоимость такого чипа почти в 10 раз и делает анализ
доступным для большой сети учреждений.
Далее работы по ранней диагностике были продолжены. На тот момент мы исходили
из того, что любая диагностика должна быть доступна, в том числе и экономически,
быстра и достоверна. Если взять диагностические методы, которые уже были
разработаны – реакция Манту, иммуноферментный анализ (ИФА), ПЦР-анализ, то
однозначного результата они не давали, одни – из-за низкой чувствительности,
другие – из-за низкой специфичности. И мы, что называется, «начали с начала» —
детально проработали литературу, чтобы понять, а что вообще творится в этой
области. И выяснилось, что у микобактерии туберкулёза более 1500 белков, но из
них функционально значимых для практики около 200, а среди этих 200 есть два
белка, всего два(!), которые позволяют достичь и специфичности, и
чувствительности анализа на уровне 96-100%. Но не в традиционных на тот момент
Но не в традиционных на тот момент
технологиях, а в новых – Т-клеточных технологиях. Суть их в следующем: когда в
организм попадает какой-то возбудитель, на него реагируют, прежде всего, именно
Т-клетки иммунной системы, которые в результате сложного взаимодействия образуют
Т-клеточные комплексы. Эти комплексы отличаются от других и могут быть
определены высокоспецифичными методами. И оказалось, что в случае туберкулёза
Т-клеточный комплексы образуется именно с двумя видоспецифическими только для
микобактерий туберкулёза секреторным белками. При этом исключается образование
комплекса с белками каких-либо сопутствующих заболеваний, таких как гепатит или
ВИЧ. Это позволяет на очень ранних стадиях определить, инфицирован человек или
нет, потому что с помощью этого метода можно найти всего одну клетку макрофага,
инфицированную микобактерией туберкулеза, когда ещё цитология и флюорография
чистая, антител тоже нет, а человек уже является инфицированным. И если у вас
И если у вас
обнаруживается 1-5 таких клеток, вы уже должны встать на учёт. И что ещё очень
важно, Т-клеточные технологии различают иммунные ответы на белки, введённые при
вакцинации БЦЖ и белки «диких» штаммов.
Т-клеточные технологии предоставляют практическим врачам и учёным огромные
возможности и могут использоваться для очень широкого применения. Доработка и
сертификация этой технологии потребует финансовой поддержки и времени – 3-4
года. Кроме того, для внедрения Т-клеточных технологий потребуется,
соответствующая приборная база, а эти приборы достаточно дороги (сейчас есть
несколько таких приборов в Москве, а у нас в Сибири один прибор в Институте
иммунологии в Новосибирске и у нас, на «Векторе», т.е. всего два прибора на всей
территории от Урала до Дальнего Востока). Ещё одна особенность Т-клеточных
технологий – для них необходимы живые клетки. Естественно, они требуют и особо
бережного отношения. Т.е. это — новый уровень развития диагностических
это — новый уровень развития диагностических
лабораторий. Однако общемировая тенденция заключается в том, что дорогостоящее
оборудование не может быть доступно каждой больнице. Им оснащаются какие-то
межрегиональные центры. И таким образом, возникает только организационный вопрос
– как быстро и каким образом доставлять образцы в эти центры. В Германии
пациенты, чтобы сдать аналогичный анализ, выезжают за 100-200 км, а это огромное
расстояние по масштабам Германии, либо образец передаётся в специализированный
диагностический центр, потому что далеко не любая клиника «потянет» такое
клиническое оборудование. Отсюда возникает система использования диагностических
методов: с начала используются самые простые и дешёвые методы, далее – более
сложные и дорогостоящие, и, наконец, дело может дойти и до очень специфических и
дорогих технологий, когда надо уже окончательно поставить диагноз или вести
мониторинг за конкретным больным.
В России Т-клеточные технологии пока не внедрены. А в мире эти технологии уже
внедрены в Германии и США, в специализированных крупных центрах, что надо делать
и нам. Там не только есть центры, но действует система иммунологического
мониторинга и система мониторинга генотипов микобактерии туберкулёза. Это
позволяет реально оценивать эффективность всех противотуберкулёзных мероприятий,
позволяет изучать процессы, которые реально происходят с микобактерией
туберкулёза, вовремя выявлять эпидемические очаги, а не работать, как это делали
раньше, по территориям в целом.
Работы по изучению туберкулёза всегда велись учёными «Вектора» в плотном
контакте с фтизиатрической службой. В частности, с Новосибирским НИИ
туберкулёза, зона ответственности которого простирается от Урала и до Дальнего
Востока. Возглавляет его профессор Краснов. У нас готовятся к выходу совместные
публикации, в которых мы оценили эпидемиологическую ситуацию в Новосибирской
области, оценили генетическое разнообразие штаммов микобактерий туберкулёза,
которые здесь циркулируют, попытались изучить взаимосвязи между клиническими
проявлениями и какими-то специальными генетическими структурами или генотипом,
чтобы дать какой-то инструмент для того, чтобы оценить процесс, который
происходит. Аналогичные творческие очень хорошие связи у нас с городским
Аналогичные творческие очень хорошие связи у нас с городским
противотуберкулёзным диспансером. Совместно мы тоже выполнили ряд совместных
исследований, часть из которых была опубликована. Цель работ – изучить
эффективность применения новых технологий для определения лекарственной
устойчивости микобактерий туберкулёза. Не менее интересные работы проводятся у
нас и с Сибирским государственным медицинским университетом.
Осенью 2007 года мы были приглашены для работы в Туберкулёзном кластере.
Туберкулёзный кластер – это российское добровольное сообщество учёных,
работающих над проблемой туберкулёза. Они устраивают меж собой взаимный обмен
информацией, координируют свои усилия и в том числе пытаются лоббировать в
хорошем смысле этого слова интересы своего научного сообщества в государственных
кругах. Пригласили нас, т.к. знали по работам и, кроме того, поступили
рекомендации из разных источников. В работе кластера принимали участие и ведущие
специалисты из Европы, и наиболее сильные группы, занимающиеся изучением
молекулярной эпидемиологии туберкулёза из Центрального НИИ туберкулёза, из
Санкт-Петербурга, Московского института им. Сеченова, СО РАМН. Прошло это в виде
Сеченова, СО РАМН. Прошло это в виде
двухдневной конференции, были представлены результаты по эпидемиологии и
молекулярной иммунологии туберкулёза в Европе по разным странам, по возможным
подходам к поиску вакцинных препаратов, прозвучали доклады москвичей,
санкт-петербуржцев, наш доклад, схлестнулись разные точки зрения по научным
концепциям. Наш доклад вызвал большой интерес и у представителей Европейского
бюро ВОЗ, которые принимали участие в работе кластера. Результатом работы
кластера явилось соглашение, в котором определилась цель его работы, определены
координаторы, в частности, по Новосибирску и Западной Сибири координатором
определён С.И.Татьков, что, несомненно, свидетельствует о высокой оценке работ,
проведённых учёными «Вектора». Ну, а каким будет продолжение работ и будет ли
оно вообще – покажет время.
Систематический обзор и метаанализ
Ethiop J Health Sci. 2019 Янв; 29 (1): 945–956.
, 1 , 2 , 3 и 4
Мейсам Бехзадифар
1 Исследовательский центр гепатита, Лорестанский университет медицинских наук, Хоррамабад, Иран
Сананд Хейдар
Бахрам Хейдар Педиатрическая больница Тегеранского университета медицинских наук, Тегеран, Иран
Масуд Бехзадифар
3 Центр исследований экономики и управления здравоохранением, Иранский университет медицинских наук, Тегеран, Иран
Никола Луиджи Брагацци
4 Школа общественного мнения Здравоохранение, Департамент медицинских наук (DISSAL), Университет Генуи, Генуя, Италия
1 Исследовательский центр гепатита, Лорестанский университет медицинских наук, Хоррамабад, Иран
2 Педиатрическая больница Бахрами, Тегеранский университет медицинских наук, Тегеран, Иран
3 Научно-исследовательский центр управления здравоохранением и экономики, Иранский университет наук, Тегеран, Иран
4 Школа общественного здравоохранения, Департамент медицинских наук (DISSAL), Генуэзский университет, Генуя, Италия
Автор, ответственный за переписку.
Финансирование: Районное бюро здравоохранения Бона и частная клиника Абем.
Конкурирующие интересы: Авторы заявляют, что эта рукопись была одобрена всеми авторами в ее форме и что конкурирующих интересов не существует.
Поступила 28.06.2018; Принято 15 июля 2018 г.
Copyright © 2018 Meysam Behzadifar, B. et al.
Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Эта статья цитируется в других статьях в PMC.
Реферат
Предпосылки
Инфекция вирусом гепатита С (ВГС) увеличивает гепатотоксичность противотуберкулезных препаратов. Целью этого систематического обзора и метаанализа является определение распространенности инфекции ВГС у пациентов с туберкулезом (ТБ).
Методы
Поиск в PubMed / MEDLINE, ISI / Web of Sciences, CINAHL, EMBASE, Кокрановской библиотеке и Scopus проводился с января 2000 г. по март 2018 г.Общая распространенность ВГС у пациентов с туберкулезом была рассчитана с использованием модели случайных эффектов с 95% доверительным интервалом (ДИ). Для оценки неоднородности использовался тест I 2 . Регрессионный тест Эггера был использован для проверки систематической ошибки публикации.
по март 2018 г.Общая распространенность ВГС у пациентов с туберкулезом была рассчитана с использованием модели случайных эффектов с 95% доверительным интервалом (ДИ). Для оценки неоднородности использовался тест I 2 . Регрессионный тест Эггера был использован для проверки систематической ошибки публикации.
Результаты
Двадцать одна статья была выбрана для окончательного анализа на основании критериев включения / исключения. Всего в исследованиях приняли участие 15 542 пациента с туберкулезом. Общая распространенность инфекции HCV у пациентов с ТБ составляла 7% [95% ДИ: 6–9].Анализ подгрупп показал, что диагностический тест (P = 0,0039), географическое происхождение (P = 0,0076) и гендерное распределение (P = 0,0672) были статистически значимыми модераторами. У мужчин риск ВГС был выше, чем у женщин (отношение шансов, OR = 2,02; 95% ДИ: 1,28–3,18).
Заключение
Результаты этого исследования подчеркнули важность скрининга на ВГС у больных ТБ. Информация о том, присутствует ли ВГС у этих пациентов, может помочь в их эффективном лечении.
Информация о том, присутствует ли ВГС у этих пациентов, может помочь в их эффективном лечении.
Ключевые слова: Распространенность, вирус гепатита С, туберкулез, систематический обзор, метаанализ
Введение
Туберкулез (ТБ) признан одной из наиболее важных проблем общественного здравоохранения после синдрома приобретенного иммунодефицита (СПИД), вторая ведущая причина смерти в мире.Ежегодно страны выделяют значительные средства на то, чтобы должным образом справиться с этим заболеванием (1,2). В своем последнем доступном отчете Всемирная организация здравоохранения (ВОЗ) подсчитала, что в 2016 году около 10,4 миллиона человек в мире болели туберкулезом. Самая высокая заболеваемость (45%) была в Юго-Восточной Азии, за которой следовала Африка (25%), Регион Западной части Тихого океана (17%), Регион Восточного Средиземноморья (7%) и Европа и Америка (3%) (3).
Вирус гепатита С (ВГС) — еще одна серьезная проблема здоровья как в развивающихся, так и в развитых странах, которая может вызывать острые и хронические заболевания у людей. Около 1,1% населения мира было инфицировано ВГС: 80 миллионов имели хронический ВГС и 495 тысяч умерли в 2015 году (4,5). Большинство людей, инфицированных ВГС, не знают о своем заболевании, что подвергает их риску цирроза или рака печени (6,7).
Около 1,1% населения мира было инфицировано ВГС: 80 миллионов имели хронический ВГС и 495 тысяч умерли в 2015 году (4,5). Большинство людей, инфицированных ВГС, не знают о своем заболевании, что подвергает их риску цирроза или рака печени (6,7).
Что касается распространенности ВГС у больных туберкулезом и воздействия инфекции на этих пациентов, то во всем мире было проведено мало исследований, и все еще имеется мало доказательств по этой теме (8). Одним из основных клинически значимых побочных эффектов при лечении туберкулеза является гепатотоксичность, которая нарушает процесс лечения и может привести к прекращению лечения пациента (9,10).Гепатотоксичность — один из побочных эффектов краткосрочного курса лечения под непосредственным наблюдением (DOTS), препаратов первой линии, включая рифампицин, пиразинамид и изониазид (11–16). Инфекция ВГС увеличивает гепатотоксичность противотуберкулезных препаратов, и пациенты с ТБ должны быть проверены на ВГС до начала лечения (9).
Целью данного исследования является предоставление подробных сведений о распространенности ВГС у пациентов с ТБ. Мы считаем, что снижение последствий инфекции гепатита С у этих пациентов может быть достижимой целью, если есть точные данные о его распространенности.Целью этого систематического обзора и метаанализа является определение распространенности инфекции ВГС у пациентов с ТБ, чтобы предоставить доказательства для врачей и лиц, ответственных за разработку политики и принятие решений в области здравоохранения.
Мы считаем, что снижение последствий инфекции гепатита С у этих пациентов может быть достижимой целью, если есть точные данные о его распространенности.Целью этого систематического обзора и метаанализа является определение распространенности инфекции ВГС у пациентов с ТБ, чтобы предоставить доказательства для врачей и лиц, ответственных за разработку политики и принятие решений в области здравоохранения.
Материалы и методы
Стратегия поиска для выявления релевантных исследований : Поиск в PubMed / MEDLINE, ISI / Web of Sciences (WoS), CINAHL, EMBASE, в базах данных Cochrane Library и Scopus проводился с января 2000 по март 2018 года. Стратегия поиска был основан на следующей строке ключевых слов: (распространенность ИЛИ частота ИЛИ эпидемиология ИЛИ серологическая распространенность ИЛИ сероэпидемиология ИЛИ доля ИЛИ частота) И (вирус гепатита С ИЛИ ВГС ИЛИ вирусный гепатит ИЛИ вирусный гепатит С) И (туберкулез ИЛИ Mycobacterium tuberculosis OR микобактерии ИЛИ ТБ). Кроме того, списки литературы включенных исследований были просмотрены и просканированы на предмет возможных релевантных исследований.
Кроме того, списки литературы включенных исследований были просмотрены и просканированы на предмет возможных релевантных исследований.
Критерии включения : Исследования включались, если они были эпидемиологическими исследованиями, разработанными как поперечные, продольные исследования или исследования случай-контроль. Они сохранялись, если они изучали распространенность ВГС у пациентов с туберкулезом, были опубликованы на английском языке, имели достаточно данных для расчета распространенности и использовали валидированные стандартизованные диагностические тесты, такие как связанный иммуносорбентный анализ (ELISA), рекомбинантный анализ. иммуноблоттинг (RIBA) или полимеразная цепная реакция (ПЦР) для диагностики HCV.Кроме того, были отобраны исследования, опубликованные с января 2000 г. по март 2018 г.
Критерии исключения : Исследования были исключены, если они были спланированы как клинические испытания с привлечением пациентов с ТБ, которые также были ВИЧ-положительными, содержащие перекрывающиеся данные, или исследования, данные которых не были достаточно подробными для оценки уровня распространенности.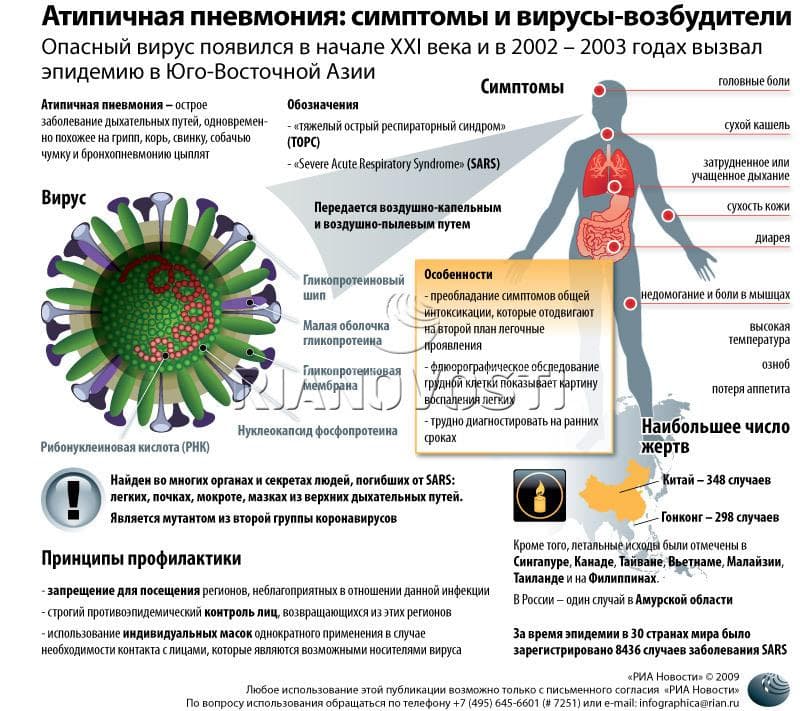
Два исследователя независимо друг от друга проверили названия и аннотации исследований на соответствие критериям отбора. После выбора исследований были просмотрены полные тексты.Если между двумя независимыми исследователями возникали разногласия по поводу выбора исследований, в качестве финального судьи привлекался третий человек, и обсуждение разрешалось. Отбор исследований производился с помощью программы EndNote X8.
Извлечение данных : Из включенных статей мы получили следующую информацию: имя первого автора, год публикации, страна, географическое положение / происхождение в зависимости от континента, на котором проводилось исследование, средний возраст участников, диагностика используемый тест, размер выборки, количество участников ТБ с ВГС, оценки распространенности, тип больных ТБ (страдающих латентным или активным ТБ) и уровень дохода на основе определения Всемирного банка.
Оценка риска: Внутренняя и внешняя валидность, частота ответов и обобщение использовались для оценки результатов исследований с использованием критерия Hoy et al (17). Этот критерий состоит из 10 пунктов, которые оцениваются на основе ответов «Да» и «Нет». За каждый ответ «Да» дается один балл, а за каждый ответ «Нет» присваивается балл. На основании полученных баллов исследования были разделены на три категории. Исследования, получившие от 0 до 4 баллов, относились к группе высокого риска, от 5 до 7 баллов — к умеренному риску и от 8 до 10 — к низкому риску.
Этот критерий состоит из 10 пунктов, которые оцениваются на основе ответов «Да» и «Нет». За каждый ответ «Да» дается один балл, а за каждый ответ «Нет» присваивается балл. На основании полученных баллов исследования были разделены на три категории. Исследования, получившие от 0 до 4 баллов, относились к группе высокого риска, от 5 до 7 баллов — к умеренному риску и от 8 до 10 — к низкому риску.
Статистический анализ : Все данные анализировали с использованием коммерческого программного обеспечения Stata Ver.12 (Stata Corp, College Station, TX, USA). Общая распространенность ВГС у пациентов с туберкулезом была рассчитана с использованием модели случайных эффектов в соответствии с подходом Дер-Симоняна и Лейрда с 95% доверительным интервалом (ДИ) (18). Для оценки неоднородности использовался тест I 2 . Считалось, что значения 25%, 50% и 75% указывают на низкую, умеренную и высокую степень неоднородности соответственно (19).Для обеспечения стабильности результатов был проведен анализ чувствительности. В этом анализе был изучен эффект исключения каждого исследования на раз (20). Затем исследования были ранжированы в соответствии с годом публикации и размером выборки, и был проведен кумулятивный метаанализ для определения влияния этих факторов на распространенность ВГС (21).
В этом анализе был изучен эффект исключения каждого исследования на раз (20). Затем исследования были ранжированы в соответствии с годом публикации и размером выборки, и был проведен кумулятивный метаанализ для определения влияния этих факторов на распространенность ВГС (21).
Для изучения возможных источников неоднородности был проведен анализ подгрупп на основе года публикации исследования, размера выборки, качества исследований, диагностического теста, географического происхождения, уровня дохода (на основе определения Всемирного банка ) и тип ТБ (активный или латентный).
Мета-регрессия также проводилась на основе года публикации исследования. Для проверки систематической ошибки публикации использовался тест Эггера (22). Для оценки эффекта потенциально пропущенных исследований (систематическая ошибка публикации) использовался метод Дюваля и Твиди, размер эффекта которого, возможно, мог повлиять на предполагаемый уровень распространенности ВГС (23).
Коэффициент Каппа Коэна использовался для количественной оценки согласия между исследователями по выбору исследований, извлечению данных и методологической оценке качества (24). Все цифры с двусторонним значением P <0,05 считались статистически значимыми.
Все цифры с двусторонним значением P <0,05 считались статистически значимыми.
Результаты
Выбор исследования : Отчетность по результатам этого систематического обзора и метааналитического исследования проводилась в соответствии с «Предпочтительными элементами отчетности для систематических обзоров и метаанализов» (PRISMA) (25). Процесс отбора этюдов наглядно представлен в.
Блок-схема выбора исследований
В ходе первоначального поиска было найдено 535 исследований из различных научных баз данных.После удаления дубликатов поиски привели к пулу из 354 исследований. После просмотра названия и аннотации исследований осталось 43 исследования. Были рассмотрены полные тексты исследований, и 21 был выбран для окончательного анализа на основе критериев включения / исключения (9,26–45). Согласие между двумя независимыми исследователями при отборе исследований составило 92,17%.
Исследование и характеристики участников : В исследованиях приняли участие 15 542 пациента с ТБ. Семь исследований были проведены в Европе, 6 исследований в Азии, 5 исследований в Америке и 3 исследования в Африке. показаны основные характеристики включенных исследований.
Семь исследований были проведены в Европе, 6 исследований в Азии, 5 исследований в Америке и 3 исследования в Африке. показаны основные характеристики включенных исследований.
Таблица 1
Характеристики включенных исследований
| Первый автор | Год | Страна | Возраст (Среднее ± стандартное отклонение) | Тест | Распространенность | Количество участников | 2006 | Джорджия | 35 | ELISA | 22% | 272 |
| Кунихольм | 2008 | Грузия | NA | ELISA00% | 300 | ||||
| Pando | 2008 | Аргентина | 34,8 ± 14,1 | ELISA | 11,80% | 187 | |||
| Халили | 27,45% | 102 | |||||||
| Хан | 2010 | Великобритания | NA | ELISA | 2,00% | 245 | |||
| NA 2010 9016 9016 9016 9016 9016 9016 9016 10% | 295 | ||||||||
| Ван | 2011 | Тайвань | NA | PCR | 6. 70% 70% | 360 | |||
| Рейс | 2011 | Бразилия | NA | ELISA | 7,50% | 402 | |||
| Badawy | NA | Египет | 135 | ||||||
| Ломтадзе | 2013 | Грузия | 21–92 | ELISA | 21% | 326 | |||
| Ахтар | 2013 | ELISA | 9,10% | 110 | |||||
| Beasley | 2013 | Великобритания | NA | ELISA | NA | 192 | 3,80% | 2296 | |
| Potter | 2014 | Великобритания | 37,7 ± 15,3 | ELISA | 2,00% | 302 | 9016 ELISA | 3. 60% 60% | 1421 |
| Agha | 2015 | Египет | NA | PCR | 17.02% | 94 | |||
| Ahmadi Nooredinv16 16 | % | 429 | |||||||
| Абдаллах | 2015 | Судан | 36,03 ± 13,3 | ELISA | 1% | 98 | |||
| Bushnell 20116 9016 | 4. На 20% На 20% | 20% | 138 |
Риск систематической ошибки в исследованиях : После обзора статей 12 (57,14%) из них были признаны группой низкого риска, 6 (28,57%) имели умеренный риск и 3 (14 .29%) относились к группе высокого риска. Согласие между двумя независимыми исследователями по оценке риска составило 84,26%.
Общая распространенность ВГС у больных ТБ : Распространенность ВГС у больных ТБ составляла от 2% до 27%. На основе модели случайных эффектов общая распространенность составила 7% [95% ДИ: 6–9]. Гетерогенность между исследованиями была высокой (I = 94,2%; P <0,0001) ().
Распространенность ВГС у больных ТБ с 95% доверительным интервалом для каждого включенного исследования
Результаты анализа подгрупп : Уровни распространенности на основе диагностического теста, размера выборки, географического фона, оценки риска исследования и пола исследователя. участники показаны в.
участники показаны в.
Таблица 2
Анализ подгрупп распространенности ВГС у больных ТБ. Сокращения: нс (статистически не значимо)
| Переменные | Количество исследований | Количество участников | Объединенная распространенность (95% ДИ) | Значение неоднородности 181 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| I 2 (%) | Значение P | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Диагностический тест | 7 0168 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ELISA | 18 | 14950 | 7% (5–8) | 94,3% | <0,0001 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCR | 167 3 | 3 | 88,4% | <0,0001 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Размер выборки | <0,0001 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 6–9) | 93. 1% 1% | <0,0001 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| > 250 | 11 | 14027 | 7% (5–9) | 95,2% | <0,0001 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Африка | 3 | 327 | 11% (1–23) | 93. 9% 9% | 3377 | 7% (4–11) | 94.6% | <0,0001 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Америка | 5 | 9772 | 7% (4–10) | 93,5% | <0,0001 | 9% (4–13) | 96,0% | <0,0001 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Риск смещения | 13742 | 9% (7–11) | 95. 5% 5% | <0,0001 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Умеренный | 6 | 1061 | 9% (4–13) | 94,3% | <0,0001 | высокий | 2% (1–3) | 0,0% | нс | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Пол | 0,0672 | 94. 1% 1% | <0,0001 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Женский | 8 | 3838 | 3% (1–4) | 74,0% | <0,0001 | <0,0001 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Нижнее среднее | 7 | 1335 | 14% (6–21) | 95,3% | <0,00016 | верхнее 6 | 3339 | 9% (6–13) | 95. 6% 6% | <0,0001 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Высокий | 8 | 10868 | 3% (2–4) | 81,3% | <0,0001 | TB Тип | TB | <0,0001 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Активный | 18 | 14676 | 9% (7–10) | 95,0% | <0,00016 | 3 | 866 | 2% (1–3) | 0.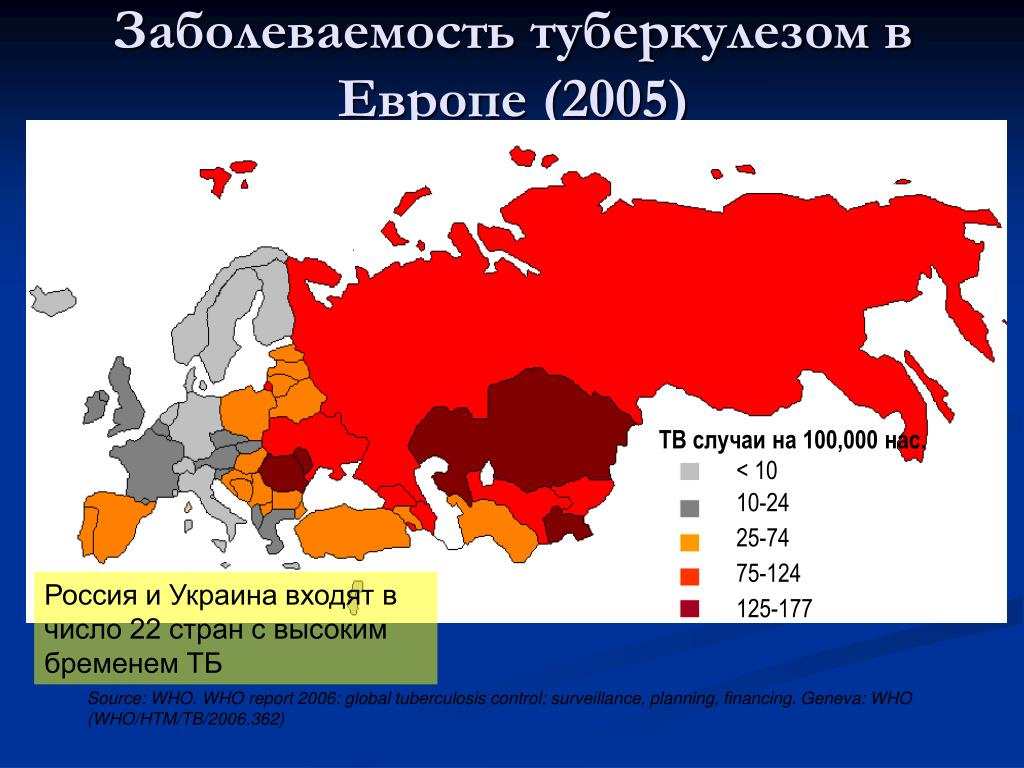 0% 0% | нс | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Диагностический тест : ELISA-тесты использовались для выявления ВГС в 13 исследованиях с распространенностью 7% [95% ДИ: 5–8]. ПЦР-тесты проводились в 3 исследованиях с распространенностью 14% [95% ДИ: 23–23]. Эта разница была статистически значимой (P = 0,0039).
Размер выборки : Расчетная распространенность в исследованиях с размером выборки не более 250 участников была выше (9% [95% ДИ: 6–9]) по сравнению с исследованиями с размером выборки более 250 ( 7% [95% ДИ: 5–9]).Однако эта разница не была статистически значимой.
Географический фон : Самая высокая распространенность была обнаружена в Африке (11% [95% ДИ: 1-23]), затем следуют Европа (9% [95% ДИ: 4-13]), Америка (7% [ 95% ДИ: 4–10]) и Азии (7% [95% ДИ: 4–11]). Эта разница была статистически значимой (P = 0,0076).
Риск систематической ошибки : Распространенность, стратифицированная в соответствии с риском систематической ошибки, составила 9% [95% ДИ: 11–7] в 12 исследованиях с низким риском систематической ошибки, 9% [95% ДИ: 13–4] в 6 исследований с умеренным риском и 2% [95% ДИ: 1–3] в исследованиях с высоким риском. Эти различия не были значительными.
Эти различия не были значительными.
Распространенность ВГС и пол : Данные о распространенности ВГС у мужчин с туберкулезом были получены из 8 исследований (10% [95% ДИ: 14–16]) и у женщин из других 8 исследований (2% [95% ДИ : 1–4]). Это различие было статистически значимым (P = 0,0672). Этот результат показал, что у мужчин риск ВГС выше, чем у женщин (отношение шансов, OR = 2,02 [95% ДИ: 1,28–3,18]) ().
Мета-анализ отношения шансов (ОШ) распространенности ВГС у пациентов мужского пола по сравнению с женщинами
Уровень дохода : Распространенность ВГС при ТБ составляла 14% [95% ДИ: 6– 21] в странах с уровнем дохода ниже среднего, 9% [95% ДИ: 6–13] в контексте дохода выше среднего и 3% [95% ДИ: 2–4] в странах с высоким уровнем дохода.
Тип ТБ : Распространенность составила 9% [95% ДИ: 7–10] в исследованиях с активными пациентами ТБ и 2% [95% ДИ: 1-3] в исследованиях с пациентами с активным или латентным ТБ.
Мета-регрессия : Распространенность ВГС у больных ТБ оценивалась на основе опубликованных лет, и наблюдались значительные изменения (P = 0,049).
Анализ чувствительности : Путем исключения каждого исследования оценивалось его влияние на общий уровень распространенности, и анализ чувствительности показал, что результаты до и после не изменились существенно, что указывает на стабильность результатов.
Кумулятивный метаанализ : Кумулятивный метаанализ был проведен путем сортировки исследований на основе года публикации и размера выборки. Когда исследования были отсортированы по году публикации, их 95% доверительный интервал за годы выпуска исследования показал увеличение частоты ВГС у больных ТБ. Кроме того, когда исследования были отсортированы по размеру выборки, 95% доверительный интервал показал снижение частоты ВГС у больных туберкулезом.
Смещение публикации : Смещение публикации было вычислено с помощью регрессионного теста Эггера, и результаты указывают на смещение в опубликованных исследованиях (P = 0. 000). Из-за этой систематической ошибки был проведен тест «Обрезать и заполнить», в результате которого было обнаружено 7 подвергнутых цензуре исследований и их возможное влияние на уровень распространенности.
000). Из-за этой систематической ошибки был проведен тест «Обрезать и заполнить», в результате которого было обнаружено 7 подвергнутых цензуре исследований и их возможное влияние на уровень распространенности.
Факторы риска ВГС при ТБ : Некоторые избранные исследования выявили факторы риска ВГС у больных ТБ. К этим факторам риска относятся: история инфекций, передаваемых половым путем (ИППП), татуировки и пирсинг, история тюремных или исправительных служб, история употребления инъекционных наркотиков (ПИН), история хирургии, переливание крови, стоматологические услуги, курение, употребление алкоголя, семейный анамнез гепатита С, использование чужих личных вещей и бездомность.
Обсуждение
Насколько нам известно, это исследование является первым метаанализом, который всесторонне рассматривает распространенность ВГС у больных ТБ во всем мире. Всего было отобрано 21 исследование с использованием комплексной стратегии поиска в проверенных базах данных. Анализ чувствительности подтвердил, что результаты были стабильными. Кумулятивный метаанализ, основанный на году публикации, выявил снижение частоты ВГС.
Анализ чувствительности подтвердил, что результаты были стабильными. Кумулятивный метаанализ, основанный на году публикации, выявил снижение частоты ВГС.
Согласно некоторым литературным исследованиям, распространенность ВГС у больных ТБ, о которой сообщалось в этом исследовании, была выше, чем частота ВГС у ВИЧ-положительных пациентов (46,47).Кроме того, согласно недавнему метааналитическому исследованию, распространенность в этом исследовании выше, чем заболеваемость ВГС среди населения в целом (48). С другой стороны, по сравнению с пациентами, находящимися на гемодиализе, было обнаружено, что распространенность ВГС у больных ТБ ниже (49).
Постоянно растущий уровень распространенности туберкулеза во всем мире побудил ВОЗ предложить подход, основанный на DOTS. Эта стратегия, предусматривающая лечение пациентов в течение 6 месяцев, является наиболее эффективным, практичным и правильным способом лечения заболевания (50,51).
Оценки гепатотоксичности, вызванной рифампицином, изониазидом и пиразамидом, трудно вычислить из-за различий между пациентами с точки зрения физических и психологических характеристик. Хронические заболевания печени, такие как вирусные инфекции, могут усиливать гепатотоксичность (52–54). У больных ТБ с гепатитом С риск гепатотоксичности выше, чем у больных ТБ, не страдающих гепатитом С (11,55). Исследования показывают, что инфекция ВГС у больных ТБ может вызвать значительное изменение количества T CD4 + лимфоцитов (56–58).У больных туберкулезом уровень ВГС увеличивает концентрацию ферментов печени. Однако до сих пор нет четкой связи между гепатитом С и повышенным риском гепатотоксичности (56–58).
Хронические заболевания печени, такие как вирусные инфекции, могут усиливать гепатотоксичность (52–54). У больных ТБ с гепатитом С риск гепатотоксичности выше, чем у больных ТБ, не страдающих гепатитом С (11,55). Исследования показывают, что инфекция ВГС у больных ТБ может вызвать значительное изменение количества T CD4 + лимфоцитов (56–58).У больных туберкулезом уровень ВГС увеличивает концентрацию ферментов печени. Однако до сих пор нет четкой связи между гепатитом С и повышенным риском гепатотоксичности (56–58).
Наши результаты показали, что заявленная распространенность значительно различалась в зависимости от используемых диагностических тестов: из-за географического фона самая высокая распространенность ВГС среди больных ТБ наблюдалась в африканских странах. Состояние здоровья в странах играет важную роль в распространении различных заболеваний, включая ВГС и ТБ.Общественное здравоохранение и службы здравоохранения имеют проблемы с реализацией программ, которые сильно влияют на распространенность инфекционных заболеваний в этих странах.
Во многих странах, включая развивающиеся, многие должностные лица общественного здравоохранения не осведомлены о влиянии инфекционных заболеваний и, к сожалению, не обеспечивают надлежащих условий для обследования и оказания медицинской помощи (63). В предыдущих исследованиях было мало информации о различиях между социальным, медицинским, культурным и экономическим происхождением.Эти различия следует отметить в будущих исследованиях.
Результаты этого исследования показали, что распространенность ВГС у мужчин, больных ТБ, была выше, чем у женщин (ОР = 1,89). В исследованиях о поведении высокого риска сообщалось больше у мужчин, чем у женщин, что делало их более подверженными риску заражения ВГС. Некоторые исследования показали, что такие формы поведения, как употребление инъекционных наркотиков, использование обычных шприцев, татуировок, пирсинг и употребление алкоголя, были выше у мужчин, чем у женщин, и, следовательно, уровень распространенности ВГС был выше (64, 65).![]()
Мета-регрессия в зависимости от года публикации исследований указала на снижение частоты ВГС у больных ТБ. Это может быть связано с несколькими факторами. За последние десятилетия улучшились условия здоровья и более широкий доступ к услугам здравоохранения во всем мире для профилактики и борьбы с ВГС. Скрининг и обучение групп высокого риска (потребители наркотиков, заключенные) и особых групп населения системой здравоохранения в различных странах также значительно и положительно повлияли на контроль и лечение инфекционных заболеваний (66).
Факторы риска ВГС у больных ТБ, о которых сообщалось в отдельных исследованиях, являются одними из наиболее признанных факторов риска, упомянутых в различных исследованиях в мире. Лица, принимающие решения и политики в области здравоохранения, а также поставщики первичной медико-санитарной помощи должны внедрять специальные программы для людей из группы риска. Внимание к этим людям значительно снижает распространенность заболевания (67–69).
Однако, несмотря на некоторые сильные стороны, включая новизну и широкую и всеобъемлющую стратегию поиска, это исследование имеет следующие ограничения:
Из-за методологического разнообразия исследований в этом метаанализе существует значительная неоднородность, что может повлиять на результаты и их обобщение.
Во многих частях мира не проводились исследования, которые могли бы повлиять на общий оценочный уровень распространенности ВГС у больных ТБ.
Диагностические тесты, используемые в исследованиях, гендерный и географический контекст в качестве потенциальных источников неоднородности и систематической ошибки, наблюдаемой в исследованиях, позволяют интерпретировать результаты с осторожностью.
Принимая во внимание вышеупомянутые недостатки, результаты этого исследования подчеркнули важность проведения скрининга на ВГС у больных туберкулезом.Информация о том, присутствует ли ВГС у этих пациентов, может помочь в их эффективном лечении. Лица, принимающие решения в сфере здравоохранения, и директивные органы должны реализовать специальных мер для просвещения и скрининга групп с высоким риском развития ВГС и ТБ.
Лица, принимающие решения в сфере здравоохранения, и директивные органы должны реализовать специальных мер для просвещения и скрининга групп с высоким риском развития ВГС и ТБ.
Благодарности
Мы благодарны доктору Хоми Разави и доктору Бехзаду Хаджаризаде за их комментарии и советы по более ранним версиям этой статьи.
Ссылки
1. Kizza FN, List J, Nkwata AK, Okwera A, Ezeamama AE, Whalen CC, et al.Распространенность латентной инфекции туберкулеза и связанные с ней факторы риска в городских условиях Африки. BMC Infect Dis. 2015; 15: 165. [Бесплатная статья PMC] [PubMed] [Google Scholar] 2. Шарма А., Хилл А., Курбатова Е., Ван дер Вальт М., Квасновский С., Тупаси Т.Э. и др. Оценка будущего бремени туберкулеза с множественной и широкой лекарственной устойчивостью в Индии, на Филиппинах, в России и Южной Африке: исследование с математическим моделированием. Lancet Infect Dis. 2017; 17 (7): 707–715. [Бесплатная статья PMC] [PubMed] [Google Scholar] 4. Stanaway JD, Flaxman AD, Naghavi M, Fitzmaurice C, Vos T., Abubakar I, et al. Глобальное бремя вирусного гепатита с 1990 по 2013 год: результаты исследования глобального бремени болезней, 2013 год. Lancet. 2016; 388 (10049): 1081–1088. [Бесплатная статья PMC] [PubMed] [Google Scholar] 5. Гауэр Э., Эстес С., Блах С., Разави-Ширер К., Разави Х. Глобальная эпидемиология и распределение генотипов инфекции вируса гепатита С. J Hepatol. 2014; 61 (1 приложение): S45 – S57. [PubMed] [Google Scholar] 6. Рантала М., ван де Лаар М.Дж. Эпиднадзор и эпидемиология гепатитов B и C в Европе — обзор.Euro Surveill. 2008; 13 (21): 18880. [PubMed] [Google Scholar] 7. Мессина Дж. П., Хамфрис И., Флаксман А., Браун А., Кук Г. С., Пибус О. Г. и др. Глобальное распространение и распространенность генотипов вируса гепатита С. Гепатология. 2015; 61 (1): 77–87. [Бесплатная статья PMC] [PubMed] [Google Scholar] 8. Lorent N, Sebatunzi O, Mukeshimana G, Van den Ende J, Clerinx J. Частота и факторы риска серьезных побочных эффектов во время противотуберкулезного лечения в Руанде: проспективное когортное исследование.
Stanaway JD, Flaxman AD, Naghavi M, Fitzmaurice C, Vos T., Abubakar I, et al. Глобальное бремя вирусного гепатита с 1990 по 2013 год: результаты исследования глобального бремени болезней, 2013 год. Lancet. 2016; 388 (10049): 1081–1088. [Бесплатная статья PMC] [PubMed] [Google Scholar] 5. Гауэр Э., Эстес С., Блах С., Разави-Ширер К., Разави Х. Глобальная эпидемиология и распределение генотипов инфекции вируса гепатита С. J Hepatol. 2014; 61 (1 приложение): S45 – S57. [PubMed] [Google Scholar] 6. Рантала М., ван де Лаар М.Дж. Эпиднадзор и эпидемиология гепатитов B и C в Европе — обзор.Euro Surveill. 2008; 13 (21): 18880. [PubMed] [Google Scholar] 7. Мессина Дж. П., Хамфрис И., Флаксман А., Браун А., Кук Г. С., Пибус О. Г. и др. Глобальное распространение и распространенность генотипов вируса гепатита С. Гепатология. 2015; 61 (1): 77–87. [Бесплатная статья PMC] [PubMed] [Google Scholar] 8. Lorent N, Sebatunzi O, Mukeshimana G, Van den Ende J, Clerinx J. Частота и факторы риска серьезных побочных эффектов во время противотуберкулезного лечения в Руанде: проспективное когортное исследование. PLoS One. 2011; 6 (5): e19566. [Бесплатная статья PMC] [PubMed] [Google Scholar] 9.Бушнелл Г., Стеннис Н.Л., Дробник А.М., Пропс Д.К., Ахуджа С.Д., Борншлегель К. и др. Характеристики и исходы лечения туберкулеза у больных туберкулезом с вирусным гепатитом, Нью-Йорк, 2000–2010 гг. Epidemiol Infect. 2015; 143 (9): 1972–1981. [PubMed] [Google Scholar] 10. Ким В.С., Ли С.С., Ли С.М., Ким Х.Дж., Ха СиЙ, Ким Х.Дж. и др. Гепатит С, а не вирус гепатита В, является фактором риска поражения печени, вызванного противотуберкулезными препаратами. BMC Infect Dis. 2016; 16:50. [Бесплатная статья PMC] [PubMed] [Google Scholar] 11. Ю WW, Leung CC.Противотуберкулезные препараты и гепатотоксичность. Респирология. 2006. 11 (6): 699–707. [PubMed] [Google Scholar] 12. Schechter M, Zajdenverg R, Falco G, Barnes GL, Faulhaber JC, Coberly JS и др. Еженедельное введение рифапентина / изониазида или ежедневного приема рифампицина / пиразинамида при латентном туберкулезе среди домашних контактов. Am J Respir Crit Care Med.
PLoS One. 2011; 6 (5): e19566. [Бесплатная статья PMC] [PubMed] [Google Scholar] 9.Бушнелл Г., Стеннис Н.Л., Дробник А.М., Пропс Д.К., Ахуджа С.Д., Борншлегель К. и др. Характеристики и исходы лечения туберкулеза у больных туберкулезом с вирусным гепатитом, Нью-Йорк, 2000–2010 гг. Epidemiol Infect. 2015; 143 (9): 1972–1981. [PubMed] [Google Scholar] 10. Ким В.С., Ли С.С., Ли С.М., Ким Х.Дж., Ха СиЙ, Ким Х.Дж. и др. Гепатит С, а не вирус гепатита В, является фактором риска поражения печени, вызванного противотуберкулезными препаратами. BMC Infect Dis. 2016; 16:50. [Бесплатная статья PMC] [PubMed] [Google Scholar] 11. Ю WW, Leung CC.Противотуберкулезные препараты и гепатотоксичность. Респирология. 2006. 11 (6): 699–707. [PubMed] [Google Scholar] 12. Schechter M, Zajdenverg R, Falco G, Barnes GL, Faulhaber JC, Coberly JS и др. Еженедельное введение рифапентина / изониазида или ежедневного приема рифампицина / пиразинамида при латентном туберкулезе среди домашних контактов. Am J Respir Crit Care Med.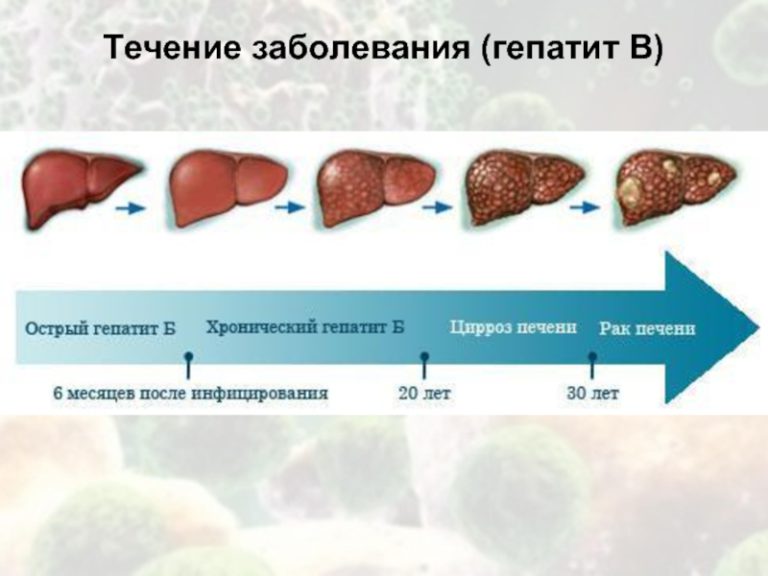 2006. 173 (8): 922–926. [Бесплатная статья PMC] [PubMed] [Google Scholar] 13. Дай С. Глобальная эпидемиология туберкулеза. Ланцет. 2006. 367 (9514): 938–940. [PubMed] [Google Scholar] 14. Кунимото Д., Варман А., Бекон А., Деринг Д., Меленка Л.Тяжелая гепатотоксичность, связанная с профилактической терапией рифампицином-пиразинамидом, требующей трансплантации, у человека с низким риском гепатотоксичности. Clin Infect Dis. 2003; 36 (12): e158 – e161. [PubMed] [Google Scholar] 15. ван Хест Р., Баарс Х., Кик С., ван Гервен П., Тромпенаарс М.С., Калисваарт Н. и др. Гепатотоксичность профилактической терапии рифампицином-пиразинамидом и изониазидом и лечения туберкулеза. Clin Infect Dis. 2004. 39 (4): 488–496. [PubMed] [Google Scholar] 16. Забудьте EJ, Menzies D. Побочные реакции на противотуберкулезные препараты первого ряда.Экспертное мнение Drug Saf. 2006. 5 (2): 231–249. [PubMed] [Google Scholar] 17. Хой Д., Брукс П., Вульф А., Блит Ф., Марч Л., Бейн С. и др. Оценка риска систематической ошибки в исследованиях распространенности: модификация существующего инструмента и свидетельство согласия между экспертами.
2006. 173 (8): 922–926. [Бесплатная статья PMC] [PubMed] [Google Scholar] 13. Дай С. Глобальная эпидемиология туберкулеза. Ланцет. 2006. 367 (9514): 938–940. [PubMed] [Google Scholar] 14. Кунимото Д., Варман А., Бекон А., Деринг Д., Меленка Л.Тяжелая гепатотоксичность, связанная с профилактической терапией рифампицином-пиразинамидом, требующей трансплантации, у человека с низким риском гепатотоксичности. Clin Infect Dis. 2003; 36 (12): e158 – e161. [PubMed] [Google Scholar] 15. ван Хест Р., Баарс Х., Кик С., ван Гервен П., Тромпенаарс М.С., Калисваарт Н. и др. Гепатотоксичность профилактической терапии рифампицином-пиразинамидом и изониазидом и лечения туберкулеза. Clin Infect Dis. 2004. 39 (4): 488–496. [PubMed] [Google Scholar] 16. Забудьте EJ, Menzies D. Побочные реакции на противотуберкулезные препараты первого ряда.Экспертное мнение Drug Saf. 2006. 5 (2): 231–249. [PubMed] [Google Scholar] 17. Хой Д., Брукс П., Вульф А., Блит Ф., Марч Л., Бейн С. и др. Оценка риска систематической ошибки в исследованиях распространенности: модификация существующего инструмента и свидетельство согласия между экспертами. J Clin Epidemiol. 2012; 65 (9): 934–939. [PubMed] [Google Scholar] 18. DerSimonian R, Laird N. Мета-анализ в клинических испытаниях. Контрольные клинические испытания. 1986. 7 (3): 177–188. [PubMed] [Google Scholar] 19. Хиггинс Дж. П., Томпсон С. Г.. Количественная оценка неоднородности в метаанализе.Stat Med. 2002. 21 (11): 1539–1558. [PubMed] [Google Scholar] 20. Thakkinstian A, McElduff P, D’Este C, Duffy D, Attia J. Метод мета-анализа исследований молекулярных ассоциаций. Stat Med. 2005. 24 (9): 1291–1306. [PubMed] [Google Scholar] 21. Маллен Б., Мюллерлейле П., Брайант Б. Кумулятивный мета-анализ: рассмотрение показателей достаточности и стабильности. Pers Soc Psychol Bull. 2001. 27 (11): 1450–1462. [Google Scholar] 22. Эггер М., Дэйви Смит Г., Шнайдер М., Миндер С. Смещение в метаанализе обнаруживается с помощью простого графического теста.BMJ. 1997. 315 (7109): 629–634. [Бесплатная статья PMC] [PubMed] [Google Scholar] 23. Дюваль С., Твиди Р. Обрезать и заполнить: простой метод тестирования и корректировки с учетом систематической ошибки публикации в метаанализе, основанный на графике воронки.
J Clin Epidemiol. 2012; 65 (9): 934–939. [PubMed] [Google Scholar] 18. DerSimonian R, Laird N. Мета-анализ в клинических испытаниях. Контрольные клинические испытания. 1986. 7 (3): 177–188. [PubMed] [Google Scholar] 19. Хиггинс Дж. П., Томпсон С. Г.. Количественная оценка неоднородности в метаанализе.Stat Med. 2002. 21 (11): 1539–1558. [PubMed] [Google Scholar] 20. Thakkinstian A, McElduff P, D’Este C, Duffy D, Attia J. Метод мета-анализа исследований молекулярных ассоциаций. Stat Med. 2005. 24 (9): 1291–1306. [PubMed] [Google Scholar] 21. Маллен Б., Мюллерлейле П., Брайант Б. Кумулятивный мета-анализ: рассмотрение показателей достаточности и стабильности. Pers Soc Psychol Bull. 2001. 27 (11): 1450–1462. [Google Scholar] 22. Эггер М., Дэйви Смит Г., Шнайдер М., Миндер С. Смещение в метаанализе обнаруживается с помощью простого графического теста.BMJ. 1997. 315 (7109): 629–634. [Бесплатная статья PMC] [PubMed] [Google Scholar] 23. Дюваль С., Твиди Р. Обрезать и заполнить: простой метод тестирования и корректировки с учетом систематической ошибки публикации в метаанализе, основанный на графике воронки. Биометрия. 2000. 56 (2): 455–463. [PubMed] [Google Scholar] 24. Вьера AJ, Гарретт JM. Понимание соглашения между наблюдателями: статистика каппа. Fam Med. 2005. 37 (3): 360–363. [PubMed] [Google Scholar] 25. Либерати А., Альтман Д.Г., Тецлафф Дж., Малроу С., Готше П.С., Иоаннидис Дж. П. и др. Заявление PRISMA для составления систематических обзоров и метаанализов исследований, оценивающих медицинские вмешательства: объяснение и уточнение.BMJ. 2009; 339: b2700. [Бесплатная статья PMC] [PubMed] [Google Scholar] 26. Абдалла Т.М., Идрисс М.И., Ахмед А.М., Али А.А., Саид ОК. Распространенность вирусов гепатита B и C среди туберкулезных больных в Кассале, Восточный Судан. Glob J Infect Dis Clin Res. 2015; 1 (1): 001–003. [Google Scholar] 27. Ага М.А., Эль-Махалави II, Селим Х.М., Хельва М.А. Распространенность вируса гепатита С у больных туберкулезом и его влияние на частоту гепатотоксичности, вызванной противотуберкулезными препаратами. Египет J Chest Dis Tuberc.2015; 64 (1): 91–96. [Google Scholar] 28.
Биометрия. 2000. 56 (2): 455–463. [PubMed] [Google Scholar] 24. Вьера AJ, Гарретт JM. Понимание соглашения между наблюдателями: статистика каппа. Fam Med. 2005. 37 (3): 360–363. [PubMed] [Google Scholar] 25. Либерати А., Альтман Д.Г., Тецлафф Дж., Малроу С., Готше П.С., Иоаннидис Дж. П. и др. Заявление PRISMA для составления систематических обзоров и метаанализов исследований, оценивающих медицинские вмешательства: объяснение и уточнение.BMJ. 2009; 339: b2700. [Бесплатная статья PMC] [PubMed] [Google Scholar] 26. Абдалла Т.М., Идрисс М.И., Ахмед А.М., Али А.А., Саид ОК. Распространенность вирусов гепатита B и C среди туберкулезных больных в Кассале, Восточный Судан. Glob J Infect Dis Clin Res. 2015; 1 (1): 001–003. [Google Scholar] 27. Ага М.А., Эль-Махалави II, Селим Х.М., Хельва М.А. Распространенность вируса гепатита С у больных туберкулезом и его влияние на частоту гепатотоксичности, вызванной противотуберкулезными препаратами. Египет J Chest Dis Tuberc.2015; 64 (1): 91–96. [Google Scholar] 28. Ахтар Дж., Камар М.Ю., Хаким А., Вахид А., Сарвар Ф., Анвар Дж. Серологическая распространенность ВГВ и ВГС у больных туберкулезом в больнице шейха Зайда Рахим Яр-хана, Пакистан. Биомедика. 2013; 29: 69–72. [Google Scholar] 29. Бадави М., Таха М., Мохамед Л., Фати А. Инфекция вируса гепатита С среди больных туберкулезом в провинции Сохаг: распространенность серы и связанные факторы риска. Eur Respir J. 2011; 38 (Дополнение 55): 4896. [Google Scholar] 30. Бисли В.Е., Андерс Р., Дармалингам М.Ретроспективное исследование для оценки фоновой заболеваемости гепатитом B и C у пациентов с туберкулезом и латентным туберкулезом в больнице Whipps Cross. Торакс. 2013; 68 (Приложение 3): A117 – A118. [Google Scholar] 31. Кампо М., Шреста А., Орен Э., Тид Х., Дучин Дж., Нарита М. и др. Характеристика инфекции гепатита С у больных туберкулезом в городском городе США. Epidemiol Infect. 2014; 142 (7): 1459. [PubMed] [Google Scholar] 32. Chien JY, Huang RM, Wang JY, Ruan SY, Chien YJ, Yu CJ и др.Инфекция вирусом гепатита С увеличивает риск гепатита во время противотуберкулезного лечения.
Ахтар Дж., Камар М.Ю., Хаким А., Вахид А., Сарвар Ф., Анвар Дж. Серологическая распространенность ВГВ и ВГС у больных туберкулезом в больнице шейха Зайда Рахим Яр-хана, Пакистан. Биомедика. 2013; 29: 69–72. [Google Scholar] 29. Бадави М., Таха М., Мохамед Л., Фати А. Инфекция вируса гепатита С среди больных туберкулезом в провинции Сохаг: распространенность серы и связанные факторы риска. Eur Respir J. 2011; 38 (Дополнение 55): 4896. [Google Scholar] 30. Бисли В.Е., Андерс Р., Дармалингам М.Ретроспективное исследование для оценки фоновой заболеваемости гепатитом B и C у пациентов с туберкулезом и латентным туберкулезом в больнице Whipps Cross. Торакс. 2013; 68 (Приложение 3): A117 – A118. [Google Scholar] 31. Кампо М., Шреста А., Орен Э., Тид Х., Дучин Дж., Нарита М. и др. Характеристика инфекции гепатита С у больных туберкулезом в городском городе США. Epidemiol Infect. 2014; 142 (7): 1459. [PubMed] [Google Scholar] 32. Chien JY, Huang RM, Wang JY, Ruan SY, Chien YJ, Yu CJ и др.Инфекция вирусом гепатита С увеличивает риск гепатита во время противотуберкулезного лечения. Int J Tuberc Lung Dis. 2010; 14 (5): 616. [PubMed] [Google Scholar] 33. Costi C, Grandi T, Halon ML, Silva MS, Silva CM, Gregianini TS и др. Распространенность вируса гепатита С и вируса иммунодефицита человека в группе пациентов с впервые диагностированным активным туберкулезом в Порту-Алегри, Южная Бразилия. Mem Inst Oswaldo Cruz. 2017; 112 (4): 255–259. [Бесплатная статья PMC] [PubMed] [Google Scholar] 34. Халили Х., Дашти-Хавидаки С., Расуледжад М., Резайе Л., Этминани М.Гепатотоксичность, связанная с противотуберкулезными препаратами; заболеваемость, факторы риска, характер изменений ферментов печени и исход. Дару. 2009. 17 (3): 163–167. [Google Scholar] 35. Хан С., Асгедди М., Абдулла М., О’Донохью М., Лалвани А., Кэмпбелл Л. и др. Распространенность вирусного гепатита у пациентов, получающих противотуберкулезную терапию в Западном Лондоне. Кишечник. 2010; 59 (Приложение 2): A42. [Google Scholar] 36. Кунихолм М.Х., Марк Дж., Аладашвили М., Шубладзе Н., Хечинашвили Г., Церцвадзе Т.
Int J Tuberc Lung Dis. 2010; 14 (5): 616. [PubMed] [Google Scholar] 33. Costi C, Grandi T, Halon ML, Silva MS, Silva CM, Gregianini TS и др. Распространенность вируса гепатита С и вируса иммунодефицита человека в группе пациентов с впервые диагностированным активным туберкулезом в Порту-Алегри, Южная Бразилия. Mem Inst Oswaldo Cruz. 2017; 112 (4): 255–259. [Бесплатная статья PMC] [PubMed] [Google Scholar] 34. Халили Х., Дашти-Хавидаки С., Расуледжад М., Резайе Л., Этминани М.Гепатотоксичность, связанная с противотуберкулезными препаратами; заболеваемость, факторы риска, характер изменений ферментов печени и исход. Дару. 2009. 17 (3): 163–167. [Google Scholar] 35. Хан С., Асгедди М., Абдулла М., О’Донохью М., Лалвани А., Кэмпбелл Л. и др. Распространенность вирусного гепатита у пациентов, получающих противотуберкулезную терапию в Западном Лондоне. Кишечник. 2010; 59 (Приложение 2): A42. [Google Scholar] 36. Кунихолм М.Х., Марк Дж., Аладашвили М., Шубладзе Н., Хечинашвили Г., Церцвадзе Т.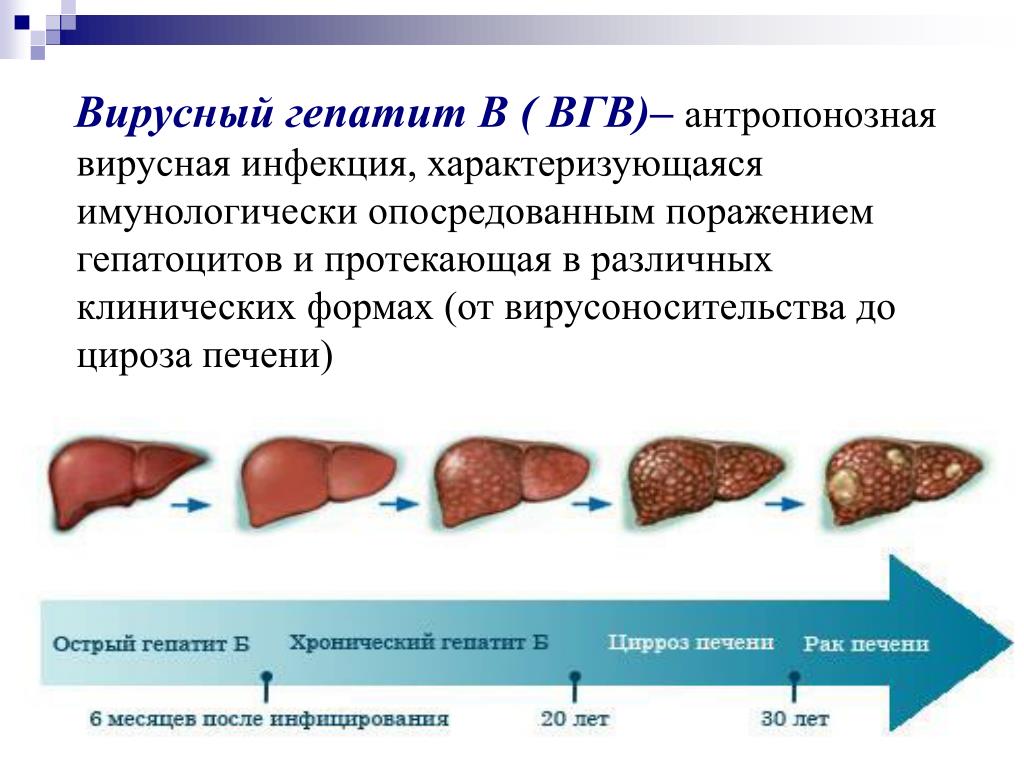 и др. Факторы риска и алгоритмы выявления гепатита C, гепатита B и ВИЧ у больных туберкулезом в Грузии.Int J Infect Dis. 2008. 12 (1): 51–56. [Бесплатная статья PMC] [PubMed] [Google Scholar] 37. Ломтадзе Н., Купреишвили Л., Салакая А., Вашакидзе С., Шарвадзе Л., Кемпкер Р. Р. и др. Коинфекция вируса гепатита С увеличивает риск гепатотоксичности, вызванной противотуберкулезными препаратами, у пациентов с туберкулезом легких. PLoS One. 2013; 8 (12): e83892. [Бесплатная статья PMC] [PubMed] [Google Scholar] 38. Мерза М.А., Хаджи С.М., Альшарафани А.М., Мухаммед С.У. Низкая распространенность гепатита B и C среди больных туберкулезом в провинции Духок, Курдистан: являются ли параметры HBsAg и анти-HCV обязательными параметрами скрининга в программе борьбы с туберкулезом? Int J Mycobacteriol.2016; 5 (3): 313–317. [PubMed] [Google Scholar] 39. Норединванд Х.А., Коннелл Д.В., Асгедди М., Абдулла М., О’Донохью М., Кэмпбелл Л. и др. Распространенность вирусных гепатитов у больных активным и латентным туберкулезом.
и др. Факторы риска и алгоритмы выявления гепатита C, гепатита B и ВИЧ у больных туберкулезом в Грузии.Int J Infect Dis. 2008. 12 (1): 51–56. [Бесплатная статья PMC] [PubMed] [Google Scholar] 37. Ломтадзе Н., Купреишвили Л., Салакая А., Вашакидзе С., Шарвадзе Л., Кемпкер Р. Р. и др. Коинфекция вируса гепатита С увеличивает риск гепатотоксичности, вызванной противотуберкулезными препаратами, у пациентов с туберкулезом легких. PLoS One. 2013; 8 (12): e83892. [Бесплатная статья PMC] [PubMed] [Google Scholar] 38. Мерза М.А., Хаджи С.М., Альшарафани А.М., Мухаммед С.У. Низкая распространенность гепатита B и C среди больных туберкулезом в провинции Духок, Курдистан: являются ли параметры HBsAg и анти-HCV обязательными параметрами скрининга в программе борьбы с туберкулезом? Int J Mycobacteriol.2016; 5 (3): 313–317. [PubMed] [Google Scholar] 39. Норединванд Х.А., Коннелл Д.В., Асгедди М., Абдулла М., О’Донохью М., Кэмпбелл Л. и др. Распространенность вирусных гепатитов у больных активным и латентным туберкулезом. Мир J Gastroenterol. 2015; 21 (29): 8920–8926. [Бесплатная статья PMC] [PubMed] [Google Scholar] 40. Пандо М.А., Де Сальво С., Баутиста С.Т., Эйсагирре Л., Падаль Г., Феола М. и др. Вирус иммунодефицита человека и туберкулез в Аргентине: распространенность, генотипы и факторы риска. J Med Microbiol. 2008. 57 (Pt 2): 190–197.[PubMed] [Google Scholar] 41. Potter JL, Hyams C, Shaukat M, Babiker ZO, Macavei VM, Jayasekera N, et al. Следует ли проводить скрининг на хронический вирусный гепатит у больных туберкулезом с хорошими рекомендациями? Торакс. 2014; 69 (Приложение 2): A159. [Google Scholar] 42. Рейс Н.Р., Лопес С.Л., Телес С.А., Матос М.А., Карнейро М.А., Мариньо Т.А. и др. Инфекция вирусом гепатита С у больных туберкулезом в Центральной Бразилии. Int J Tuberc Lung Dis. 2011. 15 (10): 1397–1402. [PubMed] [Google Scholar] 43. Ричардс Д.К., Микиашвили Т., Пэррис Дж. Дж., Курбатова Е. В., Уилсон Дж. К., Шубладзе Н. и др.Высокая распространенность вируса гепатита С, но не сочетанной инфекции ВИЧ, среди больных туберкулезом в Грузии.
Мир J Gastroenterol. 2015; 21 (29): 8920–8926. [Бесплатная статья PMC] [PubMed] [Google Scholar] 40. Пандо М.А., Де Сальво С., Баутиста С.Т., Эйсагирре Л., Падаль Г., Феола М. и др. Вирус иммунодефицита человека и туберкулез в Аргентине: распространенность, генотипы и факторы риска. J Med Microbiol. 2008. 57 (Pt 2): 190–197.[PubMed] [Google Scholar] 41. Potter JL, Hyams C, Shaukat M, Babiker ZO, Macavei VM, Jayasekera N, et al. Следует ли проводить скрининг на хронический вирусный гепатит у больных туберкулезом с хорошими рекомендациями? Торакс. 2014; 69 (Приложение 2): A159. [Google Scholar] 42. Рейс Н.Р., Лопес С.Л., Телес С.А., Матос М.А., Карнейро М.А., Мариньо Т.А. и др. Инфекция вирусом гепатита С у больных туберкулезом в Центральной Бразилии. Int J Tuberc Lung Dis. 2011. 15 (10): 1397–1402. [PubMed] [Google Scholar] 43. Ричардс Д.К., Микиашвили Т., Пэррис Дж. Дж., Курбатова Е. В., Уилсон Дж. К., Шубладзе Н. и др.Высокая распространенность вируса гепатита С, но не сочетанной инфекции ВИЧ, среди больных туберкулезом в Грузии. Int J Tuberc Lung Dis. 2006; 10 (4): 396. [PubMed] [Google Scholar] 44. Ван Дж.Й., Лю СН, Ху ФК, Чанг ХК, Лю Дж.Л., Чен Дж.М. и др. Факторы риска гепатита при противотуберкулезном лечении и последствия вирусной нагрузки гепатита. J Infect. 2011. 62 (6): 448–455. [PubMed] [Google Scholar] 45. Zhang L, Zhang D, Chen W, Zou X, Ling L. Высокая распространенность ВИЧ, ВГС и туберкулеза и связанное с ними рискованное поведение среди новых участников клиник поддерживающей терапии метадоном в провинции Гуандун, Китай.PLoS One. 2013; 8 (10): e76931. [Бесплатная статья PMC] [PubMed] [Google Scholar] 46. Платт Л., Истербрук П., Гауэр Э., Макдональд Б., Сабин К., Макгоуэн С. и др. Распространенность и бремя коинфекции ВГС у людей, живущих с ВИЧ: глобальный систематический обзор и метаанализ. Lancet Infect Dis. 2016; 16 (7): 797–808. [PubMed] [Google Scholar] 47. Azevedo TCL, Zwahlen M, Rauch A., Egger M, Wandeler G. Гепатит C у ВИЧ-инфицированных: систематический обзор и метаанализ предполагаемой распространенности в Африке.
Int J Tuberc Lung Dis. 2006; 10 (4): 396. [PubMed] [Google Scholar] 44. Ван Дж.Й., Лю СН, Ху ФК, Чанг ХК, Лю Дж.Л., Чен Дж.М. и др. Факторы риска гепатита при противотуберкулезном лечении и последствия вирусной нагрузки гепатита. J Infect. 2011. 62 (6): 448–455. [PubMed] [Google Scholar] 45. Zhang L, Zhang D, Chen W, Zou X, Ling L. Высокая распространенность ВИЧ, ВГС и туберкулеза и связанное с ними рискованное поведение среди новых участников клиник поддерживающей терапии метадоном в провинции Гуандун, Китай.PLoS One. 2013; 8 (10): e76931. [Бесплатная статья PMC] [PubMed] [Google Scholar] 46. Платт Л., Истербрук П., Гауэр Э., Макдональд Б., Сабин К., Макгоуэн С. и др. Распространенность и бремя коинфекции ВГС у людей, живущих с ВИЧ: глобальный систематический обзор и метаанализ. Lancet Infect Dis. 2016; 16 (7): 797–808. [PubMed] [Google Scholar] 47. Azevedo TCL, Zwahlen M, Rauch A., Egger M, Wandeler G. Гепатит C у ВИЧ-инфицированных: систематический обзор и метаанализ предполагаемой распространенности в Африке. J Int AIDS Soc.2016; 19 (1): 20711. [Бесплатная статья PMC] [PubMed] [Google Scholar] 48. Mohd Hanafiah K, Groeger J, Flaxman AD, Wiersma ST. Глобальная эпидемиология вирусной инфекции гепатита С: новые оценки возрастных антител к серологической распространенности ВГС. Гепатология. 2013. 57 (4): 1333–1342. [PubMed] [Google Scholar] 49. Harfouche M, Chemaitelly H, Mahmud S, Chaabna K, Kouyoumjian SP, Al Kanaani Z, et al. Эпидемиология вируса гепатита С среди гемодиализных пациентов на Ближнем Востоке и в Северной Африке: систематический синтез, метаанализы и мета-регрессии.Epidemiol Infect. 2017; 145 (15): 3243–3263. [PubMed] [Google Scholar] 50. Обермейер З., Эбботт-Клафтер Дж., Мюррей С.Дж. Улучшила ли стратегия DOTS выявление случаев или успех лечения? Эмпирическая оценка. PLoS One. 2008; 3 (3): e1721. [Бесплатная статья PMC] [PubMed] [Google Scholar] 51. Raviglione MC, Uplekar MW. Новая стратегия ВОЗ «Остановить туберкулез». Ланцет. 2006. 367 (9514): 952–955. [PubMed] [Google Scholar] 52.
J Int AIDS Soc.2016; 19 (1): 20711. [Бесплатная статья PMC] [PubMed] [Google Scholar] 48. Mohd Hanafiah K, Groeger J, Flaxman AD, Wiersma ST. Глобальная эпидемиология вирусной инфекции гепатита С: новые оценки возрастных антител к серологической распространенности ВГС. Гепатология. 2013. 57 (4): 1333–1342. [PubMed] [Google Scholar] 49. Harfouche M, Chemaitelly H, Mahmud S, Chaabna K, Kouyoumjian SP, Al Kanaani Z, et al. Эпидемиология вируса гепатита С среди гемодиализных пациентов на Ближнем Востоке и в Северной Африке: систематический синтез, метаанализы и мета-регрессии.Epidemiol Infect. 2017; 145 (15): 3243–3263. [PubMed] [Google Scholar] 50. Обермейер З., Эбботт-Клафтер Дж., Мюррей С.Дж. Улучшила ли стратегия DOTS выявление случаев или успех лечения? Эмпирическая оценка. PLoS One. 2008; 3 (3): e1721. [Бесплатная статья PMC] [PubMed] [Google Scholar] 51. Raviglione MC, Uplekar MW. Новая стратегия ВОЗ «Остановить туберкулез». Ланцет. 2006. 367 (9514): 952–955. [PubMed] [Google Scholar] 52. Ли Б.Х., Кох В.Дж., Чой М.С., Сух Г.Й., Чанг М.П., Ким Х. и др. Состояние неактивного носителя поверхностного антигена гепатита В и гепатотоксичность во время противотуберкулезной химиотерапии.Грудь. 2005. 127 (4): 1304–1311. [PubMed] [Google Scholar] 53. Hwang SJ, Wu JC, Lee CN, Yen FS, Lu CL, Lin TP и др. Проспективное клиническое исследование повреждения печени, вызванного изониазид-рифампицин-пиразинамидом, в эндемичной для гепатита B области. J Gastroenterol Hepatol. 1997. 12 (1): 87–91. [PubMed] [Google Scholar] 54. Амарапуркар Д. Н., Прабхудесай П. П., Калро Р. Х., Десаи Г. Г.. Гепатит, индуцированный противотуберкулезными препаратами, и носители HBsAg. Tuber Lung Dis. 1993. 74 (3): 215–216. [PubMed] [Google Scholar] 55. Рамаппа V, Айтал, GP.Гепатотоксичность, связанная с противотуберкулезными препаратами: механизмы и лечение. J Clin Exp Hepatol. 2013; 3 (1): 37. [Бесплатная статья PMC] [PubMed] [Google Scholar] 56. Квон Ю.С., Ко В.Дж., Сух Г.Й., Чанг М.П., Ким Х., Квон О.Дж.
Ли Б.Х., Кох В.Дж., Чой М.С., Сух Г.Й., Чанг М.П., Ким Х. и др. Состояние неактивного носителя поверхностного антигена гепатита В и гепатотоксичность во время противотуберкулезной химиотерапии.Грудь. 2005. 127 (4): 1304–1311. [PubMed] [Google Scholar] 53. Hwang SJ, Wu JC, Lee CN, Yen FS, Lu CL, Lin TP и др. Проспективное клиническое исследование повреждения печени, вызванного изониазид-рифампицин-пиразинамидом, в эндемичной для гепатита B области. J Gastroenterol Hepatol. 1997. 12 (1): 87–91. [PubMed] [Google Scholar] 54. Амарапуркар Д. Н., Прабхудесай П. П., Калро Р. Х., Десаи Г. Г.. Гепатит, индуцированный противотуберкулезными препаратами, и носители HBsAg. Tuber Lung Dis. 1993. 74 (3): 215–216. [PubMed] [Google Scholar] 55. Рамаппа V, Айтал, GP.Гепатотоксичность, связанная с противотуберкулезными препаратами: механизмы и лечение. J Clin Exp Hepatol. 2013; 3 (1): 37. [Бесплатная статья PMC] [PubMed] [Google Scholar] 56. Квон Ю.С., Ко В.Дж., Сух Г.Й., Чанг М.П., Ким Х., Квон О.Дж. Инфекция вируса гепатита С и гепатотоксичность во время противотуберкулезной химиотерапии. Грудь. 2007. 131 (3): 803–808. [PubMed] [Google Scholar] 57. Фернандес-Вильяр А., Сопенья Б., Васкес Р., Уллоа Ф., Флюитерс Е., Мостейро М. и др. Гепатотоксичность изониазида среди потребителей наркотиков: роль гепатита С.Clin Infect Dis. 2003. 36 (3): 293–298. [PubMed] [Google Scholar] 58. Унго Дж. Р., Джонс Д., Ашкин Д., Холлендер Э. С., Бернштейн Д., Альбанезе А. П. и др. Гепатотоксичность, вызванная противотуберкулезными препаратами. Роль вируса гепатита С и вируса иммунодефицита человека. Am J Respir Crit Care Med. 1998; 157 (6 Pt 1): 1871–1876. [PubMed] [Google Scholar] 59. Parry JV, Истербрук П., Сэндс АР. Стратегия одного или двух серологических тестов для диагностики инфекции HBV и HCV? Использование прогнозного моделирования. BMC Infect Dis.2017; 17 (Приложение 1): 705. [Бесплатная статья PMC] [PubMed] [Google Scholar] 60. Батул А, Хан М.И., Бано К.А. Эффективность иммунохроматографического теста на определение антител к гепатиту С.
Инфекция вируса гепатита С и гепатотоксичность во время противотуберкулезной химиотерапии. Грудь. 2007. 131 (3): 803–808. [PubMed] [Google Scholar] 57. Фернандес-Вильяр А., Сопенья Б., Васкес Р., Уллоа Ф., Флюитерс Е., Мостейро М. и др. Гепатотоксичность изониазида среди потребителей наркотиков: роль гепатита С.Clin Infect Dis. 2003. 36 (3): 293–298. [PubMed] [Google Scholar] 58. Унго Дж. Р., Джонс Д., Ашкин Д., Холлендер Э. С., Бернштейн Д., Альбанезе А. П. и др. Гепатотоксичность, вызванная противотуберкулезными препаратами. Роль вируса гепатита С и вируса иммунодефицита человека. Am J Respir Crit Care Med. 1998; 157 (6 Pt 1): 1871–1876. [PubMed] [Google Scholar] 59. Parry JV, Истербрук П., Сэндс АР. Стратегия одного или двух серологических тестов для диагностики инфекции HBV и HCV? Использование прогнозного моделирования. BMC Infect Dis.2017; 17 (Приложение 1): 705. [Бесплатная статья PMC] [PubMed] [Google Scholar] 60. Батул А, Хан М.И., Бано К.А. Эффективность иммунохроматографического теста на определение антител к гепатиту С. J Ayub Med Coll Abbottabad. 2009. 21 (3): 38–39. [PubMed] [Google Scholar] 63. Мохамед А.А., Эльбедеви Т.А., Эль-Серафи М., Эль-Тухи Н., Ахмед В., Али Эль-Дин З. Вирус гепатита С: глобальный взгляд. Мир J Hepatol. 2015; 7 (26): 2676–2680. [Бесплатная статья PMC] [PubMed] [Google Scholar] 64. Ольмедо DB, Precioso PM, Lugdero-Correia A, da Silva G, dos Santos AMG, Pôrto LC.Распространенность источника воздействия связана с полом у пациентов с вирусом гепатита С из Рио-де-Жанейро, Бразилия. Mem Inst Oswaldo Cruz. 2017; 112 (9): 632. [Бесплатная статья PMC] [PubMed] [Google Scholar] 65. Толмане И., Розентале Б., Кейс Дж., Арса Ф., Бригис Дж., Звайгзне А. Распространенность вирусного гепатита С в Латвии: популяционное исследование. Медицина (Каунас) 2011; 47 (10): 532–535. [PubMed] [Google Scholar] 67. Буономо А.Р., Скотто Р., Пинчера Б., Коппола Н., Монари С., Мачера М. и др. Эпидемиология и факторы риска генотипов вируса гепатита С в регионе с высокой распространенностью в Италии.New Microbiol.
J Ayub Med Coll Abbottabad. 2009. 21 (3): 38–39. [PubMed] [Google Scholar] 63. Мохамед А.А., Эльбедеви Т.А., Эль-Серафи М., Эль-Тухи Н., Ахмед В., Али Эль-Дин З. Вирус гепатита С: глобальный взгляд. Мир J Hepatol. 2015; 7 (26): 2676–2680. [Бесплатная статья PMC] [PubMed] [Google Scholar] 64. Ольмедо DB, Precioso PM, Lugdero-Correia A, da Silva G, dos Santos AMG, Pôrto LC.Распространенность источника воздействия связана с полом у пациентов с вирусом гепатита С из Рио-де-Жанейро, Бразилия. Mem Inst Oswaldo Cruz. 2017; 112 (9): 632. [Бесплатная статья PMC] [PubMed] [Google Scholar] 65. Толмане И., Розентале Б., Кейс Дж., Арса Ф., Бригис Дж., Звайгзне А. Распространенность вирусного гепатита С в Латвии: популяционное исследование. Медицина (Каунас) 2011; 47 (10): 532–535. [PubMed] [Google Scholar] 67. Буономо А.Р., Скотто Р., Пинчера Б., Коппола Н., Монари С., Мачера М. и др. Эпидемиология и факторы риска генотипов вируса гепатита С в регионе с высокой распространенностью в Италии.New Microbiol.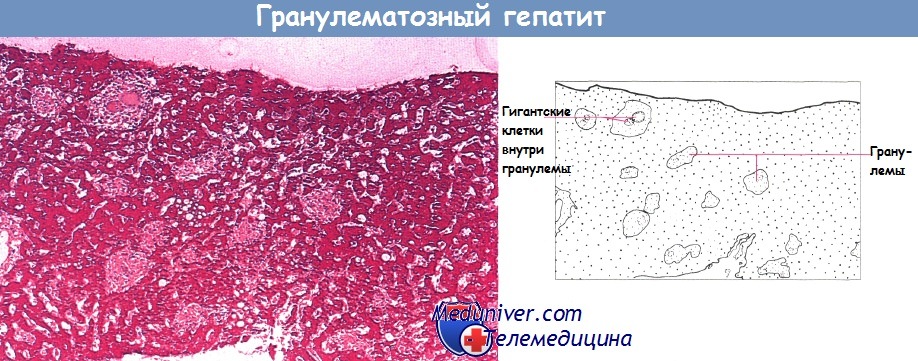 2018; 41 (1): 26–29. [PubMed] [Google Scholar] 68. Венгер П.Дж., Роттнек Ф., Паркер Т., Криппин Дж.С. Оценка факторов риска гепатита С и распространенности инфекции среди заключенных. Am J Public Health. 2014. 104 (9): 1722–1727. [Бесплатная статья PMC] [PubMed] [Google Scholar] 69. He Y, Zhang J, Zhong L, Chen X, Liu HM, Wan LK и др. Распространенность и факторы риска заражения вирусом гепатита С среди доноров крови в Чэнду, Китай. J Med Virol. 2011. 83 (4): 616–621. [PubMed] [Google Scholar]
2018; 41 (1): 26–29. [PubMed] [Google Scholar] 68. Венгер П.Дж., Роттнек Ф., Паркер Т., Криппин Дж.С. Оценка факторов риска гепатита С и распространенности инфекции среди заключенных. Am J Public Health. 2014. 104 (9): 1722–1727. [Бесплатная статья PMC] [PubMed] [Google Scholar] 69. He Y, Zhang J, Zhong L, Chen X, Liu HM, Wan LK и др. Распространенность и факторы риска заражения вирусом гепатита С среди доноров крови в Чэнду, Китай. J Med Virol. 2011. 83 (4): 616–621. [PubMed] [Google Scholar]
ВИЧ, туберкулез и гепатит | ВОЗ
Программа по ВИЧ, туберкулезу и гепатиту (HTH) объединяет бывшие программы по ВИЧ / СПИДу, туберкулезу и гепатиту.
Бремя ВИЧ, туберкулеза и гепатита в регионе Африки
ВИЧ : По оценкам, по состоянию на 2016 год 25,6 миллиона человек в регионе AFRO жили с ВИЧ, в том числе 1,9 миллиона детей в возрасте до 15 лет. В 2016 году в регионе произошло 1,2 миллиона новых случаев инфицирования ВИЧ, и было зарегистрировано 720 000 случаев СПИДа. связанных смертей — на 5% меньше по сравнению с 760 000 смертей в регионе в 2015 году. В 2016 году во всем регионе продолжалось расширение масштабов антиретровирусной терапии.В настоящее время АРТ получают 13,8 миллиона взрослых и детей, что на 15% больше, чем в регионе с 2015 года, и на 83% с 2012 года.
связанных смертей — на 5% меньше по сравнению с 760 000 смертей в регионе в 2015 году. В 2016 году во всем регионе продолжалось расширение масштабов антиретровирусной терапии.В настоящее время АРТ получают 13,8 миллиона взрослых и детей, что на 15% больше, чем в регионе с 2015 года, и на 83% с 2012 года.
Туберкулез : Из 20 стран мира с самым высоким бременем туберкулеза (ТБ) 8 расположены в Африканском регионе ВОЗ. Почти 3 миллиона из 10,4 миллиона человек, заразившихся туберкулезом в 2015 году, проживают в странах Африки к югу от Сахары, и 750 000 из этих людей умерли от этой болезни. Коинфекция ТБ / ВИЧ и ТБ с множественной лекарственной устойчивостью (МЛУ-ТБ), в частности, создают проблемы для профилактики, лечения и контроля в регионе AFRO.Из 2,7 миллиона африканцев, заболевших туберкулезом в 2015 году, 834 000 были также ВИЧ-положительными, а 110 000 — больными МЛУ-ТБ.
Гепатит : Инфекция вирусами гепатита A, B, C, D и E стала причиной 1,34 миллиона смертей во всем мире в 2015 году. Это почти равно количеству смертей от туберкулеза и превышает количество смертей от ВИЧ в мире. в том же году и иллюстрирует бремя вирусного гепатита как проблему глобального здравоохранения. В регионе AFRO более 70 миллионов человек в настоящее время живут как минимум с одной формой вирусного гепатита.По состоянию на 2015 год, согласно оценкам, 6,1% населения в африканском регионе ВОЗ больны гепатитом B, а еще 1% — гепатитом C. На Африку к югу от Сахары также приходится 136000 смертей от вирусного гепатита ежегодно — 10% от общей смертности в мире. от гепатита.
Это почти равно количеству смертей от туберкулеза и превышает количество смертей от ВИЧ в мире. в том же году и иллюстрирует бремя вирусного гепатита как проблему глобального здравоохранения. В регионе AFRO более 70 миллионов человек в настоящее время живут как минимум с одной формой вирусного гепатита.По состоянию на 2015 год, согласно оценкам, 6,1% населения в африканском регионе ВОЗ больны гепатитом B, а еще 1% — гепатитом C. На Африку к югу от Сахары также приходится 136000 смертей от вирусного гепатита ежегодно — 10% от общей смертности в мире. от гепатита.
О программе
ВИЧ : Целью подразделения по ВИЧ / СПИДу программы HTH является оказание поддержки государствам-членам в прекращении эпидемии ВИЧ / СПИДа как угрозы общественному здоровью к 2030 году. Группа по ВИЧ помогает государствам-членам принять и реализовать меры по спасению жизни вмешательства для повышения рентабельности профилактики, лечения, ухода и поддержки в связи с ВИЧ для 25. 6 миллионов человек, живущих с ВИЧ / СПИДом, в Африканском регионе ВОЗ. Это включает уделение первоочередного внимания профилактике ВИЧ, расширение услуг по тестированию на ВИЧ с использованием разнообразных подходов и расширение масштабов антиретровирусной терапии за счет внедрения инновационных моделей предоставления услуг при одновременном укреплении систем здравоохранения в контексте всеобщего доступа.
6 миллионов человек, живущих с ВИЧ / СПИДом, в Африканском регионе ВОЗ. Это включает уделение первоочередного внимания профилактике ВИЧ, расширение услуг по тестированию на ВИЧ с использованием разнообразных подходов и расширение масштабов антиретровирусной терапии за счет внедрения инновационных моделей предоставления услуг при одновременном укреплении систем здравоохранения в контексте всеобщего доступа.
TB : Отделение туберкулеза (ТБ) программы HTH стремится снизить бремя ТБ в африканском регионе. В частности, как указано в рамках реализации Стратегии «Положить конец туберкулезу в Африканском регионе (2016–2020 гг.)», Которая поддерживает адаптацию и реализацию Глобальной стратегии в странах с учетом их контекстуальных обстоятельств, AFRO стремится сократить число смертей от туберкулеза. на 35%, количество больных туберкулезом на 20% и доведение до 0% семей, затронутых туберкулезом, которые несут катастрофические расходы из-за туберкулеза.Подразделение по борьбе с туберкулезом также сосредотачивает усилия на конкретных вопросах сочетанной инфекции ТБ и ВИЧ (на которую приходится 1/3 смертей от ТБ в регионе) и растущего бремени ТБ с множественной лекарственной устойчивостью
Гепатит : Подразделение по гепатиту программы HTH стремится снизить бремя вирусного гепатита, вызванного инфицированием вирусами A, B, C, D и E, и устранить его как серьезную угрозу общественному здоровью в регионе AFRO. к 2030 году. При этом AFRO предоставляет рекомендации и техническую поддержку государствам-членам в Регионе для содействия
к 2030 году. При этом AFRO предоставляет рекомендации и техническую поддержку государствам-членам в Регионе для содействия
Осуществление первой в истории Глобальной стратегии сектора здравоохранения по вирусному гепатиту, в рамках которой планируется ликвидировать передачу гепатита во всем мире с использованием системы всеобщего охвата.Подробности этой стратегии изложены в документе «Профилактика, уход и лечение вирусного гепатита в Африканском регионе: рамки действий на 2016–2020 годы».
Д-р Хьюг Лаго
Руководитель группы Программа по ВИЧ / туберкулезу и гепатиту / Кластер инфекционных заболеваний
Эл. Почта: lagoh [at] who.int
ВИЧ и коинфекции | Лечение, уход и профилактика для людей с ВИЧ | Клиницисты | ВИЧ
Тестирование и лечение
Анализы крови используются для выявления вирусных гепатитов.Тесты могут обнаружить вирус, даже если у человека нет симптомов. В случае гепатита B анализы крови могут помочь определить, есть ли у людей гепатит B, и, если нет, будет ли им польза от вакцины против гепатита B. Если скрининговый тест на гепатит С положительный, необходимо провести повторный тест, чтобы определить, есть ли у человека гепатит С или инфекция исчезла.
Если скрининговый тест на гепатит С положительный, необходимо провести повторный тест, чтобы определить, есть ли у человека гепатит С или инфекция исчезла.
Лечение вирусного гепатита различается. Инфекция гепатита А обычно проходит со временем, хотя некоторым людям может потребоваться госпитализация.Большинство людей, заболевших гепатитом А, полностью выздоравливают и не имеют стойких повреждений печени. Для некоторых людей, особенно с проблемами со здоровьем, гепатит А может вызвать смерть. Гепатит В можно лечить противовирусными препаратами, но не всех можно и нужно лечить. Лечение гепатита B является пожизненным и может отсрочить или ограничить последствия повреждения печени. Лечение гепатита С может вылечить болезнь с помощью курса пероральных лекарств (таблеток) с небольшими побочными эффектами, принимаемого в течение нескольких месяцев.
Для людей, живущих с ВИЧ, коинфекция вирусного гепатита может осложнить лечение ВИЧ. Поскольку вирусный гепатит часто является серьезным заболеванием у людей с ВИЧ и может привести к более быстрому повреждению печени, CDC рекомендует, чтобы все люди с ВИЧ прошли тестирование на гепатит B и гепатит C. CDC также рекомендует всем, кто родился с 1945 по 1965 год, а также молодым людям. с определенными факторами риска, пройти хотя бы один тест на гепатит С.
CDC также рекомендует всем, кто родился с 1945 по 1965 год, а также молодым людям. с определенными факторами риска, пройти хотя бы один тест на гепатит С.
Коинфекции ВИЧ / гепатит В и ВИЧ / гепатит С можно эффективно лечить у многих людей, но лечение является сложным.Людям с коинфекцией следует искать поставщиков медицинских услуг, имеющих опыт лечения как ВИЧ, так и вирусных гепатитов.
CDC выпустил 5-минутный онлайн-инструмент оценки риска гепатита, который позволяет людям отвечать на вопросы в частном порядке и получать индивидуальные рекомендации для обсуждения со своим врачом. Этот инструмент также может определить, какие тесты и вакцины подходят человеку.
Для получения дополнительной информации посетите Центр контроля заболеваний вирусным гепатитом.
Распространенность вируса гепатита С у больных туберкулезом и его влияние на частоту гепатотоксичности, вызванную противотуберкулезными препаратами
Резюме
Предпосылки
Распространенность инфекции вирусом гепатита С среди больных туберкулезом не выявлена. были широко исследованы, и существуют очень ограниченные данные о частоте сочетанной инфекции ВГС среди пациентов с ТБ.Гепатотоксичность является основным побочным эффектом трех противотуберкулезных препаратов первого ряда: изониазида (INH), рифампицина (RIF) и пиразинамида (PZA). Хроническое заболевание печени повышает риск гепатотоксичности во время противотуберкулезного лечения, в три-пять раз больше, чем у больных туберкулезом, не инфицированных вирусами.
были широко исследованы, и существуют очень ограниченные данные о частоте сочетанной инфекции ВГС среди пациентов с ТБ.Гепатотоксичность является основным побочным эффектом трех противотуберкулезных препаратов первого ряда: изониазида (INH), рифампицина (RIF) и пиразинамида (PZA). Хроническое заболевание печени повышает риск гепатотоксичности во время противотуберкулезного лечения, в три-пять раз больше, чем у больных туберкулезом, не инфицированных вирусами.
Цель
Оценить распространенность инфекции ВГС у больных туберкулезом и ее влияние на частоту гепатотоксичности, вызванной противотуберкулезными препаратами.
Субъекты и методы
Распространенность ВГС у пациентов с впервые диагностированным легочным или внелегочным туберкулезом оценивалась с помощью полимеразной цепной реакции (ПЦР). Затем пациенты были разделены на 2 группы: I группа (пациенты с коинфекцией HCV-TB) и II группа (HCV-серонегативные туберкулезные пациенты). Базовое и ежемесячное измерение уровня трансаминаз печени проводилось до и после начала противотуберкулезной терапии 1-й линии.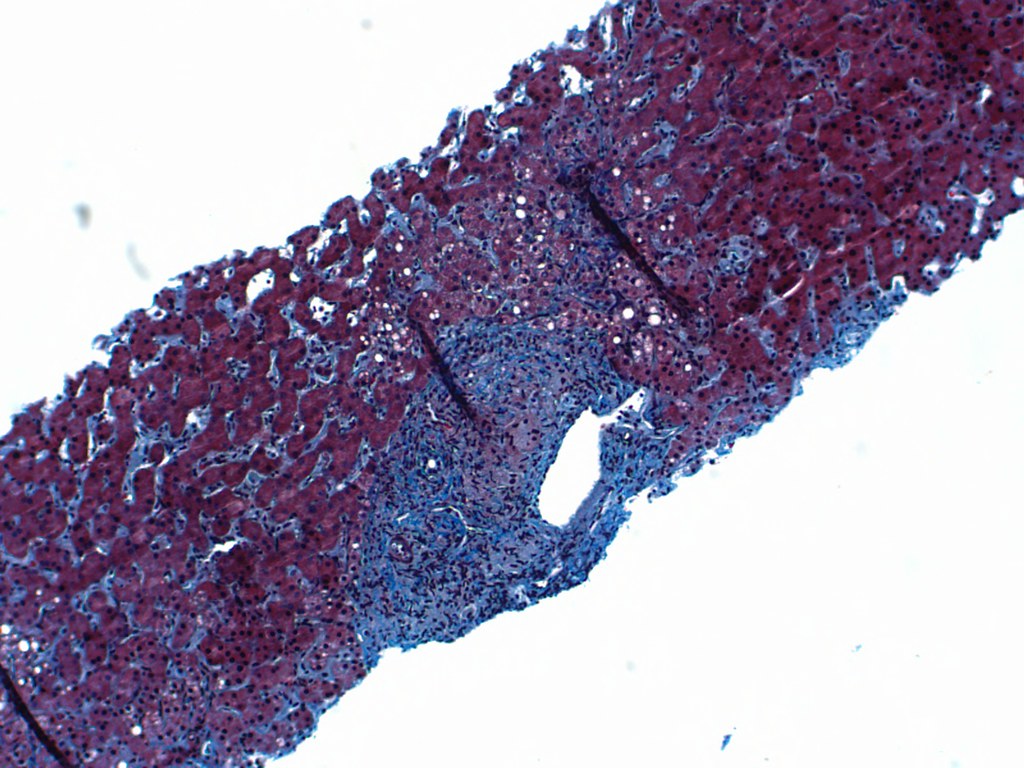
Результаты
Распространенность ВГС среди больных ТБ составила 17.02%. Что касается DIH, в группе I; В 6 (40%) случаях наблюдалось преходящее повышение уровня трансаминаз и в 6 (40%) случаях развился ДГГ. Во II группе; В 11 (20,75%) случаях развилось преходящее повышение уровня трансаминаз и только в 2 (3,78%) случаях развился ДГГ, при этом между обеими группами была очень значимая разница (<0,01). Что касается тяжести ДИГ, в группе I; 4 случая были легкими, один случай средней тяжести и один случай тяжелым. В группе II случаев тяжелой ДИГ не было. Факторы риска развития ДИГ во время противотуберкулезной терапии: возраст ≥40, высокие исходные уровни трансаминаз, ЩФ и общий билирубин и низкий ИМТ.Большинство случаев ДИГ произошло в первые 4 недели от начала противотуберкулезной терапии (66,7% и 50% в группе I и группе II соответственно).
Выводы
Коинфекция туберкулезом и вирусом гепатита С является обычным явлением, и повышение функций печени во время противотуберкулезной терапии не является редкостью. Пациенты с туберкулезом, инфицированные ВГС, должны находиться под тщательным наблюдением во время лечения, особенно если у них были повышенные исходные функции печени, пожилой возраст и низкий ИМТ. Мониторинг должен включать весь период лечения, особенно первые 2 месяца.
Пациенты с туберкулезом, инфицированные ВГС, должны находиться под тщательным наблюдением во время лечения, особенно если у них были повышенные исходные функции печени, пожилой возраст и низкий ИМТ. Мониторинг должен включать весь период лечения, особенно первые 2 месяца.
Ключевые слова
ВГС
Туберкулез
Гепатотоксичность
Рекомендуемые статьи Цитирующие статьи (0)
Авторское право © 2014 Египетское общество болезней грудной клетки и туберкулеза. Производство и хостинг Elsevier B.V.
Рекомендуемые статьи
Ссылки на статьи
Туберкулез | CATIE — Канадский источник информации о ВИЧ и гепатите C
Резюме
Туберкулез (ТБ) вызывается бактериями, называемыми комплексом Mycobacterium tuberculosis , и обычно поражает легкие.Однако у людей, коинфицированных туберкулезом и ВИЧ, часто поражаются части тела за пределами легких; это называется внелегочным туберкулезом.
Микробы, вызывающие туберкулез, распространяются, когда человек вдыхает крошечные капельки, производимые людьми, которые больны инфекционным или активным туберкулезом легких. Заражение туберкулезом может привести к двум различным состояниям — латентной инфекции (без симптомов) или активной инфекции.
Заражение туберкулезом может привести к двум различным состояниям — латентной инфекции (без симптомов) или активной инфекции.
Если не лечить туберкулез, он может быть смертельным и передаваться другим людям. Однако своевременное лечение, состоящее из комбинированной терапии антибиотиками, может вылечить как латентный, так и активный туберкулез.Наличие туберкулеза в прошлом — как латентной, так и активной формы заболевания — не защищает человека от заражения туберкулезными бактериями в будущем.
Что такое туберкулез?
Туберкулез (ТБ) — это инфекция, вызываемая бактериями, называемыми комплексом Mycobacterium tuberculosis . Обычно поражаются легкие, но у людей, инфицированных одновременно туберкулезом и ВИЧ, часто поражаются части тела за пределами легких; это называется внелегочным туберкулезом.
Бактерии, вызывающие туберкулез, чаще всего передаются при вдыхании крошечных капель, выпущенных инфицированным человеком в воздух во время следующих действий:
- кашель
- чихание
- говорящий
Эти крошечные капли невидимы и могут оставаться в воздухе в течение нескольких часов после их выпуска.
Передача бактерий, вызывающих туберкулез, от инфекционного человека зависит от многих факторов, включая следующие:
- как близко и как долго человек подвергался воздействию
- степень заразности больного туберкулезом
- тип общей среды, в которой имел место контакт
Исследования показали, что люди с туберкулезом, чья мокрота (густая смесь, выделяемая при кашле у людей с инфекциями грудной клетки) содержит вызывающие туберкулез бактерии, вероятно, передают эти бактерии.Кроме того, люди с полостями в легких, вызванными туберкулезом, очень заразны.
В странах с высоким уровнем доходов, таких как Канада, ВИЧ-инфицированные люди, подвергшиеся воздействию микробов, вызывающих ТБ, склонны к заражению вызывающими ТБ бактериями других частей тела, включая следующие:
- оболочки, окружающие мозг
- лимфатические узлы
- селезенка
- печень
- почки
- кости
Инфекция, вызывающая туберкулез, может привести к одной из двух форм инфекции:
- латентная туберкулезная инфекция — человек не имеет симптомов и не заразен
- активная инфекция ТБ — человек имеет симптомы болезни и может распространять бактерии, вызывающие ТБ
Кто подвержен риску заболевания туберкулезом?
Риск развития активного заболевания у человека от бактерий, вызывающих ТБ, после заражения зависит от многих факторов, включая следующие:
- их общее состояние здоровья
- возраст — у пожилых людей более слабая иммунная система
- среди ВИЧ-положительных людей чем ниже число CD4, тем выше риск развития туберкулеза
Как правило, после контакта с бактериями, вызывающими ТБ, болезнь не возникает сразу.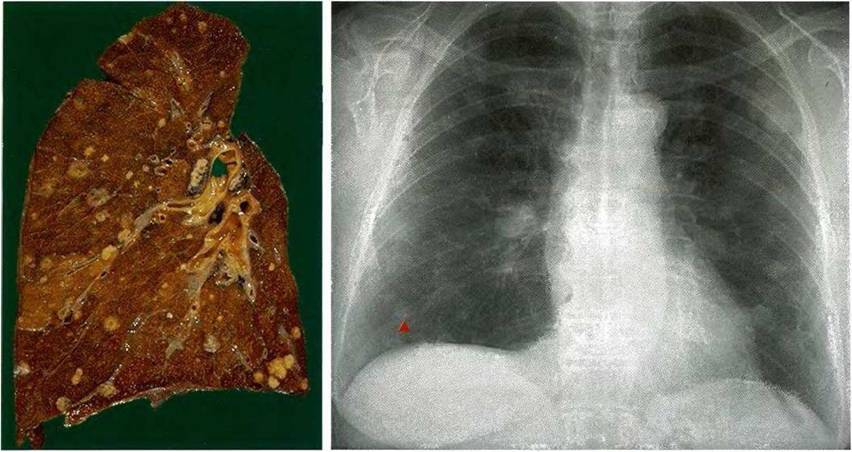 Вместо этого, когда бактерии попадают в легкие, обычно происходит то, что они захватываются клетками иммунной системы. Иногда иммунная система способна уничтожить эти бактерии. В других случаях бактерии способны подорвать защиту иммунной системы и продолжить инфицировать клетки иммунной системы. Как только это произойдет, инфекция начнет медленно распространяться. У большинства людей, по крайней мере на начальном этапе, их иммунная система, если она не убивает бактерии, способна перевести инфекцию в латентное состояние.Однако люди, иммунная система которых ослаблена следующими факторами, подвержены риску в конечном итоге развития активного туберкулеза:
Вместо этого, когда бактерии попадают в легкие, обычно происходит то, что они захватываются клетками иммунной системы. Иногда иммунная система способна уничтожить эти бактерии. В других случаях бактерии способны подорвать защиту иммунной системы и продолжить инфицировать клетки иммунной системы. Как только это произойдет, инфекция начнет медленно распространяться. У большинства людей, по крайней мере на начальном этапе, их иммунная система, если она не убивает бактерии, способна перевести инфекцию в латентное состояние.Однако люди, иммунная система которых ослаблена следующими факторами, подвержены риску в конечном итоге развития активного туберкулеза:
- ВИЧ-инфекция
- алкоголизм
- диабет
- уличные инъекции наркотиков
- использование препаратов для трансплантации
- курительный табак
Симптомы
Люди с латентным туберкулезом не имеют симптомов; необходимы тесты, чтобы помочь оценить их состояние.
Симптомы активного туберкулеза могут различаться в зависимости от человека и пораженной системы органов. Однако относительно часто встречаются следующие симптомы:
Однако относительно часто встречаются следующие симптомы:
- неожиданная усталость
- лихорадка
- ночные поты
- непреднамеренная потеря веса
- увеличение лимфатических узлов
В случаях, когда туберкулез поражает центральную нервную систему (ЦНС) — головной и спинной мозг — дополнительные симптомы могут включать следующее:
- сильная головная боль
- путаница
- очень жесткая шея
В случаях, когда бактерии, вызывающие туберкулез, распространились по организму, могут присутствовать следующие симптомы:
- ночные поты
- потеря аппетита
- слабость
В случаях, когда туберкулез поражает легкие, могут возникнуть следующие симптомы:
- непрекращающийся кашель
- кашляет кровью
- боль в груди
При обследовании человека с активным туберкулезом врачи могут обнаружить отек следующих частей тела:
Диагностика
Скрытый TB
Чтобы помочь диагностировать латентный туберкулез, медсестры могут вводить очищенный белок из вызывающих туберкулез бактерий прямо под кожу (это не вызывает инфекцию). У людей с латентным туберкулезом очень высока вероятность реакции — обычно опухоль или шишка в месте инъекции в течение 48–72 часов.
У людей с латентным туберкулезом очень высока вероятность реакции — обычно опухоль или шишка в месте инъекции в течение 48–72 часов.
Тест несовершенный, и у людей с сильно ослабленной иммунной системой может не быть реакции. В других случаях реакция может развиться у людей, инфицированных бактериями, близкими к тем, которые вызывают туберкулез. В некоторых клиниках анализ крови также может использоваться для выявления людей с латентным туберкулезом. Эти тесты проверяют наличие химического сигнала — гамма-интерферона — вырабатываемого иммунной системой.
Активный TB
Врачи полагаются на несколько вспомогательных средств, помогающих им диагностировать активный туберкулез, в том числе следующие:
- Рентген
- исследование жидкости, взятой из пораженного лимфатического узла или органа под микроскопом
- попытка выращивания бактерий туберкулеза в лаборатории из образцов жидкости, взятых из опухшего лимфатического узла или пораженного органа
Лечение
Скрытый TB
Обычно назначают длительный курс (от шести до девяти месяцев) антибиотика изониазида. Лечение продлевается, потому что антибиотики действуют при делении туберкулезных бактерий, а в случае латентного туберкулеза эти бактерии растут очень медленно.
Лечение продлевается, потому что антибиотики действуют при делении туберкулезных бактерий, а в случае латентного туберкулеза эти бактерии растут очень медленно.
Активный TB
Из-за широкого использования антибиотиков и других факторов, включая неправильное соблюдение режима лечения, у бактерий, вызывающих туберкулез, выработалась различная степень устойчивости к терапии. В странах с высоким уровнем доходов, таких как Канада, США, Австралия и Западная Европа, после постановки диагноза активного ТБ часто стандартной процедурой является взятие образца жидкости (из легких или другой пораженной ткани) и тестирование на бактерии ТБ. в лаборатории за их способность противостоять антибиотикам.
Лечение туберкулеза преследует две цели:
- улучшить здоровье людей, больных туберкулезом, вылечив их от этой инфекции
- сделать пациентов неинфекционными
Наиболее распространенным препаратом первой линии активного туберкулеза является комбинация следующих антибиотиков:
- изониазид
- рифампицин
- пиразинамид
- этамбутол
Дополнительные агенты первой линии включают следующие:
- рифабутин (микобутин) — иногда назначают вместо рифампицина ВИЧ-инфицированным
- стрептомицин — обычно не используется в странах с высоким уровнем дохода
У ВИЧ-инфицированных врачи начинают мощную комбинированную терапию от ВИЧ (обычно называемую АРТ) как можно скорее после постановки диагноза ТБ, поскольку это помогает повысить шансы на выздоровление и выживание. Врачам также, возможно, придется скорректировать схемы приема антибиотиков или АРТ, чтобы уменьшить потенциальные лекарственные взаимодействия.
Врачам также, возможно, придется скорректировать схемы приема антибиотиков или АРТ, чтобы уменьшить потенциальные лекарственные взаимодействия.
ВИЧ-инфицированных, инфицированных туберкулезом, подвержены риску развития ВСВИ — воспалительного синдрома восстановления иммунитета. Это происходит потому, что, когда начинается АРТ, иммунная система укрепляется и начинает распознавать микробы, которые раньше не могли распознавать и бороться с ними, и бороться с ними. В результате симптомы инфекции (например, туберкулеза) могут временно появиться или временно ухудшиться.Симптомы ВСВИ могут появиться от двух недель до двух лет после начала АРТ и связаны с воспалением. Они могут включать жар, увеличение лимфатических узлов и другие симптомы в зависимости от типа инфекции и пораженного органа.
В некоторых случаях, например при ВСВИ, связанном с туберкулезом, для уменьшения симптомов, вызванных воспалением, могут быть прописаны такие препараты, как кортикостероиды. ВСВС обычно возникает у людей с очень низким уровнем CD4 (менее 50 клеток).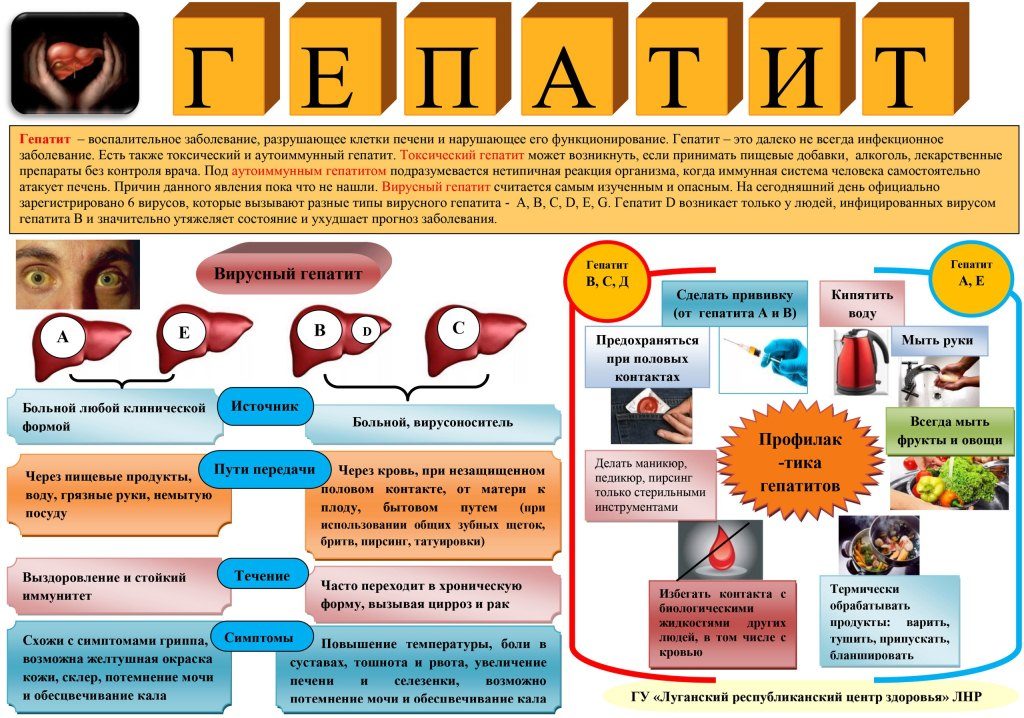
Доступны дополнительные антибиотики для лечения туберкулеза, но они, особенно препараты второго ряда, как правило, имеют больше побочных эффектов, могут потребоваться инъекции и могут потребоваться длительные курсы терапии.Это имеет место при лечении ТБ с множественной лекарственной устойчивостью (МЛУ).
Тестируются новые антибиотики для лечения туберкулеза.
Устойчивость к лекарствам
Вскоре после появления антибиотиков в 1950-х годах у бактерий, вызывающих туберкулез, появилась устойчивость к одному или нескольким агентам. Устойчивость к терапии является важной проблемой при лечении ТБ по следующим причинам:
- Антибиотики, обычно используемые для лечения туберкулеза, на несколько десятилетий старше новых антибиотиков, которые обычно используются для лечения других бактериальных заболеваний.Неудивительно, что противотуберкулезные препараты обладают неприятными побочными эффектами — факторами, которые не способствуют регулярному приему таблеток.

- Через несколько недель или месяцев лечения туберкулеза люди начинают чувствовать себя лучше и могут прийти к ошибочному выводу, что они излечены. Следовательно, они могут преждевременно прекратить прием антибиотиков.
- В некоторых случаях, например при коинфекции ВИЧ, антибиотики туберкулеза могут плохо всасываться.
Заражение лекарственно-устойчивыми бактериями ТБ может иметь серьезные последствия для пораженных людей.Мало того, что схемы лечения становятся более сложными и дорогими, но и повышается риск смерти. Например, исследователи из Квебека обнаружили, что устойчивость к антибиотику пиразинамиду связана с повышенным риском смерти. Исследователи из Центров США по контролю и профилактике заболеваний (CDC) обнаружили, что люди с туберкулезом, устойчивым к рифампицину или рифабутину, также подвергаются повышенному риску смерти.
Терапия второй линии
В Канаде препараты второго ряда доступны для лечения лекарственно-устойчивого туберкулеза. Однако препараты, используемые в терапии второго ряда, обычно имеют больше побочных эффектов, могут потребоваться инъекции и менее эффективны, чем препараты первого ряда. Примеры препаратов, используемых для терапии второй линии, включают следующее:
Однако препараты, используемые в терапии второго ряда, обычно имеют больше побочных эффектов, могут потребоваться инъекции и менее эффективны, чем препараты первого ряда. Примеры препаратов, используемых для терапии второй линии, включают следующее:
- моксифлоксацин, левофлоксацин
- амикацин, капреомицин, канамицин
- этионамид
- циклосерин
- пара-аминосалициловая кислота
- тиацетазон
Агенты третьей линии
Штаммы туберкулезных бактерий, устойчивые к двум или более антибиотикам, называются множественной лекарственной устойчивостью (МЛУ-ТБ).Факторы риска развития устойчивости к терапии второго ряда включают ВИЧ-положительный статус, наличие МЛУ-ТБ и начальное лечение ТБ любыми препаратами второго ряда. В таких случаях устойчивости используются препараты третьей линии, которые могут включать антибиотики, такие как линезолид (зивокс, зивоксам), клофазимин и кларитромицин. Обычно они не тестировались в крупных клинических испытаниях для лечения туберкулеза. Несколько лекарств разрабатываются для лечения туберкулеза.
Несколько лекарств разрабатываются для лечения туберкулеза.
Штаммы туберкулезных бактерий, устойчивые как минимум к изониазиду и рифампицину, как минимум к моксифлоксацину или левофлоксацину и как минимум к одному инъекционному антибиотику второго ряда, называются чрезвычайно лекарственно-устойчивыми (ШЛУ-ТБ).Такие штаммы туберкулеза очень тяжело поддаются лечению и требуют длительных курсов антибиотиков.
Профилактика
Вакцина с бациллами Кальметта-Герена (БЦЖ) частично защищает от инфекции ТБ. В Канаде эта вакцина широко не используется и предоставляется только детям из коренных народов и инуитов с высоким уровнем заболеваемости туберкулезом.
АРТ снижает риск заболеваний, вызванных инфекциями, связанными со СПИДом, но исследования показывают, что ВИЧ-положительные люди по-прежнему имеют повышенный риск развития ТБ по сравнению со здоровыми ВИЧ-отрицательными людьми.
Начало АРТ до того, как иммунная система будет серьезно ослаблена, и сдача анализов на латентную инфекцию ТБ — важные шаги по снижению риска развития заболевания, вызванного ТБ.
Список литературы
O’Donnell MR, Saukkonen JJ. Глава 168. Антимикобактериальные агенты. В: Longo DL, Fauci AS, Kasper DL, Hauser SL, Jameson JL, Loscalzo J, ред. Принципы внутренней медицины Харрисона . 18 изд. Нью-Йорк: Макгроу-Хилл; 2012 г.
Raviglione MC, O’Brien RJ. Глава 165. Туберкулез. В: Longo DL, Fauci AS, Kasper DL, Hauser SL, Jameson JL, Loscalzo J, ред. Принципы внутренней медицины Харрисона . 18 изд. Нью-Йорк: Макгроу-Хилл; 2012.
Fauci AS, Lane HC. Глава 189. Болезнь, вызванная вирусом иммунодефицита человека: СПИД и родственные заболевания. В: Longo DL, Fauci AS, Kasper DL, Hauser SL, Jameson JL, Loscalzo J, ред. Принципы внутренней медицины Харрисона . 18 изд. Нью-Йорк: Макгроу-Хилл; 2012 г.
Ершова Ю.В., Курбатова Е.В., Мунан П.К. и др. Приобретенная устойчивость к препаратам второго ряда среди больных туберкулезом в США. Клинические инфекционные болезни . 2012 декабрь; 55 (12): 1600-7.
Йи Д.П., Мензис Д., Брассард П. Клинические результаты микобактерий туберкулеза, устойчивых к пиразинамиду, в Квебеке. Международный журнал туберкулеза и болезней легких . 2012 Май; 16 (5): 604-9.
Fox W., Wiener A, Mitchison DA, et al. Распространенность лекарственно-устойчивых микобактерий туберкулеза у нелеченых больных туберкулезом легких; национальное обследование, 1955-56 гг. Туберкула . 1957 Апрель; 38 (2): 71-84.
Кешавджи С., Фармер П.Е. Туберкулез, лекарственная устойчивость и история современной медицины. Медицинский журнал Новой Англии . 2012 6 сентября; 367 (10): 931-6.
Althomsons SP, Cegielski JP. Влияние устойчивости к препаратам второго ряда на результаты лечения туберкулеза в Соединенных Штатах: МЛУ-ТБ достаточно плох. Международный журнал туберкулеза и болезней легких . 2012 Октябрь; 16 (10): 1331-4.
Au-Yeung C, Kanters S, Ding E, et al.Смертность от туберкулеза у ВИЧ-инфицированных: международная систематическая оценка. Клиническая эпидемиология . 2011 19 января; 3: 21-9.
Клиническая эпидемиология . 2011 19 января; 3: 21-9.
Альбанна А.С., Мензис Д. Туберкулез с лекарственной устойчивостью: каковы варианты лечения? Наркотики. 2011 7 мая; 71 (7): 815-25.
Усман О.А., Оквунду С., Гбенга К. и др. Оптимальное время начала антиретровирусной терапии для ВИЧ-инфицированных взрослых с впервые диагностированным туберкулезом легких: систематический обзор и метаанализ. Анналы внутренней медицины .2015 7 июля; 163 (1): 32-9.
Бриггс М.А., Эмерсон С., Моди С. и др. Использование профилактической терапии изониазидом для профилактики туберкулеза среди людей, живущих с ВИЧ / СПИДом: обзор литературы. ДЖЭЙДС . 2015, 15 апреля; 68 Приложение 3: S297-305.
Мдлули К., Канеко Т., Аптон А. Открытие и разработка лекарств от туберкулеза и новые цели в области лекарств. Перспективы Колд-Спринг-Харбор в медицине . 2015 29 января; 5 (6).
Моделирование коинфекций туберкулеза и гепатита B
Math. Модель. Nat. Феном. Vol. 5, No. 6, 2010, стр.
Модель. Nat. Феном. Vol. 5, No. 6, 2010, стр.
196-242
Моделирование туберкулеза и гепатита B
Коинфекции
С. Бовонг 1 , 2 , 4 * и Дж. Куртс 2 , 3
1
Лаборатория прикладной математики кафедры математики и информатики
Естественных наук, факультет естественных наук, Университет Дуала, Дуала, П.О.
Box 24157, Камерун
2
Постдамский институт исследований воздействия на климат (ПИК),
Телеграфенберг A 31,
14412
Потсдам, Германия
3
Физический факультет Университета Гумбольдта в Берлине,
12489
Берлин, Германия
4
UMI 209 IRD / UPMC UMMISCO, Бонди, Projet MASAIE INRIA Grand Est, Франция
Projet Grimcape, LIRIMA, Камерун
* Автор, ответственный за переписку: E-mail:
sbowong @ gmail. com
com
Аннотация
Туберкулез (ТБ) — основная причина смерти среди людей, инфицированных
вирус гепатита В (HBV). Изучение совместной динамики HBV и TB представляет собой серьезную проблему.
математические проблемы из-за того, что модели передачи достаточно
отчетливый. Мы формулируем и анализируем детерминированную математическую модель, которая включает
ко-динамики гепатита В и туберкулеза. Две подмодели, а именно: только HBV и
В первую очередь рассматриваются подмодели только для ТБ.В отличие от подмодели только для HBV, которая имеет
глобально-асимптотически стабильное равновесие без болезней, когда
число репродукций меньше единицы, субмодель только TB подвергается феномену
обратная бифуркация, при которой стабильное равновесие без болезней сосуществует со стабильным
эндемическое равновесие, для определенного диапазона ассоциированного числа воспроизводств менее чем
единство. Таким образом, для ТБ классическое требование наличия ассоциированного воспроизводства
Таким образом, для ТБ классическое требование наличия ассоциированного воспроизводства
число меньше единицы, хотя и необходимо, но недостаточно для его устранения.Также показано, что полная модель сочетанной инфекции HBV-TB подвергается обратной бифуркации.
явление. С помощью моделирования мы в основном обнаруживаем, что: i) эти две болезни будут сосуществовать
когда их частичное репродуктивное число превышает единицу; (ii) усиление прогрессирования
частота из-за экзогенного повторного заражения от латентного до активного туберкулеза у лиц с коинфекцией может
играют важную роль в росте распространенности туберкулеза; и (iii) увеличение
темпы прогрессирования инфекции HBV от острой стадии до хронической увеличили
уровни распространенности ВГВ и ТБ.
Классификация предметов по математике: 34A34 / 34D23 / 34D40 / 92D30
Ключевые слова: нелинейные динамические системы / эпидемиологические модели / туберкулез / гепатит B / стабильность
Лекарства пролонгированного действия от малярии, туберкулеза и гепатита C
Перепрофилирование ключевых лекарств в составы длительного действия может произвести революцию в профилактике и лечении
Проблемы
Когда лекарства принимаются неправильно, их эффективность снижается, что ведет к болезням, распространению болезней и смерти. Плохое соблюдение режима также помогает инфекционным микробам становиться устойчивыми к лекарствам, используемым для их лечения. Устойчивость к лекарствам — главное препятствие в борьбе с такими мировыми эпидемиями, как малярия, туберкулез и ВИЧ / СПИД.
Плохое соблюдение режима также помогает инфекционным микробам становиться устойчивыми к лекарствам, используемым для их лечения. Устойчивость к лекарствам — главное препятствие в борьбе с такими мировыми эпидемиями, как малярия, туберкулез и ВИЧ / СПИД.
Составы длительного действия могут доставлять лекарства в таких форматах, как пластыри или инъекции, которые могут длиться недели или месяцы, освобождая людей от ежедневного приема таблеток. Однако разработка препаратов длительного действия для некоторых лекарств, которые имеют критически важное значение для стран с низким и средним уровнем доходов, отстает.
Малярия, туберкулез и гепатит С (ВГС) непропорционально сильно поражают детей, бедные и маргинализованные сообщества, людей, употребляющих наркотики, и людей, живущих с ВИЧ. Около 90 процентов случаев заражения и смерти от малярии, 95 процентов инфекций и смертей от туберкулеза и 75 процентов случаев гепатита С происходят в странах с низким и средним уровнем дохода.
Решения
Продукты длительного действия произвели революцию в таких областях, как шизофрения и контрацепция, и могут значительно улучшить ответ на основные заболевания, от которых страдают страны с низким и средним уровнем дохода.Unitaid взяла на себя обязательство ускорить процесс разработки технологий длительного действия для удовлетворения потребностей стран с ограниченными ресурсами, а также работает над тем, чтобы лекарства длительного действия вводились быстрее и оставались доступными.
В рамках пятилетнего проекта LONGEVITY, возглавляемого Ливерпульским университетом, будут разработаны версии лекарств длительного действия для лечения гепатита С и профилактики малярии и латентного туберкулеза с целью подачи заявки на одобрение регулирующих органов. Грант создаст условия для коммерциализации продуктов длительного действия в наиболее пострадавших странах.
В рамках проекта также будет создан Центр передового опыта в области терапии длительного действия со специальной лабораторией для ускорения разработки продуктов и центром знаний, где можно будет делиться информацией между заинтересованными сторонами.
«Примерно десять лет назад, в 2009 году, появились сообщения о инъекционных препаратах длительного действия для лечения ВИЧ, и именно здесь эта концепция широко использовалась в отношении инфекционных заболеваний. Наш проект направлен на разработку лекарств длительного действия от других инфекционных заболеваний, которые несут серьезное бремя в странах с низким и средним уровнем доходов.”
Профессор Эндрю Оуэн, главный исследователь проекта ДОЛГОЛЕТИЯ
Эффект, которого мы добиваемся
Ожидается, что проект поможет пациентам добиться успеха в лечении, спасти и улучшить жизнь, бороться с устойчивостью к противомикробным препаратам и остановить распространение болезней.
Родственная инициатива Unitaid, проект GLAD, разрабатывает инъекции длительного действия для лечения ВИЧ.
Патентный пул лекарственных средств, финансируемый Unitaid, тем временем работает над тем, чтобы препараты длительного действия, разработанные в рамках новых проектов, были доступны в странах, где они необходимы.

 2
2