Уплотнение междолевой плевры. | Портал радиологов
Пнд, 03/11/2014 — 20:33
#1
Не на сайте
Был на сайте: 3 дня 17 часов назад
Зарегистрирован: 20.12.2009 — 17:28
Публикации: 7060
1. Не думаю, что это косая м\долевая плевра…там есть и в передне-медиальном отделе плевральный компонент.
2. А как вам правая в\доля?….все ли там спокойно?
Пнд, 03/11/2014 — 21:29
#2
Не на сайте
Был на сайте: 1 день 10 часов назад
Зарегистрирован: 13.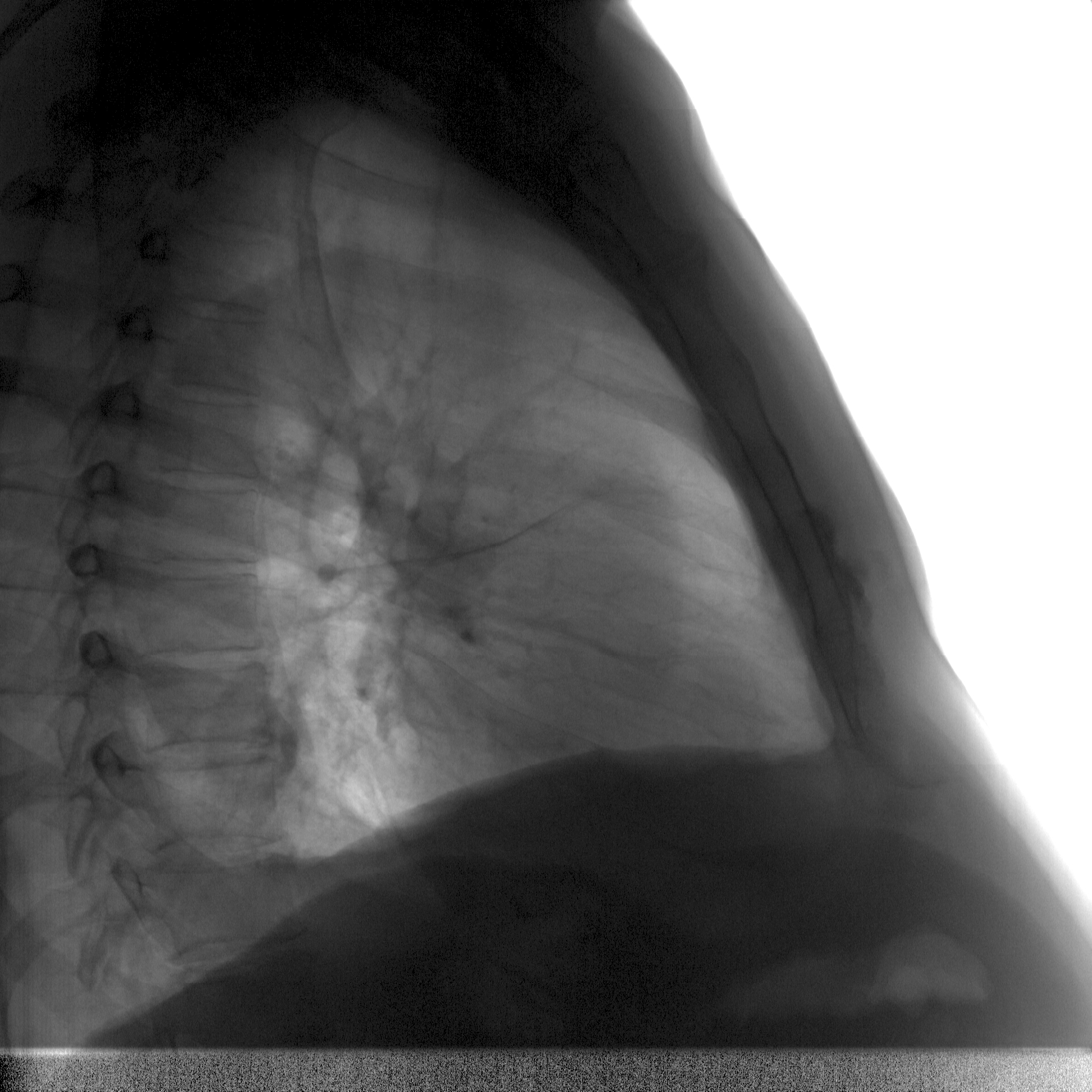 09.2011 — 22:55
09.2011 — 22:55
Публикации: 8480
Изменения в S2 правого лёгкого и кругляшка на первом ребре слева. Отмеченное похоже на ателектаз, но не видно по боковому.
Втр, 04/11/2014 — 10:13
#3
Не на сайте
Был на сайте: 11 месяцев 2 недели назад
Зарегистрирован: 26.12.2013 — 17:53
Публикации: 1015
stovbav, да, согласен с Вами, не всё там спокойно.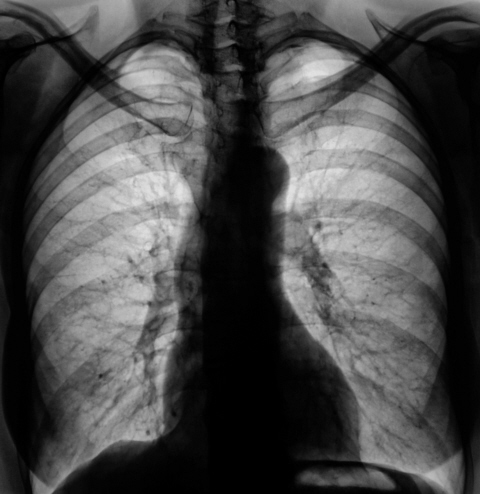 Будем вызывать опрашивать, дообследовать.
Будем вызывать опрашивать, дообследовать.
Втр, 04/11/2014 — 10:15
#4
Не на сайте
Был на сайте: 11 месяцев 2 недели назад
Зарегистрирован: 26.12.2013 — 17:53
Публикации: 1015
Я тоже так подумал насчёт ателектаза, но засомневался…
Втр, 04/11/2014 — 18:05
#5
Не на сайте
Был на сайте: 9 часов 47 минут назад
Зарегистрирован: 21. 12.2010 — 20:37
12.2010 — 20:37
Публикации: 4250
Левая косая междолевая щель свободна. Вдоль правой есть измения . Чем вызваны изменения на обзором снимке? Ответить затрудняюсь. Жду мнения коллег. См рисунок.
Втр, 04/11/2014 — 18:34
#6
Не на сайте
Был на сайте: 10 часов 2 минуты назад
Зарегистрирован: 25.11.2013 — 20:50
Публикации: 16886
Уважаемый Nikolas, а почему не наоборот? Жёлтым -правая, а красным — левая. А справа S 2 мне не нравится, как раз же за ребром прячется участок сгущенного легочного рисунка.
А справа S 2 мне не нравится, как раз же за ребром прячется участок сгущенного легочного рисунка.
«Слушай всех, прислушивайся к немногим, решай сам».©
Втр, 04/11/2014 — 19:13
#7
Не на сайте
Был на сайте: 9 часов 47 минут назад
Зарегистрирован: 21.12.2010 — 20:37
Публикации: 4250
Левая косая междолевая щель выше правой на высоту одного грудного позвонка. Особенно это хорошо видно при просмотре КТ фрагментов. Вначале появляется левая, затем правая косая междолевая щель.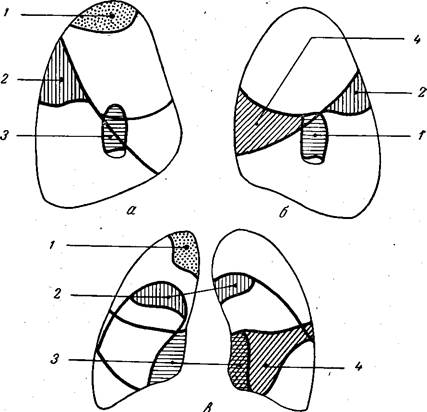 Пусть меня поправят. Найдем истину.
Пусть меня поправят. Найдем истину.
Синдром утолщения плевры. | Портал радиологов
Втр, 14/04/2009 — 09:14
#1
Не на сайте
Был на сайте: 4 года 8 месяцев назад
Зарегистрирован: 20.02.2009 — 12:27
Публикации: 227
Пациентка 48 лет, злоупотребляющая алкоголем, суицидальная попытка (уксусная эссенция). Снимок выполнен лежа.
В собранном при поступлении анамнезе — онкология по гинекологии (оперирована в 1996 году, не наблюдается), аппендэктомия, холецистэктомия. Заболевания легких отрицает.
Заболевания легких отрицает.
Век живи — век учись…
Втр, 14/04/2009 — 21:07
#2
Не на сайте
Был на сайте: 1 неделя 5 дней назад
Зарегистрирован: 14.04.2009 — 20:43
Публикации: 28
Пневмоторакс справа с признаками напряжения — смещение органов средостения влево. Причины в легком искать бессмысленно на фоне коллабированного легкогоя(я имею в виду mts). Но обратите внимание на задний отрезок IX ребра: перелома нет?
Наличие четкой круглой тени под правой ключицей от заглушки катетера в ВПВ наталкивает на мысль: не так уж часто (но бывает) легкое прокалывают анестезиологи при КВПВ.
Втр, 14/04/2009 — 21:26
#3
Не на сайте
Был на сайте: 6 месяцев 4 недели назад
Зарегистрирован: 07.06.2008 — 19:41
Публикации: 1779
Как то под «напряженный» пневмоторакс не подходит, учитывая анамнез данной пациентки и если коллега ни чего не утоила, то такое бывает и довольно часто.
«Знаешь, у некоторых врачей есть комплекс мессии — им необходимо спасать мир. А у тебя комплекс Рубика — тебе необходимо решать головоломки.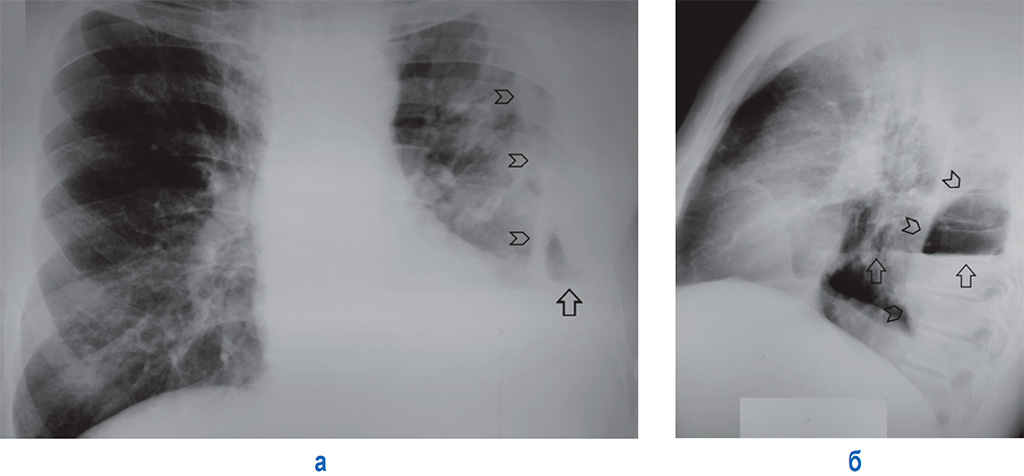 «
«
Втр, 14/04/2009 — 21:35
#4
Не на сайте
Был на сайте: 1 неделя 5 дней назад
Зарегистрирован: 14.04.2009 — 20:43
Публикации: 28
Не уловил: что бывает часто?
Синдром уплотнения легочной ткани при оценке компьютерно-томографических изображений органов грудной клетки в практике клинициста: патогенез, значение, дифференциальный диагноз | Карнаушкина
1. Тюрин И.Е. Компьютерная томография органов грудной полости. СПб: ЭЛБИ-СПб; 2003.
Тюрин И.Е. Компьютерная томография органов грудной полости. СПб: ЭЛБИ-СПб; 2003.
2. Verschakelen J.A., De Wever W. Computed Tomography of the Lung. A Pattern Approach. Springer; 2007.
3. Collins, J. CT signs and patterns of lung disease. Radiol. Clin. North. Am. 2001; 39 (6): 1115–1135.
4. Reed J.C. Chest Radiology. Plain Film Patterns and Differential Diagnoses. Mosby; 2011.
5. Тюрин И.Е. Рентгенодиагностика тяжелой пневмонии и гриппа. Лучевая диагностика и терапия. 2016; (1): 13–16. DOI: 10.22328/2079-5343-2016-1-13-16.
6. Reed J.C. Chest Radiology: Patterns and Differential Diagnoses. Elsevier; 2017.
7. Muller N.L., Silva C.I.S. The Teaching Files: Chest. Elsevier; 2009.
8. Winningham P.J., Martínez-Jiménez S., Rosado-de-Christenson M.L. et al. Bronchiolitis: A practical approach for the general radiologist. RadioGraphics. 2017; 37 (3): 777–794. DOI: 10.1148/rg.2017160131.
9. Аверьянов А.В. Лесняк В.Н. Коган Е.А. Редкие заболевания легких: диагностика и лечение. М.: Медицинское информационное агентство; 2016.
10. Georgiadou S.P., Sipsas N.V., Marom E.M., Kontoyiannis D.P. The diagnostic value of halo and reversed halo signs for invasive mold infections in compromised hosts. Clin. Infect. Dis. 2011; 52 (9): 1144–1155. DOI: 10.1093/cid/cir122.
11. Тюрин И.Е. Рентгенодиагностика внебольничных пневмоний. Поликлиника. 2013; (3-1): 7–11.
Тюрин И.Е. Рентгенодиагностика внебольничных пневмоний. Поликлиника. 2013; (3-1): 7–11.
12. Ланге С., Уолш Д. Лучевая диагностика заболеваний органов грудной клетки. Пер. с англ. под ред. С.К.Тернового, А.И.Шехтера. М.: ГЭОТАР-Медиа; 2010.
13. MacMahon H., Naidich D.P., Goo J.M. et al. Guidelines for Management of Incidental Pulmonary Nodules Detected on CT Images: From the Fleischner Society 2017. Radiology. 2017; 284 (1): 228–243. DOI: 10.1148/radiol.2017161659.
14. Reduced lung-cancer mortality with low-dose computed tomographic screening. The National Lung Screening Trial Research Team. N. Engl. J. Med. 2011; 365 (5): 395–409. DOI: 10.1056/NEJMoa1102873.
Клинический случай злокачественной мезотелиомы плевры
В. В. Прокопив, В.Н. Зеленый, А.С. Федорченко, Г.П. Демченко, А.Т. Биляч, Узловая больница станции Чернигов
В. Прокопив, В.Н. Зеленый, А.С. Федорченко, Г.П. Демченко, А.Т. Биляч, Узловая больница станции Чернигов
Злокачественная мезотелиома плевры (ЗМП) — синономы: карциносаркома плевры,
саркоматозная эндотелиома, рак плевры — агрессивная опухоль, которая развивается
при трансформации мезотелиальных клеток и характеризуется поражением как
париетальной, так и висцеральной плевры (Бычков М.Б. и соавт, 2005; Robinson
B.W., Lare R.A., 2005; Яблонський П.К., Петров А.С., 2006). Это относительно
редкое злокачественное новообразование встречается в любом возрасте, но чаще
после 40 лет, преимущественно у мужчин, которые в молодости работали или имели
длительный контакт с асбестом.
Среди этиологических факторов ЗМП ученые называют контакт с асбестом, что
показал в своих исследованиях I. Serikoff (1965), другими химическими
канцерогенами (силикатами, бериллием, жидким парафином), ионизирующее излучение.
В последние годы появились сообщения об этиологической роли вирусов (вируса
обезьян), а также генетической предрасположенности (Testa J. R. et al., 1998;
R. et al., 1998;
Shivapyrkal N. et al., 1999; Roushdy — Hammady et al., 2001).
По данным С. Boutin, в 92% случаев заболевание манифестирует развитием
гидроторакса, выявляемого с помощью объективных и рентгенологических методов
исследования. При этом рентгенография позволяет лишь заподозрить наличие ЗМП по
следующим признакам: утолщение париетальной плевры, гидроторакс, уменьшение
объема гемоторакса, смещение средостения в сторону поражения. Основным методом
диагностики ЗМП является компьютерная томография (КТ). Наиболее характерные
признаки ЗМП на томограмме: выпот в плевральной полости; узловое утолщение
париетальной плевры; расширение междолевых щелей; опухолевидные массы,
окружающие и сдавливающие легкое; уменьшение размеров гематоракса, смещение
средостения.
По данным J. Hierholzer, чувствительность КТ при диагностике ЗМП составляет 93%,
специфичность — 87%.
Окончательный диагноз, как правило, устанавливают после цитологического
исследования плеврального экссудата, торакоскопии и биопсии плевры (Aisher J. ,
,
Bueno R. еt al., 2004).
При гистологическом исследовании выделяют три морфологических варианта
мезотелиомы плевры: эпителиальный (50–70%), саркоматозный (7–20%) и смешанный
(20–25%). Наименее прогностически благоприятным считают саркоматозный вариант
заболевания (Kindler H.L., Vogelzang N.J., 1999; Гарин А.М., 2000).
В последние годы основное внимание отечественных и зарубежных исследователей
было уделено различным способам лечения ЗМП, однако ввиду небольшого числа
пациентов, биологических особенностей опухоли, отсутствия рандомизированных
исследований вопросы диагностики и лечения ЗМП остаются малоизученными.
Представляем наблюдаемый нами случай ЗМП.
Больная М., 38 лет, телефонистка, обратилась в поликлинику 06.12.2006 г. с
жалобами на общую слабость, боль в левой половине грудной клетки при кашле,
периодический кашель, одышку при ходьбе, повышенную температуру тела,
потливость, периодические ознобы.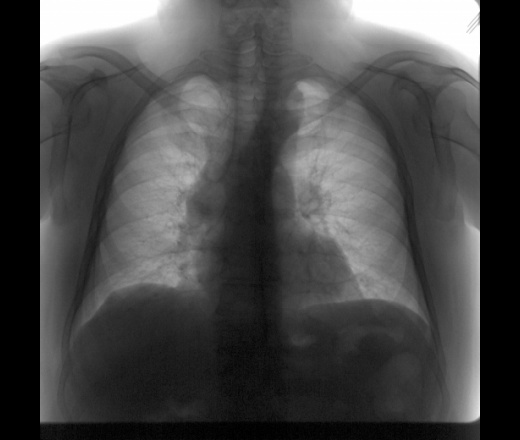 Считает себя больной на протяжении 2 недель,
Считает себя больной на протяжении 2 недель,
когда впервые отметила описанные симптомы, которые со временем стали проявляться
сильнее и чаще. Свое заболевание пациентка связывала с переохлаждением. При
объективном обследовании у пациентки отмечались крепитирующие хрипы в левых
задних отделах легких ниже угла лопатки, а также ослабление дыхания и
притупление перкуторного звука в этих областях. Правые отделы легких — без
особенностей. Общий анализ крови: эритроциты — 4,2 × 1012/л; гемоглобин — 132
г/л; цветовой показатель — 0,9; лейкоциты — 7,0 × 109/л; скорость оседания
эриторицитов — 20 мм/ч. Общий анализ мочи — без патологических изменений. На
рентгенограмме от 07.12.2006 г. отмечалось гомогенное затемнение ниже ІV ребра с
ровным контуром в плевральной полости. Для уточнения диагноза больная была
направлена на консультацию в областной противотуберкулезный диспансер. Был
установлен диагноз: левосторонняя нижнедолевая плевропневмония, осложненная
экссудативным плевритом. Назначено лечение: антибиотики, общеукрепляющие и
Назначено лечение: антибиотики, общеукрепляющие и
симптоматические средства.
Через 2 недели лечения состояние пациентки улучшилось, но продолжали беспокоить
кашель и боль в левой половине грудной клетки. На контрольной рентгенограмме от
19.12.2006 г. слева по реберному краю на всем протяжении от нижнего отрезка ІV
ребра книзу определяется интенсивное гомогенное затемнение с четким ровным
контуром за счет выпота в плевральной полости (количество его незначительно
уменьшилось по сравнению с данными от 07.12.2006 г.). Справа — без особенностей.
На КТ органов грудной клетки от 22.12.2006 г.: левое легочное поле незначительно
уменьшено в объеме; отмечается утолщение пристеночной, медиастинальной плевры и
междолевой плевры слева; в нижнем отделе плевральной полости слева имеется
свободная и осумкованная жидкость; органы средостения подтянуты влево за счет
массивных фиброзных тяжей.
Лимфатические узлы средостения и бронхопульмональной группы не дифференцируются
из-за плевральных наслоений медиастинальной плевры. Деструктивных изменений со
Деструктивных изменений со
стороны нижнегрудного отдела позвоночника не выявлено. Заключение: левосторонняя
плевропневмония. Плевральные наслоения в нижней доле левого легкого.
Данные бронхофиброскопии: сужение базальных бронхов слева за счет сдавливания.
10.01.2007 г. с помощью ультразвукового исследования (УЗИ) в левой плевральной
полости обнаружено умеренное количество жидкости, вероятнее всего осумкованной.
Пациентка продолжала назначенное лечение, но состояние ее не улучшилось. Она
была госпитализирована в областной противотуберкулезный диспансер, где
находилась с 17.01 по 1.02.2007 г. с диагнозом: левосторонний экссудативный
неспецифический плеврит. При повторной бронхофиброскопии выявлен диффузный
катаральный эндобронхит. Общий анализ крови: эритроциты — 4,2 × 1012/л;
гемоглобин — 120 г/л; лейкоциты — 6,2 × 109/л; эозинофилы — 2%; сегментоядерные
— 60%; моноциты — 1%; лимфоциты — 32%; скорость оседания эритроцитов — 10 мм/ч;
уровень глюкозы — 4,5 ммоль/л. Общий анализ мочи без патологических изменений.
Общий анализ мочи без патологических изменений.
Биохимический анализ крови в пределах нормы; проба на RW — отрицательная. На
электрокардиограмме — ритм синусовый, частота сокращений сердца — 78 в 1 минуту,
признаки гипертрофии левого желудочка. При исследовании мокроты в 3 пробах
микобактерии туберкулеза не выявлены. Анализ крови на ВИЧ — отрицательный. При
УЗИ органов брюшной полости патологии не выявлено. На рентгенограмме органов
грудной клетки от 29.01.2007 г. (прямая и боковая проекции) обнаружено
увеличение количества свободного выпота в базально-переднем отделе плевральной
полости слева (по сравнению с данными от 19.12.2006 г.) и появление его в
небольшом количестве сзади по реберному краю.
Проведенное лечение — цефтриаксон, оспамокс, десенсибилизирующая,
общеукрепляющая терапия и симптоматические средства — успеха не имело.
В связи с этим пациентка направлена на консультацию в Институт фтизиатрии и
пульмонологии имени Ф. Г. Яновского, где находилась на стационарном лечении с
Г. Яновского, где находилась на стационарном лечении с
02.02. по 05.03.2007 г. с диагнозом: левосторонний неспецифический экссудативный
плеврит. Проведено лечение — антибиотикотерапия, плевральные пункции с введением
антибиотиков, симптоматическая терапия.
Больной было рекомендовано дальнейшее лечение по месту жительства и повторная
консультация через 1 месяц. Состояние пациентки улучшилось. На контрольной
рентгенограмме от 03.03.2007 г. отмечалось уменьшение экссудата в левой
плевральной полости.
10.03.2007 г. состояние пациентки ухудшилось и она снова обратилась за
медпомощью в Узловую больницу с жалобами на слабость, кашель, утомляемость,
потливость, боль в грудной клетке слева, повышенную температуру тела,
периодический озноб.
Общий анализ крови при поступлении: эритроциты — 4,0 × 1012/л; гемоглобин — 120
г/л; лейкоциты — 5,6 × 109/л; скорость оседания эритороцитов — 15 мм/ч; уровень
глюкозы в крови — 4,4 ммоль/л. Общий анализ мочи без особенностей.
Биохимический анализ крови в пределах нормы. LE-клетки не выявлены. На повторной
КТ от 28.03.2007 г. отмечено уменьшение левого легкого в объеме. На всем
протяжении наблюдалось утолщение и уплотнение паракостальной плевры до 0,8 см. В
нижних отделах левой костальной плевральной полости определяется осумкованная
жидкость. Легкие без очаговых инфильтративных изменений. Просветы трахеи и
бронхов свободны на всех уровнях. Лимфатические узлы больше 1 см не
определяются. Со стороны органов средостения изменений не обнаружено.
Заключение: левосторонний адгезивный плеврит. Проведено лечение: авелокс 400 мг
— 7 дней, иммунокорригирующая терапия, мочегонные, гормонотерапия,
симптоматическая и общеукрепляющая терапия. Состояние пациентки улучшилось, и
30.03.2007 г. она была выписана с рекомендацией продолжить амбулаторное лечение.
Однако через месяц ее состояние снова ухудшилось. В связи с отсутствием эффекта
от проводимого ранее лечения больная была госпитализирована в торакальное
отделение областного противотуберкулезного диспансера с подозрением на
мезотелиому плевры, где находилась с 14.05 по 06.06.2007 г. Ей была проведена
операция — диагностическая торакотомия, декортикация, плевроэктомия. По
результатам цитологического исследования биопсийного материала установлен
заключительный диагноз: злокачественная мезотелиома плевры слева Т3 Nх, Mх рТх,
рNх, рМх; стадия ІІІ; клиническая группа ІІІ. Для дальнейшего лечения пациентка
переведена в областной онкологический диспансер, где проходит курсы лучевой
химиотерапии. Состояние больной удовлетворительное.
ХАРАКТЕРИСТИКА ОЧАГОВ В ЛЕГКИХ, ВЫЯВЛЕННЫХ ПРИ КОМПЬЮТЕРНОЙ ТОМОГРАФИИ У ДЕТЕЙ И ПОДРОСТКОВ ИЗ ГРУПП РИСКА ПО ТУБЕРКУЛЕЗУ | Шепелева
1. Лазарева Я.В. Компьютерная томография в диагностике туберкулеза органов дыхания: Дис. … д-ра мед. наук. М.; 2002.
2. Власов П.В., Нуднов Н.В., Шейх Ж.В. Компьютерно-томографическая семиотика в пульмонологии. Медицинская визуализация. 2010; 6: 75–83.
3. Воробьев А.А., Ловачева О.В., Варшавский О.В. и др. Возможности КТ-исследования органов грудной клетки больных туберкулезом легких на предоперационном этапе. Проблемы туберкулеза и болезней легких. 2005; 8: 23–6.
4. Колесникова Е.К., Георгиади С.Г. Компьютерно-томографическая картина лимфатических узлов средостения в норме. Вестник рентгенологии и радиологии. 1990; 4: 72–7.
5. Остроумова О.М., Ивановский В.Б., Грицай И.Ю. Компьютерная томография в комплексной диагностике туберкулеза органов дыхания. Туберкулез и болезни легких. 2011; 5: 88–9.
6. Харченко В.П., Котляров П.М. Методы медицинской визуализации в диагностике заболеваний органов дыхания. Пульмонология. 1999; 9: 48–52.
7. Webb W.R. High-resolution CT of the lung parenchyma. Radiol. Clin. North. Am. 1998; 27: 1085–97.
8. Aziz Z.A., Padley S.P., Hansell D.M. CT techniques for imaging the lung: recommendations for multi-slice and single slice computed tomography. Eur. J. Radiol. 2004; 24: 119–36.
9. Миллер С.В., Фролова И.Г., Величко С.А., Тузиков С.А. Одиночные округлые образования в легком, тактика ведения. Бюллетень сибирской медицины. 2012; 5: 80–2.
Органы грудной клетки здорового человека в рентгеновском изображении | Саламов Р.Ф., Семенова Н.А.
Теневая картина органов грудной клетки представляет собой плоскостное изображение всех органов и тканей, входящих в ее состав. Чтобы правильно расшифровать теневую картину рентгенограммы, необходимо на основе знаний топографической анатомии грудной полости суметь перевести анатомические понятия в скиалогические. Основная трудность заключается в том, что анатомические образования, расположенные на разной глубине грудной клетки, могут изобразиться на снимке рядом или накладываясь друг на друга. Следует учитывать, что на рентгенограмме не удается получить истинных размеров анатомических образований из-за расходящегося хода рентгеновских лучей. Большое значение в правильном истолковании теневого изображения имеют и технические параметры, которые используют при получении каждого конкретного снимка. Поэтому, чтобы во всей полноте изучить теневую картину органов грудной клетки и избежать ошибок при ее расшифровке, лучевой диагност должен учитывать все эти факторы и строго придерживаться алгоритма исследования рентгенограммы:
1) Оценка качества рентгенограммы грудной клетки.
2) Оценка теневой картины органов грудной клетки:
а) изучение мягких тканей;
б) изучение костной системы;
в) изучение диафрагмы и синусов;
г) изучение корней легких;
д) изучение легочных полей;
е) изучение органов средостения.
Оценка качества рентгенограммы
Качество технического исполнения рентгенограммы грудной клетки включает в себя: паспортную часть рентгенограммы, полноту охвата грудной клетки, положение больного во время снимка, контрастность рентгенограммы, жесткость и четкость, наличие артефактов. Все характеристики хорошего качества мы приведем для наиболее часто используемой передней прямой проекции, которая выполняется при ортопозиции пациента, плотно прилегающего передней поверхностью грудной стенки к кассете с пленкой, а рентгеновский луч по отношению к исследуемому направлен сзади наперед.
Паспортная часть рентгенограммы содержит: фамилию, имя, отчество, возраст пациента, дату и место проведения исследования. Полнота охвата грудной клетки включает в себя изображение всей грудной клетки, от верхушек легких до реберно-диафрагмальных синусов.
Положение больного во время снимка должно быть правильным, что оценивается по симметричному расположению грудинно-ключичных сочленений относительно средней линии, проведенной через остистые отростки позвонков. Расстояние между грудинно-ключичными сочленениями и срединной линией, проведенной через остистые отростки позвонков, должно быть одинаковым. В оценку правильности установки больного входит также отсутствие на легочных полях теней лопаток — они должны находиться кнаружи от легочных полей.
Критерием четкости рентгенограммы является одноконтурность изображения передних отрезков видимых на рентгенограмме ребер, поскольку они являются наиболее подвижными органами. Их смещения возможны даже при поверхностном дыхании пациента, что приводит к нечеткости рентгеновского снимка.
Контрастность рентгенограммы определяется ее цветовой гаммой — от белого до черного, т. е. при изучении контрастности снимка следует сравнить изображение органов, дающих максимальную плотность, с органами, почти не задерживающими рентгеновское излучение. Наиболее плотные тени дают органы средостения и печень — их принимают за абсолютное затемнение. Участки легочных полей, проецирующиеся в межреберные промежутки представлены на рентгенограммах просветлениями, так как рентгеновское излучение они почти не задерживают. Разница в цветовом изображении затемнений и просветлении дает представление о контрастности снимка.
Жесткость рентгенограммы зависит от жесткости рентгеновского излучения, т.е. от его проникающей способности или от длины волны. Известно, что рентгеновское излучение обладает меньшей или большей проникающей способностью в зависимости от длины волн. В зависимости от конституции пациента условия съемки должны быть подобраны так, чтобы получился снимок средней жесткости. Критерием оптимальной (средней) жесткости является видимость на рентгенограмме тел 3—4 верхних грудных позвонков; все остальные позвонки могут быть видны в виде единой колонны на фоне органов средостения или сливаться с ним (рис. 1). При недостаточной жесткости, т.е. на мягком снимке, позвоночный столб не дифференцируется. Рентгенограмму следует считать жесткой, если позвоночный столб виден состоящим из тел позвонков, отделенных друг от друга просветлениями межпозвоночных дисков. Мягкие и жесткие рентгенограммы делают по особым показаниям. Стандартными являются снимки средней жесткости, которые обладают таким достоинством, как максимальная контрастность.
Обязательность отсутствия артефактов или изображения посторонних предметов на снимке не требует пояснений. Чтобы достичь этого, необходимо полностью освободить от одежды изучаемую область и проверить, не попали ли в рентгеновские кассеты посторонние предметы.
Если рентгенограмма удовлетворяет всем предъявляемым к ней техническим требованиям, то она как объективный клинический документ подлежит изучению.
Оценка теневой картины органов грудной клетки
Мягкие ткани
Сразу оговоримся, что к “мягким тканям” относят все образования, покрывающие снаружи грудную клетку и дающие на хороших по качеству рентгенограммах теневые изображения, которые могут симулировать патологические процессы. К ним относят грудинно-ключично-сосцевидные мышцы, которые создают симметричные затемнения с четким наружным контуром в медиальных отделах обеих верхушек. Наружная граница грудинно-ключично-сосцевидной мышцы проекционно переходит в четкий контур дубликатуры кожной складки над ключицей, представленной малоинтенсивной тенью шириной не более 0,3 см, расположенной параллельно ключице. Эта полоска обычно отсутствует у лиц с выполненной жировой клетчаткой надключичной ямкой.
Грудные мышцы отображаются в виде симметрично или односторонне расположенных теней средней плотности, треугольной формы, с направленной к головке плечевой кости вершиной и подчеркнутым нижнелатеральным контуром, обычно уходящим за пределы костного остова грудной клетки. Они видны чаще у мужчин в верхнелатеральных отделах легочных полей (рис. 2).
Тени молочных желез занимают нижние отделы легочных полей и в зависимости от размера дают симметрично расположенные тени разной интенсивности (рис. 3). При провисающем типе молочных желез отчетливо видны их нижние выпуклые границы за счет дубликатуры кожной складки. При пуговчатом типе молочных желез, когда отсутствует дубликатура кожи, их тени не имеют четкого нижнего контура. У мужчин молочные железы видны в пожилом возрасте и на рентгенограмме сходны с провисающими молочными железами женщин. Соски молочных желез отображаются с одной или с обеих сторон симметрично в виде крупно- или среднеочаговых теней средней плотности с довольно четкими контурами. Геометрическая форма соска — цилиндр, усеченный конус или сегмент шара. Соски видны чаще у мужчин, поскольку в отличие от женщин во время производства рентгенограмм их небольшие молочные железы не смещаются.
Костная система
При изучении костного остова грудной клетки следует обратить внимание на симметричность обеих ее половин, ребер и межреберных промежутков, вертикальное положение позвоночного столба, остистые отростки которого служат для рентгенолога осью симметрии. Наиболее ясно видны тела первых 3—4 позвонков, чему способствует светлая полоска, отображающая трахею, которая содержит воздух и ослабляет в верхней части плотность тени средостения. На этом же уровне определяются тени поперечных отростков.
Контуры ребер четкие, ровные, за исключением нижних контуров задних отделов. Структура ребер мелкопетлистая, больше выраженная в передних отделах. Полосообразные тени ребер, проецирующиеся на прозрачном легочном фоне, четко определяются в количестве 6—7 пар, видны также боковые и задние отрезки большинства нижних ребер. Передние отрезки ребер стоят значительно ниже задних и направлены изнутри снизу вверх. Места прикрепления ребер к грудине у взрослых людей не видны, так как медиальные участки их передних отделов представлены хрящом, который на рентгенограмме не определяется. Окостенения в хрящевой части ребер обусловливает появление конгломератов неправильной формы или очаговоподобных разновеликих теней во внутренних зонах легочных полей. Раньше всех окостеневает передний отрезок I ребра, что может наблюдаться уже с возраста 16—18 лет. Задние, более плотные концы ребер дают интенсивные тени, которые направлены в продолжение передних концов снаружи внутрь и вверх к соответствующему позвонку. В некоторых случаях из-за суммации теней внутреннего конца заднего отрезка ребра с поперечным отростком позвонка могут образовываться крупные очаговоподобные тени в паравертебральной области и в проекции корней легких.
К анатомическим особенностям следует отнести наличие вилочкообразных (ребра Люшка) и добавочных шейных ребер, которые могут быть расценены как патологические процессы. Ребра Люшка могут располагаться односторонне, симметрично, несимметрично (рис. 4). Раздвоение чаще локализуется в переднем отделе ребра, реже — в заднем и боковом.
Тень ключиц проецируется на верхние участки легочных полей. При правильной установке пациента медиальные концы ключиц симметрично отстоят от тени рукоятки грудины и позвоночника и расположены на уровне третьего межпозвонкового пространства. Костная структура ключиц не везде равномерна. В области медиального отрезка ключицы костные трабекулы могут располагаться более концентрированно ближе к компактному ее веществу, оставляя прозрачным внутреннюю часть ключицы и симулируя полость в легком.
Тень грудины на прямой рентгенограмме может быть видна частично: справа и слева от срединной тени выступают лишь фасетки рукоятки грудины, расположенные несколько ниже внутренних концов ключицы. При неправильной трактовке эти тени могут быть приняты за увеличенные лимфатические узлы средостения.
Диафрагма и синусы
Диафрагма ограничивает снизу легочные поля куполообразной тенью. В своей центральной части она стоит наиболее высоко, к периферии легочных полей тень диафрагмы довольно круто спускается книзу и образует острые реберно-диафрагмальные углы — синусы. В медиальных отделах тень диафрагмы образует с тенью органов средостения кардиодиафрагмальные синусы, которые менее глубоки, чем реберно-диафрагмальные, а острота их углов значительно варьирует, особенно слева — от острого до тупого. Высота стояния диафрагмы изменяется в зависимости от возраста и конституции. У взрослых людей при глубоком вдохе купол диафрагмы расположен справа на уровне переднего отрезка V—VI ребер, слева — на 1 ребро ниже. В положении глубокого вдоха средняя часть купола диафрагмы уплощается. При значительной дыхательной экскурсии, что наблюдается обычно у спортсменов, контур диафрагмы может быть зубчатым, причем зубцы расположены достаточно симметрично и каждый зубец подходит к верхним краям передних концов ребер, что отражает места прикрепления отдельных групп мышц сухожильными волокнами к верхним краям ребер. Правый купол диафрагмы сливается с тенью печени, под левым куполом обычно видно одно или два просветления, отображающие газ в своде желудка и в селезеночном углу толстой кишки.
Корни легких
Корни легких с точки зрения анатомии представляют собой совокупность определенным образом топографически расположенных анатомических элементов: легочной артерии, легочной вены, бронхов, лимфатических сосудов и узлов, нервов, клетчатки, плевры. При этом следует учитывать, что на большом своем протяжении указанные образования лежат экстрапульмонально, а потому на рентгенограмме скрыты плотной тенью средостения. Общепринятое в рентгенологии деление тени корня легкого на верхнюю часть (или головку), среднюю (или тело) и нижнюю (или хвостовую), не воспроизводит анатомических частей корня, но по практическим соображениям сохраняется (рис. 5). Основная роль в тенеобразовании корня легкого принадлежит легочной артерии, в меньшей степени — легочным венам, при обязательном сопровождении их бронхами, вносящими элемент контрастности в изображение корня, а потому “рентгеновский” корень легкого представляет собой совокупность сосудисто-бронхиальных элементов (рис. 6, 7). Остальные анатомические составляющие корня принимают ничтожное участие в его тенеобразовании.
Расположение корней легких с обеих сторон неодинаково, что отражает отсутствие их анатомической симметрии. Так, правый корень представлен лентовидной дугообразно искривленной в верхнем отделе и суживающейся книзу тенью средней плотности с верхней границей на уровне II ребра — II межреберья. Между тенью правого корня и тенью средостения отчетливо определяется просветление, обусловленное промежуточным и нижнедолевым бронхами. Слева тень корня обычно в большей или меньшей степени скрыта тенью сердца, только у 3—5% пациентов левый корень виден полностью. В соответствии с особенностями анатомического положения левой легочной артерии, верхняя граница тени левого корня располагается на одно ребро выше правого.
Тень корня легкого средней плотности, никогда не бывает однородной: она состоит из тяжеобразных, овальных, округлых теней, представляющих собой проекционное наложение на легочную артерию ее собственных разветвлений, а также верхних и нижних зональных и сегментарных легочных вен. В отдельных местах плотность тени корней уменьшается продольной или поперечной проекцией наслаивающихся на них бронхов. Видимость на рентгенограмме указанных анатомических образований определяет структуру корня легкого.
Наружная граница тени корня не представляет собой сплошную ровную линию: от нее в сторону расходится большое количество сосудистых теней, обусловленных разветвлениями легочных артерий и вен. Направление артерий более вертикальное, вены идут преимущественно горизонтально. На отдельных участках контур корня легкого становится менее четким из-за наслоения просветлений от бронхов. Обрезав мысленно сосудистые и бронхиальные разветвления, можно ясно наметить границы компактной части тени корня, которая имеет несколько вогнутое или прямолинейное направление. Нижняя часть корня (хвост) образована местом разветвления легочной артерии и вен. Тени корней, расположенные по обе стороны средостения, тянутся почти до уровня диафрагмы. Ширина корней легких представляет собой ширину главного артериального ствола и в норме равна ширине просвета основного бронха, отделяющего сосудистый ствол от тени средостения. Размер этот не должен превышать 1,5 см.
Легочные поля
На прямой рентгенограмме можно видеть правое и левое легочные поля, которые представляют собой проекцию легких на плоскость рентгеновской пленки. Правое легочное поле короткое и широкое, левое — узкое и длинное за счет особенностей расположения органов средостения и куполов диафрагмы. Окружая органы средостения, легкие как бы окутывают их и потому частично проецируются на срединную тень. Эти части легкого, а также области легкого, прикрытые диафрагмой, на прямой рентгенограмме не видны. Лучше всего их видно в боковых и косых проекциях.
Для удобства легочные поля принято делить на 3 пояса и 3 зоны. Проведенные на уровне нижних краев II и IV ребер горизонтальные линии делят легочное поле на 3 пояса — верхний, средний и нижний. Надключичная область или верхушки легких ни к одному из поясов не относятся. Вертикальные линии, проведенные через точку пересечения ключицы с наружным реберным контуром и через середину отрезка ключицы, проецирующегося на фоне легочного поля, делят легочное поле на 3 зоны — внутреннюю, среднюю и наружную.
Основная характеристика легочных полей — их прозрачность, которая определяется тремя основными факторами: воздухонаполнением, кровенаполнением сосудов, количеством паренхимы легкого. Соотношение этих факторов обусловливает степень прозрачности легочных полей. Очевидно, что прозрачность прямо пропорциональна количеству воздуха, содержащегося в легких, и обратно пропорциональна количеству кровеносных сосудов и легочной ткани на единицу объема.
Помимо внутрилегочных факторов на прозрачность легочных полей влияет и состояние грудной стенки. Так, прозрачность зон и поясов в нормальных условиях неодинакова из-за проеционного наложения на них мягких тканей грудной клетки. Поэтому у мужчин наиболее прозрачны нижние пояса, затем — верхние и наименее прозрачны средние пояса; у женщин — наименее прозрачны нижние пояса из-за наложения теней молочных желез, наиболее прозрачны верхние пояса. Прозрачность зон как у мужчин, так и у женщин убывает от средней к латеральной и внутренней зонам.
Легочные поля имеют хорошо выраженный и сложный легочный рисунок. Анатомическим субстратом легочного рисунка в нормальных условиях являются легочные сосуды — артерии и вены. Роль стенок бронхов и других внутрилегочных элементов в образовании легочного рисунка чрезвычайно мала. В основном легочный рисунок представлен тяжеобразными переплетающими тенями неравномерной интенсивности. Эти тени местами усиливаются от перекреста с другими сосудистыми веточками или ослабляются от перекреста с бронхами, лежащими в продольной и поперечной проекциях. Наряду с тяжеобразными тенями в легочных полях отмечаются округлые и овальные большой плотности теневые образования (поперечные сечения сосудов), рядом с которыми заметны кольцевидные затемнения с просветлениями внутри (просветы бронхов).
В силу уменьшения калибра кровеносных сосудов по направлению к периферии характер легочного рисунка в разных отделах легочного поля неодинаков. Если проследить за его особенностями по горизонтали в соответствии с делением легочного поля на зоны, видно, что легочный рисунок наиболее богат в медиальных зонах, где располагаются крупные сосудистые стволы. В средних зонах он становится беднее вследствие уменьшения калибра кровеносных сосудов. В латеральных зонах прослеживаются лишь отдельные сосудистые веточки. В краевой каемке легочных полей шириной 1—1,5 см легочный рисунок не должен быть виден. По вертикали закономерности образования легочного рисунка те же, что и в зональном направлении. Наиболее густой легочный рисунок отмечается в нижних поясах, где проецируется большое количество конечных разветвлений легочных артерий и вен. В верхних отделах легочный рисунок постепенно становится более бедным, а в области верхушек совсем не прослеживается или едва виден.
Долевое и сегментарное строение легких
На обзорных снимках отображается преимущественно суммированная масса всей легочной ткани. Большинство легочных долей наслаиваются друг на друга за исключением над- и подключичной областей, наружных реберно-диафрагмальных углов, куда соответственно проецируются верхняя и нижняя доли. Поэтому нет никаких опорных пунктов, на основании которых можно точно очертить границы отдельных долей. Однако при уплотнении листков плевры или совпадении направления рентгеновских лучей с ходом междолевых борозд на прямой рентгенограмме можно увидеть изображение добавочной междолевой щели в виде тонкой линии затемнения, горизонтально идущей на уровне III межреберья — IV ребра. Видимость на прямом снимке добавочной междолевой щели позволяет точно определить нижнюю границу верхней и верхнюю границу средней доли.
На боковой рентгенограмме и при тех же условиях отчетливо определяются тонкие тени главной и добавочной междолевой борозд, являющихся анатомическими границами верхней, средней и нижней доли (рис. 8). Чаще на прямых рентгенограммах нормальной грудной клетки проекции легочных долей определяются ориентировочно. При этом необходимо принимать во внимание известные основные топографо-анатомические данные о расположении междолевых границ.
Границы отдельных долей на передней прямой рентгенограмме грудной клетки проецируются следующим образом: известно, что граница правой главной междолевой борозды начинается сзади от уровня II грудного позвонка. Отсюда она идет косо снаружи и вниз в направлении передних отделов ребер и спускается к диафрагме на уровне IV ребра. Верхняя граница левой главной междолевой борозды находится несколько выше правой, спуск ее к диафрагме менее пологий. Добавочная междолевая щель у большинства людей имеется только в правом легком. Начинаясь от главной междолевой борозды на уровне IV ребра, она отделяет верхнюю долю от нижней и имеет горизонтальное направление. Таким образом, правое легочное поле делится на область проекций верхней, средней и нижней долей. Верхняя доля проецируется от верхушки до IV ребра. Здесь ее нижняя граница может определятся в виде очень тонкой горизонтальной линии, ниже которой расположена средняя доля. Средняя доля лежит в передневнутреннем отделе нижней части правой грудной полости. Ее верхняя плоскость граничит с основанием верхней доли, снаружи ее граница проекционно совпадает с направлением переднего конца VI ребра. Таким образом, нижненаружный участок правого легочного поля, расположенный ниже переднего конца VI ребра, занимает боковые отделы только нижней доли. С учетом анатомических особенностей уровня расположения передних концов ребер и тел позвонков изображение всей нижней доли справа проецируется на область легочного поля, начиная от II ребра вплоть до диафрагмы. Таким образом, от II до IV ребра нижняя доля проекционно наслаивается на верхнюю, а выше II ребра в над- и подключичное пространство проецируется только верхняя доля.
Слева проекция верхней доли соответствует сумме проекций верхней и средней долей справа. Нижняя доля слева занимает те же участки легочных полей, что и справа. Таким образом, в левом легочном поле, как и справа, изолированно без суперпозиций в над- и подключичное пространство проецируется верхняя доля, ниже и латеральнее переднего отрезка VI ребра у края грудной стенки — только нижняя доля.
Наиболее постоянными являются главные и правая добавочная междолевые борозды. Однако могут наблюдаться гомологичные междолевые борозды. В этом случае легкое может состоять из большего числа долей. Так, если в легком имеется задняя междолевая борозда, как продолжение кзади добавочной междолевой щели, то верхушка нижней доли правого легкого является самостоятельной задней долей. Слева возможно наличие язычковой доли — гомолога средней доли справа, отделенной от верхней, как и справа, добавочной междолевой щелью. Околосердечная доля образуется за счет медиального отдела нижней доли, обычно справа. Размеры этой доли могут быть различными в зависимости от участка нижней доли, отсеченного косо расположенной добавочной междолевой бороздой.
По механизму образования несколько особняком стоит добавочная доля непарной вены (lobus venae azygos). Ее образование ставится в связь с пороком развития. В процессе онтогенеза v.azygos должна расположиться на верхнем контуре правого главного бронха, обойдя медиально верхушку легкого. При нормальном состоянии эта вена проецируется в виде овальной, довольно плотной тени в месте перехода правого контура трахеи в верхний контур правого главного бронха. Если v.azygos не огибает верхушку легкого, а как бы прорезает ее, увлекая за собой висцеральный и париетальный листки плевры, то образуется глубокая борозда, включающая четыре листка плевры, которая отделяет тот или иной участок верхней доли правого легкого. На рентгенограмме отшнурованная внутренняя часть верхушки легкого ограничена снаружи тонкой гладкой линейной тенью, которая книзу заканчивается каплеобразной тенью (проекцией непарной вены). Добавочная доля непарной вены может иметь различные размеры, прозрачность ее, как правило, снижена.
Каждая доля легкого состоит из определенного числа независимых участков — сегментов легкого. Самостоятельность этих отдельных частей обусловлена наличием определенного бронхососудистого пучка, который ветвится в строго определенном отделе каждой доли. Согласно Международной схеме принято выделять 10 основных легочных сегментов справа и 9 сегментов слева (рис. 9).
Боковая рентгенограмма производится в ортопозиции пациента, плотно прижатого к кассете исследуемой стороной, с поднятыми на голову руками. Снимок делают на высоте вдоха. Хорошего качества рентгенограмма включает в себя достаточную полноту охвата, контрастность, четкость, правильную установку, отсутствие артефактов. Контрастность рентгенограммы устанавливается сравнением плотной тени правого поддиафрагмального пространства со светлым участком легкого, проецирующегося в ретростернальное пространство за рукояткой грудины. Достаточная разница в цветовом изображении затемнений и просветлений свидетельствует о контрастности снимка. Четкость определяется по одноконтурности костных образований. О правильной установке больного свидетельствует строго в профиль расположенная грудина.
Тени мягких тканей на боковом снимке по отдельности не дифференцируются, но они более интенсивны в верхних отделах снимка, куда проецируются массивные мышцы спины, плечевого пояса и шеи. Вследствие этого достаточная прозрачность легочного поля в боковой проекции обычно начинается только от уровня I межреберья, из-за чего верхушка легкого плохо видна.
Из теней костного скелета определяется внутренний конец прилежащей ключицы, которая спускается косо вниз и кпереди, образуя ясно видное грудинно-ключичное сочленение. Ниже внутреннего конца ключицы спереди в профиль располагается грудина, дифференцирующаяся на рукоятку, тело, мечевидный отросток. Тень позвоночника видна не на всем протяжении — раздельно определяются тела II—XI позвонков, на которые наслаивается прозрачное легкое. На задние отделы тел позвонков наслаиваются округлые тени ортоградно идущих поперечных отростков. Тени лопаток видны не полностью — в основном они сливаются с мягкими тканями спины, а наружный край лопаток проецируется на тень позвоночника или перед ним. Тени ребер прилежащей к пленке стороны начинаются от округлых теней осевой проекции поперечных отростков. Вначале лентообразные тени ребер образуют крутые дуги кзади от позвонков, достигают передней стенки грудной клетки, не выходя спереди за изображение грудины. Тени I ребра не видно, поэтому счет ребер ведется от II ребра прилежащей стороны, которая легко определяется по месту его соединения с грудиной — у сочленения ее рукоятки с телом. Сзади, напротив переднего отрезка II ребра лежит тело VI позвонка. Тени ребер противоположной стороны более широкие и проекционно не совпадают с одноименными ребрами прилежащей стороны, которые более узки, структурны, контуры их видны резче. Костные ориентиры используют для определения границы между долями, когда линейные тени междолевых листков плевры на боковых снимках не видны. Так, соединив мысленно тело IV позвонка с передним костодиафрагмальным синусом можно получить проекцию главной междолевой щели. Проведя горизонтальную линию по переднему отрезку IV ребра (от корня легкого перпендикулярно грудине) — проекцию добавочной междолевой щели.
Верхушечный сегмент верхней доли расположен в куполе легочного поля (рис. 9). Сзади к нему прилежит II задний сегмент верхней доли, кпереди и кнаружи — III передний сегмент верхней доли. В средней доле IV сегмент — наружный, расположен в углу между горизонтальной и нижней частью косой междолевой щели. Кпереди от наружного находится V внутренний сегмент.
Верхушку нижней доли занимает сегмент, нижняя граница которого определяется линией, мысленно продолженной кзади от добавочной междолевой щели. Остальные сегменты располагаются в основании нижней доли таким образом, что на боковой рентгенограмме VII сегмент наслаивается на VIII, IX и на Х, занимая по площади разные участки. Так, VII медиально-базальный примыкает к нижней части главной междолевой щели и заходит в передний костодиафрагмальный синус; XI — латерально-базальный, находясь между VIII и X сегментами, частично перекрывает заднебазальный сегмент и заходит в область наружного синуса. Х заднебазальный сегмент вверху граничит с VI сегментом и занимает большой объем заднемедиальных отделов нижней доли.
Слева локализация и число сегментов несколько иные, чем справа. Так, I и III сегменты чаще объединяются в один задневерхушечный из-за общего вентилирующего их бронха. Средней доли слева нет. Ее гомолог — язычковый сегмент, обычно не отделенный от верхней доли междолевой щелью, делится на IV верхний язычковый и V нижний язычковый сегменты, так что на боковой рентгенограмме IV сегмент располагается над V. Кроме того, слева отсутствует VII сегмент.
Органы средостения
Рентгенологическое исследование органов грудной клетки завершает изучение тени органов средостения. Занимая несколько асимметричное положение, сердце большей своей частью располагается в левой половине грудной клетки, формируя на внутренней поверхности легкого вдавления и борозды. Тень сердца по структуре однородна и имеет большую плотность. Положение сердца в зависимости от конституции человека — косое, горизонтальное или вертикальное. Соответствие размеров сердца размерам грудной клетки определяется по сердечно-грудному индексу, который в норме равен 0,5, и по уровню расположения кардиовазального угла.
Таким образом, стандартными проекциями, наиболее часто используемыми в практике для изучения органов грудной клетки, являются передняя прямая, правая и левые боковые, I и II косые проекции. Информация, полученная при их изучении, позволяет получить объективное представление о состоянии органов грудной клетки. Знание нормы — это та основа, на которой строится возможность разграничения здоровья и болезни.
| Приложения к статье |
| Рис. 1. Рентгенограмма органов грудной клетки А. Средней жесткости, видны тени молочных желез. |
| Рис. 1. Рентгенограмма органов грудной клетки Б. Малой жесткости (мягкая). В. Высокой жесткости (жесткая). |
| Рис. 2. Тени больших грудных мышц. |
| Рис. 3. Вариант нормы: справа видна тень провисающей, слева — пуговчатой молочной железы. |
| Рис. 4. Вилочкообразное ребро справа. |
| Рис. 5. На рентгенограмме видны корни легких с обеих сторон. |
| Рис. 6. Ангиограмма легочных артерий. |
| Рис. 7. Прямая бронхограмма. |
| Рис. 8. Боковая рентгенограмма хорошего качества с видимыми междолевыми бороздами. |
| Рис. 9. Схема сегментарного строения легких. |
.
Ответы
Рак левой молочной железы T3h2Mo 3 a ст 2 кл гр л/у слева, очаг в левом легком
Архивная запись
Здравствуйте,у тети обнаружили рак, подскажите пожалуйста, какие прогнозы возможны при таком диагнозе и какое лечение наиболее оптимально. Молочные железы D=S, сосково ареолярные комплексы выражены хорошо, выделений нет, пальпаторно справа уплотнений нет, слева на границе наружних квадрантов опухоль до 8 см.Региональные лимфоузлы не пальпируются.
Цитология:структуры протокового рака.
Маммография: Рак левой м/железы.Умеренно выраженная фиброзно-кистозная мастопатия.
УЗИ: признаки поражения единичных подмышечных л-у слева. Одиночный л/у в средней яремной обл.слева, трудно дифф-ть реактивный от пораженного.
Рентген: рак л/м ж с поражением подмышечных лимфоузлов.Пневмосклероз базальных отделах левого легкого.Очаговые утолщения костальной и междолевой плевры слева-очаговый фиброз.
УЗС ОМТ-параовариальная киста справа, миома матки.
План лечения — комплексное неодъювантная пхт до 6 курсов, осмотр после 4 курса
Показатели крови в пределах нормы
Расписан 1 курс по схеме АС рост 161 вес 72 S 1,76
доксорубицин 88 мг в/в 1 день
циклофосфан 880 мг в/в 1 день
Лечение на фоне антиэметической, дезинтоксикационной терапии.
Жалобы на данный момент
Головные боли, недомогание, утомляемость, зубная боль.
Прошедшие обследования
— не указано —
Данные биопсии и гистологии
рост инвазивной протоковой карциномы G2
Предшествующее лечение
Проведен 1 курс химиотерапии (23.03.12)
Плевральный выпот: история вопроса, анатомия, этиология
Диас-Гусман Э., Двейк Р.А. Диагностика и лечение плеврального выпота: практический подход. Компр Тер . 2007 Зима. 33 (4): 237-46. [Медлайн].
Ноппен М. Нормальный объем и клеточный состав плевральной жидкости. Curr Opin Pulm Med . 2001 июл.7 (4): 180-2. [Медлайн].
Sahn SA. Дифференциальный диагноз плеврального выпота. Вест Дж. Мед .1982 августа 137 (2): 99-108. [Медлайн]. [Полный текст].
Sahn SA. Плевральный выпот внесосудистого происхождения. Clin Chest Med . 2006 июн. 27 (2): 285-308. [Медлайн].
Легкий RW. Недиагностированный плевральный выпот. Clin Chest Med . 2006 июн. 27 (2): 309-19. [Медлайн].
Кулотта Р., Тейлор Д. Заболевания плевры. Али Дж., Саммер WR, Левицки М.Г., ред. Легочная патофизиология .2-е изд. Нью-Йорк: Lange Medical Books / McGraw-Hill; 2005. 194–212.
Askegard-Giesmann JR, Caniano DA, Kenney BD. Редкие, но серьезные осложнения при установке центральной линии. Semin Pediatr Surg . 2009 Май. 18 (2): 73-83. [Медлайн].
Гарсия-Видаль С., Карратала Дж. Ранняя и поздняя неудача лечения внебольничной пневмонии. Semin Respir Crit Care Med . 2009 Апрель 30 (2): 154-60. [Медлайн].
Heffner JE.Диагностика и лечение злокачественных плевральных выпотов. Респирология . 2008 13 января (1): 5-20. [Медлайн].
Бурос Д., Пневматикос И., Цувелекис А. Поражение плевры при системных аутоиммунных заболеваниях. Дыхание . 2008. 75 (4): 361-71. [Медлайн].
Sahn SA. Значение анализа плевральной жидкости. Am J Med Sci . 2008, январь 335 (1): 7-15. [Медлайн].
Beers SL, Abramo TJ.Плевральный выпот. Скорая педиатрическая помощь . 2007 май. 23 (5): 330-4; викторина 335-8. [Медлайн].
Йинон Й, Келли Э, Райан Дж. Фетальные плевральные выпоты. Best Practices Clin Obstet Gynaecol . 2008 22 февраля (1): 77-96. [Медлайн].
Берроуз С.М., Мэтьюз В.С., Кольт Х.Г. Прогнозирование выживаемости у пациентов с рецидивирующими симптоматическими злокачественными плевральными выпотами: оценка прогностической ценности физиологических, морфологических показателей и показателей качества жизни степени заболевания. Сундук . 2000, январь, 117 (1): 73-8. [Медлайн].
Мериджи Ф. Злокачественный плевральный выпот: предстоит еще долгий путь. Rev Последние клинические испытания . 2018 3 декабря [Medline].
Мусани А.И. Варианты лечения злокачественного плеврального выпота. Curr Opin Pulm Med . 2009 июл.15 (4): 380-7. [Медлайн].
[Рекомендации] Робертс М.Э., Невилл Э., Беррисфорд Р.Г., Антунес Дж., Али, штат Нью-Джерси, Группа рекомендаций по заболеваниям плевры BTS.Лечение злокачественного плеврального выпота: Руководство Британского торакального общества по заболеваниям плевры, 2010 г. Thorax . 2010 августа 65 Приложение 2: ii32-40. [Медлайн].
Khaleeq G, Musani AI. Новые парадигмы в лечении злокачественных плевральных выпотов. Респир Мед . 2008 июл.102 (7): 939-48. [Медлайн].
Фрударакис МЭ. Диагностическое обследование плеврального выпота. Дыхание . 2008. 75 (1): 4-13. [Медлайн].
Wong CL, Holroyd-Leduc J, Straus SE. У этого пациента плевральный выпот? JAMA . 2009 21 января. 301 (3): 309-17. [Медлайн].
Калантри С., Джоши Р., Лоханде Т., Сингх А., Морган М., Колфорд Дж. М. младший и др. Точность и достоверность физических признаков в диагностике плеврального выпота. Респир Мед . 2007 Март 101 (3): 431-8. [Медлайн].
Сарая Т, Лайт RW, Такидзава Х, Гото Х.Черный плевральный выпот. Am J Med . 2013 июл. 126 (7): 641.e1-6. [Медлайн].
Light RW, Macgregor MI, Luchsinger PC, Ball WC Jr. Плевральные выпоты: диагностическое разделение транссудатов и экссудатов. Энн Интерн Мед. . 1972 Октябрь 77 (4): 507-13. [Медлайн].
Heffner JE, Brown LK, Barbieri CA. Диагностическая ценность тестов, которые различают экссудативный и транссудативный плеврит. Исследователи первичного исследования. Сундук . 1997 Apr.111 (4): 970-80. [Медлайн].
Легкий RW. Использование натрийуретического пептида N-терминального про-головного мозга плевральной жидкости и натрийуретического пептида головного мозга для диагностики плеврального выпота из-за застойной сердечной недостаточности. Сундук . 2009 Сентябрь 136 (3): 656-8. [Медлайн].
Ромеро-Кандейра С., Фернандес С., Мартин С., Санчес-Пайя Дж., Эрнандес Л. Влияние диуретиков на концентрацию белков и других компонентов плевральных транссудатов у пациентов с сердечной недостаточностью. Am J Med . 2001 15 июня. 110 (9): 681-6. [Медлайн].
Burgess LJ. Биохимический анализ плевральных, перитонеальных и перикардиальных выпотов. Clin Chim Acta . 2004 г., май. 343 (1-2): 61-84. [Медлайн].
Kolditz M, Halank M, Schiemanck CS, Schmeisser A, Hoffken G. Высокая диагностическая точность NT-proBNP для кардиального происхождения плевральных выпотов. Eur Respir J . 2006 июл.28 (1): 144-50. [Медлайн].
Porcel JM, Martinez-Alonso M, Cao G, Bielsa S, Sopena A, Esquerda A.Биомаркеры сердечной недостаточности в плевральной жидкости. Сундук . 2009 Сентябрь 136 (3): 671-7. [Медлайн].
Wilcox ME, Chong CA, Stanbrook MB, Tricco AC, Wong C, Straus SE. Есть ли у этого пациента экссудативный плевральный выпот? Систематический обзор рациональной клинической экспертизы. JAMA . 2014 18 июня. 311 (23): 2422-31. [Медлайн].
Мензис С.М., Рахман Н.М., Райтсон Дж. М. и др. Бактериальный посев крови из плевральной жидкости при плевральной инфекции. Грудь . 2011 Август 66 (8): 658-62. [Медлайн].
Abouzgheib W, Bartter T, Dagher H, Pratter M, Klump W. Проспективное исследование объема плевральной жидкости, необходимое для точной диагностики злокачественного плеврального выпота. Сундук . 2009 апр. 135 (4): 999-1001. [Медлайн].
Свидерек Дж., Моркос С., Донтиредди В. и др. Проспективное исследование для определения объема плевральной жидкости, необходимой для диагностики злокачественного новообразования. Сундук .2010, январь, 137 (1): 68-73. [Медлайн].
Сакураба М., Масуда К., Хебисава А., Сагара Ю., Комацу Х. Уровень аденозиндезаминазы (АДА) плеврального выпота и скрытый туберкулезный плеврит. Ann Thorac Cardiovasc Surg . 2009 15 октября (5): 294-6. [Медлайн].
Гурунг П., Голдблатт М., Хаггинс Дж. Т. и др. Анализ плевральной жидкости, рентгенографические, сонографические и эхокардиографические характеристики гидроторакса печени. Сундук . 2011 27 января.[Медлайн].
Patel PA, Ernst FR, Gunnarsson CL. Под контролем УЗИ сокращаются осложнения и затраты, связанные с процедурами плевроцентеза. J Clin Ультразвук . 2012 март-апрель. 40 (3): 135-41. [Медлайн].
Mercaldi CJ, Дорожки SF. Ультразвуковое наблюдение снижает количество осложнений и снижает стоимость лечения пациентов, перенесших плевроцентез и парацентез. Сундук . 2013 г. 1. 143 (2): 532-8. [Медлайн].
Дункан Д.Р., Моргенталер Т.И., Рю Дж.Х., Дэниэлс К.Э. Снижение ятрогенного риска при плевроцентезе: внедрение передовой практики посредством практического обучения в среде с нулевым риском. Сундук . 2009 Май. 135 (5): 1315-20. [Медлайн].
Феллер-Копман Д. Лечебный торакоцентез: роль ультразвукового исследования и плевральной манометрии. Curr Opin Pulm Med . 2007 июл.13 (4): 312-8. [Медлайн].
Зарогулидис К., Зарогулидис П., Дарвиче К. и др.Злокачественный плевральный выпот и алгоритм лечения. Дж. Торак Дис . 2013 Сентябрь 5, Приложение 4: S413-9. [Медлайн]. [Полный текст].
Метинтас М, Ак Г, Дундар Э и др. Медицинская торакоскопия против биопсии плевральной иглой по Абрамсу под контролем КТ для диагностики пациентов с плевральным выпотом: рандомизированное контролируемое исследование. Сундук . 2010 июн.137 (6): 1362-8. [Медлайн].
Goligher EC, Leis JA, Fowler RA, et al. Полезность и безопасность дренирования плеврального выпота у пациентов с искусственной вентиляцией легких: систематический обзор и метаанализ. Crit Care . 2011 г. 2 февраля. 15 (1): R46. [Медлайн].
Shebl E, Paul M. Парапневмония, плевральные выпоты и эмпиема грудной клетки. 2018, январь [Medline]. [Полный текст].
Colice GL, Curtis A, Deslauriers J, et al. Медикаментозное и хирургическое лечение парапневмонических выпотов: научно обоснованное руководство. Сундук . 2000 Октябрь 118 (4): 1158-71. [Медлайн].
Efthymiou CA, Masudi T, Thorpe JA, Papagiannopoulos K.Злокачественный плевральный выпот при застревании легкого. Пятилетний опыт использования туннельных катетеров PleurX. Interact Cardiovasc Thorac Surg . 2009 Декабрь 9 (6): 961-4. [Медлайн].
Fysh ET, Waterer GW, Kendall P, Bremner P, Dina S, Geelhoed E, et al. Постоянные плевральные катетеры сокращают количество дней пребывания в стационаре по сравнению с плевродезом при злокачественном плевральном выпоте. Сундук . 2012 8 марта [Medline].
Феллер-Копман Д., Паркер М.Дж., Шварцштейн Р.М.Оценка плеврального давления при оценке плеврального выпота. Сундук . 2009 январь 135 (1): 201-9. [Медлайн].
Cafarotti S, Dall’Armi V, Cusumano G, et al. Дренируемые грудные клетки с малым проходом через проволоку: безопасность, переносимость и эффективность при пневмотораксе, злокачественных выпотах и эмпиеме плевры. J Thorac Cardiovasc Surg . 2011 Март 141 (3): 683-7. [Медлайн].
Safiyeh M, Huang D. Новые стратегии лечения сложных плевральных выпотов. Crit Care . 2012 22 мая. 16 (3): 312. [Медлайн].
West SD, Davies RJ, Lee YC. Плевродез при злокачественных плевральных выпотах: текущие разногласия и вариации в практике. Curr Opin Pulm Med . 2004 июл.10 (4): 305-10. [Медлайн].
Шоу П., Агарвал Р. Плевродез при злокачественных плевральных выпотах. Кокрановская база данных Syst Rev . 2004. CD002916. [Медлайн].
Родригес-Панадеро Ф, Ромеро-Ромеро Б.Лечение злокачественных плевральных выпотов. Curr Opin Pulm Med . 2011 июл.17 (4): 269-73. [Медлайн].
Патнэм Дж. Б. Младший, Уолш Г. Л., Свишер С. Г. и др. Амбулаторное лечение злокачественного плеврального выпота с помощью постоянного постоянного плеврального катетера. Энн Торак Хирург . 2000 Февраль 69 (2): 369-75. [Медлайн].
Тан С., Седракян А., Браун Дж., Свифт С., Треже Т. Доказательства эффективности лечения злокачественного плеврального выпота: систематический обзор. евро J Cardiothorac Surg . 2006 май. 29 (5): 829-38. [Медлайн].
Dresler CM, Olak J, Herndon JE 2nd, et al. Фаза III межгрупповое исследование объема талька в сравнении со склерозом тальковой суспензии при злокачественном плевральном выпоте. Сундук . 2005 Март 127 (3): 909-15. [Медлайн].
Van Meter ME, McKee KY, Kohlwes RJ. Эффективность и безопасность туннельных плевральных катетеров у взрослых со злокачественными плевральными выпотами: систематический обзор. J Gen Intern Med .2011 26 января (1): 70-6. [Медлайн]. [Полный текст].
Дэвис Х.Э., Мишра Е.К., Кахан BC и др. Эффект постоянного плеврального катетера по сравнению с плевродезом через дренажную трубку и тальком для облегчения одышки у пациентов со злокачественным плевральным выпотом: рандомизированное контролируемое исследование TIME2. JAMA . 2012 13 июня. 307 (22): 2383-9. [Медлайн].
Puri V, Pyrdeck TL, Crabtree TD и др. Лечение злокачественного плеврального выпота: анализ экономической эффективности. Энн Торак Хирург . 2012 августа 94 (2): 374-9; обсуждение 379-80. [Медлайн]. [Полный текст].
Редди С., Эрнст А., Лэмб С., Феллер-Копман Д. Быстрый плевродез при злокачественных плевральных выпотах: пилотное исследование. Сундук . 2011 июн. 139 (6): 1419-23. [Медлайн].
Freeman RK, Ascioti AJ, Mahidhara RS. Соответствующее предрасположенность сравнение плевродеза или туннельного плеврального катетера у пациентов, которым проводится диагностическая торакоскопия по поводу злокачественных новообразований. Энн Торак Хирург . 2013 июл.96 (1): 259-63: обсуждение 263-4. [Медлайн].
[Рекомендации] Hooper C, Lee YC, Maskell N, BTS Pleural Guideline Group. Исследование одностороннего плеврального выпота у взрослых: Руководство по заболеваниям плевры Британского торакального общества, 2010 г. Thorax . 2010 августа 65 Дополнение 2: ii4-17. [Медлайн].
[Рекомендации] Симофф М.Дж., Лалли Б., Слэйд М.Г., Голдберг В.Г., Ли П., Мишо Г.К. и др. Управление симптомами у пациентов с раком легких: Диагностика и лечение рака легких, 3-е изд: Руководящие принципы клинической практики Американского колледжа грудных врачей, основанные на фактических данных. Сундук . 2013 май. 143 (5 доп.): E455S-97S. [Медлайн].
Основы практики, дифференциация экссудата от транссудата, дальнейший анализ экссудата
Автор
Александр Брейси, доктор медицины Врач-резидент, отделение неотложной медицины, университетская больница Стоуни-Брук
Александр Брейси, доктор медицины, является членом следующих медицинских обществ: Американский колледж врачей неотложной помощи, Ассоциация резидентов неотложной медицины
Раскрытие информации: ничего расскрыть.
Соавтор (ы)
Уильям Д. Голденберг, доктор медицины Доцент кафедры неотложной медицины Университета медицинских наук для военнослужащих; Врач скорой помощи, военно-морской госпиталь Сан-Диего
Уильям Д. Голденберг, доктор медицины, является членом следующих медицинских обществ: Американской академии неотложной медицины, Американского колледжа врачей неотложной помощи, Американской медицинской ассоциации, Ассоциации резидентов скорой медицинской помощи, Общества неотложной академической помощи Медицина
Раскрытие: нечего раскрывать.
Специальная редакционная коллегия
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Получил зарплату от Medscape за работу. для: Medscape.
Пол Блэкберн, DO, FACOEP, FACEP Лечащий врач, Отделение неотложной медицины, Медицинский центр Марикопа
Пол Блэкберн, DO, FACOEP, FACEP является членом следующих медицинских обществ: Американский колледж врачей скорой помощи, Медицинская ассоциация Аризоны , Американский колледж врачей экстренной остеопатии, Американская медицинская ассоциация
Раскрытие информации: нечего раскрывать.
Главный редактор
Роберт О’Коннор, доктор медицины, магистр здравоохранения Профессор и заведующий кафедрой неотложной медицины, Система здравоохранения Университета Вирджинии
Роберт О’Коннор, доктор медицины, магистр здравоохранения является членом следующих медицинских обществ: Американская академия неотложной помощи Медицина, Американский колледж врачей неотложной помощи, Американская кардиологическая ассоциация, Американская медицинская ассоциация, Национальная ассоциация врачей скорой медицинской помощи, Общество академической неотложной медицины
Раскрытие информации: раскрывать нечего.
Дополнительные участники
Майкл С. Бисон, доктор медицины, магистр делового администрирования, FACEP Профессор экстренной медицины, Колледж медицины и фармации Северо-Восточного Университета Огайо; Посещение факультета, Общий медицинский центр Акрона
Майкл С. Бисон, доктор медицины, магистр делового администрирования, FACEP является членом следующих медицинских обществ: Американского колледжа врачей скорой помощи, Национальной ассоциации врачей скорой помощи, Совета директоров ординатуры по неотложной медицине, Общества академических наук. Неотложная медицина
Раскрытие информации: нечего раскрывать.
C Crawford Mechem, MD, MS, FACEP Профессор, факультет неотложной медицины, Медицинский факультет Пенсильванского университета; Директор службы неотложной медицинской помощи, Департамент пожарной охраны Филадельфии
C Кроуфорд Мехем, доктор медицины, магистр медицины, FACEP является членом следующих медицинских обществ: Американского колледжа врачей неотложной помощи, Национальной ассоциации врачей скорой помощи, Общества академической неотложной медицины
Раскрытие информации: Нечего раскрывать.
Благодарности
Фредрик Мелик Абрамян, DO, FACEP Адъюнкт-профессор медицины Калифорнийского университета в Медицинской школе Лос-Анджелеса; Директор по образованию для программы резидентуры по неотложной медицине, консультант, Департамент неотложной медицины, Калифорнийский университет Олив Вью в Медицинском центре Лос-Анджелеса
Раскрытие: Ничего не нужно раскрывать.
Радиологический обзор опухолей плевры
Abstract
Опухоли плевры не редкость, и диагноз устанавливается на основе комбинированной визуализации и клинической корреляции. Злокачественные опухоли встречаются чаще, чем доброкачественные. Первоначальные методы визуализации — это рентгенография грудной клетки и компьютерная томография (КТ). Может потребоваться дальнейшая характеристика с использованием ультразвуковой диагностики (УЗИ), магнитно-резонансной томографии (МРТ) и ПЭТ-КТ. Биопсия остается золотым стандартом. В этой статье освещаются различные распространенные и необычные опухоли плевры и характерные результаты визуализации.
Ключевые слова: Фиброма, мезотелиома, узловое утолщение плевры, плевра
Введение
Радиологическая оценка опухолей плевры требует полного знания анатомии плевры. Различные доброкачественные, злокачественные и опухолевидные состояния могут поражать плевру. Чаще встречаются злокачественные новообразования плевры. Наиболее частым опухолевидным заболеванием плевры является утолщение плевры. Радиологические признаки заболевания плевры могут иметь различный спектр, включая плевральный выпот, плевральные бляшки и узловое утолщение плевры.Дифференциация плевральных новообразований от легочных и экстраплевральных новообразований имеет решающее значение для постановки правильного диагноза.
Анатомия
Плевра представляет собой серозную оболочку, состоящую из мезотелиальных клеток и рыхлой соединительной ткани. Он делится на париетальную плевру и висцеральную плевру. Париетальная плевра снова делится на реберную, диафрагмальную, средостенную и шейную плевру []. У здоровых людей в двух слоях плевры может присутствовать до 5 мл жидкости. Нормальная толщина плевры, включая плевральную полость, равна 0.2-0,44 мм. Обычно плевра не видна отдельно, если она не очерчена жидкостью, воздухом, жиром или фасцией. Обычно это проявляется в виде больших, малых и дополнительных трещин (два инвагинированных листа висцеральной плевры) или в виде соединительных линий (состоящих из четырех листов плевры) []. Бесполая щель состоит из четырех слоев плевры. Нет сообщения между правой и левой плевральными полостями. Париетальная плевра иннервируется чувствительными нервами. Париетальная плевра имеет системное кровоснабжение, тогда как висцеральная плевра снабжается легочными и бронхиальными артериями.
Линейная диаграмма плевры, показывающая различные компоненты плевры
Линейная диаграмма, показывающая соединительные линии, образованные плевральными инвагинациями
Дифференциация плевральных, легочных и экстраплевральных новообразований
Легочные новообразования обычно имеют острые углы относительно грудной стенки, сосредоточены в легком , и охватить легочную сосудистую сеть. Новообразование плевры имеет тупые углы с боковой стенкой грудной клетки с заостренными краями [рисунки и], смещает легочную сосудистую сеть, меняет свое расположение при дыхании и может показывать неполный пограничный знак на рентгенограмме грудной клетки — i.е. на рентгенограмме грудной клетки отображается только часть предела массы. Следующим шагом является дифференциация плеврального от экстраплеврального происхождения образования. Экстраплевральные новообразования могут возникать из экстраплеврального жира, ребер, межреберных мышц и сосудисто-нервного пучка; типичные плевральные новообразования не вызывают эрозии ребер и не смещают экстраплевральный жир наружу, в то время как экстраплевральные новообразования вытесняют экстраплевральный жир внутрь [].
Локализованная эмпиема: (A) Рентгенограмма грудной клетки, показывающая помутнение на основе плевры (стрелка) с сужающимися тупыми краями в левом гемитораксе; (B) компьютерная томография с усилением аксиального контраста, показывающая локализованный скопление (стрелка) с периферическим усилением толстых стенок
Кальцинированная эмпиема: (A) Рентгенограмма грудной клетки, показывающая потерю объема правого гемиторакса с вуалевидным кальцинированным (стрелка) помутнением плевры; (B) компьютерная томография с усилением аксиального контраста, показывающая признаки кальцинированной хронической эмпиемы (стрелка) с пролиферацией экстраплеврального жира и скоплением ребер, указывающими на потерю объема в правом гемитораксе
Таблица 1
Дифференциация плевральных, легочных и экстраплевральных новообразований
Опухоли и опухолевидные состояния с вовлечением плевры
Различные доброкачественные, злокачественные и опухолевидные состояния могут поражать плевру [].Злокачественные новообразования встречаются чаще, чем доброкачественные новообразования. Опухоли плевры могут иметь различный спектр изображений — могут быть односторонними или двусторонними, кальцифицированными или некальцифицированными, а также очаговыми или диффузными.
Таблица 2
Доброкачественные и злокачественные патологии плевры
Утолщение плевры
Утолщение плевры может быть очаговым или диффузным. Диффузное утолщение плевры определяется как утолщение плевры (более 5 мм) с комбинированной областью поражения более 25% грудной стенки при двустороннем поражении и 50% при одностороннем поражении.[1] Апикальное утолщение плевры — это нормальный процесс старения, но если утолщение превышает 2 см, требуется дальнейшее обследование []. На компьютерной томографии (КТ) злокачественное утолщение плевры узловое (> 1 см), показывает периферическое поражение и вовлекает плевру средостения. На изображениях доброкачественное утолщение плевры выглядит как диффузное поражение плевры. Утолщение плевры более 5 см в ширину, 8 см в краниокаудальном направлении и 3 мм в толщину обычно указывает на доброкачественную этиологию [].[2] Причинами диффузного утолщения плевры являются эмпиема, асбестоз, гемоторакс, фиброз легких, облучение, перенесенные ранее хирургические вмешательства, травмы и лекарства. В развивающихся странах туберкулез — важная причина утолщения плевры. Поражение плевры при туберкулезе происходит либо из-за разрыва субплеврального казеозного очага в легком, гематогенного распространения, либо из-за поражения соседнего лимфатического узла. Туберкулезное поражение плевры может проявляться в виде плеврального выпота, утолщения плевры, эмпиемы, бронхоплевральной или плеврокожной фистулы или кальцификатов.На изображениях потеря объема, кальцификаты и разрастание экстраплеврального жира указывают на диффузное доброкачественное утолщение плевры. Компьютерная томография с эмиссией позитронов фтордезоксиглюкозы фтор-18 ( 18 F-FDG PET CT) не может надежно дифференцировать доброкачественное и злокачественное утолщение плевры. Однако стандартизованное значение поглощения (SUVmax) более 2 требует дальнейшей оценки с помощью клинической корреляции или биопсии под визуальным контролем. [3,4] Плевральные бляшки представляют собой отложения гиалинизированных коллагеновых волокон в париетальной плевре.Плевральные бляшки могут быть кальцифицированными или некальцифицированными. На снимках плевральные бляшки видны как очаговое утолщение плевры.
Апикальное утолщение плевры: рентгенограмма грудной клетки показывает апикальное утолщение плевры (стрелка) в левой апикальной области
Таблица 3
Солитарная фиброзная опухоль
Солитарная фиброзная опухоль плевры (SFTP) также известна как локализованная фиброзная опухоль или локализованная мезотелиома плевры. [5] Обычно это наблюдается в возрастной группе 45-60 лет. Большинство этих опухолей доброкачественные, но в 20% случаев они могут быть злокачественными.Опухоль обычно возникает из висцеральной плевры в 80% случаев. На изображениях SFTP выглядит как новообразование на основе плевры мягких тканей с участками некроза, кровоизлияния и кистозных изменений [Рисунки и]. Кальцификация может наблюдаться до 26% случаев. Гетерогенное усиление наблюдается после контрастирования. На магнитно-резонансной томографии (МРТ) гипоинтенсивная сплошная масса видна на T1- и T2-взвешенных изображениях. Изменения некроза и кистозной дегенерации показывают высокую интенсивность сигнала Т2. При визуализации трудно дифференцировать доброкачественные и злокачественные фиброзные опухоли.Признаками злокачественной фиброзной опухоли являются кальциноз, выпот, ателектаз, смещение средостения и инвазия грудной клетки [Рисунки и]. [6,7] Наличие стебля также указывает на доброкачественную природу. На КТ ножка определяется как линейная мягкая ткань, переходящая в плевру / междолевую щель / ворот. Наличие стебля подтверждается также изменением его расположения при дыхании. Ассоциациями SFTP являются клубность, гипертрофическая остеоартропатия (синдром Пьера – Мари – Бамбергера) и гипогликемия (синдром Доге – Поттера).Гипогликемия возникает в результате производства этими опухолями инсулиноподобного фактора роста II (IGF-II) [8]. Гипертрофическая остеоартропатия возникает в результате выработки вещества, похожего на эктопический гормон роста, и чаще встречается при опухолях размером более 7 см. Гистологически морфология сходна с неоплазмой веретеноводства низкой степени злокачественности.
Доброкачественная солитарная фиброзная опухоль: (A) Рентгенограмма грудной клетки, показывающая помутнение плевры (стрелка) в правом гемитораксе с периферическими тупыми краями; (B) КТ с усилением аксиального контраста, показывающая неоднородное увеличение массы на основе плевры (стрелка), которая оказалась доброкачественной фиброзной опухолью плевры
Фиброма плевры: (A) Рентгенограмма грудной клетки, показывающая дольчатое помутнение на основе плевры (стрелка) в правой апикальной области; (B) КТ с усилением аксиального контраста, показывающая неоднородное усиление поражения периферических масс (стрелка) в подтвержденном биопсией случае доброкачественной фибромы плевры
Злокачественная солитарная фиброзная опухоль плевры: обычная аксиальная компьютерная томография, показывающая поражение мягких тканей плевры с периферическими а также внутренний кальциноз (стрелка), примыкающий к печени
Злокачественная фиброзная опухоль плевры: КТ с усилением аксиального контрастирования, показывающая неоднородно увеличивающееся массовое поражение левого гемиторакса (стрелка), вызывающее смещение средостения вправо
Злокачественная мезотелиома
Мезотелиома — это мезотелиома. высокозлокачественная и местно-агрессивная опухоль, наблюдаемая на шестом или седьмом десятилетии жизни.Это связано с воздействием асбеста со средней задержкой развития в 35-40 лет. Гипертрофическая остеоартропатия и перемежающаяся гипогликемия встречаются реже, чем SFTP. Наиболее канцерогенной формой асбеста является крокидолит. Наибольшему риску подвергаются теплоизоляционные рабочие, рабочие верфей, строительные рабочие, рабочие отопительных предприятий и горняки асбеста. К другим факторам, предрасполагающим к развитию мезотелиомы, относятся лучевая терапия, туберкулез и хроническая эмпиема. На изображениях обычно видны диффузное узловое утолщение плевры, плевральные бляшки и плевральный выпот [Рисунки и].Латентный период образования плевральных бляшек обычно составляет 20 лет, и наличие плевральных бляшек является убедительным показателем воздействия асбеста. Обычно плевральная бляшка видна рядом с ребрами, затрагивая с шестого по девятое ребра. Реже поражаются плевры вдоль межреберных промежутков, реберно-диафрагмальных углов и верхушек легких. Также можно увидеть большой плевральный выпот без смещения средостения [Рисунки и]. Наблюдаются кальцификации, вовлекающие диафрагмальную париетальную плевру []. [9,10] На МРТ поражения показывают низкую или среднюю интенсивность сигнала на изображениях T1-W и высокую интенсивность сигнала на изображениях T2-W с пост-контрастным усилением.Дифференцировать от метастатической карциномы сложно; однако одностороннее поражение и потеря объема пораженного гемиторакса благоприятствуют мезотелиоме. Критерии визуализации для неоперабельности включают закрытие диафрагмы и поражение экстраплеврального жира, ребер или других структур средостения [11].
Злокачественная мезотелиома: КТ с усилением аксиального контрастирования, показывающая усиление узлового утолщения плевры (стрелки), вовлекающее реберную и средостенную плевру, распространяющееся в большую трещину (наконечник стрелки) с скоплением ребер, указывающее на изменения потери объема в левом гемитораксе
Злокачественная мезотелиома : КТ с усилением аксиального контраста, показывающая однородно увеличивающееся узловое утолщение плевры (стрелки) с вовлечением средостения и реберной плевры с изменениями потери объема в левом гемитораксе
Мезотелиома в виде плевральных скоплений: КТ-сканирование с усиленным аксиальным контрастом показывает узловое утолщение плевры с вовлечением справа гемиторакс с небольшими скоплениями плевры (стрелки)
Мезотелиома в виде плеврального выпота: КТ с контрастированием в осевом направлении показывает умеренный левый плевральный выпот в виде локализованного скопления с утолщением плевры (стрелки) в случае мезотелиомы
Мезотелиома и плевральные бляшки: (A ) Аксиальная простая компьютерная томография. кальцифицированные (стрелки) и некальцинированные (острие стрелки) плевральные бляшки; (B) аксиальное простое изображение компьютерной томографии, показывающее кальцинированную бляшку (черная стрелка), классически поражающая диафрагмальную париетальную плевру у рабочего-строителя
Лимфома
Как лимфома Ходжкина, так и неходжкинская лимфома могут поражать плевру.На изображениях можно увидеть выпот, плевральные узелки, очаговое или диффузное утолщение плевры, которые демонстрируют однородное усиление контраста. Также наблюдается ассоциированная медиастинальная и внутригрудная лимфаденопатия [Рисунки и]. После химиотерапии наблюдаются кистозно-некротические изменения и кальцификация. Окружное поражение плевры при лимфоме встречается реже.
Плевральная лимфома: КТ с усилением аксиального контрастирования, показывающая неоднородно увеличивающееся дольчатое образование, вовлекающее диафрагмальную плевру (стрелка) и вторгающееся в грудную стенку в случае лимфомы высокой степени злокачественности
Плевральная лимфома: КТ с усилением осевого контраста показывает однородность усиление узлового утолщения плевры (стрелки) с вовлечением реберной плевры с медиастинальной лимфаденопатией (звездочка)
Кальцифицирующая фиброзная псевдоопухоль
Термин кальцифицирующая фиброзная псевдоопухоль был введен Fetsch et al .в 1993 году. [12] Раньше эти опухоли называли «детской фиброзной опухолью с телами псаммомы». Эти новообразования возникают у детей и молодых людей. Предыдущее воспаление в анамнезе является предпосылкой для постановки диагноза. На снимках видны обширные одиночные или мультифокальные образования с кальцификациями [Рисунки и]. [13,14]
Кальцифицирующая фиброзная псевдоопухоль: (A) Рентгенограмма грудной клетки, показывающая кальцинированное помутнение на основе плевры (стрелка), левый гемиторакс с неполным пограничным знаком; (B) простое аксиальное изображение компьютерной томографии, показывающее кальцинированное поражение плевры (стрелка) без разрушения нижележащих ребер
Кальцифицирующая фиброзная псевдоопухоль: обычная аксиальная компьютерная томография, показывающая кальцинированную плевральную непрозрачность в правом гемитораксе (стрелка)
Плевральные метастазы
Аденокарциномы, как известно, вызывают метастазы в плевре чаще, чем другие гистологические типы рака.Обычно первичные очаги находятся в легких, груди, лимфоме и яичнике [Рисунки -]. Инвазивная тимома также может поражать плевру []. На снимках наиболее частой находкой является плевральный выпот. Может наблюдаться диффузное или очаговое узловое утолщение плевры. Повышенное поглощение 18 F-FDG на ПЭТ-КТ наблюдается при злокачественном утолщении и выпоте плевры. [2]
Плевральные метастазы: КТ с аксиальным контрастированием, показывающая неоднородное усиление мягких тканей плевры (белая стрелка) с деструкцией ребер (черная стрелка) в случае плевральных метастазов из почечно-клеточной карциномы
Плевральные метастазы: КТ с аксиальным контрастированием Сканирование, показывающее узловое утолщение плевры (стрелки) с вовлечением реберной и медиастинальной плевры со злокачественным плевральным выпотом в случае метастатической аденокарциномы яичника
Метастазы в плевральной капле в инвазивной тимоме: КТ-изображение с аксиальным контрастированием, показывающее гетерогенное увеличение массы переднего средостения (стрелка) с мягкий плевральный выпот и ипсилатеральные плевральные имплантаты (стрелки)
Плевральные метастазы: КТ-сканирование с аксиальным контрастированием, показывающее неоднородно увеличивающееся образование плевры (стрелка) в левом гемитораксе с экстраторакальным распространением в случае метастатической аденокарциномы
опухоль Аскина
Опухоль Аскина — агрессивная злокачественная опухоль. mor примитивного нейроэктодермального происхождения, принадлежащий к семейству опухолей Юинга.Большинство этих опухолей возникает из мягких тканей грудной стенки или периферии легких. Обычно это наблюдается у детей и подростков. При гистопатологии видны злокачественные маленькие круглые клетки с розетками Гомера – Райта. Сбалансированная реципрокная хромосомная транслокация между хромосомами 11 и 22 является диагностической. На снимках одностороннее поражение обычно проявляется в виде узлового утолщения плевры. Проникновение в грудную стенку, средостение и симпатическую цепь является патогномоничным. Плевральный выпот и разрушение ребер могут быть, а могут и не быть замечены [].
Опухоль Аскина: (A) Рентгенограмма грудной клетки показывает неоднородную непрозрачность (стрелка) правого гемиторакса, затемняющего правое полушарие без смещения средостения; (B) КТ с усилением аксиального контраста, показывающая неоднородное усиление узловых поражений плевры (стрелки) с вовлечением реберной и средостенной плевры с характерным поражением симпатической цепи (наконечник стрелки) в правой параспинальной области
Редкие патологии плевры
Плевральная липома
Липома плевры часто бывает случайной находкой.Это одна из самых распространенных доброкачественных опухолей плевры. На КТ липома показывает плотность жира и отсутствие контрастного усиления. Наличие увеличивающихся перегородок в образовании указывает на липосаркому.
Плевральный спленоз
Плевральный спленоз возникает в результате смещения ткани селезенки в грудную клетку после травмы слева. На снимках видны множественные поражения мягких тканей различного размера, имплантированные на плевру, с усилением, аналогичным тканям селезенки. Золотым стандартом диагностики является сцинтиграфия с использованием 99m Tc, меченных тепловым повреждением эритроцитов.
Другими редкими патологиями плевры являются мезотелиальные кисты, эпителиоидная гемангиоэндотелиома, болезнь Кастлемана, саркомы [], злокачественная фиброзная гистиоцитома, лейкемическая инфильтрация, болезнь Эрдхейма – Честера и экстраскелетная остеосаркома. Внескелетная остеосаркома — редкое злокачественное новообразование, составляющее 1,2% всех сарком мягких тканей. Это следует учитывать при дифференциальной диагностике быстрорастущего кальцинированного плеврального образования у пожилых людей. Другими причинами злокачественной кальцификации плевры являются метастазы из остеосаркомы, хондросаркомы, паростеальной остеосаркомы и мезотелиомы.[15]
Веретено-клеточная саркома плевры: (A) Рентгенограмма грудной клетки, показывающая полное помутнение правого гемиторакса (стрелка) со смещением средостения влево; (B) КТ с усилением аксиального контраста, показывающая неоднородное усиление узловых поражений плевры с плевральным выпотом, смещающим сердце влево
Плевральная псевдоопухоль [16] представляет собой скопление жидкости в трещине легкого. Наиболее частым местом возникновения псевдоопухоли является небольшая трещина. Распространенными причинами псевдоопухоли плевры являются застойная сердечная недостаточность, цирроз и почечная недостаточность.На рентгенограммах грудной клетки в щели видны классические двояковыпуклые или двояковыпуклые помутнения. Обычно он проходит после терапии мочегонными средствами.
Патологические скопления воздуха в грудной клетке у пациентов в отделении интенсивной терапии: данные рентгенограммы коррелируют с КТ | Взгляд на визуализацию
Плевральная полость и грудная стенка анатомически разделены на несколько слоев (рис. 1), и аномальный воздух преимущественно собирается в каждом анатомическом пространстве (рис. 1). Плевральная полость — это область между висцеральной и париетальной плеврами (рис.1). Висцеральная плевра покрывает легкое и складывается обратно в основании легкого (легочные ворота), образуя париетальную плевру (рис. 1). Плевральная полость обычно содержит небольшое количество жидкости (от 1 до 5 мл) [18], и плевральная полость не визуализируется на рентгенограммах или КТ без плеврального выпота или пневмоторакса. Плевральное пространство в первую очередь подразделяется на переднемедиальное, подлегочное, апиколатеральное и заднемедиальное [19, 20].
Рис. 1
Анатомическая схема плевральной полости и грудной стенки и заболевание аномального скопления воздуха в каждом анатомическом пространстве.Осевая КТ грудной клетки 50-летнего мужчины с хронической эмпиемой показывает скопление жидкости в плевральной полости и утолщение плевры. КТ показывает висцеральную плевру (белые стрелки), плевральную полость (PC), париетальную плевру (черные стрелки), экстраплевральный жир (EF), самые внутренние межреберные мышцы и эндоторакальную фасцию (белые звездочки) и межреберный жир (IF). Самая внутренняя межреберная мышца обычно повреждена на дорсальной медиастинальной стороне грудной стенки.
Пневмоторакс
Пневмоторакс — это заболевание, характеризующееся скоплением воздуха в одном или нескольких полостях плевральной полости [21].Здесь мы описываем пневмоторакс в каждом пространстве; напряженный пневмоторакс, являющийся неотложным состоянием; и состояния, требующие дифференциальной диагностики пневмоторакса. Основными симптомами пневмоторакса являются внезапная боль в груди, одышка и сухой кашель. Пневмоторакс вызывается разрывом пузыря, травмой и ятрогенными осложнениями после вмешательства, такими как плевроцентез и вентиляция с положительным давлением [4]. В отделениях интенсивной терапии пневмоторакс обычно вызван баротравмой, связанной с вентиляцией [4].Пневмоторакс встречается почти у 20% пациентов с травмой грудной клетки [4]. Лечится грудным дренажем. В соответствии с Рекомендациями Британского торакального общества 2010 г., большой пневмоторакс определяется на рентгенограммах грудной клетки в вертикальном положении как воздушное пространство, которое находится на расстоянии более 2 см от плевральной поверхности до края легкого на уровне ворот [22]. Большой пневмоторакс обычно требует плевроцентеза, а экстренный плевроцентез необходим для лечения напряженного пневмоторакса [22]. И наоборот, пациенты с небольшим пневмотораксом и без значительной одышки обычно проходят через клиническое наблюдение [22].У эректильных пациентов воздух в основном собирается в апиколатеральном пространстве. Saeki [23] сообщил, что 62 из 73 (84,9%) пневмотораксов были обнаружены в апиколатеральном пространстве на рентгенограммах в вертикальном положении. Рентгенологический признак пневмоторакса у эрегированных пациентов характеризуется визуализацией тонкой висцеральной плевральной линии в апиколатеральном пространстве без сосудистых отметин за этой линией [19]. Поскольку в апиколатеральном пространстве мало перекрывающихся структур, таких как средостение, пневмоторакс можно легко идентифицировать на рентгенограмме в вертикальном положении.У пациентов, находящихся в положении лежа на спине, пространства, в которых собирается воздух, отличаются, поскольку воздух в плевральной полости находится под влиянием силы тяжести, отдачи легких из-за спаек и анатомии плевральной полости [19, 24]. Tocino et al. [20] сообщили, что пространство для сбора воздуха было переднемедиальным у 44%, сублегочным у 29%, апиколатеральным у 13% и заднемедиальным в 13% из 68 случаев пневмоторакса у пациентов в отделении интенсивной терапии в положении лежа на спине [20].
Пневмоторакс в переднемедиальном пространстве (I-1)
У пациентов в положении лежа на спине переднемедиальное пространство является наименее зависимым плевральным пространством [19, 20, 24].Поэтому пневмоторакс в переднемедиальном пространстве чаще всего наблюдается у пациентов в положении лежа на спине [20]. Переднемедиальное пространство делится воротами на надхилярное пространство и подхиларное пространство.
Рентгенологические признаки пневмоторакса в надбровном переднемедиальном пространстве включают резкое очертание верхней полой вены (ВПВ) и непарной вены справа, резкое очертание левой подключичной артерии и левой верхней межреберной вены слева и резкое очертание левой подключичной артерии и левой верхней межреберной вены. очертание передней линии соединения и верхней легочной вены на стороне поражения (рис.2) [19, 25]. Линия переднего соединения — это нормальная анатомическая структура, которая наблюдается на рентгенограмме грудной клетки и обусловлена тем, что висцеральные и париетальные плевры обоих легких встречаются спереди по средней линии [26].
Рис. 2
Пневмоторакс в надбровном переднемедиальном пространстве у мужчины 83 лет с энтеритом. a Рентгенограмма в положении лежа на спине показывает четкое очертание верхней полой вены (ВПВ) (наконечник стрелки), правой брахиоцефальной вены (белая стрелка) и линии переднего соединения (черная стрелка). b Осевое КТ-изображение на уровне ВПВ показывает скопление воздуха в плевральной полости с правой стороны ВПВ (наконечник стрелки) и переднюю линию соединения (черная стрелка)
Рентгенологические признаки пневмоторакса в подгрудном переднемедиальном пространстве включают резкое очертание границы сердца, нижней полой вены (НПВ), перикардиальной жировой подушки и глубокой передней сердечно-диафрагмальной борозды (рис. 3) [19]. На рентгенограмме жировая подушечка перикарда имитирует опухоль или сегментарный коллапс легкого, который легко дифференцировать с помощью КТ.Признак глубокой передней сердечно-диафрагмальной борозды представляет собой аномальное углубление и прозрачность передней сердечно-диафрагмальной борозды из-за скопления воздуха (рис. 3). КТ четко выявляет скопление воздуха в передней сердечно-диафрагмальной борозде (рис. 3). Когда переднемедиальное пространство велико, пораженное поле легкого может казаться сверхсветовым по сравнению с противоположной стороной, а также может выглядеть как округлая или овальная область повышенной прозрачности (т.е. «черный овал»).
Рис. 3
Пневмоторакс в подгрудном переднемедиальном пространстве у 39-летней женщины из-за травмы в дорожно-транспортном происшествии. a Рентгенограмма в положении лежа на спине показывает резкую границу левой границы сердца (стрелка) и глубокую переднюю сердечно-диафрагмальную борозду (звездочка). b Осевая компьютерная томография основания легкого показывает значительный сбор воздуха в плевральной полости в передней сердечно-диафрагмальной борозде (звездочка) и на левой стороне границы сердца (стрелка)
Пневмоторакс в подлегочном пространстве (I-2)
Подлегочное пространство является вторым по распространенности пространством сбора воздуха у пациентов с пневмотораксом в положении лежа на спине [20].К сожалению, рентгенологическая анатомия этого пространства недостаточно изучена, и это может привести к высокой частоте неудач, связанной с обнаружением подлегочного пневмоторакса [19].
Рентгенологические признаки пневмоторакса в подлегочном пространстве включают сверхсветовой верхний квадрант живота, визуализацию нижней поверхности легкого, резко очерченную диафрагму, резкое очертание НПВ правого легкого, «глубокую борозду». знак и знак «двойная диафрагма» (рис.4) [19, 27, 28]. Кроме того, диафрагмальный купол слегка приподнимается при коллапсе легкого.
Рис. 4
Пневмоторакс в подлегочном пространстве у 36-летней женщины с интерстициальной пневмонией. a Рентгенограмма в положении лежа на спине показывает сверхсветовой верхний квадрант живота (черная звездочка). Также видны нижняя поверхность легкого (наконечники стрелок), резко очерченная диафрагма (черные стрелки), резкое очертание нижней полой вены (НПВ) (белая стрелка) и знак «глубокая борозда» (белая звездочка). b КТ-изображение коронарной артерии четко отображает нижнюю поверхность легкого (стрелки) , резко очерченную диафрагму (черные стрелки), резкое очертание НПВ и знак «глубокая борозда» (белая звездочка)
Признак «глубокой борозды» появляется на рентгенограммах как аномальное углубление и прозрачность латеральной реберно-диафрагмальной борозды, которая простирается в сторону подреберья (рис. 4) [19, 27, 28]. Этот признак вызван воздухом, который скапливается в латеральной сублегочной плевральной полости [19, 27, 28].
Признак «двойной диафрагмы» вызван аэрированием легкого, которое очерчивает диафрагмальный купол, и воздухом в плевральной полости, который очерчивает передний реберно-диафрагмальный угол [27, 29]. Сагиттальная КТ выявляет скопление воздуха в переднем реберно-диафрагмальном углу.
Пневмомедиастинум и пневмоперитонеум могут имитировать подлегочный пневмоторакс. В отличие от сублегочного пневмоторакса, центральная часть диафрагмы в этих условиях может быть очерчена воздухом (т. Е. Знаком «сплошная диафрагма»).
Пневмоторакс в апиколатеральном пространстве (I-3)
Апиколатеральное пространство — это плевральная впадина, в которой анатомически сложно скапливаться воздуху у пациентов, лежащих на спине [20]. Ему предшествует сбор воздуха в переднемедиальном и подлегочном пространстве (рис. 5) [19, 20].
Рентгенологическим признаком пневмоторакса в апиколатеральном пространстве является тонкая висцеральная плевральная линия без сосудистых отметин за этой линией (рис. 5) [19]. Сосудистые отметины за чертой часто наблюдаются, когда отдача легких отличается при наличии паренхиматозных заболеваний [19].Визуализация плевральной линии требует вентиляции легких и наличия воздуха в плевральной полости; следовательно, линия плевры может быть не видна в случаях паренхиматозных заболеваний легких, таких как пневмония и острый респираторный дистресс-синдром (ОРДС), плевральный выпот и очаговые плевральные спайки [19].
Рис. 5
Пневмоторакс в апиколатеральном пространстве мужчины 77 лет. Перфорация пищевода, вызванная эндоскопическим расслоением подслизистой оболочки при раке пищевода, привела к пневмомедиастинуму, пневмотораксу и подкожной эмфиземе. a Рентгенограмма в положении лежа на спине показывает висцеральную плевральную линию (черные стрелки) в апиколатеральном пространстве. Черные стрелки указывают на париетальную плевру. Также видны пневмоторакс в переднемедиальном пространстве (черная звездочка) и подлегочном пространстве (белая звездочка), пневмомедиастинум и подкожная эмфизема (красный овал). За пределами висцеральной плевральной линии нет сосудистых отметин. Подкожная эмфизема большой грудной мышцы имеет линейное расположение, которое повторяет направление мышечных волокон. b КТ-изображение коронарной артерии показывает висцеральную плевральную линию (черная стрелка) и отсутствие каких-либо структур в плевральной полости. Также наблюдаются париетальная плевра (наконечник стрелки), пневмоторакс в переднемедиальном пространстве (черная звездочка) и пневмоторакс в подлегочном пространстве (белая звездочка). c КТ-изображение коронарной артерии показывает линейное расположение подкожной эмфиземы, которое следует направлению мышечных волокон большой грудной мышцы (красные овалы)
Пневмоторакс в заднемедиальном пространстве (I-4)
Пневмоторакс в заднемедиальном пространстве возникает при коллапсе нижней доли или паренхиматозных заболеваниях [19, 20].Рентгенологические находки включают прозрачный треугольник с вершиной в воротах и V-образное основание, очерчивающее реберно-позвоночную борозду (рис. 6) [19, 20]. Медиальная поверхность треугольника — это параспинальная линия и нисходящая аорта, а боковая поверхность треугольника — это медиальная поверхность спавшейся нижней доли, которая смещена от средней линии [19, 20]. КТ выявляет коллапс нижней доли, которая прикреплена к средостению с помощью нижней легочной связки (IPL) и скопления воздуха в заднемедиальном пространстве (рис.7) [19]. Пневмомедиастинум может имитировать пневмоторакс в заднемедиальном пространстве. Первый часто продолжается в забрюшинное пространство или проходит по средней линии, тогда как второй остается над диафрагмой, заканчивается у реберно-позвоночной борозды и не проходит по средней линии [19].
Рис. 6
Пневмоторакс в заднемедиальном пространстве у мужчины 82 лет с хронической обструктивной болезнью легких. a Рентгенограмма в положении лежа на спине показывает прозрачный треугольник (красная пунктирная линия) с частично сжатой левой нижней долей (черная звездочка).Просветленный треугольник соответствует пространству для сбора воздуха с вершиной в воротах и V-образным основанием, которое очерчивает реберно-позвоночную борозду между параспинальной линией / нисходящей аортой и медиальной поверхностью частично спавшейся нижней доли. b На аксиальном КТ-изображении оснований легких виден пневмоторакс в заднемедиальном пространстве (белая звездочка). Хорошо видна левая нижняя легочная связка (стрелка), которая представляет собой линейную структуру между средостением и левой нижней долей (черная звездочка)
Рис.7
Напряженный пневмоторакс из-за дорожной травмы у мужчины 18 лет. a Рентгенограмма в положении лежа на спине показывает левый пневмоторакс со смещением средостения вправо (черные стрелки) и частично перевернутой левой гемидиафрагмой (черные стрелки). Левое легкое коллапсирует с ушибом (звездочка). b КТ-изображение коронарной артерии четко показывает смещение средостения вправо (черные стрелки) и перевернутое левое полушарие (черные стрелки)
Напряженный пневмоторакс (I-5)
Напряженный пневмоторакс характеризуется аномальным увеличением давления задействована грудная полость.Односторонний клапан между пораженным легким и плеврой приводит к постоянной утечке воздуха в плевральную полость и вызывает накопление воздуха в плевральной полости [30]. Затем происходит коллапс ипсилатерального легкого, средостение смещается от пораженной стороны, а ипсилатеральная диафрагма смещается вниз (особенно при вентиляции с положительным давлением) и может перевернуться вниз [30]. Сердечный выброс снижается из-за нарушения венозного возврата [30], и в конечном итоге наступает остановка сердца [30].Напряженный пневмоторакс — опасное для жизни событие, которое происходит в отделении интенсивной терапии; таким образом, его следует идентифицировать немедленно, особенно у пациентов, получающих искусственную вентиляцию легких с положительным давлением. В таких случаях обязательна немедленная декомпрессия грудной клетки [12].
Рентгенологические данные легкого при напряженном пневмотораксе такие же, как и на легком при простом пневмотораксе. Кроме того, смещение средостения, инверсия диафрагмы, увеличение межреберного промежутка и полный или субтотальный коллапс легких отражают расширение пораженного гемиторакса (рис.7) [19, 31]. Более важным признаком напряженного пневмоторакса является уплощение границы сердца, ВПВ и НПВ [19]. Этот признак отражает нарушение венозного возврата [19].
Имитация пневмоторакса (I-6)
Рентгенологические данные многих ситуаций, таких как кожные складки, междолевые трещины, буллы на верхушках и скопление воздуха во внутригрудном экстраплевральном пространстве [4, 12], имитируют пневмоторакс.
Кожные складки
При проведении портативной рентгенографии грудной клетки рентгеновская кассета располагается позади пациента, и между грудной стенкой и кассетой могут образоваться кожные складки [4].Кожные складки чаще встречаются у пожилых и кахексических пациентов с дряблой кожей.
В отличие от плевральной линии при пневмотораксе кожные складки проявляются как широкая рентгеноконтрастная полоса, которая может выходить за теменную плевральную линию или среднюю линию с сосудистыми отметками за линиями складок (рис. 8) (4, 12, 18, 31). Кожные складки обычно проходят парами или по три за раз. Кроме того, кожные складки могут быть множественными, двусторонними или внезапно исчезнуть [19]. Наблюдается отрицательный эффект Маха, усиливающий кожные складки [19, 32].Одежда или простыни также могут производить аналогичный артефакт [12].
Рис. 8
Кожная складка, имитирующая пневмоторакс, на рентгенограмме у 66-летней женщины с глиобластомой. Кожная складка выглядит как широкая рентгеноконтрастная полоса (черные стрелки), которая примыкает к рентгенопрозрачной полосе (белые стрелки), что отражает отрицательный эффект полосы Маха в левом поле легкого на рентгенограмме в положении лежа на спине. Выходит за пределы плевральной полости. Сосудистые отметины (черная стрелка) видны за его краем
Междолевые трещины
При наличии междолевого плеврального выпота или утолщения междолевых или добавочных трещин междолевые трещины могут напоминать висцеральную плевру, наблюдаемую при пневмотораксе.Более того, если нормальная междолевая щель параллельна рентгеновскому лучу, она может быть видна и имитировать висцеральную плевру, которая наблюдается при пневмотораксе на рентгенограммах (рис. 9). Однако, в отличие от пневмоторакса, сосудистые отметины также видны за пределами трещины (рис. 9).
Рис. 9
Большая трещина, имитирующая пневмоторакс, на рентгенограмме у мужчины 71 года. Ему выполнена частичная резекция правой S6 по поводу метастаза рака пищевода в легкие. a Основная трещина выглядит как толстая линейная непрозрачность (черные стрелки) в области правого легкого на рентгенограмме в положении лежа на спине.Он напоминает висцеральную плевру при пневмотораксе. В отличие от пневмоторакса, сосудистые отметины (черная стрелка) видны за пределами утолщенной трещины. b На аксиальном КТ-изображении показана большая трещина, простирающаяся в переднезаднем направлении с небольшим наклонным углом (черные стрелки). Некоторая потеря объема в правой нижней доле привела к смещению трещины кзади; следовательно, он кажется видимым на переднезадней рентгенограмме
Буллы
Буллы, особенно гигантские буллы, на периферии легких могут имитировать пневмоторакс (рис.10) [4]. Булла — это четко очерченное воздушное пространство тонкой стенкой диаметром более 1 см [21]. Он находится в паренхиме легких и возникает в результате разрушения альвеолярной ткани. Кроме того, пузыри часто сопровождаются эмфизематозными изменениями [21, 33]. Гигантские буллы занимают более 30% гемиторакса [34] и могут быть ошибочно диагностированы как пневмоторакс, даже если лечение этих двух состояний отличается [34]. Большинство пациентов с гигантскими пузырями при буллезной эмфиземе курят сигареты и обычно проявляют прогрессирующую одышку в течение нескольких месяцев [33].И наоборот, пациенты с пневмотораксом обычно проявляют внезапную одышку и боль в груди.
Рис. 10
Гигантский булла, имитирующий пневмоторакс на рентгенограмме у 67-летнего мужчины. У него хроническая обструктивная болезнь легких и пристрастие к сигаретам. a Гигантский булла на рентгеновском снимке в вертикальном положении выглядит как рентгенопрозрачность овальной формы (черные стрелки) в верхушке правого легкого. Он напоминает пневмоторакс в апиколатеральном пространстве. Буллезная эмфизема существует в обоих легких, а в верхушке левого легкого (наконечник стрелки) наблюдается большой булл. b На КТ-изображении коронарной артерии виден гигантский булла (черные стрелки) в верхушке правого легкого. Большая булла (черная стрелка) также существует в верхушке левого легкого в дополнение к буллезным изменениям в обоих легких
Рентгенографические данные, указывающие на буллы, включают отсутствие края легкого, округлый характер булл, выпуклых к легкому, и наличие множественных булл в другом месте [4]. В отличие от плевральной линии, линия, ограничивающая буллу, обычно более горизонтальна [33].
Мультимодальный подход к визуализации средостения и плевры: жемчуг и подводные камни
Эта статья аккредитована для получения одного кредита SA-CME.Посетите applicationradiology.org/SAM2 для получения полной информации по SA-CME.
Диагностическая интерпретация изображений поперечного сечения средостения и плевры представляет уникальные и серьезные проблемы даже для опытного радиолога. Средостение имеет сложную анатомическую структуру и состоит из множества структур, разделенных на несколько анатомических отделов, которые могут вызывать широкий спектр патологий. Кроме того, плевральная полость тонкая и многоплоскостная, что может затруднить оценку и количественную оценку аномалий плевры.
Здесь мы рассматриваем методы визуализации средостения и плевры и представляем жемчужины визуализации и подводные камни, которые могут помочь при рентгенологической интерпретации. Это будет включать в себя общие образования, которые присутствуют при рутинной визуализации грудной клетки, а также ключевые функции визуализации, которые помогают различать их с помощью компьютерной томографии (КТ), магнитно-резонансной томографии (МРТ) и позитронно-эмиссионной томографии / компьютерной томографии 18F-фтордезоксиглюкозы. (ФДГ-ПЭТ / КТ).
Знание распространенных патологий средостения и плевры, присутствующих на поперечных изображениях, позволит рентгенологу сделать информированную диагностическую радиологическую интерпретацию и направить соответствующее вмешательство и наблюдение.
Анатомия средостения
Стандартная радиологическая классификация анатомии средостения основана на трехкомпонентной модели (передний, средний и задний) на основе ориентиров на боковом рентгеновском снимке грудной клетки. 1,2 С грудным входом, образующим верхнюю границу, и диафрагмой, представляющей нижнюю границу в этой системе, передний отдел включает структуры, расположенные впереди перикарда. Средний отсек включает структуры между сердцем и позвоночником.Задний отдел включает структуры в параспинальной локализации. Это наиболее широко используемая система.
Совсем недавно Японская ассоциация исследований тимуса (JART) представила новую схему классификации, основанную на компьютерной томографии, 3 , которая позже была пересмотрена Международной группой по изучению злокачественных новообразований тимуса (ITMIG). 4,5 В этой системе средостение также имеет три отсека, при этом входное отверстие в грудном отделе формирует верхнюю границу, а диафрагма — нижнюю границу. 4 Эти компартменты известны как периваскулярные, висцеральные и паравертебральные компартменты; эта система считается более точным подходом к анатомической характеристике в эпоху поперечной визуализации.
Визуализация средостения
Рентгенография грудной клетки
Рентгенография грудной клетки остается наиболее распространенным начальным тестом для выявления патологии средостения. Дифференциальный диагноз патологии средостения учитывает вовлеченный отдел средостения и скорость развития, а также такие факторы, как возраст пациента, пол и сопутствующие заболевания.Для определения локализации поражения используется несколько хорошо известных рентгенологических признаков; к ним относятся потеря интерфейсов средостения и силуэтный знак. 1,2 Чувствительность рентгеновских лучей грудной клетки при выявлении небольших поражений средостения, однако, низкая, особенно для поражений заднего средостения (чувствительность 6%), по сравнению с паратрахеальным расположением (чувствительность 69%). 6 Чувствительность можно улучшить, получив рентгенограммы грудной клетки спереди и сбоку.
CT
КТ — метод выбора для характеристики патологии средостения. 7 Превосходное разрешение современной компьютерной томографии позволяет точно локализовать и предоставляет информацию о текстуре ткани и агрессивности. Измерение аттенюации тканей на КТ может помочь дифференцировать жир (жидкость 0-20 HU, мягкие ткани 20-40 HU и кровотечение 40-60 HU), 8 , который наиболее точно измеряется без внутривенного (IV) контраста. Внутривенное усиление часто дает дополнительную информацию о васкулярности, текстурной неоднородности и улучшенном определении границ поражения.Во многих случаях КТ предоставляет достаточно информации о том, следует ли вмешиваться терапевтически и как это делать.
МРТ
МРТ контраст тканей превосходит КТ и иногда используется для уточнения дифференциального диагноза, особенно когда доброкачественный диагноз может быть достоверно установлен во избежание инвазивной биопсии. МРТ можно использовать для различения твердой ткани и белковой жидкости, оба из которых могут демонстрировать одинаковое ослабление при КТ. На КТ мягкие ткани обычно демонстрируют промежуточную интенсивность сигнала по сравнению с гладкими мышцами на изображениях Т1 и Т2, а белковая жидкость демонстрирует высокую интенсивность сигнала по сравнению с гладкими мышцами на последовательностях Т1 и Т2. 9 МРТ также можно использовать для характеристики тканей, обогащенных железом, таких как продукты крови; для обнаружения микроскопического жира, например, при гиперплазии тимуса; 10 и для характеристики внутренней сложности кистозных образований, которые не всегда видны на КТ. МРТ с диффузионно-взвешенной визуализацией (DWI) показала ценность в различении неопластических и неопухолевых поражений, считающихся неопределенными на КТ. 11
FDG-PET / CT
В дополнение к обнаружению скрытого злокачественного новообразования при постановке рака, FDG-PET / CT может использоваться для дальнейшей характеристики поражения средостения, подозрительного на злокачественное новообразование, на КТ или МРТ.Неопределенное поражение, обнаруженное на ПЭТ / КТ с высокой активностью в отношении ФДГ, может потребовать биопсии или, в случае известного первичного злокачественного новообразования, эмпирической терапии. И наоборот, при двусмысленном поражении на КТ, которое не обнаружено на ПЭТ / КТ, можно лечить консервативно. Однако ФДГ-ПЭТ / КТ страдает некоторыми ограничениями по чувствительности и специфичности в отношении новообразований. К ним относятся более низкая точность для небольших поражений (<6-8 мм) в условиях малозависимых или непостоянных злокачественных новообразований, таких как некоторые муцин-продуцирующие немелкоклеточный рак легкого, 12 лимфома низкой степени злокачественности, 13 а также некоторые злокачественные новообразования щитовидной железы, а также при активном ФДГ незлокачественном заболевании, таком как саркоидоз. 14 В результате общая чувствительность и специфичность FDG-PET / CT для отличия злокачественной ткани от доброкачественной средостения составила 83% и 58% соответственно, 15 , хотя в некоторых случаях она может быть более чувствительной и специфичной. клинические условия, такие как большинство неходжкинских лимфом. 16 Помимо выявления злокачественности, авидность при ФДГ-ПЭТ / КТ может указывать на агрессивную гистологию. Например, степень авидности ФДГ может использоваться для различения тимом высокого и низкого риска, а также тимомы и карциномы тимуса. 17
Применение мультимодальной визуализации в средостении
Псевдопоражения средостения
Несколько нормальных анатомических структур и анатомических вариантов могут имитировать заболевание в различных модальностях визуализации. Ниже приведены несколько часто встречающихся ошибок при рентгенологической интерпретации средостения:
Выемки перикарда. Перикард охватывает не только сердце, но и легочные артерии, легочные вены, восходящую аорту и верхнюю полую вену.Жидкость может скапливаться в полостях перикарда и быть ошибочно принята за лимфаденопатию (рис. 1). Правильный диагноз может быть поставлен путем тщательного анализа взаимосвязи находки с соседними сосудистыми структурами и характеристиками жидкости на КТ или МРТ. 18
Cysterna Chylli. Хиловая цистерна представляет собой мешковидное расширение лимфатических стволов, поскольку они сходятся, образуя начало грудного протока, и могут быть видны в правом латеральном парааортальном ретрокруральном пространстве.Если цистерна выступающая, то ее можно принять за ретрокруральную лимфаденопатию (рис. 2). Ключи к правильному диагнозу включают знакомство с расположением этой структуры и характеристиками затухания жидкости на КТ или МРТ. 19,20
Псевдотромб . Тромб ушка левого предсердия — хорошо документированное осложнение у пациентов с фибрилляцией предсердий; однако это может быть имитировано застоем и плохим смешиванием крови и контрастного вещества на КТ, что приводит к ошибочному диагнозу.Использование отсроченной фазы на КТ или МРТ может избежать этой ловушки, предоставив больше времени для соответствующего смешивания внутривенного контраста в придатке предсердия. 21,22
Липоматоз средостения. Это чрезмерное отложение жира в средостении, часто связанное с ожирением и стероидным лечением, может имитировать патологию средостения на рентгенограмме грудной клетки; но его можно легко охарактеризовать как аморфный неинкапсулированный жир на КТ с отсутствующими внутренними твердыми компонентами или свидетельствами массового воздействия на соседние структуры, 23 , что позволяет отличить его от злокачественного жировосодержащего новообразования, липосаркомы.
Дифференциация доброкачественных и злокачественных образований
Гиперплазия тимуса
В течение жизни вилочковая железа постепенно становится инволютированной и жировой, при этом к 50 годам остается мало твердой ткани тимуса. Однако в некоторых клинических условиях доброкачественную гиперплазию тимуса можно принять за новообразование. Это состояние может возникнуть de novo , но чаще является реактивным в ряде клинических сценариев, включая недавнюю химиотерапию, ожоги, аутоиммунные заболевания, хроническое воспаление и миастению.Во многих случаях гиперплазию тимуса можно заподозрить на КТ у пациентов с однородными мягкими тканями с вкраплениями жира в ожидаемом распределении тимуса.
Когда гиперплазия тимуса выглядит более однородно твердой и похожей на массу, отличить ее от новообразования на КТ невозможно. 24 Там, где есть высокая степень подозрения на новообразование, например, при пролеченной лимфоме или миастении, МРТ может быть полезной для характеристики доброкачественной ткани тимуса.Диагноз гиперплазии тимуса может быть подтвержден на МРТ с высокой степенью уверенности, если наблюдается диффузное падение тканевого сигнала при переходе от синфазного к не синфазному изображению T1, что указывает на присутствие липидов и воды в одних и тех же вокселях ( Рисунок 3). 25 Однако, поскольку не вся доброкачественная ткань тимуса будет демонстрировать потерю сигнала от синфазного к не синфазному, диффузионно-взвешенная визуализация была предложена как потенциально полезная для отличия доброкачественной ткани тимуса от предполагаемой лимфомы в переднем средостении. 26 Поскольку гиперплазия тимуса и многие новообразования, как правило, являются зависимыми от ФДГ на ПЭТ / КТ, этот метод не считается полезным при диагностике этих состояний. 27
Белковые цисты
Кисты развития, такие как перикардиальные или бронхогенные кисты, обычно измеряют простое затухание жидкости на КТ и как низкий сигнал T1 и высокую интенсивность сигнала T2 относительно мышцы на МРТ. 28 Однако эти поражения могут иногда становиться белковыми при значениях ослабления CT в диапазоне мягких тканей (20-40 HU) и представляют собой диагностическую проблему.Гладкие края, тонкие стенки, хроническое заболевание и отсутствие усиления внутреннего внутривенного контраста могут указывать на доброкачественную этиологию. МРТ может дать окончательный диагноз белковой кисты, демонстрируя однородную высокую интенсивность сигнала на изображениях T1 и T2. 9 Для пациентов, проходящих ФДГ-ПЭТ / КТ, эти поражения не будут жадными до ФДГ.
Киста тимуса
Доброкачественные кисты тимуса могут возникать в процессе развития или, чаще, приобретаться в контексте множества хронических воспалительных заболеваний, включая вирус иммунодефицита человека (ВИЧ), 29 и синдром Шегрена. 30 На КТ эти поражения измеряют затухание жидкости и имеют гладкую границу с тонкими стенками и без внутреннего усиления IV или твердых компонентов. Отсутствие внутренней сложности может быть подтверждено с помощью МРТ, которая имеет преимущество перед КТ в характеристике внутренней сложности кистозных поражений на последовательностях T2 (Рисунок 4). Наличие внутренних твердых компонентов или внутренних улучшений должно вызывать опасения по поводу кистозного новообразования, такого как кистозная тимома или карцинома тимуса. 9,28,31 Доброкачественные кисты также не должны быть зависимы от ФДГ на ПЭТ / КТ.
Зрелые кистозные тератомы. Зрелая кистозная тератома — это доброкачественная опухоль из половых клеток, обычно диагностируемая в переднем средостении у бессимптомных молодых людей, но иногда она может проявляться симптоматически из-за местного массового воздействия на соседние структуры или, реже, до разрыва. Классический внешний вид изображений отражает присутствие всех трех компонентов слоев зародышевых клеток в различных пропорциях. На КТ эти поражения четко очерчены и имеют гладкие границы, содержащие смесь жира, кальция, жидкости и ослабления мягких тканей в различной пропорции (рис. 5).Внешний вид на МРТ обычно неоднороден по ослаблению сигнала на последовательностях T1 и T2. Последовательности подавления жира позволяют обнаруживать макроскопический жир; наличие уровня жировой жидкости очень специфично для тератом, хотя и встречается редко. 32,33 Злокачественная трансформация этой опухоли встречается редко; однако в основном солидное поражение или присутствие усиливающего твердого компонента может указывать на злокачественность. 34
Нейрогенные опухоли. Нейрогенные опухоли являются наиболее частыми поражениями заднего средостения, хотя они могут расти в различных анатомических местах, включая другие отделы средостения и грудную стенку.Эти опухоли делятся на опухоли вегетативной нервной системы и опухоли нервных оболочек, и они могут быть доброкачественными или злокачественными. Как правило, доброкачественные опухоли оболочек нервов демонстрируют низкое ослабление на КТ, низкое ослабление сигнала на изображениях Т1 и высокое ослабление сигнала на изображениях Т2 и однородно усиливаются при внутривенном контрастировании. Эти поражения иногда можно увидеть в ипсилатеральном нервном отверстии грудного отдела позвоночника (рис. 6). Ганглионеврома — доброкачественная опухоль вегетативной нервной системы, обнаруживаемая у маленьких детей, которая обычно видна на КТ как четко очерченное поражение с низким затуханием, демонстрирующее легкое усиление после введения контрастного вещества.Мелкие кальцификаты наблюдаются примерно у 20% пациентов. На МРТ ганглионевромы имеют однородную интенсивность на всех последовательностях, иногда демонстрируя внутреннюю область криволинейных полос низкой интенсивности.
Шванномы — это доброкачественные опухоли оболочек нервов, расположенные эксцентрично по отношению к пораженному нерву.
На КТ шванномы видны как образования мягких тканей, которые могут содержать области с низким ослаблением из-за кистозного или жирового компонента и содержат очаги кальция примерно в 10% случаев; маленькие шванномы увеличиваются однородно.На МРТ эти поражения демонстрируют промежуточную интенсивность T1 и высокую интенсивность T2 по сравнению с мышцами, с внутренними усиливающими твердыми компонентами.
Нейрофибромы, также доброкачественные опухоли оболочек нервов, имеют общие визуальные характеристики с шванномами. Однако нейрофибромы обычно расположены в центре нерва, чаще связаны с эрозиями соседних костей и содержат внутренний кальциноз на КТ и небольшую неоднородность сигнала Т2 с более ярким периферическим сигналом Т2 на МРТ.
Необычные злокачественные аналоги этих поражений не будут обсуждаться, но обычно характеризуются более неоднородным изображением на КТ и МРТ. ПЭТ / КТ может играть дополнительную роль в различении доброкачественных и злокачественных опухолей оболочки нервов. Исследование Benz et al. Показало, что FDG-PET / CT имеет чувствительность 94% и специфичность 91% для злокачественных новообразований в опухолях нервной оболочки, когда поражения имеют стандартное значение поглощения (SUV) 6,1 или выше. 35
Анатомия плевры
Плевра представляет собой перепончатую структуру, состоящую из двух слоев, висцеральной плевры и париетальной плевры, которые создают барьер замкнутого пространства вокруг каждого легкого.Висцеральная плевра плотно прилегает к паренхиме легкого с расширением в междолевые щели и получает кровоснабжение от бронхиальных артерий. Париетальная плевра выстилает внутреннюю поверхность грудной стенки, средостения и диафрагмы и получает кровоснабжение от межреберных артерий. Эти два слоя обычно плотно прилегают друг к другу и смазываются несколькими миллилитрами жидкости, которая помогает удерживать слои вместе за счет капиллярного действия. 36,37 У здорового пациента плевра не всегда видна на КТ, особенно глубоко в задней борозде, где никакое легкое не соответствует нижнему отражению плевры.В среднем границы плевры находятся на 2–3 см выше первого ребра, на уровне 6 или 7 ребра спереди снизу и ниже 12 ребра сзади снизу.
Визуализация плевры
Рентгенография грудной клетки
Утолщение, кальциноз и жидкость плевры можно легко определить на рентгенографии грудной клетки, хотя КТ обычно более чувствительна для оценки плевры. Передняя и боковая проекции предпочтительны для оценки задней борозды на боковой проекции.Поражение может быть заподозрено на плевральной основе, если оно расположено рядом с плевральной поверхностью и имеет тупые углы к плевральной поверхности, при этом его внутренняя граница имеет резко очерченный край, а его внешняя граница плохо очерчена ( знак неполной границы , рис. 7). . 38
УЗИ
Трансторакальное ультразвуковое исследование чрезвычайно чувствительно к наличию плевральной жидкости и полезно для определения сложности плевральной жидкости. Его низкая стоимость и простота использования позволяют быстро и точно оценить плевральную жидкость, которую можно провести у постели больного и использовать для проведения торакоцентеза.В экстренных случаях УЗИ также можно использовать для быстрого выявления пневмоторакса. 39
CT
КТ — это метод выбора для рутинной оценки плевры, обеспечивающий визуализацию всей плевры с высоким разрешением, позволяющий обнаруживать и характеризовать тонкие плевральные аномалии, включая утолщение плевры, кальциноз и образование жидкости. Плевральные находки, подозрительные на злокачественные новообразования, включают: толщину более 1 см, узловатость и утолщение плевры средостения. 40 Внутривенный контраст может значительно помочь в оценке плевры. При подозрении на эмпиему сильное увеличение плевры вокруг плеврального выпота (признак разделения плевры) очень наводит на мысль об эмпиеме. 41 При злокачественных новообразованиях плевры внутривенный контраст обеспечивает более заметную видимость опухоли и может помочь в обнаружении инвазии грудной стенки, средостения или диафрагмы.
МРТ
Благодаря превосходному контрасту тканей, МРТ может быть очень полезной для определения степени поражения плевры.Например, МРТ обычно используется для оценки диафрагмальной инвазии при злокачественной мезотелиоме плевры, которая может быть недооценена на КТ. Есть доказательства того, что усиление плевры с отсроченной фазой может быть полезно при МРТ-оценке злокачественной мезотелиомы плевры. 42 МРТ также полезен для дальнейшей характеристики тканей плевральных поражений, что может привести к достоверному диагнозу, например, для обнаружения обогащенных железом плевральных отложений при плевральном спленозе. Диффузионно-взвешенная визуализация и динамическое усиление контраста также могут быть полезны для дифференциации доброкачественной и злокачественной плевральной ткани. 43
FDG-PET / CT
FDG-PET / CT предоставляет информацию о метаболической активности плеврального заболевания и в основном используется в качестве инструмента решения проблем для поражений, которые не определены на КТ, а также для определения стадии злокачественного новообразования. При злокачественной мезотелиоме плевры степень авидности опухоли и объем метаболически активной опухоли при отрицательном результате ФДГ-ПЭТ / КТ коррелируют с выживаемостью. 44-46 FDG-PET имеет очень высокую чувствительность 95%, но только умеренную специфичность 82% 47 для злокачественных новообразований плевры.Снижение специфичности объясняется активными FDG, неопухолевыми воспалительными причинами утолщения плевры. Активное воспаление плевры, например, вызванное тальковым плевродезом, недавним облучением, недавней операцией или фоном плевральных бляшек, также может затруднить интерпретацию FDG-PET / CT и ограничить специфичность для злокачественного новообразования.
Приложения для мультимодальной визуализации плевры
Псевдопоражения средостения:
Функциональное утолщение плевры. Явное фокальное утолщение плевры на субсантиметр в зависимых базальных частях легкого, вызванное фокальным альвеолярным коллапсом, является обычным явлением и может быть связано с прилегающей матовой матовой прозрачностью в субплевральной паренхиме. Эти псевдоповреждения обычно исчезают при сканировании в положении лежа. 48
Псевдоопухоль плевры. Очаговое скопление плевральной жидкости в междолевой щели, обычно в правой горизонтальной щели, может имитировать опухоль на рентгенограмме грудной клетки.Чаще всего плевральное положение этой коллекции можно уточнить на рентгенограмме грудной клетки сбоку. В случае сомнений КТ грудной клетки демонстрирует типичное расположение и значения затухания, которые подтверждают диагноз. 49
Общие проблемы при визуализации плевры
Характеристика плевральной жидкости
Сложный характер плевральной жидкости можно предположить на рентгенограмме грудной клетки по признакам локализации жидкости. На КТ возможно подробное распределение плевральной жидкости, а также информация о ее составе на основе значений ослабления, которые могут быть в диапазоне от жира (хилоторакс), простой жидкости (плевральный выпот) или кровоизлияния (гемоторакс).Если наличие жира или продуктов крови сомнительно, может быть полезна МРТ, хотя обычно торакоцентез выполняется для характеристики неопределенного скопления плевральной жидкости. Хилоторакс может измерять уменьшение содержания жира или жидкости. Плевральные выпоты обычно измеряют простое уменьшение жидкости (0-20 HU), а острый гемоторакс демонстрирует высокое ослабление (40-50 HU).
Плевральный выпот и узловатость могут быть признаком злокачественного новообразования плевры. В этом случае плевральный выпот обычно сопровождается узловатостью плевры, хотя в некоторых случаях опухоль плевры не определяется на КТ.При подозрении на новообразование плевры. FDG-PET / CT может быть очень полезным для определения степени заболевания. Комбинированная ФДГ-ПЭТ / КТ показала чувствительность и специфичность 93,5% и 92,6% соответственно. 50 Двухэнергетическая КТ и ультразвук также продемонстрировали некоторую полезность для характеристики злокачественных плевральных выпотов. 51,52
Диффузное утолщение плевры
Утолщение плевры может быть доброкачественным или злокачественным. Доброкачественное утолщение обычно гладкое, толщиной <5 мм и не затрагивает плевру средостения.Обычно это результат воспаления, чаще всего из-за хронического плеврального выпота, эмпиемы или гемоторакса. Доброкачественное диффузное утолщение плевры может кальцифицироваться, чаще всего после гемоторакса или эмпиемы, особенно при эмпиеме с M. tuberculosis и, реже, после аутоиммунного плеврита. 53 Как доброкачественные, так и злокачественные причины утолщения плевры могут быть вызваны ФДГ на ПЭТ / КТ; Полезность МРТ при обнаружении кальцификации ограничена. Узловатое периферическое утолщение плевры с вовлечением медиальной плевры и толщиной> 10 мм считается подозрительным на злокачественное новообразование. 54
Плевральные бляшки
Дискретные очаговые зоны бляшечного утолщения плевры могут возникать после воздействия асбеста, часто сопровождаясь некоторой степенью кальцификации, и называются «плевральными бляшками» (рис. 8). Эти поражения обычно распространяются вдоль диафрагмы и нижних заднебоковых ребер. Хотя эти изменения обычно можно увидеть на компьютерной рентгенографии, КТ является методом выбора для характеристики утолщения плевры. 53 МРТ ограничивает обнаружение кальцификации.Эти поражения часто являются FDG-зависимыми, что иногда может ограничивать полезность FDG-PET для характеристики предполагаемого очага плеврального новообразования на фоне связанных с асбестом бляшек.
Злокачественная мезотелиома плевры (МПМ)
Признаки очаговой узловатости плевры мягких тканей или роста на месте плевральной бляшки, связанной с асбестом, могут указывать на развитие MPM, осложнения, которое может развиться в течение 20-30 лет после воздействия асбеста. МПМ может проявляться в виде утолщения плевры, связанного с кожурой, отдельных отдельных плевральных узелков или, что реже, единичного плеврального образования.Хотя КТ часто видна на КТ, предпочтительным вариантом является КТ, в идеале с усилением внутривенного контраста. FDG-PET / CT обычно используется для определения стадии, а МРТ часто используется для определения наличия или отсутствия локальной инвазии 54 (Рисунок 9).
Список литературы
- Fraser RS, Colman NC, Pare PD. «Диагноз болезней грудной клетки» Фрейзера и Паре. 4-е изд. Филадельфия: W.B. Компания Сондерс; 1999.
- Felson, B. Рентгенология грудной клетки. 1-е изд. Филадельфия: W.B. Компания Сондерс; 1973.
- Фудзимото К., Хара М., Томияма Н. и др. Предложение по новой классификации отсеков средостения изображений поперечной плоскости в соответствии с Общими правилами исследования опухолей средостения Японской ассоциации исследований тимуса (JART). Oncol Rep. 2014; 31 (2): 565-572.
- Картер Б.В., Томияма Н., Бхора Ф.Й. и др. Современное определение компартментов средостения. J Thorac Oncol. 2014; 9 (9 приложение 2): S97-101.
- Картер Б.В., Бенвенисте М.Ф., Мадан Р. и др. ITMIG классификация компартментов средостения и мультидисциплинарный подход к опухолям средостения. Радиография. 2017; 37 (2): 413-436.
- Вернеке К., Вассалло П., Поттер Р. и др. Опухоли средостения: чувствительность обнаружения с помощью сонографии по сравнению с КТ и рентгенографией. Радиология. 1990; 175 (1): 137-143.
- Томияма Н., Хонда О, Цубамото М. и др. Опухоли переднего средостения: диагностическая точность КТ и МРТ. Eur J Radiol. 2009; 69 (2): 280-288.
- Миллер В.Т. Диагностическая визуализация брюшной полости. 1-е изд. Нью-Йорк: McGraw-Hill Education; 2012.
- Мадан Р., Ратанапрасатпорн Л., Ратанапрасатпорн Л. и др. Кистозные образования средостения и роль МРТ. Clin Imaging. 2018; 50: 68-77.
- Инаока Т., Такахаши К., Минета М. и др. Гиперплазия тимуса и опухоли вилочковой железы: дифференциация с помощью МРТ с химическим сдвигом. Радиология. 2007; 243 (3): 869-876.
- Шин К.Е., Йи КА, Ким Т.С. и др. Диффузионно-взвешенная МРТ для отличия неопухолевых кист от солидных образований в средостении: решение проблем при образовании средостения с неопределенными внутренними характеристиками на КТ. Eur Radiol. 2014; 24 (3): 677-684.
- Шим С.С., Хан Дж. ФДГ-ПЭТ / КТ-изображение в оценке немелкоклеточного рака легкого, продуцирующего муцин, с патологической корреляцией. Ann Nucl Med. 2010; 24 (5): 357-362.
- Карам М., Новак Л., Цириак Дж. И др.Роль позитронно-эмиссионной томографии фтор-18 фтор-дезоксиглюкозы в оценке и последующем наблюдении пациентов с лимфомами низкой степени злокачественности. Рак. 2006; 107 (1): 175-183.
- Чанг Дж. М., Ли Х. Дж., Гу Дж. М. и др. Ложноположительные и ложноотрицательные результаты ФДГ-ПЭТ при различных заболеваниях грудной клетки. Korean J Radiol. 2006; 7 (1): 57-69.
- Proli C, De Sousa P, Jordan S и др. Диагностическое когортное исследование точности 18-фтордезоксиглюкозы ((18) ФДГ) позитронно-эмиссионной томографии (ПЭТ) -КТ для оценки злокачественных новообразований в поражениях переднего средостения: исследование DECiMaL. BMJ Open. 2018; 8 (2): e019471.
- Чесон Б.Д., Фишер Р.И., Баррингтон С.Ф. и др. Рекомендации по первоначальной оценке, стадированию и оценке ответа на лимфому Ходжкина и неходжкинскую лимфому: классификация Лугано. J Clin Oncol. 2014; 32 (27): 3059-3068.
- Benveniste MF, Moran CA, Mawlawi O, et al. ФДГ-ПЭТ-КТ помогает в предоперационной оценке пациентов с впервые выявленными злокачественными новообразованиями эпителия тимуса. J Thorac Oncol. 2013; 8 (4): 502-510.
- Бродерик Л.С., Брукс Г.Н., Кульман Дж. Э. Анатомические подводные камни сердца и перикарда. Радиография. 2005; 25 (2): 441-453.
- Пинто П.С., Сирлин С.Б., Андраде-Баррето О.А. и др. Cisterna chyli на рутинной МРТ брюшной полости: нормальная анатомическая структура в ретрокруральном пространстве. Радиография. 2004; 24 (3): 809-817.
- Киёнага М., Мори Х., Мацумото С. и др. Грудной проток и цистерна хили: оценка с помощью мультидетекторной КТ. Br J Radiol. 2012; 85 (1016): 1052-1058.
- Чен Дж, Чжан Х, Чжу Д. и др. МРТ сердца для выявления тромба левого предсердия / ушка левого предсердия у пациентов с фибрилляцией предсердий: метаанализ и систематический обзор. Herz. 2018.
- Zou H, Zhang Y, Tong J, et al. Многодетекторная компьютерная томография для обнаружения тромба левого предсердия / ушка левого предсердия: метаанализ. Intern Med J. 2015; 45 (10): 1044-1053.
- Molinari F, Bankier AA, Eisenberg RL.Жиросодержащие поражения на изображениях грудной клетки взрослых. AJR Am J Roentgenol. 2011; 197 (5): W795-813.
- Нассери Ф., Эфтехари Ф. Клинический и радиологический обзор нормального и аномального тимуса: жемчуг и подводные камни. Радиография. 2010; 30 (2): 413-428.
- Priola AM, Priola SM, Ciccone G и др. Дифференциация рикошета и лимфоидной гиперплазии тимуса от опухолей переднего средостения с помощью МРТ-визуализации с двойным эхо-химическим сдвигом во взрослом возрасте: надежность отношения химического сдвига и индекса интенсивности сигнала. Радиология. 2015; 274 (1): 238-249.
- Priola AM, Priola SM, Gned D и др. Нормальный тимус без подавления при МР-томографии с химическим сдвигом и лимфома переднего средостения: дифференциация с помощью МР-визуализации, взвешенной по диффузии, с использованием кажущегося коэффициента диффузии. Eur Radiol. 2018; 28 (4): 1427-1437.
- Джерушалми Дж., Френкель А., Бар-Шалом Р. и др. Физиологическое поглощение 18F-FDG в тимусе у детей и молодых людей: оценка заболеваемости, паттернов и взаимосвязи с лечением с помощью ПЭТ / КТ. J Nucl Med. 2009; 50 (6): 849-853.
- Jeung MY, Gasser B, Gangi A, et al. Визуализация кистозных образований средостения. Радиография. 2002; 22 Номер спецификации: S79-93.
- Kontny HU, Sleasman JW, Kingma DW и др. Мультилокулярные кисты тимуса у детей с инфекцией вируса иммунодефицита человека: клинико-патологические аспекты. J Pediatr. 1997; 131 (2): 264-270.
- Кондо К., Миёси Т., Сакияма С. и др. Мультилокулярная киста тимуса, ассоциированная с синдромом Шегрена. Ann Thorac Surg. 2001; 72 (4): 1367-1369.
- Ackman JB, Wu CC. МРТ вилочковой железы. AJR Am J Roentgenol. 2011; 197 (1): W15-20.
- Moeller KH, Rosado-de-Christenson ML, Templeton PA. Зрелая тератома средостения: особенности визуализации. AJR Am J Roentgenol. 1997; 169 (4): 985-990.
- Пател И.Дж., Сяо Э., Ахмад А.Х. и др. Лучшие случаи AIRP в лучевой-патологической корреляции: зрелая кистозная тератома средостения. Радиография. 2013; 33 (3): 797-801.
- Gaerte SC, Meyer CA, Winer-Muram HT, et al. Жиросодержащие поражения грудной клетки. Радиография. 2002; 22 Номер спецификации: S61-78.
- Бенц М.Р., Чернин Дж., Драй С.М. и др. Количественная позитронно-эмиссионная томография F18-фтордезоксиглюкозы точно характеризует опухоли оболочки периферических нервов как злокачественные или доброкачественные. Рак. 2010; 116 (2): 451-458.
- Charalampidis C, Youroukou A, Lazaridis G, et al. Анатомия плеврального пространства. J Thorac Dis. 2015; 7 (Дополнение 1): С27-32.
- Финли DJ, Руш VW. Анатомия плевры. Thorac Surg Clin. 2011; 21 (2): 157-163, vii.
- Сюй СС, Генри Т.С., Чунг Дж. Х. и др. Неполный пограничный знак. J Визуализация грудной клетки. 2014; 29 (4): W48.
- Маркетти Г., Аронди С., Багливо Ф. и др. Новые взгляды на использование ультразвукового исследования плевры для диагностики и лечения заболеваний плевры. Clin Respir J. 2018; 12 (6): 1993-2005.
- Леунг А.Н., Мюллер Н.Л., Миллер Р.Р. КТ в дифференциальной диагностике диффузного поражения плевры. AJR Am J Roentgenol. 1990; 154 (3): 487-492.
- Kraus GJ. Признак расщепленной плевры. Радиология. 2007; 243 (1): 297-298.
- Patel AM, Berger I, Wileyto EP, et al. Значение улучшенной визуализации с задержкой фазы при злокачественной мезотелиоме плевры. J Thorac Dis. 2017; 9 (8): 2344-2349.
- Кулен Дж., Де Кейзер Ф., Нафтё П. и др. Злокачественное заболевание плевры: диагностика с помощью диффузионно-взвешенной и динамической МР-томографии с контрастным усилением — первоначальный опыт. Радиология. 2012; 263 (3): 884-892.
- Китадзима К., Дои Х., Курибаяси К. и др. Прогностическая ценность количественных (18) параметров ПЭТ / КТ F-FDG на основе объема до лечения у пациентов со злокачественной мезотелиомой плевры. Eur J Radiol. 2017; 86: 176-183.
- Новак А.К., Фрэнсис Р.Дж., Филлипс М.Дж. и др. Новая прогностическая модель злокачественной мезотелиомы, включающая количественную визуализацию FDG-PET с клиническими параметрами. Clin Cancer Res. 2010; 16 (8): 2409-2417.
- Фрэнсис Р.Дж., Бирн М.Дж., ван дер Шааф А.А. и др. Раннее прогнозирование ответа на химиотерапию и выживаемости при злокачественной мезотелиоме плевры с использованием нового полуавтоматического трехмерного анализа серийных ПЭТ-сканирований 18F-FDG на основе объема. J Nucl Med. 2007; 48 (9): 1449-1458.
- Treglia G, Sadeghi R, Annunziata S, et al. Диагностическая точность 18F-ФДГ-ПЭТ и ПЭТ / КТ в дифференциальной диагностике злокачественных и доброкачественных поражений плевры: систематический обзор и метаанализ. Акад. Радиол. 2014; 21 (1): 11-20.
- Claude-Desroches M, Bierry G, Touitou-Gottenberg D, et al. Очаговое зависимое утолщение плевры при МДКТ: поражение плевры или функциональная аномалия? Диагностика интервальной визуализации. 2012; 93 (5): 360-364.
- de Paula MC, Escuissato DL, Belem LC, et al. Очаговые опухолевидные состояния плевры: узелки и образования за пределами мезотелиомы и метастазов. Respir Med. 2015; 109 (10): 1235-1243.
- Sun Y, Yu H, Ma J, et al.Роль 18F-FDG PET / CT интегрированной визуализации в различении злокачественного плеврального выпота от доброкачественного. PLoS One. 2016; 11 (8): e0161764.
- Zhang X, Duan H, Yu Y, et al. Дифференциальная диагностика доброкачественного и злокачественного плеврального выпота с помощью двухэнергетической спектральной КТ. PLoS One. 2018; 13 (4): e0193714.
- Bugalho A, Ferreira D, Dias SS, et al. Диагностическая ценность трансторакальных ультразвуковых особенностей в прогнозировании злокачественных новообразований при недиагностированном плевральном выпоте: проспективное обсервационное исследование. Дыхание. 2014; 87 (4): 270-278.
- Walker CM, Takasugi JE, Chung JH, et al. Опухолевые состояния плевры. Радиография. 2012; 32 (4): 971-985.
- Никелл Л.Т., Лихтенбергер Дж. П., Хорашади Л. и др. Мультимодальная визуализация для характеристики, классификации и определения стадии злокачественной мезотелиомы плевры. Радиография. 2014; 34 (6): 1692-1706.
Некоторые материалы в этой рукописи были представлены на 41-м курсе «Диагностическая визуализация на мысе Пенн».Рисунки являются оригинальными для этой рукописи.
Back To Top
Произошла ошибка при настройке вашего пользовательского файла cookie
Произошла ошибка при настройке вашего пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно.Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки вашего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.
Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie. - Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере. - Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.
Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт
не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к
остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Локализованный междолевой выпот при застойной сердечной недостаточности
Локализованный междолевой выпот при застойной сердечной недостаточности (фантомная или исчезающая опухоль (и) легкого) является редкостью, но хорошо известен.83-летний мужчина обратился с жалобой на одышку, опухшие ноги и сухой кашель в течение пяти дней. На рентгенограмме грудной клетки (CXR) обнаружена массивная, резко очерченная, округлая / овальная однородная плотная тень размером 10 × 7 см в правой нижней доле. Лечение петлевыми диуретиками и уменьшение потребления жидкости привело к полному разрешению наблюдаемого круглого / овального опухолевидного изображения на контрольной рентгенограмме через три дня. Радиологическое появление подобной массы конфигурации у пациентов с застойной сердечной недостаточностью требует коррекции основного состояния сердца до проведения дальнейшего диагностического исследования, чтобы избежать ненужных, дорогостоящих и, возможно, вредных диагностических и лечебных ошибок.
1. Введение
Фантомная или исчезающая опухоль означает локализованное транссудативное междолевое скопление плевральной жидкости при застойной сердечной недостаточности. Название происходит от его частого сходства с опухолью на рентгеновском снимке и от его тенденции исчезать после соответствующего лечения сердечной недостаточности.
2. История болезни
83-летний мужчина обратился с жалобой на одышку, опухшие ноги и сухой кашель в течение пяти дней. У него в анамнезе был сахарный диабет II типа, гипертония, фибрилляция предсердий и застойная сердечная недостаточность, и он лечился инсулином, метилдигоксином, фуросемидом и пероральными добавками калия.Тонкие, влажные и слабокрепитирующие вдохи были слышны у основания слева, а приглушенные звуки дыхания присутствовали у основания справа. Частота дыхания 32 / мин. Его частота сердечных сокращений составляла 99 в минуту, артериальное давление — 165/105 мм рт.ст., и у него был систолический шум 3/6 над проекцией аортального клапана. Анализ газов артериальной крови показал pH = 7,448, pCO 2 = 4,33 кПа, pO 2 = 7,67 кПа, HCO 3 = 22,0 ммоль / л, избыток основания -1,1 ммоль / л и SaO 2 = 91 .4%. Лабораторные исследования показали нормальный общий анализ крови, незначительно повышенный уровень креатинина в сыворотке — 143 мк моль / л и трехкратно повышенный уровень GGT. Эхокардиограмма, полученная при поступлении, показала концентрическую гипертрофию левого желудочка, стеноз аорты и умеренную митральную регургитацию, сопровождающиеся расширением левого предсердия и нарушением систолической функции левого желудочка с фракцией выброса 39%.
Рентгенография показала массивную, резко очерченную круглую / овальную однородную плотную тень размером в правой нижней доле (рис. 1 (а)).Архивная рентгенограмма, сделанная 1 и 4 года назад, выявила периодическое появление похожих опухолевидных теней в той же области правой доли (рис. 2). Ультразвуковое исследование легких подтвердило скопление плевральной жидкости в косой междолевой щели правой доли легкого. Немедленно была начата парентеральная диуретическая терапия. В связи с клиническим и субъективным улучшением за период наблюдения пациент был выписан на лечение в домашних условиях с рекомендацией увеличить пероральную терапию диуретиками с уменьшением потребления жидкости.Три дня спустя контрольная рентгенография показала полное разрешение (рис. 1 (b)) наблюдаемого круглого / овального изображения, похожего на опухоль.
3. Обсуждение
Локализованные междолевые выпоты при застойной сердечной недостаточности (фантомные или исчезающие опухоли легких) являются редкими, но хорошо известными явлениями [1–3]. Из-за небольшого количества зарегистрированных случаев заболеваемость трудно оценить. В 1928 году Стюарт первым назвал это заболевание «междолевым гидротораксом» [4]. Фантомные опухоли преимущественно возникают у мужчин в правом гемитораксе, причем три четверти зарегистрированных случаев — в пределах правой поперечной щели и реже — в косой щели.Одновременное возникновение обеих трещин было зарегистрировано примерно в одной пятой случаев, тогда как в левом гемитораксе описывались только спорадически [5]. Предполагается, что ключевая роль в их патогенезе связана со спайками и облитерацией плевральной полости по краю щели из-за плеврита. В таких условиях фантомные опухоли возникают всякий раз, когда транссудация из легочного сосудистого пространства превышает резорбтивную способность плевральных лимфатических сосудов. Однако такое атипичное внутрифиссуральное распределение плевральных выпотов также можно объяснить локальным усилением упругой отдачи соседнего, частично ателектатического легкого, что дает эффект «присоски» и способствует локализации жидкости даже при отсутствии плевральных спаек [6, 7] .Правосторонняя предрасположенность фантомной опухоли лучше всего объясняется большим гидростатическим давлением, существующим на этой стороне по сравнению с левым, при застойной сердечной недостаточности, что приводит к нарушению венозного и лимфатического дренажа, вызывающего локализацию жидкости [8]. Дифференциальный диагноз локализованных плевральных выпотов внутри трещины включает следующее: транссудаты, вызванные недостаточностью левого желудочка или почечной недостаточностью, экссудаты (парапневмонические плевральные выпоты, злокачественные плевральные выпоты и доброкачественные плевральные выпоты, связанные с асбестом), а также гемоторакс, хилоторакс и фиброзные опухоли, происходящие из висцеральной плевры междолевой щели [9].
В представленном случае произошло обострение застойной сердечной недостаточности. Обнаружена характерная задне-передняя рентгенологическая фантомная опухоль легкого: правосторонняя, хорошо очерченная легочная масса с гладкими краями. Неинвазивное неионизирующее ультразвуковое исследование легких помогло установить диагноз. Быстрое разрешение псевдоопухоли после лечения левой сердечной недостаточности предоставило дополнительные доказательства для диагноза. Рентгенограммы нескольких архивных пациентов выявили периодическое появление подобных опухолевидных теней в той же области правой доли во время обострения застойной сердечной недостаточности, подтверждая, что фантомные опухоли могут рецидивировать во время эпизодов сердечной декомпенсации (рис. 2).
4. Заключение
Этот случай подтверждает эффективность консервативного лечения (петлевые диуретики и ограниченное потребление жидкости) локализованного междолевого выпота при застойной сердечной недостаточности. Возможность фантомной опухоли легкого следует учитывать и исключать у любого пациента с застойной сердечной недостаточностью и очевидной массой легких на рентгенограмме.
