Лечение вирусной пневмонии у взрослых в Ижевске, симптомы и диагностика пневмонии, вызванной вирусом
Вирусная пневмония – острое воспаление легких, вызываемое бактериальной либо вирусно-бактериальной флорой. В случае несвоевременного обращения за медицинской помощью значительно возрастают риски развития сердечной, дыхательной и почечной недостаточности, септического шока. Преимущественно воспаление провоцируют вирусы гриппа А и В, парагриппа, простого герпеса, аденовирусы.
В терапевтическом отделении клиники Елены Малышевой успешно проводится лечение вирусной пневмонии у взрослых. Прогрессирующие течение и угроза тяжелых осложнений требует немедленной госпитализации, проведения комплексного обследования, интенсивной терапии.
Симптомы вирусной пневмонии у взрослых
У большинства пациентов развивается двухсторонняя пневмония, протекающая в зависимости от типа возбудителя с различной степенью тяжести, осложнений и исходов. Среди характерных признаков заболевания:
- кашель;
- одышка;
- боли в грудной клетке;
- повышение температуры тела до 38-400;
- катар верхних дыхательных путей;
- лимфаденопатия;
- ринит;
- хрипы в легких;
- менингеальные знаки (головная боль, фотофобия, измененное состояние сознания).

Симптомы вирусной пневмонии часто сопровождаются рвотой, судорогами, повышенным беспокойством, раздражительностью. Для легких форм характерны слабовыраженные проявления, в тяжелых случаях состояние осложняется лихорадкой, кислородной и дыхательной недостаточностью, геморрагическим синдромом. Возможно присоединение вторичной инфекции, что приводит к абсцессу легких с развитием септического шока.
Диагностика
Ранняя диагностика позволяет избежать тяжелых осложнений. Идентификация возбудителя возможна после тщательного изучения анамнеза, физикального и лабораторно-инструментального обследования. По показаниям назначают:
- анализы мочи, крови;
- пульсоксиметрию;
- исследование отделяемого секрета по Грамму;
- функциональные пробы Мюллера и Вальсальвы;
- бактериологию мокроты;
- ЭКГ, ЭхоКГ.
С полной уверенностью диагноз подтверждается после рентгенографии легких, которая выявляет патологические изменения анатомических структур и мелкоочаговые тени в нижних долях. С целью исключения онкологических процессов и туберкулеза, а также при отсутствии положительной динамики на фоне терапии, проводится бронхо-и ангиография, консультации фтизиатра и онколога.
С целью исключения онкологических процессов и туберкулеза, а также при отсутствии положительной динамики на фоне терапии, проводится бронхо-и ангиография, консультации фтизиатра и онколога.
Лечение вирусной пневмонии у взрослых
После постановки диагноза подбирается индивидуальная схема лечения, к основным направлениям относят:
- антибактериальную терапию;
- дезинтоксикацию организма;
- применение обезболивающих, антигистаминных, противокашлевых средств;
- иммуностимуляцию.
Для исключения риска осложнений после устранения острой симптоматики может быть назначена физиотерапия, ЛФК, массаж. Лечение вирусной пневмонии у взрослых проводится до полного выздоровления и нормализации состояния, которое определяется на основании результатов повторных лабораторных исследований и рентгена.
Преимущества лечения в клинике Елены Малышевой
В медицинском центре Елены Малышевой используется комплексный подход, тактика ведения больного зависит от выявленных причин заболевания, а также тяжести состояния. Клиника оснащена оборудованием экспертного класса, что обеспечивает безошибочную постановку диагноза. Специалисты с высоким уровнем подготовки в ежедневной практике успешно применяют классические и инновационное технологии лечения. Индивидуальный подход и доброжелательное отношение медперсонала создают предпосылки для быстрой реабилитации.
Клиника оснащена оборудованием экспертного класса, что обеспечивает безошибочную постановку диагноза. Специалисты с высоким уровнем подготовки в ежедневной практике успешно применяют классические и инновационное технологии лечения. Индивидуальный подход и доброжелательное отношение медперсонала создают предпосылки для быстрой реабилитации.
Следует помнить, что вирусная пневмония характеризуется стремительным течением и представляет опасность для людей с хроническими патологиями. При появлении температуры, кашля и симптомов недомогания не откладывайте визит к врачу!
Позвоните по телефону (3412) 52-50-50 или заполните форму обратной связи, и специалисты клиники свяжутся с вами в ближайшее время.
Диагностика и лечение пневмонии в Челябинске у взрослых и детей цена, отзывы
Семейная Клиника Александровская предлагает пройти обследование, диагностику и лечение пневмонии в Челябинске с комфортом, без очередей, ежедневно к выбранному Вами времени, в том числе и в выходные, и во второй половине дня с 16.
00 до 20.00.
- Консультации детских врачей (педиатров и врачей — детских специалистов…) на дому
- Консультации врачей для взрослых (терапевтов и взрослых врачей-специалистов…) на дому
Отзывы о специалистах и клинике
17.09.2021
Боброва В.С.
Боброва В.С. была с дочкой на приеме у педиатра Зариповой Юлии Раулевны: приемом осталась довольна, врач была дружелюбна и добра, нашла общий язык с моей дочерью, внимательно провела осмотр, составила план лечения, спасибо еще раз!
читать ответ
- Благодарим вас за предоставленный отзыв о нашем враче и клинике! Желаем вам крепкого здоровья!
10.
09.2021
Павлов Д. Ю.
Павлов Д. Ю. был на приеме у терапевта Антоновой Ирины Валерьевны: хочу еще раз поблагодарить врача за ее вежливость и доброжелательность, была очень коммуникабельна со мной, хороший специалист, назначила мне четкое лечение, я очень рада, что доверилась именно ей!
читать ответ
- Выражаем Вам признательность за выбор клиники и нашего врача!
09.09.2021
Дернева П.Г.
Дернева П.Г. была на приеме у пульмонолога Решетовой Людмилы Раисовны: хочу еще раз вас поблагодарить, спасибо вам огромное за ваше сочувствие, врач очень внимательно слушала меня, а главное слышала! Грамотно составила ход лечения, во время всего приема ощущалась не безразличность врача! Спасибо вам.
читать ответ
- Благодарим вас за предоставленный отзыв о нашем враче!
08.09.2021
Тумбаева Е.
В.
Тумбаева Е.В. была на приеме у врача терапевта Антоновой Ирины Валерьевны: огромная благодарность врачу за оказанную помощь! Пришла на прием сегодня уже повторно, после пройденного курса лечения. Самочувствие отличное, я полностью здорова. Грамотный специалист! Доктор который реально помогает!
читать ответ
- Выражаем Вам признательность за выбор клиники и нашего врача!
04.09.2021
Маслова А.К.
Маслова А.К. с ребенком была на приеме у врача аллерголога-иммунолога Банновой Натальи Николаевны: это лучшая консультация, на которой я только была! Сразу видно, что доктору важно действительно вылечить ребенка, помочь ему, а не выписать «стандартное» лечение, как у всех или из интернета. Консультация длилась достаточно по времени, чтобы внимательно осмотреть ребенка и установить необходимый план лечения. Я осталась очень довольна, теперь будем посещать данного специалиста и следовать всем рекомендациям.
читать ответ
- Благодарим вас за предоставленный отзыв о нашем враче!
02.09.2021
Павлова А.И.
Павлова А.И. была на приеме у пульмонолога Решетовой Людмилы Раисовны: выбрала именно этого врача по хорошим, положительным отзывам от знакомых, врач действительно очень грамотный, отвечала на все интересующие мне вопросы, была тактична и расположила к себе, составила и объяснила план моего лечения, хочу еще раз вас поблагодарить!
читать ответ
- Спасибо вам за выбор наших специалистов и посещение Александровской! Желаем вам и вашим близким здоровья!
01.09.2021
Глушко П.Г.
Глушко П.Г. была на приеме у аллерголога Банновой Натальи Николаевны: врач понравился, с моей проблемой я думаю мы вместе справимся, назначила лечение, анализы можно сдать не выходя из клиники это огромный плюс, спасибо вам еще раз огромное!
читать ответ
- Спасибо вам за выбор наших специалистов и посещение Александровской! Желаем вам и вашим близким здоровья!
01.
09.2021
Дятчук И.П.
Дятчук И.П. была на приеме с сыном у педиатра Зариповой Юлии Раулевны: на прием зашли вовремя, моему сыну понравился врач, действительно умеет находить общий язык с детьми, несмотря на ее небольшой опыт, я вполне осталась довольно, грамотна все объяснила, составила лечение, спасибо вам.
читать ответ
- Спасибо вам за выбор наших специалистов и посещение Александровской! Желаем вам и вашим близким здоровья!
21.08.2021
Григоренко Л.И.
Григоренко Л.И. была на приеме у массажиста Сотовой Людмилы Ивановны: делала массаж шеи, спасибо большое врачу! Золотые руки, очень общительная, время пролетело незаметно, мне очень полегчало однозначно могу сказать, обязательно как-нибудь возьму весь курс массажа!
читать ответ
- Благодарим вас за предоставленный отзыв о нашем враче и клинике! Желаем вам крепкого здоровья!
17.
08.2021
Колабахина Е.В.
Колабахина Е.В. была на приеме у массажиста Сотовой Людмилы Ивановны: мне все очень понравилось, зашла на прием без задержек, врач была очень вежлива, тактична, после приема мне стало намного легче, поэтому я сразу для себя решила оплатить весь курс, спасибо вам еще раз.
читать ответ
- Спасибо вам за выбор наших специалистов и посещение Александровской! Желаем вам и вашим близким здоровья!
03.09.2020
Пяткова И.К.
Пяткова И.К. была на приеме у пульмонолога Антонова Владимира Николаевича: врач грамотный, индивидуально подбирает лечение, уделяет достаточно времени на приеме, внимательно выслушал, все объяснил по лечению, дал рекомендации, меня все устроило. Я довольна приемом.
читать ответ
- Выражаем Вам признательность за выбор клиники и нашего врача!
29.
07.2020
Михайловская А.Г.
Михайловская А.Г. была на приеме у пульмонолога Антонова Владимира Николаевича: о докторе сложилось положительное мнение. Все, что хотелось узнать, я узнала. Доктор очень тактичен, все объяснил. Я получила рекомендации по лечению. Я рада, что попала на прием именно к нему. Спасибо.
читать ответ
- Благодарим вас за отзыв и желаем здоровья!
Публикация настоящих отзывов осуществляется с согласия и разрешения пациентов на обработку и использование персональных данных согласно 152-ФЗ, все пациенты ознакомлены с правилами и политикой обработки персональных данных в ООО «Семейная Клиника Александровская».
Наши телефоны:
+7(922)750-61-43
Пневмония у взрослых: симптомы и признаки, диагностика и лечение
«Не дайте себя обмануть». С приходом холодного времени года увеличивается частота простудных заболеваний. Под их «маской» может скрываться более серьезная проблема, о которой больной человек может даже не подозревать.
Под их «маской» может скрываться более серьезная проблема, о которой больной человек может даже не подозревать.
О такой патологии, как пневмония, мы беседуем с кандидатом медицинских наук, доцентом кафедры пропедевтики внутренних болезней Курского государственного медицинского университета, врачом-пульмонологом ООО «Клиника Эксперт Курск» Поляковым Дмитрием Викторовичем.
- Дмитрий Викторович, что представляет собой пневмония и чем она опасна?
Это острое инфекционное заболевание, в основе которого — воспаление легочной ткани.
Через легкие осуществляется поступление в организм кислорода и выделение из него углекислого газа. Нарушение этих функций, а также прогрессирование инфекционного процесса могут вызывать расстройство деятельности жизненно важных органов, приводя в далеко зашедших случаях к летальному исходу.
- Если пневмония расценивается как инфекционное заболевание, то это означает, что болезнь заразна?
Да, передача ее от человека к человеку в принципе возможна, однако здесь имеет значение, в частности, разновидность пневмонии, а также сопротивляемость организма лиц, контактирующих с больным человеком.
- А какие бывают пневмонии? Их как-то классифицируют?
Да, классификаций достаточно много. Их могут подразделять на группы по причине возникновения — этиологическому фактору (например, бактериальная, вирусная, грибковая, смешанная), степеням тяжести (средней степени, тяжелая), по локализации (право- и левосторонняя, сегментарная, долевая, очаговая), по месту встречаемости (внутри- и внебольничная) и т.д.
- Насколько распространена пневмония в России?
В нашей стране регистрируется ежегодно более пяти миллионов случаев этой патологии. Смертность же от нее составляет порядка 1,2 на 10 тысяч человек.
– Существует ли зависимость частоты возникновения пневмонии и времени года?
Безусловно. В холодное время года она регистрируется гораздо чаще.
- Каковы причины и механизм возникновения пневмонии?
Этиологических факторов много. Статистически более часто встречаются бактериальные поражения легочной ткани. Для запуска развития воспалительного процесса необходим контакт причинного фактора с тканью легкого, с альвеолами. Он может попасть сюда с кровью, лимфой, при травме, а также непосредственно через дыхательные пути. При этом патоген оказывает на них непосредственное повреждающее действие. В ответ на атаку, организм реагирует запуском процессов воспаления. Возникают как местные реакции в виде прилива крови к области внедрения микроорганизмов, отека, накопления в альвеолах воспалительной жидкости (экссудата), так и общие. Развивающиеся патологические изменения и обусловливают появление признаков этого заболевания.
Для запуска развития воспалительного процесса необходим контакт причинного фактора с тканью легкого, с альвеолами. Он может попасть сюда с кровью, лимфой, при травме, а также непосредственно через дыхательные пути. При этом патоген оказывает на них непосредственное повреждающее действие. В ответ на атаку, организм реагирует запуском процессов воспаления. Возникают как местные реакции в виде прилива крови к области внедрения микроорганизмов, отека, накопления в альвеолах воспалительной жидкости (экссудата), так и общие. Развивающиеся патологические изменения и обусловливают появление признаков этого заболевания.
— Какие группы населения входят в группы риска по возникновению пневмонии?
Таких людей немало. Назову некоторые категории повышенного риска:
— болеющие любой ОРВИ;
Что такое ОРВИ? Рассказывает врач-педиатр «Клиника Эксперт Смоленск» Чемова Ульяна Владимировна
— ВИЧ-инфицированные или имеющие другие проблемы с иммунной системой — например, аутоиммунные патологии, состояния после химиотерапии по поводу онкологических заболеваний или иммуносупрессивной терапии;
— больные с тяжелыми хроническими заболеваниями, прежде всего дыхательной и сердечно-сосудистой систем;
— курильщики;
— перенесшие сильное переохлаждение.
Как жить с хронической обструктивной болезнью лёгких, не теряя качества жизни? Узнать здесь
- Расскажите, пожалуйста, о симптомах пневмонии у взрослого человека. Как понять, что обратиться к врачу необходимо?
Типичными проявлениями болезни являются выраженные в разной степени лихорадка, кашель, затруднение дыхания, одышка, общая слабость, быстрая утомляемость, потливость. Если воспаление захватывает и плевру (тонкую пленку, покрывающую легкое снаружи), то могут отмечаться боли в грудной клетке.
На число этих симптомов и их выраженность в каждом конкретном случае влияют, в частности, возраст пациента, наличие у него перенесенных и имеющихся в данный момент заболеваний, факт самолечения до обращения к врачу.
Как нетрудно заметить, некоторые симптомы, встречающиеся при пневмонии, отмечаются и при других заболеваниях дыхательной системы — например при ОРВИ. В связи с этим, при любой простуде нужно всегда допускать возможность того, что это может быть воспаление легкого. Поэтому не следует заниматься самолечением, а сразу обращаться к врачу.
Поэтому не следует заниматься самолечением, а сразу обращаться к врачу.
- Всегда ли пневмония сопровождается температурой и кашлем?
Нет, не всегда — эта болезнь в ряде случаев протекает и без этих симптомов. На наличие и выраженность кашля и лихорадки оказывает влияние множество факторов — в частности: возраст больного; сопутствующие заболевания; объем пораженной легочной ткани; стадия воспалительного процесса; самолечение какими-то препаратами, которые могли «смазать» проявления заболевания.
Таким образом, отсутствие кашля и лихорадки не исключает возможного наличия пневмонии.
- Дмитрий Викторович, какие диагностические методы имеют решающее значение в диагностике пневмонии?
Это комплекс исследований, включающий:
— сбор анамнеза и осмотр пациента с обязательным проведением выслушивания грудной клетки;
— рентгенологические методы исследования органов грудной клетки: флюорография, обзорная рентгенография, компьютерная томография. С их помощью можно с уверенностью говорить о наличии воспалительных изменений в легких;
С их помощью можно с уверенностью говорить о наличии воспалительных изменений в легких;
— лабораторные методы. Основные их задачи — определение причинного фактора, вызвавшего пневмонию, и его чувствительности к лекарственным препаратам;
— спирометрия для оценки функциональной способности легких.
- Какая тактика лечения применяется при пневмонии? Обязательно ли нахождение больного в стационаре или же возможно лечение дома?
Если пациент страдает тяжелой пневмонией, то здесь ответ однозначный: такие больные должны обязательно лечиться в условиях стационара.
Если диагностирована пневмония средней тяжести, по решению врача можно проходить лечение амбулаторно, под строгим контролем и с выполнением всех его назначений.
- Каковы принципы лечения пневмонии в условиях больницы?
Основа терапии — воздействие на причинный фактор. Назначаются антибактериальные препараты двух, а иногда и более разновидностей. При необходимости используются отхаркивающие и жаропонижающие средства.
Как правильно применять антибиотики? Инструкция по применению
- Сколько по времени занимает лечение воспаления лёгких?
Очень условно этот срок составляет 10-14 дней. Однако в зависимости от тяжести патологии, возраста больного, наличия сопутствующих заболеваний продолжительность лечения может существенно увеличиваться.
- Как вы считаете, нужна ли взрослому прививка от пневмонии?
Правильнее говорить о вакцинация против этиологического фактора, вызывающего пневмонию — чаще всего это пневмококк. При отсутствии противопоказаний она целесообразна: научные исследования показали, что ее проведение снижает как частоту возникновения заболевания, так и риск развития осложнений, включая летальные.
- По отзывам пациентов и вашим наблюдениям, после прививки от пневмонии часто возникают побочные эффекты?
Они возникают не чаще, чем от других вакцин.
- Врач какой специальности лечит пневмонию? К кому обратиться за помощью?
В идеале нужно сразу обратиться к пульмонологу.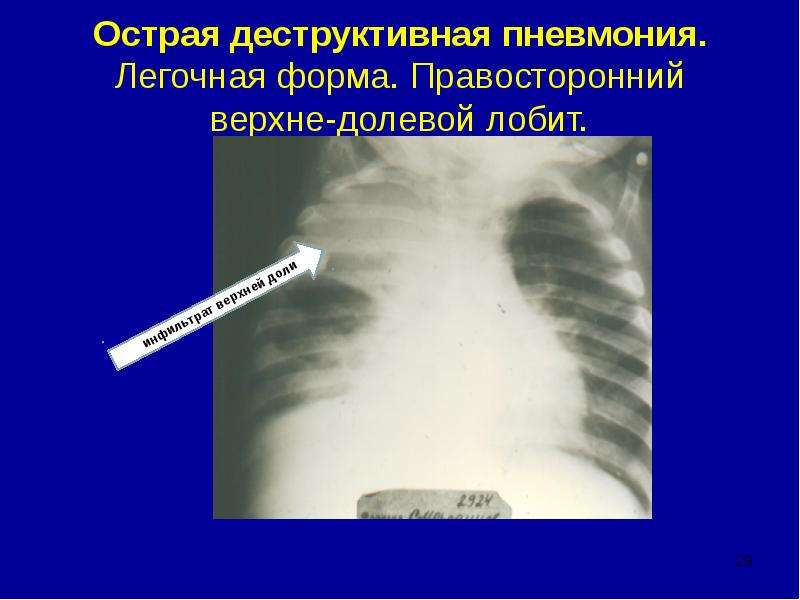 Если такой возможности нет — к терапевту или врачу общей практики.
Если такой возможности нет — к терапевту или врачу общей практики.
Записаться на прием к врачу-пульмонологу можно здесь
внимание: услуга доступна не во всех городах
Для справки
Поляков Дмитрий Викторович
Окончил лечебный факультет Курского государственного медицинского университета в 2004 году.
С 2004 по 2006 год проходил обучение в клинической ординатуре на базе кафедры пропедевтики внутренних болезней. Имеет специализацию врача-терапевта и врача-пульмонолога. Получена дополнительная квалификация – преподаватель высшей школы.
С 2006 года является ассистентом кафедры пропедевтики внутренних болезней вышеназванного ВУЗа.
В 2009 году защитил кандидатскую диссертацию, автор более 60 научных и учебно-методических публикаций.
С 2010 года является заместителем декана международного факультета.
С 2012 года – доцент кафедры пропедевтики внутренних болезней.
В настоящее время работает в качестве врача-пульмонолога в ООО «Клиника Эксперт Курск»
симптомы, диагностика и лечение воспаления легких
Проникшие в легкие человека воздушно-капельным путем, бактерии и вирусы приводят к воспалению легких. Попав в благоприятные для себя условия микроорганизмы начинают размножаться в носоглотке, а затем достигают альвеол легкого. Когда объем вдыхаемой инфекции становится значительным или иммунная защита человека ослаблена, происходит заражение легких. Стремительный иммунный ответ человека повреждает легочную ткань, что приведет к затруднению транспорта кислорода.
Какие бывают пневмонии?
Если человек заболел пневмонией вне больницы, то пневмония называется внебольничной.
Внутрибольничная пневмония, напротив развивается в условиях больниц, домов престарелых. К ней относят и пневмонию, связанную с ИВЛ.
Разделение болезни по ее происхождению помогает выбрать необходимые антибиотики в первые часы болезни.
Чем больше участков легких будет охвачено воспалением, тем драматичнее развитие пневмонии. В зависимости от расположения зон воспаления различают односторонние, двусторонние, полисегментарные, долевые.
«Атипичная» и «типичная» пневмонии
Любая пневмония опасна, если она вовремя не выявлена и не назначено правильное лечение. Слово «атипичная» закрепилось после появления SARS в 2003. Эта пневмония требовала совершенно иного лечения. У атипичной пневмонии жалобы и симптомы могут отличаться от классической — не высокая температура, симптомы больше похожи на ОРВИ.
Типичная пневмония вызывается «классическими» возбудителями. К ним относятся Streptococcus pneumonia (пневмококк), а также Haemophilus influenza(гемофильная палочка) .
Неклассические микроорганизмы вызывают атипичную пневмонию. Например, Legionella, Mycoplasma pneumoniae, Chlamydia pneumoniae, Chlamydia psittaci, Coxiella burnetiid.
Пневмонии, вызванные респираторными вирусами группируются обособленно — Грипп A, Грипп B, Риновирусы, Парагрипп, Аденовирус, Респираторно синцитиальный вирус, Метапневмовирус, Коронавирусы (SARS Cov- 1, SARS Cov-2, MERS).
Различия между «атипичной» и «типичной» условное. Если сделать рентген легких, то возможно предположить атипичный возбудитель по особенностям полученной рентгенограммы.
От чего зависит тяжесть пневмонии?
- Пневмония может ограничиться лихорадкой, кашлем с мокротой без нарушения дыхания. Это описание легкой формы.
- Тяжелое течение проявляется дыхательными расстройствами, полиорганной недостаточностью, сепсисом.
- Иммунный ответ человека определяет степень повреждений легких. Чем массивней ответ, тем тяжелее болезнь.
- Ожирение, хронические болезни сердца и легких, диабет ухудшают прогноз болезни.
Кто чаще болеет пневмониями?
- Чем старше человек, тем выше риск болезни.
- Пациенты, страдающие ХОБЛ, бронхоэктазами, астмой, хроническими болезнями сердца (сердечная недостаточность), инсультом, сахарным диабетом.
- Перенесенная вирусная инфекция (ОРВИ) провоцирует бактериальную или грибковую пневмонию.

- Курение и чрезмерное употребление алкоголя способствует заболеванию
- Другие факторы образа жизни – например, тюрьмы, приюты для бездомных, воздействие экологических токсинов (например, растворителей, красок или бензина)
Симптомы и признаки пневмонии
Жалобы при пневмонии носят внезапный характер. Лихорадка, озноб, усталость, боль в груди в сочетании с кашлем (с мокротой или без), одышка, затрудненное дыхание , учащение дыхания возникают и нарастают в течение нескольких часов.
Анализы крови помогут в диагностике болезни: лейкоцитоз или лейкопения являются результатами воспалительного ответа организма. Воспалительные маркеры, такие как СОЭ, C-реактивный белок и прокальцитонин могут нарастать, хотя последний в значительной степени специфичен для бактериальных инфекций.
Обязательным исследованием для диагностики пневмонии считают рентгенографию легких.
Пневмония при инфекции КОВИД 19.
Течение болезни не выходит за рамки общих представлений о пневмонии. Классические симптомы присутствуют: лихорадка, озноб, боли в мышцах, кашель.
Классические симптомы присутствуют: лихорадка, озноб, боли в мышцах, кашель.
80 % болеют пневмонией без нарушения дыхания и в домашних условиях.
У 20% тяжелые проявления болезни: затруднено дыхание, человек начинает дышать часто, возникает потребность использовать дополнительно кислород. При ухудшении может возникнуть отказ важных органов- сердца, почек. Чем дольше пациент находится в больнице, тем больше вероятности присоединения больничной инфекции и грибов.
Обязательно необходима госпитализация при пневмонии COVID 19?
Нет, госпитальное лечение требуется не всегда.
Амбулаторный режим возможен для пациентов с легкой пневмонией. Пациенты, которые исходно здоровы, с нормальным дыханием, без сопутствующих заболеваний лечатся в домашних условиях.
Госпитализация необходима для пациентов, у которых насыщение кислородом менее 94% , они часто дышат.
Мне кажется, что мне тяжело дышать. У меня дыхательная недостаточность?
Самый простой способ понять, что у вас развивается дыхательная недостаточность – подсчитать «вдох-выдох» за минуту. Если более 21, то следует вызвать врача. Другой способ — это измерить кислород в крови. Пульсоксиметр уже есть у многих дома. Этим прибором можно следить за сатурацией — если она ниже 94%, то расценить эту ситуацию как ухудшение и обратиться за помощью к врачам.
Если более 21, то следует вызвать врача. Другой способ — это измерить кислород в крови. Пульсоксиметр уже есть у многих дома. Этим прибором можно следить за сатурацией — если она ниже 94%, то расценить эту ситуацию как ухудшение и обратиться за помощью к врачам.
Применение КТ в диагностике вирусных пневмоний.
Компьютерная томография имеет высокую чувствительность по сравнению с рентгенографией, обнаруживает изменения лёгких на начальных этапах заболевания раньше результатов лабораторных тестов.
- преимущество метода — в выявлении изменений в лёгких даже у людей, инфицированных COVID-19, но у которых отсутствуют симптомы инфекции.
- Несмотря на высокую чувствительность, КТ не может дать точного ответа о причинах пневмонии (бактерии, вирусы, грибы).
Что такое «матовое стекло» в заключении КТ?
Уплотнения лёгочной ткани “матовое стекло” — это начальная фаза воспаления легких. Возникает при постепенном заполнении альвеол жидкостью.
Когда бронхи и альвеолы заполнятся жидкостью, возникнут участки уплотнения, которые называются консолидацией. Консолидация лёгочной ткани возникает при длительном воспалительном процессе.
У меня COVID 19 и КТ-2 Что это означает?
Важно понять сколько легочной ткани поражено. Чем больше вовлечено легочной ткани в воспаление, тем более затруднено получение кислорода из вдыхаемого воздуха. Без кислорода человек быстро погибает. Например, при пневмонии, вызванной COVID 19, ухудшение в легких занимает несколько часов. Чем раньше будет принято решение о госпитализации, кислородотерапии и лечении, тем больше шансов вылечиться.
Для оценки изменений подсчитывается сколько процентов легких повреждено пневмонией. Измерение проводится «на глаз». Полученный результат сопоставляется с шкалой распространённости изменений:
- КТ-0 – нет признаков пневмонии
- КТ-1 – до 25%
- КТ-2 – от 25 до 50%
- КТ-3 – от 50 до 75%
- КТ-4 – свыше 75%
Процентная оценка сортирует пациентов, кому срочно требуется госпитальное лечение и тех, кто может лечиться в домашних условиях.
Если у вас КТ 2, это соответствует легкой пневмонии. Такие изменения не сопровождаются затрудненным дыханием, не требуют госпитализации. Но КТ 2 может при неправильном лечении перейти в КТ 3 и 4. Поэтому наблюдение со стороны врача обязательно!
Если врач не слышит хрипы в легких при прослушивании, значит у меня нет пневмонии?
Это неверно. Постановка диагноза требует демонстрации изменений в легочной ткани при рентгенографии (КТ) и клинических проявлений (например, лихорадка, одышка, кашель и образование мокроты), изменений в анализах крови.
Лечение пневмонии
Для лечения пневмонии необходимо знать название инфекции. У пациентов название возбудителя в самом начале болезни неизвестно, поэтому применяется эмпирическая терапия антибиотиками – лечение, направленное на вероятного возбудители. Для всех пациентов с ВП разработаны схемы лечения, нацеленные на уничтожение S.pneumoniae и атипичных возбудителей.
Для большинства больных используют комбинированную терапию с бета-лактамными антибиотиками либо макролидами. Альтернативные схемы включают монотерапию фторхинолоном.
Лечение SARS CoV-2
- Принципы лечение пневмонии общие. Назначение противовирусной и антибактериальной терапии.
- В тяжелых случаях, в условиях больницы назначение высокопоточной кислородотерапии, моноклональных антител, антикоагулянтов, легочной вентиляции.
- Антибиотики на вирус COVID 19 не действуют.
Реабилитация после пневмонии
Помимо лекарственной терапии, направленной на бактерии, вирус и воспаление, необходимо восстановление функции легких до исходного здорового уровня..
После перенесенной болезни в легких формируются изменения. Это и «матовое стекло» и фиброз легочной ткани, пневмофиброз. В этих участках затруднен газообмен, нарушено питание альвеол и бронхов, защита бронхов снижается. Инфекция и пневмония действуют на человека одновременно лишая сил, уверенности, снижается качество жизни Необходимо приложить усилия и предотвратить фиброзные изменения в легких. Решает задачу реабилитационная программа, состоящая из комплекса лечебных процедур, ингаляций, дыхательных тренажеров, упражнений ЛФК.
Подробнее о реабилитации
Наши специалисты
Чикина Светлана Юрьевна
Кандидат медицинских наук, врач-пульмонолог высшей категории. Официальный врач эксперт конгрессов РФ по пульмонологии.
Опыт работы 30 лет
Мещерякова Наталья Николаевна
Кандидат медицинских наук, врач-пульмонолог высшей категории, доцент кафедры пульмонологии им. Н.И. Пирогова.
Опыт работы 26 лет
Никитина Наталия Владимировна
Зам. главного врача, пульмонолог аллерголог высшей категории. Действительный член Европейской академии аллергологии и иммунологии.
Опыт работы 15 лет
Стоимость услуг
| Консультативный прием пульмонолога | ✕| |
|---|---|
| Первичная консультация пульмонолога | 3500 |
| Повторная консультация пульмонолога | 3000 |
| Первичная консультация главного врача, пульмонолога Кулешова А.В. | 5000 |
| Повторная консультация главного врача, пульмонолога Кулешова А.В. | 3000 |
Клинические особенности диагностики пневмонии у взрослых в учреждениях первичной медико-санитарной помощи: систематический и мета-обзор
Колин М., и др. . Глобальные и региональные причины смерти: модели и тенденции, 2000–15 гг. (2017).
Cillóniz, C., Cardozo, C. & García-Vidal, C. Эпидемиология, патофизиология и микробиология внебольничной пневмонии. Анналы исследовательских больниц , 2 (1) (2018).
Леви, М.Л. и др. . Краткое изложение первичной медико-санитарной помощи Рекомендаций Британского торакального общества по ведению внебольничной пневмонии у взрослых: обновление 2009 г. Одобрен Королевским колледжем врачей общей практики и Респираторным обществом первичной медико-санитарной помощи Великобритании. Prim Care Respir J 19 (1), 21–7 (2010).
Артикул
Google ученый
Mandell, L.A. et al. . Общество инфекционных болезней Америки / Консенсусное руководство Американского торакального общества по ведению внебольничной пневмонии у взрослых. Клинические инфекционные болезни 44 (Приложение_2), S27 – S72 (2007).
CAS
Статья
Google ученый
Линч, Т. и др. . Систематический обзор диагностики детской бактериальной пневмонии: когда золото — это бронза. Plos One 5 (8), e11989 (2010).
ADS
Статья
Google ученый
Нидерман, М.С. Визуализация для лечения внебольничной пневмонии: что делать, если рентгенограмма грудной клетки ясна. СУНДУК 153 (3), 583–585 (2018).
Артикул
Google ученый
AI_Mulhim, F.A. et al . Правило клинического прогноза легочных инфильтратов. Саудовский медицинский журнал 19 (3), 306–312 (1998).
Google ученый
Diehr, P. et al. . Прогнозирование пневмонии у амбулаторных больных с острым кашлем — статистический подход. Журнал хронических болезней 37 (3), 215–225 (1984).
MathSciNet
CAS
Статья
Google ученый
Gennis, P. et al . Клинические критерии выявления пневмонии у взрослых: Руководство по заказу рентгенограммы грудной клетки в отделении неотложной помощи. Journal of Emergency Medicine 7 (3), 263–268 (1989).
CAS
Статья
Google ученый
Graffelman, A. W. et al. . Могут ли только анамнез и обследование достоверно предсказать пневмонию? J Fam Pract 56 (6), 465–70 (2007).
CAS
PubMed
Google ученый
Heckerling, P. S. et al . Правило клинического прогноза легочных инфильтратов. Annals of Internal Medicine 113 (9), 664–670 (1990).
CAS
Статья
Google ученый
Мур, М. и др. . Предикторы пневмонии при инфекциях нижних дыхательных путей: проспективное когортное исследование кашля 3C. Eur Respir J , 50 (5) (2017).
Артикул
Google ученый
Сингал Б. М., Хеджес Дж. Р. и Радак К. Л. Правила принятия решений и клиническое прогнозирование пневмонии: оценка критериев низкой эффективности. Annals of Emergency Medicine 18 (1), 13–20 (1989).
CAS
Статья
Google ученый
Rambaud-Althaus, C. et al. . Клинические особенности диагностики пневмонии у детей младше 5 лет: систематический обзор и метаанализ. Инфекционные болезни Lancet 15 (4), 439–450 (2015).
Артикул
Google ученый
Moher, D. et al. . Предпочтительные элементы отчетности для систематических обзоров и метаанализов: Заявление PRISMA. PLOS Medicine 6 (7), e1000097 (2009).
Артикул
Google ученый
Whiting, P. F. et al. . QUADAS-2: Пересмотренный инструмент для оценки качества исследований диагностической точности. Annals of Internal Medicine 155 (8), 529–536 (2011).
Артикул
Google ученый
Decks, J. J. Систематические обзоры в здравоохранении: Систематические обзоры оценок диагностических и скрининговых тестов. BMJ-British Medical Journal-International Edition 323 (7305), 157–162 (2001).
Артикул
Google ученый
Граймс, Д. А. и Шульц, К. Ф. Уточнение клинического диагноза с помощью отношений правдоподобия. Ланцет 365 (9469), 1500–1505 (2005).
Артикул
Google ученый
Эбелл, М. Х., Уайт, Л., и Касо, Т. Систематический обзор истории болезни и физикальное обследование для диагностики гриппа. J Am Board Fam Pract 17 (1), 1–5 (2004).
Артикул
Google ученый
Арендс, Л. Р. и др. .Двумерный метаанализ случайных эффектов ROC-кривых. Принятие медицинских решений 28 (5), 621–638 (2008).
CAS
Статья
Google ученый
R Development Core Team, R., Язык и среда для статических вычислений: Вена , Австрия (2016).
Европейская сеть оценки технологий здравоохранения Метаанализ исследований точности диагностических тестов.(2014).
Рейцма, Дж. Б. и др. . Двумерный анализ чувствительности и специфичности дает информативные сводные показатели в диагностических обзорах. Журнал клинической эпидемиологии 58 (10), 982–990 (2005).
Артикул
Google ученый
Эбрагимзаде, А. и др. . Клинические и лабораторные данные у пациентов с острыми респираторными симптомами, указывающими на необходимость рентгенографии грудной клетки при внебольничной пневмонии. Iran J Radiol 12 (1), e13547 (2015).
MathSciNet
PubMed
PubMed Central
Google ученый
Flanders, S. A. et al. . Проведение прикроватного теста на С-реактивный белок в диагностике внебольничной пневмонии у взрослых с острым кашлем. Американский журнал медицины 116 (8), 529–535 (2004).
CAS
Статья
Google ученый
Holm, A. et al. . Этиология и прогноз пневмонии при инфекциях нижних дыхательных путей в первичной медико-санитарной помощи. Br J Gen Pract 57 (540), 547–54 (2007).
PubMed
PubMed Central
Google ученый
Holm, A. et al. . Прокальцитонин в сравнении с С-реактивным белком для прогнозирования пневмонии у взрослых с инфекциями нижних дыхательных путей в первичной медико-санитарной помощи. Br J Gen Pract 57 (540), 555–60 (2007).
PubMed
PubMed Central
Google ученый
Хопстакен Р. М. и др. . Вклад симптомов, признаков, скорости оседания эритроцитов и С-реактивного белка в диагностику пневмонии при острой инфекции нижних дыхательных путей. Br J Gen Pract 53 (490), 358–64 (2003).
CAS
PubMed
PubMed Central
Google ученый
Hopstaken, R.M., Cals, J. W. & Dinant, G.J. Точность липополисахарид-связывающего белка (LBP) и фибриногена по сравнению с C-реактивным белком (CRP) в дифференциации пневмонии от острого бронхита в первичной медико-санитарной помощи. Prim Care Respir J 18 (3), 227–30 (2009).
Артикул
Google ученый
Melbye, H., Straume, B. & Brox, J. Лабораторные тесты на пневмонию в общей практике: диагностические значения зависят от продолжительности болезни. Scand J Prim Health Care 10 (3), 234–40 (1992).
CAS
Статья
Google ученый
Melbye, H. et al. . Диагноз взрослой пневмонии в общей практике. Диагностическая ценность анамнеза, физического осмотра и некоторых анализов крови. Scand J Prim Health Care 6 (2), 111–7 (1988).
CAS
Статья
Google ученый
Моберг, А. Б. и др. . Внебольничная пневмония в первичной медико-санитарной помощи: клиническая оценка и применимость рентгенографии грудной клетки. Scand J Prim Health Care 34 (1), 21–7 (2016).
CAS
Статья
Google ученый
Нолт Б. Р. и др. . Аномалии жизненно важных функций как предикторы пневмонии у взрослых с острым кашлем. Американский журнал неотложной медицины 25 (6), 631–636 (2007).
Артикул
Google ученый
Steurer, J. et al. . Помощь в принятии решений, позволяющая исключить пневмонию и сократить ненужные назначения антибиотиков пациентам первичной медико-санитарной помощи с кашлем и лихорадкой. BMC Med 9 , 56 (2011).
Артикул
Google ученый
van Vugt, S. F. et al . Использование сывороточных концентраций C-реактивного белка и прокальцитонина в дополнение к симптомам и признакам для прогнозирования пневмонии у пациентов, обращающихся в первичную медико-санитарную помощь с острым кашлем: диагностическое исследование. Bmj 346 , f2450 (2013).
Артикул
Google ученый
Wang, K. et al. . Клинические симптомы и признаки для диагностики Mycoplasma pneumoniae у детей и подростков с внебольничной пневмонией. Кокрановская база данных Syst Rev 10 , Cd009175 (2012).
PubMed
Google ученый
Кретикос, М.А. и др. . Частота дыхания: запущенный жизненный знак. Медицинский журнал Австралии 188 (11), 657–659 (2008).
PubMed
Google ученый
Schierenberg, A. et al. . Внешняя проверка моделей прогнозирования пневмонии у пациентов первичного звена с инфекцией нижних дыхательных путей: метаанализ индивидуальных данных пациента. PLoS One 11 (2), e0149895 (2016).
Артикул
Google ученый
Müller, F. et al. . Уровни прокальцитонина предсказывают бактериемию у пациентов с внебольничной пневмонией: проспективное когортное исследование. Сундук 138 (1), 121–129 (2010).
Артикул
Google ученый
Чан, Ю.-Л. и др. . Прокальцитонин как маркер бактериальной инфекции в отделении неотложной помощи: обсервационное исследование. Critical Care 8 (1), R12 (2003).
Артикул
Google ученый
Крист-Карин, М. Прокальцитонин при бактериальных инфекциях — шумиха, надеюсь, более или менее? Швейцарский медицинский еженедельник, 135 (3132) (2005).
Berg, P. & Lindhardt, B. Ø. Роль прокальцитонина у взрослых пациентов с внебольничной пневмонией — систематический обзор. Dan Med J 59 (3), A4357 (2012).
PubMed
Google ученый
Лю Д. и др. . Прогностическое значение прокальцитонина при пневмонии: систематический обзор и метаанализ. Respirology 21 (2), 280–288 (2016).
Артикул
Google ученый
Meili, M. et al. . Ведение пациентов с респираторными инфекциями в первичной медико-санитарной помощи: прокальцитонин, С-реактивный белок или оба? Экспертный обзор респираторной медицины 9 (5), 587–601 (2015).
CAS
Статья
Google ученый
Simon, L. et al. . Уровни прокальцитонина и С-реактивного белка в сыворотке как маркеры бактериальной инфекции: систематический обзор и метаанализ. Клинические инфекционные болезни 39 (2), 206–217 (2004).
CAS
Статья
Google ученый
Falk, G. & Fahey, T. C-реактивный белок и внебольничная пневмония в амбулаторной помощи: систематический обзор исследований диагностической точности. Семейная практика 26 (1), 10–21 (2008).
Артикул
Google ученый
Minnaard, M. C. et al. . Дополнительная диагностическая ценность пяти различных устройств для тестирования С-реактивного белка в месте оказания медицинской помощи при выявлении пневмонии в учреждениях первичной медико-санитарной помощи: вложенное исследование «случай-контроль». Scand J Clin Lab Invest 75 (4), 291–5 (2015).
CAS
Статья
Google ученый
Диагностика и лечение внебольничной пневмонии у детей и взрослых | Журнал этики
Внебольничная пневмония (ВП) — это часто диагностируемое заболевание, определяемое как «острая инфекция паренхимы легких, приобретенная вне больницы» [1].Этиология ВП часто остается неустановленной, потому что трудно получить прямой образец инфицированной ткани для культивирования. Это может стать проблемой при диагностике и лечении ВП. Хотя взрослые с ВП обычно проявляются кашлем, лихорадкой, выделением мокроты и плевритическими болями в груди, наряду с наличием острого инфильтрата на рентгенограмме грудной клетки [2], широкий спектр проявлений у детей может затруднить их диагностику. В то время как ВП может проявляться как острое лихорадочное заболевание с клинической декомпенсацией у некоторых детей, небольшой процент педиатрических пациентов в возрасте до 5 лет может просто иметь лихорадку и боль в животе без респираторного дистресса [3].В этой статье будут рассмотрены текущие клинические рекомендации по диагностике и лечению внебольничной пневмонии у ранее здоровых детей и взрослых; аспирация и небактериальная пневмония в обсуждение не включаются.
Дети в возрасте от 60 дней до 18 лет (которые не были госпитализированы в течение 7 дней с момента обращения)
Диагностика . Сбор анамнеза и полное физическое обследование имеют решающее значение для диагностики ВП у детей. Анамнез пациента должен включать возраст ребенка, тип симптомов и дату начала, статус иммунизации (особенно Streptococcus pneumoniae и грипп), возможность аспирации и недавнее заражение туберкулезом.Полный медицинский осмотр, включая жизненно важные признаки, часто может помочь определить тяжесть пневмонии. Тяжелобольных детей следует обследовать на предмет признаков парапневмонического выпота или эмпиемы, включая одышку, сухой кашель, плевритную боль в груди, шум трения при аускультации или ослабление дыхания. У детей с менее острым заболеванием следующие комбинации клинических данных являются наиболее вероятными прогностическими факторами тяжелой ВП [3]:
- У младенцев младше 12 месяцев: расширение носа и сатурация кислорода (SpO2) менее 96 процентов при комнатной температуре, частота дыхания выше 50 и втягивание межреберных промежутков.
- У детей от 1 до 5 лет: SpO2 менее 96 процентов и частота дыхания более 40.
- У детей старше 5 лет: SpO2 менее 96 процентов и частота дыхания более 30.
Дальнейшие лабораторные исследования и визуализирующие исследования, такие как рентген грудной клетки, следует заказывать только на основании клинических данных и высокого индекса подозрения [3]. У детей полный анализ крови (CBC) следует рассматривать только в том случае, если эта дополнительная информация может помочь определить использование антибиотиков, поскольку ценность CBC для детей с признаками и симптомами пневмонии не подтверждена убедительными доказательствами.Обычно при бактериальных инфекциях количество лейкоцитов составляет 15 000 на мм или более [3]. В клинических рекомендациях CAP 2009 г. Техасской детской больницы посев крови обычно не рекомендуется при неосложненной бактериальной пневмонии, особенно в амбулаторных условиях. Однако он может быть полезен для детей с более тяжелым заболеванием, если его собрать до введения антибиотиков. Туберкулиновая кожная проба должна быть проведена, если путешествия и анамнез предполагают возможное заражение туберкулезом, а у детей с кашлем продолжительностью более 2 недель можно получить полимеразную цепную реакцию коклюша (ПЦР) из мазка из носоглотки.
Лечение . В общем, лечение антибиотиками не следует откладывать в ожидании результатов лабораторных исследований. При выборе антибактериальной терапии следует принимать во внимание условия лечения (стационарное или амбулаторное) и возраст ребенка, которые могут влиять на возбудитель болезни и его восприимчивость к лечению. Большинство неосложненных пневмоний у здоровых детей можно лечить амбулаторно. Показания к госпитализации включают тяжелое обезвоживание, непереносимость пероральной регидратации или приема лекарств, респираторный дистресс от умеренной до тяжелой степени, измененное психическое состояние, потребность в кислороде, плохое соблюдение режима лечения или отсутствие последующего наблюдения после выписки или безуспешное амбулаторное лечение [3].
В амбулаторных условиях высокие дозы амоксициллина (80-100 мг на кг в день) оказались разумным вариантом лечения ВП, поскольку Streptococcus pneumoniae является распространенным патогеном (наиболее распространенным в некоторых возрастных группах) среди детей. . Согласно клиническим рекомендациям Детской больницы Texas, амбулаторное лечение различается в зависимости от возрастной группы:
- Дети от 3 месяцев до 2 лет: высокие дозы амоксициллина в течение 10 дней для покрытия Streptococcus pneumoniae .Детей младше 2 лет, которые не переносят пероральные препараты, следует лечить одной внутримышечной дозой цефтриаксона из расчета 50 мг на кг.
- Дети в возрасте от 2 до 5 лет: амоксициллин в высоких дозах в течение 10 дней плюс макролид для лечения атипичных патогенов. Можно рассмотреть вариант монотерапии амоксициллином, если нет опасений по поводу атипичных патогенов, но следует добавить второй антибиотик, если нет ответа после 24-48 часов монотерапии.
- Дети старше 5 лет: амоксициллин в высоких дозах в течение 10 дней плюс макролид.
В условиях стационара, не в отделении интенсивной терапии, рекомендованная терапия в соответствии с возрастными группами:
- От 3 месяцев до 2 лет: ампициллин или цефотаксим для покрытия Streptococcus pneumoniae .
- От 2 до 5 лет: ампициллин или цефотаксим с макролидом, если необходимо, чтобы покрыть Streptococcus pneumoniae и атипичные патогены.
- Старше 5 лет: ампициллин или цефотаксим с макролидом, если необходимо, чтобы покрыть Streptococcus pneumoniae и атипичные патогены.
Дети, переходящие на пероральные антибиотики, должны получать антибиотики не менее 10 дней, когда клиническое улучшение будет продемонстрировано с помощью данной терапии.
Антибактериальную терапию следует применять в соответствии с антибиотикограммой и характером чувствительности / резистентности Streptococcus pneumoniae , наблюдаемым в каждой конкретной больнице. Особые соображения и соответствующие рекомендации по лечению применимы к детям с осложненной пневмонией или плевральным выпотом, тем, кто нуждается в интенсивной терапии, и тем, у кого не наблюдается клинических улучшений по сравнению с предлагаемой терапией.
Взрослые старше 18 лет (которые не были госпитализированы в течение 7 дней с момента обращения)
Диагностика . У взрослых ВП обычно представляет собой совокупность симптомов, указывающих на кашель, лихорадку, выделение мокроты и плевритную боль в груди, наряду с наличием острого инфильтрата на рентгенограмме грудной клетки с микробиологическими данными или без них [2]. Как и у детей, лечение и прогноз ВП у взрослых зависят от первоначальной оценки тяжести заболевания.Еще раз, важными частями оценки являются анамнез и физикальное обследование. Если есть инфильтрат на рентгенограмме грудной клетки у здорового взрослого человека, следует настоятельно рассмотреть внебольничную пневмонию.
При оценке взрослых с ВП прогностические модели (например, индекс тяжести PORT или CURB-65) могут быть полезны для определения тяжести и, следовательно, условий лечения заболевания [4]. Согласно руководству по клинической практике Американского общества инфекционных заболеваний (IDSA) 2010 г., критерии тяжелой ВП включают, помимо прочего, учащенное дыхание (более 30 вдохов в минуту), гипоксемию, уремию, измененные сенсорные ощущения, лейкопению, гипотонию. требующие жидкости или вазопрессоров и многодолевых инфильтратов.Критерии госпитализации и выписки также должны учитывать комплаентность и поддержку в амбулаторных условиях [2].
За исключением рентгенограммы грудной клетки, большинство других лабораторных тестов у взрослых с явным клиническим подтверждением ВП не являются обязательными в амбулаторных условиях. Рекомендации IDSA включают конкретные указания для более обширных диагностических исследований, таких как посев крови, посев мокроты, анализ мочи на легионеллу и пневмококковый антиген, а также исследования грибков и туберкулеза [4].
Лечение . Как и у детей, лечение антибиотиками не следует откладывать в ожидании результатов лабораторных анализов и следует учитывать условия лечения. Для амбулаторного лечения взрослых без сопутствующих заболеваний макролиды или доксициклин являются приемлемыми препаратами первой линии. У взрослых с сопутствующими заболеваниями, такими как диабет, злокачественные новообразования, хроническая обструктивная болезнь легких или другие хронические заболевания, в качестве монотерапии можно использовать респираторный фторхинолон (например, моксифлоксацин, гемифлоксацин или левофлоксацин) или передовые макролиды (азитромицин или кларитромицин) [ 2, 4].Также можно использовать бета-лактамы (такие как амоксициллин в высоких дозах или амоксициллин-клавуланат) с макролидами. В регионах с 25-процентным или более высоким уровнем инфицирования устойчивым к макролидам Streptococcus pneumoniae высокого уровня, пациентов с сопутствующими заболеваниями или без них следует лечить респираторным фторхинолоном или комбинированной терапией бета-лактамным агентом и макролидом, как указано выше. [2, 4].
В условиях стационара клиницист должен проконсультироваться с антибиотикограммой в конкретной больнице для определения восприимчивости и резистентности распространенных возбудителей ВП.Лечение первой линии ВП у взрослых в медицинском отделении должно состоять из монотерапии респираторным фторхинолоном или, для некоторых пациентов, комбинацией передовых макролидов с бета-лактамным агентом, таким как цефотаксим, цефтриаксон, ампициллин или эртапенем. Если псевдомонадная инфекция вызывает особую озабоченность, следует назначать антипневмококковые и антипсевдомональные бета-лактамы, такие как цефепим, имипенем, меропенем или пиперациллин-тазобактам, в комбинации с ципрофлоксацином или левофлоксацином [2, 4].
Как всегда, особое внимание следует уделять пациентам с осложненной пневмонией или признаками плеврального выпота, а также пациентам, нуждающимся в интенсивной терапии.
Список литературы
Медицинский центр детской больницы Цинциннати. Рекомендации по оказанию помощи, основанные на фактических данных: внебольничная пневмония у детей в возрасте от 60 дней до 17 лет; Декабрь 2005 г. http://www.cincinnatichildrens.org / assets / 0/78/1067/2709/2777/2793/9199 / 1633ae60-cbd1-4fbd-bba4-cb687fbb1d42.pdf. По состоянию на 7 июля 2011 г.
Американское общество инфекционных болезней. Карманная карта с рекомендациями: внебольничная пневмония у взрослых; 2010. http://guidelinecentral.com/viewers/community_acquired_pneumonia.html. По состоянию на 14 июля 2011 г.
Центр доказательной медицины Техасской детской больницы. Клинические рекомендации по внебольничной пневмонии (ВП); Февраль 2009 г.
Манделл Л.А., Бартлетт Дж. Г., Доуэлл С. Ф., Файл TM мл., Мушер Д. М., Уитни С. Общество инфекционных болезней Америки. Обновление практических рекомендаций по ведению внебольничной пневмонии у иммунокомпетентных взрослых. Clin Infect Dis . 2003; 37 (11): 1405-1433.
Цитата
Виртуальный наставник. 2011; 13 (8): 551-554.
DOI
10.1001 / virtualmentor.2011.13.8.cprl1-1108.
Точки зрения, выраженные в этой статье, принадлежат авторам и не обязательно отражают взгляды и политику AMA.
Информация об авторе
Ю-Сян «Клара» Линь, доктор медицины , второй год учится по комбинированной программе ординатуры по внутренним болезням и педиатрии в Медицинском колледже Бейлора в Хьюстоне, штат Техас.У нее широкий круг исследовательских интересов, включая инфекционные заболевания как у взрослых, так и у детей.
Ануп Агравал, доктор медицины , доцент кафедры комбинированной внутренней медицины и педиатрии в Медицинском колледже Бейлора в Хьюстоне, штат Техас. Он является медицинским директором клиники непрерывного ухода за пациентами.
Внебольничная пневмония — подход к диагностике
Обновленную информацию о диагностике и лечении сопутствующих состояний во время пандемии см. В нашей теме «Управление сопутствующими заболеваниями в контексте COVID-19».
Анамнез пациента и физический осмотр являются важными частями диагностики и могут выявить симптомы, соответствующие ВБП, иммунным дефектам и / или потенциальному воздействию определенных патогенов. Однако для окончательного диагноза пневмонии необходимо наличие нового инфильтрата на рентгенограмме грудной клетки.
История болезни
Целью сбора анамнеза должно быть выявление симптомов, соответствующих ВП, дефектов иммунитета и возможного риска воздействия конкретных патогенов.
Факторы риска включают возраст> 65 лет, пребывание в медицинском учреждении, ХОБЛ, ВИЧ-инфекцию, воздействие сигаретного дыма, злоупотребление алкоголем, плохую гигиену полости рта, контакт с детьми и употребление определенных наркотиков (например,g., кислотоснижающие препараты, ингаляционные кортикостероиды, нейролептики, противодиабетические препараты, опиоиды). Сахарный диабет и хронические заболевания печени или почек также связаны с ВП.
Обычно присутствуют клинические признаки и признаки инфекции (лихорадка или озноб и лейкоцитоз) и респираторных симптомов (включая кашель, часто с увеличением выделения мокроты, отхаркивание, одышку, плевритную боль и кровохарканье). Могут сообщаться неспецифические симптомы, такие как миалгия и артралгия.У пациентов пожилого возраста, пациентов с хроническими заболеваниями и пациентов с ослабленным иммунитетом признаки и симптомы легочной инфекции могут быть менее выраженными, а пневмония может остаться нераспознанной из-за наличия недыхательных симптомов.
Некоторые причины пневмонии (например, легионеллез) могут иметь специфический анамнез. Легионеллез может проявляться головной болью, спутанностью сознания, пищеварительными проявлениями, такими как диарея, и клиническими проявлениями гипонатриемии.
Инфекция Mycoplasma pneumoniae чаще всего встречается у молодых пациентов и пациентов, которые лечились антибиотиками до того, как у них возникла пневмония.Он может проявляться внелегочными проявлениями, такими как мирингит, энцефалит, увеит, ирит и миокардит. [18] Torres A, Barberán J, Falguera M, et al. Междисциплинарные рекомендации по ведению внебольничной пневмонии [на испанском языке]. Med Clin (Barc). 2 марта 2013 г .; 140 (5): 223.e1-223.e19.
http://www.ncbi.nlm.nih.gov/pubmed/23276610?tool=bestpractice.com
[65] Менендес Р., Торрес А., Аспа Дж. И др. Внебольничная пневмония: новые рекомендации Испанского общества болезней грудной клетки и торакальной хирургии (SEPAR) [на испанском языке].Arch Bronconeumol. Октябрь 2010; 46 (10): 543-58.
http://www.archbronconeumol.org/en/linkresolver/neumonia-adquirida-comunidad-nueva-normativa/S0300289610002000
http://www.ncbi.nlm.nih.gov/pubmed/20832928?tool=bestpractice.com
Физический осмотр
Проведите медицинский осмотр. У пациента может быть лихорадка, тахикардия и одышка в покое. При аускультации грудной клетки могут быть обнаружены потрескивания, хрипы или бронхиальное дыхание, а также может наблюдаться притупление перкуссии или тактильной голосовой фермита.
Визуализация
Как можно скорее закажите рентген грудной клетки всем пациентам, поступившим в больницу с подозрением на ВП, чтобы подтвердить или исключить диагноз. Нет необходимости делать рентген грудной клетки амбулаторным пациентам с подозрением на ВП, если диагноз не вызывает сомнений, пациент не отвечает на лечение удовлетворительно или считается, что у пациента имеется риск основной патологии легких. [66] Лим В.С., Бодуэн С.В., Джордж Р.К. и др .; Комитет по рекомендациям по пневмонии Комитета по стандартам лечения BTS.Рекомендации Британского торакального общества по ведению внебольничной пневмонии у взрослых: обновление 2009 г. Thorax. 2009 октябрь; 64 (приложение 3): iii1-iii55.
https://thorax.bmj.com/content/64/Suppl_3/iii1.long
http://www.ncbi.nlm.nih.gov/pubmed/19783532?tool=bestpractice.com
Задне-передняя и латеро-латеральная проекции увеличивают вероятность диагностики пневмонии и полезны для определения степени тяжести заболевания.
Приоритет рентгена грудной клетки в диагностике ВП оспаривается исследованиями с использованием УЗИ легких и компьютерной томографии (КТ) грудной клетки.Рассмотрите возможность заказа УЗИ легких, если рентген грудной клетки отрицательный, пациент пожилой и слабый или клинические подозрения сомнительны. Рассматривайте КТ грудной клетки только у пациентов с неопределенным диагнозом после рентгена грудной клетки и УЗИ. [67] Niederman MS. Визуализация для лечения внебольничной пневмонии: что делать, если рентгенограмма грудной клетки четкая. Грудь. Март 2018; 153 (3): 583-5.
http://www.ncbi.nlm.nih.gov/pubmed/29519296?tool=bestpractice.com
УЗИ легких представляет собой простой и доступный метод диагностики ВП.Он не содержит радиации, и его использование особенно ценно, когда рентген грудной клетки недоступен. Диагноз ВБП с помощью прикроватного ультразвукового исследования легких в основном зависит от выявления консолидации. Однако консолидация не всегда присутствует при ВП, поскольку пневмония может быть интерстициальной или проявляться в виде диффузных легочных инфильтратов. [68] Reissig A, Gramegna A, Aliberti S. Роль УЗИ легких в диагностике и последующем наблюдении внебольничных пневмония. Eur J Intern Med. 2012 июл; 23 (5): 391-7.
http: // www.ncbi.nlm.nih.gov/pubmed/22726366?tool=bestpractice.com
Систематические обзоры показали, что УЗИ легких позволяет с высокой точностью диагностировать пневмонию у взрослых, в том числе в отделениях неотложной помощи. [69] Ллама-Альварес А.М., Тенца-Лозано Е.М., Латур-Перес Дж. Точность ультразвукового исследования легких в диагностике пневмонии у пациентов. взрослые: систематический обзор и метаанализ. Грудь. 2017 Февраль; 151 (2): 374-82.
http://www.ncbi.nlm.nih.gov/pubmed/27818332?tool=bestpractice.com
[70] Орсо Д., Гульельмо Н., Копетти Р.УЗИ легких в диагностике пневмонии в отделении неотложной помощи: систематический обзор и метаанализ. Eur J Emerg Med. 2018 Октябрь; 25 (5): 312-21.
http://www.ncbi.nlm.nih.gov/pubmed/2
51?tool=bestpractice.com
КТ грудной клетки может улучшить диагностику ВП, поскольку рентгенография грудной клетки может привести к ошибочному диагнозу. КТ грудной клетки дает подробную информацию о паренхиме легких и средостении. Однако основные ограничения включают воздействие радиации, высокую стоимость и невозможность тестирования у постели больного.Одно исследование показало, что у пациентов, поступающих в отделение неотложной помощи с подозрением на ВП, ранние результаты компьютерной томографии, когда КТ используется в дополнение к рентгену грудной клетки, заметно влияют как на диагностику, так и на клиническое ведение. [71] Классенс Й.Е., Дебрей М.П., Тубач Ф. и др. Раннее сканирование с помощью компьютерной томографии грудной клетки для диагностики и принятия решения о лечении при подозрении на внебольничную пневмонию. Am J Respir Crit Care Med. 2015 15 октября; 192 (8): 974-82.
http://www.ncbi.nlm.nih.gov/pubmed/26168322?tool=bestpractice.ком
[28] ] Wunderink RG, Waterer G. Успехи в причинах и лечении внебольничной пневмонии у взрослых. BMJ. 10 июля 2017 г .; 358: j2471.
http://www.ncbi.nlm.nih.gov/pubmed/28694251?tool=bestpractice.com
Микробиология
Первоначальное лечение антибиотиками в большинстве случаев является эмпирическим.Определение микробной этиологии сокращает ненадлежащее использование антибиотиков широкого спектра действия и помогает обеспечить соответствующую антибактериальную терапию, что является важным фактором снижения смертности. Он также определяет устойчивые патогены и патогены, которые могут иметь последствия для общественного здравоохранения (например, Legionella ).
Посев мокроты и крови:
Получите предварительное окрашивание по Граму и посев секретов нижних дыхательных путей и посевы крови у следующих пациентов в условиях больницы: [17] Metlay JP, Waterer GW, Long AC, et al.Диагностика и лечение взрослых с внебольничной пневмонией. Официальное руководство по клинической практике Американского торакального общества и Американского общества инфекционных заболеваний. Am J Respir Crit Care Med. 1 октября 2019; 200 (7): e45-e67.
https://www.atsjournals.org/doi/full/10.1164/rccm.201908-1581SThttp://www.ncbi.nlm.nih.gov/pubmed/31573350?tool=bestpractice.com
Пациенты с тяжелой ВБП согласно критериям Американского торакального общества (ATS) / Американского общества инфекционных заболеваний (IDSA) для определения тяжелой ВП (см. Раздел «Диагностические критерии»), особенно если они интубированы. лечение от метициллин-резистентного Staphylococcus aureus (MRSA) или Pseudomonas aeruginosa
Пациенты, ранее инфицированные MRSA или P aeruginosa , особенно пациенты с предшествующей инфекцией дыхательных путей
- был госпитализирован и получал парентеральные антибиотики в течение последних 90 дней.
Эти тесты обычно не рекомендуются для других стационарных пациентов и не рекомендуются в амбулаторных условиях. Принимая во внимание местные протоколы контроля противомикробных препаратов, местные этиологические факторы и клиническую картину, принимайте решение о проведении этих тестов. [17] Metlay JP, Waterer GW, Long AC, et al. Диагностика и лечение взрослых с внебольничной пневмонией. Официальное руководство по клинической практике Американского торакального общества и Американского общества инфекционных заболеваний.Am J Respir Crit Care Med. 1 октября 2019; 200 (7): e45-e67.
https://www.atsjournals.org/doi/full/10.1164/rccm.201908-1581SThttp://www.ncbi.nlm.nih.gov/pubmed/31573350?tool=bestpractice.com
Окраска по Граму мокроты является чувствительной и высокоспецифичной для определения возбудителей болезни у пациентов с ВП. Мета-анализ показал, что этот тест является высокоспецифичным для выявления Streptococcus pneumoniae , Haemophilus influenzae , S aureus и грамотрицательных бацилл.Однако доля ложноотрицательных результатов колебалась от 22% (для H influenzae ) до 44% (для S pneumoniae ), что указывает на то, что отрицательный результат не является окончательным подтверждением отсутствия возбудителей, вызывающих заболевание, и следует проводить антибактериальную терапию. не обязательно прекращать на основании отрицательного результата окрашивания мокроты по Граму. [72] Del Rio-Pertuz G, Gutiérrez JF, Triana AJ, et al. Полезность окрашивания мокроты по грамму для этиологической диагностики внебольничной пневмонии: систематический обзор и метаанализ.BMC Infect Dis. 2019 10 мая; 19 (1): 403.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6509769http://www.ncbi.nlm.nih.gov/pubmed/31077143?tool=bestpractice.com
Пневмококковая инфекция и Legionella Анализ мочи на антиген:
Анализ мочи на пневмококковый антиген у пациентов с тяжелой ВП. Проведите анализ мочи на антиген Legionella у пациентов с эпидемиологическими факторами (например, связь со вспышкой легионеллы или недавнее путешествие) или пациентов с тяжелой ВП.Одновременно собирайте секреты нижних дыхательных путей для посева Legionella или амплификации нуклеиновых кислот у пациентов с тяжелой ВП. Тестирование мочи на антигены было связано со снижением смертности в крупных обсервационных исследованиях, и это важно учитывать, учитывая увеличение числа инфекций Legionella , особенно среди тяжелых пациентов. [17] Metlay JP, Waterer GW, Long AC, et al. . Диагностика и лечение взрослых с внебольничной пневмонией.Официальное руководство по клинической практике Американского торакального общества и Американского общества инфекционных заболеваний. Am J Respir Crit Care Med. 1 октября 2019; 200 (7): e45-e67.
https://www.atsjournals.org/doi/full/10.1164/rccm.201908-1581SThttp://www.ncbi.nlm.nih.gov/pubmed/31573350?tool=bestpractice.com
Тестирование на вирус гриппа:
Тест на вирус гриппа с использованием экспресс-молекулярного анализа гриппа (а не тестов обнаружения на основе антигенов), когда вирусы гриппа циркулируют в сообществе.Тестирование также может быть рассмотрено в периоды низкой активности гриппа. [17] Metlay JP, Waterer GW, Long AC, et al. Диагностика и лечение взрослых с внебольничной пневмонией. Официальное руководство по клинической практике Американского торакального общества и Американского общества инфекционных заболеваний. Am J Respir Crit Care Med. 1 октября 2019; 200 (7): e45-e67.
https://www.atsjournals.org/doi/full/10.1164/rccm.201908-1581SThttp://www.ncbi.nlm.nih.gov/pubmed/31573350?tool=bestpractice.ком
Лабораторные исследования
Заказать общий анализ крови, уровень глюкозы в крови, электролиты сыворотки, азот мочевины крови и функциональные пробы печени у госпитализированных пациентов. Повышенное количество лейкоцитов указывает на инфекцию. Хроническая болезнь почек и хроническая болезнь печени являются факторами риска смерти и осложнений у пациентов, госпитализированных с ВП.
Измерение газов артериальной крови у тяжелобольных или госпитализированных пациентов. Оксиметрия неинвазивна и может использоваться постоянно.
Рассмотрите возможность заказа таких биомаркеров, как C-реактивный белок (CRP) и прокальцитонин (PCT). Было обнаружено, что эти биомаркеры полезны для прогнозирования неадекватной реакции хозяина. Высокие уровни CRP или PCT при первичном обращении представляют собой фактор риска неадекватной реакции хозяина [73] Menéndez R, Cavalcanti M, Reyes S, et al. Маркеры неэффективности лечения госпитализированной внебольничной пневмонии. Грудная клетка. 2008 Май; 63 (5): 447-52.
http://thorax.bmj.com/content/63/5/447.long
http: // www.ncbi.nlm.nih.gov/pubmed/18245147?tool=bestpractice.com
тогда как низкие уровни являются защитными. У пациентов с подозрением на пневмонию уровень CRP> 10 мг / дл делает вероятной пневмонию [74] Woodhead M. Новые рекомендации по лечению инфекций нижних дыхательных путей у взрослых. Eur Respir J. 2011 декабрь; 38 (6): 1250-1.
http://erj.ersjournals.com/content/38/6/1250.long
http://www.ncbi.nlm.nih.gov/pubmed/22130759?tool=bestpractice.com
Повышенные значения ПКТ коррелируют с бактериальной пневмонией, тогда как более низкие значения коррелируют с вирусной и атипичной пневмонией.PCT особенно повышается при пневмококковой пневмонии. [75] Menéndez R, Sahuquillo-Arce JM, Reyes S, et al. На паттерны активации цитокинов и биомаркеры влияют микроорганизмы при внебольничной пневмонии. Грудь. 2012 июнь; 141 (6): 1537-45.
http://www.ncbi.nlm.nih.gov/pubmed/22194589?tool=bestpractice.com
[76] Угаджин М., Ямаки К., Хирасава Н. и др. Прогностическая ценность полуколичественного теста на прокальцитонин и общих биомаркеров для клинических исходов внебольничной пневмонии.Respir Care. 2014 Апрель; 59 (4): 564-73.
http://rc.rcjournal.com/content/59/4/564.full
http://www.ncbi.nlm.nih.gov/pubmed/24170911?tool=bestpractice.com
Первоначальную эмпирическую антибактериальную терапию следует начинать у пациентов с клинически подозреваемой и рентгенологически подтвержденной ВП независимо от исходного уровня ПКТ в сыворотке. [17] Metlay JP, Waterer GW, Long AC, et al. Диагностика и лечение взрослых с внебольничной пневмонией. Официальное руководство по клинической практике Американского торакального общества и Американского общества инфекционных заболеваний.Am J Respir Crit Care Med. 1 октября 2019; 200 (7): e45-e67.
https://www.atsjournals.org/doi/full/10.1164/rccm.201908-1581ST
http://www.ncbi.nlm.nih.gov/pubmed/31573350?tool=bestpractice.com
Рассмотрите возможность аспирации и посева плевральной жидкости у всех пациентов с плевральным выпотом. Парапневмонические выпоты — это экссудаты; положительная окраска плевральной жидкости по Граму указывает на эмпиему.
Бронхоскопия
Рассмотрите возможность проведения бронхоскопии у пациентов с ослабленным иммунитетом, у пациентов с тяжелой формой ВП и в случае неэффективности лечения.Наиболее распространенными методами отбора проб являются бронхоальвеолярный лаваж (БАЛ) и защищенная чистка образцов (PSB). Пороговое значение 10⁴ колониеобразующих единиц (КОЕ) / мл в образцах БАЛ указывает на инфекцию. Для PSB рекомендуется пороговое значение 10³ КОЕ / мл, чтобы отличить колонизацию от инфекции. [77] Sirvent JM, Vidaur L, Gonzalez S, et al. Микроскопическое исследование внутриклеточных организмов в защищенной бронхоальвеолярной жидкости мини-лаважа для диагностики вентилятор-ассоциированной пневмонии. Грудь. 2003 Февраль; 123 (2): 518-23.http://www.ncbi.nlm.nih.gov/pubmed/12576375?tool=bestpractice.com
Молекулярные методы
Обычные бактериальные культуры слишком медленны, чтобы немедленно стать терапевтически полезными. Тесты амплификации нуклеиновых кислот, такие как полимеразная цепная реакция, улучшили диагностическую точность при ВП. Молекулярные методы обеспечивают высокую чувствительность и специфичность в диагностике одиночных или полимикробных инфекций, а также могут помочь определить устойчивость к противомикробным препаратам (как это может происходить с Staphylococcus aureus , неферментирующими грамотрицательными палочками и Enterobacteriaceae), ассоциированными с тяжелой ВП.[78] Мердок ДР. Как недавние достижения в области молекулярных тестов могут повлиять на диагностику пневмонии. Эксперт Rev Mol Diagn. 2016; 16 (5): 533-40.
http://www.ncbi.nlm.nih.gov/pubmed/268
?tool=bestpractice.com
Венепункция и флеботомия: анимированная демонстрация
Диагностика пневмонии у пациентов с острым кашлем: клиническая оценка по сравнению с рентгенографией грудной клетки
Реферат
Пневмонию часто диагностируют и лечат эмпирически. Мы намеревались определить диагностическую точность клинического суждения на основе признаков и симптомов для выявления рентгенографической пневмонии у пациентов с острым кашлем в первичной медико-санитарной помощи.
У 2810 европейских пациентов с острым кашлем врачи общей практики (ВОП) записали, считали ли они наличие пневмонии («да» или «нет») сразу после анамнеза и физического осмотра. Рентгенография грудной клетки была выполнена в течение 1 недели местными радиологами, не имеющими отношения к другим характеристикам пациентов.
У
140 пациентов была рентгенологическая пневмония (5%), из которых у 41 (29%) была диагностирована такая пневмония. У 31 (1%) пациента был клинический диагноз, не подтвержденный рентгенографией (n = 2670).При клиническом подозрении на пневмонию у 57% пациентов впоследствии была диагностирована рентгенологическая пневмония. Отрицательная прогностическая ценность (NPV), чувствительность и специфичность клинической оценки терапевтов составляли 96%, 29% и 99% соответственно. По сравнению с пациентами с клиническим диагнозом пневмония, менее тяжелые симптомы были обнаружены в случаях рентгенологической пневмонии, не подозреваемых клинически (p <0,05).
Прогностическая ценность клинической оценки терапевтов, особенно высокие значения NPV, полезны при повседневном уходе.Тем не менее, большинство диагнозов рентгенологической пневмонии не было заподозрено на основании клинических данных. Существует необходимость в дальнейшей поддержке выявления клинически значимой пневмонии в учреждениях первичной медико-санитарной помощи.
Аннотация
Существует необходимость в дальнейшей поддержке выявления клинически значимой пневмонии в учреждениях первичной медико-санитарной помощи http://ow.ly/mxw6Z
Введение
Острый кашель и симптомы со стороны нижних дыхательных путей являются одними из наиболее частых причин обращения за первичной медицинской помощью.У большинства пациентов с этими симптомами в первичной медико-санитарной помощи диагностируется острый бронхит, у меньшинства — пневмония. Как правило, пневмония требует лечения антибиотиками под тщательным наблюдением, в то время как острый бронхит проходит само по себе и не приносит значимой пользы от лечения антибиотиками [1–3]. Врачи общей практики (ВОП) обычно должны диагностировать или исключать пневмонию только на основании анамнеза, симптомов и признаков, поскольку выполнение рентгенограммы грудной клетки у всех пациентов с острым кашлем или симптомами нижних дыхательных путей невозможно и нецелесообразно.Поэтому первоначальные решения о наиболее вероятном диагнозе, лечении и дополнительном обследовании чаще всего основываются на клинической оценке терапевтов.
Однако эффективность этого клинического заключения в значительной степени неизвестна. В нескольких исследованиях первичной медико-санитарной помощи оценивалась диагностическая ценность признаков и симптомов по отдельности или в комбинации для диагностики пневмонии [4, 5], но есть ограниченные данные о точности клинических суждений врачей общей практики, независимо от формальной диагностической модели в более низкой степени. инфекция дыхательных путей (ИДПТ).Macfarlane et al. [1] обнаружил, что врачи общей практики не могут с достаточной точностью определить необходимость лечения антибиотиками у пациентов с ИДП, у которых были микробиологические доказательства бактериальной инфекции. Melbye et al. [5] сравнил клинический диагноз пневмонии, поставленный врачами общей практики, с результатами рентгенограмм грудной клетки и обнаружил, что врачи общей практики поставили клинический диагноз пневмонии только у меньшинства пациентов, которым был поставлен рентгенологический диагноз пневмонии. Однако эти исследования ограничены небольшим количеством включенных в них случаев пневмонии.
Знания о выполнении эмпирической диагностики пневмонии в повседневной общей врачебной практике важны для разработки и внедрения диагностических инструментов, таких как формальные диагностические модели и тесты, проводимые рядом с пациентом. Поэтому мы намеревались оценить диагностическую точность чисто клинического диагноза пневмонии с рентгенографическим обнаружением пневмонии в качестве эталона для большой выборки пациентов с острым кашлем в системе первичной медико-санитарной помощи.
Методы
Дизайн и исследование населения
294 терапевта в 16 исследовательских сетях первичной медико-санитарной помощи в 12 европейских странах включили 3106 последовательных пациентов с острым кашлем в исследовании GRACE-09 («Геномика для борьбы с устойчивостью к антибиотикам у ИДП, приобретенных сообществом в Европе»; www.grace-lrti.org) в период с октября 2007 г. по апрель 2010 г. Набранные сети имели доступ как минимум к 20 000 пациентов и имели опыт проведения исследований. Координатор национальной сети и координатор национальной сети взяли на себя ответственность за создание своей сети, набор персонала и управление данными. Подходящие для исследования пациенты были ≥18 лет, с острым или обостренным кашлем (продолжительность ≤28 дней) в качестве основного симптома или с любой клинической картиной, которую терапевт считал вызванной ИДП, и которые консультировались впервые по поводу этого эпизода заболевания.Критериями исключения были беременность, кормление грудью и любое серьезное состояние, связанное с нарушением иммунитета. Все участники дали письменное информированное согласие, и комитеты по медицинской этике участвующих центров одобрили исследование.
Оценка терапевта и рентгенологические заключения
врачей общей практики регистрировали симптомы, признаки, сопутствующие заболевания пациентов (диабет, респираторные и сердечно-сосудистые заболевания), прием лекарств и, непосредственно после этого, его или ее предполагаемый диагноз (открытый вопрос) при обращении.Все пациенты прошли рентгенографию грудной клетки в местных службах в течение 1 недели. Рентгенограммы оценивались местными радиологами, которые не обращали внимания на текущую клиническую информацию пациентов, но знали критерии включения в исследования и имели свободный доступ к предыдущим рентгенограммам, если таковые были. Радиологи поставили рентгенологический диагноз, выбрав один из следующих фиксированных вариантов ответа: «нормальный рентген», «острый бронхит», «крупозная или бронхопневмония» или «другое». Был вариант с произвольным текстом, чтобы указать «другое».Радиологам было разрешено проинформировать ответственных терапевтов, если они обнаружат консолидацию или поставят какой-либо диагноз, требующий дальнейшего исследования. Во всех остальных случаях врачи получали результаты после завершения исследования.
Подмножество из 1544 рентгенограмм грудной клетки, которые были доступны для повторной оценки, были повторно оценены независимым радиологом (П.А. де Йонг) в Университетском медицинском центре Утрехта (Утрехт, Нидерланды), и была определена вариабельность между наблюдателями [6–8].
Анализ данных
Отсутствовали клинические характеристики пациентов <1%.Отсутствующие данные редко возникают полностью случайно, поэтому вменение с использованием методов множественной регрессии применялось в соответствии с рекомендациями многих методистов [9, 10].
Эмпирические диагнозы
врачей общей практики были разделены на: «пневмония», «обострение хронической обструктивной болезни легких (ХОБЛ) / астма», «инфекция верхних дыхательных путей (ИВДП)», «ИНДП» (неуточненная или вирусная причина), «острый кашель. »Или« другое », и были рассчитаны доли этих диагнозов в каждой стране.
Впоследствии мы разделили диагнозы врачей общей практики на «пневмонию» или «отсутствие пневмонии» и рассчитали чувствительность, специфичность, положительную прогностическую ценность (PPV), отрицательную прогностическую ценность (NPV) и отношения правдоподобия (LR) клинической оценки наличия или отсутствия пневмонии.
Поскольку рентгенографическая пневмония в некоторых сетях диагностировалась реже, чем ожидалось, на основании предыдущих исследований распространенности [1, 11], мы повторили анализ, исключив все страны с распространенностью пневмонии <3% (Польша, Франция и Италия).
Мы сравнили пациентов с рентгенологической пневмонией, у которых была диагностирована пневмония на клинических основаниях, с пациентами с рентгенологической пневмонией, но которые не получили этот диагноз на эмпирических основаниях с точки зрения симптомов, признаков и баллов по степени тяжести пациентов.
Данные были проанализированы с помощью SPSS (версия 17.0; SPSS Inc., Чикаго, Иллинойс, США).
Результаты
Характеристики пациента
Из 3106 подходящих пациентов с острым кашлем 296 были исключены из-за того, что рентгенография грудной клетки не проводилась (n = 258) или была недостаточно качественной (n = 28), а 10 из-за отсутствия результатов клинической оценки терапевтов (рис. 1). Средний возраст оставшихся 2810 пациентов составлял 50 лет, 40% составляли мужчины и 28% курили в настоящее время (таблица 1).У 140 (5%) пациентов была рентгенологическая пневмония. Наблюдаемое пропорциональное согласие между исходным и вторым рентгенологическим диагнозом составило 1445 (94%) у 1544 пациентов. Каппа составляла 0,45 (95% ДИ 0,36–0,54: умеренное согласие). Наблюдаемое положительное согласие (48%) было намного ниже, чем отрицательное согласие (97%). Характеристики пациентов существенно не различались между проанализированными пациентами и исключенными пациентами (из-за отсутствия результатов рентгенографии или клинической оценки), за исключением возраста. Исключенные пациенты были моложе (средний возраст 44 года) (результаты не показаны).
Рисунок 1-
Блок-схема исследования и участников. GP: терапевт.
Таблица 1-
Характеристики пациентов, включая симптомы и признаки, у 2810 пациентов с острым кашлем в первичной медико-санитарной помощи
диагнозов врачей общей практики
У 72 (3%) пациентов была диагностирована пневмония врачами общей практики. Доля диагностированных обострений ХОБЛ / астмы составляла 4%, ИВДП — 16%, острого бронхита — 73%, из которых 61% «не указано иначе» и 12% указаны как вирусные причины.У 4% пациентов был диагностирован симптом, а не расстройство («острый кашель»), а у трех пациентов — «другие диагнозы» (головная боль, сердечная недостаточность или коклюш). Доля наиболее распространенных диагнозов различалась между 12 европейскими странами (таблица 2). 91% пациентов прошли рентгенографию грудной клетки в течение 5 дней, а средняя длительность ± стандартное отклонение между первой консультацией по поводу острого кашля и рентгенографией грудной клетки составила 1,6 ± 2,6 дня.
Таблица 2-
Врачи общей практики поставили диагнозы 2810 пациентам с острым кашлем в разбивке по странам
Клиническое заключение врачей общей практики о пневмонии
Заключение врачей общей практики о наличии или отсутствии пневмонии совпало с рентгенологическим диагнозом у 2680 (95%) пациентов (таблица 3).Из всех пациентов, у которых была диагностирована рентгенологическая пневмония, 29% были диагностированы врачами общей практики после анамнеза и физического обследования (чувствительность). Специфичность, PPV и NPV составляли 99%, 57% и 96% соответственно. Положительные и отрицательные значения LR для клинической оценки терапевтов составили 24 и 0,72 соответственно. Согласие между клиническими и рентгенологическими диагнозами после исключения сетей, базирующихся в Польше, Франции и Италии, также показано в таблице 3, и это привело к чувствительности, специфичности, PPV и NPV 30%, 99%, 59% и 96%. соответственно.
Таблица 3–
Клиническая оценка врачей общей практики о пневмонии по сравнению с рентгенографией грудной клетки
Клиническое значение клинически неустановленной рентгенологической пневмонии
Пациенты, которым не был поставлен клинический диагноз пневмонии, но у которых была рентгенографическая пневмония (n = 99), имели более низкие оценки тяжести симптомов по самооценке и менее тяжелые индивидуальные симптомы, такие как лихорадка, хрипы и признаки синдрома системной воспалительной реакции, когда по сравнению с пациентами, у которых был как эмпирический клинический диагноз, так и рентгенологический диагноз пневмонии (n = 41) (таблица 4).
Таблица 4–
Характеристики клинически идентифицированных и нераспознанных рентгенологических пневмоний
Обсуждение
Основные выводы
У пациентов с острым кашлем в отделениях первичной медико-санитарной помощи врачи общей практики диагностировали пневмонию только на основании клинических данных у 29% всех пациентов, у которых впоследствии была обнаружена рентгенологическая пневмония (положительный LR 24). У пациентов без рентгенологической пневмонии (n = 2670) врачи общей практики диагностировали пневмонию только у 31 (1%) пациента на основании клинических данных. NPV оценки врачей общей практики составила 96%.
Сильные стороны и ограничения
Насколько нам известно, это первое исследование, посвященное диагностической оценке пневмонии при остром кашле с адекватным числом случаев пневмонии. Сильные стороны нашего исследования включают запись клинического суждения в условиях, аналогичных условиям обычного лечения, сразу после сбора анамнеза и проведения физического обследования, а также всех пациентов, проходящих аналогичный эталонный тест на пневмонию, независимо от клинического заключения терапевтов. Ограничением относительно эталонного стандарта является то, что все рентгенограммы грудной клетки были исследованы местными радиологами в европейских центрах.Мы попытались повысить единообразие оценки, используя протокол отчетности. Вариабельность между наблюдателями оставалась, но умеренная невзвешенная каппа 0,45 была аналогична другим исследованиям [6, 8]. Более того, повторный анализ с рентгенографической пневмонией в качестве эталонного теста, диагностированный вторым специалистом по оценке, показал сопоставимые результаты (чувствительность, специфичность, PPV и NPV 20%, 98%, 42% и 94% соответственно).
Второе возможное ограничение нашего исследования касается того факта, что, учитывая распространенность ИДП, в период набора было бы проконсультировано гораздо больше подходящих пациентов, чем было набрано.Следовательно, мы, вероятно, не достигли цели набора последовательных подходящих пациентов (, например, . сети, базирующиеся во Франции, Словакии и Словении, не включали пациентов с клиническим диагнозом пневмонии). Тем не менее, мы полагаем, что результаты исследования имеют низкий риск систематической ошибки отбора, поскольку отзывы от набора врачей во время и после исследования показали, что время, необходимое для набора и оценки каждого пациента, сделало невозможным последовательный набор каждого подходящего пациента.В недавнем обсервационном исследовании [12], проведенном в той же сети набора первичной медико-санитарной помощи, использовалось то же определение случая и очень похожая форма записи исходного случая, но его было намного проще реализовать, и в это исследование были включены пациенты с характеристиками, аналогичными текущему исследованию (, например, ). y возраст 45 лет, 37% мужчин и 26% сопутствующих заболеваний легких, сердечных заболеваний или сахарного диабета).
Сравнение с другими исследованиями
В нескольких предыдущих исследованиях первичной медико-санитарной помощи оценивалась диагностическая ценность сбора анамнеза и физикального обследования для выявления пневмонии [4, 5].В ходе валидационного исследования моделей клинического прогнозирования у пациентов первичной медико-санитарной помощи было обнаружено, что PPV находится в диапазоне от 17 до 47%, а NPV — от 79% до 88% [11], но не включает клиническую оценку терапевтов. В двух предыдущих исследованиях оценивали эмпирические клинические суждения врачей общей практики о пациентах первичной медико-санитарной помощи с ИДП. Macfarlane et al. [1] оценил клиническое заключение врачей общей практики в отношении 318 взрослых с ИНДП и не обнаружил взаимосвязи между их клинической оценкой и микробиологическими данными о бактериальных и / или атипичных патогенных микроорганизмах].Melbye et al. [5] изучили 402 взрослых с ИНДП, из которых 20 имели пневмонию при рентгенографии грудной клетки, и обнаружили, что врачи общей практики выявили семь из 20 случаев рентгенологической пневмонии на клинических основаниях. Они также диагностировали пневмонию у 22 пациентов без рентгенологической пневмонии. Наши результаты подтверждают, что врачи общей практики делают клиническую оценку пневмонии у меньшинства пациентов, у которых впоследствии обнаруживается пневмония при рентгенографии грудной клетки.
Значение результатов
Было показано, что многие клиницисты оправдывают свое использование антибиотиков широкого спектра действия тем, что не хотят пропустить случай пневмонии [13].Поэтому полезно, что мы обнаружили, что NPV клинической оценки достигает 96%. Это может помочь терапевтам полагаться на свою способность исключить пневмонию и отказаться от лечения антибиотиками у значительной части своих пациентов [12].
Тем не менее, большая часть рентгенологических пневмоний, не диагностированных только на основании клинических данных, может вызывать беспокойство. Однако в случаях рентгенологической пневмонии, которые в нашем исследовании не были выявлены клинически, симптомы тяжелого заболевания (, например, , лихорадка и боль в груди) реже при обращении (таблица 4).Ранее было показано, что более легкие случаи пневмонии, не заподозренные клинически, могут иметь относительно более доброкачественное течение [14]. Более того, мы предполагаем, что серьезные негативные последствия для здоровья «пропущенной» пневмонии у амбулаторных пациентов могут быть ограничены путем инструктирования пациентов о повторном посещении, если симптомы сохраняются или ухудшаются. Будет сложно улучшить оценку NPV врачей общей практики до 96%. Однако два небольших исследования показали, что добавление уровня С-реактивного белка к признакам и симптомам может привести к ЧПС на 97% [4, 15]. Необходимы дальнейшие исследования диагностической ценности тестов на С-реактивный белок в медицинских учреждениях первичной медико-санитарной помощи в более крупных когортах.
Выводы
Хотя прогностическая ценность клинической оценки терапевтов полезна в повседневном ведении пациентов, и особенно NPV клинической оценки высока, большинство рентгенографических пневмоний не распознавались только на основании клинических данных. Существует необходимость в дальнейшей поддержке выявления клинически значимой пневмонии в учреждениях первичной медико-санитарной помощи.
Благодарности
Мы хотели бы поблагодарить всю команду GRACE за их усердие, опыт и энтузиазм.Наконец, мы в долгу перед всеми пациентами, которые согласились участвовать в GRACE, без которых это исследование было бы невозможно.
Сноски
Получите аккредитацию CME, отвечая на вопросы по этой статье. Вы найдете их на обратной стороне печатной копии этого выпуска или на сайте www.erj.ersjournals.com/misc/cmeinfo.xhtml
Заявление о поддержке: Эта работа была поддержана 6-й рамочной программой Европейской комиссии (LSHM-CT-2005-518226) и во Фландрии, Бельгия, эта работа была поддержана Исследовательским фондом (G · 0274 · 08N).
Конфликт интересов: раскрытие информации можно найти вместе с онлайн-версией этой статьи на сайте www.erj.ersjournals.com
- Получено 18 июля 2012 г.
- Принято 3 декабря 2012 г.
Лаборатория диагностика пневмонии в молекулярном возрасте
Abstract
Пневмония остается мировой проблемой здравоохранения с высоким уровнем заболеваемости и смертности. Идентификация микробных патогенов, вызывающих пневмонию, является важной областью для оптимального клинического ведения пациентов с пневмонией и представляет собой большую проблему для традиционных микробиологических методов.Разработка и внедрение молекулярных диагностических тестов на пневмонию в последние годы явились крупным достижением в микробиологической диагностике респираторных патогенов. Однако с новыми знаниями о микробиоме, а также с признанием того, что легкие представляют собой динамическую микробиологическую экосистему, наша нынешняя концепция пневмонии не совсем реалистична, поскольку эта новая концепция пневмонии включает дисбиоз или изменение микробиома легких. Таким образом, возникла новая проблема для микробиологов и клиницистов.Многое предстоит узнать в отношении информации, предоставляемой этой новой диагностической технологией, которая приведет к сокращению времени до антибиотикотерапии, целевому выбору антибиотиков и более эффективной деэскалации и улучшению управления пациентами с пневмонией. В статье представлен обзор современных методов лабораторной диагностики пневмонии в молекулярном возрасте.
Реферат
Интеграция новых диагностических средств для быстрой идентификации микробов повлияет на лабораторную диагностику пневмонии http: // ow.ly / 2aJh404NuCn
Введение
В 1930 году пневмония была третьей по частоте причиной смерти в США [1]. Сейчас, почти столетие спустя, несмотря на появление антибиотиков в 1950-х годах, пневмония и другие респираторные инфекции остаются четвертой по частоте причиной смерти во всем мире [2]. Хотя реализация программ вакцинации во всем мире снизила заболеваемость пневмонией, особенно среди групп риска [3, 4], пневмония по-прежнему представляет собой серьезное бремя с точки зрения заболеваемости, смертности и затрат на здоровье, а также количества рабочих дней. проиграл [5–8].
Микробиологическая диагностика пневмонии имеет основополагающее значение для обеспечения надлежащей антибактериальной терапии, которая связана со снижением смертности [9]. Однако этиологический диагноз устанавливается только у половины пациентов, и начальный режим антибиотикотерапии следует выбирать эмпирически, чтобы избежать задержки с назначением соответствующей терапии, связанной со значительной летальностью [10, 11].
Руководящие принципы Американского общества инфекционистов / Американского торакального общества (IDSA / ATS) по внебольничной пневмонии (ВП) рекомендуют дополнительный микробиологический диагностический тест в легких и легких случаях пневмонии, который следует выбирать по клиническим показаниям [ 12].Однако рутинная микробиология должна выполняться в случае патогенов, которые могут значительно повлиять на эмпирические решения, таких как вирус гриппа, Mycobacterium tuberculosis , Pseudomonas aeruginosa и особенно устойчивый к метициллину Staphylococcus aureus (текущий MRSA), Рекомендации по лечению тяжелой ВП — эмпирическая терапия β-лактамом с макролидом или фторхинолоном, которые могут не обеспечить адекватной защиты от MRSA [12].Посев мокроты рекомендуется только пациентам, достаточно больным, чтобы им требовалась госпитализация в отделение интенсивной терапии (ОИТ). Это означает, что в зависимости от эпидемиологии микробной этиологии эмпирические методы лечения выбираются и назначаются пациентам как можно скорее после сбора образца культуры.
В настоящее время большинство пациентов с ВП можно лечить в соответствии с рекомендациями. Использование баллов может помочь выявить пациентов с потенциальным риском патогенов с множественной лекарственной устойчивостью или пациентов, которым требуется нестандартное лечение.[13–15] У этих пациентов молекулярная информация, в дополнение к обычным методам, может быть очень полезной. Текущая клиническая практика имеет три основных последствия. 1) Адекватность исходного антибиотика является ключевым фактором прогноза. Известно, что смертность увеличивается с каждым часом отсрочки начала правильной терапии пневмонии [16–19]. 2) Многие пациенты получают терапию антибиотиками широкого спектра действия до тех пор, пока не станут доступны посевы, и деэскалация не может быть выполнена быстро; Таким образом, более вероятно неправильное использование антибиотиков [20, 21].3) Появление устойчивых к антибиотикам патогенов связано с давлением отбора из-за чрезмерного использования антибиотиков во всем мире [22, 23].
Устойчивость к противомикробным препаратам грамположительных кокков и грамотрицательных бацилл является серьезной проблемой во всем мире [18, 23, 24]. В главе Доклада о состоянии антибиотиков в мире за 2015 год [25], посвященной использованию антибиотиков человеком, сообщается, что потребление антибиотиков продолжает расти (сравнительные данные за 2000–2010 годы) и что лечение антибиотиками нецелесообразно в 20–50% случаев.Данные о потреблении на душу населения по классам и странам выявляют значительные различия между географическими местоположениями, и это подчеркивает, насколько разные страны могут реагировать на проблему [25]. Общественные кампании, поощряющие реализацию конкретных мер, оказались успешными [26, 27]. Большинство кампаний такого рода включают призывы и предупреждения о необходимости более качественного и более быстрого диагностического тестирования, чтобы сократить введение антибиотиков и увеличить использование терапии, направленной на микробов. Проблема микробной устойчивости настолько серьезна, что в прошлом году президент Обама обратил внимание на угрозу, которую она представляет, и призвал к увеличению финансирования исследований [28].Однако открытие новых классов антибиотиков более или менее приостановлено, поскольку дорогостоящий и неэффективный процесс является проблемой для фармацевтических компаний, которые отказались от своих инвестиций в разработку новых противомикробных препаратов. Создание стимулов к антибиотикам сейчас (GAIN) — это новое постановление Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA), направленное на обеспечение экономических стимулов для открытия лекарств-антибиотиков путем предложения эксклюзивности на рынке и ускорения процессов утверждения лекарств. Постановление расширяет эксклюзивность, с которой антибиотики, которые лечат серьезные или опасные для жизни заболевания, могут продаваться без конкуренции с дженериками, на 5 лет.Он также предоставляет дополнительные 6 месяцев эксклюзивности фармацевтической или биотехнологической компании, которая определяет сопутствующий диагностический тест. Кроме того, FDA дает возможность ускорить утверждение нового противомикробного препарата [29].
Быстрые молекулярные методы (рис. 1 и таблица 1) обещают стать эффективным инструментом, который поможет направить соответствующую терапию и избавиться от антибиотиков широкого спектра действия. Однако, как и любые новые медицинские технологии, они нуждаются в апробации в клинической практике.
РИСУНОК 1
График разработки диагностических тестов и появления резистентных патогенов. MRSA: метициллин-устойчивый Staphylococcus aureus ; CA-MRSA: внебольничный метициллин-устойчивый Staphylococcus aureus ; МЛУ: множественная лекарственная устойчивость: PDR: общая лекарственная устойчивость; ШЛУ: широкая лекарственная устойчивость.
ТАБЛИЦА 1
Экспресс-микробиологические тесты для диагностики пневмонии
В этой статье мы оцениваем самую последнюю информацию о немолекулярных и молекулярных методах обнаружения респираторных патогенов, таких как бактерии и вирусы.Выводы этого обзора заключаются в том, что для большинства патогенов, вызывающих пневмонию, существует возможность использования быстрых методов, которые могут помочь клиницистам использовать более целенаправленное лечение антибиотиками и противовирусными препаратами. Тестирование на месте будет лучшим способом внедрения этих методов в клиническую практику. Однако перед внедрением этих методов необходимо провести хорошо спланированные исследования для определения их экономической эффективности.
Диагностика инфекций нижних дыхательных путей, вызванных обычными бактериями
Обычная микробиологическая диагностика
У пациентов с ВП микробиологическое исследование должно включать как минимум посев мокроты, анализ мочи на антиген на Streptococcus pneumoniae и Legionella pneumophila , и посев крови [12].Может быть проведено дополнительное серологическое исследование на атипичные бактериальные патогены [12]. В исследованиях, включающих интенсивное микробиологическое исследование пациентов с ВП, этиология была выявлена в 53–75% выборки [30–32]. Наиболее частыми патогенами, идентифицированными в этих исследованиях, были S. pneumoniae , Mycoplasma pneumoniae и Haemophilus influenzae .
Посев крови, проведенный перед назначением антибактериальной терапии, имеет очень высокую специфичность, но дает положительный результат менее чем в 20% случаев [12, 33].Посевы крови пациентов с тяжелой ВП имеют более высокий результат, поскольку такие патогены, как S. aureus и грамотрицательные палочки, часто выделяются и на них не влияет эмпирическая терапия [12].
Плевральный выпот присутствует примерно в 40% случаев ВП [34]. Специфичность посева плеврального экссудата очень высока, хотя чувствительность низкая из-за низкой частоты инвазии плевры [34]. Чувствительность окраски по Граму составляет примерно 80% в случае пневмококковой пневмонии [35] и 78% для стафилококковой пневмонии со специфичностью 93–96% [36].
Обнаружение
S. pneumoniae с помощью ПЦР
ПЦР — это метод молекулярной диагностики, основанный на обнаружении ДНК, который дает преимущество в виде получения результатов в течение нескольких часов. Кроме того, поскольку для ПЦР не требуются жизнеспособные бактерии, на нее меньше влияет антимикробная терапия. В исследовании Johansson et al. [37], из 184 последовательно госпитализированных пациентов с диагнозом ВП, 80% случаев с положительным результатом ПЦР-теста и отрицательным посевом мокроты лечились антибиотиками перед забором мокроты.В другом исследовании влияния лечения антибиотиками на точность диагностики инвазивного пневмококкового заболевания с использованием культуральных или молекулярных методов этиологический диагноз был установлен с использованием молекулярных методов после 4 дней или более лечения антибиотиками и только в первые 2 дня лечения с использованием общепринятые методы диагностики [38].
Обнаружение S. pneumoniae на основе ПЦР зависит от амплификации генов, специфичных для пневмококка. Специфическими характеристиками для этого вида являются выработка токсинов, таких как пневмолизин ( Ply ), а также присутствие поверхностных антигенов, таких как пневмококковый поверхностный адгезин A ( PsaA ) и пневмококковый аутолизин A ( LytA ) [39] .Однако исследования ПЦР, направленных на ген ply , показали недостаточную чувствительность и специфичность в отношении пневмококковой инфекции [40]. Также было показано, что ген ply присутствует у некоторых видов флоры ротовой полости Streptococcal , таких как Streptococcus mitis и Streptococcus oralis [41]. Чтобы исследовать, могут ли гены-мишени, отличные от гена ply , быть более специфичными, Carvalho et al. [41] сравнил две другие мишени: ген lytA и ген psaA .Они показали, что ПЦР, предназначенная для нацеливания на ген lytA , была на 100% специфичной, в то время как для гена psaA была специфична 98%. Другое исследование подтвердило высокую специфичность гена lytA , при котором не было обнаружено положительных результатов у здоровых контрольных субъектов [52]. Диагностика пневмококка с помощью тестов ПЦР может быть применена к респираторным образцам, мазкам из носоглотки и крови.
Мокрота: ПЦР
по сравнению с культурой
В нескольких исследованиях изучалась способность ПЦР обнаруживать S.pneumoniae в мокроте [37, 53–55]. В двух скандинавских исследованиях была собрана мокрота для проведения ПЦР и посева. В первом исследовании у 128 и 127 пациентов с ВП был проанализирован по крайней мере один образец мокроты с помощью посева и ПЦР в реальном времени соответственно; ПЦР нацелена на ген пневмолизина ( ply ) из S. pneumoniae [37]. ПЦР мокроты дала положительный результат у 34 пациентов (27%), а посев мокроты — у 19 пациентов (15%) (p <0,001). Шестнадцать из 19 пациентов с положительной культурой (84%) также имели положительные результаты с ПЦР в реальном времени, а 17 из 34 пациентов с положительной ПЦР в реальном времени (50%) имели отрицательные результаты посева.Четырнадцать из этих 17 пациентов (82%) получали антибиотики перед забором мокроты. Во втором исследовании посев мокроты был проведен у 112 пациентов, а ПЦР - у 103 пациентов: 36 пациентов (32%) имели положительные культуры и 55 пациентов (53%) имели положительные результаты ПЦР [56]. Эти исследования показывают, что ПЦР мокроты является более чувствительным методом, чем посев мокроты, для обнаружения S. pneumoniae у пациентов, госпитализированных с ВП, особенно у тех, кто ранее лечился антибиотиками.
Кровь / плазма: ПЦР
против культуры
Культуры крови имеют низкую чувствительность для обнаружения S.pneumoniae инфекций [30]; Бактериемия присутствует примерно в 20% случаев ВП, когда используются обычные культуры крови [33]. ПЦР может повысить эту чувствительность. Одно исследование, в котором оценивалась роль ПЦР в цельной крови при нацеливании на ген ply , показало положительный результат у 22 из 40 пациентов (55%) с пневмококковой пневмонией, в то время как посев крови имел чувствительность 28% (11 из 40 пациентов). ПЦР дала отрицательный результат у всех 30 пациентов с непневмококковой пневмонией, что дало 100% специфичность [57].Два исследования на взрослых пациентах определили чувствительность положительных результатов ПЦР по сравнению с положительными культурами крови в качестве золотого стандарта. В первом исследовании у 10 пациентов с ВП была пневмококковая бактериемия, ПЦР для lytA имела чувствительность 70% (семь из 10) [58]. Второе исследование показало положительный результат ПЦР lytA у 10 из 13 пациентов (77%) с бактериемией S. pneumoniae [59]. Кроме того, в обзоре, оценивающем ценность ПЦР для диагностики пневмококковой бактериемии, чувствительность составила 57.Сообщалось об 1% (95% ДИ 45,7–67,8%). Специфичность ПЦР 98,6% (95% ДИ 96,4–99,5%) была определена в популяции «пациентов без болезней», определяемых как здоровые люди или пациенты с бактериемией, вызванной другими бактериями [60].
Другие исследования ПЦР, нацеленные на ген lytA , показали лучшие результаты при ПЦР, чем при посеве крови. В проспективном исследовании, в котором участвовали дети младше 15 лет и взрослые с ВП, при ПЦР было выявлено значительно больше случаев определенной пневмококковой пневмонии, чем при посеве крови (27.1% против 5,0%; р <0,005). ПЦР в плазме был отрицательным в контрольной группе из 50 взрослых [52]. В другом исследовании с участием детей в возрасте 0–16 лет инвазивная пневмококковая инфекция была диагностирована у 47 из 292 пациентов (16%). Из этих пациентов 45 (15,4%) дали положительный результат с помощью ПЦР и 11 (3,8%) дали положительный результат с помощью посева. Таким образом, ПЦР была значительно более чувствительной, чем культура, в выявлении бактериемической пневмонии (OR 30,6, 95% ДИ 5,8–97,5; p <0,001) [61]. Результаты этих двух исследований показали, что молекулярные методы обладают более высокой чувствительностью, чем посев крови у пациентов с бактериемией.Одним из объяснений может быть то, что ПЦР также может обнаруживать ДНК нежизнеспособных бактерий. В последнем случае на чувствительность посевов крови может влиять тот факт, что лечение антибиотиками было начато до сбора посевов. В одном исследовании у пациентов с ВП, получавших лечение антибиотиками перед госпитализацией, чувствительность ПЦР была в 7,0 раз выше, чем у культуральных (p = 0,043) [38].
После получения положительного результата ПЦР в респираторных образцах важно определить, отражает ли этот результат бактериальную колонизацию или инфекцию.Недавно количественные ПЦР-анализы были выполнены в различных клинических образцах (цельная кровь, мокрота и образцы из носоглотки), которые могут различать колонизацию и инфекцию. В этих исследованиях пороговое значение от 10 4 до 10 5 колониеобразующих единиц на мл пневмококковой ДНК было описано у пациентов, не инфицированных ВИЧ [58, 62, 63]. Кроме того, есть некоторые свидетельства того, что количественный подход также может использоваться для прогнозирования проявления и тяжести заболевания, которые могут коррелировать с уровнями ДНК пневмококков в клинических образцах ПЦР.В проспективном исследовании 353 пациентов с диагнозом ВП Rello et al. [64] показали, что среднее число копий на мл S. pneumoniae ДНК в образцах цельной крови было значительно выше у пациентов, у которых развился септический шок. В двух других исследованиях более высокая нагрузка ДНК S. pneumoniae в образцах крови также была связана с наличием более тяжелого заболевания [59, 65]. Еще одно полезное применение ПЦР заключается в том, что этот диагностический метод можно использовать для серотипирования пневмококков в случаях бактериемии [61, 66].Это важно для идентификации серотипов, которые могут быть причиной тяжелых случаев ВП. Эти новые тесты также могут быть полезны для определения циркулирующих серотипов пневмококка, чтобы оценить эффект вакцинации против пневмококка.
Кроме того, ПЦР может распознавать гены, индуцирующие устойчивость к антибиотикам [67]. Однако в настоящее время традиционные культуры остаются золотым стандартом для определения устойчивости к антибиотикам.
Диагностика вирусной и атипичной пневмонии
Вирусные и атипичные патогены являются частыми причинами пневмонии во всем мире, составляя 10–22% и 11–28% всех случаев ВП, соответственно [68–72].В недавнем исследовании Jain et al. [68] проанализировав 2320 случаев пневмонии, в которых применялась интенсивная микробиологическая диагностика, в частности вирусные молекулярные методы, микробная этиология была выявлена в 853 (38%) случаях. Тремя основными обнаруженными возбудителями были респираторные вирусы (23%), бактериальная этиология (11%) и сопутствующие инфекции (3%). Это исследование имело особенно важное значение для рассмотрения двух вопросов в контексте. 1) Выделение вирусов при ВП происходит гораздо чаще, чем считалось ранее, благодаря молекулярным методам; и 2) Хотя молекулярные методы лучше, чем микробиологические культуры, эти методы не идеальны с точки зрения эксплуатационных качеств.
Диагностика обычно включает тесты на антигены, культуральные, серологические и молекулярные анализы, каждый из которых имеет свои преимущества и ограничения (таблица 2), такие как: тип образца, место и время сбора в отношении начала заболевания, а также вероятность предварительного тестирования. (, например, сезонных пиков), которые могут существенно повлиять на производительность теста [73–75]. Тестирование обычно рекомендуется госпитализированным пациентам, поскольку доступны специфические противомикробные препараты (, например, ингибиторов нейраминидазы для гриппа или макролиды, фторхинолоны или доксициклин для атипичных патогенов), а диагностика может способствовать эффективному применению мер предосторожности при изоляции [70, 73, 74, 76 , 77].
ТАБЛИЦА 2
Лабораторная диагностика Streptococcus pneumoniae , атипичных патогенов и респираторных вирусов в клинических условиях
Грипп (сезонный, пандемический, птичий) является наиболее важной причиной вирусной пневмонии, приводящей к высокой заболеваемости и смертности; однако клинический диагноз недостоверен [73, 74]. Быстрые диагностические тесты на грипп (RIDT, иммуноанализы на антигены) удобны, коммерчески доступны и высокоспецифичны (90–95%). Главный недостаток — их низкая чувствительность (40–70%), что означает, что отрицательный результат не может исключить заражение гриппом [74, 78–80].Эффективность тестов действительно улучшается, если их применять в течение 48–72 часов с момента начала заболевания, до того, как произойдет значительное снижение вирусной нагрузки [74, 75]. Аналогичные соображения применимы и к иммунофлуоресцентным анализам антигенов, хотя они, как правило, более чувствительны (50–85%), могут использоваться в образцах из верхних и нижних дыхательных путей (, например, трахеальный аспират , бронхоальвеолярный лаваж) и могут обнаруживать ряд респираторных вирусов (). например, респираторно-синцитиальный вирус (RSV), вирус парагриппа), если он включен в панель.Важны лабораторные знания и доступность качественных образцов с большим количеством эпителиальных клеток для окрашивания [73, 74]. Как правило, серология и посев не могут помочь в лечении пациентов из-за их ретроспективных или медленных результатов, но они полезны для надзора и исследовательских целей (, например, для идентификации штаммов и тестирования фенотипической устойчивости) [74, 81, 82].
Там, где это возможно, ПЦР в настоящее время считается предпочтительным тестом из-за ее высокой чувствительности и специфичности, большего временного окна для обнаружения и короткого времени выполнения [73, 74, 80].Он может обнаруживать все подтипы гриппа A с помощью универсальных праймеров (нацеленные на M-ген, как для гриппа B) или отдельные подтипы с использованием конкретных праймеров (, например, h2, h4, H5, H7) [83]. Эта информация может иметь значение для лечения ( например, препандемический h2N1 устойчив к осельтамивиру) и может идентифицировать возможные новые или птичьи штаммы (, например, h2N1pdm09 и H7N9 изначально «нетипируемы» при использовании существующих праймеров) [78, 81, 83 , 84].
Даже при использовании ПЦР могут быть получены отрицательные результаты с образцами из носоглотки в случае гриппозной пневмонии из-за дифференциальных вирусных кинетических изменений в дыхательных путях.Поэтому следует рассмотреть возможность дополнительного тестирования с образцом из нижних дыхательных путей (в котором вирусная нагрузка обычно выше) [75, 78, 84, 85].
Примечательно, что ПЦР не дает информации об инфекционности, и мертвые фрагменты вирусной РНК могут быть обнаружены, хотя и на низком уровне, даже после клинического разрешения [83]. Полуколичественные анализы в реальном времени могут быть полезны для мониторинга вирусологического ответа (пороговые значения цикла использовались в качестве альтернативных оценок) [75, 82, 85]. Быстрое прямое определение генотипической устойчивости также возможно с помощью ПЦР для известных мутаций ( e.грамм. h375Y в h2N1pdm09) [81–83].
Поскольку проявления гриппа неотличимы от других респираторных патогенов, множественные платформы ПЦР, которые выявляют ряд распространенных вирусов (, например, гриппа, RSV, метапневмовирус человека, вирус парагриппа, риновирус) и атипичные патогены (, например M. pneumoniae , Chlamydophila pneumoniae ) все чаще используются в клинических условиях [68, 72, 80, 86]. Совсем недавно для выявления вирусов гриппа и других вирусов у постели больного стали доступны молекулярные тесты в месте оказания медицинской помощи (петлевая изотермическая амплификация (LAMP) нуклеиновых кислот, ПЦР в реальном времени), обеспечивающая степень точности, сравнимую с обычные лабораторные ПЦР [77, 80].Однако влияние этих молекулярных анализов на клинические исходы и их экономическая эффективность остаются неясными и заслуживают дальнейшей оценки [87].
RSV вызывает серьезные заболевания у детей и пожилых людей с бременем, проявлениями и тяжестью, сопоставимыми с гриппом. Специальные противовирусные препараты (, например, ингибиторов слияния) находятся в разработке [88, 89]; однако диагностика может быть затруднена из-за низкой чувствительности анализов на антигены (20–60%, выше у детей), а также из-за медленного и технически сложного процесса посева [87, 88].Более чувствительные методы ПЦР (одноплексные, мультиплексные) становятся предпочтительными тестами, особенно у взрослых, которые обычно имеют более низкую вирусную нагрузку [80, 87, 94]. Аналогичным образом, при пневмонии, вызванной RSV, следует рассматривать образцы нижних дыхательных путей, включая мокроту, если таковые имеются; Было предложено использование качественного образца мокроты и способы преодоления трудностей при его обработке [72, 85, 87]. Тестирование на другие вирусы (обычно с помощью мультиплексных тестов) приобретает все большее значение из-за растущего признания их роли в возникновении инфекций нижних дыхательных путей, госпитализаций и госпитализаций; клинические испытания широкого спектра или вирус-специфических агентов продолжаются ( e.грамм. нитазоксанид-NCT01227421, фавипиравир-NCT01728753 и DAS181-NCT01644877) [68, 72, 77, 83, 88]. Уроки эпидемий, вызванных возникающими патогенами, предполагают, что тщательная лабораторная оценка недиагностированной пневмонии с помощью молекулярных (, например, h2N1pdm09, H7N9) и культуральных (, например, , коронавирус тяжелого острого респираторного синдрома, коронавирус ближневосточного респираторного синдрома) вместе с применением передовых методов такие методы, как секвенирование следующего поколения, важны для их быстрого обнаружения [78, 88, 92].
Традиционно атипичные бактериальные патогены обычно не диагностируются из-за трудностей при проведении посевов и отсутствия надежных тестов [69, 70]. Тесты на IgM с одним титром обеспечивают более быстрые результаты, но ограничены их умеренной чувствительностью (, например, раннее заболевание, ослабленный ответ IgM у взрослых) и специфичностью (, например, перенесенная инфекция, другие инфекционные / неинфекционные заболевания) [95, 98] .
Недавние исследования указывают на высокую чувствительность быстрых молекулярных тестов ( e.грамм. LAMP, singleplex PCR, multix PCR), который может применяться к ряду респираторных образцов, включая мокроту и бронхоальвеолярный лаваж [80, 98]. Тем не менее, методы не стандартизированы (, например, праймеров-мишеней), и оптимальные типы образцов остаются неопределенными. Срочно необходимы улучшения в диагностике для направления специфической терапии из-за появления во всем мире резистентности к макролидам (Азия 30–100%, США / Европа 10–30%) и проблемы, которую это создает для эмпирических схем лечения ВП (обычно β-лактам плюс макролид) [95].Аналогичные проблемы существуют для серологической и молекулярной диагностики острой инфекции C. pneumoniae , включая длительное бессимптомное носительство и отсутствие стандартизации [93]. В отличие от этого, методы диагностики инфекции, вызванной L. pneumophila , хорошо известны и описаны в текущих руководствах по лечению пневмонии [93, 99]. Вкратце, тесты на антиген в моче обладают высокой чувствительностью (75–80%) и специфичностью (99–100%), но надежно диагностируют только самую распространенную серогруппу (серогруппа 1).Более свежие данные показывают, что ПЦР образцов нижних дыхательных путей, включая мокроту, позволяет диагностировать раннюю, низкую бактериальную нагрузку и инфекции, не относящиеся к серогруппе 1. Однако наличие сухого кашля может ограничить его использование. Сочетание ПЦР с анализом мочи может максимизировать диагностическую ценность [68, 93, 100].
Диагностика пневмонии, вызванной потенциально бактериями с множественной лекарственной устойчивостью
Наиболее частыми бактериями с множественной лекарственной устойчивостью, вызывающими пневмонию, являются MRSA, P. aeruginosa , Acinetobacter baumannii и различные Enterobacteriaceae [18, 23, 101–103] ].Эталонными диагностическими методами, используемыми для идентификации бактерий, вызывающих инфекции дыхательных путей, остаются окрашивание по Граму и полуколичественная обычная культура из прямых респираторных образцов с последующей идентификацией бактерий с использованием MALDI-TOF (время пролета лазерной десорбции / ионизации с использованием матрицы) масс-спектрометрия [48, 104, 105] и определение чувствительности потенциального патогена [106]. Помимо трудности дифференциации колонизации и инфекции, этот процесс занимает минимум 2 дня и имеет низкую чувствительность, особенно если образец взят после начала лечения антибиотиками [39].Как следствие, многие пациенты получают неправильное лечение антибиотиками, что может увеличить заболеваемость и смертность [16, 96, 97, 107]. Это утверждение справедливо и для обычных бактерий.
Текущие рекомендации руководства по патогенам с множественной лекарственной устойчивостью (MRSA, P. aeruginosa и лекарственно-устойчивые S. pneumoniae ) включают использование респираторного фторхинолона или ß-лактама плюс макролид в амбулаторных условиях. Для стационарных пациентов, пациентов интенсивной терапии и подозреваемых P.инфекции aeruginosa , использование антипневмококкового, антипсевдомонадного ß-лактама в сочетании с ципрофлоксацином или левофлоксацином; бета-лактам плюс аминогликозид; или ß-лактам плюс аминогликозид и антипневмококковый фторхинолон. При внебольничном MRSA рекомендуется добавить ванкомицин или линезолид.
Существует несколько систем оценки для выявления пациентов с ВП с факторами риска приобретения патогенов с множественной лекарственной устойчивостью. Из них две системы, клинические оценки Shorr et al. [14] и Алиберти и др. [13] классифицируют факторы риска по группам: В системе, разработанной Shorr et al. [14], баллы начисляются за недавнюю госпитализацию (4 балла), проживание в доме престарелых (3 балла), гемодиализ (2 балла) и поступление в ОИТ (1 балл). Пациенты с менее чем 3 баллами имеют распространенность патогенов с множественной лекарственной устойчивостью 20%, тогда как пациенты с более чем 5 баллами имеют распространенность 75%. Система, разработанная Aliberti et al. [13] присваивает баллы госпитализированным пациентам с ВП с хронической почечной недостаточностью (5 баллов), предшествующей госпитализацией (4 балла), проживанием в доме престарелых (3 балла) и другими факторами риска (0.По 5 баллов). Пациенты, набравшие не менее 3 баллов, имеют распространенность патогенов с множественной лекарственной устойчивостью 38%, тогда как пациенты с оценкой ≤0,5 баллов имеют распространенность 8%. Молекулярная диагностика, например, с помощью специальных ПЦР-тестов, частично преодолела упомянутые трудности [90]. В последние годы были разработаны молекулярные методы, основанные на мультиплексной ПЦР, для одновременной идентификации и количественного определения нескольких респираторных патогенов из разных типов образцов за одну процедуру (таблица 3) [44, 49–51, 91].
ТАБЛИЦА 3
Лабораторная диагностика пневмонии, вызванной потенциально мультирезистентными бактериями
Другой проблемой для быстрой диагностики респираторных инфекций является раннее выявление профиля устойчивости к антибиотикам различных бактерий [42]. Самым большим препятствием при использовании молекулярных методов определения устойчивости является несоответствие генотипа и фенотипа [108]. Постоянно открываются новые механизмы устойчивости, и в результате потенциальное присутствие неизвестных механизмов может привести к ложноотрицательным результатам с использованием молекулярных методов [109].Дополнительной проблемой является обнаружение генотипических маркеров, фенотипически не обнаруживающих клинически значимой резистентности [108].
Несмотря на недостатки молекулярных методов, ранняя информация о профиле резистентности с большей вероятностью улучшит эмпирическое лечение, чем отсутствие информации вообще [109]. В настоящее время разрабатывается анализ, основанный на мультиплексной ПЦР, который может обнаруживать некоторые маркеры бактериальной устойчивости, участвующие в возникновении респираторной инфекции, включая гены, связанные с устойчивостью к β-лактамам ( mecA , bla TEM , bla SHV , bla CTX-M , bla DHA , bla EBC , bla OXA-51 и bla KPC / macrolides (макролиды 90/90) ermB , ermC , msrA и mefA ), фторхинолоны (обнаружение изменений аминокислотных кодонов gyrA83 и gyrA87 в GyrA и ParC) и маркеры интегронов класса 1 (int1 и sul1) [110].
Недавно появилась новая группа молекулярных методов, основанная на LAMP [45]. В отличие от обычных ПЦР, в которых для амплификации нуклеиновых кислот требуется серия циклов изменения температуры, эти методы позволяют амплификацию при постоянной температуре. Zhang et al. [46] применил этот метод для быстрой диагностики основных патогенных бактерий ( S. pneumoniae , S. aureus , Escherichia coli , Klebsiella pneumoniae , P.aeruginosa , A. baumannii , Stenotrophomonas maltophilia и H. influenzae ) в 120 образцах мокроты пациентов с подозрением на обострение хронической обструктивной болезни легких. LAMP дал более положительные результаты, чем обычные культуры, а также более высокую корреляцию с клиническими симптомами.
В недавнем исследовании Koncan et al. [47], была разработана новая методология под названием «respFISH», которая объединила классическую флуоресцентную технологию гибридизации in situ (FISH) с флуоресцентно-меченными молекулярными маяками ДНК в качестве зондов.Это было использовано для анализа 165 респираторных проб, в том числе 85 мокроты, 79 бронхиальных секретов (75 бронхиальных аспиратов и четыре бронхиальных лаважа) и одного трахеального аспирата. Чувствительность этой методики составила 94,39%, а ее специфичность — 87,93%. Практическое время анализа составляло примерно 30 минут.
Винсент и др. [112] описал ПЦР с последующей масс-спектрометрией с ионизацией электрораспылением, с помощью которой можно было обнаружить более 800 инфекционных патогенов кровотока в одном анализе у пациентов с сепсисом и / или пневмонией, связанной со здоровьем, пневмонией, связанной с вентилятором, или тяжелой ВП.Это исследование показало, что применение этого диагностического метода позволило идентифицировать микроорганизмы в крови в три раза чаще, чем при использовании стандартных культур, и, что более важно, изменило лечение антибиотиками у 57% включенных пациентов.
Микробиом легких
В последние годы новые методы, не зависящие от культуры, показали, что легкие, которые ранее считались стерильными, имеют разнообразные микробные сообщества [111, 113]. Эти сообщества существуют в отсутствие инфекции и видоизменяются в случае острой или обострившейся инфекции [111].Патогенные микроорганизмы, обнаруживаемые при пневмонии (, например, S. pneumoniae ), являются лишь некоторыми из тех, которые имеют доступ к нижним дыхательным путям, но также могут быть идентифицированы в микробиоте легких пациентов без острой пневмонии [114].
Чен и др. [114] изучали микробиом в образцах мокроты 45 пациентов с ВП. Они обнаружили сходство со здоровым контролем на уровне филы, а на уровне родов они обнаружили стабильность для Streptococcus spp.и Neisseria spp. но изменения в Moraxella spp. и Rothia spp. Они пришли к выводу, что Rothia spp. может быть эндогенным возбудителем пневмонии. У пожилых пациентов с пневмонией Wouter et al. [115] наблюдали три профиля микробиоты, тесно связанные с пневмонией: лактобациллы, S. pneumoniae и Rothia spp. Они предположили, что пневмония у пожилых пациентов с дисбактериозом микробиома верхних дыхательных путей имела избыточный бактериальный рост одного вида и отдельных анаэробных бактерий.
Abeles et al. [116] изучали действие двух наиболее часто назначаемых антибиотиков в США (амоксициллин и азитромицин), чтобы определить, оказывает ли кратковременное применение антибиотиков какое-либо продолжительное воздействие на микробиоту человека. Поскольку антибиотики часто всасываются через желудочно-кишечный тракт и распределяются по тканям через кровоток , они ожидали, что каждый из них будет влиять на микрофлору каждой исследуемой поверхности тела (кишечник, кожа и рот). Авторы обнаружили, что всего 3 дня лечения наиболее часто назначаемыми антибиотиками могут привести к устойчивому снижению разнообразия микробиоты, что может иметь последствия для поддержания здоровья человека и устойчивости к болезням.
Хотя впереди еще долгий путь, мы уверены, что в ближайшие годы более глубокие знания и понимание микробиома легких (и кишечника) изменят наши взгляды на физиопатологию, лечение и профилактику пневмонии.
Молекулярные методы в клинической практике
Экспресс-диагностические тесты идентифицируют конкретный патоген или помогают отличить бактериальную инфекцию от вирусной; предоставить информацию о чувствительности к антибиотикам; контролировать реакцию на антибактериальную терапию; оценить прогноз; помощь в управлении антимикробными препаратами; и предоставить информацию для наблюдения за заболеваниями.
Эти технологии могут быть применены к различным группам пациентов, от амбулаторных пациентов (позволяющих безопасную выписку) до пациентов, нуждающихся в лечении в отделении интенсивной терапии. Быстрые результаты (1-2 часа) могут быть полезны при принятии решений у критических пациентов, особенно при быстром начале соответствующей противомикробной терапии, фактора, связанного со смертностью. Кроме того, быстрое выявление патогенов, устойчивых к антибиотикам, имеет решающее значение для своевременной изоляции пациентов [19]. Однако есть еще две серьезные проблемы.1) Различие между колонизацией и инфекцией по-прежнему является проблемой для клиницистов, за исключением, вероятно, случая S. pneumoniae , и у нас нет достаточных доказательств для всех этих методов, чтобы сделать выводы относительно этого. 2) Относительные затраты и результаты диагностического тестирования должны учитываться, когда решение о внедрении этих экспресс-тестов принимается системами здравоохранения — необходимы дальнейшие исследования экономической эффективности.
Выводы и реализация
Сочетание новых и старых методов улучшит нашу способность более точно и быстро обнаруживать микробы, вызывающие пневмонию.Эта стратегия гарантирует, что пациенты получат наиболее подходящую противомикробную терапию, и может сократить использование антибиотиков широкого спектра действия, тем самым снизив устойчивость к антибиотикам (рисунок 1). Поскольку большинство исследований, описанных в этом обзоре, демонстрируют потенциальные преимущества молекулярных методов, такие как повышенная чувствительность и более высокая скорость постановки микробиологического диагноза, необходимы дополнительные исследования для систематической и тщательной оценки их рабочих характеристик, определения того, как эти новые технологии улучшат диагностическое тестирование на респираторные патогены и влияние на лечение пациентов при их дальнейшем внедрении в повседневную практику.Чтобы различать колонизацию и инфекцию, рекомендуется использовать количественный порог количества колониеобразующих единиц (≥10 -5 КОЕ · мл -1 , как описано в предыдущих исследованиях) [43, 58 , 62, 63]. Для реализации этих методов необходимо обсудить с отделением микробиологии и лечащим специалистом, какие молекулярные тесты необходимо использовать и на какие патогены следует воздействовать. Хотя недавние публикации, касающиеся очевидной полезности мультиплексных молекулярных процедур для обнаружения патогенов ВП, обнадеживают, серьезные опасения остаются [58, 62, 63].Протокол, решающий эти проблемы, должен быть разработан и оценен. Ключевой вопрос в этой оценке заключается в том, нужно ли менять нашу текущую клиническую практику. Произойдут ли изменения в назначении антибиотиков и, если да, улучшится ли это использование антибиотиков? Кроме того, необходимо провести тщательную оценку затрат. Наконец, концепции, касающиеся микробиома легких, очень многообещающие и в настоящее время являются предметом многих исследований. Мы считаем, что эти концепции изменят наше представление о легочной инфекции, о том, как ее предотвратить и как улучшить ее лечение.
- Получено 9 июня 2016 г.
- Принято 17 сентября 2016 г.
Диагностика и лечение внебольничной пневмонии
1. Манделл Л.А., Вундернк Р.Г., Анзуэто А. и др. (2007). Общество инфекционных болезней Америки / Американское торакальное общество согласовали руководящие принципы ведения внебольничной пневмонии у взрослых. Clinical Infectious Diseases , 44 (Suppl. 2), S27–72. Найдите этот ресурс:
2. Falguera M, Carratalà J, Ruiz-Gonzalez A, et al.(2009). Факторы риска и исход внебольничной пневмонии, вызванной грамотрицательными бациллами. Respirology , 14 (1), 105–11. Найдите этот ресурс:
3. Martin-Loeches I, Rodriguez A, Bonastre J и рабочая группа H2N1 SEMICYUC. (2011). Тяжелая пандемия (h2N1) против гриппа A: отчет о первых смертях в Испании. Respirology , 16 (1), 78–85. Найдите этот ресурс:
4. Cillóniz C, Ewig S, Ferrer M, et al. (2011). Внебольничная полимикробная пневмония в отделении интенсивной терапии: этиология и прогноз. Critical Care , 15 (5), R209. Найдите этот ресурс:
5. Choi SH, Hong SB, Ko GB, et al. (2012). Вирусная инфекция у пациентов с тяжелой пневмонией, требующих госпитализации в реанимацию. Американский журнал респираторной медицины и реанимации , 186 (4), 325–32. Найдите этот ресурс:
(стр. 538)
6. Вудхед М., Блази Ф., Эвиг С. и др. (2011). Рекомендации по лечению инфекций нижних дыхательных путей у взрослых. Клинические микробиологические инфекции , 17 (Приложение 6), E1–59. Найдите этот ресурс:
7. Аневлавис С., Петроглу Н., Цаварас А. и др. (2009). Проспективное исследование диагностической полезности окрашивания мокроты по Граму при пневмонии. Journal of Infection , 59 , 83–9. Найдите этот ресурс:
8. Aramburo A, van Schaik S, Louie J, et al. (2011). Роль полимеразной цепной реакции обратной транскрипции в реальном времени для обнаружения респираторных вирусов у детей в критическом состоянии с респираторными заболеваниями: пора ли изменить алгоритм? Педиатрическая реанимация , 12 (4), e160–5.Найдите этот ресурс:
9. Rello J, Lisboa T, Lujan M, et al. (2009). Тяжесть пневмококковой пневмонии, связанная с бактериальной нагрузкой на геном. Chest , 136 (3), 832–40. Найдите этот ресурс:
10. Templeton KE, Scheltinga SA, Graffelman AW, et al. (2003). Сравнение и оценка ПЦР в реальном времени, амплификации на основе последовательностей нуклеиновых кислот в реальном времени, стандартной ПЦР и серологии для диагностики Mycoplasma pneumoniae. Журнал клинической микробиологии , 41 (9), 4366–71.Найдите этот ресурс:
11. Чалмерс Дж. Д., Мандал П., Синганаягам А. и др. Инструменты оценки тяжести для госпитализации в ОИТ при внебольничной пневмонии: систематический обзор и метаанализ. Отделение интенсивной терапии , 37 (9), 1409–20. [Обзор.] Найдите этот ресурс:
12. Барлоу Дж., Натвани Д. и Дэйви П. (2007). Показатель тяжести пневмонии CURB65 превосходит показатели общего сепсиса и раннего предупреждения в прогнозировании смертности при внебольничной пневмонии. Thorax , 62 , 253–9. Найдите этот ресурс:
13. Рамирес П., Феррер М., Марти В. и др. (2011). Воспалительные биомаркеры и прогноз для поступления в отделение интенсивной терапии при тяжелой внебольничной пневмонии. Critical Care Medicine , 39 , 2211–17. Найдите этот ресурс:
14. Gamble JM, Eurich DT, Marrie TJ и Majumdar SR. Прием гипогликемии и повышение летальности у пациентов, госпитализированных с пневмонией. Американский журнал медицины , 123 , 556 , e11–16.Найдите этот ресурс:
15. Мартинес Дж. А., Хоркахада Дж. П., Алмела М. и др. (2003). Добавление макролида к эмпирической схеме приема антибиотиков на основе бета-лактама связано с более низкой внутрибольничной смертностью у пациентов с бактериемической пневмококковой пневмонией. Клинические инфекционные заболевания , 36 , 389–95. Найдите этот ресурс:
16. Конфалониери М., Урбино Р., Потена А. и др. Инфузия гидрокортизона при тяжелой внебольничной пневмонии: предварительное рандомизированное исследование. Американский журнал респираторной медицины и реанимации , 171 (3), 242–8. Найдите этот ресурс:
17. Snijders D, Daniels JM, de Graaff CS, et al. (2010). Эффективность кортикостероидов при внебольничной пневмонии: рандомизированное двойное слепое клиническое исследование. Американский журнал респираторной медицины и реанимации , 181 , 975–82. Найдите этот ресурс:
18. Meijvis SC, Hardeman H, Remmelts HH, et al. (2011). Дексаметазон и продолжительность пребывания в больнице у пациентов с внебольничной пневмонией: рандомизированное двойное слепое плацебо-контролируемое исследование. Lancet , 377 (9782), 2023–30. Найдите этот ресурс:
19. File TM, Garau J, Jacobs MR, et al. (2005). Эффективность новой фармакокинетически усиленной композиции амоксициллина / клавуланата (2000/125 мг) у взрослых с внебольничной пневмонией, вызванной Streptococcus pneumoniae, включая штаммы, устойчивые к пенициллину. International Journal of Antimicrobial Agents , 25 , 110–19. Найдите этот ресурс:
20. Менендес Р. и Торрес А.(2007). Неэффективность лечения внебольничной пневмонии. Chest , 132 (4), 1348–55. Найдите этот ресурс:
Дифференциальный диагноз пневмонии — wikidoc
Главный редактор: C. Майкл Гибсон, M.S., M.D. [1]; Заместитель главного редактора (ов): Хамид Кази, доктор медицины, бакалавр наук [2], Приямвада Сингх, доктор медицины [3] Сайед Хассан А. Казми, бакалавр, доктор медицины [4]
Обзор
Пневмонию следует дифференцировать от других состояний, вызывающих кашель, лихорадку, одышку и тахипноэ, таких как астма, ХОБЛ, ХСН, рак, ГЭРБ, легочная эмболия.
Дифференциация пневмонии от других заболеваний
Дифференциальный диагноз
| Причины Полости легких | Отличительные особенности | Дифференциальные радиологические результаты | Подтверждение диагноза |
|---|---|---|---|
|
| ||
|
| ||
|
| ||
| |||
|
| ||
| |||
| |||
|
|
Таблица 1: Дифференциация пситтакоза от других болезней
Ключ;
+, встречается в некоторых случаях
++, встречается во многих случаях,
+++, встречается часто
Пнемонию следует дифференцировать от других заболеваний, вызывающих атипичную пневмонию, таких как Ку-лихорадка и легионеллезная пневмония:
| Болезнь | Выдающиеся клинические особенности | Результаты лабораторных исследований | Рентген грудной клетки |
|---|---|---|---|
| Ку-лихорадка |
ПЦР | Ку-лихорадочная пневмония — — Случай любезно предоставлен Королевской респираторной больницей Мельбурна, Radiopaedia.org, rID 21993 | |
| Mycoplasma пневмония | Микоплазменная пневмония — случай любезно предоставлен доктором Альборзом Джахангири, Радиопедия.org, RID 45781 | ||
| Легионеллез | Легионелла пневмония — случай любезно предоставлен доктором Генри Книпом, Radiopaedia.org, rID 31816 | ||
| Хламидийная пневмония | Хламидиоз-пневмония — Случай любезно предоставлен доктором Эндрю Диксоном, Radiopaedia.org, rID 14567 |
Другие дифференциалы
Пневмонию следует дифференцировать от других заболеваний, проявляющихся кашлем, лихорадкой, одышкой и тахипноэ.Дифференциалы включают следующие: [18] [19] [20] [21] [22] [23] [24] [25] [26] [27] [28] [29] [30] [31] [32] [33] [34] [35] [36] [37]
| Болезни | Диагностические тесты | Медицинский осмотр | Симптомы | История болезни | Прочие результаты | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| КТ и МРТ | ЭКГ | Рентген грудной клетки | Тахипноэ | Тахикардия | Лихорадка | Боль в груди | Кровохарканье | Одышка при физической нагрузке | Свистящее дыхание | Нежность груди | Изъязвление носоглотки | Каротидный брюшко | |||
| Тромбоэмболия легочной артерии |
| ✔ | ✔ | ✔ (Низкая оценка) | ✔ | ✔ (В случае массивного ПЭ) | ✔ | — | — | — | — | ||||
| Застойная сердечная недостаточность |
| ✔ | ✔ | ✔ | — | — | ✔ | — | — | — | — | ||||
| Перкардит |
|
| ✔ | ✔ | ✔ (Низкая оценка) | ✔ (С облегчением от сидения и наклона вперед) | — | ✔ | — | — | — | — |
| ||
| Пневмония |
| ✔ | ✔ | ✔ | ✔ | — | ✔ | ✔ | — | — | — | ||||
| Васкулит | Однородное периферическое набухание стенки сосуда | ✔ | ✔ | ✔ | ✔ | ✔ | ✔ | — | ✔ | ✔ | ✔ | ||||
| Хроническая обструктивная болезнь легких (ХОБЛ) |
| ✔ | ✔ | — | — | — | ✔ | ✔ | — | — | — | ||||
Список литературы
- ↑ Шиле Ф, Мюллер Дж, Колине Э, Сист Дж, Арцоглу П, Бретчнайдер Х; и другие.(1992). «Межлабораторное исследование метода IFCC для аланинаминотрансферазы, проведенное с использованием частично очищенного стандартного материала». Clin Chem . 38 (12): 2365–71. PMID 1458569.
- ↑ Кастро-Гвардиола А, Арменгу-Арке А, Вьехо-Родригес А, Пеньярроха-Матутано Г, Гарсия-Брагадо Ф (2000). «Дифференциальная диагностика внебольничной пневмонии и непневмонических заболеваний грудной клетки в отделении неотложной помощи». Eur J Intern Med . 11 (6): 334–339. PMID 11113658.
- ↑ Ансьё, Свен (1935). «Вклад в дифференциальную диагностику пневмонии у детей». Acta Paediatrica . 17 (3): 439–446. DOI: 10.1111 / j.1651-2227.1935.tb07697.x. ISSN 0803-5253.
- ↑ 4,0 4,1 Чаудхури М.Р. (1973). «Первичные кавитирующие карциномы легких». Грудь . 28 (3): 354–66. PMC 470041. PMID 4353362.
- ↑ Mouroux J, Padovani B, Elkaïm D, Richelme H (1996).«Следует ли рассматривать кавитированный бронхолегочный рак в отдельную сущность?». Ann. Грудной. Сургут . 61 (2): 530–2. DOI: 10.1016 / 0003-4975 (95) 00973-6. PMID 8572761.
- ↑ Onn A, Choe DH, Herbst RS, Correa AM, Munden RF, Truong MT, Vaporciyan AA, Isobe T, Gilcrease MZ, Marom EM (2005). «Опухолевая кавитация при немелкоклеточном раке легкого I стадии: экспрессия рецептора эпидермального фактора роста и прогноз неблагоприятного исхода». Радиология . 237 (1): 342–7.DOI: 10.1148 / radiol.2371041650. PMID 16183941.
- ↑ 7.0 7.1 Langford CA, Hoffman GS (1999). «Редкие заболевания.3: гранулематоз Вегенера». Грудь . 54 (7): 629–37. PMC 1745525. PMID 10377211.
- ↑ Ли К.С., Ким Т.С., Фудзимото К., Мория Х., Ватанабе Х., Татейши У., Ашизава К., Джоко Т, Ким Э.А., Квон О.Дж. (2003). «Грудные проявления гранулематоза Вегенера: результаты КТ у 30 пациентов». евро Радиол . 13 (1): 43–51. DOI: 10.1007 / s00330-002-1422-2. PMID 12541109.
- ↑ Баумэн Р.П., Тейрштейн А.С., Джадсон М.А., Россман, доктор медицины, Йегер Х., Бресниц Э.А., ДеПало Л., Ханнингхак Г., Яннуцци М.С., Джонс СиДжей, МакЛеннан Г., Моллер Д.Р., Ньюман Л.С., Рабин Д.Л., Роуз С., Рыбицки Б. , Вайнбергер С.Е., Террин М.Л., Кнаттеруд Г.Л., Черняк Р. (2001). «Клинические характеристики пациентов в исследовании случай-контроль саркоидоза». г. J. Respir. Крит. Care Med . 164 (10 Pt 1): 1885–9.DOI: 10.1164 / ajrccm.164.10.2104046. PMID 11734441.
- ↑ Браунер М.В., Гренье П., Момпоинт Д., Ленуар С., де Крему Х. (1989). «Легочный саркоидоз: оценка с помощью КТ высокого разрешения». Радиология . 172 (2): 467–71. DOI: 10.1148 / radiology.172.2.2748828. PMID 2748828.
- ↑ Мерфи Дж., Шнайдер П., Герольд С., Флауэр С. (1998). «Облитерирующий бронхиолит, вызывающий пневмонию, имитирующую карциному бронхов». евро Радиол . 8 (7): 1165–9. DOI: 10.1007 / s003300050527. PMID 9724431.
- ↑ 12,0 12,1 Аль-Ганем С., Аль-Джахдали Х., Бамефле Х., Хан А.Н. (2008). «Облитерирующий бронхиолит с организующейся пневмонией: патогенез, клинические особенности, визуализация и обзор терапии». Энн Торак Мед . 3 (2): 67–75. DOI: 10.4103 / 1817-1737.39641. PMC 2700454. PMID 19561910.
- ↑ Cordier JF, Loire R, Brune J (1989). «Идиопатический облитерирующий бронхиолит с организующейся пневмонией.Определение характерных клинических профилей в серии из 16 пациентов ». Chest . 96 (5): 999–1004. PMID 2805873.
- ↑ Ли К.С., Кулльниг П., Хартман Т.Э., Мюллер Н.Л. (1994). «Криптогенная организующая пневмония: результаты компьютерной томографии у 43 пациентов». AJR Am J Roentgenol . 162 (3): 543–6. DOI: 10.2214 / ajr.162.3.8109493. PMID 8109493.
- ↑ Suri HS, Yi ES, Nowakowski GS, Vassallo R (2012). «Легочный гистиоцитоз из клеток Лангерганса». Орфанет J Редкие диски . 7 : 16. DOI: 10.1186 / 1750-1172-7-16. PMC 3342091. PMID 22429393.
- ↑ Мур А.Д., Годвин Д.Д., Мюллер Н.Л., Найдич Д.П., Хаммар С.П., Бушман Д.Л., Такасуги Дж.Э., де Карвалью С.Р. (1989). «Легочный гистиоцитоз X: сравнение результатов рентгенографии и компьютерной томографии». Радиология . 172 (1): 249–54. DOI: 10.1148 / radiology.172.1.2787035. PMID 2787035.
- ↑ 17,0 17,1 17,2 17.3 Ирфан М., Фаруки Дж., Хасан Р. (2013). «Внебольничная пневмония». Curr Opin Pulm Med . 19 (3): 198–208. DOI: 10.1097 / MCP.0b013e32835f1d12. PMID 23422417.
- ↑ Бренес-Салазар Ж.А. (2014). «Признаки Вестермарка и Паллы при острой и хронической тромбоэмболии легочной артерии: все еще актуальны в нынешнюю эпоху компьютерной томографии». J Emerg Trauma Shock . 7 (1): 57–8. DOI: 10.4103 / 0974-2700.125645. PMC 37. PMID 24550636.
- ↑ «КТ-ангиография легочной эмболии: диагностические критерии и причины неправильного диагноза | Радиография».
- ↑ Bĕlohlávek J, Dytrych V, Linhart A (2013). «Легочная эмболия, часть I: эпидемиология, факторы риска и стратификация риска, патофизиология, клинические проявления, диагностика и нетромботическая легочная эмболия». Exp Clin Cardiol . 18 (2): 129–38. PMC 3718593. PMID 23940438.
- ↑ «Легочная эмболия: симптомы — Национальная медицинская библиотека — PubMed Health».
- ↑ Ramani GV, Uber PA, Mehra MR (2010). «Хроническая сердечная недостаточность: современная диагностика и лечение». Mayo Clin. Proc . 85 (2): 180–95. DOI: 10.4065 / mcp.2009.0494. PMC 2813829. PMID 20118395.
- ↑ Blinderman CD, Homel P, Billings JA, Portenoy RK, Tennstedt SL (2008). «Симптоматика и качество жизни у пациентов с тяжелой застойной сердечной недостаточностью». J Устранение болевых симптомов . 35 (6): 594–603.DOI: 10.1016 / j.jpainsymman.2007.06.007. PMC 2662445. PMID 18215495.
- ↑ Хокинс Н.М., Петри М.С., Джунд П.С., Чалмерс Г.В., Данн Ф.Г., МакМюррей Дж.Дж. (2009). «Сердечная недостаточность и хроническая обструктивная болезнь легких: подводные камни диагностики и эпидемиология». евро. J. Сердечная недостаточность . 11 (2): 130–9. DOI: 10.1093 / eurjhf / hfn013. PMC 2639415. PMID 1
10. - ↑ Такасуги Дж. Э., Годвин Дж. Д. (1998). «Радиология хронической обструктивной болезни легких». Радиол. Clin. North Am . 36 (1): 29–55. PMID 9465867.
- ↑ Wedzicha JA, Donaldson GC (2003). «Обострения хронической обструктивной болезни легких». Respir Care . 48 (12): 1204–13, обсуждение 1213–5. PMID 14651761.
- ↑ Накава, Миссури, Хокинс С, Барбанди Ф (2013). «Астма, хроническая обструктивная болезнь легких (ХОБЛ) и синдром перекрытия». J Am Board Fam Med . 26 (4): 470–7.DOI: 10.3122 / jabfm.2013.04.120256. PMID 23833163.
- ↑ Khandaker MH, Espinosa RE, Nishimura RA, Sinak LJ, Hayes SN, Melduni RM, Oh JK (2010). «Заболевания перикарда: диагностика и лечение». Mayo Clin. Proc . 85 (6): 572–93. DOI: 10.4065 / mcp.2010.0046. PMC 2878263. PMID 20511488.
- ↑ Bogaert J, Francone M (2013). «Заболевания перикарда: значение КТ и МРТ». Радиология . 267 (2): 340–56. DOI: 10.1148 / радиол.13121059. PMID 23610095.
- ↑ Гариб А.М., Стерн Э.Дж. (2001). «Радиология пневмонии». Med. Clin. North Am . 85 (6): 1461–91, х. PMID 11680112.
- ↑ Шмидт WA (2013). «Визуализация при васкулите». Лучшая практика Res Clin Rheumatol . 27 (1): 107–18. DOI: 10.1016 / j.berh.2013.01.001. PMID 23507061.
- ↑ Суреш Э. (2006). «Диагностический подход к пациентам с подозрением на васкулит». Postgrad Med J . 82 (970): 483–8. DOI: 10.1136 / pgmj.2005.042648. PMC 2585712. PMID 168
.
- ↑ Штейн П.Д., Дален Дж. Э., Макинтайр К. М., Сасахара А. А., Венгер Н. К., Уиллис П. У. (1975). «Электрокардиограмма при острой тромбоэмболии легочной артерии». Prog Cardiovasc Dis . 17 (4): 247–57. PMID 123074.
- ↑ Warnier MJ, Rutten FH, Numans ME, Kors JA, Tan HL, de Boer A, Hoes AW, De Bruin ML (2013). «Электрокардиографические характеристики больных хронической обструктивной болезнью легких». ХОБЛ . 10 (1): 62–71. DOI: 10.3109 / 15412555.2012.727918. PMID 23413894.
- ↑ Штейн П.Д., Матта Ф., Экках М., Салех Т., Джанджуа М., Патель Ю.Р., Хадра Х. (2012). «Электрокардиограмма при пневмонии». г. Дж. Кардиол . 110 (12): 1836–40. DOI: 10.1016 / j.amjcard.2012.08.019. PMID 23000104.
- ↑ Hazebroek MR, Kemna MJ, Schalla S, Sanders-van Wijk S, Gerretsen SC, Dennert R, Merken J, Kuznetsova T, Staessen JA, Brunner-La Rocca HP, van Paassen P, Cohen Tervaert JW, Heymans S ( 2015).«Распространенность и прогностическая значимость поражения сердца при ANCA-ассоциированном васкулите: эозинофильный гранулематоз с полиангиитом и гранулематоз с полиангиитом». Внутр. Дж. Кардиол . 199 : 170–9. DOI: 10.1016 / j.ijcard.2015.06.087. PMID 26209947.
- ↑ Деннерт Р.М., ван Паассен П., Шалла С., Кузнецова Т., Алзанд Б.С., Стаессен Дж. А., Велтуис С., Крайнс Х. Дж., Терверт Дж. В., Хейманс С. (2010). «Поражение сердца при синдроме Чарджа-Стросса». Rheum артрита . 62 (2): 627–34. DOI: 10.1002 / art.27263. PMID 20112390.
Шаблон: WH
Шаблон: WS.


 00 до 20.00.
00 до 20.00.  09.2021
09.2021  В.
В.
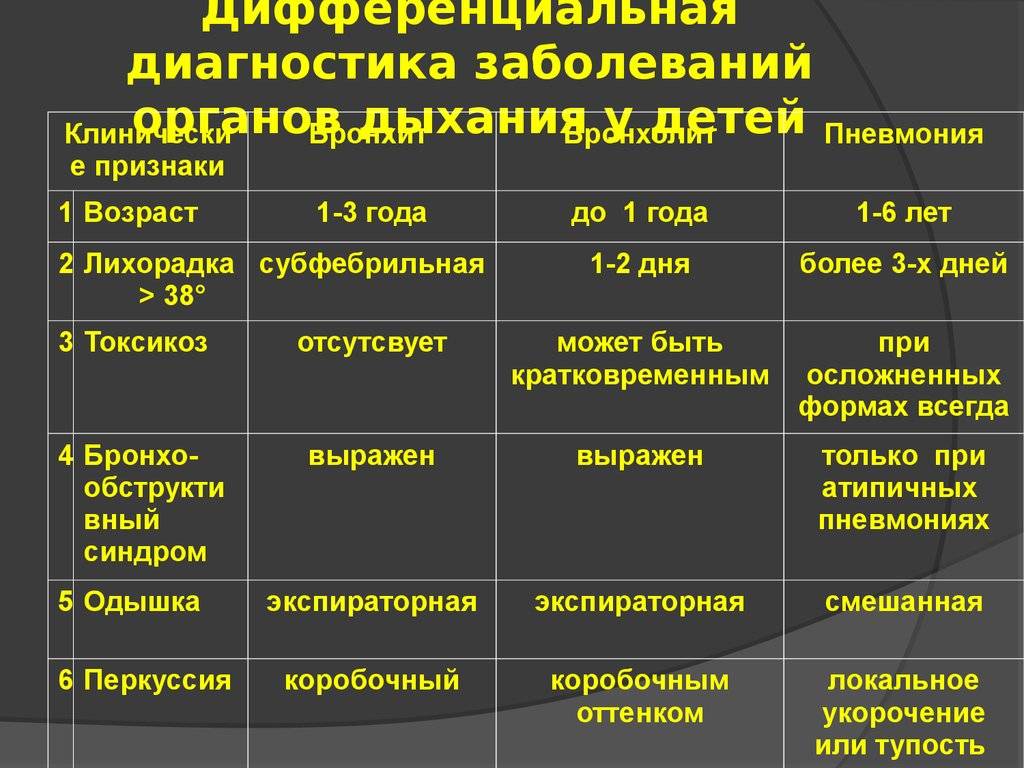 09.2021
09.2021  08.2021
08.2021  07.2020
07.2020 