История болезни — терапия (острая левосторонняя нижнедолевая пневмония) реферат по медицине
Этот файл взят из коллекции Medinfo http://www.doktor.ru/medinfo http://medinfo.home.ml.org E-mail: [email protected] or [email protected] or [email protected] FidoNet 2:5030/434 Andrey Novicov Пишем рефераты на заказ — e-mail: [email protected] В Medinfo для вас самая большая русская коллекция медицинских рефератов, историй болезни, литературы, обучающих программ, тестов. Заходите на http://www.doktor.ru — Русский медицинский сервер для всех! ПАСПОРТНАЯ ЧАСТЬ Ф.И.О. x Возраст: 36 лет Место жительства: Профессия: медицинская сестра Место работы: АОЗТ «Выбор» Дата госпитализации: 5 октября 1996 года STATUS PRAESЕNS SUBJECTIVUS Жалобы на момент осмотра: на колющие, слабые боли слева в нижней части грудной клетки, постоянные, усиливающиеся при глубоком дыхании и кашле, уменьшающиеся, когда больная лежит на больном боку, на сухой кашель и слабость. Жалобы на момент поступления: на интенсивные, постоянные, режуще- колющие боли в левой половине грудной клетки, усиливающиеся при глубоком дыхании и ослабляющиеся при сдавлении левой половины грудной клетки, на кашель с выделением мокроты с прожилками крови, на слабость, тошноту, одышку и потрясающие ознобы. ANAMNESIS MORBI Считает себя больной со 2 октября, когда остро поднялась температура тела до 39-40 F 0B 0С, внезапно почувствовала слабость, тошноту. К вечеру присоединился непродуктивный кашель и появились слабые, ноющие боли в левой половине грудной клетке. Принимала аспирин, но самочувствие ухудшалось: ночью кашель стал сильнее, появилось небольшое количество прозрачной мокроты. 3 октября вызвала участкового терапевта; после его осмотра был поставлен диагноз «Острое респираторное заболевание» и назначено лечение (ингаляции, бромгексин), больная принимала и ацетилсалициловую кислоту, и эффералган-UPSA. Самочувствие больной не изменялось. Ночью 5 октября самочувствие ухудшилось: усилился кашель, появилась мокрота с прожилками крови, нарастала слабость, тошнота, появилась одышка, температура тела не снижалась (39 F 0B 0), усилились постоянные, колюще-режущие боли в левой половине грудной клетки. Утром 5 октября больная вызвала участкового терапевта. После осмотра был поставлен диагноз «Левосто- ронняя нижнедолевая пневмония» и больная была направлена в больницу Святой Преподобной Мученицы Елизаветы с жалобами на постоянные, колюще-режущие боли в левой половине грудной клетки, усиливающиеся при глубоком дыхании и ослабляющиеся при сдавлении левой половины грудной клетки, на кашель с выделением мокроты с прожилками крови, на слабость, одышку, тошноту и потрясающие ознобы.
ANAMNESIS MORBI Считает себя больной со 2 октября, когда остро поднялась температура тела до 39-40 F 0B 0С, внезапно почувствовала слабость, тошноту. К вечеру присоединился непродуктивный кашель и появились слабые, ноющие боли в левой половине грудной клетке. Принимала аспирин, но самочувствие ухудшалось: ночью кашель стал сильнее, появилось небольшое количество прозрачной мокроты. 3 октября вызвала участкового терапевта; после его осмотра был поставлен диагноз «Острое респираторное заболевание» и назначено лечение (ингаляции, бромгексин), больная принимала и ацетилсалициловую кислоту, и эффералган-UPSA. Самочувствие больной не изменялось. Ночью 5 октября самочувствие ухудшилось: усилился кашель, появилась мокрота с прожилками крови, нарастала слабость, тошнота, появилась одышка, температура тела не снижалась (39 F 0B 0), усилились постоянные, колюще-режущие боли в левой половине грудной клетки. Утром 5 октября больная вызвала участкового терапевта. После осмотра был поставлен диагноз «Левосто- ронняя нижнедолевая пневмония» и больная была направлена в больницу Святой Преподобной Мученицы Елизаветы с жалобами на постоянные, колюще-режущие боли в левой половине грудной клетки, усиливающиеся при глубоком дыхании и ослабляющиеся при сдавлении левой половины грудной клетки, на кашель с выделением мокроты с прожилками крови, на слабость, одышку, тошноту и потрясающие ознобы. За время пребывания в больнице больной были проведены исследования: осмотр, рентгенография грудной клетки в 3-х проекциях, клинический анализ крови, биохимический анализ крови, микроскопическое исследование мокроты, посев мокроты; был уточнен диагноз («Острая плевропневмония слева в нижней доле») и назначено лечение (карбенициллин, гепарин, гемодез, эуфиллин, витаминотерапия). Самочувствие больной улучшилось: уменьшились слабость и кашель, он стал непродуктивным, прошла тошнота, снизилась температура тела, уменьшились боли в грудной клетке. ANAMNESIS VITAE Родилась 10 сентября 1960 года в городе Ленинграде в семье рабочих 1-м ребенком. Физически и интеллектуально развивалась нормально, от сверстников не отставала. С 7-ми лет пошла в школу. Училась хорошо. По окончании 9-ти классов училась в медучилище. После окончания которого Сосудистый пучок не выходит за пределы грудины в 1-м и 2-м межреберьях Аускультация Тоны сердца ритмичные, ясные, звучные; соотношение тонов не изменено. Артериальное давление 110/70 мм рт.
За время пребывания в больнице больной были проведены исследования: осмотр, рентгенография грудной клетки в 3-х проекциях, клинический анализ крови, биохимический анализ крови, микроскопическое исследование мокроты, посев мокроты; был уточнен диагноз («Острая плевропневмония слева в нижней доле») и назначено лечение (карбенициллин, гепарин, гемодез, эуфиллин, витаминотерапия). Самочувствие больной улучшилось: уменьшились слабость и кашель, он стал непродуктивным, прошла тошнота, снизилась температура тела, уменьшились боли в грудной клетке. ANAMNESIS VITAE Родилась 10 сентября 1960 года в городе Ленинграде в семье рабочих 1-м ребенком. Физически и интеллектуально развивалась нормально, от сверстников не отставала. С 7-ми лет пошла в школу. Училась хорошо. По окончании 9-ти классов училась в медучилище. После окончания которого Сосудистый пучок не выходит за пределы грудины в 1-м и 2-м межреберьях Аускультация Тоны сердца ритмичные, ясные, звучные; соотношение тонов не изменено. Артериальное давление 110/70 мм рт. ст. ДЫХАТЕЛЬНАЯ СИСТЕМА Осмотр Дыхание через нос, свободное, ритмичное, поверхностное. Тип дыхания- грудной. Частота дыхательных движений 22 в минуту. Форма грудной клетки правильная, симметричная, левая половина грудной клетки отстает от правой во время дыхания. Ключицы и лопатки симметричны. Лопатки плотно прилежат к задней стенки грудной клетки. Ход ребер косой. Надключичные и подключичные ямки выражены хорошо. Межреберные промежутки прослеживаются. Пальпация Грудная клетка эластичная, безболезненная. Голосовое дрожание усилено слева в нижней части грудной клетки. Перкуссия Топографическая перкуссия. Нижние границы правого легкого: по l. parasternalis- верхний край 6-го ребра по l. medioclavicularis- нижний край 6-го ребра по l. axillaris anterior- 7 ребро по l. axillaris media- 8 ребро по l. axillaris posterior- 9 ребро по l. scapuiaris- 10 ребро по l. paravertebralis- на уровне остистого отростка 11-го грудного позвонка Нижние границы левого легкого: по l. parasternalis- ——- по l.
ст. ДЫХАТЕЛЬНАЯ СИСТЕМА Осмотр Дыхание через нос, свободное, ритмичное, поверхностное. Тип дыхания- грудной. Частота дыхательных движений 22 в минуту. Форма грудной клетки правильная, симметричная, левая половина грудной клетки отстает от правой во время дыхания. Ключицы и лопатки симметричны. Лопатки плотно прилежат к задней стенки грудной клетки. Ход ребер косой. Надключичные и подключичные ямки выражены хорошо. Межреберные промежутки прослеживаются. Пальпация Грудная клетка эластичная, безболезненная. Голосовое дрожание усилено слева в нижней части грудной клетки. Перкуссия Топографическая перкуссия. Нижние границы правого легкого: по l. parasternalis- верхний край 6-го ребра по l. medioclavicularis- нижний край 6-го ребра по l. axillaris anterior- 7 ребро по l. axillaris media- 8 ребро по l. axillaris posterior- 9 ребро по l. scapuiaris- 10 ребро по l. paravertebralis- на уровне остистого отростка 11-го грудного позвонка Нижние границы левого легкого: по l. parasternalis- ——- по l. medioclavicularis- ——- по l. axillaris anterior- 7 ребро по l. axillaris media- 9 ребро по l. axillaris posterior- 9 ребро по l. scapuiaris- 10 ребро по l. paravertebralis- на уровне остистого отростка 11-го грудного позвонка Верхние границы легких: Спереди на 3 см выше ключицы. Сзади на уровне остистого отростка 7 шейного позвонка. Активная подвижность нижнего легочного края правого легкого по средней аксилярной линии: на вдохе 4 см на выдохе 4 см Активная подвижность нижнего легочного края левого легкого по средней аксилярной линии: на вдохе 2 см на выдохе 2 см Сравнительная перкуссия: Над симметричными участками легочной ткани определяется ясный легочный звук. Определяется притупление перкуторного звука слева в подлопаточной области. Аускультация Дыхание жесткое. Ослабление дыхания слева в подлопаточной области. Тамже выслушиваются влажные мелкопузырчатые хрипы и слабый шум трения плевры. ПИЩЕВАРИТЕЛЬНАЯ СИСТЕМА Осмотр Живот правильной формы, симметричный, не участвует в акте дыхания, пупок втянут.
medioclavicularis- ——- по l. axillaris anterior- 7 ребро по l. axillaris media- 9 ребро по l. axillaris posterior- 9 ребро по l. scapuiaris- 10 ребро по l. paravertebralis- на уровне остистого отростка 11-го грудного позвонка Верхние границы легких: Спереди на 3 см выше ключицы. Сзади на уровне остистого отростка 7 шейного позвонка. Активная подвижность нижнего легочного края правого легкого по средней аксилярной линии: на вдохе 4 см на выдохе 4 см Активная подвижность нижнего легочного края левого легкого по средней аксилярной линии: на вдохе 2 см на выдохе 2 см Сравнительная перкуссия: Над симметричными участками легочной ткани определяется ясный легочный звук. Определяется притупление перкуторного звука слева в подлопаточной области. Аускультация Дыхание жесткое. Ослабление дыхания слева в подлопаточной области. Тамже выслушиваются влажные мелкопузырчатые хрипы и слабый шум трения плевры. ПИЩЕВАРИТЕЛЬНАЯ СИСТЕМА Осмотр Живот правильной формы, симметричный, не участвует в акте дыхания, пупок втянут. Пальпация Поверхностная: Живот мягкий, безболезненный. Глубокая: Сигмовидная кишка пальпируется в левой подвздошной области в виде эластического цилиндра, с ровной поверхностью шириной 1,5 см, подвижная, не урчащая, безболезненная. Слепая кишка пальпируется в типичном месте в виде цилиндра эластической консистенции, с ровной поверхностью, шириной 2 см, подвижная, не урчащая, безболезненная. Поперечно-ободочная кишка не пальпируется. Желудок не пальпируется. Нижний край печени острый, ровный, эластичный, безболезненный, не выходит из-под края реберной дуги; поверхность печени гладкая. Желчный пузырь не пальпируется. Симптомы Мерфи, Ортнера, френикус- отрицательные. Селезенка не пальпируется. Перкуссия Размеры печени по Курлову: по правой среднеключичной линии 10 см, по передней срединной линии 9 см, по левой реберной дуге 7 см. Верхняя граница селезенки по левой среднеоксилярной линии на 9 ребре, нижняя на 11 ребре. МОЧЕВЫДЕЛИТЕЛЬНАЯ СИСТЕМА В области поясницы видимых изменений не обнаружено.
Пальпация Поверхностная: Живот мягкий, безболезненный. Глубокая: Сигмовидная кишка пальпируется в левой подвздошной области в виде эластического цилиндра, с ровной поверхностью шириной 1,5 см, подвижная, не урчащая, безболезненная. Слепая кишка пальпируется в типичном месте в виде цилиндра эластической консистенции, с ровной поверхностью, шириной 2 см, подвижная, не урчащая, безболезненная. Поперечно-ободочная кишка не пальпируется. Желудок не пальпируется. Нижний край печени острый, ровный, эластичный, безболезненный, не выходит из-под края реберной дуги; поверхность печени гладкая. Желчный пузырь не пальпируется. Симптомы Мерфи, Ортнера, френикус- отрицательные. Селезенка не пальпируется. Перкуссия Размеры печени по Курлову: по правой среднеключичной линии 10 см, по передней срединной линии 9 см, по левой реберной дуге 7 см. Верхняя граница селезенки по левой среднеоксилярной линии на 9 ребре, нижняя на 11 ребре. МОЧЕВЫДЕЛИТЕЛЬНАЯ СИСТЕМА В области поясницы видимых изменений не обнаружено. Почки не паль- пируются. Симптом поколачивания по поясничной области отрицательный. ПРЕДВАРИТЕЛЬНЫЙ ДИАГНОЗ И ЕГО ОБОСНОВАНИЕ (ПЕРВИЧНОЕ ПРЕДСТАВЛЕНИЕ О БОЛЬНОМ) Больная-женщина средних лет без особых конституциональных особенностей, вид соответствует возрасту и нормальному социальному положению. Ведущими симптомами у нее являются постоянные, не интенсивные, колющие боли слева в подлопаточной области, усиливающиеся при глубоком дыхании и кашле, и уменьшающиеся при сдавлении левой половины грудной клетки, сухой кашель и слабость. При поступлении ведущими симптомами были высокая температура тела (39 F 0B 0С)-не снижающаяся несколько дней, постоянные, интенсивные, колюще-режущие боли в левой половине грудной клетки, усиливающиеся при глубоком дыхании и кашле и ослабляющиеся при сдавлении левой половины грудной клетки, кашель с выделением мокроты с прожилками крови, одышка, сильная слабость, тошнота. Из анамнеза заболевания обращает на себя внимание острое развитие всех симптомов, высокая лихорадка (39-40 F 0B 0С),не проходящая несколько дней, нарастание болей в левой половине грудной клетки (с 2 по 5 октября) от слабых до интенсивных, учащение кашля и появление большого количества мокроты с прожилками крови, нарастающая одышка, слабость и тошнота; причем проводимое лечение (бромгексин, ингаляции, аспирин) не помогало.
Почки не паль- пируются. Симптом поколачивания по поясничной области отрицательный. ПРЕДВАРИТЕЛЬНЫЙ ДИАГНОЗ И ЕГО ОБОСНОВАНИЕ (ПЕРВИЧНОЕ ПРЕДСТАВЛЕНИЕ О БОЛЬНОМ) Больная-женщина средних лет без особых конституциональных особенностей, вид соответствует возрасту и нормальному социальному положению. Ведущими симптомами у нее являются постоянные, не интенсивные, колющие боли слева в подлопаточной области, усиливающиеся при глубоком дыхании и кашле, и уменьшающиеся при сдавлении левой половины грудной клетки, сухой кашель и слабость. При поступлении ведущими симптомами были высокая температура тела (39 F 0B 0С)-не снижающаяся несколько дней, постоянные, интенсивные, колюще-режущие боли в левой половине грудной клетки, усиливающиеся при глубоком дыхании и кашле и ослабляющиеся при сдавлении левой половины грудной клетки, кашель с выделением мокроты с прожилками крови, одышка, сильная слабость, тошнота. Из анамнеза заболевания обращает на себя внимание острое развитие всех симптомов, высокая лихорадка (39-40 F 0B 0С),не проходящая несколько дней, нарастание болей в левой половине грудной клетки (с 2 по 5 октября) от слабых до интенсивных, учащение кашля и появление большого количества мокроты с прожилками крови, нарастающая одышка, слабость и тошнота; причем проводимое лечение (бромгексин, ингаляции, аспирин) не помогало. Из объективных данных интерес представляет неравномерное участие в акте дыхания правой и левой половин грудной клетки, поверхностное дыхание, усиление голосового дрожания слева в нижней части грудной клетки, преобладание тамже притупленного перкуторного звука, уменьшение активной подвижности нижнего края левого легкого, жесткое дыхание, ослабление дыхания и влажные, мелкопузырчатые хрипы слева в подлопаточной области. Перечисленный симптомокомплекс позволяет заподозрить у больной левостороннюю нижнедолевую пневмонию. Этому способствуют и сведения из анамнеза жизни: длительный контакт с ребенком, болеющим гриппом, и курение больной. Так как у больной присутствуют сильные боли, усиливающиеся при глубоком дыхании и ослабляющиеся при сдавлении грудной клетки, и шум трения плевры, можно говорить, что в процесс задействована плевра, то есть пневмонии сопутствует сухой плеврит. Диагноз будет звучать: «Острая левосторонняя нижнедолевая пневмония. Паропневмонический левосторонний фибринозный плеврит».
Из объективных данных интерес представляет неравномерное участие в акте дыхания правой и левой половин грудной клетки, поверхностное дыхание, усиление голосового дрожания слева в нижней части грудной клетки, преобладание тамже притупленного перкуторного звука, уменьшение активной подвижности нижнего края левого легкого, жесткое дыхание, ослабление дыхания и влажные, мелкопузырчатые хрипы слева в подлопаточной области. Перечисленный симптомокомплекс позволяет заподозрить у больной левостороннюю нижнедолевую пневмонию. Этому способствуют и сведения из анамнеза жизни: длительный контакт с ребенком, болеющим гриппом, и курение больной. Так как у больной присутствуют сильные боли, усиливающиеся при глубоком дыхании и ослабляющиеся при сдавлении грудной клетки, и шум трения плевры, можно говорить, что в процесс задействована плевра, то есть пневмонии сопутствует сухой плеврит. Диагноз будет звучать: «Острая левосторонняя нижнедолевая пневмония. Паропневмонический левосторонний фибринозный плеврит». Для оказания первой помощи больной необходима антибактериальная терапия антибиотиками широкого спектра действия (карбенициллин 1,0), дезинтоксикационная терапия (применение гемодеза, обильного питья, лазикса, кальция глюконата, натрия тиосульфата), для уменьшения болей-применение анальгетиков (анальгина с димедролом). Для уточнения диагноза и дифференцировки с другими патологическими нарастание болей (от слабых до интенсивных), слабости, тошноты, учащение кашля и появление большого количества мокроты с прожилками крови, присоединение одышки и неэффективность лечения; данные из анамнеза жизни: длительный контакт с ребенком, болеющим гриппом, курение больной; данные объективного исследования: отставание левой половины грудной клетки при акте дыхания, поверхностное дыхание, усиление голосового дрожания слева в нижней части грудной клетки, уменьшение подвижности нижнего легочного края левого легкого, притупление перкуторного звука слева в подлопаточной области, ослабление дыхания и наличие влажных мелкопузырчатых хрипов,шум трения плевры там же; данные лабораторно- инструментальных исследований: наличие в крови лейкоцитоза (9,2*10^9/л) с преобладанием в лейкоцитарной формуле нейтрофилов и палочкоядерных, увеличение СОЭ до 62 мм/ч, наличие в мокроте лейкоцитов (150-250 в п/ з), эритроцитов (3-15 в п/з), альвеолярных макрофагов (3-8 в п/з), при рентгенологическом исследовании грудной клетки- обнаружение тотальной пневмонической инфильтрации в нижней доле левого легкого, реактивного сужения корней легких, усиления легочного рисунка справа за счет гиперемии, затемнения левого синуса, и при бронхоскопии обнаружение острого процесса в трахеи, главных, долевых и устьев сегментарных бронхов, мы можем выделить несколько главных синдромов: болевого, интоксикационного, дыхательной недостаточности и воспаления плевры.
Для оказания первой помощи больной необходима антибактериальная терапия антибиотиками широкого спектра действия (карбенициллин 1,0), дезинтоксикационная терапия (применение гемодеза, обильного питья, лазикса, кальция глюконата, натрия тиосульфата), для уменьшения болей-применение анальгетиков (анальгина с димедролом). Для уточнения диагноза и дифференцировки с другими патологическими нарастание болей (от слабых до интенсивных), слабости, тошноты, учащение кашля и появление большого количества мокроты с прожилками крови, присоединение одышки и неэффективность лечения; данные из анамнеза жизни: длительный контакт с ребенком, болеющим гриппом, курение больной; данные объективного исследования: отставание левой половины грудной клетки при акте дыхания, поверхностное дыхание, усиление голосового дрожания слева в нижней части грудной клетки, уменьшение подвижности нижнего легочного края левого легкого, притупление перкуторного звука слева в подлопаточной области, ослабление дыхания и наличие влажных мелкопузырчатых хрипов,шум трения плевры там же; данные лабораторно- инструментальных исследований: наличие в крови лейкоцитоза (9,2*10^9/л) с преобладанием в лейкоцитарной формуле нейтрофилов и палочкоядерных, увеличение СОЭ до 62 мм/ч, наличие в мокроте лейкоцитов (150-250 в п/ з), эритроцитов (3-15 в п/з), альвеолярных макрофагов (3-8 в п/з), при рентгенологическом исследовании грудной клетки- обнаружение тотальной пневмонической инфильтрации в нижней доле левого легкого, реактивного сужения корней легких, усиления легочного рисунка справа за счет гиперемии, затемнения левого синуса, и при бронхоскопии обнаружение острого процесса в трахеи, главных, долевых и устьев сегментарных бронхов, мы можем выделить несколько главных синдромов: болевого, интоксикационного, дыхательной недостаточности и воспаления плевры. Данные объективного и лабораторно-инструментального исследований позволяют связать эти синдромы с поражением нижней доли левого легкого, характерного для пневмонии, осложненной сухим (фибринозным) плевритом. Окончательный диагноз будет звучать: «Острая левосторонняя нижнедолевая пневмония. Парапневмонический левосторонний фибринозный плеврит». Клинический диагноз: Острая левосторонняя нижнедолевая пневмония. Парапневмонический левосторонний фибринозный плеврит. ЛЕЧЕНИЕ Лечение заболевания. 1. Наибольшее значение в комплексном лечении острых пневмоний принадлежит адекватному назначению антибактериальных препаратов: антибиотиков, сульфаниламидов, препаратов нитрофуранового ряда. Основными принципами антибактериальной терапии являются раннее начало лечения, учет вида возбудителя и его чувствительности к препарату, применение адекватных доз и оптимального ритма введения, обеспечивающих лечебную концентрацию препарата в очаге поражения. До получения результатов бактериологического исследования, а также в случаях невозможности идентифицировать возбудитель антибактериальные препараты назначают с учетом характера клинической картины и тяжести заболевания.
Данные объективного и лабораторно-инструментального исследований позволяют связать эти синдромы с поражением нижней доли левого легкого, характерного для пневмонии, осложненной сухим (фибринозным) плевритом. Окончательный диагноз будет звучать: «Острая левосторонняя нижнедолевая пневмония. Парапневмонический левосторонний фибринозный плеврит». Клинический диагноз: Острая левосторонняя нижнедолевая пневмония. Парапневмонический левосторонний фибринозный плеврит. ЛЕЧЕНИЕ Лечение заболевания. 1. Наибольшее значение в комплексном лечении острых пневмоний принадлежит адекватному назначению антибактериальных препаратов: антибиотиков, сульфаниламидов, препаратов нитрофуранового ряда. Основными принципами антибактериальной терапии являются раннее начало лечения, учет вида возбудителя и его чувствительности к препарату, применение адекватных доз и оптимального ритма введения, обеспечивающих лечебную концентрацию препарата в очаге поражения. До получения результатов бактериологического исследования, а также в случаях невозможности идентифицировать возбудитель антибактериальные препараты назначают с учетом характера клинической картины и тяжести заболевания.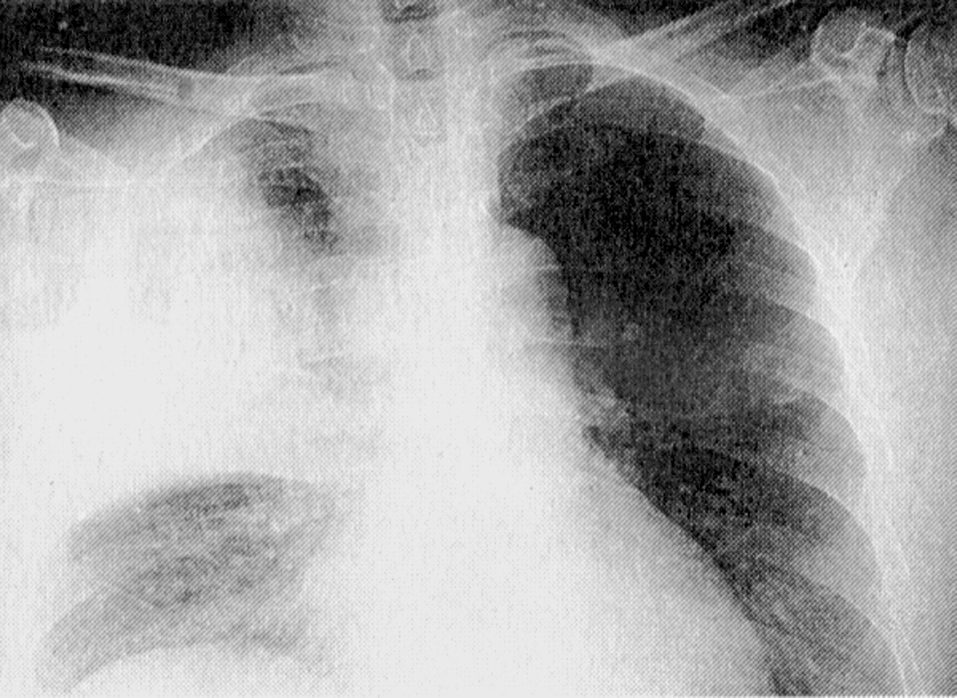 При этом применяют бактерицидные антибиотики широкого спектра действия, обычно полусинтетические пенициллины и цефалоспорины. Например: 1)Карбенициллин. Синтетический пенициллин. Обладает бактерицидным действием в отношении грамотрицательных и грамположительных микроорганизмов. Показания: инфекционные заболевания, вызванные микроорганизмами, чувствительными к этому препарату. Побочное действие: аллергические реакции. Rp.: Carbenicillini-dinatrici 1,0 D.T.D.N. 20 S. Содержимое флакона растворить в 5 мл физиологического раство- ра, вводить внутримышечно 4 раза в сутки. 2)Гентамицин. Антибиотик-аминогликозид. Обладает бактерицидным действием в отношении грамотрицательных и грамположительных микроорганизмов. Показания: инфекционные заболевания, вызванные микроорганизмами, чувствительными к этому препарату. Побочные действия: аллергические реакции, ототоксическое и нефротоксическое действие. Rp.: Sol. Gentamycini sulfatis 4%-2ml D.T.D.N. 15 S. Вводить по 2 мл внутримышечно 3 раза в сутки. 2.
При этом применяют бактерицидные антибиотики широкого спектра действия, обычно полусинтетические пенициллины и цефалоспорины. Например: 1)Карбенициллин. Синтетический пенициллин. Обладает бактерицидным действием в отношении грамотрицательных и грамположительных микроорганизмов. Показания: инфекционные заболевания, вызванные микроорганизмами, чувствительными к этому препарату. Побочное действие: аллергические реакции. Rp.: Carbenicillini-dinatrici 1,0 D.T.D.N. 20 S. Содержимое флакона растворить в 5 мл физиологического раство- ра, вводить внутримышечно 4 раза в сутки. 2)Гентамицин. Антибиотик-аминогликозид. Обладает бактерицидным действием в отношении грамотрицательных и грамположительных микроорганизмов. Показания: инфекционные заболевания, вызванные микроорганизмами, чувствительными к этому препарату. Побочные действия: аллергические реакции, ототоксическое и нефротоксическое действие. Rp.: Sol. Gentamycini sulfatis 4%-2ml D.T.D.N. 15 S. Вводить по 2 мл внутримышечно 3 раза в сутки. 2. Дезинтоксикационная терапия. Назначают: 1)Обильное питье. 2)Гемодез. Группа плазмозамещающих растворов. Механизм действия: обусловлен способностью низкомолекулярного поливинил пирролидона связывать токсины, циркулирующие в крови, и быстро выводить их из организма. Показания: для дезинтоксикации организма при токсических формах острых легочных, желудочно-кишечных заболеваний, ожоговой болезни. Побочные действия: понижение артериального давления, тахикардия, затруднение дыхания. Rp.: Sol. Haemodesi 400,0 D.T.D.N. 2 S. Вводить по 400 мл внутривенно, капельно, медленно через день. 3)Кальция глюконат. Назначаем как средство, уменьшающее проницаемость сосудов при эксудативных процессах (пневмония, выпотной плеврит) и как дезинтоксикационное средство. Побочные действия: тошнота, рвота, понос, замедление пульса. Rp.: Sol. Calcii gluconatis 10%-10ml D.T.D.N. 5 in ampull. S. Вводить по 10 мл внутри мышечно 1 раз в день-днем, через день. 4)Натрия тиосульфат. Механизм действия: оказывает противотоксическое, противовоспалительное и десинсибилизирующее действие. Показания: отравление солями тяжелых металлов, тяжелые инфекционные заболевания, кожные заболевания. Rp.: Sol. Natrii thiosulfatis 30%-10ml D.T.D.N. 5 in ampull. S. Вводить внутривенно, медленно по 10 мл 1 раз в день, через день. 5)Лазикс. (Фуросемид). Салуретик. Механизм действия: угнетение реабсорбции Na и Cl в роксимальных, дистальных извитых канальцах и в области восходящего отдела петли Генле. Показания: усиление диуреза и выведения токсических продуктов. Побочные действия: тошнота, понос, гиперемия кожи, зуд, гипотензия, интерстициальный нефрит. Rp.: Sol. «Lasix» (20mg) D.T.D.N. 3 in ampull. S. Вводить по 20 мг внутривенно 1 раз в день, через день. 3. Назначение витаминотерапии. Лечение симптоматическое или назначение поливитаминов. 4. Назначение анальгетиков для купирования болевого синдрома. 1)Анальгин. Ненаркотический анальгетик. Обладает выраженным анальгезирующим, ражопонижающим и противоваспалительным действием. Показания: боли различного происхождения. Побочные действия: угнетение кроветворения и аллергические реакции. Rp.: Sol. Analgini 50%-2ml D.T.D.N. 5 in ampull. S. Вводить внутримышечно по 2 мл по необходимости. 2)Для потенцирования действия анальгина применяем димедрол. Антигистаминный препарат. Механизм действия: блокирует Н1-рецепторы, расслабляет гладкую мускулатуру, обладает седативным действием. Показание: успокаивающее и снотворное действие. Побочные действия: сонливость и общая слабость. Rp.: Sol. Dimedroli 1%-1ml D.T.D.N. 5 in ampull. S. По 1 мл внутримышечно при необходимости. 5. Борьба с дыхательной недостаточностью. Препаратом выбора является эуфиллин. Эуфиллин. Спазмолитик. Механизм действия: расслабляет мышцы бронхов, понижает сопротивление кровеносных сосудов, понижает давление в системе легочной артерии, увеличивает почечный кровоток, оказывает диуретическое действие. Показания: гипертензия в малом круге кровообращения. Побочные явления: дерматит, лихорадочная реакция. Rp.: Sol. Euphyllini 2,4%-10ml D.T.D.N. 2 in ampull. S. Вводить внутривенно, капельно по 10 мл, предварительно развес- ти в 200 мл физиологического раствора. 6. Улучшение дренажной функции и бронхиальной проходимости достигается назначением отхаркивающих (йодид калия, мукалтин, бромгексин, термопсис), бронхолитических средств, ферментных препаратов (трипсина, химотрипсина, рибонуклеазы, камфоры). Бромгексин. Муколитик. Механизм действия: муколитический эффект связан с деполимеризацией и разжижением мукопротеиновых и мукополисахаридных волокон, стимулирует образование сурфактанта. Показания: бронхиты, пневмонии, бронхиальная астма, туберкулез легких. Побочные действия: аллергические реакции, диспепсические расстройства. Rp.: Tab. Bromhexini 0,008 D.T.D.N. 40 S. По 2 таблетки 3 раза в день. 7. Для ускорения рассасывания воспалительного процесса, улучшения дренажной функции, уменьшение вязкости мокроты назначают физиотерапевтическое лечение: ингаляции щелочей, бронхолитиков, отхаркивающих, электрофорез хлорида кальция, аскорбиновой кислоты, цинка, йода, гепарина, лидазы, УВЧ-терапия, микроволновая терапия, иглоукалывание, массаж грудной клетки, ЛФК, ПУФ носовых ходов. Лечение больного. 1. Назначаем диету № 15, режим 1. Усиление голосового дрожания и ослабления дыхания, наличие крепитации слева в подлопаточной области. Притупление перкуторного звука тамже. Живот мягкий, безболезненный. Симптом поколачивания по поясничной области отрицательный. Стул и диурез в норме. 17.10.96 36,7-36,4° С Жалобы на сухой кашель. Сознание ясное. Самочувствие удовлетворительное. Кожные покровы телесного цвета. Слизистые розовые, влажные, чистые. Пульс 70 уд/мин. АД 100/60 мм.рт.ст. Тоны сердца ясные, звучные, ритмичные. Обе половины грудной клетки одинаково участвуют в акте дыхания. Дыхание жесткое. Крепитация слева в подлопаточной области. Живот мягкий, безболезненный. Физиологические отправления в норме. Те же. Анальгин и димедрол по необходимости. 18.10.96 36,0-36,6° С Жалобы на сухой кашель. Сознание ясное. Самочувствие удовлетворительное. Кожные покровы телесного цвета. Слизистые розовые, влажные, чистые. Пульс 70 уд/мин. АД 100/60 мм.рт.ст. Тоны сердца ясные, звучные, ритмичные. Обе половины грудной клетки одинаково участвуют в акте дыхания. Дыхание жесткое. Крепитация слева в подлопаточной области. Живот мягкий, безболезненный. Физиологические отправления в норме. Те же + УВЧ-терапия грудной клетки слева, электрофорез цинка и йода в грудную клетку. 19.10.96 36,5-36,6° С Жалоб нет. Самочувствие удовлетворительное. Сознание ясное. Кожные покровы и видимые слизистые без видимых изменений. Пульс 66 уд/мин. АД 110/70 мм.рт.ст. Тоны сердца ясные, звучные, ритмичные. Дыхание везикулярное. Крепитация слева в подлопаточной области. Живот мягкий, безболезненный. Стул и диурез не изменен. Те же+ массаж грудной клетки, ПУФ носовых ходов. ПРОГНОЗ Прогноз для жизни благоприятный. Возможно полное выздоровление при адекватном лечении и проведении соответствующей реабилитации. Также возможно полное восстановление работоспособности. ПРОФИЛАКТИКА Профилактика только не специфическая — 1) проведение профилактических осмотров для выявления очагов хронической инфекции; 2) санация полости рта и зева; 3) оздоровление санитарных условий в учебных и рабочих помещениях, борьба с запыленностью воздуха; 4) своевременность и широкое проведение профилактических прививок; 5) борьба с курением и алкоголизмом; 6) закаливание организма; 7) широкая санитарно- просветительная работа среди населения. ЭПИКРИЗ Больная поступила в больницу 5 октября 1996 года с жалобами на постоянные колюще-режущие боли в левой половине грудной клетки, интенсивные, усиливающиеся при глубоком дыхании и кашле, уменьшающиеся при сдавлении левой половины грудной клетки, на кашель с выделением мокроты с прожилками крови, на слабость, одышку, тошноту и ознобы. За время пребывания в больнице больная была осмотрена и ей были проведены лабораторно-инструментальные исследования: клинический анализ крови, биохимический анализ крови, анализ мочи, микроскопическое исследование мокроты, рентгенография грудной клетки в трех проекциях, бронхоскопия. При этом было выявлено отставание левой половины грудной клетки в акте дыхания, усиление голосового дрожания, ослабление дыхания, наличие влажных мелкопузырчатых хрипов и шума трения плевры слева в подлопаточной области, уменьшение подвижности нижнего легочного края левого легкого, жесткое дыхание, притупление перкуторного звука слева в подлопаточной области; лейкоцитоз с нейтрофилёзом, повышенная СОЭ; в мокроте большое количество лейкоцитов, эритроцитов, альвеолярных макрофагов; при рентгенологическом исследовании — тотальная пневмоническая инфильтрация нижней доли левого легкого, реактивное сужение корней легких усиление легочного рисунка справа за счет гиперемии, наличии жидкости в левом синусе; наличие острого процесса в дренажной системе легких при бронхоскопии. Данные исследований позволили поставить диагноз: «Острая левосторонняя нижнедолевая пневмония. Парапневмонический левосторонний фибринозный плеврит». Проводилось лечение: медикоментозное (бромгексин, карбинициллин, гемодез, гентамицин, кальция глюконат, натрия тиосульфат, эуфиллин) и физиотерапия (УВЧ-терапия, электрофорез цинка и йода в грудную клетку, массаж грудной клетки, ПУФ носовых ходов). Самочувствие больной улучшилось: перестали беспокоить боли, прошла слабость, одышка, перестала выделяться мокрота. Для полного выздоровления показано курортно-санаторное лечение.
Дезинтоксикационная терапия. Назначают: 1)Обильное питье. 2)Гемодез. Группа плазмозамещающих растворов. Механизм действия: обусловлен способностью низкомолекулярного поливинил пирролидона связывать токсины, циркулирующие в крови, и быстро выводить их из организма. Показания: для дезинтоксикации организма при токсических формах острых легочных, желудочно-кишечных заболеваний, ожоговой болезни. Побочные действия: понижение артериального давления, тахикардия, затруднение дыхания. Rp.: Sol. Haemodesi 400,0 D.T.D.N. 2 S. Вводить по 400 мл внутривенно, капельно, медленно через день. 3)Кальция глюконат. Назначаем как средство, уменьшающее проницаемость сосудов при эксудативных процессах (пневмония, выпотной плеврит) и как дезинтоксикационное средство. Побочные действия: тошнота, рвота, понос, замедление пульса. Rp.: Sol. Calcii gluconatis 10%-10ml D.T.D.N. 5 in ampull. S. Вводить по 10 мл внутри мышечно 1 раз в день-днем, через день. 4)Натрия тиосульфат. Механизм действия: оказывает противотоксическое, противовоспалительное и десинсибилизирующее действие. Показания: отравление солями тяжелых металлов, тяжелые инфекционные заболевания, кожные заболевания. Rp.: Sol. Natrii thiosulfatis 30%-10ml D.T.D.N. 5 in ampull. S. Вводить внутривенно, медленно по 10 мл 1 раз в день, через день. 5)Лазикс. (Фуросемид). Салуретик. Механизм действия: угнетение реабсорбции Na и Cl в роксимальных, дистальных извитых канальцах и в области восходящего отдела петли Генле. Показания: усиление диуреза и выведения токсических продуктов. Побочные действия: тошнота, понос, гиперемия кожи, зуд, гипотензия, интерстициальный нефрит. Rp.: Sol. «Lasix» (20mg) D.T.D.N. 3 in ampull. S. Вводить по 20 мг внутривенно 1 раз в день, через день. 3. Назначение витаминотерапии. Лечение симптоматическое или назначение поливитаминов. 4. Назначение анальгетиков для купирования болевого синдрома. 1)Анальгин. Ненаркотический анальгетик. Обладает выраженным анальгезирующим, ражопонижающим и противоваспалительным действием. Показания: боли различного происхождения. Побочные действия: угнетение кроветворения и аллергические реакции. Rp.: Sol. Analgini 50%-2ml D.T.D.N. 5 in ampull. S. Вводить внутримышечно по 2 мл по необходимости. 2)Для потенцирования действия анальгина применяем димедрол. Антигистаминный препарат. Механизм действия: блокирует Н1-рецепторы, расслабляет гладкую мускулатуру, обладает седативным действием. Показание: успокаивающее и снотворное действие. Побочные действия: сонливость и общая слабость. Rp.: Sol. Dimedroli 1%-1ml D.T.D.N. 5 in ampull. S. По 1 мл внутримышечно при необходимости. 5. Борьба с дыхательной недостаточностью. Препаратом выбора является эуфиллин. Эуфиллин. Спазмолитик. Механизм действия: расслабляет мышцы бронхов, понижает сопротивление кровеносных сосудов, понижает давление в системе легочной артерии, увеличивает почечный кровоток, оказывает диуретическое действие. Показания: гипертензия в малом круге кровообращения. Побочные явления: дерматит, лихорадочная реакция. Rp.: Sol. Euphyllini 2,4%-10ml D.T.D.N. 2 in ampull. S. Вводить внутривенно, капельно по 10 мл, предварительно развес- ти в 200 мл физиологического раствора. 6. Улучшение дренажной функции и бронхиальной проходимости достигается назначением отхаркивающих (йодид калия, мукалтин, бромгексин, термопсис), бронхолитических средств, ферментных препаратов (трипсина, химотрипсина, рибонуклеазы, камфоры). Бромгексин. Муколитик. Механизм действия: муколитический эффект связан с деполимеризацией и разжижением мукопротеиновых и мукополисахаридных волокон, стимулирует образование сурфактанта. Показания: бронхиты, пневмонии, бронхиальная астма, туберкулез легких. Побочные действия: аллергические реакции, диспепсические расстройства. Rp.: Tab. Bromhexini 0,008 D.T.D.N. 40 S. По 2 таблетки 3 раза в день. 7. Для ускорения рассасывания воспалительного процесса, улучшения дренажной функции, уменьшение вязкости мокроты назначают физиотерапевтическое лечение: ингаляции щелочей, бронхолитиков, отхаркивающих, электрофорез хлорида кальция, аскорбиновой кислоты, цинка, йода, гепарина, лидазы, УВЧ-терапия, микроволновая терапия, иглоукалывание, массаж грудной клетки, ЛФК, ПУФ носовых ходов. Лечение больного. 1. Назначаем диету № 15, режим 1. Усиление голосового дрожания и ослабления дыхания, наличие крепитации слева в подлопаточной области. Притупление перкуторного звука тамже. Живот мягкий, безболезненный. Симптом поколачивания по поясничной области отрицательный. Стул и диурез в норме. 17.10.96 36,7-36,4° С Жалобы на сухой кашель. Сознание ясное. Самочувствие удовлетворительное. Кожные покровы телесного цвета. Слизистые розовые, влажные, чистые. Пульс 70 уд/мин. АД 100/60 мм.рт.ст. Тоны сердца ясные, звучные, ритмичные. Обе половины грудной клетки одинаково участвуют в акте дыхания. Дыхание жесткое. Крепитация слева в подлопаточной области. Живот мягкий, безболезненный. Физиологические отправления в норме. Те же. Анальгин и димедрол по необходимости. 18.10.96 36,0-36,6° С Жалобы на сухой кашель. Сознание ясное. Самочувствие удовлетворительное. Кожные покровы телесного цвета. Слизистые розовые, влажные, чистые. Пульс 70 уд/мин. АД 100/60 мм.рт.ст. Тоны сердца ясные, звучные, ритмичные. Обе половины грудной клетки одинаково участвуют в акте дыхания. Дыхание жесткое. Крепитация слева в подлопаточной области. Живот мягкий, безболезненный. Физиологические отправления в норме. Те же + УВЧ-терапия грудной клетки слева, электрофорез цинка и йода в грудную клетку. 19.10.96 36,5-36,6° С Жалоб нет. Самочувствие удовлетворительное. Сознание ясное. Кожные покровы и видимые слизистые без видимых изменений. Пульс 66 уд/мин. АД 110/70 мм.рт.ст. Тоны сердца ясные, звучные, ритмичные. Дыхание везикулярное. Крепитация слева в подлопаточной области. Живот мягкий, безболезненный. Стул и диурез не изменен. Те же+ массаж грудной клетки, ПУФ носовых ходов. ПРОГНОЗ Прогноз для жизни благоприятный. Возможно полное выздоровление при адекватном лечении и проведении соответствующей реабилитации. Также возможно полное восстановление работоспособности. ПРОФИЛАКТИКА Профилактика только не специфическая — 1) проведение профилактических осмотров для выявления очагов хронической инфекции; 2) санация полости рта и зева; 3) оздоровление санитарных условий в учебных и рабочих помещениях, борьба с запыленностью воздуха; 4) своевременность и широкое проведение профилактических прививок; 5) борьба с курением и алкоголизмом; 6) закаливание организма; 7) широкая санитарно- просветительная работа среди населения. ЭПИКРИЗ Больная поступила в больницу 5 октября 1996 года с жалобами на постоянные колюще-режущие боли в левой половине грудной клетки, интенсивные, усиливающиеся при глубоком дыхании и кашле, уменьшающиеся при сдавлении левой половины грудной клетки, на кашель с выделением мокроты с прожилками крови, на слабость, одышку, тошноту и ознобы. За время пребывания в больнице больная была осмотрена и ей были проведены лабораторно-инструментальные исследования: клинический анализ крови, биохимический анализ крови, анализ мочи, микроскопическое исследование мокроты, рентгенография грудной клетки в трех проекциях, бронхоскопия. При этом было выявлено отставание левой половины грудной клетки в акте дыхания, усиление голосового дрожания, ослабление дыхания, наличие влажных мелкопузырчатых хрипов и шума трения плевры слева в подлопаточной области, уменьшение подвижности нижнего легочного края левого легкого, жесткое дыхание, притупление перкуторного звука слева в подлопаточной области; лейкоцитоз с нейтрофилёзом, повышенная СОЭ; в мокроте большое количество лейкоцитов, эритроцитов, альвеолярных макрофагов; при рентгенологическом исследовании — тотальная пневмоническая инфильтрация нижней доли левого легкого, реактивное сужение корней легких усиление легочного рисунка справа за счет гиперемии, наличии жидкости в левом синусе; наличие острого процесса в дренажной системе легких при бронхоскопии. Данные исследований позволили поставить диагноз: «Острая левосторонняя нижнедолевая пневмония. Парапневмонический левосторонний фибринозный плеврит». Проводилось лечение: медикоментозное (бромгексин, карбинициллин, гемодез, гентамицин, кальция глюконат, натрия тиосульфат, эуфиллин) и физиотерапия (УВЧ-терапия, электрофорез цинка и йода в грудную клетку, массаж грудной клетки, ПУФ носовых ходов). Самочувствие больной улучшилось: перестали беспокоить боли, прошла слабость, одышка, перестала выделяться мокрота. Для полного выздоровления показано курортно-санаторное лечение.
Левосторонняя нижнедолевая пневмония: симптомы и терапия
Часто после посещения врача пациенты слышат диагноз — левосторонняя нижнедолевая пневмония. Недуг этот достаточно распространен и при правильном лечении не влечет за собой опасных последствий. Тем не менее, его важно вовремя диагностировать и составить верную схему лечения. Так каковы причины пневмонии? На какие симптомы стоит обратить внимание больному человеку? Можно ли как-то предупредить развитие недуга?
Что представляет собой недуг?
Для начала стоит разобраться со значением термина «левосторонняя нижнедолевая пневмония». Как известно, левое легкое состоит из двух долей, а правое — из трех. А еще каждое легкое делится на десять сегментов.
Пневмонией называют заболевание, сопровождающееся воспалением легких. Воспалительный процесс может быть односторонним (лево- или правостороннее) или двухсторонним. В зависимости от локации пневмония может быть тотальной (поражено все легкое), очаговой (есть лишь один или несколько небольших очагов воспаления), долевой (поражена определенная доля легкого) и сегментарной (воспалительный процесс ограничен одним или некоторыми сегментами). Иногда можно услышать термин «внелегочная левосторонняя нижнедолевая пневмония» — как правило, это значит, что первичный источник инфекции располагается в других органах, например, в плевральной полости.
Стоит сказать, что смертность среди пациентов составляет около 5%. Дело в том, что левосторонняя нижнедолевая/очаговая пневмония на первых этапах может протекать скрыто — пациенты обращаются за помощью слишком поздно. А еще высока вероятность распространения воспалительного процесса на сердце.
Стоит сказать, что воспаление может иметь разную степень тяжести. Есть и другая схема классификации — существует внегоспитальная левосторонняя нижнедолевая пневмония (заражение пациента происходит воздушно-капельным путем вне стен больницы) и нозокомиальное, или внутрибольничное воспаление, при котором недуг развился у пациента во время пребывания в стационаре.
Основные причины развития пневмонии
Воспалительный процесс развивается в результате попадания в организм патогенных микроорганизмов. В роли возбудителей могут выступать бактерии, вирусы, грибковые организмы. Они могут попадать из внешней среды, так как инфекции передаются воздушно-капельным путем.
Естественно, далеко не всегда проникновение патогена в дыхательную систему ведет к воспалению. К факторам риска относят курение, ослабление иммунной системы, наличие у пациента хронических заболеваний — все это повышает вероятность развития пневмонии. В некоторых случаях инфекция попадает в легкие вместе с током крови из другого очага воспаления в организме.
История болезни: левосторонняя нижнедолевая пневмония и ее признаки
На начальных этапах данная форма воспаления может и вовсе протекать бессимптомно. Пациенты отмечают лишь постоянную слабость и усталость, сонливость, снижение работоспособности. В дальнейшем ситуация усугубляется. Появляется кашель. Иногда он сухой, но чаще всего сопровождается выделением мокроты. По мере развития заболевания мокрота становится обильной, иногда в ней можно заметить прожилки крови.
Пациенты жалуются на боли в груди, особенно с левой стороны (в области сердца). Болезненность усиливается при кашле и глубоком вдохе. Из-за недостатка кислорода у больных нередко отмечается синюшность губ и общая бледность.
Температура постоянно нарастает, нередко поднимаясь до 40 градусов. У пациентов присутствуют и общие симптомы интоксикации, включая ломоту в теле, сильный озноб, тошноту и отсутствие аппетита, рвоту, сильные головные боли, нередко даже потерю сознания. Разумеется, у каждого пациента присутствует разный набор симптомов, причем в разной степени выраженности. Нередко симптомы левосторонней нижнедолевой пневмонии путают с обычным фарингитом или простудой, особенно если речь идет о маленьких детях. В этом и кроется опасность воспаления легких.
Особенности симптоматики в зависимости от возбудителя
Как уже упоминалось, левосторонняя нижнедолевая пневмония может развиваться на фоне активности вирусов или бактерий. Вышеописанные симптомы присутствуют практически при любой форме воспаления легких, но каждый возбудитель имеет некоторые особенности.
Например, вирусная пневмония сопровождается сухим кашлем и постоянной одышкой. Пациенты жалуются на быстрое утомление, лихорадку и сильную слабость в мышцах. А вот при бактериальной форме температуре тела не такая высокая, хотя жар, разумеется, присутствует. У человека можно заметить сильный мокрый кашель, сопровождающийся выделением мокроты.
Современные методы диагностики
Правильная и своевременная диагностика очень важна. При появлении первых же симптомов стоит обратиться к врачу, ведь, несмотря на существование мощных антибактериальных препаратов, воспаление легких все еще может иметь летальный исход:
- Пациент обязательно должен сдать кровь на анализ — при исследовании можно заметить повышение скорости оседания эритроцитов, а также увеличение количества лейкоцитов, что свидетельствует о воспалительном процессе.
- Проводится биохимический анализ образцов крови, а также исследование мокроты для обнаружения возбудителя.
- Важна для диагностики и рентгенография грудной клетки, которая дает возможность выявить очаги воспаления.
- В некоторых случаях проводится фибробронхоскопия, которая позволяет осмотреть бронхи пациента изнутри.
Левосторонняя нижнедолевая пневмония: лечение препаратами
Сразу стоит сказать, что заниматься самолечением в данном случае опасно. Только врач может составить эффективную схему терапии. При подозрении на бактериальную пневмонию пациенту сначала назначают антибиотики широкого спектра воздействия, в частности, фторхинолоны и цефалоспорины третьего или четвертого поколения.
За это время проводятся специфические анализы, цель которых — точно определить возбудителя. Если пневмония развилась на фоне инвазии легионеллой, пневмококком, хламидиями, гемофильной палочкой и микоплазмами, врач может назначить более эффективные антибактериальные препараты узкого спектра. Но на анализы нужно хотя бы 3-4 дня, а при воспалении легких нужно действовать быстро.
При вирусной пневмонии врачи назначают противовирусные препараты, в частности, «Занамивир», «Ремантадин», «Ацикловир». К сожалению, лекарства эффективны только в том случае, если принять их в первые 48 часов после заражения. В других же случаях больного госпитализируют и проводят симптоматическое лечение. Антибиотики при вирусном поражении бесполезны, но их все равно назначают для профилактики вторичных бактериальных осложнений.
В качестве вспомогательных средств используются нестероидные противовоспалительные средства, которые помогают устранить лихорадку и болезненность. Терапия длится около 2-4 недель в зависимости от степени тяжести недуга.
Правильный уход за пациентом
Пневмония — тяжелое заболевание, при котором больному человеку нужен тщательный уход. Пациентам показан постельный режим, минимум физической активности и отсутствие стрессов. Человеку лучше находиться в тщательно проветриваемом помещении, где регулярно проводят влажную уборку. Если лечение проходить на дому, больному нужно выделить отдельный набор посуды, чтобы предотвратить распространение инфекции.
Обильное теплое питье при воспалении обязательно, так как это помогает ускорить выведение токсинов из организма и предотвратить развитие обезвоживания. Есть пациентам нужно легкую, но высококалорийную пищу.
Когда пациенту необходима госпитализация?
Довольно часто левосторонняя нижнедолевая пневмония лечится амбулаторно, в домашних условиях. В каких случаях необходима терапия в стационарных условиях?
- Все дети возрастом до трех лет обязательно должны быть госпитализированы.
- Пациента нужно отправить в больницу при наличии сильной одышки, жаре (до 39,9 градусов) или, наоборот, снижении температуры до 35,5.
- Если во время анализов было обнаружено сильное снижение уровня гемоглобина, а также повышение уровня мочевины и креатинина, лечение лучше проводить в условиях стационара.
- Показаниями к госпитализации являются нарушение сознания, резкое снижение артериального давления.
- При появлении осложнений (включая плеврит, миокардит, артрит) пациента нужно немедленно доставить в больницу.
Профилактические мероприятия
Острая левосторонняя нижнедолевая пневмония — опасный недуг, который при отсутствии терапии приводит к опасным осложнениям, включая отек легких, шок, сепсис, менингит и перикардит, острую сердечную недостаточность.
К сожалению, вакцины от воспаления легких не существует. Поэтому единственной профилактикой является здоровый образ жизни. Правильное питание, постепенное закаливание организма, прогулки на свежем воздухе, отказ от курения и употребления спиртных напитков, регулярные физические нагрузки — все это укрепляет организм, делая его более устойчивым к патогенным микроорганизмам.
Все инфекционные и воспалительные заболевания обязательно должны поддаваться адекватному лечению, причем терапия должна длиться до полного выздоровления. Для укрепления иммунитета рекомендуется дважды в год проходить курс витаминотерапии. И, конечно, при первых же ухудшениях самочувствия стоит обратиться к специалисту, ведь у вас может быть внебольничная левосторонняя нижнедолевая пневмония.
Левосторонняя пневмония: причины, симптомы, лечение
Левосторонняя пневмония – представляет собой самую редкую форму развития инфекционного процесса в лёгких из двух существующих разновидностей. Несмотря на это, болезнь представляет большую угрозу для жизни пациента. Основной причиной развития заболевания выступает патологическое влияние болезнетворных микроорганизмов, которые проникают в левое лёгкое крайне редко и зачастую при сильном ослаблении иммунитета. Помимо этого, врачи выделяют большое количество предрасполагающих факторов.
Не занимайтесь самолечением. При первых признаках заболевания обращайтесь к врачу.
Клинические признаки поражения левого лёгкого практически ничем не отличаются от воспаления правой доли. Наиболее характерными проявлениями принято считать значительное повышение температуры, сильный кашель, жжение и боли в левой части грудной клетки.
Диагноз левосторонняя пневмония устанавливается на основании результатов инструментальных обследований, которые будут дополняться лабораторными исследованиями и физикальным осмотром.
Лечение зачастую консервативное, однако при тяжёлом протекании или развитии осложнений потребует проведения хирургического вмешательства.
Подобная разновидность очаговой пневмонии передаётся от больного человека к здоровому воздушно-капельным путём. Зачастую происходит это во время чихания, потому что из дыхательных путей выделяются болезнетворные агенты, которые совместно с частичками жидкости проникают в лёгкие окружающих.
При слабой иммунной системе такие бактерии начинают активно увеличивать свою численность, отчего возникает местный воспалительный процесс в лёгочной ткани. Примечательно то, что левое лёгкое поражается намного реже правого сегмента, что обуславливается спецификой общего кровотока и строения этого органа.
Наиболее часто в качестве возбудителей выступают:
Также довольно часто левостороння пневмония у ребёнка или взрослого выступает в качестве осложнения не полностью вылеченного заболевания вирусного или острого респираторного характера. Среди таких патологий стоит выделить:
Помимо этого, предрасполагающими факторами приято считать:
- длительное переохлаждение организма;
- протекание сахарного диабета или хронических заболеваний лёгких;
- наличие сердечной недостаточности;
- малоподвижный образ жизни, в частности, соблюдение длительного постельного режима;
- многолетнее пристрастие к вредным привычкам, в особенности к распитию алкогольных напитков;
- перенесённые ранее хирургические операции – примечательно то, что вовсе не обязательно, чтобы вмешательство проводилось в области грудной клетки. Воспаление лёгких – это одно из самых распространённых последствий любой операбельной терапии.
Все вышеуказанные факторы приводят к тому, что у человека понижается сопротивляемость иммунной системы. Стоит отметить, что основную группу риска составляют дети и люди преклонного возраста.
Воспаление лёгочной ткани при левосторонней пневмонии может протекать в нескольких формах:
- типичной – характеризуется заражением одним из вышеуказанных болезнетворных микроорганизмов;
- атипичной – развивается на фоне проникновения специфических инфекционных агентов, к которым стоит отнести – пневмоцитов, микоплазму, хламидии и легионеллу;
- аспирационной – воспаление формируется в тех случаях, когда в дыхательные пути попадают посторонние предметы, рвотные массы или частички пищи.
В зависимости от того, где произошло инфицирование, недуг делится на две формы:
- внутрибольничная левосторонняя пневмония – исходя из названия, становится понятно, что заражение произошло в медицинском учреждении. При этом воспалительный процесс может возникнуть у пациентов в первые несколько суток нахождения в условиях стационара, у больных, которым необходима искусственная вентиляция лёгких или у лиц, перенёсших пересадку донорского органа;
- внебольничная левосторонняя пневмония – это означает, что заражение произошло за пределами больницы.
Отдельно выделяют левостороннюю пневмонию, связанную с оказанием медицинской помощи.
В зависимости от особенностей клинической картины различают несколько разновидностей болезни:
- левосторонняя верхнедолевая пневмония;
- левосторонняя центральная пневмония;
- левосторонняя нижнедолевая пневмония.
Несмотря на наличие таких типов недуга, зачастую диагностируется полисегментарная пневмония.
Помимо этого, специалисты из области пульмонологии выделяют крупозную и плевропневмонию.
По характеру протекания левосторонняя полисегментарная пневмония бывает:
- хронической;
- затяжной;
- острой.
В зависимости от механизма развития подобная патология делится на:
- первичную – выступает в качестве самостоятельного недуга;
- вторичную – является осложнением сопутствующих заболеваний;
- посттравматическую;
- послеоперационную;
- инфаркт-пневмонию.
Поскольку в подавляющем большинстве случаев воспаление лёгких обуславливается патологическим влиянием инфекционных агентов, то стоит отметить, что продолжительность инкубационного периода при типичной форме будет продолжаться до трёх суток, а при атипичном течении – до трёх недель.
Наиболее часто встречается острая левосторонняя полисегментарная пневмония, для которой характерно постепенное развитие.
Первыми признаками воспалительного процесса в левом лёгком выступают:
- постоянный кашель без мокроты;
- возрастание температуры до 39 градусов;
- продолжительность лихорадки более трёх суток.
Если при выражении таких клинических проявлений обратиться за квалифицированной помощью, то можно избежать развития осложнений.
Симптомы пневмонии
По мере прогрессирования недуга, помимо вышеуказанной симптоматики появятся следующие симптомы:
- повышенное потоотделение, особенно в ночное время суток;
- слабость и разбитость;
- мышечные и суставные боли;
- учащённое дыхание;
- боли и першение в горле;
- сильные болевые ощущения в груди с левой стороны;
- приступы тошноты и рвоты;
- головные боли и головокружение;
- стильная одышка даже в состоянии покоя;
- выделение мокроты с кашлем.
Стоит отметить, что у детей недуг протекает сложнее, нежели сегментарная пневмония у взрослых. В таких случаях специфическими признаками будут служить:
- патологический румянец на лице ребёнка;
- нездоровый блеск в глазах;
- спутанность сознания;
- синюшность губ и ногтевых пластин;
- полное отсутствие аппетита;
- понижение физической активности;
- интенсивные боли в грудине, усиливающиеся во время дыхания.
Кроме этого, клиническую картину будут дополнять проявления того недуга, на фоне которого мог сформироваться воспалительный процесс верхней, центральной или нижней доли левого лёгкого.
Опасность левосторонней очаговой пневмонии заключается в том, что левое лёгкое и бронх расположен близко к сердцу. Именно по этой причине при появлении одного или нескольких из вышеуказанных симптомов необходимо как можно скорее пройти обследование у врача и начать лечение.
Чтобы поставить правильный диагноз, пульмонологу необходимы результаты лабораторно-инструментальных обследований, однако диагностика не ограничивается лишь такими мероприятиями.
Прежде всего, клиницисту необходимо:
- ознакомится с историей болезни и жизненным анамнезом пациента – для выяснения болезни-провокатора левосторонней полисегментарной пневмонии;
- провести тщательный физикальный осмотр грудной клетки и прослушать лёгкие при помощи специального инструмента – фонендоскопа;
- детально опросить пациента на предмет того, когда появились и с какой интенсивностью выражаются симптомы воспаления.
Лабораторная диагностика ограничивается осуществлением:
- общеклинического анализа крови;
- биохимии крови;
- бактериального посева крови;
- анализом мокроты, выделяемой при кашле.
Однако наибольшей диагностической ценностью обладают следующие инструментальные обследования:
- рентгенография грудины;
- фибробронхоскопия;
- эхокардиография;
- УЗИ плевральной полости;
- КТ органов грудной полости.
Рентгенограмма левосторонней пневмонии
Левосторонняя очаговая пневмония должна быть дифференцирована с воспалением правого лёгкого.
После уточнения диагноза пациента немедленно госпитализируют в отделение пульмонологии. Прежде всего, показано медикаментозное лечение левосторонней пневмонии, которое включает в себя приём:
- антибактериальных средств – это основные лекарства, используемые при терапии подобного недуга;
- отхаркивающих веществ;
- дезинтоксикационных медикаментов;
- глюкокортикостероидов;
- иммуномодуляторов;
- жаропонижающих и других препаратов, направленных на устранение симптоматики.
При тяжёлом течении полисегментарной пневмонии у детей и взрослых обращаются к кислородотерапии и искусственной вентиляции лёгких.
Хирургическое вмешательство необходимо при неэффективности консервативных методик терапии или в случаях развития осложнений.
Игнорирование симптомов или неадекватное лечение может повлечь за собой развитие как лёгочных, так и внелегочных последствий. Первая категория включает в себя:
Внелегочные осложнения представлены:
Все вышеуказанные осложнения относят как к взрослым, так и к детям.
Специфические профилактические мероприятия против левосторонней очаговой пневмонии представлены иммунизацией – введением вакцин против возбудителей подобного заболевания.
Общая профилактика воспаления левого лёгкого заключается в соблюдении таких правил:
- ведение здорового и в меру активного образа жизни;
- избегание переохлаждения организма;
- укрепление иммунитета;
- своевременное лечение патологий, которые могут привести к развитию левосторонней пневмонии;
- регулярное прохождение полного медицинского обследования.
В 70% случаев ранняя диагностика и комплексное лечение позволяют достичь полного выздоровления. Менее благоприятный прогноз наблюдается при появлении воспаления лёгких на фоне иного заболевания. В таких ситуациях высока вероятность возникновения осложнений болезни-провокатора. Летальность среди детей варьируется от 10 до 30%.
Бактериальная пневмония: основы практики, история вопроса, патофизиология
Claudius I, Baraff LJ. Неотложные педиатрические ситуации, связанные с лихорадкой. Emerg Med Clin North Am . 2010 февраля, 28 (1): 67-84, vii-viii. [Медлайн].
Хуссейн А.Н., Кумар В. Легкое. В: Кумар В., Аббас А.К., Фаусто Н., ред. Роббинс и Котран: патологические основы болезни . 7-е изд. Филадельфия, Пенсильвания: Эльзевьер Сондерс; 2005. 711-72.
[Рекомендации] Манделл Л.А., Вундеринк Р.Г., Анзуето А., Бартлетт Дж. Г., Кэмпбелл Г. Д., Дин Н. С. и др.Общество инфекционных болезней Америки / Американское торакальное общество согласовали руководящие принципы ведения внебольничной пневмонии у взрослых. Clin Infect Dis . 2007 г. 1. 44 Приложение 2: S27-72. [Медлайн].
Медицинский словарь Стедмана . 27-е изд. Балтимор, Мэриленд: Липпинкотт, Уильямс и Уилкинс; 2003.
Brundage JF, Хвостовик GD. Смертность от бактериальной пневмонии во время пандемии гриппа 1918-19 гг. Emerg Infect Dis .2008 14 августа (8): 1193-9. [Медлайн]. [Полный текст].
Ананд Н., Коллеф М.Х. Алфавитный указатель пневмонии: CAP, HAP, HCAP, NHAP и VAP. Semin Respir Crit Care Med . 2009 30 февраля (1): 3-9. [Медлайн].
Эль Солх AA. Пневмония, приобретенная в домах престарелых. Semin Respir Crit Care Med . 2009 30 февраля (1): 16-25. [Медлайн].
Kuti JL, Shore E, Palter M, Nicolau DP. Проведение эмпирической антибактериальной терапии респираторно-ассоциированной пневмонии в отделении интенсивной терапии: руководство по применению рекомендаций. Semin Respir Crit Care Med . 2009 30 февраля (1): 102-15. [Медлайн].
Чако Р., Раджан А., Лайонел П., Тилагавати М., Ядав Б., Премкумар Дж. Методы деконтаминации полости рта и пневмония, связанная с вентилятором. Br J Nurs . 2017 июн 8. 26 (11): 594-599. [Медлайн].
Bouglé A, Foucrier A, Dupont H, Montravers P, Ouattara A, Kalfon P и др. Влияние продолжительности приема антибиотиков на клинические явления у пациентов с вентилятор-ассоциированной пневмонией, вызванной Pseudomonas aeruginosa: протокол рандомизированного контролируемого исследования. Испытания . 2017 23 января. 18 (1): 37. [Медлайн]. [Полный текст].
Kollef MH, Ricard JD, Roux D и др. Рандомизированное испытание системы ингаляции амикацина фосфомицина для дополнительной терапии грамотрицательной пневмонии, связанной с вентилятором: испытание IASIS. Сундук . 2017 июнь 151 (6): 1239-1246. [Медлайн].
Kalil AC, Metersky ML, Klompas M, Muscedere J, Sweeney DA, Palmer LB и др. Краткое содержание: Ведение взрослых с внутрибольничной пневмонией и пневмонией, связанной с искусственной вентиляцией легких: Руководство по клинической практике, 2016 г., Американское общество инфекционных болезней и Американское торакальное общество. Clin Infect Dis . 2016 Сентябрь 1. 63 (5): 575-82. [Медлайн].
Чалмерс Дж. Д., Ротер С., Салих В., Эвиг С. Пневмония, связанная со здравоохранением, не позволяет точно идентифицировать потенциально устойчивые патогены: систематический обзор и метаанализ. Clin Infect Dis . 2014 Февраль 58 (3): 330-9. [Медлайн].
Эггиманн П., Питтет Д. Инфекционный контроль в отделении интенсивной терапии. Сундук . 2001 декабрь 120 (6): 2059-93. [Медлайн].
Гейнес Р., Эдвардс-младший.Обзор внутрибольничных инфекций, вызванных грамотрицательными палочками. Clin Infect Dis . 2005 15 сентября. 41 (6): 848-54. [Медлайн].
Пелег А.Ю., Хупер, округ Колумбия. Внутрибольничные инфекции, вызванные грамотрицательными бактериями. N Engl J Med . 2010 13 мая. 362 (19): 1804-13. [Медлайн].
Марик ЧП. Аспирационный пневмонит и аспирационная пневмония. N Engl J Med . 2001 г., 1. 344 (9): 665-71. [Медлайн].
Mizgerd JP.Острая инфекция нижних дыхательных путей. N Engl J Med . 2008 14 февраля. 358 (7): 716-27. [Медлайн]. [Полный текст].
Рубин Ю.Б., Янофф EN. Пневмолизин: многофункциональный фактор вирулентности пневмококков. Дж. Лаборатория Клин Мед. . 1998, январь, 131 (1): 21-7. [Медлайн].
Садикот Р.Т., Блэквелл Т.С., Кристман Дж.В., Принц А.С. Взаимодействие патоген-хозяин при пневмонии, вызванной синегнойной палочкой. Am J Respir Crit Care Med . 2005 1 июн.171 (11): 1209-23. [Медлайн]. [Полный текст].
McCullers JA. Понимание взаимодействия вируса гриппа и пневмококка. Clin Microbiol Ред. . 2006 июл.19 (3): 571-82. [Медлайн]. [Полный текст].
Morens DM, Taubenberger JK, Fauci AS. Преобладающая роль бактериальной пневмонии как причины смерти при пандемическом гриппе: последствия для готовности к пандемическому гриппу. J Заразить Dis . 2008 г., 1 октября 198 (7): 962-70.[Медлайн]. [Полный текст].
Форги С., Марри Т.Дж. Атипичная пневмония, связанная со здоровьем. Semin Respir Crit Care Med . 2009 30 февраля (1): 67-85. [Медлайн].
Центры по контролю и профилактике заболеваний. Пневмония. Доступно на http://www.cdc.gov/Features/Pneumonia/. Доступ: 13 января 2011 г.
Рестрепо М.И., Анзуэто А. Роль грамотрицательных бактерий при пневмонии, связанной с оказанием медицинской помощи. Semin Respir Crit Care Med .2009 Февраль 30 (1): 61-6. [Медлайн].
Бактериальные коинфекции в образцах легочной ткани от смертельных случаев пандемического гриппа A (h2N1) 2009 г. — США, май-август 2009 г. MMWR Morb Mortal Wkly Rep . 2009 окт. 2. 58 (38): 1071-4. [Медлайн].
Пандемия гриппа A (h2N1), 2009 г. у беременных, нуждающихся в интенсивной терапии — Нью-Йорк, 2009 г. MMWR Morb Mortal Wkly Rep . 2010 26 марта. 59 (11): 321-6. [Медлайн].
Dennis DT, Inglesby TV, Henderson DA, Bartlett JG, Ascher MS, Eitzen E, et al.Туляремия как биологическое оружие: управление медициной и общественным здравоохранением. JAMA . 6 июня 2001 г. 285 (21): 2763-73. [Медлайн].
Rello J, Ollendorf DA, Oster G, Vera-Llonch M, Bellm L, Redman R и др. Эпидемиология и исходы вентилятор-ассоциированной пневмонии в большой базе данных США. Сундук . 2002 Декабрь 122 (6): 2115-21. [Медлайн].
Американская ассоциация легких. Тенденции заболеваемости и смертности от пневмонии и гриппа.Сентябрь 2008 г. Американская ассоциация легких. Доступно на http://bit.ly/gwYJAE. Доступ: 13 января 2011 г.
Kung HC, Hoyert DL, Xu JQ, Murphy SL и Отдел статистики естественного движения населения. Смерти: окончательные данные за 2005 год. Национальные отчеты о статистике естественного движения населения. Хяттсвилл, Мэриленд: Национальный центр статистики здравоохранения, апрель 2008 г .: 56 (10). http://www.cdc.gov. Доступно на http://bit.ly/i3ATH5. Доступ: 13 января 2011 г.
Муфсон М.А., Станек Р.Дж. Бактериемическая пневмококковая пневмония в одном американском городе: 20-летнее продольное исследование, 1978–1997 гг. Am J Med . 1999 г. 26 июля. 107 (1А): 34С-43С. [Медлайн].
Cillóniz C, Ewig S, Polverino E, Marcos MA, Esquinas C, Gabarrús A, et al. Микробная этиология внебольничной пневмонии и ее отношение к степени тяжести. Грудь . 2011 Апрель 66 (4): 340-6. [Медлайн].
van der Poll T, Opal SM. Патогенез, лечение и профилактика пневмококковой пневмонии. Ланцет . 2009 31 октября. 374 (9700): 1543-56. [Медлайн].
Slovis BS, Brigham KL. Сесил Основы медицины. : Андреоли Т., Карпентер CCJ, Григгс Р.К., Лоскальцо Дж. Подход к пациенту с респираторным заболеванием . 6-е изд. WB Saunders Co: Филадельфия, Пенсильвания; 2004. 177-80.
Brown SM, Jones BE, Jephson AR, Dean NC. Подтверждение рекомендаций Американского общества инфекционистов / Американского торакального общества 2007 г. по тяжелой внебольничной пневмонии. Crit Care Med .2009 Декабрь 37 (12): 3010-6. [Медлайн]. [Полный текст].
Фанг У.Ф., Ян К.Й., Ву К.Л., Ю СиДжей, Чен С.В., Ту Сиайи и др. Применение и сравнение показателей оценки для прогнозирования исходов у пациентов с пневмонией, связанной с оказанием медицинской помощи. Crit Care . 2011 19 января 15 (1): R32. [Медлайн].
Lim WS, van der Eerden MM, Laing R, Boersma WG, Karalus N, Town GI, et al. Определение степени тяжести внебольничной пневмонии при поступлении в больницу: международное исследование и валидация. Грудь . 2003 май. 58 (5): 377-82. [Медлайн]. [Полный текст].
Fine MJ, Auble TE, Yealy DM, Hanusa BH, Weissfeld LA, Singer DE, et al. Правило прогноза для выявления пациентов с внебольничной пневмонией из группы низкого риска. N Engl J Med . 1997 23 января. 336 (4): 243-50. [Медлайн].
Агентство медицинских исследований и качества. Калькулятор индекса тяжести пневмонии. Доступно на http://pda.ahrq.gov/clinic/psi/psicalc.asp.Доступ: 13 января 2011 г.
Sligl WI, Majumdar SR, Marrie TJ. Сортировка тяжелой пневмонии: какова «оценка» по правилам прогнозирования ?. Crit Care Med . 2009 Декабрь 37 (12): 3166-8. [Медлайн].
Phua J, см. KC, Chan YH, Widjaja LS, Aung NW, Ngerng WJ, et al. Подтверждение и клиническое значение малых критериев IDSA / ATS для тяжелой внебольничной пневмонии. Грудь . 2009 Июль 64 (7): 598-603. [Медлайн].
Bloos F, Marshall JC, Dellinger RP и др.Многонациональное обсервационное исследование прокальцитонина у пациентов ОИТ с пневмонией, которым требуется искусственная вентиляция легких: многоцентровое обсервационное исследование. Crit Care . 2011 7 марта. 15 (2): R88. [Медлайн].
Knaus WA, Draper EA, Wagner DP, Zimmerman JE. APACHE II: система классификации тяжести заболевания. Crit Care Med . 1985, 13 октября (10): 818-29. [Медлайн].
Le Gall JR, Lemeshow S, Saulnier F. Новая упрощенная оценка острой физиологии (SAPS II), основанная на многоцентровом исследовании в Европе / Северной Америке. JAMA . 1993 22-29 декабря. 270 (24): 2957-63. [Медлайн].
Винсент Дж. Л., Морено Р., Такала Дж., Уиллаттс С., Де Мендонса А., Брюнинг Н. и др. Шкала SOFA (оценка отказа органа, связанного с сепсисом) для описания дисфункции / отказа органа. От имени Рабочей группы по проблемам, связанным с сепсисом Европейского общества интенсивной терапии. Intensive Care Med . 1996 22 июля (7): 707-10. [Медлайн].
El-Solh AA, Alhajhusain A, Abou Jaoude P, Drinka P.Достоверность оценок степени тяжести у госпитализированных пациентов с пневмонией, приобретенной на дому. Сундук . 2010 декабрь 138 (6): 1371-6. [Медлайн].
España PP, Capelastegui A, Gorordo I, Esteban C, Oribe M, Ortega M, et al. Разработка и проверка правила клинического прогноза тяжелой внебольничной пневмонии. Am J Respir Crit Care Med . 2006 декабрь 1. 174 (11): 1249-56. [Медлайн].
Rello J, Rodriguez A, Lisboa T, Gallego M, Lujan M, Wunderink R.Показатель PIRO для внебольничной пневмонии: новое правило прогнозирования для оценки степени тяжести внебольничной пневмонии у пациентов отделения интенсивной терапии. Crit Care Med . 2009 Февраль 37 (2): 456-62. [Медлайн].
Чарльз П.Г., Вулф Р., Уитби М., Файн М.Дж., Фуллер А.Дж., Стирлинг Р. и др. SMART-COP: инструмент для прогнозирования потребности в интенсивной респираторной или вазопрессорной поддержке при внебольничной пневмонии. Clin Infect Dis . 2008 г. 1. 47 (3): 375-84.[Медлайн].
Легкий RW. Клиническая практика. Плевральный выпот. N Engl J Med . 2002, 20 июня. 346 (25): 1971-7. [Медлайн].
Bafadhel M, Clark TW, Reid C, Medina MJ, Batham S, Barer MR, et al. Прокальцитонин и С-реактивный белок у госпитализированных взрослых пациентов с внебольничной пневмонией, обострением астмы и хронической обструктивной болезнью легких. Сундук . 28 октября 2010 г. [Medline].
Skerrett SJ.Диагностическое тестирование внебольничной пневмонии. Clin Chest Med . 1999 Сентябрь 20 (3): 531-48. [Медлайн].
Смит ПР. Какие диагностические тесты необходимы при внебольничной пневмонии ?. Med Clin North Am . 2001 ноябрь 85 (6): 1381-96. [Медлайн].
Ketai L, Jordan K, Marom EM. Визуализирующая инфекция. Clin Chest Med . 2008 29 марта (1): 77-105, vi. [Медлайн].
Купер М.С., Стюарт П.М.Кортикостероидная недостаточность у больных в острой форме. N Engl J Med . 2003 20 февраля. 348 (8): 727-34. [Медлайн].
Rivers E, Nguyen B, Havstad S, Ressler J, Muzzin A, Knoblich B, et al. Ранняя целенаправленная терапия в лечении тяжелого сепсиса и септического шока. N Engl J Med . 2001, 8 ноября. 345 (19): 1368-77. [Медлайн].
Кан Я., Квон С.И., Юн Х.И., Ли Дж.Х., Ли CT. Роль С-реактивного белка и прокальцитонина в дифференциации туберкулеза от бактериальной внебольничной пневмонии. Korean J Intern Med . 2009 24 декабря (4): 337-42. [Медлайн]. [Полный текст].
Pirracchio R, Mateo J, Raskine L, Rigon MR, Lukaszewicz AC, Mebazaa A, et al. Могут ли бактериологические образцы верхних дыхательных путей, полученные при приеме в отделение интенсивной терапии, служить ориентиром для эмпирической антибиотикотерапии при ИВЛ-ассоциированной пневмонии? Crit Care Med . 2009 Сентябрь 37 (9): 2559-63. [Медлайн].
Гариб А.М., Стерн Э.Дж. Радиология пневмонии. Med Clin North Am .2001 ноябрь 85 (6): 1461-91, x. [Медлайн].
Tarver RD, Teague SD, Heitkamp DE, Conces DJ Jr. Радиология внебольничной пневмонии. Радиол Клин Норт Ам . 2005 г., май. 43 (3): 497-512, viii. [Медлайн].
Gotway MB, Reddy GP, Webb WR, Elicker BM, Leung JW. КТ легкого высокого разрешения: паттерны болезней и дифференциальные диагнозы. Радиол Клин Норт Ам . 2005 г., май. 43 (3): 513-42, viii. [Медлайн].
[Рекомендации] Деллинджер Р.П., Леви М.М., Карлет Дж. М. и др.Кампания по выживанию при сепсисе: международные рекомендации по ведению тяжелого сепсиса и септического шока: 2008 г. Intensive Care Med . 2008, январь, 34 (1): 17-60. [Медлайн]. [Полный текст].
Семенюк Р.А., Мид М.О., Алонсо-Коэльо П., Бриэль М., Эванев Н., Прасад М. и др. Кортикостероидная терапия для пациентов, госпитализированных с внебольничной пневмонией: систематический обзор и метаанализ. Энн Интерн Мед. . 2015 Октябрь 6. 163 (7): 519-28. [Медлайн].
Арнольд Ф.В., ЛаДжой А.С., Брок Г.Н., Пейрани П., Релло Дж., Менендес Р. и др.Улучшение результатов у пожилых пациентов с внебольничной пневмонией за счет соблюдения национальных рекомендаций: результаты когортного исследования Международной организации внебольничной пневмонии. Arch Intern Med . 2009 14 сентября. 169 (16): 1515-24. [Медлайн].
МакКейб С., Киршнер С., Чжан Х., Дейли Дж., Фисман Д.Н. Согласованная с рекомендациями терапия и снижение смертности и продолжительности пребывания взрослых с внебольничной пневмонией: игра по правилам. Arch Intern Med .2009 14 сентября. 169 (16): 1525-31. [Медлайн].
[Рекомендации] Центры услуг Medicare и Medicaid, Объединенная комиссия. Руководство по техническим условиям для национальных больничных мер качества стационарных пациентов. V. 2.6b. Ручная загрузка получена в апреле 2009 г.
Калил А.С., Мурти М.Х., Хермсен Э.Д., Нето Ф.К., Сан Дж., Рупп МЭ. Линезолид по сравнению с ванкомицином или тейкопланином при внутрибольничной пневмонии: систематический обзор и метаанализ. Crit Care Med .2010 Сентябрь 38 (9): 1802-8. [Медлайн].
Лам А.П., Вундеринк Р.Г. Роль MRSA при пневмонии, связанной с оказанием медицинской помощи. Semin Respir Crit Care Med . 2009 30 февраля (1): 52-60. [Медлайн].
Центры по контролю и профилактике заболеваний. Грипп h2N1: обновленные оценки CDC случаев гриппа h2N1 в 2009 г., госпитализаций и смертей в США с апреля 2009 г. по 10 апреля 2010 г. Доступно по адресу http://www.cdc.gov/h2n1flu/estimates_2009_h2n1.htm. Доступ: 1 июня 2010 г.
Sullivan SJ, Jacobson RM, Dowdle WR, Poland GA. Грипп h2N1 2009 г. Mayo Clin Proc . 2010 январь 85 (1): 64-76. [Медлайн]. [Полный текст].
1. Филлипс Д. ACIP изменяет интервал вакцинации от пневмококка у пожилых людей из группы низкого риска. Medscape Medical News. WebMD Inc . 4 сентября 2015 г. Доступно по адресу http://www.medscape.com/viewarticle/850564.
Кобаяши М., Беннетт Н.М., Гирке Р., Альмендарес О., Мур М.Р., Уитни К.Г. и др.Интервалы между вакцинами против PCV13 и PPSV23: Рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Morb Mortal Wkly Rep . 2015 4 сентября. 64 (34): 944-7. [Медлайн].
Центры по контролю и профилактике заболеваний. Использование пневмококковой конъюгированной вакцины 13-Valent и пневмококковой полисахаридной вакцины 23-Valent для взрослых с иммунодефицитными состояниями: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Morb Mortal Wkly Rep . 2012 Октябрь 12, 61: 816-9. [Медлайн].
Tomczyk S, Bennett NM, Stoecker C, Gierke R, Moore MR, Whitney CG, et al. Использование пневмококковой конъюгированной вакцины 13-Valent и пневмококковой полисахаридной вакцины 23-Valent среди взрослых в возрасте 65 лет: рекомендации Консультативного комитета по практике иммунизации (ACIP). MMWR Morb Mortal Wkly Rep . 2014 сентябрь 19, 63 (37): 822-5. [Медлайн]. [Полный текст].
Bonten M, Bolkenbaas M, Huijts S, et al.Испытание иммунизации взрослых от внебольничной пневмонии (CAPiTA). № аннотации 0541. Пневмония 2014; 3: 95. Доступно по адресу https://pneumonia.org.au/public/journals/22/PublicFolder/ABSTRACTBOOKMASTERforwebupdated20-3-14.pdf.
Tang KL, Eurich DT, Minhas-Sandhu JK, Marrie TJ, Majumdar SR. Частота, корреляты и результаты рентгенографии грудной клетки нового диагноза рака легкого у 3398 пациентов с пневмонией. Arch Intern Med . 2011 г. 11 июля. 171 (13): 1193-8. [Медлайн].
FDA запрашивает упакованные в рамку предупреждения о фторхинолоновых противомикробных препаратах: стремится усилить предупреждения, касающиеся повышенного риска тендинита и разрыва сухожилий [пресс-релиз]. Сильвер-Спринг, Мэриленд: Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США; 8 июля 2008 г. FDA. Доступно на http://bit.ly/fkBFeA. Доступ: 14 января 2011 г.
Kollef M, et al. ASPECT-NP: рандомизированное двойное слепое исследование III фазы, сравнивающее эффективность и безопасность цефтолозана / тазобактама и меропенема у пациентов с вентилируемой нозокомиальной пневмонией (VNP).Представлен на Европейском конгрессе клинической микробиологии и инфекционных заболеваний (ECCMID) 2019 г. (P1917). Амстердам, Нидерланды. 13-16 апреля 2019 г.
Использование рентгенограмм грудной клетки для дифференциации легочных и сердечных заболеваний у собак и кошек
Существует несколько причин, по которым мы делаем рентгенограммы грудной клетки. К ним относятся отмеченный шум в сердце, скрининг на метастатическое заболевание, оценка клинических проблем, таких как лихорадка неизвестного происхождения или, как правило, для оценки пациента, кашляющего или страдающего респираторным дистресс-синдромом.В этой статье мы рассмотрим паттерны легких и распределение распространенных легочных заболеваний, а также составим клиническую картину.
Рентгенологические паттерны легких у собак и кошек
Образцы легких — это просто рентгенологические признаки заболеваний легких. См. Таблицу 1 для дифференциальной диагностики распространенных паттернов легких у собак и кошек.
Типичные образцы легких включают:
- Бронхиальный узор представляет собой диффузное утолщение стенок дыхательных путей, создающее вид толстых линий и колец в легких.Важно распознать бронхиальный паттерн, потому что, хотя он может быть нормальным вариантом у пожилого пациента, он также может быть вызван определенной подгруппой заболеваний. К ним относятся бронхит, астма, собачий кашель, микоплазменная пневмония и паразитарный пневмонит, такой как сердечный червь или болезнь легких. Редко может наблюдаться минерализация дыхательных путей при определенных нарушениях обмена веществ (например, гиперадренокортицизме).
- Неструктурированный интерстициальный узор — это просто повышенная непрозрачность мягких тканей в легких, которая частично закрывает края кровеносных сосудов из-за наличия отека, гноя, крови или другого материала в легких (рис. 1).Само по себе появление интерстициального рисунка не является специфическим для определенных заболеваний. Напротив, распределение интерстициального паттерна наводит на мысль об определенных дифференциальных диагнозах. В легких существует множество заболеваний, которые могут проявляться в виде интерстициального паттерна. К ним относятся отек легких, пневмония, тромбоэмболия легких, кровотечение или фиброз.
- Альвеолярный узор более серьезен, чем интерстициальный, поскольку это область повышенной непрозрачности мягких тканей в легких, которая полностью закрывает легочные кровеносные сосуды (рисунки 2 и 3).Бронхи, заполненные воздухом, могут проявляться как «воздушные бронхограммы», если дыхательные пути также не заполнены инфильтратом или не спавлены. Если альвеолярный инфильтрат примыкает к краям легкого, тогда будет крупный признак, который представляет собой появление непрозрачного мягкого легкого, примыкающего к нормальному, заполненному воздухом легкому. Дифференциальный диагноз для альвеолярного паттерна в основном такой же, как и для интерстициального паттерна.
- Структурированный интерстициальный легочный узор иначе известен как узелки.Узелки представляют собой круглые или яйцевидные мягкие ткани или минеральные непрозрачные структуры в легких. Дифференциальный диагноз узелков, обнаруживаемых в легких, включает неоплазию, грибковое заболевание, паразитарные кисты или гранулемы, пузыри, заполненные жидкостью / кровью, легочные остеомы или концевые кровеносные сосуды.
- A сосудистый рисунок — это когда увеличенные и / или извилистые кровеносные сосуды приводят к повышенной непрозрачности мягких тканей в легких. Дифференциальные диагнозы увеличения легочной сосудистой сети включают сердечные гельминты, застойную сердечную недостаточность с левой стороны или сердечное шунтирование слева направо, например, открытый проток
- Другие менее распространенные легочные находки включают буллы или заполненные воздухом яйцевидные структуры или везикулярный узор , который обычно связан только с перекрутом доли легкого.В этой статье мы сосредоточимся на интерстициальных и альвеолярных паттернах у наших кашляющих и страдающих пациентов, а также коснемся бронхиальных паттернов.
Рис. 1. Боковой рентгеновский снимок грудной клетки собаки, показывающий неструктурированный интерстициальный узор. Обратите внимание на повышенную непрозрачность мягких тканей в легких, которая частично закрывает края кровеносных сосудов.
Таблица 1. Дифференциальная диагностика общих паттернов легких у собак и кошек.
Рис. 2. Боковой рентгеновский снимок грудной клетки собаки с вентрально-альвеолярным паттерном.Обратите внимание на знак доли каудальной доли легкого.
Рис. 3. Боковой рентгеновский снимок грудной клетки собаки с каудодорсальным альвеолярным паттерном. Обратите внимание на воздушные бронхограммы в патологическом легком.
Рентгенологическое распределение паттернов легких у собак и кошек
Распространение легочной болезни имеет первостепенное значение при определении наиболее вероятного дифференциального диагноза. Важные примеры рентгенографических изображений легких включают следующее:
Краниовентральный интерстициальный или альвеолярный узор
Когда у нас есть пациент с краниовентральным интерстициальным или альвеолярным паттерном, дифференциальный диагноз включает аспирационную пневмонию, ателектаз, кровотечение или легочную тромбоэмболию.Менее распространенными причинами такого появления являются образования, абсцессы или перекрут доли легкого.
Пневмония — это диагноз, который обычно ставится собакам с кашлем или отрывистостью, с признаками лихорадки или без них. Важно искать пневмонию у пациентов, у которых, возможно, была рвота, которые подвергались анестезии, длительное время лежали, имели мегаэзофагус, нарушение иммунитета или восприимчивость дыхательных путей (например, ранее перенесенная операция по поводу паралича гортани). Рентгенологически пневмония проявляется как интерстициально-альвеолярный паттерн краниовентральной части легких.Это может быть фокальная доля легкого (чаще всего правая средняя) или вентральная часть всех легких. Важно включить левую и правую боковую рентгенограмму, поскольку ее можно обнаружить только с одной стороны, в зависимости от того, какое легкое поражено. Из-за вентрального распределения он может не быть очевидным на вентродорсальных проекциях из-за лежащего выше средостения.
Если имеется фокальный или мультифокальный альвеолярный инфильтрат, он обычно будет содержать воздушные бронхограммы. Важно оценить область, перекрывающую силуэт сердца на боковой проекции, потому что это обычное место для очаговой аспирационной пневмонии.Иногда, в более тяжелых случаях, может быть сопутствующий мягкий плевральный выпот. Если мы диагностируем у пациента аспирационную пневмонию на основании рентгенологических данных, лихорадки, нейтрофилии и / или истории болезни, подтверждающей это заболевание, тогда пациента следует лечить антибиотиками. В идеале антибиотики следует выбирать на основе посева из дыхательных путей, но, как правило, эмпирическая терапия будет выбрана без посева в несложных и единичных случаях.
Рис. 4. Вентодорсальный рентгеновский снимок грудной клетки собаки с аспирационной пневмонией.Обратите внимание на уплотнение правой средней доли легкого.
Обычные организмы, выделенные от собак и кошек с заболеваниями нижних дыхательных путей, включают E.coli , Pasteurella spp., Streptococcus spp., B.bronchiseptica , Enterococcus spp., Mycoplasma spp. pseudintermedius и другие коагулазо-положительные Staphylococcus spp. и Pseudomonas spp. Хотя исследований для определения продолжительности приема антибиотиков недостаточно, обычно их назначают в течение 4–6 недель.Рекомендуется перепроверить рентгенограммы грудной клетки в трех проекциях через 10–14 дней после начала приема антибиотиков. Антибиотики следует продолжать в течение 1-2 недель после того, как рентгенограммы станут нормальными.
Если у пациента была недавняя травма или у него коагулопатия (например, с отравлением родентицидами или ДВС-синдромом), то более вероятным дифференциальным диагнозом является кровотечение. Кровоизлияние обычно проникает в зависимые легкие и поэтому является вентральным. Однако при травме ушибы легких обычно находятся в области воздействия.
Ушибы легких обычно отмечаются рядом с переломами ребер или позвонков или рядом с колотыми ранами. Рентгенологические признаки ушиба легких могут появиться или ухудшиться через 24 часа после травмы и исчезнуть в течение нескольких дней у выздоравливающих пациентов. Дискретные помутнения мягких тканей, которые остаются при улучшении общей картины легких, с большей вероятностью являются гематомами, и для их устранения требуется больше времени. При травме также может быть гемоторакс и / или пневмоторакс. Это важно идентифицировать, так как может быть показан торакоцентез.В ретроспективном анализе 143 собак с ушибами легких, вызванными дорожно-транспортными происшествиями, собаки с более серьезными рентгенологическими изменениями грудной клетки при поступлении с большей вероятностью нуждались в кислороде, получали кислород в течение более длительных периодов времени и имели более длительное время госпитализации (Пауэлл и др., 1999).
Если нет истории болезни или свидетельств травмы и нет признаков пневмонии, то следует провести определенные тесты для выявления причин легочного кровотечения .К ним относятся время коагуляции и количество тромбоцитов.
Другой менее вероятной причиной вентрального альвеолярного паттерна является закупорка слизистой и ателектаз в сочетании с астмой у кошек . Это будет в сочетании с диффузным бронхиальным узором из-за утолщения бронхов. Часто из-за астмы возникает воздушная ловушка. Это может привести к тому, что грудная клетка будет иметь расширенную «бочкообразную форму» и может привести к уплощению диафрагмы на боковых изображениях и множеству краниально направленных точек на диафрагму в областях мышечных прикреплений, иначе известных как «натяжение диафрагмы».”
Если рентгенограммы и клинические признаки соответствуют астме кошек, пациента следует лечить противовоспалительными дозами глюкокортикоидов. Добавки кислорода могут быть показаны в случаях острого недомогания, вызванного астмой у кошек. Также могут быть полезны бронходилататоры, но их не следует использовать при сопутствующем сердечном заболевании. Если клинические признаки сохраняются при лечении, следует рассмотреть возможность взятия проб из дыхательных путей для цитологической оценки, посева, тестирования на микоплазмы, а также тестирования на сердечных и легочных гельминтов.
Другим, менее распространенным заболеванием легких, распространенным вентрально, является перекрут доли легкого . Это может быть альвеолярный узор, но везикулярный узор или везикулярная эмфизема, характеризующаяся локально обширными небольшими пузырьками газа в пораженном легком. Чаще всего поражается правая средняя доля легкого. Обычно наблюдается сопутствующий плевральный выпот. Перекрут бронха может быть виден рентгенологически как смещение или притупление дыхательных путей. В противном случае для окончательного диагноза показана компьютерная томография.После постановки диагноза перекрута доли легкого показано экстренное хирургическое вмешательство для лобэктомии перекрученного легкого.
Каудодорсальное распределение интерстициального или альвеолярного узора
Существует другая подгруппа заболеваний, которые вызывают каудодорсальное распространение интерстициального или альвеолярного паттерна. К ним относятся кардиогенный отек легких, некардиогенный отек легких, гематогенная, вирусная или атипичная пневмония, ушибы легких, легочная тромбоэмболия и неоплазия.
Кардиогенный отек легких представляет собой интерстициальный альвеолярный инфильтрат в перигилярной и каудодорсальной частях легких. Легочные кровеносные сосуды в этой области могут быть частично или полностью закрыты. В большинстве случаев будет сопутствующий застой в легочных венах, если только пациент уже не получает терапию лазиксом. Важно помнить, что пациенты с кардиогенным отеком легких имеют левостороннюю застойную сердечную недостаточность. Следовательно, должны быть доказательства кардиомегалии.Это может быть левосторонняя кардиомегалия из-за болезни митрального клапана, дилатационной кардиомиопатии или появления валентинки или общего увеличения сердца у кошек с кардиомиопатией. Исключение составляют пациенты с разрывом сухожильных хорд. Это редко и наблюдается у пациентов с тяжелой застойной сердечной недостаточностью и сильным шумом в сердце. Должны присутствовать другие клинические признаки застойной сердечной недостаточности. Эти признаки включают шум в сердце, тахикардию, снижение перфузии (т. Е. Плохое качество пульса и возможное переохлаждение).
Основным рентгенологическим подтверждением сердечного заболевания является кардиомегалия. Важно знать нормальный силуэт сердца, чтобы определить, есть ли конкретное увеличение камеры или генерализованная кардиомегалия. При использовании показателя сердечного ритма позвоночника VHS> 10,7 или <9,2, вероятно, является ненормальным. Эту шкалу следует использовать с осторожностью, так как у некоторых пород собак (например, английского бульдога) оценка сердечного ритма позвоночника может составлять около 12 без признаков сердечного заболевания. Вот почему также полезно использовать субъективную оценку при увеличении камеры или генерализованной кардиомегалии.
При использовании аналогии с циферблатом на вентродорсальных проекциях (рис. 5) центр часов находится на киле. Позиция 11: 30-12: 30 — это дуга аорты. Положение 1-2 часа — это главная легочная артерия. Положение на 2-3 часа — левое предсердие. Положение 4-5 часов — это левый желудочек. Позиция на 6 часов между главными каудальными бронхами — это левое предсердие. Положение 7-8 часов — это правый желудочек, а положение 9: 30-11: 30 — правое предсердие.
Рис. 5. Вендродорсальный рентгеновский снимок грудной клетки собаки, демонстрирующий аналогию с циферблатом. Обратите внимание, что 12 часов: дуга аорты (красный), 10 часов: главная легочная артерия (оранжевый), 2 часа: левое предсердие (желтое), 4-5 часов: левый желудочек (зеленый), 6 часов. Часы: левое предсердие (светло-голубой), 7-8 часов: правый желудочек (средний синий), 9-10 часов: правое предсердие (пурпурное).
На боковой проекции (рис. 6) можно также оценить левостороннюю или правостороннюю кардиомегалию.
Рисунок 6.Боковой рентгеновский снимок грудной клетки собаки, демонстрирующий аналогию с циферблатом. Обратите внимание на дугу аорты (красный), главную легочную артерию (оранжевый), левый желудочек (зеленый), левое предсердие (голубой), правый желудочек (средний синий), правое предсердие (фиолетовый).
Если провести воображаемую линию (или провести линию) от киля до вершины сердца, у здорового пациента 2/3 сердца должны располагаться краниально по отношению к линии, а 1/3 — каудально. (Рисунок 7). Если краниальнее линии сердца больше 2/3, то это свидетельствует о правосторонней кардиомегалии.Если хвостовой участок превышает 1/3, то вероятна левосторонняя кардиомегалия, в частности, увеличение левого предсердия. Эти нормы не всегда применимы к кошкам, поскольку их сердца расположены более вертикально в грудной клетке. Нормальное сердце кошки должно быть яйцевидным или миндалевидным. Округление, особенно в области предсердий, может указывать на кардиомегалию.
Рис. 7. Боковой рентгеновский снимок грудной клетки собаки. Если вы проведете воображаемую линию (или проведете линию) от киля до вершины сердца, у нормального пациента (собаки) 2/3 сердца должны располагаться краниально по отношению к линии, а 1/3 — каудально.
Увеличение левого предсердия — наиболее распространенный вид кардиомегалии, выявляемый рентгенологически. Обычно это происходит из-за расширения левого предсердия, связанного с заболеванием митрального клапана. В боковой проекции увеличение левого предсердия вызывает выпуклость мягких тканей или уплощение каудодорсальной части сердечного силуэта. Из-за увеличенной высоты левого предсердия это также может вызвать дорсальное смещение киля и главных бронхов (рис. 8). Может быть выборочное смещение, а в некоторых случаях и компрессия левого главного бронха.Эти случаи со сдавлением бронхов, вторичным по отношению к увеличению левого предсердия, часто сопровождаются кашлем.
Рис. 8. Боковой рентгеновский снимок грудной клетки собаки. Обратите внимание на увеличенный апикобазилярный размер, вызывающий дорсальное смещение киля, увеличение левого предсердия и ушной раковины и дорсолатеральное смещение каудальных бронхов.
На вентродорсальной и дорсовентральной проекциях увеличенное левое предсердие суммируется как овальное помутнение мягких тканей над средне-каудальным аспектом сердечного силуэта.Увеличенное левое предсердие может вызвать расхождение или латеральное смещение основных бронхов на этом изображении. Иногда увеличение или смещение левого предсердия (ушка левого предсердия) происходит одновременно с тяжелыми случаями увеличения левого предсердия. В этих случаях левое предсердие рассматривается как выпуклость мягких тканей на сердечном силуэте в положении 2-3 часов на вентродорсальной или дорсовентральной проекциях.
Рис. 9. Вентродорсальный рентгеновский снимок грудной клетки собаки. Обратите внимание на увеличенное левое предсердие, суммирующееся как овальное помутнение мягких тканей в середине каудальной части сердечного силуэта.Иногда увеличение или смещение левого предсердия (ушка левого предсердия) происходит одновременно с тяжелыми случаями увеличения левого предсердия. В этих случаях левое предсердие рассматривается как выпуклость мягких тканей на сердечном силуэте в положении 2-3 часов на вентродорсальной или дорсовентральной проекции.
При обследовании пациента на предмет сердечного заболевания необходимо также обращать внимание на размер и форму сосудистой сети. Расширение легочных вен происходит без увеличения артерий с перегрузкой сердечным объемом (например,грамм. левосторонняя сердечная недостаточность), миокардиальная недостаточность (например, DCM, HCM) или обструкция левого предсердия, вторичная по отношению к новообразованию или тромбу. Когда диагноз острой левосторонней застойной сердечной недостаточности ставится на основании клинических признаков, рентгенограмм и, возможно, эхокардиограммы, лечение следует начинать немедленно. Лечение включает дополнительный кислород, терапию диуретиками, например фуросемидом в виде болюсов или CRI, а также венодилататор, такой как паста из нитроглицерина.
Некардиогенный отек легких может возникать в результате обструкции дыхательных путей, судорог, поражения электрическим током, васкулита или острого повреждения легких / острого респираторного дистресс-синдрома.Клинические признаки обычно настолько серьезны, что пациенты страдают кислородной зависимостью. Рентгенологически он представляет собой двусторонний, дорсальный или диффузный, интерстициальный или альвеолярный инфильтрат. У этих пациентов редко наблюдаются кардиомегалия или застой в легочных венах.
Важно принять во внимание историю болезни, клинические признаки и другие рентгенологические признаки, чтобы определить, есть ли у пациента некардиогенный или кардиогенный отек легких. Пациенты с некардиогенным отеком легких будут получать поддерживающую терапию дополнительным кислородом, и им может потребоваться искусственная вентиляция легких.Если имеется сомнительная кардиомегалия, рассмотрите возможность проведения эхокардиограммы для оценки левого предсердия. Кроме того, можно попытаться провести испытание Lasix, и диагноз может быть поставлен на основании реакции на лечение.
Легочная тромбоэмболия (ЛТЭ) — распространенное заболевание у собак, но редко у кошек. PTE связан с многочисленными предрасполагающими условиями, вызывающими гиперкоагуляцию, застой кровотока или повреждение эндотелия. Предрасполагающие заболевания включают гиперадренокортицизм, неоплазию, иммуноопосредованную гемолитическую анемию, сердечные гельминты и энтеропатию или нефропатию с потерей белка.Наиболее частыми признаками являются одышка, тахипноэ и депрессия. Другие признаки включают кашель или кровохарканье или и то, и другое, цианоз, обморок, коллапс и внезапную смерть.
Рентгенологические признаки могут включать раннюю олигемию, то есть снижение васкуляризации области легкого. Однако, как правило, мы идентифицируем вторичный отек легких и ателектаз, что приводит к фокальному альвеолярному паттерну. Сердечно-сосудистые последствия ПТЭ зависят от степени окклюзии легочных сосудов.Значительная окклюзия легочных сосудов приводит к легочной артериальной гипертензии и увеличению постнагрузки правого желудочка (ПЖ). Тяжелые, острые изменения постнагрузки правого желудочка приводят к дилатации и дисфункции правого желудочка. Рентгенологически увеличение правого желудочка может привести к смещению верхушки сердца дорсально от грудины на боковых проекциях. На изображениях VD и DV увеличенный правый желудочек выглядит более округлым и больше выступает в правое полушарие грудной клетки, придавая сердечному силуэту вид, обратный D.
Важно не путать нормальное округление правого предсердия на дорсовентральной проекции с кардиомегалией. Это еще один пример того, почему важно использовать несколько проекций, чтобы определить, есть ли кардиомегалия и увеличение камеры. Легочная гипертензия, связанная с тромбоэмболией легочной артерии, вызывает увеличение легочной долевой артерии (или артерий) и увеличение основной легочной артерии. Увеличение основной легочной артерии, а также легочная гипертензия могут быть подтверждены с помощью эхокардиографии.Если диагноз ПТЭ установлен на основании предрасполагающего состояния, клинических признаков и рентгенологических данных, следует начать лечение. Терапия в основном поддерживающая. Успешное лечение острого ПТЭ обычно сопровождается хронической антикоагулянтной или антитромбоцитарной терапией.
Диффузные легочные паттерны
Диффузное заболевание легких может иметь форму бронхиального, интерстициального или альвеолярного рисунка. Диффузные интерстициальные или альвеолярные узоры могут быть вызваны васкулитом, острым повреждением легких (ALI), острым респираторным дистресс-синдромом (ARDS), атипичной пневмонией или неоплазией, такой как лимфома. Атипичная пневмония может быть связана с другим основным заболеванием дыхательных путей, таким как коллапс трахеи или собачий кашель. Пациент может иметь кашель, респираторную недостаточность и лихорадку. Окончательный диагноз ставится при промывании дыхательных путей. В некоторых случаях Mycoplasma spp. агент, обнаруженный у пациентов с диффузными легочными инфильтратами. Одновременно могут быть обнаружены и другие распространенные патогены. Лечение включает соответствующую терапию антибиотиками и дополнительный кислород, а также препараты для подавления кашля.
Кашель в питомнике или комплекс инфекционных респираторных заболеваний собак (CIRDC) — частая находка у молодых собак и собак, которые в анамнезе находились в приютах или интернатах. Эти собаки обычно жалуются на кашель и рвоту, а также могут иметь или не иметь лихорадку. Рентгенологически — диффузный бронхиальный узор. Также может быть сопутствующая аспирационная пневмония. Наиболее частыми возбудителями являются B. bronchiseptica , S. equi подвид zooepidemicus и Mycoplasma spp.Это самоограничивающееся заболевание, но лечение может включать в себя подавление кашля и соответствующие антибиотики, такие как доксициклин. Если пациент не отвечает на лечение в течение семи дней, следует провести забор дыхательных путей для цитологической оценки, посева и тестирования микоплазмы.
Мы надеемся, что эти советы помогут вам лучше понять типы паттернов легких, которые могут возникать у собак и кошек, а также возможные причины.
Список литературы
- Пауэлл, Л.Л., Розанский, Э.А., Тидвелл, А.С. и Раш, Дж. Э. (1999): Ретроспективный анализ ушиба легких, вторичного в результате дорожно-транспортных происшествий, у 143 собак: 1994–1997 гг. Journal of Veterinary Emergency and Critical Care, 9: 127– 136. DOI: 10.1111 / j.1476-4431.1999.tb00074.
- Tyburski, James G. MD; Коллиндж, Джулианна Д. MD; Уилсон, Роберт Ф. MD; Eachempati, Soumitra R. MD: Легочные ушибы: количественная оценка поражений на рентгеновских снимках грудной клетки и факторов, влияющих на прогноз, журнал J , журнал Trauma-Injury Infection & Critical Care, май 1999 г. — Том 46 — Выпуск 5 — стр 833- 838 .
- Тралл, Д.Э .: Учебник ветеринарной диагностической радиологии 6 -е издание , Elsevier Saunders, Сент-Луис, штат Миссури, 2013.
- Тралл Д.Э., Робертсон И.Д .: Атлас нормальной рентгенографической анатомии и анатомических вариантов у собак и кошек, Elsevier Saunders, Сент-Луис, штат Миссури, 2011.
- Buchanan JW, Bücheler J: Система вертебральной шкалы для измерения размера сердца на рентгенограммах. J Am Vet Med Assoc, 1995; 206: 194–199.
- Р. Лаппин, Дж.Блондо, Д. Бут, Э. Брайчвердт, Л. Гуардабасси, Д.Х. Ллойд, М.Г. Папич, С.С. Ранкин, Дж. Э. Сайкс, Дж. Тернидж и Дж. Weese: Руководство по применению противомикробных препаратов для лечения заболеваний дыхательных путей у собак и кошек: Рабочая группа по применению противомикробных препаратов Международного общества инфекционных болезней домашних животных, Journal of Veterinary Internal Medicine , 31, 2, (279-294), (2017) ).
- Роберт Гоггс, Ливия Бениньи, Вирджиния Луис Фуэнтес и Дэниел Л. Чан: легочная тромбоэмболия, J журнал неотложной ветеринарной и неотложной помощи, Том 19, выпуск 1, Первое издание: 27 февраля 2009 г.
К
Дайнна Стельмах, DVM, MS, DACVR |
Опубликовано в
Ветеринары
| Помечено
Кардиология, Радиология
Пневмония у детей | IntechOpen
1. Введение
Пневмония вызывает значительную заболеваемость среди детей во всем мире и является основной причиной смерти детей в развивающихся странах. Заболеваемость пневмонией наиболее высока у детей в возрасте до 5 лет, а в последние годы частота осложненных и тяжелых пневмоний, по-видимому, увеличивается.
Этиологические факторы зависят от возраста, источника инфекции (внебольничная пневмония или внебольничная пневмония) и основных дефектов хозяина (например, иммунодефицита). Вирусы являются наиболее частым этиологическим фактором у детей дошкольного возраста, хотя во многих случаях можно идентифицировать более одного возбудителя. Существует несколько новых патогенов внебольничной пневмонии у детей: вирулентные штаммы Streptococcus pneumoniae , которых нет в доступных в настоящее время вакцинах, лейкоцидин Panton-Velentine, продуцирующий Staphylococcus aureus , человеческие бокавирусы и метапневмовирусы являются наиболее важными.
Диагноз в большинстве легких случаев внебольничной пневмонии основывается только на клинической оценке, поскольку лабораторные тесты и рентгенологическое обследование не дают ключа к разгадке этиологии. Детям с тяжелой пневмонией, внутрибольничной пневмонией и детям с ослабленным иммунитетом требуется инвазивный диагностический подход.
Лечение легких и средней степени тяжести заключается в поддерживающей терапии и лечении антибиотиками. Амоксициллин рекомендуется в качестве терапии первой линии для ранее здоровых детей независимо от возраста, поскольку он обеспечивает достаточную защиту от наиболее распространенного инвазивного бактериального патогена, а именно Streptococcus pneumoniae .Первоначальное эмпирическое лечение госпитальной пневмонии должно основываться на местных моделях чувствительности к противомикробным препаратам и должно быть соответствующим образом изменено, как только будут доступны результаты микробиологических тестов.
Несмотря на то, что при правильном диагнозе и лечении пневмония проходит без остаточных изменений, в некоторых случаях из-за вирулентности патогена и / или восприимчивости к хозяину ее течение может осложняться плевральным выпотом и эмпиемой, пневмоатоцеле, абсцессом легкого или некротической пневмонией.Признанным осложнением тяжелой пневмонии является гипонатриемия и SIADH (синдром несоответствующей секреции антидиуретического гормона).
Бремя пневмонии можно уменьшить с помощью профилактических мер, начиная от простейших методов инфекционного контроля, таких как мытье рук, ограничение контакта с инфекционными заболеваниями, ограничение воздействия табачного дыма, вакцинация и в отдельных случаях пассивная иммунизация.
Объявление
2. Определение
Пневмония определяется как воспаление легочной ткани, вызванное инфекционным агентом.Обычно используемое клиническое рабочее определение Всемирной организации здравоохранения основано исключительно на клинических симптомах (кашель или затрудненное дыхание и тахипноэ) [1]. В развивающихся странах термин «инфекция нижних дыхательных путей» (ИДПТ) широко используется вместо пневмонии из-за плохого доступа к рентгену и трудностей с радиологическим подтверждением диагноза.
В зависимости от места заражения пневмонию можно разделить на:
Внебольничная пневмония (ВП)
Больничная пневмония (ВП).
Недавно у взрослых пациентов был выявлен третий тип — пневмония, связанная с оказанием медицинской помощи (HCAP).
Значение этой классификации основано на ее клинической применимости, поскольку в большинстве случаев патогены, ответственные за ВП и ГП, разные, что требует различного подхода и эмпирического лечения.
3. Внебольничная пневмония
ВП может быть определена как пневмония у ранее здоровых детей, вызванная инфекционным агентом, заразившимся вне больницы.Обычной клинической практикой является подтверждение диагноза рентгенологическим исследованием уплотнений.
4. Эпидемиология
В глобальном масштабе заболеваемость пневмонией у детей младше 5 лет в развивающихся странах составляет 0,28 эпизода на ребенка в год (150 млн / год) по сравнению с 0,05 эпизодами на ребенка в год в развитых странах [2]. Пневмония является причиной 18% смертей (2 млн / год) среди детей раннего возраста во всем мире, в основном это происходит в бедных странах с ограниченным доступом к системе здравоохранения.В более зажиточных обществах пневмония редко заканчивается смертельным исходом, однако приводит к значительной заболеваемости. Заболеваемость рентгенологически подтвержденной пневмонией у ранее здоровых детей в Европе составляет 144-147 / 100 000 детей в год и снижается с возрастом, являясь самым высоким показателем у детей младше 5 лет (328-338 / 100 000 в год и 421/100 000 в год в пожилом возрасте). 0-2 года) [3,4]. Частота госпитализаций по поводу пневмонии в этой возрастной группе составляла 122 / 100,00 / год для детей младше 16 лет и 287 / 100,000 / год для детей младше 5 лет [4].Британские исследования показывают, что частота случаев ВБП, предъявляемых к врачам общей практики у детей младше 5 лет, составляет 191/100 000 человеко-лет [5], вероятно, из-за того, что более тяжелобольные дети будут поступать непосредственно в больницу. В исследовании, проведенном в Германии, частота госпитализированных пневмоний составила 300 на 100 000 в год среди детей 0–16 лет и 658 на 100 000 в год среди детей в возрасте 0–5 лет. В 23% этих случаев присутствовали сопутствующие заболевания, и вполне возможно, что многие дети с бронхиолитом были классифицированы как имеющие пневмонию [6].
С момента введения конъюгированной пневмококковой вакцины (ПКВ7) в национальные программы иммунизации в США и Европе заболеваемость пневмококковой пневмонией снизилась (на 65% в США), а частота госпитализаций ВП снизилась для детей младше 1 года, но, похоже, увеличивается для детей старше 5 лет [7–9]. В то же время, похоже, увеличивается частота тяжелой пневмонии, требующей госпитального лечения, а также осложненной пневмонии. С 1997 по 2006 год частота местных осложнений ВП увеличилась на 77.8% (5,4 и 9,6 случая на 100 000 населения соответственно). Эмпиема составляла> 97% всех местных осложнений [8,9].
5. Этиология
Организмы, вызывающие пневмонию, разнообразны и включают бактерии, вирусы, грибы и простейшие. Большинству случаев пневмонии предшествует острый вирусный бронхит. Вирусы способствуют заражению патогенными микроорганизмами, заселяющими носоглотку. Эти патогены включают Streptococcus pneumoniae, Haemophilus influenzae и Moraxella catarrhalis .Предыдущая колонизация Streptococcus mitis и анаэробными кокками Peptostreptococcus anaerobius может иметь защитный эффект против патогенных штаммов.
Этиологический фактор пневмонии может быть идентифицирован не более чем у 65-86% пациентов при сочетании нескольких диагностических инструментов, включая посев, серологию и ПЦР [7,11]. В повседневной клинической практике эти методы используются редко, а лечение остается эмпирическим, основанным на национальных и международных рекомендациях.
Вирусы ответственны за 30-67% случаев ВП и чаще всего встречаются у детей младше 2 лет.Наиболее часто выявляются респираторно-синцитиальный вирус (RSV), выделенный у 13–29%, и риновирус (3–45%) либо в сочетании с бактериями, либо отдельно. Другие вирусы, вызывающие пневмонию, включают аденовирус (1-13%), грипп (4-22%) и вирус парагриппа (3-10%), риновирус (3-45%), метапневмовирус человека (5-12%), бокавирусы человека. (5-15%). Менее распространены энтеровирусы, вирусы ветряной оспы, герпеса и цитомегаловируса [7,11-13]. У детей старшего возраста бактериальные инфекции встречаются чаще: лидирует Streptococcus pneumoniae (30–44% ВП), за ними следуют Mycoplasma pneumoniae (22–36%) и Chlamydophila pneumoniae (5–27%) [7, 11,13-16]. Streptococcus pneumoniae остается ведущей причиной тяжелой пневмонии, требующей госпитализации, даже в странах с низким уровнем инвазивной пневмококковой инфекции [17]. С момента появления PCV7 наиболее распространенными изолятами пневмококка являются 1 (преимущественно вызывающие эмпиему), 19A, 3, 6A и 7F (все включены в 13-валентную вакцину) [18]. В отличие от предыдущих сообщений Mycoplasma pneumoniae , по-видимому, одинаково часто встречается у детей школьного и дошкольного возраста [11,13]. Менее распространенные бактериальные причины ВП у детей включают Haemophilus influenzae типа B (5-9%), Staphylococcus aureus , Moraxella catarrhalis (1.5-4%), Bordatella pertussis, Streptococcus pyogenes (1-7%), Chlamydia trachomatis и новый патоген, выявленный в 1990-х годах — Simkania negevensis [7,12]. В отличие от взрослых Legionella pneumophila является редкой причиной ВП у детей [19].
В эндемичных по малярии регионах тропической Африки серьезным этиологическим фактором пневмонии является нетифоидная сальмонелла с множественной лекарственной устойчивостью, а в регионах, где туберкулез является эндемическим, она все чаще рассматривается как причина острой пневмонии [20].
8-40% случаев представляют собой смешанную вирусно-бактериальную или бактериально-бактериальную инфекцию [3,4,7,12,16,19]. Первичная вирусная инфекция предрасполагает к бактериальной пневмонии: эпидемии гриппа в развитых странах совпадают с эпидемиями Streptococcus pneumoniae и Staphylococcus aureus пневмонии и кори или RSV-инфекции способствуют увеличению смертности от пневмонии в развивающихся странах [2].
Объявление
6. Факторы риска для ограничения вакцины
Существует несколько известных факторов риска ВП, которые следует учитывать в дополнение к иммунизационному статусу, эпидемиологическим данным и контактам с другими детьми, особенно дошкольниками.Основные сопутствующие заболевания, такие как сахарный диабет, аспления или дисфункция селезенки, хроническое сердечное заболевание, нефротический синдром, тяжелое заболевание печени, являются факторами риска инвазивного пневмококкового заболевания, включая пневмонию. К другим факторам риска ВП относятся: астма, эпизоды свистящего дыхания в анамнезе, средний отит, леченный тимпаноцентезом в первые 2 года жизни (фактор риска для детей <5 лет), воздействие табачного дыма, недоедание, иммунологический дефицит (первичный или вторичный), мукоциллярный дисфункция (муковисцидоз, цилиарная дискинезия), врожденная аномалия дыхательных путей, нарушение глотания, микроаспирация, гастроэзофагеальный рефлюкс, нервно-мышечные расстройства, лечение ингибиторами кислоты желудочного сока (фактор риска у взрослых, у детей его роль подтверждена в одном исследовании).Факторы окружающей среды, такие как загрязнение воздуха в помещении, вызванное приготовлением пищи и обогревом с использованием топлива из биомассы (например, дров или навоз), проживание в условиях скопления людей и курение родителей, также увеличивают восприимчивость ребенка к пневмонии [1,7]. Было обнаружено, что воздействие табачного дыма увеличивает риск госпитализации по поводу пневмонии у детей младше 5 лет [21]. Состояния, предрасполагающие к тяжелой пневмонии, включают возраст <5 лет и недоношенность (24–28 лет) [11]. Вирусные инфекции, особенно грипп и предшествующее воздействие антибиотиков, дополнительно предрасполагают к пневмококковой и стафилококковой пневмонии.Антибиотики изменяют бактериальную микрофлору в дыхательных путях, разрушая комменсальные бактерии, такие как альфа-гемолитические стрептококки, в то время как вирусы выделяют нейраминидазу и другие ферменты, способствующие прикреплению и экспрессии пневмококковых рецепторов на клетках-хозяевах, таких как рецептор фактора активации тромбоцитов или CD14 [17,22].
7. Клинические проявления
Типичные клинические симптомы пневмонии включают:
кашель (30% детей, поступающих в амбулаторную клинику с кашлем, за исключением детей с хрипом, имеют рентгенологические признаки пневмонии, и кашель отмечен в 76% детей с ВП) [13,23].Следует отметить, что мокрота у детей дошкольного возраста выделяется редко, поскольку они склонны ее глотать.
лихорадка (присутствует у 88-96% детей с рентгенологически подтвержденной пневмонией) [13]
токсический вид
признаки респираторного дистресса: тахипно (таблица 1), одышка или затрудненное дыхание в анамнезе — втягивание грудной клетки, расширение носа, кряхтение, использование вспомогательных дыхательных мышц. Тахипное — очень чувствительный маркер пневмонии.50-80% детей с определенным ВОЗ тахипно имели рентгенологические признаки пневмонии, и отсутствие тахипно — лучший единственный признак для исключения болезни [13,23]. У детей <5 лет тахипное имело чувствительность 74% и специфичность 67% для рентгенологически подтвержденной пневмонии, но его клиническая ценность была ниже в первые 3 дня болезни. У младенцев <12 месяцев частота дыхания 70 вдохов / мин имела чувствительность 63% и специфичность 89% для гипоксемии [7].
| Возраст | Частота дыхания в минуту |
| 0–2 месяца | «/> 60 |
| 908 168 5080/9080/ | 908 168 5080/ |
| 908 2–12 месяцев | |
| 1–4 года | «/> 40 |
| ≥ 5 лет | » /> 30 |
Таблица 1.
Тахипное определяется в соответствии с критериями ВОЗ [1]
На основании клинических симптомов пневмонию можно разделить на тяжелую, требующую госпитализации, и легкую, среднюю или нетяжелую. Признаки тяжелой пневмонии различаются с возрастом и, согласно BTS, включают: температуру 38,5 0 ° C, частоту дыхания> 70 вдохов в минуту у младенцев и> 50 вдохов в минуту у детей старшего возраста, рецессию от умеренной до тяжелой у младенцев и тяжелую. затрудненное дыхание у детей старшего возраста, расширение носа, цианоз, прерывистое апноэ, хрюканье, отказ от кормления у младенцев и признаки обезвоживания у детей старшего возраста, тахикардия, время наполнения капилляров ≥2 с [7].Ажитация может быть признаком гипоксемии. В таблице 2 представлен упрощенный подход, рекомендованный ВОЗ для внедрения в развивающихся странах, чтобы помочь медицинским работникам на местах оценить необходимость направления в больницу.
Физикальное обследование:
потрескивания (присутствуют у 33-90% детей с пневмонией), ослабление дыхательных шумов над пораженным участком, бронхиальные дыхательные звуки, характерные для дольчатой консолидации, отсутствие звуков дыхания и тупость при перкуссии, указывающая на выпот.Если пневмония сопровождается плевритом, можно услышать шум трения плевры. Хрипы и звуки бронхиального дыхания имеют чувствительность 75% и специфичность 57% при диагностике пневмонии [7].
Наличие хрипов, особенно при отсутствии лихорадки, делает диагноз типичной бактериальной пневмонии маловероятным [24]. Однако это частый признак вирусной инфекции и Mycoplasma pneumonia (до 30%) [7].
Объединение нескольких клинических симптомов в диагностический алгоритм повышает чувствительность и специфичность диагностики.Критерии ВОЗ для определения пневмонии (кашель или затрудненное дыхание и тахипноэ), исследованные в бразильском исследовании 390 детей, имеют чувствительность 94% для детей <2 лет и 62% для детей ≥2 лет и специфичность 20% и 16% соответственно. Добавление лихорадки улучшило специфичность до 44% и 50% [25]. В австралийском исследовании детей с лихорадкой <5, поступающих в отделение неотложной помощи, клинические показатели пневмонии, подтвержденные радиологически и микробиологически, включали плохое самочувствие, лихорадку ≥ 39 ° C, затрудненное дыхание, хроническое заболевание, длительное время наполнения капилляров, тахипно, хрипы при аускультации. и отсутствие вакцинации против пневмококка [26].
Важно отметить, что ни один клинический или радиологический признак по отдельности или в комбинации не является чувствительным и достаточно специфичным, чтобы различать вирусную, атипичную или типичную бактериальную этиологию пневмонии.
| Пневмония / нетяжелая пневмония | Кашель Проблемы с дыханием Тахипноэ * Признаков тяжелой пневмонии нет |
| Тяжелая пневмония | — нижняя часть грудной клетки втягивание в стенку — воспламенение из носа — хрюканье на выдохе — нет признаков очень тяжелой пневмонии |
| Очень тяжелая пневмония | Признаки тяжелой пневмонии и ≥1 — невозможность есть — цианоз 908 — тяжелая респираторная недостаточность77 — нарушение сознания или судороги |
Таблица 2.
Тяжесть пневмонии — классификация ВОЗ [2,27]
8. Дополнительные тесты
Пульсоксиметрию следует проводить у всех детей с пневмонией, поскольку ее результаты облегчают оценку тяжести и, следовательно, необходимость направления в больницу. Всем детям, находящимся в стационаре, обязательно следует проводить пульсоксиметрию [7].
Лабораторные исследования
Определение этиологии — микробиологические исследования
Определить специфический возбудитель у детей с ВП сложно.Маленькие дети не откашливают мокроту, мазки из носоглотки не надежны, поскольку бактерии, присутствующие в верхних дыхательных путях, не обязательно такие же, как бактерии, вызывающие пневмонию. Инвазивные диагностические инструменты, хотя и эффективны, вряд ли приемлемы для в остальном здоровых детей, состояние большинства из которых улучшается при эмпирическом лечении. Стандарты Британского торакального общества (BTS), руководящие принципы Общества педиатрических инфекционных заболеваний, а также положения Политики Американской академии педиатрии не рекомендуют микробиологическое исследование ребенка с пневмонией, который лечится в амбулаторных условиях.Пациентам, поступившим в больницу, особенно пациентам, поступившим в отделение интенсивной терапии и пациентам с осложнениями ВП, следует попытаться провести микробиологический диагноз.
посевы крови положительны у <10% пациентов с пневмонией и <2% пациентов, лечившихся в амбулаторных условиях. Тем не менее, они должны быть выполнены, поскольку в случае положительного результата они предоставляют информацию об этиологии ВП и устойчивости к антибиотикам [7,19]. У детей с осложненной пневмонией частота бактериемии колеблется от 7.От 8% до 26,5% при пневмонии с парапневмоническим выпотом [19].
носоглоточные аспираты или образцы носового лаважа могут быть полезны при идентификации респираторных вирусов, включая респираторно-синцитиальный вирус, вирус парагриппа, вирус гриппа и аденовирус методом иммунофлуоресценции. Результаты этих тестов особенно полезны для когортации инфицированных детей во время вспышек и в эпидемических целях [7].
У маленьких детей получить мокроту сложно.Надежный образец мокроты, в отличие от слюны, содержит <10 эпителиальных клеток на поле малой мощности [35]. Мокрота, индуцированная ингаляцией с 5% -ным гипертоническим раствором, имеет гораздо более высокий бактериальный выход и, по-видимому, является ценным инструментом микробиологической диагностики у детей с ВП [36].
детям, которым требуется искусственная вентиляция легких, следует взять трахеальный аспират для окрашивания по Граму и посева во время установки эндотрахеальной трубки [19].
Аспирированная плевральная жидкость должна быть отправлена на микроскопию, посев и определение антигена.Посевы положительны в 9–18% случаев (чувствительность 23%, специфичность 100%) [7, 37]. Обнаружение пневмококкового антигена в плевральной жидкости имеет чувствительность 90% и специфичность 95% [38]. Следует проверить плевральную жидкость на Mycobacteria .
Обнаружение пневмококковых антигенов в моче неспецифично, так как оно часто бывает положительным у маленьких детей с носоглоточной колонизацией
Серологическое тестирование: четырехкратное повышение титров антител в тесте связывания комплемента является золотым стандартом диагностики, к сожалению, бесполезным для руководство по лечению.Во многих лабораториях иммуноферментный анализ (ИФА) заменил тесты на связывание комплемента, поскольку они требуют меньше времени. Положительный титр антител класса IgM к Mycoplasma через 9–11 дней от начала заболевания также указывает на недавнюю инфекцию. Описаны перекрестные реакции с аденовирусом и Legionella pneumophila [23]. Значение измерения холодовых агглютининов ограничено — у школьников прогностическая ценность положительного результата экспресс-теста на холодовые агглютинины Mycoplasma составила 70% [7].У Chlamydophila pneumoniae наблюдается повышение уровня IgM через 3 недели и повышение уровня IgG через 6-8 недель.
Legionella pneumophila Выявление антигена в моче остается золотым стандартом диагностики легионеллеза. После острой инфекции тест остается положительным в течение нескольких недель. Антиген в моче является положительным только в случае инфицирования серогруппой 1. Антигены выводятся с мочой в начале второй недели болезни. В продаже имеются быстрые диагностические тесты с чувствительностью 80% и специфичностью 99-100%.Заражение серогруппой 1 можно исключить, если результаты трех последовательных проб мочи отрицательны.
Полимеразная цепная реакция с обратной транскриптазой в реальном времени (ОТ-ПЦР) может быть использована для исследования этиологии пневмонии. Преимущество этого метода — доступность результатов в тот же день. Однако он не предоставляет информации о чувствительности бактерий и не является легкодоступным за пределами исследовательских центров. ПЦР на основе пневмолизина все чаще используется для обнаружения Streptococcus pneumoniae в крови и плевральной жидкости с чувствительностью 100% и специфичностью 95% [7].Измерение бактериальной нагрузки с помощью ОТ-ПЦР может помочь предсказать исход ВП, поскольку взрослые пациенты с бактериальной нагрузкой> 1000 копий / мл были подвержены более высокому риску сепсиса, дыхательной недостаточности и смерти [39].
Рентгенография грудной клетки
Рис. 1.
Альвеолярные уплотнения в левой нижней доле и в правой нижней доле. Mycoplasma pneumoniaepneumonia
Рис. 2.
Круглый очаг уплотнения в левой верхней доле.Пневмония.
9. Ведение
Большинство детей с ВП можно безопасно лечить в амбулаторных условиях. Показания для направления в больницу включают:
клинических признаков тяжелой пневмонии (перечисленные выше),
признаков сепсиса или септического шока
молодой возраст — <6 месяцев жизни
гипоксемия — сатурация кислорода <92% (согласно BTS) или <90% (согласно AAP и PIDS), PaO 2 <60 мм рт. Ст. И PaCO 2 > 50 мм рт.врожденный порок сердца, муковисцидоз, бронхолегочная дисплазия, иммунодефицит
диффузные рентгенологические изменения: многодольная пневмония, плевральный выпот
амбулаторное лечение неэффективно
ВП, вызванное возбудителем. MRSA (PIDS)
неспособность родителей справиться с болезнью дома
Дети, у которых не улучшается состояние, несмотря на лечение и которые имеют затрудненную дыхательную недостаточность или шок, должны быть госпитализированы в отделение интенсивной терапии.Критерии для поступления в ОИТ включают:
потребность в инвазивной механической вентиляции или неинвазивной вентиляции с положительным давлением,
жидкий рефрактерный шок
гипоксемия, требующая FiO 2 больше, чем концентрация во вдыхаемом воздухе или возможный поток при общем уходе площадь; пульсоксиметрические измерения ≤92% при вдыхаемом кислороде ≥0,5 (согласно BTS) или ≥0,6 (согласно PIDS)
измененное психическое состояние из-за гиперкарбии, гипоксемии или в результате пневмонии
рецидивирующее апноэ, хрюканье или медленное нерегулярное дыхание
увеличение частоты дыхания и частоты сердечных сокращений с клиническими признаками тяжелого респираторного расстройства и истощения с гиперкарбией или без нее [7,19]
Реклама
10.Общее ведение
Всех детей, получающих лечение от пневмонии, следует повторно обследовать через 48 часов, если нет клинического улучшения или ухудшения состояния и сохранения лихорадки. Важно, чтобы родители детей, получающих лечение на дому, имели четкие письменные инструкции по контролю температуры, предотвращению обезвоживания, распознаванию признаков ухудшения состояния, а также по дальнейшему доступу к специалистам в области здравоохранения [7].
Госпитализированным детям с гипоксемией следует давать кислород для поддержания насыщения кислородом> 92%.Обезвоженным детям следует давать достаточное количество жидкости для рта, а если они не могут пить, им следует вводить жидкости внутривенно. Уровень электролитов и креатинина в сыворотке крови следует измерять ежедневно. На сегодняшний день не было исследований, подтверждающих положительный эффект физиотерапии грудной клетки у детей с пневмонией, поэтому физиотерапию грудной клетки проводить не следует.
Состояние ребенка должно улучшиться по клиническим симптомам и лабораторным маркерам воспаления через 48-72 часа после начала адекватного лечения.Отсутствие улучшений требует дальнейшего исследования на предмет возможных осложнений, резистентных микроорганизмов или альтернативного диагноза.
11. Лечение антибиотиками
Между экспертами нет единого мнения о том, следует ли всем детям с ВП получать антибиотики. Согласно рекомендациям BTS, выпущенным в 2011 году, всем детям с диагнозом пневмония следует лечить антибиотиками. Это контрастирует с предыдущими рекомендациями, в которых говорилось, что при подозрении на вирусную этиологию антибиотики могут быть отменены при условии, что ребенок будет повторно обследован через 24-48 часов.Причина этого изменения, несмотря на очевидные опасения по поводу повышения устойчивости бактерий к антибиотикам, а также возможных побочных реакций у детей, которых необязательно лечили антибиотиками, заключается в том, что на основе клинических, лабораторных и радиологических маркеров, отдельно или в сочетании, надежный различить вирусную и бактериальную инфекцию невозможно. У детей младше 2 лет, особенно с конъюгированной пневмококковой вакциной в анамнезе и с легкими симптомами инфекции нижних дыхательных путей, пневмония маловероятна.У таких детей антибиотики могут быть отменены при условии повторной оценки состояния ребенка, если симптомы сохраняются или наступает ухудшение [7]. В рекомендациях по PIDS, напротив, указывается, что детям дошкольного возраста с ВП обычно не требуется антибактериальная терапия, поскольку пневмония в этой возрастной группе имеет преимущественно вирусное происхождение [19].
Антибиотиком выбора для лечения ВП на местном уровне является амоксициллин 90 мг / кг / день, применяемый двумя дозами в течение 5-10 дней. Результаты двух рандомизированных испытаний короткого курса (3 дня) пероральных антибиотиков, проведенных на младенцах в развивающихся странах, трудно интерпретировать, поскольку многие из этих детей страдали бронхиолитом с хрипом или инфекцией верхних дыхательных путей и вообще не нуждались в антибиотиках [43,44]. .Амоксициллин эффективен против большинства патогенов, вызывающих ВП у детей. Он хорошо переносится и доступен по цене. Альтернативами являются коамоксиклав, цефаклор и макролиды. Для Streptococcus pneumoniae , устойчивого к пенициллину с МПК до 4,0 мкг / мл, предпочтительным лечением является цефтриаксон, а для МПК> 4,0 мкг / мл — ванкомицин, линезолид или клиндамицин, хотя устойчивость к клиндамицину, по-видимому, увеличивается на 15-40%. в определенных географических регионах [19]. Следует отметить, что интерпретация тестов на чувствительность in vitro к пенициллину зависит от пути введения.При внутривенном введении пенициллин может достигать концентрации в тканях, эффективных против организмов с минимальной ингибирующей концентрацией (МИК) ≤2,0 мкг / мл, возможно, эффективной для штаммов с МИКС 4 мкг / мл и вряд ли будет эффективен для штаммов с МИКС ≥ 8 мкг / мл. Для пенициллина, вводимого перорально, соответствующие значения составляют <0,06 мкг / мл, 0,12–1,0 мкг / мл и ≥2,0 мкг / мл для устойчивых штаммов [19]. Стандарты клинических лабораторий различаются в зависимости от региона. Те, которые приведены выше, были выпущены совместно Американским обществом инфекционных болезней (IDSA) и Американским торакальным обществом (ATS).BTS рекомендует пороговые значения для пенициллина, вводимого внутривенно, <0,1 мг / л; 0,1–1,0 мг / л и> 1,0–4,0 мг / л, и Европейское респираторное общество (ERS) рекомендует контрольные точки МИК <0,5 мг / л; 0,5–2,0 мг / л и> 2,0 мг / л соответственно [17,19]. PIDS рекомендует левофлоксацин детям в возрасте от 6 месяцев в качестве предпочтительного выбора для пероральной терапии [19]. Макролидные антибиотики могут быть добавлены при подозрении на Mycoplasma pneumoniae или Chlamydophila pneumonia , когда состояние ребенка не улучшается через 24–48 часов или в очень тяжелых случаях.Они не рекомендуются в качестве антибиотиков первого выбора, поскольку до 40% выделенных в настоящее время в США штаммов S. pneumoniae устойчивы к макролидам [19].
Как и в случае с показаниями к антибиотикам при ВП, нет единого мнения о том, как их следует вводить. Согласно рекомендациям BTS, если ребенок хорошо ест и не рвет, антибиотики следует вводить перорально. Детей с пневмонией средней степени тяжести, поступивших из-за респираторного дистресса, можно лечить пероральными антибиотиками и выписывать, когда утихнет лихорадка и респираторный дистресс [7,45].Внутривенный путь введения антибиотиков рекомендуется детям с тяжелой, осложненной пневмонией или сепсисом, которым рекомендуется внутривенное введение амоксициллина, коамоксиклава, цефуроксима, цефотаксима или цефтриаксона. Однако согласно рекомендациям PIDS, все дети, проходящие лечение в больнице, должны получать антибиотики внутривенно для обеспечения надежной концентрации в крови и тканях [19]. У госпитализированных детей с подозрением на инфекцию S. aureus к бета-лактамной терапии следует добавить ванкомицин или клиндамицин.Для детей с аллергией на пенициллин рекомендуются цефалоспорины, а в случае аллергических реакций I типа — макролиды, ванкомицин или клиндамицин. У детей, которые не переносят ванкомицин или клиндамицин, можно назначать линезолид [19]. Антибиотик следует заменить в соответствии с результатами посева и чувствительностью, если эти тесты положительны. Как только состояние ребенка улучшится, следует рассмотреть возможность перехода на пероральные антибиотики [7].
12. Осложнения
12.1. Эмпиема и парапневмонический выпот
Парапневмонический выпот определяется как скопление плевральной жидкости в сочетании с лежащей в основе пневмонией, а эмпиема определяется как накопление гнойной жидкости в плевральной полости [46]. Заболеваемость парапневмоническим выпотом увеличивается (на 70-100% в период с 1990-х до начала нынешнего века), поражая 0,6% всех детей с ВП, 2-10% госпитализаций с пневмонией и 1/3 госпитализаций с пневмококковой пневмонией [47- 50]. Преобладающие этиологические факторы — S.pneumonia (серотип 1,3,14,19A), ответственная за 10-66% случаев эмпиемы, S. aureus , включая MRSA (4-30%) и S. pyogenes. К менее распространенным относятся Haemophilus influenzae , Mycobacterium spp, Pseudomonas aeruginosa , анаэробы, Mycoplasma pneumonia и грибы [28,46,47,51,52]. Сбор жидкости обычно односторонний. Классически эмпиема подразделяется на три стадии:
Экссудативная — плевральная полость содержит свободно текущую жидкость с низким количеством лейкоцитов, так называемый парапневмонический выпот, который возникает в результате повышенной проницаемости сосудов и миграции нейтрофилов, лимфоцитов и эозинофилов в ходе воспалительного процесса.
Фибрино-гнойное заболевание возникает через 5-10 дней от начала заболевания и заключается в отложении фибрина в плевральной полости, что приводит к перегородке и образованию локализаций. Количество лейкоцитов увеличивается (эмпиема) в ответ на бактериальную инвазию через поврежденный эпителий, и если его не лечить, оно прогрессирует до
Организационная — включает инфильтрацию фибробластов и развитие толстой эластичной мембраны в плевральной полости («корка» ).Эти мембраны могут нарушить функцию легких и предотвратить повторное расширение легких. Эмпиема на этой стадии может зажить спонтанно или может развиться хроническая эмпиема [46].
Некоторые авторы выделяют «стадию сухого плеврита», которая предшествует экссудативной стадии, но не обязательно приводит к ней [53].
Эмпиему следует подозревать у каждого ребенка с пневмонией с длительной лихорадкой, тахипным в анамнезе, болью при пальпации живота, плевритической болью в груди, шинированием пораженной стороны и сохранением высоких уровней С-реактивного белка в сыворотке [50].При физикальном обследовании можно было оценить асимметрию дыхательных звуков, одностороннее уменьшение расширения грудной клетки, притупление перкуссии [27]. У некоторых детей с пневмонией при внутривенном введении антибиотиков может развиться эмпиема [50]. Одним из выявленных факторов риска бактериальной эмпиемы является прецедент ветряной оспы [49].
Рентгенограммы грудной клетки показывают однородное помутнение по всему легкому (большой выпот) (рис. 3). В небольших излияниях наблюдается восходящий ободок жидкости вдоль боковой стенки грудной клетки (признак мениска).Облитерация реберно-диафрагмального угла является первым признаком плеврального выпота. На основании рентгенограммы невозможно отличить выпот от эмпиемы [47]. Методом выбора для радиологического обследования пациентов с парапневмоническим выпотом и эмпиемой является ультразвуковое исследование. Он помогает оценить количество жидкости, ее эхогенность, обнаруживает локализации и нити фибрина и используется для проведения инвазивных процедур [28]. КТ грудной клетки не следует проводить в плановом порядке, однако она может быть полезна для диагностики основной патологии, например.опухоль в средостении или абсцесс легкого [46,53].
Рис. 3.
Помутнение левого гемиторакса со смещением средостения в противоположную сторону. Альвеолярные уплотнения в центральном поле правой доли. Долевая пневмония с плевральным выпотом, вызванная Streptococcus pneumoniae
Рис. 4.
Множественные абсцессы в правой верхней доле. Диффузные альвеолярные уплотнения с утолщением внутриальвеолярных пространств в средней и нижней правой долях. Жидкость в правой плевральной полости.Staphylococcus aureuspneumonia с абсцессами легких и плевральным выпотом.
Плевральная жидкость, полученная во время торакоцентеза или торакоскопической хирургии с использованием видео (VATS), должна быть отправлена на посев, окраску по Граму, цитологию и молекулярные методы, если таковые имеются. Всегда следует проводить бактериологические исследования, даже если они положительны в случаев, поскольку они могут предоставить полезную информацию для руководства антибактериальной терапией. Также необходимо провести окрашивание на кислотоустойчивые бациллы, посев и ПЦР [46].В большинстве случаев при бактериальной эмпиеме преобладают полиморфно-ядерные лейкоциты. В случае злокачественной опухоли жидкость может быть окрашена кровью с преобладанием лимфоцитов, хотя злокачественные клетки могут отсутствовать. При туберкулезе также преобладают лимфоциты в плевральной жидкости, хотя в 10% случаев выпот может быть нейтрофильным [46]. Критерии освещения, полезные для руководства по лечению у взрослых пациентов, не прошли надлежащую проверку у детей, и их рутинное использование не рекомендуется [46,53].
Всех детей с эмпиемой или плевральным выпотом следует лечить в стационаре [46]. Однако нет единого мнения относительно того, что является оптимальным лечением эмпиемы: только антибиотики при небольших и умеренных излияниях, введение плевральной дренажной трубки с фибринолитиками или без них или VATS для умеренных и тяжелых случаев. Различия в лечении в некоторой степени являются результатом личного опыта и доступности различных методов лечения, в том числе опытных интервенционных радиологов и детских торакальных хирургов.Как правило, двумя наиболее важными факторами, определяющими необходимость введения плевральной дренажной трубки, являются размер выпота и степень респираторной недостаточности у ребенка [19]. Существует мнение, что из-за инвазивного характера процедуры и необходимости общей анестезии у детей младшего возраста вместо повторных торакоцентеза иглой следует вводить дренаж [46]. Согласно данным PIDS, плевральный выпот можно разделить в зависимости от их размера на:
Малый: <10 мм на рентгенограмме бокового пролежня или затемняет <гемиторакс
Умеренный: ободок жидкости> 10 мм и затемняет <½ гемиторакса
Большой: затемняет> 1/2 гемиторакса
При небольших излияниях рекомендуется консервативное лечение антибиотиками.Выбор антибиотика основан на результатах посева крови или плевральной жидкости и, если они недоступны, на рекомендациях по лечению. Многие пациенты поправляются только при консервативном лечении. В американском исследовании более 50% всех пациентов с умеренными и тяжелыми излияниями выздоровели после лечения только антибиотиками [54]. Лечение умеренных излияний зависит от степени респираторного нарушения у ребенка: если клиническое состояние хорошее, целесообразно лечение антибиотиками, а если у ребенка есть признаки респираторного дистресса, лечение такое же, как и при больших излияниях: жидкость следует удалить либо с помощью торакоцентеза через зонд. (для не локализованной жидкости) или плевральной дренажной трубки с фибринолитиками или VATS (оба для локализованной жидкости) [19].После введения плевральной трубки следует удалить не более 10 мл / кг жидкости у маленьких детей и 1,5 литра жидкости у детей старшего возраста и подростков, чтобы избежать повторного расширения отека легких. Когда этот объем будет достигнут, слив следует зажать на час [46]. Нет четких доказательств преимущества в клинических исходах детей, получавших фибринолитики, по сравнению с VATS [55,56]. Рекомендуемые дозы фибринолитических агентов: [19,57,58]:
Урокиназа (недоступна в США) 10 000 ЕД каждые 12 часов в течение 3 дней для детей младше 1 года и 40 000 ЕД каждые 12 часов в течение 3 дней для детей. > 1 года
Стрептокиназа 12000 — 25000 МЕ / кг / доза ежедневно в течение 3-5 дней
Тканевый активатор плазминогена 0.1 мг / кг; максимум 3 мг три раза в день в течение 3-4 дней или 4 мг каждые 24 часа
При использовании стрептокиназы и урокиназы существует риск реакций гиперчувствительности.
Детям, у которых не наблюдается улучшения, несмотря на антибиотики, дренаж и фибринолитики, следует пройти курс VATS, чтобы удалить фибринозные спайки и удалить густую локализованную жидкость. Представляется разумным спросить мнение хирурга, если состояние пациента не улучшается после 7 дней лечения. Еще одно показание к операции — бронхоплевральный свищ при пиопневмотораксе [46].В качестве альтернативы VATS, особенно при организованной эмпиеме у ребенка с не разрешающимися признаками системной инфекции с лихорадкой, следует рассмотреть формальную торакотомию с декортикациями [19]. Согласно рекомендациям BTS показаниями для направления на операцию являются клинические признаки и симптомы, а не аберрантная рентгенологическая картина у бессимптомного ребенка [46]. Факторы риска неэффективности трубочной торакостомии включают продолжительность симптомов> 7 дней до процедуры, сложную многолучевую эмпиему, пневматоцеле, легочный некроз и основное заболевание [59, 60].Пневматический зонд можно удалить, если вывод жидкости составляет <1 мл / кг / день, рассчитанный за последние 12 часов, или 50-60 мл / день и нет утечки воздуха [19].
Более агрессивным подходом является выполнение ВАТС в первые 48 часов лечения. Это дает шанс для бактериологического диагноза и более короткого пребывания в больнице, хотя не все исследования подтверждают последнее наблюдение [54].
Оптимальная продолжительность лечения антибиотиками парапневмонического выпота и эмпиемы зависит от клинического ответа.Рекомендуемый способ введения — внутривенный до тех пор, пока не будет удалена плевральная дренажная трубка, а затем его можно переключить на пероральный путь на срок от 1 до 4 недель или дольше, если ребенок не полностью выздоровел. Однако нет рандомизированных клинических испытаний, подтверждающих этот подход [19,46]. Отдаленный исход у детей благоприятный. Рентгенологические признаки заболевания плевры полностью исчезают в течение 3 месяцев у 80% детей и к 18 месяцам у всех детей. Результаты функциональных тестов легких, а также толерантность к физической нагрузке у большинства пациентов остаются нормальными через 12 месяцев после выписки [46,52,53].Состояния, предрасполагающие к тяжелой пневмонии с плевральным выпотом и эмпиемой, включают иммунодефицит и муковисцидоз, и их следует исключить в течение периода наблюдения [46].
12.2. Абсцесс легкого
Абсцесс легкого представляет собой толстостенную полость, содержащую некротическую ткань диаметром 2 см и более, вызванную инфекцией [28]. Это может быть как первичное — у здоровых детей без патологий легких, так и вторичное — у детей с основным заболеванием, предрасполагающим к заболеванию легких.Наиболее важным механизмом образования абсцесса легкого является аспирация, особенно у детей с нервно-мышечными нарушениями. Другие факторы риска включают иммунодефицит, основное заболевание легких, такое как врожденные пороки развития, муковисцидоз, проблемы с глотанием, например. ахалазия, плохая гигиена полости рта. Абсцессы также могут возникать в результате гематогенного распространения из-за сепсиса или правостороннего бактериального эндокардита, распространения из очагов в брюшной полости или заглоточном пространстве или из-за обструкции дыхательных путей инородным телом [61,62].
Основными возбудителями обычно являются стрептококки, анаэробные бактерии, S. aureus и Klebsiella pneumonia , однако есть редкие сообщения о других возбудителях, включая Mycoplasma pneumoniae [63]. Часто встречаются смешанные инфекции. Наиболее частые места формирования абсцесса легкого в положении лежа: правая верхняя доля, левая нижняя доля и верхушечные сегменты обеих нижних долей. Когда пациент аспирирует в положении лежа на спине, обычно поражаются задние сегменты верхних долей.
Клинические симптомы включают кашель, выделение гнойной мокроты, лихорадку, одышку, боль в груди, тахипно, потерю веса, кровохарканье, недомогание / летаргию. Физические признаки не отличаются от неосложненной пневмонии, можно оценить снижение шума дыхания и тупую ноту при перкуссии. Симптомы могут сохраняться в течение нескольких недель [61].
Диагноз обычно ставится на рентгенограмме грудной клетки, на которой виден воспалительный инфильтрат паренхимы легких с полостью, содержащей воздух-жидкость. Первоначально это может выглядеть как твердое поражение, окруженное альвеолярным инфильтратом.Может присутствовать выпуклая трещина, представляющая увеличенный объем пораженной доли. КТ обычно выполняется для исключения других осложнений, таких как эмпиема, пневмотоцеле, лежащие в основе врожденные аномалии, такие как секвестрация, бронхогенная киста или аденоматоидная мальформация. Особенности, отличающие абсцесс от других образований, включают хорошо окаймленные стенки, большую плотность, чем у воды, усиление контраста в прилегающих тканях (Рисунок 4, Рисунок 5) [61].
Рис. 5.
Проникновение с уровнем воздух-жидкость в верхнем поле правой доли.Абсцесс легкого.
Основа лечения — консервативная антибактериальная терапия, спектр которой охватывает S. pneumoniae, S. aureus , а также грамотрицательные палочки и анаэробы в случае вторичного абсцесса. У пациентов с ослабленным иммунитетом антибиотики должны покрывать грибковые патогены. Антибиотик выбора — пенициллин с клиндамицином или метронидазол. Другие эксперты рекомендуют цефалоспорин и флуклоксациллин третьего поколения, тикарциллин, ампициллин / клавулановую кислоту и пиперациллин / тазобактам.Следует учитывать возможность инфицирования MRSA, особенно если абсцесс осложняет пневмонию или является результатом гематогенного распространения из других органов [61,62]. Обычно рекомендуется 2-3-недельный курс внутривенной терапии с последующим пероральным лечением в течение 4-8 недель [28]. В опытных центрах интервенционной радиологии выполняется аспирация абсцесса легкого под контролем КТ и установка катетера «косичка» в диагностических и терапевтических целях. Хирургическое вмешательство показано при абсцессах, которые не проходят, несмотря на лечение.
Общий результат благоприятный, смертность намного ниже, чем у взрослых: <5% и в основном встречается у детей с вторичными абсцессами легких или сопутствующими заболеваниями. Осложнения включают эмпиему или пиопневмоторакс, если абсцесс прорывается в плевральную полость, бронхоплевральный свищ, если связь между полостью абсцесса и плевральной полостью сохраняется, и локализованные бронхоэктазы.
12.3. Некротизирующая пневмония
Некротическая пневмония (НП), определяемая как множественные полостные поражения в консолидированных областях, является редким, но все чаще обнаруживаемым осложнением у детей.Он характеризуется разжижением и кавитацией легочной ткани [63]. Наиболее часто ассоциированным патогеном является Streptococcus pneumoniae , особенно серотипы 3 и 14. Другие вовлеченные патогены включают Streptococci группы A, Staphylococcus aureus и Mycoplasma pneumoniae [64-68]. Большинство пациентов не имеют предшествующего медицинского анамнеза. Некротическая пневмония следует подозревать у пациентов с осложненной пневмонией, состояние которых не улучшается, несмотря на оптимальное лечение.Диагноз можно установить с помощью компьютерной томографии. Рентгенологические критерии некротической пневмонии включают потерю нормальной структуры паренхимы легких и наличие участков разжижения, замененных в течение 1-2 дней множественными небольшими полостями [64]. Некротическая пневмония часто сочетается с плевральным выпотом.
Лечение заключается в длительном внутривенном введении антибиотиков, активных против возбудителей ВП, включая резистентные штаммы S. pneumoniae . Детям с НП противопоказаны интервенционные процедуры, так как они могут увеличить риск таких осложнений, как образование бронхоплевральной фистулы [35].В целом, несмотря на длительный курс лечения в стационаре и связанную с этим заболеваемость, долгосрочные результаты у большинства детей благоприятны. Летальность составляет 5,5-7% [28,65].
13. Профилактика
Чтобы предотвратить пневмонию, можно принять несколько мер, начиная с общих рекомендаций, таких как улучшение питания, жилищных условий, систем отопления, уменьшение воздействия табачного дыма, поощрение грудного вскармливания в течение первых 6 месяцев, а также более конкретные меры инфекционного контроля, такие как мытье рук, избегание людей с признаками инфекций дыхательных путей и вакцинация.Для профилактики пневмонии рекомендуется иммунизация против следующих микроорганизмов:
вирус гриппа
Streptococcus pneumoniae (конъюгированная и неконъюгированная вакцина)
Haemophilus influenzae
вирус кори
вирус ветряной оспы
Bordatella pertussiss
Mycobacterium tuberculosis
Младенцы высокого риска с гемодинамическими заболеваниями, недоношенные, недоношенные дисплазия, врожденные аномалии дыхательных путей и нервно-мышечные заболевания должны получать иммунопрофилактику с использованием специфических моноклональных антител к RSV (паливизумаб) в сезон RSV [68].
AAP рекомендует рутинное использование 13-валентной пневмококковой конъюгированной вакцины (PCV13) для здоровых детей в возрасте от 2 до 59 месяцев и для детей в возрасте от 60 до 71 месяца с основным заболеванием, которое увеличивает риск инвазивного пневмококкового заболевания (IPD). ) [69]. Основные медицинские состояния, указывающие на необходимость иммунизации против пневмококков, включают:
хроническое заболевание сердца, в частности цианотический врожденный порок сердца и сердечную недостаточность
хроническое заболевание легких, включая астму, при длительном лечении пероральными кортикостероидами в высоких дозах
сахарный диабет
утечки спинномозговой жидкости
кохлеарный имплант
функциональная или анатомическая аспления, в том числе дети с серповидноклеточной анемией и другими гемоглобинопатиями,
- , хроническая почечная недостаточность, иммунодефицитная инфекция, почечная недостаточность
заболевания, связанные с лечением иммунодепрессантами или лучевой терапией (включая злокачественные новообразования, лейкозы, лимфомы, болезнь Ходжкина, трансплантацию твердых органов) и врожденный иммунодефицит (включая дефицит B- (гуморальный) или T-лимфоцитов; com дефицит элементов, особенно C1, C2, C3 и C4, и фагоцитарные нарушения, за исключением хронической гранулематозной болезни).
Здоровые дети <5 лет и дети с сопутствующими заболеваниями <6, которые полностью иммунизированы ЦВС7, должны получить однократную дополнительную дозу ЦВС13. Дети в возрасте от 6 до 18 лет с заболеваниями, благоприятствующими ИПИ (перечисленные выше), должны получить разовую дозу PCV13 независимо от того, получали ли они ранее PCV7 или PPSV23 (рекомендуется 2 дозы PPSV23). PCV13, который в дополнение к 7 серотипам, включенным в PCV7 (4,6B, 9V, 14,18C, 19F, 23F), содержит 6 серотипов пневмококка (1,3,5,6A, 7F, 19A), ответственных за 63% случаев. Инвазивного пневмококкового заболевания у детей младше 5 лет в США был лицензирован Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США в 2010 году для использования у детей в возрасте от 2 до 71 месяца.Из-за расширенного охвата он предназначен для замены PCV7 [69].
14. Специфические бактериальные причины пневмонии
14.1.
Streptococcus pneumoniae
Streptococcus pneumoniae является наиболее частым возбудителем ВП у детей и наиболее частой причиной смертности от пневмонии у детей во всем мире. Он является причиной не менее 1,2 миллиона случаев смерти младенцев ежегодно, в основном в странах Африки к югу от Сахары и в Азии [45]. Известно 92 серотипа пневмококков, различающихся полисахаридной капсулой.Было обнаружено, что серотипы коррелируют с различными исходами пневмонии, однако результаты исследования не являются однозначными. У педиатрических пациентов серотипы 7F, 23F и 3 коррелировали с самым высоким риском смерти в ходе инвазивного пневмококкового заболевания [70]. В другом исследовании серотипы 1,6,14,19 были наиболее распространенными среди детей с осложненной пневмонией, при этом серотип 1 являлся причиной 24,4% осложненных случаев по сравнению с 3,6% неосложненных случаев [71].
S. pneumoniae обычно колонизирует эпителий носоглотки у 20-40% здоровых детей и> 60% младенцев и детей в детских садах.После колонизации новый штамм устраняет другие конкурирующие серотипы пневмококков и сохраняется в течение месяцев в состоянии носителя. Бактерии с так называемым «фенотипом стойкой колонизации» с низким риском тканевой инвазии несут ответственность за постоянную передачу в человеческих популяциях и вызывают приобретенный B-клеточный иммунитет к повторной инфекции. Чтобы облегчить их пребывание в носоглотке и избежать защиты хозяина, они используют различные механизмы, такие как поверхностные адгезии, протеаза IgA1 и ингибиторы антибактериальных пептидов.Дефекты защитных механизмов хозяина могут нарушить баланс и привести к инфекции у хозяина с ослабленным иммунитетом. Другой фенотип — так называемый «фенотип инвазивного пневмококкового заболевания» может эффективно передаваться от человека к человеку при кашле и быстро вызывать заболевание. Его основным фактором вирулентности является полисахаридная капсула, которая предотвращает механическое удаление слизистых выделений, ограничивает автолиз, снижает воздействие антибиотиков и способствует инвазии и распространению. К другим факторам вирулентности относятся: порообразующий цитотоксин — пневмолизин, который среди других патологических эффектов способен подавлять цилиарное движение эпителиальных клеток и ослаблять респираторный выброс фагоцитарных клеток.Недавнее приобретение инвазивного серотипа более важно с точки зрения дальнейшей инфекции, чем длительная колонизация, и фактически признано одним из определенных факторов риска пневмококковой пневмонии [45].
Некоторые из иммунных механизмов хозяина, необходимых для защиты от пневмококковой пневмонии, представляют собой толл-подобные рецепторы (TLR). Дети с генетической недостаточностью общего адаптивного белка TLR — белка первичного ответа миелоидной дифференцировки 88 (MyD88) или киназы 4, связанной с рецептором интерлейкина-1 (IRAK4), киназы, действующей непосредственно ниже MyD88, особенно восприимчивы к инвазивному пневмококковому заболеванию. .Другим генетическим фактором, предрасполагающим к инвазивному пневмококковому заболеванию, является полиморфизм генов, кодирующих ингибиторы ядерного фактора κΒ, и дефекты пути комплемента C3, важные для опсонизации и, следовательно, клиренса пневмококков [45].
Пневмония обычно начинается с вирусной инфекции верхних дыхательных путей. Возбудителем, который чаще всего ассоциируется с двойным инфицированием Streptococcus pneumonia , является вирус гриппа. Совместное инфицирование вирусом гриппа ослабляет иммунный ответ хозяина, уменьшая его способность устранять пневмококк.Вирус гриппа обладает нейраминидазой, которая, воздействуя на определенные рецепторы, способствует прикреплению пневмококка к респираторному эпителию [72]. Местные системы врожденной иммунной защиты, такие как мукоцилиарный клиренс, кашлевой рефлекс, антимикробные пептиды, обычно успешно устраняют патоген. В случае неудачи возникает пневмония. Клинические симптомы характерны для бактериальной пневмонии с высокой температурой, ознобом, недомоганием, кашлем и одышкой. У детей старшего возраста кашель становится продуктивным с гнойной мокротой с кровянистым оттенком.Плевральное вовлечение — довольно распространенное явление. Нелеченная пневмококковая пневмония может прогрессировать до дыхательной недостаточности, септического шока и, как следствие, смерти.
Обычное рентгенологическое проявление пневмококковой пневмонии — крупозная пневмония, часто сопровождающаяся небольшим плевральным выпотом. Изменения могут быть ограничены одним сегментом или затрагивать несколько сегментов или долей или проявляться как бронхопневмония [41].
После повсеместного внедрения пневмококковой конъюгированной 7-валентной вакцины в 2000 г. произошло снижение заболеваемости пневмококковой пневмонией у детей <5 лет [7].Однако есть опасения, что серотипы, включенные в вакцину, могут быть заменены ранее редкими, потенциально более вирулентными серотипами, такими как серотип 1 или 19A [73,74]. К счастью, эти серотипы были включены в новую конъюгированную 13-валентную вакцину.
Существует проблема увеличения антибактериальной устойчивости — до 10% культивированных изолятов пневмококка в Европе в 2008 г. не чувствительны к пенициллину, хотя влияние устойчивости in vitro на клинические исходы пациентов не так ясно.К счастью, не было зарегистрировано увеличения смертности или частоты осложнений у детей, инфицированных резистентными штаммами [71,73,74].
14.2.
Staphylococcus aureus
Заболеваемость Staphylococcus aureus пневмонией значительно возросла за последние 20 лет. Растущее число (до 76% в Техасе) ассоциированных с сообществами S. aureus устойчиво к метициллину (CA-MRSA) и в некоторых регионах стало основной причиной осложненной ВП у детей [75–77].CA-MRSA был впервые описан в 1990-х годах как причина инфекции у ранее здоровых детей и подростков раннего возраста, не госпитализированных ранее или не поступавших в медицинские учреждения для хронических больных [77]. Также наблюдается значительное увеличение носовой колонизации здоровых детей MRSA — в другом исследовании из США 36,4% здоровых детей были колонизированы S. aureus и 9,2% — MRSA. CA-MRSA имеет собственный генотип, отличный от штаммов, приобретенных в больнице [77]. Стоит отметить, что 22% штаммов MRSA имели локус гена для PVL, а в британском исследовании 11% всех S.aureus от больных пневмонией несли этот ген [78,79]. Даже если влияние носовой колонизации на риск пневмонии неясно, поскольку у 1/3 пациентов со стафилококковой инфекцией не было зарегистрировано предшествующей колонизации [80], эти данные показывают широкое распространение MRSA в сообществе.
Первичная пневмония S. aureus возникает в результате прямого проникновения в легкие через трахеобронхиальное дерево, а вторичная пневмония возникает в результате гематогенного распространения. с.aureus CAP обычно возникает у очень маленьких детей: 30% случаев возникают у детей младше 3 месяцев и 70% — у детей младше 1 года, чаще у мальчиков [60]. CA-MRSA CAP часто встречается у детей в возрасте до 3 месяцев. здоровых детей и подростков, и во многих случаях этому предшествует грипп или гриппоподобное заболевание или инфекция кожи и мягких тканей. Быстро развиваются тяжелые респираторные симптомы и гипотензия. Клон USA300 связан с венозным тромбозом и последующей септической тромбоэмболией легочной артерии [77].
S. aureus обладает множеством факторов вирулентности, включая поверхностные белки (например, протеин А), которые способствуют прилипанию и, следовательно, колонизации тканей хозяина, инвазии (лейкоцидин, киназы и гиалуронидаза), которые способствуют распространению бактерий в тканях и токсинам, повреждающим мембраны (например, упомянутый выше лейкоцидин). Было несколько сообщений о пневмонии, вызванной лейкоцидином Panton-Valentine, продуцирующим Staphylococcus aureus , у ранее здоровых детей и подростков.Пористый токсин, кодируемый генами luk-S-PV и luk-F-PV , лизирует нейтрофилы, вызывая усиленный, хотя и неэффективный воспалительный ответ. Пациенты поступают с быстро прогрессирующей некротической пневмонией, проявляющейся лихорадкой, лейкопенией и кровохарканьем, которым предшествует вирусная инфекция, наиболее распространенный грипп [75]. Лейкопения характерна для ПВЛ и считается вторичной по отношению к лейкоцидину, разрушающему лейкоциты [77]. На рентгенограмме видны множественные узловые инфильтраты, обычно односторонние, которые могут переходить в полостные поражения и пневмоцеле.Рентгенологическое прогрессирование инфильтратов может быть очень быстрым и должно повысить вероятность пневмонии S. aureus . Другой характерный рентгенологический признак — пневматоцеле — встречается более чем в половине случаев, и его размер и количество могут меняться ежечасно [61]. Стафилококковая пневмония часто осложняется эмпиемой, образованием абсцессов легких, пневмотораксом и острым респираторным дистресс-синдромом (ОРДС).
Учитывая тяжелый и потенциально смертельный характер инфекции, быстрое начало соответствующей антибактериальной терапии имеет решающее значение.Для госпитализированных пациентов с пневмонией, вызванной чувствительным к метициллину S. aureus PIDS рекомендует внутривенную терапию пенициллином, стабильным к β-лактамазе (оксациллин, клоксациллин, флуклоксациллин или нафциллин) или цефалоспорином первого поколения (цефазолин). При более тяжелых инфекциях некоторые эксперты рекомендуют комбинированную терапию аминогликозидами или рифампицином, хотя данные контролируемых клинических исследований, подтверждающих эти рекомендации, отсутствуют [19]. Первой линией лечения госпитализированных детей с подозрением на CA-MRSA является ванкомицин.Однако есть опасения по поводу адекватной концентрации препарата в жидкости эпителиальной выстилки легких — у взрослых было показано, что он достигает 18% от сывороточного уровня [77]. Альтернативными вариантами являются линезолид и клиндамицин, которые обладают дополнительным преимуществом, заключающимся в блокировании выработки токсина PVL и стафилококковых экзотоксинов, поэтому они являются препаратами выбора при лечении инфекций PVL-CA. Клиндамицин следует использовать с осторожностью, учитывая данные о местной чувствительности, и его не следует использовать при инфекциях с высоким посевом, таких как эмпиема, поскольку в этом случае существует высокий риск того, что бактерии будут постоянно продуцировать метилазу [19].Линезолид достигает более высоких концентраций в эпителиальной выстилке легких [80].
14.3.
Mycoplasma pneumoniae
Mycoplsamas — самые маленькие самовоспроизводящиеся организмы, способные жить вне клеток-хозяев. У них нет клеточной стенки, но клеточная мембрана, содержащая стерины, плохо окрашивается красителем по Граму, а антибиотики, разрушающие стенку бактериальной клетки, такие как β-лактамы, неактивны в отношении этих организмов. Mycoplasma pneumonia e пневмония обычно протекает в легкой форме.Передача происходит от человека к человеку, инкубационный период обычно составляет 1-2 недели. Эпидемии происходят примерно с 4-7-летними циклами. Рецидивирующие инфекции обычны.
Инфекции, вызываемые Mycoplasma pneumonia, — обычное явление. Антитела присутствуют у 1/3 всех младенцев от 7 до 12 месяцев жизни и более чем у 90% подростков. Очень мало инфекций возникает у младенцев в первые 6 месяцев жизни, вероятно, из-за наличия материнских антител. Недавние исследования показывают, что вопреки предыдущим сообщениям M.pneumoniae CAP также довольно часто встречается у детей младше 4 лет. Эти микроорганизмы ответственны за инфекций в этой возрастной группе [81].
Микроорганизмы передаются через дыхательные пути. В дыхательных путях они прикрепляются к рецепторам на респираторном эпителии через спайки. Повреждение легких при пневмонии M. pneumoniae связано с клеточным иммунитетом хозяина и также сопровождается цилиостазом [81].
Пациенты обращаются с симптомами инфекции верхних дыхательных путей, лихорадкой, недомоганием, головной болью.Симптомы развиваются постепенно. Кашель, который изначально непродуктивен, появляется через 3-5 дней от начала заболевания. Сопутствующие симптомы включают охриплость, озноб, боль в груди, рвоту, тошноту, диарею и миалгию. Насморк — редкая находка, плевральный выпот встречается у 5-20% пациентов. При аускультации могут присутствовать хрипы, хрипы и бронхиальное дыхание. Mycoplasma pneumonie может проявляться внелегочным поражением, включая неэкссудативный фарингит, шейную лимфаденопатию, средний отит, конъюнктивит, артрит и сыпь.Заболевание обычно проходит в течение 3-4 недель, но у детей с серповидно-клеточной анемией и синдромом Дауна оно может быть более тяжелым. Mycoplasma может вызывать обострения у пациентов с астмой [28].
Рентгенологические данные варьируют от ретикулярного и интерстициального до долевых уплотнений. Корневая лимфаденопатия встречается у 1/3 пациентов. Характерной чертой является слабая корреляция между клиническими симптомами и физическими и радиологическими данными.
Лечение выбора — антибиотики группы макролидов.
В редких случаях Mycoplasma pneumonia e Пневмония может быть тяжелой с массивной долевой консолидацией, плевральным выпотом, абсцессом легкого или образованием пневматоцеле. Иногда лихорадка и рентгенологические изменения прогрессируют, несмотря на стандартную терапию макролидами. Есть одно сообщение об успешном лечении рефрактерной пневмонии у детей метилпреднизолоном [82]. Описаны редкие осложнения — облитерирующий бронхиолит и диффузный интерстициальный фиброз. У 1/3 детей через 1–2 года после инфицирования Mycoplasma pneumoniae наблюдаются патологические изменения, включая мозаичную перфузию, бронхоэктазы, утолщение бронхиальной стенки, снижение кровоснабжения и задержку воздуха [81].Внелегочные осложнения пневмонии Mycoplasma вызывают симптомы со стороны самых разных органов и систем. К ним относятся:
нервная система: менингоэнцефалит, поперечный миелит, краниальная невропатия, миелорадикулопатия, полиомиелитоподобный синдром, психоз, синдром Гийена-Барре
кожа: эритематозная, пятнисто-пузырчатая, многопузырчатая, многопузырчатая, многопузырчатая и синусно-синяя. синдром
сердце: перикардит, миокардит, застойная сердечная недостаточность, блокада сердца
желудочно-кишечный тракт: тошнота, рвота, диарея, печеночная дисфункция, желтуха
тромбоцитологическое кровоизлияние в сосудистую анестезию
опорно-двигательного аппарата: миалгии, артралгии
мочеполовой системы: гломерулонефрит, интерстициальный тубулонефрит
15.Госпитальная пневмония
Госпитальная пневмония (ВП) определяется как пневмония, которая возникает через 48 часов или более после госпитализации у пациента, у которого не было признаков заболевания на момент обращения в больницу [83]. Его можно далее разделить на раннее начало (48–96 часов после поступления), обычно вызванное патогенами, ответственными за ВП, и позднее начало (> 96 часов после поступления), вызванное нозокомиальными патогенами с множественной лекарственной устойчивостью [84].
Пневмония, связанная с ИВЛ (ВАП), тип ГАП, поражающий пациентов с механической вентиляцией легких, определяется как пневмония, которая возникает более чем через 48 часов после интубации [83].
Третий тип, описанный совсем недавно, представляет собой пневмонию, связанную с оказанием медицинской помощи (HCAP), которая развивается у пациентов, которые соответствуют одному из следующих условий:
госпитализация на 2 или более дней в течение 90 дней после заражения
проживание в доме престарелых или учреждении длительного ухода
антибиотикотерапия или химиотерапия или уход за раной в течение 30 дней после заражения
посещение центра гемодиализа [83].
Определение HCAP не было валидировано у детей, хотя из-за растущего числа педиатрических пациентов с хроническими заболеваниями (например, церебральный паралич, синдромы врожденных пороков развития, хронические заболевания легких, сердца и почек), которые часто имеют контакты Что касается медицинского персонала, HCAP представляет собой серьезную проблему для этой группы населения.
HAP встречается у 16-29% педиатрических пациентов и составляет 10-15% всех нозокомиальных инфекций у детей и до 67% нозокомиальных инфекций у детей, госпитализированных в педиатрические отделения интенсивной терапии [85-87].ВАП встречается примерно у 3–32% пациентов в педиатрических отделениях интенсивной терапии на ИВЛ [87,88]. В Европе это самая распространенная, а в США вторая по частоте нозокомиальная инфекция у детей, находящихся на лечении в отделениях интенсивной терапии [88–90]. Смертность при ВП намного выше, чем при ВП, и составляет от 10 до 70% в зависимости от этиологических факторов и сопутствующих заболеваний [85,86,88]. HAP и VAP, в частности, увеличивают продолжительность пребывания в больнице и затраты на лечение [86,88,91].
Наиболее распространенными этиологическими факторами ГП у детей являются респираторные вирусы, включая респираторно-синцитиальный вирус, аденовирус, вирусы гриппа и парагриппа.Бактерии, ответственные за позднее начало ГП, включают грамотрицательные палочки: Pseudomonas aeruginosa, Escherichia coli, Klebsiella pneumonia, Acinetobacter spp. , Serratia spp .., грамположительные организмы, особенно. Staphylococcus aureus и коагулазо-отрицательные Staphylococci. P. aeruginosa — наиболее распространенный бактериальный патоген в детских отделениях интенсивной терапии, связанный со смертностью до 80% [90]. Большинство бактерий, вызывающих внутрибольничные инфекции, обладают множественной лекарственной устойчивостью, в том числе устойчивостью к метициллину Staphylococci (MRSA) и β-лактамазой расширенного спектра (ESBL), продуцирующей грамотрицательные палочки.Дети с ослабленным иммунитетом подвергаются особому риску заражения грибками, в частности. Aspergillus , Candida и Pneumocystis jiroveci . В 38% случаев этиология ВАП у детей полимикробная [88].
Факторы риска госпитальной пневмонии включают интубацию и искусственную вентиляцию легких (увеличивает риск в 6–21 раз), нервно-мышечную блокаду, продолжительность пребывания в больнице, иммуносупрессию, недавнее лечение антибиотиками и блокаторами h3, а также перенаселенность и нехватку персонала. палаты больницы [85,86].Генетический синдром, женский пол, реинтубация, транспортировка из отделения интенсивной терапии, хирургическое вмешательство перед поступлением в реанимацию, энтеральное питание, употребление наркотических препаратов оказались независимыми факторами риска ВАП у детей [88,91].
Нозокомиальную пневмонию следует подозревать у любого ребенка с новыми респираторными симптомами во время пребывания в больнице, гипоксемией, повышенными потребностями в кислороде или вентиляции, повышенным количеством или измененными характеристиками респираторных выделений. Большинство определений включают клинические и радиологические признаки, некоторые дополнительные бактериологические и лабораторные данные [83,92].По данным Национальной сети центров по контролю за заболеваниями (CDC) по безопасности здравоохранения, HAP может быть диагностирован у пациентов с новыми радиологическими изменениями (инфильтрат, уплотнение, кавитация, пневматоцеле у младенцев на 1 -м -м году жизни) и по крайней мере в трех клинических случаях. критерии (клинически определяемая пневмония) или два клинических и один лабораторный критерий. У детей с основным заболеванием легких или сердца рентгенологические изменения должны быть подтверждены как минимум на двух последовательных рентгенограммах. Клинические критерии, которые должны быть выполнены, включают:
лихорадка> 38 0 C без другой причины или
лейкопения (<4000 / мм 3 ) или лейкоцитоз (≥12000 / мм 3 ) и по крайней мере один (или два для клинически определяемой пневмонии) из следующего:
новое начало гнойной мокроты,
увеличение респираторного секрета,
изменение характера мокроты или респираторного секрета,
новое начало или ухудшение респираторных симптомов: кашель, тахипноэ, одышка,
аускультационные данные: хрипы, бронхиальные шумы,
повышенная потребность в кислороде, PaO 2 / FiO ≤ 240
У детей в возрасте до 12 лет клинические критерии немного отличаются, и необходимо выполнение как минимум трех (два для младенцев до 1 года). К ним относятся:
лихорадка> 38 0 C или гипотермия <36,5 0 C (или нестабильность температуры для младенцев до 1 года) без других причин или
лейкопения (<4000 / мм 3 ) или лейкоцитоз (≥15000 / мм 3 ) и ≥10% незрелых форм (младенцы ≤1 года)
новое начало гнойной мокроты,
увеличение респираторного секрета,
изменение характера мокроты или респираторного секрета,
новое начало или ухудшение респираторных симптомов: апноэ, кашель, тахипноэ, одышка,
расширение носа с втягиванием грудной стенки или хрипом, хрипы — младенцы ≤1 год в возрасте
аускультационные данные: хрипы, бронхиальные шумы,
брадикардия (<100 ударов в минуту) или тахикардия (> 170 ударов в минуту) — младенцы до 1 года
повышенная потребность в вентиляции, гипоксемия (Sat <94%) - это условие обязательно для детей младше 1 года.
Лабораторные критерии включают положительные посевы крови (не связанные с другими инфекциями), плевральную жидкость или образцы из нижних дыхательных путей (бронхоальвеолярный лаваж — БАЛ или защищенная чистка образцов щеткой), внутриклеточные бактерии, обнаруженные в ≥5% клеток, полученных из БАЛ при прямом микроскопическом исследовании — гистопатологические доказательства формирования абсцесса, очаговых уплотнений, интенсивного накопления полиморфноядерных клеток в мелких дыхательных путях, инвазии паренхимы легких гифами или псевдогифами.Диагностическая ценность БАЛ у детей с ВАП составляет 50-72% и специфичность 80-88%, а количественная оценка внутриклеточных организмов в образцах БАЛ 30-55% и 89-95% соответственно [93-96]. Лабораторные критерии HAP, вызванного атипичными бактериями ( Mycoplasma spp. , Chlamydophila spp. , Legionella spp.) Или вирусами включают: положительный посев из респираторного секрета, положительное определение антигена или антител в респираторном секрете, 4 раза Повышение уровня IgG в парных сыворотках, положительная ПЦР, обнаружение в моче Legionella pneumophila серогруппы 1 [92].
Бактериологический диагноз часто затруднен, поскольку госпитализированные пациенты обычно колонизированы патогенной флорой. Поэтому количественный критерий бактериального выхода (≥10 4 КОЕ / мл или ≥10 4 КОЕ / г ткани в случае образца паренхимы легких) был установлен для помощи в этиологической диагностике пневмонии [92]. Применимость инвазивных диагностических методов (биопсия легких) остается спорной из-за опасений осложнений у нестабильных или тяжелобольных пациентов и отсутствия данных, подтверждающих их влияние на клиническое течение или показатели смертности.
Пациенты с HAP чаще всего являются ослабленными людьми с множественными основными заболеваниями. HAP — тяжелое заболевание с высокой смертностью. Поэтому диагноз должен быть установлен как можно быстрее с использованием широкого набора диагностических инструментов и методов, а эмпирическое лечение должно проводиться незамедлительно, пока не завершены посевы и другие микробиологические исследования. Спектр антибиотиков должен быть достаточно широким, чтобы охватить грамотрицательные и грамположительные бактерии, с учетом предыдущего воздействия антибиотиков, местной флоры, моделей чувствительности к противомикробным препаратам и рекомендаций специалиста по инфекционным заболеваниям.Факторы риска приобретения устойчивых к антибиотикам грамотрицательных бактерий у пациентов педиатрического отделения интенсивной терапии (PICU) включают более молодой возраст, тяжелое общее состояние (оценивается на основе оценки PRISM {детский риск смертности}), внутривенное введение антибиотиков в предыдущие 12 месяцев, Госпитализация в ОИТ в прошлом, контакты с хроническими больными [87,94]. Несоответствующее лечение антибиотиками связано с повышенной смертностью у пациентов с ГП [90]. Детей с ранним началом HAP можно лечить как детей с CAP, если у них нет специфических факторов риска HCAP, VAP или колонизации бактериями с множественной лекарственной устойчивостью.Пациенты PICU должны получать страхование от Pseudomonas aeruginosa (аминогликозид с соответствующим β-лактамом: пиперациллин, цефтазидим или цефепим) и в больничных палатах, где заболеваемость метициллинорезистентными стафилококками или БЛРС, продуцирующими грамотрицательные бактерии, превышает 5%, производное ванкомициллина, карбреапенициллин, карбамициллин и ванкомицин. плюс ингибитор β-лактамазы, соответственно, следует включать в эмпирические схемы лечения [92]. Детям с иммунодефицитом следует назначать противогрибковые препараты.Как только станет известен возбудитель и его чувствительность, следует подбирать терапию с использованием агента самого узкого доступного спектра. Антибиотики следует вводить внутривенно и, по возможности, переходить на пероральный путь после улучшения состояния пациента.
Меры инфекционного контроля, которые необходимо тщательно выполнять, чтобы уменьшить количество HAP, включают:
надлежащую гигиену рук, использование перчаток
средства индивидуальной защиты — маски для лица, особенно в периоды повышенной заболеваемости респираторные вирусы
когорта пациентов, инфицированных или колонизированных устойчивыми микроорганизмами
сестринское дело: полулежачее положение для пациентов, находящихся на ИВЛ, уход за полостью рта
использование неинвазивной вентиляции вместо механической вентиляции у соответствующих пациентов
07
- 90 уход за медицинским оборудованием: контуры вентиляторов, отсасывающие устройства, оборудование для проверки функции легких
предотвращение перенаселенности и нехватки кадров
избегание H 2 антагонистов
разумное использование антибиотиков
- 0 методы иммунизации (как описано выше для CAP).
Благодарности
Авторы выражают благодарность Катажине Йончик-Поточна, доктору медицины, за ее прекрасную помощь в проведении радиологических исследований.
Внебольничная пневмония — легочные заболевания
Диагностика этиологии может быть затруднена. Тщательный анамнез воздействия, путешествий, домашних животных, хобби и других воздействий необходим, чтобы вызвать подозрение в отношении менее распространенных организмов.
Идентификация возбудителя может быть полезна для направления терапии и проверки чувствительности бактерий к антибиотикам.Однако из-за ограничений современных диагностических тестов и успеха эмпирического лечения антибиотиками эксперты рекомендуют ограничить попытки микробиологической идентификации (например, посевы, специфический анализ антигена), если пациенты не находятся в группе высокого риска или у них есть осложнения (например, тяжелая пневмония, иммунодефицит). , аспления, отсутствие ответа на эмпирическую терапию). В целом, чем мягче пневмония, тем меньше требуется таких диагностических исследований. Пациенты в критическом состоянии нуждаются в наиболее интенсивном обследовании, как и пациенты, у которых подозревается наличие антибиотикоустойчивого или необычного микроорганизма (например, Mycobacterium tuberculosis , P.jirovecii ) и пациентов, состояние которых ухудшается или которые не реагируют на лечение в течение 72 часов.
Рентген грудной клетки Обычно нельзя отличить один тип инфекции от другого, хотя следующие результаты наводят на мысль:
Многодолевые инфильтраты предполагают инфекцию S. pneumoniae или Legionella pneumophila .
Интерстициальная пневмония (на рентгенограмме грудной клетки проявляется в виде увеличенных интерстициальных отметин и субплевральных ретикулярных помутнений, которые увеличиваются от верхушки к основанию легких) предполагает вирусную или микоплазменную этиологию.
Кавитирующая пневмония предполагает наличие S. aureus или грибковую или микобактериальную этиологию.
Посев крови , который часто получают у пациентов, госпитализированных с пневмонией, может идентифицировать возбудителей бактериальных заболеваний, если присутствует бактериемия. Около 12% всех пациентов, госпитализированных с пневмонией, имеют бактериемию; На S. pneumoniae приходится две трети этих случаев.
Анализ мокроты может включать окрашивание по Граму и посев для идентификации патогена, но ценность этих тестов является неопределенной, поскольку образцы часто загрязнены ротовой флорой и общий диагностический результат невысок. Тем не менее, идентификация бактериального патогена в посеве мокроты позволяет провести тестирование на чувствительность. Получение образцов мокроты также позволяет проводить тестирование на вирусные патогены с помощью прямого флуоресцентного тестирования антител или полимеразной цепной реакции (ПЦР), но при интерпретации следует проявлять осторожность, поскольку 15% здоровых взрослых являются носителями респираторного вируса или потенциального бактериального патогена.У пациентов, состояние которых ухудшается, и у тех, кто не реагирует на антибиотики широкого спектра действия, следует анализировать мокроту с помощью микобактериальных и грибковых пятен и культур.
Образцы мокроты могут быть получены неинвазивным способом путем простого отхаркивания мокроты или после распыления гипертоническим солевым раствором (индуцированная мокрота) у пациентов, не способных выделять мокроту. В качестве альтернативы пациенты могут пройти бронхоскопию или эндотрахеальную аспирацию, которые легко могут быть выполнены через эндотрахеальную трубку у пациентов с механической вентиляцией легких.В противном случае забор бронхоскопии обычно проводят только у пациентов с другими факторами риска (например, с ослабленным иммунитетом, неэффективностью эмпирической терапии).
Анализ мочи на наличие антигена Legionella и пневмококкового антигена в настоящее время широко доступны. Эти простые и быстрые тесты имеют более высокую чувствительность и специфичность, чем окрашивание мокроты по Граму и посев мокроты на эти патогены. Пациенты с риском пневмонии Legionella (например, тяжелое заболевание, неэффективность амбулаторного лечения антибиотиками, наличие плеврального выпота, активное злоупотребление алкоголем, недавние поездки) должны пройти тестирование на антиген Legionella в моче, который остается в наличии еще долгое время после начала лечения. , но тест обнаруживает только л.pneumophila серогруппы 1 (70% случаев).
Тест на пневмококковый антиген рекомендуется для пациентов с тяжелыми заболеваниями; прошли безуспешное амбулаторное лечение антибиотиками; или у кого есть плевральный выпот, активное злоупотребление алкоголем, тяжелое заболевание печени или аспления. Этот тест особенно полезен, если до начала антибактериальной терапии не были получены адекватные образцы мокроты или посевы крови. Положительный тест можно использовать для подбора антибиотикотерапии, хотя он не определяет чувствительность к противомикробным препаратам.
Пневмония | SpringerLink
467997_1_En_6_MOESM1_ESM.zip (2.2 mb)
Рис. E6.1 Тонкая ретрокардиальная пневмония. ( a ) Вид спереди показывает нормальные дискретные трубчатые сосуды позади сердца (TIF 3129 kb)
467997_1_En_6_MOESM2_ESM.zip (283 kb)
Рис. E6.1 Тонкая ретрокардиальная пневмония. ( b ) Затенение сосудов позади сердца (стрелки) указывает на пневмонию (TIF 511 kb)
467997_1_En_6_MOESM3_ESM.zip (406 kb)
Рис. E6.2 Долевая пневмония (правая верхняя доля).Однородное уплотнение правой верхней доли и медиального и заднего сегментов правой нижней доли. Обратите внимание на соответствующие воздушные бронхограммы (стрелки) [1] (TIF 795 kb)
467997_1_En_6_MOESM4_ESM.zip (1.1 mb)
Рис. E6.3 Дольчатая пневмония (правая средняя доля). ( a ) Повышенное помутнение в правом основании медиально формирует правую границу сердца (TIF 1725 kb)
467997_1_En_6_MOESM5_ESM.zip (1,3 mb)
Рис. E6.3 Дольчатая пневмония (правая средняя доля). ( b ) Боковой вид показывает, что помутнение проецируется на сердечную тень (стрелки), что соответствует пневмонии правой средней доли (TIF 2078 kb)
467997_1_En_6_MOESM6_ESM.zip (825 kb)
Рис. e6.4 Дольчатая пневмония (lingula). (A) Область консолидации формирует левую границу сердца (TIF 1400 кб)
467997_1_En_6_MOESM7_ESM.zip (1020 кб)
Рис. E6.4 Дольчатая пневмония (язычок). (B) Боковой вид показывает, что помутнение проецируется на сердечную тень (стрелка), подтверждая его расположение в язычке (TIF 1792 kb)
467997_1_En_6_MOESM8_ESM.zip (1,5 mb)
Рис. E6.5 Лобулярная пневмония (мультифокальная). (A) Неоднородные области помутнения в нижних отделах легких справа (стрелка назад) и слева (белая стрелка) (TIF 2110 kb)
467997_1_En_6_MOESM9_ESM.zip (1,3 mb)
Рис. e6.5 Дольчатая пневмония (мультифокальная). (B) На виде сбоку переднее помутнение (черная стрелка) находится в правой средней доле с резким задним краем у большой трещины. Заднее помутнение (белая стрелка) находится в левой нижней доле, вырисовывается силуэт левой полушарии и дает положительный знак позвоночника (TIF 2010 kb)
467997_1_En_6_MOESM11_ESM.zip (166 kb)
Рис. E6.7 Лобулярная пневмония (мультифокальная). Нечеткие области смешанных интерстициально-альвеолярных инфильтратов в правой верхней доле, наряду с сегментарным матовым стеклом в верхнем сегменте левой нижней доли [2] (TIF 441 kb)
467997_1_En_6_MOESM12_ESM.zip (336 kb)
Рис. e6.8 Интерстициальная пневмония ( Pneumocystis jirovecii ). Диффузное двустороннее помутнение матового стекла с минимальной периферической защитой у пациента со СПИДом [1] (TIF 532 kb)
467997_1_En_6_MOESM13_ESM.zip (339 kb)
Рис. E6.9 Круглая пневмония. Помутнение мягких тканей в заднебоковой части обеих нижних долей (стрелки) с легким двусторонним выступом корней [1] (TIF 646 kb)
467997_1_En_6_MOESM14_ESM.zip (1.2 mb)
Рис. E6.10 Круглая пневмония.( a ) Рентгенограммы демонстрируют новообразование в правой нижней доле (стрелки) (TIF 1776 kb)
467997_1_En_6_MOESM15_ESM.zip (1.2 mb)
Рис. E6.10 Круглая пневмония. ( b ) Рентгенограммы демонстрируют новообразование в правой нижней доле (стрелки) (TIF 2085 kb)
467997_1_En_6_MOESM16_ESM.zip (462 kb)
Рис. E6.10 Круглая пневмония. ( c ) КТ-изображение показывает неправильную полостную массу с воздушными бронхограммами (TIF 1123 kb)
467997_1_En_6_MOESM17_ESM.zip (603 kb)
Рис. e6.10 Круглая пневмония. ( d ) После соответствующей терапии антибиотиками повторное сканирование демонстрирует исчезновение пневмонии и остаточного пневмоцеле (стрелка) (TIF 1271 kb)
467997_1_En_6_MOESM18_ESM.zip (757 kb)
Рис. E6.11 Аспирационная пневмония. Двустороннее помутнение воздушного пространства (открытые стрелки), преимущественно в задней и нижней частях легкого, у пациента с гастроэзофагеальной рефлюксной болезнью. Обратите внимание на правостороннее положение расширенного пищевода (сплошная стрелка) [3] (TIF 1463 kb)
467997_1_En_6_MOESM19_ESM.zip (514 kb)
Рис. e6.12 Липоидная пневмония после аспирации слабительного. Яйцевидное помутнение с практически патогномоничным удалением центрального жира (стрелка) в медиальном сегменте средней доли [3] (TIF 1122 kb)
467997_1_En_6_MOESM20_ESM.zip (1.1 mb)
Рис. E6.13 Постобструктивная пневмония (неспособность пневмонии к Чисто). ( a ) Исходное изображение показывает область помутнения в левом среднем легком (стрелка) (TIF 1582 кб)
467997_1_En_6_MOESM21_ESM.zip (1016 кб)
Рис. E6.13 Постобструктивная пневмония (непереносимость пневмонии). ( b ) Повторное исследование, проведенное через 6 недель после курса антибиотиков, не показало улучшения и побудило заказывать компьютерную томографию (TIF 1434 kb)
467997_1_En_6_MOESM22_ESM.zip (365 kb)
Рис. E6.13 Постобструктивное пневмония (неспособность очиститься от пневмонии). ( c ) Это демонстрирует образование неправильной формы (стрелка), которое оказалось бронхогенной карциномой (TIF 737 kb)
467997_1_En_6_MOESM23_ESM.zip (371 kb)
Рис.e6.14 Пневматоцеле. ( a ) После отравления углеводородами образовалось большое тонкостенное кистозное пространство (стрелка) (TIF 578 kb)
467997_1_En_6_MOESM24_ESM.zip (378 kb)
Рис. E6.14 Pneumatocele. ( b ) У другого пациента имеется несколько тонкостенных пневматоцеле с двух сторон, более выраженные справа [1] (TIF 631 kb)
467997_1_En_6_MOESM25_ESM.zip (1 mb)
Рис. E6.15 Пневматоцеле. В этом пожирателе огня произошли резкие изменения (стрелки) до ( a ) и после ( b ) обработки (TIF 2212 kb)
467997_1_En_6_MOESM26_ESM.zip (665 кб)
Рис. e6.15 Pneumatoceles. В этом пожирателе огня произошли резкие изменения (стрелки) до ( a ) и после ( b ) обработки (TIF 2138 kb)
467997_1_En_6_MOESM27_ESM.zip (1010 kb)
Рис. E6.15 Pneumatoceles. ( c ) Множественные пневматоцеле (стрелки) после рецидивирующих инфекций у пациента со СПИДом [5] (TIF 2424 kb)
467997_1_En_6_MOESM28_ESM.zip (472 kb)
Рис. E6.16 Абсцесс легкого ( Proteus pneumonia). Большая толстостенная полость левой верхней доли с уровнем воздух-жидкость (стрелка) и связанная с ней консолидация [1] (TIF 873 kb)
467997_1_En_6_MOESM29_ESM.zip (396 kb)
Рис. e6.17 Абсцесс легкого (стафилококковая пневмония). Множественные полости с уровнями воздух-жидкость (стрелки), связанные с диффузной консолидацией воздушного пространства и большим плевральным выпотом [1] (TIF 883 kb)
467997_1_En_6_MOESM30_ESM.zip (600 kb)
Рис. E6.18 Абсцесс легкого ( Pneumocystis jirovecii пневмония). ( a ) Консолидация левой верхней доли с уровнем воздух-жидкость (стрелки) у молодого мужчины со СПИДом (TIF 881 kb)
467997_1_En_6_MOESM31_ESM.zip (305 kb)
Рис.e6.18 Абсцесс легкого ( Pneumocystis jirovecii, пневмония). ( b ) Компьютерная томография подтверждает большой абсцесс в верхнем сегменте левой нижней доли с толстыми узловыми стенками и уровнем воздух-жидкость (стрелка) [2] (TIF 588 kb)
467997_1_En_6_MOESM32_ESM.zip (359 kb)
Рис. E6.19 Абсцесс легкого. ( a ) Полость с неправильными стенками в правом верхушке сзади (стрелки), представляющая абсцесс легкого, который развился после операции по поводу немелкоклеточного рака легкого (TIF 622 kb)
467997_1_En_6_MOESM33_ESM.zip (439 kb)
Рис. e6.19 Абсцесс легкого. ( b ) Полость с неправильными стенками в правой верхушке сзади (стрелки), представляющая абсцесс легкого, развившийся после операции по поводу немелкоклеточного рака легкого (TIF 996 kb)
467997_1_En_6_MOESM35_ESM.zip (561 kb)
Рис. e6.21 Эмпиема. Большое пятнистое помутнение над правым верхним гемитораксом представляет собой обширную эмпиему, скрывающую лежащую в основе паренхиматозную стрептококковую пневмонию. Неровная плотность воздуха внутри эмпиемы указывает на связь с бронхиальным деревом [1] (TIF 991 kb)
467997_1_En_6_MOESM37_ESM.zip (1013 kb)
Рис. e6.23 Септическая эмболия. Множественные узелковые помутнения в обоих легких у пациента с эндокардитом (TIF 1283 kb)
467997_1_En_6_MOESM38_ESM.zip (344 kb)
Рис. E6.24 Септические эмболы. Множественные узловые поражения. Обратите внимание на периферическое расположение узелков и многочисленные кавитации (TIF 594 kb)
467997_1_En_6_MOESM39_ESM.zip (332 kb)
Рис. E6.25 Септические эмболы. ( a ) Рассеянные, в основном периферические, плохо очерченные очаги уплотнения воздушного пространства, многие из которых содержат кавитацию различной степени.Обратите внимание, что некоторые из них, по-видимому, связаны с «питающими» сосудами (стрелки), что указывает на гематогенное происхождение [1] (TIF 605 kb)
467997_1_En_6_MOESM40_ESM.zip (333 kb)
Рис. E6.25 Септические эмболы. ( b ) Рассеянные, в основном периферические, плохо выраженные очаги уплотнения воздушного пространства, многие из которых содержат кавитацию различной степени. Обратите внимание, что некоторые из них, по-видимому, связаны с «питающими» сосудами (стрелки), что указывает на гематогенное происхождение [1] (TIF 594 kb)
467997_1_En_6_MOESM41_ESM.zip (545 kb)
Рис. e6.26 Хроническая эозинофильная пневмония. Консолидация воздушного пространства, ограниченная в основном периферией легкого (картина обратного отека легких) [7] (TIF 774 kb)
467997_1_En_6_MOESM42_ESM.zip (434 kb)
Рис. E6.27 Аспергиллез. На диффузный легочный инфильтрат накладываются множественные полости разного размера. Шарик гриба почти заполняет большую полость в правой верхней доле (стрелки). Правый плевральный выпот также наблюдается у этого пациента с хроническим лимфолейкозом [1] (TIF 703 kb)
467997_1_En_6_MOESM43_ESM.zip (915 kb)
Рис. e6.28 Аспергиллез. Тонкостенный полостной узелок в правом легком больного лейкемией [1] (TIF 1792 kb)
467997_1_En_6_MOESM44_ESM.zip (233 kb)
Рис. E6.29 Аспергиллез. Двусторонние большие верхнедолевые полости, содержащие грибковые шарики разных размеров у пожилого мужчины с остаточным туберкулезом [1] (TIF 484 kb)
467997_1_En_6_MOESM45_ESM.zip (513 kb)
Рис. E6.30 Инвазивный легочный аспергиллез. Узелок в заднем сегменте правой верхней доли окружен «ореолом» матового стекла (стрелки) у этого молодого нейтропенического мужчины [2] (TIF 817 kb)
467997_1_En_6_MOESM46_ESM.zip (328 kb)
Рис. e6.31 Аспергиллома. ( a ) Масса мягких тканей внутри полости ( знак воздушного полумесяца ) в правой верхней доле (TIF 636 kb)
467997_1_En_6_MOESM47_ESM.zip (358 kb)
Рис. E6.31 Аспергиллома. Осевые КТ-изображения ( b ) лежа на спине и ( c ) на животе показывают, что криволинейный воздух перемещается в независимое положение (TIF 545 kb)
467997_1_En_6_MOESM48_ESM.zip (498 kb)
Рис. E6.31 Aspergilloma. Осевые КТ-изображения ( b ) на спине и ( c ) на животе показывают, что криволинейный воздух перемещается в независимое положение (TIF 1535 kb)
467997_1_En_6_MOESM49_ESM.zip (330 kb)
Рис. e6.32 Грибковый абсцесс легкого. Большое правое апикальное толстостенное полостное поражение у остро больного актиномикозом [1] (TIF 598 kb)
467997_1_En_6_MOESM50_ESM.zip (336 kb)
Рис. E6.33 Грибковый абсцесс легкого. Большая тонкостенная полость в правом основании (стрелка), содержащая гладкую эллиптическую однородную массу (наконечники стрелок), представляющую комок грибка мукормикоза у пациента с диабетом [1] (TIF 589 kb)
467997_1_En_6_MOESM51_ESM.zip (326 kb)
Рис. .e6.34 Pneumocystis jiroveci пневмония. Тяжелое двустороннее уплотнение воздушного пространства с воздушными бронхограммами. Пациент проходил иммуносупрессивную терапию по поводу лимфомы и умер вскоре после того, как была сделана эта рентгенограмма [1] (TIF 619 kb)
467997_1_En_6_MOESM52_ESM.zip (1.1 mb)
Рис. E6.35 Pneumocystis jiroveci pneumonia. ( a ) Двусторонние, симметричные, преимущественно перихилярные помутнения (TIF 1674 kb)
467997_1_En_6_MOESM53_ESM.zip (608 kb)
Рис. E6.35 Pneumocystis jiroveci пневмония. ( b ) КТ-изображение подтверждает двусторонние широко распространенные помутнения матового стекла, а также показывает рассеянные кисты легких (стрелка) [5] (TIF 1118 kb)
467997_1_En_6_MOESM54_ESM.zip (610 kb)
Рис. E6.36 Pneumocystis jiroveve. пневмония. Двусторонние помутнения матового стекла с множественными кистами у молодого ВИЧ-положительного мужчины [2] (TIF 824 kb)
467997_1_En_6_MOESM58_ESM.zip (1 mb)
Рис. E6.39 Образец дерева в почке (респираторно-синцитиальный вирус).Периферические, плохо очерченные центрилобулярные узелки и помутнения «дерево в почке» с обеих сторон у пациента с лейкемией. Обратите внимание на разбросанные узелки в легких, окруженные ореолами матового стекла [1] (TIF 1572 kb)
467997_1_En_6_MOESM59_ESM.zip (343 kb)
Рис. E6.40 Первичный туберкулез. Комбинация очагового поражения паренхимы (стрелки) и увеличенных правых прикорневых лимфатических узлов [1] (TIF 554 kb)
467997_1_En_6_MOESM60_ESM.zip (397 kb)
Рис. E6.41 Первичный туберкулез. Односторонний правый туберкулезный плевральный выпот без поражения паренхимы или лимфатических узлов [1] (TIF 739 kb)
467997_1_En_6_MOESM61_ESM.zip (1 mb)
Рис. e6.42 Неактивный туберкулез. ( a ) Кальцифицированная периферическая гранулема (поражение Гона, черная стрелка) и кальцинированные прикорневые лимфатические узлы (белые стрелки), объединяясь в комплекс Ранке [8] (TIF 1681 kb)
467997_1_En_6_MOESM62_ESM.zip (555 kb)
Рис. E6 .42 Неактивный туберкулез. ( b ) Кальцифицированная периферическая гранулема (поражение Гона, черная стрелка) и кальцинированные прикорневые лимфатические узлы (белые стрелки), объединяясь в комплекс Ранке [8] (TIF 1521 kb)
467997_1_En_6_MOESM63_ESM.zip (1.1 mb)
Рис. e6.43 Неактивный туберкулез. Плотно кальцинированные прикорневые узлы и увеличенный кальцинированный узел в аортопульмональном окне (стрелка) (TIF 1776 kb)
467997_1_En_6_MOESM65_ESM.zip (291 kb)
Рис. E6.45 Туберкулезная аденопатия средостения. Множественные увеличенные лимфатические узлы средостения с центральными областями низкого ослабления и периферического усиления (стрелки) [1] (TIF 608 kb)
467997_1_En_6_MOESM66_ESM.zip (806 kb)
Рис. E6.46 Рецидивирующий активный туберкулез. ( a ) Спустя годы после очистки процесса на рис.6.23, это развитие нового помутнения в левой перихилярной области (стрелка) (TIF 1711 kb)
467997_1_En_6_MOESM67_ESM.zip (671 kb)
Рис. E6.46 Рецидивирующий активный туберкулез. ( b ) КТ-изображение подтверждает изменения как кавитацию (черные стрелки), а также демонстрирует окружающий узор «дерево в почке» (белая стрелка) [3] (TIF 1282 kb)
467997_1_En_6_MOESM68_ESM.zip (949 kb)
Рис. с6.47 Туберкулез в активной форме. Обширное полостное поражение с окружающим уплотнением, затрагивающее апикальный задний сегмент правой верхней доли.(Предоставлено Дианой Литманович, MD, Бостон) (TIF 1496 kb)
467997_1_En_6_MOESM69_ESM.zip (501 kb)
Рис. E6.48 Активный туберкулез. Множественные большие полости с уровнями воздух-жидкость в обеих верхних долях. Обратите внимание на хронические фиброзные изменения и втягивание хилы вверх [1] (TIF 916 kb)
467997_1_En_6_MOESM71_ESM.zip (358 kb)
Рис. E6.49 Активный туберкулез. ( b ) На нижнем изображении показаны более крупные узловые помутнения (стрелки), представляющие распространение гранулематозной инфекции на соседние альвеолы [1] (TIF 520 kb)
467997_1_En_6_MOESM72_ESM.zip (494 kb)
Рис. e6.50 Активный туберкулез с эндобронхиальным распространением. Типичный вид многочисленных диффузных, плохо выраженных узелков, некоторые из которых являются периваскулярными и центрилобулярными [1] (TIF 845 kb)
467997_1_En_6_MOESM73_ESM.zip (868 kb)
Рис. E6.51 Активный туберкулез с эндобронхиальным распространением. ( a ) Проекции максимальной интенсивности (MIPS) показывают генерализованное помутнение дерева в почке [9] (TIF 1346 kb)
467997_1_En_6_MOESM74_ESM.zip (1.1 mb)
Рис. E6.51 Активный туберкулез с эндобронхиальным распространением.( b ) Проекции максимальной интенсивности (MIPS) показывают генерализованное помутнение дерева в почке [9] (TIF 1889 kb)
467997_1_En_6_MOESM76_ESM.zip (550 kb)
Рис. E6.53 Милиарный туберкулез. Многочисленные четко очерченные узелки размером 1-2 мм, диффузно распределенные по правой нижней доле. Некоторые узелки кажутся перегородочными (стрелки) или субплевральными, тогда как другие, по-видимому, связаны с небольшими питающими сосудами, что указывает на гематогенное происхождение [1] (TIF 928 kb)
467997_1_En_6_MOESM77_ESM.zip (306 kb)
Рис. E6.54 Милиарный туберкулез. Изображение на уровне дуги аорты показывает многочисленные узелки размером 1-2 мм, случайно распределенные в обоих легких [2] (TIF 577 kb)
Пример из практики пневмонии
Тест на пневмококковый мочевой антиген:
«Тест на пневмококковый антиген в моче — полезный метод для выявления пневмококка, особенно у пациентов, которые не могут получить надежный респираторный образец или тех, кто уже принимает антибиотики».
Тест на пневмококковые антигены в моче — полезный метод выявления пневмококка, особенно у пациентов, которые не могут получить надежный образец респираторных проб или тех, кто уже принимает антибиотики. 2 RP предоставил культуру мокроты, которая была значительно загрязнена плоскоклеточными эпителиальными клетками, что позволяет предположить, что если патоген вырастет, его следует интерпретировать как потенциальную контаминант от флоры полости рта пациента. Кроме того, он несколько дней принимал антибиотики, которые, вероятно, проникли бы в его образец мокроты, чтобы подавить рост бактерий на питательной среде.
Тест на пневмококковый антиген в моче (pUAT) — полезный диагностический инструмент, особенно у пациентов с высоким риском пневмококковой пневмонии.Руководства рекомендуют выполнять ПУАТ пациентам, нуждающимся в приеме в отделении интенсивной терапии, тем, кто не прошел амбулаторную антибактериальную терапию, лейкопению, активное злоупотребление алкоголем, хроническое тяжелое заболевание печени, аспления или плевральный выпот. 2 Это относительно простой и быстрый тест для выполнения, требующий только анализа мочи от пациента и занимающий всего 15 минут. Он имеет продемонстрированную специфичность> 90%, но относительно нечувствителен (70-80%). 3-5 Он сохраняет специфичность после нескольких дней антимикробной терапии. 6 Концентрация мочи перед тестированием может повысить чувствительность, но может снизить специфичность. 7
Стоимость:
Стоимость лечения HCAP сильно варьируется в зависимости от выбранного агента. Стоимость лечения может варьироваться от 50 до 300 долларов в день. 1 При стоимости pUAT приблизительно 30 долларов, деэскалационная терапия может дать значительную экономию средств, а также дать возможность избежать дальнейшего воздействия антибиотиков широкого спектра действия.Кроме того, когда режим с тремя лекарствами меняется на режим с одним лекарством, пациент получает выгоду от более низкого риска побочных явлений, потенциальных реакций на лекарства. PUAT также полезен при лечении ВП.
Из-за необходимости охватить как типичные, так и атипичные организмы, рекомендуемым лечением ВП является либо фторхинолон-монотерапия, либо бета-лактам плюс макролид. Классы фторхинолонов и макролидов известны как кардиотоксические препараты, потенциально удлиняющие интервал QT, что может привести к внезапной сердечной смерти. 8 Возможность прекратить прием одного из этих агентов и использовать монотерапию бета-лактамом при пневмококке может ограничить частоту этих неблагоприятных сердечных явлений.
Авторские права © 2014 Alliance for the Predical Use of Antibiotics (APUA), лицензия на использование Alere Inc.
Практическое руководство по клинической медицине Калифорнийского университета в Сан-Диего
Исследование легких
Четыре основных компонента исследования легких (осмотр, пальпация, перкуссия и аускультация):
также используется для исследования сердца и живота.Изучение соответствующих техник на этом этапе
таким образом повысит вашу способность выполнять и другие обследования. Показатели жизнедеятельности,
важный источник информации, обсуждаются в другом месте.
Осмотр / наблюдение:
Большой объем информации можно получить, просто наблюдая за дыханием пациента. Платить
особое внимание на:
- Общий комфорт и характер дыхания пациента.Они выглядят огорченными,
потогонное, затрудненное? Дыхание регулярное и глубокое? - Использование дополнительных дыхательных мышц (например, лестничных мышц, грудино-ключично-сосцевидных мышц).
Их использование означает некоторый элемент затруднения дыхания. - Цвет пациента, в частности вокруг губ и
ногтевые ложа. Очевидно, синий — это плохо!Цианоз ногтевого ложа
- Положение пациента.Те, у кого тяжелая легочная дисфункция, будут
часто сижу прямо. В случае серьезного бедствия они будут наклоняться вперед, отдыхая.
их руки на коленях в так называемой позиции трипода.Пациент с эмфиземой, наклоняющийся в Tri-Pod
Позиция - Дыхание через сжатые губы, часто наблюдается при эмфиземе.
- Способность говорить. Иногда частота дыхания может быть настолько высокой и / или работать
дыхания настолько сильное, что пациенты не могут говорить полными предложениями.
Если это произойдет, обратите внимание, сколько слов они могут произнести (т. Е. Меньше слов на
дыхание, тем хуже проблема!). - Любые слышимые шумы, связанные с дыханием, например, хрипы или хрипы.
бульканье, вызванное выделениями в крупных дыхательных путях, слышно «голым»
ухо. - Направление движения брюшной стенки при вдохе. Обычно
опускание диафрагмы выталкивает внутрибрюшное содержимое вниз и стенку
наружу. В случаях сильного уплощения диафрагмы (например, эмфиземы) или паралича,
брюшная стенка может двигаться внутрь во время вдоха, что называется парадоксальным
дыхание.Если вы подозреваете, что это так, положите руку на плечо пациента.
живот во время дыхания, что должно подчеркивать его движения. - Любые явные деформации грудной клетки или позвоночника. Они могут возникнуть в результате хронического
заболевание легких (например, эмфизема), возникшее врожденным или иным образом.
В любом случае они могут нарушить способность пациента нормально дышать.Несколько
распространенные варианты включают:
Обзор анатомии легких:
Понимание легочного
экзамен значительно улучшается за счет распознавания взаимосвязей между поверхностными
структуры, скелет и основные доли легкого. Поймите, что это
может быть сложно, как некоторые поверхностные ориентиры (например, соски груди)
не всегда сохраняют свое точное отношение к нижележащим структурам.Тем не менее, поверхностные маркеры дадут вам приблизительное представление о том, что находится под
кожа. Рисунки ниже демонстрируют эти отношения. Разноцветный
области модели легкого идентифицируют точные анатомические сегменты различных
доли, которые нельзя оценить при осмотре. Обрисованы основные доли
В черном. Используются следующие сокращения: RUL = правая верхняя доля;
LUL = левая верхняя доля; RML = правая средняя доля; RLL = правая нижняя доля;
LLL = левая нижняя доля.
Вид спереди
Вид сзади
Вид сбоку справа
Вид сбоку слева
Пальпация:
Пальпация относительно второстепенная
роль в исследовании нормальной грудной клетки как интересующей структуры
(легкое) покрыто ребрами и поэтому не пальпируется.Конкретные ситуации
где это может быть полезно, включают:
- Акцентирование внимания на нормальной экскурсии грудной клетки: возложите руки на
спину с большими пальцами, направленными к позвоночнику. Не забудьте сначала потереть
руки вместе, чтобы они не были слишком холодными перед прикосновением к пациенту.
Ваши руки должны подниматься симметрично наружу, когда пациент принимает
глубокий вдох.Процессы, которые приводят к асимметричному расширению легких,
возникают, когда что-либо заполняет плевральное пространство (например, воздух или жидкость), затем может
будет обнаружен, поскольку рука на пораженной стороне будет двигаться наружу к меньшей
степень. Перед этой асимметрией должно быть много плевральных заболеваний.
можно определить на экзамене.Обнаружение экскурсии грудной клетки
- Tactile Fremitus: Нормальное легкое передает ощутимые вибрационные ощущения.
к грудной стенке.Это называется fremitus и может быть обнаружено.
плотно прижав локтевые части обеих рук к любой стороне
грудной клетки, пока пациент произносит слова «Девяносто девять». Этот маневр
повторяется до тех пор, пока не будет покрыта вся задняя часть грудной клетки. Костлявые аспекты
рук используются, поскольку они особенно чувствительны для обнаружения
эти колебания.Оценка Fremitus
Патологические состояния изменят fremitus. В частности:
- Уплотнение легких: уплотнение происходит при нормальном заполнении воздухом
паренхима легких наполняется жидкостью или тканью, чаще всего
в условиях пневмонии.Если достаточно большой сегмент паренхимы
участвует, это может изменить передачу воздуха и звука. в
наличие уплотнения, фремитус становится более выраженным. - Плевральная жидкость: жидкость, известная как плевральный выпот, может скапливаться в
потенциальное пространство, которое существует между легким и грудной стенкой,
смещение легкого вверх.Fremitus над выпотом будет уменьшен.
В общем, fremitus — довольно сложная находка, и ее не следует
считается основным средством определения консолидации
или плевральная жидкость.Однако он может предоставить подтверждающие доказательства, если другие
результаты (см. ниже) предполагают наличие любого из этих процессов.Выпоты и инфильтраты, возможно, могут
быть более понятным
используя губку, чтобы изобразить легкое.В этой модели инфильтрат
изображается синим цветом, который проник на губку
сама (губка слева). Излияние изображено синим
жидкость, на которой плавает легкое (губка справа). - Уплотнение легких: уплотнение происходит при нормальном заполнении воздухом
- Исследование болезненных участков: если пациент жалуется на боль в определенных
очевидно, что важно внимательно прощупать эту область.Кроме того, особые ситуации (например, травма) требуют тщательной пальпации.
искать доказательства перелома ребра, подкожный воздух (похоже на ваш
нажимая на рисовые криспи или пузырчатую бумагу) и т. д.
Ударные:
В этой технике используется
Тот факт, что удары по поверхности, покрывающей структуру, заполненную воздухом (например,грамм.
нормальное легкое) будет воспроизводить резонансную ноту при повторении того же маневра
над полостью, заполненной жидкостью или тканью, издает относительно глухой звук.
Если нормальная, заполненная воздухом ткань была вытеснена жидкостью (например, плевральной
выпот) или инфильтрирован лейкоцитами и бактериями (например, пневмония),
перкуссия вызовет приглушенный тон. В качестве альтернативы, процессы, которые
привести к хроническим (например,грамм. эмфизема) или острый (например, пневмоторакс) захват воздуха
в легком или плевральном пространстве, соответственно, будет производить гиперрезонансный
(т. е. более барабанные) ноты на перкуссии. Сначала вы обнаружите, что
этот навык немного неудобен для выполнения. Позвольте вашей руке свободно раскачиваться
на запястье, ударяя пальцем по мишени в нижней части
инсульт вниз.Жесткое запястье заставляет вас прижать палец к цели
который не будет воспроизводить правильный звук. Кроме того, требуется время, чтобы
развить ухо к тому, что звучит, а что нет. Несколько вещей, которые следует запомнить:
- Если вы ударяете правой рукой, встаньте немного левее
спины пациента. - Попросите пациента скрестить руки на груди, сжимая
противоположное плечо каждой рукой. Это поможет вытянуть лопатки.
сбоку, от ударного поля. - Пройдите по «аллее», которая существует между лопаткой и позвоночником.
столбец, который поможет вам избежать ударов по кости. - Постарайтесь сосредоточиться на поражении дистального межфалангового сустава (т. Е.
последний сустав) среднего пальца левой руки кончиком среднего пальца правой руки
Палец. Воздействие должно быть четким, поэтому вы можете подстричь ногти до
свести к минимуму кровопускание! - Последние 2 фаланги среднего пальца левой руки должны плотно прилегать к
спина пациента.Постарайтесь, чтобы остатки пальцев не касались
пациента, или положите на них только кончики, если в противном случае это слишком неудобно,
чтобы свести к минимуму какое-либо ослабление перкссионных нот. - При ударе по одной точке достаточно двух или трех резких ударов.
не стесняйтесь делать больше, если хотите. Затем опустите руку на несколько промежутков вниз.
и повторите маневр.В общем, перкуссия в 5 или около того разных местах
должен охватывать одну половину грудной клетки. После того, как вы ударили по левой груди,
переместите руки и повторите ту же процедуру с правой стороны.
Если вы обнаружите какую-либо аномалию с одной стороны, рекомендуется сдвинуть
руки передаются другому для сравнения. Таким образом, одна грудная клетка служит
как контроль для другого.Как правило, перкуссия ограничивается задней частью
легочные поля. Однако, если аускультация (см. Ниже) выявляет отклонения от нормы
в передних или боковых полях перкуссия по этим областям может помочь
определить его причину.Ударная техника
- Цель состоит в том, чтобы распознать, что в какой-то момент по мере вашего движения вниз к
основание легких, качество звука меняется.Это обычно
возникает при выходе из грудной клетки. Не особо важно
определить точное расположение диафрагмы, но если вы можете
обратите внимание на разницу в уровне между максимальным вдохом и выдохом,
тем лучше. В конечном итоге вы разовьете чувство того, где нормальный
легкое должно заканчиваться простым взглядом на грудь.Точный позвоночный уровень
в котором это происходит, на самом деле не имеет значения. - «Скоростная перкуссия» может помочь подчеркнуть разницу между тупым
и резонансные области. Во время этой техники экзаменующий перемещается влево.
(т. е. не перкуссирующая) рука с постоянной скоростью вниз по спине пациента,
постоянно нажимая на него, пока он продвигается к нижней части
грудная клетка.Это приводит к тому, что точка перегиба (т. Е. Изменение резонансного
тусклым) более выраженным.
Тренируйтесь на ударных! Попробуйте найти свой собственный желудочный пузырь, который должен быть
вокруг левого реберного края. Обратите внимание, что из-за расположения сердца,
постукивание по левой груди будет издавать другой звук, чем при выполнении
над вашим правом.Ударьте стены (если это листовой камень) и попытайтесь найти
шпильки. Постучите по посуде, наполненной различным количеством воды. Это не
только помогает вам развить чувство различных тонов, которые могут воспроизводиться
но также позволяет практиковать технику.
Аускультация:
Перед прослушиванием
в любой области груди, напомните себе, какая доля легкого слышна
лучше всего в этой области: нижние доли занимают нижнюю 3/4 задней части
поля; правая средняя доля слышна в правой подмышечной впадине; язычок в левой подмышечной впадине;
верхние доли в передней части грудной клетки и в верхней 1/4 задних полей.Это может быть очень полезно при попытке определить местоположение патологического
процессы, которые могут быть ограничены анатомическими границами (например, пневмония).
Многие патологические процессы (например, отек легких, бронхоспазм) носят диффузный характер,
получение аномальных результатов в нескольких областях.
- Наденьте стетоскоп так, чтобы вкладыши были направлены от
ты.Отрегулируйте головку прицела так, чтобы диафрагма вошла в зацепление. Если
вы не уверены, слегка поцарапайте диафрагму, которая должна произвести
шум. Если нет, поверните голову и попробуйте еще раз. Осторожно потрите головку
стетоскоп на рубашке, чтобы не было слишком холодно перед тем, как надеть
это на коже пациента. - Верхняя часть задних полей (i.е. к вершине
спина пациента). Слушайте одно место, а затем двигайтесь
стетоскоп в то же положение на противоположной стороне и повторите.
Здесь снова используется одно легкое для сравнения с другим.
Всю заднюю часть грудной клетки можно покрыть прослушиванием примерно в 4-х местах.
с каждой стороны. Конечно, если вы услышите что-то ненормальное, вам нужно будет
слушайте в большем количестве мест.Аускультация легких
- Язычок и правые средние доли можно исследовать, пока вы
стоя позади пациента. - Затем двигайтесь вперед и слушайте передние поля в
такая же мода.Обычно это делается, пока пациент все еще сидит.
в вертикальном положении. Если попросить пациенток лечь, их грудь
отпадают вбок, что может облегчить эту часть обследования.
Мысли об «управлении платьем» и уместное / уважительное прикосновение
Ваши пациенты:
Существует несколько источников напряжения, связанных с физическим осмотром в целом, а именно:
действительно выдвинуто на первый план во время осмотра груди.К ним относятся:
- Обследуемая зона должна быть в достаточной степени обнажена, но при этом пациент должен быть покрыт
возможно - Необходимость пальпировать чувствительные области для проведения точного исследования — требуется
прикасаться к людям, с которыми вы мало знакомы — неловко, особенно если
противоположный пол - Как новичок в медицине, вы особенно знаете, что этот аспект экзамена
является «неестественным» и, следовательно, очень чувствительным.. Что хорошо!
Ключи к проведению деликатного, но тщательного обследования:
- Объясните, что вы делаете («почему), прежде чем делать это → подтвердите
«слон в комнате»! - Обнажайте минимально необходимое количество кожи — для этого требуется
«искусное» использование халата и драпировки (мужские и женские) - Исследование сердца и легких пациенток:
- Попросите пациента заранее снять бюстгальтер (вы не можете хорошо слышать сердце
ткань) - Открывайте сундук только до необходимой степени.Для исследования легких вы можете
прислушивайтесь к передним полям, открывая только верхнюю часть
грудь (см. рисунок ниже). - Обратитесь за помощью к пациенту, попросив его поднять грудь до
положение, которое расширяет вашу способность слушать свое сердце
- Попросите пациента заранее снять бюстгальтер (вы не можете хорошо слышать сердце
- Не торопитесь, не действуйте бессердечно и не причиняйте боли
- ПОЖАЛУЙСТА… не исследуйте части тела через платье как:
- Отражает Плохую технику
- Вы будете скучать по вещам
- Вы потеряете баллы на экзаменах (ОБСЕ, CPX, USMLE)!
Помните — не осматривайте одежду или
«змеиный» стетоскоп пуховые рубашки / халаты
Хорошие варианты экзамена
Стоит отметить еще несколько моментов.
- Попросите пациента сделать медленные глубокие вдохи ртом, пока
вы сдаете экзамен. Это заставляет пациента двигаться больше.
объем воздуха при каждом вдохе, увеличивая продолжительность, интенсивность и
таким образом, можно обнаружить любые аномальные звуки дыхания, которые могут присутствовать. - Иногда бывает полезно, чтобы пациент несколько раз откашлялся перед
начало аускультации.Это очищает дыхательные пути и открывает небольшие
ателектатические (т. е. спавшиеся) области у основания легких. - Если пациент не может сесть (например, в случае неврологического заболевания,
послеоперационный
состояний и др.), аускультация может проводиться в лежачем
на их стороне. Обратитесь за помощью, если пациент не может двигаться самостоятельно.
В тех случаях, когда даже это не может быть выполнено, минимальное обследование
может выполняться путем прослушивания сбоку / сзади, как пациент
останки
лежа на спине. - Просьба к пациенту с силой выдохнуть иногда помогает
акцентировать ненормальные звуки дыхания (в частности, хрипы), которые могут
не слышно, когда они дышат с нормальной скоростью потока.
Что вы можете ожидать услышать? Несколько основных звуков для прослушивания:
- Здоровый человек дышит через рот в норме
дыхательные объемы
издает мягкий вдох при вдыхании воздуха в легкие,
с небольшим
шум, производимый по истечении срока годности.Они называются
вессикулярное дыхание
звуки. - Хрипы — это свистящие звуки, издаваемые во время выдоха.
(и иногда
вдох), когда воздух проходит через дыхательные пути, суженные
бронхоспазм,
выделения и / или связанный с ними отек слизистой оболочки. Поскольку это самое
часто встречается
в связи с диффузными процессами, которые влияют на все доли
легкое
(е.грамм. астма и эмфизема) часто слышен во всех
поля. В случае значительного сужения бронхов
экспираторная фаза дыхания (относительно вдоха)
становится заметно затяжным. Клиницисты называют это
уменьшение отношения I к E. Чем больше препятствие, тем
более длительный срок относится к вдохновению.Время от времени,
очаговые хрипы могут возникать при сужении дыхательных путей
если они ограничены одной анатомической областью, что может произойти с
препятствие
опухоль или бронхоспазм, вызванные пневмонией. Хрипы
слышал только
на вдохновение называется стридором и ассоциируется с
механический
обструкция на уровне трахеи / верхних дыхательных путей.Это может
будь лучшим
приветствуется размещением стетоскопа непосредственно на
трахея. - Хрипы (также известные как треск) — это царапающие звуки, которые
ассоциация
с процессами, которые заставляют жидкость накапливаться в
альвеолярный и
межуточные промежутки.Звук похож на звук, производимый
трение
пряди волос вместе близко к уху. Отек легких
наверное
самая частая причина, по крайней мере, у пожилого взрослого населения,
и результаты
в симметричных выводах. Обычно это происходит первым в большинстве случаев.
зависимый
части нижних долей и простираются от оснований в сторону
вершины
по мере прогрессирования болезни.С другой стороны, пневмония может привести к
в дискретном
области альвеолярного наполнения и, следовательно, треск
ограниченный
определенный участок легкого. Очень отчетливый, размытый,
треск с сухим звуком,
похожий на шум, производимый при разделении кусочков липучки,
вызваны
из-за легочного фиброза, относительно редкого состояния. - Плотное уплотнение паренхимы легких, что может произойти при
пневмония,
приводит к передаче сильных шумов в дыхательных путях (т.е.
как обычно
слышны при аускультации над трахеей … известны как трубчатые или
бронхиальный
звуки дыхания) к периферии. В этой настройке
уплотненное легкое
действует как потрясающая проводящая среда, передавая центральную
звучит прямо
к краям.Это очень похоже на шум, производимый при
дышать через
трубка. Кроме того, если вы посоветуете пациенту сказать
письмо ‘eee’
он обнаруживается во время аускультации над пораженной долей как
носовой зонд
‘ааа’. Эти изменения «eee» на «aaa» называются эгофонией.
Первое
обнаружив это, вы подумаете, что пациент на самом деле
говоря «ааа»…
попросите их повторить это несколько раз, чтобы убедиться, что они
действительно
следуя вашим указаниям! - Выделения, которые образуются / собираются в более крупных дыхательных путях, что может произойти
с участием
бронхит или другой процесс образования слизистой, может вызвать
булькающий
шум, похожий на звук, издаваемый, когда вы высасываете последние биты
из
молочный коктейль через трубочку.Эти шумы называются
рончи. - При аускультации плеврального выпота
звук.
Однако, если вы внимательно прислушаетесь к региону в верхней части
излияние
вы можете услышать звуки, указывающие на консолидацию, исходящие
из легких
который сжимается текучей средой, поднимающейся снизу вверх.Асимметричные излияния
вероятно, легче обнаружить, поскольку они будут производить разные
Выводы
при осмотре обеих сторон груди. - При аускультации пациентов с тяжелой стабильной эмфиземой
производить
очень мало звука. Эти пациенты страдают тяжелым поражением легких.
разрушение
и захват воздуха, в результате чего они дышат во время небольших приливов и отливов.
тома
которые почти не создают шума.Свистящее дыхание возникает при
наложенный
острый воспалительный процесс (см. выше).
Большинство из вышеперечисленных методов дополняют друг друга. Обнаружена тупость на
перкуссия
например, может представлять уплотнение легких или плевральный
излияние.
Аускультация в одном и том же регионе должна помочь различить
эти
возможности, поскольку уплотнение генерирует звуки дыхания бронхов, в то время как
ан
излияние связано с относительным отсутствием звука.Сходным образом,
Fremitus
будет увеличиваться при уплотнении и уменьшаться при излиянии. В качестве
такой,
может потребоваться повторить некоторые аспекты экзамена, используя один
находка
чтобы подтвердить значение другого. Некоторые находки патогномоничны.
Они
имеют наибольшее значение, когда используются вместе, чтобы рисовать больше всего
познавательный
рисунок.
Образцы звуков легких
(любезно предоставлено доктором Майклом Уилксом, доктором медицины — Медицинские школы Калифорнийского университета в Дэвисе и Калифорнийского университета в Лос-Анджелесе)
Динамическое исследование легких:
Импульсный оксиметр
Часто пациент жалуется на симптом, вызванный физической активностью.
или движение.Одышка при физической нагрузке, один из таких примеров, может быть
маркер значительной сердечной или легочной дисфункции. Первичный осмотр
может быть относительно нераскрытым. В таких случаях рассмотрите возможность передвижения по наблюдениям.
(с использованием пульсоксиметра, устройства, которое непрерывно измеряет
скорости и насыщения кислородом, если доступно) в качестве динамического расширения
кардиологические и легочные исследования.Количественная оценка толерантности пациента к физическим нагрузкам
с точки зрения пройденного расстояния и / или времени, может предоставить важную информацию
к оценке симптомов, вызванных активностью. Это может
также помочь разоблачить
болезнь, которая была бы неявной, если бы пациент не был
попросили выполнить
задача, которая поставила под сомнение их обесцененные резервы. Платить
особое внимание
скорости, с которой пациент ходит, продолжительность
активность, пройденное расстояние,
развитие одышки, изменения ЧСС и кислорода
насыщенность, способность
разговаривать во время упражнений и всего, что
пациент идентифицируется как
ограничение их деятельности.Объективные данные, полученные из
этот низкотехнологичный тест
может помочь вам в определении тяжести заболевания и симптомов,
помогая создавать
список возможных диагнозов и помощь в
рациональное использование дополнительных
тесты для дальнейшего определения характера проблемы.
Это может быть особенно
помогает в предоставлении объективной информации, когда симптомы
кажутся непропорциональными
к находкам.Или когда пациенты жалуются еще немного
кажется, имеет достойный
количество болезней. Он также будет генерировать измерение
что вы можете сослаться
назад во время последующих оценок, чтобы
определить, есть ли
произошло какое-либо реальное изменение функционального статуса.
