Обструктивные поражения дыхательных путей плода (обзор литературы и собственные наблюдения)
ФГБУ Научный центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова Минздрава России, Москва
Цель исследования. Выявление основных эхографических признаков обструктивного поражения дыхательных путей плода и оценка постнатального исхода для новорожденного на основании представленного здесь анализа данных литературы и двух собственных наблюдений.
Материал и методы. Обструктивное поражение верхних дыхательных путей диагностировано у двух плодов в сроке беременности 19 недель 1 день и 20 недель 2 дня, нижних – в 21 неделю 6 дней. Беременности закончились прерыванием.
Результаты исследования. При обструкции дыхательных путей плода основным эхографическим признаком является значительное увеличение размера и повышение эхогенности легких. Наблюдается также патологическое выпячивание купола диафрагмы в сторону брюшной полости и асцит. При обструкции верхних дыхательных путей процесс всегда двусторонний, нижних – односторонний. Отмечается, что данная патология имеет неблагоприятный постнатальный прогноз.
Отмечается, что данная патология имеет неблагоприятный постнатальный прогноз.
Заключение. Применение эхографии позволяет диагностировать внутриутробно такую редкую и неблагоприятную в прогностическом отношении патологию, как обструкция дыхательных путей плода, а полученная в результате проведенного исследования информация, позволяет решить вопрос о дальнейшей тактике ведения беременности с учетом последующего прогноза для новорожденного.
эхография
плод
врожденное обструктивное поражение верхних дыхательных путей
обструкция бронха
атрезия нижних дыхательных путей
пренатальная диагностика
1. Медведев М.В. Врожденные пороки органов грудной клетки. Медведев М.В., ред. Пренатальная эхография. Дифференциальный диагноз и прогноз. М.: Реал Тайм; 2009: 108-37.
2. Vidaeff A.C., Szmuk P., Masrobattista J.M., Rowe T.F., Ghelber O. More or less CHAOS: case report and literature review suggesting the existence of a distinct subtype of congenital high airway obstruction syndrome. Ultrasound Obstet. Gynecol. 2007; 30(1): 114-7.
Ultrasound Obstet. Gynecol. 2007; 30(1): 114-7.
3. Witters I., Fryns J.P., De Catte L., Moerman P. Prenatal diagnosis and pulmonary pathology in congenital high airway obstruction sequence. Prenat. Diagn. 2009; 29(11): 1081-4.
4. Abitayeh G., Ruano R., Martinovic J., Barthe B., Aubry M.-C., Benachi A. Prenatal diagnosis of main stem bronchial atresia using 3-dimensional ultrasonographic technologies. J. Ultrasound Med. 2010; 29(4): 633-8.
5. Simetka O., Petros M., Dolezalkova E., Kovacova H., Matura D., Dvorackova J. Prenatal diagnosis of tracheal atresia in a twin pregnancy. Ultrasound Obstet. Gynecol. 2014; 43(6): 717-8.
6. Morrison P.J., Macphail S., Williams D., McCusker G., McKeever P., Wright C., Nevin N.C. Laryngeal atresia or stenosis presenting as second-trimester fetal ascites – diagnosis and pathology in three independent cases. Prenat. Diagn. 1998; 18(9): 963-7.
7. Bonnefoy C., Blanc P., Coste K., Delabaere A., Dechelotte P.J., Laurichesse-Delmas H. et al. Prenatal diagnosis of lobar bronchial atresia. Ultrasound Obstet. Gynecol. 2011; 37(1): 110-2.
et al. Prenatal diagnosis of lobar bronchial atresia. Ultrasound Obstet. Gynecol. 2011; 37(1): 110-2.
8. Duin L.K., Marcus-Soekarman D., Baldewijns M.M.L., Robben S.G.F., Nijhuis J.G. Prenatal diagnosis of bronchial atresia, early in pregnancy. Prenat. Diagn. 2006; 26(4): 373-94.
9. Keswani S.G., Crombleholme T.M., Pawel B.R., Johnson M.P., Flake A.W., Hedrick H.L. et al. Prenatal diagnosis and management of mainstem bronchial atresia. Fetal Diagn. Ther. 2005; 20(1): 74-8.
10. Zamora I.J., Sheikh F., Olutoye O.O., Cassady C.I., Lee T.C., Ruano R., Cass D.L. Mainstem bronchial atresia: a lethal anomaly amenable to fetal surgical treatment. J. Pediatr. Surg. 2014; 49(5): 706-11.
11. Gilboa Y., Achiron R., Katorza E., Bronshtein M. Early sonographic diagnosis of congenital high-airway obstruction syndrome. Ultrasound Obstet. Gynecol. 2009; 33(6): 730-4.
12. Ruano R., Cass D.L., Rieger M., Javadian P., Shamshirsaz A.A., Olutoye O.O., Belfort M.A. Fetal laryngoscopy to evaluate vocal folds in a fetus with congenital high airway obstruction syndrome (CHAOS). Ultrasound Obstet. Gynecol. 2014; 43(1): 102-5.
Ultrasound Obstet. Gynecol. 2014; 43(1): 102-5.
13. Colnaghi M., Condo V., Gagliardi L., Mirabile L., Fumagalli M., Mosca F. Prenatal diagnosis and postnatal management of congenital laryngeal atresia in preterm infant. Ultrasound Obstet. Gynecol. 2007; 29(5): 583-5.
14. Oepkes D., Teunissen A.K., Van de Velde M., Devlieger H., Delaere P., Deprest J. Congenital high airway obstruction syndrome successfully managed with ex-utero intrapartum treatment. Ultrasound Obstet. Gynecol. 2003; 22(4): 437-9.
15. Peak B.W., Callen P.W., Kitterman J., Feldstein V.A., Farrell V.A., Harrison M.R., Albanese C.T. Successful fetal intervention for congenital high airway obstruction syndrome. Fetal Diagn. Ther. 2002; 17(5): 272-6.
Поступила 21.12.2015
Принята в печать 29.01.2016
Машинец Наталья Валериевна, к.м.н., с.н.с. отделения функциональной диагностики отдела визуальной диагностики ФГБУ НЦАГиП им. академика В.И. Кулакова Минздрава России. Адрес: 117997, Россия, Москва ул. Академика Опарина, д. 4. Телефон: 8 (906) 795-66-47. E-mail: [email protected]
Академика Опарина, д. 4. Телефон: 8 (906) 795-66-47. E-mail: [email protected]
Демидов Владимир Николаевич, д.м.н., профессор отделения функциональной диагностики отдела визуальной диагностики ФГБУ НЦАГиП им. академика В.И. Кулакова Минздрава России. Адрес: 117997, Россия, Москва ул. Академика Опарина, д. 4. Телефон: 8 (495) 438-25-29. E-mail: [email protected]
Для цитирования: Машинец Н.В., Демидов В.Н. Обструктивные поражения дыхательных путей плода (обзор литературы и собственные наблюдения). Акушерство и гинекология. 2016; 7: 93-98.
http://dx.doi.org/10.18565/aig.2016.7.93-98
Диагностика обструкции дыхательных путей умеренной степени выраженности методом импульсной осциллометрии | Савушкина
1. Каменева М. Ю., Савушкина О. И., Черняк А. В. Импульсная осциллометрия//Легочные функциональные тесты: от теории к практике. Руководство для врачей/ под ред. О. И. Савушкиной, А.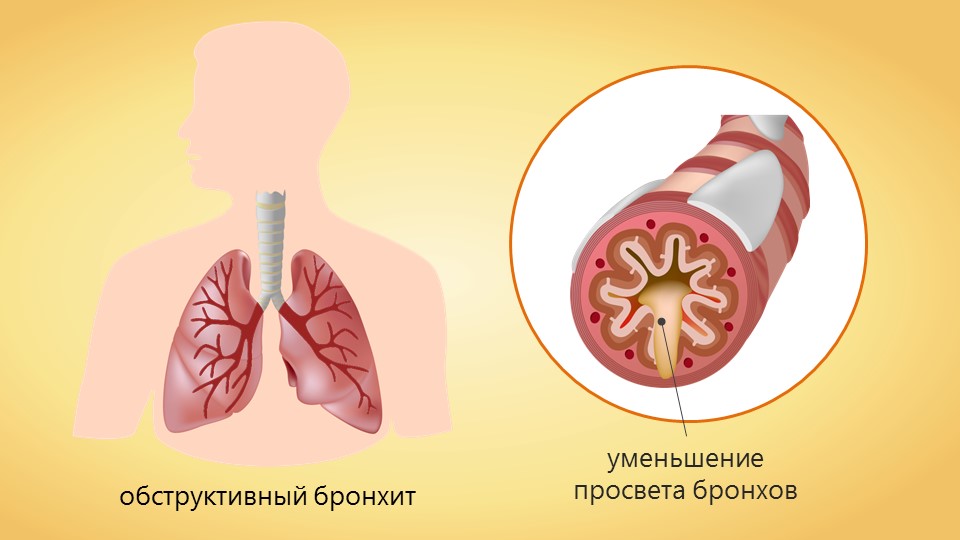 В. Черняка. М.: Фирма Стром; 2017.- С. 121-148.
В. Черняка. М.: Фирма Стром; 2017.- С. 121-148.
2. Черняк А. В., Амелина Е.Л. Применение импульсной осциллометрии у больных муковисцидозом. // Пульмонология.- 2005.- № 2.- С. 84-88.
3. Brashier B., Salvi S. Measuring lung function using sound waves: role of the forced oscillation technique and impulse oscillometry system. // Breathe.-2015.- Vol. 11, № 1.- Р. 57-65. DOI: 10.1183/20734735.020514
4. Кирюхина Л. Д., Каменева М. Ю., Новикова Л. Н. Возможности импульсной осциллометрии в диагностике рестриктивного варианта вентиляционных нарушений. Международный научно-исследовательский журнал. 2017;(5):136-141. DOI: 10.23670/IRJ.2017.59.032
5. Савушкина О. И., Черняк А. В., Каменева М. Ю., Крюков Е. В., Зайцев А. А. Информативность импульсной осциллометрии в выявлении вентиляционных нарушений рестриктивного типа. // Бюллетень физиологии и патологии дыхания.- 2018.- Вып. 67.- С. 8-16. DOI: 10.12737/article_5a9f258fe6d932.79474351
Ю., Крюков Е. В., Зайцев А. А. Информативность импульсной осциллометрии в выявлении вентиляционных нарушений рестриктивного типа. // Бюллетень физиологии и патологии дыхания.- 2018.- Вып. 67.- С. 8-16. DOI: 10.12737/article_5a9f258fe6d932.79474351
6. Савушкина О. И., Черняк А. В., Каменева М. Ю., Крюков Е. В., Зайцев А. А. Возможности импульсной осциллометрии в диагностике обструкции дыхательных путей легкой степени выраженности (в печати).
7. Vukoja M., Milicic D., Kopitovic I. Impulse oscillometry in COPD: Correlation to spirometry and whole-body plethysmography. //Eur. Respir. J. — 2014.- Vol. 44.- P. 3973
8. Wanger J., Clausen JL, Coates A et al. Standardisation of the measurement of lung volumes. // Eur. Respir. J.-2005.-Vol. 26, № 3.- P. 511-522.
9. Pellegrino R, Viegi G, Brusasco V, et al. Interpretative strategies for lung function tests. // Eur. Respir. J.- 2005.- Vol. 26, № 5.- P. 948-968.
10. Maclntyre N, Crapo RO, Viegi G, et al. Standardisation of the single-breath determination of carbon monoxide uptake in the lung. // Eur. Respir. J.-2005.- Vol. 26, № 4.- Р. 720-735.
11. Smith HJ, Reinhold P, Goldman MD. Forced oscillation technique and impulse oscillometry. Lung function testing: European Respiratory Society Monograph. Sheffield, England: European Respiratory Society. 2005.- С. 72-105.
12. Шик Л.Л., Канаев Н. Н., ред. Руководство по клинической физиологии дыхания. Ленинград: Медицина.- 1980.
13. Dellacà R. L., Santus P., Aliverti A. et al. Detection of expiratory flow limitation in COPD using the forced oscillation technique. Eur. Respir. J.- 2004.- Vol. 23.- P. 232-240. DOI: 10.1183/09031936.04.00046804
Dellacà R. L., Santus P., Aliverti A. et al. Detection of expiratory flow limitation in COPD using the forced oscillation technique. Eur. Respir. J.- 2004.- Vol. 23.- P. 232-240. DOI: 10.1183/09031936.04.00046804
14. Aarli B. B., Calverley P.M.A., Jensen R. L., Eagan T. M.L., Bakke P. S., Hardie J. A. Variability of within-breath reactance in COPD patients and its association with dyspnea. // Eur. Respir. J.- 2015.- Vol. 45.- P. 625-634. DOI: 10.1183/09031936.00051214
15. Winkler J., Hagert-Winkler A., Wirtz H., Hoheisel G. Die moderne Impulsoszillometrie im Spektrum lungenfunktioneller Messmethoden. // Pneumologie. — 2009. — № 8.- Р. 461-469. DOI: 10.1055/s-0029-1214938
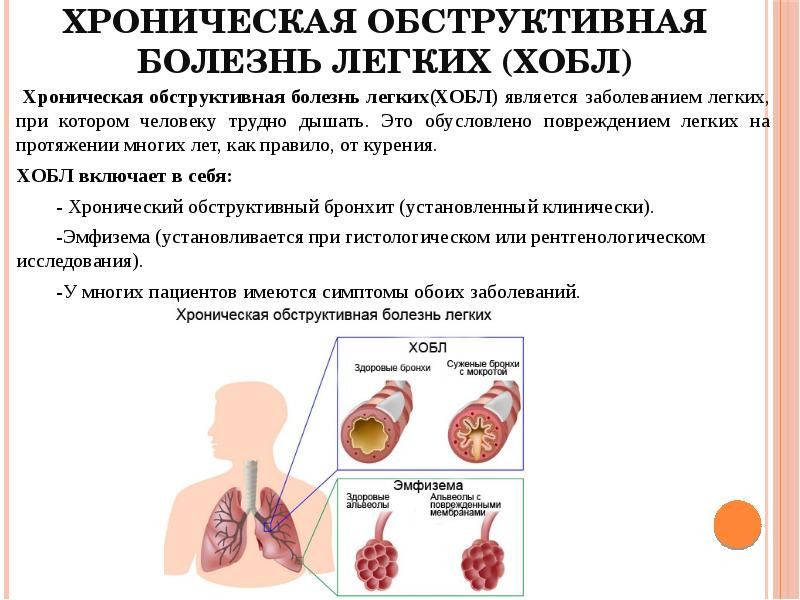
Хронические обструктивные болезни легких | ЧУЗ «КБ «РЖД-Медицина» им. Н.А. Семашко»
Хронические обструктивные болезни легких являются одними из самых распространенных: они лидируют по числу дней нетрудоспособности, причинам инвалидности, а также являются стоят на 4-м месте среди самых распространенных причин смерти.
Хронические обструктивные болезни легких — собирательное понятие, которое объединяет в себе болезни дыхательной системы:
- хронический обструктивный бронхит (ХОБ),
- эмфизема легких (ЭЛ),
- бронхиальная астма (БА) тяжелого течения.
Признак, по которому формируется группа ХОБЛ, — это медленно прогрессирующая необратимая бронхиальная обструкция с нарастающими явлениями хронической дыхательной недостаточности.
Понятие «хроническая обструктивная болезнь легких» появилось со временем при сближении трех терминов (хронический бронхит, эмфизема, хроническая пневмония), и в последующем употреблялся термин ХОБЛ (русская аббревиатура от англ. COPD — chronic obstructive pulmonary disease).
Главный фактор риска ХОБЛ в 80-90% случаев — курение. У курильщиков максимальные показатели смертности от ХОБЛ, у них быстрее развиваются необратимые обструктивные изменения функции дыхания, нарастают одышка и другие проявления болезни. Однако и среди некурящих нередки случаи возникновения и прогрессирования ХОБЛ.
Среди основных факторов риска профессиональной природы, значение которых установлено, наиболее вредоносными являются пыли, содержащие кадмий и кремний. Существенную роль в возникновении ХОБЛ играет генетическая предрасположенность. На это указывает тот факт, что не все длительно курящие становятся больными ХОБЛ.
Хронический обструктивный бронхит — заболевание, характеризующееся хроническим диффузным воспалением бронхов, ведущее к прогрессирующему нарушению вентиляции по обструктивному типу и проявляющееся кашлем, одышкой и выделением мокроты, не связанными с поражением других систем и органов. Одним из важнейших элементов ХОБ является воспаление, которое играет первичную роль в формировании всего комплекса патологических изменений. Вентиляционные нарушения при ХОБ, главным образом обструктивные, что проявляется экспираторной одышкой и снижением ОФВ1 — интегрального показателя, отражающего выраженность бронхиальной обструкции. Прогрессирование болезни, как обязательный признак ХОБ, проявляется ежегодным снижением ОФВ1 на 50 мл и более.
ХОБ — болезнь второй половины жизни, чаще возникающая после 40 лет. Эпидемиологические данные свидетельствуют о большей распространенности ХОБ среди мужчин и курящих женщин. Однако следует подчеркнуть, что в течение 10-15 лет болезнь протекает бессимптомно, т.е. ее начало может приходиться на старший детский и юношеский возраст.
Клиническая картина
Клиническая картина ХОБЛ характеризуется однотипными клиническими проявлениями — кашлем и одышкой, несмотря на неоднородность заболеваний, ее составляющих. Степень их выраженности зависит от стадии заболевания, скорости прогрессирования болезни и преимущественного уровня поражения бронхиального дерева.
Скорость прогрессирования и выраженность симптомов ХОБЛ зависит от интенсивности воздействия этиологических факторов и их суммации. Так, в стандартах Американского торакального общества подчеркивается, что появлению первых клинических симптомов у больных ХОБЛ обычно предшествует курение по крайней мере 20 сигарет в день на протяжении 20 и более лет.
Первыми признаками, с которыми пациенты обычно обращаются к врачу, являются кашель и одышка, иногда сопровождающиеся свистящим дыханием с выделением мокроты. Эти симптомы более выражены по утрам.
Наиболее ранним симптомом, появляющимся к 40-50 годам жизни, является кашель. К этому же времени в холодные сезоны начинают возникать эпизоды респираторной инфекции, не связываемые вначале в одно заболевание. Одышка, ощущаемая при физической нагрузке, возникает в среднем на 10 лет позже появления кашля. Однако в ряде случаев возможен дебют заболевания с одышки.
Мокрота выделяется в небольшом (редко > 60 мл/сутки) количестве утром, имеет слизистый характер. Обострения инфекционной природы проявляются усугублением всех признаков заболевания, появлением гнойной мокроты и увеличением ее количества.
Следует подчеркнуть, что бронхолегочная инфекция хотя и частая, но не единственная причина развития обострения. Наряду с этим возможны обострения заболевания, связанные с повышенным действием экзогенных повреждающих факторов, или в связи с неадекватной физической нагрузкой. В этих случаях признаки инфекционного поражения респираторной системы бывают минимальными.
В этих случаях признаки инфекционного поражения респираторной системы бывают минимальными.
По мере прогрессирования ХОБЛ промежутки между обострениями становятся короче.
Одышка может варьировать в очень широких пределах: от ощущения нехватки воздуха при стандартных физических нагрузках до тяжелой дыхательной недостаточности.
Диагностика
Выделяют две клинические формы заболевания — эмфизематозную и бронхитическую.
Эмфизематозную форму (тип) ХОБЛ связывают преимущественно с панацинарной эмфиземой. Таких больных образно называют «розовыми пыхтельщиками», поскольку для преодоления преждевременно наступающего экспираторного коллапса бронхов выдох производится через сложенные в трубочку губы и сопровождается своеобразным пыхтением. В клинической картине превалирует одышка в покое вследствие уменьшения диффузионной поверхности легких. Такие больные обычно худые, кашель у них чаще сухой или с небольшим количеством густой и вязкой мокроты. Цвет лица розовый, т. к. достаточная оксигенация крови поддерживается максимально возможным увеличением вентиляции.
к. достаточная оксигенация крови поддерживается максимально возможным увеличением вентиляции.
Бронхитическая форма (тип) наблюдается при центриацинарной эмфиземе. Постоянная гиперсекреция вызывает увеличение сопротивления на вдохе и выдохе, что способствует существенному нарушению вентиляции. В свою очередь, резкое уменьшение вентиляции приводит к значительному уменьшению содержания О2 в альвеолах, последующему нарушению перфузионно-диффузионных соотношений и шунтированию крови. Это и обусловливает характерный синий оттенок диффузного цианоза у больных данной категории. Такие больные тучные, в клинической картине преобладает кашель с обильным выделением мокроты. Диффузный пневмосклероз и облитерация просвета кровеносных сосудов ведут к быстрому развитию легочного сердца и его декомпенсации.
Диагностику заболеваний легких можно условно разделить на обязательный минимум, используемый у всех больных, и дополнительные методы, применяемые по специальным показаниям.
К обязательным методам диагностики заболеваний легких, помимо физикальных, относятся определение функции внешнего дыхания (ФВД), анализ крови, цитологическое исследование мокроты, рентгенологическое исследование, анализ крови и ЭКГ.
Ведущее значение в диагностике заболеваний легких и объективной оценке степени тяжести заболевания имеет исследование функции внешнего дыхания.
Лечение заболеваний легких
Целью лечения является снижение темпов прогрессирования заболевания, ведущего к нарастанию бронхиальной обструкции и дыхательной недостаточности, уменьшение частоты и продолжительности обострений, повышение толерантности к физической нагрузке и улучшение качества жизни.
Прекращение курения
Прекращение курения — первый обязательный шаг. Пациент должен четко осознавать вредоносное действие табачного дыма на его дыхательную систему. Составляется конкретная программа ограничения и прекращения курения. В случаях никотиновой зависимости целесообразно применение никотинзамещающих препаратов. Возможно привлечение психотерапевтов, иглорефлексотерапевтов.
Бронходилатирующая терапия
Согласно современным представлениям о сущности ХОБЛ бронхиальная обструкция является главным и универсальным источником всех патологических событий, развивающихся при постоянном прогрессировании заболевания и приводящих к дыхательной недостаточности.
Применение бронхорасширяющих препаратов — базисная терапия, обязательная при лечении больных ХОБЛ. Все остальные средства и методы должны применяться только в сочетании со средствами базисной терапии.
Комбинированное лечение
В лечении ХОБЛ среднего и тяжелого течения использование b2-агонистов в сочетании с холинолитиками позволяет потенцировать бронхорасширяющее действие и существенно уменьшить суммарную дозу b2-агонистов, тем самым снизить риск побочного действия последних. Преимуществами комбинации являются также воздействие на два патогенетических механизма бронхообструкции и быстрое начало бронхолитического действия. Для этой цели весьма удобны фиксированные комбинации препаратов в одном ингаляторе: Беродуал, Комбивент (беродуал = ипратропиум бромид 20 мкг + фенотерол 50 мкг; комбивент = ипратропиум бромид 20 мкг + сальбутамол 100 мкг). В последние годы стал накапливаться положительный опыт сочетанного применения холинолитиков с b2-агонистами пролонгированного действия (например, с сальметеролом).
Метилксантины
При недостаточной эффективности холинолитиков и b2-агонистов следует присоединить препараты метилксантинового ряда (теофиллин и др.). Их бронходилатирующий эффект уступает таковому b2-агонистов и холинолитиков, но прием внутрь или парентерально (ингаляционно метилксантины не назначают) вызывает ряд дополнительных действий: уменьшение системной легочной гипертензии, усиление диуреза, стимуляция центральной нервной системы, усиление работы дыхательных мышц, которые могут оказаться полезными у ряда больных.
Мукорегуляторные средства
Улучшение мукоцилиарного клиренса в значительной степени достигается при целенаправленном воздействии на бронхиальный секрет с применением мукорегуляторных препаратов.
Использование в качестве муколитических средств протеолитических ферментов недопустимо в связи с высоким риском развития серьезных побочных эффектов — кровохарканье, аллергия, бронхоконстрикция.
Глюкокортикостероидная терапия
Показанием для кортикостероидной (КС) терапии при ХОБЛ является неэффективность максимальных доз средств базисной терапии — бронхорасширяющих средств.
Коррекция дыхательной недостаточности
Коррекция дыхательной недостаточности достигается путем использования оксигенотерапии, тренировки дыхательной мускулатуры. Следует подчеркнуть, что интенсивность, объем и характер медикаментозного лечения зависят от тяжести состояния и соотношения обратимого и необратимого компонентов бронхиальной обструкции. При истощении обратимого компонента характер проводимой терапии меняется. На первое место выходят методы, направленные на коррекцию дыхательной недостаточности. При этом объем и интенсивность базисной терапии сохраняются.
Противоинфекционная терапия
В период стабильного течения ХОБЛ антибактериальная терапия не проводится.
В холодное время года у больных ХОБЛ нередко возникают обострения инфекционного происхождения. Наиболее часто их причиной являются Streptococcus pneumonia, Нaemophilus influenzae, Moraxella catarralis и вирусы. Антибиотики назначают при наличии клинических признаков интоксикации, увеличении количества мокроты и появлении в ней гнойных элементов. Обычно лечение назначается эмпирически и длится 7-14 дней. Подбор антибиотика по чувствительности флоры in vitro проводится лишь при неэффективности эмпирической антибиотикотерапии.
Обычно лечение назначается эмпирически и длится 7-14 дней. Подбор антибиотика по чувствительности флоры in vitro проводится лишь при неэффективности эмпирической антибиотикотерапии.
Большие перспективы открываются с помощью вакцинации. Она позволяет уменьшить число обострений заболевания и тяжесть их течения, тем самым снизить число дней нетрудоспособности и улучшить показатели бронхиальной проходимости.
Реабилитационная терапия
Реабилитационную терапию назначают при ХОБЛ любой степени тяжести. Врач определяет индивидуальную программу реабилитации для каждого больного. В зависимости от тяжести, фазы болезни и степени компенсации дыхательной и сердечно-сосудистой систем, программа включает режим, ЛФК, физиотерапевтические процедуры, санаторно-курортное лечение.
Слово ОБСТРУКЦИЯ — Что такое ОБСТРУКЦИЯ?
Слово состоит из 10 букв:
первая о,
вторая б,
третья с,
четвёртая т,
пятая р,
шестая у,
седьмая к,
восьмая ц,
девятая и,
последняя я,
Слово обструкция английскими буквами(транслитом) — obstrktsiya
Значения слова обструкция.
 Что такое обструкция?
Что такое обструкция?
Обструкция
ОБСТРУКЦИЯ (filibuster) Попытка препятствовать нормальному ходу работы парламента посредством затягивания дебатов. Характерна для американского Сената, в котором высоко почитается право свободного обсуждения.
Политика: толковый словарь. — М., 2001
Обструкция, прием парламентской борьбы, состоящий в том, что какая — либо не особенно сильная группа депутатов намеренно длинными речами, шумом и другими подобными приемами тормозит деятельность парламента.
Брокгауз и Ефрон. — 1907—1909
Обструкция — метод (парламентской) борьбы, состоящий в создании препятствий в принятии законопроекта или в реализации иного мероприятия. лат.Obstructio — преграда
glossary.ru
ОБСТРУКЦИЯ (filibuster) Попытка препятствовать нормальному ходу работы парламента посредством затягивания дебатов.
Характерна для американского Сената, в котором высоко почитается право свободного обсуждения.
Политика: толковый словарь. — М., 2001
Обструкция дыхательных путей
Обструкция дыхательных путей (от лат. obstructio — помеха, преграда) — синдром непроходимости респираторного тракта. Может наблюдаться на любом уровне, от глотки до бронхиол.
ru.wikipedia.org
Бронхиальная обструкция
Бронхиа́льная обстру́кция — клинический синдром, являющийся одной из форм дыхательной недостаточности, возникающей в результате нарушения проходимости бронхиального дерева…
ru.wikipedia.org
Русский язык
Обстру́кци/я [й/а].
Морфемно-орфографический словарь.
— 2002
Примеры употребления слова обструкция
Такая «обструкция» должна была еще больше завести нашу сборную, которой явно не хватало огня в глазах днем ранее.
Если у ребенка обструкция,мокрота трудно отходит.Анализ на аллергены нужно сделать.Кошек вы зря похерили.Наверняка у вас есть ковры,перьевые подушки,быт.химия,дезодоранты,плесень,пыль,пищевые аллергены, неподходящая смесь,неправильная диета при ГВ, прикорм.
- обструкционистский
- обструкционист
- обструкционный
- обструкция
- обстряпавший
- обстряпанный
- обстряпать
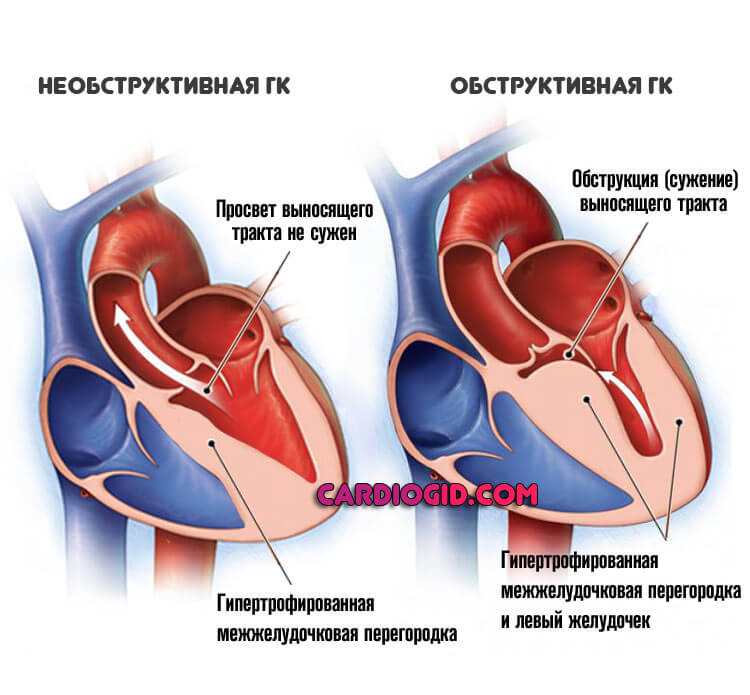
СОСТОЯНИЕ МИТРАЛЬНОГО КЛАПАНА ПРИ ГИПЕРТРОФИЧЕСКОЙ КАРДИОМИОПАТИИ И ЕГО РОЛЬ В РАЗВИТИИ ОБСТРУКЦИИ ВЫВОДНОГО ОТДЕЛА ЛЕВОГО ЖЕЛУДОЧКА | Канев
1. Elliot P.M., Anastasakis A., Borger M.A., Borggrefe M., Cecchi F., Charron P., et al. 2014 ESC guidelines on diagnosis and management of hypertrophic cardiomyopathy: the task force for the diagnosis and management of hypertrophic cardiomyopathy of the European society of cardiology (ESC). Eur. Heart J. 2014;35(39):2733–2779. DOI: 10.1093/eurheartj/ehu284.
Elliot P.M., Anastasakis A., Borger M.A., Borggrefe M., Cecchi F., Charron P., et al. 2014 ESC guidelines on diagnosis and management of hypertrophic cardiomyopathy: the task force for the diagnosis and management of hypertrophic cardiomyopathy of the European society of cardiology (ESC). Eur. Heart J. 2014;35(39):2733–2779. DOI: 10.1093/eurheartj/ehu284.
2. Nagueh S.F., Mahmarian J.J. Noninvasive cardiac imaging in patients with hypertrophic cardiomyopathy. J. Am. Coll. Cardiol. 2006;48(12):2410–2422.
3. Sherrid M.V., Gunsburg D.Z., Moldenhauer S., Pearle G. Systolic anterior motion begins at low left ventricular outflow tract velocity in obstructive hypertrophic cardiomyopathy. J. Am. Coll. Cardiol. 2000;36(4):1344–1354.
4. Kaple R.K., Murphy R.T., DiPaola L. M., Houghtaling P.L., Lever H.M., Lytle B.W., et al. Mitral valve abnormalities in hypertrophic cardiomyopathy: echocardiographic features and surgical outcomes. Ann. Thorac. Surg. 2008;85(5):1527–1535. DOI: 10.1016/j.athoracsur.2008.01.061.
M., Houghtaling P.L., Lever H.M., Lytle B.W., et al. Mitral valve abnormalities in hypertrophic cardiomyopathy: echocardiographic features and surgical outcomes. Ann. Thorac. Surg. 2008;85(5):1527–1535. DOI: 10.1016/j.athoracsur.2008.01.061.
5. Kim D.H., Handschumacher M.D., Levine R.A., Choi Y.S., Kim Y.J., Yun S.C., et al. In vivo measurement of mitral leaflet surface area and subvalvular geometry in patients with asymmetrical septal hypertrophy: insights into the mechanism of outflow tract obstruction. Circulation. 2010;122(13):1298–1307. DOI: 10.1161/CIRCULATIONAHA.109.935551.
6. Groarke J.D., Galazka P.Z., Cirino A.L., Lakdawaka N.K., Thune J.J., Bungaard H., et al. Intrinsic mitral valve alterations in hypertrophic sarcomere mutation carriers. Eur. Heart J. Cardiovasc. Imaging. 2018;19(10):1109–1116. DOI: 10.1093/ehjci/jey095.
7. Cooley D.A., Wukasch D.C., Leachman R.D. Mitral valve replacement for idiopathic hypertrophic subaortic stenosis. Results in 27 patients. J. Cardiovasc. Surg. (Toronto). 1976;17(5):380–387.
8. Sorajja P., Pedersen W.A., Bae R., Lesser J.R., Jay D., Lin D., et al. First experience with percutaneous mitral valve plication as primary therapy for symptomatic obstructive hypertrophic сardiomyopathy. J. Am. Coll. Cardiol. 2016;67(24):2811–2818. DOI: 10.1016/j.jacc.2016.03.587.
9. Bhudia S.K., McCarthy P.M., Smedira N.G., Lam B.K., Rajeswaran J., Blackstone E.H. Edge-to-edge (Alfieri) mitral repair: results in diverse clinical settings. Ann. Thorac. Surg. 2004;77(5):1598–1606. DOI: 10.1016/j.athoracsur.2003.09.090.
10. Balaram S.K., Ross R.E., Sherrid M.V., Schwartz G.S., Hillel Z., Winson G., et al. Role of mitral valve plication in the surgical management of hypertrophic cardiomyopathy. Ann. Thorac. Surg. 2012;94(6):1990–1997. DOI: 10.1016/j.athoracsur.2012.06.008.
Balaram S.K., Ross R.E., Sherrid M.V., Schwartz G.S., Hillel Z., Winson G., et al. Role of mitral valve plication in the surgical management of hypertrophic cardiomyopathy. Ann. Thorac. Surg. 2012;94(6):1990–1997. DOI: 10.1016/j.athoracsur.2012.06.008.
11. Hong J.H., Schaff H.V., Nishimura R.A., Abel M.D., Dearani J.A., Li Z., et al. Mitral regurgitation in patients with hypertrophic obstructive cardiomyopathy: implications for concomitant valve procedures. J. Amer. Coll. Cardiol. 2016;68(14):1407–1504. DOI: 10.1016/j.jacc.2016.07.735.
12. Yu E.H., Omran A.S., Wigle E.D., Williams W.G., Siu S.C., Rakowski H. Mitral regurgitation in hypertrophic obstructive cardiomyopathy: relationship to obstruction and relief with myectomy. J. Am. Coll. Cardiol. 2000;36(7):2219–2225.
13. Ponikowski P., Voors A.A., Anker S.D., Bueno H., Cleland J.G.F., Coats A.J.S., et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur. Heart J. 2016;37(27):2129– 2200. DOI: 10.1093/eurheartj/ehw128.
Ponikowski P., Voors A.A., Anker S.D., Bueno H., Cleland J.G.F., Coats A.J.S., et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur. Heart J. 2016;37(27):2129– 2200. DOI: 10.1093/eurheartj/ehw128.
14. Williams B., Mancia G., Spiering W., Rosei E.A., Azizi M., Burnier M., et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension: the task force for the management of arterial hypertension of the European society of cardiology (ESC) and the European society of Hypertension (ESH). Eur. Heart. J. 2018;36(10):1953–2041. DOI: 10.1097/HJH.0000000000001940.
15. Lang R.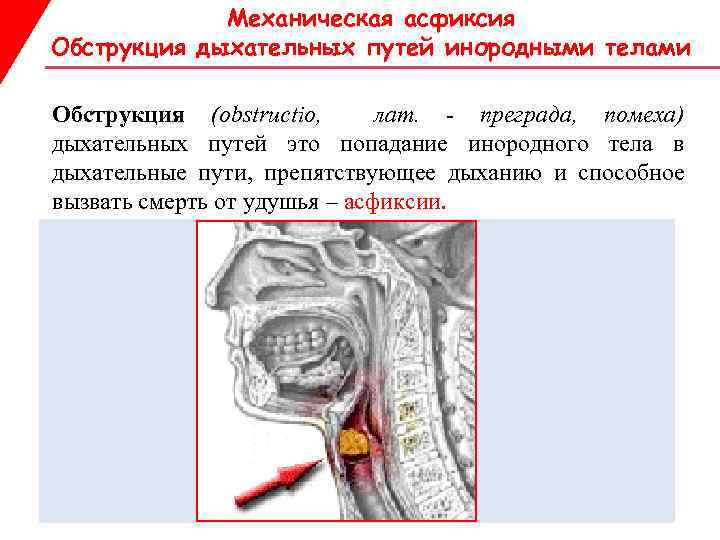 M., Badano L.P., Mor-Avi V., Afilano J., Armstrong A., Ernande L., et al. Recommendations for cardiac chamber quantification by echocardiography in adults: an update from the American society of echocardiography and the European association of cardiovascular imaging. J. Am. Soc. Echocardiogr. 2015;28(1):1–39. DOI: 10.1016/j.echo.2014.10.003.
M., Badano L.P., Mor-Avi V., Afilano J., Armstrong A., Ernande L., et al. Recommendations for cardiac chamber quantification by echocardiography in adults: an update from the American society of echocardiography and the European association of cardiovascular imaging. J. Am. Soc. Echocardiogr. 2015;28(1):1–39. DOI: 10.1016/j.echo.2014.10.003.
16. Nagueh S.F., Smiseth O.A., Appleton C.P., Byrd B.F., Dokainish H., Edvardsen T., et al. Recommendations for the evaluation of left ventricular diastolic function by echocardiography: an update from the American society of echocardiography and the European association of cardiovascular imaging. J. Am. Soc. Echocardiogr. 2016;29(4):277–314. DOI: 10.1016/j.echo.2016.01.011.
17. Zoghbi W.A., Adams D., Bonow R.O., Enriquez-Sarano M., Foster E., Grayburn P.A., et al. Recommendations for noninvasive evaluation of native valvular regurgitation: a report from the American society of echocardiography developed in collaboration with the society for cardiovascular magnetic resonance. J. Am. Soc. Echocardiogr. 2015;30(4):1– 39. DOI: 10.1016/j.echo.2017.01.007.
J. Am. Soc. Echocardiogr. 2015;30(4):1– 39. DOI: 10.1016/j.echo.2017.01.007.
18. Lang R.M., Badano L.P., Tsang W., Adams D.H., Agricola E., Buck T., et al. EAE/ASE recommendations for image acquisition and display using three-dimensional echocardiography. J. Am. Soc. Echocardiogr. 2012;25(1):3–46. DOI: 10.1016/j.echo.2011.11.010.
19. Warraich H.J., Chaudary B., Maslow A., Panzica P.J., Pugsley J., Mahmood F. Mitral annular nonplanarity: correlation between annular height/commissural width ratio and the nonplanarity angle. J. Cardiothorac. Vasc. Anest. 2012;26(2):186–190. DOI: 10.1161/CIRCULATIONAHA.107.749440.
20. Бокерия Л.А., Косарева Т.И., Макаренко В.Н., Маленков Д.А., Аносов А.А., Слепцова А.М. Анализ анатомических особенностей митрального клапана методами 2D и 3D эхокардиографии при ОГКМП.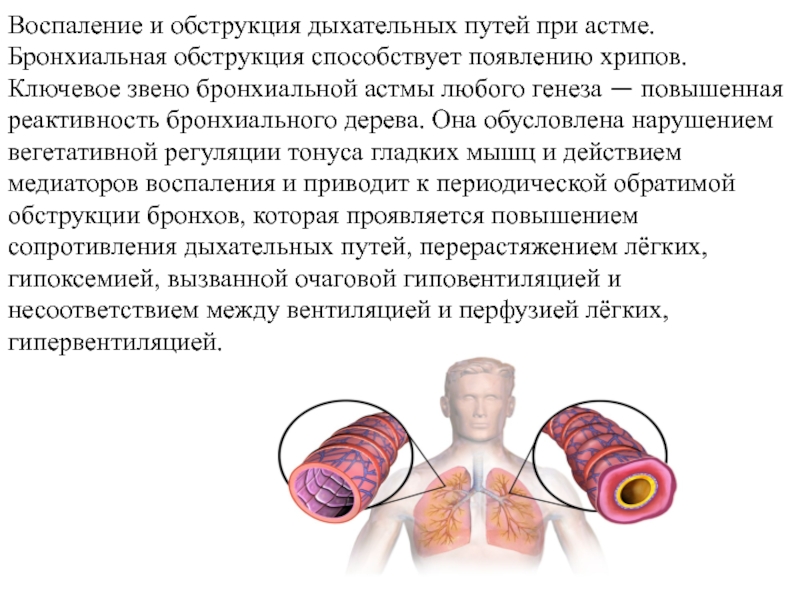 Медицинский Алфавит. 2018;14(1):34–37.
Медицинский Алфавит. 2018;14(1):34–37.
21. Maffessanti F., Gripari P., Pontone G., Andreini D., Bertella E., Mushtaq S., et al. Three-dimensional dynamic assessment of tricuspid and mitral annuli using cardiovascular magnetic resonance. Eur. Heart J. Cardiovasc. Imaging. 2013;14(10):986–995. DOI: 10.1093/ehjci/jet004.
22. Кадрабулатова С.С., Павлюкова Е.Н., Карпов Р.С., Тарасов Д.Г., Ткачев И.В. Трехмерная реконструкция интактного митрального клапана с количественным анализом. Ультразвуковая и функциональная диагностика. 2013;3:54–63.
23. Lee A.P., Jin C.N., Fan Y., Wong R.H.L., Underwood M.J., Wan S. Functional implication of mitral annular disjunction in mitral valve prolapse: a quantitative dynamic 3D echocardiographic study. JACC Cardiovasc. Imaging. 2017;10(12):1424–1433. DOI: 10.1016/j.jcmg.2016.11.022.
2017;10(12):1424–1433. DOI: 10.1016/j.jcmg.2016.11.022.
24. Кадрабулатова С.С., Павлюкова Е.Н., Карпов Р.С. Морфометрический анализ митрального клапана при болезни Барлоу (по данным трехмерной чреспищеводной эхокардиографии и количественного анализа митрального клапана). Сибирский медицинский журнал. 2013;28(3):14–19.
25. Dal-Bianco J.P., Levine R.A. Anatomy of the mitral valve apparatus: role of 2D and 3D echocardiography. Cardiol. Clin. 2013; 31(2): 151–164. DOI: 10.1016/j.ccl.2013.03.001.
26. Critoph C.H., Pantazis A., Tome Esteban M.T., Salazar-Mendiguchía J., Pagourelias E.D., Moon J.C., et al. The influence of aortoseptal angulation on provocable left ventricular outflow tract obstruction in hypertrophic cardiomyopathy. Open Heart. 2014;1:e000176. DOI: 10.1136/openhrt-2014-000176.
DOI: 10.1136/openhrt-2014-000176.
27. Raut M., Maheshwari A., Swain B. Awareness of ‘Systolic Anterior Motion’ in Different Conditions. Clin. Med. Insights Cardiol. 2018; 12. DOI: 10.1177/1179546817751921.
СРАВНИТЕЛЬНЫЙ АНАЛИЗ ЭФФЕКТИВНОСТИ РЕИМПЛАНТАЦИИ МОЧЕТОЧНИКОВ ПРИ ПУЗЫРНО-МОЧЕТОЧНИКОВОМ РЕФЛЮКСЕ И ОБСТРУКЦИИ УРЕТЕРОВЕЗИКАЛЬНОГО СЕГМЕНТА С ИСПОЛЬЗОВАНИЕМ ВЕЗИКОСКОПИЧЕСКОГО ДОСТУПА У ДЕТЕЙ | Пирогов
1. Okamura K, Ono Y, Yamada Y, Kato T, Tsuji Y, Ohshima S, Miyake K. Endoscopic trigonoplasty for primary vesicoureteric reflux. Br J Urol. 1995;75(3):390-4.
2. Gill IS, Ponsky LE, Desai M, Kay R, Ross JH. Laparoscopic cross-trigonal Cohen ureteroneocystostomy: novel technique. J Urol. 2001;166(5):1811-4.
J Urol. 2001;166(5):1811-4.
3. Yeung CK, Sihoe JD, Borzi PA. Endoscopic cross-trigonal ureteral reimplantation under carbon dioxide bladder insufflation: a novel technique. J Endourol. 2005;19(3):295-9. doi: 10.1089/end.2005.19.295
4. Kulikov A, Guzzo TJ, Canter DJ, Casale P. Initial experience with laparoscopic transvesical ureteral reimplantation at the Children’s Hospital of Philadelphia. J Urol. 2006;176(5):2222-5. doi: 10.1016/j.juro.2006.07.082
5. Canon SJ, Jayanthi VR, Patel AS. Vesicoscopic crosstrigonal ureteral reimplantation: a minimally invasive option for repair of vesicoureteral reflux. J Urol. 2007;178(1):269-73. doi: 10.1016/j.juro.2007.03.059
6. Jayanthi V, Patel A. Vesicoscopic ureteral reimplantation: a minimally invasive technique for the definitive repair of vesicoureteral reflux. Adv Urol. 2008:973616. doi: 10.1155/2008/973616
Vesicoscopic ureteral reimplantation: a minimally invasive technique for the definitive repair of vesicoureteral reflux. Adv Urol. 2008:973616. doi: 10.1155/2008/973616
7. Valla JS, Steyaert H, Griffin SJ, Lauron J, Fragoso AC, Arnaud P, Léculée R. Transvesicoscopic Cohen ureteric reimplantation for vesicoureteral reflux in children: a single-centre 5-year experience. J Pediatr Urol. 2009;5(6):466-71. doi: 10.1016/j.jpurol.2009.03.01
8. Hong CH, Kim JH, Jung HJ, Im YJ, Han SW. Single-surgeon experience with transvesicoscopic ureteral reimplantation in children with vesicoureteral reflux. Urology. 2011;77(6):1465-9. doi: 10.1016/j.urology.2010.11.023
9. Chung MS, Han SW, Jung HJ, Im YJ, Han HH, Na JC, Hong CH. Transvesicoscopic ureteral reimplantation in children with bilateral vesicoureteral reflux: surgical technique and results. J LaparoendoscAdvSurgTech A. 2012;22(3):295-300. doi: 10.1089/lap.2011.0318
J LaparoendoscAdvSurgTech A. 2012;22(3):295-300. doi: 10.1089/lap.2011.0318
10. Emir H, Mammadov E, Elicevik M, Buyukunal C, Soylet Y. Transvesicoscopic cross-trigonal ureteroneocystostomy in children: a single-center experience. J Pediatr Urol. 2012;8(1):83-6. doi: 10.1016/j.jpurol.2010.10.005
11. Roslan M, Markuszewski MM, Kłącz J, Krajka K. Laparoendoscopic single-site transvesicalureteroneocystostomy for vesicoureteral reflux in an adult: a one-year follow-up. Urology. 2012;80(3):719-23. doi: 10.1016/j. urology.2012.06.028
12. Bi Y, Sun Y. Laparoscopic pneumovesical ureteral tapering and reimplantation for megaureter. J Pediatr Surg. 2012;47(12):2285-8. doi: 10.1016/j.jpedsurg.2012.09.020
13. Шмыров О.С., Врублевский С.Г., Врублевская Е.Н., Врублевский А.С. Эндохирургические вмешательства в коррекции патологии уретеро-везикального сегмента у детей. Детская хирургия. 2014;4:25-28.
Шмыров О.С., Врублевский С.Г., Врублевская Е.Н., Врублевский А.С. Эндохирургические вмешательства в коррекции патологии уретеро-везикального сегмента у детей. Детская хирургия. 2014;4:25-28.
14. Schober MS, Jayanthi VR. Vesicoscopic ureteral reimplant: is there a role in the age of robotics? UrolClinNorthAm. 2015;42(1):53-9. doi: 10.1016/j.ucl.2014.09.005
15. Soh S, Kobori Y, Shin T, Suzuki K, Iwahata T, Sadaoka Y, Sato R, Nishi M, Iwamura M, Okada H. Transvesicoscopic ureteral reimplantation: Politano-Leadbetter versus Cohen technique. Int J Urol. 2015;22(4):394-9. doi: 10.1111/iju.12702
16. Choi H, Park JY, Bae JH. Initial experiences of laparoscopic intravesicaldetrusorraphy using the Politano-Leadbetter technique. J PediatrUrol. 2016;12(2):110.e1-7. doi: 10.1016/j.jpurol.2015.07.014
doi: 10.1016/j.jpurol.2015.07.014
17. Ansari MS, Yadav P, Arora S, Singh P, Sekhon V. Bilateral Transvesicoscopic Cross-trigonal Ureteric Reimplantation in Children: Surgical Subtleties and a Prospective Summary. Urology. 2017;101:67-72. doi: 10.1016/j. urology.2016.11.034
18. Kim SW, Lim NL, Lee YS, Han SW, Im YJ. Laparoscopic Intravesical Detrusorrhaphy With Ureteral Plication for Megaureter: A Novel Technique. Urology. 2015;86(1):187-91. doi: 10.1016/j.urology.2015.02.023
19. Liu X, Liu JH, Zhang DY, Hua Y, Lin T, Wei GH, He DW. Retrospective study to determine the short-term outcomes of a modified pneumovesical Glenn-Anderson procedure for treating primary obstructing megaureter. J PediatrUrol. 2015;11(5):266.e1-6. doi: 10.1016/j. jpurol.2015.03. 020
020
20. Naitoh Y, Oishi M, Kobayashi K, Yamada Y, Nakamura T, Johnin K, Hongo F, Naya Y, Okihara K, Kawauchi A. Transvesical laparoscopic surgery for double renal pelvis and ureter with or without ureterocele. Int J Urol. 2016;23(4):332-6. doi: 10.1111/iju.13049
21. Marte A, Cavaiuolo S, Esposito M, Pintozzi L. Vesicoscopic Treatment of Symptomatic Congenital Bladder Diverticula in Children: A 7-Year Experience. Eur J Pediatr Surg. 2016;26(3):240-4. doi: 10.1055/s-0035-1551564
22. DuckeƩ JW, Walker RD, Weiss R. Surgical results: International Reflux Study in Children—United States branch. J Urol. 1992;148:1674-5.
23. Hjälmås K, Löhr G, Tamminen-Möbius T, Seppänen J, Olbing H, Wikström S. Surgical results in the International Reflux Study in Children (Europe). J Urol. 1992;148:1657- 61.
Surgical results in the International Reflux Study in Children (Europe). J Urol. 1992;148:1657- 61.
24. Elder JS, Diaz M, Caldamone AA, Cendron M, Greenfi eld S, Hurwitz R, Kirsch A, Koyle MA, Pope J, Shapiro E. Endoscopic therapy for vesicoureteral reflux: ametaanalysis. I. Reflux resolution and urinary tract infection. J Urol. 2006;175(2):716-22. doi: 10.1016/S0022- 5347(05)00210-7
Болевой синдром в послеоперационном периоде при устранении орофарингеальной обструкции у пациентов с синдромом обструктивного апноэ во сне
Pain syndrome in the postoperative period after elimination of oropharyngeal obstruction in patients with obstructive sleep apnea syndrome
Ya.E. Yaromenka, V.A. Кarnialiuk, L.E. Makaryna-Kibak, K.S. Tsishkevich
One of the components characterizing the course of the postoperative period is pain. The article analyzes the severity of pain in the postoperative period in patients with uncomplicated snoring and obstructive sleep apnea of varying severity after the surgical treatment of upper respiratory tract obstruction at the oropharyngeal level. Significant differences were found in the severity of pain in patients with uncomplicated snoring and severe obstructive sleep apnea on the 3rd, 7th, 10th and 14th days of the postoperative period. It was found that in patients with obstructive sleep apnea of moderate to severe degree, the severity of pain and dysphagia in the postoperative period and the duration of pain medication use is the greatest (p
Significant differences were found in the severity of pain in patients with uncomplicated snoring and severe obstructive sleep apnea on the 3rd, 7th, 10th and 14th days of the postoperative period. It was found that in patients with obstructive sleep apnea of moderate to severe degree, the severity of pain and dysphagia in the postoperative period and the duration of pain medication use is the greatest (p
keywords: pain syndrome, oropharyngeal obstruction, visual analogue scale
for references: Ya.E. Yaromenka, V.A. Кarnialiuk, L.E. Makaryna-Kibak, K.S. Tsishkevich. Pain syndrome in the postoperative period after elimination of oropharyngeal obstruction in patients with obstructive sleep apnea syndrome. Neotlozhnaya kardiologiya i kardiovaskulyarnye riski [Emergency cardiology and cardiovascular risks], 2020, vol. 4, no. 1, pp. 830–833
1. Kasty’ro I.V., Demina E.N., Gulinov K.A. Bolevoy sindrom i vegetativny’y otvet posle septoplastiki kostnogo otdela peregorodki nosa [Pain syndrome and vegetative response after septoplasty of the nasal septum]. Ros J Boli, 2014, vol. 42, no. 1, pp. 36. (in Russian). 2. Ovechkin, A.M. Politov M.E. Posleoperacionnoe obezbolivanie s tochki zreniya dokazatel’noy mediciny’ [Postoperative pain management from the point of view of evidence-based medicine]. Vestn intensiv terapii, 2016, no. 2, pp. 51-60. (in Russian).
Ros J Boli, 2014, vol. 42, no. 1, pp. 36. (in Russian). 2. Ovechkin, A.M. Politov M.E. Posleoperacionnoe obezbolivanie s tochki zreniya dokazatel’noy mediciny’ [Postoperative pain management from the point of view of evidence-based medicine]. Vestn intensiv terapii, 2016, no. 2, pp. 51-60. (in Russian).
3. Ovechkin A. M. Hirurgicheskiy stress-otvet, ego patofiziologicheskaya znachimost’ i sposoby’ modulyacii [Surgical stress response, its pathophysiological significance and modulation methods]. Regionarnaya anesteziya i lechenie ostroy boli, 2008, vol. 2, no. 2, pp. 49-62. (in Russian).
4. Kolyadich J.V., Tishkevich E.S., Gudny’y G.V., Doldova V.S. Osobennosti posleoperacionnogo perioda u pacientov s apnoe` vo sne [Features of the postoperative period in patients with sleep apnea]. Otorinolaringologiya. Vost Evropa, 2014, no. 1, pp. 136-140. (in Russian).
5. Ramudu R.V., Giridhar T., Mahendra T., Reddy K.G., Rohith R. Relationship between surgical stress and serum cortisol level: a comparative study among elective and emergecive surgery. Indo Am J Pharm Res, 2015, vol. 5, no. 12, pp. 3759-3764.
Indo Am J Pharm Res, 2015, vol. 5, no. 12, pp. 3759-3764.
6. Abdelmageed W.M., Elquesny K.M., Shabana R.I., Abushama H.M., Nassar A.M. Analgesic properties of a dexmedetomidine infusion after uvulopalatopharyngoplasty in patients with obstructive sleep apnea. Saudi J Anaesth, 2011, vol. 5, no. 2, pp. 150-156.
7. Zhao Y.Q., Wang H.M., Ma Y., Yang H.A., Jiang X.J. Clinical research about the consecutive pain and flubiprofen axetil analgesia following uvulopalatopharyn-goplasty. Lin Chung Er Bi Yan Hou Tou Jing Wai Ke Za Zhi, 2017, vol. 31, no. 7, pp. 504-509.
8. Zhang L., Shao D., Gu B., Liang Z., Li H., Wang D. Comparison of the effects of different analgesic methods after UPPP. Lin Chung Er Bi Yan Hou Tou Jing Wai Ke Za Zhi, 2015, vol. 29, no. 11, pp. 991-993.
9. Ayatollahi V. Effect of intravenous vitamin C on postoperative pain in uvulopalatopharyngoplasty with tonsillectomy. Clin. Otolaryngol, 2017, vol. 42, no. 1, pp. 139-143.
10. Nikanne E., Virtaniemi J., Aho M. , Kokki H. Ketoprofen for postoperative pain after uvulopalatopharyngoplasty and tonsillectomy: two-week follow — up study. Otolaryngol Head Neck Surg, 2003, vol. 129, no. 5, pp. 577-581.
, Kokki H. Ketoprofen for postoperative pain after uvulopalatopharyngoplasty and tonsillectomy: two-week follow — up study. Otolaryngol Head Neck Surg, 2003, vol. 129, no. 5, pp. 577-581.
11. Tierney W.S. Gabarain G., Kominsky А.Н. Healthcare usage after uvulopalatopharyngoplasty – Impact of analgesic regimen. Am J Otolaryngol, 2017, vol. 38, no. 2, pp. 193-197.
12. Huskisson E. C. Measurement of pain. Lancet, 1974, vol. 2, no. 7889, рр. 1127–1131.
Непроходимость кишечника или кишечная непроходимость
Непроходимость кишечника — это когда закупорка препятствует перемещению пищи и жидкостей по пищеварительному тракту. Это также можно назвать кишечной непроходимостью, закупоркой кишечника или желудочно-кишечной непроходимостью.
Есть много возможных причин непроходимости кишечника. Это чаще встречается у людей с определенными видами рака и у людей с запущенным раком.
Полная непроходимость требует неотложной медицинской помощи и может потребовать хирургического вмешательства. Частичная непроходимость также является серьезной проблемой и требует немедленного лечения. Если вы испытываете какие-либо симптомы непроходимости кишечника, важно поговорить со своим лечащим врачом.
Частичная непроходимость также является серьезной проблемой и требует немедленного лечения. Если вы испытываете какие-либо симптомы непроходимости кишечника, важно поговорить со своим лечащим врачом.
Лечение побочных эффектов — важная часть лечения рака. Этот вид лечения называется паллиативной или поддерживающей терапией. Поговорите со своим лечащим врачом о любых симптомах, которые у вас есть, включая новые симптомы или изменения. Это помогает им как можно раньше обнаружить побочные эффекты, такие как непроходимость кишечника.
Что такое желудочно-кишечный тракт?
Ваш пищеварительный тракт или желудочно-кишечный тракт состоит из пищевода, желудка, тонкой и толстой кишок. Это часть вашей пищеварительной системы.
Тонкий кишечник переваривает питательные вещества из пищи и жидкостей и всасывает их в кровеносные сосуды. Эти питательные вещества включают белки, жиры и углеводы. Оставшаяся пища, которая не может быть переварена, перемещается из тонкой кишки в толстую. Ободочная кишка поглощает воду из отходов и накапливает их до следующего испражнения, которое выводит отходы из организма в виде стула (фекалий).
Ободочная кишка поглощает воду из отходов и накапливает их до следующего испражнения, которое выводит отходы из организма в виде стула (фекалий).
На этом рисунке показаны 5 отделов толстой и прямой кишки. Восходящая ободочная кишка является началом толстой кишки, в которую впадает тонкий кишечник; он начинается в нижней правой части живота, а затем ведет к поперечной ободочной кишке. Поперечная ободочная кишка пересекает верхнюю часть живота справа налево, приводя к нисходящей ободочной кишке, которая выводит отходы вниз по левой стороне. Наконец, сигмовидная кишка внизу выводит отходы еще на несколько дюймов вниз до прямой кишки.Поперечный разрез прямой и сигмовидной кишки показывает, где отходы выходят из организма через задний проход. Авторское право 2004 г. Американское общество клинической онкологии. Роберт Морреале / Визуальные объяснения, ООО.
Каковы признаки непроходимости кишечника?
Непроходимость кишечника может произойти в тонком кишечнике (непроходимость тонкого кишечника) или толстом кишечнике (непроходимость толстого кишечника). Во время непроходимости кишечника часть или вся пища и жидкости, которые проходят через пищеварительный тракт, не могут пройти через закупорку.Кишечная непроходимость может быть вызвана тем, что что-то внутри желудочно-кишечного тракта блокирует кишечник или что-то за пределами желудочно-кишечного тракта давит на кишечник и вызывает его коллапс.
Во время непроходимости кишечника часть или вся пища и жидкости, которые проходят через пищеварительный тракт, не могут пройти через закупорку.Кишечная непроходимость может быть вызвана тем, что что-то внутри желудочно-кишечного тракта блокирует кишечник или что-то за пределами желудочно-кишечного тракта давит на кишечник и вызывает его коллапс.
Непроходимость кишечника вызывает физические симптомы, в том числе:
Тошнота и рвота
Сильная боль в животе (животе)
Спастическая боль, вызванная перистальтикой, сокращениями, при которых пища перемещается по желудочно-кишечному тракту
Видимые волны движения по животу от перистальтических сокращений
Вздутие живота
Ощущение застревания пищи при движении по желудочно-кишечному тракту
Отсутствие дефекации (запор) или газов
Что вызывает непроходимость кишечника?
Распространенные причины обструкции желудочно-кишечного тракта при раке:
Трудный стул, который трудно пройти
Заворот кишечника
Рубцовая ткань в кишечнике
Воспаление кишечника после лучевой терапии
Опухоль или опухоль в желудочно-кишечном тракте
Опухоль или опухоли, давящие на внешнюю часть желудочно-кишечного тракта
Какие виды рака могут вызвать непроходимость кишечника?
Обструкция ЖКТ может возникать при многих типах рака.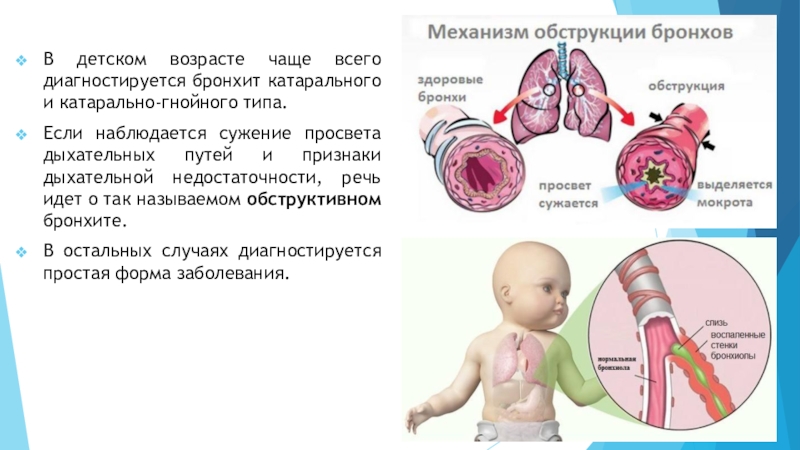 Они чаще встречаются у людей с:
Они чаще встречаются у людей с:
Как диагностируется непроходимость кишечника?
Чтобы диагностировать непроходимость кишечника, ваш врач проведет физический осмотр. Во время этого обследования они будут прощупывать ваш живот и с помощью стетоскопа послушают ваш живот.
Непроходимость кишечника часто можно подтвердить с помощью рентгена. Но не все непроходимости кишечника можно увидеть на рентгеновском снимке, поэтому вам может потребоваться компьютерная томография или бариевая клизма.
Как лечится непроходимость кишечника?
Большинство людей с непроходимостью кишечника нуждаются в госпитализации.Лучшее лечение непроходимости кишечника зависит от того, чем она вызвана. Вот некоторые способы лечения или устранения непроходимости кишечника:
Получение жидкости через внутривенный зонд, который вводится в вену на руке. Отказ от еды и питья в течение нескольких дней может помочь восстановить и обратить вспять искривление кишечника.
 Если через несколько дней закупорка не улучшится, вам может потребоваться внутривенное питание.
Если через несколько дней закупорка не улучшится, вам может потребоваться внутривенное питание.Клизмы или лекарства для разжижения и / или смягчения твердого стула, вызывающего закупорку.
Использование трубки для удаления воздуха и жидкости из желудка, чтобы предотвратить усиление боли. Эта трубка, называемая назогастральным зондом, проходит через нос и опускается в желудок.
Принимая лекарство, врач рекомендует уменьшить тошноту и рвоту, диарею, отек или боль.
Если эти варианты не работают, ваш врач может предложить:
Операция по устранению закупорки и расчистке пути прохождения пищи через желудочно-кишечный тракт.
Одноразовая трубка, называемая стентом.
 Это временно удерживает заблокированную область желудочно-кишечного тракта.
Это временно удерживает заблокированную область желудочно-кишечного тракта.Илеостомия. Эта операция может помочь заживлению толстой и прямой кишки после закупорки. Во время илеостомии временное или постоянное отверстие (стома) размещается от самой нижней части тонкой кишки к внешней стороне живота. Отходы собираются в мешочке, который носят снаружи вашего тела и не должны проходить через толстую или толстую кишку.
Колостома. Эта операция может помочь в заживлении частей толстой и прямой кишки после закупорки. Во время колостомы делается временное или постоянное отверстие (стома) от толстой кишки к внешней стороне живота. Отходы собираются в мешочке, который надевается на внешнюю часть вашего тела и не проходит через прямую кишку.
Вопросы, которые следует задать бригаде здравоохранения
Является ли непроходимость кишечника частым побочным эффектом того типа рака, который у меня есть?
Если я подвержен риску закупорки, на какие признаки или симптомы мне следует обращать внимание?
С кем мне связаться, если у меня появятся какие-либо признаки или симптомы непроходимости кишечника? Как скоро?
Что вызывает непроходимость кишечника? Как это лечить?
Можно ли принимать лекарства для облегчения симптомов непроходимости кишечника?
При необходимости какую операцию вы порекомендовали бы для лечения непроходимости кишечника? Каким будет мое выздоровление?
Следует ли мне отслеживать дефекацию или побочные эффекты рака во время лечения? Если да, то как лучше их отслеживать?
Связанные ресурсы
Обезвоживание
Как жить с мешком для стомы
Как добиться успеха, живя с мешком для стомы
Дополнительная информация
Национальный институт рака: желудочно-кишечные осложнения
Непроходимость кишечника — что вам нужно знать
- CareNotes
- Непроходимость кишечника
Этот материал нельзя использовать в коммерческих целях, в больницах или медицинских учреждениях. Несоблюдение может повлечь за собой судебный иск.
Несоблюдение может повлечь за собой судебный иск.
ЧТО НУЖНО ЗНАТЬ:
Что такое непроходимость кишечника?
Непроходимость кишечника возникает, когда толстый или тонкий кишечник полностью или частично заблокирован. Блокировка препятствует нормальному прохождению пищи и отходов.
Что вызывает непроходимость кишечника?
- Спайки — это полосы рубцовой ткани, которые могут образоваться после операции.Спайка прикрепляет кишечник к соседнему органу или стенке живота. Это может вывести кишечник из места и вызвать непроходимость.
- Грыжа возникает, когда часть кишечника выпирает через мышечную стенку брюшной полости. Грыжа может вызвать непроходимость, если кишечник застрянет.
- Опухоль может вызвать закупорку кишечника.
- Инородное тело может заблокировать кишечник. Инородное тело — это нечто иное, чем проглоченная еда.
- Скольжение или складывание части кишечника в другую часть кишечника может вызвать непроходимость кишечника.

- Заболевания , такие как болезнь Крона и дивертикулит, вызывают изменения в кишечнике, которые могут вызвать непроходимость кишечника.
- Скручивание кишечника может вызвать непроходимость кишечника.
Каковы признаки и симптомы непроходимости кишечника?
- Тошнота и рвота
- Боль в животе
- Живот увеличенный
- Уменьшение или отсутствие дефекации или газов
Как диагностируется непроходимость кишечника?
- Анализы крови могут показать, есть ли у вас инфекция или обезвоживание.Обезвоживание может развиться, когда ваш кишечник не может должным образом всасывать жидкость.
- Рентгеновский снимок делает снимки внутренних органов брюшной полости. Картинки используются для поиска препятствий.
- Для получения снимков кишечника можно использовать компьютерную томографию или магнитно-резонансную томографию . На фотографиях может быть показано место и причина блокировки.
 Вам могут дать краситель перед тем, как сделать снимок, чтобы медицинские работники лучше увидели закупорку. Сообщите врачу, если у вас когда-либо была аллергическая реакция на контрастный краситель.Не входите в кабинет МРТ с металлическими предметами. Металл может нанести серьезную травму. Сообщите врачу, если на вашем теле есть металл.
Вам могут дать краситель перед тем, как сделать снимок, чтобы медицинские работники лучше увидели закупорку. Сообщите врачу, если у вас когда-либо была аллергическая реакция на контрастный краситель.Не входите в кабинет МРТ с металлическими предметами. Металл может нанести серьезную травму. Сообщите врачу, если на вашем теле есть металл. - Ультразвук использует звуковые волны для отображения изображений вашего кишечника на мониторе. Чтобы определить место обструкции, может быть проведено ультразвуковое исследование.
Как лечится непроходимость кишечника?
- IV можно использовать для питья и питания. Возможно, вы не сможете ничего есть или пить, пока ваш лечащий врач не скажет, что это нормально.
- В нос можно ввести назогастральный зонд . Трубка проходит через горло и вводится в желудок. Трубка будет прикреплена к всасывающему устройству, которое удаляет воздух и жидкость из желудка.
- Антибиотики могут быть назначены для лечения или предотвращения инфекции, вызванной бактериями.

- Хирургическое вмешательство может быть выполнено для устранения причины закупорки.
Когда мне следует связаться с поставщиком медицинских услуг?
- У вас тошнота и рвота.
- Ваш живот увеличен.
- Вы не можете опорожнить кишечник или газы.
- Вы худеете, не стараясь.
- У вас кровь в кишечнике.
- У вас есть вопросы или опасения по поводу вашего состояния или ухода.
Когда мне следует немедленно обратиться за медицинской помощью или позвонить по номеру 911?
- У вас сильная боль в животе, которая не проходит.
- Ваше сердце бьется быстрее, чем обычно.
- У вас жар.
Соглашение об уходе
У вас есть право помочь спланировать свое лечение. Узнайте о своем состоянии здоровья и о том, как его можно лечить. Обсудите варианты лечения со своими поставщиками медицинских услуг, чтобы решить, какое лечение вы хотите получать. Вы всегда имеете право отказаться от лечения. Вышеуказанная информация носит исключительно учебный характер. Он не предназначен для использования в качестве медицинского совета по поводу индивидуальных состояний или лечения. Поговорите со своим врачом, медсестрой или фармацевтом перед тем, как следовать любому лечебному режиму, чтобы узнать, безопасно ли оно для вас и эффективно.
Вышеуказанная информация носит исключительно учебный характер. Он не предназначен для использования в качестве медицинского совета по поводу индивидуальных состояний или лечения. Поговорите со своим врачом, медсестрой или фармацевтом перед тем, как следовать любому лечебному режиму, чтобы узнать, безопасно ли оно для вас и эффективно.
© Copyright IBM Corporation 2020 Информация предназначена только для использования Конечным пользователем и не может быть продана, распространена или иным образом использована в коммерческих целях. Все иллюстрации и изображения, включенные в CareNotes®, являются собственностью A.D.A.M., Inc. или IBM Watson Health
, охраняемой авторским правом.
Подробнее о непроходимости кишечника
Сопутствующие препараты
IBM Watson Micromedex
Симптомы и лечение
Справочник клиники Майо
Дополнительная информация
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, отображаемая на этой странице, применима к вашим личным обстоятельствам.
Заявление об отказе от ответственности за медицинское обслуживание
Непроходимость тонкого кишечника: основы практики, предпосылки, патофизиология
Мензис Д., Эллис Х. Кишечная непроходимость из-за спаек — насколько велика проблема ?. Ann R Coll Surg Engl . 1990, январь 72 (1): 60-3. [Медлайн].
Hasnain SQ, Ахмед М. Кишечная непроходимость у взрослых в больнице Университета Ага Хана. Дж. Пак Мед Ассо . 1994 июн 44 (6): 143-5. [Медлайн].
Markogiannakis H, Messaris E, Dardamanis D, Pararas N, Tzertzemelis D, Giannopoulos P, et al.Острая механическая непроходимость кишечника: клиническая картина, этиология, лечение и исход. Мир Дж. Гастроэнтерол . 2007 21 января. 13 (3): 432-7. [Медлайн].
Томпсон В.М., Килани Р. К., Смит Б.Б., Томас Дж., Яффе Т.А., Делонг Д.М. и др. Точность рентгенографии брюшной полости при острой непроходимости тонкой кишки: имеет ли значение опыт рецензента ?. AJR Am J Roentgenol . 2007 Март 188 (3): W233-8. [Медлайн].
К., Смит Б.Б., Томас Дж., Яффе Т.А., Делонг Д.М. и др. Точность рентгенографии брюшной полости при острой непроходимости тонкой кишки: имеет ли значение опыт рецензента ?. AJR Am J Roentgenol . 2007 Март 188 (3): W233-8. [Медлайн].
Полсон Э.К., Томпсон ВМ.Обзор непроходимости тонкой кишки: диагноз и когда беспокоиться. Радиология . 2015 май. 275 (2): 332-42. [Медлайн].
Зери М., Сехрист CW, Керчер К.В., Синг РФ, Мэтьюз Б.Д., Хенифорд Б.Т. Лапароскопическое лечение непроходимости тонкой кишки. Am J Surg . 2007 декабрь 194 (6): 882-7; обсуждение 887-8. [Медлайн].
Хайкин М., Шнейдерайт Н., Сера С., Сэндс Д., Эфрон Дж., Вайс Э.Г. и др. Сравнение лапароскопических и открытых операций по поводу острой спаечной непроходимости тонкой кишки: результаты для пациентов и экономическая эффективность. Эндоскопическая хирургия . 2007 май. 21 (5): 742-6. [Медлайн].
Эндоскопическая хирургия . 2007 май. 21 (5): 742-6. [Медлайн].
Тейлор М.Р., Лалани Н. Обструкция тонкой кишки у взрослых. Acad Emerg Med . 2013 июн.20 (6): 528-44. [Медлайн].
van der Wal JB, Iordens GI, Vrijland WW, van Veen RN, Lange J, Jeekel J. Профилактика спаек во время лапаротомии: долгосрочное наблюдение за рандомизированным клиническим исследованием. Энн Сург . 2011 июн. 253 (6): 1118-21. [Медлайн].
Феванг Б.Т., Феванг Дж., Стангеланд Л., Сорейде О, Сванес К., Висте А.Осложнения и смерть после хирургического лечения непроходимости тонкой кишки: 35-летний опыт работы в учреждении. Энн Сург . 2000 апр. 231 (4): 529-37. [Медлайн]. [Полный текст].
Daneshmand S, Hedley CG, Stain SC. Полезность и надежность компьютерной томографии в диагностике непроходимости тонкой кишки. Am Surg . 1999 Октябрь 65 (10): 922-6. [Медлайн].
Am Surg . 1999 Октябрь 65 (10): 922-6. [Медлайн].
Lappas JC, Reyes BL, Maglinte DD. Результаты рентгенографии брюшной полости при непроходимости тонкой кишки: актуальность для сортировки для дополнительной диагностической визуализации. AJR Am J Roentgenol . 2001, январь 176 (1): 167-74. [Медлайн].
Diaz JJ Jr, Bokhari F, Mowery NT, Acosta JA, Block EF, Bromberg WJ, et al. Рекомендации по лечению непроходимости тонкой кишки. J Trauma . 2008 июнь 64 (6): 1651-64. [Медлайн].
Раптопулос В., Шварц Р.К., МакНиколас М.М., Мовсон Дж., Перлман Дж., Иоффе Н. Мультипланарная спиральная КТ-энтерография у пациентов с болезнью Крона. AJR Am J Roentgenol .1997 Декабрь 169 (6): 1545-50. [Медлайн].
Bodily KD, Fletcher JG, Solem CA, Johnson CD, Fidler JL, Barlow JM, et al. Болезнь Крона: затухание и толщина стенок при КТ-энтерографии с контрастированием — корреляция с эндоскопическими и гистологическими данными воспаления. Радиология . 2006 Февраль 238 (2): 505-16. [Медлайн].
Болезнь Крона: затухание и толщина стенок при КТ-энтерографии с контрастированием — корреляция с эндоскопическими и гистологическими данными воспаления. Радиология . 2006 Февраль 238 (2): 505-16. [Медлайн].
Енгин Г. Компьютерная томография энтероклиза в диагностике кишечных заболеваний. J Comput Assist Tomogr .2008 янв-фев. 32 (1): 9-16. [Медлайн].
Раджеш А., Маглинт Д.Д. Мультисрезовый КТ энтероклиза: техника и клиническое применение. Клин Радиол . 2006 января 61 (1): 31-9. [Медлайн].
Gollub MJ. Многодетекторная компьютерная томография энтероклиза пациентов с непроходимостью тонкой кишки: объемная «хирургическая перспектива». J Comput Assist Tomogr . 2005 май-июнь. 29 (3): 401-7. [Медлайн].
Каппелл М. С., Батке М.Механическая непроходимость тонкой и толстой кишки. Мед Клин Норт Ам . 2008 май. 92 (3): 575-97, viii. [Медлайн].
С., Батке М.Механическая непроходимость тонкой и толстой кишки. Мед Клин Норт Ам . 2008 май. 92 (3): 575-97, viii. [Медлайн].
Sheedy SP, Earnest F 4th, Fletcher JG, Fidler JL, Hoskin TL. КТ ишемии тонкой кишки, связанной с обструкцией, у пациентов отделения неотложной помощи: оценка диагностической эффективности. Радиология . 2006 Декабрь 241 (3): 729-36. [Медлайн].
Сури С., Гупта С., Судхакар П.Дж., Венкатараму Н.К., Суд Б., Парик Д.Д.Сравнительная оценка простых снимков, УЗИ и КТ в диагностике кишечной непроходимости. Acta Radiol . 1999 Июль 40 (4): 422-8. [Медлайн].
Kim JH, Ha HK, Sohn MJ, Shin BS, Lee YS, Chung SY и др. Полезность МРТ при заболеваниях тонкой кишки: сравнение с КТ. Корейский J Radiol . 2000 янв-март. 1 (1): 43-50. [Медлайн]. [Полный текст].
Риган Ф, Билл Д.П., Больман М.Э., Хазан Р., Суфи А., Шефер, округ Колумбия. Быстрая МРТ и обнаружение непроходимости тонкой кишки. AJR Am J Roentgenol . 1998 июн.170 (6): 1465-9. [Медлайн].
Rubio EI, Blask AR, Badillo AT, Bulas DI. Пренатальный магнитный резонанс и результаты ультразвукового исследования при непроходимости тонкого кишечника: ключи к изображениям и послеродовые исходы. Педиатр Радиол .2017 23 января [Medline].
Jang TB, Schindler D, Kaji AH. Прикроватное ультразвуковое исследование для выявления непроходимости тонкой кишки в отделении неотложной помощи. Emerg Med J . 2011 28 августа (8): 676-8. [Медлайн].
Emerg Med J . 2011 28 августа (8): 676-8. [Медлайн].
Di Saverio S, Coccolini F, Galati M, Smerieri N, Biffl WL, Ansaloni L и др. Болонские рекомендации по диагностике и лечению спаечной непроходимости тонкой кишки (ASBO): обновление 2013 г. основанных на фактических данных рекомендаций рабочей группы ASBO Всемирного общества экстренной хирургии. Мир J Emerg Surg . 2013 10 октября. 8 (1): 42. [Медлайн].
Скотт М., Мове Ф., Бубенхайм М. и др. Использование водорастворимого контрастного вещества (гастрографина) не снижает ни необходимость оперативного вмешательства, ни продолжительность пребывания в больнице при неосложненной острой спаечной непроходимости тонкой кишки? Многоцентровое рандомизированное клиническое исследование (исследование адгезивной непроходимости тонкого кишечника) и систематический обзор. Хирургия . 2017 10 января [Medline].
Cirocchi R, Abraha I, Farinella E, Montedori A, Sciannameo F.Сравнение лапароскопических и открытых операций при непроходимости тонкой кишки. Кокрановская база данных Syst Rev . 2010 17 февраля. CD007511. [Медлайн].
Wancata LM, Abdelsattar ZM, Suwanabol PA, Campbell DA Jr, Hendren S. Исходы после операции по поводу доброкачественной и злокачественной непроходимости тонкой кишки. Дж Гастроинтест Сург . 2017 21 февраля (2): 363-71. [Медлайн].
Алхилли М.М., Эль-Нашар С.А., Гарретт А.Т., Уивер А.Л., Фамуйде А.О. Использование компьютерной томографии в диагностике осложнений кишечника после гинекологических операций. Акушерский гинекол . 2013 6 ноября [Medline].
Хендерсон Д. Послеоперационная КТ может не выявить непроходимость кишечника. Medscape [сериал онлайн]. Доступно на http://www.medscape.com/viewarticle/814341. Доступ: 18 ноября 2013 г.
Medscape [сериал онлайн]. Доступно на http://www.medscape.com/viewarticle/814341. Доступ: 18 ноября 2013 г.
Fevang BT, Fevang JM, Soreide O, Svanes K, Viste A. Задержка в оперативном лечении пациентов с непроходимостью тонкой кишки. Scand J Surg . 2003. 92 (2): 131-7. [Медлайн].
Langer JC.Нарушения ротации кишечника и заворот средней кишки. Surg Clin North Am . 2017 Февраль 97 (1): 147-59. [Медлайн].
Сохандон Ф., Аль-Катиб С., Бахура Л., Копелан А., Джордж Д., Скола Д. Многодетекторная КТ-энтерография очаговых поражений тонкой кишки: радиологически-патологическая корреляция. Abdom Radiol (Нью-Йорк) . 2016 20 декабря. [Medline].
Ян К. Х., Ли ТБ, Ли Ш., Ким Ш., Чо Й., Ким Х. Врожденная спаечная лента, вызывающая непроходимость тонкой кишки: в чем разница между детьми и взрослыми в разных возрастных группах? BMC Surg . 2016 7 декабря. 16 (1): 79. [Медлайн].
2016 7 декабря. 16 (1): 79. [Медлайн].
Врожденная спаечная повязка, вызывающая непроходимость тонкого кишечника: в чем разница между детьми и взрослыми в разных возрастных группах? | BMC Surgery
Хотя врожденные спайки обычно выявляются у педиатрических пациентов, они могут вызывать SBO в любом возрасте. Частота возникновения врожденных спаек все еще остается неопределенной. Сообщалось, что частота спаек без предыдущих операций колеблется от 3.От 3 до 28% при вскрытии [9, 10]. Хотя настоящее исследование ограничено региональными ограничениями, частота встречаемости составила 5,9% (15/251). Клинические проявления врожденной спаечной повязки варьируются от легких симптоматических проявлений до удушения кишечника, что требует незамедлительного хирургического вмешательства. Однако поставить точный предоперационный диагноз сложно, так как не существует специальных тестов для диагностики врожденной спаечной повязки. Исключение других факторов, которые могут вызвать непроходимость кишечника, в настоящее время является лучшим методом диагностики. По этим причинам у пациентов с кишечной непроходимостью из-за врожденного сращения часто возникают поздняя диагностика и лечение. КТ использовалась для исключения других заболеваний во многих случаях [11–13], а также в настоящем исследовании. В конечном итоге как для диагностики, так и для лечения необходимо обследование. Более того, диагноз зависит от высокого индекса подозрительной механической непроходимости, особенно для пациентов, не ранее перенесших абдоминальные операции.
По этим причинам у пациентов с кишечной непроходимостью из-за врожденного сращения часто возникают поздняя диагностика и лечение. КТ использовалась для исключения других заболеваний во многих случаях [11–13], а также в настоящем исследовании. В конечном итоге как для диагностики, так и для лечения необходимо обследование. Более того, диагноз зависит от высокого индекса подозрительной механической непроходимости, особенно для пациентов, не ранее перенесших абдоминальные операции.
Настоящее исследование выявило несколько интересных клинических особенностей, различающихся в зависимости от возраста.У более молодых пациентов наблюдалась большая тенденция к осложнению случаев заворота или удушения, и хирургическое лечение проводилось на ранней стадии. Более того, объем хирургической процедуры был шире в педиатрической группе по сравнению с взрослой. Однако никаких статистически значимых различий между двумя группами обнаружено не было. Это могло быть связано с небольшим количеством случаев в каждой возрастной группе, учитывая редкость клинического проявления.
Предыдущие исследования показали, что наиболее частая анатомическая локализация врожденной спаечной ленты — вокруг терминальной части подвздошной кишки, за которой следуют корень брыжейки, тощая кишка, печень и сальник [5–8].В соответствии с этими предыдущими исследованиями, настоящее исследование также показало, что в обеих возрастных группах полоса чаще всего располагалась вокруг брыжейки подвздошной кишки и корня брыжейки. Однако расположение бандажа не влияет на клиническую картину или лечение.
Происхождение врожденных полос спаек имеет эмбриологическую основу, такую как стойкая или неполная регрессия желточного кровообращения плода или остаток теории вентральной брыжейки, и может быть связано с генетическими дефектами, нарушающими эмбриогенез [14–16].Кроме того, с формированием повязки могут быть связаны другие факторы, например, внутриутробная мезотелиома-травма [17]. Врожденные спайки могут быть также результатом внутриутробного воздействия определенных инфекционных агентов или ишемических событий. Несколько отчетов продемонстрировали доказательства иммунологического механизма как в экспериментах in vitro, так и in vivo [17–19]. Учитывая эмбриологическое происхождение, мы можем предположить, что врожденная спайка существует с рождения и поэтому может вызвать клиническое проявление раньше.Хотя эти факторы могут объяснить педиатрические случаи, они не объясняют надлежащим образом взрослые случаи. Вместо этого взрослые случаи могут быть объяснены как спайки de novo, которые показаны в исследовании аутопсии [9, 20]. Таким образом, различия в клинических характеристиках между возрастными группами, наблюдаемые в настоящем исследовании, могут быть связаны с многофакторными процессами, лежащими в основе развития врожденной спаечной полосы.
Несколько отчетов продемонстрировали доказательства иммунологического механизма как в экспериментах in vitro, так и in vivo [17–19]. Учитывая эмбриологическое происхождение, мы можем предположить, что врожденная спайка существует с рождения и поэтому может вызвать клиническое проявление раньше.Хотя эти факторы могут объяснить педиатрические случаи, они не объясняют надлежащим образом взрослые случаи. Вместо этого взрослые случаи могут быть объяснены как спайки de novo, которые показаны в исследовании аутопсии [9, 20]. Таким образом, различия в клинических характеристиках между возрастными группами, наблюдаемые в настоящем исследовании, могут быть связаны с многофакторными процессами, лежащими в основе развития врожденной спаечной полосы.
Кроме того, врожденные спайки могут вызывать обструкцию внутренней грыжей, о чем обычно сообщают в спорадических педиатрических случаях [11, 21].Однако в настоящем исследовании клинические случаи варьировались от новорожденных до пожилых людей, и только один случай внутренней грыжи был в педиатрической группе. Случай с внутренней грыжей показал тяжелую клиническую ситуацию с ущемлением пораженного сегмента, что потребовало оперативной хирургической резекции. Настоящее исследование немного отличалось от предыдущих исследований в отношении ведения, особенно в педиатрической группе, поскольку существовала тенденция к выполнению ранней операции и сегментарной резекции [4, 6].Это могло быть связано с относительно высокой долей новорожденных и младенцев в педиатрической группе, потому что SBO в этих возрастных группах связаны с высокой частотой неудач при консервативном лечении и обычно переходят к хирургическому лечению [22–24]. Более того, в предыдущих исследованиях сообщалось, что хирургическое вмешательство, которое включает резекцию кишечника, лучше для людей с более молодым возрастом и более длительным интервалом времени до операции более 2 дней [25]. Однако настоящее исследование не выявило значимой корреляции между временным интервалом до операции и необходимостью резекции кишечника.
Случай с внутренней грыжей показал тяжелую клиническую ситуацию с ущемлением пораженного сегмента, что потребовало оперативной хирургической резекции. Настоящее исследование немного отличалось от предыдущих исследований в отношении ведения, особенно в педиатрической группе, поскольку существовала тенденция к выполнению ранней операции и сегментарной резекции [4, 6].Это могло быть связано с относительно высокой долей новорожденных и младенцев в педиатрической группе, потому что SBO в этих возрастных группах связаны с высокой частотой неудач при консервативном лечении и обычно переходят к хирургическому лечению [22–24]. Более того, в предыдущих исследованиях сообщалось, что хирургическое вмешательство, которое включает резекцию кишечника, лучше для людей с более молодым возрастом и более длительным интервалом времени до операции более 2 дней [25]. Однако настоящее исследование не выявило значимой корреляции между временным интервалом до операции и необходимостью резекции кишечника.
В последнее время лапароскопическая процедура все чаще используется в случаях SBO с высоким показателем успеха (46 ~ 87%) [26–31]. Мы также попробовали лапароскопический подход в нескольких взрослых случаях с хорошими результатами, но не пробовали этот подход в педиатрических случаях из-за ограниченного рабочего пространства и высокого риска повреждения кишечника у педиатрических пациентов. Тем не менее, лапароскопическая процедура может быть отличным методом для диагностики и последующего лечения в случаях SBO, вызванного врожденной связкой.Учитывая трудности в диагностике, в отдельных случаях необходимо агрессивно предпринимать лапароскопические процедуры, независимо от возраста. Сообщается, что летальность, связанная с SBO, составляет менее 10% [32, 33]. Высокий уровень смертности в основном связан с задержкой постановки диагноза, которая с годами уменьшалась, а также со случаями, сопровождающими тяжелое основное заболевание.
Мы также попробовали лапароскопический подход в нескольких взрослых случаях с хорошими результатами, но не пробовали этот подход в педиатрических случаях из-за ограниченного рабочего пространства и высокого риска повреждения кишечника у педиатрических пациентов. Тем не менее, лапароскопическая процедура может быть отличным методом для диагностики и последующего лечения в случаях SBO, вызванного врожденной связкой.Учитывая трудности в диагностике, в отдельных случаях необходимо агрессивно предпринимать лапароскопические процедуры, независимо от возраста. Сообщается, что летальность, связанная с SBO, составляет менее 10% [32, 33]. Высокий уровень смертности в основном связан с задержкой постановки диагноза, которая с годами уменьшалась, а также со случаями, сопровождающими тяжелое основное заболевание.
Настоящее исследование имеет некоторые ограничения, в основном касающиеся количества случаев, которые были получены из опыта одного центра с региональными ограничениями.Однако, учитывая, что врожденные спайки являются редкой причиной SBO, представленные результаты для разных возрастных групп предоставляют ценную клиническую информацию.
Непроходимость тонкого кишечника
Обновление автора 2019: Табита Форд, доктор медицины, Университет Юты; Меган Фикс, Университет Юты,
Редактор обновления: Пратикша Наик, Мэриленд
Автор оригинала: Меган Фикс, доктор медицины; Университет штата Юта, Солт-Лейк-Сити, Юта
Оригинальные редакции: Дэвид Гордон, доктор медицины; Университет Дьюка, Дарем, Северная Каролина
Пример из практики
43-летняя женщина со значимым анамнезом для исследовательской лапаротомии с резекцией селезенки 10 лет назад обратилась с двухдневной болью в животе с рвотой.Три дня назад у нее было два эпизода некровавой диареи, и последние два дня у нее не было дефекации. По ее словам, в это время не было никаких газов. Вчера у нее началась некровавая рвота, а сегодня она не может принимать внутрь. При осмотре вы обнаруживаете неудобную женщину с тахикардией и вздутым животом, диффузно болезненным при пальпации, без ощущения отскока или осторожности.
Цели
По завершении этого модуля самообучения вы должны уметь:
- Составить список распространенных причин непроходимости тонкой кишки.
- Опишите классический вид и результаты физикального обследования непроходимости тонкой кишки.
- Обсудите доступные методы диагностики для диагностики непроходимости тонкой кишки.
- Опишите приоритеты лечения непроходимости кишечника.
- Определите, какие пациенты нуждаются в экстренном хирургическом вмешательстве или хирургической консультации.
Введение
Непроходимость кишечника следует рассматривать как потенциально неотложную хирургическую помощь, если у пациента возникает острая боль в животе.Это происходит, когда нормальный поток кишечного содержимого прерывается. Наиболее частыми причинами являются спайки, за которыми следуют опухоли и грыжи. Другие причины включают стриктуры, инвагинацию, заворот кишечника, болезнь Крона, инородные тела и камни в желчном пузыре. Обструкция классифицируется как непроходимость тонкой кишки (SBO) или непроходимость толстой кишки (LBO) в зависимости от уровня непроходимости. LBO чаще вызывается злокачественными новообразованиями и не будет подробно обсуждаться в этом модуле.
Обструкция классифицируется как непроходимость тонкой кишки (SBO) или непроходимость толстой кишки (LBO) в зависимости от уровня непроходимости. LBO чаще вызывается злокачественными новообразованиями и не будет подробно обсуждаться в этом модуле.
SBO начинается, когда нормальный просвет кишечного содержимого прерывается и тонкий кишечник проксимальнее непроходимости расширяется.При полном SBO секретам не разрешается проходить дистально. Со временем вздутие живота приводит к тошноте и рвоте, а также к невозможности перорального приема. Бактерии могут ферментировать проксимальный отдел кишечника и вызывать рвоту. По мере продолжения процесса стенка кишечника становится все более и более отечной, что приводит к транссудативной потере жидкости в брюшную полость. Это увеличивает степень дегидратации и электролитных нарушений, которые присутствуют у этих пациентов. Также могут наблюдаться снижение диуреза, тахикардия, азотемия и гипотензия.
Непроходимость кишечника можно определить как частичную или полную, простую или задушенную. Частичная закупорка — это когда газы или жидкий стул могут пройти через точку сужения, а полная закупорка — это когда никакие вещества не могут пройти. Частичная непроходимость далее характеризуется как высокая или низкая степень в зависимости от степени сужения и часто лечится консервативно. Полная непроходимость кишечника чаще приводит к неудачам при консервативной терапии и обычно требует оперативного вмешательства.Удушение является наиболее серьезным осложнением непроходимости тонкой кишки и требует неотложной хирургической помощи. Это происходит, когда отек стенки кишечника нарушает перфузию кишечника и возникает некроз. Если не вмешаться, это в конечном итоге приведет к перфорации, перитониту и смерти.
Частичная закупорка — это когда газы или жидкий стул могут пройти через точку сужения, а полная закупорка — это когда никакие вещества не могут пройти. Частичная непроходимость далее характеризуется как высокая или низкая степень в зависимости от степени сужения и часто лечится консервативно. Полная непроходимость кишечника чаще приводит к неудачам при консервативной терапии и обычно требует оперативного вмешательства.Удушение является наиболее серьезным осложнением непроходимости тонкой кишки и требует неотложной хирургической помощи. Это происходит, когда отек стенки кишечника нарушает перфузию кишечника и возникает некроз. Если не вмешаться, это в конечном итоге приведет к перфорации, перитониту и смерти.
Первоначальные действия и первичное обследование
Как и в случае со всеми пациентами, в первую очередь беспокоят непосредственные угрозы жизни. Осмотрите дыхательные пути, определив, не вызывает ли обильная рвота возможность аспирации. Пациенту с рвотой, который плохо себя чувствует, может потребоваться интубация для защиты дыхательных путей. Рвоту можно контролировать с помощью противорвотных средств и / или введения назогастрального зонда. Затем оцените дыхание пациента, при необходимости применив дополнительный кислород. У пациента, который выглядит остро больным с изменениями гемодинамики, такими как тахикардия или гипотензия, получите двусторонний внутривенный доступ и введите болюс кристаллоидных жидкостей по мере завершения обследования.
Пациенту с рвотой, который плохо себя чувствует, может потребоваться интубация для защиты дыхательных путей. Рвоту можно контролировать с помощью противорвотных средств и / или введения назогастрального зонда. Затем оцените дыхание пациента, при необходимости применив дополнительный кислород. У пациента, который выглядит остро больным с изменениями гемодинамики, такими как тахикардия или гипотензия, получите двусторонний внутривенный доступ и введите болюс кристаллоидных жидкостей по мере завершения обследования.
Презентация
История болезни
Пациент с непроходимостью тонкой кишки обычно проявляет боль в животе, вздутие живота, рвоту и неспособность отводить газы.При проксимальной обструкции более распространены тошнота и рвота. Боль часто описывается как спастическая и перемежающаяся с простой обструкцией. Если боль становится более сильной, это может указывать на развитие удушения или ишемии. Пациенты также могут жаловаться на диарею на ранних этапах непроходимости кишечника с невозможностью отхождения газов и непроходимостью, возникающей после опорожнения дистальной части кишечника (до 12-24 часов).
Важно установить анамнез предшествующих операций на брюшной полости, поскольку спайки являются наиболее частой причиной непроходимости тонкой кишки.Также важно иметь в анамнезе желудочно-кишечные расстройства, такие как болезнь Крона. Пациенту с непроходимостью тонкого кишечника без хирургического вмешательства в анамнезе следует обратиться к поиску основных причин, таких как опухоль или грыжа.
Физикальное обследование
Результаты физикального обследования включают вздутие живота (чаще встречается при дистальных обструкциях), гиперактивные кишечные шумы (ранние) или гипоактивные кишечные шумы (поздно). Лихорадка, тахикардия и перитонеальные признаки могут быть связаны с удушением.Также важно искать возможные причины непроходимости, такие как паховые грыжи, поэтому всегда проводите обследование мочеполовой системы. Ректальное исследование также важно, потому что макроскопический анализ крови или стул с гемоккультами могут указывать на удушение или злокачественное новообразование.
Диагностическое тестирование
Обычная рентгенография
Простая рентгенограмма представляет собой удобный диагностический метод благодаря низкой стоимости и доступности. Однако эти исследования ограничены низкой чувствительностью (всего 66–85%).У пациента с подозрительным обследованием брюшной полости целесообразно получить снимок грудной клетки в вертикальном положении, ища доказательства перфорации, предполагаемой свободным воздухом (требующей немедленной хирургической консультации), с последующей рентгенограммой брюшной полости в вертикальном положении / на спине.
Результаты на простой пленке, которые предполагают, что SBO включают уровни жидкости и воздуха в тонкой кишке или расширенных петлях тонкой кишки. Отсутствие воздуха в толстой или прямой кишке предполагает полную непроходимость, в то время как наличие воздуха в толстой кишке предполагает частичную непроходимость.Обычные рентгенограммы могут ввести в заблуждение в сложных случаях, а обычная простая пленка не исключает SBO.
Тонкая кишка Серия
Диагноз и степень непроходимости тонкой кишки могут быть подтверждены последующим обследованием тонкой кишки или энтероклином (двенадцатиперстная кишка закапывается воздухом и контрастом). Эти исследования раньше считались золотым стандартом для определения того, была ли обструкция частичной или полной. В последнее время КТ заменяет последующее наблюдение за тонкой кишкой для окончательного диагноза.
Компьютерная томография
Компьютерная томография заменила серию исследований тонкой кишки в качестве исследования выбора для дифференциации частичной и полной непроходимости, определения места и причины непроходимости, а также раннего выявления удушения. КТ одновременно чувствительна (более 96%) и специфична (до 100%) при диагностике СБО.
Обструкция присутствует, если петля тонкой кишки расширена более чем на 2,5 см в диаметре проксимальнее отчетливой переходной зоны спавшейся кишки диаметром менее 1 см. Гладкий клюв указывает на простую обструкцию без сосудистых нарушений; зазубренный клюв может указывать на удушение. Утолщение стенки кишечника, пневматоз и газ в воротной вене предполагают удушение.
Гладкий клюв указывает на простую обструкцию без сосудистых нарушений; зазубренный клюв может указывать на удушение. Утолщение стенки кишечника, пневматоз и газ в воротной вене предполагают удушение.
CT может также различать этиологию SBO; то есть внешние причины, такие как спайки и грыжи, вызванные внутренними причинами, такими как новообразования или болезнь Крона. Кроме того, он может определять множество других причин острой боли в животе, таких как абсцесс, грыжа, опухоль или воспаление.
При подозрении на полную непроходимость кишечника пероральный контраст часто не требуется, и его введение может вызвать у пациента дополнительный дискомфорт в дополнение к задержке постановки диагноза. Пациентам, у которых есть опасения по поводу частичного SBO, пероральный контраст может помочь в диагностике, а также может быть терапевтическим. Изображения с внутривенным контрастированием могут быть добавлены к неулучшенной КТ, чтобы помочь очертить альтернативные диагнозы и лучше продемонстрировать ишемию кишечника, если таковая имеется.
Рис.1.Обструкция тонкой кишки продемонстрирована расширением тонкой кишки на 2,97 см. Исходное изображение создано доктором Дженнифер Коттон, доктором медицины. Используется с разрешения. Контент предоставлен CC BY-NC-SA. Никаких изменений не было. 2019
Ультразвук в месте оказания помощи
В руках квалифицированного оператора УЗИ в месте оказания медицинской помощи (POCUS) можно использовать у постели больного для быстрой диагностики SBO, избегая радиационного воздействия. Чувствительность составляет 84–97,7% при специфичности 84–100%.
Результаты, указывающие на SBO, включают расширенные петли тонкой кишки (> 2.5 см), а также вихревое или возвратно-поступательное движение внутрипросветного содержимого в тонкой кишке. Визуализация свободной жидкости между расширенными петлями кишечника, отсутствие перистальтики и утолщение стенки кишечника> 3 мм предполагает наличие SBO, осложненного ишемией кишечника. Как и в случае обычных рентгенограмм, нормальные результаты POCUS не исключают SBO, и могут потребоваться дальнейшие исследования.
Как и в случае обычных рентгенограмм, нормальные результаты POCUS не исключают SBO, и могут потребоваться дальнейшие исследования.
FOAMed ресурсы для получения дополнительной информации о POCUS для SBO:
http: // www.ultrasoundpodcast.com/2012/10/episode-36-small-bowel-obstruction/
Лечение
Первоначальное лечение непроходимости тонкого кишечника состоит из следующих целей:
- Реанимация и замена электролитов
- Определение тяжесть и причина обструкции
- Декомпрессия желудочно-кишечного тракта
- Симптоматическое лечение
- Определение того, показано ли хирургическое вмешательство
Если пациент остро болен и / или имеет перитонеальные признаки, следует обратиться за неотложной хирургической консультацией и агрессивной реанимацией.Замена кристаллоида должна начинаться с 2 литров широко открытого кристаллоида со стандартным кислородом и мониторингом в соответствии с протоколом. Если остро необходимо хирургическое вмешательство, могут быть назначены профилактические антибиотики.
Если остро необходимо хирургическое вмешательство, могут быть назначены профилактические антибиотики.
У стабильного пациента, которому поставлен диагноз SBO, важно проконсультироваться с хирургом, чтобы определить, оправдано ли оперативное лечение. Если обследование пациента или компьютерная томография предполагают удушение (перитонит, утолщение стенки кишечника и т. Д.), Необходимо оперативное вмешательство.Если нет никаких признаков надвигающегося удушения, тогда может быть целесообразным неоперативное лечение.
Безоперационное лечение включает декомпрессию желудочно-кишечного тракта с помощью назогастрального зонда, внутривенное введение жидкости, покой кишечника, энтеральное введение водорастворимого контрастного вещества и симптоматическое лечение. Частая переоценка важна, чтобы убедиться, что у пациента не появляются признаки удушения. При необходимости следует вводить внутривенные препараты для снятия боли и тошноты.Пациент должен быть госпитализирован для наблюдения и проведения серийных обследований брюшной полости. Если улучшения не наблюдается, следует приступить к оперативному лечению.
Если улучшения не наблюдается, следует приступить к оперативному лечению.
Распоряжение
- ИЛИ: Пациентам с признаками удушения, перфорации, ишемии кишечника, непроходимости инородным телом или неэффективности консервативной терапии необходимо своевременно провести оперативное обследование и вмешательство.
- ОИТ: Пациенты с тяжелыми электролитными нарушениями или нуждающиеся в интубации для защиты дыхательных путей должны быть госпитализированы в ОИТ.Иногда очень больным пациентам требуется реанимация и оптимизация в ОИТ, прежде чем можно будет безопасно выполнить оперативное вмешательство.
- Этаж: Пациенты, которые клинически стабильны и не имеют осложнений, могут наблюдаться в стационаре с пробной консервативной терапией. Исследования показали более низкую заболеваемость и смертность у пациентов, поступивших в хирургические службы, а не в медицинские учреждения. Пациентов НЕ следует выписывать домой с частичной или полной непроходимостью кишечника.

Жемчуг и ловушки
- Спайки, перенесенные после хирургических вмешательств, являются наиболее частой причиной непроходимости тонкой кишки.
- На рентгенограммах брюшной полости может быть не обнаружена непроходимость тонкой кишки в 25% случаев, после чего следует выполнить КТ, если диагноз не ясен.
- Если возможно, ультразвук можно использовать для диагностики SBO без радиационного воздействия. Если подозрение остается, после отрицательного УЗИ следует выполнить КТ.
- Удушение является наиболее смертельным осложнением непроходимости тонкой кишки и может протекать без перитонеальных признаков при осмотре.
- Адекватная реанимация, ранняя консультация хирурга по поводу надвигающегося ущемления, декомпрессия желудочно-кишечного тракта и симптоматический контроль являются основой терапии.
Пример из практики
Пациенту из начала главы был обеспечен двусторонний внутривенный доступ и введен болюс жидкости с улучшением тахикардии. Лаборатории были важны для гипокалиемического, гипохлоремического метаболического алкалоза, и уровень калия был восполнен. Прикроватное ультразвуковое исследование показало заполненные жидкостью петли тонкой кишки, расширенные до 2.9 см, внутрипросветный гиперэхогенный материал многократно перемещается вперед и назад. Был установлен назогастральный зонд, и пациенту внутривенно вводили поддерживающую жидкость и анальгетики. В анамнезе у нее не было SBO, и точка перехода была неясна на УЗИ, поэтому была проведена компьютерная томография, которая продемонстрировала дистальную точку перехода тонкой кишки с признаками спаек. Ее поместили в общую хирургическую службу, консервативное лечение не удалось, и в конечном итоге ее отправили в операционную, где были лизированы спаечные процессы.У нее не было признаков ущемления или ишемии кишечника, и ее послеоперационное течение в больнице было ничем не примечательным.
Ссылки
Diaz JJ Jr, Bokhari F, Mowery NT, Acosta JA, Block EF, Bromberg WJ, et al. Рекомендации по лечению непроходимости тонкой кишки. J Trauma. Июнь 2008 г .; 64 (6): 1651-64.
Каппелл М.С., Батке М. Механическая непроходимость тонкой и толстой кишки. Med Clin North Am. Май 2008 г .; 92 (3): 575-97, viii.
Басс К.Н., Джонс Б., Балкли ГБ.Текущее лечение непроходимости тонкой кишки. Adv Surg. 1997; 31: 1-34.
Horton KM. Непроходимость тонкой кишки. Crit Rev Comput Tomogr. 2003; 44 (3): 119-28.
Кахи CJ, Рекс ДК. Непроходимость кишечника и псевдообструкция. Гастроэнтерол Clin North Am. Декабрь 2003 г.; 32 (4): 1229-47.
Tintinalli J, Kelen GD, Stapczynski JS. Кишечная непроходимость. В: Tintinalli J, ed. Медицина неотложной медицинской помощи: комплексное учебное пособие. 6-е изд. Макгроу-Хилл; 2004: 523-26.
Long B, Робертсон Дж., Койфман А.Оценка неотложной медицины и лечение непроходимости тонкой кишки: рекомендации, основанные на фактах. J. Emerg. Med. 2019; 56: 2: 166-176.
Непроходимость кишечника у собак
Непроходимость кишечника или закупорка кишечника — обычное явление у собак. Собаки — одни из самых любопытных животных на этой планете, и им нравится жевать и есть все, что попадает в их поле зрения.Если вы владелец собаки, то наверняка вам это хорошо известно.
Все собаки подвержены риску поражения кишечника, но более молодые собаки подвергаются наибольшему риску. Щенки более любопытны и стремятся положить что-нибудь в рот. Часто это происходит из-за того, что у них прорезываются зубы, и они хотят что-нибудь жевать — как младенцы!
В случае, если непроходимость кишечника действительно происходит, важны незамедлительная помощь и медицинская помощь для минимизации последствий. Продолжайте читать, чтобы узнать больше.
Что такое непроходимость кишечника у собак?
Непроходимость кишечника — это частичная или полная закупорка кишечника или желудка, которая препятствует прохождению жидкостей или твердых веществ через желудочно-кишечный тракт собаки. Этот тип закупорки может ограничить кровоток и привести к повреждению частей кишечника в дополнение к всасыванию токсичного содержимого. Линейные посторонние предметы, такие как волокна ковра, веревка и веревка, могут вызвать слипание кишечника друг с другом, как в телескоп.Подобные засоры могут быть вызваны либо проглатыванием посторонних материалов или предметов. Однако в некоторых случаях, особенно у пожилых собак, это может быть образование или опухоль.
Каковы признаки засорения чаши?
- Слабость
- Потеря аппетита
- Диарея
- Рвота, особенно повторяющаяся
- Боль в животе
- Вздутие живота
- Ныть или сутулиться
- Обезвоживание из-за невозможности удерживать жидкости
Что вызывает непроходимость кишечника у собак?
Чаще всего непроходимость кишечника у собак возникает, когда собака проглатывает посторонний материал или объект, например кость, камень, игрушку, веревку и т. Д.Подобные предметы не могут пройти через кишечник. В некоторых случаях они могут привести к перфорации кишечника и желудка.
Редко встречаются заболевания, которые могут вызвать непроходимость кишечника, такие как опухоли или образования, перекручивание кишечника, сужение прохода от желудка собаки к тонкому кишечнику, кишечные паразиты и грыжи.
Как диагностируют и лечат?
Если вы считаете, что ваша собака не может что-то проглотить, важно немедленно обратиться за медицинской помощью к ветеринару.Если его не лечить, ваша собака испытает сильный дискомфорт. Кроме того, ваша собака может потерять много жидкости, испытать разрыв кишечника или даже умереть. Пока вы не сможете отвезти собаку к ветеринару, не позволяйте ей есть что-нибудь еще.
Ваш ветеринар, скорее всего, проведет медицинский осмотр и ультразвуковое исследование или рентгенографию, чтобы попытаться подтвердить наличие инородного тела или образования. В некоторых случаях, если объект все еще находится в желудке или имеет подходящий размер, ветеринар может провести эндоскопию.Эндоскопия состоит из вставки тонкой трубки с камерой, прикрепленной к крошечному зажимному механизму в горле, в попытке извлечь объект.
Ветеринар может дать вашей собаке жидкости, чтобы предотвратить обезвоживание, и назначит лекарства, чтобы уменьшить тошноту, рвоту и боль. Если посторонний предмет не проходит через стул или если ветеринар считает, что предмет находился там слишком долго, может потребоваться операция. Это позволит ветеринару открыть кишечник или желудок, чтобы удалить объект, вызывающий закупорку.
Имейте в виду, что вы, как владелец собаки, никогда не должны пытаться вытащить посторонний предмет, если вы видите, как он выступает из прямой кишки собаки, поскольку это может привести к очень серьезным повреждениям.
После лечения обязательно следуйте инструкциям ветеринара и внимательно следите за своей собакой на предмет любых повторяющихся симптомов. Уровень активности должен оставаться низким, что означает запрет на длительные прогулки или бег в течение нескольких дней. Следует придерживаться мягкой диеты и на некоторое время отказаться от лакомств, поскольку вы постепенно начнете возвращать собаку к обычному рациону.Кроме того, убедитесь, что у вашей собаки достаточно пресной воды, чтобы предотвратить обезвоживание.
Как можно предотвратить непроходимость кишечника у собак?
В конечном счете, самый эффективный способ предотвратить непроходимость кишечника у собак — это отговорить вашу собаку есть определенные виды камней, палочек, костей и других подобных предметов, которые, как вы знаете, ей не следует пытаться есть. Держите свою собаку подальше от токсичных продуктов и других соблазнов. Вы также должны научить свою собаку команде «Оставь это:», так как это может помешать ей исследовать вредные предметы.Вашей собаке следует давать только те лакомства и игрушки, которые можно безопасно жевать. Если вы подозреваете что-то необычное, немедленно обратитесь к ветеринару.
Если у вас есть вопросы, свяжитесь с нами в HVSE.
Слезная закупорка: что теперь?
Взрослые пациенты с приобретенной обструкцией слезной дренажной системы жалуются на слезотечение — частую жалобу, которая может расстраивать как пациентов, так и практикующих врачей. Симптомы могут быть неспецифическими, односторонними или двусторонними, постоянными или прерывистыми.Пациенты могут жаловаться на явное появление эпифора, образование корок на веках или просто нечеткое зрение. Ведение варьируется в зависимости от уровня обструкции, и все сокращения для лечения начинают напоминать алфавитный суп. Чтобы прояснить ситуацию, вот обзор вариантов хирургического вмешательства на слезах у взрослого пациента с непроходимостью слезной железы.
Обзор анатомии
Эпифора возникает в результате обструкции на любом уровне аппарата слезного дренажа. После того, как слезы накапливаются в слезном озере, их
активно дренируются через слезную дренажную систему, трубчатую сеть диаметром от 35 до 37 мм, начинающуюся от точки ( См. Рис. 1A, ) и заканчивающуюся в слезной дренажной системе. нижний носовой ход.Слезная точка является воротами в систему оттока слезной железы; они открываются в трубчатые каналы ( см. рис. 1B, ), которые стекают в слезный мешок на клапане Розенмюллера ( см. рис. 1C, ). У большинства людей нижний и верхний канальцы сливаются, образуя общий канальец, прежде чем достичь клапана Розенмюллера. Слезный мешок простирается вниз и становится носослезным протоком, в конечном итоге впадая в нижний носовой ход у клапана Хаснера ( см. Рис. 1D, ).Согласно общепринятой номенклатуре, точка считается дистальным концом слезной дренажной системы, а клапан Хаснера — самой проксимальной структурой.
Приобретенная обструкция носослезного протока чаще всего возникает из-за воспаления и обструктивного фиброза, но может быть вторичной по отношению к более опасным процессам. Таким образом, тщательный сбор анамнеза и клиническая оценка важны для исключения этиологии, такой как травма, предшествующая операция, инфекция, системные воспалительные состояния или новообразования. Когда причину установить невозможно, используется термин первичная приобретенная обструкция носослезного протока (PANDO).В одном исследовании Нэнси Такер, доктор медицины, и ее коллеги из Университета Макгилла в Монреале выполнили биопсию слезного мешка у 150 пациентов, перенесших DCR по поводу клинически подозреваемого PANDO. Гистопатологические данные у 147 пациентов соответствовали воспалению или фиброзу, и только у трех из них была выявлена основная этиология (саркоидоз, онкоцитома и лимфома).
Обнаружение закупорки
При нормальном моргании и исследовании переднего сегмента необходимо оценить проходимость слезной дренажной системы.Вы можете локализовать препятствие путем систематического тестирования. Пальпация слезного мешка может выявить вздутие или выделение жидкости из точки, таким образом диагностируя обструкцию, открытые каналы и закупорку проксимальнее слезного мешка или носослезного протока. Следует избегать дальнейшего зондирования, чтобы предотвратить ятрогенное рубцевание. Значительное воспаление или инфекция мешка может указывать на дакриоцистит из-за застоя на фоне обструкции носослезного протока. Тяжелые случаи могут быть связаны с пресептальным целлюлитом, орбитальным целлюлитом или системной инфекцией, и этим пациентам следует госпитализировать внутривенно антибиотики.
Для борьбы с острой инфекцией может потребоваться разрез и дренирование, а после лечения острой инфекции следует рассмотреть возможность хирургической коррекции обструкции основного носослезного протока. (Наличие дакриоцистита является диагностическим, и дополнительное зондирование не требуется, особенно при острой инфекции.)
Если слезный мешок в норме, проходимость можно дополнительно оценить с помощью теста исчезновения флуоресцеинового красителя (FDDT), теста Джонса I, Джонса II тест и / или зондирование слезы и орошение.Рентгенографические методы, такие как сцинтилография слезной железы и дакриоцистография, являются вариантами, но редко используются в клинических условиях. Не существует стандартного алгоритма тестирования, и опрос членов Американского общества офтальмопластической и реконструктивной хирургии показал, что чуть меньше половины хирургов полагались в основном на орошение слезной жидкости, 21 процент использовали тест Джонса, 19 процентов использовали FDDT и 13 процентов. процентов использовали тестирование Ширмера.
Для выполнения FDDT закапайте одну каплю флуоресцеина в нижний тупик, подождите пять минут, затем повторно осмотрите пациента.Минимальный уровень флюоресцеина в слезном озере указывает на патентованную дренажную систему, а оставшийся флюоресцеин указывает на нарушение дренажа. Это особенно полезно в односторонних случаях, когда бессимптомный глаз можно использовать в качестве контроля. Хотя тест Джонса полезен в концептуальном плане, немногие врачи проводят его, и большинство полагается только на FDDT и промывание слезной жидкости. Начинается орошение слезы
| Рис. 2. Трубка Джонса предназначена для легкого удаления, так как она удерживается на месте только за счет трения и небольшого воротника. |
с расширением точечной точки, отмечая какие-либо признаки стеноза точки. Затем через точку и в каналец осторожно вводится слезная канюля, которая останавливается, если возникает какое-либо сопротивление. Каналлюс является проходимым, если канюля легко продвигается кнутри, пока не будет достигнута жесткая остановка на переносице (слезной ямке), но это можно дополнительно оценить с помощью зонда Боумена. Как только сопротивление встречается, либо во время продвижения, либо в слёзной ямке, систему орошают, внимательно наблюдая за обеими точками на предмет рефлюкса.Немедленный рефлюкс через ту же точку указывает на обструкцию дистального канальца, тогда как рефлюкс из противоположного канальца указывает на закупорку за пределами общего канальца, скорее всего, в носослезном протоке. Если жидкость может попасть в носовой ход под давлением, имеется неполная, но функциональная непроходимость нижней слезной системы. Если жидкость легко проходит в нос без особого давления, система свободно патентована. Однако ирригация оказывает давление на слезную систему, и проходимость в нефизиологических условиях не исключает частичной непроходимости.
Канальцевая непроходимость
После локализации непроходимости лечение заключается в обходе или реканализации места обструкции. Дистальные обструкции, затрагивающие канальцы, могут быть особенно сложными и часто требуют полного обхода аппарата слезного дренажа. Конъюнктиводакриоцисториностомия (CDCR) с размещением стеклянной трубки Джонса является золотым стандартом в лечении. Эта процедура соединяет слезное озеро и носовую полость с помощью хирургической стомы и использует стеклянную трубку для поддержания проходимости канала с течением времени.Показатели успеха достигают 90 процентов, но пациенты могут испытывать трудности с переносимостью и обслуживанием трубки Джонса. По своей конструкции трубка Джонса легко снимается для проведения частой очистки, необходимой для предотвращения закупорки и образования биопленки. Она удерживается на месте простым трением и небольшим воротником для предотвращения миграции внутрь ( см. Рис. 2, ), и, следовательно, смещение и экструзия трубки могут происходить почти у половины пациентов. Пациенты также могут испытывать периодические закупорки, неправильное положение, трудности с достижением желаемой скорости оттока слезы и ретроградный поток воздуха при чихании или использовании CPAP.
Перед CDCR следует учитывать высокий уровень осложнений, и были предприняты альтернативные методы, чтобы избавить пациентов от бремени трубки Джонса. В случаях дистальной обструкции с открытыми верхними или нижними канальцами не менее 8 мм, продолжающимися с точкой, можно попытаться применить каналикуло-DCR. Для этой процедуры выполняется наружная дакриоцисториностомия, как описано в следующем разделе, с последующим зондированием каналов до точки закупорки. Обструкцию резецируют, и открытый каналец анастомозируют непосредственно в слезный мешок.Наилучшие результаты достигаются при небольших препятствиях, расположенных рядом с общим канальцем или внутри него. Долгосрочный успех этой технически сложной процедуры случается редко, и в этих случаях часто требуется последующий CDCR с трубкой Джонса.
В качестве альтернативы обходу непроходимости заблокированный каналец можно реканализовать с помощью трепанации. Для этой процедуры в канальцевую систему вводят полую трубку с режущей кромкой внутри защитного иглы. При обнаружении препятствия игла вынимается и выполняется трепанация, осторожно вращая инструмент.Это продолжается до тех пор, пока инструмент не достигнет твердой слезной ямки, соблюдая особую осторожность, чтобы избежать образования ложного прохода по пути. Показатели успеха могут варьироваться в зависимости от местоположения обструкции и опыта хирурга. В одном недавнем исследовании сообщалось о 78-процентном функциональном успехе и 84-процентном анатомическом успехе через шесть месяцев в сочетании с эндоскопической ДКР и стентированием силиконовой трубки. Анатомический успех увеличился до 95 процентов для хирургов со стажем более пяти лет.Этот метод применялся как начальное хирургическое вмешательство или после ранее неудачной операции DCR.
Обструкция носослезного протока
Дакриоцисториностомия является основным методом лечения обструкции носослезного протока без поражения канальцев. DCR создает канал между слезным мешком и носовой полостью и может выполняться наружно или эндоназально.
Наружная процедура DCR начинается с начального разреза на уровне медиального кантального сухожилия, которое расширяется на 15-20 мм снизу-латерально вдоль боковой части носа.Тупая диссекция используется для обнажения надкостницы, которая отражается и обнажает неповрежденный слезный мешок. После извлечения мешка из слезной ямки в слезной ямке создается стома для доступа к слизистой оболочке носа, которая анастомозирует со слизистой оболочкой слезного мешка. Успешный DCR соединяет открытую канальцевую систему с носовым каналом на уровне слезного мешка, минуя любую дополнительную обструкцию носослезного протока проксимально.
Endonasal DCR выполняет ту же задачу, но обеспечивает доступ к слезному мешку через носовую полость.Эндоназальный доступ предлагает определенные преимущества, такие как отсутствие внешнего рубца, меньшая частота осложнений, более короткое время операции и полное сохранение помповой функции за счет исключения любых манипуляций с orbicularis oculi. Однако эндоназальный DCR часто составляет
| Рис. 3. Расширение баллонного катетера может быть эффективным у некоторых пациентов, страдающих обструкцией носослезного протока. |
дороже и оборудование менее доступно.Также подозревались более низкая эффективность и более высокая частота рецидивов при эндоназальном применении DCR. Однако недавний Кокрановский обзор показывает, что показатели успеха механической эндоназальной ДКР сопоставимы с внешней ДКР в опытных руках (примерно 95% в обеих процедурах) и что такие осложнения, как инфекция раны и послеоперационное кровотечение, могут быть менее вероятными.
Стентировать или нет
Моноканаликулярные или биканаликулярные стенты с силиконовыми трубками можно устанавливать во время наружной или эндоназальной хирургии DCR.Было предпринято несколько попыток предотвратить закрытие отверстия устья с ограниченной эффективностью. Показатели успешности DCR без стентирования превосходны, и исследования не показали каких-либо явных преимуществ стентирования. Кроме того, эта практика не совсем безобидна, а осложнения, связанные со стентированием, включают пролапс, истирание роговицы, каналикулит, спайки, образование ложных проходов во время интубации и разводку точек в точке.
Альтернативные методы
Хотя DCR является золотым стандартом, были изучены другие процедуры, направленные на реканализацию носослезного протока.Сообщается о некотором успехе при использовании дилатации баллонного катетера для лечения приобретенного частичного NLDO у пациентов ( см. Рис. 3 ). В небольшом проспективном исследовании 60 процентов пациентов сообщили о субъективном улучшении, а 73 процента были объективно патологическими после ирригации через шесть месяцев. Также была предпринята попытка зондирования NLD с адъювантом митомицином C, при этом в одном исследовании сообщалось о 84-процентной проходимости через девять месяцев. Группа китайских хирургов сообщает об использовании высокочастотного электрического прижигания для реканализации NLD с 87-процентной вероятностью успеха.Хотя доказательства далеко не окончательные, эти минимально инвазивные методы могут предложить пациентам дополнительные возможности в ожидании дальнейшего исследования.
Взрослых пациентов с слезоточивостью сложно оценить, но правильный диагноз имеет решающее значение для выбора лечения. Хирургическое лечение основано на уровне обструкции, поэтому необходимо тщательное понимание анатомии и физиологии слезной системы в сочетании с хорошей систематической оценкой. Имейте в виду, что тщательный анамнез может выявить серьезную патологию, требующую дополнительного обследования и лечения, помимо коррекции слезотечения.
Д-р Лютер в настоящее время является резидентом по офтальмологии на втором курсе Бостонского университета. Доктор Армстронг — директор отделения окулопластики, орбитальной и реконструктивной хирургии в Бостонском университете, где она также является доцентом офтальмологии.
Рекомендуемая литература:
1. Cannon PS, Chan W, Selva D. Частота закрытия канальцев при эндоназальной дакриоцисториностомии без интубации при первичной обструкции носослезного протока. Офтальмология 2013; 120: 8: 1688-1692.
2. Chen D, Ge J, Wang L, et al. Доказано, что простой и эволюционный подход к реканализации обструкции носослезного протока. Br J Ophthalmol 2009; 93: 11: 1438-1443.
3. Conway ST. Оценка и лечение «функциональной» носослезной блокады: результаты исследования Американского общества офтальмопластической и реконструктивной хирургии. OPRS 1994; 10: 185-188.
4. Chong KKL, Lai FHP, Ho M, Luk A, Wong BW, Young A. Рандомизированное испытание силиконовой интубации при эндоскопической механической дакриоцисториностомии (SEND) при первичной обструкции носослезного протока.Офтальмология 2013; 120: 10: 2139-2145.
5. Daubert J, Nik N, Chandeyssoun PA, el-Choufi L. Анализ потока слезы через верхнюю и нижнюю системы. Ophthal Plast Reconstr Surg 1990; 6: 3: 193-196.
6. Доан MG. Мигание и механика слезооттока. Офтальмология 1981; 88: 8: 844-851.
7. Dolmetsch AM. Нелазерная эндоскопическая эндоназальная дакриоцисториностомия с добавлением митомицина С при обструкции носослезного протока у взрослых. Офтальмология 2010; 117: 5: 1037-1040.
8. Фэн Й, Цай Дж, Чжан Дж, Хань Х.Метаанализ первичной дакриоцисториностомии с силиконовой интубацией и без нее. Кан Ж. Офтальмол 2011; 46: 6: 521-527.
9. Фостер Дж. А., Картер К. Д., Дурайрадж В. Д., Кавана М. С., Корн Б. С., Нельсон С. С., Хартштейн М. Е.. Курс фундаментальных и клинических наук, Раздел 07: Орбиты, веки и слезная система. Сан-Франциско: Американская академия офтальмологии, 2016-2017: 251-256, 267-276, 284-285.
10. Jawaheer L, MacEwen CJ, Anijeet D. Сравнение эндоназальной и наружной дакриоцисториностомии при обструкции носослезного протока.Кокрановская база данных Syst Rev 2017 24 февраля; 2: CD007097.
11. Калин-Хайду Э, Кадет Н, Булос ПР. Споры слезной системы. Surv Ophthalmol 2016; 61: 3: 309-313.
12. Кашкоули М.Б., Бейги Б., Мурти Р., Астбери Н. Приобретенный стеноз наружной точки: этиология и связанные с ней данные. Am J Ophthalmol 2003; 136: 6: 1079-1084.
13. Kong YJ, Choi HS, Jang JW, Kim SJ, Jang SY. Хирургические результаты канальцевой трепанации в сочетании с эндоскопической дакриоцисториностомией у пациентов с дистальной или общей канальцевой обструкцией.Корейский журнал J Ophthalmol 2015; 29: 6: 368-374.
14. Лиаракос В., Боборидис К., Маврикакис Э., Маврикакис И. Лечение канальцевой непроходимости. Курр Опин Офтальмол 2009; 20: 5: 395-400.
15. Линберг, СП, Маккормик С.А. Первичная приобретенная непроходимость носослезного протока. Клинико-патологический отчет и методика биопсии. Офтальмология 1986; 93: 8: 1055-1063.
16. Натху Н.А., Рат С., Ван Д., Баффам Ф. Трепанация канальцевой непроходимости: опыт в 45 глазах. Орбита 2013; 32: 5: 281-284.
17. Патель BC.Лечение приобретенной обструкции носослезного протока: Наружная и эндоназальная дакриоцисториностомия. Есть ли третий способ? Br J Ophthalmol 2009; 93: 11: 1416-1419.
18. Патринели JR, Андерсон RL. Обзор хирургии слезного дренажа. Ophthal Plast Reconstr Surg 1986; 2: 2: 97-102.
19. Perry JD, Maus M, Nowinski TS, Penne RB. Расширение баллонного катетера для лечения взрослых с частичной обструкцией носослезного протока: предварительный отчет. Am J Ophthalmol 1998; 126: 6: 811-816.
20. Rose GE, Welham RA.Шунтирование слезных канальцев Джонса: опыт двадцати пяти лет. Eye (Лондон) 1991; 5 (Pt 1): 13-19.
21. Стил EA. Конъюнктиводакриоцисториностомия с трубкой Джонса: история и обновления. Curr Opin Ophthalmol 2016; 27: 5: 439-442.
22. Цай СС, Кау ХК, Као СК, Сюй ВМ, Лю Дж. Х. Эффективность зондирования носослезного протока с дополнительным митомицином-C для эпифора у взрослых. Офтальмология 2002; 109: 1: 172-174.
23. Tucker N, Chow D, Stockl F, Codere F, Burnier M. Клинически подозреваемая первичная приобретенная обструкция носослезного протока: Клинико-патологический обзор 150 пациентов.Офтальмология 1997; 104: 11: 1882-1886.

 Характерна для американского Сената, в котором высоко почитается право свободного обсуждения.
Характерна для американского Сената, в котором высоко почитается право свободного обсуждения. — 2002
— 2002 Если через несколько дней закупорка не улучшится, вам может потребоваться внутривенное питание.
Если через несколько дней закупорка не улучшится, вам может потребоваться внутривенное питание. Это временно удерживает заблокированную область желудочно-кишечного тракта.
Это временно удерживает заблокированную область желудочно-кишечного тракта.
 Вам могут дать краситель перед тем, как сделать снимок, чтобы медицинские работники лучше увидели закупорку. Сообщите врачу, если у вас когда-либо была аллергическая реакция на контрастный краситель.Не входите в кабинет МРТ с металлическими предметами. Металл может нанести серьезную травму. Сообщите врачу, если на вашем теле есть металл.
Вам могут дать краситель перед тем, как сделать снимок, чтобы медицинские работники лучше увидели закупорку. Сообщите врачу, если у вас когда-либо была аллергическая реакция на контрастный краситель.Не входите в кабинет МРТ с металлическими предметами. Металл может нанести серьезную травму. Сообщите врачу, если на вашем теле есть металл.