симптомы, лечение метастаз в печени, сколько живут с метастазами печени, МТС печени
Что такое метастазы рака в печень?
Метастазами называют вторичные очаги, которые возникают, когда раковые клетки из основной, «материнской», опухоли отрываются и мигрируют с током крови или лимфы в разные части тела. Метастазы могут возникать в разных органах. Зачастую их обнаруживают в печени.
Если опухоль изначально развивается из печеночной ткани, возникает первичный рак печени. Метастатический рак называют вторичным — он всегда происходит из других органов. Большинство злокачественных опухолей печени — вторичный рак.
Мне поставили метастазы в печени с первичным очагом в кишечнике. Очень надеялся, что успеем пролечить кишечник, но не успели — я долго тянул с бумагами в другой клинике. Так вот, когда они обнаружились — у меня, естественно, опустились руки, и я уже мысленно представил себе оставшиеся недели. Благо, в современное обезболивание я верю, а в то, что с поражениями в печени можно выжить — не верилось. Так оно и было бы, если бы я не попал к доктору Пылёву. Он нашёл выход. И это меня спасло.
Показать полностью »
Не помню точное название операции — оно очень длинное, с какими-то индексами, но, по сути, как Андрей Львович объяснил мне на пальцах — на моё счастье, три очага образовались в одной доле печени. На моё несчастье — в той что больше, а значит, важнее. Просто взять и отрезать её нельзя. Оставшийся кусок не выдержит нагрузки.
Решение состояло из двух операций. Первая — он как-то перенаправил кровоток в печени таким образом, чтобы меньшая часть печени получала больше крови чем та, что больше. За счет этого, малая доля начала расти! И значит, стала принимать на себя всё больше нагрузки. Чуть меньше чем через месяц она уже была такого размера, которого хватает на почти нормальную работу печени как органа.
Второй операцией он удалил заражённую долю. И малая теперь работает в одиночку, но адаптируется к нагрузкам.
Не думал, конечно, что мне в жизни придётся обо всём этом узнать, а тем более испытать на себе. Но, как сказал доктор, ещё недавно такие операции не проводились совсем. Вот уже прошло полгода после первоначального диагноза. Я думаю, их у меня не было бы, если бы не моя удача — попасть к этим докторам.
Хватит ли вообще каких-то слов, чтобы выразить благодарность от меня и детей? Не думаю. Но всё равно, спасибо им.
Откуда раковые клетки метастазируют в печень?
Метастатический рак печени часто происходит из легких, желудка, толстой и прямой кишки, молочных желез, пищевода, поджелудочной железы.
При раке легких, желудка и колоректальном раке метастазы в печени обнаруживаются в 50% случаев, при раке груди, меланоме — в 30% случаев.
Редко в печень метастазируют злокачественные опухоли матки и яичников, глотки, полости рта, мочевого пузыря, почек. Метастазы в печени при раке головного мозга практически не встречаются.

Почему многие опухоли метастазируют в печень?
Печень — один из самых больших органов. Она выполняет важные функции: очищает кровь от токсинов, вырабатывает желчь, производит разные белки, ферменты, хранит запасы гликогена, который является источником энергии.
Через печень проходит огромное количество крови — примерно 1,5 литра в минуту. Около 30–35% крови поступает по артериям, остальные 70–75% — по воротной вене от кишечника. Внутри печени находятся особые синусоидные капилляры (синусоиды), в которых кровоток замедляется, артериальная кровь смешивается с венозной, вместе они возвращаются к сердцу по нижней полой вене.
Такая особенная система кровоснабжения печени способствует распространению раковых клеток.

Прежде чем основать собственную «колонию» — метастатическую опухоль — в печени, раковой клетке приходится проделать длинный путь. Она должна оторваться от материнской опухоли, проникнуть в кровеносный или лимфатический сосуд, совершить путешествие по организму и осесть в печеночной ткани. Она может погибнуть (и многие раковые клетки погибают) на любом этапе.
До определенного момента материнская опухоль и иммунитет сдерживают рост метастазов. Мигрировавшие раковые клетки либо неактивны, либо размножаются очень медленно. Затем начинается их бурный рост. Ученым до конца не известно, почему это происходит. По мере того как раковых клеток в метастазе становится больше, они начинают вырабатывать факторы роста, которые стимулируют рост новых сосудов, питающих опухоль.
Как проявляются метастазы рака в печень? При каких симптомах нужно обратиться к врачу?
На ранних стадиях, как и при многих злокачественных опухолях, метастазы рака в печени никак себя не проявляют. Со временем очаги увеличиваются, начинают мешать кровотоку и оттоку желчи. Работа печени нарушается, возникают различные симптомы:
- Слабость, утомляемость, снижение работоспособности.
- Снижение веса вплоть до крайней степени истощения — кахексии.
- Ухудшение аппетита вплоть до анорексии.
- Тошнота, рвота.
- Землистый цвет кожи или желтуха.
- Тупые боли под правым ребром. Чувство тяжести, распирания, давления.
- Увеличение живота из-за водянки (асцита).
- Расширенные вены под кожей живота (зачастую картина весьма характерна: вены расходятся во все стороны от пупка и напоминают «голову медузы»).
- Сосудистые звездочки на коже.
- Учащение сердцебиения.
- Повышение температуры.
- Кожный зуд.
- Нарушение работы кишечника, вздутие живота.
- Кровотечения в пищеводе.
- Гинекомастия (увеличение и нагрубание молочных желез у мужчин).
Такие расстройства встречаются не только при раке печени. Конечно, нет поводов для паники, если из этого списка вас беспокоит только слабость, повышенная температура и вздутие живота.
Самые грозные симптомы, которые должны стать поводом для немедленного визита к врачу: упорная рвота: более 1 дня, более 2-х раз в день, рвота с кровью, быстрая необъяснимая потеря веса, стул черного цвета, сильное увеличение живота, желтуха.
Метастазы в любом органе, в том числе в печени, могут стать причиной постоянных мучительных болей.
Как диагностируют метастазы рака в печень?
Обследование может включать разные исследования и анализы:
- УЗИ печени — простой и доступный метод диагностики, его часто используют для скрининга. Но он не всегда помогает найти метастазы и получить о них нужную информацию.
- Методы визуализации: мультиспиральная КТ, МРТ, ПЭТ, ангиография (исследование, во время которого в сосуды вводят контрастное вещество). Помогают не только обнаружить метастазы в печени, но и оценить их размеры, количество, расположение, характер роста, обнаружить нагноение и распад, распространение в соседние ткани и органы.
- Зачастую для того чтобы назначить эффективное лечение, врачу нужно знать, какое строение опухолевая ткань имеет на микроскопическом уровне, насколько сильно раковые клетки отличаются от нормальных. Для этого проводят биопсию: фрагмент опухолевой ткани получают при помощи иглы (тонкоигольная аспирационная биопсия) или специального инструмента — трепана (кор-биопсия, трепанобиопсия). Процедуру проводят под контролем УЗИ.
- Анализы крови, в частности, на уровень печеночных ферментов, помогают понять, насколько сильно нарушена работа печени.
«Во время биопсии в опухоль втыкают иглу. Могут ли из-за этого раковые клетки отрываться и метастазировать?»
Это миф. Биопсия не повышает риск метастазирования.
Зачастую во время обследования сначала выявляют метастазы в печени, а затем начинают искать первичную опухоль. Задачу облегчает биопсия: зная, как выглядят под микроскопом раковые клетки, врач может понять, из какого органа они происходят.
Как лечат метастазы в печени?
Тактика лечения будет зависеть от некоторых факторов:
- Количество метастазов: являются ли они одиночными или множественными.
- Тип рака.
- Выраженность нарушений работы печени и других органов.
Основные методы лечения — те же, что и при других онкологических заболеваниях. Одиночные метастазы (или несколько небольших) можно удалить хирургическим путем. Проводят долевую, сегментарную, атипичную резекцию (удаление части органа).
Назначают курсы химиотерапии, лучевой терапии.
Врачи Европейской онкологической клиники применяют современный метод лечения метастатического рака печени, который часто практикуется в зарубежных клиниках — чрескожную чреспеченочную радиочастотную аблацию (РЧА).
Результаты лечения
 3A — метастазы рака в печени 3A — метастазы рака в печени3В — редукция опухоли после проведенной химиоэмболизации 3C — уменьшение метастазов после радиочастотной аблации (РЧА) 3D — результат терапии через 6 месяцев |
Во время процедуры в метастаз вводят специальную иглу-электрод и подают через неё радиоволны, которые уничтожают раковые клетки. В итоге происходит контролируемый асептический некроз опухоли без повреждения окружающих здоровых тканей. Это позволяет значительно повысить выживаемость и снизить риск рецидива.
РЧА уникальна тем, что её можно применять повторно, если в печени выявлены новые метастазы. Методику успешно применяют при первичном раке печени, когда одновременно имеется цирроз и высокий риск печеночной недостаточности.
Например, мы смогли добиться стойкой ремиссии и, возможно, полного выздоровления у одной пациентки, у которой был диагностирован рак молочной железы с одиночными метастазами в печени. Врачи Европейской онкологической клиники выполнили радикальную мастэктомию и долевую резекцию печени, которые были дополнены курсом химиотерапии.
Также хороший результат был достигнут у пациента с раком толстой кишки и пятью небольшими метастазами в разных долях печени. Мы выполнили резекцию (удалили часть кишки), провели курс химиотерапии и радиочастотную аблацию печени.
Лечение метастазов рака в печень имеет некоторые сложности. Например, метастатический рак часто не реагирует на препараты, которые помогали против первичной опухоли. Приходится подбирать оптимальную терапию, комбинировать разные виды лечения. Плохо реагируют метастазы в печени и на системную химию. Наилучший эффект дает введение препаратов в печеночную артерию.
Химиопрепараты помогают замедлить рост метастазов, уменьшить их количество, продлить жизнь больного и избавить от мучительных симптомов. На ранних стадиях курс химиотерапии снижает риск метастазирования. В случаях, когда это необходимо, врачи Европейской онкологической клиники применяют имплантируемые венозные и артериальные порт-системы, регионарную инфузию химиопрепаратов внутриартериально.
Лучевая терапия при метастазах рака в печень помогает избавиться от боли, но не увеличивает продолжительность жизни.
Таргетная терапия предусматривает использование препаратов, которые имеют конкретную «мишень» — определенную молекулу, необходимую для роста и выживания раковых клеток. При метастатическом раке печени используют единственный таргетный препарат с доказанной эффективностью — сорафениб. Он зарегистрирован более чем в 60 странах мира для лечения первичного и метастатического рака печени.
Эмболизация — перспективный метод лечения метастазов в печени и других злокачественных опухолей, который применяется в отделении интервенционной онкологии и эндоваскулярной хирургии в Европейской онкологической клинике. Суть метода состоит в том, что в сосуд, питающий опухоль, вводят специальный препарат, который нарушает приток крови.
Наиболее эффективна химиоэмболизация, когда в сосуд вводят микросферы, которые выделяют химиопрепарат. Химиоэмболизация в настоящее время — «золотой стандарт» лечения в случаях, когда не удается выполнить хирургическое удаление опухоли или трансплантацию.
Во время химиоэмболизации достигается двойной эффект. Микросферы перекрывают кровоток, лишая опухоль необходимых веществ, а выделяющийся химиопрепарат атакует опухолевые клетки.
В Европейской онкологической клинике доступны все существующие препараты для химиоэмболизации.
О возможностях современной высокотехнологичной медицины в лечении опухолей печени в программе Health Kitchen на телеканале Дождь.
Восстановление печени после удаления метастаза
Если после хирургического лечения по поводу метастазов в печени при 4 стадии рака в органе больше не обнаруживаются раковые клетки, врач порекомендует делать снимки (УЗИ, КТ или МРТ) и сдавать анализы (на уровень альфа-фетопротеина, веществ, которые характеризуют функцию печени) раз в 3–6 месяцев в течение первых двух лет, затем — раз в 6–12 месяцев. Это помогает вовремя обнаружить рецидив или возможные побочные эффекты лечения.
Ускорить восстановление печени и всего организма помогает здоровая диета, физическая активность в соответствии с рекомендациями врача.
Какие могут возникать осложнения? Когда нужны экстренные меры?
Опухоль в печени может сдавить воротную вену, нижнюю полую вену, желчные протоки. В последнем случае нарушается отток желчи. Содержащийся в ней токсичный продукт распада гемоглобина — билирубин — начинает поступать в кровь. Кожа, склеры и слизистые оболочки окрашиваются в желтый цвет — возникает механическая желтуха. Это состояние опасно тем, что билирубин токсичен для головного мозга и других органов, сильное повышение его уровня может привести к гибели. Кроме того, из-за механической желтухи невозможно выполнить операцию и провести курс химиотерапии.
Отток желчи восстанавливают хирургическим путем, под контролем УЗИ (пункционная холангиография) или рентгенотелевидения. Дренирование бывает двух видов:
- Наружное — желчь выводится наружу.
- Наружно-внутреннее: часть желчи выводится наружу, часть — в просвет кишечника.
Если опухоль сдавливает несколько желчных протоков в разных частях печени, устанавливают несколько дренажей. Врачи Европейской онкологической клиники применяют современный метод одномоментного стентирования. При этом наружный дренаж оставляют всего на 1–2 дня, либо можно обойтись вовсе без него.
Каковы прогнозы при метастазах рака в печень?
Пациентов, которые поступают в Европейскую онкологическую клинику с таким диагнозом, в первую очередь волнует вопрос: «можно ли вылечить метастазы в печени при раке 4 стадии?». Эффективность лечения будет зависеть от типа рака, его молекулярно-генетических характеристик, местоположения и степени злокачественности опухоли. Большинство пациентов, после того как у них впервые выявлены метастазы в печени, живут в течение 6–18 месяцев. При раке толстой и прямой кишки, после больших циторедуктивных операций прогноз более благоприятен.
Если метастазы имеются не только в печени, но и в других частях тела, например, метастазы в печени и костях, прогноз ухудшается. Но и при этом возможно хирургическое лечение.
Врачи Европейской клиники имеют большой опыт в комбинированном лечении метастазов в печени. Благодаря этому мы можем существенно продлевать жизнь пациентов. Самые лучшие результаты удается получать, когда в печень метастазирует рак толстой кишки. У нас разработаны четкие критерии, руководствуясь которыми, иногда мы можем воздержаться от хирургического лечения, если очаги обнаружены в обеих долях печени. В таких случаях лечение начинается с курса химиотерапии.
Если метастазы в печени возникли при опухоли легкого, поджелудочной железы, желудка и др., удаление части печени как самостоятельный метод лечения малоэффективно, но оно может хорошо работать в сочетании с химиотерапией.
Если одновременно имеются метастазы в печени и лимфатических узлах, это существенно ухудшает прогноз. Пятилетняя выживаемость снижается примерно в два раза. Но и в этом случае все еще возможно лечение.
Где лечить метастазы печени в России?
Многие российские пациенты, столкнувшись с этим страшным диагнозом — «рак с метастазами» — считают, что это приговор, и ничего сделать уже нельзя, либо эффективную помощь получить можно, но лишь за границей. На самом деле в России, в Москве, доступны все современные технологии и препараты. Современную квалифицированную помощь можно получить в Европейской онкологической клинике.
Мы считаем, что помочь можно всегда, и поэтому беремся за лечение пациентов с онкологическими заболеваниями на любой стадии. Наши доктора имеют большой опыт, проводят сложные инвазивные процедуры и хирургические вмешательства, химиотерапию по международным протоколам. Мы знаем, как помочь.
Список литературы:
[1] The prognostic value of tumor cells blood circulation after liver surgery for cancer lesions — Patiutko IuI, Tupitsyn NN, Sagaĭdak IV, Podluzhnyĭ DV, Pylev AL, Zabezhinskiĭ DA. — Khirurgiia (Mosk). 2011;(6): 22–6.
[2] Surgical and combined treatment of multiple and bilobar metastatic affection of the liver. — Patiutko IuI, Sagaĭdak IV, Pylev AL, Podluzhnyĭ DV. — Khirurgiia (Mosk). 2005;(6): 15–9.
[3] Современные подходы к лечению метастазов колоректального рака в печени — А. Л. Пылёв, И. В. Сагайдак, А. Г. Котельников, Д. В. Подлужный, А. Н. Поляков, Патютко Ю.И.,.. — Вестник хирургической гастроэнтерологии — Номер: 4 Год: 2008 Страницы: 14–28.
[4] Десятилетняя выживаемость больных злокачественными опухолями печени после хирургического лечения — Ю. И. Патютко, А. Л. Пылёв, И. В. Сагайдак, А. Г. Котельников, Д. В. Подлужный, М. Г. Агафонова,.. — Анналы хирургической гепатологии 2010.
[5] Surgical and combined treatment of patients with metastatic liver and lymph nodes invasion by colorectal cancer — Patiutko IuI, Pylev AL, Sagaĭdak IV, Poliakov AN, Chuchuev ES, Abgarian MG, Shishkina NA. — Khirurgiia (Mosk). 2010;(7): 49–54.
Метастазы в печени: симптомы и лечение, что делать, как лечить рак, отзывы
В современном мире раковые заболевания поражают все больше и больше людей. Вторичный рак печени – это распространенная патология среди онкологических больных. Он отличается сложностью распознавания из-за скудной клинической симптоматики. В этой статье мы поговорим о том, почему появляются метастазы в печени и насколько это опасно, можно ли вылечиться.
Что это такое?
Печень (гепар) выполняет огромное количество функций в нашем организме. Одной из главных ее задач является очищение. Каждую минуту через гепар проходит больше полутора литров крови. Она поступает в орган не только из артерий, но и из вен. В синусоидах печени ток крови замедляется. Это способствует тому, что злокачественные клетки оседают именно в этом органе.
Печень – это уязвимый для метастазирования орган. Наличие в органе вторичного очага является неблагоприятным признаком рака и свидетельствует о прогрессировании опухоли, а также распространении ее по организму. Метастазы в печени – это злокачественные вторичные опухоли, которые вышли за границы пораженного органа.
Они выделяют токсины, которые вмешиваются в работу внутренних систем, разрушают ткани и отравляют организм. Вторичные опухоли могут поражать как один, так и сразу несколько участков органа. Метастазы в печени – это нередкий феномен. Согласно статистике, около трети пациентов со злокачественными новообразованиями имеют вторичные очаги в этом органе.
Важно! Все опухолевые клетки изначально являются нормальными клетками нашего организма.
Как и другие опухоли, метастазы в печени длительное время остаются бессимптомными. По мере разрастания патологических очагов появляются боли в правом подреберье, ощущение тяжести, нарушение пищеварения, желтуха. При метастатическом поражении нарастают симптомы печеночной недостаточности. Сложно дать прогноз длительности жизни пациентов с метастазами.
Если они спровоцировали четвертую стадию рака, то развивается бесконтрольный и необратимый процесс. Метастазы в печени быстро развиваются, и за короткий срок могут сильно нарушить слаженную работу фильтрующего органа. Наличие вторичных опухолей – это еще не приговор и не повод опускать руки. Решившись на терапию, можно получить шанс на излечение и значительно продлить жизнь. Бороться нужно до последнего!
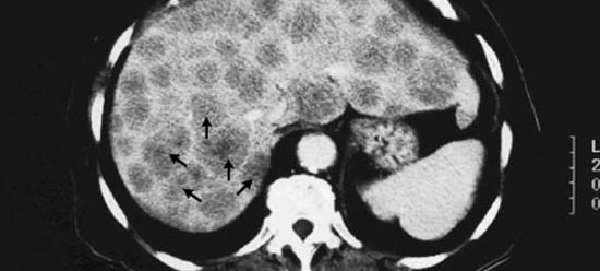
Метастазирование в печень – это показатель неэффективности проводимой терапии рака
Скорость роста атипичных клеток зависит от кровоснабжения печени и иммунного статуса. Из-за появления метастатических очагов печень теряет свои функциональные свойства. В итоге орган может просто отказать.
Причины
Каждый день в человеческом организме происходят генетические сбои, которые потенциально могли бы вызвать раковое перерождение здоровой клетки. Если иммунитету удается вовремя определить и устранить этот дефект, патологическая трансформация будет ликвидирована.
Опухоль начинает беспрепятственно делиться из-за ослабления защитных сил. Это может происходить как на фоне внутренних (хронических заболеваний), так и внешних (радиация) причин. Атипичные клетки из «материнской» опухоли отрываются и мигрируют с током крови и лимфы. Они могут распространяться из различных органов:
- легких,
- желудка,
- кишечника,
- пищевода,
- молочных желез (РМЖ),
- поджелудочной железы.
Реже первичный очаг обнаруживается в простате, матке, яичниках, почках. Рак головного мозга практически не метастазирует в печень. После проникновения в печень аномальные клетки прикрепляются к органу и начинают активно расти. До определенного этапа иммунная система сдерживает распространение раковых опухолей.
Сначала метастазы медленно развиваются или вовсе неактивны, однако затем происходит их бурный рост. Ученые до сих пор не могут понять патогенез (механизм развития) этого явления. В зависимости от этиологических факторов, вторичный печеночный очаг классифицируют следующим образом:
- отдаленный. Первичное новообразование находится далеко от вторичной опухоли;
- гематогенный. Атипичные клетки были занесены в печень с током крови;
- имплантационный. Перерожденные клетки случайно перенеслись на другие ткани;
- ортоградный. Распространение опухоли лимфогенным путем в сторону естественного тока крови;
- ретроградный – перенос в обратную сторону кровотока.
Атака печени раковыми клетками происходит поэтапно. Сначала они отделяются от материнской опухоли и выходят за пределы органа. Далее происходит инфильтрация пораженного участка. Затем атипичные клетки проникают в кровь и лимфу. В конце концов они прикрепляются к сосудистой стенке и проникают в печень, где и дают начало новой опухолевой инвазии.
Симптомы
Одной из особенностей печени является ее способность к регенерации, то есть самовосстановлению. Поэтому чаще всего патологии органа обнаруживаются в довольно запущенных состояниях, так как длительное время они никак себя не проявляют. Ранние симптомы метастазов в печени неспецифичны. Это значит, что их возникновение не наводит на мысль о раке. Если размер узлов не превышает двух сантиметров, пациентов могут вообще не беспокоить симптомы.
По мере роста злокачественной опухоли появляются такие признаки метастазов в печени:
- боли в правом боку;
- тошнота, рвота;
- вздутие живота после еды;
- изжога;
- потеря веса, вплоть до анорексии;
- желтушность кожи и слизистых оболочек;
- ухудшение аппетита;
- слабость, снижение работоспособности;
- горечь во рту;
- повышение температуры тела;
- бледность кожи;
- зуд;
- лицо становится серым с большим количеством сосудистых звездочек;
- боль при дыхании;
- учащенное сердцебиение;
- расстройства кишечника;
- асцит – скопление жидкости в брюшной полости.

Определить рак печени на ранних стадиях довольно сложно. Его симптомы схожи со многими желудочно-кишечными заболеваниями
Параллельно с увеличением узлов нарастает интенсивность распирающих и тупых болей в области печени. Важно заметить, что все вышеперечисленные симптомы появляются вторично, то есть в результате разрастания первичного очага. Так, при раке кишечника могут быть следующие симптомы:
- появление гноя, крови и слизи в фекалиях;
- боль в животе;
- интоксикация;
- запор, сменяющий диарею.
При меланоме формируются черные очаги на коже, а также увеличиваются и уплотняются регионарные лимфатические узлы. Если же первичным очагом представлен рак молочной железы, в груди появляется бугристый, плотный, болезненный и практически неподвижный нарост.
Внимание! Прогнозы при метастазировании в печень зависят от тяжести поражения органа, стадии рака и общего состояния больного. Однозначно можно сказать, что диагностирование вторичного очага не является приговором.
Рак печени характеризуется появлением и других признаков:
- устойчивые отеки;
- усиление венозного рисунка;
- потемнение кожи, особенно на ладонях;
- диспепсические расстройства;
- спонтанные носовые кровотечения;
- увеличение молочных желез у мужчин.
Вторичный рак печени опасен тем, что он повреждает гепатоциты – клетки, выполняющие множество жизненно важных функций. Сдавливание крупных желчных протоков приводит к развитию механической желтухи, отеков, кровотечений. Атипичные клетки не только нарушают нормальную работу органа, но и вызывают отравление всего организма. Распространение раковых клеток бывает единичным.
В этом случае пациентов беспокоят боли в правом подреберье. Наблюдается увеличение печени в размерах. При множественном метастазировании наблюдаются более выраженные проявления и осложнения. Если было установлено, что опухоль в печени одиночная, это вовсе не означает, что она маленького размера. При быстром развитии она хорошо прощупывается и отличается от нормальной печеночной паренхимы.
Диагностика
Пациентам, прошедшим лечение раковой опухоли, следует регулярно делать обследование для своевременного обнаружения патологического воздействия в органе. С целью уточнения локализации новообразования проводится обследование иммунохимических онкомаркеров. С помощью ультразвуковой диагностики можно уточнить размер метастазов, а также их связь с крупными сосудами и протоками.
УЗИ – это простой и доступный диагностический метод, который часто проводят для скрининга. Однако он не всегда помогает обнаружить метастазы и получить о них полную информацию. Для получения дополнительной информации о патологическом процессе и принятия решения о целесообразности проведения операции, назначается МРТ и КТ.
В том случае если врачи сомневаются в отношении природы патологического очага, потребуется проведение пункционной биопсии. Во время процедуры проводится забор биологического материала для гистологического исследования. Ангиография дает информацию о происхождении и локализации вторичных опухолей. Комплексная диагностика также включает в себя осмотр пациента, пальпацию передней брюшной стенки, общий и биохимический анализ крови (АЛТ, АСТ).
Лечение
Что делать, если была выявлена опухоль? Лечение метастазов в печени отличается от терапии первичных раковых опухолей. Оно подбирается с учётом материнского новообразования и количества мигрировавших раковых клеток.
 Как называется врач, который лечит печень?
Как называется врач, который лечит печень?
Современные методы борьбы с патологией включают следующее:
- лучевую терапию;
- химиотерапию;
- хирургическую операцию;
- радиочастотную абляцию;
- химиоэмболию;
- таргетную терапию;
- трансплантацию;
- радиоэмболизацию.
Новые методики позволяют облучить непосредственно злокачественную опухоль, при этом здоровые ткани не повреждаются. В основу лучевой терапии ложиться использование радиоактивных препаратов. Они помогают замедлить рост новообразования и даже уменьшить его в размере.
Химиотерапия помогает при метастазах в печени, однако она имеет большое количество побочных эффектов
Что касается проведения химиотерапии, то в этом случае лекарственные средства вводятся в орган через вену. Процедура позволяет замедлить рост опухоли и даже избавиться от мелких новообразований. Однако химиотерапия связана с появлением побочных эффектов, которые доставляют огромный дискомфорт пациентам.
Из наиболее распространённых нежелательных реакций можно выделить тошноту, рвоту, выпадение волос, головокружение. Вот почему к химиотерапии в настоящее время прибегают крайне редко. Удаление опухоли хирургическим путем в настоящее время назначается довольно редко.
Обычно операция назначается в целях продления жизни больного и облегчения его страданий. Этот радикальный метод применяется при единичных метастазах. Он подразумевает долевую или сегментарную резекцию печени. Пациентам с первичными опухолями легких и кожи операция по частичному удалению органа противопоказана.
При радиочастотной абляции на одиночные метастазы воздействуют радиочастоты. Их источник подводится к опухоли через кожу и печеночную ткань путем прокола. Данная методика отличается высокой точностью и отсутствием травматичности. Он позволяет прицельно воздействовать на само новообразование, при этом не повреждая окружающие ткани. К радиочастотной абляции прибегают и в случаях рецидива, когда в печени появляются новые вторичные очаги.
Химиоэмболизация опухоли блокирование кровеносных сосудов, которые питают опухоль, химиопрепаратами. В итоге к новообразованию перестает поступать кровь, поэтому она погибает и разрушается. К химиоэмболизации обычно прибегают при наличии противопоказаний к проведению оперативного вмешательства и радиочастотной абляции.
Таргетная терапия – это еще один современный метод, с помощью которого можно вылечить метастазы в печени. Специалисты используют препарат Сорафениб, который препятствует росту и делению раковых клеток. Радиоэмболизация подразумевает введение радиоактивных веществ через вену.
Процедуру назначают при неоперабельном раке и наличии противопоказаний к проведению хирургической операции. Согласно данным статистики, в 70–95% случаев эмболизация при раке печени приводит к облегчению клинических симптомов. Она относится к паллиативным методам лечения, то есть направлена на улучшение состояние, а не на избавление от самой проблемы.
Это технически сложная методика, которая сочетает в себе и лучевую терапию, и эмболизацию кровеносных сосудов. Процедура занимает около часа. Пересадка печени при правильном подборе донора значительно увеличивает продолжительность жизни пациентов. Трансплантация проводится крайне редко. Это объясняется сложностями самой операции, трудностями транспортировки и необходимостью специального дорогостоящего оборудования.
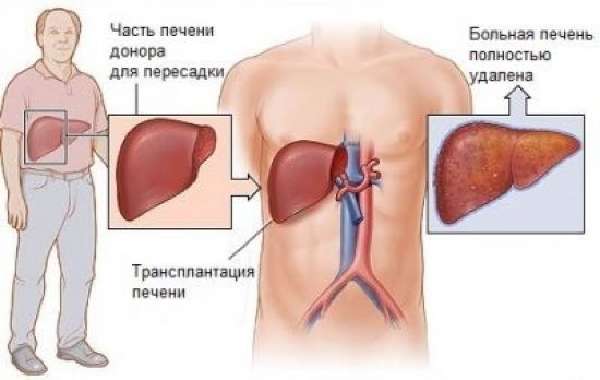
На фото схематически показана суть проведения трансплантации печени
Лечение метастазов в печени включает в себя также соблюдение диетического питания. С целью уменьшения нагрузки на печень выбирать следует продукты, богатые клетчаткой, ненасыщенными жирами, а также содержащие легкоусваиваемый белок. Рацион должен быть сбалансированным и витаминизированным. Следует ограничить потребление соли до 5 г в день. Больным показано дробное питание небольшими порциями.
Народные средства
Пациенты, которые предпочитают народные средства традиционным медикаментозным средствам, теряют драгоценное время. Одной из причин появления метастазов является позднее обращение к специалисту. Рецепты народников рекомендуют применять в качестве вспомогательной помощи.
Не нужно ожидать от лекарственных трав чудодейственного исцеления. Народная медицина поможет поддержать работу печени и снизить выраженность клинических проявлений, на большее можно не рассчитывать.
Важно! Опасность народного лечения заключается в рисках возникновения аллергических реакций на растения.
Большой популярностью пользуется средство на основе болиголова. Для приготовления настойки понадобится 25 г семян и 500 мл водки. В течение десяти дней средство должно настаиваться в темном месте. Периодически его следует перемешивать. Процеженную настойку принимают за полчаса до еды.
В первый день одну каплю средства разводят в ста миллилитрах воды. Каждый день дозировку увеличивают по одной капле, доводя до 40. Если во время лечения появилась слабость, тошнота, сыпь, кишечные расстройства, дозировку следует уменьшить.
Чистотел – это еще одно известное средство, которое часто применяют раковые больные. В его состав входят ядовитые компоненты, поэтому принимать растение следует предельно осторожно. Превышение дозировки может серьезно навредить. Лекарства на основе чистотела обладают анальгезирующими свойствами.
Препараты готовят на воде или спирте. Есть немало сведений в отношении того, что средства на основе чистотела разрушают структуру пораженных гепатоцитов. Начинать лечение следует с небольших доз. Максимальная продолжительность приема не должна превышать трех месяцев.
Отзывы
Виктор, 55 лет:
Диагноз «рак» звучит как приговор. Ты никогда не можешь быть к этому готов. Первичный очаг у меня обнаружился в поджелудочной железе с метастазами в печень. Мне был назначен курс химиотерапии. Без побочных эффектов не обошлось. Я очень страдал от тошноты и рвоты, у меня выпали волосы, голова постоянно кружилась. После трех курсов химиотерапии анализы улучшились, что не может не радовать. Сейчас продолжаю борьбу с болезнью.
Евгения, 50 лет:
Метастазы в печени излечимы, в этом я убедилась на своем примере. Обнаружили у меня онкологию чисто случайно во время обследования. На тот период у меня не было никаких симптомов, поэтому я сильно удивилась. Мне была назначена радиочастотная абляция. Врач настоятельно рекомендовал соблюдать диету. Также я использовала народные рецепты. В комплексе все это помогло мне выздороветь.
Татьяна, 28 лет:
У моего отца выявили рак легких, а затем обнаружили метастазы в печени. Долгое время его не беспокоили никакие симптомы. В последнее время появились боли в правом боку, он это списывал на неправильное питание. Я решила отвезти на УЗИ, где нас ошарашили диагнозом «рак». Опухоль была уже неоперабельна. Для улучшения самочувствия отцу назначили радиоэмболизацию. В вену вводили радиоактивные вещества. Процедура дала результаты, перед смертью он не мучился.
Ключевые мысли
Обнаружение метастазов в печени – это еще не приговор. Бороться нужно до последнего. Затруднения в диагностике раковых опухолей связаны с тем, что на ранних стадиях симптомы схожи с проявлениями безобидных патологий желудочно-кишечного тракта.
Современные методики лечения включают в себя проведение лучевой терапии, химиоэмболизацию, радиочастотную абляцию, трансплантацию. Врач подбирает метод лечения в зависимости от стадии рака, степени поражения органа, общего состояния пациента.
 Загрузка…
Загрузка…
Прогноз срока жизни при метастазах в печени
Точно сказать, сколько живут с метастазами в печени, проблематично – прогноз находится в зависимости от их количества и вида рака, а также от эффективности выбранного метода борьбы с ними. В среднем специалисты говорят о сроках, колеблющихся от 4 месяцев до нескольких лет, что обусловлено и регенерационными свойствами печени. При этом важно правильно лечить заболевание.
Содержание статьи:
Что такое метастазы
Метастазы – злокачественные образования, развивающиеся от раковой материнской опухоли. Онкологические клетки распространяются, как правило, двумя путями – через кровь и лимфу. Они могут исходить не только из внутренних органов, но и от злокачественных участков кожи (меланомы). В печень патогенные клетки попадают в основном через кровь, поскольку главной питающей артерией органа является воротная вена.

Клиническая картина – виды, симптомы
Прогноз при метастазах в печени не бывает однозначным, ввиду того, что они зачастую обнаруживаются не сразу. Вторичные узлы разделяются по методу проникновения в орган на виды:
- Отдаленный. Больные клетки развиваются вдали от эпицентра болезни (желудок, брюшная полость и так далее).
- Имплантационный. Возникает при непроизвольном попадании злокачественных клеток в здоровый орган.
- Гематогенный. Развивается при перемещении злокачественных клеток по кровеносным сосудам.
- Лимфогенный. В здоровые участки ткани патологические клетки попадают вместе с лимфой.
- Ретроградный. Возникает при перемещении раковых образований в обратном естественному направлению движению лимфы или крови.
О том, сколько живут с раком и метастазами в печени, сложно говорить еще и потому, что симптоматика заболевания может проявляться достаточно поздно. При обширных поражениях органа можно обнаружить такие признаки, как:
- Потеря массы тела.
- Увеличение печени.
- Болезненность органа.
- Чувство тяжести, локализованное в правом подреберье.
- Лихорадка.
- Снижение аппетита.
- Слабость и недомогание.
- Изменение оттенка кожи на «землистый».
- Привкус горечи во рту.
-
 Сбой в работе кишечника.
Сбой в работе кишечника. - Изменение цвета мочи на более темный.
- Зуд и высыпания на коже.
- Желтуха.
- Светлые каловые массы.
- Болезненные ощущения в грудной клетке и области поджелудочной при глубоком вздохе.
Самыми грозными признаками считается ежедневная частая рвота и черный кал. Такие симптомы являются показанием к немедленному обращению за медицинской помощью.
Важно знать! При первой стадии заболевания симптомы зачастую не дают о себе знать, либо проявляются слабо.
Диагностические методы
Прогноз срока жизни при метастазах в печени обусловлен и своевременностью обнаружения проблемы. Сегодня существует несколько диагностических методов, позволяющих выявить образование вторичных очагов.
Лабораторные методы:
- Исследование онкомаркеров. Проводится для уточнения магнилизации новообразования.
- Биопсия. Небольшую частичку опухолевой ткани извлекают с помощью тонкой иглы, чтобы на микроскопическом уровне определить строение злокачественного участка.
- Анализ крови для определения уровня печеночных ферментов. Позволяет установить степень нарушения работы печени.
Инструментальные методы:
- Ангиография и мультиспиральная КТ, МРТ, ПЭТ. Позволяют определить наличие метастаз, их количество, размеры, расположение, распад или нагноение клеток, характер их роста, распространение в соседние органы и ткани.
-
 УЗИ. Метод, с помощью которого можно увидеть не только размеры патогенных образований, но и выявить их связь с крупными сосудами и протоками печени.
УЗИ. Метод, с помощью которого можно увидеть не только размеры патогенных образований, но и выявить их связь с крупными сосудами и протоками печени.
Печень подлежит обследованию при любом виде онкологии. Установить точный диагноз и назначить соответствующее лечение возможно только при проведении комплексного анализа.
Методы лечения
Продолжительность жизни при метастазах в печени в большинстве своем обусловлено и тактикой терапии. Определяет ее специалист, в зависимости от клинической картины и от таких факторов, как размер новообразований и их количество.
Оперативное вмешательство
При раннем обнаружении метастаз и их небольшом количестве в органе рекомендовано оперативное вмешательство, выживаемость после которого имеет высокий процент. Суть операции заключается в частичной резекции печени. В дальнейшем происходит регенерация клеток, орган в незначительной степени восстанавливается.
Возможно выполнение операции несколькими способами:
- Удаление доли – лобэктомия.
- Устранение участка – сегментомия.
- Атипичная резекция – клиновидная, поперечная, плоскостная, краевая.
Радиоэмболизация
Радиоэмболизация в терапии данного заболевания позволяет устранить злокачественные клетки почти у 70% больных. Суть методики заключается в следующем:
- Тонкую иглу вводят через бедренные сосуды непосредственно в печеночную артерию, которая ведет к узлу метастаза.
- Через нее вводят закрепленный на микросфере радиоизотоп (зачастую иттрий-90).
- Микросфера закупоривает артерию, что ведет к прекращению поступления к узлу крови.
- Радиоизотоп разрушает клетки онкологии.
Важно знать! В сочетании с химиотерапией радиоэмболизация позволяет в несколько раз улучшить качество жизни пациента и продлить ее. Даже при множественных метастазах в печени прогноз после процедуры оптимистичный.
Химиотерапия
Химиотерапия в классическом ее варианте при метастазах в печени считается не слишком эффективной. На сегодняшний день в медицине широко применяют химиоэмболизацию, которая является более действенной, но менее токсичной, нежели «химия».
Химиоэмболизация разделяется на два вида:
- Химиоэмболизация микросферами. В просвет артерии вводят микросферу, выполненную из специального материала с высоким абсорбирующим эффектом. Это обеспечивает продолжительный контакт опухоли с препаратами-цитостатиками.
- Масляная химиоэмболизация. Эмболизатор, в котором содержится цитостатический химиопрепарат, вводят в вену, через нее он попадает в опухоль и перекрывает ее сосуды. На протяжении непродолжительного времени из эмболы выделяется противораковое лекарство.
Применение данной методики, как и химиотерапии, возможно на разных стадиях заболевания. Наиболее эффективно оно проявляет себя в комплексном лечении онкологии, ввиду чего можно прогнозировать его благоприятный исход.
Лучевая терапия
Суть лучевой терапии заключается в воздействии на пораженную область ионизирующего излучения для устранения раковых клеток. Имеется несколько видов данного лечения:
-
 наружная;
наружная; - стереотаксическая;
- трехмерная конформная.
Выживание после ее проведения имеет достаточно высокий процент. Но проводить лучевую терапию в повышенных дозах не рекомендовано, так как излучение повреждает и здоровые клетки печени.
Таргетная терапия
При лечении метастазирования печени хорошие результаты показала и таргетная терапия. Она проводится с помощью одного из современных препаратов «Сорафениб» («Нексавар»), который способен остановить прогрессирующую болезнь. Это происходит за счет того, что лекарство блокирует попадание кислорода и питательных веществ в злокачественные клетки.
Внимание! Таргетные препараты также могут стимулировать иммунитет и вводить в раковые клетки токсины, тем самым тормозя их развитие. В данном случае здоровые области не затрагиваются.
Паллиативная терапия
Паллиативная терапия является методом, который назначают в случаях, когда иные способы не приносят должного эффекта. Применяют ее не только при единичном или множественном метастазировании в печень, но и при лечении РМЖ, рака ЖКТ и других видов онкологии.
Данный вид терапии может включать в себя различные виды:
- радиотерапия;
- химиотерапия;
- обезболивание.
Общий прогноз на выздоровление при метастазах в печени
Вероятность выздоровления при метастазах в печени зависит от множества факторов, от влияния которых напрямую зависит дальнейший прогноз на выздоровление.  Очень редко врачи могут точно предположить вероятную продолжительность жизни, поскольку не всегда понятно, какой ответ даст организм на то или иное лечение.
Очень редко врачи могут точно предположить вероятную продолжительность жизни, поскольку не всегда понятно, какой ответ даст организм на то или иное лечение.
Основные факторы, влияющие на эффективность лечения:
- Стадия заболевания. Чем раньше была обнаружена проблема, тем больше шансов на то, что лечение будет эффективным. Самая опасная – четвертая степень, при которой орган поражается многочисленными метастазами, полностью подавляющими его нормальную работу.
- Темп прогрессирования. Патогенные клетки разносятся по всему организму с разной скоростью. Чем раньше будет поставлен диагноз, тем больше шансов на купирование метастаз и их развитие.
- Размер злокачественной опухоли, количество патологических очагов, гистологическая структура.
- Локализация относительно жизненно важных структур.
- Возраст. Терапия онкологии у пожилых может иметь ряд жизненно угрожающих противопоказаний. Поэтому для данной категории людей подходят далеко не все методы лечения, что приводит к высокому проценту смертности.
- Наличие сопутствующих заболеваний. Если у больного помимо онкологии имеются еще некоторые болезни (проблемы с сердечно-сосудистой системой, сахарный диабет и прочее), то лечение будет более длительным и сложным.
Как повысить продолжительность жизни при метастазах
Улучшить качество жизни больного с метастазами в печени можно. Для этого нужно соблюдать ряд мер, которые также направлены и на продление ее срока:
- соблюдение всех рекомендаций врача;
- регулярные обследования;
- исключение из жизни вредных привычек;
- соблюдение диеты;
- внимательное отношение к своему здоровью в целом.
Если пациент своевременно обратится за врачебной помощью, то прогнозы могут быть весьма оптимистичными. Частичное удаление органа и очага заболевания вкупе с другими методами лечения дают шанс на возможность прожить еще несколько лет.
можно ли обойтись без операции?
Метастазы в печень, вызванные опухолями других локализаций (метастатический рак печени, метастатическое поражение печени) встречаются гораздо чаще, чем злокачественные опухоли, развивающиеся из клеток печени (первичный рак печени). О том, как выглядит современная диагностика и лечение метастазов в печень — сегодняшний материал.
Откуда возникают метастазы в печень?
Метастазы в печень, как правило, являются гематогенными — распространяются с кровотоком от опухолей, располагающихся вблизи крупных кровеносных сосудов. После разрастания злокачественного новообразования в просвет вены или артерии, частицы опухоли начинают циркуляцию в организме. Печень — природный “фильтр”, в котором кровь очищается, замедляя скорость своего течения. Именно поэтому циркулирующие микрометастазы с высокой долей вероятности оседают в тканях органа, вызывая рост вторичной опухоли — метастаза в печени.
Какие опухоли чаще всего дают метастазы в печень?
Учитывая активную роль печени в фильтрации крови, она — распространенный “орган-мишень” для метастазов рака ряда локализаций
- рак поджелудочной железы;
- рак кишечника;
- рак желудка;
- рак молочной железы;
- рак пищевода.
Почти все из опухолей этих локализаций могут протекать скрытно даже на момент начала метастазирования, поэтому нередки случаи, когда метастазы в печень демонстрируют более выраженную симптоматику, чем первичная опухоль, и становятся поводом обращения к врачу. При обнаружении опухолевого процесса в печени, еще до проведения морфологического исследования с целью выявления типа опухолевых клеток, из которых состоит новообразование, врач, владеющий статистикой метастазирования различных видов рака в печень, получает ценный сигнал для поиска первичной опухоли — источника метастазов.
Симптомы метастазов в печень
Симптоматика при метастатическом раке печени, в целом, аналогична симптомам других заболеваний печени — вздутие живота, тошнота, тяжесть в правом подреберье, нарушения стула, интоксикация, слабость. Более точные симптомы зависят от размера и расположения новообразования в каждом из конкретных клинических случаев.
При лечении первичных опухолей, часто метастазирующих в печень важна не столько выраженность симптомов, сколько само их наличие. Настороженность врача и пациента к возможному возникновению симптомов поражения печени позволяет своевременно выявить и начать лечение метастазов рака в печень.
Метастазы в печень — диагностика
Повышает шансы пациентов с метастазами в печень высокая доступность такого метода регулярного контроля, как ультразвуковое исследование. УЗИ печени неинвазивно, стоит недорого, проводится быстро, обеспеченность данным видом исследований высока даже в небольших городах уровня районного центра.
Однако, при появлении симптоматики, указывающей на нарушения работы печени, которые могут быть вызваны метастазами первичной опухоли (например, рака желудка), требуется привлечение более информативных диагностических методов. Чаще всего диагностика и последующее лечение метастазов в печень требует данных компьютерной томографии (КТ), реже — магнитно-резонансной томографии (МРТ) или позитронно-эмиссионной томографии (ПЭТ).
После подтверждения наличия новообразования в органе мировые стандарты онкологии предусматривают проведение биопсии метастаза в печень (забора фрагмента новообразования) для последующего морфологического изучения, в т.ч. иммуногистохимия. Тонкоигольная биопсия печени, проводимая в зоне расположения метастаза под контролем УЗИ или КТ, позволяет дать ответ о типе и особенностях клеток, из которых состоит метастаз. Это помогает выявить источник метастазов в печень — первичную опухоль, а также указывает на дополнительную возможность для комплексной терапии — иммуногистохимия может показать чувствительность опухоли и ее метастаза в печень к таргетному лечению или иммунотерапии.
Радикальное лечение метастазов в печень
Традиционно, метастазы в печень, независимо от типа первичного рака, удаляются хирургическим путем вместе с поврежденными опухолью структурами и тканями органа. Недостаток хирургии в качестве единственного метода радикального лечения метастазов в печень — значительная травматичность операции и ограничения по возможности ее проведения — ослабленный лечением первичной опухоли (хирургия, лучевая терапия, химиотерапия) организм зачастую не в состоянии будет выдержать еще одно вмешательство под общим наркозом.
Развитие технологий в медицине открыло пациентам с метастатическим раком печени иные виды щадящего радикального лечения:
- химиоэмболизация, заключающаяся в краткосрочном подведении к печени вместо крови препаратов химиотерапии в более высокой концентрации, чем при системном введении;
- радиочастотная абляция, представляющая собой воздействие на опухоль радиоволнами высокой частоты, что приводит к разрушению биологических тканей метастаза в печень вследствие их нагрева до значительных температур;
- таргетная терапия, воздействующая на клеточном уровне лишь на первичную опухоль и ее метастазы при условии ряда особенностей строения раковых клеток;
- иммунотерапия, основанная на природном механизме разрушения злокачественных клеток.
Радиохирургическое лечение метастазов в печень (КиберНож, TrueBeam STx и др.)
Наиболее совершенным методом радикального лечения метастазов в печень, является радиохирургия на КиберНоже. Также, радиохирургию позволяют реализовать некоторые модели современных линейных ускорителей, например, специализированный линейный ускоритель TrueBeam STx, который работает в отделении радиохирургии Онкологической клиники МИБС.
Высокая точность лечения метастазов в печень на линейном ускорителе TrueBeam STx: на плане лечения представлен предварительный расчет, который показывает, что высокую дозу получит только зона внутри синего контура, отвечающая по своей пространственной форме контуру метастаза в печени. Задача врачей задать контуры здоровых и пораженных тканей, а количество, формы и траекторию, по которым суперсовременный медицинский роботизированный комплекс подаст поля облучения, рассчитает мощнейший программный комплекс. Но контроль все равно за человеком – каждый план лечения утверждают медицинский физик и лучевой терапевт
Подводимая при радиохирургии на этих установках высокая (абляционная) доза ионизирующего излучения приводит к остановке биологических процессов в заданном объеме метастаза в печень. При этом повреждение здоровых тканей сведено к минимуму — разрезов не требуется, а требуемая доза губительного для тканей метастаза в печень излучения складывается из одиночных доз каждого из множественных тонких пучков. При этом каждый пучок излучения подается точно по заданной траектории, проходя через различные участки организма, не передавая дозы, способной нанести необратимое воздействие на здоровые ткани.
Преимущества метода радиохирургии:
- радикальность воздействия на заданный объем опухолевого поражения;
- безопасность для окружающих тканей;
- минимальная инвазивность, позволяющая проводить лечение амбулаторно;
- невысокая общая стоимость лечения, ввиду короткого срока пребывания в онкологической клинике и отсутствие потребности в реабилитации.
Точность радиохирургии на КиберНоже обеспечивается предварительным формированием цифровой пространственной модели формы и объема расположения метастаза в печени пациента. Визуальная модель, которая будет использована для задания параметров плана радиохирургии (зона высокой дозы, ее значение, зоны нулевой дозы для защиты критических органов и структур), строится на основе слияния нескольких источников диагностической информации, чаще всего, массивов снимков КТ и МРТ.
Метастатический рак печени — причины, симптомы, диагностика и лечение, прогноз
Метастатический рак печени – вторичная опухоль печени, возникшая в результате распространения злокачественных клеток из первичного очага, расположенного в другом органе. Сопровождается неспецифическими симптомами онкологического заболевания (гипертермией, потерей веса и аппетита), увеличением печени и ее болезненностью при пальпации. На поздних стадиях печень становится бугристой, возникают асцит, прогрессирующая желтуха и печеночная энцефалопатия. Диагноз выставляют с учетом анамнеза, клинической симптоматики, результатов лабораторных и инструментальных исследований. Лечение – химиотерапия, эмболизация, радиочастотная абляция, хирургическое вмешательство.
Общие сведения
Метастатический рак печени – самое распространенное метастатическое поражение при онкологических заболеваниях. Наблюдается примерно у 1/3 больных злокачественными опухолями различной локализации. Выявляется у каждого второго пациента, страдающего раком желудка, раком толстого кишечника, раком легких и раком молочной железы. На начальных стадиях протекает бессимптомно, что затрудняет своевременную диагностику, особенно при одновременном скрытом течении первичной опухоли.
До недавнего времени метастатический рак печени считался неоперабельным вне зависимости от вида, размера, локализации и количества вторичных очагов, однако в наши дни эта точка зрения постепенно подвергается пересмотру. Лечение осуществляют специалисты в области онкологии, гастроэнтерологии и абдоминальной хирургии.
Метастатический рак печени
Причины метастазов в печень
Метастатический рак печени особенно часто возникает при висцеральных новообразованиях, поскольку кровь от органов брюшной полости поступает в печень через систему воротной вены. Является распространенным осложнением рака желудка, рака поджелудочной железы, рака желчного пузыря и рака прямой кишки. Вместе с тем, злокачественные клетки могут попадать в печень и из органов, не дренируемых системой воротной вены. Метастатический рак печени часто возникает при раке легких, меланоме и раке молочной железы, нередко диагностируются при раке яичников, раке простаты и опухолях почки.
К числу злокачественных новообразований, редко метастазирующих в печень, относятся рак мочевого пузыря, рак глотки, рак полости рта и рак кожи. В ряде случаев метастатический рак печени бывает трудно отличить от первичной опухоли органа. Заподозрить вторичное поражение в подобных случаях можно по раннему появлению асцита, обусловленного обсеменением брюшной полости злокачественными клетками. Больные с вторичным новообразованием в печени нередко погибают от ракового перитонита, не успевая дожить до значительного увеличения органа.
Патанатомия
При метастатическом раке печени преобладают узловые формы. Очаги могут быть как одиночными, так и множественными, локализуются в центре печени или на ее поверхности. Диаметр метастазов колеблется от нескольких миллиметров до нескольких сантиметров. При множественных очагах метастатического рака печени может выявляться так называемая «каштановая» печень – орган, покрытый многочисленными новообразованиями, напоминающими лесные орехи. Иногда вторичные опухоли развиваются преимущественно в центре органа, не выявляются при пальпации и становятся видны только на разрезе.
Гистологическая структура метастатического рака печени обычно соответствует структуре первичного очага. Большинство метастазов представляют собой белесоватые узлы округлой либо неправильной формы. При первичном раке яичников в печени обычно выявляются множественные светлые очаги мягкой консистенции с четкими контурами. При светлоклеточном раке почки консистенция узлов метастатического рака печени практически не отличается от консистенции нормальной ткани органа. Узлы светло-коричневые, контуры четкие. При первичных эндокринных новообразованиях цвет метастазов – от беловатого или желтоватого до темно-коричневого. Консистенция – немного плотнее ткани печени. Как и в других случаях, метастазы имеют четкие контуры.
Реже выявляется несоответствие патологоанатомических характеристик первичной опухоли и метастатического рака печени, обусловленное различиями в степени дифференцировки злокачественных клеток. Иногда гистологическая дифференцировка первичного и метастатического очага представляет собой сложную задачу из-за сходства структуры первичного процесса в печени и опухолей внепеченочной локализации. Подобная проблема может возникать, например, при различении метастазов аденокарциномы пищеварительного тракта и холангиоцеллюлярного рака печени, имеющих похожее строение.
Симптомы метастазов в печень
На ранних стадиях метастатический рак печени протекает бессимптомно. У пациентов могут выявляться общие признаки онкологического заболевания: слабость, повышенная утомляемость, повышение температуры тела, снижение аппетита и потеря веса. При пальпации определяется некоторое увеличение печени. Печень плотная, иногда болезненная. В отдельных случаях при аускультации выявляются шумы. Возможно увеличение селезенки.
Желтуха обычно отсутствует или слабо выражена за исключением метастатического рака печени, расположенного поблизости от желчных путей. Выявляется увеличение уровня лактатдегидрогеназы и щелочной фосфатазы. Нередко возникает ранний асцит, обусловленный одновременным обсеменением брюшины. На поздних стадиях метастатического рака печени наблюдаются выраженное увеличение органа, нарастающая желтуха и печеночная энцефалопатия. Многие больные не успевают дожить до этих симптомов. Причиной гибели становится раковый перитонит, обусловленный множественными метастазами в брюшной полости.
Диагностика
Диагноз устанавливается на основании анамнеза (наличие онкологического заболевания), жалоб, данных объективного осмотра, результатов инструментальных и лабораторных исследований. Пациентов с подозрением на метастатический рак печени направляют на УЗИ и КТ. В большинстве случаев данные методики достаточно результативны, однако при мелких метастазах и изменениях печени, вызванных доброкачественными опухолями и хроническими заболеваниями неопухолевой природы, возможны диагностические затруднения.
Для оценки печеночных функций назначают биохимический анализ крови. В сомнительных случаях метастатический рак печени подтверждают на основании результатов биопсии печени. Для повышения точности диагностики биопсия может выполняться под контролем УЗИ или в процессе лапароскопии.
Кроме того, больного метастатическим раком печени направляют на УЗИ органов брюшной полости, рентгенографию грудной клетки, КТ головного мозга и другие исследования для выявления вторичных новообразований в других органах. Если метастазы в печень обнаружены при первичном обращении, а основное онкологическое заболевание протекает бессимптомно, назначают расширенное обследование.
КТ ОБП С+. Множественные гиподенсные/гиповаскулярные вторичные очаги в печени с тонким гиперваскулярным ободком по периферии у пациента с первичной опухолью толстой кишки.
Лечение метастатического рака печени
Хирургические методы
Долгое время метастатический рак печени рассматривался как свидетельство близкого летального исхода. Из-за особенностей строения и васкуляризации органа проведение хирургических вмешательств было сопряжено с высоким операционным риском, поэтому резекции печени в первой половине ХХ века проводились очень редко. Совершенствование хирургических методик и появление новых способов лечения позволило изменить подход к терапии метастатического рака печени, хотя проблема увеличения продолжительности жизни при данной патологии по-прежнему остается крайне актуальной.
Наилучшие отдаленные результаты оперативного лечения наблюдаются у пациентов с раком толстой кишки. К сожалению, всего около 10% метастатического рака печени являются операбельными на момент постановки диагноза. В остальных случаях операции не показаны из-за слишком крупной опухоли, близости новообразования к крупным сосудам, большого количества очагов в печени, наличия метастазов внепеченочной локализации или тяжелого состояния больного.
В последние годы список показаний к хирургическому вмешательству при метастатическом раке печени расширился. Иногда онкологи рекомендуют резекцию при наличии метастазов не только в печени, но и в легких. Операцию выполняют в два этапа: вначале убирают очаг в печени, затем – в легком. Статистические данные об изменении продолжительности жизни при подобных вмешательствах пока отсутствуют.
Противоопухолевая терапия
При неоперабельном метастатическом раке печени показана химиотерапия. Пациентам назначают 5-фторурацил (иногда – в сочетании с кальция фолинатом), оксалиплатин. Средняя продолжительность жизни после медикаментозного лечения колеблется от 15 до 22 месяцев.
В некоторых случаях химиотерапия позволяет уменьшить рост опухоли и провести хирургическое вмешательство при метастатическом раке печени, который до начала лечения рассматривался, как неоперабельный. Резекция становится возможной примерно у 15% пациентов. Средняя продолжительность жизни – такая же, как при изначально операбельных опухолях. Во всех случаях после удаления метастатического рака печени в отдаленные сроки возможно появление новых вторичных очагов в различных органах. При операбельных печеночных метастазах проводят повторную резекцию. При метастатическом поражении других органов назначают химиотерапию.
Малоинвазивные методы
Наряду с классическими оперативными вмешательствами и химиотерапией, при метастатическом раке печени применяют эмболизацию печеночной артерии и воротной вены, радиоабляцию, криодеструкцию и введение этилового спирта в область новообразования. В результате эмболизации питание опухоли нарушается, в тканях возникают некротические изменения. Одновременное введение химиопрепаратов через катетер позволяет создать очень высокую концентрацию лекарственных веществ в ткани новообразования, что еще больше увеличивает эффективность методики. Химиоэмболизация может применяться в качестве самостоятельного метода лечения метастатического рака печени или использоваться на этапе подготовки больного к резекции органа.
Целью радиочастотной абляции, криодеструкции и введения этилового спирта также является разрушение ткани опухоли. Специалисты отмечают перспективность этих методик, но не сообщают статистические данные об изменении выживаемости после их применения, поэтому оценить отдаленные результаты пока затруднительно.
Прогноз
Резекция одиночного метастаза размером до 5 см позволяет увеличить среднюю пятилетнюю выживаемость больных раком прямой кишки до 30-40%. При множественном поражении прогноз после оперативного лечения метастатического рака печени менее благоприятный, однако, при удалении всех очагов удается достичь средней трехлетней выживаемости 30%. Смертность в послеоперационном периоде составляет 3-6%. При первичных злокачественных опухолях других локализаций за исключением рака прямой кишки (раке легких, раке молочной железы и т. д.) прогноз после резекций печеночных метастазов менее оптимистичный.
Смертность больных с метастатическим раком печени при использовании малоинвазивных методов составляет около 0,8%. В запущенных случаях, когда проведение оперативного лечения, химиотерапии, эмболизации, радиоабляции или криодеструкции невозможно из-за тяжелого состояния пациента, назначают симптоматические средства, позволяющие смягчить проявления заболевания. Продолжительность жизни при метастатическом раке печени в подобных случаях обычно не превышает нескольких недель или месяцев.
Метастазы в печени: симптомы, лечение, прогноз
Диагностируются единичные или множественные метастазы в печени часто. Это связано с тем, что орган снабжен обширной сосудистой сетью, и именно с кровью онкоклетки разносятся по организму, поражая самые уязвимые органы и системы. Важно обнаружить патологию своевременно, тогда удастся остановить рост метастазов и улучшить прогноз на выздоровление. В противном случае благоприятный исход маловероятен, также это существенно сокращает продолжительность жизни больного.

Разновидности
Метастазы печени (MTS) имеют разнообразную классификацию. Учитывая место локализации опухоли, различают такие виды:
- Билобарные. В таком случае метастазирование распространено на обе доли органа.
- Унилобарные. Поражена лишь одна доля.
А также существует характеристика по количественному признаку. Поражение МТС в печени бывает:
- Одиночное. Образуется не более 3 узелков.
- Множественное. На КТ-снимках визуализуются десятки опухолевых новообразований.
Вернуться к оглавлению
Причины появления
 Диагноз установит врач назначив необходимые исследования.
Диагноз установит врач назначив необходимые исследования.
Метастатическое поражение печени прогрессирует вследствие распространения онкологических клеток из других органов кровотоком. При отдаленном характере метастазирования в печеночные структуры можно говорить о том, что онкопроцесс запущен и достиг последней, 4 степени, когда пораженная печень неоперабельна, поэтому хирургическое удаление не может помочь.
Вторичные метастазы проникают в орган кровотоком из первичных злокачественных опухолей, которые чаще всего локализуются в таких структурах, как:
- поджелудочная железа;
- легочные ткани;
- молочные железы;
- органы пищеварения.
Рак желчного пузыря, кишечника, желудка более чем в половине случаев сопровождается распространением метастазов в печень. Поэтому, когда у человека диагностирован онкопроцесс в этих органах, во время каждого диагностического исследования проверяется состояние печени, потому что на 2—3 стадии заболевания отдельные метастазы зачастую проявляются в органе.
Вернуться к оглавлению
Печеночный рак
Это тяжелая и опасная патология, прогноз жизни при которой неблагоприятен, особенно когда удалось определить проблему на запущенных стадиях. Первые симптомы зачастую невыраженные, поэтому очень редко удается диагностировать онкологию в самом начале развития. На 4 стадии патологический процесс распространяется быстро, в печени происходят необратимые процессы, метастазы стремительно распространяются по организму, состояние больного каждый день ухудшается. Пораженная опухолью печень отказывает, излечение от онкологии невозможно.
Вернуться к оглавлению
Рак кишечника
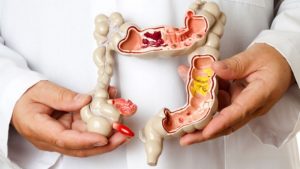 Метостазы в печени могут быть признаком рака желудка.
Метостазы в печени могут быть признаком рака желудка.
На начальном этапе прогрессирования колоректального рака характерные признаки патологии отсутствуют. У человека появляются жалобы на расстройство пищеварения, тяжесть в животе, ухудшение аппетита. Однако по мере прогрессирования патологии симптомы обостряются. Появляются боли в нижней части живота, видны изменения во внешности больного. Рак кишечника зачастую провоцирует метастазы в печени, чем раньше диагностировать и избавиться от опухоли, тем благоприятнее прогнозы на излечение.
Вернуться к оглавлению
Онкология поджелудочной железы
Метастазирование печени из первичного очага, локализованного в тканях поджелудочной, происходит часто. На запущенных этапах растут и определяются метастазы в легких, почечных тканях. Такая распространенность онкоклеток объясняется тесной функционально анатомической взаимосвязью между этими органами. Симптомы метастаз начинают проявляться на 4 стадии рака поджелудочной.
Вернуться к оглавлению
Онкология желудка
Рак желудка с метастазами в печень зачастую диагностируется на самом первом приеме. Такая картина свидетельствует о запущенности болезни, когда основная опухоль в желудке стала способной распространять отдельные патологические клетки по всему организму. В этом случае лечение метастаз в печени будет зависеть от разнообразных параметров. Если шансы на восстановление есть, применяется комплексный подход, куда входит операция по удалению злокачественных очагов, химио- и радиотерапия.
Вернуться к оглавлению
Без первичного очага
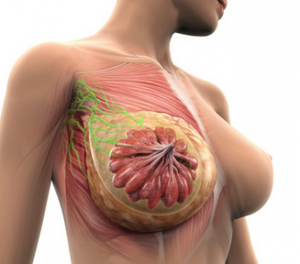 Рак молочной железы провоцирует появление метастазов в печени.
Рак молочной железы провоцирует появление метастазов в печени.
Метастазы в печени с отсутствием основного очага также встречаются часто. Зачастую патологические клетки распространяются по организму из тканей молочных желез либо органов пищеварительного тракта, при этом беспокоящие признаки начинают проявляться на последних этапах прогрессирования онкологии. Если пошли метастазы в печень без первичного очага, обычно назначается хирургическое лечение, перед которым проводится химиотерапия.
Вернуться к оглавлению
Симптомы онкологии
Одиночные метастазы печени могут продолжительное время расти и распространяться по органу, при этом человек не будет подозревать о наличии патологии. По истечении определенного срока станет видно, что организм функционирует не так, как всегда, больного начнут беспокоить такие симптомы:
- тупые, а затем острые боли в правом подреберье, усиливающиеся после приема пищи;
- тошнота, нередко сопровождающаяся рвотой;
- изменение оттенка кожи на землистый или грязно-желтый;
- слабость, ухудшение работоспособности;
- асцит.
По мере прогрессирования онкопроцесса повышается температура тела, ухудшается аппетит, больной стремительно теряет вес. Боли беспокоят на протяжении всего дня, состояние не улучшается при соблюдении диеты и отказе от вредных привычек. При таких симптомах запрещено самостоятельно пытаться улучшить состояние медикаментозными или народными методами. Чем раньше проведена диагностика метастазов и назначено лечение, тем больше шансов на продление жизни человека.
Вернуться к оглавлению
Диагностика
 При постановке диагноза без анализа крови необойтись.
При постановке диагноза без анализа крови необойтись.
При подозрении на метастазы в печеночных тканях, пациента направляют на такие диагностические мероприятия:
- клинический и биохимический анализ крови, с помощью которых проверяются показатели активности печеночных трансаминаз, онкомаркеров, лейкоцитов;
- лабораторное исследование образцов кала и мочи;
- пункционная биопсия;
- МРТ, КТ и УЗИ печени.
Вернуться к оглавлению
Лечение онкологии
Хирургическое удаление
Вылечить метастазы в печени можно оперативным методом, однако успех хирургии и прогнозы на полноценное восстановление зависят от степени запущенности патологии, общего состояния больного. Когда метастазы одиночные, при этом функционирование органа не нарушено, проводится лапароскопия, во время которой удаляются злокачественные узлы, после чего назначается лечение химическими препаратами и радиотерапия. А также операция оправдана, когда обнаружен солитарный метастаз при онкологии кишечника, но важным условием является операбельность основной опухоли, отсутствие метастазирования в другие органы и системы.
При обширном распространении проводится радикальная резекция с удалением пораженной части органа. Если онкология поразила более 75% печени, лечить больного хирургическим путем нет смысла. В этой ситуации проводится паллиативная терапия, основная цель которой — обезболить и улучшить моральное состояние человека перед смертью. На последнем этапе прогрессирования пациенту осталось жить в среднем 3—6 мес.
Вернуться к оглавлению
Пересадка печени
Трансплантация не позволяет избавиться от онкологического заболевания, но для продления жизни пациента к такой методике тоже иногда прибегают. Благоприятного прогноза удастся достичь при незапущенном раке кишечника и отсутствии метастазов в другие органы. Но после процедуры часто возникают осложнения.
Вернуться к оглавлению
Химиотерапия, радиотерапия
 Химиотерапия-как один из методов борьбы с проблемой.
Химиотерапия-как один из методов борьбы с проблемой.
Основная цель — уничтожить мелкие метастазы и приостановить рост крупных новообразований. Во время химиотерапии внутривенно вводятся высокотоксические химические препараты, которые концентрируются в опухоли и уничтожают ее. При проведении такого курса часто развиваются побочные эффекты в виде тошноты, нарушения пищеварения, потери волосяного покрова. Больные выглядят изможденными, чтобы поддержать иммунитет параллельно назначаются иммуновостанавливающие средства и витаминные комплексы.
У радиотерапии тоже похожее предназначение — замедление роста и развития опухоли. Процедура состоит из нескольких сеансов, во время которых в организм вводятся радиоактивные вещества, накапливающиеся в онкопораженных тканях. Химио- и радиотерапию рекомендуется делать перед хирургическим вмешательством или в случае, когда операция неэффективна, но есть возможность на время остановить рост и метастазирование злокачественной опухоли.
Вернуться к оглавлению
Диета при печеночных МТС
Питание при метастазах в печени должно быть сбалансированным, щадящим. Рекомендуется отказаться от мясных, острых, жирных и соленых блюд. В меню должны преобладать продукты растительного происхождения, приготовленные на пару или отварные. Питаться полезно часто, но понемногу, чтобы печень не перегружалась.
Комплексная терапия и диета при метастазах в печени помогут улучшить прогноз на восстановление и продлить жизнь больного.
Вернуться к оглавлению
Народные методы
Если онкологическая болезнь не запущена, в комплексе с традиционной терапией можно проводить лечение народными средствами, предварительно согласовав рецепты и схему приема с врачом. Приостановить увеличение опухоли в размерах и распространение метастаз помогут травы:
- болиголов;
- чистотел;
- полынь.
Для ощелачивания организма народные целители предлагают воспользоваться содой. Полезно каждое утро выпивать натощак стакан воды с 1 ложечкой разведенной в ней содой. Согласно исследованиям, в щелочной среде онкоклетки не в состоянии размножаться и увеличиваться в размерах, поэтому заболевание перестает прогрессировать, а состояние человека постепенно улучшается.
Метастазы в печени: симптомы и какой прогноз
На сегодняшний день раковые заболевания, к сожалению, не являются редкостью. Запущенные формы онкологических болезней сопровождаются метастазами. Метастазирование именно в печени встречается очень часто. Все потому, что орган насыщен сосудистой сетью, постоянным богатым кровообращением. Каждую минуту печень пропускает себя до полутора литров крови, которая заражена раковыми клетками. Это и объясняет высокий риск метастазирования печени. Метастазы в печени могут появиться при различных раковых заболеваниях. Это не обязательно должен быть рак печени. Сколько живут с метастазами в печени точно не известно. Врачи делают прогнозы исходя из индивидуальных особенностей организма больного.
Виды печеночных метастаз
Метастазы печени определяются у трети больных онкологическим заболеванием. Если раковая опухоль локализуется в желудке, молочных железах, толстой кишке, легких, метастазы проникают в печень у 50% больных. Немного реже наблюдается метастазирование печени при раке пищевода, поджелудочной железы. В случае опухолей яичников или простаты, метастазы в печени наблюдаются очень редко.
Специалисты утверждают, что именно метастатический рак печени встречается гораздо чаще, нежели первичная опухоль. В медицине есть классификация метастаз печени. Так, первая классификация определяется по месту расположения и проникновения этих метастаз:
- Билобарные. Происходит поражение обеих долей печени.
- Унилобарные. Поражается только одна доля печени (как правило, правая).
Классифицируют метастазирование железы и по количеству печеночных метастаз. Так, в органе могут диагностироваться множественные опухоли и узлы. В этом случае опухолей насчитывается до десяти и более. Если метастазирование одиночное, узлов наблюдается не более 2-3. Это стандартная классификация онкологических образований печени. Также, среди других видов метастаз можно отметить отдаленные (первичный очаг находится далеко от печени).
Имплантационные метастазы в печени возникают из-за переноса раковых клеток в здоровые ткани организма. Лимфогенные метастазы печени появляются в результате поражения органа через лимфу. Наличие любых метастаз является опасным осложнением. Ведь это указывает на наличие опухоли в организме уже длительный период времени.
Причины появления метастаз в печени
Образование метастаз в печени происходит на фоне распространения онкологических клеток общим кровотоком. Если метастазирование печени является отдаленным, значит в организме больного опухоль имеет запущенный характер. Чаще все, имеет место рак 4 степени. В таких случаях выздоровление пациента практически невозможно. Обычно, метастазы в печени появляются при наличии рака других внутренних органов:
- Желудок;
- Молочные железы;
- Поджелудочная железа;
- Желчный пузырь;
- Легкие.
Если опухоль локализуется именно в данный органах, у 50% всех больных раком наблюдается активное метастазирование в печени. Чуть реже метастазы в печени распространяются на фоне рака пищевода, меланом. Отдаленный онкологический процесс редко провоцирует поражение железы.
Опухоль поджелудочной железы
Данный орган является очень важным для всей системы пищеварения. Вместе с печенью, орган вырабатывает необходимую для переваривания пищи желчь. Если наблюдается онкологический процесс железы, метастазы очень быстро поражают не только печень, но и желчный пузырь, легкие. Причиной этому служит близкое анатомическое расположение. В медицине даже определили гепатопанкреатодуоденальную зону. При таком расположении опухоли, метастазирование начинается уже на 4 стадии рака.
Рак прямой и слепой кишки
Данный вид рака называется колоректальным. На начальном этапе развития онкологического процесса, больной может жаловаться на просто расстройство пищеварительной системы. Рак прямой или слепой кишки характеризуется метастазами только в печень. Стоит отметить, что такой вид заболевания излечим. Выживаемость составляет до 35% даже при наличии осложнений в виде метастаз. Но, все зависит от степени поражения тканей онкологическими клетками.
Рак печени 4 стадии
Онкологический процесс в печени достаточно сложно поддается терапии. 4 стадия рака печени считается необратимой. Лечение рака печени 4 стадии невозможно излечить. Все связано с тем, что онкопроцесс бесконтрольно разрастается, поражает ткани органа. Так как печень постоянно перекачивает кровь, клетки рака стремительно распространяются по организму. Смертность в таком случае очень велика. Пораженная раком печень может перестать выполнять свои функции в любой момент. Симптоматика последней стадии рака очень яркая и интенсивная.
Метастазирование без наличия первичного очага
Не редкостью являются метастазы в печени без определения первичной опухоли. Такой вариант метастазирования очень часто возникает из-за онкологии молочных желез. Симптоматика достаточно скудная. Поэтому определить наличие метастаз можно только после компьютерной томографии, ультразвукового исследования.
Такое осложнение может носить и иной характер возникновения. Так, врачи отмечают яркую инфильтрацию стомы больного органа. Стоит отметить, что раковые клетки могут проникать даже через стенки кровеносных сосудов. Множественные количественные метастазы в печени встречаются не так часто. Второе место по метастазированию после печени занимают легкие. Это основные органы-мишени для рака.
Симптомы метастаз в печени
Начальный этап развития заболевания может протекать абсолютно бессимптомно. Сначала отмечаются не специфические проявления. Так, можно отметить вялость, потерю веса, лихорадку, анорексию. Распознать патологию можно как самостоятельно, так и при помощи профессионального исследования организма. При проведении ультразвукового исследования покажет увеличение органа в размерах, некоторые уплотнения в печеночной ткани.
Редко, но все же, встречаются признаки метастазирования печени такие, как шумы брюшной полости, боль в грудной клетке, спленомегалия. Характерными и яркими симптомами метастаз в печени являются следующие признаки:
- Боль с правом подреберье;
- Тошнота, рвота;
- Тяжесть в животе;
- Желтуха;
- Высветление кала, потемнение мочи;
- Повышение температуры тела;
- Зуд кожных покровов;
- Бледность;
- Асцит;
- Кровотечения.
Стоит отметить, что данная симптоматика считается характерной для любого тяжелого заболевания печени. Поэтому, при обнаружении одного их проявлений стоит немедленно обратиться к доктору. Так как при метастазах в печени часто наблюдаются метастазы и в легких, стоит знать и такую симптоматику. Для метастазирования легких характерным можно назвать постоянный сухой кашель, одышку, выделение мокроты и крови во время сильного кашля, высокую температуру тела.
Боль указывает на сложный процесс течения заболевания. Болевой синдром возникает из-за растяжения капсулы больного органа, что говорит о стремительном увеличении печени. Как только больной узнает о наличии рака, лечение нужно проводить незамедлительно. Ведь начальная стадия онкологического процесса излечима. И только запущенные случаи приводят к метастазированию и смерти.
Диагностика
Перед любым лечением необходимо произвести полноценную диагностику всего организма. Так, пациенту нужно сдать ряд анализов, провести некоторые инструментальные исследования. Так, для выявления метастаз печени врачи назначают биохимический анализ крови. Также, необходимо сдать кровь из вены на маркеры онкологического заболевания. Биохимический анализ показывает такие важные показатели:
- Билирубин;
- АЛТ, АСТ;
- Щелочная фосфатаза;
- Тимоловая проба;
- Гаптоглобин;
- С-реактивный протеин;
- Альбумин;
- Мочевина;
- Креатинин.
Так, высокий уровень АЛТ и АСТ указывает на дисфункцию гепатобилиарной системы организма. Высокий билирубин объясняет происхождение желтухи. О наличии опухоли и метастаз в печени говорит отклонение от нормы такого показателя, как гаптоглобин. Печеночная недостаточность определяется по высокому уровню (более пяти) тимоловой пробы.
Среди инструментальных методов исследования врачи используют ультразвуковую диагностику, компьютерную томографию, магниторезонансную томографию. На данных препаратах метастазы в печени выглядят в виде небольших солитарных депозитов. При подозрении на такое распространение опухоли, чаще всего, специалисты проводят компьютерную томографию. Этот метод максимально информационный, безопасный. Снимок покажет печень, как увеличенный узловатый орган.
Если у больного наблюдаются ярко выраженные признаки онкологического процесса в железе, доктора принимают решение о проведении непосредственной пункционной биопсии. Только гистологическое исследование тканевого образца точно определит проблему. Процедура забора образца проводится под местным наркозом, поэтому болевых ощущений больной не испытывает. Иногда, для выявления метастаз в печени проводят лапароскопию. Так, доктор может приступить к проведению операции сразу же после диагностики. Ведь метастазы можно удалять путем резекции и отсечения.
Лечение метастазов печени
Метастазы печени трудно поддаются лечению. Но, терапию нужно проводить обязательно. Терапию против рака стоит начинать незамедлительно, после постановки диагноза. При метастазировании химиотерапия является обязательным условием для лечения пациента. В таких случаях назначаются препараты цитостатики: 5-фторурацил, Циспластин, Циклофсофамид. Выбор конкретного препарата полностью зависит от показателей первичной опухоли. И только доктор устанавливает длительность курса химиотерапии.
Лечение метастазов печени радиотерапией дает хорошие результаты. Доза лучевого облучения, которая подается на пораженный орган, определяется каждому пациенту индивидуально. Химиотерапия и радиотерапия отлично сочетаются друг с другом. Химиотерапия может уменьшить первичную опухоль в размерах, приостановить процесс развития рака. Это и продлит жизнь больному. Радиотерапия утоляет болевой синдром, и другую симптоматику, но не продлевает жизнь. Одиночные метастазы поддаются лечению при помощи резекции.
Вторичные и первичные печеночные опухоли питаются кровью из печеночной артерии. Иногда в питании принимает участие и воротная вена. В связи с этим, нередко доктора вводят препараты цитостатики непосредственно в артерию вены. Наличие метастазирования подразумевает обязательного удаления желчного пузыря. Химиотерапия при первичном раке прямой или толстой кишки дает более позитивные прогнозы. Так, продолжительность жизни больных увеличивается до 26 месяцев. Трансплантацию печени проводят достаточно редко в связи с тем, что найти подходящего донора очень сложно, а ждать нет времени. Во время проведения резекции одиночных метастаз хирург может принять решение и об отсечении части органа.
Прогноз жизни
Прогноз жизни больного зависит от количества метастаз, характера первичной опухоли, своевременности проведения терапии. В среднем, смерть наступает спустя год после выявления метастаз в печени. Опухоль прямой и толстой кишки имеет более положительный прогноз. Так, после резекции кишки пациент может прожить с метастазами еще 12-18 месяцев. Если большая часть печеночной ткани замещена соединительной, узлами, метастазами, прогноз крайне плох. Летальный исход наступает быстро. Ведь метастазы распространяются только на последней стадии рака.
Диетическое питание при метастазировании печени
В комплексе с медикаментозной терапией, больному важно соблюдать диету. Так, рацион должен быть максимально насыщенным витаминами, быть сбалансированным. Пациент обязан ежедневно употреблять в пищу свежие овощи, богатые на клетчатку. При метастазах в печени питание дробится на несколько приемов пищи в день. Все блюда должны быть только отварными, запеченными, или приготовленными на пару. Жареная еда категорически запрещена к употреблению.
Рацион больного должен состоять из таких продуктов:
- Серый хлеб;
- Крупы, каши;
- Макаронные изделия из твердых сортов пшеницы;
- Нежирные супы, бульоны, борщи;
- Свежие ягоды и фрукты;
- Диетические виды мяса;
- Нежирные морепродукты;
- Кисель;
- Чай травяной;
- Молочная продукция.
Из рациона полностью исключается опасная пища. Это любые консервы, специи, приправы, маринады. Также, под запретом находится свежий хлеб, жирное мясо и рыба, бобовые, большое количество соли и сахара, алкоголь, шоколад, жареные куриные яйца. Врачи рекомендуют соблюдать средиземноморскую диету, которая помогает не дает нагрузку на печень, помогает органу бороться с патологией. В большинстве случаев вылечить и избавить больного от метастаз в печени невозможно. Но, при правильной терапии можно немного продлить жизнь пациенту.
Метастаз в печени — Libre Pathology
A Метастаз в печени — это злокачественное метастатическое новообразование в печени, возникшее в другом месте. Метастазы в печень встречаются чаще, чем первичные новообразования печени.
Он также известен как метастатическое заболевание печени и метастаз в печени .
Метастатические заболевания в целом рассматриваются в статье «Метастазы ».
Общие
- Метастазы очень распространены — часто из желудочно-кишечного тракта, например.г. колоректальный рак.
- Биопсия большинства новообразований печени не проводится … поскольку первичное поражение очевидно. [1]
- В зависимости от степени заболевания метастаз CRC в печень можно излечить с помощью резекции печени.
- Заболевание брюшины, то есть злокачественный узелок брюшины, в контексте метастазов в печень плохо себя чувствует и считается противопоказанием к резекции печени. [2]
- Важно учитывать опухоли зародышевых клеток при DDx, поскольку они могут быть излечены химиотерапией.
- Светлоклеточный вариант ГЦК может быть ошибочно диагностирован как метастатическая светлоклеточная карцинома.
- Межпеченочная холангиокарцинома — это аденокарцинома, которая может выглядеть как метастатическое поражение.
Макропатология / радиология
Особенности:
Радиология:
- Классический гипоаттенуирующий узел на КТ — рентгенологически можно принять за абсцесс. [3]
- Гиподензивные образования в венозной фазе на КТ с контрастированием. [4] [5]
Изображения
Метастазы в печени (поджелудочная железа).(ТУАЛЕТ)
Микроскоп
Особенности:
- Гистологические признаки зависят от первичной и степени дифференцировки.
Классический метастаз в печень (колоректальный рак):
- Железа, образующая столбчатые клетки с псевдостратифицированными гиперхроматическими сигарообразными ядрами.
DDx:
Изображение
Метастаз в печени — аденокарцинома. (WC / Нефрон)
IHC
- Метастазы обычно отрицательны для HepPar-1 .
- HepPar-1 (гепатоциты, антитело к парафину 1) — метки гепатоцеллюлярных митохондрий. [7]
Панель А:
- СК7, СК20, TTF-1, CDX2, CA-125. [8]
Примечание:
- Если первичное поражение уже установлено в результате патологии, и это не грудь, и клиническое впечатление является метастазом, нет необходимости проводить ИГХ, если морфология поражения в печени совместима с установленным первичным поражением.
Выйти
Аденокарцинома
Поражение печени, основная биопсия: - АДЕНОКАРЦИНОМА, СЛАБО ДИФФЕРЕНЦИРОВАННАЯ, см. Комментарий. Комментарий: Опухоль состоит из круглых клеток с округлыми ядрами и малозаметными ядрышками. Он находится в плохо сформированных железах. Опухоль окрашивается следующим образом: ПОЛОЖИТЕЛЬНО: CK7, CA-125. ОТРИЦАТЕЛЬНЫЙ: CK20, CDX2, TTF-1. Результаты соответствуют первичной передней кишке (поджелудочная железа, желудок, желчные протоки, двенадцатиперстная кишка). Предлагается клиническая и рентгенологическая корреляция.
Печатные буквы
ПЕЧЕНЬ, ЧАСТЬ 2 И 3 СЕГМЕНТОВ, ОТДЕЛЕНИЕ: - МЕТАСТАТИЧЕСКАЯ АДЕНОКАРЦИНОМА. - ЗАЗОР ОТДЕЛЕНИЯ 2 ММ. - СТЕАТОЗ ПЕЧЕНИ ЛЕГКИЙ.
Micro
На разрезе показана паренхима печени с инвазивной аденокарциномой. Аденокарцинома
имеет хорошо сформированные железы с грязным некрозом. Ядра кажутся переполненными и
имеют форму эллипсоида. Очагово присутствуют зоны некроза. См. Фон печени.
ФОН ПЕЧЕНЬ (ТОЛЬКО НА ОСНОВЕ H&E)
Фиброз: не идентифицирован.
Фиброзные перегородки: отсутствуют.
Перегородки с изогнутыми контурами: отсутствуют.
Крупнокапельный стеатоз (% гепатоцитов): легкий (20%).
Раздувание гепатоцитов: не идентифицировано.
Тела Мэллори-Денк: не опознаны.
Воспаление воротной вены: присутствует, легкое.
Активность интерфейса: не идентифицировано.
Дольчатое некровоспаление: не идентифицировано.
Воздуховоды: присутствуют в нормальном количестве.
Травма протока: не идентифицирована.
Протоковая реакция: не идентифицировано.
Холестаз: присутствует перитуморальный, в остальном отсутствует.
Терминальные печеночные венулы: есть.
Клетки из матового стекла с обычным окрашиванием: не идентифицировано.
Метастаз рака толстой кишки в печень
Метастаз рака толстой кишки в печень. A. Синяя стрелка показывает рак толстой кишки с большими ацинусами. Зеленая стрелка показывает некротическую опухоль. Черная стрелка показывает синусоидальную дилатацию, пример неспецифического изменения, связанного с опухолью, которое не должно считаться системным по своей природе. B. Удлиненные ядра, перпендикулярные ацинарной границе (зеленые стрелки) и грязный некроз просвета (черная стрелка), характерны для рака толстой кишки.C. Иммуноокрашивание для CK7. Положительные группы могут иметь очаговое окрашивание опухолью, но более вероятно, что это остаточные желчные протоки. D. Иммуноокрашивание на CK20 более диффузно положительно и определенно в опухоли.
Метастаз плоскоклеточного рака в печень
Метастаз плоскоклеточного рака в печень. A. Темно-синие опухолевые группы, замещающие печень B. Карциноматозные гнезда демонстрируют скудное разделение стромы, при этом отдельные раковые клетки являются краем некротического пространства C. На огромных ядрах видны ядрышки с редкими веретенообразными клеточными ядрами.Выражен индивидуальный некроз клеток. Цитоплазма скудная. Иммуноокрашивание на CK7. Положительные группы могут иметь очаговое окрашивание опухолью, но более вероятно, что это остаточные желчные протоки. D. Иммуноокрашивание на P63 положительное; CK7, CK20, хромогранин, синаптофизин и TTF1 были отрицательными
Метастатическая низкодифференцированная нейроэндокринная карцинома легочного происхождения. Опухоль представляет собой массу (Ряд 1 слева 40X). Опухоль заменяет большую часть триады; обратите внимание на остаточный межлобулярный желчный проток [стрелка] (ряд 1 справа 200X).Опухолевые клетки образуют плесень, имеют скудную цитоплазму и выраженный анионуклеоз, более крупный, чем обычная мелкоклеточная карцинома (ряд 2 слева, 400X). Опухолевые клетки положительны на CK7 (ряд 2 справа 400X). Опухолевые клетки положительны на TTF1 (ряд 3 слева, 400X). Опухолевые клетки положительны на CD56 (Ряд 3 справа 400X).
Метастатическая карцинома щитовидной железы. A. Карцинома с открытыми пространствами представляет собой часть нормальной доли печени [стрелка] (40X). B. Лист с ацинусами [стрелки] указывает только на аденокарциному (400X). C. Настоящий сосочек с сосудистыми полостями [стрелки] указывает на папиллярную карциному (400X).D. В некоторых местах показаны ядра опухоли с включениями [стрелки] (400X). E. Ядра опухоли являются TTF1-положительными, что также наблюдается при раке легких (IHC 400X). F. Определенная положительная реакция на тиреоглобулин сделала известный диагноз (IHC 400X).
Метастазы почечно-клеточного рака в печень. A. Верхняя часть ядра показывает голубой некроз; остаток показывает замещение опухолью. B. Частично цитоплазма обильная и амфофильная, что свидетельствует о гепатоцеллюлярной карциноме. C. Частично опухоль имеет чистую цитоплазму, что вызывает альтернативные объяснения.D. Высокая мощность прозрачной области показывает мелко сетчатую цитоплазму с резкими межклеточными границами. Ядра причудливой формы, часто с ядрышками. Стрелка показывает аномальный митоз. E. Иммуноокрашивание при ПКР доказывает почечно-клеточную карциному.
Меланома
Меланома с метастазами в печень. A. Низкое увеличение контрастирует нормально сохраненную печень (стрелка) с остаточной массой рака [2x]. B. Некроз слева упирается в коричневые пигментированные клетки справа [200X]. C. Видимые ацинусы (зеленые стрелки), вакуоли (синяя стрелка) и сосочки (черные стрелки) могут привести к неправильному диагнозу [200X].D. Видимая стенко-подобная оболочка эпителия (зеленые стрелки) и гигантские клетки (синие стрелки) могут вызвать неправильный диагноз, который пигмент (черные стрелки) должен препятствовать [400X]. E. Внутриядерные включения (зеленая стрелка), эксцентрично расположенные ядра (синие стрелки) и пигмент (черные стрелки) предполагают правильный диагноз [400X]. F. Иммуноокрашивание MART 1 является положительным в жизнеспособных раковых клетках [400X].
Поражение печени, основная биопсия: - МЕТАСТАТИЧЕСКАЯ ЗЛОКАЧЕСТВЕННАЯ МЕЛАНОМА, см. Комментарий. Комментарий: Опухоль окрашивается следующим образом: ПОЛОЖИТЕЛЬНО: S-100, HMB-45, Melan A.ОТРИЦАТЕЛЬНЫЙ: CK7, CK20, TTF-1. Опухоль состоит из круглых клеток с округло-эллипсовидными ядрами, незаметные ядрышки и умеренное количество серой цитоплазмы. Присутствуют ядерные псевдовключения.
См. Также
Список литературы
- ↑ OA. 29 ноября 2009 г.
- ↑ Elias, D .; Rougier, P .; Mankarios, H .; Fahrat, F .; Лассер, П. (март 1993 г.). «[Резектабельные метастазы в печени и синхронные внепеченочные участки колоректального происхождения. Хирургические показания].». Presse Med 22 (11): 515-20. PMID 8511077.
- ↑ Yoon, KH .; Yun, KJ .; Ли, JM .; Ким, CG .. «Одиночные некротические узелки в печени, имитирующие метастазы в печень: отчет о двух случаях». Korean J Radiol 1 (3): 165-8. DOI: 10.3348 / kjr.2000.1.3.165. PMID 11752949.
- ↑ URL: http://www.radiologyassistant.nl/en/p446f010d8f420/liver-masses-i-characterization.html. Доступ: 4 августа 2016 г.
- ↑ Kanematsu, M .; Кондо, Х.; Goshima, S .; Kato, H .; Tsuge, U .; Hirose, Y .; Kim, MJ .; Морияма, Н. (май 2006 г.). «Визуализация метастазов в печени: обзор и обновление». Eur J Radiol 58 (2): 217-28. DOI: 10.1016 / j.ejrad.2005.11.041. PMID 16406434.
- ↑ Kondo, Y .; Накадзима, Т. (сентябрь 1987 г.). «Псевдогландулярная гепатоцеллюлярная карцинома. Морфогенетическое исследование». Рак 60 (5): 1032-7. PMID
.
Метастазы в печень — хирургическое лечение
2.2.1. Резектабельный CLM
Резекция печени предлагает единственный шанс на долгосрочное выживание для пациентов с CLM, первая большая серия выводов о пользе хирургического вмешательства у отдельных пациентов с CLM, о которых сообщалось в 1978 г. [35]. 5-летняя выживаемость для этих пациентов увеличилась примерно с 30% два десятилетия назад до почти 60% в настоящее время, а 10-летняя общая выживаемость составляет 20-25% для радикально удаленных пациентов [36].
Критерии резектабельности
Уровень резектабельности улучшился благодаря предоперационным методам визуализации, отбору пациентов, хирургическим методам, послеоперационному уходу и новым цитотоксическим и биологическим агентам для предоперационного и послеоперационного лечения. Таким образом, критерии резектабельности этих случаев резко изменились. Количество очагов (от 1 до 3 однодольных метастазов), размер очага (менее 5 см), временной интервал (желательно не менее 12 месяцев после резекции первичной опухоли), минимальная граница 1 см в ширина и отсутствие внутригрудной лимфаденопатии или внепеченочного заболевания больше не считаются определяющими факторами при рассмотрении возможности операции.
Количество метастазов не является фактором риска для долгосрочного выживания при условии, что была выполнена резекция R0 (полная резекция без микроскопической остаточной опухоли) [37]. Некоторые исследования показали, что степень ответа на химиотерапию является более сильным предиктором долгосрочной выживаемости, чем количество метастазов. Хотя отчеты противоречивы, данные показывают, что размер — это не фактор резектабельности, а фактор, связанный с агрессивностью опухоли. Точно так же ширина хирургического края не влияет на выживаемость, если край микроскопически отрицательный [38-40], хотя при планировании резекции следует стремиться к оптимальному краю, т.е.е. шириной более одного сантиметра. Еще несколько лет назад внепеченочное заболевание считалось противопоказанием к резекции печени. Сообщалось о пятилетней выживаемости от 12% до 37% после резекции печени у выбранных пациентов, независимо от локализации внепеченочного заболевания (легкое, первичный колоректальный рецидив, забрюшинные или печеночные лимфатические узлы на ножке, перитонеальный карциноматоз и др.) [41 -45]. У большинства пациентов заболевание брюшины рассматривается как противопоказание к резекции печени, но может рассматриваться в случаях стабильного или химиотерапевтического заболевания, когда резекция R0 достижима.Этих пациентов следует классифицировать как имеющих пограничную резектабельность [46]. Положительные внутригрудные лимфатические узлы связаны с плохой выживаемостью и также обычно рассматриваются как противопоказание к резекции печени при CLM. Однако, опять же, некоторые исследования показали длительную выживаемость у некоторых пациентов, особенно если пораженные узлы ограничены гепатодуоденально-ретропанкреатической областью [47, 48], хотя эти узлы обычно не удаляются.
Короче говоря, универсально значимыми являются только два критерия резектабельности: (1) должна быть возможность удалить все болезни с отрицательной границей; (2) Должен быть достаточный остаточный печеночный резерв.Единственным традиционным прогностическим индикатором рецидива, исключающим долгосрочное выживание, является положительный край резекции [34].
Соответственно, CLM считаются операбельными, когда они могут быть полностью резекции, два соседних сегмента печени могут быть сохранены, поддерживая адекватный приток и отток сосудов и желчный дренаж, а объем будущего остатка печени (FLR) является адекватным (при не менее 20% от общего расчетного объема для печени с нормальной паренхимой, 30–60% для печени с химиотерапией, стеатозом или гепатитом, 40–70% для печени с циррозом) [46].Для клинической оценки резектабельности полезно оценить отношение FLR к массе тела, которое должно быть больше 0,5. Однако не существует общепринятых рекомендаций по «резектабельности» первичного или метастатического рака печени, и зачастую опыт отдельного хирурга играет важную роль.
Химиотерапия
Неясны оптимальные схемы и время проведения химиотерапии при возможной резекции печени. Эффективность периоперационной химиотерапии в отношении выживаемости при резектабельных метастазах в печени не была подтверждена.Некоторые авторы предполагают, что лечение операбельной CLM при отсутствии признаков высокого риска должно начинаться с хирургического вмешательства, а затем рассматривать возможность адъювантной химиотерапии [2]. Доказательств в пользу неоадъювантной химиотерапии у пациентов с операбельным заболеванием нет [49]. Более того, поскольку около 7% опухолей будут прогрессировать во время химиотерапии, этот подход может снизить шансы некоторых пациентов на выздоровление при регулярном использовании. При наличии признаков высокого риска большинство врачей предпочитают короткий курс системной предоперационной химиотерапии.Пациенты с перфорированной опухолью или значительной лимфатической нагрузкой считаются кандидатами на неоадъювантную химиотерапию перед операцией на печени. В исследовании EORTC 40983 оценивалась периоперационная химиотерапия по сравнению с одной только хирургической операцией при резектабельных метастазах в печени и не было продемонстрировано явного преимущества предоперационной химиотерапии у пациентов с резектабельной ХЛМ. Это исследование также не могло определить, была ли лучше неоадъювантная, адъювантная или периоперационная химиотерапия. В этом исследовании частота послеоперационных осложнений была значительно выше у пациентов, получавших периоперационную химиотерапию, по сравнению с только хирургическим вмешательством.Некоторые из этих осложнений включали желчный свищ, печеночную недостаточность, внутрибрюшную инфекцию и необходимость повторной операции. Сторонники периоперационного лечения отмечают, что операция облегчается и что лечение дает информацию о биологии опухоли. То же исследование показало, что ни у одного пациента не развилось неоперабельное состояние, что короткие циклы лечения обеспечивали минимальную токсичность для печени и что выживаемость улучшилась в подгруппе химиотерапии [50]. Печень, пораженная химиотерапией, обычно более жесткая, более трудная в управлении и склонна к более легкому кровотечению во время операции.Более того, вопросы о лечении «призрачных поражений» после полного ответа, которые не могут быть обнаружены с помощью IOUS, остаются без ответа.
Если резекция считается целесообразной, обязательно провести высококачественную КТ (или МРТ) брюшной полости в течение месяца с даты операции. В это время следует сделать КТ грудной клетки.
Резекция
Детальное знание анатомии печени, контроля притока и оттока, низкого центрального венозного давления, ВМС, ультразвуковой диссекции, коагуляции аргоновым лучом и т. Д.способствуют снижению кровопотери при резекции КЛМ. Интраоперационное кровотечение является основной причиной послеоперационной заболеваемости и смертности, поскольку переливание крови связано с уменьшением долгосрочной выживаемости, увеличением периоперационной смертности, более высокой частотой осложнений, более длительным пребыванием в больнице и повышенным риском инфекционных осложнений [51].
Сегментэктомия печени с использованием сегментов Куино предпочтительна для локализации поражений; Несегментарная резекция может быть технически более сложной и нарушить кровоснабжение соседней остаточной печени.Тем не менее, IOUS необходимо использовать перед попыткой клиновидной резекции явно поверхностного узла. Для более крупных или множественных CLM необходимо использовать стандартные анатомические резекции. Кроме того, рекомендуется использовать терминологию анатомии и резекций печени Брисбена 2000 г., чтобы избежать путаницы в терминах, используемых при описании хирургических методов [52].
Невозможность получить свободный хирургический край во время резекции печени по поводу CLM не должна быть противопоказанием к операции при условии достижения полного макроскопического удаления всех метастатических поражений (положительный край или резекция R1), поскольку выживаемость аналогична выживаемости при резекции R0 , несмотря на более высокую частоту рецидивов (5-летняя и 10-летняя общая выживаемость составляет 61% и 43% в R0 vs.57% и 37% в R1) [53].
Лапароскопическая резекция печени в настоящее время выполняется чаще, чем первая, о которой было сообщено в 1992 году [54]. Он показывает преимущества в краткосрочной перспективе по сравнению с открытой операцией, но до сих пор нет данных, указывающих на влияние этой процедуры на долгосрочный результат.
Смертность составляет менее 5%, а заболеваемость составляет около 30%, учитывая широкий диапазон хирургической агрессивности. Послеоперационная печеночная недостаточность может быть летальным осложнением. Это зависит от объема и функции остаточной печени.В целом, чем больше размер резекции печени, тем выше вероятность послеоперационных осложнений. Другие осложнения, которые могут способствовать или быть связаны с послеоперационной печеночной недостаточностью, включают кровотечение, подтекание желчи, внутрибрюшной сепсис и сердечно-легочную дисфункцию.
Что касается хирургии синхронной и метахронной ХЛМ, одновременная резекция толстой кишки и печени оказалась безопасной и эффективной, поскольку прогноз не зависит от времени резекции ХЛМ.
2.2.2. Изначально неоперабельная CLM
Некоторые методы могут использоваться, когда CLM не может быть резектабельна вначале из-за недостаточного FLR. Стратегии увеличения объема печеночного остатка включают конверсионную химиотерапию, окклюзию воротной вены, поэтапную резекцию печени и комбинацию этих процедур. Кроме того, абляционные методы могут рассматриваться отдельно или в сочетании с резекцией.
Химиотерапия
Химиотерапия улучшает выживаемость пациентов с неоперабельной ХЛМ.В этих случаях предварительная химиотерапия у бессимптомных пациентов по сравнению с резекцией первичной опухоли, по-видимому, не оказывает значительного влияния на выживаемость. Однако без резекции печени 60% пациентов живы через 2 года, поэтому при раке прямой кишки рекомендуется резекция первичного очага по паллиативным причинам и местному контролю [55].
Целью конверсионной химиотерапии является уменьшение размера опухоли для повторного рассмотрения ее резекции. Новые химиотерапевтические схемы, сочетающие 5-ФУ, фолиновую кислоту и оксалиплатин (FOLFOX) и / или иринотекан (FOLFIRI), улучшили частоту ответа (примерно 50%), что позволяет оперировать 10-30% пациентов с изначально неоперабельным заболеванием [56] .В сочетании с биологическими агентами, которые нацелены на ангиогенез (бевацизумаб) и рецептор эпидермального фактора роста (EGFR) в опухолях K-ras дикого типа (цетуксимаб), достигаются показатели ответа до 70% [34]. Повторное обследование на предмет резекции должно проводиться через 2 или 3 месяца дооперационной химиотерапии и каждые 2 месяца после этого. Инфузия химиотерапии в печеночную артерию (HAI) может быть добавлена к системной терапии, чтобы получить более высокую концентрацию лекарств в печени с меньшей системной токсичностью. Хотя показатели ответа выше, чем при системной химиотерапии, выживаемость пока не меняется.Кроме того, частота его осложнений настолько высока (57%), что от него отказываются в качестве первого варианта.
Химиотерапию следует прекратить, когда размеры CLM уменьшены до точки, при которой возможна резекция печени, чтобы снизить токсичность для печени и избежать полного клинического ответа. Полный ответ на КТ не означает излечения, так как более чем в 80% случаев в начальном месте метастаза находятся жизнеспособные раковые клетки [57]. Эти призрачные очаги должны быть удалены или устранены с учетом FLR [58-60].
Прогрессирование опухоли связано с плохим исходом даже после потенциально излечивающей гепатэктомии. Таким образом, контроль опухоли перед операцией имеет решающее значение для обеспечения возможности длительной ремиссии у пациентов с множественными метастазами [56]. Можно ожидать, что только 50% опухолей покажут частичный ответ на химиотерапию. Пациенты, которые могут быть подвергнуты операции во время системного лечения, должны рассматриваться в качестве кандидатов на хирургическое вмешательство независимо от связанных с ними неблагоприятных прогностических факторов.
Периоперационные осложнения, включая гепатобилиарные осложнения, чаще возникают при длительной предоперационной химиотерапии, вероятно, связанных с длительным и последовательным использованием нескольких режимов [61].Адъювантное лечение, обычно FOLFOX, может использоваться после операции, но HAI в сочетании с системной химиотерапией также является вариантом. Испытания, изучающие роль адъювантной химиотерапии, трудно провести из-за быстро меняющихся режимов химиотерапии и лекарств [62]. Поскольку послеоперационная заболеваемость влияет на долгосрочную выживаемость [63], необходимо учитывать продолжительность химиотерапевтического лечения. В последние годы все больше и больше пациентов со стабильным длительным заболеванием (более 20 месяцев) обращаются к хирургическому лечению.
Окклюзия воротной вены
При недостаточной FLR следует рассмотреть возможность окклюзии воротной вены. В 1990 году Макуучи представил эмболизацию воротной вены (ЭВВ) правой воротной ветви, чтобы вызвать гипертрофию левой стороны печени, что позволило более безопасно удалить большие или множественные опухоли, в основном расположенные в правом полушарии и сегменте IV [64]. Обоснование этого подхода состоит в том, чтобы вызвать атрофию несущей опухоль доли с последующей гипертрофией контралатеральной доли путем отклонения кровотока воротной вены в участок печени, который, как ожидается, останется.Как правило, могут использоваться два метода окклюзии воротной вены: ПВЭ или хирургическая перевязка воротной вены (ПВЛ). Ни одна из техник не имеет явного преимущества.
Окклюзия портала увеличивает FLR на 10–46% в течение 2–8 недель и позволяет выполнить резекцию R0 в 70–100% отдельных случаев. Однако у некоторых пациентов после ЭПЭ наблюдается прогрессирование опухоли, но неясно, является ли это лишь вопросом времени (от окклюзии воротной вены до операции) или вызвано стимулами роста опухоли, вызванными индуцированной регенерацией печени.Окклюзия воротной вены также представляет собой динамический предоперационный тест на способность печени реагировать на хирургическую агрессию: если достигается гипертрофия более 5%, существует низкий риск тяжелой послеоперационной печеночной недостаточности [65] .
Сопутствующее введение химиотерапии может уменьшить как опухолевую нагрузку, так и количество послеоперационных рецидивов. Химиотерапия, похоже, не влияет на гипертрофию, вызванную ПВЭ. В нескольких исследованиях с использованием бевазуцимаба рекомендуется 6-недельный период ожидания перед операцией, хотя его влияние на гипертрофию неясно.
Чрескожный ПВЭ обычно хорошо переносится с минимальными побочными эффектами, такими как лихорадка, тошнота и преходящие отклонения от нормы функционального теста печени, и с частотой осложнений менее 5% [66]. Крупные операции на печени после ПВЭ имеют частоту осложнений 1% для самой ПВЭ и 8,8% осложнений при последующей резекции [67]. Это увеличивает возможность резекции печени на 19%. Актуарный коэффициент выживаемости после операции составляет 40% через 5 лет, что аналогично таковому у пациентов, удаленных без ПВЭ [68].
Двухэтапная гепатэктомия
Это комбинация двух последовательных и плановых резекций печени, когда невозможно удалить все метастазы печени за одну процедуру, сохранив при этом не менее 30% функционального объема печени, чтобы избежать послеоперационного периода. отказ печени. Во время первой операции предпринимается попытка резекции большей части ХЛМ и гипертрофии остаточной печени. Технику следует спланировать заранее, чтобы добиться полного удаления, учитывая, что около 30% пациентов не будут спасены при второй гепатэктомии.
Обычно при первой гепатэктомии FLR удаляется от опухолей неанатомической резекцией и / или радиочастотной абляцией, или, самое большее, резекцией одного сегмента [69]. Этот первый этап также может выполняться вместе с лапароскопической или открытой колоректальной резекцией. После периода выздоровления продолжительностью от 4 до 6 недель и последующей гипертрофии доли, свободной от опухоли, удаление опухоли завершается резекцией большей опухолевой массы в контралатеральной доле печени. Большинство пациентов, у которых этот подход оказался безуспешным, сделали это, потому что за это время у них развилось прогрессирование болезни.
В качестве другого варианта, через две-четыре недели после первого этапа может быть проведено ПВЭ [70]. Вторую операцию можно провести на четвертой или пятой неделе после ЭП, когда компьютерная томография подтвердит, что достигнута адекватная гипертрофия неэмболизированной полу-печени. В качестве альтернативы окклюзию воротной вены можно выполнить во время первой гепатэктомии путем перевязки и алкоголизации правой воротной вены, которая чаще всего подвергается эмболизации [71,72]. Эта модификация основана на доказательствах того, что PVL вызывает аналогичный или лучший регенеративный ответ, чем PVE, и может безопасно применяться даже в сочетании с частичной гепатэктомией левого полушария.
В современной серии двухэтапной резекции после ПВЭ от 69% до 72% пациентов завершили второй этап, наиболее частой причиной выбывания из исследования было прогрессирование опухоли. Пациенты, ответившие на химиотерапию и завершившие резекцию, имеют 5-летнюю выживаемость 32-51% [73,74]. Если обнаружены новые CLM или внепеченочные поражения, такие как локализованные имплантаты брюшины, резекция все равно может быть выполнена, если может быть достигнута резекция R0. Предоперационная химиотерапия может проводиться в течение всего процесса.
Связь перегородки печени и лигирования воротной вены для поэтапной гепатэктомии (ALPPS)
Этот метод был недавно описан [75] Это новая концепция двухэтапной расширенной правой гепатэктомии с начальным хирургическим исследованием, правой ЛВЛ и расщепление на месте (ISS) вдоль правой стороны серповидной связки, чтобы вызвать быструю гипертрофию левой боковой доли у пациентов с малооперабельными или первично неоперабельными первичными и метастатическими опухолями печени.
Избирательная эмболизация или лигирование портальных ветвей сегмента IV при планировании расширенной правой гепатэктомии оказывает значительное влияние на гипертрофию FLR. Однако полнота эмболизации ветви сегмента IV требует оптимального доступа и часто может быть неполной. Комбинирование PVL с ISS путем почти полного рассечения паренхимы вызывает медианную гипертрофию 74% (выше, чем достигается только PVL или PVE) через средний временной интервал в 9 дней.
Этот короткий промежуток времени примерно в одну неделю для гипертрофии перевешивает риск прогрессирования опухоли.Хотя для некоторых пациентов ALPPS может быть единственным шансом вообще разрешить резекцию, необходимо провести дальнейшие исследования краткосрочных и долгосрочных результатов, таких как ускоренное развитие микрометастазов в будущей остаточной печени, системные реакции на стресс, влияющие на вторую. этап резекции и паттерны выживаемости и прогрессирования [76]. Чтобы оценить онкологические преимущества этого нового подхода, был создан регистр [77].
Лапароскопия также использовалась в этой технике, что показало, что она осуществима и может оказаться полезной в опытных руках [78,79].
Некоторые авторы выделили возможные недостатки ALPPS, такие как повышенная заболеваемость и смертность в первой опубликованной серии [80], наличие деваскуляризованного некротического сегмента 4 у пациентов, которые не могли быть кандидатами на вторую стадию из-за недостаточной гипертрофии [81]. ] и незначительные преимущества по сравнению с предыдущими методами [82], рекомендуя зарезервировать ALPPS на случай неожиданного распространения опухоли [83].
Технические преимущества ALPPS включают более легкую вторую процедуру (быстрая гипертрофия остаточной печени позволяет провести вторую операцию до развития спаек), более быстрое выздоровление пациента с возможностью более раннего восстановления химиотерапии и эффективность колоректальная резекция одновременно с первым этапом процедуры, включая очистку от опухоли FLR (что минимизирует риск осложнений, связанных с послеоперационной печеночной недостаточностью) [84].Конечно, необходимы уточнение технических аспектов и оптимизация отбора пациентов для этой процедуры (рис. 1).
Рисунок 1.
Первый этап ALPPS
Абляционные техники
Точная роль абляционной терапии еще не установлена. Его можно использовать у пациентов с сопутствующей патологией, исключающей резекцию, и у пациентов, которые отказываются от операции, хотя процедура сопряжена со значительными рисками. Также пациенты с излечимым внепеченочным заболеванием или опухоли которых были уменьшены химиотерапией, но не подлежат резекции, могут быть рассмотрены для абляционной терапии.
При радиочастотной абляции (РЧА) игла вводится в центр метастаза. Переменный ток вызывает тепло от трения, которое может достигать 100 ° C, вызывая коагуляционный некроз и необратимое повреждение тканей. Зона абляции различается по форме и размеру. Сосуды, расположенные рядом с удаленной тканью, мешают абляционной технике из-за «эффекта теплоотвода». Незначительные осложнения возникают у 2,4–12% пациентов; серьезные осложнения возникают до 5,6%; смертность составляет примерно 0.5% [85]. Лечение РЧА может обеспечить 3-летнюю выживаемость 25%. Было показано, что комбинация РЧА и системной химиотерапии обеспечивает 5-летнюю выживаемость 30% [86–88].
Лазерно-индуцированная термотерапия (ЛИТТ) заключается в локальном воздействии лазерного света на опухоль с помощью волокон кристалла кварца. Эффект нагрева разрушает ткань. Заболеваемость и смертность аналогичны РЧА. Местный контроль опухоли через 6 месяцев достигается примерно у 97% пациентов [85].
Для микроволновой абляции (MWA) микроволны используются для перемешивания молекул воды в ткани и выработки теплоты трения, что приводит к большим объемам коагуляционного некроза. Передача не ограничивается высыханием и обугливанием тканей, как в РЧА, что обеспечивает более высокую внутриопухолевую температуру, большую зону абляции, более короткое время лечения и более полное уничтожение опухоли. Сообщается, что пятилетняя выживаемость составляет 32%.
Сфокусированный ультразвук высокой интенсивности (HIFU) — это инновационный метод экстракорпорального лечения опухолей различных масс.Лечение проводится с помощью датчика, сфокусированного на линзе, который повышает температуру ткани до 60 ° C. Кроме того, механическое воздействие ультразвука высокой интенсивности способствует разрушению опухолевых клеток. Побочные эффекты кажутся незначительными [89].
В криотерапии используется жидкий азот или аргон для охлаждения опухолевой ткани до -180 ° C. Образование внутриклеточных кристаллов льда приводит к механическому разрушению интерстиция. Клетки на границе зоны абляции разрушаются за счет обезвоживания и окклюзии мелких сосудов.Повторяющиеся циклы замораживания и оттаивания используются для обеспечения необратимого повреждения клеток. Об осложнениях сообщается примерно в 30% всех случаев. Уровень смертности от 1,5% до 4%. «Растрескивание льда» в ткани печени наблюдается у 5–28% пациентов, получающих лечение. Сообщается о пятилетней и 10-летней выживаемости 44% и 19% соответственно [90]. Повышенная частота местных рецидивов и высокая частота осложнений привели к сокращению использования этого метода.
.
Роль карциноэмбрионального антигена в метастазах в печени и терапевтические подходы
Метастазирование — это очень сложный и последовательный процесс, при котором первичный рак распространяется на вторичные органические участки. Печень — хорошо известный орган с метастазами колоректального рака. Карциноэмбриональный антиген (CEA) экспрессируется в большинстве клеток рака желудочно-кишечного тракта, груди и легких. Сверхэкспрессия CEA тесно связана с метастазами в печень, которые являются основной причиной смерти от колоректального рака.CEA широко используется в качестве диагностического и прогностического онкомаркера у онкологических больных. Он влияет на многие стадии метастазирования в печень из клеток колоректального рака. CEA подавляет гибель циркулирующих раковых клеток. CEA также связывается с гетерогенным ядерным РНК-связывающим белком M4 (hnRNP M4), рецептором клеток Купфера, и активирует клетки Купфера для секреции различных цитокинов, которые изменяют микроокружение для выживания клеток колоректального рака в печени. CEA также активирует молекулы, связанные с клеточной адгезией.Тесная корреляция между CEA и раком стимулировала исследование многих подходов, нацеленных на CEA, в качестве противораковых терапевтических средств. Понимание подробных функций и механизмов CEA при метастазах в печени откроет большие возможности для улучшения противоопухолевых подходов к лечению колоректального рака. В этом отчете рассматривается роль CEA в метастазировании печени и противоопухолевые методы, нацеленные на CEA.
1. Введение
Колоректальный рак (CRC) — проблема здоровья в большинстве промышленно развитых стран мира.В глобальном масштабе это третья по частоте причина смерти от рака [1, 2]. По данным Всемирного фонда исследований рака (http://www.wcrf.org), в 2012 году было диагностировано около 1,4 миллиона новых случаев CRC. CRC диагностируется почти в 10% всех случаев рака, следующих за раком легких (13%) и рак груди (12%) и является третьим по распространенности раком у мужчин и вторым по частоте у женщин. Южная Корея имеет самый высокий уровень диагностированного CRC (45 человек на миллион), за ней следует Словакия (42.7 человек на миллион) и Венгрии (42,3 человека на миллион). Около 54% случаев приходится на более развитые страны. Самый высокий уровень заболеваемости CRC зарегистрирован в Океании и Европе, а самый низкий — в Африке и Азии. Уровень заболеваемости и диагностики КРР постепенно увеличивался из-за изменения привычек питания и увеличения распространенности ожирения и курения [3–5]. Основной причиной смерти, связанной с CRC, является метастазирование в печень, которое встречается у 20–70% пациентов в зависимости от прогрессирования рака [6].Лишь небольшая часть метастазов в печени поддается лечению современными терапевтическими методами.
Карциноэмбриональный антиген (CEA, также известный как CEACAM5 или CD66e) был обнаружен в злокачественных опухолях энтодермального эпителия желудочно-кишечного тракта и поджелудочной железы [7]. С момента открытия CEA почти пять десятилетий назад было обнаружено, что он сверхэкспрессируется в большинстве карцином человека [7, 8]. CEA имеет иммуноглобулиноподобные структурные характеристики и множество сайтов модификации гликозилирования [9].Тесная взаимосвязь между экспрессией CRC и CEA побудила использовать CEA в качестве онкомаркера [10, 11]. Измерение уровня CEA в сыворотке клинически полезно и надежно для диагностики CRC. Повышение уровня CEA является прогностическим индикатором состояния пациентов с CRC [12, 13]. При CRC основным местом метастазирования является печень [14]. Сверхэкспрессия CEA связана с метастазированием в печень [15, 16]. CEA также помогает на нескольких этапах метастазирования в печень, связанных с CRC [15, 16]. В частности, пять аминокислот (Pro-Glu-Leu-Pro-Lys, PELPK), существующие между доменами N и A1 CEA, имеют решающее значение при метастазировании в печень [17, 18].
РЭА влияет на метастазы в печени в основном в три этапа. На первом этапе CEA защищает циркулирующие раковые клетки толстой кишки от гибели в крови [19–21]. Когда клетки отделяются от тканей, индуцируется аноикис-опосредованная гибель клеток. Однако CEA может предотвратить гибель циркулирующих клеток за счет ингибирования аноикиса. На втором этапе СЕА связывается с гетерогенным ядерным РНК-связывающим белком M4 (hnRNP M4), рецепторным белком клетки Купфера [17, 22–23]. Клетки Купфера — это макрофаги, защищающие печень. После связывания СЕА с hnRNP M4 клетки Купфера изменяют микросреду печени в пользу клеток CRC, что увеличивает вероятность метастазирования [24–27].На третьем этапе CEA активирует молекулы клеточной адгезии для метастазирования [9].
Хотя множество экспериментальных и клинических данных подтвердили важную роль CEA в метастазировании в печень из клеток CRC, подробные механизмы CEA-опосредованного метастазирования в печень еще предстоит выяснить. Из-за тесной связи между CEA и метастазами в печени были предприняты попытки различных терапевтических подходов, которые могут блокировать функцию CEA. Этот обзор будет сосредоточен на текущих знаниях о CEA-опосредованной регуляции метастатических стадий в печени и нацеленных на CEA подходах к терапии рака.
2. CEA
CEA является членом суперсемейства белков иммуноглобулинов (Ig). Семейство генов CEA человека содержит 29 генов / псевдогенов, 18 из которых экспрессируются [28–30]. Некоторые гены из семейства генов CEA также экспрессируются у других млекопитающих, включая мышей, крыс и собак. Семейство генов CEA можно разделить на три группы на основе сходства последовательностей и функций: группа CEA-связанных молекул клеточной адгезии (CEACAM), группа специфичных для беременности гликопротеинов (PSG) и группа псевдогенов [31].
Группа CEACAM состоит из одного N-концевого домена и максимум шести внутренних доменов с дисульфидной связью. Группа содержит 12 белков (CEACAM1, 3–8, 16, 18–21) (рис. 1). Их N-концевой домен подобен домену распознавания антигена Ig. Другие домены группы CEACAM аналогичны доменам Ig C2-типа [31]. Внеклеточные домены группы CEACAM функционируют как гомофильные и гетерофильные молекулы или рецепторы клеточной адгезии [32–34]. Члены группы CEACAM могут действовать как димеры или олигомеры с другими мембранными молекулами, которые выполняют различные функции [9, 35, 36].CEACAM1, CEA (CEACAM5) и CEACAM6 изучались в отношении прогрессирования рака [32, 37, 38]. В отличие от CEA и CEACAM6, CEACAM1 содержит трансмембранный домен и имеет альтернативные варианты сплайсинга. Соотношение экспрессии длинной (CEACAM1-L) и короткой (CEACAM1-S) изоформы CEACAM1 связано с онкогенезом [39–42].
Метастазы в печени наиболее тесно связаны с РЭА. Молекулярная масса белка СЕА в нормальных клетках составляет 72 кДа. Однако CEA с молекулярной массой примерно от 180 до 200 кДа был обнаружен в линиях раковых клеток и у пациентов, что отражает многочисленные сайты модификации гликозилирования и различные паттерны гликозилирования в раковых клетках [8, 43].О других сайтах модификации, кроме гликозилирования, не сообщалось. CEA представляет собой связанный с гликофосфатидилинозитом (GPI-) заякоренный в мембране белок, который подвергается воздействию клеточной поверхности, обращенной к внеклеточному матриксу. Заякоренная в мембране область CEA может быть расщеплена фосфолипазой C и фосфолипазой D. Продукты расщепления растворимы и циркулируют по кровеносным сосудам [44]. Таким образом, CEA может присутствовать в виде секретируемой и закрепленной на клеточной поверхности форм.
CEA функционально связан с клеточным взаимодействием, клеточной адгезией, иммунным ответом, устойчивостью к аноикису и стимулированием метастазов в печень [9, 19, 45–47].Сверхэкспрессия CEA связана со многими типами рака, включая рак желудочно-кишечного тракта, органов дыхания и мочеполовой системы, а также рак груди [8]. CEA присутствует в апикальной мембране нормальной ткани, но сверхэкспрессируется в CRC и занимает всю поверхность клеточных мембран у пациентов с колоректальным раком [8, 48].
CEA — один из старейших и наиболее широко используемых онкомаркеров для мониторинга рецидива опухоли после хирургической резекции и прогноза. Небольшое повышение уровня CEA может быть предиктором рецидива после хирургического вмешательства по поводу CRC за год до появления клинических симптомов [49].Достижения в новых методах визуализации и нацеливания выявили другие опухолевые маркеры [10]. Однако CEA остается наиболее надежным и чувствительным биомаркером CRC. Уровень экспрессии CEA в сыворотке является важным фактором для определения стадии рака толстой кишки и принятия решений относительно будущих терапевтических стратегий [10, 11]. Уровни экспрессии белка CEA и мРНК в сыворотке крови являются полезными ранними маркерами рецидива у пациентов с раком поджелудочной железы и CRC. Может произойти повышение уровня CEA в сыворотке на 50–60% [50, 51].CEACAM1, CEACAM6 и NCA-90 также используются прогностически для прогнозирования рецидива рака груди, легких и колоректального рака [42, 52–55].
Связанный с CRC и сверхэкспрессированный CEA циркулирует по кровеносным сосудам и попадает в печень. Там он, вероятно, влияет на несколько этапов метастазирования в печень. CEA защищает от аноикис-опосредованной гибели клеток циркулирующих клеток CRC. CEA также может влиять на метастазы в легких. В этом обзоре основное внимание будет уделено роли СЕА в выживании клеток CRC в ткани печени и метастазировании в печень от колоректального рака.
3. CEA и метастазы в печень
Метастазирование — это многоступенчатый процесс, при котором злокачественные клетки распространяются из исходного участка опухолевого органа и колонизируют удаленные участки органа [56, 57]. Метастатический каскад включает очень сложные биологические процессы в клетке. Чтобы метастазировать, раковые клетки должны пережить строку
.
Результаты и возможные факторы прогноза
Предпосылки . Метастазы рака груди в печень — это гематогенное распространение первичной опухоли. Однако это может быть выражением изолированного повторения. Хирургическая резекция часто возможна, но спорно. Методы . Мы сообщаем о 29 пациентах женского пола, прооперированных по поводу изолированного метастаза рака груди в печень в течение шести лет. До операции все метастазы казались резектабельными. Метастазирование в печень было диагностировано через 55 месяцев (в среднем от 1 до 177) после первичной операции. Результаты . Полная резекция метастазов произведена у 21 пациента. Интраоперационная стадия не подтвердила предоперационные рентгенологические данные в 14 случаях, что в целом не привело к неоперабельности. Годовая выживаемость составила 86% у пациентов с резекцией и 37,5% у пациентов без резекции. Существенными прогностическими факторами были резекция R0, низкие T- и N-стадии, а также низкосортная гистопатология первичной опухоли, меньшее количество метастазов в печень и более длительный интервал времени между первичной операцией и возникновением метастазов в печень. Выводы . Полная резекция метастазов была возможна у трех четвертей пациентов. Некоторые из изученных факторов имеют прогностическое значение и, следовательно, могут повлиять на показания к резекции в будущем.
1. Введение
Метастазы — наиболее частая причина смерти онкологических больных [1]. Рак груди может распространяться через кровоток и вызывать метастазы в печени. Это может возникнуть одновременно или через десятилетия после первичной опухоли. Метастазы часто являются единственным признаком рецидива рака груди.Ссылки показывают, что 2–12% пациентов с раком груди имеют метастазы в печень [2, 3], которые, однако, в некоторых случаях могут быть изолированными. У пациентов с резектабельным колоректальным метастазом в печень хирургическая резекция является единственным методом лечения, если исключена дополнительная неоперабельная внепеченочная опухоль. В источниках 5-летняя выживаемость у этих пациентов составляет от 30 до 47% [4-7]. Поэтому хирургическое лечение рекомендуется в немецких рекомендациях S3 по лечению колоректального рака [8]. В отличие от этого данные об изолированном метастазе в печень у пациентов с раком груди не столь однозначны.
После публикации первоначального исследования резекции неколоректальных ненейроэндокринных метастазов в печень [9] последовало множество аналогичных исследований [10–15]. Общим знаменателем этих исследований является широкий спектр опухолевых образований, включая пациентов с раком груди. Рак груди, однако, составляет лишь небольшую часть исследованных опухолей и, как утверждается, имеет сравнительно хороший прогноз [10, 12–15]. Сообщается, что выживаемость эквивалентна таковой при колоректальных метастазах [9, 15].Таким образом, логическим следствием этого стало недавнее увеличение количества публикаций по удалению изолированных метастазов печени у пациентов с раком груди [16–30], в которых, однако, просто обобщались результаты серии случаев, тогда как вероятные прогностические факторы рассматривались лишь иногда.
Как показано в предыдущем исследовании, пациенты с резектабельными метастазами в печень от гинекологических онкологических заболеваний получают преимущество от хирургического лечения по сравнению с пациентами, у которых интраоперационно были неоперабельные метастазы [31].Целью настоящего исследования было доказать это преимущество выживаемости после резекции изолированного метастаза в печень только у пациентов с раком груди, а также выявить предоперационные и интраоперационные факторы, которые могут повлиять на выживаемость после резекции.
2. Пациенты и методы
Пациенты, получавшие лечение в течение шестилетнего периода (с февраля 2001 г. по январь 2007 г.), были взяты из предполагаемого банка данных (Access для Windows; версия 2002, © Microsoft Corporation, Редмонд, Вашингтон, США) ), включая всех пациентов, перенесших операцию на печени в Университетской больнице Саара.За оценочный период проведено 29 операций 24 пациентам с изолированными метастазами рака молочной железы в печень. Трем пациентам потребовалось два хирургических вмешательства, одному пациенту — три. Пациенты были в возрасте (от 38 до 77) лет и имели индекс массы тела (от 18,2 до 32,0) кг / м 2 2 на момент операции на печени. T- и N-олень
.

 Сбой в работе кишечника.
Сбой в работе кишечника. УЗИ. Метод, с помощью которого можно увидеть не только размеры патогенных образований, но и выявить их связь с крупными сосудами и протоками печени.
УЗИ. Метод, с помощью которого можно увидеть не только размеры патогенных образований, но и выявить их связь с крупными сосудами и протоками печени. наружная;
наружная;