развитие, возбудитель, симптомы и течение, лечение
Пневмоцистная пневмония (пневмоцистоз) – патологический процесс, развивающийся в легочной ткани под воздействием Pneumocystis на фоне выраженной дисфункции иммунной системы. Пневмоцисты долгое время занимали промежуточное положение между простейшими и грибами. Современные ученые доказали, что эти внеклеточные микробы благодаря своему особому строению и физиологическим свойствам больше напоминают дрожжеподобные грибы. Они широко распространены в природе и паразитируют исключительно в живых организмах. Pneumocystis jiroveci — единственный вид, патогенный и специфичный для человека. Животные не заражаются этой инфекцией. Микробы распространяются по воздуху, проникают в альвеолы и вызывают их воспаление, которое медленно прогрессирует и проявляется симптомами дыхательной недостаточности.
Заболевание развивается только у лиц с иммунодефицитом:
- ВИЧ-инфицированных,
- Пациентов со злокачественными опухолями, туберкулезом, циррозом печени,
- Больных, длительно принимавших иммунодепрессанты,
- Перенесших трансплантационные операции.

Пневмоцистная пневмония — оппортунистическая, СПИД – ассоциированная, ВИЧ-индикаторная болезнь. Микробы обнаруживаются в легких здоровых людей и являются представителя условно-патогенной микрофлоры. Они вызывают болезнь только при значительном снижении резистентности организма. В группу риска также входят недоношенные дети из-за незрелости иммунитета и недоразвитости дыхательного тракта.
Пневмоцистная пневмония – атипичная форма воспаления легочной ткани, отличающаяся непредсказуемым течением и жестоким отношением к своей «жертве». Она остается долгое время инфекцией-невидимкой и лишает многих больных единственного шанса на спасение. Патология не имеет сезонности, поскольку на ее возникновение влияет только функциональная активность иммунитета. Эпидемий данная инфекция также не вызывает — для нее характерна спорадическая заболеваемость. Риск заражения максимален у лиц с иммунодефицитом, находящихся в одном коллективе с носителями пневмоцист.
Диагностика пневмоцистоза включает инновационные методы идентификации возбудителя – лабораторные и инструментальные. Пневмоцисты обнаруживают в мокроте с помощью микроскопии и ПЦР. Больным выполняют рентгенологическое или томографическое исследование легких, позволяющее определить неспецифические признаки пневмонии. Проводят сцинтиграфию пораженного органа, спирографию, гистологический анализ биоптата легочной ткани. Лечение патологии этиотропное, направленное на уничтожение возбудителя. Для этого специалисты выбирают препараты без побочных эффектов – «Ко-тримоксазол», «Триметоприм», «Пентамидин», «Дапсон». Больных изолируют в отдельную палату, обеспечивают их индивидуальными средствами гигиены, назначают диету. Для ВИЧ-инфицированных лиц пневмоцистоз легких представляет смертельную опасность – при отсутствии лечения заболевание неизбежно заканчивается летальным исходом.
Пневмоцисты обнаруживают в мокроте с помощью микроскопии и ПЦР. Больным выполняют рентгенологическое или томографическое исследование легких, позволяющее определить неспецифические признаки пневмонии. Проводят сцинтиграфию пораженного органа, спирографию, гистологический анализ биоптата легочной ткани. Лечение патологии этиотропное, направленное на уничтожение возбудителя. Для этого специалисты выбирают препараты без побочных эффектов – «Ко-тримоксазол», «Триметоприм», «Пентамидин», «Дапсон». Больных изолируют в отдельную палату, обеспечивают их индивидуальными средствами гигиены, назначают диету. Для ВИЧ-инфицированных лиц пневмоцистоз легких представляет смертельную опасность – при отсутствии лечения заболевание неизбежно заканчивается летальным исходом.
Этиология и патогенез
Pneumocystis jiroveci
Возбудитель пневмоцистной пневмонии — простейший, одноклеточный микроорганизм рода Pneumocystis, который по генетическим и морфологическим признакам напоминает дрожжеподобные грибы. Этот условно-патогенный микроб живет в легочной ткани и является безвредным для здоровых людей. Он вызывает пневмонию только при наличии иммунодефицитных состояний. Pneumocystis jiroveci – относительно «молодой» паразит, впервые выделенный и подробно изученный в середине 19 века.
Этот условно-патогенный микроб живет в легочной ткани и является безвредным для здоровых людей. Он вызывает пневмонию только при наличии иммунодефицитных состояний. Pneumocystis jiroveci – относительно «молодой» паразит, впервые выделенный и подробно изученный в середине 19 века.
Пневмоцистная инфекция распространяется аэрогенным способом, который реализуется двумя основными путями — воздушно-капельным и воздушно-пылевым. Заражение происходит при общении с ВИЧ-инфицированными людьми. Известны случаи заражения плода от больной матери трансплантационным путем. Гемотрансфузионный путь встречается крайне редко. Воспаление развивается при иммунологической неполноценности. Оно проявляется признаками интоксикационного и респираторного синдромов.
Пневмоцистной пневмонией болеют лица с выраженным иммунодефицитом. У людей с нормальным иммунным статусом пневмоцисты, попав в организм, элиминируются специальными Т-клетками и не вызывают воспаления. Около 70% случаев патологии регистрируется у ВИЧ-инфицированного контингента. Именно поэтому такой диагноз относится к СПИД-ассоциированным, оппортунистическим заболеваниям. Pneumocystis jiroveci является патогенным микробом. Он проникает в легкие, персистирует годами в альвеолах, не причиняя никакого вреда. Заболевание развивается даже при незначительном ослаблении иммунитета. Группу риска составляют:
Именно поэтому такой диагноз относится к СПИД-ассоциированным, оппортунистическим заболеваниям. Pneumocystis jiroveci является патогенным микробом. Он проникает в легкие, персистирует годами в альвеолах, не причиняя никакого вреда. Заболевание развивается даже при незначительном ослаблении иммунитета. Группу риска составляют:
- Пожилые люди, проживающие в домах-интернатах,
- Дети организованных коллективов,
- Пациенты с гематологическими недугами,
- Онкобольные, получающие химиотерапию и лучевую терапию,
- ВИЧ-инфицированные,
- Лица с туберкулезом,
- Пациенты, получающие длительную гормонотерапию,
- Недоношенные новорожденные,
- Дети с тяжелыми врожденными патологиями,
- Больные с аутоиммунными расстройствами,
- Пациенты, перенесшие трансплантационные операции,
- Лица старше 65 лет, имеющие в анамнезе хронические заболевания в стадии декомпенсации,
- Больные с бронхолегочным острым недугом тяжелой формы,
- Заядлые курильщики,
- Люди, работающие в опасных условиях.

Перенесенная инфекция не оставляет стойкого иммунитета. В 10% случаев заболевание повторяется. У каждого четвертого ВИЧ-инфицированного диагностируются рецидивы – возникновение болезни в течение полугода после лечения. Если пневмония появляется позже, значит произошло реинфицирование – повторное заражение. Каждый последующий рецидив протекает тяжелее предыдущего. Подобное явление связывают с формированием устойчивой резистентности пневмоцист к лекарственным препаратам.
Патогенетические звенья пневмонии:
- Проникновение возбудителя в респираторный тракт,
- Его внедрение в просвет бронхиол и альвеол,
- Крепкое соединение микроба со стенкой альвеоцита,
- Его активное размножение путем деления,
- Развитие местного воспаления,
- Увеличение количества цист и слущивание альвеолярного эпителия,
- Паразитирование цист и нарушение целостности альвеол,
- Проникновение токсинов и продуктов обмена в кровь,
- Интоксикация,
- Воспалительная инфильтрация стенок альвеол,
- Гиперемия, отек и утолщение альвеолярных перегородок,
- Уменьшение просвета альвеол,
- Гиперпродукция экссудата,
- Заполнение легочных пузырьков жидкостью,
- Их обструкция,
- Нарушение газового обмена,
- Выключение из дыхания больших участков легких,
- Развитие гипоксемии и гиперкапнии,
- Выраженная дыхательная недостаточность.

Жизненный цикл Pneumocystis jirovecii
При отсутствии своевременной и адекватной терапии болезнь прогрессирует. Функционально активная ткань легких замещается фиброзными волокнами. Оксигенация крови снижается, нарастает гипоксия. Процесс становится необратимым. Самыми частыми осложнениями патологии являются эмфизема и пневмоторакс. Значительное ослабление иммунной защиты приводит к генерализации инфекции – возбудитель проникнет в костный мозг, почки, сердце и прочие жизненно важные органы. Выраженная нехватка кислорода может закончиться летальным исходом.
Пневмония, вызванная пневмоцистами, указывает на резкое снижение защитных свойств организма и требует неотложной медицинской помощи.
Симптоматика
Инкубационный период пневмоцистной инфекции длится недолго и в среднем составляет 7-10 суток.
Пневмоцистная пневмония протекает в три стадии: отечная – до десяти дней, ателектатическая – около четырех недель, эмфизематозная – различной продолжительности.
- Стадия отека характеризуется накоплением слизи в альвеолоцитах и проявляется симптомами астении: слабостью, вялостью, апатией, быстрой утомляемостью, снижением работоспособности, нарушением сна и аппетита, головной болью, одышкой при нагрузке, а также редким, постепенно усиливающимся, сухим кашлем. На рентгене признаки патологии отсутствуют. Аускультативно выявляется жесткое дыхание.
- Вторая стадия – развитие альвеолярно-капиллярного блока. Она начинается с подъема температуры тела до фебрильных значений, сильного, мучительного кашля с трудноотделяемой пенистой мокроты, синюшностью кожи, одышкой в покое и прочими признаками кардиопульмональной дисфункции. У пациентов появляется боль в груди, усиливающаяся при вдохе, кашле, движении. Она обусловлена раздражением рецепторов плевры и формированием сухого плеврита. Больные начинают дышать поверхностно, чтобы уменьшить боль. Это приводит к еще большему усилению дыхательной недостаточности.
 На КТ – ателектатические изменения легких. При аускультации выслушиваются различные хрипы.
На КТ – ателектатические изменения легких. При аускультации выслушиваются различные хрипы. - Эмфизематозная стадия возникает не всегда. Это период выздоровления или возникновения осложнений. Своевременное и эффективное лечение приводит к регрессу процесса. Слабый кашель проходит постепенно за 2-3 недели. Хрипы в легких со временем уменьшаются и исчезают. При неблагоприятном исходе патологии недуг рецидивирует, развивается пневмофиброз и эмфизема легких.
У ВИЧ-инфицированных заболевание протекает вяло и без характерных симптомов — одышки и кашля. Патологический процесс развивается годами. Пациенты жалуются на ухудшение общего состояния. При малейшем подозрении на инфекцию необходимо пройти флюорографию. Вторичное бактериальное инфицирование приводит к появлению лихорадки и продуктивного кашля. Температура тела повышается до 40 градусов и держится 2-3 месяца. Больные резко худеют. Их мучает сухой кашель, одышка и прочие признаки нарастающей дыхательной дисфункции.
У грудных детей заболевание имеет неблагоприятный прогноз при отсутствии раннего и должного лечения: от данной патологии умирает каждый третий ребенок. Заболевание протекает тяжело и сопровождается беспокойством, плохим сном, отказом от груди, метеоризмом, коклюшеподобным грубым лающим кашлем с выделением вязкой пенистой серой мокроты, частым плачем, осиплостью голоса, одышкой, втяжением межреберных промежутков, тахикардией, цианозом, чрезмерной возбудимостью или вялостью, апатичностью. Обычно дети испытывают ночные приступы удушья. Если медицинская помощь оказана вовремя и в полном объеме, ребенок полностью выздоравливает. Детский организм восстанавливается намного быстрее, чем взрослый.
Особенности пневмоцистного воспаления легких:
- Распространение инфильтратов от корней к периферии органа, представляющих собой скопления пораженных клеток с примесью крови и лимфы,
- Признаки пневмофиброза на рентгенограмме – уплотнение некоторых участков легочной ткани,
- «Ватные легкие» или «снежные хлопья» – легкие на снимке напоминают вату, вуаль или матовое стекло.

Специалисты выделяют три степени тяжести заболевания:
- Легкая – слабая интоксикация, отсутствие одышки, небольшие затемнения на рентгене,
- Средняя – умеренные признаки интоксикационного синдрома, тахикардия, одышка, кашель, ночной гипергидроз,
- Тяжелая – лихорадка, сердцебиение более 100 ударов в минуту, на рентгене массивная инфильтрация легких.
Пневмоцистная пневмония может протекать атипично и клинически напоминать банальную простуду или обструктивный бронхит. Если болезнь плохо поддается стандартной терапии, врач должен сделать соответствующие выводы. Воспаление легких, вызванное пневмоцистами, бывает абортивным — симптомы патологии резко исчезают и внезапно появляются вновь. Подобная ситуация также затрудняет диагностику. Опасность заболевания в том, что оно умело «прячется» до определенного момента. Симптомы остаются незамеченными, пока не наступит крайне тяжелая стадия болезни.
Осложнения пневмоцистной пневмонии делятся на легочные – эмфизема, абсцесс, пневмоторакс, плеврит, бронхообструкция, острая дыхательная недостаточность, а также внелегочные — диссеминация пневмоцист во внутренние органы: печень, головной мозг, селезенку, лимфатические узлы, костный мозг, почки, поджелудочную железу, а также развитие инфекционно-токсического шока и острого легочного сердца.
Диагностические мероприятия
Диагностика пневмоцистной пневмонии вызывает определенные трудности у специалистов, поскольку заболевание не имеет ярко выраженной и специфической симптоматики. Большинство клинических проявлений общие, не позволяющие выявить ранние стадии патологии.
Пневмоцистная пневмония диагностируется с помощью комплекса мероприятий, включающих сбор жалоб и анамнеза, изучение клинической картины, физикальное обследование, инструментальные методы, лабораторные анализы. Пульмонологи собирают анамнестические данные и выясняют, не был ли пациент в контакте с инфекционными больными, не относится ли он к группе риска по ВИЧ-инфекции, не принимал ли иммунодепрессанты. Результаты физикального осмотра: одышка, тахикардия, цианоз, гепатоспленомегалия, дыхательная недостаточность. Аускультативно – жесткое дыхание и хрипы, перкуторно – притупление перкуторного звука, появление коробочного оттенка.
Чтобы поставить диагноз и назначить лечение, необходимы результаты рентгенографического и томографического исследований, которые демонстрируют картину патологического процесса. Основной диагностический критерий — симптом «матового стекла». В крови определяется пониженная оксигенация, а в мокроте – предполагаемый патогенный микроорганизм. Для постановки окончательного диагноза также необходимы данные микроскопии биоптата легочной ткани — характерные кисты, отечность альвеолярных перегородок, скопление экссудата.
Основной диагностический критерий — симптом «матового стекла». В крови определяется пониженная оксигенация, а в мокроте – предполагаемый патогенный микроорганизм. Для постановки окончательного диагноза также необходимы данные микроскопии биоптата легочной ткани — характерные кисты, отечность альвеолярных перегородок, скопление экссудата.
Схема обследования пациента при подозрении на воспаление легких:
- Гемограмма – лейкоцитоз, лимфоцитоз, моноцитоз, анемия, увеличение СОЭ,
- ОАМ — патологические включения при интоксикации,
- БАК – повышение ЛДГ,
- Иммунофлуоресцентный или иммуногистохимический анализ – серологические исследования, выявляющие антитела к пневмоцистам в крови больного,
- Иммунограмма – снижение Т-лимфоцитов-хелперов до 200 в 1 мкл,
- ПЦР — обнаружение в мокроте генетического материала возбудителя,
- Микробиологическое исследование – выделение и идентификация пневмоцист до рода и вида,
- Микроскопия экссудата с окраской препарата по Романовскому-Гимзе – обнаружение цист в мокроте или бронхиальных смывах,
- Спирография – снижение показателей функции внешнего дыхания,
- Рентгенография органов грудной клетки – усиление легочного и сосудистого рисунка, очаговые тени, участки повышенной прозрачности, билатеральные инфильтраты, синдром «вуали» или «снежных хлопьев», расширение легочных корней,
- КТ – диффузные изменения в легочной ткани, эффект «матового стекла», кистозные образования, распад легочной ткани, наличие в ней полостей,
- Бронхоскопия – взятие биоптата альвеолярной ткани для выявления в ней пневмоцист.

Пневмоцистная пневмония – тяжелое заболевание, которое в большинстве случаев приводит к смерти больных. Быстрая и правильная постановка диагноза имеет особенно важное значение.
Как лечить недуг
Лечение пневмоцистной пневмонии — сложный процесс, поскольку возбудитель патологии устойчив к большинству противомикробных средств. Те медикаменты, которые уничтожают патогенов, обладают негативными побочными эффектами. Подобная терапия опасна для пациента, особенно ВИЧ-инфицированного человека или маленького ребенка.
Больных с пневмоцистной пневмонией госпитализируют в стационар, где проводят комплексное лечение. Болезнь отличается непредсказуемым течением, развитием грозных осложнений и высоким риском заражения окружающих. Лечение пневмоцистной пневмонии осуществляется специалистами в области пульмонологии, иммунологии, терапии. Оно направлено на купирование легочных симптомов и стимуляцию защитных свойств организма.
- Противопневмоцистные лекарства – «Триметоприм», «Сульфаметоксазол”, “Бисептол», «Дапсон”, “Атоваквон”, “Пентамидин”.
 Выбор дозы и длительности терапии зависит от степени выраженности дыхательной недостаточности, состояния больного, клинической картины, возраста и ряда других показателей. Все эти препараты токсичны для человека. Они могут спровоцировать подъем температуры, сыпь на коже, нейропатию, пищеварительную дисфункцию.
Выбор дозы и длительности терапии зависит от степени выраженности дыхательной недостаточности, состояния больного, клинической картины, возраста и ряда других показателей. Все эти препараты токсичны для человека. Они могут спровоцировать подъем температуры, сыпь на коже, нейропатию, пищеварительную дисфункцию. - Симптоматическое лечение заключается в назначении больным муколитических и отхаркивающих препаратов – “Амброксола», «АЦЦ», «Бромгексина», “Флюдитека», «Бронхикума». Лекарства разжижают мокроту и облегчают ее выведение из легких. При пневмоцистозе она особенно густая и вязкая.
- Бронхолитики, устраняющие бронхоспазм и улучшающие вентиляционную функцию легких – «Эуфиллин», «Беродуал», «Сальбутамол».
- Пневмоцистную пневмонию лечат кортикостероидами, обладающими мощным противовоспалительным и бронходилатирующим действием – «Преднизолон», «Медрол», «Дексаметазон».
- Антиретровирусная терапия проводится при ослаблении иммунной защиты. Чтобы предупредить еще большее угнетение иммунитета, необходимо использовать препараты, оказывающие влияние на сам ВИЧ и предотвращающие дальнейшее размножение пневмоцист.

- Детоксикационное лечение — внутривенное введение коллоидных и кристаллоидных растворов, способствующих выведению токсинов, улучшающих метаболизм и нормализующих газовый состав крови.
- В тяжелых случаях больным назначают оксигенотерапию – вдыхание кислорода через маску под давлением. Если человек находится без сознания, его подключают к аппарату ИВЛ.
Профилактика
Мероприятия, позволяющие предупредить развитие пневмоцистной пневмонии:
- Раннее выявление и изоляция больных лиц,
- Дезинфекция в очаге пневмоцистоза,
- Соблюдение личной гигиены,
- Исключение контактов с больными людьми,
- Профилактический прием «Ко-тримоксазола» лицами из группы риска,
- Полноценное витаминизированное питание,
- Ежедневная влажная уборка в помещении, проветривание и увлажнение воздуха,
- Регулярное прохождение медосмотров,
- Укрепление иммунитета,
- Закаливание организма,
- Занятия спортом,
- Борьба с вредными привычками.

Прогноз пневмоцистной пневмонии неутешительный. Он индивидуален для каждого пациента и во многом зависит от функционального состояния иммунной системы. При отсутствии грамотной терапии больные с ВИЧ-инфекцией погибают в 100% случаев. У недоношенных детей смертность доходит до 50%. Легочные осложнения уменьшают шансы на выздоровление. В большинстве случаев причиной летального исхода становится выраженная дыхательная недостаточность. Своевременная диагностика и эффективное лечение сводят показатели летальности к минимуму. При данном заболевании необходимо найти квалифицированного специалиста, регулярно у него наблюдаться и выполнять все его предписания.
Пневмоцистная пневмония – инфекционное заболевание, возникающее на фоне выраженного иммунодефицита и отличающееся высокой смертностью. Ослабленному организму сложно справиться с тяжелой патологией. Ранняя диагностика и качественное лечение повышают шансы больных на выздоровление, продлевают жизнь и улучшают ее качество.
Видео: лекция о пневмоцистной пневмонии
Видео: пневмоцистная пневмония у пациента без ВИЧ
Видео: пневмоцистная пневмония у больной артериитом Такаясу
Мнения, советы и обсуждение:
Пневмоцистоз (пневмоцистная пневмония) — симптомы болезни, профилактика и лечение Пневмоцистоза (пневмоцистной пневмонии), причины заболевания и его диагностика на EUROLAB
Что такое Пневмоцистоз (пневмоцистная пневмония) —
Пневмоцистоз — протозойное заболевание, обусловленное Pneumocystis carinii, которая является одной из самых частых причин развития пневмоний у лиц с ослабленным иммунитетом.
Что провоцирует / Причины Пневмоцистоза (пневмоцистной пневмонии):
Возбудитель пневмоцистоза — Pneumocystis carina (Delanoe M., Delanoe P., 1912) — одноклеточный микроорганизм. По морфологическим признакам и чувствительности к антипротозойным препаратам их длительное время относили к типу простейших. Постепенно у пневмоцист начали выявлять черты, характерные для грибов. Попытки отнести их к грибам или простейшим наталкивались на нечеткость систематических критериев. По некоторым показателям они близки к Protozoa: по морфологии, наличию мейоза, присутствию в составе клеточной оболочки холестерола (а не эргостерола, как у грибов, что делает их чувствительными к антипаразитарным препаратам и нечувствительными к противогрибковому средству амфотерицину В), невозможности их культивирования на питательных средах для грибов. С грибами их сближает то, что пневмоцисты содержат структуры, подобные аскоспорам у грибов, а также фитостеролы, которых лишены животные клетки.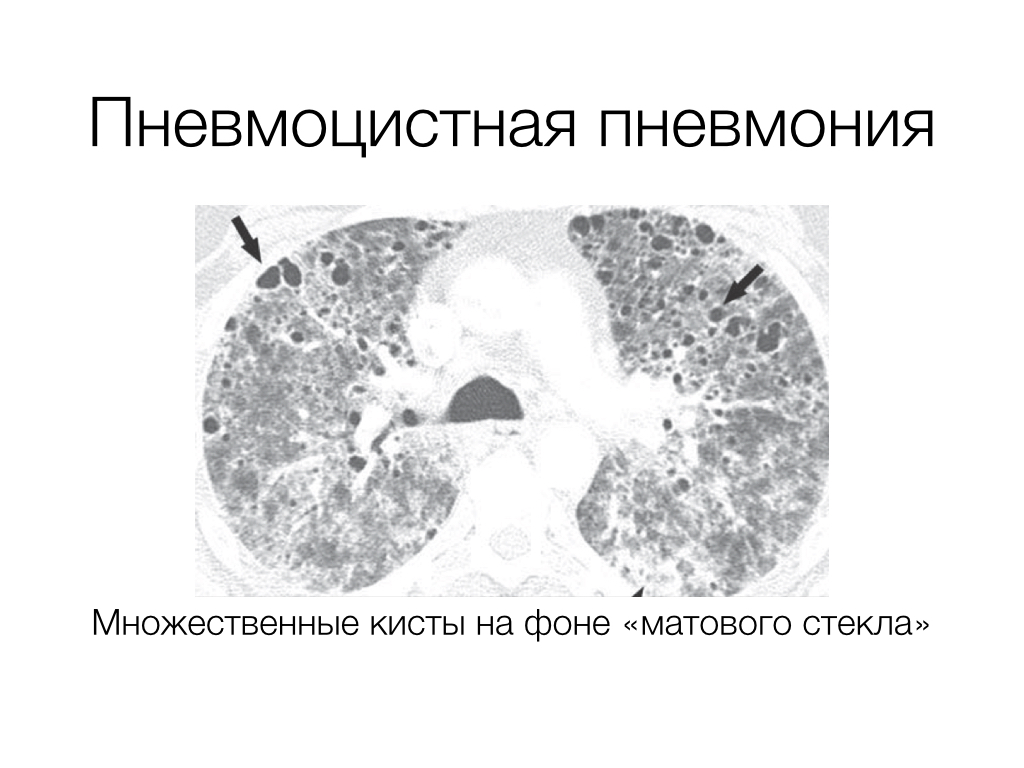
Метаболизм у P. carinii (синтез ароматических аминокислот, тимидина и др.) происходит, как у грибов; кроме того, у пневмоцист отсутствует спорогония, характерная для простейших. В 1988 г. Edman и Stringer, применив методы молекулярной генетики, показали, что последовательность нуклеотидов в т-РНК пневмоцист имеет высоую степень гомологии с последовательностью нуклеотидов т-РНК грибов, относящихся к дрожжам (Saccharomycetes serevisiae). Для сравненения — аналогичные последовательности изучались также у разных видов простейших: токсоплазм, плазмодиев, акантамеб и др. По генетическим признакам пневмоцисты были ближе всего к грибам. Но это грибы, которые имеют ряд черт, сближающих их с простейшими. Так, м-ДНК P. carinii содержит гены дегидрогеназы и цитохромоксидазы, которые на 60% подобны генам грибов и только на 20% генам простейших. Аналогичные свойства были установлены и у других видое грибов.
По последним данным пневмоцисты относят к грибам возможно, к актиномицетам или высшим грибам — аско- или базидомицетам. Одновременно некоторые исследователи считают P. carinii филогенетически древним возбудителем неопределенного систематического положения, который в процессе эволюции утратил характерные таксономические признаки (Т. В. Бейер, 1989 г.). Современный молекулярно-биологический и молекулярно-генетический анализ не может окончательно определить их видовую принадлежность. Для решения этого вопроса необходимо ультраструктурное исследование возбудителя, изучение его филогенеза и усовершенствование техники культивирования пневмоцист.
Одновременно некоторые исследователи считают P. carinii филогенетически древним возбудителем неопределенного систематического положения, который в процессе эволюции утратил характерные таксономические признаки (Т. В. Бейер, 1989 г.). Современный молекулярно-биологический и молекулярно-генетический анализ не может окончательно определить их видовую принадлежность. Для решения этого вопроса необходимо ультраструктурное исследование возбудителя, изучение его филогенеза и усовершенствование техники культивирования пневмоцист.
P. carinii — внеклеточный паразит, тропный к легочной ткани. В цикле развития пневмоцисты выделяют вегетативную форму (трофозоит), предцисту и цисту с внутрицистными тельцами.
Трофозоиты — клетки размером 1-8 мкм, покрытые тонкой оболочкой. Их форма разнообразная и мобильная (овальная, амебоподобная и др.). Она зависит от формы структур, к которым они прилегают. От поверхности трофозоита отходят микровыросты и длинные отростки в виде филоподий. За их счет пневмоцисты соединяются между собой и прикрепляются к клеткам хозяина. Ядро ограничено двумя мембранами. В цитоплазме выявляются митохондрии, свободные рибосомы, мелкие и крупные вакуоли, полисахариды, капли липидов. Иногда встречаются сдвоенные клетки, что может свидетельствовать о делении или копуляции. По данным электронно-микроскопических исследований, трофозоиты плотно прилегают к альвеолоцитам первого порядка. Филоподий могут углубляться в клетку легкого хозяина, не разрывая ее оболочку. Одновременно мембрана альвеолоцита может входить в тело трофозоита, не повреждая его. Физиологический контакт возбудителя с хозяином осуществляется через систему микропиноцитарных пузырьков.
За их счет пневмоцисты соединяются между собой и прикрепляются к клеткам хозяина. Ядро ограничено двумя мембранами. В цитоплазме выявляются митохондрии, свободные рибосомы, мелкие и крупные вакуоли, полисахариды, капли липидов. Иногда встречаются сдвоенные клетки, что может свидетельствовать о делении или копуляции. По данным электронно-микроскопических исследований, трофозоиты плотно прилегают к альвеолоцитам первого порядка. Филоподий могут углубляться в клетку легкого хозяина, не разрывая ее оболочку. Одновременно мембрана альвеолоцита может входить в тело трофозоита, не повреждая его. Физиологический контакт возбудителя с хозяином осуществляется через систему микропиноцитарных пузырьков.
Предцисты — овальные клетки диаметром 2-5 мкм, лишенные пелликулярных выростов. В них происходит деление ядер. Цисты P. carinii округлой или овальной формы размером 3,5 — 10 мкм, иногда до 30 мкм (рис. 20). Они покрыты плотной трехслойной оболочкой и внешней мембраной. В цитоплазме содержится от 1 до 8 внутрицистных телец, которые выходят в просвет альвеолы после разрыва оболочки цисты.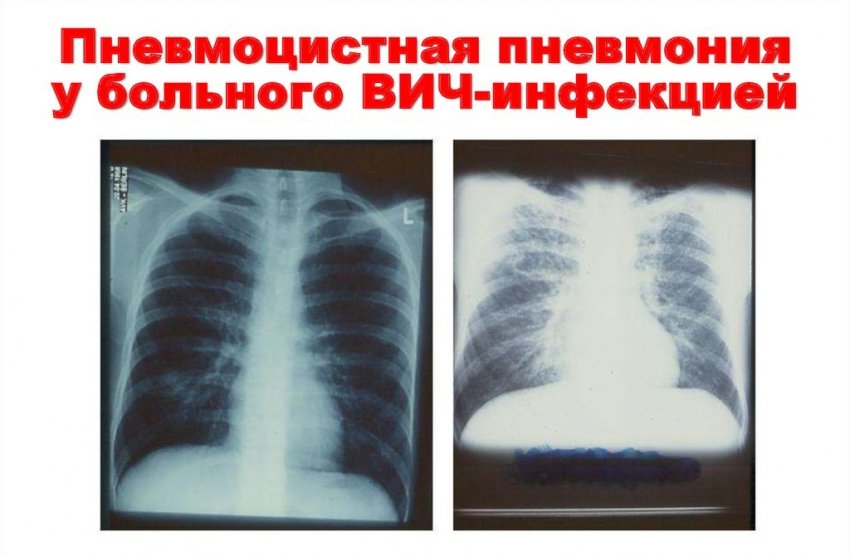 Пустые цисты имеют неправильную форму, чаще в виде полумесяца, иногда в них выявляются внутрицистные тельца. Размер последних 1-2 мкм. Пелликула внутрицистных телец вновь образуется после выхода из разрушенной цисты. Они становятся внеклеточными трофозоитами и начинают новый раунд жизненного цикла.
Пустые цисты имеют неправильную форму, чаще в виде полумесяца, иногда в них выявляются внутрицистные тельца. Размер последних 1-2 мкм. Пелликула внутрицистных телец вновь образуется после выхода из разрушенной цисты. Они становятся внеклеточными трофозоитами и начинают новый раунд жизненного цикла.
Среди больных СПИДом пневмоцистоз является одной из самых частых оппортунистических инфекций (более 80%) и при отсутствии лечения почти всегда приводит к летальному исходу. У других больных с ослабленным иммунитетом пневмоциста выделяется в 40% случаев. По данным экспериментов на животных инкубационный период длится от 4 до 8 нед.
Патогенез (что происходит?) во время Пневмоцистоза (пневмоцистной пневмонии):
Патогенез пневмоцистоза определяется биологическими свойствами возбудителя и состоянием иммунной системы хозяина. Пропагативные формы пневмоцист, которые до настоящего времени не описаны, минуют верхние дыхательные пути, достигают альвеол и начинают жизненный цикл в организме нового хозяина. Прикрепление трофозоитов к альвеолоцитам первого порядка опосредуется многими механизмами, в частности большим количеством поверхностных гликопротеинов у P. carinii, которые взаимодействуют с протеинами легочной ткани через маннозные рецепторы на клетках хозяина, особенно макрофагах. Поверхностные гликопротеины пневмоцист высоко иммунногенные. Прикрепление пневмоцист сопровождается пролиферацией возбудителя, его взаимодействием с сурфактантом, освобождением токсических метаболитов. Защиту организма хозяина от P. carinii осуществляют Т-лимфоциты, альвеолярные макрофаги, специфические AT. Взаимодействие микро- и макроорганизма остается на субклиническом уровне, пока иммунная система не нарушена. Компроментация иммунной системы стимулирует рост численности пневмоцист.
Прикрепление трофозоитов к альвеолоцитам первого порядка опосредуется многими механизмами, в частности большим количеством поверхностных гликопротеинов у P. carinii, которые взаимодействуют с протеинами легочной ткани через маннозные рецепторы на клетках хозяина, особенно макрофагах. Поверхностные гликопротеины пневмоцист высоко иммунногенные. Прикрепление пневмоцист сопровождается пролиферацией возбудителя, его взаимодействием с сурфактантом, освобождением токсических метаболитов. Защиту организма хозяина от P. carinii осуществляют Т-лимфоциты, альвеолярные макрофаги, специфические AT. Взаимодействие микро- и макроорганизма остается на субклиническом уровне, пока иммунная система не нарушена. Компроментация иммунной системы стимулирует рост численности пневмоцист.
У здорового человека P. carinii размножаются медленно, однако болезнь резко активизируется при подавлении иммунной реакции и за время инкубационного периода количество пневмоцист в легких увеличивается от 10.000 до более чем 1. 000.000.000 клеток. Они постепенно заполняют альвеолярное пространство. Это ведет к появлению пенистого, «сотовидного» экссудата, повреждению мембраны альвеолярных лейкоцитов, увеличению их проницаемости, разрушению альвеолоцитов первого порядка. Плотное прилегание пневмоцист к альвеолоцитам приводит к сокращению дыхательной поверхности легких. Механическое повреждение интерстициальной ткани легкого возбудителем и воспалительными клетками, инфильтрация стенки альвеол мононуклеарами, а клеток интерстиция — плазматическими клетками приводят к утолщению альвеолярной стенки в 5 — 20 раз, вследствие чего развивается альвеолярно-капиллярный блок.
000.000.000 клеток. Они постепенно заполняют альвеолярное пространство. Это ведет к появлению пенистого, «сотовидного» экссудата, повреждению мембраны альвеолярных лейкоцитов, увеличению их проницаемости, разрушению альвеолоцитов первого порядка. Плотное прилегание пневмоцист к альвеолоцитам приводит к сокращению дыхательной поверхности легких. Механическое повреждение интерстициальной ткани легкого возбудителем и воспалительными клетками, инфильтрация стенки альвеол мононуклеарами, а клеток интерстиция — плазматическими клетками приводят к утолщению альвеолярной стенки в 5 — 20 раз, вследствие чего развивается альвеолярно-капиллярный блок.
При СПИДе число паразитов в альвеолах и бронхах настолько большое, что нарушается альвеолярная вентиляция, и больной умирает от нарастающей легочной недостаточности. Разрушение альвеолярно-капиллярной мембраны может приводить к диссеминации пневмоцист с основного места локализации.
На гистологических срезах легких, пораженных пневмоцистами, возникает картина, характерная только для пневмоцистоза. Расширенные бронхиолы, альвеолы и мелкие бронхи заполнены эозинофильной пенистой массой. Альвеолярный эпителий, контактирующий с возбудителем, гипертрофирован, стенки альвеол утолщены за счет расширения капилляров и инфильтрации лимфоидно-гистиоцитарными элементами. Вокруг сосудов наблюдаются обильные скопления плазмоцитов. На стенках бронхов и альвеол видны отдельные круглые формы и пласты пневмоцист, стелящиеся по стенкам альвеол. Выявляются разорванные цисты P. carinii с выбросом в окружающее пространство внутрицистных телец, которые наращивают цитоплазму и превращаются в трофозоиты, а потом дозревают до цист. Гистологическая картина легких напоминает альвеолярный липопротеиноз с явлениями экссудации, лейкоцитоза и сетчатого склероза. Заполненные пенистой массой группы альвеол и альвеолярные ходы чередуются с участками компресионного ателектаза и эмфиземы.
Расширенные бронхиолы, альвеолы и мелкие бронхи заполнены эозинофильной пенистой массой. Альвеолярный эпителий, контактирующий с возбудителем, гипертрофирован, стенки альвеол утолщены за счет расширения капилляров и инфильтрации лимфоидно-гистиоцитарными элементами. Вокруг сосудов наблюдаются обильные скопления плазмоцитов. На стенках бронхов и альвеол видны отдельные круглые формы и пласты пневмоцист, стелящиеся по стенкам альвеол. Выявляются разорванные цисты P. carinii с выбросом в окружающее пространство внутрицистных телец, которые наращивают цитоплазму и превращаются в трофозоиты, а потом дозревают до цист. Гистологическая картина легких напоминает альвеолярный липопротеиноз с явлениями экссудации, лейкоцитоза и сетчатого склероза. Заполненные пенистой массой группы альвеол и альвеолярные ходы чередуются с участками компресионного ателектаза и эмфиземы.
Для построения собственной клеточной оболочки P. carinii использует фосфолипиды (ненасыщенный фосфатидилхолин) сурфактанта хозяина. Это приводит к общему повреждению сурфактантного обмена: дисбалансу в уровнях сурфактантных фосфолипидов и протеинов, гиперсекреции сурфактанта. Выраженное размножение и созревание P. carinii прямо коррелирует с пиком активности сурфактантной системы. Гиперпродукция сурфактанта на фоне развивающейся дисфункции альвеолярных макрофагов приводит к заполнению альвеол относительно гомогенной пенистой массой. Механическое разрушение и инактивация сурфактанта белками экссудата усугубляют гипоксическое состояние тканей, активируют фиброзирование межальвеолярных перегородок. Происходит снижение секреторной функции альвеолоцитов второго порядка и возрастание их пролиферативной активности. Плоский альвеолярный эпителий замещается кубическим. У больных СПИДом размножение в альвеолах P.carinii часто происходит в составе смешанной инфекции (бактериальная флора, грибы). Это создает патоморфологическую картину пневмоцистоза.
Это приводит к общему повреждению сурфактантного обмена: дисбалансу в уровнях сурфактантных фосфолипидов и протеинов, гиперсекреции сурфактанта. Выраженное размножение и созревание P. carinii прямо коррелирует с пиком активности сурфактантной системы. Гиперпродукция сурфактанта на фоне развивающейся дисфункции альвеолярных макрофагов приводит к заполнению альвеол относительно гомогенной пенистой массой. Механическое разрушение и инактивация сурфактанта белками экссудата усугубляют гипоксическое состояние тканей, активируют фиброзирование межальвеолярных перегородок. Происходит снижение секреторной функции альвеолоцитов второго порядка и возрастание их пролиферативной активности. Плоский альвеолярный эпителий замещается кубическим. У больных СПИДом размножение в альвеолах P.carinii часто происходит в составе смешанной инфекции (бактериальная флора, грибы). Это создает патоморфологическую картину пневмоцистоза.
После проведенного лечения и выздоровления полного восстановления сурфактантной системы легких не происходит. Это является причиной колонизации дыхательной системы больных СПИДом нозокомиальными, стойкими к антибиотикам широкого спектра действия штаммами микроорганизмов. Поэтому рецидивирующие пневмонии у больных СПИДом — нередкое явление.
Это является причиной колонизации дыхательной системы больных СПИДом нозокомиальными, стойкими к антибиотикам широкого спектра действия штаммами микроорганизмов. Поэтому рецидивирующие пневмонии у больных СПИДом — нередкое явление.
Показано, что у ВИЧ-негативных больных с хроническими неспецифическими заболеваниями легких также существует тенденция к увеличению степени обсемененности дыхательных путей микрофлорой. При нарастании числа цист P. carinii в мокроте расширяется видовой состав микрофлоры и увеличивается частота выделения микробных ассоциаций из легких (Ю. И. Фещенко и др., 2003 г.). Наши данные также свидетельствуют о том что у больных с острыми и хроническими неспецифическим!/ заболеваниями легких, инфицированных P. carinii, микробные ассоциации, в состав которых входит кокковая флора (кокки диплококки, стрептококки), в большом количестве выявляются в 77% случаев, в незначительном и умеренном количестве — i 15%. У пациентов без пневмоцистоза — соответственно у 65% и 28%. Эти данные могут быть свидетельством роли пневмоциа как компонента микробиоценоза легких в патологии дыхательной системы.
Эти данные могут быть свидетельством роли пневмоциа как компонента микробиоценоза легких в патологии дыхательной системы.
При тяжелых формах иммунодефицита у ВИЧ-инфицированных больных возможна генерализация пневмоцистоза с раз витием диссеминированной формы. У таких лиц P. carinii выявляют в костном мозге, сердце, почках, червеобразном отростке, поражениях кожи, суставов, органа слуха. В некоторых случаях внелегочного пневмоцистоза у больных отсутствует патология легких или симптомы поражения пневмоцистой внутренних органов опережают патологию легких, которая развивается позже. Это может свидетельствовать о персистенции определенных форм P. carinii в ретикуло-эндотелиальной системе.
Пневмоцистная пневмония развивается у лиц с подавленным клеточным иммунитетом, а также при нарушениях гуморального иммунитета. Экспериментальную модель пневмоцистной пневмонией получают длительным введением лабораторным животным (крысам, кроликам, хорькам и др.) кортикостероидов. Наиважнейшее значение в патогенезе пневмоцистоза придается снижению Т-лимфоцитов-хелперов (CD4+).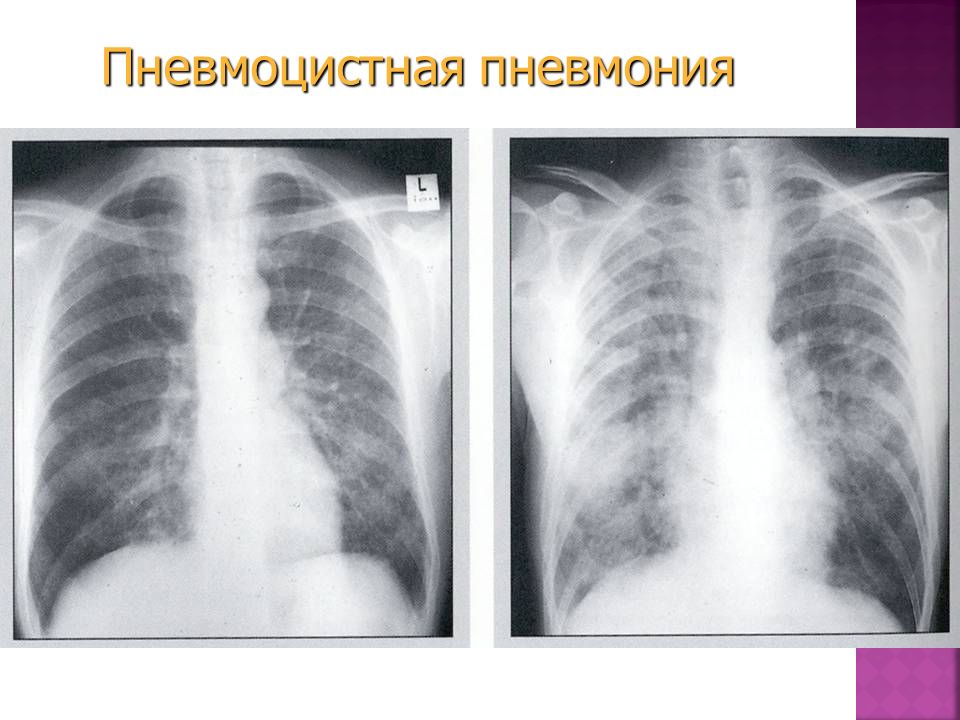 Более 90% всех случаев пневмоцистной пневмониии развивается при снижении CD4+ в периферической крови менее 200 клеток в 1 мкл (при норме 640 — 1360 клеток в 1 мкл). Значительно угнетена также функция Т-лимфоцитов-киллеров (СД8).
Более 90% всех случаев пневмоцистной пневмониии развивается при снижении CD4+ в периферической крови менее 200 клеток в 1 мкл (при норме 640 — 1360 клеток в 1 мкл). Значительно угнетена также функция Т-лимфоцитов-киллеров (СД8).
Отмечена также важность гуморального иммунитета в защите организма от пневмоцистоза. Кортикостероиды опосредованно снижают фагоцитарную и цитолитическую активность альвеолярных магкрофагов, повреждая Fc-рецептор на их мембране. Макрофаги переваривают, разрушают и убивают пневмоцисты, реализуя цитокиновый механизм и включая реактивные оксиданты.
У недоношенных детей с белковой недостаточностью нарушается специфический синтез иммуноглобулинов и развивается пневмоцистная пневмония, что также свидетельствует о роли гуморального иммунитета в патогенезе болезни. В пенистом экссудате больных с пневмоцистной пневмонией выявляется комплекс специфических IgG, IgM, IgA. В сыворотке периферической крови не наблюдается общего дефицита антител, но выявляется дефицит некоторых изотипов антипневмоцистных антител. При назначении экспериментальным животным гипериммунной сыворотки отмечается положительный терапевтический эффект. Прекращение введения кортикостероидов лабораторным животным ведет к обратному развитию болезни.
При назначении экспериментальным животным гипериммунной сыворотки отмечается положительный терапевтический эффект. Прекращение введения кортикостероидов лабораторным животным ведет к обратному развитию болезни.
Симптомы Пневмоцистоза (пневмоцистной пневмонии):
Пневмоцистоз у детей развивается обычно на 4-6-м месяце жизни (недоношенные, больные рахитом, гипотрофией, поражениями ЦНС) и в более старших возрастных группах (при гемобластозе, злокачественных новообразованиях, СПИДе). Заболевание начинается постепенно — у ребенка снижается аппетит, прекращается нарастание массы тела, появляются бледность и цианоз носогубного треугольника, легкое покашливание. Нормальная в начале заболевания температура сменяется субфебрильной с подъемами до фебрильной. В легких появляются непостоянные мелко- и среднепузырчатые хрипы. Появляются одышка (до 50-70 в 1 мин), цианоз, кашель коклюшеобразного характера. Нередко кашель сопровождается выделением пенистой мокроты, в которой могут обнаруживаться пневмоцисты. Рентгенологически регистрируются очаговые тени разной величины и плотности, дающие картину «облаковидного» легкого. В крови обнаруживается лейкоцитоз, умеренная эозинофилия и увеличение СОЭ.
Рентгенологически регистрируются очаговые тени разной величины и плотности, дающие картину «облаковидного» легкого. В крови обнаруживается лейкоцитоз, умеренная эозинофилия и увеличение СОЭ.
Иногда пневмоцистоз у детей протекает под маской острого ларингита, обструктивного бронхита или бронхиолита. В ряде случаев наступает летальный исход при клинической картине отека легких.
У взрослых пневмоцистоз развивается у лиц, получающих иммуно-супрессивную терапию (обычно — кортикостероиды), и у больных СПИДом. При медикаментозной иммуносупрессии заболевание часто манифестируется на фоне снижения дозы кортикостероидов. Продромальный период длится обычно 1-2 нед, а у больных СПИДом он достигает 10 нед. Постепенно появляется субфебрилитет, умеренная одышка при физической нагрузке, сухой кашель, боли в грудной клетке. Через 1-2 нед могут появиться лихорадка, одышка в покое, усиливается сухой кашель (продуктивный кашель отмечается редко). При осмотре обнаруживается тахипноэ, тахикардия, цианоз. В легких часто выслушиваются сухие, реже — влажные хрипы. Количество лейкоцитов обычно зависит от фонового заболевания. При газовом анализе крови обнаруживают прогрессирующую гипоксемию, повышение альвеолярно-артериального кислородного градиента и респираторный алкалоз.
В легких часто выслушиваются сухие, реже — влажные хрипы. Количество лейкоцитов обычно зависит от фонового заболевания. При газовом анализе крови обнаруживают прогрессирующую гипоксемию, повышение альвеолярно-артериального кислородного градиента и респираторный алкалоз.
Пневмоцистная пневмония при СПИДе обычно характеризуется вялым хроническим течением. Первоначально аускультативная симптоматика не выявляется, рентгенологическая картина тоже может оставаться без патологических изменений. По мере прогрессирования заболевания появляются двухсторонние прикорневые инфильтраты, трансформирующиеся затем либо в фокусные, либо интерстициальные изменения. Изредка обнаруживаются солитарные узелки, которые могут кавернизироваться с образованием обширной центральной полости. Причиной абсцедирования, вероятно, является присоединение бактериальных и микозных инфекций.
Осложнения. Ведущим осложнением, чаще всего обусловливающим летальность, является дыхательная недостаточность, связанная с резким нарушением вентиляции и газообмена. Возможны также такие осложнения, как абсцессы, спонтанный пневмоторакс (на фоне образования мелких легочных кист), экссудативный плеврит.
Диагностика Пневмоцистоза (пневмоцистной пневмонии):
Учитывая, что клинические проявления пневмоцистной пневмонии малоспецифичны, а развернутая клинико-рентгенологическая картина появляется значительно отсроченно от начала заболевания (особенно при СПИДе), ранняя этиологическая диагностика приобретает огромное значение, так как позволяет своевременно начать соответствующее лечение.
Пневмоцисты в мокроте больных обнаруживают крайне редко, а способов культивирования пневмоцист человека пока еще не разработано. Серологические методы признаны весьма ненадежными. По этим причинам основной возможностью идентификации возбудителя является гистологическое исследование жидкости бронхоальвеолярного лаважа (ЖБАЛ) и трансбронхиальных биоптатов, осуществляемое при помощи фибробронхоскопии. Открытая биопсия легких в настоящее время применяется все реже.
Дифференциальная диагностика на ранних этапах заболевания проводится обычно с другими интерстициальными пневмониями. Одна
Пневмоцистная пневмония. Прогноз. Эпидемиология. Распространенность. Профилактика пневмоцистной пневмонии. | EUROLAB
Прогноз пневмоцистной пневмонии.
Среди недоношенных детей смертность от пневмоцистной пневмонии составляет 50%, но рецидивов практически не наблюдается. При пневмоцистной пневмонии у взрослых, не страдающих СПИДом, прогноз более благоприятный и определяется тяжестью фонового заболевания. У больных СПИДом при отсутствии лечения пневмоцистной пневмонии всегда приводит к летальному исходу. При поздней диагностике летальность при первичном эпизоде — около 40%, своевременно начатое лечение позволяет снизить летальность до 25%. Однако даже через несколько месяцев возможны рецидивы (от 10 до 30%) пневмоцистной пневмонии. Лечение рецидивов проходит значительно труднее, так как у 50 — 80% больных развиваются выраженные побочные реакции на бактрим и пентамидин, и летальность увеличивается уже до 60%.
Эпидемиология пневмоцистной пневмонии.
Пневмоцисты широко распространены среди многих видов диких и домашних животных. Их выявляют у мышей, крыс, хорьков, кроликов, крупного рогатого скота, свиней, собак и др. Спонтанное носительство P. carinii считается обычным явлением. По морфологическим признакам пневмоцисты от разных видов животных почти идентичны. Иммунологические, цитохимические и генетические методы исследований последних лет свидетельствуют об отличиях между P. carinii, выделенными от различных видов животных. Так, антитела к P. carinii, которые образуются у одного вида животных, перекрестно не реагируют с антигенами P. carinii других видов животных. Хромосомы пневмоцист от человека, мышей, хорьков сходны по размерам, но имеют индивидуальный кариотип. В экспериментальных условиях попытки передачи пневмоцист от человека и различных видов животных другим видам животных, даже иммунодефицитным, закончились неудачей. Это свидетельствует о строгой видовой специфичности P. carinii. Циркуляция возбудителя среди людей происходит без дополнительных хозяев.
Пневмоцистоз человека — антропоноз. Источник инфекции — человек.
Основной механизм передачи — капельный. Главное место локализации патологического процесса при пневмоцистозе — дыхательные органы. При кашле, который является наиболее частым симптомом болезней органов дыхания, образуется мелкодисперсный аэрозоль. Его частицы не оседают, а находятся во взвешенном состоянии. Заражение пневмоцистами происходит при вдыхании воздуха, контаминированного возбудителем. Выявить цисты в воздухе и других объектах внешней среды до настоящего времени не удавалось. Только с помощью молекулярно-биологических исследований в образцах воздуха помещений, где находились больные пневмоцистозом, были обнаружены генетические носители (фрагменты ДНК) пневмоцист.
Описана возможность вертикальной передачи пневмоцистоза от зараженных пневмоцистами ВИЧ-инфицированных женщин плоду. Этот путь реализуется редко. Зарегистрированы единичные случаи мертворождений, когда в аутопсийном материале из легких выявляли макрофаги, содержащие цисты P. carinii. При этом в локусах некроза плаценты также обнаруживали P. carinii. Развитие пневмоцистной пневмонии у детей первого года жизни, которые родились от ВИЧ-инфицированных матерей с пневмоцистозом, также может свидетельствовать о внутриутробном заражении младенцев.
При тяжелых формах иммунодефицита у ВИЧ-инфицированных больных циркуляция пневмоцист может происходить в кровеносной системе. Имеются указания на возможность выявления фрагментов ДНК пневмоцист в крови и внутренних органах вне иммуносупрессии. Учитывая возможность пребывания возбудителя в кровеносной системе, фактором передачи, очевидно, может быть кровь. Пропагативная форма, обеспечивающая персистенцию P. carinii в организме хозяина и сохранение в окружающей среде, морфологически не описана.
Исследования показали, что число цист P. carinii у отдельных больных с неспецифическими заболеваниями легких колеблется в широких пределах — от 5 до 1500 цист в 1 мл мокроты, а по средним показателям в отдельных контингентах — от 140 ± 45 до 235 ± 30. Из-за невозможности выделения возбудителя из внешней среды сроки выживаемости пневмоцист в воздухе, других объектах не определены.
Существует возможность возникновения вспышек пневмоцистоза. В литературе описаны вспышки в стационарах для детей раннего возраста, в детском туберкулезном санатории, домах ребенка, школах, интернатах. Они характеризовались растянутостью во времени (1,5 — 2,5 мес. с момента выявления первых случаев), втягиванием в эпидемический процесс большого количества больных (34 — 84%) и медицинского персонала (38 — 75%), полиморфизмом клинических проявлений пневмоцистоза, преобладанием среди зараженных пневмоцистами лиц носителей, а у больных с клиническими проявлениями — регистрацией случаев пневмоцистной пневмонии, особенно у детей раннего возраста.
Исследования, проведенные среди ВИЧ-отрицательных и ВИЧ-положительных больных с неспецифическими заболеваниями легких и медицинских работников отделенния СПИДа и пульмонологических отделений, показали, что зараженность P. carinii больных колеблется от 28% до 84%, количество выделяемых цист в мокроте — от 155 до 330 в 1 мл. Зараженность P. carinii медицинских работников, обследованных по клиническим показаниям (наличие кашля, мокроты, патологии дыхательных путей), — 100%, число выделяемых пневмоцист — 165 цист в 1 мл мокроты. Учитывая частое и длительное пребывание больных в стационаре, назначение им инвазивных методов исследования (бронхо-, трахеоскопия), переуплотненность палат и отсутствие боксированных помещений, а также значительную зараженность P. carinii медицинского персонала, можно предположить возможность легкой передачи пневмоцистоза в отделениях. Его можно рассматривать как внутрибольничную инфекцию с капельным механизмом передачи.
Распространенность пневмоцистной пневмонии.
Пневмоциста является условно-патогенным возбудителем, ее патогенные свойства проявляются только при угнетении естественной резистентности организма, в частности, при иммуннодефиците разного происхождения.
По данным литературы, пневмоцистная пневмония чаще всего регистрируется у детей раннего возраста, несовершенство иммунитета у которых обусловлено недоношенностью, дефектами иммунной системы (гипо- или агаммаглобулинемия), проявлениями рахита, пороками сердца, цитомегаловирусной инфекцией. Большинство исследователей связывают пневмоцистоз с детским возрастом. P. carinii выявляли у 10 — 40% обследованных детей в странах Европы и у 7% — в странах Африки. Однако допускается, что действительная зараженность пневмоцистами выше. По данным серологических исследований (РИФ, ИФА, метод встречного электрофореза), в США из 120 здоровых детей в возрасте до 1 года 33% имели AT к P. carinii, в возрасте 3-4 лет — 83%. В Дании исследование в РИФ сывороток 300 детей выявило AT к P. carinii у 20% детей до 1 года, у 33% — в возрасте 1 года, у 58% -2 лет, у 75% — 3 — 5 лет, и у 71% — 11 — 15 лет.
Основными группами риска развития пневмоцистной пневмонии являются взрослые и дети с системными заболеваниями крови и соединительной ткани, онкологические больные, реципиенты трансплантированных органов, пациенты с другими болезнями, для лечения которых используют иммуносупрессивную терапию (кортикостероиды, цитостатики, облучение).
Частота развития пневмоцистной пневмонии в группе больных с гемобластозами составляет в среднем 2%. Она зависит от характера заболевания (при лимфопролиферативных процессах — до 9%), от вида препаратов, их количества, дозы, длительности терапии. После трансплантации костного мозга пневмоцистная пневмония развивалась у 0,7 — 15% пациентов. У взрослых с неоплазмами на аутопсии пневмоцистоз выявлен у 5% умерших. К группам риска заражения пневмоцистами и развития пневмоцистной пневмонии относятся лица пожилого возраста, больные диабетом.
Имеются сообщения о выявлении пневмоцист у больных с неспецифическими заболеваниями легких. По некоторым данным литературы (микроскопическое исследование свободно отходящей мокроты), зараженность P. carinii этой группы больных составляет в среднем 56% с колебаниями среди отдельных контингентов от 28% до 84%. Зараженность P. carinii больных с острыми и хроническими НЗЛ в среднем составляет 56 ± 2% от числа обследованных лиц, число цист в 1 мл мокроты — 175 ± 20. Установлено, что пол и возраст не влияют на уровень пораженности пневмоцистозом больных с НЗЛ. Отмечено достоверное повышение экстенсивных показателей пневмоцистоза: в холодный сезон года; при наличии в анамнезе жизни производственной вредности (контакт с физическими и химическими аэро
Пневмоцистная пневмония. Этиология. Патогенез пневмоцистоза. Клиника. Диагностика. | EUROLAB
Пневмоцистоз — оппортунистическая инфекция с преимущественным поражением легких, у больных с иммунодефицитом способная к генерализации. Относится к числу наиболее распространенных СПИД-индикаторных болезней.
Этиология.
Возбудитель пневмоцистоза — Pneumocystis carina (Delanoe M., Delanoe P., 1912) — одноклеточный микроорганизм. По морфологическим признакам и чувствительности к антипротозойным препаратам их длительное время относили к типу простейших. Постепенно у пневмоцист начали выявлять черты, характерные для грибов. Попытки отнести их к грибам или простейшим наталкивались на нечеткость систематических критериев. По некоторым показателям они близки к Protozoa: по морфологии, наличию мейоза, присутствию в составе клеточной оболочки холестерола (а не эргостерола, как у грибов, что делает их чувствительными к антипаразитарным препаратам и нечувствительными к противогрибковому средству амфотерицину В), невозможности их культивирования на питательных средах для грибов. С грибами их сближает то, что пневмоцисты содержат структуры, подобные аскоспорам у грибов, а также фитостеролы, которых лишены животные клетки.
Метаболизм у P. carinii (синтез ароматических аминокислот, тимидина и др.) происходит, как у грибов; кроме того, у пневмоцист отсутствует спорогония, характерная для простейших. В 1988 г. Edman и Stringer, применив методы молекулярной генетики, показали, что последовательность нуклеотидов в т-РНК пневмоцист имеет высоую степень гомологии с последовательностью нуклеотидов т-РНК грибов, относящихся к дрожжам (Saccharomycetes serevisiae). Для сравненения — аналогичные последовательности изучались также у разных видов простейших: токсоплазм, плазмодиев, акантамеб и др. По генетическим признакам пневмоцисты были ближе всего к грибам. Но это грибы, которые имеют ряд черт, сближающих их с простейшими. Так, м-ДНК P. carinii содержит гены дегидрогеназы и цитохромоксидазы, которые на 60% подобны генам грибов и только на 20% генам простейших. Аналогичные свойства были установлены и у других видое грибов.
По последним данным пневмоцисты относят к грибам возможно, к актиномицетам или высшим грибам — аско- или базидомицетам. Одновременно некоторые исследователи считают P. carinii филогенетически древним возбудителем неопределенного систематического положения, который в процессе эволюции утратил характерные таксономические признаки (Т. В. Бейер, 1989 г.). Современный молекулярно-биологический и молекулярно-генетический анализ не может окончательно определить их видовую принадлежность. Для решения этого вопроса необходимо ультраструктурное исследование возбудителя, изучение его филогенеза и усовершенствование техники культивирования пневмоцист.
P. carinii — внеклеточный паразит, тропный к легочной ткани. В цикле развития пневмоцисты выделяют вегетативную форму (трофозоит), предцисту и цисту с внутрицистными тельцами.
Трофозоиты — клетки размером 1-8 мкм, покрытые тонкой оболочкой. Их форма разнообразная и мобильная (овальная, амебоподобная и др.). Она зависит от формы структур, к которым они прилегают. От поверхности трофозоита отходят микровыросты и длинные отростки в виде филоподий. За их счет пневмоцисты соединяются между собой и прикрепляются к клеткам хозяина. Ядро ограничено двумя мембранами. В цитоплазме выявляются митохондрии, свободные рибосомы, мелкие и крупные вакуоли, полисахариды, капли липидов. Иногда встречаются сдвоенные клетки, что может свидетельствовать о делении или копуляции. По данным электронно-микроскопических исследований, трофозоиты плотно прилегают к альвеолоцитам первого порядка. Филоподий могут углубляться в клетку легкого хозяина, не разрывая ее оболочку. Одновременно мембрана альвеолоцита может входить в тело трофозоита, не повреждая его. Физиологический контакт возбудителя с хозяином осуществляется через систему микропиноцитарных пузырьков.
Предцисты — овальные клетки диаметром 2-5 мкм, лишенные пелликулярных выростов. В них происходит деление ядер. Цисты P. carinii округлой или овальной формы размером 3,5 — 10 мкм, иногда до 30 мкм (рис. 20). Они покрыты плотной трехслойной оболочкой и внешней мембраной. В цитоплазме содержится от 1 до 8 внутрицистных телец, которые выходят в просвет альвеолы после разрыва оболочки цисты. Пустые цисты имеют неправильную форму, чаще в виде полумесяца, иногда в них выявляются внутрицистные тельца. Размер последних 1-2 мкм. Пелликула внутрицистных телец вновь образуется после выхода из разрушенной цисты. Они становятся внеклеточными трофозоитами и начинают новый раунд жизненного цикла.
Патогенез пневмоцистоза определяется биологическими свойствами возбудителя и состоянием иммунной системы хозяина. Пропагативные формы пневмоцист, которые до настоящего времени не описаны, минуют верхние дыхательные пути, достигают альвеол и начинают жизненный цикл в организме нового хозяина. Прикрепление трофозоитов к альвеолоцитам первого порядка опосредуется многими механизмами, в частности большим количеством поверхностных гликопротеинов у P. carinii, которые взаимодействуют с протеинами легочной ткани через маннозные рецепторы на клетках хозяина, особенно макрофагах. Поверхностные гликопротеины пневмоцист высоко иммунногенные. Прикрепление пневмоцист сопровождается пролиферацией возбудителя, его взаимодействием с сурфактантом, освобождением токсических метаболитов. Защиту организма хозяина от P. carinii осуществляют Т-лимфоциты, альвеолярные макрофаги, специфические AT. Взаимодействие микро- и макроорганизма остается на субклиническом уровне, пока иммунная система не нарушена. Компроментация иммунной системы стимулирует рост численности пневмоцист.
У здорового человека P. carinii размножаются медленно, однако болезнь резко активизируется при подавлении иммунной реакции и за время инкубационного периода количество пневмоцист в легких увеличивается от 10.000 до более чем 1.000.000.000 клеток. Они постепенно заполняют альвеолярное пространство. Это ведет к появлению пенистого, «сотовидного» экссудата, повреждению мембраны альвеолярных лейкоцитов, увеличению их проницаемости, разрушению альвеолоцитов первого порядка. Плотное прилегание пневмоцист к альвеолоцитам приводит к сокращению дыхательной поверхности легких. Механическое повреждение интерстициальной ткани легкого возбудителем и воспалительными клетками, инфильтрация стенки альвеол мононуклеарами, а клеток интерстиция — плазматическими клетками приводят к утолщению альвеолярной стенки в 5 — 20 раз, вследствие чего развивается альвеолярно-капиллярный блок.
При СПИДе число паразитов в альвеолах и бронхах настолько большое, что нарушается альвеолярная вентиляция, и больной умирает от нарастающей легочной недостаточности. Разрушение альвеолярно-капиллярной мембраны может приводить к диссеминации пневмоцист с основного места локализации.
На гистологических срезах легких, пораженных пневмоцистами, возникает картина, характерная только для пневмоцистоза. Расширенные бронхиолы, альвеолы и мелкие бронхи заполнены эозинофильной пенистой массой. Альвеолярный эпителий, контактирующий с возбудителем, гипертрофирован, стенки альвеол утолщены за счет расширения капилляров и инфильтрации лимфоидно-гистиоцитарными элементами. Вокруг сосудов наблюдаются обильные скопления плазмоцитов. На стенках бронхов и альвеол видны отдельные круглые формы и пласты пневмоцист, стелящиеся по стенкам альвеол. Выявляются разорванные цисты P. carinii с выбросом в окружающее пространство внутрицистных телец, которые наращивают цитоплазму и превращаются в трофозоиты, а потом дозревают до цист. Гистологическая картина легких напоминает альвеолярный липопротеиноз с явлениями экссудации, лейкоцитоза и сетчатого склероза. Заполненные пенистой массой группы альвеол и альвеолярные ходы чередуются с участками компресионного ателектаза и эмфиземы.
Для построения собственной клеточной оболочки P. carinii использует фосфолипиды (ненасыщенный фосфатидилхолин) сурфактанта хозяина. Это приводит к общему повреждению сурфактантного обмена: дисбалансу в уровнях сурфактантных фосфолипидов и протеинов, гиперсекреции сурфактанта. Выраженное размножение и созревание P. carinii прямо коррелирует с пиком активности сурфактантной системы. Гиперпродукция сурфактанта на фоне развивающейся дисфункции альвеолярных макрофагов приводит к заполнению альвеол относительно гомогенной пенистой массой. Механическое разрушение и инактивация сурфактанта белками экссудата усугубляют гипоксическое состояние тканей, активируют фиброзирование межальвеолярных перегородок. Происходит снижение секреторной функции альвеолоцитов второго порядка и возрастание их пролиферативной активности. Плоский альвеолярный эпителий замещается кубическим. У больных СПИДом размножение в альвеолах P.carinii часто происходит в составе смешанной инфекции (бактериальная флора, грибы). Это создает патоморфологическую картину пневмоцистоза.
После проведенного лечения и выздоровления полного восстановления сурфактантной системы легких не происходит. Это является причиной колонизации дыхательной системы больных СПИДом нозокомиальными, стойкими к антибиотикам широкого спектра действия штаммами микроорганизмов. Поэтому рецидивирующие пневмонии у больных СПИДом — нередкое явление.
причины, симптомы, диагностика и лечение
Пневмоцистоз – оппортунистическая инфекция дыхательных путей, чаще поражающая детей раннего возраста, а также лиц с ослабленным иммунитетом. Пневмоцистоз может протекать в форме ОРЗ, ларингита, обструктивного бронхита, обострения ХЗЛ, интерстициальной пневмонии. Диагностика пневмоцистоза основана на обнаружении пневмоцист в мокроте и бронхиальном секрете с помощью микроскопии и ПЦР; данных гистологического исследования биоптатов бронхов; рентгенографии и КТ легких, сцинтиграфии, спирографии. Для проведения противопневмоцистной терапии используются препараты сульфаметоксазол+триметоприм, пентамидин, комбинация триметоприма с дапсоном и другие схемы лечения.
Общие сведения
Пневмоцистоз – легочная инвазия, вызываемая пневмоцистами и протекающая преимущественно в виде пневмоцистной пневмонии. Пневмоцистоз является иммунодефицит-ассоциированным инфекционным заболеванием, которым чаще всего болеют недоношенные дети, а также пациенты с первичными и вторичными иммунодефицитами. Смертельную опасность пневмоцистоз представляет для больных ВИЧ/СПИДом: при отсутствии лечения заболевание неизбежно заканчивается летальным исходом. Пневмоцистоз может возникать как спорадическая или внутрибольничная инфекция в отделениях педиатрии, гемобластозов, пульмонологии, противотуберкулезных инфекционных стационарах.
Пневмоцистоз
Причины пневмоцистоза
На сегодняшний день вопрос с видовой принадлежностью возбудителя пневмоцистоза окончательно не решен. В течение длительного времени микроорганизм Pneumocystis Carinii относили к простейшим класса споровиков. Однако в настоящее время доминирует точка зрения, что пневмоцисты занимают промежуточное положение между низшими и высшими грибами. В своем развитии пневмоцисты претерпевают 4 стадии: трофозоита, предцисты, цисты и спорозоита, протекающие на альвеоцитах. При разрыве оболочки созревшей цисты из нее выходят спорозоиты, которые проникают в легочные альвеолы, запуская очередной цикл стадийного развития пневмоцист новой генерации.
Источником эпидемиологической опасности выступает инвазированный человек (больной или носитель), выделяющий спорозоиты с частицами слизи во внешнюю среду при кашле или чихании. Передача возбудителей пневмоцистоза происходит по аспирационному механизму, воздушно-капельным, воздушно-пылевым, ингаляционным или аэрогенным путями. Считается, что среди клинически здоровых лиц до 10% являются носителями пневмоцист, однако у людей с нормально функционирующей иммунной системой инвазия протекает бессимптомно. Риску заболеваемости манифестными формами пневмоцистоза, главным образом, подвержены недоношенные новорожденные; дети с гипогаммаглобулинемией, гипотрофией, рахитом; больные ВИЧ/СПИДом и туберкулезом; пациенты, получающие иммуносупрессивную терапию по поводу коллагенозов, злокачественных новообразований, гематологических и лимфопролиферативных заболеваний, трансплантации органов и пр.
Пневмоцистоз развивается при снижении количества СД4+ клеток (Т-хелперов) в 4 и более раз по сравнению с нормой и достижении уровня менее 200 клеток в 1 мкл. При нарушении клеточного и гуморального иммунитета пневмоцисты начинают активно размножаться в альвеолах, вызывая развитие реактивного альвеолита, образование пенистого альвеолярного экссудата, содержащего пневмоцисты, лейкоциты, клеточный детрит и фибрин. При прогрессировании патологического процесса возникают участки ателектазов в легких, буллезное вздутии легочной ткани, что сопровождается нарушением вентиляции и газообмена, развитием дыхательной недостаточности.
Симптомы пневмоцистоза
В клиническом течении пневмоцистоза выделяют отечную (1-7 недель), ателектатическую (около 4-х недель) и эмфизематозную стадии. У части больных пневмоцистоз может протекать в виде ларингита, обструктивного или астматического бронхита, бронхиолита; в остальных случаях развивается пневмоцистная пневмония.
Инкубационный период пневмоцистоза занимает от 10 дней до 2-5 недель. Проявления отечной стадии развиваются постепенно и на ранних этапах включают в себя субфебрилитет, слабость, вялость. В конце первого периода присоединяется сухой кашель, тахипноэ, одышка. Признаками развивающегося пневмоцистоза у грудных детей может служить вялое сосание, отказ от кормления, плохая прибавка в массе тела, цианоз носогубного треугольника. Рентгенологические изменения в легких в отечной стадии пневмоцистоза отсутствуют; аускультативно определяется жестковатое дыхание, мелко- и среднепузырчатые хрипы; перкуторно — тимпанит в верхних отделах грудной клетки.
В ателектатической стадии пневмоцистоза лихорадка достигает фебрильных значений; появляется навязчивый коклюшеподобный кашель с пенистой мокротой; при минимальной нагрузке возникает одышка. Объективно выявляются постоянный цианоз, тахипноэ, тахикардия, увеличение межреберных промежутков, ослабленное дыхание, мелкопузырчатые хрипы. При рентгенографии легких определяются признаки пневмоцистной пневмонии – инфильтраты неоднородной плотности и ателектазы (так называемые «ватные легкие»). У иммунокомпрометированных лиц, кроме интерстициальной пневмонии, возможны внелегочные проявления пневмоцистоза в виде пневмоцистного ретинита, тиреоидита, отита, мастоидита или гайморита.
В ателектатической стадии пневмоцистоз может осложниться развитием пневмоторакса, экссудативного плеврита, легочного сердца, отека легких, а в случае присоединения бактериальной или грибковой инфекции – абсцессом легких. Летальные исходы в этот период обычно обусловлены дыхательной и сердечной недостаточностью. Третья, эмфизематозная стадия пневмоцистоза характеризуется уменьшением одышки и улучшением общего состояния больных. В исходе пневмоцистоза развивается эмфизема легких, сопровождающаяся значительным снижением показателей функции внешнего дыхания.
Диагностика пневмоцистоза
Клинические, физикальные и рентгенологические данные при пневмоцистозе не являются патогномоничными, что затрудняет своевременную диагностику заболевания. Между тем, пневмоцистную пневмонию всегда следует исключать у иммунокомпрометированных пациентов. С целью верификации пневмоцистоза проводится комплекс лабораторных и инструментальных исследований.
На рентгенограммах и КТ легких в типичных случаях определяется облаковидное понижение прозрачности легочных полей, получившее название «хлопьев снега» или «ватного легкого». Иногда рентгенологические изменения отсутствуют или имеют атипичную картину. С помощью ФВД обнаруживаются признаки дыхательной недостаточности по рестриктивному типу; исследование газового состава крови свидетельствует о гипоксемии.
Для подтверждения диагноза пневмоцистоза выполняется бронхоскопия с забором бронхиального секрета, трансбронхиальная биопсия легкого, сцинтиграфия легких с галлием-67. Для лабораторной детекции P.carinii микроскопически исследуются окрашенные мазки мокроты, бронхиальный и трахеальный аспират; выполняется гистологическое исследование биоптатов, исследование мокроты методом ПЦР. Проводится иммунологическая диагностика: определение титра противопневмоцистных IgG и IgM в сыворотке крови с помощью РИФ и ИФА. Дифференциальную диагностику пневмоцистоза необходимо проводить с цитомегаловирусной, хламидийной, уреаплазменной, бактериальной пневмонией, туберкулезом легких, саркомой Капоши и др.
Лечение и прогноз пневмоцистоза
Лечение пневмоцистоза проводится в стационаре. Лица с иммунодефицитом и недоношенные дети должны быть помещены в отдельные стерильные палаты с ламинарным воздушным потоком. В большинстве случаев для проведения специфической фармакотерапии пневмоцистоза используется комбинированные препараты (сульфаметоксазол+триметоприм, триметоприм+дапсон), пентамидин, эфлорнитин, атоваквон в течение 2-3 недель. Для устранения побочных эффектов терапии назначают фолиевую кислоту, глюкокортикоиды. Проводится инфузионная терапия (введение гамма-глобулина, солевых растворов, глюкозы, плазмы крови, альбумина и др.), кислородотерапия. У больных ВИЧ-инфекцией этиотропная терапия пневмоцистной пневмонии сочетается с высокоактивной антиретровирусной терапией.
Выживаемость при пневмоцистозе составляет 75-90%, а при повторном развитии пневмоцистной пневмонии – 60%. У 25-60% ВИЧ-инфицированных в течение года отмечаются рецидивы заболевания, поэтому больные нуждаются в проведении противорецидивного курса химиотерапии.
Пневмоциста : структура и жизненный цикл
Диагностика пневмоцистной инфекции
Учитывая тот факт, что симптомы пневмоцистной пневмонии не являются специфическими и часто заболевание протекает без выраженных клинических явлений, но с фульминантным течением – этиологическая верификация в данном случае очень важна для своевременного лечения.
Клинические проявления не являются патогномоничными, поэтому по данным анамнеза и объективного обследования доктор может определить только наличие пневмонии, а ее характер трудно заподозрить.
Важным фактом анамнеза является наличие у пациента онкопатологии, лечения цитостатиками, ВИЧ-инфицирования. Это позволяет заподозрить именно этот вид пневмонии на фоне значительного снижения реактивности иммунитета. Поэтому важно такой контингент больных очень тщательно исследовать и проводить профилактические меры.
Поэтому лабораторные и инструментальные методы диагностики – ведущие в верификации диагноза.
Рентгенография легких – обязательный метод диагностики и подтверждения пневмонии. Характерные изменения – это явление «белого легкого» или «облачного легкого», но эти симптомы не так часто встречаются и на начальных стадиях эти изменения еще не развиваются. У детей пневмоцистоз может выражаться на рентгенограмме по типу интерстициальной пневмонии.
Бронхоскопию рекомендуют проводить для получения смыва с бронхов и дальнейшего исследования секрета.
Пневмоцисты в мокроте могут выявляться при значительном их количестве в альвеолах. Исследование мокроты является одним из достоверных методов верификации диагноза. Материалом для исследования кроме мокроты может быть бронхо-альвеолярный смыв. Используют микроскопический метод с окрашиванием материала по Романовскому-Гимзе, и при этом выявляются фиолетовые клетки с красным ядром. Но этот метод не всегда дает результат, поскольку под объектив микроскопа могло не попасть достаточное количество возбудителя. Более точный метод – паразитологический. Материал, полученный от больного, высевают на живительную среду и за несколько дней вырастает возбудитель, что подтверждает диагноз.
Данные методы редко используются в современных условиях, поскольку до получения результата проходит много времени, а также необходима лаборатория с оборудованием, что есть не в каждом медицинском учреждении. Поэтому в данное время распространены методы серологической диагностики.
Анализ на качественное определение пневмоцист можно проводить с исследованием не только мокроты, но и крови. Используют метод полимеразной цепной реакции – молекулярно-генетический метод, основанный на выявлении ДНК в материале больного.
Более простой серологический метод исследования (исследование сыворотки крови) – выявление антител к пневмоцистам. Так как на возбудителя вырабатываются иммуноглобулины, то их уровень или наличие свидетельствует об активности процесса. Определяют уровень иммуноглобулинов класса G и М методом иммуноферментного анализа или имунофлюоресцентным методом. Повышенный уровень иммуноглобулинов класса М свидетельствует об острой инфекции, а при повышении иммуноглобулинов G – возможна длительная хроническая инфекция.
[11], [12], [13], [14], [15]
Пневмоцистоза — NHI.no
Hva er pneumocystis?
Пневмококкер
Pneumocystis jiroveci (tidligere kalt P. carinii ) er en sopp som forårsaker den hyppigste оппортунистические инфекционные заболевания blant pasienter smittet (infisert) med hiv. Opportunistiske инфекционер er en betegnelse som brukes på defeksjonene du kan få når immunsystemet ditt er svekket. Lungebetennelse med Pneumocystis jiroveci er ofte den sykdommen som varsler at hiv-Infoksjonen har utviklet seg til aids.
Lungebetennelse med pneumocystis forekommer nesten utelukkende blant hiv-smittede og blant pasienter med sterkt svekket immunsystem — для расширенного медицинского обслуживания, которое требуется от Andre Grunner må bruke høangoster doser to med overs. De fleste tilfeller av lungebetennelse med pneumocystis i våre dager forekommer hos personer som ikke er klar over at de har hiv-Infoksjon.
Смитте
Forutsetningen for å bli smittet og bli syk, er at du har et betydelig svekket immunsystem.Er du smittet med hiv, og utvikler denne sykdommen, betyr det at du har utviklet aids.
Smitteoverføringen av pneumocystis er ikke fullt ut kjent. Sannsynligvis er person-til-person smitte den vanligste smittemåten ved nyfeksjon, men smitte fra miljøkilder forekommer også. Luftbåren smitte er mest sannsynlig. Ikke-infiserte personer kan være asymptomatiske bærere av pneumocystis.
Animasjon av lungebetennelse
Диагностика
Som regel har pasienten en kjent hiv-Infoksjon eller aids.Vanlige symptomer er gradvis økende tungpust, tørrhoste og lavgradig feber. Akutt tungpust med smerter i brystet når den syke puster, kan bety and det har oppstått punktert lunge (пневмоторакс). Pasienter uten aids vil typisk presentere seg med akutte pustevansker en tid etter at dosen med immunhemmende midler er blitt redusert eller økt.
Legeundersøkelsen avslører ikke funn som kan stille Diagnosen med sikkerhet.
Tilstanden kan være vanskelig å диагностика на успешных симптомах и тегах, bruk av forebyggende medisiner i beendlingen av hiv-infiserte pasienter и samtidig инфекция, мед и рекке улье микроберкет анамнез.Диагностика проводится на микроскопическом уровне по изучению пневмоцистных организмов, например, «выпад» из луны.
Hvis spyttprøven ikke viser mikroben, gjøres bronkoskopi der legen skyller luftrørene med saltvann, suger det opp igjen og mikroskoperer på jakt etter Pneumocystis jiroveci .
Røntgen eller CT av Lungene kan vise typiske forandringer, men noen ganger kan røntgenbildene være normale.
Behandling
Målet med velondlingen er å fjerne mikroorganismen, dvs.kurere Infksjonen, og sikre и pasienten overlever. Pasienter med milde symptomer på pneumocystis lungebetennelse kan bendles utenfor sykehus med tabletter og hyppige kontroller. Ведите alvorligere symptomer må pasienten innlegges og velondles på sykehus. Behandlingen er antibiotika, men det er ikke alltid at virkningen er tilfredsstillende. Bivirkninger forekommer også.
Forebyggende Beendling начинает работать с мужчиной, работающим с пациентом, и поражает его, а также в обычном случае, когда человек поражен здоровьем, а также на его основе.Pasienter som er immmunsvekket av annen årsak enn hiv, vurderes også для предшественников.
Прогноз
Forløpet av pneumocystose er sterkt varierende. Sykdommen kan i noen tilfeller være dødelig for Immunsvekkede eller aids-pasienter.
Dødeligheten er 10-20% blant aids-pasienter med førstegangs lungebetennelse med pneumocystis, men den øker sterkt ved behov для работы с респиратором. Dødeligheten blant pasienter uten help er 30-60%, avhengig av eventuell underliggende sykdom.Kreftpasienter har høyere dødelighet enn dem som har gjennomgått transplantasjon eller som har bindevevssykdom.
Vil du vite mer?
Пневмоцистная пневмония или PCP | Сидарс-Синай
Не то, что вы ищете?
Что такое пневмоцистная пневмония?
Pneumocystis pneumonia (PCP) — это
грибковая инфекция в одном или обоих легких. Часто встречается у людей со слабым иммунитетом.
системы, например, у больных СПИДом.
Заболевание реже встречается в
США, чем раньше. Когда это происходит, вам немедленно требуется медицинская помощь.
Что вызывает PCP?
Гриб Pneumocystis jiroveci
вызывает PCP. Многие люди каждый день живут с этим грибком в легких. Это общее все
по всему миру. Часто это практически не доставляет проблем людям со здоровым иммунитетом.
системы.Но если ваша иммунная система ослаблена, у вас больше шансов получить PCP.
Ваша иммунная система может быть ослаблена ВИЧ / СПИДом, раком, трансплантацией органов, лекарствами, которые
подавить иммунную систему или другое состояние, которое заставляет иммунную систему не
работают хорошо. PCP использует вашу слабую иммунную систему для атаки.
Если не начать лечение сразу, ПП может быть тяжелым и даже смертельным.
Кто подвержен риску заражения PCP?
Вероятность заразиться PCP выше, если у вас ослабленная иммунная система.
Каковы симптомы ПП?
Симптомы PCP могут развиваться в течение недель или месяцев. Наиболее частые симптомы, на которые следует обращать внимание:
- Внезапная лихорадка
- Кашель
- Проблемы с дыханием. Часто становится хуже от активности.
- Сухой кашель с небольшим количеством слизи или без нее
- Герметичность
- Похудание
- Ночные поты
Если у вас есть какие-либо из этих симптомов и вы думаете, что у вас может быть PCP, особенно если у вас есть состояние, подавляющее иммунную систему, немедленно обратитесь к своему врачу.
Как диагностируется PCP?
Ваш лечащий врач может поставить диагноз PCP на основании вашего анамнеза и медицинского осмотра. Ваш провайдер также может провести следующие тесты:
- Рентген грудной клетки. В этом тесте используется небольшое количество излучения для получения изображений внутренних тканей, костей и органов, включая легкие.
- Анализы крови. Ваш врач может сделать анализы крови, чтобы узнать, есть ли у вас инфекция и распространилась ли она на кровь. Он или она может также сделать анализ газов артериальной крови, чтобы проверить количество кислорода в вашей крови.
- Посев мокроты. Этот тест проводится на материале, который кашляет из легких и попадает в рот. Посев мокроты часто используется для проверки на наличие в легких грибка PCP.
- Бронхоскопия. Это прямой экзамен
основных дыхательных путей легких (бронхов) с помощью гибкой трубки (бронхоскопа).
Как лечится PCP?
Если у вас тяжелый PCP, ваш
поставщик, скорее всего, будет лечить вас в больнице. Вы получите лекарство внутривенно.
это комбинация двух антибиотиков. Это триметоприм (ТМП) и сульфаметоксазол.
(SMX).
Для лечения этого состояния доступны и другие лекарства.Когда вам станет лучше, вы, вероятно, сможете перейти на антибиотики в форме таблеток.
Можно ли предотвратить PCP?
Если у вас заболевание, которое ослабляет вашу иммунную систему, ваш лечащий врач будет регулярно проверять ваш анализ крови, чтобы узнать, насколько сильна ваша иммунная система. Если у вас слабая иммунная система, ваш лечащий врач может дать вам лекарство от PCP до того, как это произойдет.
Курильщики также подвергаются большему риску заразиться PCP.Если вы курите, отказ от курения сделает ваши легкие более здоровыми. Это также поможет уберечь вас от инфекций легких, таких как PCP.
Лучший способ предотвратить PCP, если вы
иметь слабую иммунную систему — регулярно сдавать анализы крови и принимать профилактические препараты
при необходимости. Вакцины против гриппа и пневмококка предотвращают заражение людей некоторыми видами
пневмония. Но они не предотвращают PCP. Кроме того, люди с ослабленной иммунной системой
не могут быть кандидатами на их использование.Поговорите со своим врачом о
прививки и какая из них может вам подойти.
Основные сведения о пневмоцистной пневмонии
Следующие шаги
Советы, которые помогут вам получить максимальную пользу от визита к врачу:
- Знайте причину вашего визита и то, что вы хотите.
- Перед визитом запишите вопросы, на которые хотите получить ответы.
- Возьмите с собой кого-нибудь, кто поможет вам задать вопросы и запомнить, что вам говорит поставщик.
- Во время посещения запишите название нового диагноза и любые новые лекарства, методы лечения или тесты. Также запишите все новые инструкции, которые дает вам ваш провайдер.
- Узнайте, почему прописано новое лекарство или лечение и как они вам помогут. Также знайте, каковы побочные эффекты.
- Спросите, можно ли вылечить ваше состояние другими способами.
- Знайте, почему рекомендуется тест или процедура и что могут означать результаты.
- Знайте, чего ожидать, если вы не примете лекарство, не пройдете тест или процедуру.
- Если вам назначена повторная встреча, запишите дату, время и цель этого визита.
- Узнайте, как вы можете связаться с вашим поставщиком медицинских услуг, если у вас возникнут вопросы.
Не то, что вы ищете?
пневмоцистная пневмония Википедия
| Pneumocystis пневмония | ||
|---|---|---|
| Другие названия | Pneumocystis jirovecii пневмония, pneumocystis carinii пневмония | |
| Специализация | Инфекционные болезни, Пульмонология | |
| Причины | Pneumocystis jirovecii | |
| Факторы риска | Ослабленная иммунная система | |
Pneumocystis pneumonia ( PCP ) — форма пневмонии, вызываемая дрожжеподобным грибком Pneumocystis jirovecii . [1] Он также известен как PJP , для P neumocystis j iroveci P neumonia. [2]
Pneumocystis образцов обычно обнаруживаются в легких здоровых людей, хотя обычно не являются причиной заболевания. [3] Однако они являются источником оппортунистической инфекции и могут вызывать инфекции легких у людей со слабой иммунной системой или другими предрасполагающими состояниями здоровья. ПЦП встречается у людей с ВИЧ / СПИДом (на которых приходится 30-40% случаев ПП), у тех, кто принимает лекарства, подавляющие иммунную систему, а также у людей с онкологическими, аутоиммунными или воспалительными состояниями и хроническими заболеваниями легких. [4]
Признаки и симптомы []
Признаки и симптомы могут развиваться в течение нескольких дней или недель [4] и могут включать: одышку и / или затрудненное дыхание (с постепенным началом), лихорадку, сухой / непродуктивный кашель, потерю веса, ночную потливость, [5] озноб и усталость. [4] В редких случаях инфекция может прогрессировать и поражать другие внутренние органы (например, печень, селезенку и почки). [5]
- Кашель — обычно сухой / непродуктивный, потому что мокрота становится слишком вязкой для откашливания. Сухой кашель отличает PCP от типичной пневмонии. [5]
Осложнения []
Рентген и КТ помутнений матового стекла и пневмоторакса при пневмоцистной пневмонии. [6]
Пневмоторакс — хорошо известное осложнение PCP. [7] Кроме того, состояние, подобное острому респираторному дистресс-синдрому (ОРДС), может возникать у пациентов с тяжелой пневмоцистной пневмонией, и таким людям может потребоваться интубация. [8]
Патофизиология []
Риск PCP увеличивается, когда уровень CD4-положительных Т-лимфоцитов составляет менее 200 клеток / мкл. У этих лиц с ослабленным иммунитетом проявления инфекции сильно различаются. [9] Заболевание поражает интерстициальную фиброзную ткань легких с заметным утолщением альвеолярных перегородок и альвеол, что приводит к значительной гипоксии, которая может быть фатальной, если не лечить ее агрессивно.В этой ситуации повышается уровень лактатдегидрогеназы и нарушается газообмен. Кислород менее способен диффундировать в кровь, что приводит к гипоксии, которая наряду с высоким уровнем углекислого газа в артериальной крови (CO
2) стимулирует гипервентиляционное усилие, вызывая тем самым одышку (одышку). [ необходима ссылка ]
Диагноз []
Диагноз может быть подтвержден характерным внешним видом рентгеновского снимка грудной клетки и уровнем кислорода в артериальной крови (PaO 2 ), который значительно ниже, чем можно было бы ожидать на основании симптомов.Снимки галлия 67 также полезны при диагностике. Они отклоняются от нормы примерно в 90% случаев и часто бывают положительными до того, как рентгенограмма грудной клетки станет аномальной. Рентген грудной клетки обычно показывает обширные легочные инфильтраты. КТ может показать кисты легких (не путать с кистообразными формами возбудителя). [ необходима ссылка ]
Рентген грудной клетки: повышенное помутнение (белизны) в нижних отделах легких.
Рентгенограммы грудной клетки двух пациентов.Оба показывают непрозрачность матового стекла. Левый рентгеновский снимок показывает гораздо более тонкий вид матового стекла, в то время как правый рентгеновский снимок показывает гораздо более грубый внешний вид матового стекла, имитирующий отек легких. [6]
Рентгеновский снимок кисты при пневмоцистной пневмонии [6]
ВРКТ кист пневмоцистной пневмонии. Обычно они множественные и двусторонние, но различаются по размеру, форме и распространению. [6]
Диагноз может быть окончательно подтвержден путем гистологической идентификации возбудителя в мокроте или бронхоальвеолярном лаваже (полоскании легких).Окрашивание толуидиновым синим, окрашивание серебром, периодическое окрашивание кислотой-Шиффом или иммунофлуоресцентный анализ показывают характерные кисты. [10] Кисты напоминают измельченные шарики для пинг-понга и присутствуют в совокупности от двух до восьми (не путать с Histoplasma или Cryptococcus , которые обычно не образуют агрегатов спор или клеток). Биопсия легкого покажет утолщенные альвеолярные перегородки с пушистым эозинофильным экссудатом в альвеолах. И утолщенные перегородки, и рыхлый экссудат способствуют нарушению диффузионной способности, характерной для этой пневмонии.
Инфекцию Pneumocystis также можно диагностировать с помощью иммунофлуоресцентного или гистохимического окрашивания образца, а в последнее время — путем молекулярного анализа продуктов полимеразной цепной реакции, сравнивая образцы ДНК. Примечательно, что простое молекулярное обнаружение P. jirovecii в жидкостях легких не означает, что у человека есть PCP или ВИЧ-инфекция. Грибок, по-видимому, присутствует у здоровых людей в общей популяции. [11]
Профилактика []
У пациентов с ослабленным иммунитетом профилактика котримоксазолом (триметоприм / сульфаметоксазол), атоваквоном [12] или регулярными ингаляциями пентамидина может помочь предотвратить ПП.
Лечение []
Противопневмоцистный препарат используется с сопутствующими стероидами, чтобы избежать воспаления, которое вызывает обострение симптомов примерно через 4 дня после начала лечения, если стероиды не используются. Безусловно, наиболее часто используемым препаратом является триметоприм / сульфаметоксазол, но некоторые пациенты не могут переносить это лечение из-за аллергии. Другие лекарства, которые используются по отдельности или в комбинации, включают пентамидин, триметрексат, дапсон, атоваквон, примахин, малеат пафурамидина (в стадии исследования) и клиндамицин.Продолжительность лечения обычно составляет около 21 дня.
Пентамидин используется реже, поскольку его основным ограничением является высокая частота побочных эффектов. К ним относятся острое воспаление поджелудочной железы, почечная недостаточность, токсичность для печени, снижение количества лейкоцитов, сыпь, лихорадка и низкий уровень сахара в крови. [ необходима ссылка ]
Эпидемиология []
Заболевание PCP относительно редко встречается у людей с нормальной иммунной системой, но часто встречается у людей с ослабленной иммунной системой, таких как недоношенные или сильно истощенные дети, пожилые люди и особенно люди, живущие с ВИЧ / СПИДом (у которых он чаще всего наблюдается. ). [1] [13] ПП также может развиваться у пациентов, принимающих иммунодепрессанты. Это может произойти у пациентов, перенесших трансплантацию солидных органов или костного мозга, а также после операции. [14] Инфекции, вызванные Pneumocystis. пневмония также часто встречается у младенцев с синдромом гипер-IgM, Х-сцепленным или аутосомно-рецессивным признаком. [ необходима ссылка ]
Организм, вызывающий PCP, распространен по всему миру [15] и Pneumocystis пневмония была описана на всех континентах, кроме Антарктиды. [15] Более 75% детей являются серопозитивными к 4 годам, что свидетельствует о высоком фоновом воздействии на организм. Посмертное исследование , проведенное в Чили с участием 96 человек, умерших от не связанных причин (самоубийство, дорожно-транспортные происшествия и т. Д.), Показало, что у 65 (68%) из них был пневмоцистоз в легких, что позволяет предположить, что бессимптомная пневмоцистная инфекция чрезвычайно высока. общий. [16] До 20% взрослых могут быть бессимптомными носителями в любой момент времени, и бессимптомная инфекция может сохраняться в течение нескольких месяцев, прежде чем будет устранена иммунным ответом. [4]
P. jirovecii первоначально был описан как редкая причина пневмонии у новорожденных. Обычно считается, что это комменсальный организм (выживание зависит от человеческого хозяина). Возможность передачи вируса от человека к человеку в последнее время стала подтверждаться доказательствами, полученными в результате множества различных исследований генотипирования изолятов P. jirovecii из ткани легких человека. [17] [18] Например, в одной вспышке из 12 случаев среди пациентов с трансплантатами в Лейдене предполагалось, что возможно, но не доказано, что распространение вируса от человека человеку могло иметь место. [19]
ПП и СПИД []
С самого начала эпидемии СПИДа PCP был тесно связан со СПИДом. Поскольку это происходит только у хозяина с ослабленным иммунитетом, это может быть первым ключом к новому диагнозу СПИДа, если у пациента нет других причин для ослабления иммунитета (например, прием иммунодепрессантов для трансплантации органов). Необычный рост числа случаев PCP в Северной Америке, замеченный, когда врачи начали запрашивать большие количества редко используемого антибиотика пентамидина, был первым ключом к разгадке существования СПИДа в начале 1980-х годов. [20] [21]
До разработки более эффективных методов лечения PCP был частой и быстрой причиной смерти людей, живущих со СПИДом. В большинстве случаев заболеваемость PCP была снижена за счет введения стандартной практики перорального применения котримоксазола (Bactrim / Septra) для предотвращения заболевания у людей с числом CD4 менее 200 / мкл. В группах населения, не имеющих доступа к профилактическому лечению, PCP по-прежнему является основной причиной смерти от СПИДа. [ необходима ссылка ]
Номенклатура []
Оба: Pneumocystis pneumonia и pneumocystis pneumonia [22] орфографически правильные; один использует название рода как таковой, а другой — основанное на нем нарицательное существительное.(Это та же самая причина, например, почему «стрептококк группы A » и «стрептококк группы A» являются действительными.) Синонимы для PCP включают пневмоцистоз [22] (пневмоцистоз + -оз), пневмоцистоз [22] (пневмоцистоз + -аз) и интерстициальная плазматическая клеточная пневмония . [22]
Старое название вида Pneumocystis carinii (которое теперь применяется только к виду Pneumocystis , который встречается у крыс [23] ) все еще широко используется.В результате, Pneumocystis pneumonia (PCP) также известна как Pneumocystis jiroveci [i] pneumonia и (неправильно) как Pneumocystis carinii pneumonia . [24] [25] [26]
Что касается номенклатуры, когда название Pneumocystis pneumonia (PCP) изменилось с P. carinii, pneumonia, на P. jirovecii pneumonia, это было при сначала спросили, следует ли «PJP» заменить «PCP». a b c d e Khan, Allen, CarolynM; Аль-Джахдали, ХамданХ; Ирион, KlausL; Аль Ганем, Сара; Гауда, Алаа (2010). «Визуализация легких проявлений ВИЧ / СПИДа». Анналы торакальной медицины . 5 (4): 201–16. DOI: 10.4103 / 1817-1737.69106. ISSN 1817-1737. PMC 2954374. Stringer, James R .; Борода, Чарльз Б.; Миллер, Роберт Ф .; Уэйкфилд, Энн Э. (сентябрь 2002 г.). «Новое название пневмоцистоза от людей и новые перспективы взаимоотношений хозяина и патогена». Emerg Infect Dis . 8 (9): 891–896. DOI: 10.3201 / eid0809.020096. PMC 2732539. PMID 12194762.
Внешние ссылки []
.




 На КТ – ателектатические изменения легких. При аускультации выслушиваются различные хрипы.
На КТ – ателектатические изменения легких. При аускультации выслушиваются различные хрипы.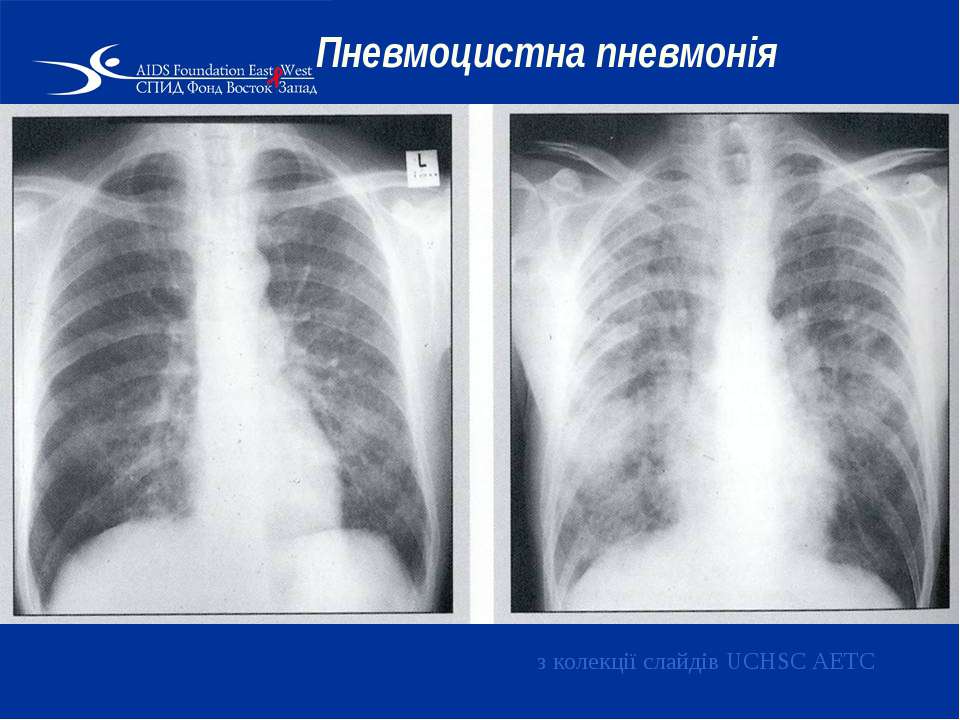

 Выбор дозы и длительности терапии зависит от степени выраженности дыхательной недостаточности, состояния больного, клинической картины, возраста и ряда других показателей. Все эти препараты токсичны для человека. Они могут спровоцировать подъем температуры, сыпь на коже, нейропатию, пищеварительную дисфункцию.
Выбор дозы и длительности терапии зависит от степени выраженности дыхательной недостаточности, состояния больного, клинической картины, возраста и ряда других показателей. Все эти препараты токсичны для человека. Они могут спровоцировать подъем температуры, сыпь на коже, нейропатию, пищеварительную дисфункцию.
