» Стеноз гортани у детей
Стеноз гортани у детей — это заболевание, которое характеризуется сужением просвета гортани. В итоге происходит затруднение поступления воздуха в легкие, что учащает дыхание ребенка. Стеноз приводит к нарушению защитной, дыхательной и голосовой функции. Сегодня данное заболевание отмечается достаточно часто и требует соответствующего лечения.
Разновидности стеноза
В зависимости от симптоматики и длительности заболевания принято различать несколько форм стеноза:
Острая форма получила наибольшее распространение. Продолжительность такого заболевания может составлять как несколько минут, так и один месяц. Следует сказать, что молниеносный стеноз, продолжительность которого может достигать нескольких минут, крайне опасен для жизни ребенка.
Подострый стеноз имеет время развития от 1 до 3 месяцев.
Хроническая форма заболевания имеет длительность более трех месяцев. Такое сужение гортани может быть приобретенным или врожденным. Достаточно часто хронический стеноз отмечается на фоне образования рубцовой ткани в гортани и доброкачественных новообразований.
Факторы, вызывающие появление стеноза у детей
Следует сказать, что вызывать данное заболевание могут различные причины. Можем сказать, что достаточно часто стеноз появляется на фоне:
- Различных воспалительных заболеваний. Так, например такое сужение трахеи может отмечаться на фоне гортанной ангины, подкладочного фарингита и ларингита.
- Различных инфекционных заболеваний.
- Заболеваний пищевода, гортани и трахеи.
- При механических травмах гортани, что может возникать при медицинском вмешательстве или же бытовым способом.
- Наличие различных врождённых аномалий гортани.
- Появление острой аллергической реакции.
- Острого отравления организма.
Симптоматика стеноза у детей
Следует сказать, что симптоматика данного заболевания напрямую зависит от его стадии. Так, например, на стадии компенсации отмечается легкое состояние у ребенка, при котором лишь отмечается учащенное дыхание. При повышенной физической нагрузке у ребенка может отмечаться одышка.
Так, например, на стадии компенсации отмечается легкое состояние у ребенка, при котором лишь отмечается учащенное дыхание. При повышенной физической нагрузке у ребенка может отмечаться одышка.
При стадии неполной компенсации отмечается средняя тяжесть состояния ребенка. На коже и слизистых появляются бледные цвета, дыхание нарушенное и имеет выраженный шум. Также у ребенка могут отмечаться признаки гипоксемии.
Стадия декомпенсации оценивается как тяжелое состояние ребенка. Внешнее дыхание нарушено, ребенок может закрывать глаза, цвет кожи существенно изменен. На слизистых оболочках отмечается цианоз. Дети быстро устают, при этом отмечается выраженное нарушение дыхания. Глубокая гипоксия тканей способствует тахикардии, аритмии и замедлению пульса.
Лечение детского стеноза
Следует сказать, что успешность проводимого лечения данного заболевания напрямую зависит от стадии, на которой выявлен стеноз у ребенка. Необходимо ликвидировать дыхательную недостаточность и приступы удушья. Лечение данного заболевания может проводиться как разнообразными физиотерапевтическими процедурами, так и приемом соответствующих лекарственных средств. В редких случаях требуется хирургическое вмешательство, что позволяет полностью устранить проблемы с дыханием у ребенка. Необходимо соблюдение всех предписаний врача, а само лечение выполняется исключительно под присмотром специалиста.
Острый стеноз гортани (=круп). Что делать?
Он же острый ларинготрахеит.
Он же ложный круп.
Состояние, при котором на фоне ОРВИ развивается:
🔹 Лающий кашель;
🔹 Осиплость голоса;
🔹 Шумный ВДОХ с затрудненным дыханием.
Причина — воспаление слизистой в области голосовых складок гортани.
Чаще всего встречается у детей до 3 лет.
Основная причина Такой реакции на ОРВИ — наследственность. У родителей, страдавших в детстве от ложного крупа, и дети, скорее всего, будут этим страдать.
Важно знать:
🔹 Эти эпизоды пройдут с возрастом.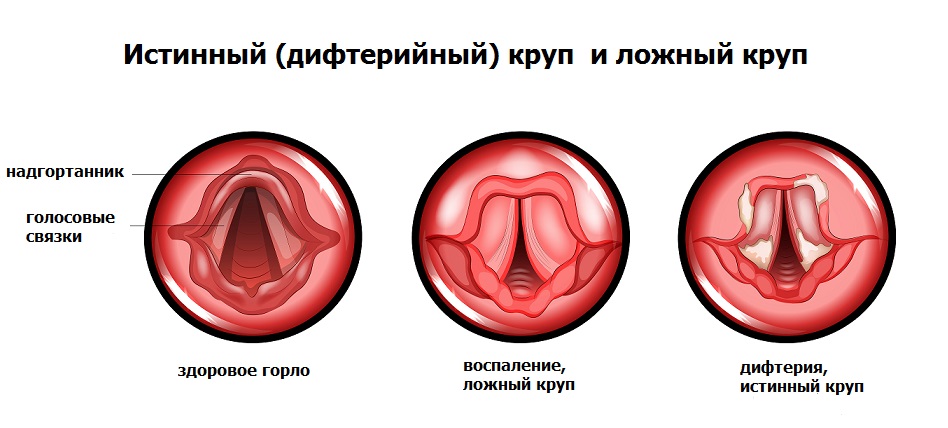
🔹 НЕ связаны с аллергией.
Типичная картина: у ребенка признаки ОРВИ (насморк, температура).
Ночью ребенок просыпается от дающего кашля и затрудненного дыхания.
Он испуган, плачет, может быть возбужден.
Что делать?
1️⃣ Успокоиться самим и успокоить ребенка. Ларинготрахеит в большинстве случаев не угрожает жизни и проходит самостоятельно (хотя выглядит это страшно, особенно в первый раз). Лечить можно дома. К тому же чем выраженнее беспокойство у ребенка, тем тяжелее ему дышать.
Возьмите на руки, утешьте, включите мультик.
2️⃣ Откройте окно, чтобы в комнате стало прохладно. Подойдите с ребенком к окну и вместе посмотрите, что там (отвлечение). Включите увлажнитель. Если его нет — идите с ребенком в ванну и включите воду.
3️⃣ Используйте глюкокортикостероиды (ГКС).
Гормоны могут быть в виде таблеток, уколов или ингаляции через небулайзер.
Нет никаких преимуществ у уколов в сравнении с таблетками, так как препарат не мгновенного действия, а эффект наступает в течение 2 часов (да, это не препарат скорой помощи, об этом написано в инструкции)
4️⃣ Доза Пульмикорта выше, чем при обструктивном бронхите — 2 мг за раз.
5️⃣ Если отвлечение, успокоение и гормоны без эффекта — ребенку все ещё тяжело дышать — вызывайте скорую.
Стеноз гортани | Медицинский центр «Президент-Мед»
Недомогание, при котором происходит сужение просвета гортани называется стенозом. Развитие патологии затрудняет процесс дыхания и глотания пищи. В группе риска прогрессирования недуга дети (особенно недоношенные), хотя часто наблюдается болезнь и у взрослых пациентов.
Стеноз гортани довольно тяжелое заболевание, оно без корректного лечения может привести к летальному исходу. В младенческом возрасте проявляется патология, если ребенок после рождения не мог самостоятельно дышать и долго находился на искусственном дыхании. У взрослых больных и детей постарше спровоцировать сужение просвета гортани могут многие факторы.
Первопричины развития стеноза гортани:
- Инфекционные болезни: сыпной и брюшной тиф, скарлатина, туберкулез, малярия, корь и другие.
- Механические травмы горла.
- Аллергическая реакция.
- Ожог гортани химическими веществами или пламенем.
- Интубация трахеи, гастроскопия и бронхоскопия.
- Опухоли гортани различного характера.
- Патологии щитовидной железы.
Перед подбором лечения важно определить причину и форму течения болезни. Стеноз гортани может быть острым (развивается быстро) или же хроническим.
Симптомы стеноза гортани
Проявление симптоматики стеноза гортани зависит от состояния иммунной системы человека и стадии развития заболевания.
Степени и признаки стеноза:
I стадия (компенсированный стеноз) – диагностируется сужение гортани до 50%, при этом у пациента диагностируется наличие затрудненного дыхания, одышки при физических нагрузках и симптомов брадикардии.
II стадия (субкомпенсированная вариация) – сужение просвета до 70%. Больному тяжело выдыхать воздух, беспричинно появляется одышка, дыхание становиться шумным.
III стадия (декомпенсированный вариант) – просвета в гортани остается очень мало, до 1% (сужение 99%). Развивается гипоксия, в результате чего появляется синюшность кожных покровов. Кроме того, пациент вынужден только сидеть, поскольку в другой позе дышать он не может, дыхание при этом очень громкое и присоединяется тахикардия.
IV стадия (асфиксия) – 100% сужение просвета. Это самая страшная степень стеноза гортани, поскольку происходит остановка дыхания, появляются судороги, больной теряет сознание и пульс не прощупывается. Без мгновенной реанимации пациент умирает.
Быстрому лечению поддаются только начальные степени стеноза гортани, поэтому при проявлении симптомов следует обратиться к отоларингологу.
Диагностика и лечение стеноза гортани
При подозрении на стеноз гортани врач назначит ларингоскопию. Такое инструментальное обследование позволит увидеть состояние трахеи, а также уточнить ширину оставшегося просвета гортани. Доктор может направить пациента на УЗИ щитовидной железы, компьютерную томографию или рентгенологическую диагностику пищевода. Обязательно проводиться бактериологический анализ мазка из зева. Все эти диагностические мероприятия помогают не только уточнить диагноз, но и выявить первопричину развития патологии, а значит, подобрать эффективную терапию.
Такое инструментальное обследование позволит увидеть состояние трахеи, а также уточнить ширину оставшегося просвета гортани. Доктор может направить пациента на УЗИ щитовидной железы, компьютерную томографию или рентгенологическую диагностику пищевода. Обязательно проводиться бактериологический анализ мазка из зева. Все эти диагностические мероприятия помогают не только уточнить диагноз, но и выявить первопричину развития патологии, а значит, подобрать эффективную терапию.
Больных стенозом лечат в стационаре реанимационного отделения. Медикаментозная терапия может включать в себя антибиотики, глюкокортикостероиды, противоотечные и противоаллергические средства. Кроме того, внутривенно вводят препараты, сужающие сосуды, а также кальций. В процессе борьбы со стенозом гортани могут применяться и специальные теплые компрессы на горло или грудь со щелочными минеральными водами, а также согревающие ножные ванны.
Если наступает удушье, проводят срочную трахеотомию (вскрытие просвета трахеи). В случае, когда диагностируется асфиксия, показана коникотомия – в определенной области шеи делают разрез и вводят в образовавшийся просвет трубку, через нее воздух поступает в дыхательные пути больного.
Лечение стеноза сложное, оно должно производиться только под четким контролем докторов. Самолечение сужения просвета гортани может привести к усугублению процесса и необратимым последствиям.
Для диагностики и лечения стеноза гортани обращайтесь в медицинские клиники «Президент-Мед» в Москве (на Коломенской и ВДНХ) и в Видном
Автор: Мамунц Цовинар Алексеевна
Главный врач Президент-Мед г. Видное
Высшее медицинское, Пермский государственный медицинский институт, лечебный факультет, специальность-лечебное дело
Записаться к врачу
ОТЗЫВЫ КЛИЕНТОВ
Ольга
Спасибо Юлие Владимировне! Врач очень опытная, внимательная, а самое главное ее очень любят дети! Приходилось уже несколько раз с ребёнком обращаться и всегда каждый приём на высоте. Как хорошо, когда есть такие хорошие врачи[…]
Как хорошо, когда есть такие хорошие врачи[…]
Щетининой О.Н.
Большое спасибо всем работникам клиники за слаженную работу и хорошее настроение. Отдельное спасибо Ивановой Ю.А. за профессионализм, отзывчивость, индивидуальный подход.[…]
Приобретенные гортаннотрахеальные стенозы у детей | #10/01
Обзор литературы
Приобретенные гортаннотрахеальные стенозы остаются одной из сложнейших проблем детской оториноларингологии. Это связано не только с трудностью и многоэтапностью восстановления просвета дыхательных путей, но и с сочетанным с дыхательным стенозом и длительным трахеальным канюленосительством развитием патологических изменений в других органах и системах организма. Такие изменения приводят к инвалидности и социальной неполноценности, что требует тесного взаимодействия специалистов нескольких педиатрических дисциплин, таких, как оториноларингология, анестезиология, реаниматология, хирургия, пульмонология, гастроэнтерология, генетика [5, 10, 13, 18].
Ведущей причиной формирования рубцовых стенозов гортани является продленная чрезгортанная назотрахеальная интубация, проводимая по поводу острого стенозирующего ларинготрахеобронхита, операций и иных экстремальных ситуаций, требующих реанимационных мероприятий и искусственной вентиляции легких [5, 7, 11, 13, 33]. Повреждение тканей гортани при проведении интубации возникает в случае превышения капиллярного давления. Это вызывает ишемию тканей с последующим развитием воспаления, отека, изъязвления слизистой оболочки и дальнейшим возникновением хондроперихондрита и некроза, что можно сравнить с развитием «гортанного пролежня» [14]. Кроме того, стенозы могут быть связаны со спортивной, бытовой, транспортной и медицинской травмами [2, 14, 34, 35].
Кроме того, стенозы могут быть связаны со спортивной, бытовой, транспортной и медицинской травмами [2, 14, 34, 35].
При бактериологическом исследовании отделяемого из трахеи у детей, нуждающихся в восстановительном лечении по поводу рубцового стеноза гортани, отмечается полимикробная флора (до восьми типов микроорганизмов одновременно), в том числе сочетание как аэробной, так и анаэробной флоры [15]; при этом, характер микробной флоры у детей и взрослых различается. Чаще всего у детей инфицирование происходит Pseudomonas aeruginosa, Staphylococcus aureus, Acinetobacter и Haemophilus influenzae [31].
Рентгенографическое исследование, являющееся наиболее распространенным дополнительным методом диагностики [2, 44], в связи с малой контрастностью тканевых структур гортани не всегда дает объективную картину [42], а ультразвуковое исследование гортани к настоящему времени еще не получило широкого распространения [4]. «Золотым стандартом» диагностики рубцового стеноза гортани и трахеи являются прямая микроларингоскопия и трахеобронхоскопия с использованием операционного микроскопа и оптических трубок [13, 18, 23, 36]. Эти методы позволяют точно оценить протяженность и степень стеноза, его характер и локализацию; следует также иметь в виду, что у 1/5–1/2 пациентов возможны комбинированные поражения на различных уровнях дыхательных путей [18, 23].
В результате повреждения дыхательных путей могут формироваться различные виды обструкции. Повреждения гортани у новорожденных и детей младшего возраста часто (до 22% случаев) протекают с явлениями хондроперихондрита, лечение которого включает в себя противовоспалительную и гормональную терапию [9]. У детей младшего возраста эндоскопическое бужирование гортани в сочетании с противовоспалительным лечением в процессе формирования рубцовой ткани при ее незрелости и остаточных воспалительных процессах на ограниченном участке может оказаться эффективным. В то же время диффузный перихондрит хрящевого каркаса гортани и сформировавшийся рубец являются противопоказаниями к проведению бужирования [11].
Наиболее тяжелое осложнение чрезгортанной интубации трахеи и трахеостомии — это развитие рубцового стеноза. Рубцы могут локализоваться в различных отделах дыхательных путей — между черпаловидными хрящами, на уровне голосовых складок, в подскладковом отделе, в шейном и грудном отделах трахеи [14, 32]. По данным Э. А. Цветкова (1996), более чем у 70% больных детей рубцовый процесс занимает подголосовой отдел гортани и гортаннотрахеальное сочленение. Согласно исследованиям А. Д. Понкратенко, Е. К. Онуфриевой (1997), среди 183 детей с рубцовым стенозом гортани рубцы локализовались в голосовом отделе у 36 больных, в подскладковом — у 118, сочетанное поражение разных отделов гортани отмечено у 29 пациентов.
Хирургическое устранение рубцового стеноза возможно двумя принципиально разными доступами — через естественные пути или с рассечением гортани и трахеи. Эндоскопические хирургические вмешательства при рубцовых стенозах всегда предпочтительнее эндоларингеальных с наружным доступом [11, 29]. Прямая микроларингоскопия и эндоларингеальная микрохирургия, особенно с использованием лазерной техники, позволяет у значительной части больных устранить рубцовый стеноз гортани и гортаннотрахеального отдела с достаточно хорошим функциональным эффектом. Лазерные операции практически бескровны, отличаются малой травматичностью и вследствие этого не сопровождаются выраженными реактивными явлениями. Другим преимуществом лазерных операций по сравнению с операцией наружным доступом является интактность хрящевого остова, что способствует более быстрому заживлению и восстановлению просвета гортани, позволяя максимально сохранить голосовую функцию [13]. Особенности процессов репарации после лазерных операций дают возможность у большинства больных, в том числе у детей младшего (до трех лет) возраста, восстанавливать просвет дыхательных путей без дополнительного применения стентов [1, 9, 13], хотя в ряде случаев их приходится использовать для поддержания воссозданного просвета [6, 48]. Лазерная хирургия рубцовых стенозов эффективна также в случаях, когда предыдущие операции с применением других методик не дали хорошего результата [37]. Катамнестические наблюдения свидетельствуют о том, что воссозданный с помощью лазерной операции просвет дыхательных путей сохраняется с ростом гортани и обеспечивает нормальную дыхательную функцию [5].
Лазерная хирургия рубцовых стенозов эффективна также в случаях, когда предыдущие операции с применением других методик не дали хорошего результата [37]. Катамнестические наблюдения свидетельствуют о том, что воссозданный с помощью лазерной операции просвет дыхательных путей сохраняется с ростом гортани и обеспечивает нормальную дыхательную функцию [5].
Одним из главных критериев отбора больных для эндоскопической лазерной хирургии является протяженность рубца, которая не должна превышать 1,5-2 см [1, 7, 13, 25]. Лечение оказывается малоэффективным при вовлечении в рубцовый процесс хрящевого скелета [7]. Кроме того, необходимо учитывать фазу формирования стеноза. В тех случаях, когда имеются явления хондроперихондрита, вопрос о необходимости лазерной операции целесообразно отложить до ликвидации воспалительных явлений [9]. Предпочтительнее всего проводить операцию через год и более после травматического повреждения гортани и формирования стеноза, однако положительного результата удается достичь и при лечении детей в ближайшие сроки (до двух месяцев) после травмы дыхательных путей [12]. При анализе результатов повторных операций по поводу рубцового стеноза гортани отмечается определенная связь: при неэффективном первичном хирургическом вмешательстве в 50% наблюдений результат повторной операции оказывается аналогичным. Показанием к повторной операции является хотя бы минимальный эффект от предыдущей — небольшое увеличение просвета дыхательной трубки [13, 29]. При удовлетворительном результате первичной операции повторная в 80-90% наблюдений приводит к дальнейшему улучшению [12].
Показаниями к операции по устранению рубцового стеноза гортани наружным доступом служат протяженный (более 1-3 см) рубец, потеря хрящевой опоры выше или в области трахеостомы, отсутствие эффекта от эндоскопических операций, в том числе проводимых с помощью лазера [13, 26]. В литературе имеется скудная информация об оптимальных сроках подобных операций у детей. В то же время случаи возникновения различного рода осложнений и гибели детей при случайной деканюляции или закупорке трахеотомической трубки коркой наблюдаются достаточно часто и составляют до 4,6% [49]. Ларингостомия и длительное формирование просвета гортани с применением Т-образной трубки у детей затруднены, так как относительно толстые стенки трубки суживают и без того неширокий просвет дыхательных путей, вызывая развитие дисфагических явлений, бронхитов, аспирационных пневмоний, асфиксии [41]; применение Т-образных трубок эффективно только у 50% пациентов в возрасте до 10 лет по сравнению с 80% больных старше 10 лет [20]. Реконструктивные операции у детей младшего возраста имеют высокий статистически значимый риск неудачи, несмотря даже на меньшую тяжесть повреждения дыхательных путей, по сравнению со старшими детьми [50]. В то же время некоторые авторы рекомендуют оперировать детей раннего возраста как можно раньше в целях восстановления нормального речевого общения; при этом хронические трахеоканюляры, по сравнению с ранее не трахеотомированными больными, требуют более агрессивной тактики лечения; они имеют меньше шансов на успех операции, у таких больных чаще развиваются осложнения в послеоперационном периоде [25]. Среди новорожденных и детей младшего возраста предрасполагающими факторами к развитию осложнений являются вес меньше 4 кг и гестационный срок меньше 30 недель [28].
В то же время случаи возникновения различного рода осложнений и гибели детей при случайной деканюляции или закупорке трахеотомической трубки коркой наблюдаются достаточно часто и составляют до 4,6% [49]. Ларингостомия и длительное формирование просвета гортани с применением Т-образной трубки у детей затруднены, так как относительно толстые стенки трубки суживают и без того неширокий просвет дыхательных путей, вызывая развитие дисфагических явлений, бронхитов, аспирационных пневмоний, асфиксии [41]; применение Т-образных трубок эффективно только у 50% пациентов в возрасте до 10 лет по сравнению с 80% больных старше 10 лет [20]. Реконструктивные операции у детей младшего возраста имеют высокий статистически значимый риск неудачи, несмотря даже на меньшую тяжесть повреждения дыхательных путей, по сравнению со старшими детьми [50]. В то же время некоторые авторы рекомендуют оперировать детей раннего возраста как можно раньше в целях восстановления нормального речевого общения; при этом хронические трахеоканюляры, по сравнению с ранее не трахеотомированными больными, требуют более агрессивной тактики лечения; они имеют меньше шансов на успех операции, у таких больных чаще развиваются осложнения в послеоперационном периоде [25]. Среди новорожденных и детей младшего возраста предрасполагающими факторами к развитию осложнений являются вес меньше 4 кг и гестационный срок меньше 30 недель [28].
Для формирования стойкого просвета гортани осуществляются различные варианты редрессации печатки перстневидного хряща [8, 11, 46], ларинготрахеальной декомпрессии с расширением просвета дыхательных путей (в области как передней, так и задней стенки), в том числе путем пересадки аутохряща (реберного, ушной раковины, перегородки носа) [17, 19, 40], васкуляризированного трансплантата из тела подъязычной кости с грудинно-подъязычной мышцей [11, 24, 27] и других тканей. Наиболее частыми причинами неудач операций, проведенных наружным доступом, являются недостаточная предоперационная диагностика гортаннотрахеального стеноза, интраоперационные дефекты, ошибки, связанные с выбором типа и длины стента и длительностью его использования, склонность к развитию келлоидных рубцов, недостаточное послеоперационное наблюдение [16], а также такая сопутствующая патология, как ларингомаляция, трахеомаляция и пролапс черпаловидных хрящей [38]. В ряде случаев для успешной деканюляции требуется несколько повторных операций наружным доступом; лечение может затягиваться на десятки лет [22]. Противопоказаниями к операции наружным доступом являются незаконченный процесс рубцевания, тяжелые поражения ЦНС, заболевания легких, неизлеченное первичное заболевание, невозможность послеоперационного наблюдения и лечения [11, 25].
В ряде случаев для успешной деканюляции требуется несколько повторных операций наружным доступом; лечение может затягиваться на десятки лет [22]. Противопоказаниями к операции наружным доступом являются незаконченный процесс рубцевания, тяжелые поражения ЦНС, заболевания легких, неизлеченное первичное заболевание, невозможность послеоперационного наблюдения и лечения [11, 25].
В последние годы появились сообщения об устранении обширных стенозов гортани и трахеи у детей путем резекции стенозированного участка с последующим наложением межтрахеального и гортаннотрахеального анастомозов [30, 39]. Показанием к операции является изолированный подскладковый или трахеальный стеноз, расположенный как минимум на 10 мм ниже голосовых складок; протяженность стеноза должна быть от 1 до 6 см [45]. При формировании анастомоза между гортанью и трахеей возникают значительные трудности из-за несоответствия размеров сшиваемых концов. Эти операции в основном используются при лечении взрослых больных; к настоящему времени отдаленные результаты такого лечения у детей еще не изучены (хотя эксперимент на кроликах показал адекватный рост дыхательных путей после резекции перстневидного хряща и первого кольца трахеи [47]), у них высок риск развития дигисценций в области анастомоза, повреждения возвратных нервов; кроме того, в случае неудачи операции дальнейшее лечение крайне затруднительно [18]. Даже незначительный отек тканей в месте анастомоза может вызывать у ребенка выраженный дыхательный стеноз, связанный с малым диаметром трахеи; при этом трахея ребенка менее толерантна к растяжению, чем у взрослого, в связи с чем резекция у ребенка возможна лишь на относительно меньшей, по сравнению со взрослым, части трахеи [21]. По мнению В. Г. Зенгера (2001), при циркулярной резекции трахеи и дополнительной мобилизации подъязычной кости происходит вмешательство в очень сложный механизм, обеспечивающий одну из важнейших функций гортани — защитную, так как возникает опасность проявления аспирационных осложнений. В случае возникновения осложнений необходимо дополнительное разобщение отрезков воздухопроводящих путей, т. е. выполнение трахеостомии и введение трахеальной канюли с раздувной манжеткой, что сводит на нет все преимущества столь сложной и небезопасной для больного операции. Поэтому возможность частичной резекции дыхательных путей с наложением анастомоза должна рассматриваться лишь в качестве крайнего варианта [3].
В случае возникновения осложнений необходимо дополнительное разобщение отрезков воздухопроводящих путей, т. е. выполнение трахеостомии и введение трахеальной канюли с раздувной манжеткой, что сводит на нет все преимущества столь сложной и небезопасной для больного операции. Поэтому возможность частичной резекции дыхательных путей с наложением анастомоза должна рассматриваться лишь в качестве крайнего варианта [3].
Несмотря на использование различных по технике операций, эффективность устранения рубцового стеноза гортани и деканюляции достигает, согласно наблюдениям различных авторов, 63–64 % [5, 11, 18, 43]. На эффективность лечения влияют степень сужения дыхательных путей и протяженность стеноза: если при стенозе гортани до 70% просвета удается деканюлировать до 100% детей, то при полной атрезии органа эффективность оперативного вмешательства снижается до 67% деканюлированных больных (в том числе и после повторных операций) [46]; кроме того, чем короче стенозированный участок, тем результативнее лечение [12]. По мнению B. Benjamin (1993), при сочетанном поражении складкового и подскладкового отделов гортани, особенно при их тотальной облитерации рубцовой тканью, реконструктивные операции достигают успеха приблизительно в 50% случаев.
Литература
- Богомильский М. Р., Гаращенко Т. И., Онуфриева Е. К. и др. Эндоскопическое применение хирургических лазеров при стойких обструктивных процессах в гортанной части глотки, гортани и трахее у детей // Вестник оторинолар. 1999. № 1. С. 39-41.
- Зенгер В. Г., Наседкин А. Н. Повреждения гортани и трахеи. М.: Медицина, 1991. 221 с.
- Зенгер В. Г. К вопросу о восстановлении просвета гортани после ее циркулярной резекции с последующей окклюзией и хроническим канюленосительством / Заболевания голосового аппарата и верхних дыхательных путей / Юбилейный сб. науч. трудов симпозиума, посвященного 10-летию Ассоциации фониатров и фонопедов, 24-27 мая 2001 г. (г. Владимир).
 Москва — Владимир, 2001. С. 193-196.
Москва — Владимир, 2001. С. 193-196. - Петухова Л. И., Солдатский Ю. Л., Быковский В. А., Романов Д. В. Ультразвуковые аспекты диагностики заболеваний гортани у детей младшего возраста // Эхография. 2000. Т. 1. № 3. С. 330-334.
- Понкратенко А. Д., Онуфриева Е. К. Отдаленные результаты эндоскопической СО2 -лазерной хирургии рубцовых стенозов гортани у детей // Вестник оторинолар. 1997. № 4. С. 16-19.
- Понкратенко А. Д., Солдатский Ю. Л., Нурмухаметов Р. Х. Применение стентов в СО2-лазерной эндоскопической хирургии рубцовых стенозов гортани у детей // Новости оториноларингологии и логопатологии. 1998. № 1. С. 80-83.
- Руин А. Г. Проблемы деканюляции у детей с хроническим трахеальным канюленосительством при рубцовых стенозах гортани и шейного отдела трахеи: Автореф. дис. … канд. мед. наук. М., 2000. 20 с.
- Савин А. Н. Ларингопластика с редрессацией задней стенки гортани при рубцовых и паралитических стенозах. Автореф. дис. … канд. мед. наук. СПб., 1997. 22 с.
- Солдатский Ю. Л., Понкратенко А. Д., Онуфриева Е. К. Лазерная хирургия постинтубационных стенозов гортани у детей младшего возраста // Лазерная медицина. 1999. Т. 3. № 2. C. 18-21.
- Фадеева И. А. Гортанно-кардиальные взаимодействия у детей // Новости оториноларингологии и логопатологии. 1998. № 1. С. 84-89.
- Цветков Э. А. Современные проблемы этиологии и лечения рубцовых стенозов гортани у детей // Новости оториноларингологии и логопатологии. 1996. № 3-4. С. 76-78.
- Чирешкин Д. Г., Зенгер В. Г., Онуфриева Е. К., Шустер А. М. Об оптимизации хирургического лечения детей с приобретенным рубцовым стенозом гортани и шейного отдела трахеи // Вестник оторинолар. 1991. № 6. С. 47-51.
- Чирешкин Д. Г. Хроническая обструкция гортанной части глотки, гортани и трахеи у детей. Этиология, клиника и методы устранения. М.: Рапид-Принт. 1994. 144 с.
- Benjamin B. Prolonged intubation injuries of the larynx: endoscopic diagnosis, classification, and management //Ann Otol Rhinol Laryngol.
 1993.Vol. 102. № 4. Pt 2. Suppl. 160. 15 p.
1993.Vol. 102. № 4. Pt 2. Suppl. 160. 15 p. - Brown O. E., Manning S. C. Microbial flora of the subglottis in intubated pediatric patients // Int. J. Pediatr Otorhinolaryngol. 1996. Vol. 35. № 2. P. 97-105.
- Choi S. S., Zalzal G. H. Pitfalls in laryngotracheal reconstruction // Arch. Otolaryngol. Head Neck. Surg. 1999. Vol. 125. № 6. P. 650-653.
- Cotton R. T., Myer C. M. 3d, O’Connor D. M., Smith M. E. Pediatric laryngotracheal reconstruction with cartilage grafts and endotracheal tube stenting: The single-stage approach // Laryngoscope. 1995. Vol. 105. № 8. Pt. 1. P. 818-821.
- Cotton R. T. Management of subglottic stenosis // Otolaryngol. Clin. Norht. Am. 2000. Vol. 33, № 1. P. 111-130.
- De Jong A. L., Park A. H., Raveh E., Schwartz M. R., Forte V. Comparsion of thyroid, auricular, and costal cartilage donor sites for laryngotracheal reconstruction in an animal model // Arch. Otolaryngol. Head. Neck. Surg. 2000. Vol. 126. № 1. P. 49-53.
- Gaissert H. A., Grillo H. C., Mathisen D. J., Wain J. C. Temporary and permanent restoration of airway continuity with the tracheal T tube // J. Thorac. Cardiovasc. Surg. 1994. Vol. 107. № 2. P. 600-606.
- Grillo H. C. Pediatric tracheal problems // Chest Surg Clin North Am. 1996. Vol. 6. № 4. P. 693-700.
- Gustafson L. M., Hartley B. E. J., Cotton R. T. Acquired total (grade 4) subglottic stenosis in children //Ann. Otol. Rhinol. Laryngol. 2001. Vol. 110. № 1. P. 16-19.
- Holinger L. D., Lusk R. P., Green C. G. Pediatric laryngology and bronchoesophagology. Philadelphia-New York: Lippincott-Raven, 1997. 402 p.
- Keghian J., Lawson G., Orban D., Remacle M. Composite hyoid-sternohyoid interposition graft in the surgical treatment of laryngotracheal stenosis // Eur. Arch. Oto-Rhino-Lar. 2000. Vol. 257. № 10. P. 542-547.
- Lesperance M. M., Zalzal G. H. Laryngotracheal stenosis in children // Eur Arch Otorhinolaryngol.
 1998. Vol. 255. № 1. P. 12-17.
1998. Vol. 255. № 1. P. 12-17. - McCaffrey T. V. Management of laryngotracheal stenosis on the basis of site and severity // Otolaryngol. Head. Neck. Surg. 1993. Vol. 109. № 3. Pt 1. P. 468-473.
- McGuirt W. F. Jr., Little J. P., Healy G. B. Anterior cricoid split. Use of hyoid as autologous grafting material // Arch. Otolaryngol. Head. Neck. Surg. 1997. Vol. 123. № 12. P. 1277-1280.
- McQueen C. T., Shapiro N. L., Leighton S., Guo X. G., Albert D. M. Single-stage laryngotracheal reconstruction. The Great Ormond experience and guidelines for patient selection // Arch. Otolaryngol. Head. Neck. Surg. 1999. Vol. 125. № 3. P. 320-322.
- Mehta A. C., Harris R. J., De Boer G. E. Endoscopic management of binign airway stenosis // Clin. Chest. Med. 1995. Vol. 16. № 3. P. 401-413.
- Monnier P., Lang F., Savary M. Partial cricotracheal resection for severe pediatric subglottic stenosis: update of the Lausanne experience // Ann Otol. Rhinol. Laryngol. 1998. Vol. 107. № 11, Pt. 1. P. 961-968.
- Morar P., Singh V., Jones A. S., Hughes J., van Saene R. Impact of tracheotomy on colonization and infection of lower airways in children requiring long-term ventilation: a prospective observational cohort study // Chest. 1998. Vol. 113. № 1. P. 77-85.
- Myer C. M.3d, Hartley B. E .J. Pediatric laryngotracheal surgery // Laryngoscope. 2000. Vol. 110. № 11. P. 1875-1883.
- Pereira K. D., Mitchell R. B., Younis R. T., Lazar R. H. Subglottic stenosis complicating cardiac surgery in children // Chest. 1997. Vol. 111. № 6. P. 1769-1772.
- Perkins J. A., Inglis A. F. Jr., Richardson M. A. Iatrogenic airway stenosis with reccurrent respiratory papillomatosis // Arch. Otolaryngol. Head. Neck. Surg. 1998. Vol. 124. № 3. P. 281-287.
- Randestad A., Lindholm C. E., Fabian P. Dimensions of the cricoid cartilage and the trachea // Laryngoscope. 2000. Vol. 110. № 11.
 P. 1957-1961.
P. 1957-1961. - Richtsmeier W. J., Scher R. L. Telescopic laryngeal and pharyngeal surgery // Ann. Otol. Rhinol. Laryngol. 1997. Vol. 106. № 12. P. 995-1001.
- Rimell F. L., Dohar J. E. Endoscopic management of pediatric posterior glottic stenosis // Ann. Otol. Rhinol. Laryngol. 1998. Vol. 107. № 4. P. 285-290.
- Rutter M. J., Link D. T., Liu J. H., Cotton R. T. Laryngotracheal reconstruction and the hidden airway lesion // Laryngoscope. 2000. Vol. 110. № 11. P. 1871-1874.
- Rutter M. J., Hartley B. E. J., Cotton R. T. Cricotracheal resection in children // Arch. Otolaryngol. Head. Neck. Surg. 2001. Vol. 127. № 3. P. 289-292.
- Silva A. B., Lusk R. P., Muntz H. R. Update on the of auricular cartilage in laryngotracheal reconstruction // Ann. Otol. Rhinol. Laryngol. 2000. Vol. 109. № 4. P. 343-347.
- Stern Y., Willging P. J., Cotton R. T. Use of Montgomery T-tube in laryngotracheal reconstruction in children: is it safe? // Ann. Otol. Rhinol. Laryngol. 1998. Vol. 107. № 12. P. 1006-1009.
- Tostevin P. M., de Bruyn R., Hosni A., Evans J. N. The value of radiological investigations in pre-endoscopic assessment of children with stridor // J. Laryngol. Otol. 1995. Vol. 109. № 9. P. 844-848.
- Triglia J. M., Nicollas R., Roman S. Management of subglottic stenosis in infancy and childhood // Eur. Arch. Oto-Rhino-Lar. 2000. Vol. 257. № 7. P. 382-385.
- Walner D. L., Ouanounou S., Donnelly L. F., Cotton R. T. Utility of radiographs in the pediatric airway obstruction // Ann. Otol. Rhinol .Laryngol. 1999. Vol. 108. № 4. P. 378-383.
- Walner D. L., Stern Y., Cotton R.T. Margins of partial cricotracheal resection in children // Laryngoscope. 1999. Vol. 109. № 10. P. 1607-1610.
- Ward R. F., Gordon M., Rabkin D., April M. M. Modifications of airway reconstruction in children // Ann. Otol. Rhinol. Laryngol. 1998. Vol. 107. № 5. Pt 1.
 P. 365-369.
P. 365-369. - Ward R. F., Triglia J. M. Airway growth after cricotracheal resection in a rabbit model and clinical application to the treatment of subglottic stenosis in children // Laryngoscope. 2000. Vol. 110. № 5. P. 835-844.
- Werkhaven J. A., Beste D. Diagnosis and management of pediatric laryngeal stenosis // Otolaryngol. Clin. North Am. 1995. Vol. 28. № 4. P. 797-808.
- Wetmore R. F., Marsh R. R., Thompson M. E., Tom L. W. C. Pediatric tracheotomy: a changing procedure? // Ann. Otol. Rhinol. Laryngol. 1999. Vol. 108. № 7. Pt 1. P. 695-699.
- Zalzal G. H., Choi S. S., Patel K. M. Ideal timing of pediatric laryngotracheal reconstruction // Arch. Otolaryngol. Head. Neck. Surg. 1997. Vol. 123. № 2. P. 206-208.
Стеноз гортани у детей как следствие ОРВИ. Что делать? | ЕвроМед клиника
По статистике при ОРВИ примерно треть детей младше трех лет страдают от стеноза – отека гортани. С чем это связано?
— Действительно, стеноз встречается очень часто.
Стенозирующий ларингит/ларинготрахеит (или ложный круп — в педиатрии это синонимы) — нарушение нормального дыхания за счет сужения просвета гортани.
Ложный круп или стеноз гортани, который развивается у детей на фоне ОРВИ, возникает потому, что у малышей в подскладочном отделе гортани очень рыхлая слизистая оболочка, и подслизистый слой очень легко отекает. При вирусной инфекции развивается отек слизистой оболочки верхних дыхательных путей, и в случае возникновения отека в гортани резко сужается свободное пространство в ее просвете, нарушается прохождение воздуха, затрудняется, становится шумным вдох, развивается, так называемая, инспираторная (затруднение вдоха) одышка. У детей до 3-4-летнего возраста особенности анатомического строения таковы, что создают предпосылки для легкого развития стеноза гортани, поэтому и встречается это состояние чаще именно в этом возрасте. Дополнительный риск создает предрасположенность ребенка к развитию аллергических реакций. В этом случае частота развития стеноза гортани выше.
В этом случае частота развития стеноза гортани выше.
Стеноз можно классифицировать по скорости возникновения: молниеносный, острый, подострый и хронический.
Молниеносный стеноз, как правило, возникает при аллергии или из-за инородного тела.
При ложном крупе, чаще всего, возникает острый стеноз. Снять его проявления можно противоотечными средствами. Звук стеноза ни с чем на спутаешь — любая мама его услышит: затруднение вдоха, хриплый, сипящий звук. Как только вы обнаружили, что у ребенка затруднен вдох, надо дать ребенку антигистаминное (снимает отек) и сделать ингаляцию небулайзером гормональными препаратами и горячую ножную ванну (при условии отсутствия высокой температуры). Если ребенок задыхается и ингаляции не помогают, срочно вызывайте Скорую помощь! Врач введет гормон, если и это не поможет, тогда стеноз является показанием к госпитализации. Ребенка укладывают в стационар, в реанимацию, обеспечивают подачу кислорода, назначают лечение гормонами, антигистаминными препаратами, при необходимости — антибиотиками, добиваясь постепенного снижения отека во всех отделах верхних дыхательных путей.
После впервыевозникшего эпизода стеноза ребенка рекомендуется обследовать на предмет возможной аллергии — сдать аллергопробы, чтобы исключить или подтвердить диагноз. К сожалению, у маленьких детей аллергопробы могут быть ложноотрицательными. Если же стенозы рецидивирующие и продолжаются у ребенка старше трех лет надо обязательно Повторить обследование.
С уважением и заботой о Вас, команда «ЕвроМед клиники».
причины, симптомы и лечение заболевания
Никого не удивляют кашель и частые насморки у детей, тем более в холодное время года. Своеобразие детской физиологии и несовершенство иммунной системы организма ребенка делают его восприимчивым к респираторным заболеваниям, а все болезни проходят тяжелее, в отличие от взрослых. Наиболее острые проявления стеноза отмечаются у детей, которые склонны к аллергии. Кашель, начинающий переходить в удушье, это симптом сужения гортани – состояния, которое требует срочные мероприятия для облегчения дыхания малыша. Родители обязаны знать, как можно оказать помощь при стенозе у детей.
Кашель, начинающий переходить в удушье, это симптом сужения гортани – состояния, которое требует срочные мероприятия для облегчения дыхания малыша. Родители обязаны знать, как можно оказать помощь при стенозе у детей.
Стеноз гортани у детей: что это такое?
Стеноз – это респираторная болезнь, при которой происходит воспалительный процесс слизистой гортани. В данном органе находятся голосовые связки. Воспаление быстро переходит и на них, потому одним из основных симптомов заболевания является осиплость голоса.
У детей гортань более узкая, нежели у взрослых. Во время воспаления увеличивается объем слизистой, сужая еще больше просвет. Это осложняет дыхание. Наибольшую опасность стеноз гортани у детей представляет для малышей до 3-х лет.
Причины стеноза гортани у детей
Причинами могут являться:
- Аллергии на табачный дым, какие-либо продукты, растения, шерсть животных, препараты бытовой химии.
- Поражение вирусной инфекцией при кори, гриппе, ОРВИ, коклюше, скарлатине. Появлению заболевания этой природы способствует слабый иммунитет у малыша, переохлаждение, простуда, частые ангины.
- Врожденные нарушения слизистой гортани, которые, как правило, к 3 годам проходят. Однако до этого вероятно периодическое повторение стеноза гортани у детей.
- Реакция ЦНС на сильное волнение.
- Лечение ангины и насморка при помощи спреев. Средства, которые впрыскиваются под давлением, проникая в горло, могут вызвать спазм голосовых связок и гортани.
- Врожденные особенности строения носоглотки и гортани.
- Попадание инородного тела в трахею.
- Сильное напряжение голосовых связок во время громкого крика.
- Загазованность, запыленность, повышенная температура и пониженная влажность окружающего воздуха.
Основные симптомы стеноза гортани у детей
Болезнь, как правило, начинается с появления в горле боли и насморка. Во время осмотра оказывается, что горло отекшее и красное. Появляется лающий характерный кашель, который связан с зудом и раздражением слизистой в горле. Поначалу кашель бывает сухим и сильным. Со временем проявляется мокрота, в ней могут находиться сгустки крови. Малышу сложно дышать из-за отека гортани. Вероятно увеличение температуры. У ребенка появляется сухость во рту, болит голова. Над верхней губой при кашле появляется синюшный треугольник.
Во время острой формы заболевания у ребенка ярко выражены симптомы. При переходе на хроническую стадию малыша беспокоит чаще всего першение в горле, появляется постоянная потребность откашляться. Изменяется тембр голоса.
Так как ребенок еще не может толком сказать, в каком месте болит, взрослые обязаны особенно внимательно относиться к разным изменениям в состоянии малыша. К общим симптомам ОРЗ, таким как повышенная капризность, вялость, насморк, добавляются свист, синева между носом и ротиком, шумы в области дыхательных путей, хриплый сильный кашель.
Вероятные осложнения
Опасность этого заболевания заключается в том, что стеноз быстро развивается и может давать тяжелые осложнения. Самым частым из них является удушье, оно наиболее характерно для патологии, которая возникает из-за аллергии. Это осложнение также может появиться у грудничков по причине несовершенства дыхательной системы.
Во время инфекционных болезней дыхательных верхних путей вероятно появление приступов ложного крупа. Гнойный воспалительный процесс вызывает заражение крови, переходит на легкие, мышцы шеи.
Степени сужения
Стеноз или нарушение дыхания, который появляется вследствие уменьшения просвета гортани и отечности слизистой, быстро развивается. Причем наблюдать можно поэтапное ухудшение здоровье.
- Стеноз первой степени (компенсация). Малыш не задыхается, однако можно отметить, что во время дыхания начинают участвовать мышцы живота выше пупка и грудины. С этим состоянием организм сможет сам справиться на протяжении нескольких дней.
- Стеноз второй степени (субкомпенсация). Ребенок становится более возбужденным, бледнеет, учащается сердцебиение, появляется носогубный синюшный треугольник. Малышу не хватает кислорода, он дышит животом и всей грудью. Это состояние может длиться 2-3 дня.
- Стеноз третьей степени (некомпенсированный). Дыхание шумное, выдох и вдох проводятся с трудом, выступает пот, ногти и губы синеют. Понижается давление, наблюдается аритмия. Втягивается нижняя часть грудины.
- Стеноз четвертой степени (асфиксия). Появляются судороги, сердцебиение замедленное, дыхание поверхностное, из-за кислородной недостаточности и большого количества в крови углекислого газа происходит потеря сознания.
Отечность гортани появляется вследствие полного или частичного воспалительного процесса слизистой оболочки из-за действия какого-то аллергена (бытовой пыли, растительной пыльцы). У малыша могут внезапно появиться симптомы асфиксии, ему больно глотать, грубеет голос.
Когда необходимо непременно звонить в скорую помощь?
Так как заболевание развиваться может довольно быстро, тем более у новорожденных детей, то во время первых симптомов затруднения дыхания взрослые обязаны немедленно обратиться в скорую помощь, а до приезда принять мероприятия для избавления от спазма гортани.
Когда у малыша появляется одышка, прерывистое дыхание и лающий кашель, это может приводить к быстрому прогрессированию стеноза и развитию сердечной недостаточности. Лечение во время стеноза 2-4 степени нуждается в госпитализации. Тем более большой риск резкого обострения заболевания у аллергиков, а также у малышей, которые имеют нервно-психические расстройства.
Такие симптомы, как одышка вместе с увеличенной температурой, частое покашливание могут являться тревожными признаками острого развивающегося стеноза. Чтобы начать правильное лечение нужно разобраться срочно в причине.
Первая помощь во время приступа стеноза
До приезда скорой помощи для облегчения дыхания и снятия спазма гортани малышу нужно подышать паром. Для чего в ванной можно включить горячую воду, для того чтобы собрался пар, и побыть в ней с ребенком. Дети постарше могут подышать над кастрюлей с картофельным отваром или с раствором соды. Паром дышать надо 7-12 минут в несколько приемов с коротким перерывом. При этом дыхание облегчается, образуется мокрота, сухой кашель ослабевает.
Смогут помочь и такие процедуры:
- Ребенок обязан пить большое количество воды. Желательно ему давать простую воду с добавлением незначительного количества соды или минеральную воду без газа.
- Снижает отечность гортани ванночка для ног с теплой водой. После этой процедуры ребенку нужно надеть теплые носки.
- Немаловажно успокоить ребенка, отвлечь его чем-то, поскольку плач и переживание лишь усилят спазм гортани.
- Дать малышу папаверин или но-шпу, которые снимают спазмы, а также антигистамины (к примеру, супрастин), для понижения чувствительности к аллергенам. Желательно выполнить инъекцию внутримышечно.
- Нужно срочно увлажнить воздух в помещении, если он очень сухой (развесить мокрые полотенца или поставить тазик с водой, разбрызгать воду).
Домашнее лечение
Если доктор необходимым не считает в стационаре держать ребенка, то производится в домашних условиях лечение стеноза. Причем нужно, чтобы выполнялся непременно постельный режим.
- Малыш не должен часто говорить. Чрезмерная нагрузка на связки приводит к их неправильному формированию. В дальнейшем у ребенка появляется сиплый голос.
- Нужно следить за чистотой помещения, свежестью и влажностью воздуха. Ребенок не должен пользоваться мягкими игрушками, поскольку в них скапливается пыль.
- Нужно часто поить. Если заболевание имеет аллергическую этиологию, то нельзя ни в коем случае давать травяные чаи, соки, компоты. Пища обязана быть не раздражающей слизистую и витаминизированной.
- Для лечения от сухого кашля в домашних условиях выполняют ножные горчичные ванночки, на спинку прикладываются горчичники. Производится физиотерапия в форме ингаляций над отваром картофеля с добавлением эвкалипта и мяты. Народные способы лечения рекомендуют применять для ингаляции настои ромашки, сосновых почек, календулы.
- С такой же целью используется раствор из 3 ч.л. соды, 3 ст.л. морской соли в одном литре воды. В него добавляется пару капель йода.
- Для снятия воспалительного процесса ребенку нужно горло полоскать настоем шалфея, зверобоя, ромашки. Они имеют сильное противовоспалительное свойство, при этом позволяют выводить мокроту. Горло полоскать также можно теплой водой с медом или соком свеклы.
- На шею в район гортани можно накладывать водяные согревающие компрессы.
Внимание: если причина появления заболевания неизвестна, то запрещается использовать растительные препараты для компрессов, полоскания горла или ингаляции, поскольку спазм гортани может являться аллергической реакцией. Перед тем как использовать какие-либо народные способы для устранения симптомов стеноза, необходимо сделать общий анализ крови на лейкоциты, анализ крови на вирусы, а также посоветоваться с врачом. Вероятно, также нужно будет выполнить пробы на разные аллергены.
Применение медикаментозных средств
По назначению врача используются различные средства, которые оказывают жаропонижающее, отхаркивающее, антиаллергенное, противовоспалительное воздействие. В каждом определенном случае подбирается индивидуально дозировка с учетом веса и возраста малыша.
- Жаропонижающие препараты. Сюда относятся эффералган, парацетамол, панадол. Для новорожденных детей изготавливаются сиропы и свечи, удобные в использовании.
- Отхаркивающие препараты. Используется либексин (с трех лет), гербион с подорожником (с двух лет), капли стоптуссин-фито (с полугода). Эти средства применяются при сухом кашле. Для дальнейшего устранения влажного кашля применяются амбробене, лазолван, бронхосан.
- Если известно точно, что причина болезни – бактериальная инфекция, то врач назначает антибиотик.
- Антигистаминные препараты. Самыми распространенными являются капли цетрин, зодак (с шести лет), кларитин (с двух лет), зиртек, фенистил (для грудничков).
- Противовоспалительные препараты. Применяются противовоспалительные нестероидные средства: ибупрофен и аналоги этого средства (нурофен, ибуфен).
Стационарное лечение
Если состояние малыша нестабильно, отмечаются симптомы стеноза 2-4 степени, то лечение производится лишь в поликлинике. После избавления от острого приступа удушья используются средства для избавления от сухого кашля и жара, выполняются ингаляции. С помощью капельницы вводятся препараты для снятия в горле отеков и воспаления. Если определится, что процесс воспаления в гортани появился из-за бактериального поражения, то для лечения прописываются антибиотики.
Во время четвертой степени стеноза детей происходит лечение в отделении реанимации. В очень тяжелом случае, если происходит асфиксия, то выполняют надрез под щитовидкой и устанавливают дыхательную трубку в саму трахею. Затем как улучшится состояние, убирают трубку.
Профилактика заболевания
Для того чтобы не допустить появления этой болезни, нужно снизить максимально контакт малыша с аллергенами, если у него отмечаются симптомы непереносимости каких-то продуктов или веществ.
Бактерии могут с легкостью попасть в гортань, если имеются больные зубы, воспалены миндалины, аденоиды. Если малыш постоянно дышит лишь ртом, то у него начинает пересыхать слизистая, что создает условия для быстрого развития и проникновения инфекции. Потому важно своевременно проверять состояние зубов и лечить ЛОР-заболевания.
Нужно с рождения закаливать ребенка, следить за его физическим правильным развитием. В помещении соблюдать нормальные гигиенические и санитарные условия. Малыш обязан хорошо высыпаться, так как это требуется для укрепления нервной системы. Здоровое питание поспособствует улучшению иммунитета.
Лечение стеноза гортани в Израиле
Терапия ларингеального стеноза в израильских клиниках базируется на широком применении малоинвазивных методик эндоскопической лазерной ларингопластики в комбинации с установкой стентов. Также наши ЛОР-хирурги практикуют чрескожную ларингостомию и конвенциональные открытые операции на гортани.
Получить цены в клинике
Методика терапии стеноза в Топ Ихилов
Стеноз гортани и трахеи, или ларингеальный стеноз, – врожденное либо приобретенное заболевание, характеризующееся патологическим сужением дыхательных путей в области гортани.
Врожденный стеноз гортани возникает примерно на 10-й неделе внутриутробного развития в результате нарушения процесса формирования просвета гортани и представляет порядка 5% всех врожденных аномалий дыхательных путей. Приобретенный стеноз является результатом постепенных морфологических изменений в гортани и близлежащих тканях. Причины хронического стеноза разнообразны – это могут быть травмы и инфекции гортани, компрессионное воздействие со стороны новообразований и прочие аномалии.
К симптомам ларингеального стеноза относятся более глубокий по сравнению с обычным вдох, уменьшение пауз между вдохом и выдохом, снижение частоты пульса. На фоне хронической гипоксии могут развиваться бронхиты, эмфизема, воспаление легких (у детей), могут увеличиваться размеры сердца, возникают другие осложнения. Лечение стеноза гортани выполняется двумя методами – хирургическим и эндоскопическим.
Современные методы эндоскопического лечения ларингеального стеноза включают в себя различные техники дилатации просвета гортани, лазерную эксцизию рубцовой ткани, ее удаление с последующим стентированием или инъекциями в прооперированную область кортизона. Эндоскопическое лечение показано при небольших размерах рубцовой ткани, отсутствии бактериальных инфекций и некоторых других осложняющих лечение факторах.
При лазерном удалении рубцовой ткани применяются современные углекислотные эндоскопические лазеры, а сама операция делится на два этапа. На первом этапе удаляется одна часть рубцового образования, а через 2 месяца – оставшаяся. Под воздействием лазера патологическая фиброзная ткань испаряется, что уменьшает кровопотерю. Чтобы предотвратить формирование нового рубца на месте удаленных тканей гортани, сразу же после лазерной эксцизии на рану наносится алкилирующее цитостатическое средство, способное останавливать деление клеток.
Еще одним эффективным эндоскопическим методом лечения стеноза является баллонная дилатация с использованием 10-14-миллиметровых баллонов за 1 или 2 последовательные процедуры (с промежутком в 7 дней). По нашим наблюдениям, пациенты после такой процедуры демонстрируют устойчивую ремиссию на промежутке до 30 месяцев и более.
Конвенциональные хирургические методы лечения включают в себя проведение трахеотомии – вскрытия гортани и создания искусственного пути для доступа воздуха в легкие, минуя суженный участок гортани. Это одна из наиболее древних хирургических процедур. Первые упоминания о подобных операциях можно найти в исторических документах, датированных еще вторым веком до нашей эры.
Одним из наиболее эффективных методов проведения данной операции является чрескожная дилатационная трахеостомия. По результатам множества клинических исследований, такая операция сравнима по своей эффективности с конвенциональной открытой трахеотомией, но позволяет использовать разрезы меньшего размера, меньше травмировать ткани гортани, понизить риск инфицирования и стоимость лечения. При проведении операции хирург устанавливает в полости трахеи с помощью катетера трубку, через которую трахея сообщается с внешней средой. Трубка одним концом выводится наружу и закрепляется в полости трахеи баллонной манжетой.
Открытая операция показана при стенозе 3-4 степени и включает удаление рубцовой ткани, а также оперативные мероприятия по предотвращению рубцевания прооперированного участка и рецидива стеноза. При этом могут использоваться хрящевые графты, позволяющие расширить просвет в обрасти гортани. В ряде случаев для стабилизации реконструированного участка гортани используются стенты – полые трубки различной длины, предотвращающие образование новой фиброзной ткани (особенно часто стенты используются, если для расширения просвета гортани использовались хрящевые графты). Эндотрахеальный стент устанавливается лишь на время. Так, после проведения одностадийной ларинготрахеопластики его удаляют уже через 7 дней, в других случаях стент может быть удален через 3-6 месяцев. Устанавливаемые в нашей клинике стенты выполнены из тефлона – прочного и инертного материала, обеспечивающего легкое извлечение стента.
После операции проводится терапия кортикостероидами, за пациентом ведется наблюдение, которое в частности может быть направлено на предотвращение развития пневмоторакса и гематом шеи. На протяжении 2-3 недель проводится терапия антибиотиками. Каждые 4 недели пациенту рекомендуется проходить профилактическую эндоскопию для наблюдения за положением стента и процессом формирования грануляционных тканей.
Диагностика стеноза гортани в Израиле
Диагностика стеноза гортани в Израиле базируется на оценке симптоматики и данных инструментальных исследований, в большинстве случаев она занимает 3-4 дня.
Первый день – приезд в клинику
После встречи в аэропорту с куратором-переводчиком пациент в его сопровождении отправляется на консультацию к ведущему ЛОР-специалисту. Врач проводит первичный осмотр и выписывает направления на диагностические процедуры.
Второй день – исследования
Второй день целиком отводится на назначенное врачом обследование.
- Эндоскопия гортани – исследование просвета и состояния слизистой оболочки гортани с помощью гибкой трубки с миниатюрной камерой на конце (основной метод диагностики стеноза).
- КТ используется для установления причин стеноза (новообразования, патологии хрящевой ткани, воспалительные процессы и т. д.).
- МРТ по информативности несколько превосходит КТ и, в отличие от последней, при МРТ-сканировании не используется рентгеновское излучение.
Третий день – выбор метода терапии
В последний день диагностики ведущий отоларинголог получает результаты обследования, анализирует их и подбирает методы лечения. Ему помогает экспертная группа врачей, которые на консилиуме принимают решение по поводу индивидуальной терапевтической программы.
Лечение стеноза гортани в Израиле – цены
Лечение стеноза гортани в Израиле по стоимости значительно отличается от стоимости в клиниках Канады, Великобритании, стран Западной Европы или Соединенных Штатов. Например, полный курс лечения стеноза в нашем медицинском центре обходится дешевле на 35-45% по сравнению с Германией и США.
Узнайте все о ценах на необходимые в вашем случае процедуры у наших консультантов – оставьте заявку или свяжитесь с нами по телефону.
Рассчитать стоимость лечения
Причины популярности Топ Ихилов – это наши преимущества
Показатель того, насколько эффективно проводится лечение стеноза гортани в Израиле, – отзывы медицинских туристов, которые уже прошли курс терапии в Топ Ихилов. В своих письмах они выражают признательность отоларингологам нашей клиники, делятся впечатлениями от израильской медицины.
- В клинике Топ Ихилов работают опытные ЛОР-специалисты, каждый из них прошел длительную специализацию в своей области.
- Эндоскопическое лечение с использованием микроскопической техники и местной кортикостероидной терапии позволяет не только восстановить нормальный просвет гортани, но и сохранить (а в ряде случаев – значительно улучшить) голосовую функцию.
- Современная диагностическая аппаратура (эндоскопическая, томографическая и т. д.) позволяет выявлять стеноз на ранних стадиях, следить за состоянием пациента после хирургического лечения.
- Каждый гость клиники на всем протяжении лечения получает полную поддержку со стороны международного отдела и представляющего его интересы куратора-переводчика. Персональный для каждого пациента куратор координирует врачей и решает любые вопросы – организационного, бытового и языкового характера.
- 5
- 4
- 3
- 2
- 1
(0 голосов, в среднем: 5 из 5)
Подсвязочный стеноз | Детская больница Филадельфии
Подсвязочный стеноз (SGS) — это сужение дыхательных путей ниже голосовых связок (над голосовыми связками) и над трахеей. Подсвязочный стеноз будет включать сужение перстневидного хряща, единственного полного хрящевого кольца в дыхательных путях. Это сужение часто вызывается рубцами в гортани чуть ниже голосовых связок, но также может затрагивать голосовые связки и влиять на голос.
Подсвязочный стеноз бывает двух форм: приобретенный и врожденный.
Эндоскопический вид врожденного стеноза подсвязочного канала.
- Приобретенный стеноз подсвязочного канала часто возникает после длительных периодов интубации и вентиляции при респираторных заболеваниях.
- Врожденный стеноз подсвязочного канала возникает как редкий врожденный дефект и может быть связан с другими генетическими синдромами и состояниями. Дыхательные пути остаются узкими, потому что хрящ дыхательных путей не сформировался должным образом до рождения.
Точная причина рубцевания в настоящее время неизвестна.В отдельных отделениях интенсивной терапии новорожденных только небольшое количество младенцев, у которых развивается это состояние, и недостаточно пациентов в каждом отдельном отделении, чтобы иметь статистически значимые данные. Чтобы лучше понять причину стеноза подсвязочного канала, необходимы многоцентровые исследования.
Однако текущие данные свидетельствуют о том, что к ряду важных факторов риска относятся длительная интубация, низкий вес при рождении, рефлюкс, сепсис и другие. Кроме того, трахеостомия может вызвать стеноз или малацию (размягчение) в месте трахеостомии, особенно если она расположена высоко в трахее.
Признаки подсвязочного стеноза включают:
- Шумное дыхание (стридор)
- Респираторный дистресс
- Повторяющийся круп
- Невозможность дышать без трахеостомической трубки
Рентгенограмма шеи показывает подсвязочное сужение (стрелки).
Для постановки диагноза важна история конкретных факторов риска. Ваш врач будет искать причины респираторного дистресс-синдрома в отношении длительной интубации и вентиляции, крайней степени недоношенности, низкого веса при рождении, хронической бронхолегочной дисплазии (заболевания легких) и гастроэзофагеального рефлюкса.
Дальнейшее обследование проводится с помощью рентгеновских лучей. Рентген шеи может выявить подсвязочные сужения или подсвязочные образования. На этих снимках трахею оценивают на предмет сужения или стеноза трахеи или полных колец. Окончательный диагноз ставится при эндоскопии с микроларингоскопией и бронхоскопией.
Хирург может определить размер дыхательных путей с помощью пластиковой эндотрахеальной трубки. Степень тяжести стеноза подсвязочного канала классифицируется, как показано на рисунке выше.
Оценка аэродинамического пищеварения
Во время посещения центра дыхательных путей ваш ребенок пройдет обследование у детского гастроэнтеролога, а также оценку питания.Детский пульмонолог также может оценить состояние легких вашего ребенка, а терапевт по речи и глотанию может оценить глотание и голос. Эти специалисты оценят вашего ребенка и определят необходимость дальнейших обследований. Наша группа по планированию хирургического вмешательства организует полное эндоскопическое обследование и обследование желудочно-кишечного тракта в операционной. Это будет включать микроларингоскопию, бронхоскопию (MLB) и эндоскопию верхних отделов желудочно-кишечного тракта (EGD), исследование импедансного зонда и легочные осциллографы.
Во время EGD биопсии будут взяты с нескольких уровней вверх и вниз по пищеварительному тракту, и они будут проверены на наличие признаков воспаления, указывающих на рефлюкс (ГЭРБ) или воспаление пищевой аллергии (эозинофильный эзофагит).Пациент считается подходящим для операции на дыхательных путях, когда стеноз созрел, ГЭРБ находится под контролем и состояние легких стабильно. Если ГЭРБ не находится под контролем, тогда лечение пациента может быть скорректировано или изменено, и потребуется повторное тестирование. В редких случаях может потребоваться антирефлюксная операция.
Кроме того, перед реконструктивной операцией на дыхательных путях ребенок будет проходить официальную оценку кормления, которая включает эндоскопическую оценку глотания (FEES), проводимую в офисе, или модифицированный глоток с барием.Если ваш ребенок не принимает пищу и полагается исключительно на зонд для кормления, то для обнаружения скопления и аспирации будет использоваться гибкий зонд с несколькими каплями зеленого красителя. Это необходимо для того, чтобы ваш ребенок мог хорошо глотать и защитить свои новые расширенные дыхательные пути после реконструкции. Если эти исследования выглядят достаточно нормально, тогда ребенку может быть проведено хирургическое лечение стеноза подсвязочного канала.
Лечение стеноза подсвязочного канала зависит от того, насколько серьезно он влияет на дыхание ребенка.Кроме того, другие заболевания пациента могут повлиять на решение о том, как лечить стеноз хирургическим путем. Существует множество вариантов лечения, которые зависят от этих и других факторов.
Лечение легких случаев
Система оценок стеноза подсвязочного канала.
Легкий стеноз подсвязочного канала: стеноз 1 и 2 степени, а также тонкие перепонки и полосы.
- Наблюдение. В самых легких случаях, когда пациенты могут оставаться бессимптомными, может потребоваться тщательное наблюдение.Чаще всего условия улучшаются со временем по мере роста дыхательных путей. Врожденный стеноз 1 степени часто проходит сам по себе и не требует вмешательства. Наблюдение имеет решающее значение для детей с легким стенозом подсвязочного канала, поскольку у них чаще возникают проблемы с дыханием при распространенных заболеваниях верхних дыхательных путей (простуда, бронхит).
- Эндоскопическая хирургия. В некоторых случаях стеноза легкой степени требуется эндоскопическое лечение. Тонкие перепонки можно разделить серповидным ножом и расширить с помощью баллона для ангиопластики.Более толстый стеноз также может быть расширен баллоном. Мягкий стеноз и стеноз подсвязочного канала, связанные с системными заболеваниями, такими как ГЭРБ и гранулематоз Вегенера, лучше всего лечить с помощью баллонной дилатации дыхательных путей. Лазеры и микродебридеры (вращающиеся лезвия с приводом, которые сбривают мягкие ткани) также используются для удаления сегментарных участков рубцовой ткани.
Лечение тяжелых случаев
Тяжелый стеноз подсвязочного канала: стеноз 3 и 4 степени.
Почти всем пациентам с тяжелым стенозом подсвязочного аппарата требуется трахеостомическая трубка для дыхания.Часто для коррекции стеноза и достижения деканюляции (удаления трахеостомической трубки) требуется открытая операция с операцией по восстановлению гортани и трахеи (LTR) или частичной резекцией крикотрахеального отдела (CTR).
Устранение подсвязочного стеноза
Обсуждение подсвязочного стеноза и его лечения — реконструкция гортани и трахеи
LTR. При операции по реконструкции гортани и трахеи хирург использует кусочки реберного хряща для расширения дыхательных путей. Хирург делает вертикальный разрез суженного дыхательного пути снаружи, чтобы восстановить поврежденный участок внутри.Хрящевым трансплантатам с помощью скальпеля придают эллиптическую форму. Задний (задний) трансплантат также имеет эллиптическую форму с выступом для фиксации его положения за срезанными краями перстневидного хряща (хряща). Трансплантаты могут быть размещены в переднем или заднем положении или в обоих одновременно. LTR может выполняться в один этап, когда трахеотомическая трубка удаляется во время операции, или в два этапа, когда операция выполняется с установленной трахеотомической трубкой. Когда дыхательные пути заживают, трахеотомическую трубку удаляют позже.Существуют определенные показания для одноэтапной или поэтапной операции LTR, и решение принимается индивидуально с учетом особенностей ребенка.
CTR. В наиболее тяжелых случаях может быть выполнена частичная резекция крикотрахеального отдела, когда рубцевание ограничивается подсвязкой и голосовые связки. В этой процедуре рубцовая ткань и большая часть переднего перстневидного хряща вырезаются, и вместо нее восстанавливается нормальная трахея. CTR также может выполняться одноэтапно в более простых ситуациях и поэтапно в более сложных случаях, таких как ревизионная операция.
Показатели долгосрочного успеха как LTR, так и CTR выдаются.
CHOP сообщил, что общий уровень деканюляции у детей, перенесших LTR заднего трансплантата, составляет 96 процентов. Это означает, что окончательная скорость деканюляции составляет 96 процентов, но некоторым детям может потребоваться более одной процедуры.
Мы обнаружили 70-процентную частоту деканюляции в зависимости от операции у пациентов, перенесших двухэтапный LTR. В конечном итоге 95 процентов этих пациентов деканюлированы. Скорость деканюляции для конкретной операции — это скорость успешной деканюляции после одной основной операции.
Мы обнаружили, что удельная скорость деканюляции составляет 92 процента для одноступенчатого LTR, а максимальная скорость деканюляции составляет 100 процентов. Эти результаты выгодно отличаются от других сообщений в литературе. Более того, общий уровень успеха зависит от многих факторов, включая патологию, состояние здоровья пациента и предыдущую неудачную операцию, а также другие неизвестные внутренние факторы.
Cheng J, Jacobs I. Ларинготрахеопластика с использованием трансплантата щитовидной железы и хряща для закрытия большого педиатрического кожно-трахеологического свища.International J Ped Otolaryngology. 2012 (в печати).
Дурден Ф., Соболь С. Баллонная ларингопластика как основное лечение стеноза подсвязочного канала. Arch Otolaryngol Head Neck Surg. 2007 август; 133 (8): 772-5.
Майер К., О’Коннор Д., Коттон Р. Предлагаемая система классификации стеноза подсвязочного канала на основе размеров эндотрахеальной трубки. Анн Отол Ринол Ларингол. 1994 апр; 103 (4, п.1): 319-23.
Rizzi MD, Thorne MC, Zur KB, Jacobs IN. Реконструкция гортани с использованием трансплантатов заднего реберного хряща: результаты в одном учреждении.Otolaryngol Head Neck Surg. 2009 Март; 140 (3): 348-53. Цитируется в PubMed; PMID 19248941.
Smith LP, Jur KB, Jacobs IN. Одноэтапная или двухэтапная реконструкция гортани и трахеи. Arch Otolaryngol Head Neck Surg. 2010 Янв; 136 (1): 60-5. Цитируется в PubMed; PMID 20083780.
Подсвязочный стеноз
Симптомы
Симптомы подсвязочного стеноза включают:
- Одышка при физической нагрузке и иногда в покое
- Шумное дыхание (стридор)
- Кашель
- Рецидивный круп
- Изменения голоса, например, охриплость
- Ощущение слизи в дыхательных путях
Причины стеноза подсвязочного канала
Стеноз подсвязочного канала может быть вызван травмой или инфекцией (приобретенной) или возникать при рождении (врожденный).
Врожденный стеноз подсвязочного канала возникает, когда хрящ дыхательных путей не развивается так, как должен был до рождения, и приводит к сужению дыхательных путей.
Приобретенный стеноз подсвязочного канала часто связан с длительным пребыванием в дыхательной трубке. Рубцы от давления трубки на дыхательные пути могут вызвать стеноз. Другие причины могут включать:
- Редкие заболевания, вызывающие воспаление дыхательных путей
- Травма, например, травма в результате вдыхания химического вещества или вещества, вызывающего ожоги
- Идиопатический (неизвестно)
Диагностика стеноза подсвязочного канала
Подсвязочный канал трудно увидеть и проверить в клинике.Детей часто безуспешно лечат от более распространенных заболеваний, таких как астма, до того, как будет поставлен диагноз подсвязочного стеноза.
Мы используем микроларингоскопию и бронхоскопию для диагностики стеноза подсвязочного канала у детей. Для этих тестов ваш ребенок ложится спать в операционной, и в дыхательные пути ребенка вводится специальный телескоп. Это используется для поиска сужения.
Мы также можем использовать рентгеновские снимки или компьютерную томографию по телефону:
- Проверьте размер дыхательных путей вашего ребенка
- Проверить степень сужения
- Поищите другие образования, которые могут давить на дыхательные пути
Лечение подсвязочного стеноза
Лечение подсвязочного стеноза зависит от тяжести симптомов у ребенка.
- Легкий стеноз подсвязочного канала — ребенку может не потребоваться вмешательство. Однако им нужно будет регулярно посещать врача.
- Умеренный или тяжелый стеноз подсвязочного канала. Ребенку может потребоваться операция, чтобы увеличить размер дыхательных путей. Это поможет им дышать легче. В некоторых случаях ваш врач может захотеть провести трахеотомию ниже уровня сужения дыхательных путей. Это обеспечит вашему ребенку безопасные дыхательные пути и облегчит дыхание.
Когда ваш ребенок будет готов, ваш врач может начать процедуры реконструктивной хирургии дыхательных путей.Это может включать:
Эндоскопическая хирургия
Этот тип хирургии используется для детей со стенозом подсвязочного канала легкой и средней степени тяжести. С помощью камеры узкие части разделяются и / или расширяются с помощью специальных воздушных шаров.
Открытая хирургия
Если у вашего ребенка сужение от умеренного до сильного, может потребоваться более сложное лечение. Эта операция проводится для увеличения участка с сужением или стенозом. Есть два основных способа проведения открытой операции.
Реконструкция гортани (LTR) или ларинготрахеопластика (LTP)
В LTR расширена суженная часть дыхательного горла, прямо под голосовым аппаратом.Для этого в дыхательные пути вводят трансплантат или кусок хряща. Большинство трансплантатов состоят из хряща ребра, но также используются хрящи уха или щитовидной железы. Операция проводится в один этап или поэтапно, в зависимости от состояния вашего ребенка.
Одноэтапный (SSLTR): если у вашего ребенка установлена трахеостомическая трубка, она будет удалена во время операции. После операции вашему ребенку через нос вставят дыхательную трубку. Дыхательная трубка поддерживает дыхательные пути и поддерживает место восстановления, пока трансплантат заживает и укрепляется.Пока дыхательная трубка находится внутри, вашему ребенку может потребоваться успокоительное и искусственное дыхание с помощью респиратора. Во многих случаях место ремонта проверяется в операционной перед тем, как вынуть дыхательную трубку.
Двойной этап (DSLTR): есть два варианта этой операции. У вашего ребенка может быть стент (устройство, подобное полой трубке), помещенное в дыхательные пути над трахеотомической трубкой (трахеотомией). ЛОР-врач может решить использовать Т-образную трубку вместо трахеи и стента. Тройник похож на трахею и стент, но все в одном.Стент или Т-образная трубка удерживают дыхательные пути ребенка открытыми, пока трансплантат заживает. Ваш врач решит, как долго Т-образная трубка или стент остается на месте.
Крикотрахеальная резекция (CTR) или трахеопластика шейным сдвигом
При CTR и шейной трахеопластике удаляется узкая часть трахеи. Затем снова прикрепляют здоровые концы трахеи. Эта операция может быть одноэтапной или поэтапной.
Позвоните врачу вашего ребенка, если:
Ваш ребенок:
- Имеет проблемы с удержанием пищи и все время ее срыгивает
- Худеет или не набирает вес
- Начинает меньше кормить и быстро утомляется во время кормления
- Борьба между едой и дыханием
Отведите ребенка в больницу, если ваш ребенок:
- Останавливает дыхание более чем на 10 секунд
- Губы темно-синего цвета, дыхание шумное
- Имеет втягивание груди или шеи, которое не прекращается при изменении положения или пробуждении ребенка
Стеноз гортани и трахеи — StatPearls — Книжная полка NCBI
Непрерывное обучение
Стеноз гортани и трахеи (LTS) — это сужение верхних дыхательных путей между гортани и трахеей с потенциально разрушительными последствиями, включая дыхательную недостаточность, остановку сердца и легочную смерть.Верхние дыхательные пути состоят из гортани, голосовой щели, подсвязочного пространства и трахеи. Трахея представляет собой трубку цилиндрической формы с передней хрящевой стенкой, образованной с-образными кольцами и задней перепончатой стенкой. Трахея ответвляется на правый и левый главные бронхи на киле, который расположен на уровне четвертого грудного позвонка (Т4). В этом упражнении рассматриваются этиология, патофизиология, клинические проявления, диагностика, лечение и осложнения стеноза гортани и трахеи.Он также охватывает роль межпрофессиональной группы по уходу за этими пациентами.
Цели:
Определить этиологию стеноза гортани и трахеи.
Просмотрите соответствующую оценку стеноза гортани и трахеи.
Опишите доступные варианты лечения стеноза гортани и трахеи.
Опишите стратегии межпрофессиональной команды для улучшения координации оказания медицинской помощи и коммуникации с целью развития стеноза гортани и трахеи и улучшения результатов.
Заработайте кредиты на непрерывное образование (CME / CE) по этой теме.
Введение
Стеноз гортани и трахеи (LTS) — это сужение верхних дыхательных путей между гортани и трахеей с потенциально разрушительными последствиями, включая дыхательную недостаточность, остановку сердечно-сосудистой системы и смерть. Верхние дыхательные пути состоят из гортани, голосовой щели, подсвязочного пространства и трахеи. Трахея представляет собой трубку цилиндрической формы с передней хрящевой стенкой, образованной с-образными кольцами и задней перепончатой стенкой.Трахея ответвляется на правый и левый главные бронхи на киле, который находится на уровне четвертого грудного позвонка (Т4).
Стеноз гортани может возникнуть в результате травмы, связанной с интубацией трахеи, новообразованием, аутоиммунным или инфекционным процессом. Это может протекать бессимптомно или приводить к симптомам обструкции верхних дыхательных путей.
Сужение гортани по любой причине требует мультидисциплинарного подхода к лечению, включая, помимо прочего, пульмонологов, реаниматологов, отоларингологов и гастроэнтерологов, а также патологов речи и языка и кардиоторакальных хирургов.Определение этиологии стеноза гортани и трахеи имеет решающее значение, поскольку оно может стимулировать лечение и предоставить пациенту прогностическую информацию.
Этиология
Некоторые этиологии связаны с развитием ларинготрахеального стеноза (LTS). [1] К признанным причинам стеноза гортани относятся: ятрогенные (например, осложнение эндотрахеальной интубации), аутоиммунные, инфекционные, неопластические, травматические и идиопатические. Аутоиммунные заболевания, такие как системная красная волчанка, ревматоидный артрит, васкулит, саркоидоз и склеродермия, среди прочего, могут вызывать стеноз гортани и трахеи.Инфекционные причины включают бактериальный трахеит, вирусный папилломатоз и туберкулез. Новообразование на уровне гортани или трахеи также может вызывать сужение дыхательных путей, причем плоскоклеточный рак и аденома являются наиболее частыми злокачественными новообразованиями в этом случае. [2] Прямое повреждение трахеи в результате травмы, ингаляционных ожогов или облучения — несколько причин травматического стеноза гортани и трахеи [3].
Острое повреждение гортани было описано как потенциальный компонент синдрома после интенсивной терапии.[4] Общие постинтубационные осложнения включают преходящую дисфонию, дисфагию и боль в горле у пациентов, перенесших операцию. Однако эти осложнения более выражены у пациентов в критическом состоянии. Эндотрахеальные трубки (ЭТТ) могут привести к повреждению гортани в результате прямого компрессионного повреждения слизистой оболочки задней голосовой щели, которое может в конечном итоге прогрессировать до фиброза и рубца, что приводит к стенозу.
Эпидемиология
Нет четких данных относительно эпидемиологии стеноза гортани и трахеи, поскольку трудно рассматривать это заболевание как единое целое, учитывая ряд различных причин.Стеноз трахеи может возникать почти у 30% пациентов с трахеостомией, хотя есть много факторов, которые могут этому способствовать, в зависимости от сопутствующих заболеваний, показаний и продолжительности трахеотомии [5].
Патофизиология
Самая узкая часть дыхательных путей взрослого человека находится в подсвязочном пространстве на уровне перстневидного хряща, который простирается от нижней части голосовых связок до нижней части перстневидного хряща. [3] Эта область имеет длину всего несколько сантиметров, но обычно может быть повреждена во время интубации трахеи, так как эндотрахеальная трубка контактирует с задней частью подсвязочного пространства во время интубации.Длительная интубация также может вызвать стеноз гортани и трахеи, когда давление в манжете превышает давление перфузии капилляров слизистой оболочки (примерно 35 мм рт. Что касается пациентов с основными аутоиммунными заболеваниями, гранулематоз с полиангиитом (ранее известный как гранулематоз Вегенера) чаще всего связан со стенозом гортани и трахеи, о чем свидетельствует некротическое гранулематозное воспаление верхних дыхательных путей с васкулитом, сохраняющим фиброзные изменения и стеноз.[7]
Анамнез и физикальное обследование
Обследование пациента с подозрением на стеноз гортани и трахеи включает подробный анамнез и физикальное обследование. В анамнезе должны быть указаны все предыдущие интубации трахеи и их продолжительность, история инфекции, аутоиммунного заболевания, васкулита, травмы, хирургического вмешательства, а также текущие симптомы. Наиболее частые симптомы LTS любой этиологии включают одышку, стридор, охриплость голоса и кашель. В условиях неотложной помощи врачу может не хватить времени для получения такой подробной информации, и в этом случае медицинский осмотр становится решающим.Необходимо уметь идентифицировать инспираторный стридор, который чаще всего встречается на шее, связанный с кашлем и одышкой. Если у пациента внегрудной стеноз, он может проявлять охриплость голоса, хрипы на вдохе, стридор и непродуктивный кашель. Внутригрудной стеноз проявляется с затруднением выдоха и лежа в положении лежа. Может быть снижение способности очищать секреты, а также свистящее дыхание, имитирующее астму, без ответа на бронходилататоры. [8] Локализация стеноза затруднена только по клиническим причинам.
Оценка
Стеноз гортани и трахеи можно оценить с помощью ларингоскопии или бронхоскопии. Врач может провести компьютерную томографию (КТ) шеи в тяжелых случаях, когда обструкция не позволяет провести прямую ларингоскопию, или у пациентов с травматическим повреждением трахеи и при планировании хирургического лечения. Компьютерная томография может продемонстрировать искусственный внетрахеальный стеноз, например, при массивном зобе, из-за зависимого положения трахеи при получении таких изображений.[2] Выполнение спирометрии у этих пациентов помогает установить исходный уровень и отслеживать их статус с течением времени. [9]
Существует три системы классификации, основанные на анатомических характеристиках, полученных на основе интраоперационных результатов. Классификация Коттона-Майера основана на проценте стеноза (I = <50% обструкции; II = от 51% до 70% обструкции; III = от 71% до 99% обструкции; IV = полная обструкция). Классификация Lano основана на вовлечении субсайта (I = вовлечение одного субсайта; II = вовлечение двух субпунктов; III = вовлечение трех субсайтов, при этом субсайт означает голосовую щель, подъязычный канал и трахею).Классификация McCaffrey основана на длине стеноза (I = подсвязочная часть или трахея <1 см; II = подсвязочная часть> 1 см; III = подсвязочная часть и трахея> 1 см; IV = любое поражение голосовой щели). Процент стеноза важен с точки зрения прогноза, индивидуального планирования лечения и стратификации риска трахеостомической зависимости. Пациенты со стенозом III и IV степени по классификации Cotton-Myer оказались зависимыми от трахеостомии по сравнению с пациентами со стенозом I и II степени.Согласно классификации Lano, более крупное поражение подсистемы было связано с более высоким риском трахеостомической зависимости, а также с более высокими стадиями по классификации McCaffrey. Для взрослых LTS классификации Лано и Маккаффри более точны, чем шкала Коттона-Майера [1].
Лечение / ведение
Обзор
Лечение стеноза гортани и трахеи является сложным, так как оно может повлечь за собой несколько процедур с возможностью рестеноза в некоторых случаях.Цели лечения — поддержание проходимости дыхательных путей, сокращение количества необходимых процедур и деканюляция у пациентов с трахеостомией. К сожалению, на данный момент нет стандартных руководящих принципов для подхода и управления LTS. Большинство методов лечения были описаны в различных исследованиях медицинской литературы по разным специальностям.
Варианты лечения LTS включают эндоскопическую дилатацию, хирургическое вмешательство, установку стента, лазерную терапию или иммуносупрессию для восстановления проходимости дыхательных путей, в зависимости от основной этиологии, а также степени и сложности стеноза.[10]
Бронхоскопический доступ
Бронхоскопия может использоваться для механической дилатации, лазерной терапии и стентирования для лечения стеноза гортани и трахеи. Эти методы лечения могут иметь ограниченное применение при стенозе подсвязочного канала из-за анатомических проблем. Расширение или лазерное лечение — варианты стриктур или гранулем; однако они подвержены риску рецидива. Установка стента может сместиться и вызвать более серьезное повреждение дыхательных путей. Лазер используется с осторожностью при стенозе подсвязочного канала из-за риска повреждения перстневидного хряща, в котором проходят гортанные нервы и которые играют роль в функции голосовых связок.Несколько исследований показали, что эффективность лазера и стентирования составляет менее 20% [3]. Бронхоскопическая терапия использовалась в случаях, когда пациент не является кандидатом на хирургическое вмешательство для облегчения симптомов.
Эндоскопическая механическая дилатация
Дилатация под эндоскопическим контролем выполняется с помощью нескольких устройств, включая бужи с кончиками десен, эндотрахеальные трубки или баллонные катетеры. Это может быть выполнено в амбулаторных условиях для выбранной группы пациентов. Этот способ дает более благоприятные результаты в отношении сохранения голоса по сравнению с пациентами со стенозом менее 2 см от голосовых складок или пациентами со стенозом на нескольких уровнях.Эндоскопическая дилатация должна быть лечением первой линии при простом стенозе, тогда как более сложные стенозы требуют межпрофессионального подхода и возможной хирургической оценки. Среднестатистический пациент может прожить около одного года, не требуя последующих дилатаций. [11]
Стентирование трахеи
Стентирование трахеи — паллиативный вариант для пациентов с прогрессирующей и неоперабельной обструкцией дыхательных путей, вызывающей рак. Как указывалось выше, стентирование — это сложный и рискованный подход, требующий беседы с пациентом о риске и пользе.Более высокий статус работоспособности перед операцией коррелирует с лучшими результатами для пациентов. Японское исследование Matsuo et al. направлена на прояснение показаний к установке стента, которые включают: 1) тяжелую обструкцию центральных дыхательных путей с одышкой и ограничением потока на кривой объем-поток, 2) прогноз будет продлен после установки стента, и 3) периферические дыхательные пути и легкие не повреждены. [ 12]
Предоперационная оценка
Несколько предоперационных оценок могут помочь в прогнозировании и выборе подходящего метода лечения.Пациента следует обследовать на предмет колонизации метициллин-резистентного золотистого стафилококка (MRSA) как минимум за две-три недели до возможной операции, поскольку инфекция может привести к большему количеству послеоперационных осложнений. Если у пациентов положительный результат теста на MRSA, их следует лечить профилактически с помощью трехдневного курса триметоприм-сульфаметоксазола двойной силы перорально и мупироцина интраназально, а также четырнадцати дней послеоперационного внутривенного введения ванкомицина, пока не будут удалены все дренажи. Перед тем, как продолжить лечение, пациенты также должны пройти оценку глотания с помощью волоконно-оптической эндоскопической оценки глотания (FEES) или модифицированного исследования глотания с барием (MBS), чтобы определить идеальный режим послеоперационного питания при родах.FEES также оценивает подвижность голосовых связок и степень стриктуры. [13]
Открытая операция
Открытая операция предлагается пациентам с III или IV степенью по Майер-Коттон, потерей хряща или стенозом более 1 см. Открытая операция возможна в случаях, когда длина твердых и рубцовых тканей превышает 1 см. Хирургические случаи имеют больше успехов, тогда как эндоскопические процедуры требуют большего количества повторных вмешательств. Открытая операция может быть разделена на 1) ларинготрахеальную резекцию с реанастомозом или 2) ларинготрахеопластику с использованием нативной и тканевой пластики.[13]
Резекция гортани и трахеи с реанастомозом
Систематический обзор Lewis et al. обнаружили, что ларинготрахеальная резекция с анастомозом была связана с уменьшением потребности в дополнительных операциях и увеличением скорости деканюляции по сравнению с эндоскопическими процедурами. Они также обнаружили, что пациентам с идиопатическим стенозом требуется меньше дополнительных операций по сравнению с пациентами со стенозом гортани и трахеи из-за травмы или интубации. [14]
Ларинготрахеопластика
Лариготрахеопластика включает в себя различные хирургические методы, которые включают одноэтапный или многоэтапный подход с использованием различных типов просветных трансплантатов или стентирования трахеи.[15] Результаты обычно благоприятные, с высоким процентом деканюляции. У них также мало послеоперационных осложнений, включая грануляционную ткань и отек голосовой щели. Их можно лечить коротким курсом дексаметазона от 24 до 48 часов, а также диурезом и подъемом изголовья кровати. [16] [17]
Трубка Монтгомери
Т-трубка Монтгомери вводится через переднюю стенку трахеи дистальнее анастомоза. Он обеспечивает стабильную проходимость дыхательных путей в течение длительных периодов (не менее шести месяцев) до рассмотрения возможности деканюляции или навсегда в неоперабельных случаях.[2] [9] [18]
Дополнительные методы лечения
В настоящее время для лечения LTS используются несколько вариантов дополнительного лечения. Обзор литературы предлагает использование дополнительных методов лечения, таких как митомицин С, стероиды и ингибиторы протонной помпы.
Митомицин C
Митомицин C — химиотерапевтическое средство, которое применяется местно в течение четырех минут после разреза. Он работает как алкилирующий агент, который подавляет деление клеток, синтез белка и пролиферацию фибробластов, в конечном итоге уменьшая образование рубцовой ткани.Сообщалось, что это может быть терапевтическим вариантом для более тонких стенозов; тем не менее, рестеноз может возникать с той же частотой через пять лет с повторным применением или без него. [19]
Стероиды
Для пациентов, подвергающихся дилатации, кортикостероиды, вводимые местно или системно в пероральной форме, имеют положительные доказательства в текущих данных, с большим успехом, отмеченным при стенозах толщиной более 1 см [20] [21].
Дифференциальный диагноз
Некоторые дифференциальные диагнозы, которые необходимо учитывать при оценке стеноза гортани, включают следующее: [22]
Прогноз
Общий прогноз превосходный для пациентов с идиопатической СНС, перенесших радикальную операцию.Прогноз при другой этиологии зависит от клинического течения основного заболевания, вызывающего LTS.
Осложнения
Острый LTS (например, LTS после экстубации) может привести к остановке дыхания, если его своевременно не выявить правильно. При идиопатической СНС осложнения включают изменения голоса, зависимость от трахеостомии без возможности деканюляции и необходимость многократных процедур.
Деканюляция трахеостомы является целевой целью открытой хирургии.Приблизительно от 63 до 95% пациентов, перенесших открытую операцию, успешно деканюлируют. Однако пациенты со стенозом III или IV степени (шкала Майера-Коттона), диабетом, гастроэзофагеальной рефлюксной болезнью, диабетом и / или индексом массы тела (ИМТ) выше 30 могут иметь более высокий уровень трахеостомической зависимости.
Кроме того, открытая операция может осложняться дисфагией из-за повреждения возвратных гортанных нервов или использования стента для поддержания проходимости дыхательных путей. [9]
Проспективное исследование Bibas et al.в Journal of Thoracic Disease обнаружено, что качество жизни пациентов со стенозом трахеи доброкачественного происхождения (например, интубация трахеи, не поддающаяся хирургическому лечению) серьезно ухудшается [23]. Качество жизни, связанное со здоровьем, влечет за собой физическое и психическое благополучие пациента и его семьи. Это исследование включало пациентов с Т-образными трубками Монтгомери, эндотрахеальными силиконовыми стентами или трахеостомией, а также способность заполнять анкету. Они исключили пациентов с хроническими сопутствующими заболеваниями, такими как хроническая обструктивная болезнь легких, тяжелая сердечная недостаточность и почечная недостаточность.
Консультации
Пациентам с LTS, как правило, требуется несколько специалистов в зависимости от клинической стадии, на которой они находятся. В острых случаях, например, когда у пациента отмечается постэкстубационный стридор, врач-реаниматолог обычно является основным консультантом по этому случаю с дополнительной помощью анестезиолога в том случае, если пациенту требуется повторная интубация трудных дыхательных путей. Также может потребоваться вмешательство специалистов по ушному носу и горлу (ЛОР), хирургов-травматологов и интервенционных пульмонологов (IP).Специалисты по IP будут необходимы для установки стентов, тогда как кардиоторакальные хирурги могут потребоваться для хирургического доступа в хронических или повторяющихся случаях. Когда таким пациентам проводятся интервенционные процедуры, очень важна координация с бригадой анестезиологов, поскольку обычно требуются усовершенствованные методы лечения проходимости дыхательных путей, такие как техника апноэ или струйная вентиляция. [1]
Сдерживание и обучение пациентов
Часто пациенты не могут быть осведомлены о необходимости эндотрахеальной интубации и возможных осложнениях, таких как LTS, из-за чрезвычайной ситуации, в которой это происходит.В случаях, когда пациенты имеют в анамнезе аутоиммунные заболевания и у них может быть LTS, их врач должен проконсультировать их относительно того, какие признаки и симптомы им не следует игнорировать, и немедленно обратиться за медицинской помощью, особенно если у них был предыдущий эпизод LTS. Кроме того, пациенты, страдающие LTS, особенно с идиопатической этиологией, могут получить пользу от онлайн-форумов, где они могут связаться с другими пациентами, которые страдают аналогичным образом, чтобы поделиться информацией, опытом и эмоциональной поддержкой.[24]
Улучшение результатов медицинской бригады
Стеноз гортани и трахеи — редкое заболевание, которое может возникать в результате различной этиологии и иметь серьезные последствия для здоровья. Врачам необходимо учитывать это у пациентов с одышкой, стридором, хрипом и / или изменениями голоса. Постановка диагноза имеет решающее значение для привлечения необходимых бригад для лечения пациента, включая врача интенсивной терапии, если есть опасения по поводу проходимости дыхательных путей и острой защиты дыхательных путей.В более коварных или хронических ситуациях целесообразно привлечь интервенционного пульмонолога и / или отоларинголога для проведения бронхоскопии или ларингоскопии для дальнейшего обследования. Ревматолог может помочь, если установлено, что LTS имеет аутоиммунную этиологию. Кардиоторакальный хирург должен быть на борту, если требуется операция, или общая хирургия в случаях, связанных с трахеостомией. Пациентам с изменениями речи может быть полезна помощь логопедов. У госпитализированных пациентов респираторные терапевты обычно оказывают помощь при трахеостомии по мере необходимости.
Непрерывное образование / обзорные вопросы
Ссылки
- 1.
- Гелбард А., Фрэнсис Д. О., Сандулаче В. К., Симмонс Дж. К., Донован Д. Т., Онгкасуван Дж. Причины и последствия стеноза гортани и трахеи у взрослых. Ларингоскоп. 2015 Май; 125 (5): 1137-43. [Бесплатная статья PMC: PMC4562418] [PubMed: 252
]
- 2.
- Наир С., Нилакантан А., Суд А., Гупта А., Гупта А. Проблемы лечения стеноза гортани. Индийская J Otolaryngol Head Neck Surg.2016 сентябрь; 68 (3): 294-9. [Бесплатная статья PMC: PMC4961642] [PubMed: 27508129]
- 3.
- D’Andrilli A, Venuta F, Rendina EA. Подсвязочный стеноз трахеи. J Thorac Dis. 2016 Март; 8 (Дополнение 2): S140-7. [Бесплатная статья PMC: PMC4775266] [PubMed: 26981264]
- 4.
- Шинн Дж.Р., Кимура К.С., Кэмпбелл Б.Р., Сан Лоури А., Вуттен, CT, Гарретт К.Г., Фрэнсис Д.О., Хиллель А.Т., Ду Л., Кейси Д.Д., Эли EW, Гелбард А. Частота и исходы острой травмы гортани после длительной механической вентиляции.Crit Care Med. 2019 декабрь; 47 (12): 1699-1706. [Бесплатная статья PMC: PMC7880159] [PubMed: 31634236]
- 5.
- Джеймс П., Пармар С., Хуссейн К., Правин П. Стеноз трахеи после трахеостомии. Br J Oral Maxillofac Surg. 2021 Янв; 59 (1): 82-85. [PubMed: 33160732]
- 6.
- Nesek-Adam V, Mrsić V, Oberhofer D, Grizelj-Stojcić E., Kosuta D, Rasić Z. Постинтубационный длинносегментный стеноз трахеи задней стенки: описание случая и Обзор литературы. Дж. Анест. 2010 августа; 24 (4): 621-5.[PubMed: 20454809]
- 7.
- Дабланка М., Маесо А., Мендес Д.Д., Ортега П. Стеноз гортани и трахеи аутоиммунной этиологии. Acta Otorrinolaringol Esp. 2017 Янв — Февраль; 68 (1): 38-42. [PubMed: 27063586]
- 8.
- Аль-Кади, Миссури, Артенштейн А.В., Браман СС. «Забытая зона»: приобретенные нарушения трахеи у взрослых. Respir Med. 2013 сентябрь; 107 (9): 1301-13. [Бесплатная статья PMC: PMC7125950] [PubMed: 23669413]
- 9.
- Rosow DE, Barbarite E. Обзор стеноза гортани и трахеи у взрослых: патогенез, лечение и исходы.Curr Opin Otolaryngol Head Neck Surg. 2016 декабрь; 24 (6): 489-493. [PubMed: 27585080]
- 10.
- Джошуа Дж., Шолтен Е., Шерер Д., Мафи М.Ф., Александр Т.Х., Кротти Александр Л.Е. Отоларингология в реанимации. Ann Am Thorac Soc. 2018 июн; 15 (6): 643-654. [Бесплатная статья PMC: PMC6207134] [PubMed: 29565639]
- 11.
- Galluccio G, Lucantoni G, Battistoni P, Paone G, Batzella S, Lucifora V, Dello Iacono R. Интервенционная эндоскопия в лечении доброкачественных стенозов трахеи: окончательное лечение при длительном наблюдении.Eur J Cardiothorac Surg. 2009 Март; 35 (3): 429-33; обсуждение 933-4. [PubMed: 120]
- 12.
- Нагано Х., Кишаба Т., Ней Й., Ямаширо С., Такара Х. Показания к стентированию дыхательных путей при тяжелой обструкции центральных дыхательных путей из-за запущенного рака. PLoS One. 2017; 12 (6): e0179795. [Бесплатная статья PMC: PMC5484493] [PubMed: 28651011]
- 13.
- Smith MM, Cotton RT. Диагностика и лечение стеноза гортани и трахеи. Эксперт Rev Respir Med. 2018 августа; 12 (8): 709-717. [PubMed: 29969925]
- 14.
- Льюис С., Эрли М., Розенфельд Р., Сильверман Дж. Систематический обзор хирургического лечения стеноза гортани и трахеи у взрослых и подростков. Ларингоскоп. 2017 Янв; 127 (1): 191-198. [PubMed: 27767216]
- 15.
- Лю И.Ю., Мендельсон А.Х., Чинг Х., Лонг Дж., Чхетри Д.К., Берке Г.С. Поэтапная ларинготрахеопластика при стенозе гортани и трахеи у взрослых: предикторы отдаленной деканюляции. JAMA Otolaryngol Head Neck Surg. 2015 Март; 141 (3): 211-8. [PubMed: 25541839]
- 16.
- Костантино К.Л., Матисен Диджей.Идиопатический стеноз гортани и трахеи. J Thorac Dis. 2016 Март; 8 (Дополнение 2): S204-9. [Бесплатная статья PMC: PMC4775268] [PubMed: 26981272]
- 17.
- Ван Х, Райт CD, Уэйн Джей Си, Отт ХК, Матисен Диджей. Идиопатический стеноз подсвязочного канала: факторы, влияющие на исход после одноэтапного ремонта. Ann Thorac Surg. 2015 ноя; 100 (5): 1804-11. [PubMed: 26296271]
- 18.
- Ху Х, Чжан Дж., Ву Ф., Чен Э. Применение Т-образной трубки Монтгомери при доброкачественном стенозе подсвязочного канала трахеи. J Thorac Dis.2018 Май; 10 (5): 3070-3077. [Бесплатная статья PMC: PMC6006128] [PubMed: 29997975]
- 19.
- Мальдонадо Ф, Лойзель А., Депью З.С., Эделл Э.С., Экбом, округ Колумбия, Малинчок М., Хаген К.Э., Алон Э., Каспербауэр Дж. Идиопатический стеноз подсвязочного канала: развивающийся терапевтический алгоритм. Ларингоскоп. 2014 Февраль; 124 (2): 498-503. [PubMed: 23818139]
- 20.
- Донахью Л., Кешавджи С. Современное лечение идиопатического ларинготрахеального стеноза. Thorac Surg Clin. 2018 Май; 28 (2): 167-175. [PubMed: 29627051]
- 21.
- Лахав Й., Шоффель-Хавакук Х., Гальперин Д. Приобретенный стеноз голосовой щели — текущая проблема: обзор этиологии, патогенеза и хирургического лечения. J Голос. 2015 сентябрь; 29 (5): 646.e1-646.e10. [PubMed: 25795359]
- 22.
- Нанн А.С., Нураи С.А., Джордж П.Дж., Сандху Г.С., Нуреи С.А. Не всегда астма: клинико-правовые последствия несвоевременной диагностики стеноза гортани и трахеи. Дело Rep Отоларингол. 2014; 2014: 325048. [Бесплатная статья PMC: PMC4281394] [PubMed: 25580336]
- 23.
- Bibas BJ, Cardoso PFG, Salati M, Minamoto H, Luiz Tamagno MF, Terra RM, Pêgo-Fernandes PM. Оценка качества жизни, связанного со здоровьем, у пациентов с доброкачественным стенозом трахеи без хирургического вмешательства. J Thorac Dis. 2018 августа; 10 (8): 4782-4788. [Бесплатная статья PMC: PMC6129892] [PubMed: 30233850]
- 24.
- Хайк Д., Кашанчи К., Тайран С., Хейлбронн С., Андерсон К., Фрэнсис Д.О., Гелбард А., Верма С.П. Группа онлайн-поддержки как сообщество: тематический контент-анализ онлайн-группы поддержки для идиопатического стеноза подсвязочного канала.Анн Отол Ринол Ларингол. 2019 Апрель; 128 (4): 293-299. [PubMed: 30607984]
Профилактика и лечение стеноза гортани у младенцев и детей
Приобретенный стеноз гортани является хорошо задокументированным осложнением эндотрахеальной интубации. Недоношенные дети, которым требуется искусственная вентиляция легких для лечения респираторного дистресс-синдрома, подвержены повышенному риску развития стеноза гортани. До недавнего времени методы лечения стеноза гортани требовали временной трахеотомии, что усложняло лечение и приводило к летальному исходу.В 1980 году было описано использование переднего перстневидного хряща для лечения стеноза гортани у младенцев. Методика была изменена: процедура переднего разделения перстневидного хряща, как первоначально описывалась, требовала одного вертикального разреза по средней линии через переднее хрящевое кольцо перстневидного хряща и верхние 2 кольца трахеи; модификация представляет собой расширение верхнего предела разреза щитовидного хряща в пределах 2 мм от надреза щитовидной железы. Методика использовалась у 45 детей в возрасте от 4 дней до 28 месяцев.Помимо того, что они представляют ценность для лечения стеноза гортани у недоношенных детей (29 пациентов), были выявлены 2 другие клинические группы детей, которым полезен продукт; 11 младенцев, у которых в первые 2 года жизни развился стеноз гортани вследствие интубации и у которых передний перстневидный разрез использовался в качестве альтернативы трахеотомии; 5 детей в возрасте до 2 лет, каждому из которых была сделана трахеотомия по поводу стеноза гортани, у которых передний перстневидный разрез использовался в качестве альтернативы более обширным методам реконструкции гортани и трахеи.Из недоношенных детей (29) 18 были успешно экстубированы, 5 все еще нуждались в трахеотомии и 6 умерли до завершения экстубации; Преобладающей причиной смерти была дыхательная недостаточность, вторичная по отношению к основной бронхолегочной дисплазии. Из 11 детей с обструкцией верхних дыхательных путей, вызванной постепенным развитием стеноза гортани, 9 были успешно вылечены без трахеотомии, а двоим потребовалась трахеотомия с последующей реконструкцией гортани и трахеи. Все 5 пациентов со стенозом гортани и трахеотомией были экстубированы.Интраоперационной летальности и серьезных осложнений не было. Результаты исследования подтверждают следующие выводы: передний перстневидный разрез является полезным методом лечения стеноза гортани у детей в возрасте до 2 лет без использования трахеотомии. У ребенка должен быть достаточный легочный резерв для проведения процедуры и последующей экстубации. Процедура требует высокого уровня медицинских, хирургических и медсестринских навыков и должна выполняться только в центрах третичной медицинской помощи.
Индексные слова
Стеноз подсвязочного канала
Стеноз гортани
трахеотомия
Рекомендуемые статьи Цитирующие статьи (0)
Полный текст
Авторские права © 1985 Издано Elsevier Inc.
Непрерывное образование
Подсвязочный стеноз можно определить как сужение верхних дыхательных путей, которые проходят между голосовыми складками и нижней границей перстневидного хряща.Причины стеноза подсвязочного канала могут быть врожденными, приобретенными или идиопатическими. В этом упражнении рассматривается оценка и лечение стеноза подсвязочного канала и подчеркивается роль межпрофессиональной команды в уходе за пациентами с этим заболеванием.
Целей:
- Опишите патофизиологию подсвязочного стеноза.
- Просмотрите соответствующий процесс оценки стеноза подсвязочного канала.
- Опишите варианты лечения стеноза подсвязочного канала.
- Обобщите важность сотрудничества между межпрофессиональной командой для улучшения ухода за пациентами с подсвязочным стенозом.
Введение
Подсвязочный стеноз можно определить как сужение верхних дыхательных путей, которые проходят между голосовыми складками и нижней границей перстневидного хряща.Обычно просвет подсвязочного канала составляет от 4,5 до 5,5 мм у доношенных новорожденных, в то время как просвет 3,5 мм является нормальным у недоношенных новорожденных. Подсвязочный диаметр 4 мм или меньше у доношенного новорожденного считается узким. Причины стеноза подсвязочного канала могут быть врожденными, приобретенными или идиопатическими . При врожденном стенозе подсвязочного канала в анамнезе нет интубации трахеи или какой-либо другой приобретенной причины стеноза. Редкое генетическое заболевание, называемое синдромом Паллистера Киллиана, вызвано мозаицизмом тетрасомии 12p и фенотипически проявляется мультисистемными морфологическими дефектами, включающими дыхательную систему и прогрессирующим стенозом подсвязочного канала.[1]
Приобретенный стеноз подсвязочного канала встречается чаще, чем врожденный, из-за введения длительной интубации в 1960-х годах, и со временем он не проходит. [2] Предотвращение трахеостомии у пациентов со стенозом подсвязочного канала имеет первостепенное значение, и это возможно благодаря достижениям в области баллонной дилатации и эндоскопических методов разделения перстневидного хряща. Деканюляция трахеостомы может быть более вероятна при реконструкции гортани и трахеальной артерии [3]. Идиопатический стеноз подсвязочного канала встречается очень редко и характеризуется периферическим стенозом в подсвязочной области и верхней части трахеи.Одноэтапная резекция и реконструкция гортани и трахеи являются предпочтительным окончательным методом лечения идиопатического стеноза подсвязочного канала [2]. Признаки и симптомы варьируются от рецидивирующего крупа и стридора при физической нагрузке до полной обструкции дыхательных путей, требующей трахеостомии. [4]
Симптомы идиопатического стеноза подсвязочного канала могут быть ошибочно приняты за астму. Когда лекарства от астмы не справляются с симптомами, пациенту ставят диагноз при эндоскопическом обследовании. В зависимости от тяжести стеноза лечение может включать технику Грилло, крикопластику или комбинацию методов резекции и увеличения с использованием трансплантатов реберного хряща.[5]
Этиология
Травма является наиболее частой причиной приобретенного стеноза подсвязочного канала, причем травма может быть внешней или внутренней. Внешняя травма чаще встречается у взрослых и возникает в результате дорожно-транспортных происшествий и травм, связанных с веревкой для белья. Травма внутренней гортани является ятрогенной, вторичной по сравнению с интубацией трахеи. Интубация составляет 90% случаев приобретенного стеноза подсвязочного канала у детей из-за полностью хрящевого кольца в верхних дыхательных путях и псевдостратифицированного реснитчатого столбчатого респираторного эпителия с рыхлой ареолярной тканью в этой области.Тяжелая травма возникает через 17 часов после интубации у взрослых и через 1 неделю у новорожденных.
Недоношенные дети переносят более длительную интубацию из-за более гибкого хряща и высокого расположения гортани новорожденного на шее с наклоном кзади и формой воронки. Размер эндотрахеальной трубки должен допускать утечку воздуха при давлении воды 20 см. Самый безопасный материал для длительной интубации — это полимерный силикон и поливинилхлорид. Назогастральный зонд также может вызвать некроз под давлением и перихондрит.Обычно в течение третьего месяца беременности просвет гортани реканализируется после завершения нормального срастания эпителия. Однако при врожденном стенозе реканализации не происходит. Другие причины включают ожоги, проглатывание, инфекцию и воспаление (гастроэзофагеальная рефлюксная болезнь, гранулематоз Вегенера).
Эпидемиология
Частота стеноза подсвязочного канала составляет менее 4% в исследованиях 1980-х годов и 0.6% в исследованиях, опубликованных после 1990-х годов. Снижение заболеваемости связано с улучшением обращения с новорожденными, которым требуется поддержка аппарата искусственной вентиляции легких. В настоящее время частота стеноза подсвязочного канала составляет от 0% до 2%. [6]
Патофизиология
При приобретенном стенозе подсвязочного канала эндотрахеальная трубка вызывает некроз под давлением в точке сопряжения с тканью, вызывая отек и изъязвление слизистой оболочки. Это нарушает нормальный цилиарный поток, вызывая нарушение мукоцилиарной системы и может привести к инфекции.Первичное заживление также предотвращается из-за подвижной и рыхлой подслизистой оболочки и недостаточной васкуляризации хряща, что приводит к стенозу, вторичному по отношению к разрастанию грануляционной ткани. Точнее, идиопатический стеноз подсвязочного канала часто локализуется в области перстневидного хряща, причем самая узкая часть находится между верхним краем хряща и первым кольцом трахеи. Это часто по окружности, хотя может быть и эксцентричным.
Гистопатология
Гистопатология идиопатического стеноза подсвязочного канала показывает плотный фиброз келоидного типа с вкраплениями фибробластов.На вышележащем эпителии наблюдается метаплазия, а хрящевые кольца в основном нормальные гистологически. Эстроген, по-видимому, играет роль в идиопатическом стенозе подсвязочного канала, но в процессе болезни не наблюдается гиперэкспрессии рецепторов эстрогена или прогестерона [7].
История и физика
При врожденном стенозе подсвязочного канала симптомы обычно появляются вскоре после рождения. Основными симптомами являются двухфазный стридор, одышка, голодание, надгрудинные, межреберные и диафрагмальные втягивания.При поражении голосовых связок возникает ненормальный крик, афония или охриплость. При приобретенном стенозе подсвязочного канала в анамнезе имеется инсульт гортани, и симптомы обычно проявляются через 3-4 недели после инсульта.
Оценка
Радиологическое обследование: Компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) полезны для установления диагноза стеноза подсвязочного канала. Более высокоскоростная компьютерная томография сокращает время визуализации.Рентгенография помогает определить точное местоположение и длину стенозированного сегмента. Техника переднезаднего высокого киловольта увеличивает видимость верхних дыхательных путей за счет увеличения столба воздуха в трахее и уменьшения акцента на костном шейном отделе позвоночника. Оптическая когерентная томография (ОКТ) — это малоинвазивный метод эндоскопической визуализации, позволяющий отслеживать прогрессирование подсвязочного поражения слизистой оболочки. ОКТ и анализ текстуры помогают в раннем обнаружении повреждения слизистой оболочки, что помогает лучше контролировать дыхательные пути и ограничивает его прогрессирование до стеноза.[8] Оценка глотания является обязательной перед реконструкцией дыхательных путей, чтобы избежать риска аспирации в послеоперационном периоде.
Эндоскопическое обследование: Прямая эндоскопическая визуализация с помощью гибкой оптоволоконной эндоскопии позволяет оценить динамику функции голосовых связок и верхних дыхательных путей, а также пищевода. Жесткий телескоп играет важную роль у детей в улучшении визуализации маленькой гортани.
Оценка гастроэзофагеальной рефлюксной болезни (ГЭРБ): Гастроэзофагеальный и гастроларингофарингеальный рефлюкс играет роль в обострении субгортального стеноза и отрицательно влияет на успешные исходы гортанно-трахеальных исходов.Следовательно, наиболее надежным является 24-часовой зонд pH пищевода с использованием метода двойного зонда.
Функциональные пробы легких: Спирометрия является полезным маркером для наблюдения у пациентов со стенозом под голосового канала. Это также является показателем послеоперационных исходов у кандидатов на операцию на дыхательных путях. Пациенты с подсвязочным стенозом имеют FEV1 / PEF> 10. Это соотношение не коррелирует с анатомической серьезностью стеноза по шкале Майера-Коттона. Согласно описанию случая, низкий пиковый поток вдоха был связан с ухудшением обструкции дыхательных путей у пациентов с подсвязочным стенозом.Некоторые авторы используют значения спирометрии в качестве неинвазивного измерения обструкции верхних дыхательных путей для измерения результатов баллонной дилатации. [9]
Лечение / менеджмент
Существует 3 основных хирургических доступа при стенозе подсвязочного аппарата, включая эндоскопию, операцию на открытой шее и трахеотомию. Эндоскопические методы включают дилатацию с помощью баллона или жесткую дилатацию. Он также включает радикальный разрез с использованием углекислотного лазера и иссечение рубца холодным ножом без расширения.Наконец, это также часто связано с установкой стента. Дополнительные методы лечения эндоскопической хирургии также включают в себя местную инъекцию митомицина и глюкокортикоидов. Митомицин обладает антифиброгенным и противоопухолевым действием. Цель этих подходов — улучшить проходимость дыхательных путей в долгосрочной перспективе и избежать симптомов одышки. [10]
Пациенты с идиопатическим стенозом подсвязочного канала в основном лечатся эндоскопически, и интервалы между дилатациями могут быть увеличены с помощью инъекции кортикостероидов.[11] Для беременных лечение первой линии является наиболее безопасным и эффективным методом лечения идиопатического стеноза под голосового канала. Это лечение позволяет выполнить расширение гортани с использованием непрерывного радиального расширения легочных баллонов с использованием неинвазивной вентиляции. [12] Баллонная дилатация может рассматриваться как лечение первой линии при приобретенном стенозе подсвязочного канала. Вероятность успеха во многом зависит от недавно приобретенного стеноза, начальной степени стеноза, более молодого возраста пациента и отсутствия трахеотомии.[13]
Зрелый и тяжелый стеноз гортани у педиатрических пациентов также можно успешно лечить у пациентов с баллонной дилатацией. В наиболее тяжелых случаях с предшествующей трахеотомией стентирование является обязательным. Баллонное расширение со стентированием также может облегчить реконструкцию гортани и трахеи [14]. Кроме того, эндоскопическая дилатация идеальна из-за того, что она неинвазивна; Таким способом управлять подсвязочным стенозом сложно из-за визуальных ограничений и риска лазерного возгорания. Радиочастотная кобляция успешно используется для удаления стеноза подсвязочного канала.Кобляция имеет преимущества, в том числе быструю и точную кобляцию, небольшое тепловое повреждение, а также более безопасную и удобную прямую визуализацию. Для этого требуется всего одна операция, которая может упростить утомительный процесс повторной абляции и уменьшить нагрузку на пациента. [15]
У ребенка, родившегося со стенозом подсвязочного канала, традиционное лечение заключается в проведении трахеостомии и доступе к дыхательным путям ребенка каждые 3 месяца, чтобы решить вопрос о необходимости реконструктивной хирургии. Второй вариант — выполнить передний или задний разрез перстневидного хряща под общей анестезией для увеличения просвета перстневидного хряща.Оптимальным методом лечения приобретенного стеноза подсвязочного канала является реконструкция гортани и трахеи. При ларинготрахеальной реконструкции делается отдельный разрез над трахеостомией на уровне перстневидного хряща и обнажается гортань от подъязычной кости вверху до трахеостомы внизу. В просвет вводят над верхней выемкой щитовидной железы, а гортань надрезают строго по средней линии. Трансплантат берется из реберного хряща и вставляется для расширения перстневидного кольца. Силастиковый стент используется для предотвращения коллапса трансплантата.Во время закрытия разреза очень важно точно противодействовать передней спайке. [16]
Дифференциальная диагностика
Патологии трахеи и гортани можно разделить на стеноз, инфекцию, новообразование и аспирацию. [17] Стеноз дыхательных путей, в частности, был вызван стенозом подсвязочного канала, стенозом трахеи, сосудистым кольцом, аберрантной безымянной артерией и перепонкой гортани [18]. Из этого списка стеноз трахеи обычно может быть вызван длительной интубацией, хирургическим вмешательством, расстройствами (аутоиммунными и воспалительными), инфекциями и ГЭРБ.[19]
Дифференциальный диагноз стеноза подсвязочного канала, в частности, может быть доброкачественным или злокачественным. Доброкачественные причины включают такие заболевания, как посттравматический статус, инфекции и ревматические заболевания, а также опухоли, такие как папиллома, гемангиома и гранулярно-клеточная опухоль. Злокачественные дифференциалы включают плоскоклеточный рак, хондросаркому и лимфому гортани. [20]
Стадия
Наиболее распространенной шкалой для диагностики стеноза подсвязочного канала является шкала Мейера-Коттона.
- Стеноз 1 степени — обструкция просвета менее 50%.
- Стеноз 2 степени — обструкция просвета от 51% до 70%.
- Стеноз 3 степени — обструкция просвета от 71% до 99%.
- Стеноз 4 степени — это полная непроходимость просвета.
Прогноз
Симптоматически субгортанный стеноз улучшается после эндоскопической дилатации, но прогноз неблагоприятный, так как частота рецидивов остается высокой.[21] Эндоскопическое лечение может быть полезным при стенозе подсвязочного канала как для начального лечения, так и в качестве дополнительной терапии (например, при рестенозе). Однако более низкая степень начального стеноза подсвязочного канала предполагает более высокую степень успеха при минимально инвазивных процедурах [22].
Осложнения
Подсвязочный стеноз может потребовать хирургического вмешательства, и хотя часто предпочтительнее эндоскопическое лечение, открытая реконструкция лучше в случаях более тяжелого стеноза.С другой стороны, трахеостомия сопряжена с множеством осложнений, и этого метода лечения следует по возможности избегать. [17]
Одно исследование показывает, что рестеноз был наблюдаемым осложнением примерно у четверти пациентов, получавших эндоскопическое или хирургическое лечение. Ревизионная операция также была осложнением, в основном из-за рестеноза или перистомиальной трахеомаляции. Наконец, введение трахеостомической трубки также создавало риск обструкции слизистой оболочки [23]. Хирургический прогноз может быть отличным, а осложнения сведены к минимуму, если принять меры во избежание натяжения анастомоза и деваскуляризации.[2]
Консультации
Консультация отоларинголога полезна при лечении обструкции верхних дыхательных путей, включая подсвязочный стеноз.
Сдерживание и обучение пациентов
Важно определить общие факторы риска стеноза подсвязочного канала, чтобы предотвратить возникновение или минимизировать тяжесть. К таким факторам относятся ГЭРБ, аутоиммунные и воспалительные заболевания, инфекции и даже хирургические процедуры и длительная интубация.[19] Поскольку это частые причины стеноза, их следует избегать или, если они неизбежны, немедленно лечить. Если необходимо хирургическое вмешательство, предпочтительнее эндоскопическое лечение. Открытое хирургическое вмешательство следует использовать только в тяжелых случаях, а трахеостомии следует вообще избегать, если это возможно.
Улучшение результатов команды здравоохранения
Медицинские работники должны убедиться, что пациенты находятся в хорошем состоянии, включая, помимо прочего, поданную жалобу.В одной статье говорится о важности межпрофессионального командного подхода и связанных с ним 6 C, обозначающих заботу, общение, смелость, сострадание, приверженность и компетентность.
Результаты были дополнительно подтверждены крупномасштабным рандомизированным контрольным исследованием, которое демонстрирует эффективность сотрудничества в интенсивной терапии. Это показывает, что совместная модель оказания интенсивной терапии пациентам с острой дыхательной недостаточностью окажется полезной для улучшения выздоровления. Например, при стенозе подсвязочного канала межпрофессиональная бригада должна включать отоларинголога, реаниматолога, анестезиолога и пульмонолога для оптимизации ухода за пациентом.[Уровень 1] [25]
Предварительный опыт работы в больнице высокоспециализированной медицинской помощи
Введение . Это ретроспективное исследование описывает наш опыт в обследовании и лечении младенцев с подсвязочным стенозом. Материалы и методы . В исследование были включены 10 пациентов в возрасте от 1 недели до 18 месяцев, 6 из которых имели врожденный стеноз подсвязочного канала и 4 случая — приобретенный стеноз подсвязочного канала. Результатов . У 6 пациентов была I степень, у 3 — II степень и у 1 пациента был стеноз подсвязочного канала III степени.На момент обращения 4 пациентам потребовалась трахеостомия. 7 пациентов успешно прошли лечение с помощью дилатации Бужи с последующим местным применением митомицина, тогда как 1 пациенту, у которого не удалось выполнить серийную дилатацию, потребовалась открытая реконструктивная процедура. Лазерное иссечение передней подсвязочной перепонки выполнено одному пациенту. Другой пациент с церебральным параличом не мог быть прооперирован, и ему была проведена трахеостомия. Заключение . Подсвязочный стеноз можно эффективно лечить с помощью эндоскопических хирургических методов, хотя количество таких необходимых сеансов зависит от типа и степени тяжести стеноза.Открытые хирургические процедуры необходимо индивидуализировать в соответствии с потребностями пациента только после того, как будут исчерпаны все другие эндоскопические возможности.
1. Введение
Подсвязочный стеноз (SGS) — это сужение подсвязочного дыхательного пути, которое располагается в перстневидном хряще, то есть ниже голосовой щели и над первым кольцом трахеи [1]. Это может быть врожденное или приобретенное. Врожденный стеноз подсвязочного канала (ВГС) имеет несколько аномальных форм. Возникает как часть врожденных генетических синдромов и считается третьей по частоте причиной стридора в этот период жизни после ларингомаляции и паралича голосовых связок [2].Врожденный стеноз подсвязочного канала можно разделить на перепончатый или хрящевой. Перепончатый — самый частый и самый легкий из врожденных стенозов. Мембранозный SGS обычно периферический, мягкий и расширяемый. Напротив, хрящевой SGS имеет различный внешний вид, включая умеренную нормальную форму с суженным просветом, или может иметь аномальную форму перстневидного хряща с выступающими боковыми полками, придающими просвету эллиптический вид.
Более 90% случаев SGS являются вторичными по отношению к интубации трахеи [3, 4].Приобретенный SGS (ASGS) — наиболее частая приобретенная аномалия гортани в детской возрастной группе и наиболее частая патология, требующая трахеотомии у детей в возрасте до одного года [5]. Структуры гортани младенца более гибкие и менее фиброзные, что делает дыхательные пути младенца более восприимчивыми к сужающемуся отеку и труднее прощупывается. Уменьшение на один миллиметр по окружности в подсвязке сокращает площадь поперечного сечения на 60%.
Стандартными методами оценки дыхательных путей являются прямая ларингоскопия и прямая бронхоскопия, в то время как хирургические методы лечения подсвязочного стеноза (SGS) включают серийную эндоскопическую дилатацию, открытую реконструкцию, передний перстневидный разрез (ACS), одномоментную ларинготрахеопластику с расширением хряща, переднюю и заднюю расщепление перстневидного хряща трансплантатами реберного хряща, размещенными спереди и сзади, и частичная резекция перстневидного хряща [1].Другие исследования включают визуализацию дыхательных путей (снимки дыхательных путей, компьютерная томография и т. Д.), А у стабильных детей старшего возраста могут быть полезны тесты функции легких.
Эндоскопическое лечение включает расширение с помощью пневматических баллонов или жестких расширителей, лазерные разрезы или холодный скальпель [6]. До 1980-х годов для лечения стеноза подсвязочного канала чаще всего использовалась эндоскопическая дилатация. Однако после публикации Fearon и Cotton [7] хирургическая реконструкция начала бурно развиваться. Это инвазивные и трудоемкие операции с госпитализацией в отделения интенсивной терапии, заболеваемостью и даже смертностью.Некоторым из этих пациентов даже потребуется послеоперационное эндоскопическое лечение для улучшения результатов [6]. Эндоскопическая дилатация была показана при стенозах I и II степени, а также при рецидивах SGS у послеоперационных пациентов с реконструкциями гортани и трахеи [8]. В настоящее время пациенты с SGS степени III также являются кандидатами на дилатацию [4].
Местные вещества, такие как стероиды, антикоагулянты и митомицин C (MMC), были использованы для оптимизации эндоскопического лечения. Хотя адъювантные методы лечения, такие как стероиды и антибиотики, были исследованы, в последние годы большое внимание было обращено на использование местного митомицина С (MMC).Митомицин, антибиотик из Streptomyces caespitosus , обладает антифибриногенной и противоопухолевой активностью, которая, как было показано, блокирует пролиферацию фибробластов и тем самым уменьшает образование рубцов при местном применении. Об использовании MMC для лечения стеноза дыхательных путей впервые было сообщено в 1998 году, и в настоящее время он обычно используется при эндоскопическом лечении стеноза гортани и трахеи [9].
2. Материалы и методы
В исследование были включены пациенты, направленные из неонатальных / педиатрических больниц третичного уровня долины, у которых в период с 2015 по 2018 год был диагностирован подъязычный стеноз.Все случаи были детально изучены, и были получены данные относительно возраста обращения, способа обращения, необходимости трахеостомии, истории интубации, пола, результатов волоконно-оптической ларингоскопии и ригидной эндоскопии, классификации и степени стеноза, любого сопутствующие заболевания, выполненная процедура и конечный результат.
Все пациенты прошли прямое ларингоскопическое и бронхоскопическое обследование под общей анестезией, дальнейшее лечение зависело от степени и типа стеноза.Стеноз классифицировали по классификации Коттона-Майера (степень I: 0–50%, степень II: 51–70%, степень III: 71–99% и степень IV: отсутствие детектируемого просвета) с использованием размера эндотрахеальная трубка прошла как направляющая. Дилатацию выполняли с помощью жестких (бужовых) расширителей увеличивающегося диаметра до достижения диаметра, соответствующего возрасту пациента. Затем результат расширения был оценен с помощью той же методики. Все диагностические и лечебные процедуры проводил один и тот же хирург, который по назначению является профессором.
3. Результаты
Всего в исследование были включены 10 пациентов в возрасте от 1 недели до 18 месяцев со средним возрастом обращения 3 месяца. Пациентов было 6 мужчин (60%) и 4 женщины (40%). У 4 пациентов был стридор, еще у 4 пациентов был стридор при физической нагрузке, и у 2 пациентов была повторная десатурация (таблица 1). Все пациенты прошли эндоскопическое обследование гортани до направления в отделение оториноларингологии, хирургии головы и шеи для окончательного лечения.Трахеостомия потребовалась 4 пациентам (40%) на момент обращения. В их число вошли 2 пациента с приобретенным подсвязочным стенозом (ASGS) и 2 пациента с врожденным подсвязочным стенозом (CSG).
| ||||||||||||||||||
Согласно классификации Коттона-Майера, у 6 пациентов был стеноз I степени, у 3 пациентов — стеноз II степени. У 1 пациента был стеноз III степени (таблица 2).
| |||||||||||||||||||||||||
Четыре пациента (40%) имели в анамнезе интубацию до развития симптомов, и при фиброоптическом ларингоскопическом обследовании (ВОЛ) у четырех пациентов (40%) был установлен подсвязочный стеноз, который был отмечен как приобретенный подсвязочный стеноз. .Две пациентки с приобретенным стенозом подсвязочного канала родились недоношенными со средним сроком беременности 28 недель и были интубированы в течение того же срока. У обоих этих пациентов сразу после экстубации развился стридор. У одного из пациентов с приобретенным стенозом подсвязочного канала развился неонатальный сепсис, и он оставался интубированным в течение 6 недель. У пациента наблюдались повторяющиеся эпизоды десатурации, которые усугублялись инфекцией верхних дыхательных путей (ИВДП). У пациента развились фиброз и грануляции преимущественно в задней части, и была сделана трахеостомия.Другой пациент с приобретенным стенозом подсвязочного канала обратился в возрасте 18 месяцев, когда он перенес повторные интубации перед несколькими операциями по поводу врожденных пузырно-мочеполовых аномалий (рис. 1–3) и нуждался в трахеостомии во время обращения. Все пациенты с приобретенным подсвязочным стенозом имели фиброзный подсвязочный стеноз I степени у двух пациентов и II степени у двух пациентов.
Шесть пациентов (60%) не имели в анамнезе интубации и были отмечены как врожденный стеноз подсвязочного канала, самый молодой из которых был в возрасте 1 недели, а самый старый — в возрасте 4 месяцев.У двух из них был стридор, у 3 — стридор при физической нагрузке, а у 1 пациента — повторная десатурация, усугубленная воспалительным инсультом. У двух пациентов с врожденным стенозом подсвязочного канала был обнаружен хрящевой стеноз и потребовалась трахеостомия, тогда как у других 4 был стеноз перепончатого подсвязочного канала.
Расширение Бужи с последующим местным применением митомицина выполнено 8 пациентам (80%). Первоначальная оценка проводилась с помощью жесткой бронхоскопии. Впоследствии было выполнено расширение области стеноза с последующим местным применением митомицина С в концентрации 0.5 мг / мл в течение 2 мин. Этим пациентам было выполнено не менее двух сеансов жесткой бронхоскопии с интервалом в 6 недель. У 4 пациентов был получен адекватный подсвязочный просвет при втором осмотре, и дальнейшее вмешательство не потребовалось. За этими пациентами внимательно наблюдали в течение 2 лет после операции, прежде чем было объявлено, что они успешно вылечены. Двум пациентам потребовалась вторая стадия дилатации, тогда как еще одному потребовалось 3 стадии дилатации плюс применение митомицина (рисунки 4–6). У одного пациента с врожденным стенозом подсвязочного канала спереди была перепончатая перепонка (рис. 7), которая была иссечена с помощью лазера CO 2 с последующим нанесением митомицина C, при втором осмотре она полностью зажила и эпителизировалась.Другой пациент с врожденным стенозом, поступивший через 4 месяца, имел церебральный паралич и лечился консервативно с трахеостомией на месте (таблица 3). У одного из двух других пациентов с трахеостомией была успешно деканюлирована после серийных дилатаций (Рисунки 8 и 9), тогда как у другого с неонатальным сепсисом h / o развилась трахеомаляция, и он был деканнулирован в возрасте одного года. Один из пациентов с врожденным стенозом подсвязочного канала с хрящевым стенозом II степени не смог отреагировать на дилатацию, и ему была назначена открытая процедура, и он не мог быть деканнулирован (Таблица 4), но пациент был потерян для последующего наблюдения.Таким образом, была достигнута скорость деканюляции 50%.
| |||||||||||||||||||||||||||||||||||||||
| Процент | |||||||||||||||||||||||||||||||||||||||
| Требуется трахеостомия | n = 10 | ||||||||||||||||||||||||||||||||||||||
| Да | 4 | 40 | |||||||||||||||||||||||||||||||||||||
| Нет | 6 | 60 | n = 4 | ||||||||||||||||||||||||||||||||||||
| Да | 2 | 50 | |||||||||||||||||||||||||||||||||||||
| Нет | 2 | 50 | |||||||||||||||||||||||||||||||||||||
.Обсуждение
В начале 20 века стеноз подсвязочного канала был редкостью. Цифры из литературных источников показали значительный разброс — от 1% до 8% [10, 11]. Начиная с 1960-х годов, в исследованиях сообщалось об увеличении частоты приобретенных SGS, при этом возраст обращения смещался в сторону младенцев. Постинтубационный стридор — обычная проблема в педиатрической реанимации (более 44% в текущей статье Schweiger et al. [12]). Тем не менее, частота осложнений со стороны дыхательных путей, связанных с интубацией, относительно низкая.Недавнее проспективное исследование показало, что частота постинтубационного стеноза подсвязочного канала у детей составляла 11,38% [13]. Это можно объяснить улучшенными методами вентиляции новорожденных в отделениях интенсивной терапии и спасением жизней детей с бронхолегочной дисплазией, заболеванием гиалиновой мембраны или неонатальной септицемией, требующим длительных периодов эндотрахеальной интубации. Задняя голосовая щель несет наибольшую тяжесть травм из-за смещения эндотрахеальной трубки кзади у основания языка и заднего угла трахеи.Это объясняет синхронное поражение задней голосовой щели и подсвязочного канала в некоторых случаях длительной интубации [14]. Последующий прогресс в искусственной вентиляции легких и широкое использование искусственных сурфактантов привели к сокращению продолжительности интубации и даже к ее полному исключению, тем самым уменьшив частоту приобретенного стеноза. Новое проспективное исследование даже показало, что недостаточная седация может быть фактором риска развития подсвязочного стеноза у интубированных детей [15].Ключевое понятие, которое возникло, заключается в том, что эндотрахеальная трубка подходящего размера — это не размер трубки, соответствующей возрасту, а, скорее, эндотрахеальная трубка, подходящая для ребенка.
Однако медицинские достижения мало повлияли на частоту врожденных стенозов [10, 16–18]. В нашем исследовании наблюдалось преобладание (60%) врожденного стеноза, а приобретенный стеноз во всех 4 случаях был связан с длительной интубацией. Во всех случаях диаметр стеноза оценивался с помощью эндотрахеальных трубок, которые можно было провести через стенозирующий сегмент во время микроларингоскопии и бронхоскопии (MLB), а степень тяжести объективно оценивалась с помощью системы оценки Майера-Коттона на основе определения размера эндотрахеальной трубки [19 ].На рентгенограммах у этих пациентов наблюдается классическое сужение воздушного столба в форме песочных часов.
Простая, эффективная, малоинвазивная терапия может оказаться очень полезной для лечения этой патологии. Вариант расширения узких дыхательных путей — один из них. Использование баллонных дилатаций дает хорошие результаты [8, 19–23]. Однако сообщений о дилатациях с помощью жестких или полужестких расширителей немного [21, 24]. Несмотря на все более частое применение лечения дилатациями, критерии выбора для оптимизации результатов еще не установлены [25].Степень успеха эндоскопического лечения варьировалась в зависимости от отчетов и используемого метода и варьировалась от 60% до 70% при баллонной дилатации [20, 23]. До 100% сообщили о жесткой дилатации, хотя это включает большой процент пациентов со стенозом 1 степени и большое количество процедур в течение длительного периода [21]. В нашей серии случаев результат был благоприятным у 87,5% пролеченных пациентов. Следовательно, мы считаем, что это лечение эффективно для всех пациентов со стенозом подсвязочного канала I – III степени.
В одном недавнем исследовании был сделан вывод, что лечение SGS с использованием жестких расширителей под эндоскопическим контролем является малоинвазивным и эффективным методом [26]. Расширение с помощью жестких расширителей может быть показано как лечение первой линии при SGS степени 1–3. Они рекомендовали 3 процедуры эндоскопической дилатации, а затем, при отсутствии ответа, рассмотрение других альтернатив лечения. Учитывая, что пациенты, которые не ответили на лечение, впоследствии были прооперированы без каких-либо трудностей, связанных с расширением, мы думаем, что первоначальное эндоскопическое лечение не мешает будущему хирургическому лечению в случае неудачи.
Лазер в основном используется для удаления грануляционной ткани и тканей гортани или подсвязочного пространства. Лечение основано на расширении стенозированной области; однако заживление раны может привести к рестенозу. Лекарства, предотвращающие разрастание фибробластов, могут замедлить или даже подавить этот процесс. Митомицин — природный антибиотик, продуцируемый Streptomyces caespitosus . В 1958 году Вакаки и др. описали митомицин С (MMC) [27]. Помимо того, что он является антибиотиком, митомицин C действует как противоопухолевый или алкилирующий агент, ингибируя синтез ДНК.Многочисленные исследования показали, что митомицин ингибирует образование фибробластов и рубцов как in vitro, так и in vivo [28, 29]. MMC был впервые использован в дыхательных путях в конце 20 века, и с тех пор немногие исследования продемонстрировали его эффективность [30, 31], тогда как другие показали его неэффективность [32]. Предыдущие исследования показали, что MMC эффективен при лечении послеоперационного стеноза [33]. Применение митомицина связано с увеличенным интервалом времени между эндоскопическими процедурами [34].В нашем исследовании всем пациентам применяли митомицин. Его использовали в сочетании с расширением бужей и лазерным лизисом ткани гортани CO 2 . После применения митомицина наблюдалось значительное уменьшение грануляционной ткани. Пациенты со стенозом I или II степени и мембранозным III степенью лечились консервативно с помощью эндоскопических вмешательств. Среднее количество эндоскопических процедур, выполненных на одного пациента, увеличивалось с увеличением степени стеноза. Открытая реконструктивная процедура была рассмотрена только у 1 пациента — случая хрящевого стеноза II степени, который не показал улучшения при консервативном эндоскопическом лечении.У пациента была неудачная попытка деканюляции из-за стридора и респираторного дистресса. Когда составлялся черновик этого исследования, пациенту была сделана трахеостомия и должна была быть проведена открытая реконструктивная процедура. Многие авторы согласны с тем, что резекция перстневидного хряща (CTR) приемлема и даже предпочтительна при субглоточном стенозе высокой степени, при этом самая большая зарегистрированная серия педиатрических резекций крикотрахеального отдела [35], достигающая показателей долгосрочной деканюляции более 90%. В этом исследовании открытая процедура была показана только в одном случае хрящевого стеноза II степени.
В заключение, опыт эндоскопии дыхательных путей имеет решающее значение в диагностике и лечении стеноза подсвязочного канала у детей. Когда присутствуют такие дети, важно провести тщательный сбор анамнеза и физикальное обследование. Медицинский осмотр должен включать тщательный осмотр головы и шеи, а также определение стридора и признаков респираторного дистресс-синдрома. Следует провести гибкое ларингоскопическое исследование. Важные вещи, которые необходимо документировать во время эндоскопии, включают внешний диаметр самого большого бронхоскопа или эндотрахеальной трубки, которая может быть проведена через стенозирующий сегмент, расположение и длину стеноза, другие отдельные участки стеноза и изменения рефлюкса.После удаления эндотрахеальной трубки или бронхоскопа с определенным размером важно осмотреть стенозирующий сегмент на предмет отека, который может привести к необходимости трахеостомии. Дети с SGS подвергаются длительному пребыванию в больнице и часто нуждаются в многопрофильном подходе, при этом главную роль играет хирург головы и шеи. Часто требуется трахеостомия. Одной консервативной эндоскопической дилатации может быть достаточно в большинстве случаев стеноза I, II и даже III степени. В более тяжелых случаях может потребоваться реконструктивная операция.LTR (ларинготрахеальная реконструкция) остается вмешательством выбора, при этом CTR является дополнением, если показано, например, при неудаче, несмотря на повторение LTR [36].
С уменьшением частоты приобретенных SGS из-за улучшения медицинского обслуживания, крупные открытые хирургические случаи и опыт в настоящее время встречаются редко. Не следует спешить с хирургическим вмешательством, пока не будут тщательно рассмотрены все возможности.
Небольшая выборка была ограничением для настоящего исследования, но с учетом редкости и снижения распространенности SGS, может быть трудно разработать точное перспективное исследование.Небольшая выборка была ограничением настоящего исследования. Тем не менее, наше исследование дает некоторое представление о текущих методах управления и результатах SGS, которые в наших руках оказались хорошими.
Доступность данных
Используемые вспомогательные данные добавлены под ссылкой. Некоторые из этих статей являются статьями с открытым исходным кодом, а доступ к другим доступен через институциональные лицензии.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Исторический обзор этиологии и лечения стеноза гортани
Arbuckle MF (1930) Причина и лечение рубцового стеноза гортани. Анн Отол Ринол Ларингол 39: 134–143
Google Scholar
Бартон Р.Т. (1953) Наблюдение за патогенезом гранулемы гортани вследствие эндотрахеальной интубации. N Engl J Med 248: 1097–1099
Google Scholar
Barwell H (1915) Два случая рубцового стеноза гортани. Ланцет 188: 16–17
Google Scholar
Barwell H (1916) Рубцовый стеноз гортани, леченный интубацией. Ланцет 190: 462–463
Google Scholar
Bergstrom J, Moberg A, Orell SR (1962) О патогенезе повреждений гортани после длительной интубации. Acta Otolaryngol (Stockh) 55: 342–346
Google Scholar
Bogdasasian RS, Olson NR (1980) Стеноз задней голосовой щели. Отоларингол Хирургия головы и шеи 88: 765–772
Google Scholar
Бончек Л.И. (1973) Успешное лечение постинтубационного стеноза подсвязочного канала с помощью стероидов внутри очага поражения. Ann Thorac Surg 15: 84–87
Google Scholar
Bouchut (1858) Цитируется в: O’Dwyer J (1885) Интубация гортани.NY Med J 42: 145–147
Google Scholar
Bryce DP, Briant TDR, Pearson FG (1968) Гортанные и трахеальные осложнения интубации. Анн Отол Ринол Ларингол 77: 442–461
Google Scholar
Cardwell EP (1946) Стеноз гортани ограниченной степени. Арка Отоларингол 44: 560–564
Google Scholar
Clerf LH (1931) Врожденный стеноз гортани: отчет о трех случаях. Анн Отол Ринол Ларингол 40: 770–779
Google Scholar
Cobb WB, Sudderth JF (1972) Внутриочаговые стероиды при стенозе гортани. Арка Отоларингол 96: 52–56
Google Scholar
Cohen SR (1981) Псевдоларингеальный паралич: постинтубационное осложнение. Анн Отол Ринол Ларингол 90: 483–488
Google Scholar
Cotton RT, Tewfik TL (1985) Стеноз гортани после углекислотного лазера при подсвязочной гемангиоме. Анн Отол Ринол Ларингол 94: 494–497
Google Scholar
Dedo HH (1979) Эндоскопический тефлоновый киль для передней перегородки голосовой щели. Анналы отологии, ринологии и ларингологии. 88: 467–473
Google Scholar
Dedo HH, Sooy FA (1968) Хирургическое лечение позднего стеноза голосовой щели.Анн Отол Ринол Ларингол 77: 435–441
Google Scholar
Dedo HH, Sooy CD (1984) Эндоскопическая лазерная пластика заднего стеноза голосовой щели, подсвязочного канала и трахеи путем разделения или микрозащитного лоскута. Ларингоскоп 94: 445–450
Google Scholar
Делаван Д. Б. (1909) Обсуждение лечения рубцового стеноза гортани. Br Med J 2: 1144–1149
Google Scholar
Delsaux V (1909) Обсуждение лечения рубцового стеноза гортани. Br Med J 2: 1141–1144
Google Scholar
Duncavage JA, Ossoff RH, Toohill RJ (1985) Лечение стеноза гортани с помощью углекислотного лазера. Анн Отол Ринол Ларингол 94: 565–569
Google Scholar
Dwyer CS, Kronenberg S, Saklad M (1949) Эндотрахеальная трубка: рассмотрение ее травматических эффектов с предложением по ее модификации.Анестезиология 10: 714–728
Google Scholar
Ehrich JB (1945) Лечение обширного рубцового стеноза гортани и трахеи. Арка Отоларингол 45: 343–350
Google Scholar
Fearon B, Cinnamond MJC (1976) Хирургическая коррекция стеноза подсвязочного канала. J Отоларингол 5: 475–478
Google Scholar
Fearon B, Ellis D (1971) Управление долгосрочными проблемами дыхательных путей у младенцев и детей. Анн Отол Ринол Ларингол 80: 669–677
Google Scholar
Figi FA (1940) Хронический стеноз гортани с особым учетом кожной пластики. Анн Отол Ринол Ларингол 49: 394–409
Google Scholar
Фиги Ф.А. (1940) Этиология и лечение рубцовых стенозов гортани и трахеи.South Med J 40: 17–26
Google Scholar
Foster JH (1939) Ведение рубцового стеноза гортани. Trans Am Laryngol Assoc 61: 112–120
Google Scholar
Freeland AP (1981) Композитный подъязычно-грудинно-подъязычный трансплантат в коррекции установленного стеноза подъязычного сустава. JR Soc Med 74: 729–735
Google Scholar
Габриэль П., Чилла Р. (1976) Eine operativ-medikamentose Kombinationstherapie narbiger Intubationsschaden. HNO 24: 280–282
Google Scholar
Gerwat J, Bryce DP (1974) Ведение стеноза подсвязочного гортани путем резекции и прямого анастамоза. Ларингоскоп 84: 940–957
Google Scholar
Grahne B (1971) Оперативное лечение тяжелого хронического травматического стеноза гортани у детей до трех лет.Acta Otolaryngol (Stockh) 72: 134–137
Google Scholar
Grahne B, Rinne J, Poppius H, Viljanen A (1980) Die Therapie chronisch-narbiger Larynxstenosen. HNO 28: 343–346
Google Scholar
Grant JD (1917) Случай гортанного стридора из-за хронического остеоартрита, облегченный путем дилатации. Proc R Soc Med 10: 79–82
Google Scholar
Hawkins DB (1977) Стеноз голосового и подсвязочного пространства эндотрахеальной интубации. Ларингоскоп 87: 339–346
Google Scholar
Holinger PH, Johnston KC (1958) Ведение хронического стеноза гортани. Анн Отол Ринол Ларингол 37: 496–515
Google Scholar
Holinger PH, Loeb WJ (1946) Стеноз гортани через трубку для кормления. Surg Gynaecol Obstet 83: 253
Google Scholar
Iglauer S (1918) Некоторые оригинальные методы лечения стеноза гортани. Trans Am Laryngol Assoc 40: 329–334
Google Scholar
Iglauer S (1939) Тяжелая травма гортани в результате постоянной двенадцатиперстной кишки. Анн Отол Ринол Ларингол 48: 886–904
Google Scholar
Jackson C (1921) Высокая трахеотомия и другие ошибки, основные причины хронического стеноза гортани.Surg Gynecol Obstet 32: 392–398
Google Scholar
Джексон С. (1936) Стеноз гортани с особым упором на лечение с помощью стержневых форм. Trans Am Laryngol Rhinol и Otol Soc 24: 12–24
Google Scholar
Джексон С., Джексон К.Л. (1932) Стеноз гортани — рост гортани как фактор лечения. Ларингоскоп 887–889
Jesberg S (1942) Постдифтериальный стеноз гортани. JAMA 120: 1000–1002
Google Scholar
Johnston WH (1929) Использование бужей с электрическим подогревом в лечении постдифтериального рубцового стеноза гортани. Анн Отол Ринол Ларингол 38: 1145–1149
Google Scholar
Джонс В.С. (1898) Хронический стеноз гортани. JAMA 30: 606–607
Google Scholar
Kirchner JA, Doberts DD (1978) Гортанные осложнения эндотрахеальной интубации. Conn Med 42: 151–155
Google Scholar
Kirchner JA, Sasaki CT (1973) Слияние голосовых связок после интубации и трахеотомии. Trans Am Acad Ophthalmol Otolaryngol 77: 88–91
Google Scholar
Knight JS (1955) Нож для расширения гортани. Trans Am Acad Ophthalmol Otolaryngol 59: 406
Google Scholar
Lack HL (1909) Обсуждение лечения рубцового стеноза гортани. Br Med J 2: 1140–1141
Google Scholar
Lefferts GM (1890) Интубация гортани при остром и хроническом сифилитическом стенозе. Med Rec 38: 369–373
Google Scholar
LeJeune F, Owens N (1935) Хронический стеноз гортани. Анн Отол Ринол Ларингол 44: 354–363
Google Scholar
Литтл Ф. Б., Куфман Дж. А., Кохут Р. И., Маршалл Р. Б. (1985) Влияние кислоты желудочного сока на патогенез стеноза голосового прохода. Анн Отол Ринол Ларингол 94: 516–519
Google Scholar
Looper EA (1938) Использование подъязычной кости в качестве трансплантата при стенозе гортани. Арка Отоларингол 28: 106–111
Google Scholar
Lynah HL (1918) Лечение стеноза гортани и трахеи после дифтерии.Ларингоскоп 28: 629–640
Google Scholar
Lynah HL (1919) Бужирование гортани. Int Rec Med 110: 838–843
Google Scholar
Lynch RC (1918) Стеноз гортани. Trans Am Acad Ophthalmol Otolaryngol 33: 355–371
Google Scholar
Lyons GD, Owens R, Lousteau RJ, Trail ML (1980) Лечение стеноза гортани лазером на углекислом газе.Арка Отоларингол 106: 255–256
Google Scholar
Maran AGD, Glover GW (1973) Модифицированный киль МакНота при стенозе задней голосовой щели. Дж. Ларингол Отол 87: 695–698
Google Scholar
Mayer E (1900) Стеноз гортани из-за осложнений со стороны хрящей щитовидной железы. JAMA 23: 1065–1067
Google Scholar
McNaught RC (1950) Хирургическая коррекция передней перепонки гортани. Ларингоскоп 60: 264–272
Google Scholar
Миддлтон П. (1966) Травматический стеноз гортани. Анн Отол Ринол Ларингол 75: 139–148
Google Scholar
Montgomery WW (1973) Задний и полный стеноз гортани (голосовой щели). Арка Отоларингол 98: 170–175
Google Scholar
Montgomery WW, Gamble JE (1970) Экспериментальное и клиническое ведение переднего стеноза голосовой щели. Арка Отоларингол 92: 560–567
Google Scholar
Негус В.Е. (1938) Лечение хронического стеноза гортани с особым акцентом на кожную пластику. Анн Отол Ринол Ларингол 47: 891–901
Google Scholar
Northrup WP (1894) Обсуждение лечения острого стеноза гортани.Br Med J 2: 1465–1478
Google Scholar
O’Dwyer J (1885) Интубация гортани. NY Med J 42: 145–147
Google Scholar
O’Dwyer J (1888) Интубация при хроническом стенозе гортани. NY Med J 255–261
O’Dwyer J (1897) Врожденный стеноз гортани. Trans Am Paediatr Soc 9: 180–181
Google Scholar
Ogura JH, Powers WE (1964) Функциональное восстановление травматического стеноза гортани. Ларингоскоп 74: 1081–1110
Google Scholar
Patterson EJ (1939) Стеноз гортани у детей. Архив отоларингологии 29: 71–77
Google Scholar
Peerless SA, Pillsbury HR III, Peerless AG (1981) Лечение стеноза гортани — новый консервативный подход.Анн Отол Ринол Ларингол 90: 512–515
Google Scholar
Pennington CL (1964) Повреждение гортани и надгортанника и стеноз в результате внешней травмы. Ларингоскоп 74: 317–344
Google Scholar
Робб Дж. М. (1949) Стеноз гортани. Анн Отол Ринол Ларингол 52: 566–576
Google Scholar
Роджерс Дж. (1905) Лечение хронической обструкции гортани и трахеи. Am J Med Sci 793–818
Rosen G, Vered IY (1975) Инъекция триамцинолона ацетонида при стенозе гортани. J Laryngol Otol 89: 1043–1046
Google Scholar
Росс Г.Т. (1902) Врожденный стеноз гортани. Trans Am Laryngol Assoc 46–47
Шефер С.Д., Клоуз Л.Г., Браун О.Е. (1986) Мобилизация фиксированного черпалоида в стенозированной задней комиссуре гортани.Ларингоскоп 96: 656–659
Google Scholar
Schlondorff G, Elies W (1985) Stimmbandstillstand mit Stridor infolge Interarytanoidfibrose — eine Komplikation in der Intensivpflege. Ларингол Ринол Отол 64: 403–404
Google Scholar
Schmiegelow E (1929) Стеноз гортани. Арка Отоларингол 9: 473–493
Google Scholar
Schoetter L von (1870) Цитируется по: Schmiegelow E (1929) Стеноз гортани. Арка Отоларингол 9: 473–493
Google Scholar
Шугар Ю.А., Сом П.М., Биллер Х.Ф. (1982) Оценка применения углекислотного лазера в лечении травматического стеноза гортани. Ларингоскоп 92: 23–26
Google Scholar
Simpson GT, Strong MS, Healy GB, Shapshay SM, Vaughan CW (1982) Факторы прогнозирования успеха или неудачи в эндоскопическом лечении стеноза гортани и трахеи.Анн Отол Ринол Ларингол 91: 384–388
Google Scholar
Sluder G (1928) Задний рубцовый стеноз гортани. Анн Отол Ринол Ларингол 37: 225–226
Google Scholar
Соболь С.М., Левин Х., Вуд Б., Такер Х.М. (1981) Надгортанная ларингопластика при осложненном стенозе. Анн Отол Ринол Ларингол 90: 409–411
Google Scholar
Solis-Cohen J (1888) Стриктура гортани. Am J Med Sci 96: 597–600
Google Scholar
Solis-Cohen J (1891) Стриктура гортани. Int Clin (Филадельфия) 1: 285–297
Google Scholar
Spencer WG (1896) Случай стеноза гортани. Дж Ларингол Отол 10: 55–56
Google Scholar
Stell PM, Maran AGD, Stanley RE, Murray JAM (1985) Хронический стеноз гортани. Анн Отол Ринол Ларингол 94: 108–113
Google Scholar
Strong MS, Healy GB, Vaughan CW, Fried MP, Shapshay S (1979) Эндоскопическое лечение стеноза гортани. Otolaryngol Clin North Am 12: 797–805
Google Scholar
Тонкин Дж. П., Харрисон Г. А. (1971) Хирургическое лечение гортанных осложнений при длительной интубации.Ларингоскоп 81: 297–307
Google Scholar
Tucker G (1925) Ларингостомия при стенозе гортани. Арка Отоларингол 1: 157–166
Google Scholar
Wagoner LG, Belenky WM, Clark CE (1973) Лечение приобретенного стеноза подсвязочного канала. Анн Отол Ринол Ларингол 82: 822–826
Google Scholar
Whited RE (1983) Стеноз задней спайки после длительной интубации. Ларингоскоп 93: 1314–1318
Google Scholar

 Москва — Владимир, 2001. С. 193-196.
Москва — Владимир, 2001. С. 193-196. 1993.Vol. 102. № 4. Pt 2. Suppl. 160. 15 p.
1993.Vol. 102. № 4. Pt 2. Suppl. 160. 15 p. 1998. Vol. 255. № 1. P. 12-17.
1998. Vol. 255. № 1. P. 12-17. P. 1957-1961.
P. 1957-1961. P. 365-369.
P. 365-369.