Грибовидный микоз | Симптомы и лечение грибовидного микоза
Патоморфология грибовидного микоза
На ранней стадии грибовидного микоза (эритематозной) гистологическая картина во многих случаях напоминает таковую при подостром или хроническом дерматите и экземе Отмечаются акантоз, гиперкератоз с отшелушиванием, мелкоочаговый паракератоз, в шиповатом слое очаговый спонгиоз, иногда с образованием подроговых везикул, экзоцитоз лимфоцитов, мелкоочаговая гидропнческая дистрофия клеток базального слоя. В дерме — небольшие, преимущественно периваскулярные инфильтраты из лимфоцитов с примесью гистиоцитов, небольшого числа плазмоцитов и зозинофилов. При более тщательном изучении в инфильтрате можно найти, хотя и в небольшом количестве, лимфоциты с церебриформными ядрами (клетки Сезари или Лутцнера).
В бляшечной стадии эпидермис обычно с выраженным акантазом и характерными для этого заболевания микроабецессами Потрие, располагающимися в различных его слоях. Отмечается экзоцитоз мононуклеарных клеток как в эпидермисе, так и в эпителии волосяных фолликулов с накоплением в последних мунинозного вещества. Пролиферат располагается большей частью полосовидно, иногда диффузно. Выраженный эпидермотропизм сопровождается гидропической дистрофией клеток базального слоя и потерей четкости зоны базальной мембраны. Субэпидермальная дерма отечна, с признаками пролиферации посткапиллярных венул. Часто пролиферат распространяется и на более глубокие отделы дермы. Он полиморфного характера, состоит преимущественно из малых и средних лимфоцитов, частично с церебриформными ядрами, иммунобластов и гистиоцитов, среди которых находятся лимфоплазмоцитоидные и плазматические клетки с примесью эозинофильных гранулоцитов. Могут наблюдаться и единичные двуядерные крупные клетки типа Ходжкина. Лимфоциты с характерными церебриформными ядрами располагаются одиночно или группами. Иммунобласты — более крупные клетки с массивной базофильной цитоплазмой, округлыми ядрами и центрально расположенным ядрышком. Энзимохимически в инфильтрате обнаружены мононуклеарные фагоциты с моноцитарными и гистиоцитарными свойствами, а иммуноцитохимически выявлено значительное число клеток, имеющих маркеры Т-лимфоцитов — CD2+, CD3+, CD4+, CD5+, CD8-, CD45RO+, CD30-, Т-клеточный рецептор аlfa-beta+, что позволяет рассматривать грибовидный микоз как Т-хелперную лимфому кожи.
Пролиферат располагается большей частью полосовидно, иногда диффузно. Выраженный эпидермотропизм сопровождается гидропической дистрофией клеток базального слоя и потерей четкости зоны базальной мембраны. Субэпидермальная дерма отечна, с признаками пролиферации посткапиллярных венул. Часто пролиферат распространяется и на более глубокие отделы дермы. Он полиморфного характера, состоит преимущественно из малых и средних лимфоцитов, частично с церебриформными ядрами, иммунобластов и гистиоцитов, среди которых находятся лимфоплазмоцитоидные и плазматические клетки с примесью эозинофильных гранулоцитов. Могут наблюдаться и единичные двуядерные крупные клетки типа Ходжкина. Лимфоциты с характерными церебриформными ядрами располагаются одиночно или группами. Иммунобласты — более крупные клетки с массивной базофильной цитоплазмой, округлыми ядрами и центрально расположенным ядрышком. Энзимохимически в инфильтрате обнаружены мононуклеарные фагоциты с моноцитарными и гистиоцитарными свойствами, а иммуноцитохимически выявлено значительное число клеток, имеющих маркеры Т-лимфоцитов — CD2+, CD3+, CD4+, CD5+, CD8-, CD45RO+, CD30-, Т-клеточный рецептор аlfa-beta+, что позволяет рассматривать грибовидный микоз как Т-хелперную лимфому кожи. Однако на практике изредка встречаются Т-супрессорные (CD4-, CD8+) иди (CD4-, CD8-) варианты.
Однако на практике изредка встречаются Т-супрессорные (CD4-, CD8+) иди (CD4-, CD8-) варианты.
При опухолевой ста
Грибовидный микоз: лечение и симптомы заболевания
25.01.2017
Грибовидный микоз представляет собой опухолевое злокачественное поражение лимфоидно-ретикулярной системы в первую очередь эпидермиса, а в дальнейшем и всех остальных органов.
Заболевание отличается сложностью лечения, очень важно выявить патологию на ранней стадии, когда возможна терапия. Только своевременное лечение позволяет значительно продлить жизнь больному, при наличии такого типа онкологии.
Особенности грибовидного микоза
Грибовидный микоз – редкий вид заболевания, который относится к типу Т-клеточной лимфомы кожи. Такой вид онкологии встречается примерно у одного из 345 тысяч людей.
Часто заболевание поражает людей в возрасте от 40 до 60 лет (около 70-80% всех случаев). Более подвержены заболеванию мужчины, у женщин болезнь встречается реже.
В основе микоза грибкового типа лежит размножение Т-лимфоцитов, которые начинают перерождаться в злокачественные клетки. Ученые пока что не смогли определить причины, в результате которых здоровые клетки начинают перерождаться в раковые. Предполагается, что далеко не последнюю роль в этом случае играет генетическая предрасположенность и хроническая антигенная стимуляция при наличии вирусной персистирующей инфекции (ВИЧ, инфекция герпеса и т.д).
Симптомы грибовидного микоза
Если говорить про грибовидный микоз, в первую очередь следует отметить его классическую форму, которая характеризуется тремя стадиями своего развития: опухолевой, бляшечной и эритемитозной.
При наличии у пациента эритематозной стадии на кожном покрове наблюдаются пятна желтовато-розового, красного и красно-синюшного цвета, которые очень сильно зудят. Они могут быть самого разного размера от нескольких миллиметров до 20 сантиметров в диаметре. Поверхность таких пятен бывает мокнущей или шелушащей. В большинстве случаев образования локализуются на туловище и в разгибательных участках ног и рук. Однако высыпания такого типа могут возникнуть совершенно на любом участке.
В большинстве случаев образования локализуются на туловище и в разгибательных участках ног и рук. Однако высыпания такого типа могут возникнуть совершенно на любом участке.
Эритематозная форма
В некоторых случаях, у больного сначала возникает зуд кожи, а только потом проявляются пятна на ней. В большинстве случаев, именно зуд считается характерным признаком наличия грибкового микоза, но также у некоторых людей он может отсутствовать. Лимфома кожи при высыпаниях является идентичной таким кожным заболеваниям, как плоский красный лишай, экзема, герпетиформный дерматит Дюринга или парапсориаз.
Некоторые медики полагают, что эритематозная стадия заболевания представляет собой тот или иной вид дерматита, которые без соответствующего лечения может переходить в грибовидный тип микоза.
После первой стадии заболевания, наблюдается ее переход в бляшечную форму, которая является второй стадией. В данном случае процесс перехода может занимать разный временной промежуток, в зависимости от формы болезни, состояния самого больного и других факторов, это занимает от нескольких месяцев до десятков лет.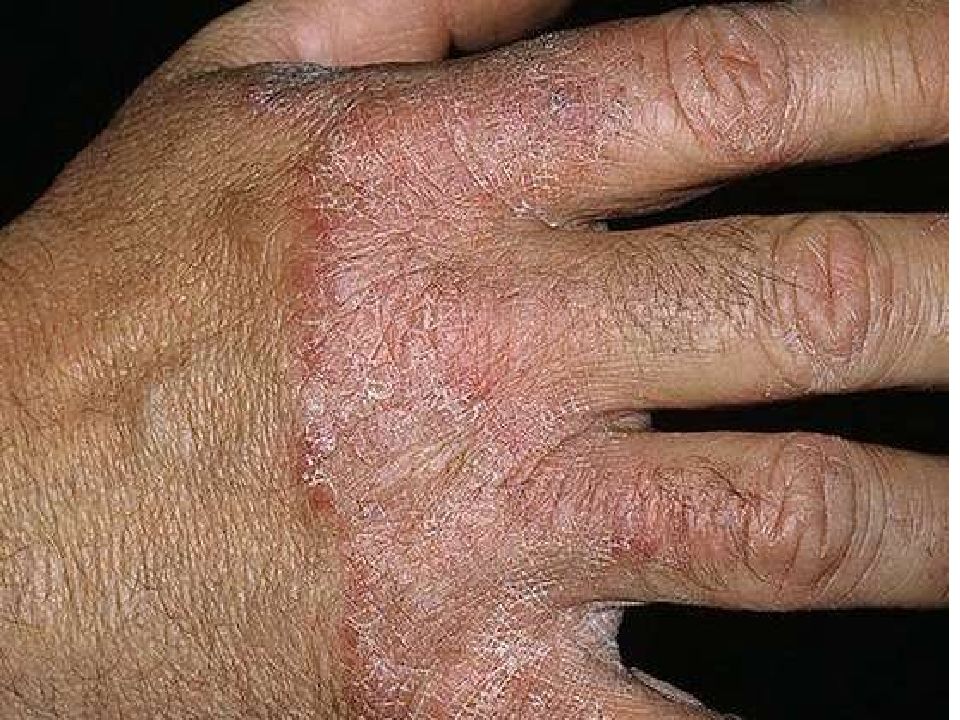
Бляшечная форма
Когда грибовидный микоз переходит в бляшечную стадию, наблюдается инфильтрация пятен. Они становятся более плотными, их контуры начинают приподниматься над поверхностью эпидермиса, постепенно превращаясь в бляшки. Без соответствующего лечения бляшки начинают увеличиваться в своей площади, они приобретают кирпично-красный или багровый оттенок, на их поверхности появляются мельчайшие бугорки. На этой стадии заболевания, больного начинает мучать сильный и изнуряющий зуд.
В некоторых случаях, со временем бляшки претерпевают обратное развитие, которое начинает развиваться с их центральной части. При этом рост бляшки не прекращается, она увеличивается в размерах по периферии, образуя своего рода кольцо. Бляшки начинают сливаться между собой в одно большое пятно, образуя причудливые формы напоминающие гирлянды или дуги.
Опухолевидная стадия
Последняя стадия грибовидного микоза является опухолевидной. Во время нее имеющиеся элементы на коже начинают перерождаться в опухоли, которые могут иметь крупные размеры, до среднего апельсина. При этом их цвет может колебаться от красновато-желтого до красновато-синего.
При этом их цвет может колебаться от красновато-желтого до красновато-синего.
Грибовидный микоз может находиться в разных стадиях, так наряду с имеющимся опухолями у больного остается проявление болезни в бляшечной форме. Спустя несколько недель наблюдается распад опухоли, на ее месте возникают глубокие язвы, имеющие покрытие из гнойно-кровянистых отделений.
Внутри них находятся жидкие массы из гниющей, отмирающей ткани. На фоне этого у больного наблюдается отсутствие аппетита, общее недомогание, снижение веса. Протекание опухолевидной стадии происходит с поражением внутренних органов, в которых возникают образования.
Любая стадия такого заболевания сопровождается увеличением лимфатических узлов, в первую очередь в области бедер и паха. В некоторых случаях у больного наблюдается ночная потливость и повышение температуры тела. Практически и 70% всех пациентов, страдающих от грибовидного микоза, наблюдаются трофические нарушения: дистрофические изменения волос и ногтевой пластины, нарушения потоотделения, кожная гиперпигментация. В редких случаях наблюдаются поражения слизистой. В таких случаях элементы инфекции наблюдаются в основном на мягком и твердом небе. Уже в скором времени на их мести наблюдаются большие, болезненные язвы.
В редких случаях наблюдаются поражения слизистой. В таких случаях элементы инфекции наблюдаются в основном на мягком и твердом небе. Уже в скором времени на их мести наблюдаются большие, болезненные язвы.
Форма заболевания Видаля-Брока (грибовидный обезглавленный микоз) причисляется к ретикулосаркоматозу кожи. Главной отличительной чертой такого заболевания можно назвать то, что при нем отсутствует бляшечная и эритематозная стадия. На коже лица и туловища у больного сразу же возникают опухолевидные образования
Говоря про эритродемальную стадию микоза Галлопо-Берье, то нудно отметить, что именно она отличается обширному распространению покраснений на всех участках кожного покрова, кроме того у больного наблюдается сильное шелушение кожи, отечность, выраженная инфильтрация. На фоне заболевания наблюдается нарушение общего самочувствия и резкое повышение температуры.
Диагностика грибовидного микоза
Определить такой вид инфекции достаточно просто, при наличии грибовидного микоза, во время сдачи анализа крови в нем определяется повышенное количество эозинофилов, лимфоцитов и лейкоцитов.
При диагностике заболевания в эритродермаческой и опухолевидной стадии у больного наблюдается снижение уровня лимфоцитов и лейкоцитов, а вот СОЭ, наоборот увеличивается. Чтобы подтвердить наличие у больного грибовидного микоза, ему назначается иммунологическое исследование.
Важно провести изучение кожных элементов, рекомендуется использовать ультразвуковое исследование новообразований на коже и с помощью дерматоскопии. Рекомендуется проведение гистологического исследования образований, путем взятия биопсии с пораженных участков. Благодаря исследованию можно подтвердить наличие раковых клеток в имеющимся опухолевидном образовании на коже.
Если у больного заболевание прибывает в бляшечной стадии, имеются резко выраженные акантозы, определяется наличие гнездовидных скоплений лимфоцитов и гистиоцитов. Во время наличия у больного опухолевой стадии распад инфильтрата наблюдается не только в слои дермы, но также в клетчатку, расположенную под клетками. В особо сложных случаях наблюдается захват расположенных рядом тканей.
При наличии у больного опухолевидной стадии с целью определения повреждений в области внутренних органов, рекомендуется провести рентгенографию грудной клетки и ультразвуковое исследований брюшной полости. Грибковый микоз дифференцируют с синдромом Сезари и остальными лимфомами, хроническим дерматитом, системными васкулитами, псориазом и остальными подобными заболеваниями кожи.
Лечение грибовидного микоза
После того, как больному был поставлен диагноз грибовидный микоз лечение должно быть назначено незамедлительно. Для лечения такого заболевания, рекомендуется использовать кортикостероиды, среди которых наиболее эффективными считается преднизолон и дексаметазон. Также рекомендуется использовать цитостаики (дипин, проспидин, циклофосфамид, фосфазин, метотрексат) и противоопухолевые антибиотики.
В большинстве случаев, для достижения положительного результата необходимо использовать комплексную терапию, с использованием препаратов приведенных выше групп. В некоторых случаях больному назначается рентгенотерапия, фототерапия, экстракорпоральная фотохимиотерапия. С целью уменьшения зуда, местно рекомендуется использовать различные кортикостероидные мази.
С целью уменьшения зуда, местно рекомендуется использовать различные кортикостероидные мази.
Прогнозы при грибовидном микозе
К сожалению, при наличии данного заболевания врачи дают весьма неблагоприятные прогнозы. В зависимости от тяжести заболевания и ее формы продолжительность жизни составляет от двух до двенадцати лет. Своевременное выявление заболевания и начало его эффективного лечения на первых двух стадиях дает возможность продолжительной ремиссии, тем самым увеличивая жизнь больного.
Вывод
При подозрении на грибовидный микоз, необходимо срочно показаться врачу. Заболевание является онкологическим, поэтому без правильного лечения становится причиной летального исхода. Ни в коем случае не пренебрегайте здоровьем, ведь вылечить болезнь в начальной стадии еще возможно.
Разновидности грибков на конечностях и органах у женщин и мужчин
26.01.2017
Наличие грибка кожи, свидетельствует о грибковой инфекции причиной возникновения которой оказываются разнообразные типы грибков.
Между собой, группы возбудителей грибковой инфекции имеют сходства, при этом заболевания могут кардинально разниться по способу заражения и своим симптомам.
Благоприятная среда для размножения
Для размножения грибковой инфекции подходит слабо-щелочная среда, но также они размножаются и в нейтральной. У здоровой кожи имеется кислая реакция, которая представляет собой защиту от поражений грибком.
Для размножения грибковой инфекции требуется повышенная влажность, поэтому грибок поражает ноги, которые у человека потеют. Заражение грибком наблюдается после посещения душевых, бассейнов, бань.
Грибковая инфекция также длительное время способна сохраниться в сухой среде, поэтому в чешуйках либо волосах, имеющих очаговое поражение, грибковая инфекция длительное время сохраняет свою жизнеспособность. Если споры окажутся на коже другого человека, то их активность также возобновляться. При этом, существуют различные виды грибка, каждый из которых отличается своей особенностью.
Условия заражения
Существует несколько условий, в результате которых человек способен заразиться грибковой инфекцией. Среди списка факторов риска, необходимо выделить, следующие:
- слабая иммунная система;
- присутствие микроорганизмов;
- повышенная температура и влажность окружающей среды;
- проблемы с эндокринной системой.
Классификация грибковой инфекции
На самом деле существуют многочисленные разновидности грибка, встречающиеся у человека. Между собой различают такие виды грибковой инфекции (микоза).
Каретомикозы – это грибковая инфекция, которая собирается на поверхностных слоях кожи, в кутикуле волоса. При поражениях отсутствует выпадение волос. К такому виду грибковой инфекции, которая встречается у человека, можно отнести, следующее:
- разноцветный лишай – на светлом покрове кожи наблюдаются пятна имеющие кофейно-молочный оттенок. Если кожа смуглая, загорелая, то пятна, наоборот, белые;
- узловатая трихоспория – на волосистой части головы наблюдается возникновение узелков.

Дерматофитии – это грибковая инфекция поражающая кожный покров, находящаяся в более глубоких слоях эпидермиса, в сравнении с кератомикозом. На фоне наличия такого типа грибковой инфекции, больной сталкивается с воспалительными процессами. В данном случае хочется выделить микроскопию, которая оставляет поражения на волосах и коже.
Заболевание еще называют «стригущий лишай». Оказавшись на коже, грибковая инфекция внедряется в эпидермис, начиная там активно размножаться. Если поражение наблюдается на волосистой области головы, то волосяной покров также будет затронут. Это одна из популярных грибковых инфекций, которой можно заразиться. Как бы странно не звучало, но именно собаки и кошки являются основными распространителями заболевания, заражение таким грибком происходит именно от них.
У человека при такой грибковой инфекции проявляются такие симптомы: на коже в месте начинающего поражения возникает пятно имеющее четкие границы, увеличивающееся постепенно в размерах.
По краям пятна виднеются границы с пузырьками и узлами. Проводить лечение рекомендуется с использованием противогрибковых средств.
Трихофития
Поражение такой грибковой инфекцией происходит через взаимодействие с больным человеком, после ношения вещей из его гардероба, к примеру, головного убора. Есть возможность подцепить инфекцию в парикмахерской, после использования зараженной расчески или ножниц.
Руброфития
Такой кожный грибок зачастую поражает складки кожи, стопы и конечности. Заражение болезнь происходит при непосредственном контакте человека с носителем грибка, а также при несоблюдении правил личной гигиены. Повышенная влажность стоп благоприятствует развитию грибковой инфекции.
Заболевание имеет следующие симптомы: между пальцами на ногах наблюдается шелушение кожи, могут появляться маленькие трещины на коже, пузырьки и узелки. Если поражение наблюдается на руках, то тыльная часть кистей становится синюшного оттенка. В области поражения всегда наблюдается валик.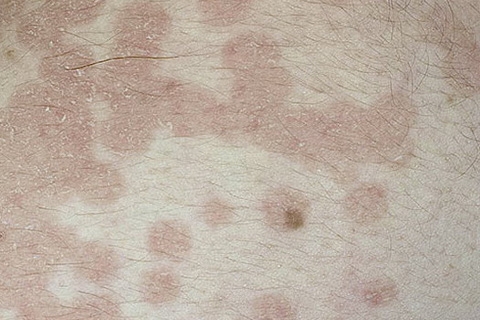
Если грибок развивается в ногтевой пластине, то ноготь приобретает белый цвет, на нем возникают полосы. Ногтевая пластина может утолщаться и приобретать серо-бурый цвет.
В качестве средств терапии применяются солевые ванночки и противогрибковые препараты.
Кандидоз
Такое грибковое заболевание может локализоваться на коже, ногтевых пластинах или слизистых оболочках. Зачастую болезнь поражает людей, страдающих от лишнего веса, склонных к чрезмерному потоотделению. Места поражения этим видом грибковой инфекции имеют белесый налет и очерченные края.
Глубокие микозы
Такой вид грибковой инфекции считается наиболее серьезным. Грибок в данном случае поражает не только грибковый покров, но и внутренние органы. В большинстве случаев на фоне инфекции возникают воспалительные процессы. Среди наиболее распространенных видов глубокого микоза, необходимо отметить:
- риноспоридоз – один из наиболее редко встречаемых видов микоза, которые характеризуется возникновением папилломных разрастаний в области носа, которые при прикосновении легко травмируются.
 Заразиться инфекцией можно во время контакта с водой из непроточного водоема, к примеру, озера. Имеющиеся на лице папилломы следует удалять оперативным способом или с использованием лазера, после чего места поражения нужно обработать противогрибковым средством;
Заразиться инфекцией можно во время контакта с водой из непроточного водоема, к примеру, озера. Имеющиеся на лице папилломы следует удалять оперативным способом или с использованием лазера, после чего места поражения нужно обработать противогрибковым средством; - хромимикоз – грибковая инфекция поражает подкожную клетчатку и кожу. После внедрения в кожу возбудителя, на этом участке возникает бугорок, кожа на котором начинает шелушиться. Через несколько месяцев радом появляются другие бугорки. Если ничего не предпринимать, то через некоторое время образования будут увеличиваться, напоминая разрастающиеся бляшки. Для лечения этого вида грибковой инфекции применяются противогрибковые препараты и раствор йодида калия;
- спортрихоз – в основном локализуется на кожной клетчатки и коже, в некоторых случаях может поражать лимфатические узлы. По внешнему виду напоминает многочисленные язвочки и абсцессы. Наиболее популярный такой вид грибковой инфекции в тропических странах. Терапия производится путем введения раствора йодида калия в организм.
 Заболевание легко поддается терапии, при своевременном обращении к врачу;
Заболевание легко поддается терапии, при своевременном обращении к врачу; - бластомикоз – представляет собой главное заболевание этой категории. Имеется три типа такого микоза, которые встречаются только в Южной и Северной Америке и Европе. Терапия заболевания крайне продолжительна и может доходить до двух лет. Больному назначают сульфаниламид. На протяжении курса лечения также рекомендован прием средств, способных укрепить иммунную систему.
Виды грибов также объединяются в группу коринобактеризов. К этой категории относят:
- Эритразма – микоз, проявляющийся появлением в паховой области пятен красного цвета. На пятнах появляется белесый налет. Такие высыпания не способны доставить особых проблем, но при наличии раздражений на коже способны вызвать экзему.
- Подмышечный трихомикоз – при наличии такого типа грибковой инфекции наблюдаются изменения внешнего типа волос в области лобка и подмышечных впадин, пот меняет свойственный ему ранее цвет.
 Чаще всего такому заболеванию подвергаются люди имеющие заболевания эндокринной системы и страдающие от повышенного потоотделения.
Чаще всего такому заболеванию подвергаются люди имеющие заболевания эндокринной системы и страдающие от повышенного потоотделения. - Актиномикоз – на фоне такого типа грибковой инфекции у человека наблюдается возникновение узлов в лимфоузлах и мышцах. Такие узлы возникают на поверхности кожи, становясь причиной ее раздражения, в результате выделения из них жидкости. Такой вид грибковой инфекции рекомендуется лечить путем соблюдения гигиены тела, определения причин сбоя в работе эндокринной системы, удаления с помощью бритвы пораженных грибком волос.
Лечение грибковых инфекций
Для лечения грибковой инфекции, после определения ее типа, врач назначает антимикробные и противогрибковые препараты. Лечение заболевания своими силами может быть крайне опасным. При выборе неправильной терапии, грибковая инфекция распространяется по всему организму, поражая все органы. Если в запущенной форме будет находиться грибковая инфекция, то больше времени потребуется на ее лечение.
В обязательном порядке при наличии грибковой инфекции человек должен придерживаться правил личной гигиены.
Для лечения грибка, рекомендуется использовать специальные мази и препараты. К распространенным и эффективным противогрибковым средства относят: флуконазол, нистатин, кетоконазол и остальные.
В том случае, если грибковая инфекция еще не успела распространиться по всему организму, можно ограничится местным лечением. В этом случае больному назначаются различные растворы для протирания и мази. Среди наиболее эффективных средств можно отметить Тридерм, Нистатиновая мазь, Микозолон, Левориновая мазь, Гризеофульвин.
При этом необходимо понимать, что в любом случае начинать лечение можно только после консультации с врачом и сдачи всех необходимых анализов. Самостоятельное лечение в данном случае может быть крайне опасным для здоровья. Грибковая инфекция на самом деле является весьма серьезным заболеванием, не ограничивающимся поражением отдельного участка кожи или ногтевой пластины. Только правильное, эффективное лечение позволит избавить от грибка и предотвратить возможные рецидив.
Причины неэффективного лечения
В некоторых случаях может быть так, что, начав лечение грибка, больной замечает, что никакого эффекта от терапии нет. Заболевание не только не становится меньше, но и начинает прогрессировать.
Почему возможные такие случае, что на самом деле является причиной отсутствия эффективности в лечении? В данном случае нужно отметить, что причиной, в результате которой лечение не приносит желаемого результата становится нарушение режима лечения со стороны пациента.
Отсутствие результата наблюдается в случаях:
- почти треть всех людей, имеющих грибковые поражения кожи и ногтевой пластины, считают, что заболевание не серьезное, отказываясь от своевременного лечения;
- практически 70% всех людей, страдающих от грибковой инфекции, не верят, что назначенное лечение способно принести положительный результат;
- практически половина всех пациентов, которые проходили ранее лечение от грибковой инфекции оказались не удовлетворены полученным результатом. При необходимости очередной терапии, они даже не надеются на хороший результат;
- практически 70% всех людей, страдающих от грибковой инфекции, сразу после получения положительного результата прекращают лечение. При этом мало кто знает, что после устранения внешних проявления грибка, лечение необходимо продолжить как минимум 2 недели, чтобы инфекция смогла полностью выйти из организма и не стать причиной рецидивов.
Вывод
Лечение грибковой инфекции напрямую зависит от ее возбудителя, тяжести процесса и области поражения. Именно по этой причине очень важно обратиться к врачу, который сможет точно определить тип грибковой инфекции и степень ее поражения организма.
Современные медикаментозные препараты, действие которых направлено на профилактику и лечение грибка позволяют избавиться от проблемы в самые короткие сроки, не прикладывая особых усилий. Берегите свое здоровье, ведь оно дается каждому человеку только раз.
Грибок кожи на теле (дерматомикоз): симптомы, фото и лечение
Микроскопические грибки окружают человека везде. Некоторые из них присутствуют в почве и воде, на бытовых приспособлениях, другие – живут на теле человека и слизистых оболочках. При крепком здоровье грибки не опасны. Угрозу человеку они представляют при снижении иммунитета. Микробы атакуют организм извне, проникают в кожу, сквозь нее. В редких случаях развиваются системные микозы.
Виды грибковых поражений кожи
Науке известно несметное количество грибковых микроорганизмов. Для удобства их классифицируют по видам. Для человека наиболее опасны нитчатые грибки, которые формируют в теле нечто наподобие мицелия и размножаются спорами. Большинство из них устойчиво во внешней среде. Микозы кожи передаются при телесных, бытовых контактах, при взаимодействии с обсемененными спорами предметами.
Самый распространенный тип грибковых поражений кожи – кератомикозы. Это отрубевидный лишай, актиномикоз, эритразма. Микробы поражают роговой слой кожи. Их споры распространяются вместе с отслоившимися частицами эпидермиса. Грибковые заболевания этого типа:
- редко передаются от человека к человеку;
- протекают в хронической форме;
- обостряются в весенний период;
- нарушают синтез меланина и пигментацию кожи;
- «боятся» ультрафиолета;
- редко излечиваются полностью.
Для кератомикозов характерно появление высыпаний в зонах повышенной потливости – под мышками, на спине, шее, груди, животе. Редко сыпь распространяется на предплечья.
Что делать если у вас грибок?!
Читать далее >> |
Наименее опасен отрубевидный лишай. Грибок никогда не проникает сквозь дерму. О поражении говорит появление на теле розово-коричневых пятен неправильной формы с фестончатыми краями. На поверхности высыпаний заметно мелкое (отрубевидное или мучнистое) шелушение. Частицы кожи отслаиваются при трении пальцем. После исчезновения коричневых пятен на пораженных участках наблюдается лейкодерма – апигментированные (очень бледные) пятна.
Эритразма и актиномикоз – опасные грибковые заболевания. Их возбудители способны проникать в кровоток и поражать внутренние органы. В зонах проникновения грибка появляются воспалительные изменения.
Второй распространенный тип микозов – дерматофитии. Это лишай фавус, микроспория, трихофития. Последняя инфекция встречается особенно часто. Передается при контакте с зараженным человеком, животным. В первом случае поражается кожа на теле. Инфекция часто остается незамеченной, переходит в хроническую форму. Антропофильные трихофитоны способны поражать только наружные слои дермы, зоофильные – проникают в ее глубинные структуры, провоцируют нагноения и абсцессы.
При трихофитии на теле появляются красноватые пятна, с четко отграниченными краями. Периферический валик состоит из везикул и узелков, которые со временем превращаются в корочки. Воспаление происходит в зоне периферии. Пятна увеличиваются, сливаются.
Если инфекция передалась от животного, чаще поражается кожа головы, лица, рук. На волосистых участках образуются круглые залысины. Трихофитоны поражают и придатки кожи. Вызывают обламывание волос у луковицы или на 1-2 мм выше кожи. По мере развития залысины становятся рельефными – значительно выпячиваются над остальными зонами, приобретают шаровидную форму. Из фолликулов выделяется инфильтрат, нередко гнойный. Выделения склеивают волосы, засыхают плотными корками. Зона воспаления болезненна, при надавливании пальцами гной может выходить струйками.
Зачастую к дерматологу приходят с грибком кожи на стопах. Заболевания конечностей объединяют в одну группу – эпидермофитии. Микоз на стопах провоцируют многие грибки, а вот симптомы поражений одинаковы.
Кожа в зоне ступней утолщается, становится грубой, сухой, растрескивается, появляются омозолелости и натоптыши. Из-за гиперкератоза и повышенного давления плотные участки покрываются трещинами разной глубины. Иногда раны инфицируются и гноятся. Размножение грибка сопровождается сильным зудом, жжением, при трещинах – болью. Пациент страдает от психоэмоционального напряжения, ведь зуд усиливается в ночное время, а пот приобретает крайне неприятный запах.
Красные высыпания в зонах потливости и складках могут быть признаком кандидоза кожи. Провокатор – кандидобактерии. По их вине развивается генитальный кандидоз и молочница слизистых оболочек рта. На теле грибок размножается редко. Благоприятные условия возникают при тяжелых иммунодефицитах.
Как сразу распознать грибок
Единственный общий симптом для всех микозов кожи – зуд. Интенсивность его варьируется зависимо от:
- размера пораженной площади;
- глубины проникновения микробов;
- активности патогенов.
Иногда появляется легкий дискомфорт, переходящий в зуд только после контакта с водой или потения. При микозах стоп зуд присутствует круглосуточно.
Второй признак грибка – появление пятен. При поражениях кожи на теле они практически всегда имеют розовый оттенок. Границы грибковых высыпаний могут быть выраженными или нечеткими, правильными или бесформенными. Пятна при грибке бывают единичными или появляются на теле густой россыпью.
Любые изменения на коже требуют пристального внимания. Зуд пятен – практически в 100% случаев указывает на грибковую природу их появления.
Грибок стоп легче распознать по внезапному огрубению. Кожа становится толстой, твердой, покрывается крупными сухими чешуйками. Они плохо отделяются, а по краям соединятся со здоровыми участками покровов. Попытки удалить чешуйки заканчиваются образованием ранок. Другой признак грибка – появление плотных папул, разных размеров с жидкостью внутри. Такие образования мешают при ходьбе, нередко провоцируют боль.
Что делать при симптомах грибка
С первыми признаками дерматомикоза необходимо обратиться к врачу. Лечением грибка занимается дерматолог. При осложненных и системных инфекциях врач дает направление к микологу.
Заподозрить микоз кожи специалист может на первом осмотре. Для уточнения диагноза потребуются дополнительные диагностические процедуры:
- дерматоскопия;
- забор соскоба с кожи для последующего микроскопического исследования;
- анализ ПЦР;
- культуральный посев.
Последний тип диагностики используется редко (при сомнениях относительно природы возбудителя). Поводом для исследования может быть затрудненная терапия микоза, когда болезнь не поддается классическому лечению.
Медикаментозная терапия дерматомикозов
Классический вариант лечения дерматомикозов – применение наружных средств с фунгицидными веществами в составе. Противогрибковые лекарства выпускают в формах:
- мазь;
- крем;
- лосьон (с капельным или спреевым дозатором).
При неосложненных дерматокмикозах достаточно препаратов с одним веществом в составе. Если грибок сопровождается бактериальной инфекцией, выраженными воспалительными реакциями, назначают комбинированные средства.
При поверхностных грибковых инвазиях рекомендуют крем или мазь Клотримазол, Кетоконзол, Сертаконазол, Бифоназол. Средства наносят на пораженные участки кожи тонким слоем, на высыпания и зону вокруг них. Зачастую достаточно 2 обработок в сутки. При трихофитии назначают нанесение раствора йода утром, серной, серно-салициловой, или серно-дегтярной мази вечером.
При грибке кожи на стопах врачи рекомендуют препараты широкого спектра действия. Назначают средства на основе Тербинафина или Нафтифина. Самые популярные лекарства – Ламизил, Экзодерил, Нитрофунгин.
Противогрибковый крем наносят на вымытые с мылом и хорошо просушенные стопы. Желательно дождаться полного впитывания препарата. После этого можно надеть хлопчатобумажные носки. Стопы обрабатывают 2 раза в день.
При трихофитии, глубоких поражениях кожи грибком повышается риск присоединения вторичной инфекции. Чтобы предотвратить ее назначают обработки антисептиками. В классическом варианте терапии применяют йод. При осложненных формах потребуются дополнительные обработки Мирамистином или Хлоргексидином.
Противовоспалительные, антибактериальные и противогрибковые свойства сочетают в себе препараты с комплексным составом. Для лечения назначают Тридерм, Белогент, Белодерм. Они содержат гормональные, фунгицидные, антибактериальные компоненты. Мази наносят на пораженные участки 2 раза в день.
Лечение наружными средствами хорошо помогает при начальных стадиях дерматомикоза. При прогрессирующем заболевании потребуются антимикотики системного действия. Особенно эффективными считаются таблетки с Тербинафином (Экзифин, Ламикон). Вещество попадает в системный кровоток, накапливается в тканях (даже в придатках кожи и поверхностном слое). Частично препарат выводится вместе с секретом потовых и сальных желез, чем способствует устранению грибка из волосяных фолликулов, ногтей.
При наличии противопоказаний или неэффективности Тербинафина врачи назначают таблетки с Кетоконазолом. Значительно реже рекомендуют препараты пролонгированного действия на основе Флуконазола. Суточная доза в 150 мг создает в организме губительные для грибка концентрации на 4-6 суток.
Нельзя использовать системные противогрибковые препараты для самолечения. Они обладают нефро- и гепатотоксичными свойствами, вызывают ряд побочных эффектов. Лечение антимикотиками требует регулярного контроля над состоянием по результатам лабораторных анализов крови.
Если не лечить грибок
Дерматомикозы причиняют больному массу дискомфорта, провоцируют появление серьезных косметических дефектов (эрозии и рубцы на коже, облысение, нарушение пигментации). Микотоксины, попавшие в системный кровоток, отравляют организм изнутри. Они обладают канцерогенными свойствами, нарушают работу печени, почек, сердца. Запущенные микозы заканчиваются развитием полиорганной недостаточности.
Большинство грибков высококонтагиозны и легко передаются от человека к человеку. Больной микозом представляет угрозу для своих близких. Особенно уязвимы перед микроскопическими грибками дети. Ввиду несовершенства иммунной системы инфекции «цепляются» к ним за короткие сроки, даже при минимальном обсеменении спорами.
Прогрессирующий грибок становится устойчивей перед действием медикаментов. Чем глубже инфекция, тем менее эффективны мази и кремы. При обширных поражениях требуются высокие дозы фунгицидных веществ, что создает дополнительную нагрузку для организма.
Лечение народными средствами усугубляет проблему. Овощные соки, продукты питания, различные масла и смеси с медом создают питательную среду для размножения грибка. Параллельно назначенному врачом лечению можно использовать травяные настои и отвары (календулы, коры дуба, череды, ромашки). Применение растительных вытяжек также нужно согласовать со специалистом.
Универсальным средством от грибков считается эфирное масло чайного дерева. Вытяжка обладает фунгицидными и фунгистатическими свойствами, однако чистое масло может спровоцировать аллергию и усложнить лечение.
Истории наших читателей
Читать статью полностью >> |
Для профилактики дерматомикозов человек должен избегать контактов с бездомными животными, следить за здоровьем домашних питомцев. Важно использовать только свои гигиенические приспособления (мочалку, расческу, полотенце), не давать личную одежду другим людям. После посещения сауны или бассейна необходимо принять горячий душ или ванну, для мытья лучше использовать обычное хозяйственное мыло.
смитомы, лечение и профилактика, стадии микоза кожи
Микоз – сборное понятие, которое используется для обозначения всех вариантов заболеваний кожи и внутренних органов человека, прогрессирующих из-за активности и распространения паразитарных грибков.
Разновидностей болезни существует много. Ученые указывают на возможность поражения организма человека несколькими сотнями типов грибков. Симптоматика в большинстве случаев одинаковая. Своевременное лечение микозов позволяет полностью избавиться от проблемы.
Причины появления микоза на коже
Главной причиной развития соответствующего заболевания является инвазия грибками. Контакт с патогенным или условно-патогенным организмом не всегда заканчивается болезнью. Микоз кожи возникает на фоне ослабленного иммунитета и наличия царапин, трещин в эпидермисе, сквозь которые проникает возбудитель.
Распространение грибка происходит при телесном контакте с зараженным пациентом, использовании его одежды, обуви или средств личной гигиены – зубная щетка расческа.
Вспомогательными факторами, повышающими риск развития микоза кожи, являются:
- Врожденный или приобретенный иммунодефицит.
- Наличие сопутствующих заболеваний.
- Хроническая травматизация кожи или природных складок эпидермиса.
- Игнорирование правил личной гигиены.
- Использование общей обуви, одежды и тому подобное.
Отдельно стоит выделить грибовидный микоз. Патология относится к числу злокачественных опухолей. Развивается новообразование в верхних слоях кожи и складках эпидермиса из-за массивной пролиферации Т-клеток. Грибовидная форма микоза дополнительно поражает лимфатические узлы и внутренние органы пациентов.
Симптомы микоза
Клиническая картина заболевания зависит от количества и агрессивности грибка. Микозы традиционно поражают кожу и складки эпидермиса в области стоп, кистей рук, лица. Грибковая инвазия сопровождается характерной симптоматикой.
Типичные признаки микоза кожи:
- Сухость эпидермиса.
- Интенсивный зуд, который трудно унять.
- Возникновение патологических кожных элементов на поверхности и в складках эпидермиса.
- Формирование опрелостей, корочек, желтоватых пленок и чешуек над участками инвазии грибка.
- Отслаивание отдельных частей рогового слоя эпидермиса.
- При втягивании в процесс ногтей, пластинка покрывается бугорками, становится шероховатой и может отпадать полностью.
Грибовидный микоз отличается клинически. Он несет большую угрозу для здоровья и жизни пациента, сокращая ее длительность при отсутствии адекватного лечения. Симптомами грибовидного микоза являются:
- Возникновение желтых, багряных или коричневых пятен на ранних этапах прогрессирования заболевания.
- Сильный зуд.
- Уплотнение пятен с образованием бляшек, которые возвышаются над поверхностью кожи.
- Постепенный рост опухолей в эпидермисе.
- Увеличение в размерах лимфатических узлов в зоне поражения кожи.
Грибовидный микоз на поздних стадиях своего развития дополнительно сопровождается поражением внутренних органов с прогрессированием соответствующих дисфункций.
Стадии развития микоза кожи
Патологические процессы протекают постепенно. Иногда можно выделить ряд стадий, которые характеризуют особенности развития конкретного заболевания. Для дерматомикозов, вызванных инвазией грибка, такое деление нехарактерно. Грибовидный микоз – исключение.
Стадии заболевания:
- Эритиматозная. Ключевой симптом – появление пятен.
- Бляшечная. Пятна организовываются, уплотняются, возвышаются над поверхностью эпидермиса.
- Опухолевая. В коже возникают злокачественные новообразования.
Прогрессирование болезни приостанавливается с помощью соответствующей терапии, которая отличается в зависимости от стадии патологии.
Виды микоза
Микоз кожи – распространенная проблема, с которой сталкиваются одинаково мужчины и женщины. Классификация болезней базируется на определении вида грибка, проникшего в верхние слои или складки эпидермиса.
Виды микозов:
- Дерматомикоз. Возбудитель – грибок Trichophyton.
- Кандидоз. Патология провоцируется грибками рода Candida.
- Онихомикоз – Trichophyton rubrum.
- Пестрый лишай – Malassezia furfur.
- Споротрихоз – Sporotrichium и другие.
Наиболее распространенными остаются первые три представителя.
Какой врач лечит микоз?
При возникновении характерной клинической картины с образованием участков шелушения, зуда в области природных кожных складок или на поверхности эпидермиса стоит обратиться к дерматологу.
Лечение грибка при установлении возбудителя может проводиться в амбулаторных условиях силами семейного врача или участкового терапевта. Грибовидный микоз требует внимания онколога и гематолога.
Диагностика
Микоз кожи – заболевание, которое хорошо поддается диагностике. Для верификации наличия патологии необходимо проанализировать характерные жалобы пациента, присутствие в анамнезе контактов с зараженным человеком, использование общей обуви, одежды или других принадлежностей.
Врачи дополнительно проводят следующие обследования:
- Общий анализ крови.
- Биохимический анализ крови.
- Биопсию пораженного лимфатического узла при грибовидном микозе.
- Микроскопическое исследование материала, взятого из патологических кожных элементов.
При необходимости проводятся дополнительные консультации с узкими специалистами – пульмонолог, гематолог, онколог.
Лечение грибка микоза
Микоз кожи – излечимая патология. Однако длительность терапии может существенно варьировать. Иногда полностью вылечить заболевание не удается. Проблема регулярно рецидивирует, доставляя пациенту много дискомфорта.
Единственной универсальной схемы оздоровления при грибковом поражении кожи не существует. Подбор индивидуального плана лечения зависит от следующих факторов:
- Вид грибка.
- Продолжительность заболевания.
- Наличие индивидуальной непереносимости отдельных медикаментов.
- Выраженность и обширность патологии.
- Параллельное развитие других заболеваний.
Как лечить микоз? Терапия базируется на применении противогрибковых (фунгицидных) препаратов. Использование носит как местный, так и системный характер. Прием специализированных средств внутрь предусмотрен при обширном поражении кожи с возможным втягиванием в патологический процесс внутренних органов. Для системной терапии назначают Гризеофульвин. Лекарство воздействует на разные типы патогенных грибков и хорошо переносится организмом пациента.
Местно наносятся мази и кремы с фунгицидным эффектом:
- Миконазол.
- Эканозол.
- Флуконазол.
- Тербинафин.
- Клотримазол.
Для терапии грибовидного микоза используют комбинацию следующих групп медикаментов:
- Цитостатики – Фторурацил, Циклофосфан. Средства блокируют деление злокачественных клеток.
- Антибиотики с противоопухолевым эффектом – Доксорубицин.
- Системные или местные глюкокортикостероиды – преднизолон, гидрокортизон.
Сочетание указанных средств тормозит пролиферацию новых злокачественных клеток и способствует переводу болезни в фазу ремиссии. Пациенты лечатся с дополнительным использованием лекарства Проспидин, которое также обладает противоопухолевым эффектом.
Осложнения
Микозы – группа заболеваний, которые трудно поддаются лечению. При отсутствии терапии они могут вызывать специфические осложнения:
- Переход болезни в хроническую форму. Из-за неправильного подбора медикаментов грибки теряют чувствительность к некоторым из лекарственных средств, что тормозит выздоровление пациента.
- Развитие хронической аллергии. Токсины и продукты жизнедеятельности грибков вызывают гиперсенсибилизацию тела человека. Организм неадекватно реагирует на внешние факторы (солнце, пыльца, продукты) с развитием аллергии.
- Вторичное инфицирование ранений. Из-за наличия трещин, царапин повышается риск проникновения бактерий в кровь человека.
Своевременное лечение снижает риск развития осложнений.
Профилактика микозов
Профилактика микозов предусматривает комплекс мероприятий:
- Использование только личных средств и предметов гигиены.
- Исключение тесного контакта с зараженными людьми.
- Соблюдение правил личной гигиены.
- Своевременное обращение к врачу при возникновении характерной симптоматики.
Микозы – неприятная группа болезней, которые не всегда легко вылечить. Зуд, изменение цвета кожи или возникновение пятен должно стать причиной для консультации с доктором. В большинстве случаев процесс оздоровления занимает от 1 до 2 месяцев.
Микоз — лечение, симптомы, причины
Микоз является грибковым заболеванием, относящимся к распространенной группе инфекционных болезней, вызываемых паразитическими патогенными и условно-патогенными микроорганизмами. Микротравмы способствуют спорам грибков попасть в кожу, а также подкожную клетчатку. Далее грибок распространяется на слизистую оболочку глаз, верхние дыхательные пути или оседает в легких в момент дыхания. Тяжесть и характер микоза кожи напрямую зависят от грибка и места поражения. Патогенез микозов провоцируют любые заболевания, вызывающие снижение иммунитета. Далее поражается множество участков кожи, слизистых оболочек, наружных половых органов, пищевод и легкие. Микозы кожи, зачастую, подвержены хроническому течению и классифицируются на две основные группы: глубокие и поверхностные. К глубоким микозам относят оппортунистические системные микозы, а также подкожные микозы (споротрихоз, хромобластомикоз). Поверхностные микозы кожи включают в себя кератомикозы, дерматомикозы, кандидоз. На сегодняшний день проблема грибковых заболеваний является острой. Микозы поражают многие органы, обезображивают кожу больного, вызывают аллергические реакции.
Микоз причины
Агрессивность грибка является различной, и об этом свидетельствует его вирулентность (заразность). Говоря о факторе агрессивности инфекции, хочется отметить, что группа людей находящихся в общих внешних условиях, заболевают все по-разному. Одни люди подхватывают грибок сразу, другие подхватывают и болеют скрыто, а некоторые вообще не заболевают. Все зависит от защитных сил организма и наличия текущих заболеваний. Распространению микоза способствует снижение иммунитета, ВИЧ-инфекция, применение антибиотиков и противоопухолевых средств, варикозное расширение вен на ногах, рожистое воспаление, ссадины, трофические язвы, микротравмы, влажность, теплота, несоблюдение санитарно-гигиенических правил, недостаток вентиляции и избыток мыла, который удаляет бактерии вместе с липидным слоем кожи. Патогенные грибы способны проникнуть в наш организм в момент определенных медицинских манипуляций.
Причинами микоза является снижение естественной сопротивляемости организма при определенных болезнях и условиях, что способствует инвазивному росту грибов. К таким болезням и условиям относят злокачественные новообразования, сахарный диабет, иммунодефицит, длительное применение антибиотиков и кортикостероидов.
Местные грибковые поражения на самочувствии людей практически не отражаются, чего не скажешь о системных микозах. Системные микозы паразитируют на внутренних половых органах и при этом широко распространяются. В настоящее время системные микозы расширились, и к ним присоединился грибковый менингит новорожденных, кандидемия, хронический генерализованный, а также диссеминированный кандидоз, висцеральный кандидоз, стрептококковая пневмония, менингит, аспергиллез легких, мозга и среднего уха.
Микозы кожи относят к патогенным многочисленным и разнообразным грибам, которые поражают животных и человека. Известны сотни грибов, представляющих опасность для человека. Для того чтобы попасть в организм грибы находят различные пути. Но основными путями служит поврежденная кожа, слизистые оболочки, увлажнение кожи, хронические заболевания, стероидная терапия, облучение, лечение цитостатиками, гормональные, а также обменные нарушения.
Возможны профессиональные случаи при длительных контактах с микроскопическими грибами, которые приводят людей к системным поражениям. Например, аллергозы у мукомолов или людей сталкивающихся с заплесневелым сырьем, занимающихся обработкой льна, конопли. Грибковое заболевание характеризуется несколькими периодами. Инкубационный период может продолжаться от семи дней и до нескольких месяцев.
Микоз симптомы
Симптомы микозов очень разнообразны. Микоз стоп и рук начинается с еле заметного шелушения кожи, которое локализуется между пальцами в складках. Пораженная кожа не только шелушится, на ней появляются болезненные гнойные пузырьки. Поверхность ног покрывается опрелостями, эпидермис грубеет и развиваются натоптыши. Волосы, а также ногтевые пластинки тускнеют, приобретая желтоватый цвет, затем утолщаются и расслаиваются, становясь ломкими. Перечисленные симптомы микозов могут сопровождаться зудом, поднятием температуры, возникновением лимфангоита, болезненных ощущений и общих недомоганий.
Клиника микозов
По своим проявлениям микозы разнообразны, а по характеру течения делятся на хронические, острые, глубокие, поверхностные, распространенные и очаговые. Зачастую регистрируются пиемии с диссеминацией и грибковые сепсисы. Выделяют следующие группы микозов: кандидоз, дерматомикозы, кератомикозы, кокцидиоидный микоз, бластомикоз, гистоплазмоз, споротрихоз, плесневые микозы, редкие микозы (хромомикоз, риноспоридиоз).
фото микоза стоп
Микоз стоп
Заболевание этой формой развивается после посещения мест общего пользования: бань, бассейнов, саун, общественных душевых, а также контакта с больными и их одеждой, обувью, всевозможными предметами обихода: полотенцами, ковриками из ванной, мочалками, маникюрными принадлежностями. Грибки очень любят влагу. И влажная среда, например, в ванной комнате на коврике, является благоприятной для грибка не на одни сутки. Вот поэтому врачи рекомендуют появляться в душе и в других местах в своих тапочках. Приживлению микоза на коже влияют следующие факторы: чрезмерная потливость, а также кожные микротравмы, потертости.
Микоз стоп способен захватить не только стопы, ногти, а и пальцевые складки. Влажная и теплая среда способствует появлению трещин, которые также свидетельствуют о заболевании. Бывает, что микоз стоп провоцирует огрубение, а также шелушение кожи на стопах и характеризуется зудящими пузырьками, огрубением кожи в виде натоптышей. Зачастую грибок, изначально начавшийся на стопе, переходит выше на голень. В местах, где нет складок кожи, микоз принимает неправильную круглую форму. Больные жалуются на болезненность, а также небольшое недомогание в очагах поражения. Способны увеличиться регионарные лимфатические узлы, возникнуть лимфангоит, а температура стать субфебрильной.
фото микоза ногтей
Микоз ногтей
Самым неприятным микозом ногтей выступает поражение, вызванное кандидами. Для заболевания характерно воспаление ногтевого валика, при этом возможны гнойные выделения. Зачастую заболевание ногтей ограничивается поражением ногтевых пластин. Сами ногти при этом расслаиваются, становятся волнистыми, однако деформации могут быть подвержены не все ногти, а лишь несколько. Люди зачастую не торопятся обращаться за лечением к врачу и делают это, когда заболевание приобретает запущенную форму и поражены уже все ногти на ногах и частично на руках. Такие формы лечатся гораздо дольше и сложнее. Многие больные пытаются самостоятельно справиться со своей проблемой и только после неудач обращаются к специалистам.
Микоз лечение
Многие противогрибковые препараты эффективны при течении заболевания не более пяти лет. В других случаях необходимы более сильные средства. Лечение микоза кожи необходимо начинать, как будет выяснен возбудитель заболевания. Некоторые формы подлежат лечению только в больнице, а некоторые успешно излечиваются в домашних условиях. Необходима еще и поддержка иммунитета организма. С этой целью назначают минеральные добавки, витамины, биологически активные добавки.
Как лечить микоз? Воздействие на микоз идет по двум направлениям: снаружи и изнутри организма. Широко применяются в лечении производные Пиримидина, а также Имидазола. Наряду с лекарственной терапией для лечения микозов подключают физиопроцедуры, массаж, диету, гигиеническую обработку обуви специальными составами. Длительное время местно в лечении применялись следующие средства: Микозалон, Клотримазол, Хинофунгин, Микосептин, Нитрофунгин, Анмарин, Октицил, пластырь Эпилиновый.
В лечении микозов хорошо зарекомендовали группы антисептиков: препараты Йода, Фенола, производные Ундециленовой кислоты.
Лечение системных микозов представляет трудности и проводится системными антигрибковыми препаратами. Такими как Орунгал, Дифлукан (Флуконазол), а также Ламизил. Этим препаратам свойственна фунгицидная, а также фунгистатическая функция. Применение в комплексе препаратов позволяет избавиться от микоза стоп и рук, а также сохранить ногти без изменений. Препараты способны быстро проникнуть в верхний роговой слой, длительный период там сохраниться, что позволит в сравнительно короткие сроки провести лечение.
Лечение микоза стоп включает немедленную дезинфекцию обуви. С этой целью используют ватный тампон, смоченный в уксусной кислоте или в растворе формалина. Далее обрабатывают этими тампонами внутренние места обуви, оставляя его в носке. Всю обувь складывают в полиэтиленовый мешок. Для дезинфекции достаточно одной ночи. Колготы, чулки, носки подлежат кипячению. Каждое посещение бань, пляжей, душевых, заканчивается обработкой межпальцевых складок, а также подошв раствором йода, жидкостью Андриасяна, Нитрофунгином, мазями Батрафен, Микоспор, Травоген, Низорал и др.
Микоз народные средства
Иногда народные средства способны значительно облегчить состояние больного. Все процедуры по лечению пораженных мест рекомендуют проводить перед сном. Пораженную часть тела следует мыть с мылом, подсушивать с помощью зеленки или йода. Широко применимо из народной медицины лечение травами ядовитых растений, но только наружно. К таким травам относят тисс, чемерицу белую, зеленую, ломонос, паслен черный, щитовник, прострел луговой. На сухие очаги поражения наносятся мази и кремы, которые готовятся на основе нутряного свиного жира или аптечного вазелина. Для приготовления такой мази необходимо основу распустить до жидкого состояния на водяной бане и добавив лекарственное растение варить от 2-х до 4-х часов. Полученную мазь хранить в холодильнике.
Антимикотические свойства присущи довольно большому перечню растений, однако использовать их необходимо только после консультации с врачом. Лечение травами эффективно при системных микозах. К примеру, ряска, вероника, чистотел, солодка, багульник — обладают иммуномодулирующими свойствами, что позволяет устранить нарушения иммунной системы.
Тысячелистник, мята, жостер, одуванчик, лабазник, горечавка, горчица, хмель — оказывают хорошее лечебное действие при грибковых поражениях ЖКТ.
Бедренец, фенхель, иссоп, дудник, истод, бузина, багульник, бузина дают лечебный эффект при бронхитах, грибковых пневмониях и бронхиальной астме.
Поражение мочевыводящих путей грибковым циститом лечат пижмой обыкновенной, лапчаткой гусиной, мареной красильной, плющом, ромашкой.
Грибковое поражение глаз излечивают отваром из тысячелистника или аира.
Способность к противогрибковым свойствам у безвременника, прострела, тисса, чистотела, позволяет осуществлять лечение микоза у онкологических больных.
Информация, представленная в данной статье, предназначена исключительно для ознакомления и не может заменить профессиональную консультацию и квалифицированную медицинскую помощь. При малейшем подозрении о наличии данного заболевания обязательно проконсультируйтесь с врачом!
Фунгоидный микоз (включая синдром Сезари) Лечение (PDQ®) — Версия для специалистов в области здравоохранения
Клиническая презентация
Грибовидный микоз и синдром Сезари являются злокачественными новообразованиями.
Т-лимфоциты, которые обычно обладают фенотипом поверхности клеток-помощников / индукторов.
Эти виды новообразований изначально проявляются поражением кожи и, как таковые, были
классифицируются как кожные Т-клеточные лимфомы. [1] Кожные Т-клеточные лимфомы следует отличать от других Т-клеточных лимфом, которые
поражают кожу, например, анапластическую крупноклеточную лимфому (CD30-положительный результат),
периферическая Т-клеточная лимфома (CD30-отрицательный, без поражения эпидермиса),
Т-клеточный лейкоз / лимфома взрослых (обычно с системным поражением), или
подкожная панникулитная Т-клеточная лимфома.[2,3] Эти гистологические типы
Т-клеточных лимфом обсуждаются в другом обзоре PDQ. (См. PDQ
краткое изложение лечения неходжкинской лимфомы у взрослых для получения дополнительной информации.)
Обычно течение грибкового микоза протекает вяло. [4] Симптомы болезни
могут проявляться в течение длительного времени, от 2 до 10 лет, потому что кожные высыпания усиливаются и ослабевают
прежде, чем они получат подтверждение биопсии. Грибовидный микоз и синдром Сезари поддаются лечению с помощью
доступная местная терапия, системная терапия или и то, и другое.На сегодняшний день лечебные методы имеют
доказано неуловимо, за возможным исключением пациентов с минимальным
заболевание, ограниченное кожей.
В
Кроме того, некоторые благоприятные или вялые состояния можно спутать с
грибовидный микоз. Консультация патологоанатома, у которого
опыт в различении этих состояний важен. [1]
Прогноз и выживаемость
Прогноз для пациентов с грибовидным микозом и синдромом Сезари основан на степени заболевания (стадии) на
презентация.[5] Наличие лимфаденопатии и вовлечение
периферическая кровь и внутренние органы увеличиваются с ухудшением кожных
[5-8] Международный консорциум кожной лимфомы провел ретроспективный обзор 1275 пациентов и обнаружил, что следующие четыре независимых прогностических маркера указывают на худшую выживаемость: [9]
- Болезнь IV стадии.
- Возраст старше 60 лет.
- Трансформация крупных клеток.
- Повышенная лактатдегидрогеназа.
Средняя выживаемость
следующий диагноз зависит от стадии. Пациенты с болезнью IA стадии
имеют среднюю выживаемость 20 лет и более. Большинство смертей из-за этого
группа не вызвана и не связана с грибовидным микозом. [10,11] Напротив, больше
более 50% пациентов со стадией III-IV болезни умирают от грибкового микоза, с
медиана выживаемости составляет примерно 5 лет. [7,9,12,13] Международный прогностический индекс кожной лимфомы использовал мужской пол, возраст старше 60 лет, бляшки, лимфатические узлы, вовлечение крови и висцеральное вовлечение в качестве плохих прогностических факторов для определения прогнозируемых факторов. общая выживаемость (ОС) и выживаемость без прогрессирования в группах как на ранней, так и на поздней стадии.[14]
В отчете о 1798 пациентах из базы данных программы Национального института рака по надзору, эпидемиологии и конечным результатам (SEER) было обнаружено увеличение числа вторичных злокачественных новообразований (стандартизированный коэффициент заболеваемости 1,32; 95% доверительный интервал [ДИ] 1,15–1,52), особенно для лимфомы Ходжкина, неходжкинской лимфомы и миеломы. [15] Другой отчет о 4459 пациентах из базы данных SEER показал, что 19,2% афроамериканцев с грибовидным микозом имеют более короткую ОС, что может быть связано с характеристиками заболевания, социально-экономическим статусом и типом терапии (отношение рисков 1.47; 95% ДИ 1,25–1,74; P <.001). [16]
Кожное заболевание может проявляться в виде экзематозного пятна или стадии налета.
покрытие менее 10% поверхности тела (Т1), покрытие стадии налета
10% или более поверхности тела (Т2) или в виде опухолей
(T3), которые часто подвергаются некротическим изъязвлениям. [17,18] Несколько ретроспективных исследований показали, что 20% пациентов прогрессируют от стадии I или II до стадии III или IV. [19-21] Синдром Сезари проявляется генерализованной эритродермией (T4 ) и вовлечение периферической крови.Однако существуют некоторые разногласия относительно того, являются ли грибовидный микоз и синдром Сезари вариантами одного и того же заболевания [22]. В том же ретроспективном исследовании со средней продолжительностью наблюдения 14,5 лет было обнаружено, что только 3% из 1422 пациентов прогрессировали от грибкового микоза до синдрома Сезари [19].
Существует консенсус в отношении того, что пациенты с синдромом Сезари (лейкемией) имеют плохой прогноз (средняя выживаемость, 4 года), с типичной генерализованной эритродермией или без нее. [23,24] Цитологическая трансформация лимфомы низкой степени злокачественности в лимфому высокой степени. -сорт
лимфома (крупноклеточная трансформация) редко (<5%) во время этих заболеваний и связана с
с плохим прогнозом.[25-27] Ретроспективный анализ 100 случаев с крупноклеточной трансформацией выявил снижение выживаемости по конкретному заболеванию при внекожной трансформации, увеличение степени поражения кожи и отрицательность CD30. [28] Частая причина смерти во время фазы опухоли:
сепсис, вызванный хронической кожей
инфицирование стафилококком, простым герпесом, опоясывающим лишаем и грибковыми кожными инфекциями. [29,30]
Фолликулотропный грибовидный микоз — это вариант грибовидного микоза, отмеченный фолликулотропными, а не эпидермотропными неопластическими инфильтратами с преимущественным расположением в голове и область шеи.[31] Фолликулотропный грибовидный микоз на ранней стадии бляшек имеет очень вялый прогноз, в то время как внекожное заболевание p
Микозы | Микология онлайн
Клинические группы по грибковым инфекциям
Можно выделить следующие клинические группы
Больше
Это поверхностные косметические грибковые инфекции кожи или стержня волоса. Никакие живые ткани не проникают и клеточный ответ от хозяина отсутствует. Эти инфекции часто настолько безобидны, что пациенты часто не подозревают о своем состоянии.
Больше
Это поверхностные грибковые инфекции кожи, волос или ногтей. Никакие живые ткани не поражаются, однако в организме хозяина происходят различные патологические изменения из-за присутствия инфекционного агента и продуктов его метаболизма.
Больше
Это хронические локализованные инфекции кожи и подкожной клетчатки после травматической имплантации этиологического агента. Все возбудители грибов — это почвенные сапрофиты, способность которых приспосабливаться к тканевой среде и вызывать заболевание чрезвычайно разнообразна.
Больше
Это грибковые инфекции, вызванные грибковыми патогенами, которые могут преодолеть защитные силы нормального человека-хозяина, изменив свою морфологическую форму. Они географически ограничены, и после вдыхания конидий первичный очаг инфекции обычно находится в легких.
Больше
Это грибковые инфекции, которые возникают почти исключительно у ослабленных пациентов, у которых нарушены нормальные защитные механизмы. Вовлеченные организмы — это космополитические грибы, которые обладают очень низкой внутренней вирулентностью.
Заявление об ограничении ответственности: Национальный справочный центр микологии не предоставляет консультации или направления пациентам. Лица, обеспокоенные грибковой инфекцией, должны проконсультироваться с зарегистрированным медицинским работником. Информация предоставляется только для образовательных и научных целей и не предназначена для замены рекомендаций зарегистрированного медицинского работника. Информация об услуге, продукте или лечении не подразумевает одобрения.
Что такое грибковый микоз? — грибковый микоз
Грибовидный микоз — разновидность лимфомы.Болезнь часто поражает кожу, но может распространяться на различные другие части тела, включая кровь и внутренние органы, с разной степенью тяжести. Подавляющему большинству пациентов с грибовидным микозом, как правило, придется жить с этим заболеванием всю оставшуюся жизнь, поскольку реальных известных способов лечения не существует. Можно только попытаться вылечить симптомы и облегчить некоторые из связанных с этим осложнений.
Почему это называется грибковым микозом?
Название «грибовидный микоз» происходит от очень специфического источника.Врач, который первым задокументировал заболевание грибовидным микозом у пациента, был французским врачом по имени Жан Луис Марк Алибер. Он назвал это грибовидным микозом из-за сходства пятен на коже с поднятыми грибами. Итак, грибовидный микоз означает грибковое заболевание, похожее на гриб. Самый первый случай заболевания был зарегистрирован в 1806 году, и доктор Алиберт дал ему название грибовидный микоз.
Причины грибкового микоза у человека
Точная причина грибкового микоза не известна, но было сделано несколько выводов о том, что это заболевание имеет негенетические или наследственные причины.Есть по крайней мере один случай, который может опровергнуть эту теорию, поскольку он может показать, что у нее есть возможные генетические связи. Это заболевание чаще встречается у мужчин, чем у женщин, и встречается у людей старше 20 лет. Наиболее распространенная группа людей, пораженных грибовидным микозом, — это люди в возрасте от 40 до 50 лет и люди, страдающие опухолями, эритродермией или лейкемией. Известно, что эти состояния чаще всего сочетаются с грибовидным микозом.
Простые тесты могут быть выполнены на биопсиях пораженной кожи, чтобы определить, есть ли у пациента грибовидный микоз.Если пациент не соответствует возрастной группе, в которой грибовидный микоз наиболее распространен, врач может не обращать внимания на состояние и неправильно диагностировать его. Важно запросить дополнительные анализы для проверки на грибковый микоз, если вы подозреваете, что он у вас есть. Даже если врач не согласен с вашим подозрением, ему / ей придется провести дополнительные анализы и скрининг, чтобы исключить возможность наличия у пациента грибовидного микоза и других заболеваний, связанных с лимфомой.
Возможные симптомы и связанные с ними осложнения
Существует множество симптомов и связанных с ними осложнений, которые могут привести к ускоренному развитию болезни.Известно, что следующие симптомы являются одними из наиболее распространенных и связанных симптомов, которые, как установлено, являются частью грибкового микоза:
- опухоли
- патчей
- очагов
- зуд
Опухоли — Так как это тип лимфомы, опухоли являются очень важным предупреждающим знаком, чтобы остерегаться этого и многих других заболеваний, которые могут поражать организм. Обычно они являются лишь индикатором и не могут реально определить, есть ли у пациента грибовидный микоз или нет, поскольку биопсия опухолей может даже не выявить никакой информации о состоянии грибовидного микоза.
Пятна — Один из наиболее распространенных индикаторов — участки кожи с обесцвечиванием, странной текстурой и т. Д. Это чаще всего путают с другими распространенными проблемами, такими как экзема или псориаз, но на самом деле все обстоит иначе. Пятна не являются спорадическими и случайными, но часто очень необычны. Таким образом, по сравнению с другими кожными заболеваниями их можно легко спутать.
Поражения — Изменение цвета и повреждение кожи грибовидным микозом могут быть довольно обширными.Лучший способ определить, вызваны ли поражения грибовидным микозом, — это провести биопсию кожных поражений и проверить их на наличие клеток типа лимфомы, которые могут присутствовать при грибовидном микозе. Поражения могут превратиться в неприятные язвы и язвы, если не позаботиться о них должным образом. Некоторые поражения, вызванные грибовидным микозом, будут расти с удивительной скоростью и должны быть проверены врачом. Очень важно тщательно проверять эти симптомы.
Зуд — 20 процентов пациентов с грибовидным микозом будут иметь приступы сильного зуда, которые могут причинить сильный дискомфорт.Это часто заставляет многих врачей думать, что это просто сухая кожа, экзема, псориаз или подобное состояние кожи. Сильный зуд с любыми другими симптомами может быть признаком грибкового микоза.
Существуют также различные стадии, которые может пройти пациент, если он / она страдает грибковым микозом. Эти этапы часто классифицируются как:
Каждый этап связан с разной степенью летальности. Очень важно, чтобы пациенты с грибовидным микозом сами регулярно обследовались, чтобы убедиться, что болезнь не перешла в гораздо более опасную стадию.Рекомендуется принять некоторые профилактические меры и лечение, чтобы снизить вероятность его прогрессирования.
Средства для лечения грибкового микоза
Не существует установленного метода лечения грибовидного микоза, и методы лечения могут дать разные результаты. Лечение обычно направлено на предотвращение распространения лимфомы. Лучше всего спросить врача, какое из следующих методов лечения может помочь контролировать распространение болезни или предотвратить ее обострение:
- простой солнечный свет
- обработка ультрафиолетом
- стероиды для местного применения
- Системная химиотерапия
- местная поверхностная лучевая терапия
- Ингибитор гистондеацетилазы
- облучение кожи электронным лучом
- биотерапия
Простой солнечный свет — Солнечный свет и его преимущества, такие как способность впитывать витамин D и кальций, могут помочь увеличить вероятность увеличения пользы для здоровья, что может помочь продвинуть болезнь в ремиссию.Эта терапия очень проста, но ее необходимо контролировать, чтобы предотвратить вторичные проблемы, такие как рак кожи.
Ультрафиолетовое лечение — Ультрафиолетовый свет очень мощный и может иметь большое влияние на лечение грибовидного микоза, если он реагирует на лечение. Ультрафиолетовый свет может вызвать гибель кожи и формирование новой кожи, возможно, удалив некоторые пятна, поражения и другие характерные кожные состояния грибовидного микоза.
Стероиды для местного применения — Стероиды могут помочь уменьшить воспаление в определенной области, а также способствовать увеличению притока кислорода к месту с расширением кровеносных сосудов, что позволяет излечить последствия грибкового микоза в этом месте.Это очень многообещающий вариант лечения, но следует также помнить, что использование стероидов может иметь побочные эффекты.
Системная химиотерапия — Химиотерапия имеет разную степень успеха и иногда может помочь удалить все следы болезни. Это одно из менее желательных методов лечения, так как оно вызывает серьезное отравление системы и может быть очень неприятным, приводя к отключению органов и вызывая серьезные побочные эффекты, которые в некоторых случаях могут даже оказаться фатальными.
Местная поверхностная лучевая терапия — Радиотерапия заставляет радиоактивные элементы убивать грибовидный микоз, по существу удаляя его из определенного места. Это лечение может иметь широкий спектр возможных результатов и может фактически препятствовать развитию болезни. Однако он также может вызвать новые осложнения, если не будет должным образом контролироваться.
Ингибитор гистон-деацетилазы — это очень многообещающий метод лечения многих заболеваний лимфомы.Он использовался для лечения грибовидного микоза и показал широкий спектр успешных результатов у нескольких пациентов. Это может помочь стабилизировать состояние пациента и замедлить развитие болезни, даже сделав возможным ремиссию.
Лечение кожи электронным лучевым излучением — Лечение с использованием электронного лучевого излучения эффективно, как и большинство видов лучевой терапии. Отличие от лечения облучением электронным пучком состоит в том, что его можно гораздо эффективнее сфокусировать на одной области, уменьшая ненужные повреждения радиацией на остальной части тела.Важно изучить доступные варианты лечения кожи электронным пучком в качестве альтернативы традиционной лучевой терапии.
Биологические методы лечения — Такие варианты, как интерфероны (животные белки, борющиеся с болезнями) и ретиноиды (лечение витамином А), могут предложить некоторое возможное облегчение и даже ремиссию грибкового микоза. Эти варианты лечения просты в применении и могут быть изменены в соответствии с индивидуальными потребностями каждого пациента.
Перспективы пациентов с грибковым микозом
Около половины людей, пораженных осложнениями грибкового микоза, не умрут, но болезнь может превратиться в нечто большее, чем поверхностная проблема.Когда болезнь распространяется на другие части тела, такие как кровь или ткани органов, это может вызвать серьезное нарушение способности организма бороться с инфекциями. Что еще хуже, это может даже прогрессировать до более высокого уровня лимфомы. Грибовидный микоз может перейти в ремиссию или стабилизацию, но на неопределенный срок и определенно может вернуться, если пациент не примет соответствующие меры для контроля над проблемой. Пациенты, у которых проявляются некоторые из наиболее заметных симптомов, должны попросить своих врачей попробовать провести еще несколько анализов, чтобы определить, страдают ли они этим заболеванием.
грибовидный микоз
грибовидный микоз (также известный как синдром Алиберта-Базена [1] или грибовидная гранулема) является наиболее распространенной формой Т-клеточной лимфомы кожи. Обычно это поражает кожу, но со временем может прогрессировать изнутри.
Грибовидный микоз был впервые описан в 1806 году французским дерматологом Жаном-Луи-Марком Алибером. [2] Название грибовидный микоз несколько вводит в заблуждение — оно означает «грибовидное грибковое заболевание».Однако это заболевание не является грибковой инфекцией, а скорее разновидностью неходжкинской лимфомы. Он был назван так потому, что Алиберт описал опухоли кожи в тяжелом случае как имеющие грибовидный вид. [3]
История
В 1806 году французский врач Жан Луи Алибер первым описал пациента с грибовидным микозом. [4]
Истоки и причины
Причина грибкового микоза неизвестна, но в подавляющем большинстве случаев она не считается наследственной или генетической.Сообщается об одном случае возможной генетической связи. [5] Это не заразно.
Заболевание редко проявляется в возрасте до 20 лет и, по-видимому, гораздо чаще встречается у мужчин, чем у женщин, особенно в возрасте старше 50 лет, где заболеваемость (риск на человека в популяции) действительно увеличивается. . Средний возраст начала заболевания составляет от 45 до 55 лет только для пациентов с болезнью пятен и бляшек, но составляет более 60 лет для пациентов с опухолями, эритродермией (красная кожа) или лейкемической формой (синдром Сезари).
Заболевание представляет собой необычную экспрессию CD4 Т-клеток, части иммунной системы. Эти Т-клетки связаны с кожей, а это означает, что они биохимически и биологически наиболее динамично связаны с кожей. Грибовидный микоз является наиболее распространенным типом «кожной Т-клеточной лимфомы» (CTCL), но существует множество других типов CTCL, которые не имеют ничего общего с грибовидным микозом, и эти заболевания лечат по-разному.
Симптомы, диагностика и стадии
Типичные видимые симптомы включают высыпания, опухоли или поражения. [3] Зуд (кожный зуд) часто встречается, возможно, у 20% пациентов, и не является универсальным.
Диагностика иногда затруднена, потому что ранние фазы заболевания часто напоминают экзему или даже псориаз. Как и в случае любого серьезного заболевания, при подозрении на заболевание рекомендуется проконсультироваться с врачом. Диагноз обычно устанавливается с помощью биопсии кожи. Рекомендуется выполнить несколько биопсий, чтобы точнее поставить диагноз. Диагноз ставится на основе клинической картины и обследования и подтверждается биопсией.
Для определения стадии заболевания могут быть назначены различные тесты для оценки узлов, крови и внутренних органов, но у большинства пациентов заболевание явно ограничено кожей в виде пятен (плоских пятен) и бляшек (слегка приподнятых или « морщинистых » пятен) .
Процедуры и лечебные средства
Грибовидный микоз можно лечить разными способами. [6]
При успешном лечении болезнь может перейти в не прогрессирующее состояние при клинически четком обследовании и различных тестах.Это называется ремиссией; это может длиться бесконечно. Лечение также может привести к тому, что болезнь не прогрессирует, пока она еще присутствует, и это называется стабильным заболеванием; это может длиться бесконечно, но это более серьезная ситуация. Заболевание также может прогрессировать, поражать узлы, кровь и внутренние органы или трансформироваться в лимфому более высокой степени.
Обычные методы лечения включают простой солнечный свет, ультрафиолет, местные стероиды, местную и системную химиотерапию, местную поверхностную лучевую терапию, ингибитор гистондеацетилазы вориностат, общее электронно-лучевое облучение кожи, фотоферез и системную терапию (например,грамм. интерфероны, ретиноиды, рексиноиды) или биологические методы лечения. Процедуры часто используются в сочетании.
Выбор лечения обычно зависит от предпочтений пациента и доступа к терапии, а также от рекомендаций врачей, стадии заболевания, установленной устойчивости к предшествующим методам лечения, аллергии пациента, клинических доказательств положительного соотношения польза: риск и т. Д. на.
Это неизлечимо, но многие пациенты проходят длительные периоды контроля над болезнью.Качество жизни является основной целью, помимо излечения, и максимальное увеличение периодов ремиссии или стабильного заболевания при минимизации лечения и токсичности — две центральные задачи в клинической помощи. Alibert JLM (1806) (на французском языке). Ван Х., Йосипович Г. (январь 2010 г.). «Новые взгляды на патофизиологию и лечение хронического зуда у пациентов с терминальной стадией почечной недостаточности, хронической болезни печени и лимфомы». Int J Dermatol. 49 (1): 1–11. DOI: 10.1111 / j.1365-4632.2009.04249.x. PMC 2871329. PMID 20465602. http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pmcentrez&artid=2871329. (первоисточник)
Дополнительная литература
- Ноулз Дэниел М. (2000). Неопластическая гематопатология . Липпинкотт Уильямс Уилкинс. п. 1957. ISBN 0683302469.
- Hwang ST, Janik JE, Jaffe ES, Wilson WH (15 марта 2008 г.). «Грибовидный микоз и синдром Сезари». Ланцет 371 (9616): 945–57. DOI: 10.1016 / S0140-6736 (08) 60420-1. PMID 18342689.
- Duvic M, Foss FM (декабрь 2007 г.). «Грибовидный микоз: патофизиология и новые методы лечения». Semin Oncol 34 (6 Приложение 5): S21–8. DOI: 10.1053 / j.Seminoncol.2007.11.006. PMID 18086343.
- Olsen E, Vonderheid E, Pimpinelli N, Willemze R, Kim Y, Knobler R, Zackheim H, Duvic M, Estrach T, Lamberg S, Wood G, Dummer R, Ranki A, Burg G, Heald P, Pittelkow M, Bernengo М.Г., Стерри В., Ларош Л., Траутингер Ф., Уиттакер С. ISCL / EORTC (15 сентября 2007 г.). «Изменения в постановке и классификации грибовидного микоза и синдрома Сезари: предложение Международного общества кожных лимфом (ISCL) и целевой группы по кожным лимфомам Европейской организации исследования и лечения рака (EORTC)». Кровь 110 (6): 1713–22. DOI: 10.1182 / кровь-2007-03-055749. PMID 17540844.
Внешние ссылки
| ||||||||||||||||
Frontiers | Противогрибковая терапия системного микоза и эра нанобиотехнологий: повышение эффективности, биораспределения и токсичности
Введение
Грибковые заболевания возникли как важная проблема общественного здравоохранения во всем мире, оказав огромное влияние на заболеваемость и смертность людей, особенно среди лиц с ослабленным иммунитетом (Denning and Hope, 2010; Shapiro et al., 2011; Кэффри и Обар, 2016; Prasad et al., 2016). Хотя поверхностные микозы являются наиболее распространенными среди грибковых инфекций, поражающими почти 25% населения мира (Havlickova et al., 2008), инвазивные грибковые инфекции вызывают большее беспокойство, поскольку они опасны для жизни, их трудно диагностировать и учитывать. ограниченное количество терапевтических возможностей (Brown et al., 2012a, b). По оценкам, системные микозы вызывают около 1,5 миллиона смертей ежегодно (Brown et al., 2012a; Caffrey and Obar, 2016).
Системные грибковые инфекции включают как условно-патогенные, так и эндемические микозы, и связаны с высокими показателями смертности, если их нелегко диагностировать и лечить (Brown et al., 2012a; Caffrey and Obar, 2016). Оппортунистические инфекции вызываются экологическими или комменсальными грибами и поражают хозяев с ослабленным иммунитетом или генетически предрасположенных, что составляет около 2 миллионов зарегистрированных случаев опасных для жизни случаев ежегодно во всем мире (Brown et al., 2012a; Polvi et al., 2015; Caffrey and Obar, 2016 ).Виды из родов Aspergillus, Candida, Cryptococcus и Pneumocystis несут ответственность за более 90% всех зарегистрированных смертей, связанных с грибками, хотя точные данные о заболеваемости официально не доступны и могут быть недооценены (Brown et al., 2012a, б).
С другой стороны, эндемические микозы вызываются термодиморфными грибами и могут поражать особенно иммунокомпетентных хозяев, которые живут в определенных географических регионах, хотя иммуносупрессия является фактором риска и способствует исходу инфекции (Goughenour and Rappleye, 2017).Диморфные грибы встречаются в окружающей среде как сапрофитные формы. После ингаляции или травматической инокуляции млекопитающим-хозяином они трансформируются в патогенные дрожжи или сферулы (Bonifaz et al., 2011; Sil and Andrianopoulos, 2015). Среди возбудителей эндемического микоза — Histoplasma capsulatum, Coccidioides immitis и C. posadasii, Paracoccidioides brasiliensis , а также P. lutzii, Blastomyces dermatitidis, Talaromyces x18orneffei и .Несмотря на то, что данные о заболеваемости инфекциями диморфными грибами обычно неточны из-за недостаточной диагностики и неполной отчетности, считается, что эндемические микозы являются причиной примерно 65000 опасных для жизни случаев ежегодно во всем мире (Brown et al., 2012a; Goughenour and Rappleye , 2017).
Тот факт, что грибы и животные эволюционно близки, делает поиск терапевтических мишеней большой проблемой, поскольку такие мишени, как синтез биомолекул, обладают большим потенциалом токсичности (Groll et al., 1998; Деннинг и Хоуп, 2010; Хейтман, 2011; Шапиро и др., 2011; Polvi et al., 2015). На сегодняшний день только десяток противогрибковых средств (таблица 1) одобрен для лечения инвазивных грибковых инфекций (Seyedmousavi et al., 2017). Противогрибковая терапия системного микоза в основном состоит из трех классов: полиенов, азолов и эхинокандинов (Polvi et al., 2015). Терапия инвазивной инфекции имеет ограничения, такие как способ введения, токсичность, лекарственные взаимодействия, а иногда и высокие затраты, учитывая госпитализацию пациентов (Denning and Hope, 2010; Brown et al., 2012b; Polvi et al., 2015). В некоторых случаях требуется более продолжительное время лечения, а также клинические вмешательства из-за побочных эффектов (Goughenour and Rappleye, 2017). В последнее время вызывает беспокойство лекарственная устойчивость (Xie et al., 2014). К сожалению, разработка противогрибковых препаратов не сопровождается прогрессирующим ростом инвазивных инфекций в результате современных медицинских вмешательств, первичных и приобретенных иммунодефицитов и иммуносупрессивных методов лечения. Кроме того, на данный момент нет одобренных человеческих вакцин против грибковых заболеваний (Brown et al., 2012б). Чтобы преодолеть эти проблемы, интересно разработать более дешевые и новые терапевтические стратегии в борьбе с грибковыми заболеваниями.
Таблица 1. Противогрибковые препараты, применяемые в настоящее время для терапии системных микозов .
В этом обзоре мы обсудим современные противогрибковые методы лечения системных инфекций и укажем на некоторые стратегии с использованием нанобиотехнологий для улучшения традиционной терапии. Мы дадим краткое введение о наноформах и дадим обзор текущих исследований, предлагающих наноструктурирование как подход к повышению эффективности и биодоступности обычных противогрибковых препаратов.
Традиционная терапия инвазивных грибковых заболеваний
В конце 1950-х годов полиены стали первым классом противогрибковых агентов. Эти молекулы продуцируются Streptomyces nodosus , обладающим высоким сродством к эргостерину, главному стеролу клеточной мембраны грибов, который отвечает за текучесть, асимметрию и целостность мембран (Odds et al., 2003; Carrillo-Muñoz et al., 2006). ; Mesa-Arango et al., 2012). Связываясь с эргостеролом, молекулы полиена образуют поры, которые дестабилизируют клеточную мембрану, делая возможным утечку клеточного содержимого и приводя к гибели грибковых клеток (Finkelstein and Holz, 1973; Georgopapadakou, 1998; Mesa-Arango et al., 2012; Адлер-Мур и др., 2016). Кроме того, индукция окислительного повреждения в грибковой клетке также способствует фунгицидной активности (Georgopapadakou, 1998; Mesa-Arango et al., 2012). К сожалению, полиеновые агенты также могут взаимодействовать с холестерином, что придает потенциальную токсичность для клеток млекопитающих (Hsuchen and Feingold, 1973; Georgopapadakou, 1998; Mesa-Arango et al., 2012). Среди полиенов амфотерицин B наиболее широко используется для лечения системных грибковых инфекций. Амфотерицин B обладает фунгицидным действием против широкого спектра грибковых патогенов и одобрен для лечения многих инвазивных микозов, таких как кандидоз, аспергиллез, криптококкоз, бластомикоз, гистоплазмоз, мукормикоз и споротрихоз (Georgopapadakou, 1998; et al., 1998; ., 2012; Адлер-Мур и др., 2016; Нетт и Андес, 2016).
Амфотерицин B был впервые представлен на рынке в 1958 году в виде раствора дезоксихолата натрия, вводимого парентерально (Bartner et al., 1958; Groll et al., 1998), и спустя почти 60 лет он по-прежнему считается золотым стандартом для лечение наиболее опасных для жизни микозов (Groll et al., 1998; Carrillo-Muñoz et al., 2006; Mesa-Arango et al., 2012). Однако этот состав связан с важными острыми и хроническими побочными эффектами, в частности нефротоксичностью (Carrillo-Muñoz et al., 2006; Ланиадо-Лаборин и Кабралес-Варгас, 2009 г .; Меса-Аранго и др., 2012; Нетт и Андес, 2016). Амфотерицин B обладает способностью стимулировать провоспалительные реакции, усиливая противогрибковую активность, хотя это также может быть связано с токсичностью (Mesa-Arango et al., 2012). Чтобы избежать проблем токсичности, были разработаны липидные составы, включая липосомы (Ambisome ® ), липидные комплексы (Abelcet ® ) и коллоидные дисперсии (Amphocil ® / Amphotech ® ) (Georgopapadakou, 1998; Géorgopapadakou, 1998; и другие., 1998; Дюпон, 2002; Меса-Аранго и др., 2012; Нетт и Андес, 2016). Однако эти альтернативы могут быть до 20 раз дороже, чем дезоксихолат натрия Амфотерицин B (Georgopapadakou, 1998; Wong-Beringer et al., 1998; Dismukes, 2000; Falci et al., 2011), что ограничивает их использование в общественном здравоохранении. системы с ограниченными ресурсами.
В конце 1960-х годов флуцитозин (5-фторцитозин), синтетический аналог пиримидина, первоначально разработанный для противоопухолевой терапии, был впервые использован для лечения инвазивного микоза (Tassel and Madoff, 1968).После импортирования в грибковую клетку цитозиновыми пермеазами 5-фторцитозин превращается в фторурацил, который встраивается в молекулы ДНК и РНК во время их синтеза, подавляя синтез белка и репликацию ДНК, тем самым нарушая функцию клетки (Groll et al., 1998; Нетт и Андес, 2016; Прасад и др., 2016). Эти агенты обладают активностью против ограниченного спектра патогенных дрожжей, таких как C. albicans , C. glabrata, C. parapsilosis, C. tropicalis и Cryptococcus spp., и малоэффективны против диморфных или нитчатых грибов (Nett and Andes, 2016; Prasad et al., 2016). Из-за быстрого возникновения резистентности во время терапии флуцитозином, особенно среди видов Candida , его клиническое использование предпочтительнее только в сочетании с другими противогрибковыми препаратами, такими как амфотерицин B, при лечении криптококкового менингита и других опасных для жизни Candida инфекции (Tassel, Madoff, 1968; Francis and Walsh, 1992; Dismukes, 2000; Sanglard et al., 2009; Нетт и Андес, 2016; Prasad et al., 2016). Кроме того, флуцитозин вызывает значительные побочные эффекты, такие как дисфункция печени и подавление костного мозга (Francis and Walsh, 1992; Groll et al., 1998; Dismukes, 2000; Nett and Andes, 2016; Prasad et al., 2016). В Соединенных Штатах флуцитозин доступен в пероральных капсулах (Groll et al., 1998; Nett and Andes, 2016).
Азолы — это синтетические циклические органические молекулы, представленные в начале 1970-х годов в дополнение к противогрибковому арсеналу. Они состоят из 5-членного азольного кольца, которое содержит два (имидазолы) или три (триазолы) атома азота, присоединенные к сложной боковой цепи (Georgopapadakou, 1998; Groll et al., 2003). Мишенью азолов является биосинтез эргостерина, который нарушается из-за ингибирования 14-α стеролдеметилазы цитохрома P-450 грибов (Vanden Bossche et al., 1995; Georgopapadakou, 1998; Groll et al., 1998, 2003; Odds et al., 2003; Каррильо-Муньос и др., 2006). Как следствие, целостность клеточной мембраны нарушается с накоплением предшественников стеролов внутри грибковой клетки и истощением эргостерола в клеточной мембране, изменяя нормальную проницаемость и текучесть (Georgopapadakou, 1998; Groll et al., 1998; Odds et al., 2003). В целом азолы обладают фунгистатическим действием, влияя на рост и пролиферацию клеток, и в конечном итоге из-за накопления токсичных метилированных стеролов может произойти гибель грибковых клеток (Groll et al., 2003; Zonios and Bennett, 2008; Sanglard et al., 2009; Арнольд и др., 2010; Шапиро и др., 2011; Прасад и др., 2016). В настоящее время азолы представляют собой самый разнообразный класс противогрибковых агентов, и в течение последних 40 лет они совершенствовались (Odds et al., 2003). Первыми появились имидазолы (Groll et al., 1998; Prasad et al., 2016), и среди них миконазол и кетоконазол были единственными доступными для системного использования (Groll et al., 2003), причем последний был первым перорально всасываемым противогрибковым средством и первой альтернативой амфотерицину B (Groll et al., 2003). др., 1998; Сейедмусави и др., 2017). Затем последовали триазолы, итраконазол в пероральных формах и флуконазол в пероральных и внутривенных формах. составы, которые лучше переносятся и более эффективны, чем кетоконазол (Dismukes, 2000), с повышенной эффективностью, расширенным противогрибковым спектром и повышенной устойчивостью к метаболической деградации (Como and Dismukes, 1994; Groll et al., 1998). Флуконазол обладает хорошей активностью против Cryptococcus spp., Coccidioides spp. И Candida spp. за исключением C. krusei и C. glabrata (Arnold et al., 2010; Denning and Hope, 2010; Nett and Andes, 2016; Seyedmousavi et al., 2017). Итраконазол обладает более широким противогрибковым спектром и эффективен против Candida spp., Cryptococcus neoformans, Aspergillus spp., Диморфных грибов и дерматофитов (Arnold et al., 2010; Деннинг и Хоуп, 2010; Нетт и Андес, 2016).
Дальнейшие модификации в молекулах привели к появлению второго поколения триазолов, в которых для системной терапии доступны вориконазол (структурно связанный с флуконазолом) и позаконазол (связанный с итраконазолом) с еще большей противогрибковой активностью и специфичностью. Спектр активности вориконазола улучшен по сравнению с триазолами первого поколения, включая C. glabrata, Fusarium spp., Scedosporium spp.(Арнольд и др., 2010; Деннинг и Хоуп, 2010; Нетт и Андес, 2016). Позаконазол обладает самым широким спектром противогрибковых свойств азолов, проявляя активность как против дрожжей, так и против плесени, включая несколько видов Mucorales (Arnold et al., 2010; Denning and Hope, 2010; Nett and Andes, 2016). Исавуконазол — это новейший триазол, представленный на рынке в 2015 году и недавно одобренный для лечения инвазивного аспергиллеза и мукормикоза в США и Европе (McCormack, 2015).
Хотя азольные противогрибковые препараты обычно хорошо переносятся (Odds et al., 2003; Carrillo-Muñoz et al., 2006), они являются субстратами и ингибиторами нескольких ферментов цитохрома P-450, что в основном является причиной их побочных эффектов, особенно гепатотоксичности (Carrillo-Muñoz et al., 2006). По этой причине азолы также могут нарушать метаболизм совместно вводимых препаратов, что приводит к снижению концентрации в плазме и неожиданной токсичности (Groll et al., 1998; Dismukes, 2000; Shapiro et al., 2011; Nett and Andes, 2016; Prasad et al. ., 2016). Кроме того, из-за тератогенного действия азолы при беременности противопоказаны (Arnold et al., 2010; Нетт и Андес, 2016). Наконец, появление устойчивости среди грибковых изолятов является еще одним ограничением и одной из мотиваций для улучшения этого класса противогрибковых средств (Dismukes, 2000; Shapiro et al., 2011; Prasad et al., 2016).
Эхинокандины — новейшая категория противогрибковых средств, состоящая из полусинтетических липопептидов грибов, состоящих из циклического гексапептида и боковой цепи переменного липида, ответственной за их противогрибковую активность (Groll et al., 2003; Odds et al., 2003). Хотя они были обнаружены в 1970-х годах, только 30 лет спустя их использование было одобрено Управлением по контролю за продуктами и лекарствами США. Эхинокандины подавляют синтез 1,3-β-глюкана, структурного полисахарида клеточной стенки грибов, который отвечает за форму и жесткость клеточной стенки, осмотическую целостность и играет важную роль в делении и росте клеток (Georgopapadakou, 2001; Groll et al., 2003; Odds et al., 2003). Эхинокандины включают каспофунгин, анидулафунгин и микафунгин, все они доступны только для i.v. администрация (Groll et al., 2003; Odds et al., 2003). Их действие зависит от вида и действует как фунгицидное средство против Candida spp. и фунгистатическое против Aspergillus spp. (Nett and Andes, 2016), с переменной активностью против дематиозных и эндемичных форм плесени (Seyedmousavi et al., 2017). Однако эхинокандины не проявляют активности против Scedosporium spp., Fusarium spp. И C. neoformans (Groll et al., 2003; Odds et al., 2003; Arnold et al., 2010; Нетт и Андес, 2016). Поскольку эхинокандины нацелены на β-глюкан, которого нет в клетке млекопитающих, они проявляют минимальные побочные эффекты у людей (Groll et al., 2003; Sanglard et al., 2009; Arnold et al., 2010; Shapiro et al., 2011; Prasad et al., 2016), которые могут включать желудочно-кишечные расстройства, головную боль и повышение аминотрансфераз печени. Сообщалось о нескольких лекарственных взаимодействиях, поскольку эхинокандины не метаболизируются с помощью ферментов цитохрома P-450 (Arnold et al., 2010; Nett and Andes, 2016).
Как указано выше, хотя противогрибковый арсенал, доступный в настоящее время для лечения системных микозов, эффективен против большинства грибковых патогенов, они имеют ограничения, такие как токсичность, лекарственные взаимодействия и появление клинической устойчивости. Чтобы преодолеть эти проблемы, используются такие стратегии, как комбинированная терапия (Mukherjee et al., 2005) и даже перепрофилирование признанных лекарств (Butts and Krysan, 2012). Чрезвычайно необходимы поиск новых соединений и новых целей вместе с улучшением существующих составов.Наноструктурирование обычных противогрибковых средств может быть интересной альтернативой для достижения лучшей противогрибковой эффективности и безопасности (рис. 1).
Рисунок 1. Преимущества нанобиотехнологических подходов для доставки противогрибковых препаратов .
Нанобиотехнологические подходы к доставке противогрибковых средств
Системы доставки лекарств, содержащие наночастицы, были объектом интенсивных исследований в течение последних десятилетий, став эффективной стратегией повышения биодоступности лекарств, снижения токсичности и усиления противогрибковой активности (Vyas and Gupta, 2006; Amaral and Felipe, 2013; de Sá et al., 2015; Stiufiuc et al., 2015). Среди преимуществ этого подхода — возможность создания составов для интеллектуальной доставки, например, нацеленных на определенные ткани и органы, такие как легкие, которые часто являются первоначальным очагом инфекции во время системных грибковых заболеваний (Amaral et al., 2009; Малати и Баласубраманиан, 2011; Мориц, Гешке-Мориц, 2015). В некоторых случаях при внутриклеточных инфекциях наночастицы могут проникать в клетки, заставляя лекарство действовать непосредственно против патогена (Borborema et al., 2011; Dube et al., 2014). С другой стороны, когда они покрыты такими веществами, как полиэтиленгликоль (ПЭГ), они могут ускользать от распознавания фагоцитарной системой, предотвращая прикрепление опсонинов и способствуя более длительному времени циркуляции (Stiufiuc et al., 2015). Исследования показали, что наночастицы также обладают желательными характеристиками для использования в качестве адъювантов в вакцинах (Van Slooten et al., 2001; Agger et al., 2008; Bhowmick et al., 2008; Ribeiro et al., 2013). В настоящее время исследуются многие типы наноструктур для доставки противогрибковых препаратов, такие как полимерные наночастицы, твердые липидные наночастицы, липосомы и магнитные наночастицы (рис. 2).
Рис. 2. Схематическое изображение различных типов наночастиц, используемых для доставки противогрибковых агентов .
Полимерные наночастицы получают из различных природных или синтетических полимеров, как гидрофильных, так и гидрофобных (Pagels and Prud’homme, 2015). Эти полимеры могут быть природного происхождения, например хитозан и альгинат, или синтетических материалов, таких как поли (молочная кислота, PLA) и поли (гликолевая кислота, PGA), или их комбинация, образующая поли (лактид- со -гликолидом). кислота, PLGA) (Bolhassani et al., 2014). При применении in vivo полимерные наночастицы подвергаются биодеградации, метаболизируются и выводятся организмом, что обеспечивает лучшую биосовместимость (Amaral and Felipe, 2013). По мере разложения полимера включенное в него лекарство высвобождается в среду и может эффективно достигать места действия.
Липосомы — это частицы, состоящие из природных или синтетических фосфолипидов. Из-за природы этих молекул при контакте с водной средой они образуют сферические структуры, содержащие водное ядро, окруженное липидным бислоем (Bozzuto and Molinari, 2015), которые могут быть подходящими для доставки как гидрофильных, так и гидрофобных веществ ( Stiufiuc et al., 2015). Из-за их чувствительности к изменениям pH можно регулировать проницаемость липосом, высвобождая лекарство в определенные места, такие как компартменты макрофагов с измененным pH во время инфекции (Wang et al., 2014; Jiang et al., 2015). Успешным примером этого класса наночастиц является коммерчески доступный липосомальный амфотерицин B, торговая марка Ambisome ® (Reis, 2015). Кроме того, твердые липидные наночастицы интенсивно исследуются, особенно для местной доставки лекарств (Kumar and Sinha, 2016; Trombino et al., 2016). Они представляют собой сферические наночастицы, состоящие из физиологических и биоразлагаемых липидов, таких как стеариновая кислота. Благодаря химическому составу твердые липидные наночастицы позволяют наноструктурировать нерастворимые лекарства и обладают низкой токсичностью.
Магнитные наночастицы привлекли особое внимание для биологических применений, в основном из-за их способности манипулировать магнитным полем, так что оно может быть направлено и доставлено, теоретически, в конкретный участок организма (Hussein et al., 2014). Этот тип наночастиц может быть получен различными химическими и физическими методами с использованием соединений железа, таких как ферриты кобальта, марганца и цинка, магнетит и маггемит. В области медицины эти магнитные наночастицы в основном используются для клинической диагностики с помощью магнитно-резонансной томографии (МРТ). Этот тип наночастиц также может быть связан с другими наноструктурами, такими как полимерные наночастицы или липосомы, чтобы сочетать характеристики как для МРТ, так и для доставки лекарств (Jain et al., 2008). Суперпарамагнитные наночастицы оксида железа, особый вид магнитных наночастиц, более эффективно реагируют на внешнее магнитное поле (Kumar et al., 2010), представляя большой потенциал для использования в качестве носителей лекарств.
Существует более 100 публикаций, в которых предлагаются новые наноформулы противогрибковых препаратов (Таблица 2). В этом обзоре мы суммируем основные результаты для наночастиц, которые доказали противогрибковую активность in vivo, и / или in vitro, .
Таблица 2. Примеры исследований, сообщающих о противогрибковых наночастицах с in vivo и / или in vitro активностью .
Нанопрепараты для полиенов
Среди противогрибковых препаратов исследования, связанные с наноструктурированными системами доставки полиенов, являются наиболее известными, большинство из них касается доставки амфотерицина B. Это неудивительно, поскольку амфотерицин B по-прежнему является золотым стандартом противогрибковой терапии тяжелых системных микозов и препаратом с наиболее сильным противогрибковым действием (Arnold et al., 2010). Наночастицы амфотерицина B исследуются с 1980-х годов, что дает возможность избежать побочных эффектов, связанных с инфузией, и нефротоксичности, которые являются основными ограничивающими факторами при терапии этим препаратом. Кроме того, из-за плохой растворимости и пероральной биодоступности амфотерицина B (Kang et al., 2010) такие составы также предназначены для улучшения этих характеристик, что делает его пригодным для пероральной доставки.
В настоящее время коммерчески доступны липидные препараты амфотерицина B (Walsh et al., 1999; Клейнберг, 2006). Наиболее успешным является Ambisome ® , который считается действительно липосомальным препаратом, в котором амфотерицин B встроен в однослойный липосомный бислой размером около 45–80 нм (Adler-Moore, 1994). Одним из преимуществ этой рецептуры является то, что она вызывает меньшую токсичность и остается на высоких пиках в кровотоке, имея высокое биораспределение. Исследование с использованием мышиной модели легочного аспергиллеза показало, что Ambisome ® способен увеличивать выживаемость животных без токсичности, позволяя вводить в 10 раз более высокую дозу, чем у животных, получавших обычную композицию с дезоксихолатом натрия (Takemoto, 2006 ).Также изучались липосомальные препараты для местного применения (Kang et al., 2010; Perez et al., 2016). Некоторые из этих препаратов предназначены для увеличения стойкости состава в месте действия, высвобождая лекарство в течение более длительного времени. К сожалению, наряду с более высокой биобезопасностью сообщалось, что противогрибковая эффективность липидных составов амфотерицина B может быть снижена по сравнению с таковой у свободных лекарств (Andes et al., 2006; Burgess et al., 2013). Кроме того, высокая стоимость является одним из ограничений их широкого использования (Dismukes, 2000; Falci et al., 2011; Italia et al., 2011; Van de Ven et al., 2012), поощряя поиск новых вариантов доставки амфотерицина B.
Чтобы снизить затраты на производство, был разработан наносомальный амфотерицин B с использованием фосфатидилхолина и холестерилсульфата натрия в качестве вспомогательных веществ, избегая использования органических растворителей или детергентов в препарате (Sheikh et al., 2010). Наносомальный амфотерицин B индуцировал меньший лизис красных кровяных телец, чем амфотерицин B натрия дезоксихолат, и был сопоставим с амбисомом ® .Никаких симптомов токсичности, смертности или значительного снижения массы тела не наблюдалось у кроликов, ежедневно получавших этот состав в течение 28 дней, без гематологических и грубых патологических отклонений. Кроме того, у мышей с диссеминированной инфекцией A. fumigatus внутривенное введение наносомального амфотерицина B привело к 90% выживаемости, в то время как выживаемость только 30% с Ambisome ® .
Анионные и липидные наночастицы ПЭГ были разработаны Jung et al. (2009) для внутривенной доставки амфотерицина B (Jung et al., 2009). Этот состав проявлял более низкую цитотоксичность в отношении клеток почек человека, чем фунгизон ® и амбисом ® , и гораздо более низкую гематотоксичность, чем у фунгизона ® . Противогрибковая активность in vitro липидных наночастиц амфотерицина B против C. albicans и A. fumigatus была лучше, чем коммерческие препараты, а введение in vivo для лечения мышиной системной аспергилломы было более эффективным, чем введение амбисомы ® .
Burgess et al. (2013) разработали состав, состоящий из белково-фосфолипидной биочастицы (NanoDisk), содержащей «суперагрегатную» форму амфотерицина B (ND-AMB) (Burgess et al., 2013). ND-AMB представлял более низкие минимальные ингибирующие концентрации C. albicans и A. fumigatus , чем наблюдаемые для Ambisome ® . Он также не вызывал токсичности почек или печени у мышей. Кроме того, у C. albicans инфицированных иммунокомпетентных мышей лечение ND-AMB было таким же эффективным, как дезоксихолат натрия амфотерицин B или амбисом ® , тогда как в лейкопенической модели кандидоза 50% эффективная доза ND-AMB была примерно в три раза ниже, чем у Ambisome ® .
В дополнение к липидным рецептурам, полимерные системы для доставки амфотерицина B были разработаны несколькими исследовательскими группами (таблица 2). Результаты доказали, что этот тип препарата является удовлетворительным для эффективной доставки этого лекарственного средства несколькими путями, например внутривенно (Amaral et al., 2009; Tang et al., 2014; Souza et al., 2015) и перорально (Italia и др., 2009, 2011, 2012). Биологический ответ может варьироваться в зависимости от типа используемого полимера или даже при сочетании различных типов полимеров.Примером является рецептура, разработанная Tang et al. (2014), в которых АМВ был инкапсулирован в PLGA вместе с ε-капролактоном. В этой комбинации авторы сообщили об эффективности инкапсуляции АМВ в 84% и таком же фунгицидном действии на C. albicans , как и на бесплатное лекарственное средство (Tang et al., 2014). Предложенный состав был менее токсичным и вызывал более низкую смертность, чем свободный AMB, доказывая, как отмечалось ранее, потенциал полимерных наночастиц для защиты от цитотоксичности, но сохраняя ту же фунгицидную эффективность (Amaral et al., 2009).
Amaral et al. (2009) разработали наноструктурированный состав амфотерицина B в составе PLGA, функционализированного димеркаптоянтарной кислотой (DMSA). Эта кислота проявляет тропизм к легким и подходит для включения в составы для доставки лекарств в этот орган (Amaral et al., 2009, 2010). В этом исследовании авторы отметили, что внутрибрюшинное введение препарата могло вызвать такой же терапевтический эффект на мышиной модели паракокцидиоидомикоза по сравнению с дезоксихолатом натрия амфотерицином B.Однако большим преимуществом этого полимерного препарата было то, что его давали животным каждые 3 дня, учитывая медленное высвобождение амфотерицина В из наночастиц, в отличие от обычного препарата, который вводили ежедневно. Дополнительные исследования, проведенные той же исследовательской группой, показали, что наночастицы PLGA амфотерицина B также сопоставимы с амбисомом ® в терапии паракокцидиоидомикоза мышей (Souza et al., 2015). Кроме того, в обоих исследованиях не сообщалось о нежелательных побочных эффектах у животных при использованной дозе.Высокие концентрации амфотерицина B были обнаружены в легких, печени и селезенке животных, получавших этот полимерный состав (Souza et al., 2015).
Van de Ven et al. (2012) показали, что как наночастицы амфотерицина B PLGA, так и наноэмульсия обладают in vitro противогрибковыми свойствами против C. albicans, A. fumigatus и Trichophyton rubrum и были менее гемолитическими, чем дезоксихолат натрия Амфотерицин B (Van de Venus et al. ., 2012). Кроме того, оба препарата были эффективны против диссеминированного аспергиллеза у мышей после внутрибрюшинного введения с аналогичной или даже лучшей противогрибковой способностью, чем у фунгизона ® и амбисома ® в эквивалентных дозах.Italia et al. (2011) предложили наночастицы амфотерицина B PLGA для пероральной доставки, которые значительно снизили грибковую нагрузку при инвазивном легочном и диссеминированном аспергиллезе (Italia et al., 2011).
В очень интересном подходе Tang et al. (2015a) разработали специализированные pH-чувствительные наночастицы PLGA амфотерицина B, конъюгированные с поли (L-гистидином) и PEG, которые обладали высоким сродством к элементам клеточной стенки грибов в кислых условиях и были дополнительно модифицированы для повышения эффективности воздействия с помощью анти- C.albicans (Tang et al., 2015a). Композиция имела пониженную гемолитическую активность и цитотоксичность в отношении эпителиальных клеток почечных канальцев человека и была эффективна против C. albicans , in vivo и in vitro после внутривенного введения. Нагруженные нистатином наночастицы PLGA, функционализированные глюкозамином, были составлены Mohammadi et al. (2017) для усиления адгезии наночастиц к клеточным стенкам C. albicans (Mohammadi et al., 2017). Наночастицы проявляли более высокую противогрибковую активность, чем свободный нистатин, что свидетельствует об увеличении уровней нистатина в мембране грибковых клеток за счет захвата полимерной матрицы.
Хитозан — это природный полисахарид с катионной природой и мукоадгезивными свойствами, который часто используется для создания биоразлагаемых полимерных наночастиц для доставки лекарств. Наночастицы хитозана амфотерицина B были разработаны Serrano et al. (2015), намереваясь избежать деградации лекарственного средства в желудочно-кишечном тракте, повысить стабильность и повысить биодоступность в органах-мишенях, таких как легкие, печень и селезенка, при одновременном уменьшении воздействия на почки (Serrano et al., 2015). Они продемонстрировали, что пероральное введение этих наночастиц было эффективным при лечении мышиных моделей висцерального лейшманиоза, кандидоза и аспергиллеза, имея сопоставимую эффективность с парентеральным амбисомом ® . Наночастицы хитозана использовали Sanchez et al. (2014) для местного введения амфотерицина B в ожоговые раны, инфицированные C. albicans , с улучшенным заживлением тканей и даже лучшей противогрибковой активностью, чем состав дезоксихолата натрия (Sanchez et al., 2014). Наночастицы, нагруженные амфотерицином B, сделанные из лецитина и хитозана, были предложены Chhonker et al. (2015) для длительного применения в глаза, например, при грибковом кератите (Chhonker et al., 2015). Состав продемонстрировал противогрибковую эффективность in vitro против C. albicans и A. fumigatus , выраженные мукоадгезивные свойства и улучшенную биодоступность по сравнению с фунгизоном ® .
Подходы к увеличению доставки амфотерицина B в центральную нервную систему (ЦНС) также изучаются.Наночастицы полибутилцианоакрилата амфотерицина B, модифицированные полисорбатом 80, использовали в качестве терапии для модели криптококкового менингита на мышах (Xu et al., 2011). Наночастицы были обнаружены в головном мозге через 30 мин после системного введения мышам с более высокой концентрацией, чем липосомы амфотерицина B. Выживаемость мышей, получавших наночастицы, была значительно выше, чем у мышей, получавших дезоксихолат натрия и липосомальный амфотерицин B, с меньшей грибковой нагрузкой на ткань мозга.Другой препарат, основанный на трансцитозе трансферрина через гематоэнцефалический барьер, был предложен Tang et al. (2015c). В этом исследовании были разработаны модифицированные амфотерицином B наночастицы PLA-PEG, модифицированные антителами к рецептору трансферрина, которые продемонстрировали значительное снижение грибковой нагрузки на ЦНС и увеличили время выживания мышей при внутривенном введении для лечения менингита, вызванного инокуляцией C. glabrata (Tang et al., 2015c).
Ширхани и др. (2015) разработали наночастицы полиметакриловой кислоты амфотерицина B для профилактики A.fumigatus на мышиной модели трансплантата с иммуносупрессией с инвазивным аспергиллезом. Композиция вводилась путем распыления и предотвращала рост грибков и воспаление легких (Shirkhani et al., 2015).
Магнитные наночастицы амфотерицина B были опубликованы Saldanha et al. (2016). В этом исследовании авторы разработали нагруженные амфотерицином B наночастицы магнетита, предварительно покрытые лауриновой кислотой, и продемонстрировали противогрибковую активность нанокомплекса как in vivo , так и n vitro против P.brasiliensis (Saldanha et al., 2016). Нанокомплекс был более цитотоксичным для грибковых клеток, чем для клеток мочи человека и перитонеальных макрофагов мыши in vitro , в то время как никаких биохимических и гистопатологических изменений не наблюдалось во время интраназальной терапии паракокцидиоидомикоза мышей. Препарат проявлял противогрибковую активность, аналогичную активности дезоксихолата натрия амфотерицина В, вводимого внутрибрюшинно, с преимуществом, позволяющим в три раза сократить количество применений и подходящим для назальной доставки.Другая магнитно-липосомная система амфотерицина B была предложена Zhao et al. (2014) с целью повышения селективности лекарств к ЦНС во время грибковых инфекций. Липосомная система вводилась через сонную артерию крысам SD и могла улучшать концентрацию лекарства и усиливать магнитное нацеливание на ткань мозга в присутствии магнитного поля. Магнитные наночастицы амфотерицина B и нистатина были также разработаны Niemirowicz et al. (2016). Обе наносистемы проявляли более сильную фунгицидную активность, чем несвязанные препараты, в отношении Candida spp.(Niemirowicz et al., 2016). При тестировании против штаммов Candida наносистемы были более эффективными, чем свободные агенты, и были способны предотвращать образование биопленок Candida более эффективно при более низкой гемолитической способности.
Некоторые грибковые патогены обладают способностью находиться внутри клеток-хозяев, таких как макрофаги. Следовательно, поглощение наночастиц клетками-хозяевами очень желательно в качестве стратегии повышения противогрибковой способности против внутриклеточных грибов. Zia et al. (2015) показали, что уничтожение внутриклеточного C.albicans после обработки наночастицами полиглутаминовой кислоты амфотерицина B была выше, чем при применении Ambisome ® (Zia et al., 2015). Амфотерицин B также используется для лечения инфекций, вызванных Leishmania spp., Которые являются внутриклеточными паразитами, поэтому были проведены интенсивные исследования с целью усиления противопаразитарных эффектов лекарств на протяжении всей нанострутурации (Asthana et al., 2015; Jain et al. др., 2015; Bose et al., 2016).
Нанопрепараты азолов
Повышение пероральной биодоступности азолов — одно из преимуществ, предоставляемых применением нанотехнологий для этого класса лекарств.Интересно отметить, что хотя приготовление состава в наномасштабе может предложить аналогичные результаты при использовании одного и того же типа наночастиц и материала, это не всегда верно. Например, исследование инкапсулирования эконазола и клотримазола как в PLGA, так и в альгинат (Pandey et al., 2005) показало, что последний, по-видимому, лучше улучшает фармакокинетические параметры. Хотя оба оказались эффективными при пероральном приеме.
Принимая во внимание серьезность некоторых грибковых инфекций, поражающих легкие, проводится поиск наноструктурированных систем доставки лекарств, способных достичь этого органа.Некоторые исследования показали тропизм для легких наночастиц PLGA. Инкапсулированный в PLGA вориконазол показал более высокое накопление в легких по сравнению со свободным вориконазолом (Das et al., 2015). Эта характеристика также наблюдалась другими исследователями, когда они также инкапсулировали вориконазол в PLGA для назального введения. Исследование продемонстрировало, что система позволяет быстро высвобождать лекарство в легких в первые 2 часа с последующим замедленным высвобождением в течение 15 дней (Sinha et al., 2013).Наночастицы итраконазола PLGA, конъюгированные с димеркаптоянтарной кислотой, были разработаны для доставки в легкие и индуцировали противогрибковое ингибирование против P. brasiliensis с более низкой цитотоксичностью in vitro , чем свободное лекарственное средство (Cunha-Azevedo et al., 2011).
Нагруженные вориконазолом наночастицы PLGA были разработаны Peng et al. (2008), чтобы улучшить биодоступность и стабильность лекарственного средства для пероральной доставки (Peng et al., 2008). Наночастицы обладали более стойким и сильным противогрибковым действием, чем свободный вориконазол, как in vitro , так и in vivo на мышиной модели системного кандидоза.
Были исследованы другие нагруженные триазолом полимерные наноструктурные препараты, которые продемонстрировали in vitro, противогрибковых активностей против A. flavus (Patel et al., 2010, 2011), A. fumigatus (Essa et al., 2012) и C. albicans (Qiu et al., 2015). Некоторые полимеры, например хитозан, обладают мукоадгезивными свойствами, и могут использоваться для приготовления систем доставки лекарств для слизистой оболочки глаз, рта и влагалища. Rençber et al. (2016) разработали буккальную мукоадгезивную наночастицу, содержащую флуконазол и EUDRAGIT ® , небиоразлагаемый и катионный сополимер, для местного лечения кандидоза полости рта.Состав проявлял противогрибковую активность in vitro против C. albicans в течение продолжительного периода времени, и не наблюдалось цитотоксического действия на клетки яичников китайского хомячка. Кроликов с кандидозом полости рта успешно лечили с помощью местного введения наночастиц один раз в день (Rençber et al., 2016). Могут быть приготовлены более сложные системы доставки лекарств, образованные разными типами наночастиц (Jøraholmen et al., 2014). Например, в одном полимере инкапсулировано лекарство, а этот полимер покрыт другим, чтобы обеспечить надлежащее применение in vivo .
Сверхгибкие липосомы, несущие миконазол, также оказались более эффективными и способны проникать через клеточный барьер, несущий лекарство. Поскольку они способны адаптировать свою форму в соответствии с характеристиками ближайшего микросреды, они могут проникать и высвобождать лекарство более эффективно (Pandit et al., 2014). Также возможно способствовать высвобождению миконазола только в кожу, не проникая в нее и не достигая эпидермиса (Elmoslemany et al., 2012), что важно для снижения токсичности.
Твердые липидные наночастицы (SLN) интенсивно исследуются для местной доставки азольных противогрибковых средств. Jain et al. (2010) разработали рецептуру гидрогеля, содержащего SLN, содержащего нитрат миконазола, для доставки через кожу (Jain et al., 2010). Исследования показали, что гидрогель, содержащий миконазол, вызывает значительно меньшее раздражение кожи по сравнению с гидрогелем и суспензией миконазола после 24 часов применения. Кроме того, лечение микозанолом SLN кожного кандидоза у крыс-альбиносов показало большую эффективность и быстрое выздоровление.Mohanty et al. (2015) исследовали СЛУ для местного введения итраконазола в глаза (Mohanty et al., 2015). Наблюдали проникновение итраконазола в свежевырезанные роговицы коз, и SLN ингибировал рост Aspergillus flavus in vitro , что указывает на противомикробную эффективность составов.
Moazeni et al. (2016) протестировали эффективность СЛУ, нагруженных флуконазолом, в отношении устойчивых к флуконазолу Candida spp. штаммы. Устойчивые к флуконазолу C. albicans, C. parapsilosis и C.glabrata после обработки флуконазолом SLN вели себя как чувствительные штаммы, что подчеркивает многообещающие преимущества наноструктурирования для доставки противогрибковых агентов.
Заключительные замечания
Высокая частота грибковых инфекций — это проблема, которая может усугубляться, главным образом, увеличением числа пожилых людей, а также пациентов с ослабленным иммунитетом. Таким образом, важно разработать новые и более эффективные методы лечения этих микозов.Одной из стратегий, которая приобрела значение для этой цели, является разработка лекарств с применением принципов нанотехнологии. Можно использовать те же самые обычные лекарства, но с целью повышения их терапевтической эффективности, а также уменьшения побочных эффектов. Таким образом, в отличие от базовой разработки новой противогрибковой молекулы, которая также имеет важное значение, эффективность обычных составов может быть улучшена за счет ресурсов нанобиотехнологии.
Авторские взносы
Все перечисленные авторы внесли существенный, прямой и интеллектуальный вклад в работу и одобрили ее к публикации.
Финансирование
Ана Камила Оливейра Соуза финансируется за счет гранта 2015 / 10390-6 от Fundação de Amparo à Pesquisa de São Paulo (FAPESP).
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Ссылки
Аггер, Э. М., Розенкрандс, И., Хансен, Дж., Брахими, К., Вандал, Б. С., Aagaard, C., et al. (2008). Катионные липосомы, содержащие синтетический микобактериальный кордфактор (CAF01): универсальный адъювант для вакцин с различными иммунологическими требованиями. PLoS ONE 3: e3116. DOI: 10.1371 / journal.pone.0003116
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Albasarah, Y. Y., Somavarapu, S., Stapleton, P., and Taylor, K. M. (2010). Противогрибковые препараты, покрытые хитозаном, для распыления. J. Pharm. Pharmacol. 62, 821–828.DOI: 10.1211 / JPP.62.05.0002
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Амарал А. К., Бокка А. Л., Рибейро А. М., Нуньес Дж., Пейшото Д. Л., Симиони А. Р. и др. (2009). Амфотерицин B в наночастицах сополимера молочной и гликолевой кислоты (PLGA) и димеркаптоянтарной кислоты (DMSA) против паракокцидиоидомикоза. J. Antimicrob. Chemother. 63, 526–533. DOI: 10.1093 / jac / dkn539
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Амарал, А.К., и Фелипе, М. С. С. (2013). Нанобиотехнология: эффективный подход к доставке нестабильных биомолекул. Curr. Protein Pept. Sci. 14, 588–594. DOI: 10.2174/13892037112032
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Amaral, A.C., Marques, A.F., Muñoz, J.E., Bocca, A.L., Simioni, A.R., Tedesco, A.C., et al. (2010). Наночастицы поли (молочная кислота-гликолевая кислота) заметно улучшают иммунологическую защиту, обеспечиваемую пептидом P10 против паракокцидиоидомикоза мышей. Br. J. Pharmacol. 159, 1126–1132. DOI: 10.1111 / j.1476-5381.2009.00617.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Андес, Д., Сафдар, Н., Марчилло, К., и Конклин, Р. (2006). Фармакокинетико-фармакодинамическое сравнение амфотерицина B (AMB) и двух липид-ассоциированных препаратов AMB, липосомального AMB и липидного комплекса AMB, на моделях мышиного кандидоза. Антимикробный. Агенты Chemother. 50, 674–684. DOI: 10.1128 / AAC.50.2.674-684.2006
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Астхана, С., Гупта, П. К., Джайсвал, А. К., Дубе, А., и Чурасия, М. К. (2015). Подход с использованием нанокапсул-опосредованной доставки груза сверхэкспрессированного рецептора маннозы макрофагов для уничтожения резидентного паразита: in vitro, и in vivo, исследований. Pharm. Res. 32, 2663–2677. DOI: 10.1007 / s11095-015-1651-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бартнер Э., Зиннес Х., Мо Р. А. и Кулеска Дж. С. (1958). Исследования нового солюбилизированного препарата амфотерицина B. Antibiot. Анну. 5, 53–58.
PubMed Аннотация | Google Scholar
Bhowmick, S., Ravindran, R., and Ali, N. (2008). gp63 в стабильных катионных липосомах обеспечивает устойчивый иммунитет к вакцине чувствительным мышам BALB / c, инфицированным Leishmania donovani . Заражение. Иммун. 76, 1003–1015. DOI: 10.1128 / IAI.00611-07
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Болхассани, А., Джаванзад, С., Салех, Т., Хашеми, М., Агхасадеги М. Р. и Садат С. М. (2014). Полимерные наночастицы. Гум. Вакцин. Immunother. 10, 321–332. DOI: 10.4161 / hv.26796
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бонифас А., Васкес-Гонсалес Д. и Перуския-Ортис А. М. (2011). Эндемические системные микозы: кокцидиоидомикоз, гистоплазмоз, паракокцидиоидомикоз и бластомикоз. J. Dtsch. Дерматол. Ges. 9, 705–715. DOI: 10.1111 / j.1610-0387.2011.07731.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Borborema, S.E., Schwendener, R.A., Osso, J. A., de Andrade, H. F. Jr., and do Nascimento, N. (2011). Поглощение и антилейшманиозная активность липосом, содержащих меглумин-антимониат, в макрофагах, инфицированных главным образом лейшманией (Leishmania). Внутр. J. Antimicrob. Агенты 38, 341–347. DOI: 10.1016 / j.ijantimicag.2011.05.012
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бозе П. П., Кумар П. и Двиведи М. К. (2016). Управляемый гемоглобином наноноситель для специфической доставки амфотерицина B к макрофагам, инфицированным Leishmania. Acta Trop. 158, 148–159. DOI: 10.1016 / j.actatropica.2016.02.026
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Браун, Г. Д., Деннинг, Д. В., Гоу, Н. А., Левиц, С. М., Нетеа, М. Г. и Уайт, Т. К. (2012a). Скрытые убийцы: грибковые инфекции человека. Sci. Пер. Med. 4, 165rv13. DOI: 10.1126 / scitranslmed.3004404
PubMed Аннотация | CrossRef Полный текст
Берджесс, Б. Л., Хе, Ю., Бейкер, М. М., Луо, Б., Кэрролл, С.Ф., Форте Т. М. и др. (2013). NanoDisk, содержащий суперагрегированный амфотерицин B: противогрибковый препарат с высоким терапевтическим индексом и повышенной эффективностью. Внутр. J. Nanomedicine 8, 4733–4743. DOI: 10.2147 / IJN.S50113
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Каррильо-Муньос, А. Дж., Джузиано, Г., Эзкурра, П. А., и Киндос, Г. (2006). Противогрибковые средства: механизм действия на дрожжевые клетки. Rev. Esp. Кимиотер. 19, 130–139.
PubMed Аннотация | Google Scholar
Casa, D.М., Карраро, Т. К., де Камарго, Л. Е., Далмолин, Л. Ф., Халил, Н. М., и Майнардес, Р. М. (2015). Наночастицы поли (L-лактида) снижают цитотоксичность амфотерицина B и поддерживают его противогрибковую активность in vitro . J. Nanosci. Nanotechnol. 15, 848–854. DOI: 10.1166 / jnn.2015.9177
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чаудхари, М. Б., Десаи, П. П., Патель, П. А. и Патравале, В. Б. (2016). Твердые липидные наночастицы амфотерицина B (AmbiOnp): in vitro и in vivo оценка безопасного и эффективного модуля для перорального лечения. Drug Deliv. Пер. Res. 6, 354–364. DOI: 10.1007 / s13346-015-0267-6
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чхонкер, Ю. С., Прасад, Ю. Д., Чандасана, Х., Вишвкарма, А., Митра, К., Шукла, П. К. и др. (2015). Амфотерицин-В, захваченные наночастицами лецитина / хитозана для длительного применения в глазах. Внутр. J. Biol. Макромол. 72, 1451–1458. DOI: 10.1016 / j.ijbiomac.2014.10.014
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кунья-Азеведо, E.П., Сильва, Дж. Р., Мартинс, О. П., Сикейра-Моура, М. П., Бокка, А. Л., Фелипе, М. С. и др. (2011). In vitro противогрибковая активность и токсичность итраконазола в наночастицах DMSA-PLGA. J. Nanosci. Nanotechnol. 11, 2308–2314. DOI: 10.1166 / jnn.2011.3576
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Das, P. J., Paul, P., Mukherjee, B., Mazumder, B., Mondal, L., Baishya, R., et al. (2015). Доставка в легкие наночастиц, нагруженных вориконазолом, обеспечивающих пролонгированный уровень лекарственного средства в легких: перспективное средство для лечения грибковой инфекции. Mol. Pharm. 12, 2651–2664. DOI: 10.1021 / acs.molpharmaceut.5b00064
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Дас, С., Суреш, П. К. (2011). Наносуспензия: новое средство для улучшения доставки лекарств к поверхности глаза. Применение к амфотерицину B. Nanomedicine 7, 242–247. DOI: 10.1016 / j.nano.2010.07.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
де Са, Ф. А., Тавейра, С.Ф., Гельфусо, Г. М., Лима, Э. М., и Гратьери, Т. (2015). Липосомальный вориконазол (VOR) для улучшения доставки в глаза. Colloids Surf. B Биоинтерфейсы 133, 331–338. DOI: 10.1016 / j.colsurfb.2015.06.036
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Дубе, А., Рейнольдс, Дж. Л., Ло, В.-К., Мапонга, К.С., Прасад, П. Н., и Морс, Г. Д. (2014). Мультимодальные наночастицы, обеспечивающие иммуномодуляцию и внутриклеточную доставку лекарств при инфекционных заболеваниях. Наномедицина 10, 831–838. DOI: 10.1016 / j.nano.2013.11.012
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Эльмослемани, Р. М., Абдаллах, О. Ю., Эль-Хордагуи, Л. К., и Халафаллах, Н. М. (2012). Липосомы пропиленгликоля как местная система доставки нитрата миконазола: сравнение с обычными липосомами. AAPS PharmSciTech 13, 723–731. DOI: 10.1208 / s12249-012-9783-6
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Эсса, С., Лоухичи, Ф., Раймонд, М., и Хильдген, П. (2012). Повышенная противогрибковая активность наночастиц ПЭГ / ПЛА, нагруженных итраконазолом. J. Microencapsul. 30, 1–13. DOI: 10.3109 / 02652048.2012.714410
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Фальчи, Д. Р., душ Сантуш, Р. П., Вирт, Ф., и Голдани, Л. З. (2011). Непрерывная инфузия дезоксихолата амфотерицина B: инновационная недорогая стратегия противогрибкового лечения. Микозы 54, 91–98.DOI: 10.1111 / j.1439-0507.2009.01805.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Финкельштейн А. и Хольц Р. (1973). Водные поры, созданные в тонких липидных мембранах полиеновыми антибиотиками нистатином и амфотерицином B. Мембраны (Базель). 2, 377–408.
PubMed Аннотация | Google Scholar
Фрэнсис П. и Уолш Т. Дж. (1992). Растущая роль флуцитозина у пациентов с ослабленным иммунитетом: новые взгляды на безопасность, фармакокинетику и противогрибковую терапию. Clin. Заразить. Дис. 15, 1003–1018.
PubMed Аннотация | Google Scholar
Гангадхар К. Н., Адхикари К. и Шричана Т. (2014). Синтез и оценка сульфата дезоксихолата натрия в качестве липидного носителя лекарственного средства для повышения растворимости, стабильности и безопасности препарата для ингаляции амфотерицина В. Внутр. J. Pharm. 471, 430–438. DOI: 10.1016 / j.ijpharm.2014.05.066
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Георгопападаков, Н.Х. (2001). Обновленная информация о противогрибковых средствах, нацеленных на клеточную стенку: сосредоточьтесь на ингибиторах β-1,3-глюкансинтазы. Мнение эксперта. Расследование. Наркотики 10, 269–280. DOI: 10.1517 / 13543784.10.2.269
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Groll, A.H., Gea-Banacloche, J.C., Glasmacher, A., Just-Nuebling, G., Maschmeyer, G., and Walsh, T.J. (2003). Клиническая фармакология противогрибковых соединений. Заражение. Дис. Clin. North Am. 17, 159–191. DOI: 10.1016 / S0891-5520 (02) 00068-5
PubMed Аннотация | CrossRef Полный текст
Гролль, А.Х., Пискителли С.С. и Уолш Т. Дж. (1998). Клиническая фармакология системных противогрибковых агентов: всесторонний обзор агентов, используемых в клинической практике, текущих исследуемых соединений и предполагаемых целей для разработки противогрибковых препаратов. Adv. Pharmacol. 44, 343–500. DOI: 10.1016 / S1054-3589 (08) 60129-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гулати М., Баджад С., Сингх С., Фердоус А. Дж. И Сингх М. (1998). Разработка липосомального препарата амфотерицина В. J. Microencapsul. 15, 137–151. DOI: 10.3109 / 0265204980
44
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гупта М., Вьяс С. П. (2012). Разработка, характеристика и оценка in vivo эффективных липидных наночастиц для дермальной доставки флуконазола против кожного кандидоза. Chem. Phys. Липиды 165, 454–461. DOI: 10.1016 / j.chemphyslip.2012.01.006
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хан, К., Miah, M.A.J., Shanmugam, S., Yong, C.S., Choi, H.-G., Kim, J.A., et al. (2007). Смешанная мицеллярная наночастица амфотерицина B и поли-стирол-блок-полиэтиленоксид снижает нефротоксичность, но сохраняет противогрибковую активность. Arch. Pharm. Res. 30, 1344–1349. DOI: 10.1007 / BF02980276
PubMed Аннотация | CrossRef Полный текст |
PPT — Грибковые заболевания (микозы) Презентация PowerPoint, скачать бесплатно
Грибковые заболевания (микозы)
Задачи обучения В конце урока учащиеся смогут: • Обсудить причины возникновения грибков. Заболевания • Сравните и сопоставьте поверхностные, кожные, подкожные, системные и условно-патогенные микозы с точки зрения характеристик / определения, примеров болезней, которые они могут вызывать, и их возбудителя, и лабораторной диагностики
Как грибки вызывают заболевание? • Рост на поверхности тела.• Вторжение в тело. • Аллергические реакции. • Токсины, выделяемые при приеме внутрь.
КЛАССИФИКАЦИЯ ГРИБКИХ ИНФЕКЦИЙ Микозы: грибковые заболевания. Имеет тенденцию быть хроническим, потому что грибки растут медленно. Грибковые заболевания подразделяются на 4 группы: • Поверхностные микозы • Кожные микозы • Подкожные микозы • Глубокие (системные) микозы
ГРИБКОВЫЕ ЗАБОЛЕВАНИЯ Оппортунистические микозы: вызываются микроорганизмами, которые, как правило, безвредны, если индивидуум не ослабил защитные силы: • СПИД и рак пациенты • Лица, принимающие антибиотики широкого спектра действия • Лица очень пожилого или очень молодого возраста (новорожденные).• Примеры: • Аспергиллез: вдыхание спор Aspergillus. • Дрожжевые инфекции или кандидоз: вызывается в основном Candida albicans. Часть нормальной микрофлоры полости рта, пищевода и влагалища.
Оппортунистические грибы Микозы • Candidia albicans • обычный одноклеточный гриб, который является частью флоры ротовой полости, влагалища и желудочно-кишечного тракта; • Они становятся оппортунистами, особенно у людей с ослабленным иммунитетом.



 Заразиться инфекцией можно во время контакта с водой из непроточного водоема, к примеру, озера. Имеющиеся на лице папилломы следует удалять оперативным способом или с использованием лазера, после чего места поражения нужно обработать противогрибковым средством;
Заразиться инфекцией можно во время контакта с водой из непроточного водоема, к примеру, озера. Имеющиеся на лице папилломы следует удалять оперативным способом или с использованием лазера, после чего места поражения нужно обработать противогрибковым средством; Заболевание легко поддается терапии, при своевременном обращении к врачу;
Заболевание легко поддается терапии, при своевременном обращении к врачу; Чаще всего такому заболеванию подвергаются люди имеющие заболевания эндокринной системы и страдающие от повышенного потоотделения.
Чаще всего такому заболеванию подвергаются люди имеющие заболевания эндокринной системы и страдающие от повышенного потоотделения.