Типы рака легких | Онкотест
Традиционная диагностика
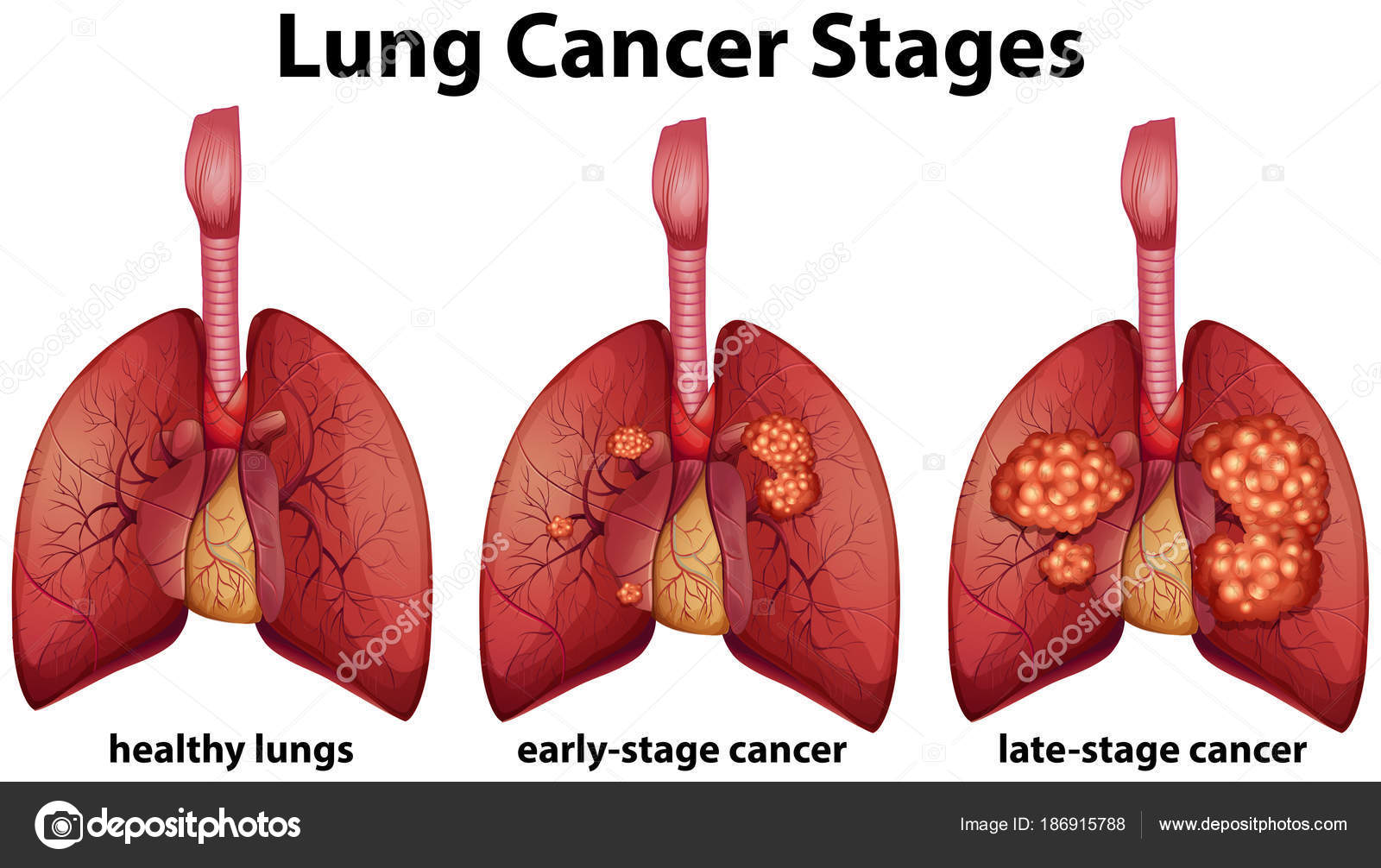
Первичный рак легких — это рак, развившийся из клеток легких. Традиционный метод диагностирования позволяет взять образец опухолевых клеток и классифицировать тип рака по виду клеток под микроскопом. Традиционная диагностика различает два главных типа рака легких: мелкоклеточная карцинома легкого, которая составляет около 15% от всех случаев рака легких, и немелкоклеточная карцинома легкого, которая более распространена и составляет около 85% от всех случаев.
Два этих типа отличаются способом роста и распространения, а также разными подходами к их лечению. Поэтому важно уметь их различать. К примеру, опухоли немелкоклеточной карциномы легкого обычно удаляют хирургическим путем, тогда как в случае мелкоклеточной карциномы легкого назначают медикаментозное лечение, иногда наряду с мерами для сдерживания распространения заболевания, например лучевой терапией.
Немелкоклеточная карцинома легкого
Этот тип рака более распространен, чем мелкоклеточная карцинома легкого, и обычно прогрессирует и метастазирует не так быстро. Этот тип можно разделить на несколько подтипов:
Аденокарцинома Аденокарцинома — самый распространенный тип рака легких, он составляет около 50% всех случаев заболеваний немелкоклеточной карциномой легкого. Кроме всего прочего, частота заболевания аденокарциномой легкого увеличилась за последние годы. Опухоль в данном случае развивается из специальных клеток в легком, которые вырабатывают муцин (слизистый секрет легкого). Наиболее частое место возникновения — поверхность легкого, где обычно возникает несколько очагов. Связи между аденокарциномой и курением не установлено, из всех типов рака легких этот тип чаще всего встречается у некурящих и у женщин. Бронхоальвеолярная карцинома — это подтип аденокарциномы, которую можно выявить с помощью рентгеноскопии.
Сквамозно-клеточная карцинома Сквамозно-клеточная карцинома составляет около 30% случаев немелкоклеточной карциномы легкого. В отличие от аденокарциномы, которая обычно образовывается на поверхности легкого, сквамозно-клеточная карцинома обычно развивается в центральных участках бронхов в легких. Существует тесная связь между этим типом рака легкого и курением, и этот тип заболевания чаще встречается у мужчин, чем у женщин.
В отличие от аденокарциномы, которая обычно образовывается на поверхности легкого, сквамозно-клеточная карцинома обычно развивается в центральных участках бронхов в легких. Существует тесная связь между этим типом рака легкого и курением, и этот тип заболевания чаще встречается у мужчин, чем у женщин.
Крупноклеточная карцинома Крупноклеточная карцинома является самым редким типом немелкоклеточной карциномы легкого. В большинстве случаев крупноклеточная карцинома образуется на поверхности легкого.
Комбинация нескольких типов Кроме опухолей трех вышеописанных типов бывают случаи рака легкого, в которых присутствуют сразу несколько или все эти типы.
Мелкоклеточная карцинома легкого
Мелкоклеточная карцинома, которую также называют овсяноклеточным раком из-за плоской формы ее мелких клеток, не так распространена и составляет около 20% всех случаев рака легкого. Этот тип опухоли считается очень аггрессивным. Он может давать метастазы на ранних стадиях заболевания, так что к моменту диагностирования заболевание уже имеет диффузный характер, что влияет на характер лечения. Опухоли этого типа обычно развиваются в центральных участках легкого и хорошо реагируют на химиотерапию и радиотерапию. Существует тесная связь между этим типом рака легкого и курением. Более 95% людей, у которых диагностирована мелкоклеточная карцинома легкого, заболели раком из-за того, что курят или курили в прошлом, и риск этого заболевания значительно повышается с увеличением числа сигарет в день, а степень риска прямо пропорциональна числу лет, в течение которых человек курит.
Молекулярная диагностика
До совсем недавнего времени в основе классификации рака легких лежала форма опухолевых клеток, наблюдаемая под микроскопом, и их соответствующее деление. Однако за последние годы наблюдается значительный прогресс в понимании механизмов развития рака легких. В результате были существенно усовершенствованы методики диагностирования и лечения заболевания.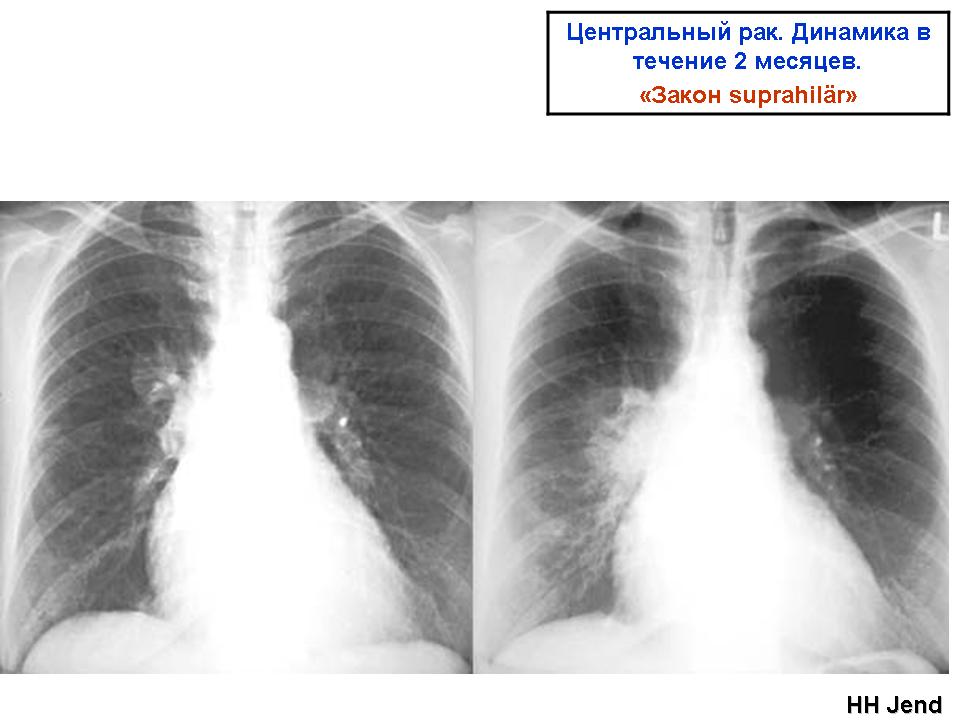 Сейчас врач может порекомендовать курс лечения, который точно и индивидуально соответствует уникальным характеристикам раковой опухоли каждого отдельного пациента. Индивидуальный подбор лечения важен, потому что рак легких — это не одно заболевание, и у разных пациентов с раком легких опухоли разного типа.
Сейчас врач может порекомендовать курс лечения, который точно и индивидуально соответствует уникальным характеристикам раковой опухоли каждого отдельного пациента. Индивидуальный подбор лечения важен, потому что рак легких — это не одно заболевание, и у разных пациентов с раком легких опухоли разного типа.
Страница не найдена |
Страница не найдена |
404. Страница не найдена
Архив за месяц
ПнВтСрЧтПтСбВс
19202122232425
2627282930
12
12
1
3031
12
15161718192021
25262728293031
123
45678910
12
17181920212223
31
2728293031
1
1234
567891011
12
891011121314
11121314151617
28293031
1234
12
12345
6789101112
567891011
12131415161718
19202122232425
3456789
17181920212223
24252627282930
12345
13141516171819
20212223242526
2728293031
15161718192021
22232425262728
2930
Архивы
Май
Июн
Июл
Авг
Сен
Окт
Ноя
Дек
Метки
Настройки
для слабовидящих
Хирургическое лечение пациентки с нейроэндокринной опухолью легкого, ассоциированной с АКТГ-эктопическим синдромом: клинический случай | Пикунов
Аннотация
Среди первичных новообразований легких доля нейроэндокринных опухолей составляет до 20–25%. Согласно базе данных Surveillance Epidemiology and End Results (SEER), с 1970 г. отмечен значительный рост диагностики первичных карциноидных опухолей разныхорганов с максимальным приростом заболеваемости в группе бронхолегочной локализации. Карциноидные опухоли легкого составляют приблизительно 2% от всех первичных опухолей легких, но только 5% этих образований связаны с продукцией АКТГ.
Согласно базе данных Surveillance Epidemiology and End Results (SEER), с 1970 г. отмечен значительный рост диагностики первичных карциноидных опухолей разныхорганов с максимальным приростом заболеваемости в группе бронхолегочной локализации. Карциноидные опухоли легкого составляют приблизительно 2% от всех первичных опухолей легких, но только 5% этих образований связаны с продукцией АКТГ.
Несмотря на выраженность клинических проявлений и быстрое прогрессирование симптомов гиперкортицизма, топическая диагностика АКТГ-эктопического синдрома зачастую вызывает определенные затруднения. Сложность диагностики эктопированных опухолейсвязана с тем, что большая часть этих образований имеет столь малые размеры, что они могут быть пропущены при стандартных методиках исследования (рентгенография, УЗИ, МСКТ или МРТ). После постановки диагноза АКТГ-эктопического синдрома единственнымоптимальным методом патогенетической терапии является радикальное удаление опухоли, которое приводит к нормализации функции коры надпочечников и ликвидации гиперкортицизма. Однако достижение этой цели во многих случаях затруднено из-за позднейтопической диагностики, распространенности опухолевого процесса и обширного метастазирования.
В работе представлено клиническое наблюдение пациентки с диагнозом “нейроэндокринная опухоль легкого с АКТГ-эктопическим синдромом”. Описаны значимость мультидисциплинарного подхода, сложности дифференциальной диагностики, особенностипериоперационного периода и отдаленные результаты лечения.
Актуальность
Нейроэндокринные опухоли (НЭО) – группа гетерогенных новообразований, происходящих из клеток диффузной эндокринной системы (нейроэндокринных клеток Кульчицкого) и обладающих рядом общих биологических свойств [1]. Наиболее часто нейроэндокринные опухоли локализованы в органах желудочно-кишечного тракта (прямая кишка, тонкий кишечник, поджелудочная железа и др.). Согласно базе данных “Скрининг, эпидемиология и заключительные результаты” (SEER) Национального онкологического института, в течение 15 лет произошло значительное увеличение заболеваемости нейроэндокринными опухолями различных органов, причем наибольший рост отмечен для новообразований бронхолегочной локализации, доля которых составляет до 30% [2]. Группа нейроэндокринных опухолей бронхолегочной локализации разнообразна по потенциалу злокачественности и прогнозу. Согласно классификации ВОЗ от 2015 г., выделяют четыре гистологических варианта НЭО легких: типичный карциноид, атипичный карциноид, крупноклеточная нейроэндокринная опухоль и мелкоклеточный рак легких [3, 4].
Группа нейроэндокринных опухолей бронхолегочной локализации разнообразна по потенциалу злокачественности и прогнозу. Согласно классификации ВОЗ от 2015 г., выделяют четыре гистологических варианта НЭО легких: типичный карциноид, атипичный карциноид, крупноклеточная нейроэндокринная опухоль и мелкоклеточный рак легких [3, 4].
Гормонально активные новообразования, ассоциированные с различными паранеопластическими синдромами (Кушинга, карциноидным, акромегалией, миастеническим, Ламберта–Итона и др.), диагностируют не более чем в 5% среди всех НЭО [5]. Лидирующее место среди НЭО-активных новообразований бронхолегочной локализации занимает АКТГ-эктопический синдром (2%), для которого характерно развитие эндогенного гиперкортицизма с клинической картиной синдрома Иценко–Кушинга [6].
В настоящей работе представлено клиническое наблюдение пациентки с НЭО бронхолегочной локализации, ассоциированной с АКТГ-эктопическим синдромом.
Описание случая
Пациентка Н. 31 года обратилась к терапевту с жалобами на мышечную слабость, эпизоды повышения артериального давления до 200/100 мм рт.ст., учащенное сердцебиение, нарушение менструального цикла, прибавку в весе в течение последних двух лет. При обследовании в эндокринологическом отделении у пациентки выявлен эндогенный гиперкортицизм (таблица).
Результаты эндокринологических лабораторных испытаний
По данным МРТ головного мозга данных о наличии аденомы гипофиза не получено. В ходе дальнейшего диагностического поиска по результатам большой дексаметазоновой пробы установлен эктопический характер продукции АКТГ. При заборе крови из нижних каменистых синусов была подтверждена эктопическая продукция АКТГ. По данным МСКТ органов грудной клетки и брюшной полости с контрастированием выявлено новообразование в средней доле (S5) правого легкого неправильной округлой формы с нечеткими контурами, расположенное по ходу субсегментарного бронха, размерами 21,8 × 13 × 13 мм, неравномерно накапливающее контрастное вещество до 48 ед. Н. Медиастинальной лимфоаденопатии нет (рис. 1). При ФГДС и колоноскопии опухолевых новообразований не выявлено.
Н. Медиастинальной лимфоаденопатии нет (рис. 1). При ФГДС и колоноскопии опухолевых новообразований не выявлено.
Рис. 1. МСКТ органов грудной клетки пациентки Н. с контрастным усилением.
Пациентка госпитализирована в отделение торакальной хирургии с диагнозом: нейроэндокринная опухоль средней доли правого легкого c T1bN0M0. АКТГ-эктопический синдром.
Выполнена видеоассистированная краевая резекция средней доли правого легкого. При срочном морфологическом исследовании картина нейроэндокринной опухоли солидно-альвеолярного строения. Определяется два митоза в одном поле зрения. Окончательный объем операции – видеоассистированная средняя лобэктомия справа, медиастинальная лимфаденэктомия. По данным планового морфологического и иммуногистохимического исследования – морфологическая картина атипичного карциноида легкого размерами 2,2 × 1,2 × 1 см. Количество митозов – 1 в 10 полях зрения при увеличении 400 (2 мм кВ). ИП Ki67 – 20%; pT1pN0(0/23)cM0;R0;L0,V0 (рис. 2).
Рис. 2. Слева: микропрепарат удаленной нейроэндокринной опухоли солидно-трабекулярного строения, два митоза в одном поле зрения (окраска гематоксилином и эозином, ×400). Справа: иммуногистохимическое исследование удаленной нейроэндокринной опухоли, реакция с антителом к Ki-67 (клон SP6, Cell Marque), индекс Ki67 около 15% (ДАБ, гематоксилин, ×400).
Кортизол периферической крови достиг уровня референсных значений в течение первого часа после операции. Динамика уровня кортизола в периоперационном периоде представлена на диаграмме (рис. 3).
Рис. 3. Периоперационная динамика уровня кортизола периферической крови.
Пациентка активизирована на вторые сутки после операции. С целью предупреждения развития острой надпочечниковой недостаточности в послеоперационном периоде проводилась заместительная гормональная терапия (гидрокортизон).
При контрольном обследовании через 6 мес пациентка отмечает значимое субъективное улучшение общего самочувствия – отсутствие подъемов артериального давления, снижение веса и нормализацию менструального цикла. Уровень утреннего кортизола через 6 мес после операции – 250 нмоль/л. Внешний вид пациентки до и после хирургического лечения представлен на рис. 4.
Уровень утреннего кортизола через 6 мес после операции – 250 нмоль/л. Внешний вид пациентки до и после хирургического лечения представлен на рис. 4.
Рис. 4. Внешний вид пациентки до операции и спустя 6 мес.
Обсуждение
Связь между мелкоклеточным раком легкого и синдромом Кушинга впервые была обнаружена в 1928 г. Определение этой болезни как синдрома описано в работе C.K. Meador и соавт., которые в 1962 г. продемонстрировали биологическую активность АКТГ при карциноидных опухолях легких [7]. Данные новообразования характеризуются отсутствием взаимосвязи с курением в отличие от рака легкого [8, 9].
Карциноидные опухоли легких возникают из нейроэндокринных клеток Кульчицкого, локализованных в слизистой оболочке бронхиального дерева, и составляют от 2 до 5% всех первичных злокачественных заболеваний легких, эктопическая гиперсекреция АКТГ происходит только у 0,5–2% этих новообразований [10, 11]. Эктопический источник АКТГ расположен в легком более чем в 45% опухолей различной локализации [12, 13]. Тимус (11%) и поджелудочная железа (8%) являются следующими наиболее распространенными органами, где могут возникать нейроэндокринные опухоли с АКТГ-эктопическим синдромом. У пациентов с АКТГ-эктопическим синдромом концентрация кортизола и скорости его секреции могут достигать свыше 2000 нмоль/л. В представленном клиническом наблюдении диагноз был установлен спустя 2 года после манифестации синдрома Иценко–Кушинга.
Диагностика АКТГ-эктопического синдрома часто представляет определенные трудности в проведении дифференциального диагноза у клиницистов. Селективный забор крови из нижних каменистых синусов считается методом выбора при проведении дифференциальной диагностики. Раннее обнаружение и удаление гормонопродуцирующей опухоли позволяет избежать вынужденной двусторонней адреналэктомии и снижает риск прогрессирования заболевания. При подтверждении АКТГ-эктопического синдрома в стандарты топической диагностики входит выполнение МРТ головного мозга, МСКТ брюшной полости и грудной клетки с контрастным усилением, ФГДС, колоноскопии. Основным методом лечения локализованных форм карциноидных опухолей бронхолегочной локализации является хирургический [14]. Характер и объем операции несколько отличаются от таковых при раке легкого, предпочтение отдается выполнению органосохраняющих операций типа сегментэктомии, бисегментэктомии, лобэктомии, резекции легких с бронхопластическими этапами. Метастазирование в лимфатические узлы группы N1 при типичных карциноидах встречается примерно в 4–5% случаев, поражение N2 описано в единичных наблюдениях, однако нет сомнений относительно необходимости выполнения медиастинальной лимфаденэктомии[15, 16].
Основным методом лечения локализованных форм карциноидных опухолей бронхолегочной локализации является хирургический [14]. Характер и объем операции несколько отличаются от таковых при раке легкого, предпочтение отдается выполнению органосохраняющих операций типа сегментэктомии, бисегментэктомии, лобэктомии, резекции легких с бронхопластическими этапами. Метастазирование в лимфатические узлы группы N1 при типичных карциноидах встречается примерно в 4–5% случаев, поражение N2 описано в единичных наблюдениях, однако нет сомнений относительно необходимости выполнения медиастинальной лимфаденэктомии[15, 16].
В последнее время дискутабельным остается вопрос целесообразности выполнения сублобарных анатомических резекций при опухоли диаметром менее 2 см. Ввиду относительной редкости карциноидов легких отсутствуют крупные многоцентровые исследования, однозначно подтверждающие или опровергающие такой подход. В данной ситуации нам представляется возможным экстраполировать результаты аналогичных исследований при неметастатическом раке легкого (НМРЛ) [17, 18], свидетельствующие о возможности выполнения сублобарных резекций без ущерба онкологическому радикализму при образованиях менее 2 см в диаметре, а также имеющие функциональные преимущества в раннем и отдаленном послеоперационном периоде по данным ряда исследований [18, 19].
В послеоперационном периоде у пациентов с АКТГ-эктопическим синдромом необходим динамический контроль уровня кортизола крови для раннего выявления и коррекции симптомов надпочечниковой недостаточности вследствие компенсаторной атрофии и неполноценной работы надпочечников.
Заключение
Карциноидные опухоли бронхолегочной локализации – медленнорастущие новообразования, характеризующиеся относительно благоприятным прогнозом, при условии своевременного радикального хирургического лечения. Нейроэндокринные опухоли легких – наиболее распространенная причина АКТГ-эктопического синдрома. Топический поиск очага при установленном АКТГ-эктопическом синдроме до настоящего времени остается сложной задачей, лежащей в области интересов врачей разных специальностей.
Основным методом лечения карциноидных опухолей легких является хирургический. Анатомическая резекция легкого (лобэктомия, сегментэктомия, бисегментэктомия) с медиастинальной лимфодиссекцией – операция выбора при карциноидных опухолях легкого вне зависимости от степени дифференцировки. Последнее время в различных исследованиях часто обсуждается возможность выполнения сублобарных резекций при ранних формах НМРЛ (размере первичного очага менее 2 см и отсутствии медиастинальной лимфаденопатии). Проведение подобных исследований в отношении новообразований с меньшим потенциалом злокачественности, таких как НЭО, остается перспективным направлением в развитии торакальной хирургии.
Дополнительная информация
Источник финансирования. Подготовка и публикация статьи осуществлены на личные средства авторского коллектива.
Согласие пациента. Пациентка добровольно подписала информированное согласие на публикацию своих медицинских данных в журнале “Эндокринная хирургия”.
Конфликт интересов. Авторы декларируют отсутствие конфликта интересов, связанных с публикацией настоящей статьи, о которых следовало бы сообщить.
Благодарности. Огромная благодарность сотрудникам патологоанатомического отделения Института хирургии им. А.В. Вишневского за сотрудничество и предоставленный материал.
1. Paladugu RR, Benfield JR, Pak HY, et al. Bronchopulmonary Kulchitzky cell carcinomas. A new classification scheme for typical and atypical carcinoids. Cancer. 1985;55(6):1303-1311. doi: 10.1002/1097-0142(19850315)55:6<1303::aid-cncr2820550625>3.0.co;2-a.
2. Travis W, Brambilla E, Burke A, et al. WHO Classification of Tumours of the Lung, Pleura, Thymus and Heart. 4th ed. Lyon: IARC Press; 2015.
4th ed. Lyon: IARC Press; 2015.
3. Travis WD, Brambilla E, Nicholson AG, et al. The 2015 World Health Organization Classification of Lung Tumors: Impact of Genetic, Clinical and Radiologic Advances Since the 2004 Classification. J Thorac Oncol. 2015;10(9):1243-1260. doi: 10.1097/JTO.0000000000000630/
4. Тер-Ованесов М.Д., Полоцкий Б.Е. Карциноидные опухоли торакальной локализации – современное состояние проблемы. // Проблемы туберкулеза и болезней легких. – 2005. – Т. 6. – №4. – С. 220-226. [Ter-Ovanesov M.D., Polotskiy B.E. Kartsinoidnye opukholitorakal'noy lokalizatsii – sovremennoe sostoyanie problemy. Probl Tuberk Bolezn Legk. 2005;6(4):220-226. (In Russ.)]
5. Чекини А.С. Нейроэндокринные опухоли легких (карциноиды) и тимуса: Дис. … канд. мед. наук. – М.; 2012. [Chekini AS. Neyroendokrinnye opukholi legkikh (kartsinoidy) i timusa. Moscow; 2012. (In Russ.)]
6. Meador CK, Liddle GW, Island DP, et al. Cause of Cushing's syndrome in patients with tumors arising from “nonendocrine” tissue. J Clin Endocrinol Metab. 1962;22:693-703. doi: 10.1210/jcem-22-7-693.
7. Fink G, Krelbaum T, Yellin A, et al. Pulmonary carcinoid: presentation, diagnosis, and outcome in 142 cases in Israel and review of 640 cases from the literature. Chest. 2001; 119(6):1647-1651. doi: 10.1378/chest.119.6.1647.
8. Gustafsson BI, Kidd M, Chan A, et al. Bronchopulmonary neuroendocrine tumors. Cancer. 2008;113(1):5-21. doi: 10.1002/cncr.23542.
9. Deb SJ, Nichols FC, Allen MS, et al. Pulmonary carcinoid tumors with Cushing's syndrome: an aggressive variant or not? Ann Thorac Surg. 2005;79(4):1132-1136; discussion 1132-1136. doi: 10.1016/j.athoracsur.2004.07.021.
Deb SJ, Nichols FC, Allen MS, et al. Pulmonary carcinoid tumors with Cushing's syndrome: an aggressive variant or not? Ann Thorac Surg. 2005;79(4):1132-1136; discussion 1132-1136. doi: 10.1016/j.athoracsur.2004.07.021.
10. Ilias I, Torpy DJ, Pacak K, et al. Cushing's syndrome due to ectopic corticotropin secretion: twenty years' experience at the National Institutes of Health. J Clin Endocrinol Metab. 2005;90(8):4955-4962. doi: 10.1210/jc.2004-2527.
11. Isidori AM, Kaltsas GA, Pozza C, et al. The ectopic adrenocorticotropin syndrome: clinical features, diagnosis, management, and long-term follow-up. J Clin Endocrinol Metab. 2006;91(2):371-377. doi: 10.1210/jc.2005-1542.
12. Scanagatta P, Montresor E, Pergher S, et al. Cushing's syndrome induced by bronchopulmonary carcinoid tumours: a review of 98 cases and our experience of two cases. Chir Ital. 2004;56(1):63-70.
13. Isidori AM, Lenzi A. Ectopic ACTH syndrome. Arq Bras Endocrinol Metabol. 2007;51(8):1217-1225. doi: 10.1590/s0004-27302007000800007.
14. Cardillo G, Sera F, Di Martino M, et al. Bronchial carcinoid tumors: nodal status and long-term survival after resection. Ann Thorac Surg. 2004;77(5):1781-1785. doi: 10.1016/j.athoracsur.2003.10.089.
15. Oberg K, Hellman P, Ferolla P, et al. Neuroendocrine bronchial and thymic tumors: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2012; 23 Suppl 7:vii120-123. doi: 10. 1093/annonc/mds267.
1093/annonc/mds267.
16. Villamizar N, Swanson SJ. Lobectomy vs. segmentectomy for NSCLC (T<2 cm). Ann Cardiothorac Surg. 2014;3(2): 160-166. doi: 10.3978/j.issn.2225-319X.2014.02.11.
17. Okada M, Mimae T, Tsutani Y, et al. Segmentectomy versus lobectomy for clinical stage IA lung adenocarcinoma. Ann Cardiothorac Surg. 2014;3(2):153-159. doi: 10.3978/j.issn.2225-319X.2014.02.10.
18. Okada M, Koike T, Higashiyama M, et al. Radical sublobar resection for small-sized non-small cell lung cancer: a multicenter study. J Thorac Cardiovasc Surg. 2006;132(4): 769-775. doi: 10.1016/j.jtcvs.2006.02.063.
19. Saito H, Nakagawa T, Ito M, et al. Pulmonary function after lobectomy versus segmentectomy in patients with stage I non-small cell lung cancer. World J Surg. 2014;38(8):2025-2031. doi: 10.1007/s00268-014-2521-3.
Доброкачественные опухоли легких. :: АЦМД
Откуда берутся доброкачественные опухоли легких? Как их диагностируют? Чем они проявляются?
Доброкачественные опухоли легких могут возникаю абсолютно из любой ткани грудной клетки (эпителиальной, соединительной, мышечной, хрящевой), а также эмбриональной (тогда опухоль возникает как нарушение развития).
Принято различать две группы доброкачественных опухолей: внутрибронхиальные и внутрилегочные.
Внутрибронхиальные опухоли
Аденома, цилиндрома, карциноид, гамартома, папиллома. Чаще всего эти опухоли располагаются в крупных бронхах. Их развитие сопровождается возникновением полиповидного узла округлой или овальной формы.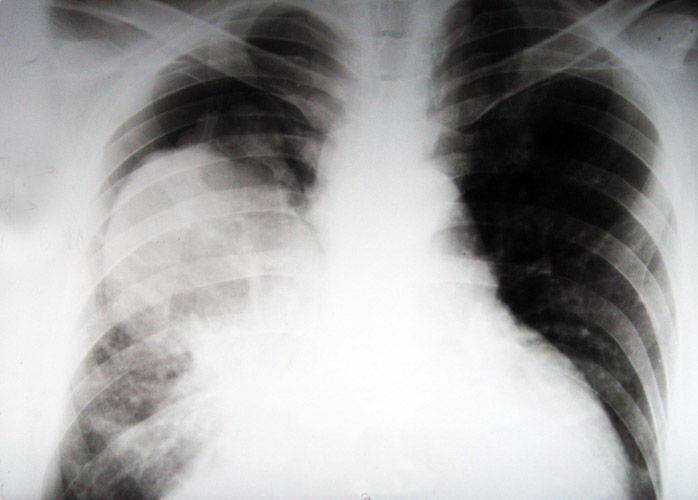 Такой узел продолжает свой рост внутрь бронха, в толщу его стенки.
Такой узел продолжает свой рост внутрь бронха, в толщу его стенки.
Доброкачественные опухоли могут перерождаться (малигнизировать) в злокачественные.
Внешние проявления наступают только тогда, когда опухоль перекрывает просвет бронха и вызывает гиповентиляцию обширного участка легкого. На этом фоне могут присоединяться кровохарканье, ателектазы, пневмония.
Диагностика: на рентгенограммах можно определить нарушение проходимости бронха различной степени, гиповентиляцию, вздутие различной степени, инфильтрацию легочной паренхимы. При выполнении спиральной компьютерной томографии можно детально определить местонахождения опухоли, соотношении опухоли и просвета бронха, определить не задеты ли соседние бронхи, детально выявить изменений, которые возникли в легочной ткани.
Внутрилегочные доброкачественные опухоли
Аденома, папиллома, гамартома и прочие. Чаще всего являются случайной находкой на профилактических осмотрах. Могут вырастать до довольно больших размеров, смещая и сдавливая рядом расположенные органы и структуры, тем самым вызывая отдышку, кровохарканье, иногда и патология сердца.
На рентгенограммах доброкачественные опухоли выглядят как одиночно расположенные небольшие образования правильной формы и однородной структуры. Признаков инфильтрации или некроза отсутствуют, легочной рисунок. Кони легких без изменений.
По частоте диагностики среди всех доброкачественных опухолей лидирует гамартома – образование, которое состоит из хрящевой, мышечной, железистой и других тканей.
Диагностика гамартом. На рентгенограмма они выглядят как как округлое или овальное образование с четким и ровным контуром. Находится они могут в любом отделе любого легкого. Размеры обычно в пределах 3-5 см, хотя известны случаи до 25 см. Внешние контуры четко очерчены, иногда могут быть волнистыми. Характерный признак гамартомы – включение солей кальция, которые легко распознать на спиральной компьютерной томографии. Окружающий легочной рисунок, плевра и корни легких не изменены. Размеры и структура гамартомы могут быть стабильны и не изменять длительные годы.
Окружающий легочной рисунок, плевра и корни легких не изменены. Размеры и структура гамартомы могут быть стабильны и не изменять длительные годы.
Осложнения: смещение и сдавление соседних бронхов.
Не думайте и не гадайте, пусть разбирается врач!
Возможно у Вас есть вопросы – задайте их мне!
Статью подготовили специалисты отделения лучевой диагностики АЦМД-МЕДОКС
Доброкачественные опухоли легких: рассказывает онколог Роман Ищенко | медицина | ЗДОРОВЬЕ
Доброкачественные опухоли легких чаще встречаются у мужчин. В случае гамартом в повышенной группе риска находятся женщины. Некоторые виды опухолей абсолютно доброкачественны, другие имеют тенденцию к озлокачествлению. Об особенностях и методах лечения патологии рассказывает заместитель главного врача по хирургической помощи Научно-клинического центра ФМБА России, д.м.н., профессор Роман Ищенко.
Чаще всего в легочной ткани встречаются гамартомы. Это абсолютно доброкачественная опухоль, не склонная к метастазам и рецидивам. Гемартромы могут быть расположены в любой части легкого. Возрастных критериев не существует, но чаще всего это пациенты старше 40 лет.
Гамартомы редко превышают в размере 5 сантиметров, однако являются показанием для хирургического удаления. Если опухоль расположена рядом с бронхами, то по мере роста начинает сдавливать ткани, нарушая отток воздуха из части легкого. Это вызывает рецидивирующую пневмонию, которая дает комплекс септических симптомов: повышение температуры, бледность кожных покровов, мышечную слабость, похудение и пр. Пациенты с гамартромой в верхних отделах легких выглядят как больные туберкулезом. Флюорография и рентгенография позволяют выявить новообразование, однако лишь гистологическое заключение может являться окончательным. Поэтому для дифференциальной диагностики производят резекцию небольшого участка легкого. В большинстве российских клиник это выполняется торакоскопически – через плевральную полость и пару небольших проколов в грудной клетке.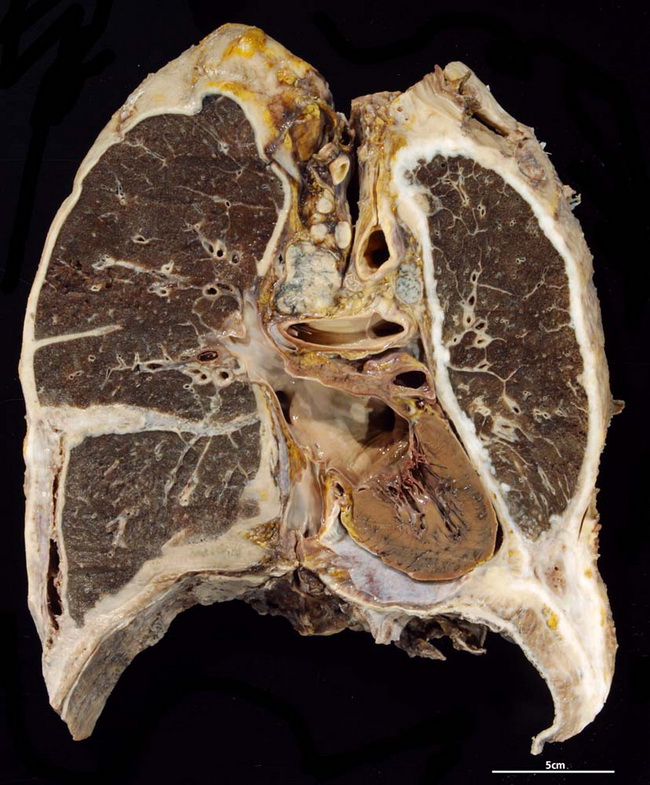
Следующая разновидность – аденомы. Они встречаются реже. Независимо от размера, подлежат обязательному удалению, поскольку имеют тенденцию к быстрому озлокачествлению. По сути аденома – это агрегатный предрак.
Наши легкие имеют протяженную сеть кровеносных сосудов, следовательно, здесь могут образовываться гемангиомы. Они бывают врожденными и приобретенными с риском развития от рождения до глубокой старости. В легких они встречаются гораздо реже чем в печени, но несут более серьезную угрозу для жизни, поскольку провоцируют кровохаркание и легочные кровотечения. Вдыхаемый нами воздух не стерилен, поэтому гемангиомы легких имеют тенденцию к инфицированию и формированию гнойно-воспалительных полостей с риском развития жизнеугрожающих состояний. Симптомы схожи с туберкулезом либо клинической картиной злокачественной опухоли.
Гемангиомы размером более 3-5 см подлежат хирургическому удалению. В этом случае хирургия дает полное выздоровление. Если через опухоль проходит питающий сосуд, проводят его склерозирование под контролем ангиографа. При наличии нескольких источников кровоснабжения, выполняется более сложное воздействие, либо торакоскопическое удаление.
Средний возраст, в котором пациенты подвергаются хирургическому лечению – 50-60 лет. При наличии множественных мелких образований, не дающих клинических проявлений, необходимо ежегодное динамическое наблюдение.
Остальные виды опухолей можно отнести к редко встречающимся. В легких содержится фиброзная ткань, поэтому, как и в бронхах, могут встречаться фибромы. В небольшом количестве присутствует нейроэндокринная ткань, из которой происходят нейроэндокринные опухоли. Раньше их относили к злокачественным, сегодня выделяют в особую группу, четко разделяя на нейроэндокринные раки и нейроэндокринные доброкачественные опухоли. Это связано с высоким уровнем морфологической диагностики и новым витком развития в изучении этой группы опухолей.
Справочно
Роман Викторович Ищенко – хирург, онколог. Специализация: злокачественные опухоли органов брюшной полости, легких, трахеи и плевры, кардиоонкология (лечение злокачественных опухолей у пациентов с сердечно-сосудистыми заболеваниями).
Консультирует пациентов в ФНКЦ ФМБА России (Москва). Записаться на очный прием можно на сайте врача или по телефону +7(495)971-71-72.
Подробнее о порядке госпитализации в московские клиники можно узнать на сервисе медицинского проекта «Здоров Я».
ОПУХОЛИ ЛЕГКИХ (РАК ЛЕГКОГО И ДР.)
Диагностика рака легкого
В последнее десятилетие благодаря использованию рентгенологических, бронхологических, морфологических (гистологических, цитологических), радионуклидных, ультразвуковых, хирургических и других методов диагностики опухолей легких удалось выработать стройную систему (алгоритм) мероприятий, цель которых – установление точного диагноза. Оптимальное планирование диагностики и лечения больных раком легкого должно основываться на следующих основных принципах.
- Первичная диагностика опухоли легкого с установлением локализации и клинико-анатомической формы.
- Уточняющая диагностика, направленная на определение распространенности опухолевого процесса (истинные размеры первичной опухоли, степень поражения внутригрудных лимфатических узлов, прорастание прилежащих органов и структур, выявления отдаленных метастазов), т.е. установление стадии заболевания.
- Морфологическая верификация опухоли с уточнением гистологической структуры и степени анаплазии (дифференцировки) опухолевых клеток.
- Определение исходного статуса больного, функциональных возможностей жизненно важных органов и систем.
Клиническая симптоматика рака легкого во многом определяется локализацией, размером и формой роста опухоли, характером метастазирования. Решающее значение, особенно на ранних этапах развития заболевания, имеет клинико-анатомическая форма опухоли.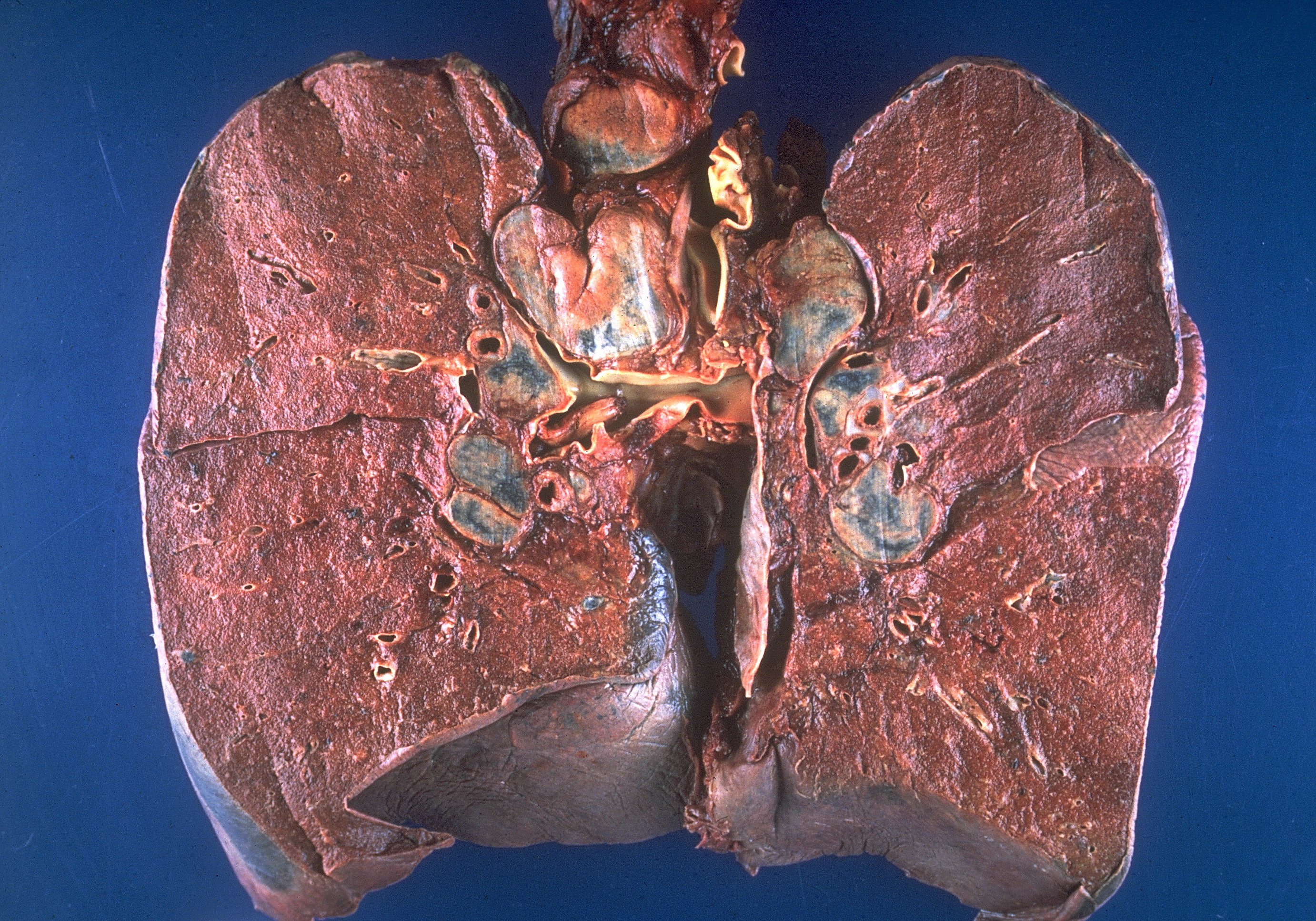
Факторы, оказывающие влияние на развитие рака легкого
Заболеваемость населения раком легкого за последние 50 лет резко возросла во многих странах мира. В настоящее время в большинстве развитых стран рак легкого является наиболее распространенной формой опухоли у мужчин и остается одной из важнейших медицинских и социально-экономических проблем. Ежегодно в мире регистрируется 1,3 млн. новых случаев рака легкого, из них 60% приходится на развитые страны.
Развитие злокачественной опухоли – многофакторный и многостадийный процесс, в основе которого лежит каскадное накопление клетками различных генетических изменений, приводящих к злокачественной трансформации. Предполагается, что для развития рака у человека необходимы изменения не менее 6-10 генетических факторов.
В патогенезе рака легкого можно условно выделить три этапа: I этап – связан с первичным контактом канцерогенного агента и легких, его активацией, взаимодействием с ДНК эпителиальной клетки, что приводит к изменению ее генома и фенотипа – образованию латентной раковой клетки. II этап – характеризуется хроническим повторным контактом канцерогенов или некоторых других повреждающих агентов (промоторов) с клетками; происходят дополнительные генные изменения, вызывающие размножение опухолевых клеток с образованием опухолевого узла. III этап – нарастание различных признаков злокачественности (атипии, инвазивного роста, метастазирования, хромосомных аберраций и др.), часто независимо друг от друга.
Факторы риска – смотри раздел «Профилактика рака».
Современная лечебная тактика
Клиническое стадирование «сTNM» с использованием современных диагностических возможностей является основополагающим (с учетом функциональных возможностей пациента) в выборе тактики лечения больного.
Патологическое или послеоперационное стадирование «pTNM» является более точным, заключительным. Оно позволяет при необходимости дополнить хирургическое лечение лучевой или лекарственной противоопухолевой терапией, скорректировать сроки мониторинга и является основой последующего изучения результатов различных методов лечения и других исследуемых показателей.
Оно позволяет при необходимости дополнить хирургическое лечение лучевой или лекарственной противоопухолевой терапией, скорректировать сроки мониторинга и является основой последующего изучения результатов различных методов лечения и других исследуемых показателей.
Морфологически рак легкого неоднороден, но преобладающим гистологическим типом (до 80%) является немелкоклеточный рак легкого – НМРЛ (плоскоклеточный, железистый, крупноклеточный). Мелкоклеточный рак в силу биологических особенностей течения и иных подходов к лечебной тактике выделяется в отдельную группу.
ОТДАЛЁННЫЕ РЕЗУЛЬТАТЫ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ МЕТАСТАЗОВ САРКОМ ОПОРНО-ДВИГАТЕЛЬНОГО АППАРАТА В ЛЁГКИХ | Стародубцев
1. Ахмедов Б. П. Метастатические опухоли. – М.: Медицина, 1984.
2. Пирогов А. И., Смулевич В. Б. Повторные оперативные вмешательства по поводу метастатических опухолей легких // Хирургия. – 1967. – № 9. – С. 32–35.
3. Поддубный Б. К. Хирургическое лечение солитарных метастатических опухолей легких: Дис. канд. мед. наук. – М., 1969.
4. Самсонов В. А. Метастазы рака почки (по данным аутопсий) // Вопросы онкологии.– 1986.– № 32.– С.78–81.
5. Чиссов В. И., Трахтенберг А. Х., Пикин О. В., Паршин В. Д. Метастатические опухоли легких // М: Гоэтар-Медиа – 2009. – С. 101–109.
6. Antunes M., Bernardo J., Salete M., Prieto D., Eugenio L., Tavares P. Excision of pulmonary metastases of osteogenic sarcoma of the limbs // Eur J Cardiotthorac Surg. – 1999. – Vol.15. –№ 5. – P.592–596.
– P.592–596.
7. Billingsley K. G., Burt M. E., Gara E., Ginsberg R. J., Woodruff J. M. Pulmonary metastases of soft tissue sarcoma: analyses of patterns diseases and postmetastases survival // Ann Surg. – 1999. – Vol. 229. – № 5. – P. 602–610.
8. Bricolli A., Ferrari S., Picci P. et al. Surgical treatment of pulmonary metastases of osteosarcoma. Apropos of 206 operated cases // Ann Chir.–1999.– Vol.53.– № 3.– p.207–214.
9. Bricolli A., Rocca., Ferrari S. et al. Surgery for lung metastases in Ewings sarcoma of bone // Eur J Surg Oncol. –2004. – Vol. 30. – № 1. – P.63–67.
10. Bross & Blumenson // Oncology. – 1976. – V.12. – P.538–542.
11. Ellis P. V., Tattersall M. H., McCaughan B., Stalley P. Osteosarcoma and pulmonary metastases: a 15-year experience from a single institution // Aust N Z J Surg. –1997. – Vol. 67. –№ 9/P.625–629.
12. Greelish J., Friedberg J. Secondary pulmonary malignancy // Surg Clin N Am., 2000.– Vol. 80.– № 2.– P.633–657.
13. van Geel AN., Pastorino U., Jauch KW. et al Surgical treatment of lung metastases: the European Organization for research and treatment of cancer – soft tissue and bone sarcoma group study of 255 patients // Cancer. – 1996/ Vol.77. – № 4. – P.675–682.
14. Muller K. M. Pulmonary metastases. Patological anatomy // Thorac and Cardiovasc. Sur. – 1986.– V.34.– P.115–119.
15. Nielsen O. Role of systemic treatment in adult soft tissue sarcomas // Eur. J. Cancer Suppl.– 2003.– Vol. 1.– № 6.– p. 249–259.
Nielsen O. Role of systemic treatment in adult soft tissue sarcomas // Eur. J. Cancer Suppl.– 2003.– Vol. 1.– № 6.– p. 249–259.
16. Piacenza G., Mantellini E., Cremonte L. G., Salio M. Metastasi Endobronchiali isolate // G. Chir.– 1986.– V.7.– P.1330–1332.
17. Vogt-Myokopl I., Meyer J., Bulzebruck H. Lungmetastasen, Therapieindication und chirurgiche. Munch. med. Wochensschr. – 1986.– V.128.– P.295–300.
18. Goorin AM, Shuster JJ, Baker A, Horowitz ME, Meyer WH, Link MP. Changing pattern of pulmonary metastases with adjuvant chemotherapy in patients with osteosarcoma: results from the multiinstitutional osteosarcoma study. J ClinOncol 1991; 9:600–5.
19. Huth JF, Eilber FR. Patterns of recurrence after resection of osteosarcoma of the extremity. Strategies for treatment of metastases. Arch Surg1989;124:122–6.
20. Meyers PA, Heller G, Healey JH, Huvos A, Applewhite A, Sun M, LaQuagliaM. Osteogenic sarcoma with clinically detectable metastasis at initialpresentation. J ClinOncol 1993;11:449–53.
21. Sternberg DI, Sonett JR. Surgical therapy of lung metastases. SeminOncol2007;34:186–96.
22. van Geel AN, Pastorino U, Jauch KW, Judson IR, van Coevorden F, BuesaJM, Nielsen OS, Boudinet A, Tursz T, Schmitz PI. Surgical treatment of lung metastases: The European Organization for Research and Treatment of Cancer-Soft Tissue and Bone Sarcoma Group study of 255 patients. Cancer1996;77:675–82.
23. van Geel AN, van CF, Blankensteijn JD, Hoekstra HJ, Schuurman B, Bruggink ED, Taat CW, Theunissen EB. Surgical treatment of pulmonary metastases from soft tissue sarcomas: a retrospective study in The Netherlands. J SurgOncol 1994;56:172–7.
van Geel AN, van CF, Blankensteijn JD, Hoekstra HJ, Schuurman B, Bruggink ED, Taat CW, Theunissen EB. Surgical treatment of pulmonary metastases from soft tissue sarcomas: a retrospective study in The Netherlands. J SurgOncol 1994;56:172–7.
24. Billingsley KG, Burt ME, Jara E, Ginsberg RJ, Woodruff JM, Leung DH, Brennan MF. Pulmonary metastases from soft tissue sarcoma: analysis of patterns of diseases and postmetastasis survival. Ann Surg 1999;229:602–10.
25. Casson AG, Putnam JB, Natarajan G, Johnston DA, Mountain C, McMurtreyM, Roth JA. Five-year survival after pulmonary metastasectomy for adult soft tissue sarcoma. Cancer 1992;69:662–8.
26. Bacci G, Briccoli A, Longhi A, Ferrari S, Mercuri M, Faggioli F, Versari M, Picci P. Treatment and outcome of recurrent osteosarcoma: experience atRizzoli in 235 patients initially treated with neoadjuvant chemotherapy. ActaOncol 2005;44:748–55.
27. van VM, Kliffen M, Krestin GP, van Dijke CF. Soft tissue sarcomas at a glance: clinical, histological, and MR imaging features of malignant extremity soft tissue tumors. EurRadiol 2009;19:1499–511.
28. Chen F, Fujinaga T, Sato K, Sonobe M, Shoji T, Sakai H, Miyahara R, BandoT, Okubo K, Hirata T, Date H. Significance of tumor recurrence beforepulmonary metastasis in pulmonary metastasectomy for soft tissue sarcoma.Eur J SurgOncol 2009;35:660–5.
29. Pfannschmidt J, Klode J, Muley T, Dienemann H, Hoffmann H. Pulmonary metastasectomy in patients with soft tissue sarcomas: experiences in 50patients. ThoracCardiovascSurg2006;54:489–92.
30. Tsuchiya H, Kanazawa Y, Abdel-Wanis ME, Asada N, Abe S, Isu K, Sugita T, Tomita K. Effect of timing of pulmonary metastases identification on prognosis of patients with osteosarcoma: the Japanese Musculoskeletal Oncology Group study. J ClinOncol2002;20:3470–7.
31. Kager L, Zoubek A, Potschger U, Kastner U, Flege S, Kempf-Bielack B, Branscheid D, Kotz R, Salzer-Kuntschik M, Winkelmann W, Jundt G, Kabisch H, Reichardt P, Jűrgens H, Gadner H, Bielack SS. Primary metastatic osteosarcoma: presentation and outcome of patients treated on neoadjuvant Cooperative Osteosarcoma Study Group protocols. J ClinOncol2003;21:2011–8.
32. Suzuki M, Iwata T, Ando S, Iida T, Nakajima T, Ishii T, Yonemoto T, TatezakiS, Fujisawa T, Kimura H. Predictors of long-term survival with pulmonary metastasectomy for osteosarcomas and soft tissue sarcomas. J CardiovascSurg (Torino) 2006;47:603–8.
Узелки в легких и доброкачественные опухоли легких: симптомы, причины и лечение
Если вы получили известие о том, что в вашем легком есть что-то «подозрительное», это может быть источником серьезного беспокойства. Первое, что может прийти в голову, — страшное слово: рак. Однако во многих случаях узелок в легких оказывается доброкачественным. Это означает, что — это не рак . Сложная часть — ждать и не знать. Вот информация, которая может немного облегчить ваше ожидание.
Что такое доброкачественные узелки и доброкачественные опухоли легких?
Узелок — это «пятно в легком», видимое на рентгеновском снимке или компьютерной томографии (КТ).Фактически, узелок обнаруживается примерно на одном из каждых 500 рентгеновских снимков грудной клетки. Нормальная легочная ткань окружает это небольшое круглое или овальное твердое разрастание ткани. Это может быть единичный или одиночный легочный узел. Или у вас может быть несколько узелков.
Это может быть единичный или одиночный легочный узел. Или у вас может быть несколько узелков.
Ваш легочный узелок с большей вероятностью будет доброкачественным, если:
- Вы моложе 40 лет.
- Вы не курите.
- В узелке кальций.
- Узелок небольшой.
Доброкачественная опухоль легкого — это ненормальное разрастание ткани, не имеющее цели и не являющееся злокачественным.Доброкачественные опухоли легких могут расти из множества различных структур легких.
Очень важно определить, является ли узелок доброкачественной опухолью или ранней стадией рака. Это потому, что раннее выявление и лечение рака легких может значительно повысить вашу выживаемость.
Каковы симптомы доброкачественных узелков и опухолей легких?
Доброкачественные узелки и опухоли легких обычно не вызывают никаких симптомов. Вот почему они почти всегда случайно обнаруживаются на рентгеновском снимке грудной клетки или компьютерной томографии.Однако они могут вызывать такие симптомы:
Каковы причины доброкачественных узелков и опухолей легких?
Причины появления доброкачественных опухолей и узелков в легких изучены недостаточно. Но в целом они часто возникают в результате таких проблем:
Воспаление от инфекций , например:
- Инфекционный гриб (например, гистоплазмоз, кокцидиоидомикоз, криптококкоз или аспергиллез)
- Туберкулез (ТБ)
- A абсцесс легкого
- Круглая пневмония (редко у взрослых)
Воспаление от неинфекционных причин, таких как:
- Ревматоидный артрит
- Гранулематоз Вегенера
- Саркоидоз
- Врожденные дефекты, такие как киста легкого или другие пороки развития легких.
Продолжение
Вот некоторые из наиболее распространенных типов доброкачественных опухолей легких:
- Гамартомы являются наиболее распространенным типом доброкачественной опухоли легкого и третьей по частоте причиной одиночных легочных узелков.
 Эти твердые, похожие на мрамор опухоли состоят из ткани слизистой оболочки легких, а также таких тканей, как жир и хрящ. Обычно они располагаются на периферии легкого.
Эти твердые, похожие на мрамор опухоли состоят из ткани слизистой оболочки легких, а также таких тканей, как жир и хрящ. Обычно они располагаются на периферии легкого. - Бронхиальные аденомы составляют около половины всех доброкачественных опухолей легких.Это разнообразная группа опухолей, которые возникают из слизистых желез и протоков дыхательного горла или крупных дыхательных путей легкого. Аденома слизистой железы является примером доброкачественной аденомы бронхов.
- Редкие новообразования могут включать хондромы, фибромы или липомы — доброкачественные опухоли, состоящие из соединительной или жировой ткани.
Как диагностируются доброкачественные узелки и опухоли в легких?
Как ваш врач узнает, доброкачественный ли узелок в легких? Помимо сбора анамнеза и медицинского осмотра, ваш врач может просто «наблюдать» за узлом, делая повторные рентгеновские снимки в течение двух лет или дольше, если узел меньше 6 миллиметров и ваш риск невелик.Если узелок остается того же размера в течение как минимум двух лет, он считается доброкачественным. Это потому, что доброкачественные узелки в легких растут медленно, если вообще растут. С другой стороны, раковые узелки в среднем увеличиваются вдвое каждые четыре месяца. Ваш врач может продолжать проверять узелок в легких каждый год в течение пяти лет, чтобы убедиться, что он доброкачественный.
Доброкачественные узелки также имеют более гладкие края и более равномерный цвет, а также более правильную форму, чем злокачественные узелки. В большинстве случаев ваш врач может проверить скорость роста, форму и другие характеристики, такие как кальциноз, на рентгеновском снимке грудной клетки или компьютерной томографии.
Продолжение
Возможно, ваш врач назначит и другие тесты, особенно если узелок изменится по размеру, форме или внешнему виду. Это может быть сделано, чтобы исключить рак или определить первопричину доброкачественного узелка. Они также могут помочь выявить любые осложнения. Вы можете пройти один или несколько из следующих тестов:
Вы можете пройти один или несколько из следующих тестов:
- Анализы крови
- Туберкулиновая кожная проба для проверки на ТБ
- Позитронно-эмиссионная томография (ПЭТ)
- Однофотоэмиссионная КТ (ОФЭКТ)
- Магнитно-резонансная томография (в в редких случаях)
- Биопсия, удаление ткани и исследование под микроскопом для подтверждения доброкачественности опухоли или злокачественной опухоли
Биопсия может быть выполнена с использованием различных методов, таких как аспирация клеток через иглу или удаление их образца с помощью бронхоскопии.Эта процедура позволяет вашему врачу осмотреть ваши дыхательные пути через тонкий прибор для просмотра.
Лечение доброкачественных узелков и опухолей легких
Во многих случаях ваш врач может просто обнаружить подозрительный узелок в легких с помощью множественных рентгеновских снимков грудной клетки в течение нескольких лет. Однако ваш врач может порекомендовать биопсию или удаление всего узла в следующих ситуациях:
- Вы курите, и узелок большой.
- У вас есть симптомы.
- Сканирование предполагает, что узелок может быть злокачественным.
- Узелок разросся.
Продолжение
Биопсию часто можно сделать с небольшими разрезами и недолгим пребыванием в больнице. Если ваш узелок доброкачественный, вам не потребуется никакого дальнейшего лечения, за исключением лечения любых основных проблем или осложнений, связанных с узлом, таких как пневмония или непроходимость.
Если вам требуется инвазивная операция по удалению опухоли, ваш врач может порекомендовать вам один или несколько тестов заранее, чтобы убедиться в вашем здоровье. Они будут включать анализы крови, функциональные тесты почек, печени и легких (легких), а также ЭКГ.
При необходимости операция может включать одну из нескольких процедур. Какая операция вам предстоит, зависит от местоположения и типа вашей опухоли или опухолей. Хирург может удалить небольшой кусочек опухоли, одну или несколько частей доли, одну или несколько долей легкого или все легкое.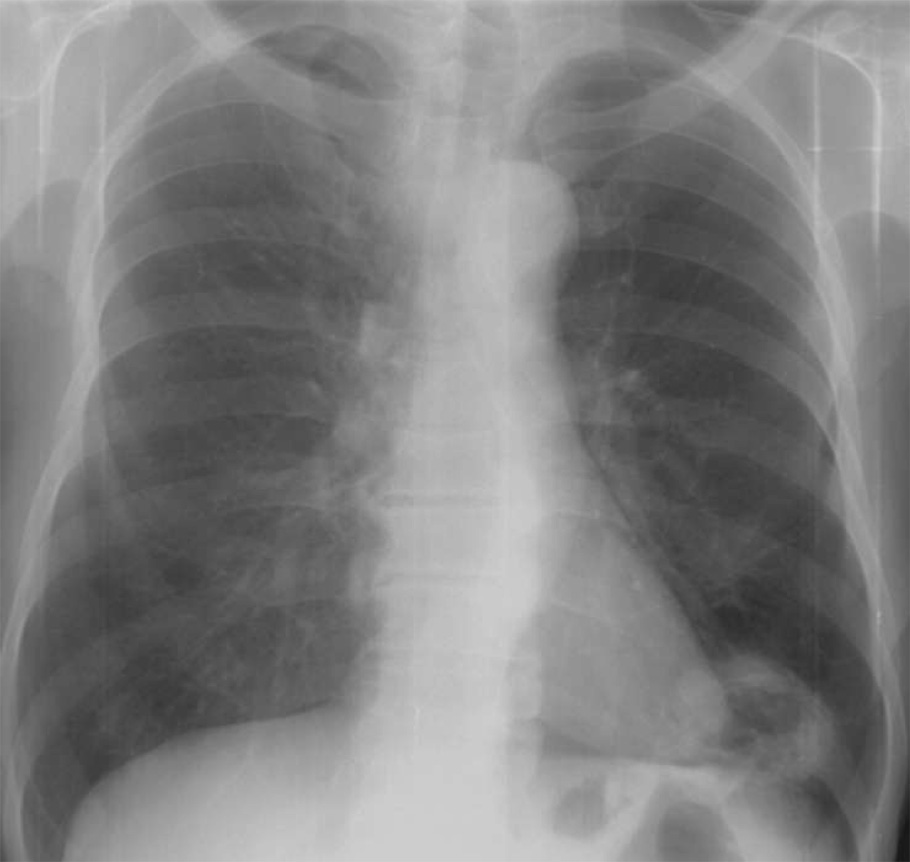 Однако хирург удалит как можно меньше тканей.
Однако хирург удалит как можно меньше тканей.
Узелки и доброкачественные опухоли легких: симптомы, причины и лечение
Если вы получили известие о том, что в вашем легком есть что-то «подозрительное», это может быть источником серьезного беспокойства.Первое, что может прийти в голову, — страшное слово: рак. Однако во многих случаях узелок в легких оказывается доброкачественным. Это означает, что — это не рак . Сложная часть — ждать и не знать. Вот информация, которая может немного облегчить ваше ожидание.
Что такое доброкачественные узелки и доброкачественные опухоли легких?
Узелок — это «пятно в легком», видимое на рентгеновском снимке или компьютерной томографии (КТ). Фактически, узелок обнаруживается примерно на одном из каждых 500 рентгеновских снимков грудной клетки.Нормальная легочная ткань окружает это небольшое круглое или овальное твердое разрастание ткани. Это может быть единичный или одиночный легочный узел. Или у вас может быть несколько узелков.
Ваш легочный узелок с большей вероятностью будет доброкачественным, если:
- Вы моложе 40 лет.
- Вы не курите.
- В узелке кальций.
- Узелок небольшой.
Доброкачественная опухоль легкого — это ненормальное разрастание ткани, не имеющее цели и не являющееся злокачественным.Доброкачественные опухоли легких могут расти из множества различных структур легких.
Очень важно определить, является ли узелок доброкачественной опухолью или ранней стадией рака. Это потому, что раннее выявление и лечение рака легких может значительно повысить вашу выживаемость.
Каковы симптомы доброкачественных узелков и опухолей легких?
Доброкачественные узелки и опухоли легких обычно не вызывают никаких симптомов. Вот почему они почти всегда случайно обнаруживаются на рентгеновском снимке грудной клетки или компьютерной томографии.Однако они могут вызывать такие симптомы:
Каковы причины доброкачественных узелков и опухолей легких?
Причины появления доброкачественных опухолей и узелков в легких изучены недостаточно.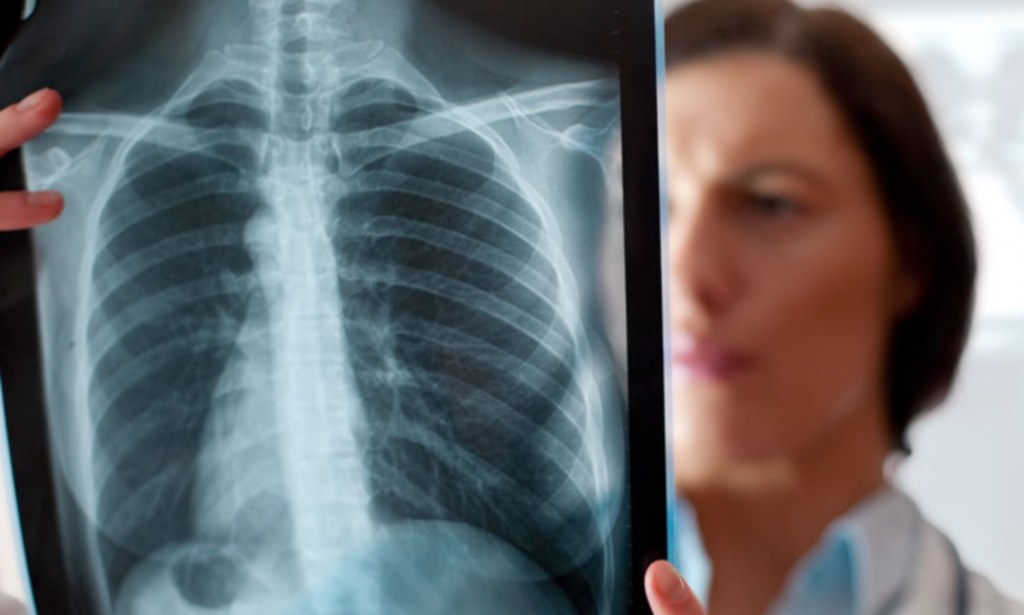 Но в целом они часто возникают в результате таких проблем:
Но в целом они часто возникают в результате таких проблем:
Воспаление от инфекций , например:
- Инфекционный гриб (например, гистоплазмоз, кокцидиоидомикоз, криптококкоз или аспергиллез)
- Туберкулез (ТБ)
- A абсцесс легкого
- Круглая пневмония (редко у взрослых)
Воспаление от неинфекционных причин, таких как:
- Ревматоидный артрит
- Гранулематоз Вегенера
- Саркоидоз
- Врожденные дефекты, такие как киста легкого или другие пороки развития легких.
Продолжение
Вот некоторые из наиболее распространенных типов доброкачественных опухолей легких:
- Гамартомы являются наиболее распространенным типом доброкачественной опухоли легкого и третьей по частоте причиной одиночных легочных узелков. Эти твердые, похожие на мрамор опухоли состоят из ткани слизистой оболочки легких, а также таких тканей, как жир и хрящ. Обычно они располагаются на периферии легкого.
- Бронхиальные аденомы составляют около половины всех доброкачественных опухолей легких.Это разнообразная группа опухолей, которые возникают из слизистых желез и протоков дыхательного горла или крупных дыхательных путей легкого. Аденома слизистой железы является примером доброкачественной аденомы бронхов.
- Редкие новообразования могут включать хондромы, фибромы или липомы — доброкачественные опухоли, состоящие из соединительной или жировой ткани.
Как диагностируются доброкачественные узелки и опухоли в легких?
Как ваш врач узнает, доброкачественный ли узелок в легких? Помимо сбора анамнеза и медицинского осмотра, ваш врач может просто «наблюдать» за узлом, делая повторные рентгеновские снимки в течение двух лет или дольше, если узел меньше 6 миллиметров и ваш риск невелик.Если узелок остается того же размера в течение как минимум двух лет, он считается доброкачественным. Это потому, что доброкачественные узелки в легких растут медленно, если вообще растут.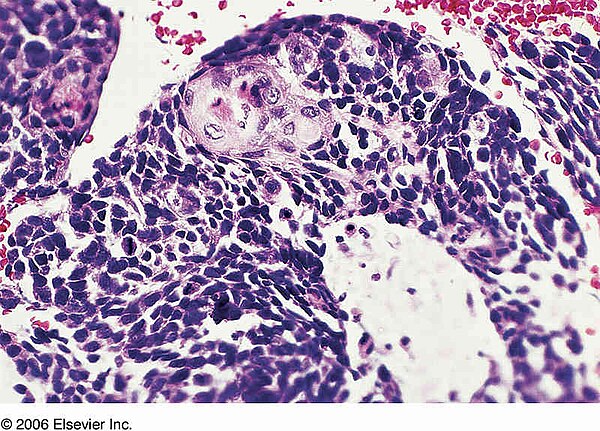 С другой стороны, раковые узелки в среднем увеличиваются вдвое каждые четыре месяца. Ваш врач может продолжать проверять узелок в легких каждый год в течение пяти лет, чтобы убедиться, что он доброкачественный.
С другой стороны, раковые узелки в среднем увеличиваются вдвое каждые четыре месяца. Ваш врач может продолжать проверять узелок в легких каждый год в течение пяти лет, чтобы убедиться, что он доброкачественный.
Доброкачественные узелки также имеют более гладкие края и более равномерный цвет, а также более правильную форму, чем злокачественные узелки. В большинстве случаев ваш врач может проверить скорость роста, форму и другие характеристики, такие как кальциноз, на рентгеновском снимке грудной клетки или компьютерной томографии.
Продолжение
Возможно, ваш врач назначит и другие тесты, особенно если узелок изменится по размеру, форме или внешнему виду. Это может быть сделано, чтобы исключить рак или определить первопричину доброкачественного узелка. Они также могут помочь выявить любые осложнения. Вы можете пройти один или несколько из следующих тестов:
- Анализы крови
- Туберкулиновая кожная проба для проверки на ТБ
- Позитронно-эмиссионная томография (ПЭТ)
- Однофотоэмиссионная КТ (ОФЭКТ)
- Магнитно-резонансная томография (в в редких случаях)
- Биопсия, удаление ткани и исследование под микроскопом для подтверждения доброкачественности опухоли или злокачественной опухоли
Биопсия может быть выполнена с использованием различных методов, таких как аспирация клеток через иглу или удаление их образца с помощью бронхоскопии.Эта процедура позволяет вашему врачу осмотреть ваши дыхательные пути через тонкий прибор для просмотра.
Лечение доброкачественных узелков и опухолей легких
Во многих случаях ваш врач может просто обнаружить подозрительный узелок в легких с помощью множественных рентгеновских снимков грудной клетки в течение нескольких лет. Однако ваш врач может порекомендовать биопсию или удаление всего узла в следующих ситуациях:
- Вы курите, и узелок большой.
- У вас есть симптомы.
- Сканирование предполагает, что узелок может быть злокачественным.

- Узелок разросся.
Продолжение
Биопсию часто можно сделать с небольшими разрезами и недолгим пребыванием в больнице. Если ваш узелок доброкачественный, вам не потребуется никакого дальнейшего лечения, за исключением лечения любых основных проблем или осложнений, связанных с узлом, таких как пневмония или непроходимость.
Если вам требуется инвазивная операция по удалению опухоли, ваш врач может порекомендовать вам один или несколько тестов заранее, чтобы убедиться в вашем здоровье. Они будут включать анализы крови, функциональные тесты почек, печени и легких (легких), а также ЭКГ.
При необходимости операция может включать одну из нескольких процедур. Какая операция вам предстоит, зависит от местоположения и типа вашей опухоли или опухолей. Хирург может удалить небольшой кусочек опухоли, одну или несколько частей доли, одну или несколько долей легкого или все легкое. Однако хирург удалит как можно меньше тканей.
Лечение рака легких
Обзор рака легких
Более чем каждый четвертый из всех диагностированных видов рака поражает легкие, и рак легких остается самой распространенной причиной смерти среди американских мужчин и женщин, связанных с раком.
В то же время вполне может быть, что очень многие виды рака легких можно предотвратить. Вдыхание канцерогенных веществ, таких как табачный дым, может привести к изменениям в легочной ткани вскоре после воздействия — так называемым предраковым изменениям. Тем не менее, сам рак обычно развивается в течение многих лет, и при обнаружении на достаточно ранней стадии его часто можно успешно лечить с помощью различных методов лечения.
начало страницы
Какие у меня варианты лечения?
Оценка перед лечением
- Перед лечением обычно проводится биопсия, чтобы определить, есть ли у пациента рак, и если да, то какого типа.

- Тесты рекомендуются для определения стадии опухоли. Эти тесты обычно включают анализы крови и визуализацию. Визуализация обычно включает компьютерную томографию (КТ) грудной клетки и может включать ПЭТ / КТ и МРТ головного мозга. Варианты лечения и ожидаемые результаты лечения зависят от стадии опухоли.
Обзор вариантов лечения
- Около одной трети пациентов с раком легкого диагностируется локализованное заболевание, которое можно лечить либо хирургической резекцией, либо, если пациент не является кандидатом на полную хирургическую резекцию, радикальной лучевой терапией.Еще у трети пациентов болезнь уже распространилась на лимфатические узлы. В этих случаях наряду с химиотерапией используется лучевая терапия, а иногда и хирургическое вмешательство. У последней трети пациентов могут быть опухоли, которые уже распространились на другие части тела через кровоток, и их обычно лечат химиотерапией, а иногда и лучевой терапией для облегчения симптомов.
- Хирургическая операция с удалением всей доли, в которой расположена опухоль, является основным методом лечения пациентов с раком на ранней стадии, которые находятся в хорошем общем состоянии.Цель операции — полностью удалить все опухолевые клетки и тем самым обеспечить лечение. К сожалению, рак легких, как правило, развивается у курильщиков старше 50 лет, которые очень часто страдают другими заболеваниями легких или серьезными заболеваниями, которые увеличивают риск хирургического вмешательства. Расположение и размер опухоли в легком определяют, насколько обширной должна быть операция. Для надлежащим образом отобранных пациентов может быть рекомендована открытая торакотомия или менее инвазивная торакальная хирургия с использованием видео, или роботизированная торакальная хирургия с использованием меньших разрезов.
- Лобэктомия , удаление всей доли легкого, является общепринятой процедурой удаления рака легкого, когда легкие функционируют нормально.
 Риск смертности составляет менее трех-четырех процентов и, как правило, наиболее высок у пожилых пациентов. Три доли справа (верхняя, средняя и нижняя) и две слева (верхняя и нижняя).
Риск смертности составляет менее трех-четырех процентов и, как правило, наиболее высок у пожилых пациентов. Три доли справа (верхняя, средняя и нижняя) и две слева (верхняя и нижняя). - Поддольная резекция может называться «клиновидная резекция» или «сегментэктомия».«Если функция легких запрещает лобэктомию или опухоль очень мала, может быть выполнена субдольная резекция, при которой небольшой рак, ограниченный ограниченной областью, может быть удален с небольшим участком окружающей легочной ткани. Сублобарная резекция может иметь более высокий риск рецидива. Субдолевые резекции связаны с меньшей потерей функции легких по сравнению с лобэктомией, так как удаляется меньшая часть легкого. Они несут риск операционной смертности 1,4 процента. Не все небольшие опухоли можно удалить с помощью субдолевой резекции.Обычно они находятся глубоко в середине доли.
- Пневмонэктомия : Если все легкое необходимо удалить с помощью «пневмонэктомии», ожидаемый уровень смертности выше (от пяти до восьми процентов), а самые старые пациенты подвергаются наибольшему риску. Это происходит, когда опухоли очень большие или находятся очень близко к крупным кровеносным сосудам (легочной артерии или вене) грудной клетки или главных бронхов.
- Медиастиноскопия: Медиастиноскопия выполняется через небольшой разрез в нижней части шеи над грудиной (грудиной) и используется для отбора проб лимфатических узлов в центральной части грудной клетки (средостение).Альтернативой медиастиноскопии является EBUS.
- Лобэктомия , удаление всей доли легкого, является общепринятой процедурой удаления рака легкого, когда легкие функционируют нормально.
- Лучевая терапия , или радиотерапия , доставляет высокоэнергетические рентгеновские лучи, которые могут разрушить быстро делящиеся раковые клетки или облегчить симптомы или облегчить симптомы. Он имеет множество применений при раке легких:
- Как первичная обработка
- Перед операцией по уменьшению опухоли
- После операции по удалению раковых клеток, оставшихся в обработанной области
- Для лечения рака легких, распространившегося на мозг или другие части тела, или для облегчения симптомов
Помимо воздействия на опухоль, лучевая терапия может помочь облегчить некоторые симптомы, вызванные опухолью, например кровотечение. При использовании в качестве начального лечения вместо хирургического вмешательства лучевая терапия может проводиться отдельно или в сочетании с химиотерапией. Сегодня многие пациенты с небольшим локализованным раком легких, которые не являются кандидатами на операцию, проходят лечение с помощью метода лучевой терапии, известного как стереотаксическая лучевая терапия тела (SBRT). К пациентам, которые не подходят для хирургического вмешательства, относятся пожилые люди, пациенты с хронической сердечной недостаточностью и пациенты, получающие разжижающие кровь препараты, которые подвергают их риску хирургического кровотечения.SBRT включает лечение множеством небольших сфокусированных лучей излучения, отслеживающих опухоль легкого вместе с ее дыхательным движением, обычно за три-пять процедур. Это лечение обеспечивает очень высокие дозы лучевой терапии для лечения рака легких у пациентов, которым операция не подходит. SBRT в основном используется на ранней стадии локализованного заболевания. См. Страницу SRS и SBRT для получения дополнительной информации о SBRT.
При использовании в качестве начального лечения вместо хирургического вмешательства лучевая терапия может проводиться отдельно или в сочетании с химиотерапией. Сегодня многие пациенты с небольшим локализованным раком легких, которые не являются кандидатами на операцию, проходят лечение с помощью метода лучевой терапии, известного как стереотаксическая лучевая терапия тела (SBRT). К пациентам, которые не подходят для хирургического вмешательства, относятся пожилые люди, пациенты с хронической сердечной недостаточностью и пациенты, получающие разжижающие кровь препараты, которые подвергают их риску хирургического кровотечения.SBRT включает лечение множеством небольших сфокусированных лучей излучения, отслеживающих опухоль легкого вместе с ее дыхательным движением, обычно за три-пять процедур. Это лечение обеспечивает очень высокие дозы лучевой терапии для лечения рака легких у пациентов, которым операция не подходит. SBRT в основном используется на ранней стадии локализованного заболевания. См. Страницу SRS и SBRT для получения дополнительной информации о SBRT.
Чаще всего лучевая терапия проводится методом внешнего пучка, при котором пучок рентгеновских лучей направляется непосредственно на опухоль.Лечение проводится в виде серии сеансов или фракций, обычно от шести до семи недель для обычных процедур и от одного до пяти процедур для пациентов, которых можно лечить с помощью SBRT. Для получения более подробной информации см. Внешнюю лучевую терапию (EBT), стр. . Трехмерная конформная лучевая терапия или лучевая терапия с модуляцией интенсивности (IMRT) — довольно новые методы, основанные на трехмерном изображении опухоли, полученном с помощью компьютерной томографии. Это изображение служит мишенью для луча высокой дозы излучения, форма и размер которого могут изменяться в соответствии с опухолью.Этот метод сводит к минимуму облучение близлежащих здоровых тканей легких. См. Страницу лучевой терапии с модуляцией интенсивности (IMRT) для получения дополнительной информации.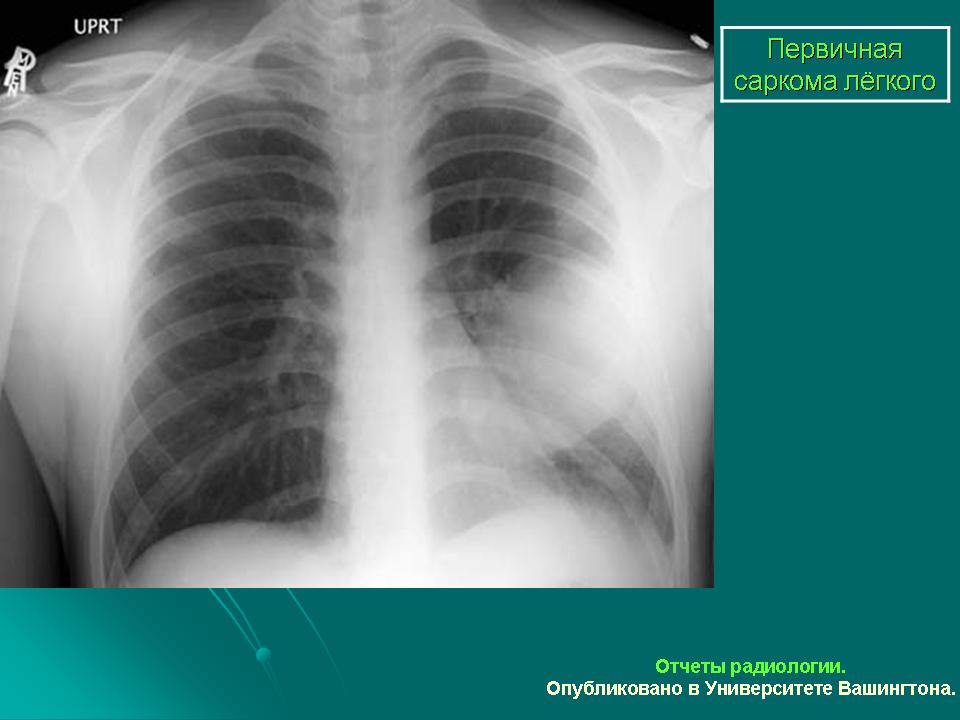
В брахитерапии излучение доставляется непосредственно к месту заболевания. Обычно это достигается с помощью хирургической процедуры, когда после резекции первичной опухоли радиоактивные семена подшиваются к краю хирургической резекции. Кроме того, при обструктивной опухоли в дыхательных путях излучение доставляется к месту обструкции через пластиковую трубку, которая временно вводится в дыхательные пути.Это может помочь облегчить тяжелые симптомы, но не вылечит рак.
Химиотерапия включает препараты, токсичные для раковых клеток. Лекарства обычно вводятся путем прямой инъекции в вену или через катетер, помещенный в крупную вену. Химиотерапия, которую часто назначают после операции по стерилизации микроскопического заболевания, также может замедлить рост опухоли и облегчить симптомы у пациентов, которые не могут перенести операцию. Используются новые биологические агенты, которые могут иметь меньше побочных эффектов, чем традиционная химиотерапия, а в некоторых случаях могут быть столь же эффективными.Это лечение используется на всех стадиях рака легких и может продлить жизнь даже пожилым людям, если у них хорошее общее состояние здоровья. Некоторые химиотерапевтические препараты увеличивают ущерб, наносимый опухолям радиационным лечением раковых клеток. Другие удерживают опухолевые клетки на той стадии, когда они наиболее восприимчивы к лучевой терапии, или нарушают способность раковых клеток восстанавливать себя после курса лучевой терапии. Появляется все больше свидетельств того, что комбинация этих препаратов в сочетании с лучевой терапией более эффективна, чем одна лучевая терапия, но существует значительный риск серьезных побочных эффектов.
Химиотерапия может вызывать серьезные побочные эффекты, такие как тошнота с рвотой и повреждение лейкоцитов, необходимых для борьбы с инфекцией, но теперь есть способы противодействовать и лечить большинство из этих эффектов.
Как зависит метод лечения от типа рака легких?
Существует два основных типа рака легких, которые имеют разные микроскопические проявления:
- Мелкоклеточный рак легкого (SCLC), также называемый овсяноклеточным раком, обычно обнаруживается у активных или бывших курильщиков сигарет.
 Хотя SCLC менее распространен, чем другой тип рака легких, это более агрессивная опухоль, которая с большей вероятностью распространяется на другие участки тела. Химиотерапия — это основа лечения МРЛ. Лучевая терапия часто используется вместе с химиотерапией для лечения опухолей легких, которые не распространились за пределы грудной клетки или других органов. Хирургия обычно не используется при SCLC из-за его тенденции к быстрому распространению. Хотя хирургическое вмешательство редко используется для лечения пациентов с SCLC, иногда оно используется для получения образцов ткани для микроскопического исследования, чтобы определить тип имеющегося рака легких.При мелкоклеточном раке легких после лечения, направленного на заболевание грудной клетки, онколог-радиолог может предложить лучевую терапию, направленную на мозг, даже если там рак не был обнаружен. Это называется профилактическим облучением черепа и проводится для предотвращения образования метастазов рака легких в этом жизненно важном месте.
Хотя SCLC менее распространен, чем другой тип рака легких, это более агрессивная опухоль, которая с большей вероятностью распространяется на другие участки тела. Химиотерапия — это основа лечения МРЛ. Лучевая терапия часто используется вместе с химиотерапией для лечения опухолей легких, которые не распространились за пределы грудной клетки или других органов. Хирургия обычно не используется при SCLC из-за его тенденции к быстрому распространению. Хотя хирургическое вмешательство редко используется для лечения пациентов с SCLC, иногда оно используется для получения образцов ткани для микроскопического исследования, чтобы определить тип имеющегося рака легких.При мелкоклеточном раке легких после лечения, направленного на заболевание грудной клетки, онколог-радиолог может предложить лучевую терапию, направленную на мозг, даже если там рак не был обнаружен. Это называется профилактическим облучением черепа и проводится для предотвращения образования метастазов рака легких в этом жизненно важном месте. - Немелкоклеточный рак легкого (НМРЛ) имеет тенденцию расти медленнее, и ему требуется больше времени, чтобы распространиться за пределы легких. Местные методы лечения, такие как хирургическое вмешательство и / или лучевая терапия, являются основным этапом лечения НМРЛ.Если используется химиотерапия, она часто используется для повышения эффективности хирургического вмешательства или химиотерапии и обычно отличается при НМРЛ от МРЛ. Различные типы химиотерапии могут использоваться для разных типов немелкоклеточного рака легкого.
Как стадия заболевания определяет лечение рака легких?
Мелкоклеточный рак легкого:
- При заболеваниях на ограниченной стадии (ограниченная грудной клеткой) химиотерапия и лучевая терапия используются в качестве лечебного лечения.Облучение обычно начинается одновременно с первой или второй дозой химиотерапии. Шесть недель облучения один раз в день или три недели облучения два раза в день являются обычными режимами облучения.
- На ограниченной стадии онколог-радиолог может предложить лучевую терапию, направленную на головной мозг, даже если рак там не обнаружен.
- При обширной стадии МРЛ только химиотерапия является основой терапии.
- Для обширной стадии онколог-радиолог может рассмотреть возможность лучевой терапии, направленной на мозг, даже если там не было обнаружено рака.Имеются менее убедительные доказательства профилактического облучения мозга, чем при заболевании ограниченной стадии.
- Можно также рассмотреть консолидационное облучение объемных участков исходной опухоли в грудной клетке.
При рецидиве заболевания или заболевании, которое сохраняется после начального лечения, лучевая терапия или химиотерапия могут помочь уменьшить боль или другие симптомы. Лучевая терапия или лазерное лечение могут держать дыхательные пути открытыми, позволяя пациенту дышать более свободно.
Немелкоклеточный рак легкого:
- Ранняя стадия: самые ранние НМРЛ представляют собой очень маленькие опухоли.Для определения основной опухоли могут потребоваться специальные тесты. Опухоли на ранней стадии лечат хирургическими методами стереотаксической или лучевой терапии.
- Продвинутая стадия: комбинированное лечение показано, когда рак распространился на структуры около легких, такие как грудная стенка, диафрагма или лимфатические узлы в грудной клетке. В зависимости от точного местоположения рака лучевая терапия может проводиться отдельно или в сочетании с хирургическим вмешательством и / или химиотерапией.
- Опухоль, распространившаяся на другие части тела: Системная терапия (химиотерапия, таргетная терапия или иммунотерапия) является основным методом лечения пациентов, опухоли которых распространились за пределы грудной клетки или в противоположное легкое.Хирургия обычно не приносит пользы людям, у которых рак распространился за пределы грудной клетки. Химиотерапия продлевает жизнь, и лучевая терапия может использоваться для облегчения симптомов, вызванных опухолью. Иногда операция на головном мозге рекомендуется пациентам с НМРЛ и пациентам, у которых НМРЛ распространился на мозг.
- Любой пациент с раком легких должен рассмотреть возможность участия в клинических испытаниях, чтобы найти более эффективные методы лечения рака легких.
Насколько эффективно лечение неоперабельного рака легких?
Чрезвычайно важно помнить, что «неоперабельный» не означает «неизлечимый», когда речь идет о раке легких.Фактически, на всех стадиях этого заболевания растет число пациентов, получающих нехирургическое лечение. Эффективность лечения зависит от стадии заболевания. На ранней стадии неоперабельного заболевания, которое лечится только лучевой терапией, типичным является контроль местного заболевания. При более запущенной стадии заболевания комбинация химиотерапии и лучевой терапии проводится с лечебной целью. Показатели излечения ниже, но все же возможно, если болезнь распространяется на лимфатические узлы в грудной клетке.Врач или онколог-радиолог может предложить комбинацию химиотерапии и лучевой терапии для активного пациента.
Когда излечение невозможно, рекомендуется паллиативное лечение. Это использование лекарств, химиотерапии, лучевой терапии или других мер для облегчения симптомов рака легких без фактического устранения опухоли. Используемые дозы лучевой терапии меньше, чтобы избежать побочных эффектов. В какой-то момент, если вы и ваш онколог или терапевт согласитесь с тем, что активное лечение больше не рекомендуется, уход в хосписе может обеспечить комфорт и поддержку.Обезболивание — очень важная часть лечения рака легких. Хотя доступно множество эффективных методов лечения и есть устройства для доставки лекарств по запросу без передозировки, многие больные раком все еще не получают адекватного обезболивания. Если потребности пациента четко выражены, лечащие врачи могут лучше предоставить соответствующую помощь.
начало страницы
Что происходит во время лучевой терапии?
Лучевая терапия — это доставка сфокусированных высокоэнергетических рентгеновских лучей (фотонов), гамма-лучей или атомных частиц.Он влияет на быстро делящиеся клетки, такие как раковые клетки, в гораздо большей степени, чем на те, которые не делятся. Большинство видов рака, включая опухоли легких, состоят из клеток, которые делятся быстрее, чем клетки нормальной ткани легких, что дает надежду на то, что опухоль может быть устранена без повреждения окружающих нормальных тканей. Радиотерапия воздействует на генетический материал — или ДНК — в опухолевых клетках, делая невозможным их рост и создание новых раковых клеток. Нормальные клетки тела также могут быть повреждены — хотя и в меньшей степени — но они способны восстанавливать себя и снова нормально функционировать.Ключевая стратегия состоит в том, чтобы давать суточные дозы радиации, достаточно большие, чтобы убить высокий процент быстро делящихся раковых клеток, и в то же время минимизировать повреждение более медленно делящихся нормальных тканевых клеток в той же области.
начало страницы
Каковы возможные побочные эффекты лучевой терапии?
- Большинство пациентов быстро устают после первого сеанса лучевой терапии. Эта усталость постепенно нарастает по мере продолжения лечения и может стать серьезной, серьезно ограничивая способность заниматься обычной повседневной деятельностью.Обычно утомляемость уменьшается через один-два месяца после завершения лучевой терапии. Если вы чувствуете усталость, важно достаточно отдыхать, но в то же время ваш врач может посоветовать вам оставаться как можно более активным.
- У некоторых пациентов наблюдается выпадение волос в области грудной стенки, попадающей в поле излучения. В зависимости от количества доставленного излучения оно может быть временным или постоянным.
- Раздражение кожи является обычным явлением после нескольких недель лучевой терапии.Пораженный участок может быть красным, сухим, болезненным и зудящим. Эта реакция может стать довольно серьезной во время длительного курса лечения. Это помогает поддерживать кожу чистой с помощью мягкого мыла и теплой воды, хорошо сушить ее и избегать очень горячей воды во время купания. Солнцезащитный крем следует использовать, когда кожа в обработанной области подвергается воздействию солнечных лучей. В зоне лечения нельзя использовать парфюмерию, косметику и дезодоранты. После ежедневных процедур можно наносить крем или лосьон без запаха.
- Возможна временная потеря аппетита.
- Эзофагит или воспаление пищевода (трубки, по которой пища передается изо рта в желудок) является обычным явлением, если лучевая терапия направлена на лимфатические узлы в центральной части грудной клетки или если опухоль находится рядом с пищеводом и может быть серьезной. Пищевод очень чувствителен к радиации, и симптомы хуже возникают у пациентов, которые также получают химиотерапию. Эзофагит может затруднить глотание, и некоторым пациентам необходимы обезболивающие или жидкости, вводимые через вену, чтобы пройти полный курс лучевой терапии.Некоторые люди испытывают эзофагит как ощущение шишки или дискомфорта, прежде чем он станет явно болезненным. Некоторые продукты (например, острая или кислая пища или хлеб) ощущаются хуже, чем другие. Важно помнить, что, хотя некоторые продукты могут вызывать боль при глотании, употребление этих продуктов не причинит вреда. Вам следует избегать продуктов, вызывающих боль, примерно в течение одного месяца после последнего дня облучения. Воспаление обычно выходит на плато к концу лечения и у большинства пациентов начинает исчезать в течение двух-трех недель после лечения.
- Воспаление легких, называемое лучевым пневмонитом, может развиться через три-шесть месяцев после окончания лучевой терапии. Он вызывает кашель и одышку, а также жар, но в большинстве случаев не требует специального лечения и проходит через две-четыре недели. Иногда это может произойти раньше и потребовать стероидов и / или кислорода.
начало страницы
Какого рода последующее лечение мне следует ожидать?
Как только курс лучевой терапии подходит к концу, ваш врач обычно хочет видеть вас через четыре-шесть недель, а затем каждые три-шесть месяцев в течение первых двух лет.После этого вас могут посещать каждые шесть месяцев в течение трех лет, а затем один раз в год. Часто ваш врач или онколог-радиолог порекомендует вам пройти компьютерную томографию (КТ) или позитронно-эмиссионную томографию (ПЭТ) примерно через четыре-восемь недель после завершения лечения, когда ожидается наибольший ответ. Эти изображения помогут оценить реакцию и сделают возможным сравнение с изображениями, полученными в ходе последующего наблюдения. Таким образом, осложнения, связанные с лечением, могут быть обнаружены на ранней стадии, и можно будет отличить рецидивирующий рак от рубцов на легких, вызванных лечением высокими дозами радиации.Регулярное получение изображений грудной клетки (как правило, не чаще двух-четырех раз в год) позволяет своевременно обнаруживать рецидивы рака и успешно лечить их повторно.
Помимо рентгена, другие анализы, такие как подсчет клеток крови и бронхоскопия, могут быть рутинной частью последующего обследования. Другие тесты, такие как бронхоскопия, могут проводиться для выявления конкретных симптомов или результатов визуализации грудной клетки. Если новые симптомы развиваются в другой части тела, могут быть проведены тесты для выявления любой потенциальной проблемы.
После лечения опухоль может исчезнуть навсегда (излечиться) или может снова вырасти в области исходной опухоли (рецидив) или может остаться после лечения (остаточная опухоль). У пациентов, у которых был один вид рака, может развиться второй, не связанный с ним первичный рак легких. Это происходит примерно у 3 процентов пациентов в год.
начало страницы
Есть ли новые разработки в лечении моей болезни?
- Менее инвазивные хирургические методы изучаются.Они требуют гораздо меньшего разреза и позволяют пациенту встать в течение нескольких часов после окончания операции.
- В иммунотерапии используются препараты, которые укрепляют иммунную систему пациента, чтобы помочь контролировать рак. Некоторые исследования, но не все, показали лучшую выживаемость при назначении этих препаратов после операции.
- Генная терапия может убивать раковые клетки или замедлять их рост, когда здоровые гены доставляются непосредственно в опухоль легкого.
- Ингибиторы ангиогенеза — это агенты, которые предотвращают образование новых кровеносных сосудов при растущем раке и могут фактически отключить кровоснабжение опухоли.Это остается экспериментальным подходом, но отчасти многообещающим, потому что он вызывает очень мало побочных эффектов.
- Генетическое тестирование проходит оценку с целью выбора пациентов для соответствующего лечения.
- Стереотаксическая лучевая терапия для тела (SBRT) может контролировать опухоли на ранней стадии со скоростью, сравнимой с хирургической.
Клинические испытания
Для получения информации и ресурсов о клинических испытаниях, а также о текущих проводимых клинических испытаниях см .:
начало страницы
Эта страница была просмотрена 17 июля 2019 г.
Вторичные опухоли легких: история вопроса, патофизиология, этиология
Seo JB, Im JG, Goo JM, Chung MJ, Kim MY.Атипичные метастазы в легкие: спектр рентгенологических данных. Рентгенография . 2001 март-апрель. 21 (2): 403-17. [Медлайн]. [Полный текст].
Дишоп М.К., Курувилла С. Первичные и метастатические опухоли легких у детей: обзор и 25-летний опыт работы в крупной детской больнице. Арч Патол Лаб Мед . 2008 июл.132 (7): 1079-103. [Медлайн].
Sato M, Tsujino I, Fukunaga M, Mizumura K, Gon Y, Takahashi N и др.Циклоспорин А индуцирует апоптоз клеток аденокарциномы легких человека через каспазозависимый путь. Противораковое лечение . 2011 июн.31 (6): 2129-34. [Медлайн].
Лу С., Моргенштерн Д., Чанг А., Онн А., Сепези Б., Вапорциан А.А. и др. Рак легкого. Bast RC Jr, Croce CM, Hait WN, Hong WK, Kufe DW, Piccart-Gebhart M, et al, eds. Онкологическая медицина Голландии-Фрея . 9 изд. Хобокен, Нью-Джерси: Джон Уайли и сыновья; 2017. 1011-36.
Varadhachary GR, Abbruzzese JL, Lenzi R.Стратегии диагностики неизвестного первичного рака. Рак . 2004 г. 1. 100 (9): 1776-85. [Медлайн].
Dennis JL, Hvidsten TR, Wit EC, Komorowski J, Bell AK, Downie I, et al. Маркеры аденокарциномы, характерные для очага происхождения: разработка диагностического алгоритма. Clin Cancer Res . 2005 15 мая. 11 (10): 3766-72. [Медлайн].
DeYoung BR, Wick MR. Иммуногистологическая оценка метастатических карцином неизвестного происхождения: алгоритмический подход. Семин Диагноз Патол . 2000 17 августа (3): 184-93. [Медлайн].
Tot T. Цитокератины 20 и 7 в качестве биомаркеров: полезность в различении первичной аденокарциномы от метастатической. евро J Рак . 2002 Апрель, 38 (6): 758-63. [Медлайн].
Kroft LJ, Geleijns J, Mertens BJ, Veldkamp WJ, Zonderland HM, de Roos A. Цифровая рентгенография устройства с зарядовой связью со щелевым сканированием в сравнении с экранно-пленочной рентгенографией AMBER и Bucky для обнаружения имитированных узелков и интерстициального заболевания в фантоме грудной клетки . Радиология . 2004 апр. 231 (1): 156-63. [Медлайн].
Swensen SJ, Aughenbaugh GL, Brown LR, Harms GF, Karsell PR, Gray JE, et al. Расширенная многолучевая рентгенография с эквалайзером: сравнение рабочих характеристик приемника с экранно-пленочной рентгенографией грудной клетки Mayo Clin Proc . 1998 июл.73 (7): 636-41. [Медлайн].
Verschakelen JA, Bogaert J, De Wever W. Компьютерная томография в определении стадии рака легкого. Eur Respir J Suppl .2002 г. 35: 40–48. [Медлайн].
Webb WR, Golden JA. Стратегии визуализации в постановке рака легких. Clin Chest Med . 1991 марта 12 (1): 133-50. [Медлайн].
Cerfolio RJ, Ojha B, Bryant AS, Bass CS, Bartalucci AA, Mountz JM. Роль FDG-PET в стадировании пациентов с немелкоклеточной карциномой. Энн Торак Хирург . 2003 Сентябрь 76 (3): 861-6. [Медлайн].
Graeter TP, Hellwig D, Hoffmann K, Ukena D, Kirsch CM, Schäfers HJ.Стадия средостения лимфатических узлов при подозрении на рак легкого: сравнение позитронно-эмиссионной томографии с F-18-фтордезоксиглюкозой и медиастиноскопии. Энн Торак Хирург . 2003, январь, 75 (1): 231-5; обсуждение 235-6. [Медлайн].
Номори Х, Хорио Х, Наруке Т., Орикаса Х, Ямазаки К., Суэмасу К. Использование коллоида олова технеция-99m для идентификации сторожевых лимфатических узлов при немелкоклеточном раке легкого. J Thorac Cardiovasc Surg . 2002 сентябрь 124 (3): 486-92.[Медлайн].
Голдсмит SJ, Костакоглу Л. Ядерная медицина визуализация рака легких. Радиол Клин Норт Ам . 2000 Май. 38 (3): 511-24. [Медлайн].
Lee JE, Jang JY, Jeong SW, Lee SH, Kim SG, Cha SW и др. Диагностическая ценность внепеченочных метастазов гепатоцеллюлярной карциномы при позитронно-эмиссионной томографии / компьютерной томографии. Мир Дж. Гастроэнтерол . 2012, 21 июня. 18 (23): 2979-87. [Медлайн]. [Полный текст].
De Wever W., Ceyssens S, Mortelmans L, Stroobants S, Marchal G, Bogaert J, et al. Дополнительная ценность ПЭТ-КТ в определении стадии рака легких: сравнение только с КТ, только с ПЭТ и визуальная корреляция ПЭТ и КТ. Евро Радиол . 2007 17 января (1): 23-32. [Медлайн].
Wahl RL, Quint LE, Greenough RL, Meyer CR, White RI, Orringer MB. Стадия немелкоклеточного рака легкого средостения с помощью ПЭТ-ФДГ, КТ и изображений слияния: предварительная проспективная оценка. Радиология . 1994 Май. 191 (2): 371-7. [Медлайн].
Antoch G, Stattaus J, Nemat AT, Marnitz S, Beyer T, Kuehl H и др. Немелкоклеточный рак легкого: двойная модальность ПЭТ / КТ в предоперационной стадии. Радиология . 2003 ноябрь 229 (2): 526-33. [Медлайн].
Cerfolio RJ, Ojha B, Bryant AS, Raghuveer V, Mountz JM, Bartolucci AA. Точность встроенного ПЭТ-КТ по сравнению с отдельным ПЭТ для определения стадии пациентов с немелкоклеточным раком легкого. Энн Торак Хирург . 2004 сентябрь 78 (3): 1017-23; обсуждение 1017-23. [Медлайн].
Shiue CY, Welch MJ. Обновленная информация о радиофармпрепаратах для ПЭТ: жизнь за пределами фтордезоксиглюкозы. Радиол Клин Норт Ам . 2004 ноябрь 42 (6): 1033-53, viii. [Медлайн].
Lacasse Y, Wong E, Guyatt GH, Cook DJ. Трансторакальная пункционная биопсия для диагностики локализованных поражений легких: метаанализ. Грудь . 1999 Октябрь.54 (10): 884-93. [Медлайн].
Schwarz Y, Mehta AC, Ernst A, Herth F, Engel A, Besser D, et al. Электромагнитная навигация при гибкой бронхоскопии. Дыхание . 2003 сентябрь-октябрь. 70 (5): 516-22. [Медлайн].
Ost DE, Ernst A, Lei X, Kovitz KL, Benzaquen S, Diaz-Mendoza J, et al. Возможности диагностики и осложнения бронхоскопии при поражении периферических легких. Результаты реестра AQuIRE. Am J Respir Crit Care Med .2016, 1. 193 (1): 68-77. [Медлайн].
[Рекомендации] Вильманн П., Клементсен П.Ф., Колелла С., Симсен М., Де Лейн П., Дюмонсо Дж. М. и др. Комбинированная эндобронхиальная и пищеводная эндосонография для диагностики и определения стадии рака легких: Рекомендации Европейского общества гастроинтестинальной эндоскопии (ESGE) в сотрудничестве с Европейским респираторным обществом (ERS) и Европейским обществом торакальных хирургов (ESTS). Эндоскопия . 2015 июн. 47 (6): 545-59. [Медлайн].[Полный текст].
Ma XJ, Patel R, Wang X, Salunga R, Murage J, Desai R и др. Молекулярная классификация рака человека с использованием количественного анализа полимеразной цепной реакции с 92 генами в реальном времени. Арч Патол Лаб Мед . 2006 Апрель 130 (4): 465-73. [Медлайн].
Блум Дж., Ян IV, Боулвар Д., Квонг К.Ю., Коппола Д., Эшрих С. и др. Мультиплатформенная, многоузловая классификация опухолей человека на основе микрочипов. Ам Дж. Патол .2004 Январь 164 (1): 9-16. [Медлайн].
Su AI, Welsh JB, Sapinoso LM, Kern SG, Dimitrov P, Lapp H, et al. Молекулярная классификация карцином человека по сигнатурам экспрессии генов. Cancer Res . 2001 15 октября. 61 (20): 7388-93. [Медлайн].
Edge S, Byrd DR, Compton CC, Fritz AG, Greene FL, Trotti A, ред. Руководство по стадированию рака AJCC . 7-е изд. Нью-Йорк: Спрингер; 2010.
Amin MB, Edge SB, Greene FL, Byrd DR, Brookland RK, Washington MK, et al, eds. Руководство по стадированию рака AJCC . 8-е изд. Чикаго: Американский колледж хирургов; 2018.
Perentes JY, Krueger T, Lovis A, Ris HB, Gonzalez M. Торакоскопическая резекция метастазов в легкие: современная практика и результаты. Crit Rev Oncol Hematol . 2015 июл.95 (1): 105-13. [Медлайн].
Cerfolio RJ, McCarty T, Bryant AS. Легочные узелки без визуализации, обнаруженные во время торакотомии для метастазэктомии путем пальпации легких. евро J Cardiothorac Surg . 2009 Май. 35 (5): 786-91; обсуждение 791. [Medline].
Кемп С.Д., Рипли Р.Т., Матур А., Стейнберг С.М., Нгуен Д.М., Фоджо Т. и др. Резекция легкого при метастатической карциноме коры надпочечников: опыт Национального института рака. Энн Торак Хирург . 2011 Октябрь 92 (4): 1195-200. [Медлайн].
[Рекомендации] Перейра П.Л., Масала С., Европейское общество сердечно-сосудистой и интервенционной радиологии (CIRSE).Стандарты практики: рекомендации по термической абляции первичных и вторичных опухолей легких. Cardiovasc Intervent Radiol . 2012 апр. 35 (2): 247-54. [Медлайн].
Ху X, Чжан Ф, Лю XR, Wu YT, Ni YM. Эффективность и потенциальный механизм микроРНК для контролируемой компьютерной томографией чрескожной радиочастотной абляции первичного рака легкого и метастазов в легкие при раке печени. Cell Physiol Biochem . 2014. 33 (5): 1261-71. [Медлайн].
Нельсон Д.Б., Там А.Л., Митчелл К.Г., Райс, округ Колумбия, Мехран Р.Дж., Сепези Б. и др.Местный рецидив после микроволновой абляции злокачественных новообразований легких: систематический обзор. Энн Торак Хирург . 2019 июн.107 (6): 1876-1883. [Медлайн].
Pusceddu C, Sotgia B, Fele RM, Melis L. Чрескожная криоаблация тонкими иглами под контролем КТ у пациентов с первичными и вторичными опухолями легких: предварительный опыт. евро J Радиол . 2013 май. 82 (5): e246-53. [Медлайн].
Luksch R, Tienghi A, Hall KS, Fagioli F, Picci P, Barbieri E, et al.Первичные метастатические семейные опухоли Юинга: результаты исследования ISG / SSG IV Итальянской группы саркомы и Скандинавской группы саркомы, включая миелоаблативную химиотерапию и тотальное облучение легких. Энн Онкол . 2012 23 ноября (11): 2970-6. [Медлайн].
Келекис А.Д., Танос Л., Милона С., Птохис Н., Малагари К., Никита А. и др. Чрескожная радиочастотная абляция опухолей легких расширяемыми игольчатыми электродами: текущее состояние. Евро Радиол . 2006 16 ноября (11): 2471-82.[Медлайн].
Кавамура М., Изуми Ю., Цукада Н., Асакура К., Сугиура Н., Яширо Н. и др. Чрескожная криоаблация малых злокачественных опухолей легких под компьютерно-томографическим контролем с местной анестезией для нехирургических кандидатов. J Thorac Cardiovasc Surg . 2006 май. 131 (5): 1007-13. [Медлайн].
Dupuy DE, DiPetrillo T, Gandhi S, Ready N, Ng T, Donat W. и др. Радиочастотная абляция с последующей традиционной лучевой терапией немелкоклеточного рака легкого I стадии, неоперабельного с медицинской точки зрения. Сундук . 2006 Март 129 (3): 738-45. [Медлайн].
Хаяси К., Ямамото Н., Карубе М., Накадзима М., Цудзи Н., Огава К. и др. Возможность использования углеродно-ионной радиотерапии для повторного облучения локально-рецидивирующих, метастатических или вторичных опухолей легких. Раковые науки . 2018 май. 109 (5): 1562-1569. [Медлайн]. [Полный текст].
Рак легкого | Отделение хирургии Колумбийского университета
Рак легкого — это заболевание, которое возникает в результате неконтролируемого чрезмерного роста клеток в легком.
Ключевая информация
- Рак легкого — одна из самых распространенных форм рака в США
- Рак легкого может быть классифицирован как мелкоклеточный или немелкоклеточный рак легкого
- Минимально инвазивная хирургия может быть вариантом в некоторых случаях рака легких
Рак легкого — одна из наиболее распространенных форм рака в США, ежегодно регистрируется более 200 000 новых случаев. Это основная причина смерти от рака. В основном это поражает людей старше 65 лет и немного чаще встречается у мужчин.
Рак легкого обычно начинается в одном легком. Если его не лечить, он может распространиться на лимфатические узлы или другие части грудной клетки, включая другое легкое. Рак легких также может распространяться по всему телу на кости, мозг, печень или другие органы.
Выживаемость рака легкого зависит от стадии рака — размера и расположения опухоли, распространился ли рак на окружающие лимфатические узлы и распространился ли он на отдаленные участки.
Типы рака легких
Рак легкого можно разделить на мелкоклеточный рак легкого и немелкоклеточный рак легкого (NCSLC) .Из двух категорий наиболее распространенной является NCSLC, на которую приходится почти 90% случаев. Часто он растет и распространяется медленнее, чем мелкоклеточный рак легкого.
Существует три типа немелкоклеточного рака легкого:
- Плоскоклеточный рак
- Аденокарцинома
- Крупноклеточный рак
Мелкоклеточный рак легкого встречается реже, но он растет быстрее и с большей вероятностью распространится на другие органы тела.
Факторы риска рака легких
Курение является самым большим фактором риска рака легких в целом, хотя у некурящих также может развиться мелкоклеточный рак легких.Также известно, что воздействие таких веществ, как асбест, радон, уран, мышьяк и выхлопные газы дизельного топлива, увеличивает риск рака легких. Семейный анамнез рака легких также может быть фактором риска.
Симптомы рака легких
Симптомы рака легких включают:
- Непрекращающийся кашель
- кровохарканье
- одышка
- хриплый голос
- рецидивирующие инфекции дыхательных путей, такие как пневмония
- необычная усталость
- потеря веса
Многие виды рака легких выявляются, когда пациенты проходят рентген грудной клетки или компьютерную томографию по несвязанной причине — простуда, кашель или другие респираторные симптомы.
КТ-скрининг / раннее обнаружение
Раннее обнаружение может значительно улучшить выживаемость. Когда рак легких лечится на самой ранней стадии, показатель излечения приближается к 90%. Современные средства визуализации для диагностики, определения стадии и мониторинга рака легких включают амбулаторное сканирование КТ с высоким разрешением, МРТ , ПЭТ , ПЭТ / КТ и бронхоскопию с электромагнитной навигацией.
Узнайте о программе КТ-скрининга легких в Колумбии »
Компьютерная томография (КТ)
Данные свидетельствуют о том, что у лиц из группы высокого риска КТ (компьютерная томография или компьютерная томография) является лучшим методом выявления рака легких на самой ранней стадии.Большинство случаев рака легких возникает в виде небольшого образования или узелка в легком. Скрининговая компьютерная томография чрезвычайно чувствительна при обнаружении узелков размером от 2 до 3 мм в легких — намного меньше, чем можно увидеть на обычном рентгеновском снимке грудной клетки. Фактически, исследования КТ-скрининга показали, что большинство случаев рака легких, обнаруженных на КТ-сканировании, не могут быть обнаружены на рентгеновском снимке грудной клетки, который проводился одновременно.
Позитронно-эмиссионная томография (ПЭТ)
ПЭТ — это мощный неинвазивный диагностический инструмент, который обнаруживает биохимические изменения в тканях организма.Чтобы обеспечить свой быстрый рост, опухоли потребляют больше глюкозы, чем здоровые ткани. ПЭТ-сканер, который создает цветное изображение химических функций организма, выявляет рак в виде красных «горячих точек» активности. ПЭТ / КТ — это сочетание методов ПЭТ и КТ в одном аппарате. Отдельные снимки ПЭТ и КТ выполняются одновременно, пока пациент остается на месте, и могут быть представлены отдельно или в виде одного перекрывающегося «слитого» изображения.
Эти два метода предоставляют разные типы информации о человеческом теле: в то время как ПЭТ показывает химическую активность, КТ показывает анатомические структуры.Например, ПЭТ-сканирование выявит повышенное потребление глюкозы опухолью, а компьютерная томография — ее физическая масса. Объединенное изображение ПЭТ / КТ представляет собой более надежную альтернативу традиционному параллельному визуальному сравнению изображений ПЭТ и КТ.
Использование ПЭТ-сканирования часто может помочь в разработке планов лечения — от определения необходимости биопсии до определения формы области для лучевой терапии и точного определения операционного поля.
Электромагнитная навигационная бронхоскопия (ENB)
Электромагнитная навигационная бронхоскопия (ENB) позволяет получить компьютерное изображение легких для выявления подозрительных узелков.Эта технология позволяет проводить биопсию узелков, которые в противном случае были бы недоступны, с меньшим риском кровотечения или других осложнений.
Лечение запущенного немалого рака легкого
Для пациентов с немелкоклеточным раком легкого (НМРЛ) химиотерапия на поздних стадиях заболевания стала рутиной с появлением более эффективных лекарств, таких как Гемзар, Навельбин, Таксол и Таксотер. Задача состоит в том, чтобы найти лучшую комбинацию и последовательность этих препаратов, и эта развивающаяся наука активно изучается.
Пациенты с НМРЛ, распространившимся на лимфатические узлы грудной клетки, но которым все еще рекомендовано хирургическое вмешательство, получат пользу от химиотерапии, проводимой до операции.
В дополнение к предоставлению специфических методов лечения рака легких, должны применяться поддерживающие меры для снятия боли, лечения анемии и облегчения других местных симптомов.
Хирургическое лечение рака легких
Лечение рака легких зависит от стадии. Для получения полной информации о стадиях рака обращайтесь в Американский объединенный комитет по раку.
Если рекомендуется операция, тип и объем операции будут зависеть от конкретной стадии, локализации и формы рака у пациента. Чем больше узелок, тем больше нужно удалить легочной ткани. Резекция легкого — это хирургическая процедура по удалению поврежденной или пораженной части легкого или всего легкого. Операция по резекции легкого предлагает лучшую возможность вылечить рак легкого, когда болезнь обнаружена на ранних стадиях.
В некоторых случаях хирургическое удаление может оказаться невозможным.Для тех пациентов, которые являются кандидатами на операцию резекции легкого, доступен ряд подходов. Если возможно, можно использовать малоинвазивные методы, которые уменьшают боль и помогают пациенту выздороветь.
Лобэктомия: видеоассистированная торакоскопическая хирургия (VATS)
В этом малоинвазивном методе хирург делает два или три однодюймовых разреза между ребрами. Камера, прикрепленная к телескопу (который увеличивает поле зрения), помещается в один из разрезов.Камера используется для исследования всей грудной клетки, включая части легкого. Затем хирург вырезает узелок и передает его патологоанатому для исследования под микроскопом. Если узелок злокачественный, хирург может удалить всю долю, в которой выросла опухоль.
Лобэктомия VATS дает пациенту значительные преимущества, поскольку сокращает период восстановления и количество послеоперационных болей, снижая потребность в обезболивающих. Пациенты, перенесшие эту процедуру, возвращаются к нормальной деятельности намного быстрее, чем пациенты, перенесшие более обширную лобэктомию через торакотомический разрез.
Подробнее о торакоскопической хирургии с видеосъемкой (VATS).
Лобэктомия: торакотомия
После неоадъювантной терапии или при очень больших размерах опухоли может потребоваться торакотомия. Между ребрами делается торакотомический разрез. Он простирается со стороны пациента, под мышкой и вверх по спине. Разрез простирается от восьми до девяти дюймов. Это требует разделения некоторых мышц грудной клетки и разведения ребер. Если для удаления рака легкого требуется торакотомический разрез, наши хирурги могут выполнить операцию с гораздо меньшим дискомфортом для пациента, чем это было возможно десять лет назад.Всем нашим пациентам ставят эпидуральный катетер, через который мы вводим послеоперационные обезболивающие. Обезболивание с помощью эпидуральной анестезии достаточно эффективно. Пациенты могут вставать с постели в первый день после операции и при необходимости ходить.
Пневмонэктомия
Иногда, если рак довольно большой или находится в самом центре легкого — близко к тому месту, где главный бронх отделяется от трахеи, — единственный способ полностью удалить рак — удалить все легкое.Эта процедура называется пневмонэктомией. Когда вы удаляете все легкое, вы, очевидно, удаляете и более жизнеспособную легочную ткань. Следовательно, с этой процедурой связана более высокая частота осложнений. По этой причине пневмонэктомия обычно не выполняется, за исключением случаев, когда это абсолютно необходимо для лечения рака.
Следующие шаги
Если вам нужна помощь при раке легких, мы готовы помочь. Люди, которые обращаются к нам для лечения рака легких, получают выгоду от объединенных ресурсов команды экспертов в различных областях.Каждую неделю наши торакальные хирурги, пульмонологи, медицинские онкологи, онкологи-радиологи, лучевые терапевты и патологи встречаются, чтобы обсудить обновления и планы для каждого из наших пациентов. Благодаря такому командному подходу пациентам предлагается индивидуальное лечение, которое может включать предоперационную или послеоперационную мультимодальную терапию, например, комбинацию химиотерапии и лучевой терапии в сочетании с хирургическим вмешательством. Было показано, что такие комплексные усилия улучшают выживаемость от рака легких.
Позвоните по телефону (212) 305-3408 для существующих пациентов, (212) 304-7535 для новых пациентов или запросите онлайн-запись, чтобы начать работу сегодня.
В сотрудничестве с отделением онкологии мы также предлагаем множество инновационных клинических исследований для пациентов со всеми стадиями рака легких. Некоторые из этих испытаний проверяют новейшие препараты против рака легких и проводятся только в Медицинском центре Ирвинга Колумбийского университета. Узнайте больше о клинических исследованиях рака легких ».
Сопутствующие услуги
Связанные темы
Новая классификация опухолей легких ВОЗ
Мин С. Цао, доктор медицинских наук, FRCPC, онкологического центра принцессы Маргарет, Торонто, выступил с пленарной презентацией во время Всемирной конференции по раку легких 2020 года, в которой изложил основные обновления, содержащиеся в 5-м издании Книга Всемирной организации здравоохранения (ВОЗ) по классификации опухолей грудной клетки . В новой книге реализовано много новых форматов, в ней участвуют новые авторы и редакторы.Новые разделы, которые будут особенно полезны патологам в их клинической практике, включают «Диагностическая молекулярная патология» и «Основные или желательные диагностические критерии».
Доктор Цао сказал, что по сравнению с предыдущим изданием, опубликованным в 2015 году, в классификацию 2020 года было добавлено несколько новых типов опухолей; все это опухоли с низкой заболеваемостью. Он кратко описал характерные особенности этих новых опухолевых образований.
Бронхиолярная аденома (реснитчатая муконодулярная папиллярная опухоль) — доброкачественная опухоль, которая обычно показывает перфорацию двух слоев мягких клеток вдоль бронхиолярного эпителия.Интересно, что эти опухоли могут содержать драйверные мутации, обнаруженные при раке легких. «Важно отличать бронхиолярную аденому от лепидной аденокарциномы или аденокарциномы in situ на основе морфологии перфорации двухслойных эпителиальных клеток», — сказал он.
Грудная недифференцированная опухоль с дефицитом SMARCA4 — это высокозлокачественная недифференцированная опухоль легких с инвазиями плевральной стенки грудной клетки или без них. Этот тип рака легких характеризуется потерей экспрессии SMARCA-4, что может быть обнаружено с помощью иммуногистохимии (ИГХ).Ген SMARCA-4 участвует в ремоделировании хроматина, и потеря экспрессии в основном происходит из-за мутации.
Мезотелиома in situ — это преинвазивная однослойная поверхностная пролиферация неопластических мезотелиальных клеток. Это заболевание обнаруживается у пациентов с невылечивающимся плевральным выпотом, с тяжелым воздействием асбеста, предшествующей лучевой терапией или с семейным анамнезом мезотелиомы. Поражение может быть диагностировано только путем демонстрации потери экспрессии BAP1 и / или MTAP в результате гомозиготной делеции IHC и / или CDKN2A с помощью флуоресцентной гибридизации in situ (FISH).Важно отметить, что это заболевание имеет высокий потенциал развития в инвазивную эпителиоидную мезотелиому, злокачественную версию.
Доктор Цао также отмечает новые важные обновления в новой классификационной книге по некоторым видам рака грудной клетки.
Подтипирование инвазивной немуцинозной аденокарциномы на основе преобладающей гистологической картины в настоящее время является стандартом для классификации и диагностики аденокарциномы легких. Эти подтипы имеют прогностическое значение. Опухоли с преобладанием лепидов имеют лучший прогноз, опухоли с преобладанием папиллярных или ацинарных тканей имеют промежуточный прогноз, а микропапиллярные / солидные опухоли имеют плохой прогноз; последнее может прогнозировать улучшение выживаемости от адъювантной химиотерапии.Однако есть дополнительные особенности опухоли, которые традиционно были связаны с прогнозом, включая ядерную и цитологическую степень, митоз, некроз и, в последнее время, распространение через воздушное пространство (STAS). В исследовании, проведенном Комитетом по патологии IASLC, было обнаружено, что наличие 20% или более вторичных паттернов высокой степени (микропапиллярные, твердые и сложные железы) поверх первичного паттерна может увеличить риск рецидива или смерти у пациента. обучающая когорта и независимо проверена на 2 дополнительных когортах пациентов.На основе этих результатов была предложена система дифференциации IASLC для инвазивной немуцинозной аденокарциномы легких, которая была включена в новую книгу классификации ВОЗ. Эта система классификации, по-видимому, улучшает стратификацию прогноза у пациентов с немуцинозной аденокарциномой на ранней стадии по сравнению с прогнозированием, основанным только на преобладающем паттерне. Кроме того, система оценки IASLC может увеличить процент пациентов (с опухолями 3 степени), которым потенциально может помочь адъювантная химиотерапия, хотя для этого требуются дополнительные подтверждающие данные.
Глава о мезотелиоме в Классификационной книге ВОЗ 2021 года содержит более подробное описание заболевания, включая различные гистологические или цитологические особенности и новую систему классификации опухоли; некоторые из них имеют прогностическое значение. В главе также даются рекомендации о том, что следует включать в патологическую отчетность по образцам биопсии или резекции для этой опухоли.
Пятое издание Торакальной классификации опухолей грудной клетки ВОЗ станет доступно весной 2021 года.Новая книга будет доступна по онлайн-подписке, которая включает доступ ко всем изображениям слайдов.
Артикул:
- Морейра АЛ. Ocampo PSS, Xia Y, et al. Система оценки инвазивной аденокарциномы легких: предложение Комитета по изучению патологии рака легких Международной ассоциации. J Thorac Oncol. 2020; 15 (10): 1599-1610.
Определите общие признаки и симптомы рака легких
Признаки и симптомы рака легких редко проявляются до тех пор, пока болезнь не перейдет на позднюю стадию.В легких мало нервных окончаний, а это означает, что опухоли могут расти, не вызывая боли или других симптомов рака легких. Даже когда другие формы лучевой терапии не рекомендуются, CyberKnife все равно может быть вариантом. CyberKnife обеспечивает высокоточную дозировку излучения в комфортных условиях лечения с минимальными побочными эффектами.
CyberKnife: для неоперабельных или рецидивирующих опухолей легких
Несмотря на то, что CyberKnife звучит как хирургическая процедура, на самом деле это нехирургический, неинвазивный и чрезвычайно точный направленный пучок излучения, предназначенный для уничтожения раковых клеток в источнике.CyberKnife предназначен для пациентов с неоперабельными опухолями легких, рецидивирующими опухолями, которые больше не могут получать стандартное облучение, или в качестве альтернативы инвазивной хирургии. Система CyberKnife — это специализированная роботизированная система лучевой терапии, управляемая сложным программным обеспечением, которая нацелена на несколько лучевых лучей с невероятной точностью.
При лечении рака легких с помощью лучевой терапии врачи сталкиваются с проблемой воздействия только на вредные раковые клетки из-за небольшого движения, возникающего во время дыхания пациента.Система CyberKnife способна решить эту проблему благодаря эксклюзивному программному обеспечению для отслеживания опухолей, которое продолжает отображать место лечения в режиме реального времени. Система способна адаптироваться к ритму дыхания пациента и направлять точечный луч излучения только на рак.
На самом деле, лучи настолько точны — с точностью до субмиллиметра — что они убивают клетки рака легких, в то же время нанося вред очень немногим окружающим здоровым клеткам. Система робототехники перемещается вокруг пациента, позволяя лучам излучения нацеливаться на раковые клетки практически под любым углом.Система CyberKnife защищает здоровые ткани и с высокой точностью уничтожает раковые клетки.
При стандартной операции на легких всегда существует риск кровотечения или инфекции. Кроме того, вы переживаете длительный период восстановления. С другой стороны, радиохирургия CyberKnife в Лос-Анджелесе стоит:
.
- Чрезвычайно точное облучение, направленное на опухоль.
- Сведение к минимуму побочных эффектов и улучшение качества жизни пациента.
- Быстрое лечение, требующее всего от одной до пяти коротких процедур — менее чем за неделю.
- Полностью неинвазивное, безоперационное и безболезненное лечение.
- Не требует анестезии.
- Процедуры проходят в комфортных амбулаторных условиях.
Поскольку нет разреза или анестезии, CyberKnife снижает риск хирургических осложнений. Хотя лечение оставляет пациентов с минимальными побочными эффектами, некоторые действительно испытывают усталость после операции.
Каковы признаки и симптомы рака легких?
Наиболее частые симптомы рака легких как у женщин, так и у мужчин включают:
- Новый кашель или переход в хронический
- Кровь, которая появляется при кашле
- Свистящее дыхание и одышка
- Боль в груди
- Охриплость
- Необъяснимая потеря веса
- Головные боли
- Боль в костях
Если вы испытываете какие-либо из этих ранних признаков и симптомов рака легких, как можно скорее обратитесь к врачу.
Кого следует обследовать на рак легких?
Так как курение является самым большим фактором риска рака легких, Американская ассоциация легких рекомендует курильщикам в возрасте от 55 до 74 лет спрашивать своих врачей о проведении компьютерной томографии с низкой дозой облучения для выявления рака. Курильщики, у которых более 30 паковок лет — курят по пачке в день в течение 30 лет или по две пачки в день в течение 15 лет — подвергаются значительному риску и должны пройти обследование на рак легких.
Люди, работающие на определенных профессиях, связанных с повышенным риском, также могут быть подвержены риску рака легких.Например, если вы работали в строительной отрасли, судостроении или производстве асбеста, у вас может быть повышенный риск рака легких, называемого мезотелиомой, из-за контакта с волокнами асбеста. Кроме того, если вы жили в доме с положительным результатом на радон, поговорите со своим врачом о скрининге.
Лечение рака легких CyberKnife
Перед первым лечением врачи проведут компьютерную томографию, чтобы определить точное местоположение вашей опухоли. Затем сканирование загружается в аппарат CyberKnife, позволяя программному обеспечению начать отображение вашего индивидуального пути лечения.Наши специалисты по онкологии — сертифицированные радиационные онкологи и медицинские физики — будут работать вместе, чтобы определить наиболее безопасную и эффективную дозу облучения.
Во время лечения вы будете лежать на кушетке, пока аппарат CyberKnife тихо перемещается вокруг вас, используя большие дозы точечных лучей радиации, нацеленных только на рак. Лечение занимает менее часа, и вам нужно прийти в онкологический центр Лос-Анджелеса всего на один-пять сеансов.
Начни сегодня
Независимо от того, обнаружили ли вы рак легких или лечитесь уже долгое время, онколог может порекомендовать лечение CyberKnife отдельно или в сочетании с другими методами лечения.Начните с того, что свяжитесь с нашим центром, чтобы назначить консультацию с одним из наших специалистов о том, подходит ли вам CyberKnife.

 Эти твердые, похожие на мрамор опухоли состоят из ткани слизистой оболочки легких, а также таких тканей, как жир и хрящ. Обычно они располагаются на периферии легкого.
Эти твердые, похожие на мрамор опухоли состоят из ткани слизистой оболочки легких, а также таких тканей, как жир и хрящ. Обычно они располагаются на периферии легкого.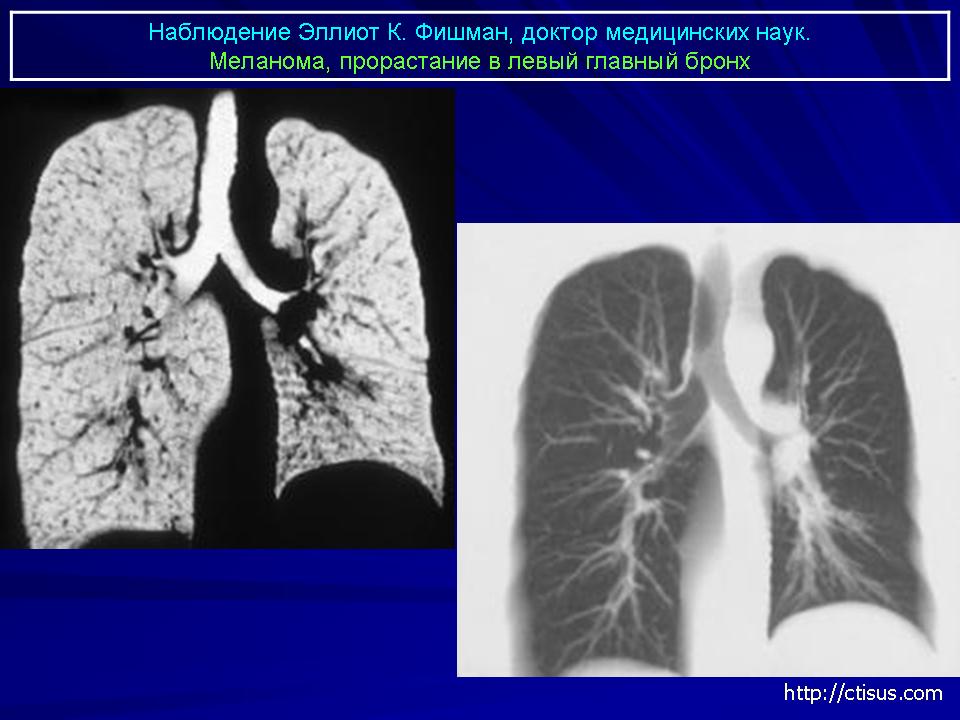

 Риск смертности составляет менее трех-четырех процентов и, как правило, наиболее высок у пожилых пациентов. Три доли справа (верхняя, средняя и нижняя) и две слева (верхняя и нижняя).
Риск смертности составляет менее трех-четырех процентов и, как правило, наиболее высок у пожилых пациентов. Три доли справа (верхняя, средняя и нижняя) и две слева (верхняя и нижняя).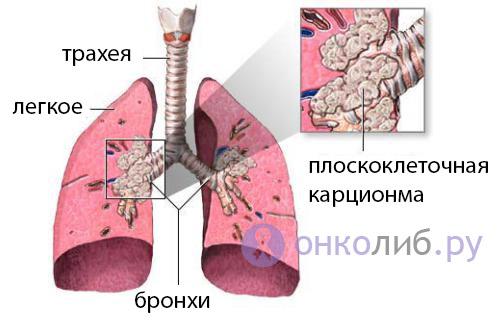 Хотя SCLC менее распространен, чем другой тип рака легких, это более агрессивная опухоль, которая с большей вероятностью распространяется на другие участки тела. Химиотерапия — это основа лечения МРЛ. Лучевая терапия часто используется вместе с химиотерапией для лечения опухолей легких, которые не распространились за пределы грудной клетки или других органов. Хирургия обычно не используется при SCLC из-за его тенденции к быстрому распространению. Хотя хирургическое вмешательство редко используется для лечения пациентов с SCLC, иногда оно используется для получения образцов ткани для микроскопического исследования, чтобы определить тип имеющегося рака легких.При мелкоклеточном раке легких после лечения, направленного на заболевание грудной клетки, онколог-радиолог может предложить лучевую терапию, направленную на мозг, даже если там рак не был обнаружен. Это называется профилактическим облучением черепа и проводится для предотвращения образования метастазов рака легких в этом жизненно важном месте.
Хотя SCLC менее распространен, чем другой тип рака легких, это более агрессивная опухоль, которая с большей вероятностью распространяется на другие участки тела. Химиотерапия — это основа лечения МРЛ. Лучевая терапия часто используется вместе с химиотерапией для лечения опухолей легких, которые не распространились за пределы грудной клетки или других органов. Хирургия обычно не используется при SCLC из-за его тенденции к быстрому распространению. Хотя хирургическое вмешательство редко используется для лечения пациентов с SCLC, иногда оно используется для получения образцов ткани для микроскопического исследования, чтобы определить тип имеющегося рака легких.При мелкоклеточном раке легких после лечения, направленного на заболевание грудной клетки, онколог-радиолог может предложить лучевую терапию, направленную на мозг, даже если там рак не был обнаружен. Это называется профилактическим облучением черепа и проводится для предотвращения образования метастазов рака легких в этом жизненно важном месте.