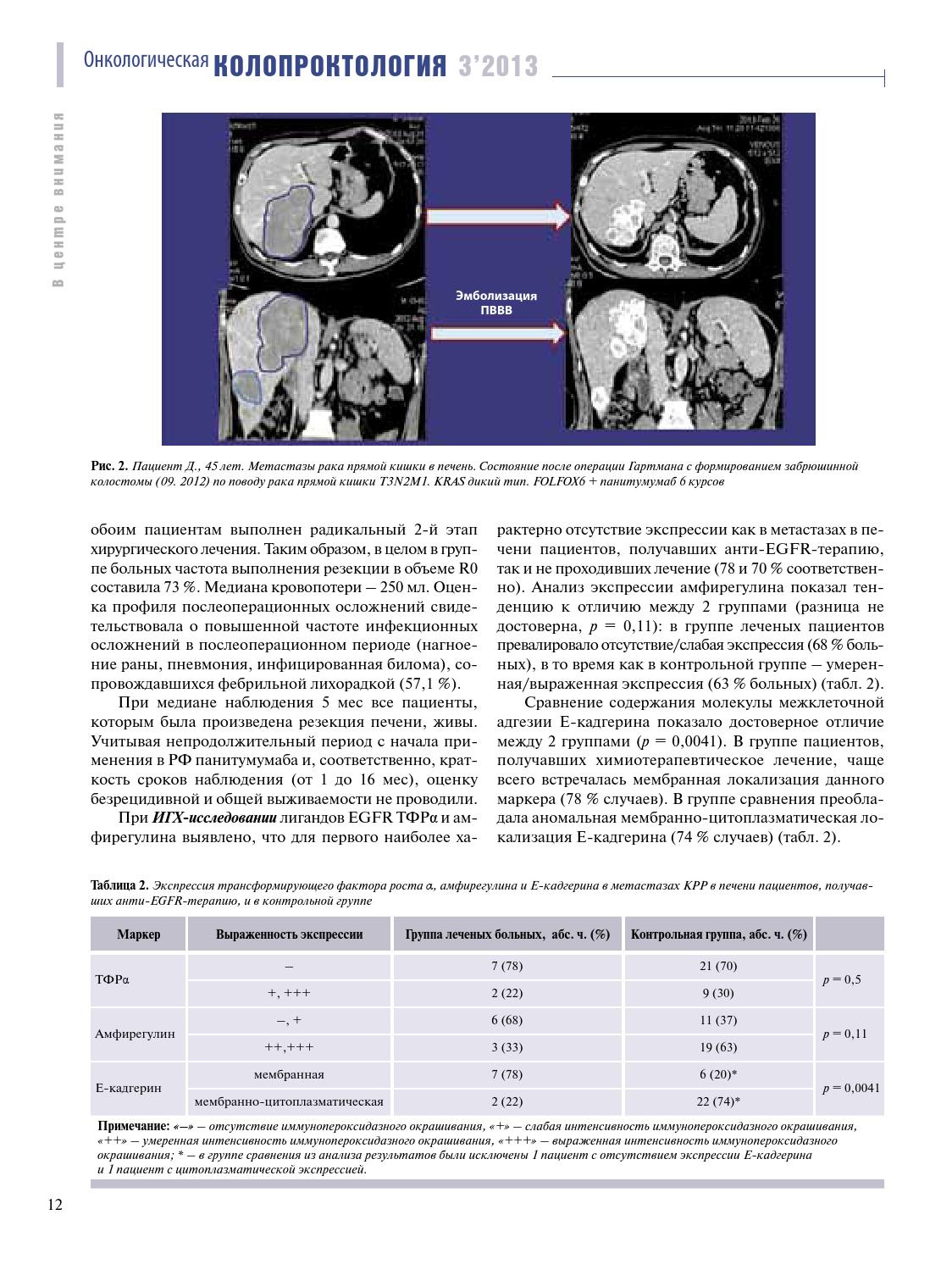
Рецидив рака прямой кишки после операции
Письмо генеральному директору
Онлайн оплата
RU
- EN
AA
+7 (495) 151-14-53
+7 (861) 238-70-54
8 800 100 14 98
+7 (812) 604-77-92
пн.-сб. с 9.00 до 21.00
работаем круглосуточно 24/7
работаем круглосуточно 24/7
пн.-пт. с 9.00 до 18.00
пн.-пт. с 9.00 до 18.00
м. Тульская, Москва
Духовской пер., д.22-б
Северная ул, 315
Большая Печерская ул, 26
Межевой канал, д.4, лит. А
Солнечная ул, 59
Клиника в Москве
- Клиника в Краснодаре
- Клиника в Санкт-Петербурге
- Представительство
в Нижнем Новгороде - Представительство
в Самаре
Работаем в штатном режиме. Соблюдаем меры безопасности. Принимаем пациентов со всей России.
- Связаться с нами
- О компании
- Наша клиника
- Отзывы
- Видео
- Мероприятия
- Качество лечения
- Новости клиники
- Менеджмент
- Врачи
- Вакансии
- Фотогалерея
- Оборудование
- 3D-тур по клинике
- Цены
- Вопросы и ответы
- 9 мифов о раке
- Можно ли заразиться раком?
- Рак и беременность
- Тревожные симптомы онкологии
- Лечение за рубежом
- Клиники
- Клиника в Москве
- Клиника в Краснодаре
- Клиника в Санкт-Петербурге
- Услуги
- Экстренная госпитализация
- Поликлиника
- Метастазы при раке
- Метастазы в головном мозге
- Метастазы в печень
- Метастазы в позвоночнике
- Метастазы в лёгких
- Метастазы рака молочной железы в плевру
- Уточнение диагноза
- Пересмотр стекол
- Консультация химиотерапевта
- Метастазы при раке
- Химиотерапия
- HIPEC
- Инфузионные порт-системы
- Таргетная терапия
- Внутрибрюшинная химиотерапия
- Последствия химиотерапии
- Волосы и химиотерапия
- Химиотерапия и сердце
- Химиотерапия и температура
- Химиотерапия рака молочной железы
- Химиотерапия рака шейки матки
- Химиотерапия при раке матки
- Химиотерапия при раке печени
- Химиотерапия рака желудка
- Химиотерапия рака яичников
- Химиотерапия при раке легкого
- Стоимость курса химиотерапии
- Чувствительность к химиопрепаратам
- Интервенционная хирургия
- Химиоэмболизация
- Химиоэмболизация печени
- Механическая желтуха
- Кава-фильтры
- Нефростомы в онкологии
- Эмболизация артерий простаты
- Стентирование мочеточника
- Радиочастотная абляция сердца
- Отделение реанимации
- Общая хирургия
- Грыжи передней брюшной стенки
- Острая кишечная непроходимость
- Операции при раке желудка
- Операции в лечении рака кишки
- Операции при раке матки
- Операции при раке желчного пузыря
- Операции при раке яичников
- Операции в онкологии
- Операции при раке прямой кишки
- Резекция толстой кишки
- Операции при раке печени
- Операции при метастазах
- Операции при меланоме
- Онкологический центр
- Условия пребывания
- Правила внутреннего распорядка
- Отделение эндоскопии
- Гастроскопия и скрининг рака желудка
- Эндоскопическое лечение рака желудка
- Эндосонография, эндоузи
- Эндоскопическое стентирование
- Стентирование трахеи
- Стентирование пищевода
- Стентирование желчных протоков
- Стентирование мочеточника
- Паллиативная помощь
- Переливание крови
- Плазмаферез
- 4-я стадия рака
- Паллиативная помощь
- Центр управления болью
- Обезболивание при раке
- Обезболивание при 4 стадии рака
- Врачи
- Онкологи
- Онкологи-маммологи
- Хирурги-онкологи
- Онкологи-гинекологи
- Дерматологи-онкологи
- Онкологи-урологи
- Химиотерапевты
- Онкогематологи
- Пациентам
- Оплата услуг онлайн
- Программы
- Полезная информация для пациентов
Рак прямой кишки: сколько живут после операции
Как правило, медицина для борьбы с онкологией подключает несколько методов терапии, но операция при раке прямой кишки является основным способом лечения. Удаление опухоли считается наиболее результативным, хотя перед оперативным вмешательством иногда назначают специальные препараты для химиотерапии.
Удаление опухоли считается наиболее результативным, хотя перед оперативным вмешательством иногда назначают специальные препараты для химиотерапии.
Показания к оперированию
В связи с возможным развитием метастаз при обнаружении злокачественного образования, контролируется не только зона поражения, но и все пространство, заполненное брюшными органами. Лечение нехирургическими методами не всегда приносит положительный результат, образование может увеличиваться. Возникает риск развития непроходимости, что жизненно опасно для человека. Когда осложнения вызывают серьезные опасения для жизни человека, становится вопрос об оперативном вмешательстве. Кроме того, если есть противопоказания к полному удалению опухоли, избежать негативных последствий, путем уменьшения образования в размере поможет операция на прямой кишке.
Вернуться к оглавлению
Виды оперативного вмешательства
Кишечник расположен в труднодоступном месте, где близко сконцентрированы артерии и волокна нервов, поэтому все операции на прямом кишечнике отличаются повышенной сложностью. Методы оперативного вмешательства можно разделить на две основные группы:
Методы оперативного вмешательства можно разделить на две основные группы:
В зависимости от локализации и стадии протекания заболевания, специалист определяет ход операционного вмешательства.
- Паллиативные. Менее травматичные, нерадикальные и органосохраняющие виды хирургического вмешательства. Проводятся в случае возникновения осложнений, несущих угрозу жизни и здоровью больного. Во время операции опухолевые ткани могут полностью не удаляться.
- Радикальные. Сложная процедура, которая направлена на полное удаление злокачественного образования и рядом расположенных тканей. Врачи разработали несколько способов резекции:
- Внутрибрюшная. Удаляется значительный объем конечной части ободочной кишки и проксимальная область прямой, околопрямокишечная клетчатка и прилегающие лимфатические узлы. Сфинктер, кровеносные сосуды и нервные волокна, которые принимают участие в выводе мочи и половой функции, сохраняются.
- Низкая передняя. Злокачественное образование вместе с близлежащими тканями удаляется через незначительный разрез в брюшной стенке.
 Сфинктер и наружное отверстие сохраняются.
Сфинктер и наружное отверстие сохраняются. - Операция Кеню-Майлса. Брюшно-промежностная ампутация направлена на резекцию прямой кишки и соседних тканей. Создается колостома, которая выводится через стенку брюшины. Проводится крайне редко, поскольку врачи стараются сохранить функции кишечника.
- Тазовая экзентерация. Проводится в ситуации, когда злокачественный процесс перешел на соседние внутренние органы.
Вернуться к оглавлению
Послеоперационное восстановление
После проведения хирургической процедуры пациенту запрещено садится и вставать первые двое суток.
Реабилитация после операции требует особенного подхода. Начинается период восстановления еще в операционной, когда под наблюдением проводится купирование возможных осложнений и остановка кровотечения. Впоследствии самыми сложными оказываются первые 2 суток. В это время нужно отслеживать работу органов сердечно-сосудистой и дыхательной систем, а также контролировать функции пищеварительного тракта.
Через 2 дня больному могут разрешить садиться и на 3—4 сутки вставать. Пренебрегать этой рекомендацией не стоит, для скорейшего восстановления физическая активность по мере сил необходима. Важным пунктом в программе реабилитации уделяется питанию. Еда должна легко усваиваться и способствовать нормализации стула. Для снижения давления на брюшную полость и поддержания живота, больному рекомендуется ношение бандажа.
Вернуться к оглавлению
Лечение после операции
Не в каждом случае операция может прекратить развитие онкологии, не всегда получается полностью извлечь образование. К сожалению, рост злокачественной опухоли может возобновиться. Поэтому после хирургического вмешательства назначается курс приема химиопрепаратов или лучевой терапии. Для снятия послеоперационных болевых ощущений больному приписывают болеутоляющие и специальные препараты для стимуляции пищеварительных процессов.
Вернуться к оглавлению
Образ жизни
Полное восстановление организма требует времени и придерживания специальной диеты, в которую входит и соблюдение водного режима.![]()
Привычное до хирургических манипуляций существование после операции меняется кардинально. Значительно изменяется работа кишечника. Человека могут беспокоить расстройства, вздутие, недержание. Со временем произойдет полное восстановление, но пока человек должен наладить рацион. Принимать разрешенную пищу следует не меньше 5 раз на день, маленькими порциями. Рекомендуется увеличить долю выпиваемой жидкости и полностью отказаться от вредных привычек.
Для повышения качества жизни важно делать специальную гимнастику, которая направлена на укрепление мышц прямой кишки.
Вернуться к оглавлению
Последствия болезни и сколько живут?
У каждого, кто слышит диагноз «онкология», возникает вопрос о проценте выживаемости. Этот показатель обуславливает глубина проникновения в ткани злокачественного процесса и присутствие метастаз. Прогноз выживаемости значительно увеличивается при своевременной диагностике и вовремя проведенных лечебных мероприятий. В таких ситуациях современная медицина озвучивает общепринятый пятилетний срок жизни после лечения. В том случае, если были обнаружены метастазы, 5 лет живут после операции около 30—50% больных. Средний показатель следующий: около 46% пациентов живут 1 год, а 54% — 5 лет.
В том случае, если были обнаружены метастазы, 5 лет живут после операции около 30—50% больных. Средний показатель следующий: около 46% пациентов живут 1 год, а 54% — 5 лет.
Прогноз выживаемости при раке кишечника 3 степени
Как любое онкологическое заболевание, рак кишечника 3 стадии представляет собой большую угрозу для жизни больного. Данная степень патологии отличается от двух предыдущих, более яркой симптоматикой, поэтому болезнь выявляется уже в запущенной форме. Заболевание прогрессирует в течение многих лет и люди не догадываются о своей проблеме.
Онкология кишечника — это злокачественная опухоль на слизистой оболочке тонкой и толстой кишки. Чаще всего перерождение клеток происходит в толстой кишке, чем в тонкой. Прогноз болезни напрямую зависит от стадий заболевания, но чаще он неутешительный.
Не каждый человек без специального образования способен понять, чем страшна онкология кишечника на 3 стадии. При данной патологии метастазы проникают в лимфоузлы и без надлежащего лечения, болезнь очень быстро переходит в последнюю, термальную степень.
Причины
Онкология 3 степени прогрессирует постепенно. Поэтому чаще всего новообразование выявляют именно на этой стадии, потому как две предыдущие протекают бессимптомно. Опухоль третьей стадии – это результат плохой диагностики и долгого нежелания обратиться за помощью к специалисту.
Среди самых распространенных причин, приводящих к заболеванию можно выделить следующие:
- наследственный фактор;
- неправильный образ жизни – злоупотребление табаком и алкоголем;
- воспалительные патологии;
- наследственный полипоз;
- неправильное питание;
- язва 12-перстной кишки;
- контактирование с канцерогенами;
- радиационное облучение;
- синдром Линча;
- дивертикулит;
- возраст старше 50 лет;
- хронические запоры;
- нарушения в работе опорно-двигательного аппарата;
- ожирение;
- болезни эндокринной системы.

Важно! Данному заболеванию чаще других подвержены люди, злоупотребляющие крепкими напитками и курением табака. Одной из главных причин перерождения здоровых клеток кишечника в раковые является наследственный полипоз. Также причиной появления опухоли считается неправильное питание. Любовь к жирному мясу, копченостям, специям, рафинированным углеводам.
Симптомы
Данная стадия отличается значительным размером опухоли. Она в размере больше, чем полуокружность кишечника. Злокачественное образование прорастает сквозь стенки кишки в брюшную полость. На данном этапе прогрессирования болезни опухоль носит первичный характер, и могут появиться региональные метастазы, поражающие находящиеся возле опухоли лимфоузлы. По степени поражения лимфоузлов, специалисты определяют прогноз жизни для пациента.
Опухоль, имеющая третью стадию, затрудняет продвижение полупереработанной пищи по кишечнику, что вызывает следующие проблемы:
- болевой синдром в животе в виде спазма;
- чередующиеся запоры и диарея;
- приступы тошноты и рвоты;
- вздутием живота;
- резкая потеря массы тела;
- после опорожнение остается чувство, что процесс выполнен не полностью;
- отвращение к любимой еде, потеря аппетита частичная или полная;
- наличие крови в каловой массе;
- непроходимость кишечника;
- боли в пораженных метастазами органах;
- изменение цвета кожи;
- слабостью, недомогание.

В связи с повреждением тканей кишки, могут развиться кровотечения, и даже перфорация. Опухоль прорастает сквозь стенку, что может привести к перитониту. При экзофитном росте опухоли развивается непроходимость кишечника. Метастазирование в отдаленные органы не наблюдается. Большое новообразование сдавливает соседние органы — поджелудочную железу, мочевой пузырь. Часто образуются язвы, которые в будущем провоцируют появление свищей.
Диагностика
При выявлении новообразования и подозрении на патологию 3 стадии врач-гастроэнтеролог назначает ряд исследований, цель которых заключается в уточнении опухоли, ее типа, степени развития, наличия метастаз и поражения других органов. Для этого используют следующие методы:
- общий анализ крови;
- исследование каловых масс на наличие скрытой крови;
- анализ на онкомаркер;
- пальцевое обследование прямой кишки;
- фиброэзофагогастродуоденоскопия;
- ректороманоскопия;
- колоноскопия;
- ультразвуковое исследование.

Обязательно необходимо провести обследование лимфатической системы. Это надо для выявления метастаз. От их количества зависит прогноз. После вынесения диагноза составляется эффективная схема лечения. Она зависит также от общего состояния больного и степени запущенности патологии.
Лечение
Третья стадия рака требует хирургического вмешательства. В противном случае прогноз будет удручающим. Во время операции будет произведена резекция пораженной кишки. Если затронута 12-перстная кишка, то врач проведет дуоденэктомию. После операции назначается курс химиотерапии.
Специалисты используют три варианта операции:
- иссечение с установкой колостомы;
- резекция небольшого поврежденного участка с кишкой;
- удаление всей поврежденной опухолью кишки.
Колостома устанавливается после операции обеспечения больному нормального процесса пищеварения, но при этом гарантий, что метастазирование прекратится — нет. Это означает, что удаление кишечника не является последней мерой лечения.
Прогноз заболевания
Пятилетний прогноз выживаемости после операции на рак желудка 3 степени зависит от организма самого больного. В последнее время, уровень выживаемости после хирургического вмешательства значительно вырос, это связано с применением современных методов диагностики.
5-летняя выживаемость с третьей стадией рака кишечника:
- IIIA — наличие метастаз в близлежащей от лимфоузлов зоне. Поэтому прогноз составляет 89%;
- IIIB — опухоль проросла далеко в ткань. Выживаемость на этом этапе 69 %;
- IIIC — злокачественное образование поразило слизистую ткань мышечной системы и затронуло от 4 до 7 лимфоузлов. Прогноз выживаемости составляет 44,3%.
Но следует учитывать, что у некоторых больных этап IIIB после очередного обследования может выявиться как IIIC или наоборот.
Важно! Для того чтобы не довести болезнь до последних стадий, необходимо ежегодно проходить профилактические осмотры.
youtube.com/embed/y1f077pr1bQ» frameborder=»0″ allowfullscreen=»allowfullscreen»/>
Рак кишечника 3 стадии: сколько осталось жить, операция
Как и любое онкологическое заболевание, рак кишечника 3 степени несет серьезную угрозу жизни человека. Данная стадия заболевания характеризуется более выраженной симптоматикой, чем две предыдущие, поэтому чаще заболевание обнаруживается уже в запущенной форме. Болезнь развивается в течение нескольких лет и люди живут, не догадываясь о наличии проблемы. Для предупреждения серьезных осложнений следует при любых нарушениях работы ЖКТ обращаться к врачу.
Онкология третей степени имеет небольшие шансы на выживание, потому следует незамедлительно проводить основную и вспомогательную терапию для спасения жизни.
Отличие 3 стадии
Данная степень отличается значительным увеличением опухоли, которая занимает уже больше, чем полуокружность кишечника. Новообразование прорастает сквозь стенку кишки и может затрагивать брюшную полость. На данном этапе развития болезни возможно наличие только первичной опухоли либо возникновение регионарных метастаз, поражающих лимфоузлы возле опухоли. В зависимости от того, насколько далеко зашло поражение лимфоузлов, специалисты определяют, сколько осталось жить пациенту.
На данном этапе развития болезни возможно наличие только первичной опухоли либо возникновение регионарных метастаз, поражающих лимфоузлы возле опухоли. В зависимости от того, насколько далеко зашло поражение лимфоузлов, специалисты определяют, сколько осталось жить пациенту.
По статистике, если рак третьей степени не вышел за границы кишечника, шанс выжить составляет не менее 99%.
Вернуться к оглавлению
Существующие жалобы
Возникает подозрение на рак кишечника третьей степени, если пациент имеет следующие жалобы:
- В кале видна кровь.
- Боли в животе, метеоризм, не зависящий от характера питания. Соблюдение диеты не помогает.
- Нарушение стула (запор сменяется диареей).
- После дефекации сохраняется чувство неполного опорожнения кишечника.
- Живот стал больше либо увеличен определенный участок.
- Ухудшение аппетита, отвращение к пище. Если для пациента стали отвратительными мясные блюда, можно говорить о наличии онкологического заболевания.

- Резкое снижение массы тела, упадок сил.
- При поражении метастазами печени и желчного пузыря кожа пациента приобретает желтый оттенок.
- Боль в органах, пораженных метастазами.
- Кишечная непроходимость.
Вернуться к оглавлению
Клиническая картина
Увеличение опухоли приводит к непроходимости кишечника. Просвет кишки перекрывается новообразованием, каловые массы не могут двигаться и накапливаются. Происходит растяжение кишечника. Поэтому данное состояние сопровождается болями, метеоризмом и признаками интоксикации: рвотой, тошнотой, упадком сил. При формировании непроходимости у человека появляется субфебрильная температура (в пределах 37,1—38,0 °C), мышцы живота напряжены. Порой болевые ощущения в правом боку способствуют постановке ошибочного диагноза — аппендицита.
Постепенно интенсивность симптомов возрастает, боли усиливаются, возникает задержка газов, запор сменяется диареей, в животе сильно урчит. Образуется частичная или полная непроходимость. Наличие подобных симптомов у людей старше 50 лет требует проведения обследования на выявление онкологических заболеваний. Даже незначительное промедление порой стоит человеку жизни.
Наличие подобных симптомов у людей старше 50 лет требует проведения обследования на выявление онкологических заболеваний. Даже незначительное промедление порой стоит человеку жизни.
Вернуться к оглавлению
Диагностика рака кишечника 3 стадии
При подозрении на рак третьей степени или при обнаружении новообразования, проводится ряд исследований, целью которых является определить природу опухоли, ее тип, этап развития, наличие метастаз, поражения других органов. Для этого применяют такие методы:
- Ректороманоскопия. Исследование состояния внутренней поверхности прямой и сигмовидной кишки посредством ректороманоскопа, который вводится через анальное отверстие.
- Биопсия. Частица ткани новообразования берется для определения в ней раковых клеток.
- Колоноскопия. Обследование внутренней поверхности толстого кишечника.

- Рентгенография, КТ.
- Анализ крови на онкомаркеры определяет наличие раковой опухоли в организме.
- Ультразвуковое исследование выявляет наличие опухоли и метастаз в других органах.
Рентгенологическое обследование — основной метод диагностики онкологических заболеваний, проводимый в рамках профилактики.
Вернуться к оглавлению
Лечение без хирургического вмешательства
Устранение рака кишечника 3 степени потребует кардинальной терапии.
В отличие от начальных этапов развития болезни, лечение 3 степени рака кишечника требует проведения комплексных мероприятий. Хирургическое вмешательство не способно решить проблему без дополнительной терапии. Поэтому в данном случае, в зависимости от особенностей протекания болезни, проводят лучевую терапию (так называемое «облучение») и химиотерапию.
Лучевая терапия подразумевает воздействие на опухоль рентгеновским излучением. В результате рост новообразования несколько замедляется. Во время химиотерапии в организм вводят специальные препараты, разрушающие опухоль. Но вместе с этим, данный метод также негативно сказывается на общем состоянии человека, так как разрушаются не только клетки рака, нарушается работа всех клеток организма. Терапия сопровождается побочными эффектами: рвотой, тошнотой, выпадением волос.
Во время химиотерапии в организм вводят специальные препараты, разрушающие опухоль. Но вместе с этим, данный метод также негативно сказывается на общем состоянии человека, так как разрушаются не только клетки рака, нарушается работа всех клеток организма. Терапия сопровождается побочными эффектами: рвотой, тошнотой, выпадением волос.
Если рак не пустил метастазы, химиотерапии достаточно. При наличии метастазов применяют лучевую терапию. Это препятствует развитию большего числа метастазов, соответственно, у человека появляется больше шансов выжить. При 3 степени развития болезни хирургическое вмешательство может быть противопоказано ввиду индивидуальных особенностей. Поэтому часто проводится паллиативный курс лучевой терапии, включающий 10 сеансов «облучения».
Вернуться к оглавлению
Народные средства
В последнее время приобретает большую популярность народный метод лечения онкологических заболеваний препаратом «АСД-2». В середине прошлого века данное средство широко использовалось для лечения людей, особенно важен этот препарат был в армии. Затем его стали применять только в ветеринарии. В настоящее время с помощью «АСД-2», которое является антисептиком-стимулятором, люди начинают самостоятельно лечить рак, чтобы избежать операции. Многочисленные случаи исцеления онкологических заболеваний с помощью этого средства подтверждают его эффективность. «АСД-2» выпуска «Армавир» можно найти только в ветеринарной аптеке, хотя инструкция к препарату информирует о применении лекарства для лечения людей. Противопоказаний у препарата нет. Тем не менее, во избежание негативных последствий, перед его применением нужно обязательно проконсультироваться с лечащим врачом.
Затем его стали применять только в ветеринарии. В настоящее время с помощью «АСД-2», которое является антисептиком-стимулятором, люди начинают самостоятельно лечить рак, чтобы избежать операции. Многочисленные случаи исцеления онкологических заболеваний с помощью этого средства подтверждают его эффективность. «АСД-2» выпуска «Армавир» можно найти только в ветеринарной аптеке, хотя инструкция к препарату информирует о применении лекарства для лечения людей. Противопоказаний у препарата нет. Тем не менее, во избежание негативных последствий, перед его применением нужно обязательно проконсультироваться с лечащим врачом.
Вернуться к оглавлению
Когда нужна операция?
Опираясь на полученные в ходе диагностики результаты, доктор назначает необходимое лечение с учетом индивидуальных особенностей. Обычно на 3 этапе развития рака операция малоэффективна и ее проводят только в случае непроходимости кишечника. Если ситуация позволяет, посредством хирургического вмешательства удаляется вся опухоль вместе с пораженной частью кишечника и затронутыми патологией лимфоузлами. Это сложная процедура, которая зачастую приводит к инвалидности пациента. Возможно выведение кишки наружу через брюшную полость. Создается фиктивное анальное отверстие. В таком случае продолжительность жизни пациента невелика.
Это сложная процедура, которая зачастую приводит к инвалидности пациента. Возможно выведение кишки наружу через брюшную полость. Создается фиктивное анальное отверстие. В таком случае продолжительность жизни пациента невелика.
Отказ от пищи животного происхождения и высока физическая активность снижает риск возникновения рака кишечника в 10−20 раз.
Вернуться к оглавлению
Профилактика и сколько осталось жить
Так как на 3 этапе развития рака кишечника под поражение попадают лимфоузлы и другие органы, прогноз неблагоприятный. Зачастую пациенты с таким диагнозом проживают около года, в лучшем случае не более 3 лет. При поражении стенок кишки шанс выжить составляет 85%. Поражение близлежащих лимфатических узлов снижает этот показатель до 66%. При метастазах в регионарных лимфоузлах — 35%. Чем большее число лимфатических узлов поражено, тем хуже прогноз.
Важно диагностировать рак как можно раньше. Для этого в рамках профилактики следует регулярно проходить медицинский осмотр, подразумевающий, в частности, УЗИ, колоноскопию. Например, в Японии люди старше 35 лет должны ежегодно проходить колоноскопию в обязательном порядке. Таким образом, в стране снижена смертность от рака кишечника в 2 раза. Возникновение любых нарушений в работе ЖКТ может свидетельствовать о ряде заболеваний, среди которых и онкологические. Потому не стоит заниматься самолечением, нужно сразу обращаться за медицинской помощью. Высокая физическая активность, правильное питание, отказ от вредных привычек, своевременное лечение возникающих заболеваний, отсутствие стрессов значительно снижают риск возникновения рака кишечника.
Для этого в рамках профилактики следует регулярно проходить медицинский осмотр, подразумевающий, в частности, УЗИ, колоноскопию. Например, в Японии люди старше 35 лет должны ежегодно проходить колоноскопию в обязательном порядке. Таким образом, в стране снижена смертность от рака кишечника в 2 раза. Возникновение любых нарушений в работе ЖКТ может свидетельствовать о ряде заболеваний, среди которых и онкологические. Потому не стоит заниматься самолечением, нужно сразу обращаться за медицинской помощью. Высокая физическая активность, правильное питание, отказ от вредных привычек, своевременное лечение возникающих заболеваний, отсутствие стрессов значительно снижают риск возникновения рака кишечника.
ЭТО действительно ВАЖНО! Желудочно-кишечный тракт нельзя запускать — это грозит раком. Копеечный продукт №1 против болей в желудке… УЗНАТЬ >>
ВАЖНО ЗНАТЬ! Даже ‘запущенный’ желудочно-кишечный тракт можно вылечить дома, без операций и больниц. Просто прочитайте что говорит Галина Савина читать рекомендацию…
Просто прочитайте что говорит Галина Савина читать рекомендацию…
Судя по тому, что вы сейчас читаете эти строки — победа в борьбе с заболеваниями желудочно-кишечного тракта пока не на вашей стороне…
И вы уже думали о хирургическом вмешательстве? Оно и понятно, ведь все органы ЖКТ — жизненно важные, а их правильное функционирование — залог здоровья и хорошего самочувствия. Частые боли в животе, изжога, вздутие, отрыжка, тошнота, нарушение стула… Все эти симптомы знакомы вам не понаслышке.
Но возможно правильнее лечить не следствие, а причину? Рекомендуем прочитать историю Галины Савиной, как она вылечила проблембы ЖКТ… Читать статью >>
Рак кишечника — лечение рака кишечника в клинике Медицина 24/7
МЕДИЦИНА 24/7 Личный кабинет
+7 (495) 230-00-01Автозаводская 16/2Facebook клиники Медицина 24/7Youtube канал клиники Медицина 24/7Instagram клиники Медицина 24/7
We speak English
Личный кабинет
МЕДИЦИНА 24/7Официальный сайт+7 (495) 230-00-01reg@medica24. ruМосква, Автозаводская ул, 16к2Мы открыты круглосуточноЗаписаться на прием
ruМосква, Автозаводская ул, 16к2Мы открыты круглосуточноЗаписаться на прием
- Онкология
- Центр онкологии
- Методы диагностики рака
- Биопсия
НазадБиопсия
- Биопсия влагалища
- Биопсия гортани
- Биопсия желудка
- Биопсия кожи
- Биопсия легких
- Биопсия пищевода
- Биопсия полового члена
- Биопсия слизистой
- Биопсия толстой кишки
- Биопсия щитовидной железы
- Биопсия шейки матки
- Ножевая биопсия шейки матки
- Биопсия почки
- Заболевания
НазадЗаболевания
- Опухоли головы и шеи
- Рак головного мозга
- Рак горла
- Рак гортани
- Рак губы
- Рак десны
- Рак нёба
- Рак пищевода
- Рак языка
- Рак желудка и пищевода
- Стадии рака желудка
- Лечение рака желудка
- Лечение рака пищевода
- Рак кишечника
- Рак кишечника
- Рак кишечника 4 стадии
- Рак тонкого кишечника
- Рак прямой кишки
- Рак толстой кишки
- Рак слепой кишки
- Рак двенадцатиперстной кишки
- Рак ободочной кишки
- Рак крови
- Рак легких
- Немелкоклеточный рак легкого
- Рак легкого 4 стадии
- Рак бронхов
- Лимфома
- Фолликулярная лимфома
- Миелома
- Рак молочной железы
- Карцинома молочной железы
- Рак Педжета (рак соска молочной железы)
- Стадии рака молочной железы
- Рак печени
- Рак печени
- Стадии рака печени
- Лечение рака печени
- Рак печени 4 стадии
- Гепатоцеллюлярный рак печени
- Нейроэндокринный рак печени
- Рак желчных протоков
- Перстневидноклеточный рак печени
- Саркомы
- Саркомы мягких тканей
- Остеосаркома
- Рак костей
- Саркома Капоши
- Онкодерматология
- Рак кожи
- Базальноклеточный рак кожи
- Плоскоклеточный рак кожи
- Меланома
- Рак кожи
- Онкогинекология
- Рак тела матки (эндометрия)
- Стадии рака матки
- Рак матки 4 стадии
- Дисплазия шейки матки
- Рак шейки матки
- Рак яичников
- Онкоурология
- Рак мочевого пузыря
- Рак мочеточника
- Рак надпочечника
- Рак почки
- Рак полового члена
- Рак простаты
- Рак яичка
- Тимома
- Рак эндокринной системы
- Рак поджелудочной железы
- Рак поджелудочной железы
- Опухоли головы и шеи
Рак 3 степени кишечника продолжительность жизни
Как и любое онкологическое заболевание, рак кишечника 3 степени несет серьезную угрозу жизни человека. Данная стадия заболевания характеризуется более выраженной симптоматикой, чем две предыдущие, поэтому чаще заболевание обнаруживается уже в запущенной форме. Болезнь развивается в течение нескольких лет и люди живут, не догадываясь о наличии проблемы. Для предупреждения серьезных осложнений следует при любых нарушениях работы ЖКТ обращаться к врачу.
Данная стадия заболевания характеризуется более выраженной симптоматикой, чем две предыдущие, поэтому чаще заболевание обнаруживается уже в запущенной форме. Болезнь развивается в течение нескольких лет и люди живут, не догадываясь о наличии проблемы. Для предупреждения серьезных осложнений следует при любых нарушениях работы ЖКТ обращаться к врачу.
ВАЖНО ЗНАТЬ! Даже «запущенный» желудочно-кишечный тракт можно вылечить дома, без операций и больниц. Просто прочитайте что говорит Галина Савина читать рекомендацию.
Отличие 3 стадии
Данная степень отличается значительным увеличением опухоли, которая занимает уже больше, чем полуокружность кишечника. Новообразование прорастает сквозь стенку кишки и может затрагивать брюшную полость. На данном этапе развития болезни возможно наличие только первичной опухоли либо возникновение регионарных метастаз, поражающих лимфоузлы возле опухоли. В зависимости от того, насколько далеко зашло поражение лимфоузлов, специалисты определяют, сколько осталось жить пациенту.
По статистике, если рак третьей степени не вышел за границы кишечника, шанс выжить составляет не менее 99%.
Существующие жалобы
Возникает подозрение на рак кишечника третьей степени, если пациент имеет следующие жалобы:
- В кале видна кровь.
- Боли в животе, метеоризм, не зависящий от характера питания. Соблюдение диеты не помогает.
- Нарушение стула (запор сменяется диареей).
- После дефекации сохраняется чувство неполного опорожнения кишечника.
- Живот стал больше либо увеличен определенный участок.
- Ухудшение аппетита, отвращение к пище. Если для пациента стали отвратительными мясные блюда, можно говорить о наличии онкологического заболевания.
- Резкое снижение массы тела, упадок сил.
- При поражении метастазами печени и желчного пузыря кожа пациента приобретает желтый оттенок.
- Боль в органах, пораженных метастазами.
- Кишечная непроходимость.
Вернуться к оглавлению
Клиническая картина
Увеличение опухоли приводит к непроходимости кишечника. Просвет кишки перекрывается новообразованием, каловые массы не могут двигаться и накапливаются. Происходит растяжение кишечника. Поэтому данное состояние сопровождается болями, метеоризмом и признаками интоксикации: рвотой, тошнотой, упадком сил. При формировании непроходимости у человека появляется субфебрильная температура (в пределах 37,1—38,0 °C), мышцы живота напряжены. Порой болевые ощущения в правом боку способствуют постановке ошибочного диагноза — аппендицита.
Просвет кишки перекрывается новообразованием, каловые массы не могут двигаться и накапливаются. Происходит растяжение кишечника. Поэтому данное состояние сопровождается болями, метеоризмом и признаками интоксикации: рвотой, тошнотой, упадком сил. При формировании непроходимости у человека появляется субфебрильная температура (в пределах 37,1—38,0 °C), мышцы живота напряжены. Порой болевые ощущения в правом боку способствуют постановке ошибочного диагноза — аппендицита.
Постепенно интенсивность симптомов возрастает, боли усиливаются, возникает задержка газов, запор сменяется диареей, в животе сильно урчит. Образуется частичная или полная непроходимость. Наличие подобных симптомов у людей старше 50 лет требует проведения обследования на выявление онкологических заболеваний. Даже незначительное промедление порой стоит человеку жизни.
Диагностика рака кишечника 3 стадии
При подозрении на рак третьей степени или при обнаружении новообразования, проводится ряд исследований, целью которых является определить природу опухоли, ее тип, этап развития, наличие метастаз, поражения других органов. Для этого применяют такие методы:
Для этого применяют такие методы:
- Ректороманоскопия. Исследование состояния внутренней поверхности прямой и сигмовидной кишки посредством ректороманоскопа, который вводится через анальное отверстие.
- Биопсия. Частица ткани новообразования берется для определения в ней раковых клеток.
- Колоноскопия. Обследование внутренней поверхности толстого кишечника.
- Рентгенография, КТ.
- Анализ крови на онкомаркеры определяет наличие раковой опухоли в организме.
- Ультразвуковое исследование выявляет наличие опухоли и метастаз в других органах.
Рентгенологическое обследование — основной метод диагностики онкологических заболеваний, проводимый в рамках профилактики.
Лечение без хирургического вмешательства
В отличие от начальных этапов развития болезни, лечение 3 степени рака кишечника требует проведения комплексных мероприятий. Хирургическое вмешательство не способно решить проблему без дополнительной терапии. Поэтому в данном случае, в зависимости от особенностей протекания болезни, проводят лучевую терапию (так называемое «облучение») и химиотерапию.
Поэтому в данном случае, в зависимости от особенностей протекания болезни, проводят лучевую терапию (так называемое «облучение») и химиотерапию.
ЭТО действительно ВАЖНО! Желудочно-кишечный тракт нельзя запускать — это грозит раком. Копеечный продукт №1 против болей в желудке. УЗНАТЬ >>
Лучевая терапия подразумевает воздействие на опухоль рентгеновским излучением. В результате рост новообразования несколько замедляется. Во время химиотерапии в организм вводят специальные препараты, разрушающие опухоль. Но вместе с этим, данный метод также негативно сказывается на общем состоянии человека, так как разрушаются не только клетки рака, нарушается работа всех клеток организма. Терапия сопровождается побочными эффектами: рвотой, тошнотой, выпадением волос.
Если рак не пустил метастазы, химиотерапии достаточно. При наличии метастазов применяют лучевую терапию. Это препятствует развитию большего числа метастазов, соответственно, у человека появляется больше шансов выжить. При 3 степени развития болезни хирургическое вмешательство может быть противопоказано ввиду индивидуальных особенностей. Поэтому часто проводится паллиативный курс лучевой терапии, включающий 10 сеансов «облучения».
При 3 степени развития болезни хирургическое вмешательство может быть противопоказано ввиду индивидуальных особенностей. Поэтому часто проводится паллиативный курс лучевой терапии, включающий 10 сеансов «облучения».
Народные средства
В последнее время приобретает большую популярность народный метод лечения онкологических заболеваний препаратом «АСД-2». В середине прошлого века данное средство широко использовалось для лечения людей, особенно важен этот препарат был в армии. Затем его стали применять только в ветеринарии. В настоящее время с помощью «АСД-2», которое является антисептиком-стимулятором, люди начинают самостоятельно лечить рак, чтобы избежать операции. Многочисленные случаи исцеления онкологических заболеваний с помощью этого средства подтверждают его эффективность. «АСД-2» выпуска «Армавир» можно найти только в ветеринарной аптеке, хотя инструкция к препарату информирует о применении лекарства для лечения людей. Противопоказаний у препарата нет. Тем не менее, во избежание негативных последствий, перед его применением нужно обязательно проконсультироваться с лечащим врачом.
Когда нужна операция?
Опираясь на полученные в ходе диагностики результаты, доктор назначает необходимое лечение с учетом индивидуальных особенностей. Обычно на 3 этапе развития рака операция малоэффективна и ее проводят только в случае непроходимости кишечника. Если ситуация позволяет, посредством хирургического вмешательства удаляется вся опухоль вместе с пораженной частью кишечника и затронутыми патологией лимфоузлами. Это сложная процедура, которая зачастую приводит к инвалидности пациента. Возможно выведение кишки наружу через брюшную полость. Создается фиктивное анальное отверстие. В таком случае продолжительность жизни пациента невелика.
Отказ от пищи животного происхождения и высока физическая активность снижает риск возникновения рака кишечника в 10−20 раз.
Профилактика и сколько осталось жить
Так как на 3 этапе развития рака кишечника под поражение попадают лимфоузлы и другие органы, прогноз неблагоприятный. Зачастую пациенты с таким диагнозом проживают около года, в лучшем случае не более 3 лет. При поражении стенок кишки шанс выжить составляет 85%. Поражение близлежащих лимфатических узлов снижает этот показатель до 66%. При метастазах в регионарных лимфоузлах — 35%. Чем большее число лимфатических узлов поражено, тем хуже прогноз.
При поражении стенок кишки шанс выжить составляет 85%. Поражение близлежащих лимфатических узлов снижает этот показатель до 66%. При метастазах в регионарных лимфоузлах — 35%. Чем большее число лимфатических узлов поражено, тем хуже прогноз.
Важно диагностировать рак как можно раньше. Для этого в рамках профилактики следует регулярно проходить медицинский осмотр, подразумевающий, в частности, УЗИ, колоноскопию. Например, в Японии люди старше 35 лет должны ежегодно проходить колоноскопию в обязательном порядке. Таким образом, в стране снижена смертность от рака кишечника в 2 раза. Возникновение любых нарушений в работе ЖКТ может свидетельствовать о ряде заболеваний, среди которых и онкологические. Потому не стоит з
выживаемости при колоректальном раке | Прогноз при колоректальном раке
Показатели выживаемости могут дать вам представление о том, какой процент людей с таким же типом и стадией рака все еще жив в течение определенного времени (обычно 5 лет) после того, как им был поставлен диагноз. Они не могут сказать вам, сколько вы проживете, но они могут помочь вам лучше понять, насколько вероятно, что ваше лечение будет успешным.
Они не могут сказать вам, сколько вы проживете, но они могут помочь вам лучше понять, насколько вероятно, что ваше лечение будет успешным.
Имейте в виду, что показатели выживаемости являются оценочными и часто основываются на предыдущих результатах большого числа людей, у которых был конкретный рак, но они не могут предсказать, что произойдет в конкретном случае.Эти статистические данные могут сбивать с толку и вызывать дополнительные вопросы. Поговорите со своим врачом о том, как эти цифры могут быть применимы к вам, поскольку он или она знакомы с вашей ситуацией.
Что такое 5-летняя относительная выживаемость?
Относительный коэффициент выживаемости сравнивает людей с таким же типом и стадией рака с людьми в общей популяции. Например, если относительная 5-летняя выживаемость для определенной стадии рака толстой или прямой кишки составляет 80%, это означает, что у людей с этим раком в среднем вероятность примерно на 80% выше, чем у людей, не страдающих этим заболеванием. иметь этот рак, чтобы жить не менее 5 лет после постановки диагноза.
иметь этот рак, чтобы жить не менее 5 лет после постановки диагноза.
Откуда эти числа?
Американское онкологическое общество полагается на информацию из базы данных SEER *, поддерживаемой Национальным институтом рака (NCI), чтобы предоставить статистику выживаемости для различных типов рака.
База данных SEER отслеживает 5-летнюю относительную выживаемость при раке прямой и толстой кишки в Соединенных Штатах, основываясь на том, как далеко распространился рак. Однако база данных SEER не группирует раковые заболевания по стадиям AJCC TNM (стадия 1, стадия 2, стадия 3 и т. Д.).). Вместо этого он группирует рак на локальные, региональные и отдаленные стадии:
- Локализованный: Нет никаких признаков того, что рак распространился за пределы толстой или прямой кишки.
- Региональный: Рак распространился за пределы толстой или прямой кишки на близлежащие структуры или лимфатические узлы.
- Отдаленный: Рак распространился на отдаленные части тела, такие как печень, легкие или отдаленные лимфатические узлы.

5-летняя относительная выживаемость при раке толстой кишки
Эти цифры основаны на людях, у которых в период с 2009 по 2015 год был диагностирован рак толстой кишки.
SEER стадия | 5-летняя относительная выживаемость |
Локализованный | 90% |
Региональный | 71% |
Дальний | 14% |
Все этапы SEER вместе | 63% |
5-летняя относительная выживаемость при раке прямой кишки
Эти цифры основаны на людях, у которых в период с 2009 по 2015 год был диагностирован рак прямой кишки.
SEER стадия | 5-летняя относительная выживаемость |
Локализованный | 89% |
Региональный | 71% |
Дальний | 15% |
Все этапы SEER вместе | 67% |
Что такое числа
- Эти цифры относятся только к стадии рака, когда он впервые диагностирован. Они не применяются позже, если рак разрастается, распространяется или возвращается после лечения.
- Эти цифры учитывают не все. Показатели выживаемости сгруппированы в зависимости от того, насколько далеко распространился рак, но ваш возраст, общее состояние здоровья, насколько хорошо рак реагирует на лечение, начался ли рак с левой или правой стороны толстой кишки, а также другие факторы также могут повлиять на ваше состояние. мировоззрение.
- Люди, у которых сейчас диагностирован рак прямой или толстой кишки, могут иметь более благоприятные перспективы, чем показывают эти цифры. Лечение со временем улучшается, и эти цифры основаны на людях, которым был поставлен диагноз и которые лечились не менее пяти лет назад.
* SEER = надзор, эпидемиология и конечные результаты
выживаемости при раке поджелудочной железы
Показатели выживаемости могут дать вам представление о том, какой процент людей с таким же типом и стадией рака все еще жив в течение определенного времени (обычно 5 лет) после того, как им был поставлен диагноз. Они не могут сказать вам, сколько вы проживете, но они могут помочь вам лучше понять, насколько вероятно, что ваше лечение будет успешным.
Имейте в виду, что показатели выживаемости являются оценочными и часто основываются на предыдущих результатах большого числа людей, у которых был конкретный рак, но они не могут предсказать, что произойдет в конкретном случае. Эти статистические данные могут сбивать с толку и вызывать дополнительные вопросы. Поговорите со своим врачом о том, как эти цифры могут быть применимы к вам, поскольку он или она знакомы с вашей ситуацией.
Что такое 5-летняя относительная выживаемость?
Относительная выживаемость сравнивает людей с таким же типом и стадией рака поджелудочной железы с людьми в общей популяции.Например, если относительная 5-летняя выживаемость для конкретной стадии рака поджелудочной железы составляет 50%, это означает, что люди, у которых есть этот рак, в среднем примерно на 50% выше, чем люди, у которых этого рака нет. рак жить не менее 5 лет после постановки диагноза.
Откуда эти числа?
Американское онкологическое общество полагается на информацию из базы данных SEER *, поддерживаемой Национальным институтом рака (NCI), чтобы предоставить статистику выживаемости для различных типов рака.
База данных SEER отслеживает 5-летнюю относительную выживаемость при раке поджелудочной железы в Соединенных Штатах на основе того, как далеко распространился рак. В базе данных SEER, однако, раковые заболевания не группируются по стадиям TNM AJCC (стадия 1, стадия 2, стадия 3 и т. Д.). Вместо этого он группирует рак на локальные, региональные и отдаленные стадии:
- Локализованный: Нет никаких признаков того, что рак распространился за пределы поджелудочной железы.
- Региональный: Рак распространился из поджелудочной железы на близлежащие структуры или лимфатические узлы.
- Отдаленный: Рак распространился на отдаленные части тела, такие как легкие, печень или кости.
5-летняя относительная выживаемость при раке поджелудочной железы
(на основе людей, у которых был диагностирован рак поджелудочной железы в период с 2009 по 2015 гг.)
SEER Этап | Относительная выживаемость за 5 лет |
Локализованный | 37% |
Региональный | 12% |
Дальний | 3% |
Все этапы SEER вместе | 9% |
Числа
- Эти цифры относятся только к стадии рака, когда он впервые диагностирован. Они не применяются позже, если рак разрастается, распространяется или возвращается после лечения.
- Эти цифры учитывают не все. Показатели выживаемости сгруппированы в зависимости от того, насколько далеко распространился рак, но ваш возраст, общее состояние здоровья, насколько хорошо рак реагирует на лечение, степень опухоли, степень резекции, уровень онкомаркера (CA 19-9) и другие факторы. также влияют на ваше мировоззрение.
- Люди, у которых сейчас диагностирован рак поджелудочной железы, могут иметь лучший прогноз, чем показывают эти цифры. Лечение со временем улучшается, и эти цифры основаны на людях, которым был поставлен диагноз и которые лечились не менее пяти лет назад.
* SEER = надзор, эпидемиология и конечные результаты
Лечение рака прямой кишки (PDQ®) — Версия профессионала здравоохранения
Заболеваемость и смертность
Трудно отделить эпидемиологические аспекты рака прямой кишки от таковых рака толстой кишки, поскольку эпидемиологические исследования часто рассматривают рак толстой и прямой кишки (т.е. колоректальный рак) вместе.
Колоректальный рак является третьей по распространенности формой рака во всем мире. По оценкам, в 2012 году было зарегистрировано 1,36 миллиона новых случаев колоректального рака и 694 000 случаев смерти [1].
Предполагаемое количество новых случаев и смертей от рака прямой и толстой кишки в США в 2020 году: [2]
- Новые случаи рака прямой кишки: 43 340.
- Новые случаи рака толстой кишки: 104610.
- Смертных: 53 200 (вместе взятых от рака прямой и толстой кишки).
Колоректальный рак почти одинаково поражает мужчин и женщин.Среди всех расовых групп в Соединенных Штатах афроамериканцы имеют самые высокие показатели заболеваемости и смертности от спорадического колоректального рака. [3,4]
Анатомия
Enlarge Анатомия нижних отделов желудочно-кишечного тракта.
Прямая кишка расположена в тазу, простирается от переходной слизистой оболочки анальной зубчатой линии до сигмовидной кишки в области перитонеального отражения; при жесткой ректороманоскопии длина прямой кишки составляет от 10 до 15 см от анального края [5]. Расположение опухоли прямой кишки обычно определяется расстоянием между анальной кромкой, зубчатой линией или аноректальным кольцом и нижним краем опухоли, причем измерения различаются в зависимости от использования жесткого или гибкого эндоскопа или цифрового исследования.[6]
Расстояние от опухоли до мускулатуры анального сфинктера влияет на возможность выполнения операции по сохранению сфинктера. Костные ограничения таза ограничивают хирургический доступ к прямой кишке, что приводит к меньшей вероятности достижения широко отрицательных границ и более высокому риску местного рецидива [5].
Факторы риска
Возраст является наиболее важным фактором риска для большинства видов рака. К другим факторам риска колоректального рака относятся следующие:
- Семейный анамнез колоректального рака у родственника первой степени родства.[7]
- В личном анамнезе колоректальные аденомы, колоректальный рак или рак яичников. [8-10]
- Наследственные заболевания, включая семейный аденоматозный полипоз (FAP) и синдром Линча (наследственный неполипозный колоректальный рак [HNPCC]) [11]. ]
- В личном анамнезе длительный хронический язвенный колит или колит Крона. [12]
- Чрезмерное употребление алкоголя. [13]
- Курение сигарет. [14]
- Раса / этническая принадлежность: афроамериканец. [15,16]
- Ожирение.[17]
Скрининг
Доказательства подтверждают, что скрининг на рак прямой кишки является частью стандартного лечения для всех взрослых в возрасте 50 лет и старше, особенно для тех, у кого есть родственники первой степени родства с колоректальным раком, по следующим причинам: Заболеваемость у лиц старше 50 лет.
(Для получения дополнительной информации см. Сводку PDQ по скринингу колоректального рака.)
Клинические характеристики
Как и при раке толстой кишки, симптомы рака прямой кишки могут включать следующее: [18]
- Ректальное кровотечение.
- Изменение привычек кишечника.
- Боль в животе.
- Кишечная непроходимость.
- Изменение аппетита.
- Похудание.
- Слабость.
За исключением обструктивных симптомов, эти симптомы не обязательно коррелируют со стадией заболевания или указывают на конкретный диагноз.[19]
Диагностическая оценка
Первоначальная клиническая оценка может включать следующее:
- Физический осмотр и анамнез.
- Цифровое ректальное исследование.
- Колоноскопия.
- Биопсия.
- Анализ карциноэмбрионального антигена (CEA).
- Тест полимеразной цепной реакции с обратной транскрипцией.
- Иммуногистохимия.
Физический осмотр может выявить пальпируемое образование и яркую кровь в прямой кишке. Аденопатия, гепатомегалия или легочные признаки могут присутствовать при метастатическом поражении.[6] Лабораторное обследование может выявить железодефицитную анемию, электролитные нарушения и нарушения функции печени.
Факторы прогноза
Прогноз для пациентов с раком прямой кишки связан с несколькими факторами, включая следующие: [6,20-28]
- Прилипание опухоли к соседним органам или инвазия в них. [20]
- Наличие или отсутствие опухолевого поражения лимфатических узлов и количество положительных лимфатических узлов. [6,21-24]
- Наличие или отсутствие отдаленных метастазов.[6,20]
- Перфорация или непроходимость кишечника. [6,28]
- Наличие или отсутствие патологических признаков высокого риска, включая следующие: [26,27,29]
- Положительные хирургические поля.
- Лимфоваскулярная инвазия.
- Периневральная инвазия.
- Слабо дифференцированная гистология.
- Край периферической резекции (CRM) или глубина проникновения опухоли через стенку кишечника. [6,25,30] Измеренный в миллиметрах, CRM определяется как забрюшинный или перитонеальный адвентициальный край мягких тканей, ближайший к самому глубокому проникновение опухоли.
Только стадия заболевания (обозначенная опухолью [T], узловым статусом [N] и отдаленным метастазом [M]) была утверждена как прогностический фактор в многоинституциональных проспективных исследованиях. [20-25] Основной объединенный анализ Оценка влияния стадий T и N и лечения на выживаемость и рецидив у пациентов с раком прямой кишки, получающих адъювантную терапию, была опубликована и подтверждает эти результаты. [31]
Большое количество исследований оценивали другие клинические, патологические и молекулярные параметры.[32-38] Пока ни одно из них не было подтверждено проспективными исследованиями в нескольких учреждениях. Например, было показано, что высокая микросателлитная нестабильность, также связанная с раком прямой кишки, связанным с синдромом Линча, связана с улучшением выживаемости независимо от стадии опухоли в популяционной группе из 607 пациентов с колоректальным раком в возрасте 50 лет или моложе в время постановки диагноза. [39] Кроме того, сообщалось, что профили экспрессии генов полезны для прогнозирования ответа аденокарцином прямой кишки на предоперационную химиолучевую терапию и для определения прогноза рака прямой кишки II и III стадий после неоадъювантной химиолучевой терапии на основе фторурацила.[40,41]
Наблюдались расовые и этнические различия в общей выживаемости (ОВ) после адъювантной терапии рака прямой кишки, причем ОВ у чернокожих короче, чем у белых. Факторы, способствующие этому несоответствию, могут включать положение опухоли, тип хирургической процедуры и наличие сопутствующих заболеваний. [42]
Последующее наблюдение после лечения
Основными целями программ послеоперационного наблюдения за раком прямой кишки являются: [43]
- Оценка эффективности начальной терапии.
- Для обнаружения новых или метахронных злокачественных новообразований.
- Для обнаружения потенциально излечимого рецидива или метастатического рака.
Рутинные периодические исследования после лечения рака прямой кишки могут привести к более раннему выявлению и лечению рецидива заболевания. [43-47] Статистически значимое улучшение выживаемости было продемонстрировано для более интенсивных протоколов последующего наблюдения в двух клинических испытаниях. Метаанализ, объединяющий эти два испытания с четырьмя другими, показал статистически значимое улучшение выживаемости пациентов, за которыми интенсивно наблюдали.[43,48,49]
Рекомендации по наблюдению после первоначального лечения
с лечебной целью колоректального рака различаются в ведущих онкологических обществах США и Европы, и оптимальные стратегии эпиднадзора остаются неопределенными. [50,51] Для достижения консенсуса, основанного на фактических данных, требуются большие, хорошо спланированные, проспективные, мультиинституциональные рандомизированные исследования. для последующей оценки.
Карциноэмбриональный антиген (CEA)
Измерение CEA, гликопротеина сыворотки крови, часто используется при ведении и последующем наблюдении пациентов с раком прямой кишки.Обзор использования этого онкомаркера для рака прямой кишки позволяет предположить следующее: [43]
- Анализ сывороточного CEA не является ценным инструментом скрининга рака прямой кишки из-за его низкой чувствительности и низкой специфичности.
- Послеоперационное тестирование CEA обычно ограничивается пациентами, которые являются потенциальными кандидатами на дальнейшее вмешательство, а именно:
- Пациенты с раком прямой кишки II или III стадии (каждые 2–3 месяца в течение как минимум 2 лет после постановки диагноза).
- Пациенты с раком прямой кишки, которые могут быть кандидатами на удаление метастазов в печени.
В одном голландском ретроспективном исследовании тотального мезоректального иссечения для лечения рака прямой кишки, исследователи обнаружили, что предоперационный уровень CEA в сыворотке был нормальным у большинства пациентов с раком прямой кишки, и тем не менее, уровни CEA в сыворотке выросли по крайней мере на 50% у пациентов с рецидивом. Авторы пришли к выводу, что нельзя отказываться от серийных послеоперационных тестов СЕА на основании нормального предоперационного уровня СЕА в сыворотке у пациентов с раком прямой кишки. [52,53]
Связанные резюме
Другие сводки PDQ, содержащие информацию, относящуюся к раку прямой кишки, включают следующее:
Ссылки
- Ferlay J, Soerjomataram I, Ervik M, et al.: GLOBOCAN 2012 v1.0, Заболеваемость и смертность от рака во всем мире. Лион, Франция: Международное агентство по изучению рака, 2013 г. База данных IARC CancerBase № 11. Доступно в Интернете. Последний доступ: 27 февраля 2020 г.
- Американское онкологическое общество: факты и цифры о раке, 2020. Атланта, штат Джорджия: Американское онкологическое общество, 2020. Доступно в Интернете. Последний доступ: 6 октября 2020 г.
- Альбано Д.Д., Уорд Э., Джемал А. и др .: Смертность от рака в США по уровню образования и расе. J Natl Cancer Inst 99 (18): 1384-94, 2007.[PUBMED Abstract]
- Kauh J, Brawley OW, Berger M: Расовые различия в колоректальном раке. Curr Probl Cancer 31 (3): 123-33, 2007 Май-июнь. [PUBMED Abstract]
- Wolpin BM, Meyerhardt JA, Mamon HJ, et al .: Адъювантное лечение колоректального рака. CA Cancer J Clin 57 (3): 168-85, май-июнь 2007 г. [PUBMED Abstract]
- Либутти С.К., Виллетт К.Г., Сальц Л.Б.: Рак прямой кишки. В: ДеВита В.Т. младший, Лоуренс Т.С., Розенберг С.А.: Рак: принципы и практика онкологии. 9 изд. Филадельфия, Пенсильвания: Lippincott Williams & Wilkins, 2011, стр. 1127-41.
- Johns LE, Houlston RS: систематический обзор и мета-анализ риска семейного колоректального рака. Am J Gastroenterol 96 (10): 2992-3003, 2001. [PUBMED Abstract]
- Imperiale TF, Juluri R, Sherer EA, et al .: Индекс риска прогрессирующей неоплазии при второй колоноскопии наблюдения у пациентов с предыдущими аденоматозными полипами . Gastrointest Endosc 80 (3): 471-8, 2014. [PUBMED Abstract]
- Сингх Х., Наджент З., Демерс А. и др.: Риск колоректального рака после диагностики рака эндометрия: популяционное исследование.J Clin Oncol 31 (16): 2010-5, 2013. [PUBMED Abstract]
- Srinivasan R, Yang YX, Rubin SC, et al .: Риск колоректального рака у женщин с предварительным диагнозом гинекологической злокачественности. J Clin Gastroenterol 41 (3): 291-6, 2007. [PUBMED Abstract]
- Mork ME, You YN, Ying J, et al .: Высокая распространенность синдромов наследственного рака у подростков и молодых людей с колоректальным раком. J Clin Oncol 33 (31): 3544-9, 2015. [PUBMED Abstract]
- Laukoetter MG, Mennigen R, Hannig CM, et al.: Риск рака кишечника при болезни Крона: метаанализ. J Gastrointest Surg 15 (4): 576-83, 2011. [PUBMED Abstract]
- Fedirko V, Tramacere I, Bagnardi V, et al .: Употребление алкоголя и риск колоректального рака: общий метаанализ и метаанализ зависимости реакции от дозы опубликованные исследования. Ann Oncol 22 (9): 1958-72, 2011. [PUBMED Abstract]
- Liang PS, Chen TY, Giovannucci E: Курение сигарет и заболеваемость колоректальным раком и смертность: систематический обзор и метаанализ. Int J Cancer 124 (10): 2406-15, 2009.[PUBMED Abstract]
- Laiyemo AO, Doubeni C, Pinsky PF, et al .: Расовый и колоректальный рак: использование медицинских услуг в сравнении с различной восприимчивостью к раку. J Natl Cancer Inst 102 (8): 538-46, 2010. [PUBMED Abstract]
- Lansdorp-Vogelaar I, Kuntz KM, Knudsen AB и др .: Вклад скрининга и различий в выживаемости в расовые различия в заболеваемости колоректальным раком. Эпидемиологические биомаркеры рака Prev 21 (5): 728-36, 2012. [PUBMED Abstract]
- Ma Y, Yang Y, Wang F, et al.: Ожирение и риск колоректального рака: систематический обзор проспективных исследований. PLoS One 8 (1): e53916, 2013. [PUBMED Abstract]
- Штейн В., Фарина А., Гаффни К. и др.: Характеристики рака толстой кишки на момент презентации. Fam Pract Res J 13 (4): 355-63, 1993. [ОПУБЛИКОВАННЫЙ РЕЗЮМЕ]
- Majumdar SR, Fletcher RH, Evans AT: Как проявляется колоректальный рак? Симптомы, продолжительность и ключи к местонахождению. Am J Gastroenterol 94 (10): 3039-45, 1999. [PUBMED Abstract]
- Compton CC, Greene FL: стадия колоректального рака: 2004 г. и позже.CA Cancer J Clin 54 (6): 295-308, ноябрь-декабрь 2004 г. [PUBMED Abstract]
- Swanson RS, Compton CC, Stewart AK, et al.: Прогноз рака толстой кишки T3N0 зависит от количества исследованных лимфатических узлов. Ann Surg Oncol 10 (1): 65-71, январь-февраль 2003 г. [PUBMED Abstract]
- Le Voyer TE, Sigurdson ER, Hanlon AL, et al .: Выживаемость рака толстой кишки связана с увеличением количества анализируемых лимфатических узлов: вторичный обзор межгруппового исследования INT-0089. J Clin Oncol 21 (15): 2912-9, 2003. [ОПУБЛИКОВАННЫЙ РЕЗЮМЕ]
- Пранди М., Лионетто Р., Бини А. и др.: Прогностическая оценка пациентов с раком толстой кишки стадии B улучшается после адекватной лимфаденэктомии: результаты вторичного анализа крупномасштабного адъювантного исследования. Ann Surg 235 (4): 458-63, 2002. [PUBMED Abstract]
- Tepper JE, O’Connell MJ, Niedzwiecki D, et al .: Влияние количества извлеченных узлов на исход у пациентов с раком прямой кишки. J Clin Oncol 19 (1): 157-63, 2001. [PUBMED Abstract]
- Balch GC, De Meo A, Guillem JG: Современное лечение рака прямой кишки: обновление 2006 года.World J Gastroenterol 12 (20): 3186-95, 2006. [PUBMED Abstract]
- Вейзер М.Р., Ландманн Р.Г., Вонг В.Д. и др.: Хирургическое спасение рецидивирующего рака прямой кишки после трансанального иссечения. Dis Colon Rectum 48 (6): 1169-75, 2005. [PUBMED Abstract]
- Fujita S, Nakanisi Y, Taniguchi H, et al .: Инвазия рака в сплетение Ауэрбаха является важным прогностическим фактором у пациентов с колоректальным синдромом pT3-pT4. рак. Dis Colon Rectum 50 (11): 1860-6, 2007. [PUBMED Abstract]
- Griffin MR, Bergstralh EJ, Coffey RJ, et al.: Предикторы выживаемости после радикальной резекции рака толстой и прямой кишки. Cancer 60 (9): 2318-24, 1987. [PUBMED Abstract]
- DeVita VT Jr, Lawrence TS, Rosenberg SA: Рак: принципы и практика онкологии. 9 изд. Филадельфия, Пенсильвания: Lippincott Williams & Wilkins, 2011.
- Wieder HA, Rosenberg R, Lordick F и др.: Рак прямой кишки: МРТ перед неоадъювантной химиотерапией и лучевой терапией для прогнозирования границ периферической резекции без опухолей и в долгосрочной перспективе выживание.Radiology 243 (3): 744-51, 2007. [PUBMED Abstract]
- Gunderson LL, Sargent DJ, Tepper JE, et al .: Влияние стадий T и N и лечения на выживаемость и рецидив адъювантного рака прямой кишки: объединенный анализ. J Clin Oncol 22 (10): 1785-96, 2004. [PUBMED Abstract]
- McLeod HL, Murray GI: Онкологические маркеры прогноза колоректального рака. Br J Cancer 79 (2): 191-203, 1999. [PUBMED Abstract]
- Jen J, Kim H, Piantadosi S, et al .: Аллельная потеря хромосомы 18q и прогноз при колоректальном раке.N Engl J Med 331 (4): 213-21, 1994. [PUBMED Abstract]
- Lanza G, Matteuzzi M, Gafá R, et al .: Утрата аллеля хромосомы 18q и прогноз при II и III стадии рака толстой кишки. Int J Cancer 79 (4): 390-5, 1998. [PUBMED Abstract]
- Roth JA: прогноз p53: парадигма или парадокс? Clin Cancer Res 5 (11): 3345, 1999. [ОПУБЛИКОВАННЫЙ РЕЗЮМЕ]
- Нишио Х., Хамади З.З., Малик Х.З. и др .: Результат повторной резекции печени по поводу колоректальных метастазов в печень. Eur J Surg Oncol 33 (6): 729-34, 2007.[PUBMED Abstract]
- Эдлер Д., Халлстрём М., Джонстон П.Г. и др.: Экспрессия тимидилатсинтазы: независимый прогностический фактор для местного рецидива, отдаленных метастазов, безрецидивной и общей выживаемости при раке прямой кишки. Clin Cancer Res 6 (4): 1378-84, 2000. [PUBMED Abstract]
- Popat S, Chen Z, Zhao D, et al .: проспективный слепой анализ экспрессии тимидилатсинтазы и p53 как прогностических маркеров в адъюванте. лечение колоректального рака. Энн Онкол 17 (12): 1810-7, 2006.[PUBMED Abstract]
- Gryfe R, Kim H, Hsieh ET, et al .: микросателлитная нестабильность опухоли и клинические исходы у молодых пациентов с колоректальным раком. N Engl J Med 342 (2): 69-77, 2000. [PUBMED Abstract]
- Liersch T., Langer C., Ghadimi BM, et al .: Состояние лимфатических узлов и экспрессия гена TS являются прогностическими маркерами при ректальной стадии II / III. рак после неоадъювантной химиолучевой терапии на основе фторурацила. J Clin Oncol 24 (25): 4062-8, 2006. [PUBMED Abstract]
- Ghadimi BM, Grade M, Difilippantonio MJ, et al.: Эффективность профилирования экспрессии генов для прогнозирования ответа аденокарциномы прямой кишки на предоперационную химиолучевую терапию. J Clin Oncol 23 (9): 1826-38, 2005. [PUBMED Abstract]
- Dignam JJ, Ye Y, Colangelo L, et al .: Прогноз после рака прямой кишки у чернокожих и белых, участвующих в рандомизированных испытаниях адъювантной терапии. J Clin Oncol 21 (3): 413-20, 2003. [PUBMED Abstract]
- Abir F, Alva S, Longo WE и др .: Послеоперационное наблюдение за пациентами с раком толстой и прямой кишки.Am J Surg 192 (1): 100-8, 2006. [PUBMED Abstract]
- Martin EW, Minton JP, Carey LC: CEA-направленная вторичная хирургия у бессимптомного пациента после первичной резекции колоректальной карциномы. Ann Surg 202 (3): 310-7, 1985. [PUBMED Abstract]
- Bruinvels DJ, Stiggelbout AM, Kievit J, et al .: Последующее наблюдение за пациентами с колоректальным раком. Метаанализ. Ann Surg 219 (2): 174-82, 1994. [PUBMED Abstract]
- Lautenbach E, Forde KA, Neugut AI: Преимущества колоноскопического наблюдения после лечебной резекции колоректального рака.Ann Surg 220 (2): 206-11, 1994. [PUBMED Abstract]
- Хури Д.А., Опелька Ф.Г., Бек Д.Е. и др.: Наблюдение за толстой кишкой после хирургии колоректального рака. Dis Colon Rectum 39 (3): 252-6, 1996. [PUBMED Abstract]
- Пьетра Н., Сарли Л., Кости Р. и др .: Роль последующего наблюдения в лечении местных рецидивов колоректального рака: перспективы, рандомизированное исследование. Dis Colon Rectum 41 (9): 1127-33, 1998. [PUBMED Abstract]
- Secco GB, Fardelli R, Gianquinto D, et al .: Эффективность и стоимость последующего наблюдения с учетом риска у пациентов после хирургии колоректального рака: проспективное, рандомизированное и контролируемое исследование.Eur J Surg Oncol 28 (4): 418-23, 2002. [PUBMED Abstract]
- Pfister DG, Benson AB, Somerfield MR: Клиническая практика. Стратегии наблюдения после лечения колоректального рака. N Engl J Med 350 (23): 2375-82, 2004. [PUBMED Abstract]
- Li Destri G, Di Cataldo A, Puleo S: Последующее наблюдение за колоректальным раком: полезно или бесполезно? Surg Oncol 15 (1): 1-12, 2006. [PUBMED Abstract]
- Kapiteijn E, Kranenbarg EK, Steup WH, et al .: Тотальное мезоректальное иссечение (TME) с предоперационной лучевой терапией или без нее при лечении первичного рака прямой кишки .Проспективное рандомизированное исследование со стандартными оперативными и гистопатологическими методами. Голландская группа рака прямой кишки. Eur J Surg 165 (5): 410-20, 1999. [PUBMED Abstract]
- Grossmann I, de Bock GH, Meershoek-Klein Kranenbarg WM, et al .: Измерение карциноэмбрионального антигена (CEA) во время наблюдения за карциномой прямой кишки полезен, даже если до операции был нормальный уровень. Ретроспективное исследование значений CEA в исследовании TME. Eur J Surg Oncol 33 (2): 183-7, 2007. [PUBMED Abstract]
Коэффициент выживаемости при раке: инструмент для понимания вашего прогноза
Показатель выживаемости при раке: что это означает для вашего прогноза
Узнайте, что показатель выживаемости может вам сказать, а что нет.Это может помочь вам увидеть статистику выживаемости в перспективе.
Персонал клиники Мэйо
Когда впервые диагностируют рак, многие люди спрашивают о своем прогнозе. Возможно, вы захотите узнать, лечить ли ваш рак относительно легко или труднее. Ваш врач не может предсказать будущее, но может сделать оценку, основываясь на опыте других людей с тем же раком.
Что такое выживаемость при раке?
Показатели выживаемости при раке или статистика выживаемости показывают процент людей, которые выживают при определенном типе рака в течение определенного периода времени.Статистика рака часто использует общую пятилетнюю выживаемость.
Выживаемость обычно указывается в процентах. Например, общая пятилетняя выживаемость при раке мочевого пузыря составляет 77 процентов. Это означает, что из всех людей, страдающих раком мочевого пузыря, 77 из 100 живут пять лет после постановки диагноза. И наоборот, 23 из 100 умирают в течение пяти лет после постановки диагноза рака мочевого пузыря.
Показатели выживаемости при раке основаны на исследованиях, собранных на основе информации о сотнях или тысячах людей с определенным раком.Общая выживаемость включает людей всех возрастов и состояний здоровья, которым был поставлен диагноз рака, включая тех, кто диагностирован очень рано, и тех, кто диагностирован очень поздно.
Ваш врач может предоставить вам более конкретную статистику в зависимости от стадии рака. Например, 56 процентов, или чуть более половины, людей, у которых диагностирована ранняя стадия рака легких, живут не менее пяти лет после постановки диагноза. Пятилетняя выживаемость для людей, у которых диагностирована поздняя стадия рака легких, который распространился (метастазировал) в другие области тела, составляет 5 процентов.
Общие коэффициенты выживаемости не указывают, продолжают ли выжившие после рака проходить лечение через пять лет или они избавились от рака (достигли ремиссии). Другие типы показателей выживаемости, которые дают более конкретную информацию, включают:
- Выживаемость без болезней. Это количество людей, у которых после лечения нет признаков рака.
- Выживаемость без прогрессирования. Это количество людей, которые прошли курс лечения от рака и у которых либо не было признаков рецидива рака, либо у которых рак оставался стабильным, но не увеличивался.
Для оценки выживаемости при раке часто используется пятилетняя выживаемость. Это не значит, что рак не может повториться дольше пяти лет. Некоторые виды рака могут повторяться через много лет после обнаружения и лечения. Для некоторых видов рака, если он не рецидивировал в течение пяти лет после первоначального диагноза, вероятность повторного рецидива очень мала. Обсудите с врачом риск рецидива рака.
Как используются показатели выживаемости при раке?
Вы и ваш врач можете использовать статистику выживаемости для:
- Узнайте свой прогноз. Опыт других людей в той же ситуации может дать вам и вашему врачу представление о вашем прогнозе — шансах на выздоровление от рака. К другим факторам относятся возраст и общее состояние здоровья. Ваш врач использует эти факторы, чтобы помочь вам понять серьезность вашего состояния.
Разработайте план лечения. Статистика также может показать, как люди с таким же типом и стадией рака реагируют на лечение. Вы можете использовать эту информацию вместе со своими целями лечения, чтобы взвесить все за и против каждого варианта лечения.
Например, если два лечения дают вам одинаковые шансы на ремиссию, но у одного больше побочных эффектов, вы можете выбрать вариант с меньшим количеством побочных эффектов.
В другом примере лечение может дать шанс на излечение, но только для 1 или 2 человек из 100. Для некоторых эти шансы достаточно многообещающие, чтобы мириться с побочными эффектами. Для других шанс на излечение не стоит побочных эффектов лечения.
Ваш врач может помочь вам понять преимущества и риски каждого лечения.
Чего вам не могут сказать показатели выживаемости при раке?
Статистика выживаемости при раке может разочаровывать. Выживаемость людей с вашим конкретным раком может быть основана на тысячах людей. Таким образом, хотя показатели выживаемости при раке могут дать общее представление о большинстве людей в вашей ситуации, они не могут дать вам индивидуальных шансов на излечение или ремиссию. По этой причине некоторые люди игнорируют статистику выживаемости от рака.
Статистика выживания не учитывает другие ваши заболевания.Если ваше здоровье в остальном идеальное, у вас, вероятно, будет больше шансов на выживание, чем предполагает статистика.
Если у вас есть другие очень серьезные заболевания, у вас может не быть шансов на выживание, о которых свидетельствует статистика. Ваш врач может помочь скорректировать статистику для вашей конкретной ситуации.
У выживаемости есть и другие ограничения. Например, они не могут:
- Дайте вам информацию о последних методах лечения. Люди, включенные в последнюю статистику рака, были диагностированы более пяти лет назад.Последствия любых недавних открытий в области лечения не повлияют на статистику выживаемости как минимум в течение пяти лет.
- Подскажите, какое лечение выбрать. Это зависит от вас и вашего врача. Для некоторых людей лечение с наибольшим шансом на ремиссию — это то, что они выберут. Но многие люди принимают во внимание другие факторы, такие как побочные эффекты, стоимость и график лечения.
Вы можете игнорировать показатели выживаемости при раке
Вам решать, хотите ли вы знать показатели выживаемости, связанные с вашим типом и стадией рака.Поскольку показатели выживаемости не могут рассказать вам о вашей ситуации, вы можете найти статистику безличной и бесполезной. Но некоторые люди хотят знать о своем раке все, что могут. По этой причине вы можете знать всю необходимую статистику.
Более подробная информация о своем раке может уменьшить ваше беспокойство по мере того, как вы анализируете возможные варианты и начинаете лечение, но статистика выживаемости может сбивать с толку и пугать. Сообщите своему врачу, если вы не хотите обращать внимание на цифры.Некоторые люди предпочитают знать «общую картину», а не подробную статистику. Сообщите своему врачу, как вы предпочитаете получать информацию. А если у вас есть какие-либо вопросы или опасения по поводу статистики, связанной с вашим раком, поговорите со своим врачом.
21 января 2020 г.
Показать ссылки
- Понимание прогноза рака. Национальный институт рака. https://www.cancer.gov/about-cancer/diagnosis-staging/prognosis. Доступ 9 января 2018 г.
- Факты и цифры о раке 2019.Американское онкологическое общество. https://www.cancer.org/research/cancer-facts-statistics/all-cancer-facts-figures/cancer-facts-figures-2019.html. По состоянию на 30 декабря 2019 г.
- Понимание статистики, используемой для прогнозирования и оценки лечения. Cancer.Net. https://www.cancer.net/navigating-cancer-care/cancer-basics/understanding-statistics-used-guide-prognosis-and-evaluate-treatment. Доступ 9 января 2018 г.
Узнать больше Подробно
.
Патологическая оценка рака прямой кишки после неоадъювантной радиотерапии (химиотерапии): прогностическое значение
Неоадъювантная радиотерапия (химиотерапия) все чаще используется при раке прямой кишки и вызывает ряд морфологических изменений, которые влияют на прогноз после лечебной хирургии, тем самым создавая новые проблемы для хирургические патологи, особенно при оценке морфологических изменений и реакции опухоли на предоперационное лечение. Хирургические патологи играют важную роль в определении многих аспектов ухода за пациентами с карциномой прямой кишки после неоадъювантного лечения.Они варьируются от правильного обращения с макроскопическими образцами до точной микроскопической оценки патологических особенностей, связанных с прогнозом пациентов. В этом обзоре представлены хорошо установленные патологические прогностические индикаторы и обсуждаются сложные особенности, чтобы предоставить как хирургическим патологам, так и лечащим врачам контрольный список, полезный в неоадъювантных условиях.
1. Введение
Предоперационная лучевая терапия с химиотерапией (РКИ) или без нее с последующим полным мезоректальным иссечением (ТМЭ) стала стандартным методом лечения местно-распространенного рака прямой кишки [1–4].Все более широкое использование РКИ при раке прямой кишки создает новые проблемы для хирургических патологов, особенно в оценке морфологических изменений и реакции опухоли на предоперационное лечение. Были предложены различные системы для оценки ответа опухоли на РКИ [5–10]. Однако большинство этих систем не всегда коррелируют с прогнозом [11–14], и их воспроизводимость низкая [11, 15–17]. Кроме того, РКИ изменяет макроскопическую и микроскопическую оценку и прогностическую значимость нескольких хорошо известных патологических признаков (т.э., опухоль и узловая стадия, периферический край резекции и лимфоваскулярная инвазия) [18–20]. Например, проблема возникает, когда при макроскопическом исследовании не удается идентифицировать оставшиеся опухоли. В этом контексте точная стадия патологической опухоли (ypT) зависит от того, насколько усердно патологи ищут остаточную опухоль, а также от количества обработанных блоков и слайдов. Кроме того, РКИ может значительно уменьшить количество извлеченных лимфатических узлов [19]. Это могло вызвать недооценку узлового статуса при отсутствии тщательного поиска лимфатических узлов.Споры также сохраняются относительно оптимальных дистальных и периферических краев [21–28]. Таким образом, патологоанатомы играют важную роль в определении многих аспектов ухода за пациентами с карциномой прямой кишки после неоадъювантного лечения. Они варьируются от правильного обращения с макроскопическими образцами до точной микроскопической оценки патологических особенностей, связанных с прогнозом пациентов.
Цель этого обзора — представить хорошо установленные патологические прогностические индикаторы и обсудить сложные особенности, особенно те, которые имеют клиническое значение, чтобы предоставить контрольный список, который будет полезен в неоадъювантных условиях как для хирургических патологов, так и для лечащих врачей.
2. Макроскопическая оценка образца TME
Техника TME основана на резком рассечении бессосудистой плоскости между вегетативными нервными сплетениями и мезоректумом. Эта операция приводит к иссечению прямой кишки, покрытой мезоректальным жировым столбиком от 2 до 3 см. В этой части обзора представлены методы оценки качества мезоректума, периферического края резекции (CRM), дистального края резекции и лимфатических узлов.
2.1. Оценка обращения с образцами Mesorectum
TME начинается с оценки качества мезоректума (Таблица 1) [29].Осмотр мезоректальной поверхности дает первое представление о ее качестве. Нарезка опухоли и мезоректума на всю толщину позволяет оценить адекватность удаления и регулярность CRM, что является вторым показателем качества резекции.
| ||||||||||||||||||||||||||||||||
| CRM, периферический край резекции. Для достижения оптимальной оценки исследуют как весь свежий образец, так и фиксированные формалином срезы. | ||||||||||||||||||||||||||||||||
2.2. Обработка образцов
Quirke et al. [29] и Nagtegaal et al. [30] разработали подход к оценке и обработке образца TME. Эта оценка выполняется путем прямого визуального осмотра свежего образца; передняя и задняя плоскости мезоректума фотографируются, чтобы документировать их гладкость или неровность.Затем наносится мезоректальный жир; Следует проявлять осторожность, чтобы не наносить мазки на перитонеализированные поверхности образца, особенно спереди, где серозная оболочка простирается ниже, так как это может привести к возникновению артефактов и затруднить интерпретацию серозного поражения опухолями верхней прямой кишки, которые расположены по окружности или спереди. [31]. Затем образец измеряется и разрезается вдоль передней поверхности сверху, при этом кишечник остается неповрежденным на уровне чуть выше перитонеального отражения.После помещения свободных, пропитанных формалином марлевых фитилей в неоткрытый сегмент прямой кишки, образец следует под натяжением прикрепить булавками к пробковой доске для минимизации усадки [32]. После оптимальной фиксации не менее 72 часов неоткрытый сегмент разрезают поперечно с интервалами 5 мм, чтобы определить область наиболее глубокой инвазии, и срезы снова фотографируют, чтобы записать качество иссеченного мезоректума, опухоли. размер, локализация и расстояние до всех хирургических полей.Что касается отбора образцов опухоли, то руководство Бельгийского проекта по раку прямой кишки (PROCARE; http://www.kankerregister.org/), адаптированное из Quirke et al. [29] и Nagtegaal et al. [30], предлагает взять пять начальных блоков с места опухоли или подозрительной области. В случаях с очевидным макроскопическим остатком опухоли, помимо взятия поверхностной и самой глубокой части опухоли, необходимо сделать срезы, показывающие наиболее близкую связь опухоли с CRM или поверхностью брюшины, а также те, которые содержат переход от подозрительных мезоректальных узлов к CRM. принято, поскольку это позволяет правильно оценить другие патологические прогностические параметры [33].Когда при макроскопическом исследовании обнаруживаются только пулы муцина, для точного определения стадии необходимо брать пробы из всей подозрительной зоны, поскольку в большинстве случаев при микроскопическом исследовании могут присутствовать остаточные жизнеспособные опухолевые клетки [7]. Очевидно, что патолог должен быть проинформирован о точном местонахождении опухоли до РКИ, чтобы эффективно проводить отбор образцов ткани.
Рекомендуемый метод взятия образцов опухоли и исследования карциномы прямой кишки после ради (химиотерапии) и хирургического вмешательства заключается в следующем.
Шаг 1. Возьмите 5 блоков от опухоли или рубцовой области (при условии, что явных опухолей не было обнаружено крупно). Они должны включать поверхностную и глубокую части опухоли, а также взаимосвязь между опухолью и CRM или перитонеальной поверхностью. Если есть какие-либо мезоректальные узелки, следует также взять блоки, содержащие их отношение к CRM.
Шаг 2. Если жизнеспособная микроскопическая опухоль не идентифицирована в пределах начальных 5 блоков, следует взять образец из всей рубцовой области.
Шаг 3. Если после исследования участков дополнительных блоков не обнаружено остаточной опухоли, необходимо прорезать три уровня в каждом блоке. Если жизнеспособные опухолевые клетки отсутствуют даже после тщательного изучения этих участков, можно обоснованно и надежно сообщить о полном патологическом ответе или ypT0.
2.3. Дистальный край
Дистальный край, хотя и менее важен, чем CRM с точки зрения частоты вовлечения и влияния на рецидив, все же важен для оценки.При рассмотрении дистального края следует иметь в виду две проблемы: степень непрерывного роста опухоли в интрамуральном и экстрамуральном направлениях и прерывистое распространение дистальной мезоректальной области через лимфатические сосуды. В 20% случаев с положительными узлами наблюдается лимфатическое распространение дистальнее первичной опухоли. Более того, во многих случаях эти положительные дистальные узлы расположены на расстоянии> 2 см от основной массы опухоли [34]. Напротив, интрамуральное дистальное распространение> 2 см наблюдается только в 3,6% случаев [35]. Zhao et al.[36] обнаружили, что частота дискретных опухолевых отложений в дистальном отделе мезоректума составляла 17,8% и что степень распространения дистального мезоректального отдела была больше, чем степень распространения внутримурально. На основании своих данных они пришли к выводу, что для достижения адекватного хирургического зазора необходимы дистальный край ректальной стенки 1,5 см и дистальный мезоректальный край 4 см. Тем не менее, во многих случаях оказалось, что дистальный край стенки прямой кишки менее 1 см достаточен для предотвращения местного рецидива, особенно в опухолях, ограниченных стенкой прямой кишки [37, 38].
Еще одна проблема, которую следует иметь в виду при измерении дистального края, — это артефакт усадки. Goldstein et al. [39] показали, что длина толстой и прямой кишки 5 см in vivo эквивалентна 3 см после резекции и 2,2 см после фиксации. Это еще раз подчеркивает важность прикрепления образца к пробковой доске для уменьшения степени усадки.
2.4. Поиск лимфатических узлов
Статус лимфатических узлов, вероятно, представляет собой единственный наиболее важный прогностический фактор у пациентов с раком прямой кишки, независимо от того, лечили ли они до операции или нет [40, 41].Международные руководящие принципы рекомендуют, чтобы для адекватного определения стадии CRC необходимо не менее 12 лимфатических узлов [42, 43]. Тем не менее, были доказательства того, что предоперационное РКИ при раке прямой кишки может снизить выход лимфатических узлов примерно на 33% [19, 44]. Несмотря на это открытие, необходимо поддерживать высокую мотивацию для извлечения как можно большего количества узлов, поскольку несколько исследований подтверждают концепцию, согласно которой чем больше узлов проверяется, тем точнее этапы. Более того, отношение количества извлеченных положительных узлов к общему количеству извлеченных узлов, так называемое соотношение метастатических лимфатических узлов, оказалось еще более значимым, связанное с местным рецидивом и выживаемостью [45–47].Ряд дополнительных методов, включая лечение алкоголем, клиренс ксилола и методы на основе эфира, был разработан для решения проблемы выхода лимфатических узлов, но для большинства из них требуется специальное оборудование или использование вредных летучих соединений [48–50] . Поэтому во многих лабораториях патологии рутинный визуальный осмотр, пальпация и диссекция по-прежнему являются стандартом практики извлечения лимфатических узлов, а тщательное обследование, а также энтузиазм исследователя являются одним из наиболее важных факторов при определении количества лимфатических узлов.
Еще раз, важно подчеркнуть, что латеральная мезоректальная поверхность, ближайшая к подозрительным узлам, должна быть взята вместе с узлами, чтобы обеспечить точную оценку CRM [33]. Таким образом, ориентация подозрительных периректальных узелков, которые тесно связаны с CRM, должна быть хорошо сохранена во время процесса разрезания, в то время как обычно выглядящие лимфатические узлы могут быть извлечены обычным способом, стараясь не пересчитывать узлы, которые появляются в более чем один ломтик из-за последовательной поперечной нарезки.
3. Микроскопическая оценка
3.1. Гистологический тип опухоли
В патологических отчетах о колоректальном раке (CRC) международно признанная гистологическая классификация колоректальных карцином, предложенная Всемирной организацией здравоохранения [51] (ВОЗ), рекомендована Коллегией американских патологов (CAP) [52] . Согласно этой классификации, большинство рака прямой кишки представляют собой аденокарциномы без особого типа. За некоторыми исключениями, гистологический тип не имеет независимого от стадии прогностического значения [52].Исключение составляют опухоли, не образующие железы, такие как карцинома из перстневых клеток, мелкоклеточная карцинома и недифференцированная карцинома, которые являются прогностически неблагоприятными [53–55], и медуллярная карцинома, которая является прогностически благоприятной [56]. В отличие от результатов нескольких исследований, в основном ограниченных однофакторным анализом, предполагающих, что муцинозная аденокарцинома может быть неблагоприятным прогностическим фактором [57–60], более крупные исследования не подтвердили, что гистология муцина является независимым от стадии предиктором неблагоприятного исхода [ 61–66].С другой стороны, муцинозная карцинома имеет тенденцию быть прогностически благоприятной, если связана с микросателлитной нестабильностью (MSI) [67–69].
Таким образом, на основании имеющихся данных можно сделать вывод, что единственными гистологическими типами CRC, которые являются прогностически значимыми, являются карцинома с перстневым кольцом и мелкоклеточная карцинома (плохой прогноз), а также медуллярная и связанная с MSI муцинозная карцинома (благоприятный прогноз). ).
3.2. Степень дифференциации опухоли
В классификации ВОЗ [70] классификация колоректальной аденокарциномы основана на степени образования железы.Следовательно, гистологические типы, не образующие железы (например, карцинома с печаткой, мелкоклеточная и недифференцированная карцинома) всегда считаются высокодифференцированными или низкодифференцированными опухолями. В большинстве случаев, однако, оценка степени железистого образования является субъективной, что приводит к вариациям между наблюдателями, главным образом в классификации хорошо и умеренно дифференцированных опухолей. Отсутствие единообразия в гистопатологической классификации еще больше усложняется наличием ряда различных систем классификации, по которым патологи не пришли к единому мнению [52, 71–73].В настоящее время имеющихся данных недостаточно для поддержки одного подхода по сравнению с другим, и этот вопрос остается проблемным. Независимо от сложности критериев, большинство систем разделяют аденокарциномы на четыре степени: (i) степень 1: хорошо дифференцированная (> 95% железистых образований), (ii) степень 2: умеренно дифференцированная (50–95% железистых образований), (iii) Степень 3: слабо дифференцированная (5-50% железистых образований), (iv) Степень 4: недифференцированная (<5% железистых образований). Тем не менее, самая последняя серия Всемирной организации здравоохранения по опухолям пищеварительной системы рекомендует использовать двухуровневая система классификации (низкая или высокая степень) при оценке колоректального рака [74].Несмотря на различия между наблюдателями в оценке и отсутствие стандартизации, гистологический класс неоднократно показывался с помощью многофакторного анализа как независимый от стадии прогностический фактор в неоадъювантной обстановке [75–77]. Однако после РКИ его влияние на выживаемость пациентов остается спорным [5, 11, 13, 78–80].
3.3. Лимфоваскулярная и периневральная инвазия
Прогностическое значение лимфоваскулярной (LVI) и периневральной (PNI) инвазии было высказано и в значительной степени подтверждено в неоадъювантных условиях [76, 77, 81–84].Венозная инвазия была продемонстрирована многочисленными многомерными анализами как независимый неблагоприятный прогностический фактор при CRC [76, 77, 81, 82, 85–87]. В серии исследований, идентифицирующих точное расположение вовлеченных сосудов (то есть заочное, а не интрамуральное расположение), было обнаружено, что заочный тип наиболее предсказуем для выживаемости [87–89]. В некоторых исследованиях LVI, без различия между венозными и лимфатическими сосудами, оказался прогностически значимым [81, 90]. О более противоречивых результатах сообщалось только при инвазии лимфатических сосудов [91, 92].Вероятно, что различия между существующими исследованиями сосудистой инвазии связаны с внутренними проблемами в патологической идентификации этой особенности. Окончательный диагноз сосудистой инвазии требует идентификации опухоли в канале, выстланном эндотелием. Однако это может быть затруднительно при наличии фиброза сосудов или деструкции эндотелия, вызванного опухолью. Кроме того, артефакт фиксации в опухоли может имитировать поражение мелких сосудов. По этим причинам различия между наблюдателями могут быть существенными в интерпретации или распознавании сосудистой инвазии.Дополнительные ограничения при обнаружении инвазии сосудов связаны с отбором образцов. Например, было показано, что воспроизводимость выявления экстрамуральной венозной инвазии увеличивается пропорционально с 59% при исследовании 2 блоков ткани на периферии опухоли до 96% при исследовании 5 блоков [89, 93, 94]. В других исследованиях было высказано предположение, что использование различных типов тканевых блоков, таких как тангенциальные, в дополнение к перпендикулярным блокам, увеличивает шансы обнаружения инвазии вне вены [94, 95].
После предоперационного РКИ прогностическое значение LVI и PNI было продемонстрировано в нескольких исследованиях, в основном с помощью одномерного анализа [96–98]. Исследование Du et al. [97] показали, что прогрессирование заболевания у пациентов с LVI в облученных опухолях было значительно замедлено по сравнению с таковым с LVI-положительными опухолями в необлученных опухолях. Они предположили, что агрессивность этих опухолевых клеток в крови или лимфатических сосудах могла быть значительно ослаблена лучевой терапией, хотя они не были полностью устранены.В этом отношении независимое от стадии прогностическое влияние LVI и PNI после РКИ необходимо подтвердить в более крупных исследованиях с многофакторным анализом.
3.4. Опухолевые отложения (TD)
Опухолевые отложения (TD) — это отдельные узелки аденокарциномы, обнаруживаемые в периколонической и периректальной жировой ткани во время рутинного гистопатологического исследования образцов продвинутого CRC. Их распространенность в мезоректуме колеблется от 6% до 64% [99–101]. TD являются гистологически гетерогенными и могут быть связаны с несколькими типами распознаваемых анатомических структур, таких как вены, лимфатические сосуды и нервы, тогда как в других случаях клетки карциномы наблюдаются разбросанными в небольших агрегатах в периректальной жировой ткани.Это может объяснить различные классификации, которым TD подвергались с течением времени [102–104], особенно в классификационной серии TNM. Таблица 2 суммирует основные изменения в последних четырех редакциях классификации TNM для колоректального рака.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ITC, изолированные опухолевые клетки. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
TNM5 ввел правило 3 мм, что привело к классификации, основанной исключительно на размере, независимо от гистологических особенностей. Соответственно, агрегаты прерывистых мезоректальных опухолевых клеток рассматривались как первичные опухоли (категория pT) при измерении ≤3 мм или как метастазы в лимфатические узлы (категория pN), если> 3 мм [105].
В TNM6 критерий размера заменен критерием формы. Основываясь на этой классификации, прерывистые мезоректальные опухолевые узелки считались венозными инвазиями, если они имеют неправильный контур, и метастазами в регионарные лимфатические узлы, если они имеют форму и гладкий контур лимфатического узла [106].
Эти две классификации имеют ограниченную ценность, поскольку классификации TD основаны на единственном морфологическом критерии (например, размере или форме). Более того, правило 3 мм было основано на неопубликованных данных, которые впоследствии не были подтверждены [102, 107], а критерий формы недостаточен, чтобы последовательно различать различные типы опухолевого поражения перивисцерального жира [108], являясь источником взаимных наблюдений. вариация [107]. В 2009 году Puppa et al. [103] предложили новую категоризацию ПД: (i) тип сосудистой инвазии (экстрамуральная венозная или лимфатическая инвазия): категория pT, (ii) тип несосудистой инвазии (гладкий контур, окруженный лимфоцитами, не связанный с венами или нервы): категория pN, (iii) агрессивные TD (картина рассеяния, не окруженная лимфоцитами, имеющая тесную связь с крупными сосудами или нервной инвазией): pM1a (транзитные метастазы).TNM7 снова внес изменения, касающиеся определения и классификации TD. В последнем издании дискретные очаги опухоли, обнаруженные в перивисцеральной жировой клетчатке или в прилегающей брыжейке вдали от переднего края опухоли и не показывающие признаков остаточной ткани лимфатических узлов, рассматриваются как TD. Если TD наблюдаются в поражениях, которые иначе классифицировались бы как T1 или T2, тогда классификация первичной опухоли не изменяется, но узел классифицируется в категории N1c [109].
Кажется, что разные редакции TNM заменяют одно субъективное определение другим.Более того, похоже, что они не проспективно тестировали эту новую классификацию TD и не оценивали ее воспроизводимость, поскольку TNM7 утверждает, что перивисцеральный узелок следует регистрировать как положительный лимфатический узел, если патолог считает узелок полностью замещенным лимфатическим узлом ( обычно имеющий ровный контур) [109].
Таким образом, хотя существующие классификации ПД нуждаются в дальнейшем улучшении с точки зрения воспроизводимости и прогностической стратификации, результаты большинства исследований пациентов, не получавших предоперационные РКИ, показали худший прогноз для пациентов с ПД: увеличение частоты местных рецидивов, усиление развития отдаленных метастазы и снижение выживаемости [107].В исследованиях Ratto et al. [99, 110], которые изучили частоту и прогностическое влияние TD в образцах рака прямой кишки после РКИ, TD встречались в 15,40% случаев, и их присутствие было связано с уменьшением безрецидивной и общей выживаемости. Напротив, Нагтегал и Квирке [107] и Квирке и др. [111] считали наличие ПД признаком хорошего ответа на РКИ. Остается под вопросом, является ли наличие ПД после РКИ независимым от стадии предиктором неблагоприятного исхода. В повседневной практике присутствие ПД должно быть включено в отчет о патологии с указанием их общего количества, размера и характера роста, чтобы создать более однородные группы пациентов для включения в клинические испытания [112].
3.5. Патологическая стадия
Патологическая стадия после полной резекции долгое время считалась наиболее сильным прогностическим индикатором при CRC [113]. То же самое можно сказать и о карциноме прямой кишки после предоперационного РКИ [114–116]. Хотя на протяжении многих лет для CRC было разработано большое количество систем стадирования, система стадирования метастазирования опухолевых узлов (TNM) Американского объединенного комитета по раку (AJCC) и Международного союза против рака (UICC), безусловно, является наиболее широко рекомендуемой.В таблице 2 перечислены основные изменения, внесенные в последние четыре редакции [109, 113, 117]. 7-е издание TNM подверглось критике, прежде всего, за новую классификацию TD, которой не хватает как научных доказательств, так и воспроизводимости [118, 119]. При сообщении CRC некоторые центры предпочитают 5-е издание классификации TNM другим редакциям, в основном из-за воспроизводимости классификации TD [118, 120]. Тем не менее, для будущей оценки прогностической значимости изменений в классификации TNM следует использовать 7-е издание, а о конфликтующей характеристике, то есть TD, следует подробно сообщить с описанием их количества, размера и модели роста.
Для точного определения стадии пролеченной карциномы прямой кишки важно помнить, что, когда микроскопические остатки опухоли не обнаружены, необходимо полностью взять образец из рубцовой области [73, 120]. Более того, если жизнеспособная опухоль отсутствует даже после исследования срезов всей рубцовой области, необходимо прорезать три уровня в каждом блоке, чтобы исключить остаточные опухолевые очаги, как было предложено в исследовании CORE фазы II [121].
3.6. Бесклеточный муцин (aMUC)
При рутинном микроскопическом исследовании образцов карциномы прямой кишки, подвергнутых неоадъювантному лечению, пулы слизи можно обнаружить в одной трети случаев [122, 123].В связи с этим несколько недавних исследований продемонстрировали, что присутствие бесклеточного муцина (aMUC) при карциноме прямой кишки после неоадъювантного РКИ не оказало значительного влияния на исход лечения пациентов [122, 124, 125]. де Кампос-Лобато и др. изучили прогностическую ценность aMUC у пациентов с раком прямой кишки, достигших ypT0 после предоперационного РКИ, и пришли к выводу, что aMUC не влияет на местный рецидив, но может указывать на более агрессивную биологию опухоли [125]. Эти данные подтверждают текущее консенсусное утверждение CAP о том, что внеклеточные пулы муцина не следует рассматривать как остаточную опухоль и что их присутствие следует регистрировать отдельно от категории ypT [122].
3,7. Местный воспалительный ответ
Воспалительный инфильтрат, связанный с опухолью, долгое время считался типом ответа хозяина и важным прогностическим фактором при раке прямой кишки [126, 127]. После предоперационного РКИ рак прямой кишки мог подвергнуться регрессии опухоли за счет уничтожения клеток карциномы и замещения фиброзными или фибровоспалительными тканями [123, 128, 129]. Nagtegaal et al. [130] и Shia et al. [123] обнаружили, что у пациентов с обширным фибровоспалительным инфильтратом вокруг опухоли частота рецидивов ниже.Два недавних исследования Debucquoy et al. [128, 129] показали лучшую выживаемость без признаков заболевания у пациентов с раком прямой кишки, у которых образцы TME содержали фибровоспалительные изменения после РКИ (рис. 1). В целом, заметный воспалительный клеточный компонент обычно не наблюдается в опухолях прямой кишки после лечения [123, 128, 129]. Shia et al. [123] сообщили, что в 60% случаев воспалительная инфильтрация была минимальной. Эти данные свидетельствуют о нарушении или подавлении иммунной функции у пациентов, получавших РКИ. Соответственно, можно предположить, что пациенты, у которых сохраняется более обширный воспалительный ответ в ложе опухоли после РКИ, имеют лучший результат, и этот фактор имеет значение для оценки прогноза этих пациентов [123, 128, 129].
3.8. Оценка терапевтического ответа
Ответ на РКИ варьируется от минимального лечебного эффекта до полного уничтожения первичной опухоли. Некоторые авторы использовали классификацию клеточного ответа, основанную на количестве остаточной жизнеспособной опухоли по отношению к фиброзу стромы [5-8, 16, 131], тогда как другие исследовали сдвиг стадии в обработанных образцах, включая стадию опухоли и узлового уровня, когда оценка ответа [11, 132, 133]. На сегодняшний день ни одна из систем оценки клеточного ответа не получила всеобщего признания [11, 134] не только потому, что большинство из них не могло последовательно предсказать исход болезни пациента [11–14], но также потому, что их воспроизводимость низкая, особенно для категорий. определение умеренных и минимальных регрессионных изменений [11, 15–17].С другой стороны, оценка понижения сцены объективна и воспроизводима. Более того, было последовательно продемонстрировано, что снижение стадии значительно коррелирует с улучшением выживаемости [11, 128, 129, 135]. Тем не менее, ни одно исследование не изучало прогностическое влияние как градации клеточного ответа, так и понижения стадии в одной и той же когорте. В некоторых исследованиях [14, 136–138] специально изучали прогностическое влияние полного патологического ответа (pCR), определяемого полным отсутствием жизнеспособных опухолевых клеток в месте первичной опухоли (ypT0).Точная классификация pCR или ypT0 может быть трудоемкой и трудоемкой задачей при условии, что во многих случаях остаточные жизнеспособные опухолевые клетки могут быть идентифицированы при тщательном микроскопическом исследовании (т. Е. Многоуровневом секционировании блоков, содержащих рубцовую область) [7, 121 ]. В этом отношении различная доля pCR, наблюдаемая в предыдущих исследованиях, могла быть связана с различиями в методах вскрытия и исследования, используемых в каждой лаборатории. Несмотря на эти различия, в нескольких рандомизированных и других исследованиях было показано, что статус pCR значительно коррелирует со снижением частоты местных рецидивов и улучшением выживаемости [137–143].
3.9. Граница кольцевой резекции (CRM)
При микроскопическом исследовании расстояние от опухоли до CRM может быть единственным наиболее важным фактором в прогнозировании местного рецидива (LR) после РКИ и хирургического вмешательства [13, 29, 37]. Вовлечение CRM опухолью также было показано в некоторых исследованиях для прогнозирования отдаленного рецидива и общей выживаемости (OS) [27, 144]. Хотя определение положительного CRM варьируется в разных исследованиях [27, 28], большинство из них с участием нескольких тысяч пациентов поддерживают использование 1 мм в качестве порогового значения для вовлеченного CRM [27].Методы, на которых основано измерение CRM, обсуждались в исследовании Nagtegaal et al. [30], которые изучали разницу в показателях LR среди случаев с положительным CRM, измеренных от самой глубокой точки инвазии первичной опухоли, и пациентов с положительным CRM, измеренных по пораженным лимфатическим узлам в периректальной клетчатке. Они показали, что у пациентов с положительным CRM из-за прямого распространения опухоли локальные рецидивы развивались чаще, чем у пациентов с положительным CRM из-за положительных узлов (22.1% против 12,4%,). Однако в том же исследовании не было различий в частоте локальных рецидивов между пациентами с положительным CRM из-за положительных узлов и пациентов с отрицательным CRM. Как описано ранее, ДП — частое явление в мезоректуме. Тем не менее, на сегодняшний день ни одно исследование не изучало прогностическую значимость измерения CRM на основе расстояния от края боковой резекции до TD. Таким образом, для проведения дальнейших исследований прогностической значимости этих двух новых методов измерения CRM (т.е., исходя из расстояния от положительных узлов или TD), рекомендуется, чтобы в случаях с положительными лимфатическими узлами или TD, практикующие патологоанатомы вели запись расстояния от края боковой резекции до этих периректальных опухолевых узлов в дополнение к сообщению о классический CRM.
4. Резюме и заключение
Предоперационное РКИ вызывает изменения как в общем виде хирургического образца, так и в его патологических характеристиках, что может повлиять на ведение пациента и исход.Прежде всего, необходима оценка мезоректума, так как это важный показатель качества резекции. Затем из резецированного образца следует взять образец и должным образом изучить его, как описано в Шагах 1, 2 и 3, гарантируя, что не будут исключены какие-либо прогностически значимые образцы, особенно те, которые содержат взаимосвязь боковых краев с первичной опухолью и мезоректальными узелками. Должны быть доступны стандартизованные протоколы отбора образцов TME, чтобы патологи, патологоанатомы и ассистенты патологов могли обращаться с этими образцами единообразно и эффективно.Патологические особенности, которые, как постоянно сообщалось, значительно влияют на исход пациента после РКИ, включают патологическую стадию после лечения (ypTNM), микроскопический статус CRM и местный фибровоспалительный ответ, тогда как независимое от стадии прогностическое значение гистологической степени, LVI, PNI и TDs требует дальнейшего исследования в условиях неоадъювантной терапии. Что касается оценки ответа на терапию, то более низкая стадия, по-видимому, лучше оценки клеточного ответа как с точки зрения воспроизводимости, так и с точки зрения прогнозирования клинических исходов.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов в отношении публикации этой статьи.
Выживание при раке желудка | Исследования рака Великобритании
Выживание зависит от множества различных факторов. Поэтому никто не может сказать вам точно, сколько вы проживете. Зависит от вашего:
- тип и стадия рака
- уровень физической подготовки
- предыдущее лечение
Это общая статистика, основанная на больших группах пациентов.Помните, они не могут сказать вам, что произойдет в вашем конкретном случае.
Ваш врач может дать вам дополнительную информацию о вашем собственном прогнозе (прогнозе). Вы также можете поговорить об этом с медсестрами британского отдела исследования рака по бесплатному телефону 0808 800 4040 с 9 до 17 часов с понедельника по пятницу.
Выживаемость по стадиям
В Великобритании нет доступных статистических данных по выживаемости при раке желудка по стадиям.
Статистика выживаемости доступна для каждой стадии рака желудка в Англии.Эти цифры относятся к людям, диагностированным в период с 2013 по 2017 год.
Имейте в виду, что эта статистика не учитывает, какое лечение люди получали.
1 этап
65 из 100 человек (65%) с раком желудка 1 стадии переживут рак в течение 5 или более лет после постановки диагноза.
2 этап
Около 35 из 100 человек (около 35%) с раком желудка 2 стадии переживут рак в течение 5 или более лет после постановки диагноза.
3 этап
Около 25 из 100 человек (около 25%) с раком желудка 3 стадии переживут рак в течение 5 или более лет после постановки диагноза.
4 этап
Статистические данные о 5-летней выживаемости при раке 4 стадии отсутствуют. Это потому, что, к сожалению, большинство людей не живут так долго после постановки диагноза.
Управление национальной статистики предоставляет статистические данные о годовой выживаемости людей с раком желудка 4 стадии.
( Пожалуйста, запомните , это не означает, что вы проживете только 1 год. Это относится к количеству людей, которые все еще живы через 1 год после того, как им поставили диагноз рака. Некоторые из этих людей могут жить дольше 1 года.)
Около 20 из 100 человек (около 20%) с раком желудка 4 стадии переживут рак в течение 1 года или более после постановки диагноза.
Выживаемость рака по стадиям на момент постановки диагноза в Англии, 2019
Управление национальной статистики
Эти статистические данные относятся к чистой выживаемости.Чистая выживаемость оценивает количество людей, переживших рак, а не количество людей, у которых диагностирован рак, которые еще живы. Другими словами, это выживаемость онкологических больных с учетом фоновой смертности, которую они испытали бы, если бы у них не было рака.
Выживаемость при всех стадиях рака желудка
Для людей с раком желудка в Англии:
- более 45 человек из 100 (более 45%) переживут рак в течение 1 года или более
- более 20 человек из 100 (более 20%) переживут рак в течение 5 лет или более
- более 15 из 100 человек (более 15%) переживут рак в течение 10 и более лет
Выживаемость рака по стадиям на момент постановки диагноза в Англии, 2019
Управление национальной статистики
Эти статистические данные относятся к чистой выживаемости.Чистая выживаемость оценивает количество людей, переживших рак, а не количество людей, у которых диагностирован рак, которые еще живы. Другими словами, это выживаемость больных раком с учетом того, что некоторые люди умерли бы от других причин, если бы у них не было рака.
Что влияет на выживаемость
Ваш прогноз зависит от стадии рака, когда он был диагностирован. Это означает, насколько он велик и распространился ли он.
Тип рака и степень злокачественности раковых клеток также могут повлиять на вашу выживаемость. Степень означает, насколько ненормально клетки выглядят под микроскопом.
Ваше общее состояние здоровья и физическая форма также влияют на выживаемость. Чем лучше вы станете, тем лучше вы сможете справиться с раком и лечиться.
Об этой статистике
Термины 1 год выживания и 5 лет не означают, что вы проживете только 1 или 5 лет. Некоторые люди живут намного дольше 5 лет.
Дополнительная статистика
Для получения более подробной информации о выживаемости и раке желудка перейдите в раздел «Статистика рака».

 Сфинктер и наружное отверстие сохраняются.
Сфинктер и наружное отверстие сохраняются.